PENGARUH KONSENTRASI BAP DAN UMUR PLANTLET
TERHADAP PERTUMBUHAN PLANTLET NENAS
(
Ananas comosus
L. Merr) VARIETAS
SMOOTH CAYENNE
HASIL KULTUR
IN VITRO
RAMADHANI DWI SANTOSO
A24070176
DEPARTEMEN AGRONOMI DAN HORTIKULTURA
FAKULTAS PERTANIAN
THE EFFECTS OF BAP CONCENTRATIONS
AND AGE GROUPING ON THE GROWTH OF
IN VITRO CULTURED
SMOOTH CAYENNE
PINEAPPLE (
Ananas comosus
L. MERR) PLANTLETS
Ramadhani Dwi Santoso1, Sobir2
Abstract
The aim of this research is to study the effects of synthetic cytokinin
(6-benzylaminopurine/ BAP) treatments on two groups of pineapple (Ananas
comosus L.Merr) plantlets differentiated by plantlet ages. The research used the
Factorial Experiment on Randomized Complete Block Design with two factors,
which are BAP concentrations (0 ppm, 25 ppm, 50 ppm, and 75 ppm) and plantlet
division by age grouping (52 days and 69 days), with three replications. It was
then followed by Tukey’s Honestly Significant Difference Test at error level of
5%.
The results show that BAP treatments with the concentration used in this
research significantly inhibits the growth of pineapple plantlets observed on four
parameters (number of leaves, leave length, plantlet height, and plantlet diameter),
while age grouping tratments didn’t show any significant effects, except on the
plantlet height at 8 and 14 weeks after treatment. There are also tratment-related
interactions which significantly affects the values of the number of leaves and
plantlet height. It was then suggested that lower concentrations of cytokinin are
required if similar research is to be conducted in the future.
Keywords : pinapple, post-acclimatization, propagation, 6-benzylaminopurine
1
Student at Department of Agronomy and Horticulture, Faculty of Agriculture, Bogor Agricultural University
2
RINGKASAN
RAMADHANI DWI SANTOSO. Pengaruh Konsentrasi BAP dan
Umur Plantlet terhadap Pertumbuhan Plantlet Nenas (
Ananas
comosus
L. Merr) Varietas
Smooth Cayenne
Hasil Kultur
In Vitro
.
(Dibimbing oleh SOBIR)
Penelitian ini bertujuan untuk mengetahui pengaruh berbagai konsentrasi
zat pengatur tumbuh (ZPT) sitokinin buatan (6-benzylaminopurine, BAP) pada
dua kelompok umur plantlet nenas (Ananas comosus L. Merr). Rancangan percobaan yang digunakan adalah percobaan faktorial dalam Rancangan
Kelompok Lengkap Teracak (RKLT) dengan dua faktor dan tiga ulangan. Faktor
pertama adalah pemberian BAP yang terdiri atas empat taraf konsentrasi (0 ppm,
25 ppm, 50 ppm, dan 75 ppm). Faktor kedua adalah pengelompokan berdasarkan
umur plantlet. Taraf perlakuan pengelompokan umur plantlet terdiri atas 52 hari
dan 69 hari, dihitung sejak aklimatisasi selesai dilakukan.
Plantlet direndam dalam larutan BAP sesuai dengan taraf yang ditetapkan,
dikeringanginkan, lalu ditanam pada bak tanam dengan jarak tanam 5 cm x 5 cm.
Pengamatan dilakukan terhadap kondisi umum pertanaman dan variabel
pertumbuhan vegetatif, yang terdiri atas jumlah daun, panjang daun, tinggi
plantlet, dan diameter tajuk.
Hasil penelitian menunjukkan bahwa pemberian BAP dalam konsentrasi
yang digunakan secara sangat nyata menekan pertumbuhan plantlet nenas pada
semua variabel yang diamati. Pengelompokan plantlet berdasarkan umur tidak
berpengaruh nyata terhadap pertumbuhan plantlet secara vegetatif, kecuali
terhadap tinggi plantlet pada 8 dan 14 MSA. Interaksi antara faktor pemberian
BAP dan pengelompokan umur berpengaruh nyata untuk tinggi plantlet dan
jumlah daun, sedangkan untuk jumlah daun dan diameter tajuk tidak berpengaruh
PENGARUH KONSENTRASI BAP DAN UMUR PLANTLET
TERHADAP PERTUMBUHAN PLANTLET NENAS
(
Ananas comosus
L. Merr) VARIETAS
SMOOTH CAYENNE
HASIL KULTUR
IN VITRO
Skripsi sebagai salah satu syarat
untuk memperoleh gelar Sarjana Pertanian
pada Fakultas Pertanian Institut Pertanian Bogor
RAMADHANI DWI SANTOSO
A24070176
DEPARTEMEN AGRONOMI DAN HORTIKULTURA
FAKULTAS PERTANIAN
Judul :
PENGARUH KONSENTRASI BAP DAN UMUR
PLANTLET
TERHADAP
PERTUMBUHAN
PLANTLET NENAS (
Ananas comosus
L. Merr)
VARIETAS
SMOOTH CAYENNE
HASIL KULTUR
IN VITRO
Nama :
RAMADHANI DWI SANTOSO
NIM :
A24070176
Menyetujui:
Pembimbing
Dr. Ir. Sobir, MSi NIP 19640512 198903 1 002
Mengetahui:
Ketua Departemen
Dr. Ir. Agus Purwito, MSc.Agr. NIP 19611101 198703 1 003
RIWAYAT HIDUP
Penulis dilahirkan di Bogor, Provinsi Jawa Barat, pada tanggal 30 April
1989. Penulis merupakan anak kedua dari Prof. Dr. Drs. Adi Santoso, MSi dan
Nina Wiyantina, SSi. Penulis lulus dari SDN Panaragan II Bogor pada tahun
2001, kemudian melanjutkan ke SLTPN IV Bogor dan lulus pada tahun 2004.
Tahun 2007, penulis lulus dari SMAN 5 Bogor, dan diterima di Institut Pertanian
Bogor melalui jalur SPMB. Penulis menjalani studi sebagai mahasiswa IPB
dengan program mayor Agronomi dan Hortikultura, Departemen Agronomi dan
KATA PENGANTAR
Segala puji syukur ke hadirat Allah Tuhan Semesta Alam yang atas
petunjuk dan rahmat-Nya penulis dapat menyusun skripsi penelitian dengan judul
”Pengaruh Konsentrasi BAP dan Umur Plantlet terhadap Pertumbuhan Plantlet
Nenas (Ananas comosus L. Merr) Varietas Smooth Cayenne Hasil Kultur In Vitro”. Skripsi ini ditulis sebagai tugas akhir penulis dalam menjalani studi sebagai mahasiswa program studi Agronomi dan Hortikultura, Fakultas Pertanian
Institut Pertanian Bogor.
Penulis menyampaikan terima kasih kepada:
1. Dr. Ir. Sobir, MSi selaku dosen pembimbing atas waktu, tenaga, pikiran dan
kesabaran beliau selama membimbing penulis dalam menyelesaikan
penelitian ini, juga menekankan dalam diri penulis untuk menjadi manusia
yang bermanfaat bagi orang lain.
2. Dr. Dewi Sukma, Sp. Msi dan Ir. Megayani S. Rahayu, MS selaku dosen
penguji, atas waktu, kerjasama dan masukan yang diberikan kepada penulis,
baik dalam hal pembuatan karya ilmiah, maupun pola pikir dan sikap yang
harus dimiliki penulis sebagai bagian dari masyarakat ilmiah.
3. Ayahanda Prof. Dr. Drs. Adi Santoso, MSi dan Ibunda Nina Wiyantina, SSi,
yang telah merawat penulis sejak dalam kandungan hingga saat ini, untuk
semua doa dan kebaikan yang tidak akan pernah cukup dituliskan dengan
kata-kata. Penulis juga berterima kasih kepada Dina Alva Prastiwi, S.P. dan
Dini Ratu Fitria, yang merupakan kakak dan adik kandung penulis yang
selalu mewarnai kehidupan sehari-hari penulis di rumah.
4. Mizana Chaerunnisa, untuk doa, motivasi dan dukungannya baik sebagai
sahabat, saudari, maupun belahan jiwa penulis. Kimi no koto, daisuki.
5. Rekan-rekan mahasiswa Program Studi Agronomi dan Hortikultura angkatan
44, teman-teman di program studi lain, maupun di luar kampus. Thanks for the company, It’s been a very wonderful years, you guys are awesome!
6. Staf pengajar dan segenap keluarga besar Departemen Agronomi dan
Hortikultura IPB, atas ilmu pengetahuan dan ilmu kehidupan yang diajarkan
ii
7. Bapak Baisuni sebagai penanggung jawab Kebun Percobaan Pusat Kajian
Buah Tropika, Pasirkuda Bogor, beserta rekan-rekan di Pusat Kajian Buah
Tropika atas kerjasama selama penelitian berjalan.
Penulis juga berterima kasih kepada semua pihak yang telah membantu sehingga
penelitian dan penyusunan skripsi ini dapat berjalan dengan baik. Semoga hasil
penelitian ini bermanfaat bagi yang membutuhkan.
Bogor, 24 Februari 2011
DAFTAR ISI
Halaman
KATA PENGANTAR ... i
DAFTAR ISI ... iii
DAFTAR TABEL ... iv
DAFTAR GAMBAR ... vi
DAFTAR LAMPIRAN ... vii
PENDAHULUAN ... 1
Latar Belakang ... 1
Tujuan ... 2
Hipotesis ... 2
TINJAUAN PUSTAKA ... 3
Nenas (Ananas comossus L. Merr) ... 3
Perbanyakan Nenas ... 6
Sitokinin ... 7
BAHAN DAN METODE ... 10
Tempat dan Waktu ... 10
Bahan dan Alat ... 10
Rancangan Percobaan ... 10
Pelaksanaan Penelitian ... 11
Pengamatan ... 12
HASIL DAN PEMBAHASAN ... 13
Kondisi Umum ... 13
Jumlah Daun ... 17
Panjang Daun ... 19
Tinggi Plantlet... 21
Diameter Tajuk ... 24
KESIMPULAN DAN SARAN ... 27
Kesimpulan ... 27
Saran ... 27
DAFTAR PUSTAKA ... 28
DAFTAR TABEL
Teks
Nomor Halaman
1. Kode Perlakuan Beserta Konsentrasi BAP dan Umur Plantlet yang Diujikan ... 10
2. Rekapitulasi Sidik Ragam Pengaruh Perlakuan terhadap Jumlah Daun pada 2-16 MSA ... 17
3. Rataan Jumlah Daun Plantlet dengan Berbagai Taraf Konsentrasi BAP pada 2, 6, dan 8-16 MSA ... 18
4. Rekapitulasi Sidik Ragam Pengaruh Perlakuan terhadap Panjang Daun pada 2-16 MSA ... 19
5. Rataan Panjang Daun Plantlet dengan Berbagai Taraf Konsentrasi BAP pada 2, 8, 10, dan 16 MSA ... 20
6. Rekapitulasi Sidik Ragam Pengaruh Perlakuan terhadap Tinggi
Plantlet pada 2-16 MSA ... 22
7. Rataan Tinggi Plantlet Plantlet dengan Berbagai Taraf Konsentrasi BAP pada 2, 6, 10, dan 16 MSA ... 23
8. Rekapitulasi Sidik Ragam Pengaruh Perlakuan terhadap Diameter Tajuk pada 2-16 MSA ... 24
9. Rataan Diameter Tajuk Plantlet dengan Berbagai Taraf Konsentrasi BAP pada 2, 6, 10, 14, dan 16 MSA ... 25
Lampiran
10. Sidik Ragam pengaruh perlakuan terhadap jumlah daun plantlet pada 2-16 MSA ... 33
11. Sidik Ragam pengaruh perlakuan terhadap panjang daun plantlet pada 2-16 MSA ... 33
12. Sidik Ragam pengaruh perlakuan terhadap tinggi plantlet pada 2-16 MSA ... 34
13. Sidik Ragam pengaruh perlakuan terhadap diameter tajuk plantlet pada 2-16 MSA ... 35
v
15. Rataan Panjang Daun Plantlet pada 2-16 MSA ... 37
16. Rataan Tinggi Plantlet pada 2-16 MSA... 37
DAFTAR GAMBAR
Nomor Halaman
1. Struktur sitokinin (Harjadi, 2009) ... 8
2. Ilustrasi Plantlet Sampel dan Variabel Pengamatan yang Diukur pada Plantlet Tersebut... 12
3. Keracunan pada Plantlet Akibat Perlakuan BAP. ... 13
4. Perbandingan Keragaan Plantlet Kontrol dan Perlakuan. ... 14
5. Timbulnya Garis Merah pada Plantlet C3U2 (4 MSA) akibat
perlakuan BAP ... 15
6. Perkembangan Tunas Pada Plantlet C3U1(1):10 ... 16
7. Grafik Perubahan Jumlah Daun dengan Berbagai Konsentrasi BAP pada 2-16 MSA ... 18
8. Grafik Perubahan Panjang Daun (cm) dengan Berbagai Konsentrasi BAP pada 2-16 MSA ... 20
9. Grafik Perubahan Tinggi Plantlet dengan Berbagai Konsentrasi BAP pada 2-16 MSA ... 22
DAFTAR LAMPIRAN
Nomor Halaman
1. Denah Lahan Penelitian ... 32
2. Sidik Ragam Pengaruh Perlakuan terhadap Pertumbuhan
Vegetatif ... 33
PENDAHULUAN
Latar Belakang
Perbanyakan bibit merupakan tahapan yang penting dalam pengembangan
varietas baru. Varietas baru yang telah dikembangkan dari penelitian para ahli
dapat dirasakan manfaatnya apabila diperbanyak dan didistribusikan kepada
masyarakat. Varietas baru tersebut harus diperbanyak sedemikian rupa sehingga
mampu memenuhi tiga syarat, yaitu kualitas prima, harga yang bersaing, dan
ketersediaan yang konsisten, dalam arti produk dapat tersedia tepat waktu dan
jumlahnya sesuai dengan yang diinginkan. Ketiga syarat tersebut memungkinkan
untuk dicapai apabila produksi dilakukan dalam skala komersial.
Bahan tanam untuk produksi benih nenas varietas baru yang
dikembangkan, tersedia hanya dalam jumlah yang terbatas, padahal produksi
nenas dalam skala komersial membutuhkan bahan tanam 29 000 hingga 86 000
tanaman per hektar (Hepton, 2003). Kebutuhan tersebut tidak dapat dipenuhi
dengan metode perbanyakan konvensional, karena membutuhkan waktu yang
lama dan jumlah bahan tanam yang dihasilkan juga sedikit.
Kultur jaringan merupakan metode untuk menghasilkan plantlet nenas
yang bebas penyakit, seragam, dengan jumlah yang besar dan dalam waktu
singkat (Khan et.al, 2004). Penerapan teknologi kultur jaringan di banyak negara berkembang, masih menemui kendala yang disebabkan oleh tingginya biaya yang
diperlukan untuk penerapan teknologi tersebut (Savangikar, 2004). Hal tersebut
berimbas kepada tingginya harga plantlet hasil kultur jaringan.
Perbanyakan konvensional terhadap bahan tanam kultur jaringan
merupakan alternatif yang dapat dijadikan solusi untuk masalah tersebut. Semua
bibit kentang bersertifikat di Irlandia dan Skotlandia saat ini berasal dari tanaman
kultur jaringan yang menghasilkan umbi mikro. Umbi-umbi tersebut ditanam
bukan untuk menghasilkan kentang untuk dipanen, namun diperbanyak dengan
sebanyak 2-4 kali untuk dijadikan bahan tanam. Selain harga yang lebih murah
dan kualitas bibit yang tinggi, petani mendapatkan tipe umbi kentang yang sama
dengan yang sudah biasa mereka tanam. Para petani tebu di Punjab, India pun saat
2
tanaman kultur jaringan yang diperbanyak dengan stek sebanyak 3-4 kali.
Departemen Pertanian di Thailand memproduksi tanaman krisan untuk dijual
kepada para petani, yang kemudian oleh petani diperbanyak dengan stek untuk
keperluan produksi bunga potong. Tanaman ubi dan singkong hasil kultur
jaringan di Cina dan Vietnam didistribusikan secara langsung kepada para petani.
Para petani kemudian memperbanyak tanaman tersebut untuk menghasilkan
bahan tanam sehat untuk ditanam di lahan mereka (Ahloowalia, 2004).
Penelitian ini merupakan upaya untuk mengamati pengaruh pemberian
sitokinin buatan (6-benzylaminopurine, BAP) terhadap plantlet nenas hasil kultur
jaringan. Sitokinin, menurut Ashari (1995) merupakan zat pengatur tumbuh (ZPT)
yang berperan dalam proses pembelahan sel, pembentukan organ, dan
pembentukan mata tunas pada tumbuhan.
Pemberian sitokinin diharapkan dapat memicu pertumbuhan tunas pada
plantlet, sehingga perbanyakan plantlet nenas secara vegetatif dapat dilaksanakan
lebih awal, bahkan sebelum plantlet tumbuh menjadi tanaman dewasa. Pengaruh
sitokinin terhadap pertumbuhan vegetatif plantlet nenas juga dipelajari melalui
pengamatan terhadap variabel pertumbuhan vegetatif, sehingga kelayakan metode
yang digunakan dalam penelitian ini dapat dipertimbangkan untuk penelitian
selanjutnya.
Tujuan
Tujuan dari penelitian ini adalah mengetahui pengaruh pemberian berbagai
konsentrasi BAP pada dua kelompok umur plantlet terhadap pertumbuhan plantlet
nenas (Ananas comosus L. Merr) hasil kultur in vitro.
Hipotesis
1. Perbedaan konsentrasi BAP berpengaruh terhadap pertumbuhan plantlet
nenas hasil kultur in vitro.
2. Perbedaan umur plantlet berpengaruh terhadap pertumbuhan plantlet nenas
hasil kultur in vitro.
3. Terdapat interaksi antara konsentrasi BAP dan umur plantlet yang
TINJAUAN PUSTAKA
Nenas (Ananas comossus L. Merr)
Nenas (Ananas comosus L. Merr) adalah tumbuhan yang berasal dari Amerika Selatan. Bangsa Indian diduga mengadakan seleksi dari tumbuhan nenas
liar sehingga diperoleh A.comosus yang enak dimakan dan banyak dibudidayakan di dunia saat ini (Ashari, 1995).
Nenas saat ini merupakan komoditas buah terpenting ke-3 setelah pisang
dan jeruk. Produk utama yang diperjualbelikan di pasar internasional adalah buah
segar dan olahannya, seperti buah kalengan dan jus. Pasar internasional nenas
didominasi oleh perusahaan-perusahaan multinasional yang mengembangkan
infrastruktur untuk pemrosesan maupun pemasaran nenas. Thailand dan Indonesia
dapat tergolong pengecualian, di mana komoditas nenas dikembangkan dalam
kegiatan prosesing kecil dan bersifat lokal. Walaupun nenas dalam kemasan
kaleng sangat diminati, 70% nenas di pasar internasional diperdagangkan dalam
bentuk buah segar dan dipasarkan di negara penghasilnya. Negara produsen nenas
yang penting seperti Brazil, India, Cina, Nigeria, Meksiko dan Kolumbia
memproduksi nenas untuk konsumsi buah segar di dalam negeri (Rohrbach et al., 2003).
Indonesia menempati urutan ketiga sebagai negara pengekspor nenas
terbesar di dunia setelah Thailand dan Filipina (Purba, 2008). Produksi nenas
segar Indonesia selama tahun 2006-2010 rata-rata sebesar 1 612 682,6 ton dengan
sedikit fluktuasi. Produksi tertinggi nenas Indonesia adalah sebesar 2 237 858 ton
pada tahun 2007, namun pada tahun-tahun berikutnya terjadi penurunan nilai
produksi, hingga mencapai 1 406 445 ton pada tahun 2010 (Deptan, 2011).
Ekspor nenas segar Indonesia berdasarkan pangsa pasarnya relatif masih kecil
dibandingkan negara produsen dan eksportir nenas lainnya. Suprehatin (2006)
dalam penelitiannya mengenai analisis daya saing ekspor nenas segar Indonesia
menyatakan bahwa pangsa pasar nenas Indonesia hanya mencapai rata-rata 0,21
persen per tahun pada tahun 2000 hingga 2004.
Nenas merupakan tanaman herba monokotil tahunan yang buah
4
pertama, tunas-tunas baru pada tumbuhan ini berkembang dan menumbuhkan
tegakan yang mampu memproduksi buah baru. Tumbuhan yang sama mampu
mengalami serangkaian siklus produksi buah, namun di banyak pertanaman
komersial, satu tanaman tidak dibiarkan tumbuh menjadi dua atau tiga tegakan
sekaligus karena ukuran dan keseragaman buahnya dapat berkurang. Oleh karena
itu, pertanaman secara teratur dibongkar kemudian ditanami kembali setiap
musim tanam. Bahan tanam yang digunakan dapat berasal dari tunas
tanaman-tanaman sebelumnya, atau menggunakan bahan lain, seperti mahkota buah, atau
tunas yang tumbuh di bagian dasar buah.
Tumbuhan nenas dewasa memiliki ukuran tinggi 1-2 m dengan lebar 1-2
m. Tinggi batangnya 25-50 cm dan lebarnya 2-5 cm pada bagian dasar dan 5-8 cm
di bagian atasnya. Bagian atas batang tumbuh tegak, sedangkan bentuk batang
bagian bawahnya ditentukan oleh jenis bahan tanam yang digunakan. Bentuknya
sangat melengkung apabila berasal dari tunas yang tumbuh dari dasar buah (slip), agak melengkung jika berasal dari tunas samping, dan tegak apabila berasal dari
mahkota.
Daun nenas tumbuh mengitari 2/3 bagian dari tinggi batangnya. Filotaksis
daun bervariasi, yaitu 5/13 pada tanaman berbuah besar yang dibudidayakan dan
3/8 pada tumbuhan liar yang berbuah kecil (Kerns et al., 1936 dalam
d’Eeckenbrugge dan Leal, 2003). Jumlah daun nenas bervariasi untuk tiap
kultivarnya, namun berkisar antara 40-80 helai. Daun-daun yang tumbuh di
bagian bawah batang berukuran kecil (5-20 cm) dibandingkan dengan daun-daun
yang lebih muda yang tumbuh di bagian atas, di mana panjangnya dapat me1ebihi
1.6 m dan lebarnya mencapai 7 cm. Ukuran daun ditentukan oleh jenis kultivar
dan kondisi lingkungan. Daunnya kaku dengan irisan tegak berbentuk menyerupai
bulan sabit. Daun tumbuhan nenas berwarna hijau atau hijau tua, atau merah tua
dan ungu jika mengandung pigmen antosianin. Permukaan tepi daun berduri,
namun ada beberapa kultivar yang durinya sedikit atau tidak berduri sama sekali.
Akar primer nenas ditemukan hanya pada nenas yang baru memasuki
tahap perkecambahan. Akar-akar tersebut mati dan kemudian digantikan oleh
akar-akar adventif, yang membentuk perakaran yang pendek namun padat di
5
dengan kedalaman mencapai 0.85 m. Jumlah akar yang tumbuh ditentukan oleh
bobot tunas yang digunakan sebagai bahan tanam. Mahkota buah diketahui
menghasilkan lebih banyak akar dibandingkan dengan tunas
Bagian dasar buah dan pembungaan berkembang dari meristem apikal.
Bunga tunggal yang tumbuh dapat berjumlah di bawah 50 hingga di atas 200. Di
atas bunga tumbuh bagian mahkota yang terdiri atas batang pendek yang
ditumbuhi dedaunan (jumlah daun dapat mencapai 150 helai). Bagian buah yang
dapat dimakan merupakan ovarium, dasar kelopak bunga dan bagian korteks
batang. Kulit buahnya merupakan jaringan kelopak bunga dan ujung dari ovarium
(Okimoto, 1948 dalam d’Eeckenbrugge dan Leal, 2003). Pembungaan biasanya memerlukan waktu satu hari, dan bunga dapat bertahan 10-15 hari, hingga dalam
waktu yang tidak teratur, tergantung dari jenis kultivar yang ditanam. Bunga
nenas adalah hermaphrodit, dengan tiga mahkota dan tiga kelopak bunga. Stamen
–nya berjumlah enam buah, sedangkan putiknya terdiri atas satu pistil
tricarpellate. Mahkota bunganya berwarna putih di dasarnya dan biru keunguan di bagian ujungnya (d’Eeckenbrugge dan Leal, 2003).
Nenas dapat tumbuh di sekitar daerah khatulistiwa antara 250 LU/LS. Tumbuhan ini tidak tahan terhadap temperatur dingin. Jenis Cayenne tumbuh di
ketinggian 100 hingga 1 100 m diatas permukaan laut. Buahnya lebih kecil dan
kandungan asamnya lebih tinggi, apabila ditanam pada tempat yang lebih tinggi.
Tanaman ini tahan kekeringan, karena memiliki sel penyimpan air yang efektif
(sukulenta). Curah hujan yang sesuai untuk pertumbuhan nenas adalah 500 – 2000
mm/tahun, namun produksi optimal terjadi di daerah dengan curah hujan 1000 –
1100 mm/tahun. Nenas dapat tumbuh di segala jenis tanah, asalkan memiliki
drainase yang baik, karena tanaman ini tidak toleran terhadap genangan air. Nilai
pH tanah yang baik untuk penanaman nenas adalah antara 5-6,5 (Ashari, 1995).
Varietas nenas yang dikenal dan biasa dibudidayakan petani di Indonesia
adalah Smooth Cayenne dan Queen. Terdapat varietas nenas lain yang jarang
ditanam, yaitu Spanish (Red Spanish dan Green Spanish). Smooth Cayenne
mempunyai ciri tepi daun tidak berduri atau duri hanya terletak pada bagian ujung
daun, mata lebar, daging buah berwarna kuning pucat dan tembus cahaya
6
menjadi buah kalengan. Nenas varietas Queen umumnya dikonsumsi dalam
bentuk segar, mempunyai ciri tepi daun berduri, buah berukuran kecil, mata kecil
dan menonjol, daging buah kuning keemasan, renyah, dan tidak transparan. Nenas
varietas Spanish mempunyai ciri daun berduri dengan warna duri merah dan hijau,
mata datar dan lebih lebar dibandingkan dengan Smooth Cayenne, daging buah
mengandung banyak air, berserat, dan transparan, serta rasa kurang manis
dibanding Smooth Cayenne dan Queen (Indriyani dan Hadiati, 2010)
Perbanyakan Nenas
Tanaman nenas secara konvensional dapat diperbanyak dengan
menggunakan bibit vegetatif seperti tunas anakan yang tumbuh di bagian batang
di bawah tanah, tunas samping yang tumbuh pada batang, tunas mahkota di atas
buah, dan tunas-tunas yang tumbuh di tangkai buah (slip) (Ashari, 1995).
Penelitian mengenai metode perbanyakan makro (macropropagation) secara efektif telah beberapa kali dilakukan. Weerasinghe dan Siriwardana (2006)
menyatakan bahwa perbanyakan nenas menggunakan irisan batang yang
diperbanyak sebanyak dua kali siklus perbanyakan dapat menghasilkan 1050
tunas dalam waktu 16 bulan.
Agogbua dan Osuji (2011) melakukan penelitian mengenai pengaruh
perusakan meristem apikal pada mahkota buah terhadap pertumbuhan tunas
aksilar nenas Smooth Cayenne yang diperbanyak dengan metode SCT (Splitted Crown Technique). Ditemukan bahwa terdapat dominansi apikal tinggi pada mahkota dengan meristem utuh (tidak tumbuh tunas), sedangkan mahkota yang
telah dipotong memiliki laju pertumbuhan tunas yang bervariasi. Mahkota yang
dibagi menjadi empat memiliki jumlah tunas terbesar (543), dibandingkan dengan
mahkota yang dibagi menjadi dua bagian (375), dan mahkota yang hanya dirusak
jaringan meristemnya (166).
Perbanyakan nenas secara konvensional memiliki kelebihan menghasilkan
tanaman klon dengan mutu yang sama, akan tetapi bukan merupakan metode yang
sesuai apabila bahan tanam dibutuhkan dalam jumlah besar. Solusi untuk masalah
7
Kiss et al. (1995) menyatakan bahwa satu plantlet nenas yang diperbanyak secara in vitro dengan metode perpanjangan tunas dapat menghasilkan kira-kira 80 000 plantlet per tahun. Almeida et al. (2002) menyatakan bahwa perbanyakan
in vitro nenas dengan eksplan potongan melintang mata tunas, yang dikulturkan dalam media cair yang mengandung 1.5 mg/l BAP dapat memaksimalkan laju
proliferasi tunas. Diperkirakan dengan metode tersebut, jumlah plantlet yang
diproduksi dapat mencapai 161 080 plantlet dalam waktu 8 bulan, dari
perbanyakan mata tunas satu tanaman yang memiliki delapan slip dan jumlah mata tunas 10 buah tiap slip.
Perbanyakan nenas secara in vitro dapat dilakukan melalui dua jalur, yaitu organogenesis dan embriogenesis. Kedua teknik tersebut dapat dimanfaatkan
untuk berbagai kebutuhan seperti perbanyakan bibit, konservasi plasma nutfah,
perbaikan tanaman melalui variasi somaklonal ataupun manipulasi genetik, hingga
pemisahan tanaman khimera, serta pemeliharaan tanaman mutan yang
menguntungkan (Roostika dan Mariska, 2003).
Akbar et al., (2003) mengemukakan bahwa kalus yang tumbuh pada plantlet nenas yang berasal dari meristem mahkota buah, setelah melalui
serangkaian proses tertentu dapat meregenerasi tunas yang ketika ditanam di
lapangan, memiliki keseragaman morfologi dengan bentuk daun dan pola
pertumbuhan normal.
Pemberian kolkisin pada media juga dapat dilakukan untuk menghasilkan
variasi morfologis pada kultur tanaman nenas. Sebanyak 5% dari kalus yang
diberikan kolkisin menunjukkan gejala albino, mengindikasikan rendahnya
kandungan klorofil a dan b. Potensi regenerasi tunas dan akar dan pertumbuhan
kalus yang diberi perlakuan kolkisin lebih rendah dibandingkan dengan plantlet
normal. Kultur ujung tunas dan kalus dari sumber yang sama secara terus menerus
menghasilkan keturunan yang bervariasi dalam 4-5 siklus perbanyakan in vitro
(Mujib, 2005).
Sitokinin
8
perkembangan tumbuhan. Zat Pengatur Tumbuh (ZPT) dapat merupakan
golongan hormon tumbuhan (fitohormon) maupun zat kimia sintetik yang
memiliki pengaruh hormonal ketika secara eksogen diaplikasikan kepada
tanaman. Sitokinin merupakan golongan hormon yang penting dalam
pertumbuhan karena bersifat esensial dalam pembelahan sel. Sitokinin juga
berperan dalam mengurangi atau menunda senescence, dan memperlambat kerusakan klorofil dan protein seluler (Hartmann et al., 1997). Aktivitas biologis dan kimia dari sitokinin telah diketahui dengan baik, akan tetapi cara kerjanya
belum banyak diketahui, dan baru belum lama ini gen sitokinin dalam tumbuhan
berhasil teridentifikasi (Mok et al. , 2000).
Sitokinin merupakan senyawa pengganti adenin yang meningkatkan
pembelahan sel dan fungsi pengaturan pertumbuhan. Cara kerjanya sama dengan
kinetin (6-furfurylaminopurine). Sitokinin alami yang pertama diisolasi adalah
zeatin dalam biji jagung muda. Zeatin merupakan sitokinin yang paling sering
ditemukan pada hampir semua tumbuhan tinggi, lumut, cendawan patogenik dan
nonpatogenik, bakteri, serta tRNA sel mikroorganisme dan sel hewan. Dewasa ini
ada lebih dari 200 sitokinin alami dan sintetik.
Gambar 1. Struktur sitokinin (Harjadi, 2009)
Peran sitokinin bagi tumbuhan adalah mengatur pembelahan sel,
pembentukan organ, pembesaran sel dan organ, pencegahan kerusakan klorofil,
pembentukan kloroplas, penundaan senesens, pembukaan dan penutupan stomata,
serta perkembangan mata tunas dan pucuk (Harjadi, 2009).
Zat kimia sintetik yang memiliki efek menyerupai sitokinin salah satunya
9
tumbuh sudah banyak diteliti. Mullins (1967) mengemukakan bahwa aplikasi
pemberian BAP dapat meningkatkan keberhasilan infloresens pada stek anggur
(Vitis vinifera). Rangsangan pertumbuhan infloresens oleh BAP diikuti oleh penurunan pertumbuhan vegetatif, dan perkembangan pigmen merah pada
infloresens dan daun.
Williams dan Cartwright (1980) menyatakan bahwa BAP yang
diaplikasikan pada tanaman gandum yang sudah mencapai fase primordium glume
pada batang utamanya dapat meningkatkan hasil panen sebesar 57 persen, akan
tetapi hasil serupa tidak ditemukan pada gandum yang telah mencapai fase
primordium bunga, saat mengalami perpanjangan batang. Sitokinin juga diketahui
meningkatkan keseragaman ukuran dan bobot biji di antara batang utama dan
anakan pada tanaman gandum.
Media kultur jaringan yang mengandung auksin dan sitokinin dapat
merangsang terjadinya organogenesis. Menurut Heylen dan Vendrig (1988),
media kultur jaringan tembakau (Nicotiana tabacum) yang diberikan auksin dan sitokinin dapat merangsang infloresens. Aktivitas organogenesis akibat sitokinin
dan auksin sangat tergantung kepada struktur molekuler zat pengatur tumbuh yang
diberikan. Naqvi (1995) menyatakan bahwa pada media dengan konsentrasi
auksin dan sitokinin tinggi, sel membelah secara amorf tanpa mengalami
diferensiasi. Konsentrasi sitokinin yang lebih tinggi daripada auksin menginduksi
pembentukan tajuk, sedangkan apabila sebaliknya maka akan memicu
pertumbuhan akar.
Danso et al. (2008) mengemukakan bahwa pemberian BAP dengan konsentrasi 5 mg/l pada media cair kultur jaringan nenas varietas MD2 dapat
meningkatkan laju multiplikasi sebesar 2 atau 5 kali lipat, dibandingkan dengan
BAHAN DAN METODE
Tempat dan Waktu
Penelitian dilaksanakan di rumah plastik Kebun Percobaan Pusat Kajian
Buah Tropika IPB, Pasir Kuda Bogor, pada bulan Februari hingga Mei 2011.
Bahan dan Alat
Bahan tanam yang digunakan adalah plantlet nenas varietas Smooth Cayenne yang telah melewati proses hardening dan sedang dalam proses pertumbuhan di pembibitan sebelum ditanam di lapang. Zat pengatur tumbuh
yang digunakan adalah 6-benzylaminopurine (BAP) dalam bentuk serbuk. Bahan
lain yang digunakan adalah NaOH sebagai pelarut BAP. Media tanam yang
digunakan adalah arang sekam. Peralatan yang digunakan adalah batu bata, hand sprayer (kapasitas 2 liter), penggaris, alat-alat tulis, kertas label, kamera digital, dan alat-alat pertanian umum.
Rancangan Percobaan
Rancangan yang digunakan dalam penelitian ini adalah percobaan
faktorial dalam Rancangan Kelompok Lengkap Teracak (RKLT). Terdapat dua
faktor yang diujikan, yaitu taraf konsentrasi BAP dan umur plantlet. Perlakuan
BAP diterapkan dalam empat taraf konsentrasi, yaitu 0 ppm (C0), 25 ppm (C1),
50 ppm (C2), dan 75 ppm (C3), sedangkan umur diuji dalam dua taraf, yaitu 52
hari (U1) dan 69 hari (U2) sejak aklimatisasi selesai dilakukan.
Tabel 1. Kode Perlakuan Beserta Konsentrasi BAP dan Umur Plantlet yang Diujikan
Kode Perlakuan Konsentrasi BAP (ppm) Umur Plantlet (hari)
C0U1 (kontrol) 0 52
C0U2(kontrol) 0 69
C1U1 25 52
C2U1 50 52
C3U1 75 52
C1U2 25 69
C2U2 50 69
11
Setiap perlakuan diulang sebanyak tiga kali sehingga terdapat 24 satuan
percobaan. Satu unit percobaan terdiri atas 50 plantlet nenas, dengan sampel
pengamatan setiap unitnya berjumlah 10 plantlet, sehingga jumlah plantlet yang
diamati adalah sebanyak 240 plantlet.
Model rancangan yang digunakan dalam penelitian ini adalah :
Yijk = + Ki + Cj + Uk + (C*U)jk + ijk
Keterangan :
Yijk : Nilai pengamatan pada perlakuan kelompok ulangan ke-i,
perlakuan BAP ke-j, dan ulangan ke-k : Nilai rataan umum
Ki : Pengaruh ulangan ke-i (i : 1,2,3)
Cj : Pengaruh taraf konsentrasi BAP ke-j (j : 1,2,3,4)
Uk : Pengaruh umur ke-k (k : 1,2)
(C*U)jk : Interaksi antara taraf konsentrasi BAP ke-j dengan umur ke-k ijk : Galat percobaan
Hasil pengamatan yang diperoleh dianalisis dengan sidik ragam, dan
dilanjutkan dengan uji beda nyata jujur Tukey (Tukey’s Honestly Significant Difference Test) apabila hasil menunjukkan nilai yang berbeda nyata. Taraf kesalahan yang digunakan untuk uji BNJ adalah 5%.
Pelaksanaan Penelitian
Bak tanam berukuran 13 m x 1 m dibuat menggunakan batu bata yang
disusun di lantai rumah plastik. Media tanam arang sekam kemudian diisikan ke
dalam bak tanam secara merata. Larutan BAP disiapkan dengan konsentrasi 25
ppm, 50 ppm, dan 75 ppm. Volume larutan BAP adalah sebanyak 2 liter untuk
setiap konsentrasinya. Aplikasi BAP dilakukan dengan merendam plantlet nenas
ke dalam larutan BAP selama 30 menit. Plantlet kemudian dikeringanginkan, lalu
ditanam pada bak tanam dengan jarak tanam 5 cm x 5 cm. Aplikasi dilakukan
pada tanggal 31 Januari 2011 pukul 19.00 WIB
Perawatan plantlet terdiri atas pemupukan dan pengendalian gulma dan
organisme pengganggu tanaman (OPT). Pemupukan dilakukan dengan
12
volume semprot 2 L. Pemupukan dilakukan pada 2, 6, 10, dan 14 minggu setelah
aplikasi (MSA), mengikuti aturan pemakaian pada kemasan pupuk (4 minggu
sekali). Pengendalian gulma dan OPT dilakukan apabila dibutuhkan.
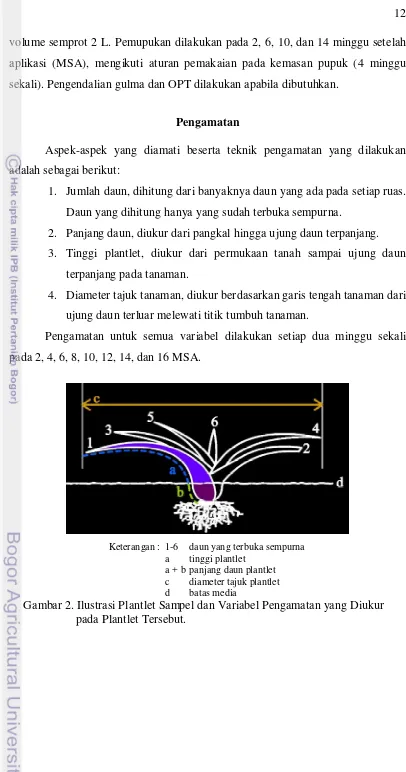
Pengamatan
Aspek-aspek yang diamati beserta teknik pengamatan yang dilakukan
adalah sebagai berikut:
1. Jumlah daun, dihitung dari banyaknya daun yang ada pada setiap ruas.
Daun yang dihitung hanya yang sudah terbuka sempurna.
2. Panjang daun, diukur dari pangkal hingga ujung daun terpanjang.
3. Tinggi plantlet, diukur dari permukaan tanah sampai ujung daun
terpanjang pada tanaman.
4. Diameter tajuk tanaman, diukur berdasarkan garis tengah tanaman dari
ujung daun terluar melewati titik tumbuh tanaman.
Pengamatan untuk semua variabel dilakukan setiap dua minggu sekali
pada 2, 4, 6, 8, 10, 12, 14, dan 16 MSA.
Keterangan : 1-6 daun yang terbuka sempurna a tinggi plantlet
a + b panjang daun plantlet c diameter tajuk plantlet d batas media
HASIL DAN PEMBAHASAN
Kondisi Umum
Berdasarkan pengamatan secara visual, diketahui bahwa pemberian BAP
menekan pertumbuhan plantlet nenas. Hal ini terlihat pada 1-3 MSA, di mana
plantlet menunjukkan gejala keracunan dan mengalami kematian. Kematian
plantlet terbanyak ditemukan pada kelompok dengan perlakuan BAP 75 ppm dan
umur plantlet 52 hari, sebesar 15% dari keseluruhan kelompok perlakuan.
(a) (b)
Gambar 3. Keracunan pada Plantlet Akibat Perlakuan BAP. Gejala keracunan berupa daun yang mengering pada 1 MSA (a). Kematian plantlet pada kelompok plantlet C3U1 pada 2 MSA (b).
Gejala keracunan pada seluruh plantlet yang diberi perlakuan BAP mulai
berkurang pada umur 4 MSA, akan tetapi keragaan plantlet yang diberi perlakuan
BAP tidak sebaik kontrol (BAP 0 ppm). Kondisi tersebut berlangsung hingga
periode pengamatan berakhir pada 16 MSA. Pertumbuhan yang terhambat
menunjukkan bahwa konsentrasi sitokinin di dalam jaringan terlalu tinggi, di
mana hal tersebut menghambat pertumbuhan akar, sehingga pertumbuhan plantlet
juga menjadi terhambat (Ashari, 1995).
Mullins (1967) dalam penelitiannya mengenai pengaruh BAP terhadap
pertumbuhan stek batang anggur mengemukakan bahwa BAP bersifat toksik pada
konsentrasi diatas 20 mg/l. Efek toksik yang ditimbulkan pada stek batang anggur
14
pengaruh BAP terhadap pertumbuhan vegetatif plantlet nenas kultivar Queen di lapangan juga menyatakan bahwa semakin tinggi konsentrasi BAP yang
digunakan, ukuran tanaman menjadi lebih kecil akibat terhambatnya pertumbuhan
tanaman. Konsentrasi optimum BAP untuk pertumbuhan tanaman adalah 0.5-1
mg/l.
0 MSA 2 MSA 16 MSA
Kontrol (BAP 0 ppm, umur plantlet 69 hari)
Perlakuan (BAP 50 ppm, umur plantlet 69 hari))
Gambar 4. Perbandingan Keragaan Plantlet Kontrol dan Perlakuan; terlihat plantlet kontrol menunjukkan keragaan yang lebih baik daripada plantlet yang diberikan perlakuan.
Terdapat perubahan warna pada daun plantlet yang diberi perlakuan BAP.
Perubahan warna tersebut berupa timbulnya garis merah di sekitar garis tengah
daun. Perubahan tersebut tidak terjadi pada semua plantlet yang diberikan
perlakuan, tetapi hanya terdapat pada sebagian kecil plantlet C3U2 (konsentrasi
BAP 75 ppm, umur 69 hari). Gejala serupa sebelumnya ditemukan oleh Mullins
(1967) pada stek batang tanaman anggur. Stek yang ditumbuhkan dalam media
yang mengandung 10 mg/l atau lebih BAP, daunnya berwarna merah-hijau,
sedangkan daun pada stek yang ditumbuhkan dalam media air berwarna hijau
normal. Agustina (2005) juga menemukan bahwa terdapat variasi pada tanaman
yang diberi perlakuan BAP dalam konsentrasi tinggi (2 dan 4 mg/l). Salah satu
jenis variasi tersebut adalah berupa variegasi pada warna daun. Semakin tinggi
konsentrasi BAP yang diberikan, maka kemungkinan munculnya keragaman atau
15
Gambar 5. Timbulnya Garis Merah pada Plantlet C3U2 (4 MSA) akibat perlakuan BAP
Terdapat cekaman lingkungan yang dialami kelompok plantlet C1U2
(BAP 25 ppm, umur plantlet 69 hari). Cekaman tersebut adalah kelembaban
tinggi, yang disebabkan oleh dekatnya lokasi penanaman dengan sumber air.
Akibatnya kelompok plantlet tersebut mengalami penghambatan pertumbuhan
yang signifikan, yang diketahui dari nilai rataan semua variabel pengamatan yang
paling paling rendah dibandingkan dengan kelompok plantlet yang lain.
Kelembaban yang tinggi mengakibatkan proses pertukaran gas di dalam
media terganggu, kadar CO2 dalam media meningkat, sementara kadar O2 menurun. Hal ini mengakibatkan akar tanaman kekurangan oksigen dan
pertumbuhan tanaman menjadi terhambat (Malézieux et al., 2003). Laju difusi oksigen dalam air adalah 10-4 kali lebih rendah dibandingkan di udara, sehingga laju pencukupan kebutuhan oksigen dari dalam media bagi tanaman yang berada
di media dengan kadar air tinggi menjadi jauh lebih rendah (Hale dan Orcutt,
1987).
Aplikasi BAP dalam penelitian ini tidak memicu pembentukan tunas. Hal
ini disebabkan oleh konsentrasi yang terlalu tinggi, umur plantlet yang terlalu
muda, atau keduanya. Hanya satu plantlet yang menumbuhkan tunas baru dari 240
plantlet yang dijadikan tanaman sampel. Tunas baru tersebut diamati pada 4 MSA
hingga akhir periode pengamatan. Tunas tersebut diketahui memiliki tinggi sekitar
1-1.50 cm pada akhir periode pengamatan.
16
pertumbuhan akar pada stek daun Begonia. Konsentrasi yang tinggi tersebut memaksimalkan pembentukan tunas adventif, namun mengurangi kualitasnya.
Tidak terjadinya pembentukan tunas tersebut pada penelitian ini disebabkan oleh
konsentrasi sitokinin yang terlalu tinggi (25, 50, dan 75 ppm). Konsentrasi
sitokinin yang tinggi pada tanaman menghambat pertumbuhan akar, sehingga
tanaman tidak dapat menyerap nutrisi dari media dengan baik. Penyerapan nutrisi
yang tidak baik dapat menghambat pertumbuhan, dan apabila dikaitkan dengan
kemampuan plantlet yang terbatas untuk menyediakan energi melalui fotosintesis,
maka hal ini dapat menjelaskan mengapa plantlet tidak menghasilkan tunas
walaupun diberikan tambahan sitokinin.
Gambar 6. Perkembangan tunas pada plantlet C3U1(1):10. Tanda panah dan lingkaran kuning menunjukkan letak tunas; (a) 4 MSA, (b) 10 MSA, (c) 16 MSA
Umur plantlet yang terlalu muda tidak memungkinkan plantlet
menghasilkan energi yang cukup untuk proses pembentukan tunas baru. Walau
diketahui BAP dapat meningkatkan laju proliferasi tunas pada plantlet nenas
dalam media kultur jaringan (Almeida et al., 2002), hal ini tidak berlaku pada penelitian ini, karena plantlet yang tumbuh di lapangan harus berfotosintesis
untuk menyediakan energinya sendiri, tidak seperti plantlet in vitro yang mendapatkan sebagian besar energi dari media tumbuhnya.
Pembentukan tunas pada plantlet nenas yang dikulturkan dalam media in vitro yang mengandung BAP telah beberapa kali diteliti. Enggaringati (2006) menyatakan bahwa eksplan pangkal batang nenas yang dikulturkan dalam media
17
sebanyak 13.9 tunas per eksplan dalam waktu 6 minggu. Saif et al. (2011) mengemukakan bahwa tunas dapat tumbuh pada plantlet nenas yang ditanam
dalam kondisi in vitro. Plantlet ditanam pada media MS yang diberi tambahan 2 mg/l BAP. Tunas tumbuh dengan laju pertumbuhan 23 tunas per 60 hari inkubasi
untuk setiap plantlet.
Jumlah Daun
Pengamatan jumlah daun dilakukan untuk setiap daun baru yang tumbuh.
Sidik ragam menunjukkan bahwa pemberian BAP berpengaruh sangat nyata,
kecuali pada 6 MSA, di mana perlakuan tersebut berpengaruh nyata.
Pengelompokan umur plantlet tidak berpengaruh nyata terhadap jumlah daun
selama periode pengamatan. Interaksi antar dua faktor perlakuan tidak
berpengaruh nyata terhadap nilai rataan jumlah daun, kecuali pada 6 MSA, di
mana interaksi berpengaruh nyata.
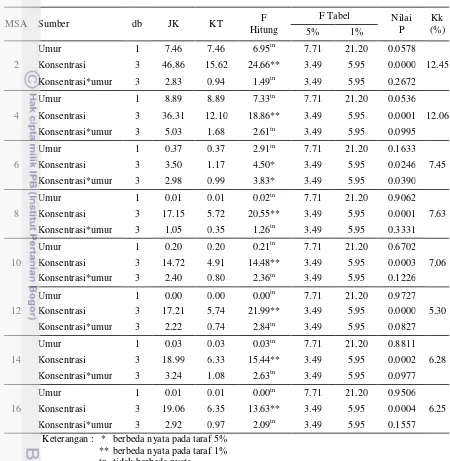
Tabel 2. Rekapitulasi Sidik Ragam Pengaruh Perlakuan terhadap Jumlah Daun pada 2-16 MSA
MSA Konsentrasi (C)
Umur (U)
Interaksi C x U
Koefisien keragaman (%)
2 ** tn tn 12.45
4 ** tn tn 8.53
6 * tn * 7.45
8 ** tn tn 7.63
10 ** tn tn 7.06
12 ** tn tn 5.30
14 ** tn tn 6.28
16 ** tn tn 6.25
18
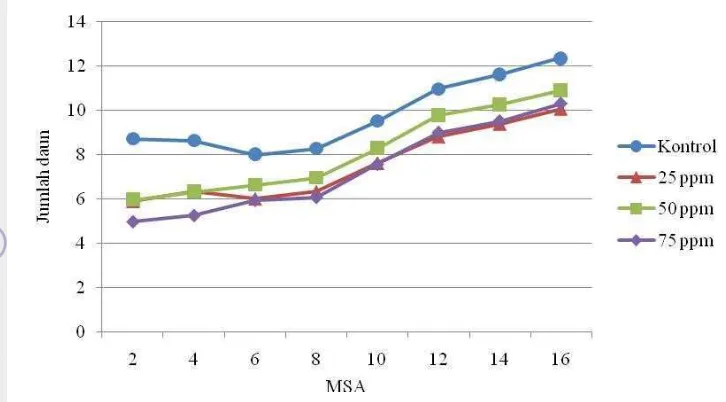
Gambar 7. Grafik Perubahan Jumlah Daun dengan Berbagai Konsentrasi BAP pada 2-16 MSA
Jumlah daun mengalami peningkatan seiring pertumbuhan helai-helai daun
baru selama periode pengamatan (Gambar 7). Plantlet kontrol memiliki jumlah
daun berbeda nyata dibandingkan dengan plantlet yang diberi perlakuan pada 2, 8,
14 dan 16 MSA (Tabel 3).
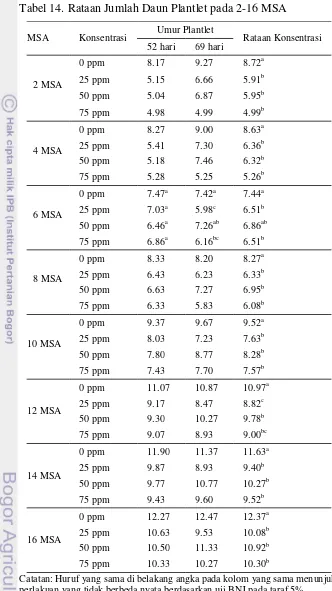
Tabel 3. Rataan Jumlah Daun Plantlet dengan Berbagai Taraf Konsentrasi BAP pada 2, 6, dan 8-16 MSA
Konsentrasi
Jumlah Daun (helai) 2
MSA
6 MSA 8 MSA
12 MSA
14 MSA
16 MSA U1 U2
0 ppm 8.72a* 7.47a 7.42a 8.27a 10.97a 11.63a 12.37a 25 ppm 5.91b 7.03a 5.98c 6.33b 8.82c 9.40b 10.08b 50 ppm 5.95b 6.46a 7.26ab 6.95b 9.78b 10.27b 10.92b 75 ppm 4.99b 6.86a 6.16bc 6.08b 9.00bc 9.52b 10.30b Keterangan : U1 umur plantlet 52 hari
U2 umur plantlet 69 hari
* Huruf yang sama di belakang angka pada kolom yang sama menunjukkan pengaruh perlakuan yang tidak berbeda nyata berdasarkan uji BNJ pada taraf 5%.
Pengaruh interaksi dapat dilihat pada Tabel 3. Interaksi pada 6 MSA
menghasilkan nilai rataan jumlah daun yang berbeda untuk kedua kelompok umur
plantlet yang diujikan. Pada kelompok umur U1(umur plantlet 52 hari), tidak
terdapat beda nyata baik di antara kontrol maupun semua perlakuan, namun pada
kelompok U2 (umur plantlet 69 hari), terlihat perlakuan 50 ppm memiliki nilai
rataan jumlah daun yang tidak berbeda nyata baik dengan kontrol maupun dengan
19
Perlakuan BAP 75 ppm menghasilkan nilai rataan yang tidak berbeda nyata
dengan 25 ppm, namun berbeda nyata dengan kontrol. Perlakuan BAP
memberikan hasil yang berbeda nyata di antara semua taraf konsentrasi pada 12
MSA, kecuali pada plantlet dengan perlakuan BAP 75 ppm, di mana jumlah
daunnya tidak berbeda nyata dengan 50 ppm.
Nilai rataan jumlah daun tertinggi dihasilkan oleh plantlet kontrol, yaitu
sebesar 12.37 helai, dan nilai rataan terendah dihasilkan kelompok plantlet dengan
taraf konsentrasi 25 ppm, yaitu sebesar 10.08 helai.
Panjang Daun
Berdasarkan sidik ragam, perlakuan BAP diketahui memberikan pengaruh
sangat nyata terhadap panjang daun. Pengelompokan plantlet berdasarkan umur
tidak berpengaruh nyata terhadap panjang daun plantlet selama periode
pengamatan. Interaksi antara pengelompokan plantlet berdasarkan umur dan
pemberian BAP memberikan pengaruh nyata pada 4, 10, dan 16 MSA. Interaksi
tersebut berpengaruh sangat nyata pada 8 MSA, sedangkan pada 2,6, dan 12-14
MSA, interaksi tersebut tidak berpengaruh nyata terhadap nilai rataan panjang
daun.
Tabel 4. Rekapitulasi Sidik Ragam Pengaruh Perlakuan terhadap Panjang Daun pada 2-16 MSA
MSA Konsentrasi (C)
Umur Plantlet
(U)
Interaksi C x U
Koefisien keragaman (%)
2 ** tn tn 7.34
4 ** tn * 6.72
6 ** tn tn 6.37
8 ** tn ** 6.32
10 ** tn * 6.49
12 ** tn tn 6.85
14 ** tn tn 6.85
16 ** tn * 5.66
20
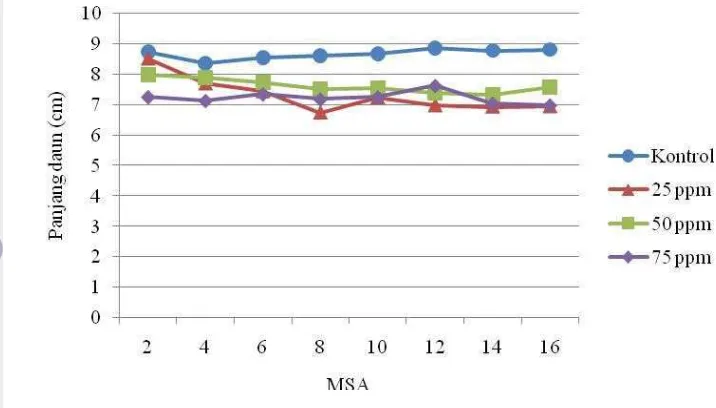
Gambar 8. Grafik Perubahan Panjang Daun (cm) dengan Berbagai Konsentrasi BAP pada 2-16 MSA
Panjang daun plantlet kontrol cenderung tetap selama periode pengamatan
(Gambar 8). Plantlet yang diberi BAP mengalami penurunan nilai rataan panjang
daun selama periode tersebut. Hal ini menunjukkan pemberian BAP dalam
konsentrasi tinggi berpengaruh negatif terhadap nilai rataan panjang daun
maksimal plantlet nenas, sejalan dengan pernyataan Mullins (1967) dan Agustina
(2005) mengenai penghambatan pertumbuhan tanaman akibat perlakuan BAP.
Nilai pengaruh tersebut bisa terlihat pada Tabel 5, di mana nilai rataan jumlah
daun pada plantlet yang diberikan perlakuan BAP cenderung lebih rendah pada 8
hingga 16 MSA dibandingkan pada 2 MSA.
Tabel 5. Rataan Panjang Daun Plantlet dengan Berbagai Taraf Konsentrasi BAP pada 2, 8, 10, dan 16 MSA
Konsentrasi
Panjang Daun (cm)
2 MSA 8 MSA 10 MSA 16 MSA
U1 U2 U1 U2 U1 U2
0 ppm 8.73a* 8.46a 8.76a 8.64a 9.08a 8.40a 9.22a 25 ppm 8.53a 7.84ab 5.65c 7.52ab 6.45c 7.34b 6.57c 50 ppm 8.00ab 7.25b 7.79ab 7.10b 7.73b 7.30b 7.88b 75 ppm 7.27b 7.49ab 6.89b 7.41ab 6.89bc 7.15b 6.83c
Keterangan : U1 umur plantlet 52 hari U2 umur plantlet 69 hari
21
Taraf BAP 25 ppm pada 2 MSA menghasilkan nilai rataan lebih tinggi
dibandingkan dengan 2 taraf lainnya. Nilai rataan panjang daun dipengaruhi oleh
interaksi antara konsentrasi BAP dan umur plantlet. Interaksi tersebut
memberikan pengaruh yang berbeda pada dua kelompok umur. Pada kelompok
U1, nilai rataan panjang daun plantlet dengan konsentrasi BAP 25 dan 75 ppm
tidak menunjukkan perbedaan nyata baik terhadap kontrol maupun kelompok
plantlet dengan perlakuan BAP 50 ppm. Perlakuan BAP 50 ppm memiliki nilai
rataan panjang daun lebih rendah secara nyata dari kontrol. Hal ini terjadi pada 8
dan 10 MSA, sedangkan pada 16 MSA, ketiga perlakuan menunjukkan nilai
berbeda nyata dibandingkan dengan kontrol, namun tidak berbeda nyata satu sama
lain.
Perlakuan 50 ppm menunjukkan nilai rataan yang lebih tinggi
dibandingkan dua perlakuan lainnya pada kelompok umur U2. Nilai tersebut tidak
berbeda nyata dengan nilai rataan panjang daun plantlet dengan perlakuan 75 ppm
pada 8 MSA, namun berbeda nyata dengan perlakuan lainnya pada 10 dan 16
MSA.
Diketahui bahwa pada 16 MSA plantlet kontrol dengan umur plantlet 69
hari memiliki nilai rataan panjang daun terbesar (9.22 cm), sedangkan plantlet
yang diberi perlakuan konsentrasi BAP 25 ppm dengan umur plantlet 69 hari
memiliki nilai rataan panjang daun terkecil (6.57 cm).
Tinggi Plantlet
Sidik ragam menunjukkan bahwa pemberian BAP pada plantlet
mempengaruhi tinggi plantlet secara sangat nyata pada 2 dan 8-16 MSA,
sedangkan pada 4 hingga 6 MSA, perlakuan BAP mempengaruhi tinggi plantlet
secara nyata. Pengelompokan berdasarkan umur plantlet tidak berpengaruh nyata
terhadap tinggi plantlet, kecuali pada 8 dan 14 MSA, di mana hal tersebut
berpengaruh nyata. Terdapat interaksi antara pengelompokan umur plantlet dan
perlakuan konsentrasi BAP terhadap tinggi plantlet. Diketahui interaksi tersebut
mempengaruhi tinggi plantlet secara nyata selama periode pengamatan, kecuali
22
Tabel 6. Rekapitulasi Sidik Ragam Pengaruh Perlakuan terhadap Tinggi Plantlet pada 2-16 MSA
MSA Konsentrasi (C)
Umur Plantlet (U)
Interaksi C x U
Koefisien keragaman (%)
2 ** tn tn 8.39
4 * tn tn 7.35
6 * tn * 6.97
8 ** * tn 5.66
10 ** tn * 6.39
12 ** tn * 6.12
14 ** * * 7.22
16 ** tn * 5.58
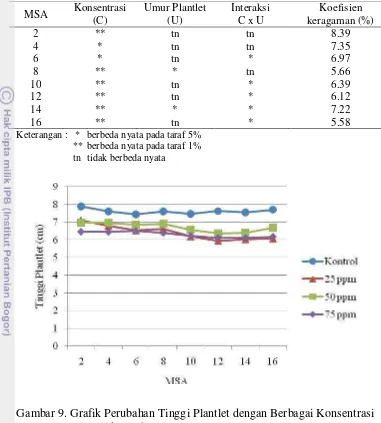
[image:35.595.111.492.117.540.2]Keterangan : * berbeda nyata pada taraf 5% ** berbeda nyata pada taraf 1% tn tidak berbeda nyata
Gambar 9. Grafik Perubahan Tinggi Plantlet dengan Berbagai Konsentrasi BAP pada 2-16 MSA
Tinggi plantlet cenderung tetap selama periode pengamatan. Hal ini
disebabkan tinggi plantlet diukur mengikuti panjang daun terpanjang, sehingga
nilainya cenderung mengikuti nilai variabel panjang daun. Plantlet dengan
perlakuan BAP memiliki ukuran tinggi berbeda nyata dibandingkan dengan
kontrol. Hal ini secara konsisten terlihat mulai periode 2 hingga 16 MSA (Tabel
23
Tabel 7. Rataan Tinggi Plantlet Plantlet dengan Berbagai Taraf Konsentrasi BAP pada 2, 6, 10, dan 16 MSA
Konsentrasi
Tinggi Plantlet (cm)
2 MSA 6 MSA 10 MSA 16 MSA
U1 U2 U1 U2 U1 U2
0 ppm 7.90a 7.47a* 7.42a 7.37a 7.59a 7.40a 8.03a 25 ppm 7.12ab 7.03a 6.08c 6.75ab 5.67c 6.37b 5.81c 50 ppm 6.95ab 6.46a 7.26ab 6.33b 6.81ab 6.30b 7.07b 75 ppm 6.46b 6.86a 6.16bc 6.57ab 5.91bc 6.17b 6.20bc Keterangan : U1 umur plantlet 52 hari
U2 umur plantlet 69 hari
* Huruf yang sama di belakang angka pada kolom yang sama menunjukkan pengaruh perlakuan yang tidak berbeda nyata berdasarkan uji BNJ pada taraf 5%.
Pemberian BAP memberikan pengaruh negatif terhadap nilai rataan tinggi
tanaman. Hal ini dapat dilihat dari nilai rataan yang menurun, misal di antara 2,
10, dan 16 MSA (Tabel 7). Konsentrasi perlakuan 25 ppm menghasilkan nilai
rataan lebih tinggi dibandingkan 2 konsentrasi lainnya pada 2 MSA.
Interaksi antara konsentrasi BAP dan pengelompokan berdasarkan umur
plantlet dapat diamati pada Tabel 7. Interaksi tersebut memberikan pengaruh yang
berbeda pada dua kelompok umur yang diujikan. Nilai rataan plantlet pada
kelompok umur U1 tidak berbeda nyata untuk semua konsentrasi yang diujikan,
namun pada 10 MSA terlihat perbedaan, di mana perlakuan 50 ppm berbeda nyata
dibandingkan kontrol, namun tidak berbeda nyata dibandingkan dengan dua
perlakuan BAP lainnya. Plantlet yang diberi perlakuan BAP memiliki nilai tinggi
plantlet yang berbeda nyata dengan kontrol pada 16 MSA, namun tidak berbeda
nyata antar masing-masing perlakuan. Nilai rataan pada plantlet kelompok U2
berbeda, di mana konsentrasi BAP 50 ppm memberikan hasil yang lebih tinggi
dibandingkan dengan konsentrasi 25 dan 75 ppm. Plantlet dengan perlakuan BAP
25 ppm memiliki nilai berbeda nyata dengan BAP 50 ppm, namun tidak berbeda
nyata dengan plantlet dengan konsentrasi BAP 75 ppm.
Kelompok plantlet yang memiliki ukuran tinggi plantlet terbesar pada 16
MSA adalah kontrol dengan usia plantlet 69 hari (8.03 cm), sedangkan plantlet
dengan perlakuan konsentrasi BAP 25 ppm dan umur plantlet 69 hari memiliki
24
Diameter Tajuk
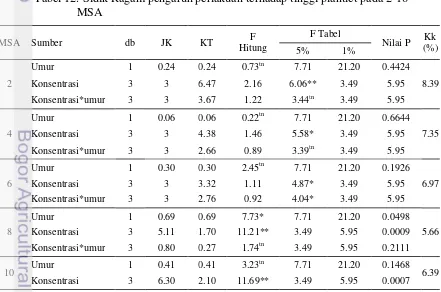
Rekapitulasi sidik ragam menunjukkan bahwa pemberian BAP
memberikan pengaruh sangat nyata terhadap diameter tajuk, kecuali pada 4 MSA,
di mana perlakuan BAP berpengaruh nyata. Pengelompokan berdasarkan umur
plantlet tidak berpengaruh nyata pada 2 - 16 MSA. Interaksi yang terjadi antara
faktor perlakuan BAP pengelompokan berdasarkan umur plantlet memberikan
pengaruh nyata pada 2-6 dan 10 MSA, sedangkan pada 12 MSA berpengaruh
sangat nyata. Interaksi tidak berpengaruh nyata terhadap diameter tajuk plantlet
pada 14 hingga 16 MSA.
Tabel 8. Rekapitulasi Sidik Ragam Pengaruh Perlakuan terhadap Diameter Tajuk pada 2-16 MSA
MSA Konsentrasi (C)
Umur Plantlet
(U)
Interaksi C x U
Koefisien keragaman (%)
2 ** tn * 8.53
4 * tn * 12.06
6 ** tn * 7.81
8 ** tn tn 7.50
10 ** tn * 6.92
12 ** tn ** 6.74
14 ** tn tn 6.93
16 ** tn tn 7.60
Keterangan : * berbeda nyata pada taraf 5% ** berbeda nyata pada taraf 1% tn tidak berbeda nyata
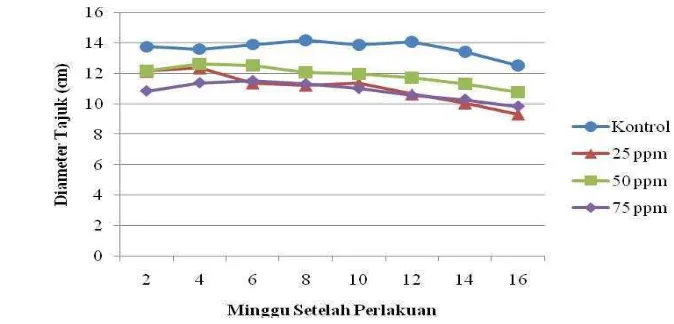
Nilai rataan diameter tajuk menurun seiring periode pengamatan (Grafik
4). Nilai tersebut dipengaruhi nilai rataan panjang daun, sehingga ketika panjang
daun mengalami penurunan, nilai rataan diameter tajuk juga menurun. Perlakuan
BAP memberikan pengaruh negatif terhadap diameter tajuk plantlet. Hal ini
terlihat dari nilai rataan yang berbeda nyata antara plantlet kontrol dan plantlet
yang diberi perlakuan (Gambar 9 dan Tabel 9). Penurunan nilai rataan diameter
tajuk juga dialami oleh plantlet kontrol. Hal ini disebabkan oleh persaingan antar
25
Gambar 10. Grafik Perubahan Diameter Tajuk (cm) dengan Berbagai Konsentrasi BAP pada 2-16 MSA
Tabel 9. Rataan Diameter Tajuk Plantlet dengan Berbagai Taraf Konsentrasi BAP pada 2, 6, 10, 14, dan 16 MSA
Konsentrasi
Diameter Tajuk (cm)
2 MSA 6 MSA 10 MSA 14
MSA 16 MSA
U1 U2 U1 U2 U1 U2
0 ppm 14.10a 13.45a 13.83a 13.84a 13.52a 14.24a 13.44a 12.51a 25 ppm 12.70ab 11.58ab 11.99a 10.74b 12.26ab 10.49b 10.06b 9.34c 50 ppm 10.93b 13.43a 11.68a 13.36a 11.27b 12.65a 11.32b 10.76b 75 ppm 11.23b 10.50b 12.74a 10.36b 11.75ab 10.32b 10.30b 9.84bc Keterangan : U1 umur plantlet 52 hari
U2 umur plantlet 69 hari
* Huruf yang sama di belakang angka pada kolom yang sama menunjukkan pengaruh perlakuan yang tidak berbeda nyata berdasarkan uji BNJ pada taraf 5%.
Plantlet yang diberi BAP memiliki nilai rataan hasil berbeda nyata
dibandingkan dengan kontrol. Interaksi antara dua faktor perlakuan memberikan
pengaruh berbeda pada dua kelompok umur yang diujikan pada 2, 6, dan 10 MSA.
Nilai rataan diameter tajuk plantlet kelompok U1 dengan perlakuan BAP
50 ppm pada 2 MSA berbeda nyata dengan kontrol, sedangkan pada kelompok
umur U2 tidak berbeda nyata. Kelompok perlakuan BAP 75 ppm pada kelompok
umur U1 tidak berbeda nyata dengan perlakuan 50 ppm, namun pada kelompok
umur U2 berbeda nyata. Nilai rataan plantlet dengan perlakuan BAP 25 ppm tidak
berbeda nyata baik dengan kontrol maupun dengan perlakuan BAP lainnya.
Nilai rataan diameter tajuk kelompok plantlet U1 pada 6 MSA tidak
berbeda nyata pada semua konsentrasi yang diujikan, namun pada kelompok U2,
perlakuan BAP 25 ppm dan kontrol tidak berbeda nyata, namun keduanya berbeda
26
kontrol dalam kelompok U1 pada 10 MSA tidak berbeda nyata dengan perlakuan
25 dan 75 ppm, namun berbeda nyata dengan perlakuan 50 ppm, sedangkan pada
plantlet dengan perlakuan BAP 50 ppm, nilai rataan diameter tajuknya tidak
berbeda nyata dengan kedua perlakuan lainnya.
Diketahui bahwa pada 16 MSA plantlet kontrol menghasilkan nilai rataan
tertinggi untuk variabel diameter tajuk (12.61 cm), sedangkan perlakuan
konsentrasi BAP 25 ppm menghasilkan nilai rataan terendah (8.70 cm) pada akhir
KESIMPULAN DAN SARAN
Kesimpulan
Pemberian BAP dalam konsentrasi 25 ppm, 50 ppm, dan 75 ppm
menekan pertumbuhan plantlet nenas. Perlakuan BAP berpengaruh sangat nyata
terhadap semua variabel yang diamati.
Tidak terdapat nilai yang berbeda nyata pada pertumbuhan vegetatif di
antara dua kelompok plantlet yang dibagi berdasarkan umur (52 hari dan 69 hari),
kecuali pada tinggi plantlet pada 8 dan 14 MSA.
Interaksi antara faktor pemberian BAP dan pengelompokan umur
berpengaruh nyata untuk variabel tinggi plantlet dan jumlah daun, sedangkan
untuk jumlah daun dan diameter tajuk tidak berpengaruh nyata.
Saran
Aplikasi BAP pada plantlet nenas sebaiknya dilakukan dengan konsentrasi
yang lebih rendah dari 25 ppm untuk menghindari efek negatif ZPT tersebut
DAFTAR PUSTAKA
Agogbua, J. U. dan J. O. Osuji. 2011.Split crown technique for mass propagation of Smooth Cayenne pineapple in South-South Nigeria. Afr. J. Plant Sci. 5(10): 591-598.
Agustina, G. G. R. 2005. Studi pertumbuhan vegetatif tanaman nanas (Ananas comosus L. Merr) kultivar Queen hasil kultur in vitro. Skripsi. Departemen Budidaya Pertanian Fakultas Pertanian Institut Pertanian Bogor. Bogor. 41 hal.
Ahloowalia, B.S., 2004. Integration of technology from lab to land. Low cost options for tissue culture technology in developing countries (Prosiding). International Atomic Energy Agency (IAEA). Vienna. Hal 87-89.
Akbar, M. A., B. K. Karmakar dan S. K. Roy. 2003. Callus induction and high-frequency plant regeneration of Pineapple (Ananas comosos (L.) Merr). Plant Tissue Cult. 13(2): 109-116.
Almeida, W. A. B. D., G. S. Santana, A. P. M. Rodriguez, M. A. O. D. C. Costa. 2002. Optimization of a protocol for the micropropagation of pineapple. Rev. Bras. Frutic., Jaboticabal – SP. 24(2): 296-300.
Al-Saif, A. M., A. B. M. Sharif Hossain, R. M. Taha. 2011. Effects of benzylaminopurine and naphtalene acetic acid on proliferation and shoot growth of pineapple (Ananas comosus L. Merr) in vitro. Afr. J. Biotechnol. 10(27): 5291-5295.
Ashari, S. 1995. Hortikultura: Aspek Budidaya. Penerbit Universitas Indonesia. Jakarta. 485 hal.
Danso, K. E., K. O. Ayeh, V. Oduro, S. Amiteye dan H. M. Amoatey. 2008. Effect of 6-Benzylaminopurine and ·-Naphthalene Acetic Acid on In vitro Production of MD2 Pineapple Planting Materials. World Appl. Sci.J. 3(4): 614-619.
d’Eeckenbrugge dan F. Leal. 2003. Morphology, anatomy and taxonomy. hal. 13-32. Dalam Bartholomew, D.P., R.E. Paull dan K.G. Rohrbach (Eds). The Pinapple: Botany, Production and Uses. CABI Publishing. New York.
29
Hale, M. G dan D. M. Orcutt. 1987. The Physiology of Plants under Stress. John Wiley and Sons, Inc. New York. 206 hal.
Hartmann, H. T., D.E. Kester, F. T. Davies, Jr. 1997. Plant Propagation: Principles and Practices, Sixth Edition. Prentice-Hall International, Inc. London. 647 hal.
Harjadi, S. S. 2009. Zat Pengatur Tumbuh: Pengenalan dan Petunjuk Penggunaan pada Tanaman. Penebar Swadaya. Jakarta. 76 hal.
Hepton, A. 2003. Cultural system. hal. 109-142. Dalam Bartholomew, D.P., R.E. Paull dan K.G. Rohrbach (Eds). The Pinapple: Botany, Production and Uses. CABI Publishing. New York.
Heylen, C. dan J. C. Vendrig. 1988. The influence of different cytokinins and auxins on flower neoformation in thin clee layers of Nicotiana tabacum L. Plant Cell Physiol. 29(4):665-671.
Indriyani, N. L. P dan S. Hadiati. 2010. Menciptakan nenas varietas baru. Warta Penelitian dan Pengembangan Pertanian. 32(6): 10-12.
Khan, S., A. Nasib, dan B. A. Saeed. 2004. Employment of in vitro technology for large scale multiplication of pineapples (Ananas comosos). Pak. J. Bot. 36(3): 611-615.
Kementrian Pertanian Republik Indonesia. 2011. Produksi Hortikultura Nasional Tahun 2000-2009 dan 2010. http://deptan.go.id/. [13 Februari 2012]
Kiss, E., J. Kiss, G. Gyulai, dan L. E. Hezky. 1995. A novel method for rapid micropropagation of pineapple. HortScience. 30(1): 127-129.
Malézieux, E., F. Côte, D. P. Bartholomew. 2003. Crop environment, plant growth and physiology, hal. 69-107. Dalam Bartholomew, D.P., R.E. Paull dan K.G. Rohrbach (Eds). The Pinapple: Botany, Production and Uses. CABI Publishing. New York.
Mok, M. C., R. C. Martin, dan D. W. S. Mok. 2000. Cytokinins: biosynthesis, metabolism and perception. In Vitro Cell. Dev. Biol.-Plant. 36: 102-107.
Mujib, A. 2005. Colchicine induced morphological variants in pineapple. Plant Tissue Cult. & Biotech. 15(2): 127-133.
30
Naqvi, S. S. M. 1995. Plant growth regulators: the natural hormones (growth promotors and Inhibitors, p. 527-556. Dalam M. Pessarakli (Ed). Handbook of Plant and Crop Physiology. Marcel Dekker, Inc. New York.
Purba, F. H. K. 2008. Perkembangan ekspor nenas Indonesia sebagai salah satu potensi komoditas pertanian dalam daya saing pasar dunia. http://pphp.deptan.go.id/. [22 Februari 2012]
Rohrbach, K.G, F. Leal, dan G.C. d’Eeckenbrugge. 2003. History, distribution and world production, hal. 1-10. Dalam Bartholomew, D.P., R.E. Paull dan K.G. Rohrbach (Eds). The Pinapple: Botany, Production and Uses. CABI Publishing. New York.
Roostika, I dan I. Mariska. 2003. In Vitro culture of pineapple by organogenesis and somatic embryogenesis: its utilization and prospect. Buletin AgroBio. 6(1): 34-40.
Savangikar, V.A., 2004. Role of low cost options in tissue culture. Low cost options for tissue culture technology in developing countries (Prosiding). International Atomic Energy Agency (IAEA). Vienna. Hal 11-15.
Suprehatin. 2006. Analisis daya saing ekspor nenas segar Indonesia. J. Ilmu. Pert. Indonesia. 11(3): 42-48.
Weerasinghe, S. S. dan A. U. Siriwardana. 2006.Fast propagation of pineapple (Ananas comosus) with stem cuttings. The Journal of Agricultural Sciences. 2(2): 55-59.
32
Lampiran 1. Denah Lahan Penelitian
Ulangan
1 2 3
Kontrol
U1 C0U1(1) C0U1(2) C0U1(3)
U
Kontrol
U2 C0U2(1) C0U2(2) C0U2(3)
C3 C3U1(1) C3U1(2) C3U1(3)
C2 C2U1(1) C2U1(2) C2U1(3)
C1 C1U1(1) C1U1(2) C1U1(3)
U2
C3 C3U2(1) C3U2(2) C3U2(3)
C2 C2U2(1) C2U2(2) C2U2(3)
C1 C1U2(1) C1U2(2) C1U2(3)
33
[image:46.595.85.535.133.594.2]Lampiran 2. Sidik Ragam Pengaruh Perlakuan terhadap Pertumbuhan Vegetatif
Tabel 10. Sidik Ragam pengaruh perlakuan terhadap jumlah daun plantlet pada 2-16 MSA
MSA Sumber db JK KT F
Hitung
F Tabel Nilai P
Kk (%) 5% 1%
2
Umur 1 7.46 7.46 6.95tn 7.71 21.20 0.0578
12.45 Konsentrasi 3 46.86 15.62 24.66** 3.49 5.95 0.0000
Konsentrasi*umur 3 2.83 0.94 1.49tn 3.49 5.95 0.2672
4
Umur 1 8.89 8.89 7.33tn 7.71 21.20 0.0536
12.06 Konsentrasi 3 36.31 12.10 18.86** 3.49 5.95 0.0001
Konsentrasi*umur 3 5.03 1.68 2.61tn 3.49 5.95 0.0995
6
Umur 1 0.37 0.37 2.91tn 7.71 21.20 0.1633 7.45 Konsentrasi 3 3.50 1.17 4.50* 3.49 5.95 0.0246 Konsentrasi*umur 3 2.98 0.99 3.83* 3.49 5.95 0.0390
8
Umur 1 0.01 0.01 0.02tn 7.71 21.20 0.9062 7.63 Konsentrasi 3 17.15 5.72 20.55** 3.49 5.95 0.0001 Konsentrasi*umur 3 1.05 0.35 1.26tn 3.49 5.95 0.3331
10
Umur 1 0.20 0.20 0.21tn 7.71 21.20 0.6702 7.06 Konsentrasi 3 14.72 4.91 14.48** 3.49 5.95 0.0003 Konsentrasi*umur 3 2.40 0.80 2.36tn 3.49 5.95 0.1226
12
Umur 1 0.00 0.00 0.00tn 7.71 21.20 0.9727 5.30 Konsentrasi 3 17.21 5.74 21.99** 3.49 5.95 0.0000 Konsentrasi*umur 3 2.22 0.74 2.84tn 3.49 5.95 0.0827
14
Umur 1 0.03 0.03 0.03tn 7.71 21.20 0.8811 6.28 Konsentrasi 3 18.99 6.33 15.44** 3.49 5.95 0.0002 Konsentrasi*umur 3 3.24 1.08 2.63tn 3.49 5.95 0.0977
16
Umur 1 0.01 0.01 0.00tn 7.71 21.20 0.9506 6.25 Konsentrasi 3 19.06 6.35 13.63** 3.49 5.95 0.0004 Konsentrasi*umur 3 2.92 0.97 2.09tn 3.49 5.95 0.1557
Keterangan : * berbeda nyata pada taraf 5% ** berbeda nyata pada taraf 1% tn tidak berbeda nyata
Tabel 11. Sidik Ragam pengaruh perlakuan terhadap panjang daun plantlet pada 2-16 MSA
MSA Sumber db JK KT F
Hitung
F Tabel Nilai P
Kk (%)
5% 1%
2
34
Konsentrasi 3 5.84 1.95 7.06** 3.49 5.95 0.0054 Konsentrasi*umur 3 3.16 1.05 3.82* 3.49 5.95 0.0393
6
Umur 1 0.33 0.33 2.12tn 7.71 21.20 0.2187 6.37 Konsentrasi 3 5.26 1.75 7.15** 3.49 5.95 0.0052 Konsentrasi*umur 3 2.38 0.79 3.23tn 3.49 5.95 0.0607
8
Umur 1 1.43 1.43 4.87tn 7.71 21.20 0.0920 6.32 Konsentrasi 3 11.38 3.79 16.82** 3.49 5.95 0.0001 Konsentrasi*umur 3 6.89 2.30 10.19** 3.49 5.95 0.0013
10
Umur 1 0.09 0.09 0.41tn 7.71 21.20 0.5559 6.49 Konsentrasi 3 8.08 2.69 10.83** 3.49 5.95 0.0010 Konsentrasi*umur 3 4.07 1.36 5.45* 3.49 5.95 0.0134
12
Umur 1 0.11 0.11 0.72tn 7.71 21.20 0.4453 6.85 Konsentrasi 3 13.18 4.39 16.21** 3.49 5.95 0.0002 Konsentrasi*umur 3 2.89 0.96 3.55* 3.49 5.95 0.0477
14
Umur 1 0.05 0.05 0.76tn 7.71 21.20 0.4328 6.85 Konsentrasi 3 3 13.03 4.34 16.33** 3.49 5.95 Konsentrasi*umur 3 3 2.34 0.78 2.94tn 3.49 5.95
16
Umur 1 0.28 0.28 6.36tn 7.71 21.20 0.0653 5.58 Konsentrasi 3 9.99 3.33 24.03** 3.49 5.95 0.0000 Konsentrasi*umur 3 1.68 0.56 4.04* 3.49 5.95 0.0337
[image:47.595.93.534.451.743.2]Keterangan mengikuti Tabel 10
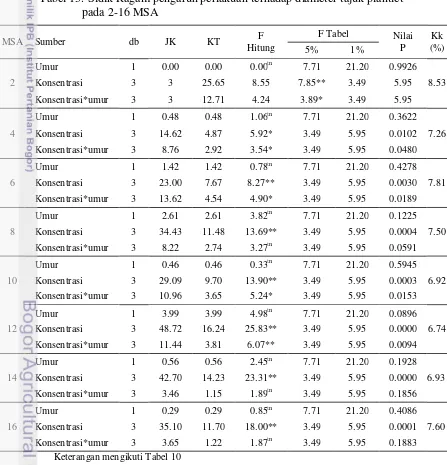
Tabel 12. Sidik Ragam pengaruh perlakuan terhadap tinggi plantlet pada 2-16 MSA
MSA Sumber db JK KT F
Hitung
F Tabel
Nilai P Kk (%)
5% 1%
2
Umur 1 0.24 0.24 0.73tn 7.71 21.20 0.4424 8.39 Konsentrasi 3 3 6.47 2.16 6.06** 3.49 5.95
Konsentrasi*umur 3 3 3.67 1.22 3.44tn 3.49 5.95
4
Umur 1 0.06 0.06 0.22tn 7.71 21.20 0.6644 7.35 Konsentrasi 3 3 4.38 1.46 5.58* 3.49 5.95
Konsentrasi*umur 3 3 2.66 0.89 3.39tn 3.49 5.95
6
Umur 1 0.30 0.30 2.45tn 7.71 21.20 0.1926 6.97 Konsentrasi 3 3 3.32 1.11 4.87* 3.49 5.95
Konsentrasi*umur 3 3 2.76 0.92 4.04* 3.49 5.95
8
Umur 1 0.69 0.69 7.73* 7.71 21.20 0.0498 5.66 Konsentrasi 3 5.11 1.70 11.21** 3.49 5.95 0.0009 Konsentrasi*umur 3 0.80 0.27 1.74tn 3.49 5.95 0.2111
10 Umur 1 0.41 0.41 3.23
tn
35
Konsentrasi*umur 3 2.43 0.81 4.52* 3.49 5.95 0.0243
12
Umur 1 0.23 0.23 1.49tn 7.71 21.20 0.2891 6.12 Konsentrasi 3 10.49 3.50 21.90** 3.49 5.95 0.0000 Konsentrasi*umur 3 2.14 0.71 4.48* 3.49 5.95 0.0249
14
Umur 1 0.31 0.31 12.29* 7.71 21.20 0.0248 7.22 Konsentrasi 3 8.95 2.98 13.41** 3.49 5.95 0.0004 Konsentrasi*umur 3 2.47 0.82 3.70* 3.49 5.95 0.0429
16
Umur 1 0.04 0.04 0.37tn 7.71 21.20 0.5735 5.66 Konsentrasi 3 13