ABSTRACT
PATRICIA NOREVA. Susceptibility of Candida albicans which Isolated from Poultry Abattoirs and Traditional Markets to Antifungal Agents of Ketoconazole, Itraconazole and Griseofulvin. Supervised by EKO SUGENG PRIBADI and
HERLIEN KRISNANINGSIH.
Candidiasis, caused by Candida albicans, is the important mycoses in poultry. In accordance with the development of feed technology, many factors are affecting the health of poultry.Using some antifungals for candidiasis medication are being emerging antifungal-resistant Candida albicans. The study have evaluated sensitivity of C. albicans, which isolated from crops, intestines, and water samples, to the antifungals ketoconazole, itraconazole, and griseofulvin. The result showed that isolated C. albicanswere killed by the antifungal ketoconazole, itraconazole, and griseofulvin except C. albicansthat isolated from intestine sample at TPU Jambu Raya was killed by ketoconazole, and C. albicansthat isolated by intestine and crop samples at RPH Bubulak were killed itraconazole, respectively. There were no significant differences between isolated and reference C. albicans sensitivity (p>0.05) toketoconazole and itraconazole, except to griseofulvin were more sensitive. The ketokonazole was more effective to kill C. albicans than itraconazole and griseofulvin.
PATRICIA NOREVA.KepekaanCandida albicans yangDiisolasidari Beberapa Tempat Pemotongan Unggasdan Pasar Tradisional terhadap Obat Anticendawan Ketokonazol, Itrakonazol dan Griseofulvin.Dibimbing oleh EKO SUGENG PRIBADI dan HERLIEN KRISNANINGSIH.
Kandidiasis, yang disebabkan oleh Candida albicans, merupakan salah satu penyakit mikosis terpenting dalam peternakan unggas. Seiring dengan berkembangnya teknologi pakan ternak, banyak faktor yang ikut mempengaruhi kesehatan unggas. Penggunaan anticendawan untuk pengobatan kandidiasis akan mempengaruhi resistensi anticendawan terhadap Candida albicans. Penelitian ini bertujuan untuk mengetahui kepekaan C. albicans, yang diisolasi dari tembolok, usus dan air, terhadap anticendawan ketokonazol, itrakonazol, dan griseofulvin. Penelitian ini juga menunjukkan bahwa C. albicansmasih peka terhadap pemberian anticendawan ketokonazol, itrakonazol, dan griseofulvin kecuali isolat C. albicans yang berasal dari potongan usus TPU Jambu Raya terhadap ketokonazol serta isolat C. albicans yang berasal dari potongan usus dan tembolok RPH Bubulak terhadap itrakonazol. Tidak terdapat perbedaan nyata (p>0,05) dalam kepekaan anticendawan antara C. albicans yang diisolasi dari contoh dengan referensi, kecuali griseofulvin yang lebih peka. Ketokonazol lebih efektif membunuh isolat C. albicans dibandingkan itrakonazol dan griseofulvin.
KEPEKAAN Candida albicans YANG DIISOLASI DARI
BEBERAPA TEMPAT PEMOTONGAN UNGGAS DAN
PASAR TRADISIONAL TERHADAP OBAT
ANTICENDAWAN KETOKONAZOL,
ITRAKONAZOL DAN
GRISEOFULVIN
PATRICIA NOREVA
FAKULTAS KEDOKTERAN HEWAN
INSTITUT PERTANIAN BOGOR
Dengan ini saya menyatakan bahwa skripsi dengan judul KepekaanCandida albicans yangDiisolasidari Beberapa Tempat Pemotongan Unggasdan Pasar Tradisional terhadap Obat Anticendawan Ketokonazol, Itrakonazol dan Griseofulvinadalah karya saya dengan arahan dari pembimbing dan belum diajukan dalam bentuk apa pun kepada perguruan tinggi mana pun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir skripsi ini.
Bogor, April 2012
ABSTRACT
PATRICIA NOREVA. Susceptibility of Candida albicans which Isolated from Poultry Abattoirs and Traditional Markets to Antifungal Agents of Ketoconazole, Itraconazole and Griseofulvin. Supervised by EKO SUGENG PRIBADI and
HERLIEN KRISNANINGSIH.
Candidiasis, caused by Candida albicans, is the important mycoses in poultry. In accordance with the development of feed technology, many factors are affecting the health of poultry.Using some antifungals for candidiasis medication are being emerging antifungal-resistant Candida albicans. The study have evaluated sensitivity of C. albicans, which isolated from crops, intestines, and water samples, to the antifungals ketoconazole, itraconazole, and griseofulvin. The result showed that isolated C. albicanswere killed by the antifungal ketoconazole, itraconazole, and griseofulvin except C. albicansthat isolated from intestine sample at TPU Jambu Raya was killed by ketoconazole, and C. albicansthat isolated by intestine and crop samples at RPH Bubulak were killed itraconazole, respectively. There were no significant differences between isolated and reference C. albicans sensitivity (p>0.05) toketoconazole and itraconazole, except to griseofulvin were more sensitive. The ketokonazole was more effective to kill C. albicans than itraconazole and griseofulvin.
PATRICIA NOREVA.KepekaanCandida albicans yangDiisolasidari Beberapa Tempat Pemotongan Unggasdan Pasar Tradisional terhadap Obat Anticendawan Ketokonazol, Itrakonazol dan Griseofulvin.Dibimbing oleh EKO SUGENG PRIBADI dan HERLIEN KRISNANINGSIH.
Kandidiasis, yang disebabkan oleh Candida albicans, merupakan salah satu penyakit mikosis terpenting dalam peternakan unggas. Seiring dengan berkembangnya teknologi pakan ternak, banyak faktor yang ikut mempengaruhi kesehatan unggas. Penggunaan anticendawan untuk pengobatan kandidiasis akan mempengaruhi resistensi anticendawan terhadap Candida albicans. Penelitian ini bertujuan untuk mengetahui kepekaan C. albicans, yang diisolasi dari tembolok, usus dan air, terhadap anticendawan ketokonazol, itrakonazol, dan griseofulvin. Penelitian ini juga menunjukkan bahwa C. albicansmasih peka terhadap pemberian anticendawan ketokonazol, itrakonazol, dan griseofulvin kecuali isolat C. albicans yang berasal dari potongan usus TPU Jambu Raya terhadap ketokonazol serta isolat C. albicans yang berasal dari potongan usus dan tembolok RPH Bubulak terhadap itrakonazol. Tidak terdapat perbedaan nyata (p>0,05) dalam kepekaan anticendawan antara C. albicans yang diisolasi dari contoh dengan referensi, kecuali griseofulvin yang lebih peka. Ketokonazol lebih efektif membunuh isolat C. albicans dibandingkan itrakonazol dan griseofulvin.
© Hak Cipta milik IPB, tahun 2012
Hak Cipta dilindungi Undang-Undang
Dilarang mengutip sebagian atau seluruh karya tulis ini tanpa mencantumkan atau menyebutkan sumbernya. Pengutipan hanya untuk kepentingan pendidikan, penelitian, penulisan karya ilmiah, penyusunan laporan, penulisan kritik, atau tinjauan suatu masalah; dan pengutipan tersebut tidak merugikan kepentingan yang wajar IPB
KEPEKAAN Candida albicans YANG DIISOLASI DARI
BEBERAPA TEMPAT PEMOTONGAN UNGGAS DAN
PASAR TRADISIONAL TERHADAP OBAT
ANTICENDAWAN KETOKONAZOL,
ITRAKONAZOL DAN
GRISEOFULVIN
PATRICIA NOREVA
Skripsi
sebagai salah satu syarat untuk memperoleh gelar Sarjana Kedokteran Hewan pada
Fakultas Kedokteran Hewan
FAKULTAS KEDOKTERAN HEWAN
INSTITUT PERTANIAN BOGOR
Judul Skripsi : KepekaanCandida albicans yangDiisolasidari Beberapa Tempat Pemotongan Unggasdan Pasar Tradisional terhadap Obat Anticendawan Ketokonazol, Itrakonazol dan Griseofulvin Nama : Patricia Noreva
NIM : B04070171
Disetujui,
Dr. drh. Eko Sugeng Pribadi, MS. Pembimbing I
drh.Herlien Krisnaningsih, MM. Pembimbing II
Diketahui,
drh. H, Agus Setiyono, MS., PhD, APVet Wakil Dekan Fakultas Kedokteran Hewan
Institut Pertanian Bogor
dan hidayah-Nya penelitian serta penulisan skripsi dengan judul
KepekaanCandida albicans yangDiisolasidari Beberapa Tempat Pemotongan Unggasdan Pasar Tradisional terhadap Obat Anticendawan Ketokonazol, Itrakonazol dan Griseofulvindapat diselesaikan. Skripsi ini disusun sebagai salah satu syarat untuk memperoleh gelar sarjana pada Fakultas Kedokteran Hewan, Institut Pertanian Bogor.
Proses penulisan skripsi ini tidak terlepas dari dukungan berbagai pikah. Maka dari itu, penulis mengucapkan terima kasih yang sebesar-besarnya kepada kedua dosen pembimbing Dr. drh. Eko Sugeng Pribadi, MS. dan drh. Herlien Krisnaningsih, MM. yang senantiasa memberikan arahan, bimbingan, motivasi, kesabaran, pemikiran, dan waktu selama proses penelitian serta penulisan skripsi. Terima kasih pula penulis ucapkan kepada Dr. drh. Eko Sugeng Pribadi, MS. selaku dosen pembimbing yang selalu memberikan motivasi serta arahan untuk menjadi pribadi yang lebih baik, Prof. Dr. drh. Agik Suprayogi, MSc. yang selalu memberikan dukungan serta semangatnya, kepada seluruh pihak dari Dinas Peternakan Kota Bogor (Ibu Osliana, drh. Arif, drh. Mustika) serta seluruh staf bagian Mikrobiologi FKH IPB (pak Agus, mbak Selin, pak Said, pak Ismet, bu Esih, pak Jumli) atas bantuan serta kerjasamanya dalam menyelesaikan penelitian ini.
Ucapan terima kasih juga penulis sampaikan kepada Papa dan Mama tercinta, Nur Syamsu, SE. dan Evelyne Engelica, SE. atas segala kasih sayang, motivasi, semangat, serta doa yang selalu menyertai. Selain itu penulis juga mengucapkan terima kasih kepada teman-teman satu penelitian (Danah, Desi, Alvi), teman-teman satu bimbingan akademik (Arpha, Dara, Isma, Lina, Yasmin, dan Ardha), orang-orang terdekat (Wisnu, Gita, Astri, Fuji, Kenyo, Cholill, Nova, Ridwan, Dani, Arie, Dora, Rifqi, Sovie, Kak Winda, Wayan, Sri, Medina, Vidy) atas kebersamaan, dukungan, bantuan, serta semangatnya, serta keluarga besar GIANUZZI dan HKSA atas segala pertemanan dan pengalaman yang sangat berharga, serta semua pihak yang baik sengaja maupun tidak sengaja membantu penulis menyelesaikan skripsi ini.
Penulis menyadari bahwa penulisan skripsi ini masih jauh dari sempurna, karena itu penulis sangat berterima kasih dan terbuka untuk kritik dan saran yang membangun. Semoga karya ini bermanfaat bagi perkembangan ilmu pengetahuan.
Bogor, April2012
RIWAYAT HIDUP
Penulis dilahirkan di Jakarta pada tanggal 17 Desember 1989 dari ayah pasangan Nur Syamsu, SE. dan Evelyne Engelica, SE. Penulis merupakan anak tunggal.
Penulis memulai pendidikan di TK Ratna Kusuma pada tahun 1993-1995, kemudian penulis memulai pendidikan formal pada tahun 1995 di SD Kartika XI-2, Jakarta dan lulus pada tahun 2001. Pada tahun yang sama penulis melanjutkan pendidikan ke SMP Negeri 49 Jakarta dan lulus pada tahun 2004, kemudian melanjutkan pendidikan ke SMA Negeri 14 Jakarta dan lulus pada tahun 2007. Tahun 2007 penulis diterima di Fakultas Kedokteran Hewan, Institut Pertanian Bogor melalui jalur Seleksi Penerimaan Mahasiswa Baru (SPMB).
DAFTAR TABEL ... xii
Kasus Kandidiasis (Candidiasis) pada Ayam ... 8
Antibiotika dan Anticendawan dalam budidaya Ayam ... 10
Amfoterisin B ... 12
Waktu dan Tempat Penelitian ... 17
Bahan dan Alat ... 17
Metode ... 17
Pengambilan Contoh ... 17
Pengolahan Contoh ... 18
Pengamatan Terhadap Koloni C. albicans ... 18
Identifikasi Isolat C. albicans ... 18
Uji Kepekaan Anticendawan ... 19
Uji Penentuan Kadar Minimum Penghambatan (Minimum Inhibitory Concentration –MIC) ... 20
Analisis Data ... 21
BAB 4 HASIL DAN PEMBAHASAN ... 22
Lokasi Pemotongan Ayam ... 22
Identifikasi C. albicans ... 25
xi
BAB 5 SIMPULAN DAN SARAN ... 36
Simpulan ... 36
Saran ... 36
DAFTAR PUSTAKA ... 37
Halaman
1 Obat anticendawan yang digunakan pada unggas dan burung ... 12 2 Lokasi dan jumlah pengambilan contoh ... 25 3 Hasil uji kecambah dan asimilasi gula-gula terhadap koloni yang diduga C.
albicans ... 27 4 Koloni khamir yang berhasil ditumbuhkan dari contoh yang diperiksa ... 28 5 Nilai MIC terhadap beberapa isolat C. albicans yang diperoleh dari contoh
yang diperiksa ... 31 6 Nilai MIC terhadap beberapa isolat C. albicans dari contoh yang diperiksa
DAFTAR GAMBAR
Halaman
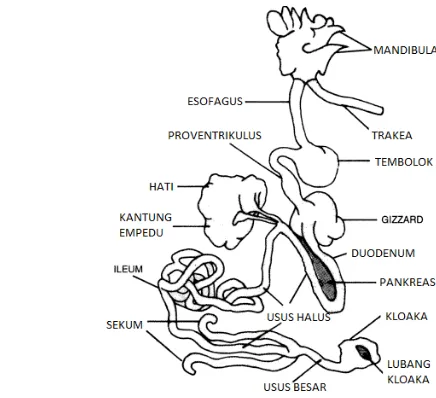
1 Anatomi saluran pencernaan ayam ... 6
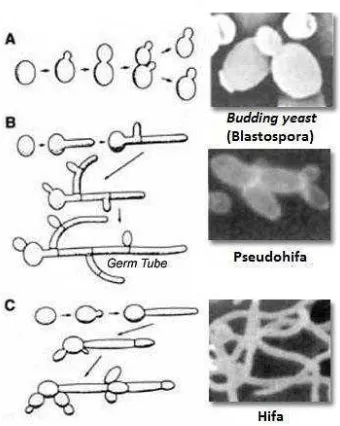
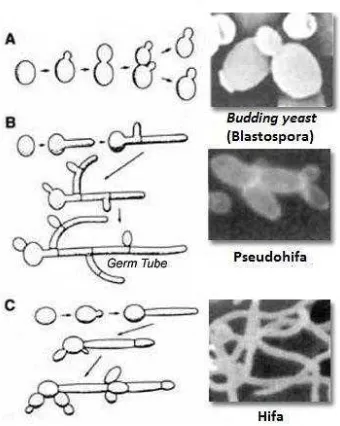
2 Fase C. albicans ... 8
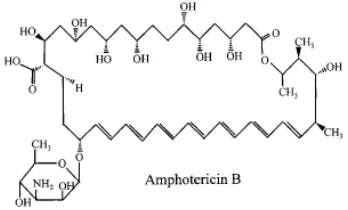
3 Struktur kimia pembentuk amfoterisin B ... 13
4 Struktur kimia pembentuk flukonazol ... 13
5 TPU Jambu Raya ... 23
6 (a) Salah satu tembolok yang dijadikan contoh ... 24
(b) Salah satu potongan usus yang dijadikan contoh ... 24
7 Hasil pemeriksaan natif yang diwarnai dengan LPCB memperlihatkan C. albicans dalam bentuk sel khamir (blastospora) yang membentuk tunas (budding yeast) ... 26
8 Tabung kecambah yang dibentuk oleh koloni yang diduga sebagai C. albicans ... 27
Halaman
1 Hasil analisis statistika MIC ketokonazol terhadap C. albicans berdasarkan lokasi menggunakan perangkat lunak SAS ... 42 2 Hasil analisis statistika MIC itrakonazol terhadap C. albicans berdasarkan
lokasi menggunakan perangkat lunak SAS ... 44 3 Hasil analisis statistika MIC griseofulvin terhadap C. albicans berdasarkan
lokasi menggunakan perangkat lunak SAS ... 46 4 Hasil analisis statistika MIC ketokonazol terhadap C. albicans berdasarkan
contoh yang diperiksa menggunakan perangkat lunak SAS... 48 5 Hasil analisis statistika MIC itrakonazol terhadap C. albicans berdasarkan
contoh yang diperiksa menggunakan perangkat lunak SAS... 50 6 Hasil analisis statistika MIC griseofulvin terhadap C. albicans berdasarkan
contoh yang diperiksa menggunakan perangkat lunak SAS ... 52 7 Hasil analisis statistika perbandingan nilai MIC antar anticendawan
BAB 1
PENDAHULUAN
Latar Belakang
Daging ayam merupakan salah satu bahan makanan utama mayoritas
masyarakat Indonesia. Hal ini disebabkan oleh karena harga daging ayam dapat
dijangkau oleh masyarakat luas. Daging ayam mengandung protein yang tinggi
serta berlemak rendah. Murtidjo (2003) memaparkan bahwa daging ayam juga
memiliki tekstur yang lebih halus dan lebih lunak jika dibandingkan dengan
dagingsapi dan ternak lain sehingga lebih mudah dicerna. Namun, sebelum
mendapatkan mutu daging ayam yang baik dan layak untuk dimakan oleh
masyarakat, perlu diperhatikan faktor-faktor yang mempengaruhi mutu daging
ayam tersebut. Beberapa faktor yang berpengaruh dalam budidaya ayam
pedaging komersil diantaranyapengelolaan pemeliharaan, pemberian pakan,
pencegahan dan penanggulangan terhadap penyakit, pengangkutan, pemotongan,
dan faktor-faktor lain.
Pakan merupakan faktor yang berperan sangat besar dalam keberhasilan
suatu usaha budidaya ayam. Menurut Ahmad (2009), pakan merupakan sumber nutrisi utama bagi ternak. Komponen utama penyusun pakan adalah biji-bijian seperti jagung. Biji-bijian umumnya mengandung air, karbohidrat, protein termasuk enzim, lemak, mineral, dan vitamin sehingga bahan pakan tersebut mudah tercemari cendawan. Bahan pakan lainnya yang biasa digunakan sebagai penyusun ransum adalah bungkil kedelai, tepung tulang, dedak, polar putih, bungkil kelapa, garam, vitamin, mineral, antelmintik, pemacu pertumbuhan, dan tepung ikan. Pakan yang baik mempunyai kandungan nutrisi yang sesuai dengan kebutuhan ternak, palabilitas tinggi, imbuhan pakan tepat, dan bebas dari cemaran mikroba patogen.
menyerang saluran pencernaan terutama tembolok, dan kadang-kadang rongga mulut, esofagus, dan proventrikulus.
Candida merupakan salah satu khamir yang secara normal berada di
sistem pencernaan manusia dan hewan yang sehat. Namun, jika khamir ini
terdapat dalam tubuh dalam jumlah yang banyak dapat menyebabkan penyakit
yang disebut kandidiasis (Candidiasis). Penyakit ini mungkin saja menyerang ternak ayam yang diakibatkan oleh sanitasi peternakan yang sangat buruk atau akibat ayam sering diberi antibiotika terus-menerus (Fadilah dan Polana 2004). Berdasarkan penelitian yang dilakukan oleh Hastiono (1987), pemberian antibiotika ke dalam pakan sebagai imbuhan pakan (feed additive)dapat merangsang pertumbuhan dan meningkatkan jumlah khamir secara sangat nyata dalam tembolok ayam pedaging. Hal ini disebabkan oleh adanya kemampuan khamir menggunakan antibiotika untuk merangsang pertumbuhannya.
Selain antibiotika, anticendawan juga merupakan salah satu bahan tambahan yang dicampurkan ke dalam pakan ayam. Salah satu contoh anticendawan yang biasa ditambahkan dalam pakan adalah nistatin. Menurut Tabbu (2000), pemberian nistatin dalam pakan ayam dapat menurunkan jumlah
Candida dalam saluran pencernaan ayam sehingga dapat mencegah terjadinya kandidiasis. Selain itu, Fadilah dan Polana (2004) juga memaparkan bahwa pemberian nistatin pada pakan juga dapat mencegah serta menekan terjadinya kasus aspergillosis. Maka dari itu, pemberian anticendawan secara berkala dipercaya dapat menurunkan jumlah kasus mikosis.
3
Tujuan
Penelitian ini bertujuan untuk mendapatkan informasi mengenai spesies C.
albicans yang berada di pasar tradisional dan tempat pemotongan ayam yang
tahan terhadap obat-obatanticendawan.
Hipotesis
H0 : Ada beberapa spesies C. albicans dari pasar tradisional dan tempat
pemotongan ayam yang tahan terhadap obat-obatanticendawan
H1 : Tidak ditemukan spesies C. albicans dari pasar tradisional dan
tempat pemotongan ayam yang tahan terhadap
Ayam Pedaging
Ayam umumnya dapat menghasilkan daging maupun telur. Istilah
“pedaging” yang diperoleh ayam pedaging dapat diberikan kepada seluruh jenis ayam yang dapat memproduksi daging. Namun Rasyaf (2008) mendefinisikan
ayam pedaging sebagai ayam jantan dan ayam betina yang berumur di bawah
delapan minggu dan ketika dijual memiliki bobot tubuh tertentu, mempunyai
pertumbuhan yang cepat, serta mempunyai dada yang lebar, serta mempunyai
timbunan daging yang baik dan banyak. Pengertian ini menyebabkan ayam ras
pedaging lebih identik sebagai ayam pedaging jika dibandingkan dengan ayam
buras. Namun di Indonesia, salah satu ayam buras, yaitu ayam buras, juga banyak
digunakan sebagai ayam yang dijadikan bahan makanan,terutama di daerah
pedesaan yang umumnya memelihara ayam.
Ayam ras pedaging adalah ayam hasil rekayasa genetik yang memiliki
karakteristik ekonomis. Ayam ini memiliki pertumbuhan yang sangat cepat, angka
konversi pakan yang rendah, siap dipotong saat berumur relatif muda, dan
menghasilkan daging berserat lunak. Biasanya ayam ini dipasarkan saat berumur
6–8 minggu. Umumnya ayam jantan menunjukkan pertumbuhan lebih cepat 10–
15% dengan efisiensi penggunaan pakan yang lebih baik dan persentase
karkasnya lebih besar (Murhananto dan Purbani 2008)
Ayam ras pedaging memiliki beberapa sifat, antara lain mempunyai sifat
dan mutu daging yang baik (meatness), laju pertumbuhan dan bobot badan (rate
of gain) tinggi, warna kulit kuning, konversi pakan rendah, bebas dari
kanibalisme, sehat dan kuat, kaki tidak mudah bengkok, tidak temperamental dan
cenderung malas dengan gerakan lamban, daya hidup tinggi (95%) tetapi tingkat
kematian rendah, serta kemampuan membentuk karkas tinggi (Yuwanta 2004).
Namun Murhananto dan Purbani (2008) menyatakan bahwa ayam ras pedaging
tergolong hewan yang mudah stres sehingga pemeliharaannya harus dilakukan di
tempat yang tenang dan agak jauh dari pusat-pusat keramaian. Ayam ini juga
5
Ayam buras (bukan ras) merupakan jenis ayam yang banyak dipelihara
oleh masyarakat di Indonesia, terutama di daerah pedesaan. Ayam buras yang
biasa digunakan untuk bahan makanan dikenal sebagai ayam buras. Ayam ini
merupakan ayam jinak yang telah terbiasa hidup di tengah masyarakat, memiliki
daya adaptasi ayam ini sangat tinggi, karena mampu menyesuaikan diri dengan
berbagai situasi, lingkungan, dan iklim yang ada (Sarwono 2003).
Menurut Nuroso (2010), pemeliharaan ayam buras sangat mudah karena
tahan terhadap kondisi lingkungan dan pengelolaan yang buruk, tidak
memerlukan lahan yang luas dan dapat dipelihara di lahan sekitar rumah, harga
jualnya stabil dan relatif lebih tinggi dibandingkan dengan ayam pedaging lain,
serta tidak mudah stres terhadap perlakuan yang kasar dan daya tahan tubuhnya
lebih kuat dibandingkan dengan ayam pedaging lainnya. Namun, Cahyono (1996)
mengungkapkan bahwa ayam ini memiliki kelemahan jika dibandingkan dengan
memelihara ayam ras pedaging, yaitu umumnya bertubuh kecil, memiliki
pertumbuhan yang lambat, produksi telur yang rendah dan berukuran kecil, serta
memiliki daya alih (konversi) pakan menjadi produk protein (daging) yang rendah
dibanding dengan ayam ras.
Saluran Pencernaan Ayam
Sistem pencernaan unggas berbeda dengan sistem pencernaan pada hewan
lainnya. Unggas tidak memiliki gigi sehingga tidak terjadi proses pengunyahan
pakan. Pakan akan melewati esofagus dan langsung menuju tembolok. Pakan di
dalam tembolok akan mendapatkan sekreta mukus yang berfungsi untuk
menghaluskan pakan. Setelah melewati tembolok, pakan menuju lambung
kelenjar (proventrikulus) yang merupakan organ berdinding tebal dan berada di
depan lambung otot (gizzard). Pakan disimpan secara sementara di proventrikulus
dan dicampur dengan enzim pepsin dan amilase yang dihasilkan oleh organ
tersebut. Setelah itu, pakan masuk ke lambung otot, yang merupakan organ
tersusun dari otot yang kuat, yang berisi bebatuan atau pasir, dan di dalamnya
pakan akan dihancurkan. Pakan kemudian berpindah menuju usus halus, sekum
cepat karena membutuhkan waktu cerna hanya 2½ jam pada ayam petelur dan
8-12 jam pada ayam lain (Scanes et al. 2004).
Gambar 1 Anatomi saluran pencernaan ayam (Bell 2002)
Tembolok adalah modifikasi dari esofagus. Fungsi utama dari organ ini
adalah untuk menyimpan pakan sementara, terutama pada saat ayam makan dalam
jumlah banyak. Bolus berada di tembolok selama dua jam.
Kapasitas tembolok mampu menampung pakan 250 g. Pada tembolok
terdapat saraf yang berhubungan dengan pusat kenyang-lapar di hipotalamus
sehingga banyak sedikitnya pakan yang terdapat dalam tembolok akan
memberikan respon pada saraf untuk makan atau menghentikan makan (Yuwanta
2004).
Tembolok mensekresikan mukus yang berfungsi sebagai cairan lubrikasi
yang dapat menghaluskan pakan. Jika ayam lapar, pakan akan melewati tembolok
dan menuju langsung ke proventrikulus dan lambung otot. Selama proses
memakan, tembolok mulai terisi dan bertindak sebagai organ penyimpanan
(Scanes et al. 2004).
Usus besar, atau kolon, pada unggas tergolong pendek dan mempunyai
struktur yang mirip dengan usus halus. Usus besar dianggap tidak memiliki
peranan yang nyata dalam proses pencernaan dan penyerapan.
Sekum merupakan organ berbentuk tabung yang buntu pada perbatasan
7
sekum yang besar, sedangkan pada tipe unggas lainnya hanya terdapat satu
kantung rudimenter bahkan terdapat beberapa unggas yang tidak memiliki sekum
sama sekali (Scanes et al. 2004).
C. albicans
C. albicans adalah khamir komensal (normal) di mukosa mulut, saluran
pencernaan dan vagina. Namun, khamir ini bisa menjadi masalah bila fase
pertumbuhannya berubah dari fase khamir ke fase kapang ketika berada di
membran mukosa inang. Kejadian ini biasa disebut kandidiasis (Berman dan
Sudbery 2002).
Blastospora (sel khamir) berbentuk bulat sampai oval dan selnya terpisah
satu sama lain. Selain blastospora, C. albicans juga dapat membentuk hifa sejati
dan pseudohifa. Hifa sejati adalah sel yang panjang dan berkutub dengan sisi yang
pararel tanpa ada batas yang jelas. Pseudohifa adalah sel khamir berbentuk
elipsoida yang tetap menempel satu sama lain dan dibatasi oleh septa. Perbedaan
antara hifa sejati dan pseudohifa adalah hifa sejati terbentuk dari blastospora dan
cabang dari hifa sejati lain, sedangkan pseudohifa terbentuk dari blastospora atau
pertunasan dari hifa dan sel baru tersebut tetap menempel pada sel induknya dan
tetap menjulur (Calderone 2002). Fase-fase yang dapat dibentuk oleh C. albicans
ditunjukkan pada Gambar 2 di bawah ini.
Perubahan bentuk C. albicans dari khamir ke kapang bisa terjadi karena
pengaruh berbagai macam faktor lingkungan, antara lain perubahan dari
komposisi media, penambahan serum, tumbuh pada kondisi kadar CO2 yang
tinggi atau semi anaerobik, pH dan suhu. Suhu dan pH yang optimal bagi
blastospora C. albicans berubah menjadi hifa adalah lebih dari 35oC dan 6,5-7,0
atau mendekati suasana basa. C. albicans juga dapat membentuk khlamidospora.
Khlamidiospora merupakan berntuk pertahanan yang dibentuk pada kondisi
Gambar 2 Fase pada C. albicans (Anonim 2010)
Menurut Sen dan Baksi (2009), klasifikasi C. albicans adalah sebagai
berikut:
Kingdom : Fungi
Filum : Ascomycota
Subfilum : Ascomycotina
Kelas : Ascomycetes
Ordo : Saccharomycetales
Famili : Saccharomycetaceae
Genus : Candida
Spesies : C. albicans
Kasus Kandidiasis (Candidiasis) pada Ayam
Candidadapat menyebabkan kandidiasis pada ayam. Kondisi yang dapat
memacu terjadinya kandidiasis antara lain adalah umur ayam. Ayam yang lebih
muda umumnya lebih rentan terhadap penyakit ini. Sanitasi kandang ataupun
peralatan, kondisi kandang dengan populasi yang padat, serta timbulnya cekaman
merupakan faktor-faktor lain yang dapat memicu terjadinya kandidiasis. Di
Indonesia, penyakit ini dapat dijumpai pada berbagai peternakan ayam komersial
yang tersebar di berbagai daerah. Penyakit tersebut kerapkali ditemukan juga pada
9
mempunyai tingkat sanitasi yang kurang memadai. Penyakit ini dapat ditemukan
pada berbagai jenis unggas pada semua tingkatan umur, terutama ayam, kalkun,
burung merpati, burung merak, burung puyuh, dan angsa. Manusia dan hewan
peliharaan juga peka terhadap kandidiasis. Faktor pendukung kejadian kandidiasis
adalah tingkat higienis dan sanitasi yang tidak memadai, penggunaan antibiotika
yang berlebihan, penurunan kondisi tubuh/kelemahan umum, dan berbagai
cekaman, misalnya kepadatan kandang yang tinggi dan defisiensi nutrisi (Tabbu
2000;Janmaat dan Morton 2010).
C. albicans merupakan spesies utama penyebab kandidiasis, meskipun
spesies Candida non-albicans juga telah diisolasi dari unggas sehat maupun sakit.
Dalam survei terhadap tembolok yang berasal dari ayam ras pedaging, 95% dari
isolat terdiri atas C. albicans, dan sisanya diidentifikasikan sebagai C. ravautii, C.
salmonicola, C. guilliermondii, C. parapsilosis, C. catenulata, atau C. brumptii.
Berdasarkan hasil penelitian, hanya C. albicans dan C. parapsilosis yang
berhubungan dengan kasus mikosis pada tembolok. Berdasarkan hasil isolasi dari
kalkun yang terjangkit candidiasis, terdeteksi C. albicans, C. rugosa, C. famata,
C. tropicalis, dan C. guilliermondii dengan hanya C. rugosa yang terisolasi dari
beberapa tembolok yang terinfeksi (Kunkle 2003).
Menurut Butcher dan Miles (2009), gejala klinis dari ayam yang menderita
kandidiasis berupa hilangnya berat badan, terjadi muntah secara berkala, dan
terlihat lesu. Gejala lain adalah menurunnya laju pertumbuhan pada ayam muda,
diare, dan terhambatnya pengosongan dan perbesaran tembolok. Selain gejala
klinis di atas, gejala lain yang biasanya muncul adalah terjadinya lesio di mulut
berupa peradangan kaseosa pada mulut. Lesio ini serupa dengan lesio pada
defisiensi vitamin A dan lesio proliferasi pada avian pox bentuk basah. Pada tahap
yang lebih parah, lesio pada mulut menjadi obstruktif dan dapat mengganggu
respirasi dan pencernaan, sehingga menyebabkan kelesuan dan terhambatnya
pertumbuhan serta penambahan bobot badan.
Tingginya kasus kandidiasis pada tembolok dikarenakan fungsi tembolok
sebagai tempat untuk menampung pakan sementara. Sisa-sisa pakan, terutama
spora jamur yang mencemari pakan, akan bertahan lama di dalam tembolok,
Kandidiasis tidak menular dari ayam satu ke ayam lainnya. Penyakit ini
dapat menular melalui oral karena memakan pakan atau meminum air minum atau
karena kontak dengan bahan/lingkungan yang tercemar oleh khamir tersebut.
Penyakit ini dapat menular dengan mudah melalui air minum yang kotor yang
tercemar oleh C. albicans (Tabbu 2000).
Antibiotika dan Anticendawan dalam Budidaya Ayam
Imbuhan pakan (feed additive) sering digunakan dalam pakan untuk
merangsang pertumbuhan dan kinerja ayam, seperti menghasilkan telur,
memperbaiki efisiensi pakan, dan berguna untuk memberikan pengendalian
terhadap kesehatan atau metabolisme ternak. Salah satu bahan yang sering
digunakan sebagai pakan tambahan adalah antibiotika (Scanes et al.
2004).Berdasarkan pengamatan yang dilakukan oleh Bahri et al. (2005), hampir semua pabrik pakan menambahkan obat hewan berupa antibiotika ke dalam pakan komersial, sehingga sebagian besar pakan komersial yang beredar di Indonesia mengandung antibiotika.
Menurut Windisch et al. (2008), antibiotika digolongkan sebagai feed
additive, karena tidak termasuk dalam kategori pakan meskipun dalam peternakan
ayam memiliki peranan penting dalam merangsang pertumbuhan dan
memperbaiki efisiensi penggunaan pakan. Antibiotika ini sanggup menekan
pertumbuhan mikroorganisme yang menyebabkan penyakitterutama bakteri
patogen sehingga absorpsi nutrisi dalam sistem pencernaan. Selain itu, pemberian
antibiotika ke dalam pakan juga memiliki dampak negatifkarena dapat
menimbulkan resistensi terhadap antibiotika.
Menurut Murtidjo (1987),penggunaan aureomisin (khlortetrasiklin),
teramisin (oksitetrasiklin) dan penisilin yang dicampurkan dalam pakan ternak
unggas berpengaruh merangsang pertumbuhan yang baik dibandingkan dengan
ternak unggas yang memakan pakan tanpa dicampur antibiotika. Sedangkan
antibiotika seperti basitrasin, streptomisin, dan lainnya tidak dapat dipergunakan
karena berpengaruh buruk.
Pemberian CO2, kedap udara, fumigan (fosfin/PH3)dan metil bromida pada
11
Sedangkan untuk mencegah terjadinya timbulnya penyakit yang disebabkan oleh kapang ataupun khamir dapat dilakukan dengan pemberian nistatin melalui pakan (Ahmad 2009; Tabbu 2000)
Penggunaan antibiotika sebagai feed additive di Eropa dalam upaya untuk
meningkatkan produksi hewan telah dilarang. Namun, antibiotika ionofor masih
dipergunakan sebagai feed additive untuk mengontrol koksidiosis, meskipun
dalam aplikasinya juga dipergunakan sebagai pemacu pertumbuhan (Elwinger et
al. 1998). Menurut Hastiono (1987), antibiotika juga dapat menyebabkan jumlah
khamir, terutama khamir yang bersifat patogen, meningkat secara sangat nyata
dalam tembolok ayam pedaging. Keberadaan khamir yang terlacak di dalam
penelitian tersebut diantaranya C. albicans, C. guillermondii, C. krusei, C.
parapsilopsis, C. pseudotropicalis, C. tropicalis, Geotrichum sp., Rhodotula sp.,
Saccharomyces sp., Torulopsis sp., dan Trichosporon sp.Peningkatan jumlah
khamir oleh pemberian antibiotika ini terjadi karena khamir mempunyai
kemampuan menggunakan antibiotika, dalam hal ini penisilin dan tetrasiklin,
sebagai sumber nitrogen bagi pertumbuhannya.Selain itu, antibiotika juga
membunuh bakteri yang berfungsi untuk menyaingi khamir dalam memperoleh
zat-zat hara serta mengurangi ataupun menghilangkan jasad yang menghasilkan
bahan-bahan anticendawan.
Menurut Rochette et al. (2003), sejumlah anticendawan yang digunakan
untuk mengobati kandidiasis pada unggas adalah amfoterisin B (amphotericin B),
flukonazol (fluconazole), itrakonazol (itraconazole), ketokonazol (ketoconazole),
mikonazol (miconazole), nystatin (nystatin), dan parkonazol (parconazole) seperti
yang tercantum pada Tabel 1.
Dun (1999) mengungkapkan bahwa sejak diperkenalkannya anticendawan
golongan azol, sediaan ini lebih dipilih penggunaannya untuk mengobati infeksi
akibat Candida. Hal ini disebabkan karena terapi dan pengobatan dengan
menggunakan sediaan anticendawan dari golongan azol menghasilkan efek
samping yang lebih sedikit dan mengeliminasi cendawan sama baiknya dengan
Tabel 1 Obat anticendawan yang digunakan pada unggas dan burung (Rochette et
al. 2003)
Anticendawan Rute penggunaan Untuk infeksi oleh
Amfoterisin B Injectable lotions 3%, i.v.,
intratrakeal, nebulisasi
Aspergillus, Candida
Klotrimazol Nebulisasi Aspergillus
Flukonazol Oral (sediaan tablet, cair) Candida sistemik
Flusitosin Oral Aspergillus
Enilkonazol Spray Aspergillus pada mesin penetas
Itrakonazol Oral, sediaan di dalam
kapsul
Aspergillus, Candida
Ketokonazol Oral (tablet) Candida (Aspergillus)
Mikonazol Nebulisasi Aspergillus
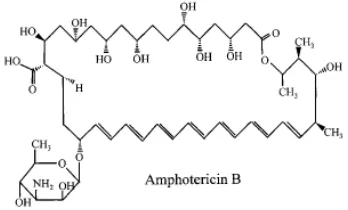
Parkonazol Bubuk di dalam pakan Candida (trush) pada ayam
mutiara
Tiabendazol Smoke tablet Aspergillus
Amfoterisin B
Amfoterisin A dan B merupakan hasil fermentasi oleh Streptomyces
nodosus. Amfoterisin B menyerang sel yang sedang tumbuh dan sel dewasa.
Antibiotika ini bersifat fungistatik atau fungisidal tergantung dari dosis dan
kepekaan cendawan yang dipengaruhi. Aktivitas anticendawan ini sangat terlihat
nyata pada pH 6,0-7,5 dan berkurang pada pH yang lebih rendah.
Mekanisme kerja amfoterisin B adalah dengan cara berikatan kuat dengan
sterol yang terdapat pada membran sel cendawan. Ikatan ini akan menyebabkan
membran sel bocor sehingga terjadi kehilangan beberpa bahan intrasel dan
mengakibatkan kerusakan yang permanen pada sel (Bahry dan Setiabudy 1995).
Amfoterisin B telah digunakan untuk mengobati infeksi cendawan baik
secara sistemik maupun topikal pada unggas. Formulasi intravena telah diberikan
dengan rute injeksi secara intravena, melalui trakea menggunakan kateter, atau
diinjeksikan ke kantung hawa yang terinfeksi. Formulasi intravena juga digunakan
melalui nebulisasi pada burung berparuh bengkok(psittacines) dan burung
13
Gambar 3 Struktur kimia pembentuk amfoterisin B (Ghannoum dan Rice 1999)
Flukonazol
Flukonazol adalah turunan dari triazol dan bersifat fungistatik. Gugus
derivat triazol, seperti imidazol (kloritomazol, ketokonazol, dll.), mempunyai
mekanisme kerja mengubah membran sel cendawan yang mempunyai kepekaan
terhadap anticendawan tersebut, sehingga meningkatkan permeabilitas dan
membiarkan komponen di dalam sel bocor dan mengganggu ikatan prekusor purin
dan pirimidin (Plumb 1999)
Flukonazol merupakan obat yang dapat diserap sempurna melalui saluran
cerna tanpa dipengaruhi adanya pakan ataupun keasaman lambung. Oleh karena
itu, flukonazol dikatakan ditoleransi dengan baik. Efek samping yang sering
ditemukan akibat penggunaan flukonazol adalah gangguan saluran pencernaan
(Bahry dan Setiabudy 1995).
Gambar 4 Struktur kimia pembentuk flukonazol (Ghannoum dan Rice 1999)
Berdasarkan penelitian Dun (1999) yang membandingkan efikasi
flukonazol dengan amfoterisin B dalam morbiditas dan mortalitas pada pasien
yang mengalami kandidiasis, menunjukkan bahwa flukonazol sama efektifnya
dengan amfoterisin dalam mengobati infeksi Candida sistemik. Selain itu, secara
nyata flukonazol juga memberikan efek samping yang jauh lebih sedikit
Itrakonazol
Itrakonazol merupakan anticendawan sistemik turunan triazol yang erat
hubungannya dengan ketokonazol dan dapat diberikan secara peroral. Aktivitas
anticendawannya diduga lebih luas sedangkan efek samping yang ditimbulkan
lebih kecil dibandingkan dengan ketokonazol. Itrakonazol dapat diserap lebih
sempurna bila diberikan bersama pakan (BahrydanSetiabudy 1995).
Penyerapan itrakonazol sangat bergantung pada pH lambung dan
kehadiran pakan. Bioavabilitas itrakonazol hanya mencapai 50% atau kurang
ketika diberikan saat lambung kosong. Bioavabilitas akan mencapai 100%jika di
dalam lambung terdapat pakan. Itrakonazol mampu mengikat protein dan
disalurkan ke seluruh tubuh, terutama ke dalam jaringan yang memiliki
kandungan lemak yang tinggi karena obat ini bersifat lipofilik (Plumb 1999).
Ketokonazol
Ketokonazol digunakan untuk infeksi khamir sistemik maupun lokal.
Pengobatan dengan menggunakan ketokonazol secara peroral mencegah dan
mengobati kandidiasis pada tembolok di kalkun. Anticendawan ini juga efektif
untuk melawan kandidiasis di ayam (Roschette et al. 2003).
Ketokonazol merupakan anticendawan sistemik peroral yang diserap baik
melalui saluran pencernaan dan menghasilkan kadar plasma yang cukup untuk
menekan aktivitas berbagai jenis cendawan. Sebanyak 84% ketokonazol di dalam
plasma darah berikatan dengan protein plasma, terutama albumin. Lima belas
persen berikatan dengan sel darah dan 1% dalam bentuk bebas. Sebagian besar
dari obat ini mengalami metabolisme lintas pertama (Bahry dan Setiabudy 1995).
Menurut Plumb (1999), ketokonazol berifat fungistatik terhadap cendawan
yang peka. Pada kadar yang lebih tinggi untuk periode yang lama atau pada
organisme yang sangat peka, ketokonazol dapat bersifat fungisidal. Ketokonazol
dipercaya dapat meningkatkan permeabilitas membran sel dan menyebabkan efek
metabolis sekunder dan menghambat pertumbuhan cendawan. Mekanisme kerja
secara pasti dari ketokonazol tidak diketahui. Kemungkinan karena ketokonazol
bekerja melalui sintesis ergosterol. Aktifitas fungisidal dari ketokonazol mungkin
15
Pemberian ketokonazol pada pakan unggas diberikan pada pakan atau air
minum. Pada air minum,dosis yang diberikan adalah 200mg/L untuk 7-14 hari
pada pH normal. Sedangkan pada pakan, dosis yang diberikan adalah 10-20
mg/kg untuk 7-14 hari dengan cara dimasukkan langsung ke dalam pakan atau
dihancurkan (Plumb 1999).
Mikonazol
Mikonazol merupakan turunan imidazol sintetik yang relatif stabil,
mempunyai spektrum anticendawan yang luas baik terhadap jamur sistemik
maupun cendawan dermatofita. Mekanisme kerja obat ini belum diketahui
sepenuhnya. Mikonazol menghambat sintesis ergosterol yang menyebabkan
permeabilitas membran sel jamur meningkat. Mungkin pula terjadi gangguan
sintesis asam nukleat atau penimbunan peroksida dalam sel cendawan yang akan
menimbulkan kerusakan (Bahry dan Setiabudy 1995).
Nistatin
Nistatin merupakan suatu antibiotika polien yang dihasilkan oleh
Streptomyces noursel. Nistatin bekerja dengan cara menghambat pertumbuhan
berbagai cendawan dan ragi, tetapi tidak aktif terhadap bakteri, protozoa dan
virus. Anticendawan ini hanya efektif pada berbagai macam jenis cendawan,
namun secara klinis digunakan untuk mengobati infeksi Candida topikal,
osofaringeal, dan gastrointestinal. Nistatin mempunyai mekanisme kerja yang
sama dengan amfoterisin B. Nistatin hanya akan diikat oleh khamir atau kapang
yang sensitif. Aktivitas anticendawan tergantung dari adanya ikatan dengan sterol
pada membran sel kapang atau khamir, terutama ergosterol. Akibat terbentuknya
ikatan antara sterol dengan anticendawan ini adalah terjadinya perubahan
permeabilitas membran sel sehingga sel akan kehilangan berbagai molekul kecil.
C. albicans hampir tidak memperlihatkan resistensi terhadap nistatin (Bahry dan
Parkonazol
Parkonazol digunakan untuk mengobati kandidiasis di ayam mutiara.
Parkonazol mempunyai toksisitas yang renndah dan residu daily intake di bawah
ADI (acceptable daily intake), meskipun telah diberikan setelah 24 jam
BAB 3
METODE PENELITIAN
Waktu dan Tempat Penelitian
Penelitian ini dilakukan sejak bulan Mei 2011 sampai dengan bulan
Desember 2011. Kegiatan ini dilakukan di laboratorium Bagian Mikrobiologi
Medik Departemen Ilmu Penyakit Hewan dan Kesehatan Masyarakat Veteriner,
Fakultas Kedokteran Hewan, Institut Pertanian Bogor.
Bahan dan Alat
Alat yang digunakan dalam penelitian ini adalah gelas objek, kaca
penutup, mikroskop, cawan petri, tabung reaksi, rak tabung reaksi, öse, bunsen,
inkubator, ice box, pinset, vortex, cotton swab, mikropipet, tabung Durhamdan
pipet.
Bahan yang digunakan antara lain tembolok ayam, contoh air yang
digunakan sebagai sumber air bersih dan limbah hasil pencucian, potongan usus
besar, Lactophenol Cotton Blue (LPCB), Potatoes Dextrose Agar (PDA), putih
telur bebek, larutan NaCl, air suling sucihama, antibiotika (kloramfenikol), larutan
Potatoes Dextrose Broth (PDB)dan anticendawan (itrakonazol, ketokonazol, dan
griseofulvin)
Metode
Pengambilan Contoh
Contoh pemeriksaan yang digunakan dalam penelitian adalah tembolok
dan potongan usus besar ayam pedaging ras dan ayam bukan ras (ayam buras), air
bersih yang digunakan untuk pencucian karkas, sertalimbah air hasil pencucian di
pasar tradisional Pasar Gunung Batu, Pasar Anyar, dan Pasar Warung Jambu dan
tempat pemotongan unggas (TPU) Jambu Raya, TPU Pondok Rumput, dan RPH
Pengolahan Contoh
Pengolahan contoh dilakukan berdasarkan metode yang dilakukan oleh
Hastiono (1987) yang mengacu pada Thompson (1969). Contoh diproses di ruang
inokulasi. Pengolahan tiap-tiap tembolok dilakukan secara “dilution plating”
(pengolahan bahan pemeriksaan ke dalam cawan-cawan petri yang mengandung
medium perbiakan dengan pengenceran secara bertingkat). Tahapan-tahapan
yang dilakukan adalah
(a) tembolok, potongan usus, air bersih untuk pencucian karkas, dan air limbah
hasil pencucian dimasukkan ke dalam kantung plastik kosong sucihama
berkode lengkap. Sebanyak 1 g potongan usus dan tembolok, serta 1 mL air
bersih untuk pencucian karkas dan air limbah hasil pencucian kemudian
dibubuhi larutan NaCl fisiologis yang sucihama sebanyak sembilan kali bobot
potongan tembolok sehingga diperoleh pengenceran 1/10;
(b) masing-masing contoh yang telah dimasukkan ke dalam larutan NaCl
dihomogenisasikan dengan menggunakan vortexdan cairan suspensi yang
dihasilkan dimasukkan ke dalam cawan petri masing-masing sebanyak 1,0
mL dan 0,1mL agar didapatkan pengenceran 1:10 dan 1:100;
(c) cawan-cawan yang telah terisi suspensi kemudian di tuangi media PDA yang
telah dicairkan dan telah ditambahkan antibiotika kloromfenikol 0,05 mg/mL
medium, dihomogenkan sampai bercampur dan dibiarkan membeku. Media
yang sudah diolah ini lalu diinkubasi di dalam inkubator pada suhu 37 oC
selama 48 jam.
Pengamatan Terhadap Koloni C. albicans
Koloni yang tumbuh pada pembiakan PDA diamati warna, bentuk, dan
baunya. Kemudian secara mikroskopik diperhatikan ukuran dan bentuk selnya,
ada tidaknya miselium, kapsul dan ciri-ciri morfologik yang lain (Hastiono 1987)
Identifikasi isolat C. albicans
Identifikasi isolat C. albicans dilakukan menurut cara Al-Doory (1980).
Pengidentifikasian isolat pertama kali dilakukan dengan cara pemeriksaan natif.
19
tembolok, usus besar, air limbah maupun air bersih yang digunakan untuk
membersihkan daging ayam dan diteteskan dengan pewarna LPCB diatas gelas
objek,ditutup dengan kaca penutup dan diperiksa dengan mikroskop.
Tahap selanjutnya adalah dilakukan inokulasi pada suhu 37ºC. Hal ini
dilakukan untuk memastikan apakah isolat tersebut patogen atau tidak. Isolat
murni diinokulasikan kembali ke dalam media PDA baru, lalu dinkubasikan pada
suhu 37 oC.
Uji tabung-kecambah (germ tube test) dilakukan untuk mengidentifikasi
spesies dari Candida yang telah diisolasi. Jika terbentuk tabung kecambah, maka
biakan tersebut kemungkinan adalah C. albicans atau C. stellaoidea. Uji ini
dilakukan dengan cara biakan murni berumur 24 jam dibiakkan ke dalam 0,5 mL
putih telur bebek dan kemudian diinkubasikan pada suhu 37oC selama 2-4 jam.
Setelah dua jam, biakan diperiksa dengan mikroskop untuk mengetahui ada
tidaknya tabung kecambah.
Uji asimilasi gula-gula dilakukan untuk memastikan spesies isolat C.
albicans. Uji ini menggunakan tabung reaksi yang berisi media cair Sugar
assimilation medium yang terdiri dari glukosa, galaktosa, sukrosa, maltosa,
laktosa, dan manitol. Sedikit koloni khamir dipindahkan menggunakan öse atau
jarum ke dalam tabung reaksi yang di dalamnya terdapat 2mL air suling
sucihama, kemudian dilakukan pengadukan dengan menggunakan vortex hingga
merata. Suspensi khamir yang dihasilkan disamakan kepekatannya dengan larutan
McFarland #1. Sebanyak 0,2mL suspensi khamir dimasukkan ke tabung-tabung
gula-gula yang telah disiapkan. Tabung-tabung tersebut diinkubasi pada suhu
30ºC selama tujuh hari. Hasil positif ditandai dengan adanya pertumbuhan dan
terjadinya kekeruhan pada tabung jika dibandingkan dengan tabung kontrol
(tabung yang tidak diimbuhi dengan gula).
Uji Kepekaan Anticendawan
Uji pembentukan zona hambat dilakukan untuk melihat kepekaan isolat C.
albicans terhadap anticendawan yang digunakan. Metode yang digunakan dalam
penelitian ini berdasarkan metode yang digunakan oleh Kusumaningtyas et al.
Media disiapkan terlebih dahulu dengan cara menuangkan 20 mL PDA ke
dalam cawan Petri dan dibiarkan memadat. Masing-masing suspensi C.
albicans,yang setara dengan kandungan khamir sejumlah 106cfu/mL, kemudian
dioleskan secara merata pada permukaan media dengan menggunakan spatula atau
cotton swab. Setelah permukaan mengering, kurang lebih 20 menit, dibuatlah
lubang dengan diameter lima milimeter dan kedalaman 0,5 cm dengan
menggunakan tabung Durhamsucihama. Setiap lubang diisi dengan 25µL
anticendawan yang telah diencerkan dengan menggunakan mikropipet. Kemudian
diinkubasi selama 24 jam pada suhu 37◦C dan dilihat pembentukan zona
hambatnya. Anticendawan yang digunakan adalah ketokonazol dengan kadar
mulai dari 0,125 µg/mL, itrakonazol dengan kadar mulai dari 0,125 µg/mL, dan
griseofulvin dengan kadar mulai dari 0,25 µg/mL dan kadar masing-masing obat
terus dinaikkan sampai membentuk zona hambat pada masing-masing isolat.
Uji Penentuan Kadar Minimum Penghambatan (Minimum Inhibitory Concentration- MIC)
Tahap akhir dari tata kerja penelitian ini adalah dilakukan penentuan kadar
hambat minimum (minimum inhibition concentration,MIC). Uji ini digunakan
untuk mengetahui kadar terendah anticendawan yang dapat menghambat
pertumbuhan koloni khamir hingga 80% dari pertumbuhan koloni khamir. Uji ini
mengikuti teknik yang telah dilakukan oleh Espinel-Ingroff dan Cantón (2007).
Uji ini digunakan untuk mengetahui kadar terendah anticendawan yang
dapat menghambat pertumbuhan koloni C. albicansyang ada dalam tembolok dan
usus ayam maupun air bersih yang akan digunakan untuk mencuci karkas ayam
serta air limbah pencucian ayam.
Uji ini diawali dengan menempatkan koloni C. albicans umur 24 jam ke
tabung reaksi yang di dalamnya terdapat sembilan mililiter air suling
sucihama.Dilakukan pengadukan hingga menyatu. Suspensi C. albicans yang
dihasilkan disamakan kepekatannya dengan larutan McFarland #1 yang setara
dengan kandungan khamirsejumlah 108 CFU/mL. Kemudian,suspensi C.albicans
diencerkan dengan cara memindahkan sebanyak 1 mL larutan suspensi C.
albicans ke dalam 9 mL larutan PDB untuk menghasilkan larutan suspensi yang
21
dengan memindahkan suspensi yang telah dihasilkan tersebut sebanyak 1mL ke
dalam 9 mL larutan PDB untuk menghasilkan larutan suspensi yang mengandung
khamir sejumlah 106 CFU/mL. Setelah itu sebanyak 11,25 µL anticendawan yang
akan diujiditambahkan ke dalam suspensi khamir terakhir. Anticendawan yang
digunakan dalam penelitian ini adalah ketokonazol dengan kadar 8 µg/mL, 2
µg/mL, 0,5 µg/mL, dan 0,125 µg/mL; itrakonazol dengan kadar 16 µg/mL, 4
µg/mL, 0,5 µg/mL, dan 0,125 µg/mL; serta griseofulvin dengan kadar 128µg/mL,
16µg/mL, 2 µg/mL, dan 0,25 µg/mL. Suspensi C. albicans yang telah ditambahi
dengan anticendawandiencerkan sampai ke tingkat pengenceran 10-7. Sebanyak
satu mililiterdari masing-masing tabung pengenceran 10-3 sampai 10-7 dituangkan
ke dalam satu cawan petri. Setelah itu, ke dalam semua cawan dituangi media
PDA yang mengandung sebelumnya telah diimbuhi antibiotika kloramfenikol
dengan dosis 0,05 mg/mL medium. Pencampuran harus merata sehingga cawan
yang telah ditambahkan media dihomogenkan dengan cara membentuk angka 8
beberapa saat untuk seterusnya didiamkan hingga media agar memadat. Seluruh
cawan diinkubasi pada suhu 37oC selama 24 jam. Koloni yang tumbuh setelah
masa inkubasi dicapai dihitung koloni dengan aturan hanya cawan yang
diperkirakan koloni yang tumbuh pada kisaran 25-250 CFU saja yang akan
dihitung.
Analisis Data
Data kepekaan anticendawan terhadap C. albicans yang dihasilkan pada
penelitian kali ini diolah dengan menggunakan analisis One Way ANOVA
Lokasi Pemotongan Ayam
Pemotongan unggas dilakukan untuk memenuhi kebutuhan masyarakat.
Pemotongan ini biasanya dilakukan di rumah potong unggas (RPU), tempat
pemotongan unggas (TPU), dan pasar tradisional. RPU merupakan kompleks
bangunan dengan rancangan dan konstruksi khusus yang memenuhi persyaratan
teknis dan higiene yang digunakan sebagai tempat memotong unggas untuk
kebutuhan masyarakat umum (SNI 1999). Pemotongan unggas juga dilakukan
TPU dan pasar tradisional untuk memenuhi kebutuhan masyarakat terhadap
daging ayam karena ini tidak dapat diimbangi oleh RPU. Namun, pola
pemotongan yang dilakukan oleh TPU, terutama TPU pada skala rumah tangga,
dan pasar tradisional,seringkali tidak memenuhi persyaratan higiene dan sanitasi.
Oleh karena itu, sering muncul kekhawatiran terhadap status aman, sehat, utuh
dan halal (ASUH) dari karkas ayam yang dihasilkan (Ditjennak 2010; Sutrisno
2010)
Penelitian ini dilakukan dengan cara mengambil contoh dari tiga TPU dan
tiga pasar tradisional. TPU tempat dilakukannya pengambilan contoh adalah TPU
Jambu Raya, TPU Pondok Rumput, dan RPH Bubulak. Sedangkan untuk pasar
tradisional dilakukan di Pasar Gunung Batu, Pasar Anyar, dan Pasar Warung
Jambu. Penentuan tempat pengambilan contoh ini didasari oleh beberapa faktor,
antara lain sumber air yang digunakan untuk pencucian, jenis ayam yang
dipotong, dan kondisi tempat pemotongan.
Sumber air yang digunakan untuk pencucian karkas ayam pada tempat
dilakukannya pengambilan contoh umumnya berasal dari PDAM. Lokasi yang
menggunakan sumber air PDAM, yaitu Pasar Gunung Batu, Pasar Anyar, TPU
Jambu Raya, TPU Pondok Rumput, dan RPH Bubulak. Sedangkan Pasar Warung
Jambu menggunakan air sungai untuk pencucian karkas ayam. Berdasarkan
penelitian yang dilakukan Noverita (2009), sumber air minum maupun air sungai
telah tercemar oleh kapang dan khamir, sehingga membahayakan untuk kesehatan
23
lokasi. PadaPasar Gunung Batu,air yang digunakan untuk mencuci umumnya
ditampung terlebih dahulu oleh pedagang, setelah itudigunakan untuk mencuci
dan air hasil cucian pun tetap ditampung pada suatu tempat penampungan.
Sedangkan di tempat pemotongan lain,yaitu Pasar Anyar; Pasar Warung Jambu;
TPU Jambu Raya; TPU Pondok Rumput; dan RPH Bubulak, air bersih yang
digunakan untuk mencuci merupakan air yang mengalir dan air hasil
pencuciannya mengalir ke dalam suatu saluran berupa parit setelah ditampung
dahulu di suatu wadah tertentu. Teknik ini mempengaruhi sanitasi dari lokasi
tempat pemotongan ayam sehingga tingkat kehigienisan berbeda-beda.
Jenis ayam yang dipotong pada tempat pemotongan ayam biasanya adalah
ayam ras pedaging. Tetapi, berdasarkan hasil pengamatan yang dilakukan, masih
dilakukan pemotongan ayam buras di Pasar Anyar. Hal ini dimungkinkan oleh
masih tingginya permintaan ayam buras dari konsumen. Menurut Rasyaf (2008),
ayam buras memiliki kelebihan jika dibandingkan dengan ayam ras pedaging,
yaitu memiliki daging yang liat sehingga untuk masakan yang harus mengalami
proses perebusan dengan waktu yang lama, daging ayam buraslebih cocok karena
tidak akan hancur. Selain itu, sebagian masyarakat juga berpendapat rasa daging
ayam buras lebih gurih sehingga lebih memilih daging ayam buras sebagai bahan
makanan.
Perhatian terhadap sanitasi di tempat pemotongan sangat mempengaruhi
mutu cemarandan mutu daging yang dihasilkan. Seperti yang diperlihatkan
dalam Gambar 5 di bawah ini.
TPU Jambu Raya, yang ditampilkan dalam Gambar 5, menunjukkan salah
satu tempat pemotongan unggas yang menurut penilaian Ditjennak termasuk TPU
yang memadai (Ditjennak 2010). Area pemotongan dinilai cukup higienisdan
pekerjanya diharuskan memakai perlengkapan yang telah dibakukan. Upaya
penciptaan kondisi seperti ini akan mempengaruhi jumlah mikroorganisme yang
mencemari daging, karkas, maupun organ dalam yang akan digunakan sebagai
bahan makanan, terutama cemaran mikroorganisme pada saat penanganannya.
Setelah dilakukan penentuan tempat, contoh diambil untuk mendapatkan
ada tidaknya C. albicansdi contoh-contoh tersebut. Jenis contoh yang diambil
dibagi menjadi empat jenis contoh, yaitu tembolok, potongan usus, air bersih
untuk pencucian karkas, serta air limbah bekas pencucian. Gambar 6
menunjukkan contoh organ yang diambil (tembolok dan usus) yang diambil untuk
diidentifikasi ada tidaknya C. albicans di dalam organ tersebut.
(a) (b)
Gambar6Salah satutembolok (a) dan potongan usus (b) yang dijadikan contoh
Menurut Tabbu (2000), kandidiasis umumnya menginfeksi saluran
pencernaan terutama tembolok, sehingga menjadi pertimbangan utama mengapa
dilakukan isolasi C. albicans dari organ tersebut. Selain itu, air bersih untuk
pencucian maupun air limbah bekas pencucian juga dijadikan contoh. Noverita
(2009) menyatakan bahwa di perairan, seperti sungai, kolam, danau, maupun laut,
dapat ditemukan berbagai macam khamir yang dapat menimbulkan penyakit,
salah satunya adalah Candida spp. Selain itu, Cook dan Schlitzer (1981) juga
mengisolasi adanya C. albicans dari aliran sungai serta parit. Namun jumlah C.
25
Tabel 2 menunjukkan data jumlah contoh yang diambil pada setiap lokasi
dengan tujuan untuk mengetahui keberadaan C. albicans yang terdapat pada
contoh yang diambil tersebut.
Tabel 2 Lokasi dan jumlah pengambilan contoh
Lokasi pengambilan contoh
Jumlah contoh yang diambil berdasarkan jenis
Jumlah Tembolok Air-1 Air-2 Potongan
usus
Catatan: Air-1: air bersih yang digunakan untuk mencuci karkas. Air-2: air limbah
Penelitian ini menggunakan 119 contoh yang terdiri dari 60 contoh berasal
dari tembolok, 42 contoh berasal dari potongan usus, 7 contoh berasal dari sumber
air bersih yang digunakan untuk mencuci karkas, dan 10 contoh lainnya berasal
dari air limbah yang telah digunakan untuk mencuci karkas ayam. Tembolok yang
dijadikan contoh terdiri dari dua jenis, yakni 13 contoh tembolok berasal dari
ayam buras, yaitu 12 contoh diambil di Pasar Anyar dan 1 contoh diambil di Pasar
Gunung Batu, sedangkan 47 contoh lainnya merupakan tembolok dari ayam ras
pedaging. Potongan usus yang digunakan menjadi contoh juga dibagi menjadi dua
kelompok, yaitu 10 contoh potongan usus yang berasal dari ayam buras dan 32
contoh lainnya berasal dari ayam ras pedaging. Potongan usus dari ayam buras
hanya diperoleh di Pasar Anyar.
Identifikasi C. albicans
Isolasi dilakukan untuk mengidentifikasi adanya C. albicans dari contoh
yang diambil. Isolasi awal dilakukan dengan mengidentifikasi koloni yang diduga
sebagai C. albicans dari contoh yang telah diolah secara dilution plating.
Kemudian koloni tersebut diinkubasi pada suhu 37oC selama 24 jam dan setelah
masa inkubasinya tercapai, koloni yang tumbuh diamati dengan pemeriksaan
Secara makroskopik, dapat dilihat bahwa koloni yang diduga C. albicans
telihat koloni berbentuk bulat, berwarna putih, mempunyai permukaan yang halus
dan licin, serta memiliki bau seperti ragi. Hasil pemeriksaan mikroskopik
menunjukkan C. albicans dalam fase sel khamir (blastospora). Fase ini
merupakan fase normal, dimana C. albicans berkembang biak dengan cara
membentuk tunas atau yang biasa disebut budding cell (Gambar 7). Sedangkan
beberapa C. albicans terlihat dalam fase sel hifa sejati. Ada beberapa faktor yang
mempengaruhi fase ini, seperti perubahan komposisi media, penambahan serum,
tumbuh pada kondisi kadar CO2 yang tinggi atau semi anaerobik, pH dan suhu
(Calderone 2002)
Gambar 7 Hasil pemeriksaan natif yang diwarnai dengan
LPCB memperlihatkan C. albicans dalam
bentuk sel khamir (blastospora) yang
membentuk tunas (budding cell)
Tabel 3 menunjukkan hasil pemeriksaan biokimiawi terhadap
koloni-koloni yang diduga sebagai koloni-koloni Candida. Uji yang dilakukan terdiri dari uji
asimilasi gula-gula untuk menentukan spesies Candida yang diisolasi dari contoh
dan uji tabung kecambah. Uji ini merupakan salah satu uji biokimiawi didasari
oleh kemampuan khamir untuk melakukan metabolisme oleh enzim yang
27
Catatan: T3A, T9B, dan T5B berasal dari tembolok. AB1B berasal dari air bersih yang digunakan untuk mencuci karkas. Glu= Glukosa, Gal= Galaktosa, Suk= Sukrosa, Mal= Maltosa, Lak= Laktosa, Man= Manitol
Tanda positif pada uji asimilasi menunjukkan bahwa media berubah
menjadi keruh. Kekeruhan tersebut menandai adanya pertumbuhan dari khamir
karena khamir mampu memanfaatkan nutrisi berupa karbohidrat yang terdapat
pada media yang diberikan.
Tanda positif pada uji tabung kecambah menunjukkan bahwa terbentuknya
tabung kecambah (Gambar 8) pada isolat khamir tersebut. Uji tabung kecambah
dilakukan dengan membiakkan isolat C. albicans dalam putih telur bebek dan
diinkubasi pada suhu 37◦C dalam waktu 2-4 jam. Uji ini dilakukan untuk melihat
kemampuan membentuk tabung kecambah yang dilakukan koloni khamir untuk
menghindari bentuk blastospora dan membentuk hifa berfilamen. Namun, tabung
kecambah ini hanya dapat dibentuk oleh C. albicans dan C. stellatoidea. Hasil
positif tabung kecambah dari C. parapsilosis, C. rugosa, dan C. krusei
berdasarkan Tabel 3 kemungkinan merupakan hasil positif palsu yang
dikarenakan pembiakan yang terlalu lama (Al-Doory 1980; Abu-Elteen dan
Hamad 2007)
Gambar8Tabung kecambah yang dibentuk oleh isolat
C. albicans yang diperoleh dari contoh-contoh yang diperiksa dari
beberapa lokasi dipaparkan pada Tabel 4di bawah ini.
Tabel4 Koloni khamir yang berhasil ditumbuhkan dari contoh yang diperiksa
Lokasi pengambilan contoh
Dugaan koloni yang diisolasi dari contoh
Tembolok Air-1 Air-2 Potongan usus
Pasar Gunung Batu C. abicans - C. albicans C. krusei
C. albicans C. albicans C. albicans C.albicans C. rugosa
TPU Jambu Raya C. albicans - - C. albicans
TPU Pondok Rumput C. albicans. - - C.albicans.
RPH Bubulak C. albicans - - C. albicans
Catatan: Air-1: air bersih yang digunakan untuk mencuci karkas. Air-2: air limbah
Berdasarkan Tabel 4diatas, terdapat beberapa spesies Candida dari
contoh-contoh yang diambil. Secara normal, spesies Candida dapat ditemukan
sebagai mikroflora normal di dalam saluran pencernaan yang sehat, begitu pula
dengan khamir lain yang dapat ditemukan di saluran pencernaaan seperti
Rhodotorula sp., Saccharomyces sp., Torulopsis sp., dan Trichosporon sp.
(Hastiono 1987; Kunkle 2003).
Berdasarkan hasil yang terdapat di dalam Tabel 4, C. albicansmerupakan
khamir yangmendominasi di dalam baik usus maupun tembolok ayam jika
dibandingkan dengan jenis khamir lainnya. Hal ini dikarenakan C. albicans
umumnya terdapat pada saluran pencernaan ayam, baik ayam sehat maupun ayam
sakit. Penelitian Kunkle (2003) memberikan data bahwa sebanyak 95% C.
albicansdiisolasi dari tembolokayam ras pedaging.Selain pada saluran
pencernaan, C. albicans secara normal juga dapat ditemukan di sistem reproduksi
dan urinari (Vieira dan Coutinho2009). Selain C. albicans terdapat pula C. rugosa
dan C. parapsilosis di dalam tembolok serta C. krusei dan C. rugosa di dalam
potongan usus. Hal ini sejalan dengan penelitian yang dilakukan Hastiono (1987)
yang menyatakan adanya isolasi dari C. albicans,C. guillermondii, C. krusei, C.
parapsilosis, C. pseudotropicalis, C. tropicalis, C. rugosa, C. parakrusei, C.
29
Berdasarkan penelitian-penelitian yang sudah dilakukan, hanya C. albicans dan C.
parapsilosis yang berkaitan dengan mikosis pada tembolok (Kunkle 2003)
Contoh air bersih untuk mencuci karkas maupun air limbah hasil cucian
umumnya tidak tercemar oleh khamir yang dicari. Namun, beberapa tempat masih
menunjukkan adanya cemaran dari Candida sp. Berdasarkan hasil penelitian
Noverita (2009), terbukti bahwa 70% dari contoh air terdapat cemaran khamir.
Candida sp. merupakan salah satu jenis khamir yang ditemukan dan spesiesnya
yang dapat membahayakan kesehatan, yaitu C. albicans ditemukan di dalam
perairan.
Kadar Hambat Minimum (MIC)
MIC ditentukan berdasarkan kadar terendah anticendawan yang dapat
menghambat pertumbuhan koloni cendawan sebanyak 80% (Espinel-Ingroff dan
Cantón 2007).Umumnya, penentuan MIC dilakukan dengan metode baik
makrodilusi maupun mikrodilusi. Metode makrodilusihanya menggunakan satu
isolat cendawan dan satu zat anticendawan yang terlarut dengan kadar
tertentuyang kemudian dilakukan perbandingan dengan kontrol menggunakan
spektofotometri. Namun, metode ini dianggap kurang efektif untuk pemeriksaan
dalam jumlah besar. Metode mikrodilusi merupakan metode umum yang
digunakan oleh laboratorium klinis untuk meneliti kepekaan isolat dalam jumlah
besar terhadap agen anticendawan dengan menggunakan mikrotiter dan kemudian
dilihat kejernihannya(Espinel-Ingroff dan Cantón 2007; Moran et al. 2007).
Penelitian ini menggunakan metode dilusi agar untuk menentukan
kepekaan anticendawan. Metode ini dapat menggambarkan hasil MIC secara
kuantitatif jika dibandingkan dengan metode zona hambat yang hanya dapat
menggambarkan secara kualitatif (Hanlon et al. 2007).
Sebagai uji pendahuluan, dilakukan uji zona hambat untuk menentukan
kisaran anticendawan yang mungkin efektif untuk isolat C. albicans dari
masing-masing lokasi pengambilan contoh. Keefektifan dari anticendawan diketahui
dengan terbentuk atau tidaknya zona hambat seperti yang ditunjukkan pada
Gambar 9. Namun keefektifan anticendawan yang digunakan tidak dapat