LABORATORIUM
DIAN INDRAWATIE
MAYOR TEKNOLOGI DAN MANAJEMEN PERIKANAN TANGKAP DEPARTEMEN PEMANFAATAN SUMBERDAYA PERIKANAN
FAKULTAS PERIKANAN DAN ILMU KELAUTAN INSTITUT PERTANIAN BOGOR
Dengan ini saya menyatakan bahwa skripsi Pengujian Umpan Buatan (Arginin
dan Leusin) terhadap Ikan Kerapu Macan pada Skala Laboratorium adalah karya saya sendiri dengan arahan dosen pembimbing dan belum pernah diajukan dalam bentuk apapun kepada perguruan tinggi manapun. Sumber data dan informasi yang berasal atau dikutip dari karya ilmiah yang diterbitkan sebelumnya maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam daftar pustaka di bagian akhir skripsi ini.
DIAN INDRAWATIE, C44051524. Pengujian Umpan Buatan (Arginin dan Leusin) terhadap Ikan Kerapu Macan pada Skala Laboratorium. Dibimbing oleh ARI PURBAYANTO dan MOCHAMMAD RIYANTO.
Ikan kerapu macan (Epinephelus fuscoguttatus) merupakan ikan karang ekonomis penting. Penangkapan ikan karang paling efektif dengan menggunakan bubu (perangkap) yang dalam pengoperasiannya dibutuhkan umpan. Syarat umpan yang baik harus disukai oleh ikan. Penelitian yang pernah dilakukan sebelumnya didapatkan arginin dan leusin dapat dijadikan rangsangan kimiawi. Penelitian ini ditujukan untuk mengetahui pola pergerakan ikan kerapu macan dalam merespons umpan buatan dan menguji respons ikan kerapu macan terhadap komposisi umpan buatan (arginin dan leusin) yang berbeda. Metode penelitian yang digunakan adalah metode eksperimental laboratorium. Berdasarkan hasil penelitian pola pergerakan ikan kerapu macan dalam merespons umpan buatan diidentifikasi menjadi tiga pola. Pada kondisi dengan pencahayaan ikan merespons umpan sampai dengan fase finding, sedangkan pada kondisi tanpa pencahayaan ikan hanya merespons sampai dengan fase searching. Berdasarkan penghitungan waktu rata-rata respons arousal dan searching didapatkan hasil waktu respons tercepat terdapat pada umpan A. Perbedaan umpan memberikan pengaruh nyata terhadap waktu respons arousal dan searching baik pada kondisi dengan pencahayaan maupun tanpa pencahayaan. Namun perbedaan umpan tidak memberikan pengaruh yang nyata terhadap waktu respons finding pada kondisi pencahayaan.
© Hak cipta IPB, Tahun 2010 Hak cipta dilindungi Undang-Undang
1) Dilarang mengutip sebagian atau seluruh karya tulis ini tanpa mencantumkan atau menyebutkan sumber:
a. Pengutipan hanya untuk kepentingan pendidikan, penelitian, penulisan karya ilmiah, penyusunan laporan, penulisan kritik atau tinjauan suatu masalah.
b. Pengutipan tidak merugikan kepentingan yang wajar IPB.
DIAN INDRAWATIE
Skripsi
Sebagai salah satu syarat untuk memperoleh gelar Sarjana Perikanan pada
Departemen Pemanfaatan Sumberdaya Perikanan
MAYOR TEKNOLOGI DAN MANAJEMEN PERIKANAN TANGKAP DEPARTEMEN PEMANFAATAN SUMBERDAYA PERIKANAN
FAKULTAS PERIKANAN DAN ILMU KELAUTAN INSTITUT PERTANIAN BOGOR
Nama Mahasiswa : Dian Indrawatie
NIM : C44051524
Mayor : Teknologi dan Manajemen Perikanan Tangkap
Disetujui:
Pembimbing I
Prof. Dr.Ir.Ari Purbayanto, M.Sc. NIP: 19660121 199002 1 001
Pembimbing II
Mochammad Riyanto,S.Pi., M.Si. NIP: 19821025 200701 1 001
Diketahui :
Ketua Departemen Pemanfaatan Sumberdaya Perikanan
Dr. Ir. Budy Wiryawan, M.Sc. NIP: 19621223 198703 1 001
Skripsi ditujukan untuk memenuhi syarat memperoleh gelar Sarjana Perikanan pada Mayor Teknologi dan Manajemen Perikanan Tangkap Departemen Pemanfaatan Sumberdaya Perikanan, Fakultas Perikanan dan Ilmu Kelautan, Institut Pertanian Bogor. Judul skripsi ini adalah Pengujian Umpan Buatan (Arginin dan Leusin) terhadap Ikan Kerapu Macan pada Skala Laboratorium. Penelitian dilaksanakan selama enam bulan. Penelitian ini dilakukan pada dua tempat, yaitu: di Laboratorium Teknologi Penangkapan Ikan
(Flume Tank Room) dan di Laboratorium Pascapanen, Balai Besar Litbang
Pascapanen Pertanian, Cimanggu-Bogor. Pada kesempatan ini penulis ingin mengucapkan terima kasih kepada :
1. Prof. Dr. Ir. Ari Purbayanto, M.Sc. dan Mochammad Riyanto, S.Pi., M.Si selaku dosen pembimbing atas segala saran dan arahan selama penelitian; 2. Ir. Ronny Irawan Wahyu, M.Phil. selaku dosen penguji tamu;
3. Dr. Ir. Mohammad Imron, M.Si. selaku Ketua Komisi Pendidikan;
4. Program Hibah Kompetensi tahun 2009, Direktorat Jenderal Perguruan Tinggi, Kementerian Pendidikan Nasional dengan judul kegiatan Pengembangan Umpan Buatan (Artificial Bait) untuk Meningkatkan Efektivitas Penangkapan Ikan yang telah memfasilitasi kegiatan penelitian; 5. Kedua orang tua yang tak henti-hentinya memberikan doa dan motivasi; 6. Bang Giri, Bang Panji, Leo, Novel dan Bapak Danu yang telah membantu
dalam proses pengambilan data dan pemeliharaan ikan;
7. Seluruh dosen dan staf Departemen PSP yang telah memberikan arahan dan dukungan hingga terselesaikannya penulisan skripsi ini; dan
8. Yosep Hadinata, S.Pi dan angkatan 42 untuk dukungan dan semangat.
Penulis menyadari bahwa skripsi ini masih jauh dari sempurna sehingga
diharapkan saran dan kritik yang bersifat membangun demi kesempurnaan skripsi ini. Semoga skripsi ini dapat bermanfaat bagi semua pihak yang membutuhkan.
Penulis dilahirkan di Surabaya pada tanggal 9 Juli
1987 dari pasangan Koestijono Djajusman dan Cicilia Endang Agustin. Penulis adalah anak ke tiga dari tiga bersaudara. Tahun 1992 penulis mengawali pendidikan di Taman Kanak-kanak Santo Markus II Jakarta Timur dan pada tahun 1993 penulis melanjutkan pendidikan di Sekolah Dasar Santo Markus II Jakarta Timur. Tahun 1999 penulis melanjutkan pendidikan ke Sekolah Menengah Pertama Santo Markus II Jakarta Timur dan pada tahun 2002 penulis melanjutkan pendidikan di Sekolah Menengah Umum Negeri 48 Jakarta Timur.
Penulis diterima di Institut Pertanian Bogor pada tahun 2005 melalui jalur Seleksi Penerimaan Mahasiswa Baru (SPMB) dan terdaftar sebagai mahasiswa Fakultas Perikanan dan Ilmu Kelautan pada Departemen Pemanfaatan Sumberdaya Perikanan Mayor Teknologi dan Manajemen Perikanan Tangkap. Selama menjadi mahasiswa, penulis aktif dalam berbagai kegiatan organisasi. Penulis pernah menjabat sebagai anggota Departemen Eksternal HIMPATINDO periode 2006-2007 dan menjabat sebagai anggota Departemen Kewirausahaan HIMAFARIN periode 2007-2008. Selain itu, penulis juga menjadi asisten Mata Kuliah Manajemen Operasi Penangkapan Ikan (MOPI) tahun 2008-2009.
DAFTAR TABEL ... iii 2.1 Morfologi dan Klasifikasi Ikan Kerapu Macan (Epinephelus fuscoguttatus) ... 3
2.2 Tingkah Laku Makan Ikan Kerapu ... 4
2.3 Reaksi Penciuman Ikan terhadap Rangsangan Bau ... 5
2.4 Tingkah Laku Ikan Mendekati Umpan ... 6
2.5 Organ Penglihatan (Visual Organ) ... 8
2.6 Organ Penciuman(Olfactory Bulb) ... 10
2.7 Otak dan Bagian-bagiannya ... 11
2.8 Umpan ... 13
2.9 Arginin dan Leusin ... 14
2.10 Pengamatan Skala Laboratorium ... 14
3 METODOLOGI 3.1 Waktu dan Tempat Penelitian ... 16
3.2 Sarana, Bahan dan Alat Penelitian ... 16
3.2.1 Sarana penelitian... 16
3.2.2 Bahan penelitian dan alat penelitian ... 17
3.3 Metode Penelitian ... 18
3.4 Prosedur Percobaan ... 18
3.4.1 Pembuatan umpan buatan ... 18
3.4.2 Uji kimia umpan buatan ... 19
3.4.3 Uji respons tingkah laku ikan terhadap umpan ... 20
3.5 Analisis Data ... 23
4 HASIL DAN PEMBAHASAN 4.1 Hasil Penelitian ... 26
4.1.1 Kondisi bak penelitian... 26
4.1.2 Tingkah laku ikan kerapu macan selama pemeliharaan ... 28
4.1.3 Tingkah laku ikan mendekati umpan buatan ... 29
4.1.4 Respons ikan kerapu macan terhadap umpan buatan ... 32
4.1.5 Pengaruh perbedaan jenis umpan terhadap waktu respons penciuman ... 35
4.2 Pembahasan ... 39
4.2.1 Hubungan perbedaan umpan dan waktu respons ikan ... 39
4.2.2 Komposisi kimia umpan buatan ... 41
5 KESIMPULAN DAN SARAN 5.1 Kesimpulan ... 43
5.2 Saran ... 43
DAFTAR PUSTAKA ... 44
DAFTAR TABEL
Halaman
1. Bagian utama dan sub bagian otak ikan ... 11
2. Alat dan bahan yang digunakan ... 18
3. Rancangan komposisi arginin dan leusin berdasarkan penelitian sebelumnya ... 19
4. Rancangan perlakuan formulasi komposisi kimia umpan buatan (berat total umpan 8 gr) ... 19
5. Rancangan perlakuan perbedaan warna umpan buatan ... 19
6. Daftar analisis ragam Rancangan Acak Lengkap (RAL) ... 24
7. Kondisi lingkungan bak pemeliharaan selama penelitian ... 28
8. Uji ANOVA berdasarkan perbedaan waktu arousal kondisi dengan pencahayaan ... 35
9. Uji ANOVA berdasarkan perbedaan waktu arousal kondisi tanpa pencahayaan ... 35
10. Uji ANOVA berdasarkan perbedaan waktu searching kondisi dengan pencahayaan ... 36
11. Uji ANOVA berdasarkan perbedaan waktu searching kondisi tanpa pencahayaan ... 36
12. Uji ANOVA berdasarkan perbedaan waktu finding kondisi dengan pencahayaan ... 36
13. Kandungan asam amino umpan buatan dan pakan ... 37
14. Perbandingan nilai arginin dan leusin yang seharusnya dan hasil uji ... 38
15. Data waktu respons ikan kerapu macan terhadap umpan buatan pada kondisi dengan pencahayaan ... 52
DAFTAR GAMBAR
Halaman
1. Ikan kerapu macan ... 4
2. Bentuk hidung ikan dan bagiannya ... 10
3. Otak Epinephelus fuscoguttatus ... 12
4. Akuarium perlakuan ... 17
5. Pembagian fase respons ikan terhadap umpan ... 22
6a. Pola tingkah laku ikan (1) ... 29
6b. Pola tingkah laku ikan (2) ... 30
6c. Pola tingkah laku ikan (3) ... 30
7. Pola tingkah laku ikan ... 31
8a. Grafik data waktu arousal kondisi dengan pencahayaan ... 32
8b. Grafik data waktu arousal kondisi tanpa pencahayaan ... 33
9a. Grafik waktu searching kondisi dengan pencahayaan ... 34
9b. Grafik waktu searching kondisi tanpa pencahayaan ... 34
10. Grafik nilai arginin sebenarnya dan hasil uji ... 38
DAFTAR LAMPIRAN
Halaman
1. Sarana penelitian ... 49
2. Bahan penelitian ... 50
3. Alat penelitian ... 51
4. Data waktu respons ikan kerapu macan terhadap umpan buatan ... 52
5. Uji one-way ANOVA berdasarkan perbedaan umpan dan waktu rata-rata arousal pada kondisi dengan pencahayaan ... 54
6. Uji one-way ANOVA berdasarkan perbedaan umpan dan waktu rata-rata arousal pada kondisi tanpa pencahayaan ... 55
7. Uji one-way ANOVA berdasarkan perbedaan umpan dan waktu rata-rata searching pada kondisi dengan pencahayaan ... 56
8. Uji one-way ANOVA berdasarkan perbedaan umpan dan waktu rata-rata searching pada kondisi tanpa pencahayaan ... 57
1
PENDAHULUAN
1.1 Latar Belakang
Ikan kerapu macan (Epinephelus fuscoguttatus) merupakan ikan karang konsumsi yang banyak diminati oleh masyarakat terutama masyarakat manca negara. Menurut data Departemen Kelautan dan Perikanan (2006) volume ekspor kerapu tahun 2006 bisa mencapai 1.800 ton atau US$ 24 juta dari total produksi perikanan sebesar 12.000 ton. Menurut Soelaiman (2007) permintaan ekspor ikan kerapu dengan tujuan negara Hongkong bisa mencapai 2.868 kg
dengan nilai US$ 5.736,36 juta. Selain Hongkong ikan kerapu juga cukup diminati oleh negara Singapura dengan jumlah ekspor sebesar 32,80 kg dengan nilai US$ 87,90 juta.
Tingginya tingkat permintaan ekspor ikan kerapu membuat para nelayan melakukan segala cara untuk mendapatkan komoditi ini. Kegiatan penangkapan ikan kerapu yang dilakukan oleh nelayan biasanya dengan menggunakan bubu, pancing, bahan peledak dan bius (potassium cyanide). Penggunaan bahan peledak dan bius dapat mengakibatkan kerusakan terumbu karang. Ikan yang didapatkan dengan menggunakan bahan peledak dalam kondisi tidak segar atau sudah mati, sehingga memiliki harga yang rendah dan tidak dapat diekspor.
Penggunaan bubu dan pancing dalam penangkapan ikan tidak merusak ekosistem terumbu karang dan sumber daya ikan lainnya, hal ini disebabkan karena bubu dan pancing merupakan alat tangkap pasif. Terdapat perbedaan kondisi hasil tangkapan dari kedua alat tangkap pasif ini, hasil tangkapan ikan dengan menggunakan pancing kondisinya segar tetapi terdapat luka yang diakibatkan oleh mata pancing yang tajam sedangkan hasil tangkapan dengan bubu kondisinya segar dan tidak terdapat luka.
Faktor penunjang keberhasilan penangkapan alat tangkap pasif adalah
ikan segar. Sedangkan umpan buatan adalah umpan yang sengaja dibuat oleh manusia.
Penelitian mengenai umpan telah dilakukan oleh beberapa peneliti sebelumnya antara lain Uji Coba Beberapa Macam Umpan Tiruan pada Penangkapan Ikan dengan Huhate di Perairan Bone-Bone, Kota Bau-Bau Sulawesi Tenggara (Syafrie, 2008); Analisis Indera Penglihatan Ikan Kerapu Macan (Epinephelus fuscoguttatus) dan Hubungannya dalam Merespons Umpan (Natsir, 2008) dan Respons Penciuman Ikan Kerapu Macan (Epinephelus
fuscoguttatus) terhadap Umpan (Sejati, 2008); Respons Penciuman Ikan Kerapu Macan terhadap Umpan Buatan (Riyanto, 2008) dan Respons Penglihatan dan Penciuman Ikan terhadap Umpan Terkait dengan Efektivitas Penangkapan (Fitri, 2008).
Berdasarkan penelitian sebelumnya didapatkan hasil komposisi umpan buatan asam amino arginin dan leusin dapat digunakan sebagai atraktan yang berperan pada respons penciuman ikan. Oleh karena itu perlu dilakukan penelitian lanjutan tentang pengaruh komposisi asam amino (arginin dan leusin) dan perbedaan warna umpan buatan terhadap respons tingkah laku ikan.
1.2 Tujuan
Tujuan penelitian ini adalah:
1) Mengetahui pola pergerakan ikan kerapu macan dalam merespons umpan buatan; dan
2) Menguji respons ikan kerapu macan terhadap umpan buatan yang berbeda.
1.3 Manfaat
Manfaat dari penelitian ini adalah:
1) Memberikan informasi tentang respons tingkah laku ikan kerapu macan terhadap umpan;
2.1 Morfologi dan Klasifikasi Ikan Kerapu Macan (Epinephelus
fuscoguttatus)
Ikan kerapu (Epinephelus sp) atau dikenal dengan nama dagang groupers
merupakan salah satu komoditas perikanan yang bernilai ekonomis tinggi dan
berpeluang dipasarkan baik di domestik maupun internasional. Ada beberapa
macam ikan kerapu di pasaran, diurut dari nilai ekonomis yang tertinggi, yaitu
ikan kerapu lodi, kerapu macan, kerapu lumpur, kerapu tikus, kerapu bebek dan
lainnya. Di pasaran ikan kerapu yang banyak dijumpai adalah jenis ikan kerapu
macan (Epinephelus fuscoguttatus) (Bahar, 2006).
Ikan kerapu macan dalam perdagangan internasional, dikenal dengan nama
carped cod. Ikan kerapu ini mirip dengan kerapu lumpur, namun ukuran
tubuhnya lebih tinggi dengan noda-noda pada tubuhnya yang lebih rapat dan
berwarna gelap. Seluruh tubuh berwarna cokelat kemerahan atau merah, termasuk
sirip-siripnya (Murtidjo, 2001). Menurut Andreas dan Soeharmoko (1997),
ciri-ciri morfologis dari ikan kerapu macan (Epinephelus fuscoguttatus) bentuknya
agak bulat memanjang dan mempunyai ukuran badan lebih tinggi, sirip dada
berwarna kemerahan dan sirip lainnya mempunyai tepi kecoklatan. Bentuk dari
ikan kerapu macan dapat dilihat pada Gambar 1.
Menurut Heemstra dan Randall (1993) sistematika pengklasifikasian ikan
Sumber: www.fishyforum.com (2009)
Gambar 1 Ikan kerapu macan (Epinephelus fuscoguttatus).
2.2 Tingkah Laku Makan Ikan Kerapu
Kerapu merupakan ikan yang bersifat nokturnal. Pada malam hari aktif
bergerak di kolom perairan untuk mencari makan sedangkan pada siang hari lebih
banyak bersembunyi di liang-liang karang (Valenciennes, 1828). Kemudian
Tampubolon dan Mulyadi (1989) yang dikutip oleh Maryati (2004) menyatakan
ikan kerapu mempunyai kebiasaan makan pada siang hari dan malam hari, namun
lebih aktif lagi pada waktu fajar dan senja hari. Menurut Indonesia Corel Reef
Foundation (2004), kerapu termasuk ikan jenis crepuscular, yang merupakan ikan
yang aktif di antara waktu siang dan malam hari.
Ikan kerapu termasuk jenis karnivora. Kerapu dewasa memangsa ikan-ikan
kecil, kepiting dan udang-udangan, sedangkan pada saat larva memangsa larva
moluska (trokofor), rotifera, mikro crustacea, copepoda dan zooplankton.
Sebagai ikan karnivor, kerapu cenderung menangkap mangsa yang aktif bergerak
di kolom air (Nybakken, 1988).
Ikan kerapu biasanya mencari makan dengan cara menyergap mangsa dari
tempat persembunyiannya. Ikan kerapu juga bersifat kanibalisme jika kekurangan
makanan. Kanibalisme biasanya mulai terjadi pada larva berumur 30 hari, dimana
pada saat itu cenderung berkumpul di suatu tempat dengan kepadatan tinggi
(Direktorat Jenderal Perikanan, 1999 yang dikutip oleh Maryati, 2004)
2.3 Reaksi Penciuman Ikan terhadap Rangsangan Bau
Menarik perhatian ikan dengan menggunakan umpan merupakan cara
pertama yang dilakukan manusia untuk menangkap ikan (Gunarso, 1985). Jenis
1) Rangsangan kimiawi (chemical stimulating), yaitu rangsangan yang akan
merangsang indera penciuman dan perasa;
2) Rangsangan berdasarkan penglihatan (optical stimulating), yaitu rangsangan
yang diberikan atau ditimbulkan untuk merangsang penglihatan sebagai akibat
dari gerak, bentuk maupun warna;
3) Rangsangan berdasarkan pendengaran (acoustic stimulating), yaitu rangsangan
yang diberikan atau ditimbulkan untuk indera pendengaran dan indera peraba
atau linea lateris;
4) Rangsangan listrik (electrical stimulating), yaitu memberikan rangsangan pada
kemampuan merasakan arus listrik; dan
5) Rangsangan berupa tempat-tempat berlindung untuk mengumpulkan ikan.
Dalam perikanan pancing, jenis rangsangan yang paling berpengaruh dalam
keberhasilan penangkapan ikan adalah rangsangan kimia yang berasal dari umpan.
Umpan yang baik adalah umpan yang dapat dideteksi oleh ikan pada jarak yang
lebih jauh. Rangsangan penglihatan dapat membantu ikan menemukan lokasi
umpan.
Umpan yang mengandung asam amino diidentifikasi dapat menjadi stimulus
dan atraktor makan pada ikan dan crustacea (Engas dan Lokkerborg, 1994 dikutip
oleh Fitri, 2008). Berdasarkan hasil beberapa analisis elektrofisiologi bahwa asam
amino merupakan atraktan (stimuli) yang efektif untuk organ penciuman dan rasa
pada ikan (Sola dan Tongiorgi, 1998 dikutip oleh Fitri, 2008). Asam amino yang
sangat efektif sebagai stimulus pada sistem penciuman ikan atlantik salmon
adalah glutamin dan alanin (Caprio, 1982 dikutip oleh Fitri, 2008). Lebih lanjut
dijelaskan pula bahwa efektifitas relatif stimulus organ penciuman dari kandungan
asam amino sebanyak 10-4 M adalah alanin, glutamin, lystein dan methionin.
Kandungan alanin terdapat pada jaringan organisme cacing, moluska, crustacea
dan ikan teleostei. Sedangkan untuk arginin terdapat pada jaringan organisme
moluska dan crustacea. Pengetahuan yang mendasari bahwa untuk ikan catfish
reseptor penciuman sangat besar responsnya pada kandungan lystein dan
methionin dan pada reseptor rasa sangat besar reseptornya pada kandungan alanin
dan arginine masih belum diketahui. Nukkleosid, nukleotid dan tiga jenis asam
diidentifikasi sebagai stimulan makanan (Lokkerberg, 1990 dikutip oleh Fitri,
2008).
Pada ikan cod asam amino yang dapat menstimuli ikan adalah Leusin,
metionin, asparagin, glutamin, alanin dan threonin menurut Yacob et al (2004)
Menurut Hara (2006) dikutip oleh Fitri (2008) yang asam amino yang dapat
menstimuli ikan air tawar adalah sistein, arginin dan glutamin.
2.4 Tingkah Laku Ikan Mendekati Umpan
Tingkah laku ikan adalah suatu gerakan total secara menyeluruh baik
gerakan dari dalam maupun dari luar tubuh yang diperagakan dalam bentuk
tingkah laku untuk merespons perubahan lingkungannya. Menurut Mulyadi
(2001) tingkah laku dapat diartikan sebagai reflek atau respons ikan terhadap
segala bentuk stimulan yang datang dari luar maupun dari dalam dan
diaktualisasikan dalam bentuk gerak berpola sesuai dengan jenis stimulan yang
mempengaruhi.
Tingkah laku ikan biasanya didasarkan pada indera ikan, salah satunya
adalah indera penciuman. Pada jenis tertentu indera ini lebih berkembang
daripada mata dalam mencari mangsa, misalnya ikan hiu. Tingkah laku ini
dimanfaatkan pada pengopersian alat tangkap dengan umpan misalnya bubu dan
rawai. Secara umum ikan menggunakan saraf penciuman, penglihatan atau
keduanya secara bersamaan dan pendengaran untuk mendeteksi makanan di
sekitarnya. Oleh karena itu, dalam memilih umpan disesuaikan dengan kesukaan
makanan ikan. Sasaran dan kecenderungan ikan dalam mendeteksi makanan
(Wudianto et al., 1993).
Hal tersebut diperkuat oleh Zarochman (1996) yang mengatakan bahwa
keberhasilan penggunaan umpan untuk penangkapan direkayasa sesuai dengan
kebiasaan terpenting dalam kehidupan hewan melakukan perburuan mencari
makanan. Oleh sebab itu pengetahuan mengenai kebiasaan makan akan
membantu dalam memahami hubungan antara ikan sasaran dengan alat tangkap
yang dipasangi umpan.
Menurut Ferno dan Olsen (1994) ada empat fase tingkah laku ikan terhadap
1) Timbul selera (arousal)
Fase ini disebabkan oleh karena ikan dapat mendeteksi keberadaan umpan.
Respons ikan akibat kehadiran umpan sebagai makanan merupakan salah satu
yang penting dalam proses rangkaian aktivitas mencari makan bagi ikan. Pada
umumnya ikan menggunakan organ olfactory bulb untuk mendeteksi jarak atau
keberadaan makanan (umpan).
Ikan dapat mengetahui keberadaan makanan atau umpan akibat adanya
organ chemosensory yang dapat mendeteksi jarak atau posisi dimana ikan itu
berada. Dari hasil penelitian didapat adanya pengaruh lama perendaman pancing
terhadap hasil tangkapan pancing dengan menggunakan umpan ikan segar.
Umpan mackerel yang digunakan dalam keadaan segar dan lama waktu
perendaman selama 24 jam menghasilkan tangkapan 50% dari rata-rata hasil
tangkapan. Hal tersebut membuktikan bahwa umpan ikan yang telah lama
terendam akan kehilangan bau amisnya dan tidak dapat lagi menarik ikan-ikan
yang menjadi target tangkapan (Lokkerberg, 1996 dikutip oleh Fitri, 2008).
2) Menentukan lokasi (location phase)
Setelah fase pertama, ikan-ikan akan berorientasi untuk dapat mencari lokasi
umpan yang telah dideteksinya melalui organ chemoreceptor ataupun organ
deteksi lainnya. Biasanya pada tahap ini ikan-ikan akan menggunakan organ
penglihatannya untuk menemukan makanan atau umpan. Pada fase ini arus juga
memegang peranan penting begi keberhasilan ikan dalam menemukan makanan
atau umpan tersebut, karena arus merupakan media transfer bau yang baik di
perairan.
Pengamatan di lapangan terhadap tingkah laku ikan Gadus meriangus
(whitting) menuju umpan pada pancing dan diterangkan pula bahwa lebih banyak
ikan yang tertarik menuju umpan dalam kondisi perairan berarus. Hal ini
disebabkan rangsangan bau aroma dapat dibawa oleh arus pada jangkauan yang
lebih jauh, sedangkan dalam kondisi air tenang atau berarus lemah daya hantar
aroma dari umpan semakin lemah sehingga ikan yang tertarik kepada umpan
jumlahnya sedikit. Sumber makanan dengan cepat lebih mudah ditemukan oleh
sampai tenang lokasi umpan hanya ditemukan secara alami (Ferno dan Olsen,
1994).
Jenis ikan catfish (Ictalarus sp) dan hiu (Sphyrna sp) akan berenang zig-zag
dalam mencari makan atau umpan, kemungkinan pada jenis ikan-ikan ini
pencarian makanan melalui adaptasi chemo-orientation memiliki konsentrasi yang
berbeda.
3) Mengidentifikasikan umpan (up take)
Pada fase ini ikan akan berhasil menemukan umpan dan akan mencari tahu
apakah umpan ini cocok untuk dimakan atau tidak. Berdasarkan hasil
pengamatan di laboratorium ikan yang menemukan umpan akan berhenti sejenak
sebelum mulai memakannya (Riyanto, 2008).
Menurut Ferno dan Olsen (1994) ikan-ikan akan menggunakan
penglihatannya dan mechanoreceptor untuk mengidentifikasi dan memutuskan
makanan yang layak atau tidak untuk dimakan. Hal yang sama juga diungkapkan
oleh Lokkerborg (1996) yang mangatakan bahwa sosok atau wujud umpan yang
tertampak oleh penglihatam merupakan fakor penting dalam penerimaan umpan.
4) Fase masuknya makanan (umpan) ke dalam mulut ikan (food ingestion)
Fase ini adalah dimana umpan mulai masuk ke dalam mulut ikan. Pada fase
inilah kesempatan mata pancing mengait ikan. Hal yang sangat berpengaruh pada
fase ini adalah ukuran dan bentuk umpan, dimana umpan yang terlalu besar tidak
akan termakan oleh ikan yang berukuran kecil. Sedangkan umpan yang terlalu
kecil akan sulit terdeteksi atau terlihat oleh ikan.
2.5 Organ Penglihatan (Visual Organ)
Mata (penglihatan) pada ikan merupakan salah satu indera yang sangat
penting untuk mencari makan, menghindari predator/pemangsa atau dari
kepungan suatu alat tangkap. Ketajaman pada mata ikan dapat dijadikan dasar
untuk mengetahui area kekuatan pandang untuk melihat suatu objek benda
melalui metode tingkah laku ikan (Muntz, 1974 yang dikutip oleh Purbayanto,
1999)
Sumbu penglihatan (visual axis) diidentifikasikan untuk mengetahui
Sumbu penglihatan diperoleh setelah nilai kepadatan sel kon tiap bagian sel dari
retina mata diketahui, dengan cara menarik garis lurus dari bagian retina yang
memilki nilai kepadatan sel kon yang tertinggi menuju titik pusat lensa mata
(Tamura, 1957). Kepadatan sel kon yang tinggi dimungkinkan untuk mengetahui
ketajaman penglihatan dan sumbu penglihatan (Blaxter, 1980).
Menurut Natsir (2008) susunan sel reseptor dari retina mata ikan kerapu
macan (Epinephelus fuscoguttatus) terdiri dari sel kon tunggal (single cone cell)
dan sel kon ganda (twine cone cell) yang membentuk mozaik, sedangkan sel rod
tidak terdapat pada susunan tersebut. Sel kon merupakan reseptor penglihatan
untuk color vision dan ketajaman penglihatan (visual acuity). Ukuran diameter
lensa akan meningkat sejalan dengan bertambahnya ukuran tubuh ikan.
Kepadatan sel kon berbanding terbalik dengan ukuran panjang tubuh.
Semakin besar ukuran panjang tubuh Epinephelus fuscoguttatus maka kepadatan
sel konnya akan semakin menurun. Hal ini dikarenakan ukuran sel sel kon akan
tetap selama ikan hidup (Natsir, 2008). Menurut Purbayanto (1999) bahwa
diameter lensa mata ikan akan meningkat dengan bertambahnya ukuran tubuh
sementara itu kepadatan sel kon cenderung menurun dengan meningkatnya
pertambahan panjang tubuh.
Berdasarkan hasil penelitian Natsir (2008) diketahui bahwa Epinephelus
fuscoguttatus memiliki sumbu penglihatan yang mengarah ke depan-naik (
upper-fore). Hal ini dapat dilihat dari padatnya sel kon pada bagian ventro-temporal,
dengan menarik garis lurus melalui lensa mata maka terlihatlah arah penglihatan
ikan kerapu macan.
2.6 Organ Penciuman (Olfactory Bulb)
Menurut Hoar dan Randall (1971) “hidung” pada ikan teleost merupakan sepasang cekungan penciuman (olfactory) yang biasanya terletak di sisi dorsal
bagian kepala dan sedikit agak jauh dari posisi mulut.
Secara umum olfactory serupa dengan organ nasal untuk penciuman
manusia. Akan tetapi dari struktur bentuk dan sistematika fungsinya ada
perbedaan antara manusia dan ikan. Lubang atau cuping hidung pada ikan jarang
epithelium penciuman atau mukosa berupa lipatan/lamella berbentuk ros (Pitcher,
1993). Susunan bentuk dan lipatan perkembangan lamella sangat bervariasi pada
setiap spesies. Bentuk hidung ikan dan bagian-bagiannya dapat dilihat pada
Gambar 2.
Keterangan:
(a) Posisi cuping hidung teleostei, (b) epithelium olfactory; (vo) hidung depan; (ho) hidung belakang; (H) kulit yang menahan pergerakan air masuk ke dalam hidung depan; (F) lamella Sumber: Harder (1975) yang dikutip oleh Fujaya (2004)
Gambar 2 Bentuk hidung ikan dan bagiannya.
Reseptor pembau mendeteksi rangsangan kimia dalam bentuk sinyal elektrik
yang berasal dari cilia, disebabkan oleh arus lemah yang melewati lamella,
selanjutnya informasi tersebut diteruskan ke sistem saraf pusat. Sistem saraf
olfactory yang menuju ke otak memiliki dua konfigurasi.
Ikan mendeteksi adanya reseptor pembau dalam bentuk stimuli kimia.
Stimuli tersebut melalui lubang hidung (nostril) dan dirubah dalam bentuk signal
elektrik yang berasal dari gerakan silia yang kemudian melewati olfactory lamella
yang berbentuk rosette (bunga mawar). Sinyal yang dihasilkan pada olfactory
lamella diteruskan pada olfactory bulb dan olfactory tract yang kemudian
diterjemahkan pada otak telencephalon.
Penciuman ikan sangat sensitif terhadap bahan organik maupun anorganik
yang dikenal melalui indera penciuman (Syandri, 1988). Selanjutnya dijelaskan
pula bahwa ikan dapat mengenal bau mangsanya, predator dan spesies sendiri.
Bau tersebut melarut dalam air dan merangsang reseptor pada organ penciuman
Organ penciuman sebagai alat bantu sensor untuk mengetahui banyaknya
makanan yang tersedia di habitatnya (Wudianto et al., 1993). Lebih lanjut
dijelaskan pula oleh Gunarso (1985), bahwa organ penciuman merupakan salah
satu organ penting lainnya pada tubuh ikan yang berhubungan untuk mempelajari
natural behavior.
2.7 Otak dan Bagian-bagiannya
Menurut Bone dan Marshall (1982) otak merupakan cerminan berkembang
tidaknya fungsi organ-organ sensoris pada hewan. Otak ikan memiliki
bagian-bagian yang menunjukan susunan yang berbeda pada kelompoknya. Secara
umum, otak ikan dibagi ke dalam tiga bagian besar, yaitu otak depan (forebrain)
disebut juga prosencephalon, otak tengah (mesencephalon) dan otak belakang
(rhombencephalon). Pembagian otak ikan dapat dilihat pada Tabel 1.
Tabel 1 Bagian utama dan sub bagian otak ikan
No Bagian Utama Sub Bagian
1 Forebrain (prosencephalon)
Lobus olfactoris
Telencephalon (cerebral hemisphere) Diencephalon (between brain) 2 Midbrain (mesencephalon) Lobus opticus
3 Hindbrain (rhombencephalon) Metencephalon (cerebellum)
Myelencephalon (medulla oblongata) Sumber: Bone dan Marshall (1982)
Telencephalon merupakan pusat penciuman pada bagian otak depan.
Bagian ini disebut juga otak depan (forebrain). Pada ikan, telencephalon
merupakan tempat penerimaan, elaborasi dan meneruskan impuls aroma (bau).
Ukurannya bervariasi, sesuai dengan peranan relatif yang dimainkannya bagi
kehidupan ikan yang diuji.
Mesencephalon merupakan otak tengah (midbrain), pada ikan relatif besar
terdiri dari lobus opticus dorsal, di bagian dorsal terdapat dua lobus opticus dan
ventral tegmentum. Lobus opticus merupakan bagian depan dari retina yang
diteruskan proyeksinya ke dalam bagian belakang contra-lateral dari lobus
Perkembangan otak depan yang sangat besar dibandingkan dengan
kelompok ikan bertulang sejati maupun hewan vertebrata lainnya, merupakan
indikasi bahwa hewan predator seperti ikan cucut, buaya dan anjing sangat
mengandalkan indera penciuman sebagai detektor mangsanya dari jarak yang
cukup jauh (Razak, 2006).
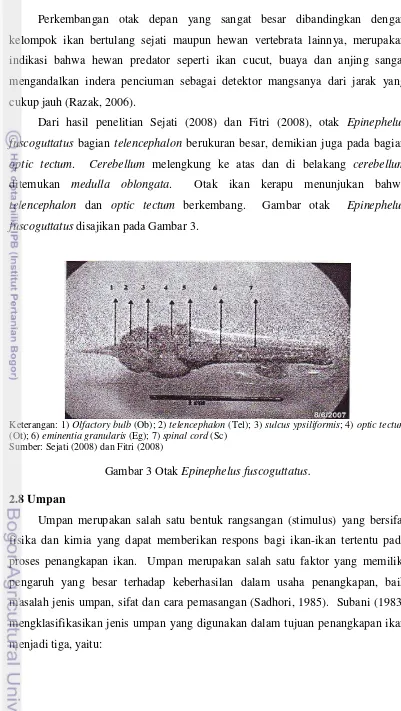
Dari hasil penelitian Sejati (2008) dan Fitri (2008), otak Epinephelus
fuscoguttatus bagian telencephalon berukuran besar, demikian juga pada bagian
optic tectum. Cerebellum melengkung ke atas dan di belakang cerebellum
ditemukan medulla oblongata. Otak ikan kerapu menunjukan bahwa
telencephalon dan optic tectum berkembang. Gambar otak Epinephelus
fuscoguttatus disajikan pada Gambar 3.
Keterangan: 1) Olfactory bulb (Ob); 2) telencephalon (Tel); 3) sulcus ypsiliformis; 4) optic tectum (Ot); 6) eminentia granularis (Eg); 7) spinal cord (Sc)
Sumber: Sejati (2008) dan Fitri (2008)
Gambar 3 Otak Epinephelus fuscoguttatus.
2.8 Umpan
Umpan merupakan salah satu bentuk rangsangan (stimulus) yang bersifat
fisika dan kimia yang dapat memberikan respons bagi ikan-ikan tertentu pada
proses penangkapan ikan. Umpan merupakan salah satu faktor yang memiliki
pengaruh yang besar terhadap keberhasilan dalam usaha penangkapan, baik
masalah jenis umpan, sifat dan cara pemasangan (Sadhori, 1985). Subani (1983)
mengklasifikasikan jenis umpan yang digunakan dalam tujuan penangkapan ikan
1) Umpan tipuan (artificial bait), yaitu jenis umpan yang dibuat asal saja, artinya
tidak dibuat menyerupai umpan alami dan dibuat dari bahan tertentu misalnya:
bulu ayam atau bulu domba;
2) Umpan tiruan (imitation bait), yaitu jenis umpan yang dibuat mnyerupai
umpan alami (ada yang menyerupai ikan baik warna maupun bentuknya, ada
yang menyerupai udang atau cumi-cumi). Misalnya: umpan dari plastic yang
berbentuk mirip udang atau cumi-cumi yang digunakan untuk pancing dengan
joran; dan
3) Umpan alami (natural bait), yaitu jenis umpan yang didapatkan dari alam
(ikan segar, potongan daging ikan dan sebagainya).
Syarat umpan yang baik (Djatikusumo, 1975 yang dikutip oleh Piterurbinas,
2000)
1) Tahan lama artinya tidak mudah busuk;
2) Mempunyai ukuran yang memadai;
3) Harga terjangkau;
4) Mempunyai bau yang spesifik yang dapat merangsang;
5) Mempunyai warna yang mudah dilihat; dan
6) Disenangi oleh ikan yang menjadi tujuan penangkapan.
King (1991) menjelaskan bahwa umpan pada bubu dan perangkap
digunakan untuk menangkap ikan dan crustacea. Prinsipnya ikan tertarik oleh
umpan, lalu masuk ke dalam bubu melalui mulut bubu dan sulit untuk melarikan
diri. Akan tetapi tidak semua jenis ikan akan merespons jenis ikan yang sama,
dimana masing-masing spesies memiliki pilihan jenis umpan yang berbeda.
Umpan yang mengandung asam amino diidentifikasikan dapat menjadi
stimulus dan atraktor makan pada ikan dan crustacea, dan hampir semua studi
mengenai rangsangan kimia untuk tingkah laku makan menunjukan bahwa
rangsangan makan pada ikan dan crustacea akan hilang seiring dengan hilangnya
kandungan asam amino pada umpan (makanan) (Engas dan Lokkerborg, 1994
dikutip oleh Fitri, 2008). Menurut pendapat Hansen dan Reutter (2004) bahwa
ikan predator (buas) yang memakan makanan yang tidak hidup (umpan)
menggunakan sistem penciuman mereka untuk dapat merangsang makan dan
2.9 Arginin dan Leusin
Arginin (Arg atau disingkat R) adalah α-asam amino yang merupakan
asam amino yang paling umum. Pada mamalia, arginin diklasifikasikan sebagai
semiessensial atau asam amino esensial kondisional, tergantung pada tahap
perkembangan dan status kesehatan individu. Rumus kimia dari arginin adalah
C6H14N4O2 dengan massa molekul 174,2 g mol -1 (Wikipedia, 2009). Menurut
Riyanto (2008) didapatkan hasil komposisi arginin yang dapat dijadikan atraktan
ikan kerapu macan adalah 40 mg/g.
Leusin merupakan asam amino essensial yang paling umum dijumpai pada
protein yang diperlukan dalam perkembangan atau pertumbuhan. Leusin berperan
dalam menjaga perombakan dan pembentukan protein otot. Rumus kimia leusin
adalah C6H13NO2 dengan massa molekul 131,18 g mol-1 (Wikipedia, 2009).
Menurut Riyanto (2008) didapatkan hasil komposisi leusin yang dapat dijadikan
atraktan ikan kerapu macan adalah 50 mg/g.
2.10 Pengamatan Skala Laboratorium
Untuk mengembangkan suatu alat tangkap agar lebih efektif dan efisien,
perlu dilakukan percobaan-percobaan terhadap alat tangkap yang masih
mempunyai kendala dalam pengoperasiannya serta mempelajari pola tingkah laku
ikan target, dimana pengujian dilakukan terlebih dahulu dalam skala laboratorium.
Gunarso (1985) menyatakan terdapat beberapa cara untuk mengamati
tingkah laku ikan, antara lain:
1) Pengamatan langsung dengan bantuan penyelam pada waktu siang hari;
2) Pengamatan dilakukan melalui akuarium atau tangki percobaan. Hal ini
dilakukan untuk mengamati tingkah laku ikan terhadap benda yang diam atau
bergerak. Pengamatan ini bisa dibantu dengan kamera atau handycam; dan
3) Pengamatan secara tidak langsung dalam hubungannya dengan alat
penangkapan yang dioperasikan di laut dengan bantuan berbagai peralatan
seperti sonar yang diatur dengan pengontrol jarak jauh.
Penelitian yang dilakukan dalam skala laboratorium, seoptimal mungkin
kondisinya disesuaikan dengan kondisi alam yang sebenarnya.
Parameter-parameter lingkungan, terutama dalam bak selalu dijaga agar tetap optimal. Hal
air optimum untuk pertumbuhan ikan kerapu berkisar 22-28°C, jika suhu air turun
sampai di bawah 15°C akan menyebabkan metabolisme tubuh ikan menurun
sehingga ikan tidak mau makan dan aktivitsnya berkurang, sedangkan jika suhu
terlalu tinggi (panas) akan menyebabkan metabolisme respirasi berlangsung cepat
dan proses metabolism terhenti. Untuk salinitas optimal berkisar 28-32 ppt.
Derajat keasaman (pH) perairan yang optimum untuk kehidupan ikan
berkisar 5-8,7. Ikan kerapu macan dapat hidup pada derajat keasaman (pH) 6,5-8.
Ikan dihindarkan dari perubahan pH perairan secara mendadak agar tidak stress
dan dapat bertahan hidup (Fridudin, 2007).
Sebelum ikan diuji, dilakukan aklimatisasi ikan laut terhadap lingkungan
yang baru diperlakukan waktu rata-rata empat hari agar ikan dapat beradaptasi.
Pemberian makanan dua kali sehari selama aklimatisasi. Frekuensi pemberian
makan yang tepat ditujukan agar pertumbuhan ikan baik, karena berkaitan dengan
3.1 Waktu dan Tempat Penelitian
Penelitian dilaksanakan selama enam bulan dari bulan September 2009
sampai Pebruari 2010. Penelitian ini dilakukan pada dua tempat, untuk respons
tingkah laku ikan terhadap umpan dilakukan di Laboratorium Teknologi
Penangkapan Ikan (Flume Tank Room). Sedangkan untuk analisis kimia umpan
dilakukan di Laboratorium Pascapanen, Balai Besar Litbang Pascapanen
Pertanian, Cimanggu-Bogor.
3.2 Sarana, Bahan dan Alat Penelitian
3.2.1 Sarana penelitian
1) Bak pemeliharaan
Bak yang digunakan untuk pemeliharaan ikan kerapu terbuat dari fiber glass
dengan ukuran 1,5 x 0,6 x 0,8 m (p x l x t) dan tinggi air 0,4 m. Bak ini
dilengkapi dengan sistem filtrasi dan aerasi. Sistem filtrasi yang digunakan
adalah sistem filtrasi eksternal. Sistem filtrasi membutuhkan wadah sendiri.
Selama penelitian ini sistem filtrasi yang digunakan akuarium bersekat
berukuran 1 x 0,4 x 0,6 m (p x l x t). Sekat ini berfungsi untuk membagi sistem
filtrasi menjadi tiga bagian yakni filtrasi fisik, kimia dan biologi. Pada bak
pemeliharaan dipasangi pompa berselang untuk memompa air laut dari bak
pemeliharaan ke akuarium filter. Sedangkan air dari akuarium filter dialirkan ke
bak pemeliharaan dengan bantuan gaya gravitasi, akuarium filter dipasangi pipa
paralon sehingga air akan keluar dan mengalir ke bak pemeliharaan. Pada bak
pemeliharaan juga dipasang protein skimmer yang berfungsi sebagai pengurai
protein. Gambar bak pemeliharaan dan akuarium filter dapat dilihat pada
Lampiran 1a dan 1b.
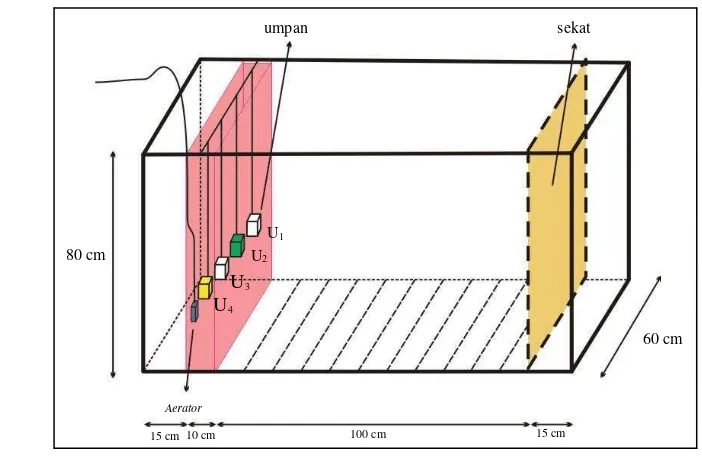
2) Bak perlakuan
Bak yang digunakan untuk perlakuan adalah bak yang sama dengan bak
yang digunakan untuk pemeliharaan. Pada saat memulai perlakuan bak
dikondisikan tidak terdapat benda yang bisa menghalangi pergerakan ikan.
dibagi menjadi tiga area (Gambar 4), yaitu 15 cm pertama sebagai area start yang
merupakan posisi awal ikan, kemudian 115 cm berikutnya merupakan area ikan
untuk menentukan keberadaan umpan. Pada area start dipasangi sekat. Sekat
dipasang setelah ikan digiring ke area start, kemudian sekat diangkat ketika
memulai perlakuan.
Keterangan: U1 = umpan kontrol; U2 = umpan dengan pewarna hijau;
U3 = umpan tanpa pewarna; dan U4 = umpan dengan pewarna kuning
Gambar 4 Akuarium perlakuan.
3.2.2 Bahan penelitian dan alat penelitian
1) Bahan penelitian
Bahan yang digunakan dalam penelitian ini antara lain:
(1) Ikan kerapu macan (Epinephelus fuscogutatus) sebanyak lima ekor,
dengan sebaran ukuran panjang total 25-30 cm dalam kondisi sehat;
(2) Makanan ikan selama berada di bak pemeliharaan, berupa pakan ikan
(pelet) dari Pabrik Grobest tipe PG2;
(3) Umpan percobaan berupa umpan buatan dengan campuran arginin
A5006-100G dan leusin L8000-A5006-100G (asam amino yang akan diujikan), pewarna
(4) Air laut yang didatangkan dari Ancol, Jakarta.
Bahan penelitian pada Lampiran 2.
2) Alat penelitian
Alat-alat yang digunakan dalam penelitian dan kegunaanya ditunjukan pada
Tabel 2. Gambar alat dan bahan yang digunakan pada saat penelitian dapat dilihat
pada Lampiran 3.
Tabel 2 Alat dan bahan yang digunakan selama penelitian
No. Alat dan Bahan Kegunaan
1. Timbangan digital (ketelitian 0,1 gram)
Menimbang bahan-bahan yang digunakan untuk membuat umpan
2. Alat pencetak umpan Mencetak umpan
3. Termometer Mengukur suhu air
4. Refraktometer Mengukur kadar garam
5. pH paper Mengukur kadar asam
6. Test kadar amonia Mengukur kadar amonia
7. Sekat Menghalangi ikan bergerak maju sebelum perlakuan
dimulai
8 Kayu Media mengantungkan umpan
9. Benang jahit Mengantungkan umpan
10. Stopwatch Mengukur waktu perlakuan
11. Kamera Mendokumentasikan selama penelitian
12. Handycam Merekam selama pengambilan data
3.3 Metode Penelitian
Metode yang digunakan dalam penelitian ini adalah eksperimen murni (true
experiment). Penelitian ini dilakukan dengan metode eksperimen di laboratorium
(laboratory experiment). Penelitian laboratorium dilakukan untuk menentukan
komposisi kandungan kimia umpan buatan (asam amino arginia dan leusina).
3.4 Prosedur Percobaan
3.4.1 Pembuatan umpan buatan
Pada penelitian ini akan dilakukan penyempurnaan formulasi umpan buatan
dengan beberapa komposisi kimia asam amino dan warna umpan. Formulasi
umpan buatan dilakukan dengan tujuan untuk menimbulkan daya tarik ikan
melalui organ penciumannya, formulasi tersebut dilakukan dengan menguji
beberapa komposisi asam amino jenis arginin dan leusin, mengacu pada penelitian
warna, biru dan hijau) untuk menimbulkan daya tarik ikan melalui organ
penglihatannya. Kedua faktor penentu formulasi umpan (komposisi asam amino
dan warna umpan) tersebut di atas merupakan perlakuan yang akan diuji dalam
penelitian ini. Berdasarkan hasil penelitian sebelumnya nilai arginin dan leusin
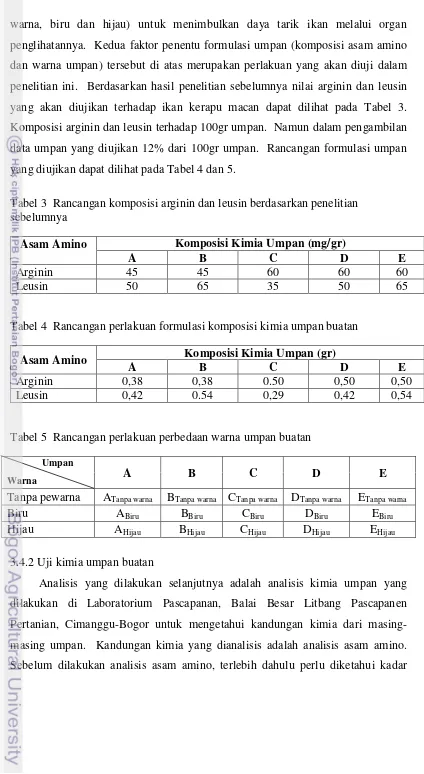
yang akan diujikan terhadap ikan kerapu macan dapat dilihat pada Tabel 3.
Komposisi arginin dan leusin terhadap 100gr umpan. Namun dalam pengambilan
data umpan yang diujikan 12% dari 100gr umpan. Rancangan formulasi umpan
yang diujikan dapat dilihat pada Tabel 4 dan 5.
Tabel 3 Rancangan komposisi arginin dan leusin berdasarkan penelitian sebelumnya
Asam Amino Komposisi Kimia Umpan (mg/gr)
A B C D E
Arginin 45 45 60 60 60
Leusin 50 65 35 50 65
Tabel 4 Rancangan perlakuan formulasi komposisi kimia umpan buatan
Asam Amino Komposisi Kimia Umpan (gr)
A B C D E
Arginin 0,38 0,38 0.50 0,50 0,50
Leusin 0,42 0.54 0,29 0,42 0,54
Tabel 5 Rancangan perlakuan perbedaan warna umpan buatan
Umpan
Analisis yang dilakukan selanjutnya adalah analisis kimia umpan yang
dilakukan di Laboratorium Pascapanan, Balai Besar Litbang Pascapanen
Pertanian, Cimanggu-Bogor untuk mengetahui kandungan kimia dari
masing-masing umpan. Kandungan kimia yang dianalisis adalah analisis asam amino.
protein sampel. Metode yang digunakan untuk analisis tersebut menggunakan
metode kjehdal (AOAC, 1999). Analisis asam amino menggunakan metode High
Performance Liquid Chromatography (HPLC) dengan pereaksi ortoftaldelhida
(OPA) untuk membentuk senyawa yang berflourensi. Senyawa tersebut dapat
dideteksi oleh detektor flouresensi.
3.4.3 Uji respons tingkah laku ikan terhadap umpan
Tahap-tahap dalam pengujian respons tingkah laku ikan terhadap umpan
adalah:
1) Persiapan bak fiber pemeliharaan dan perlakuan
Tahap persiapan dilakukan dengan mempersiapkan bak fiber untuk
pemeliharaan ikan, akuarium filter dan bak fiber untuk perlakuan. Bak fiber yang
digunakan untuk pemeliharaan ikan uji berukuran 1,5 x 0,6 x 0,8 m (p x l x t) dan
tinggi air 0,4 m. Bak fiber yang digunakan untuk perlakuan berukuran sama
dengan bak pemeliharaan hanya tinggi airnya yang berbeda ± 15 cm. Bak tersebut
dibersihkan dengan air tawar untuk menghilangkan kotoran yang menempel.
Alat-alat sirkulasi juga dibersihkan sebelum dipasang. Bak diisi dengan air laut
dan dihubungkan dengan pipa ke akuarium filter dengan menggunakan pompa.
Salinitas dan suhu air laut dalam bak setiap hari dikontrol agar tetap optimal. Bak
pemeliharaan ikan disirkulasi selama dua minggu sebelum ikan dimasukan ke
dalam bak.
2) Persiapan dan pemeliharaan ikan kerapu
Ikan kerapu macan yang digunakan dalam penelitian berasal dari keramba
jaring apung. Ikan dibawa dalam kantung plastik yang telah berisi air laut dan
diberi oksigen. Sebelum dimasukan ke dalam bak pemeliharaan, ikan kerapu
terlebih dahulu diaklimatisasi. Aklimatisasi bertujuan untuk mengatasi ikan yang
stress selama perjalanan, Aklimatisasi mengkondisikan ikan agar secara perlahan
menyesuaikan diri dengan lingkungan baru. Aklimatisasi dilakukan sampai ikan
mulai bisa menyesuaikan diri dengan lingkungannya.
Selama aklimatisasi ikan diberi makan dua kali sehari, yaitu pada pagi dan
sore hari. Ukuran makanan disesuaikan dengan ukuran bukaan mulut ikan.
Penyiponan bak dilakukan dua kali seminggu dan penggantian air laut sebanyak
25% dilakukan dua minggu sekali.
3) Pelaparan ikan uji
Pelaparan dilakukan sebelum perlakuan yang bertujuan untuk
mengondisikan ikan dalam keadaan lapar sehingga ikan benar-benar memberikan
respons terhadap umpan. Berdasarkan uji coba pendahuluan, ikan menunjukkan
respons yang baik terhadap umpan setelah dilaparkan selama 3 x 24 jam.
4) Pengambilan data
Pengambilan data dilakukan dengan dua kondisi perlakuan pencahayaan,
yakni: kondisi tanpa cahaya dan cahaya redup. Pada saat kondisi tanpa cahaya
bak fiber perlakuan dikelilingi oleh plastik mulsa untuk menciptakan ruang gelap.
Ruang gelap dimaksudkan agar pada saat uji coba ikan hanya mengandalkan
organ penciuman dalam mendeteksi umpan. Sedangkan pada perlakuan dengan
pencahayaan redup bak perlakuan tidak dipasangi dengan plastik mulsa.
Pengambilan rekaman pada saat kondisi tanpa cahaya menggunakan mode night
shoot.
Ikan yang akan diuji sudah dipindahkan dari bak pemeliharaan ke bak
perlakuan dan ikan sudah dilaparkan selama 3 x 24 jam. Pengujian diawali
dengan menggiring ikan ke ujung bak perlakuan dan sekat dipasang. Umpan yang
dipasang selama satu kali perlakuan ada empat jenis umpan dengan komposisi
arginin dan leusin yang sama dengan tiga warna umpan yang berbeda dan satu
umpan sebagai kontrol. Umpan diletakkan pada jarak 105 cm dari sekat. Desain
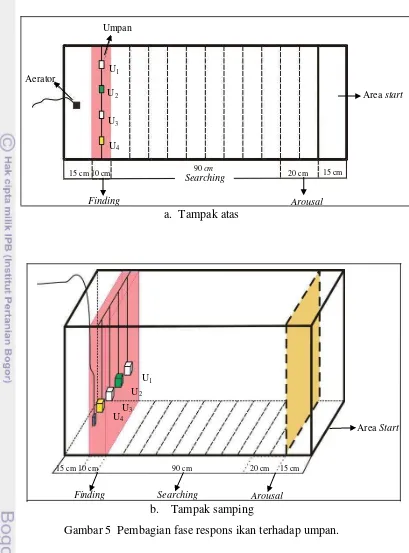
bak perlakuan dapat dilihat pada Gambar 4.
Sekat dibuka secara perlahan agar ikan tidak kaget dan stress. Waktu
pengamatan dilakukan saat sekat mulai dibuka hingga ikan memberikan respons
dengan bergerak mendekati umpan. Prosedur pengambilan data dari perlakuan
dengan cahaya redup sama dengan perlakuan tanpa cahaya. Gambar bak
perlakuan tampak atas dan tampak samping serta pembagian area fase respons
a. Tampak atas
b. Tampak samping
Gambar 5 Pembagian fase respons ikan terhadap umpan.
3.5 Analisis Data
Untuk mengetahui respons indera penciuman ikan uji terhadap umpan
buatan yang diujicobakan, maka akan dilakukan pengambilan data respons ikan
terhadap setiap jenis umpan buatan dengan melakukan pengamatan tingkah laku
ikan mendekati umpan. Data yang dikumpulkan adalah waktu ikan mendekati
umpan yang dibedakan dalam tiga fase. Fase arousal adalah fase dimana ikan Umpan
Aerator
Finding Arousal
Searching
Area start
Finding Searching Arousal
Area Start
15 cm 10 cm 90 cm 20 cm 15 cm
15 cm 10 cm 90 cm 20 cm 15 cm
U1
U3
U2
U4
U1
U2
U3
mulai bereaksi karena rangsangan bau atau melihat umpan. Fase searching adalah
fase dimana ikan mulai mencari keberadaan umpan dan fase finding adalah ketika
ikan telah menemukan umpan dan melakukan uptake (mengambil/memakan
umpan). Analisis tingkah laku ikan mendekati umpan yang telah direkam dengan
handycam dilakukan secara deskriptif dan analisis juga dilakukan terhadap
tingkah laku ikan selama pemeliharaan.
Data mengenai waktu respons arousal, search dan finding merupakan nilai
rataan yang ditampilkan dalam bentuk grafik secara sederhana sesuai dengan jenis
umpan. Data tersebut selanjutnya dibandingkan untuk mengetahui besarnya
pengaruh perbedaan umpan terhadap waktu respons penciuman ikan kerapu
macan dengan analisis ragam satu arah (ANOVA). Dalam penelitian ini
diasumsikan bahwa tidak ada pengaruh antara jenis umpan dan waktu respons
ikan.
Untuk unit percobaan diasumsikan sebagai berikut:
1) Kondisi air dalam bak mendekati kondisi sebenarnya di alam;
2) Ikan di laboratorium dan ikan di perairan terbuka dalam merespon umpan
memiliki peluang yang sama;
3) Keadaan ikan dianggap sama pada setiap perlakuan; dan
4) Kondisi umpan dianggap sama pada setiap perlakuan.
Model observasi yang digunakan adalah sebagai berikut:
Yij=μ + τi+ εij,
Langkah-langkah analisis ragam untuk rancangan acak lengkap adalah
sebagai berikut:
1) Menghitung Faktor Koreksi (FK), Jumlah Kuadrat Total (JKT), Jumlah
Kuadrat Perlakuan (JKP) dan Jumlah Kuadrat Sisa (JKS). Jika n dan p adalah
2) Menentukan derajat bebas masing-masing perlakuan, sisa dan total.
db perlakuan = n - 1
db sisa = n.p–n
db total = n.p– 1
3) Masing-masing Kuadrat Tengah (KT) ditentukan melalui pembagian antara JK
dan derajat bebasnya, yaitu:
4) Menyusun daftar analisis ragam seperti terlihat pada Tabel 6.
Tabel 6 Daftar analisis ragam Rancangan Acak Langkap (RAL)
Sumber Keragaman db JK KT F
hitung
Perlakuan n– 1 JKP KTP KTP/KTS
Sisa n.p - n JKS KTS
Total n.p - 1 JKT
Hipotesis yang diuji melalui model analisis ini adalah:
H0: τ1= τ2 (tidak ada pengaruh perbedaan umpan terhadap waktu respons)
H1 : τ1≠ τ2 (terdapat pengaruh perbedaan umpan terhadap waktu respons)
Kaidah pengambilan keputusan hipotesis yaitu Fhitung > Ftabel maka tolak H0,
yang berarti perbedaan jenis umpan berpengaruh nyata terhadap waktu respons
ikan, tetapi apabila Fhitung < Ftabel maka gagal tolak H0 yang berarti perbedaan
4.1 Hasil Penelitian
4.1.1 Kondisi bak penelitian
Kondisi bak yang digunakan selama penelitian dikontrol, sehingga keadaannya mendekati habitat asli ikan kerapu macan di alam. Menurut Indonesia Coral Reef Foundation (2004), kerapu termasuk ikan jenis crepuscular, yang merupakan ikan yang aktif di antara waktu siang dan malam hari, oleh karena itu selama pemeliharaan kondisi dari bak pemeliharaan dibuat redup. Bak pemeliharaan dilengkapi dengan sistem filtrasi. Sistem filtrasi yang digunakan merupakan sistem filtrasi eksternal karena menggunakan akuarium filter yang terpisah dari bak pemeliharaan. Akuarium filtrasi ini mencakup filtrasi fisik,
biologi dan kimia. Pembuatan sistem filtrasi dibutuhkan waktu kurang lebih tiga minggu untuk menumbuhkan bakteri baik pengurai nitrat dan nitrit. Selama bakteri tersebut belum muncul maka sistem filtrasi dapat dikatakan belum siap digunakan untuk pemeliharaan.
Suhu merupakan salah satu parameter yang penting dalam mengontrol kondisi lingkungan pemeliharaan ikan. Suhu air selama pemeliharaan dijaga agar berkisar pada suhu 28-30°C. Suhu tersebut merupakan suhu optimum untuk kelangsungan hidup dari ikan kerapu macan. Apabila suhu lingkungan berada di bawah kisaran suhu optimum, maka ikan akan mengalami penurunan nafsu makan. Hal ini diperkuat dengan pernyataan dari Sudjiharno (1998) yang diacu dalam Irawati (2002) yang menyatakan jika suhu air turun sampai di bawah 15°C akan menyebabkan metabolisme tubuh ikan menurun sehingga aktivitasnya berkurang dan ikan tidak mau makan.
Salinitas air laut di bak pemeliharaan dikontrol sehingga berada pada kisaran 30-31 ppt. Selama pemeliharaan ikan, air laut mengalami sirkulasi dan terjadi penguapan sehingga terjadi perubahan salinitas. Apabila salinitas air laut meningkat maka perlu ditambahkan air tawar untuk mengembalikan air laut pada salinitas yang optimal.
pH atau kadar asam selama pemeliharaan dikontrol pada kisaran 7-8.
8,1-8,4 oleh karena itu pH dari air laut selama pemeliharaan dikontrol sehingga tidak melibihi kisaran tersebut. Perubahan pH air laut ditandai dengan berubahnya warna dan bau air laut.
Selain suhu, salinitas dan pH parameter lain yang perlu dikontrol selama pemeliharaan adalah kadar amonia. Kadar amonia air laut dijaga pada kisaran 0-0,25 mg/l. Jika kadar ammonia melebihi angka tersebut, maka dapat membahayakan kelangsungan hidup ikan bahkan dapat menyebabkan kematian. Amonia yang tinggi diakibatkan oleh banyaknya sekresi ikan yang dikeluarkan namun bakteri pengurai yang berada pada filter air belum mencukupi. Dalam menjaga tingkat amoniak ini juga dapat dibantu dengan protein skimmer namun alat ini sebenarnya kurang banyak membantu karena yang dapat diurai hanya sebagian kecil.
Perubahan kondisi lingkungan yang drastis dapat menyababkan ikan menjadi stres dan tidak mau makan. Kondisi bak pemeliharaan sudah dibuat sedemikian rupa agar mendekati dengan kondisi habitat asli ikan namun masih terdapat perbedaan kondisi. Ikan yang biasanya dapat bergerak bebas di perairan selama pemeliharaan hanya dibatasi pada bak pemeliharaan yang sempit. Ikan yang mengalami stres mudah terjangkit penyakit baik bakteri, jamur ataupun parasit. Apabila pada tubuh ikan kerapu sudah mulai timbul jamur maka ikan tersebut membutuhkan perlakuan khusus, yaitu dilakukan perendaman dalam air tawar selama kurang lebih lima menit. Lama perendaman bisa lebih dari lima menit tergantung daya tahan ikan.
Tabel 7 Kondisi lingkungan bak pemeliharaan selama penelitian
4.1.2 Tingkah laku ikan kerapu macan selama pemeliharaan
Ikan kerapu macan merupakan ikan nokturnal. Pada malam hari aktif bergerak di kolom perairan untuk mencari makan sedangkan pada siang hari lebih banyak bersembunyi di liang-liang karang (Valenciennes, 1828). Selama pemeliharaan ikan kerapu macan bersifat pasif, cenderung bersembunyi dan tidak melakukan aktifitas, selalu berada pada sudut-sudut bak atau bersembunyi di bawah pompa dan protein skimmer. Dalam mencari tempat persembunyian, ikan harus saling bersaing untuk mendapatkan tempat persembunyian yang nyaman. Bak pemeliharaan tidak dipasang shelter (tempat persembunyian) sehingga tempat persembunyian yang nyaman adalah berada di bawah pompa dan protein skimmer. Ikan biasanya menggunakan bagian depan mulutnya untuk saling mendorong dengan ikan lainnya dalam memperebutkan tempat persembunyian.
Tingkah laku makan ikan kerapu sama seperti saat ikan saling memperebutkan tempat persembunyian. Ikan saling bersaing untuk lebih cepat mendapatkan pakan. Pada awal pemeliharaan biasanya ikan tidak langsung menyukai pakan yang diberikan. Pakan yang telah dilempar ditunggu sampai
berada pada dasar bak. Ikan mulai mendekati pakan dan berhenti sejenak. Ikan mengidentifikasi benda yang berada di depannya. Bila ikan menyukainya maka
4.1.3 Tingkah laku ikan mendekati umpan buatan
Selama perlakuan dilakukan dengan dua kondisi pencahayaan, tanpa pencahayaan dan pencahayaan yang redup. Pada kondisi ada pencahayaan ikan mengunakan indera penglihatan dan penciuman dalam mendeteksi umpan. Sedangkan pada kondisi tanpa pencahayaan ikan diharapkan hanya mengunakan indera penciuman dalam mendeteksi umpan. Tingkah laku ikan dalam mendekati umpan dapat kita bagi menjadi dua, yakni:
1) Tingkah laku ikan mendekati umpan dalam kondisi pencahayaan redup
Perlakuan diawali dengan memasang sekat. Ikan digiring ke ujung bak kemudian dipasangi sekat. Pada ujung bak lain umpan yang akan diuji mulai dipasang. Setelah itu sekat mulai diangkat perlahan. Posisi awal ikan sebelum sekat dibuka berada di pojok dan sudut bak perlakuan. Setelah sekat dibuka, ikan
masih tetap dalam kondisi diam di pojok. Ikan satu demi satu mulai berenang menyusuri sisi bak perlakuan kurang lebih tiga menit setelah sekat dibuka. Ikan berenang menyusuri sisi dari ujung bak satu ke ujung bak yang lain dan ada pula yang berenang menyilang. Hal ini bisa dikarenakan karena ikan mulai beraksi terhadap umpan atau ikan hanya mulai mengadaptasikan diri dengan lingkungannya setelah sekat dibuka. Tingkah laku ikan ini dapat kita lihat pada Gambar 6a, 6b, dan 6c.
Gambar 6a Pola tingkah laku ikan (1).
Gambar 6b Pola tingkah laku ikan (2).
Gambar 6c Pola tingkah laku ikan (3).
Pola gerak tingkah laku ikan yang pertama dapat dilihat pada Gambar 6a, yang digambarkan dengan anak panah, dimulai dengan melakukan pergerakan menyusuri dinding bak perlakuan hingga kembali ke tempat semula. Dalam pendataan waktu yang diperoleh dimasukan ke dalam fase arousal ketika ikan mulai melewati area start dan fase searching ketika ikan mulai berada di sekitar umpan.
Pada Gambar 6b pola tingkah laku ikan berbeda dengan pola tingkah laku
ikan yang pertama. Ikan tidak sampai melewati umpan, hanya berenang maju tidak jauh dari area start lalu kembali lagi ke posisi awal. Pada pola tingkah laku
ikan ini data waktu yang didapatkan hanya sampai dengan fase searching.
Pergerakan ikan mulai melewati area start disebut dengan fase arousal. Hal ini dimungkinkan karena ikan mengunakan organ penglihatanya dalam mendeteksi umpan. Untuk membuktikan hal di atas dilakukan pengujian dengan dengan kondisi tanpa pencahayaan.
2) Tingkah laku ikan mendekati umpan dalam kondisi tanpa pencahayaan
Persiapan yang dilakukan saat perlakuan tanpa pencahayaan hampir sama dengan perlakuan dengan pencahayaan redup. Pembeda dari kedua perlakuan ini
adalah bila tanpa pencahayaan bak perlakuan dipasangi plastik mulsa untuk menciptakan kondisi yang gelap. Pada kondisi tanpa pencahayaan ikan berenang menyusuri dinding-dinding bak dari ujung yang satu ke ujung yang lain. Hal ini diduga untuk mempermudah ikan dalam mengorientasikan diri dalam kondisi gelap.
Selama perlakuan dengan kondisi tanpa pencahyaan ikan hanya maju dan mundur berenang menyusuri dinding. Ikan tidak pernah menyentuh umpan. Akan tetapi selama pendataan kegiatan ini tetap dimasukan sampai dengan fase
searching. Pada perlakuan kontrol, kondisi tanpa pencahayaan dan tanpa umpan setelah sekat dibuka ikan berenang maju dan mundur menyusuri dinding. Pergerakan ikan dalam kondisi tanpa pencahayaan dapat dilihat pada Gambar 7.
Gambar 7 Pola tingkah laku ikan.
umpan
aerator
searching arousal
searching
4.1.4 Respons ikan kerapu macan terhadap umpan buatan
Pendataan hasil pengujian respons ikan kerapu macan dibagi menjadi tiga bagian berdasarkan fase, yakni:
1) Waktu rata-rata arousal
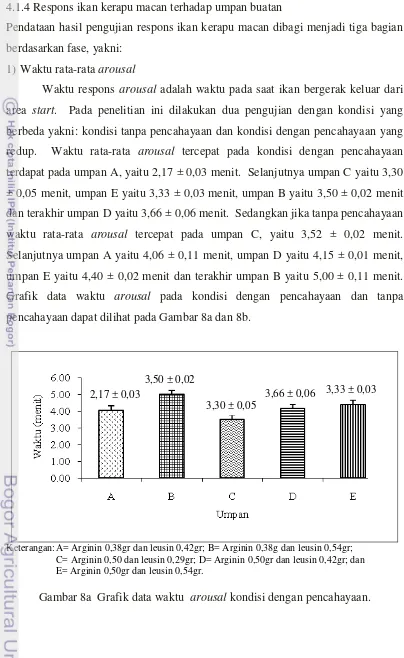
Waktu respons arousal adalah waktu pada saat ikan bergerak keluar dari area start. Pada penelitian ini dilakukan dua pengujian dengan kondisi yang berbeda yakni: kondisi tanpa pencahayaan dan kondisi dengan pencahayaan yang redup. Waktu rata-rata arousal tercepat pada kondisi dengan pencahayaan terdapat pada umpan A, yaitu 2,17 ± 0,03 menit. Selanjutnya umpan C yaitu 3,30 ± 0,05 menit, umpan E yaitu 3,33 ± 0,03 menit, umpan B yaitu 3,50 ± 0,02 menit dan terakhir umpan D yaitu 3,66 ± 0,06 menit. Sedangkan jika tanpa pencahayaan
waktu rata-rata arousal tercepat pada umpan C, yaitu 3,52 ± 0,02 menit. Selanjutnya umpan A yaitu 4,06 ± 0,11 menit, umpan D yaitu 4,15 ± 0,01 menit, umpan E yaitu 4,40 ± 0,02 menit dan terakhir umpan B yaitu 5,00 ± 0,11 menit. Grafik data waktu arousal pada kondisi dengan pencahayaan dan tanpa pencahayaan dapat dilihat pada Gambar 8a dan 8b.
Keterangan: A= Arginin 0,38gr dan leusin 0,42gr; B= Arginin 0,38g dan leusin 0,54gr; C= Arginin 0,50 dan leusin 0,29gr; D= Arginin 0,50gr dan leusin 0,42gr; dan E= Arginin 0,50gr dan leusin 0,54gr.
Gambar 8a Grafik data waktu arousal kondisi dengan pencahayaan. 2,17 ± 0,03
3,50 ± 0,02
3,30 ± 0,05
Gambar 8b Grafik data waktu arousal kondisi tanpa pencahayaan.
2) Waktu rata-rata searching
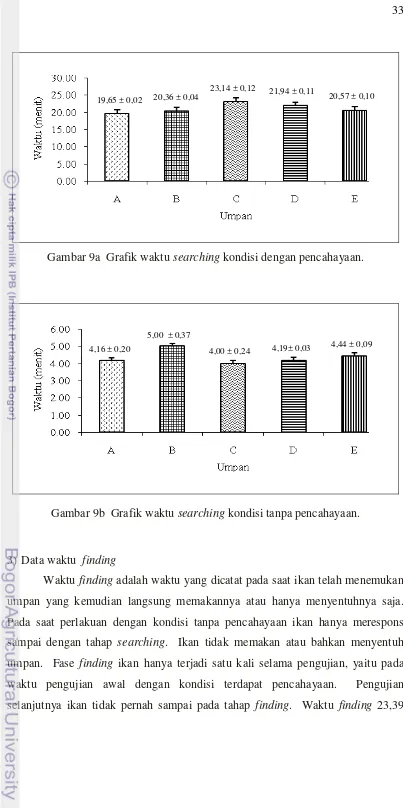
Waktu searching adalah waktu yang dicatat pada saat ikan mulai bergerak kembali untuk menemukan keberadaan umpan. Setelah sebelumnya melakukan
arousal dan berhenti sejenak di depan area start untuk identifikasi umpan. Waktu rata-rata searching tercepat pada kondisi dengan pencahayaan terdapat pada umpan A, yaitu 19,65 ± 0,12 menit. Selanjutnya umpan B yaitu 20,36 ± 0,04 menit, umpan E yaitu 20,57 ± 0,10 menit, umpan D yaitu 21,94 ± 0,11 menit dan terakhir umpan C yaitu 23,14 ± 0,12 menit. Sedangkan jika tanpa pencahayaan waktu rata-rata searching tercepat pada umpan C, yaitu 4,00 ± 0,24 menit.
Selanjutnya umpan D yaitu 4,19 ± 0,03 menit, umpan E yaitu 4,44 ± 0,09 menit, umpan A yaitu 4,16 ± 0,10 menit dan terakhir umpan B yaitu 5,00 ± 0,37 menit.
Grafik waktu searching pada kondisi dengan pencahayaan dan kondisi tanpa pencahayaan dapat dilihat pada Gambar 9a dan 9b.
4,06 ± 0,11
Gambar 9a Grafik waktu searching kondisi dengan pencahayaan.
Gambar 9b Grafik waktu searching kondisi tanpa pencahayaan.
3) Data waktu finding
Waktu finding adalah waktu yang dicatat pada saat ikan telah menemukan umpan yang kemudian langsung memakannya atau hanya menyentuhnya saja. Pada saat perlakuan dengan kondisi tanpa pencahayaan ikan hanya merespons sampai dengan tahap searching. Ikan tidak memakan atau bahkan menyentuh umpan. Fase finding ikan hanya terjadi satu kali selama pengujian, yaitu pada waktu pengujian awal dengan kondisi terdapat pencahayaan. Pengujian selanjutnya ikan tidak pernah sampai pada tahap finding. Waktu finding 23,39
19,65 ± 0,02 20,36 ± 0,04
23,14 ± 0,12 21,94 ± 0,11
20,57 ± 0,10
4,16 ± 0,20
5,00 ± 0,37