KAJIAN KANDUNGAN LOGAM BERAT TIMBAL (Pb) DAN
SENG (Zn) PADA AIR, SEDIMEN, DAN MAKROZOOBENTOS
DI PERAIRAN WADUK CIRATA, PROVINSI JAWA BARAT
MUHAMMAD AMIEN H
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
PERNYATAAN MENGENAI TESIS DAN
SUMBER INFORMASI
Dengan ini saya menyatakan bahwa tesis yang berjudul Kajian Kandungan Logam Berat Timbal (Pb) dan Seng (Zn) Pada Air, Sedimen, dan Makrozoobentos di Perairan Waduk Cirata, Provinsi Jawa Barat adalah karya saya dengan arahan dari komisi pembimbing dan belum diajukan dalam bentuk apa pun kepada perguruan tinggi mana pun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir tesis ini.
Bogor, Nopember 2007
ABSTRACT
Muhammad Amien H. Study on the Content of Heavy Metal Timbal (Pb) and Zinc (Zn) in Water, Sediment, and Makrozoobenthic in Waters of Cirata Reservoir, Provinsi West Java. Under direction of D.Djokosetiyanto and Suprihatin
Heavy metal is a chemical elements which are considered as the cause of water pollution and could endanger the life of organsimt. Heavy metal could also indirectly harm human health. This research was conducted in the waters of Cirata reservoir, Provinsi West Java, with the objective of learning the contents of heavy metal Pb and Zn in water, sediment, and makrozoobenthic. Analysed deite relate at Government regulation No. 82, Year 2001 and In order to know the significan level between the parameters, the data wer analysed using a sample regression. The samples were analysed using AAS (Atomic Absorption Spectrofometer) based on the Standart National Indonesia (SNI). Result of laboratory analysis showed that in the water, contents of metal Pb were 0,01-0,0213 mg/l, Zn 0,036-0,067 mg/l, amonia 0,36-0,616 mg/l, nitrat 0,0914-0,57 mg/l, nitrit 0,02-0,036-0,067 mg/l. In the sediment, contents of Pb were 20,5-39,4 mg/kg dan Zn 73,34-111 mg/kg. In makrozoobenthic, the contents of Pb were 31,62-43,65 mg/kg and Zn 11,79-17,85 mg/kg. In the case, metal Zn and ammonia content exceeded the water quality standard (Government regulation No. 82, Year 2001). Result of calculation of makrozoobenthic relative composition are as follows: class Gastropoda 38 %, Oligochaeta, Diftera, dan Odonata 14%, Pelecypoda 10 %, class Coleoptera and Lepidoptera 5 % and average density ranged between 65,4 -325,4 (indiv/m2), diversity indexen (H|) were 1,18-1,83, keseragaman (E) were 0,527-0,683, dan dominance (C) were 0,363-0,58. Results of regression and correlation analysis conserning of heavy metal Pb which showed close correlation were as follows: heavy metal content in water with sediment, those in water with macrozoobenthic, and those in sediment with macrozoobenthic.
RINGKASAN
Muhammad Amien H. Kajian Kandungan Logam Berat Timbal (Pb) dan Seng (Zn) Pada Air, Sedimen dan Makrozoobentos di Perairan Waduk Cirata, Provinsi Jawa Barat. Dibimbing oleh D.Djokosetiyanto dan Suprihatin.
Logam berat merupakan unsur kimia yang dianggap sebagai penyebab pencemaran air dan dapat membahayakan kehidupan organisme serta efeknya secara tidak langsung dapat merugikan kesehatan manusia. Penelitian ini dilakukan di perairan Waduk Cirata, Provinsi Jawa Barat dengan tujuan mengkaji kandungan logam Pb dan Zn dalam air, sedimen, dan makrozoobentos. Analisis data mengacu pada Peraturan Pemerintah No. 82 Tahun 2001 and analisis regresi dan korelasi untuk mengetahui keeratan hubungan antar parameter yang diukur. Metode yang digunakan adalah Standar Nasional Indonesia (SNI) dengan menggunakan Atomic Absorption Spectrofotometer (AAS). Hasil analisis laboratorium diperoleh rata-rata kandungan logam Pb di air sebesar 0,01-0,0213 mg/l, Zn 0,036-0,067 mg/l, kadar amonia 0,36-0,616 mg/l, nitrat 0,0914-0,57 mg/l, nitrit 0,02-0,067 mg/l, sedangkan sedimen Pb sebesar 20,5-39,4 mg/kg dan Zn 73,34-111 mg/kg, makrozoobentos Pb 31,62-43,65 mg/kg dan Zn 11,79-17,85 mg/kg, dimana Logam Zn dan ammonia tidak memenuhi baku mutu air (PP.No. 82 Tahun 2001). Hasil analisis komposisi relatif makrozoobentos, yaitu; kelas Gastropoda 38 %, Oligochaeta, Diftera dan Odonata 14 %, Pelecypoda 10 %, kelas Coleoptera dan Lepidoptera 5 % dan rata-rata kepadatan berkisar antara 65,4-325,4 (indiv/m2), indeks keanekaragaman (H|)1,18-1,83, keseragaman (E) 0,527-0,683, dan dominansi (C) 0,363-0,58. Hasil analisis korelasi dan regresi menunjukkan bahwa hanya logam berat Pb yang memiliki hubungan erat, yaitu: kandungan logam berat dalam air dengan sedimen, air dengan makrozoobentos, dan sedimen dengan makrozoobentos.
@ Hak Cipta milik IPB, tahun 2007 Hak Cipta dilindungi Undang-undang
1. Dilarang mengutip sebagian atau seluruh karya tulis ini tanpa mencantumkan atau menyebutkan sumber
a. Pengutipan hanya untuk kepentingan pendidikan, penelitian, penulisan karya ilmiah, penyusunan laporan, penulisan kritikan atau tinjauan suatu masalah
b. Pengutipan tidak merugikan kepentingan yang wajar IPB
KAJIAN KANDUNGAN LOGAM BERAT TIMBAL (Pb) DAN
SENG (Zn) PADA AIR, SEDIMEN, DAN MAKROZOOBENTOS
DI PERAIRAN WADUK CIRATA, PROVINSI JAWA BARAT
MUHAMMAD AMIEN H
Tesis
Sebagai salah satu syarat untuk memperoleh gelar Magister Sains
pada Pengelolaan Sumberdaya Alam dan Lingkungan
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
Judul Tesis : Kajian Kandungan Logam Berat Timbal (Pb) dan Seng (Zn) Pada Air, Sedimen, dan Makrozoobentos di Perairan Waduk Cirata, Provinsi Jawa Barat
Nama : Muhammad Amien H NIM : P052040371
Disetujui
Komisi Pembimbing
Dr. Ir. D. Djokosetiyanto, DEA Dr. Ir. Suprihatin, Dipl. Eng
Ketua Anggota
Diketahui
Plh, Ketua Program Studi Pengelolaan Dekan Sekolah Pascasarjana Sumberdaya Alam dan Lingkungan
Dr. Ir. Etty Riani, MS Prof. Dr. Ir. Khairil A. Notodiputra, MS
PRAKATA
Puji dan syukur penulis panjatkan kepada Allah SWT atas segala karunianya sehingga karya ilmiah ini berhasil diselesaikan dengan judul Kajian Kandungan Logam Berat Timbal (Pb) dan Seng (Zn) Pada Air, Sedimen, dan Makrozoobentos di Perairan Waduk Cirata, Provinsi Jawa Barat. Penelitian ini dilaksanakan sejak bulan Desember 2006 - Maret 2007 di Perairan Waduk Cirata Provinsi Jawa Barat.
Pada kesempatan yang berbahagia ini penulis mengucapkan banyak terima kasih kepada:
1. Dr. Ir. D. Djokosetiyanto, DEA dan Dr. Ir. Suprihatin, Dipl. Eng selaku komisi pembimbing yang telah meluangkan waktu dan dengan kesabaranya dalam membimbing sehingga penulis dapat menyelesaikan penulisan tesis.
2. Ibu Dr. Ir. Etty Riani, MS selaku penguji luar komisi atas masukannya bagi perbaikan tesis ini.
3. Bapak Dr. Ir. Surjono H. Sutjahjo, MS selaku Ketua Program Studi Pengelolaan Sumberdaya Alam dan Lingkungan (PSL) dan stafnya yang telah banyak memberikan pelayanan dan bantuan kepada penulis selama pendidikan di PS-PSL sehingga penulis dapat menyelesaikan studi.
4. Ayahanda Hadaming dan Ibunda Hasmawati yang telah membesarkan dengan penuh cinta kasih, mendidik, mendoakan, dan memberikan dukungan atau kesempatan kepada penulis dalam menyelesaikan pendidikan selama ini. 5. Istri tercinta Tashria Nanrang, anak-anak saya yaitu: Dzun-nuun Muh.
Taqiyuddin Yahya, Miqdad Muh. Yasin, dan Dzulkarnain Al-Islam, yang selalu mendokan dan penuh kesabaran dalam menemani dalam menempuh pendidikan sampai menyelesaikan studi.
6. Adik Suryani yang telah banyak memberikan bantuan dan dukungan selama menempuh pendidikan pada Program Magister PS-PSL di Institut Pertanian Bogor (IPB).
7. Pemda Provinsi Kalimantan Timur dan Kota Tarakan yang telah memberikan bantuan beasiswa simultan selama pendidikan sehingga penulis dapat menyelesaikan studi ini.
8. Bapak Ir. H. Aziz Kahar Muzakkar, MS yang telah memberikan bantuan dan motivasi selama pendidikan
9. Rekan-rekan di Pondok Pesantren Hidayatullah Cabang Kota Tarakan Kalimantan Timur
10. Rekan-rekan mahasiswa angkatan tahun 2005 PS-PSL IPB.
Bogor, Nopember 2007
RIWAYAT HIDUP
Penulis dilahirkan di Allu Kabupaten Bulukumba Provinsi Sulawesi- Selatan pada tanggal 14 April 1974 dari ayah Hadaming dan ibu Hasmawati. Penulis merupakan anak pertama dari 3 bersaudara.
DAFTAR ISI
Halaman
DAFTAR TABEL ... xii
DAFTAR GAMBAR ... xiii
DAFTAR LAMPIRAN ... xv
1. PENDAHULUAN ... 1
1.1. Latar Belakang ... 1
1.2. Kerangka Pemikiran ... 4
1.3. Perumusan Masalah ... 7
1.4. Tujuan Penelitian ... 8
1.5. Manfaat Penelitian ... 8
1.6. Hipotesis ... 9
II. TINJAUAN PUSTAKA ... 10
2.1. Perairan Waduk ... 10
2.2. Pencemaran Perairan ... 12
2.3. Sumber Logam Berat ... 14
2.4. Logam Berat ... 17
2.4.1. Timbal (Pb) ... 17
2.4.2. Seng (Zn) ... 20
2.5. Logam Berat Dalam Ekosistem Perairan ... 21
2.6. Logam Berat Dalam Sedimen ... 23
2.7. Cara Penyerapan Logam Oleh Organisme ... 26
2.8. Hewan Bentos ... 27
2.8.1. Pengertian Bentos ... 27
2.8.2. Struktur Komunitas Makrozoobentos ... 29
III. METODE PENELITIAN ... 32
3.1. Tempat dan Waktu Penelitian ... 32
3.2. Bahan dan Alat ... 32
3.3. Prosedur Kerja ... 32
3.4. Analisis Data ... 35
3.4.1. Kondisi Perairan Secara Fisika-Kimia, dan Biologi Air ... 35
3.4.2. Hubungan Antara Kandungan Logam Pb dan Zn Dalam Air dan Sedimen, Dengan Makrozoobentos ... 37
IV. HASIL DAN PEMBAHASAN ... 39
4.1. Kondisi Perairan Secara Fisika-Kimia Air ... 39
4.1.1. Suhu ... 39
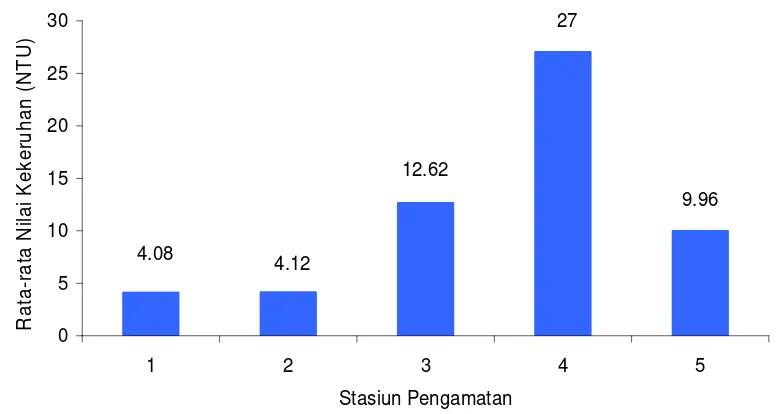
4.1.2. Kekeruhan ... 40
4.1.3. Alkalinitas ... 42
4.1.4. Nilai pH ... 43
4.1.5. Amonia ... 45
4.1.6. Nitrat ... 47
4.1.8. Kandungan Logam Pb dan Zn Dalam Air, Sedimen, dan
Makrozoobentos ... 49
4.1.8.1. Timbal (Pb) ... 49
4.1.8.2. Seng (Zn) ... 59
4.2. Kondisi Perairan Secara Biologi ... 63
4.2.1. Komposisi Relatif dan Kepadatan Makrozoobentos ... 64
4.2.2. Indeks Keanekaragaman (H|) dan Keseragaman Jenis (E) ... 68
4.2.3. Dominansi Jenis (C) ... 71
4.3. Keterkaitan Antar Parameter ... 72
4.3.1. Hubungan Kandungan Logam Pb dan Zn Dalam Air Dengan Sedimen ... 72
4.3.2. Hubungan Kandungan Logam Pb dan Zn Dalam Air Dengan Makrozoobentos ... 75
4.3.3. Hubungan Kandungan Logam Pb dan Zn Dalam Sedimen Dengan Makrozoobentos ... 79
4.3.4. Hubungan Total Kandungan Logam Pb dan Zn Dalam Air dan Sedimen Dengan Makrozoobentos ... 81
V. KESIMPULAN DAN SARAN ... 83
5.1. Kesimpulan ... 83
5.2. Saran ... 83
DAFTAR PUSTAKA ... 85
LAMPIRAN ... 91
DAFTAR TABEL
Halaman
1. Waduk serbaguna di Indonesia ... 11 2. Nama dan ukuran partikel sedimen menurut Skala Went Worth ... 24 3. Klassifikasi ukuran partikel sedimen ... 24 4. Klassifikasi hewan bentos berdasarkan ketahanannya terhadap
pencemaran air ... 30 5. Beberapa kriteria kualitas air berdasarkan indeks keanekaragaman
Shannon-Wiener dari hewan bentos makro ... 31 6. Parameter-parameter kualitas air, sedimen, dan biota air yang diamati . 35 7. Hasil analisis korelasi dan regresi antara logam Pb dan Zn dalam
air (x) dengan sedimen (y) ... 73 8. Hasil korelasi dan regresi antara kandungan logam Pb dan Zn dalam
air (x) dengan makrozoobentos (y) ... 76 9. Hasil analisis korelasi dan regresi antara kandungan logam Pb dan Zn
dalam sedimen (x) dengan makrozoobentos (y) ... 79
DAFTAR GAMBAR
Halaman
1. Diagram kerangka pemikiran penelitian ... 6
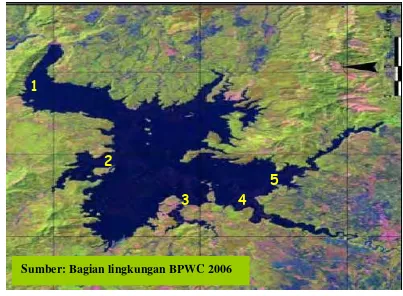
2. Peta lokasi pengambilan sampel di Waduk Cirata ... 34
3. Rata-rata suhu pada setiap stasiun pengamatan ... 39
4. Rata-rata kekeruhan pada setiap stasiun pengamatan ... 41
5. Rata-rata alkalinitas pada setiap stasiun pengamatan ... 43
6. Rata-rata nilai pH pada setiap stasiun pengamatan ... 44
7. Rata-rata amonia (NH3-) pada setiap stasiun pengamatan ... 46
8. Rata-rata nitrat (NO3-) pada setiap stasiun pengamatan ... 47
9. Rata- rata nitrit (NO2-) pada setiap stasiun pengamatan ... 49
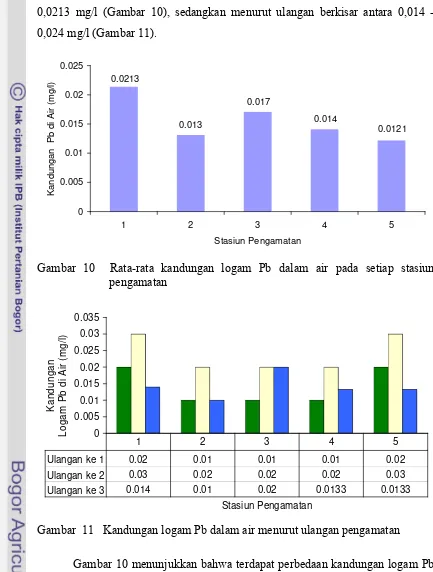
10. Rata-rata kandungan logam Pb dalam air pada setiap stasiun pengamatan ... 50
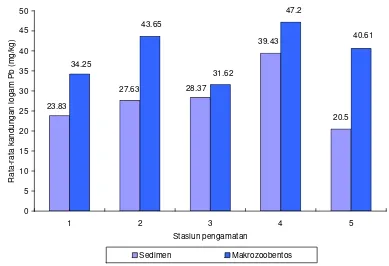
11. Kandungan logam Pb dalam air menurut ulangan pengamatan ... 50
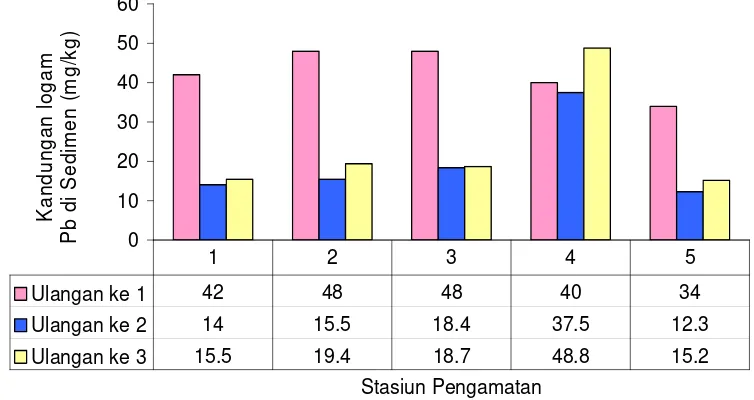
12. Rata-rata kandungan logam Pb dalam sedimen dan makrozoobentos di setiap stasiun pengamatan ... 53
13. Kandungan logam Pb dalam sedimen menurut ulangan pengamatan ... 54
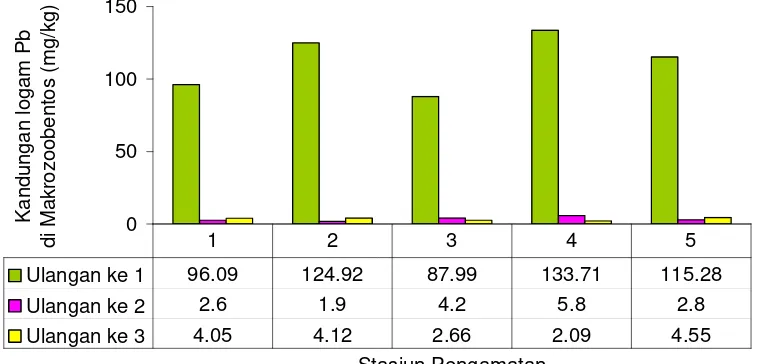
14 Kandungan logam Pb dalam makrozoobentos menurut ulangan pengamatan ... 56
15. Rata-rata kandungan logam Zn dalam air pada setiap stasiun pengamatan ... 60
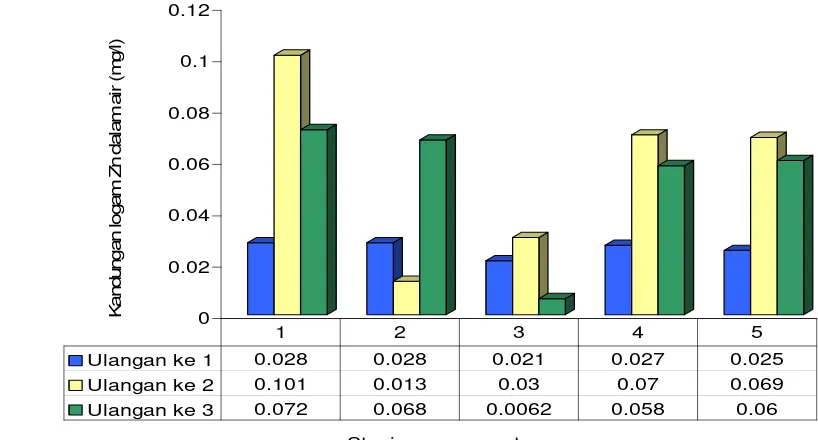
16. Kandungan logam Zn dalam air menurut ulangan pengamatan ... 60
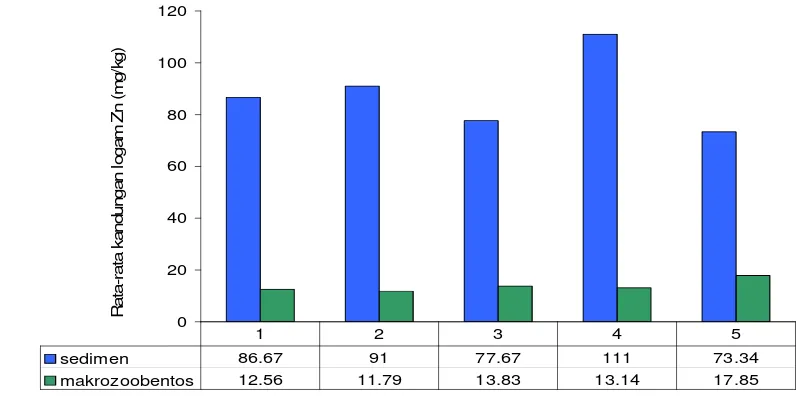
17. Rata-rata kandungan logam Zn dalam sedimen dan makrozoobentos di setiap stasiun pengamatan ... 61
18. Kandungan logam Zn dalam sedimen menurut ulangan pengamatan ... 62
19. Kandungan logam Zn dalam makrozoobentos menurut ulangan pengamatan ... 62
20. Komposisi relatif kelas makrozoobentos di perairan Waduk Cirata ... 65
21. Rata-rata kepadatan makrozoobentos pada setiap stasiun pengamatan ... 66
22. Kepadatan makrozoobentos menurut ulangan pengamatan ... 66
23. Rata-rata keanekaragaman jenis makrozoobentos pada setiap stasiun pengamatan ... 69
24. Rata-rata indeks keseragaman makrozoobentos di setiap stasiun
pengamatan ... 69 25. Rata-rata indeks dominansi makrozoobentos di setiap stasiun
pengamatan ... 71
DAFTAR LAMPIRAN
Halaman
1. Hasil pengukuran nilai parameter fisika-kimia air berdasarkan
stasiun dan ulangan selama penelitian di Waduk Cirata ... 91 2. Data (debit air) total air masuk (m3/detik) di perairan Waduk Cirata
berdasarkan ulangan selama pengamatan ... 93 3. Kandungan logam Pb pada air, sedimen, dan makrozoobentos menurut
stasiun dan ulangan di perairan Waduk Cirata ... 94 4. Kandungan logam Zn pada air, sedimen, dan makrozoobentos menurut
stasiun dan ulangan di perairan Waduk Cirata... 95 5. Jumlah jenis makrozoobentos dari kelas Gastropoda yang terdapat
di Waduk Cirata ... 96 6. Hasil identifikasi jenis makrozoobentos yang diperoleh pada setiap
stasiun pengamatan di perairan Waduk Cirata ... 97 7. Hasil analisis regresi kandungan logam Pb dan Zn dalam air dengan
sedimen di perairan Waduk Cirata ... 98 8. Hasil analisis regresi kandungan logam berat Pb dan Zn dalam air
dengan Makrozoobentos ... 99 9. Hasil analisis regresi kandungan logam Pb dan Zn dalam sedimen
dengan makrozoobentos ... 100 10. Data output Program SPSS korelasi antara logam Pb dan Zn dalam air,
sedimen, dan makrozoobentos pada setiap stasiun pengamatan ... 101 11. Hasil total korelasi dan regresi kandungan logam Pb dan Zn dalam air
dengan sedimen, air dengan makrozoobentos, dan sedimen
dengan makrozoobentos ... 106
I. PENDAHULUAN
1.1. Latar Belakang
Waduk adalah genangan air besar yang sengaja dibuat dengan membendung aliran sungai, sehingga dasar sungai tersebut yang menjadi bagian terdalam dari sebuah waduk. Waduk merupakan penampung alami dalam pengumpulan unsur hara, bahan padatan dan bahan kimia toksik yang akhirnya mengendap di dasar perairan dan lebih banyak terkontaminasi dari pada sungai, kontaminasi terjadi dari unsur minyak, pestisida, dan substansi toksik yang dapat merusak kehidupan di dasar perairan dan ikan yang hidup di dalamnya. Kondisi hujan asam dan asam dari aliran air yang mengalir ke danau atau waduk, merupakan masalah yang serius pada danau atau waduk karena asam dapat tertimbun di dalamnya (Darmono, 2001).
Waduk Cirata merupakan salah satu waduk yang dibangun di DAS Citarum pada tahun 1988 yang terletak antara Waduk Saguling dan Waduk Jatiluhur dan pada saat pembangunannya ditujukan sebagai Pembangkit Listrik Tenaga Air (PLTA). Waduk Cirata berada pada ketinggian 221m dpl mempunyai luas 6.200 Ha, dan kedalam rata-rata 34,9 m
Waduk Cirata mempunyai karakteristik ekosistem perairan umum yang memiliki berbagai potensi, seperti: tempat budidaya ikan (Sistem Keramba Jaring Apung), sumber pengairan, tempat rekreasi (pariwisata), dan sarana perhubungan. Di antara potensi tersebut yang paling berkembang, yaitu: budidaya ikan sistem KJA yang menempati sebagian besar perairan Waduk Cirata (± 40.000 unit). Secara umum potensi tersebut daya gunanya sangat tergantung pada kualitas air waduk, dimana jika kualitas air menurun atau tercemar akan mengurangi atau menghilangkan potensi-potensi tersebut. Oleh sebab itu, maka kualitas air waduk dipertahankan pada kisaran kondisi yang mampu mendukung berbagai kegiatan yang diperlukan (Garno, 2002).
yang merupakan bahan asing bagi perairan alami akibat aktifitas manusia, akan menyebabkan terjadinya pencemaran perairan yang dapat mengakibatkan perubahan sifat fisik, kimia dan biologi perairan tersebut.
Pergeseran atau berubahnya tatanan lingkungan dari kondisi semula ke kondisi yang buruk dapat terjadi sebagai akibat masuknya bahan-bahan pencemar. Suatu lingkungan hidup dikatakan tercemar apabila telah terjadi perubahan-perubahan dalam tatanan lingkungan tersebut, sehingga tidak sama lagi dengan bentuk aslinya, sebagai akibat dari masuknya suatu zat atau benda asing ke dalam lingkungan (Palar, 2004). Pada ekosistem perairan seperti sungai, danau, waduk dan pesisir serta tambak, pencemaran dapat terjadi karena masuknya limbah dari berbagai kegiatan manusia seperti: domestik, industri, peternakan, pertanian dan perikanan. Limbah yang masuk ke ekosistem perairan dikategorikan dalam 2 jenis, yaitu: limbah anorganik yang sulit atau tidak dapat terurai oleh
mikroorganisme dan limbah organik yang mudah terurai oleh mikroorganisme. Limbah logam berat yang masuk ke perairan Waduk Cirata berasal dari:
industri, pertanian, dan permukiman di sekitar Kabupaten Bandung, Cianjur, dan Purwakarta yang mengakibatkan pencemaran logam berat berada dalam taraf yang mengkhawatirkan. Menurut hasil pemantauan kualitas air Waduk Cirata Desember 2002 yang dilakukan tim terpadu dari instansi terkait di Pemda Jawa Barat dengan ITB Bandung dikemukakan bahwa konsentrasi beberapa jenis logam berat seperti: Pb (0,010-0,015 mg/l), Zn (0,019-0,038 mg/l ), Cr (0,002-0,005 mg/l), Cu (0,0034-0,0068 mg/l), Cd (0,006 mg/l), As (0,025-0,038 mg/l), dan Hg (0,00012-0,00017 mg/l) yang terdapat di Waduk Cirata meskipun konsentrasinya belum melewati batas ambang baku mutu (PP. No. 82 Tahun 2001), tetapi berpotensi atau mengindikasikan kearah pencemaran logam berat tersebut (DKP, 2002).
sebagai beriku: Cr (16,25 mg/kg), Cu (17,99 mg/kg), Pb (38,82 mg/kg), dan Zn (57,10 mg/kg). Hal tersebut menunjukkan bahwa logam berat Pb dan Zn mempunyai konsentrasi yang tinggi.
Menurut catatan BPWC (Badan Pengelola Waduk Cirata) tahun 2004, bahwa limbah bahan anorganik yang masuk di Waduk Cirata berasal dari industri di bagian hulu Sungai Citarum (berasal dari mata air gunung Wayang) dan kebanyakan industri tersebut terdapat di daerah cekungan Bandung yang membuang limbahnya ke Sungai Citarum yang akhirnya masuk kedalam Waduk Cirata.
Pada limbah industri seringkali terdapat bahan pencemar yang sangat membahayakan seperti logam berat (Palar, 2004). Air limbah industri umumnya mengandung unsur logam berat beracun seperti Hg, Cd, Pb, Cu, Zn, dan Ni (Sanusi, 1985). Logam berat yang masuk ke dalam peairan akan mencemari perairan. Selain mencemari perairan, logam berat juga akan mengendap pada sedimen yang mempunyai waktu tinggal (residence time) sampai ribuan tahun dan logam berat juga akan terakumulasi dalam tubuh mahluk hidup melalui beberapa jalan yaitu; melalui saluran pernafasan, saluran makanan, dan melalui kulit (Darmono, 2001).
Perairan waduk merupakan media hidup beranekaragam organisme akuatik yang mempunyai batas-batas toleransi tertentu terhadap bahan pencemar. Salah satu hewan air yang sensitif terhadap perubahan kualitas lingkungan perairan yaitu: bentos. Pada ekosistem perairan, bentos dapat digunakan sebagai indikator biologi tingkat pencemaran perairan, karena sifatnya hidup menetap atau pergerakannya sangat lambat di permukaan atau dalam substrat pada dasar perairan dan distribusi makrozoobentos yang luas. Beberapa jenis organisme makrozoobentos mempunyai daya tahan tinggi terhadap kualitas air yang jelek, sehingga organisme tersebut dapat digunakan sebagai indikator kualitas air suatu perairan (Wilhm, 1975). Perubahan komunitas makrozoobentos secara umum disebabkan oleh masukan bahan organik, bahan kimia beracun, dan perubahan substrat dasar (APHA, 1989).
Adanya kecendrungan peningkatan pencemaran yang terjadi di perairan Waduk Cirata, maka perlunya dilakukan pengkajian tentang kandungan logam berat Pb dan Zn pada air, sedimen, dan makrozoobentos.
1.2. Kerangka Pemikiran
Upaya pembangunan ditempuh dengan mendayagunakan sumberdaya alam yang tersedia pada setiap wilayah maupun yang berasal dari luar. Pemanfaatan sumberdaya alam dan lingkungan tersebut diupayakan untuk memenuhi kebutuhan hidup manusia, yang diselenggarakan secara rasional dan bijaksana, yaitu dengan tetap menjaga kelestarian lingkungan disekitarnya. Kegiatan pembangunan seperti domestik (permukiman), pertanian, transfortasi, industri, dan lainnya dengan mendayagunkan sumberdaya alam, akan menghasilkan limbah. Limbah tersebut dapat berasal dari proses pembangunan yang memanfaatkan sumberdaya alam sebagai bahan baku, bahan tambahan, maupun bahan katalis dan sangat mungkin terdiri dari unsur logam berat.
Sumber logam berat banyak berasal dari industri dan juga berasal dari lahan pertanian yang menggunakan pupuk atau antihama yang mengandung logam serta buangan limbah domestik (permukiman penduduk). Perhitungan besarnya beban pencemaran yang masuk ke perairan tergantung pada kegiatan yang ada di sekitar perairan tersebut. Untuk daerah permukiman beban pencemaran biasanya diperhitungkan melalui kepadatan penduduk dan rata-rata buangan limbah perorangnya. Untuk kegiatan industri, jenis limbah yang dihasilkan yaitu; limbah cair, gas, dan limbah padat. Limbah cair yang dihasilkan sangat bervariasi tergantung jenis dan ukuran industri, derajat penggunaan air, dan derajat pengolahan air limbah yang ada, sedangkan limbah padat (sampah) dan gas merupakan beban pencemaran yang dapat masuk ke perairan baik secara langsung maupun tidak langsung dapat membahayakan biota yang terdapat di dalamnya.
bermuara ke perairan danau atau waduk dan pengaruh logam berat terhadap kualitas air dapat merubah sifat fisika-kimia dan biologi perairan. Pola arus air sungai akan menentukan keberadaan logam berat yang terkandung dalam air dan sedimen. Keberadaan logam berat tersebut akan menimbulkan dampak terhadap lingkungan perairan waduk, yaitu peningkatan kandungan logam berat di dalam perairan yang akan mengakibatkan perubahan dan penurunan kualitas lingkungan perairan. Perubahan dan penurunan kualitas lingkungan tersebut akan mempengaruhi organisme yang hidup dan berkembang biak di lingkungan tersebut.
Setiap spesies organisme perairan mempunyai daya toleransi yang berbeda-beda terhadap kondisi perubahan lingkungan. Tinggi rendahnya kadar pencemaran logam berat akan mengakibatkan terjadinya perubahan struktur komunitas organisme suatu perairan dan logam berat yang terkandung dalam sedimen akan diserap oleh makrozoobentos, baik secara langsung maupun tidak langsung. Secara langsung, makrozoobentos menyerap logam berat lewat tubuhnya dan secara tidak langsung, makrozoobentos menyerap logam melalui makanan yang terakumulasi logam berat. Logam berat termasuk sebagai zat pencemar karena sifatnya tidak dapat diuraikan secara biologis, sehingga dapat tersebar jauh dari tempatnya semula (sumber) dan kadar logam berat akan mengalami pengenceran, apabila semakin jauh dari sumbernya yang di bawa oleh aliran air, sehingga konsentrasi logam berat semakin jauh dari limbah pembuangannya. Pengetahuan tentang seberapa jauh tingkat pencemaran yang terjadi di Waduk Cirata perlu diketahui dan dapat dijadikan atau digunakan sebagai dasar di dalam pengelolaan dan pemanfaatan perairan tersebut. Adapun kerangka pemikiran dapat dilihat pada Gambar 1.
Gambar 1. Diagram kerangka pemikiran penelitian Keterangan :
KLB = Konsentrasi Logam Berat KBM = Konsentrasi Baku Mutu
Aktivitas Manusia
Domestik (Rumah Tangga)
Industri Pertanian
Sumber Pencemar
Pencemaran Sungai
Penurunan Kualitas Perairan
Struktut Komunitas Makrozoobentos (Kepadatan, Indeks keanekaragaman, Keseragaman, Indeks Dominansi)
Peningkatan Kandungan logam berat (Pb & Zn) pada Air, Sedimen & Makrozoobentos
KLB>KBM atau
KLB<KBM Pencemaran Waduk Cirata
1.3. Perumusan Masalah
Kemajuan teknologi yang diciptakan manusia telah banyak memberikan kemudahan-kemudahan bagi manusia. Sebagai contoh kemajuan dalam teknologi kimia yang diwujudkan dengan penemuan-penemuan pestisida, farmasi, maupun yang berhubungan langsung dengan industri makanan, minuman, dan sebagainya. Di samping memberikan keuntungan dari pesatnya teknologi juga memberikan dampak yang kurang baik bagi manusia. Limbah dari proses industri kadangkala mempunyai daya racun yang kuat dan bahkan menyebabkan kematian dari tumbuhan, hewan, maupun manusia.
Waduk Cirata merupakan salah satu waduk yang kualitas perairannya diduga sudah tercemar berbagai jenis logam berat, yang disebabkan banyaknya limbah yang masuk ke perairan tersebut yang dibawa oleh aliran sungai yang bermuara di dalamnya, dan salah satunya adalah Sungai Citarum. Sumber bahan pencemar (limbah) yang memasuki DAS Citarum dan akhirnya memasuki Waduk Cirata berasal dari Pengalengan, Kawasan industri di Majalaya, Banjaran, Ranjaekek, Deyeuhkolot, Ujung Berung, Cimahi, dan Padalarang (limbah dibuang saat hujan atau saat banjir), limbah rumah tangga (deterjen, dan lain-lain), dan pertanian (DKP, 2002).
Dengan semakin meningkatnya aktivitas manusia di sekitar waduk tersebut, akan meningkatkan kandungan logam berat di Waduk Cirata. Bahan buangan yang mengandung logam berat akan mempengaruhi kualitas lingkungan perairan waduk dan membahayakan organisme perairan, serta dapat mengganggu kesehatan atau bahkan mengakibatkan kematian bagi manusia yang mengkonsumsinya, seperti yang pernah terjadi di Jepang (penyakit mina mata). Toksikan yang sangat berbahaya umumnya berasal dari buangan industri, terutama yang melibatkan logam berat dalam prosesnya
Keberadaan logam-logam berat di perairan dalam batas tertentu masih dapat ditoleransi oleh biota yang mempunyai tingkat toleransi yang tinggi terhadap toksikan. Respon yang ditimbulkan oleh biota perairan terhadap senyawa logam berat (toksikan) bermacam-macam diantaranya menimbulkan kematian, bioakumulasi, perubahan tingkah laku dan sebagainya. Terhadap komunitas logam berat akan berdampak pada perubahan komposisi spesies dan
penurunan jumlah atau hilangnya spesies dari komunitas tersebut (Hawkes, 1979 dalam Yoga dan Sudarso, 1999).
Keberadaan logam berat dalam perairan akan berpengaruh negatif terhadap kehidupan biota. Logam berat yang terikat dalam tubuh organisme akan mempengaruhi aktivitas dari organisme tersebut. Bagi ikan, udang, dan moluska zat pencemar akan mempengaruhi syaraf, sifat genetis atau fisiologis serta perilaku seperti food habitat migration. Pada makrozoobentos yang berada di sungai atau di waduk mengalami akumulasi berbagai jenis logam berat. Akumulasi tersebut sehubungan dengan kualitas air, sedimen terdapat berbagai jenis logam.
Berdasarkan hal tersebut maka beberapa permasalahan dapat dirumuskan pada penelitian ini, antara lain:
1. Akibat adanya aktivitas manusia, seperti industri, domestik atau rumah tangga (deterjen, dan lain-lain), dan pertanian akan meningkatkan kandungan logam berat Timbal (Pb) dan Zeng (Zn) di Waduk Cirata.
2. Keberadaan logam berat di perairan dapat mengakibatkan akumulasi logam berat dalam tubuh makrozoobentos.
1.4. Tujuan penelitian
Tujuan dari penelitian ini adalah:
1. Mengkaji kandungan logam Pb dan Zn dalam air, sedimen, dan makrozoobentos di perairan Waduk Cirata
2. Mengetahui struktur komunitas makrozoobentos yang terdapat di perairan Waduk Cirata
3. Mengetahui hubungan antara kandungan logam Pb dan Zn dalam air dengan sedimen, dan makrozoobentos
1.5. Manfaat Penelitian
Adapun manfaat penelitian ini adalah:
2. Sebagai bahan informasi mengenai tingkat pencemaran logam berat di Waduk Cirata.
3. Sebagai bahan masukan bagi pihak yang berkepentingan di daerah tersebut, terutama untuk memantau, memelihara, serta memanfaatkan waduk dengan lebih baik, sehingga dapat berlangsung secara berkelanjutan.
1.6. Hipótesis
Hipotesis yang akan diajukan pada penelitian ini adalah:
1. Kandungan logam Pb dan Zn dalam air telah melewati ambang batas baku mutu peruntukannya.
2. Struktur komunitas makrozoobentos mengalami perubahan akibat bahan pencemar yang masuk di perairan Waduk Cirata
3. Terdapat hubungan yang erat antara kandungan logam Pb dan Zn dalam air, sedimen, dan makrozoobentos
II.
TINJAUAN PUSTAKA
2.1. Perairan Waduk
Habitat air tawar dapat dibagi dua, yaitu (1) perairan menggenang atau habitat lentik, misalnya waduk, danau, kolam, rawa, dan (2) habitat perairan mengalir atau habitat lotik, misalnya mata air dan sungai (Koesoebiono, 1979). Habitat lotik terbagi lagi menjadi dua zone, yaitu habitat lotik dingin, dangkal dan sering mempunyai dasar aliran yang berbatu-batu dan habitat lotik hangat, lebih dalam dengan dasar yang berlumpur.
Salah satu perairan tergenang yang mempunyai fungsi multi guna, yaitu: waduk. Waduk adalah badan air yang terbentuk karena pembendungan aliran sungai dan salah satu bentuk reservoir tempat menampung aliran sungai dalam satu sistem jaringan sungai dalam suatu sistem DAS. Waduk merupakan badan air yang karakteristik fisik, kimia, dan biologi berbeda dari sungai yang di bendungnya serta kualitas perairan waduk lebih stabil di bandingkan dengan sungai asalnya (Ilyas dkk, 1990).
Suwignyo (1981) menyatakan bahwa waduk dapat dibentuk dari sungai (river in reservoir) maupun dari rawa (food lake), karena bentuk perairan waduk yang selintas mirip dengan perairan danau, maka waduk dikenal juga sebagai danau buatan manusia. Waduk dikatakan sebagai danau buatan manusia, karena dibuat dan diciptakan oleh manusia untuk tujuan tertentu. Tujuan pembangunan waduk antara lain: sebagai pencegah banjir, Pembangkit Tenaga Listrik (PLTA), pemasok air untuk kepentingan irigasi/pertanian, industri, permukiman, perikanan (Keramba Jaring Apung), dan pariwisata.
Salah satu waduk yang terdapat di Jawa Barat adalah Waduk Cirata. Menurut Sudarjat (2000), menyatakan bahwa secara umum Waduk Cirata berfungsi sebagai sumberdaya air untuk kegiatan dibidang: (1) pertanian (sumber air baku), (2) industri (sumber air baku untuk kegiatan industri), (3) penyedia air baku untuk rumah tangga (reservoir air), (4) energi (penggerak mesin pembangkit listrik), (5) perikanan tangkap, (6) perikanan budidaya (akuakultur), (7) transfortasi (sarana angkutan), (8) pengendalian banjir, (9) rekreasi, dan (10) tempat pembuangan limbah.
Tabel 1. Waduk serbaguna di indonesia
Luas Kedalaman Kedalaman Ketinggian Fungsi Tahun (ha) Maksimum Rata-rata (m dpl) Utama dibangun Tempat dan
Nama Waduk
(m) (m)
Jawa Barat
Saguling 5.34 90 18 625 E,F,I 1985
Cirata 6.2 106 34 250 E,F,I 1987
Jatiluhur (Juanda) 8.3 95 37 110 W,I,E,F 1965
Jawa Tengah
Wonogiri 8.8 28 8 140 I, F, E 1981
Wadaslintang 1.46 85 30 115 I, F, E 1987
Kedungombo 6.1 50 16 100 I, F, E 1989
PB. Soedirman 1.5 - 13 231 E,F,1 1989
Sempor 1.3 45 - 77 I,F,E 1987
Jawa Timur
Karangkates 1.5 70 23 270 I, E, F 1972
Selorejo 400 46 16 600 E, I, F 1970
Lahor 260 50 14 300 I, E, F 1977
Wlingi 380 28 6 163 I, E, F 1983
Bening 570 10 8 11 I, F 1933
Sengguruh 290 24 7 296 E, I 1987
Nusa Tenggara
Batujai 890 14 2 4 I, F, W 1983
Kalimantan Selatan
Riam Kanan 9.2 50 18 - I, E, F 1983
Lampung
Way Rarem 1.4 25 6 60 I,F 1982
Way Jepara 220 - 15 - I,F 1976
Sumber: Ilyas dkk, (1990)
Waduk merupakan penampung alami dalam pengumpulan unsur hara, bahan padat tersuspensi, dan bahan kimia toksik yang akhirnya mengendap di dasarnya. Penampungan bahan-bahan tersebut berlangsung bertahun-tahun pada waduk, sehingga proses pendangkalan tidak dapat dihindari. Kontaminasi terjadi dari unsur, minyak, pestisida, dan substansi toksik yang dapat merusak di dasar waduk dan ikan yang hidup di dalamnya.
Menurut Koswara (1999) dalam Djunaedi (2000) menyatakan bahwa sumber atau penyebab permasalahan waduk atau danau yaitu: pembuangan limbah organik biodegradable, pembuangan nutrien dari air limbah, pencemaran nutrien tersebar (non-point sources pollution) terutama dari pertanian, hujan asam yang disebabkan oleh polutan udara seperti SO2 dan NOx, pembuangan zat-zat toksik
dari industri atau pertanian, dan pembuangan panas.
Waduk selalu menerima masukan air dari daerah sekitarnya (DAS), dengan demikian waduk cenderung menerima bahan-bahan terlarut yang terangkut bersamaan dengan air yang masuk. Konsentrasi ionik perairan waduk merupakan resultante ionik dari air yang masuk. Adanya kegiatan manusia disekitar DAS seringkali menyebabkan pencemaran perairan waduk. Pertumbuhan penduduk yang cepat dan diikuti dengan perrtumbuhan industri dan kegiatan lainnya akan menghasilkan limbah yang kemudian dibuang ke lingkungan. Limbah kemudian dapat masuk ke waduk melalui aliran sungai atau rembesan air tanah.
2.2. Pencemaran Perairan
Pencemaran air adalah penurunan kualitas air sehingga air tersebut tidak (kurang) memenuhi syarat atau bahkan mengganggu pemanfaatan. Menurut Organisasi Kesehatan Dunia (World Health Organitation atau WHO) air dinyatakan tercemar apabila terjadi perubahan komposisi atau keadaan kandungannya sebagai akibat kegiatan manusia secara langsung atau tidak langsung, sehingga air tersebut tidak atau kurang sesuai dengan fungsi atau tujuan pemanfaatan asalnya. Di dalam UU Nomor 4 tahun 1982 mengenai lingkungan hidup, pencemaran lingkungan didefinisikan sebagai dimasukkannya makhluk hidup, zat energi dan atau komponen lain ke dalam lingkungan oleh kegiatan manusia atau proses alam, sehingga kualitas lingkungan turun sampai pada tingkat tertentu yang menyebabkan lingkungan menjadi kurang atau tidak berfungsi lagi sesuai dengan peruntukannya.
Menurut Peraturan Pemerintah Republik Indonesia Nomor 82 tahun 2001 tentang pengendalian pencemaran air dan pengelolaan kualitas air, dinyatakan bahwa pencemaran air adalah masuk atau dimasukkannya mahluk hidup, zat, energi, dan atau komponen lain ke dalam air oleh kegiatan manusia, sehingga kualitas air turun sampai ketingkat tertentu yang menyebabkan air tidak berfungsi lagi sesuai dengan peruntukan.
Menurut Haynes (1978) dalam Nurifdinsyah (1993) mengemukakan bahwa pencemaran terhadap badan air dapat mengakibatkan masuknya zat-zat beracun, bertambahnya padatan tersuspensi, terjadinya deoksidasi dan naiknya temperatur. Pencemaran perairan yang disebabkan oleh kegiatan di darat dapat digolongkan menjadi empat kategori, yaitu (1) pencemaran yang disebabkan oleh limbah industri (industrial pollution), (2) pencemaran yang disebabkan karena sampah atau limbah rumah tangga (sewage pollution), (3) pencemaran disebabkan karena sedimentasi (sedimentation pollution), dan (4) pencemaran yang disebabkan karena kegiatan pertanian (agricultural pollution).
Berdasarkan sifat toksiknya, pencemaran dibedakan menjadi dua, yaitu (Effendi, 2003):
1. Polutan tak toksik
berlebihan sehingga dapat mengganggu kesetimbangan ekosistem melalui perubahan proses fisika-kimia perairan.
2. Polutan toksik
Polutan toksik dapat mengakibatkan kematian (lethal) maupun bukan kematian (sub-lethal), misalnya terganggunya pertumbuhan, tingkah laku, dan karakteristik morfologi berbagai organisme akuatik. Polutan toksik ini biasanya berupa bahan-bahan yang bukan bahan alami, misalnya pestisida, detergen, dan bahan-bahan yang lain.
2.3. Sumber Logam Berat
Istilah logam secara fisik mengandung suatu arti yang merupakan konduktor listrik yang baik dan mempunyai konduktivitas panas, rapatan, kemudahan ditempa, kekerasan, dan keelektropositifan yang tinggi. Meskipun demikian, beberapa unsur (boron, silikon, germanium, arsen, dan tellirium) yang diketahui sebagai metaloid, mempunyai satu atau lebih sifat-sifat tersebut. Tetapi tidaklah cukup membedakannya dalam kekhasan untuk memungkinkan suatu pemisahan yang persis logam atau bukan logam. Lebih jauh, bentuk alotrofik dari beberapa unsur di garis batas mungkin juga memperlihatkan sifat-sifat yang berbeda (Wittman, 1979 dalam Connel dan Miller, 2006)
Logam berasal dari kerak bumi berupa bahan-bahan murni, organik, dan anorganik. Secara alami siklus perputaran logam adalah dari kerak bumi kemudian ke lapisan tanah, kemudian ke mahluk hidup (tanaman, hewan, dan manusia), ke dalam air, mengendap dan akhirnya kembali ke kerak bumi (Darmono, 1995).
logam lainnya, dan untuk logam yang padat, dapat ditempa dan dibentuk (Palar, 2004).
Logam adalah unsur alam yang dapat di peroleh dari laut, dari erosi batuan tambang, vulkanisme dan sebagainya. Logam dapat dibagi kedalam 3 kelompok, yaitu:
1. Logam ringan (seperti natrium, kalium, dan sebagainya), biasanya sebagai kation aktif di dalam larutan encer.
2. Logam transisi (seperti besi, tembaga, kobalt, dan mangan) diperlukan dalam konsentrasi yang rendah, tetapi dapat menjadi racun dalam konsentrasi yang tinggi.
3. Logam berat dan metaloid (seperti raksa, timah hitam, timah, selenium, dan arsen), umumnya tidak diperlukan dalam kegiatan metabolisme dan sebagai racun bagi sel pada konsentrasi rendah.
Logam-logam di atmosfir berdasarkan sumber alamiahnya berasal dari: (1) debu-debu dari kegiatan gunung berapi, (2) erosi dan pelapukan tebing dan tanah, (3) asap dan kebakaran hutan, dan (4) aerosol dan partikulasi dari permukaan laut. Kegiatan manusia juga merupakan sumber utama pemasukan logam ke dalam lingkungan perairan. Masuknya logam berasal dari buangan langsung dari berbagai jenis limbah yang beracun, gangguan pada cekungan-cekungan perairan, presifitasi dan jatuhan atmosfir. Sumber utam pemasukan logam dirangkum sebagai berikut (Wittman, 1979 dalam Connel dan Miller, 2006):
1. Kegiatan Pertambangan
Eksploitasi timbunan biji dalam membongkar dalam permukaan batu bara dan sejumlah besar sisa-sisa batu atau tanah untuk mempercepat kondisi pelapukan. Hal ini menyebabkan masalah kualitas air yang serius, yang mengakibatkan tingginya kadar logam seperti besi (Fe), mangan ( Mn), seng (Zn), kobalt (Co), nikel (Ni), dan tembaga (Cu).
2. Cairan Limbah Rumahtangga
Jumlah logam runutan yang cukup besar disumbangkan ke dalam cairan limbah rumahtangga oleh sampah-sampah metabolik, korosi pipa-pipa air (Cu,
Pb, Zn, dan Cd) dan produk-produk konsumer (misalnya formula deterjen yang mengandung Fe, Mn, Cr, Ni, Co, Zn, Cr, dan As).
3. Limbah dan Buangan Industri
Beberapa logam runutan yang dibuang ke dalam lingkungan perairan melalui caiarn limbah industri demikian juga dengan penimbunan dan pencucian lumpur industri. Emisi logam dari pembakaran bahan bakar fosil juga merupakan sumber utama logam dari udara yang ada di dalam air alamiah dan daerah aliran sungai.
4. Aliran Pertanian
Sifat yang berbeda-beda mengenai kegiatan dan praktek pertanian di seluruh dunia mempersulit pengujian sumber-sumber logam ini secara keseluruhan. Namun demikian, sangat banyak endapan yang mengandung logam, hilang dari daerah pertanian sebagai akibat dari erosi tanah.
Sumber utama emisi logam arsen (As), kadmium (Cd), timbal (Pb), dan merkuri (Hg) adalah pada proses peleburan dan pemurnian logam non-ferous (bukan besi). Emisi logam tersebut dapat terjadi pada saat pemrosesan primer (pemrosesan dari konsentrat mineral) maupun pemrosesan sekunder (pemrosesan dalam pabrik). Pemrosesan primer ialah pemrosesan pada daerah tambang.
Logam berat adalah suatu logam dengan bobot jenis besar. Logam ini memiliki karakter seperti berkilau, lunak, atau dapat ditempa (malleability), bersifat dapat mengalir (ductility), mempunyai daya hantar panas dan listrik yang tinggi dan bersifat kimiawi, yaitu sebagai dasar pembentukan reaksi dengan asam. Selain itu, logam berat adalah unsur yang mempunyai densitas yang lebih besar dari 5 gram per cm3, mempunyai nomor atom lebih besar dari 21 dan dapat di bagian tengah daftar periodik. Beberapa macam logam berat sangat beracun terhadap tumbuh-tumbuhan, hewan, dan manusia. Logam-logam tersebut bersifat tahan lama dan keracunannya bisa bertahan dalam waktu yang sangat lama. Unsur logam berat dalam jumlah yang berlebihan akan bersifat racun. Toksisitas (daya racun) logam berat tergantung pada jenis, kadar, efek sinergis-antagonis, dan bentuk fisika-kimianya (Connell dan Miller, 2006).
dihasilkan bila logam berat tersebut berikatan dan atau masuk ke dalam tubuh organisme hidup. Sebagai contoh, bila unsur logam besi (Fe) masuk ke dalam tubuh, meski dalam jumlah yang berlebihan, biasanya tidak menimbulkan pengaruh yang buruk terhadap tubuh. Karena unsur besi (Fe) dibutuhkan dalam darah untuk mengikat oksigen. Sedangkan unsur logam berat baik itu logam berat beracun yang dipentingkan seperti tembaga (Cu), bila masuk ke dalam tubuh dalam jumlah berlebihan akan menimbulkan pengaruh-pengaruh buruk terhadap fungsi fisiologis tubuh. Jika yang masuk ke dalam tubuh organisme hidup adalah unsur logam beracun seperti merkuri (Hg), maka organisme dapat mengakibatkan keracunan (Palar, 2004).
2.4. Logam Berat
2.4.1. Timbal (Pb)
Timbal mempunyai nomor atom 83, berat atom 207,9, titik cair 327,5oC dan titik didih 1725oC. Timbal di alam dalam bentuk sulfida (gelena), Pb Carbonat (Cerussite), PbSO4 (Angelisite), sedangkan Timbal dalam air berada
dalam bentuk Pb2+, PbCO3, Pb(CO3)22-, PbOH+ dan Pb (OH)2. Secara alamiah
Timbal tersebar luas pada batua-batuan dan lapisan kerak bumi. Saeni (1989) menyatakan sumber utama timbal di atmosfir dan daratan dapat berasal dari bahan bakar bertimbal sedangkan batuan kapur dan gelena (PbS) merupakan sumber timbal pada perairan alami. Timbal muncul dalam air dalam bentuk bilangan oksida +II. Ion timbal terhidrolisis sebagian di dalam air dengan reaksi : Pb2+ + H2O PbOH+ + H+. Selanjutnya Saeni (1989) menyatakan timbal masuk
ke perairan melalui pengendapan, jatuhan debu yang mengandung timbal yaitu: dari hasil pembakaran bensin yang mengandung timbal tetraetil, erosi, dan limbah industri.
Menurut Darmono (1995) mengemukakan penggunaan timbal dalam yang besar seperti: industri percetakan tinta, pelapis pipa sebagai anti korosif dan digunakan dalam campuran pembuat cat sebagai bahan pewarna karena daya larutnya yang rendah dalam air. Sedangkan Williams et al, (2000) dalam Oktavianus dan Salami (2005) mengungkapkan bahwa timbal (Pb) berasal dari industri-industri seperti pabrik baterai, amunisi, kawat, logam campuran, dan cat.
Secara alamiah, timbal masuk ke perairan melalui pengkristalan timbal di udara dengan bantuan air hujan dan proses korotifikasi batu-bataun mineral. Timbal masuk ke perairan sebagai dampak aktivitas manusia seperti buangan industri, buangan pertambangan biji timah, dan buangan industri kaleng.
Logam timbal dalam konsentrasi yang tinggi dalam perairan dapat bersifat racun karena bioakumulatif dalam tubuh organisme air dan akan terus diakumulasi hingga organisme tersebut tidak mampu lagi mentolerir kandungan logam berat tersebut dalam tubuhnya (Connel dan Miller, 2006). Karena sifat bioakumulatif logam timbal, maka dapat terjadi konsentrasi logam tersebut dalam bentuk terlarut dalam air adalah rendah, tetapi dalam sedimen meningkat akibat proses fisik, kimia, biologi perairan, dan dalam tubuh hewan air meningkat sampai beberapa kali lipat (biomagnifikasi). Selanjutnya Rompas (1998) dan Manahan (2002) menjelaskan bahwa apabila konsentrasi logam berat tinggi dalam air, ada kecendrungan konsentrasi logam berat tersebut tinggi dalam sedimen dan akumulasi logam berat dalam tubuh hewan demersial.
Menurut Manahan (2002) bahwa akumulasi logam berat dalam tubuh hewan air dipengaruhi oleh banyak faktor antara lain:
1. Konsentrasi logam berat dalam air 2. Konsentrasi logam berat dalam sedimen 3. Nilai pH air dan pH sedimen dasar perairan
Nilai pH air dan pH sedimen dapat mempengaruhi akumulasi logam berat dalam tubuh hewan air, karena semakin rendah pH air dan pH sedimen maka logam berat semakin larut dalam air (bentuk ion) sehingga semakin mudah masuk kedalam tubuh hewan tersebut, baik melalui insang, dan bahan makanan ataupun difusi.
4. Tingkat pencemaran air dalam bentuk COD (chemical oxygen demand)
Apabila COD dalam perairan relatif tinggi, maka ada kecendrungan kandungan logam berat dalam air dan sedimen juga akan tinggi. COD menunjukkan kadar bahan organik yang bersifat non biodegradable yang umumnya bersumber dari industri.
6. Kadar sulfur (S) dalam sedimen juga mempengaruhi kandungan logam berat dalam sedimen, karena unsur sulfur sangat mudah berikatan dengan logam berat membentuk logam-sulfida yang mengendap di dasar perairan.
7. Jenis hewan air
8. Umur dan bobot tubuh dan 9. Fase hidup (telur dan larva).
Apabila timbal (Pb) memasuki lingkungan perairan, maka timbal tersebut akan diserap oleh sedimen atau lumpur, plankton, algae, invertebrata, tanaman akuatik dan lain-lain. Sedimen dan tanah merupakan sink (pengendapan) utama bagi timbal di lingkungan. Konsentrasi timbal dalam air semakin meningkat karena garam yang diekskresikan ikan ke air cenderung bertambah. Kenaikan konsentrasi timbal dalam sistem akuatik secara berurutan : air < mangsa ikan < ikan < sedimen (DVGM, 1985 dalam Oktavianus dan Salami, 2005). Selanjutnya diungkapkan bahwa peningkatan konsentrasi timbal pada ikan (proses uptake) merupakan peningkatan eksponensial, artinya: bahwa semakin tinggi konsentrasi timbal dalam air, semakin tinggi pula konsentrasi timbal dalam ikan Nila (Oreochromis niloticus).
Hasil penelitian Sitorus (2004), mengungkapkan bahwa kadar logam berat timbal dalam tubuh kerang di perairan pesisir Belawan mencapai 0,042 ppm dan di Tanjung Balai mencapai 0,033 ppm. Hal ini berhubungan, karena kerang hidup di lapisan sedimen dasar perairan, bergerak sangat lambat dan makanannya detritus di dasar perairan, sehingga peluang masuknya logam berat kedalam tubuh sangat besar. Kadar logam berat timbal 0,5 ppm dapat menyebabkan kematian pada ikan dan organisme perairan lainnya.
Logam berat timbal dapat mempengaruhi hewan air yaitu; menganggu sistem organ seperti insang dalam proses respirasi dan ginjal dalam proses osmoregulasi, kemudian akan mempengaruhi keseimbangan energi dalam ikan, sehingga mempengaruhi mortalitas, pertumbuhan, reproduksi serta aktivitas (Lloyd, 1992 dalam Oktavianus dan Salami, 2004).
manusia, akan menyebabkan dampak negatif yang serius, antara lain: (1) menghambat aktivitas enzim, sehingga proses metabolisme terganggu, (2) menyebabkan abnormalitas kromoson (gen), (3) menghambat perkembangan janin, (4) menurunkan fertilitas wanita, (5) menghambat pembentukan sperma pada pria (spermatogenesis), (6) mengurangi konduksi syaraf tepi, (7) menghambat pembentukan hemoglobin, (8) menyebabkan kerusakan ginjal, (9) menyebabkan kekurangan darah, (10) pembengkakan kepala, (11) menyebabkan gangguan emosional dan tingkah laku (Fergusson, 1990)
2.4.2. Seng (Zn)
Seng (Zn) termasuk dalam kelompok logam berat. Seng (Zn) mempunyai nomor atom 30, berat atom 65,37 dan seng memiliki valensi +2. Titik cair Zn berada pada suhu 419,6oC dan titik leburnya pada suhu 906oC (Heslop dan Robinson, 1960). Logam berat Zn merupakan suatu logam berat putih keperakan dan dapat larut dalam air. Sumber logam berat Zn terbagi dua yaitu: (1) secara alamiah dapat berasal dari batu dan lumpur lahar, (2) berasal dari aktivitas manusia seperti: proses produksi elektroda, baterai kimia, dan juga dalam air buangan penambangan logam berat serta industri baja besi. Logam berat seng dimanfaatkan dalam produksi cat, bahan keramik, gelas, lampu dan pestisida (Darmono, 1995).
Seng (Zn) adalah metal yang didapat antara lain pada industri alloy, keramik, kosmetik, pigmen dan karet (Hardjojo dan Djokosetiyanto, 2005). Pada dasarnya Zn bukanlah unsur radioaktif sehingga unsur tersebut pada konsentrasi rendah memiliki fungsi secara biologis. Hal tersebut karena Zn memiliki daya afinitas yang tinggi dan rendah untuk mengikat enzim. Zn dibutuhkan untuk proses metabolisme dalam tubuh, tetapi dalam kadar tinggi dapat bersifat racun. Bagi mikroorganisme termasuk mikroalga, Zn berfungsi sebagai penstabil struktur dari protein, reaksi redoks dan hidrolisis serta menjadi pemicu suatu rangkaian proses.
banyak, maka dapat menimbulkan pencemaran perairan. Senyawa Zn mempunyai kemanpuan melarut yang relatif tinggi, maka logam tersebut tersebar luas di perairan (Llyod, 1992 dalam Damaiyanti, 1997). Apabila konsentrasi logam berat Zn dalam perairan berada pada konsntrasi yang tinggi, maka kemungkinan besar logam Zn dapat terakumulasi dalam tubuh biota air.
Pada konsentrasi yang tinggi logam berat Zn dapat bersifat racun bagi mikroorganisme. Kadar Zn sebesar 0,015 ppm dapat menurunkan aktivitas fotosintesa tumbuhan perairan dan konsentrasi 0,02 ppm dapat menurunkan proses pertumbuhan fitoplankton (Clark, 1986).
2.5. Logam Berat Dalam Ekosistem Perairan
Logam-logam dalam lingkungan perairan umumnya berada dalam bentuk ion. Ion-ion tersebut ada yang merupakan ion-ion bebas, pasangan ion organik, ion-ion kompleks dan bentuk-bentuk ion-ion lain. Dalam badan perairan ion-ion logam juga bereaksi membentuk kompleks organik dan kompleks anorganik. Kelarutan dari unsur-unsur logam dan logam berat dalam badan perairan dikontrol oleh: (1) pH badan air, (2) jenis dan konsentrasi logam dan khelat, (3) keadaan komponen mineral teroksidasi dan sistem yang berlingkungan redoks (Leckie dan James (1974 dalam Palar, 2004).
Menurut Smith et al. (1980 dalam Kusumahadi, 1998), pada prinsipnya penyebaran logam berat dalam ekosistem perairan dicirikan oleh adanya keberadaan kandungan logam berat dalam wilayah perairan tertentu, karena pengaruh kondisi perairan tersebut. Konsentrasi logam berat yang berbeda dalam ekosistem perairan disebabkan oleh adanya pencampuran berbagai bentuk senyawa kompleks. Reaksi yang terjadi dapat mempengaruhi atau mengubah konsentrasi, termasuk juga perubahan valensi kation. Selain itu, kemungkinan juga terjadinya penyerapan oleh bahan partikel yang kemudian mengendap di dasar, dan adanya proses pengenceran. Keadaan tersebut mempengaruhi proses kimia dan fisika dari pencemar tersebut dalam ekosistem perairan.
Dalam badan air tawar, penyerapan logam yang dilakukan oleh partikel-pertikel dan kompleks-kompleks ligand lebih bervariasi bila dibandingkan dengan air laut. Perbedaan tersebut berkenaan dengan tingkat kompleksitas dan
kekentalan dari badan perairan. Lautan merupakan badan air yang kompleksitas yang sangat tinggi. Secara lebih rinci perbedaan tersebut disebabkan oleh: (1) adanya perbedaan kekuatan ion-ion, (2) perbedaan konsentrasi dari logam-logam yang ada dan juga terlarut dalam badan perairan, (3) perbedaan konsentrasi antara kation-kation dengan anion-anion utama yang ada dalam badan perairan, dan (4) dalam badan air tawar konsentrasi ligand organik lebih besar.
Logam-logam berat yang terlarut dalam badan perairan pada konsentrasi tertentu akan berubah fungsi menjadi sumber racun bagi kehidupan perairan. Meskipun daya racun yang ditimbulkan oleh satu jenis logam berat terhadap semua biota perairan tidak sama, namun kehancuran dari satu kelompok dapat terjadi terputusnya satu mata rantai kehidupan. Pada tingkat tertentu, keadaan tersebut dapat menghancurkan satu tatanan suatu ekosistem perairan.
Pencemaran logam berat dapat merusak lingkungan perairan dalam hal stabilitas, keanekaragaman, dan kedewasaan ekosistem. Dari aspek ekologis, kerusakan ekosistem perairan akibat pencemaran logam berat dapat ditentukan oleh faktor kadar dan kesinambungan zat pencemar yang masuk dalam perairan, sifat toksisitas, dan bioakumulasi. Pencemaran logam berat akan menyebabkan terjadinya perubahan struktur komunitas perairan, jaringan makanan, efek fisiologi, genetik, dan resistensi.
Darmono (2001) menyatakan bahwa ada beberapa faktor yang mempengaruhi daya toksisitas logam dalam air terhadap mahluk yang hidup di dalamnya, yaitu:
1. Bentuk ikatan kimia dari logam yang terlarut
2. Pengaruh interaksi antara logam dan jenis toksikan lainnya
3. Pengaruh lingkungan seperti suhu, kadar garam, pH, dan kadar oksigen yang terlarut dalam air.
4. Kondisi hewan, fase siklus hidup (telur, larva, dewasa), besarnya ukuran organisme, jenis kelamin, dan kecukupan kebutuhan nutrisi.
5. Kemanpuan hewan untuk menghindar dari pengaruh pencemar
6. Kemanpuan organisme untuk beraklimatisasi terhadap bahan toksik logam.
2.6. Logam Berat Dalam Sedimen
Sedimen adalah kerak bumi (regolith) yang diangkut melalui proses hidrologi dari tempat ke tempat lain, baik secara vertikal maupun secara horizontal (Friedman dan Sanders, 1978). Sedimentasi merupakan fenomena alam yang secara langsung berhubungan dengan angin dan erosi tanah. Proses ini dapat dipercepat oleh faktor-faktor seperti: badai, peningkatan aliran sungai ”Run off”, peningkatan erosi dari daerah sekitarnya akibat pembersihan yang berlebihan, dan keberadaan partikulat hasil buangan industri.
Sedimen dapat diklasifikasikan menurut asalnya dan ukuran partikelnya. Menurut asalnya Gross (1978) menggolongkan sedimen menjadi tiga bagian yaitu: (1) sedimen berasal dari batuan (lythogenous), umumnya berupa mineral silikat yang berasal dari hancuran batuan, (2) sedimen yang berasal dari organisme (biogeneus) berupa sisa-sisa tulang, gigi atau cangkang organisme, dan (3) sedimen yang dibentuk oleh reaksi kimia yang terjadi di laut (hydrogenous).
Partikel sedimen mempunyai ukuran yang bervariasi, mulai yang besar sampai halus. Buchanan dan Kain (1991) mengklasifikasikan partikel sedimen seperti pada Tabel 2.
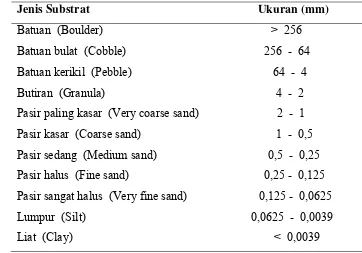
Tabel 2. Nama dan ukuran partikel sedimen menurut skala Went Worth
Jenis Substrat Ukuran (mm)
Batuan (Boulder) > 256 Batuan bulat (Cobble) 256 - 64 Batuan kerikil (Pebble) 64 - 4 Butiran (Granula) 4 - 2 Pasir paling kasar (Very coarse sand) 2 - 1 Pasir kasar (Coarse sand) 1 - 0,5 Pasir sedang (Medium sand) 0,5 - 0,25 Pasir halus (Fine sand) 0,25 - 0,125 Pasir sangat halus (Very fine sand) 0,125 - 0,0625 Lumpur (Silt) 0,0625 - 0,0039 Liat (Clay) < 0,0039
[image:39.595.147.509.104.357.2]Sedangkan menurut Parson dkk (1977 dalam Bachtiar (1994) bahwa klasifikasi ukuran partikel sedimen disajikan pada Tabel 3.
Tabel 3. Klasifikasi ukuran partikel sedimen
Jenis Substrat Ukuran (mm)
Pasir (sand) 2,000 - 0,050 Lumpur (silt) 0,050 - 0,002 Liat (clay) < 0,002
Dahuri et al. (1996) menyatakan bahwa perairan yang sedimentasinya tinggi dapat membahayakan kehidupan di lingkungan perairan. Pengaruh sedimen terhadap biota air secara garis besar melalui beberapa mekanisme, yaitu: 1. Sedimen menutupi tubuh biota perairan terutama yang hidup di dasar perairan
(organisme bentik).
2. Sedimen menyebabkan peningkatan kekeruhan air dengan menghalangi penetrasi cahaya yang masuk kedalam air sehingga dapat mengganggu kehidupan organisme air.
3. Sedimen selain mampu mengikat unsur-unsur hara, juga dapat menyerap (mengabsorpsi) logam berat. Kondisi ini dapat menyebabakan kontaminasi zat-zat tersebut kedalam jaringan tubuh biota di perairan dan manusia melalui rantai makan jaring-jaring makanan.
Pada sedimen dapat terjadi reaksi-reaksi kimia, yaitu: (1) penyerapan (absorpsi) dan pelarutan ion, senyawa, gas antara air, dan sedimen, (2) perubahan nilai potensial redoks (Eh) dan pH sedimen, (3) transfer senyawa hasil reduksi dari lapisan bawah ke lapisan atas sedimen, (4) siklus karbon, nitrogen, sulfur, dan fosfor, dan (5) perubahan konsentrasi ion dalam jaringan organisme maupun di sedimen (Rhoods, 1974).
Salah satu hewan air yang dapat berinteraksi langsung dengan sedimen adalah hewan bentos. Perubahan sedimen dasar dapat mempengaruhi komposisi dan kelimpahan makrozoobentos (Odum, 1998). Faktor yang mempengaruh langsung terhadap komposisi dan distribusi organisme bentos di dasar perairan, yaitu: partikel-partikel sedimen seperti lempung, pasir, liat, dan substrat keras.
dengan partikel mineral, pengikatan oleh partikel organik dan pengikatan oleh sekresi lendir organisme.
2.7. Cara Penyerapan Logam Berat Oleh Organisme
Logam berat masuk ke dalam jaringan tubuh mahluk hidup melalui beberapa jalan, yaitu: (1) saluran pernapasan, absorbsi logam melalui saluran pernapasan biasanya sangat besar, baik pada hewan air yang masuk melalui insang, maupun hewan darat yang masuk melalui debu di udara ke saluran pernapasan, (2) pencernaan, absorbsi melalui saluran pencernaan hanya beberapa persen, tetapi jumlah logam yang masuk melalui saluran pencernaan biasanya cukup besar, walaupun persentase absorbsinya kecil, dan (3) penetrasi melalui kulit, logam yang masuk melalui kulit jumlah dan absorbsinya relatif kecil (Darmono, 2001).
Menurut Darmono dan Arifin (1989) dalam Kusumahadi (1998), ada tiga teori mengenai mekanisme penyerapan logam dalam jaringan organisme, yaitu: 1. Penyerapan logam melalui mekanisme pengangkutan yang berhubungan
dengan mekanisme osmoregulasi, yaitu pengaturan tekanan osmosis oleh organisme terhadap air di sekitarnya.
2. Pengikatan ion-ion logam menyentuh bagian tertentu dari permukaan jaringan dan masuk ke dalam sitoplasma
3. Logam dalam bentuk kristal kecil atau larutan yang segera ditangkap oleh sel epitel dan secara endositosis logam tersebut di bawa masuk dan dilepas ke dalam sitoplasma.
anorganik disimpan dalam jaringan, kemudian ditransfer ke ginjal dan diekresikan, sedangkan logam organik tidak diekresikan, tetapi terakumulasi dalam jaringan otot. Selain itu, masuknya logam berat ke dalam tubuh ikan juga dapat melalui rantai makanan, dan (5) manusia, logam berat masuk ke dalam tubuh dapat melalui air secara langsung atau melalui rantai makanan, kemudian terakumulasi dalam tubuh manusia, terutama hati dan ginjal.
Menurut Simkis dan Mason (1983), logam masuk ke dalam jaringan tubuh biota secara umum melalui tiga cara yaitu:
1. Endositosis dimana pengambilan partikel dari permukaan sel dengan perpindahan oleh membran plasma. Proses ini berperan dalam pengambilan logam berat dalam bentuk tidak terlarut.
2. Diserap dari air, sembilan puluh persen kandungan logam dalam jaringan berasal dari penyerapan oleh sel epitel insang. Insang diduga sebagai organ yang menyerap logam berat dari air.
3. Diserap dari makanan dan sedimen. Penyerapan logam berat dari makanan dan sedimen oleh biota bergantung pada strategi mendapat makanan.
2.8. Hewan Bentos
2.8.1. Pengertian Bentos
Menururt Odum (1971), bentos merupakan organisme yang hidup pada permukaan atau di dalam substrat pada dasar perairan. Berdasarkan cara makannya, makrozoobentos dikelompokkan menjadi filter feeder dan deposit feeder. Filter feeder merupakan organisme yang memakan bahan tersuspensi dengan cara menyaring (contoh kerang) sedangkan deposit feeder adalah organisme pemakan deposit (misalnya jenis siput). Sedangkan Lind (1979) dalam Nurifdinsyah (1993) memberikan definisi bahwa bentos adalah semua organisme yang hidup pada lumpur, pasir, batu, kerikil, dan sampah baik di dasar danau atau waduk, kolam, dan sungai.
Berdasarkan sebaran vertikalnya, bentos yang hidup di atas permukaan dasar disebut epifauna dan yang hidup di dalam dasar perairan disebut infauna. Bentos berdasarkan ukurannya dibagi menjadi 3 golongan, yaitu: (1) makrozoobentos, dengan ukuran lebih besar dari 1 mm (contoh: Oligochaeta,
Crustacea, Mollusca, Gastropoda, dan Palecypoda), (2) meiobentos dengan ukuran antara 0,1 mm, (3) mikrobentos dengan ukuran kurang dari 0,1 mm. Dalam ekosisitem perairan, makrozoobentos memegang beberapa peran penting seperti dalam proses dekomposisi bahan-bahan organik dan posisinya dalam rantai makanan terutama rantai makanan detritus.
Menurut Perkins (1974) menyatakan bahwa berdasarkan ukurannya bentos dibagi menjadi tiga yaitu: (1) organisme yang tertahan pada saringan berukuran 2,0 – 0,5 mm termasuk ke dalam makrobentos atau oleh saringan dengan ukuran nomor 30 US Standard, (2) organisme yang lolos pada saringan berukuran 1,0 – 0,5 mm tetapi tertahan pada saringan berukuran 0,04 – 1,0 mm termasuk ke dalam meiobentos, dan (3) organisme yang lolos pada saringan 0,04 mm termasuk mikrobentos.
Sebagai organisme dasar perairan, bentos mempunyai habitat yang relatif tetap. Dengan sifatnya yang demikian, perubahan-perubahan kualitas air dan substrat tempat hidupnya sangat mempengaruhi komposisi maupun kelimpahannya. Komposisi dan kelimpahannya bergantung pada toleransi atau sensitivitasnya terhadap perubahan lingkungan (makrozoobentos dapat bersifat toleran maupun bersifat sensitif), sehingga jenis tersebut dapat dijadikan indikator pencemaran suatu perairan.
Menurut Hawkes (1979) dalam Astuti dan Trihadiningrum (2000), makroinvertebrata dapat berlaku sebagai monitor kontinyu air, tidak seperti halnya kualitas fisik dan kimia air yang hanya berlaku sesaat. Bahkan respon dari komunitas bentos lebih luas dari polutan air. Mempertimbangkan beberapa penemuan metode pendugaan biologis yang berdasarkan pada hewan makroinvertebrata dan fakta bahwa makroinvertebrata telah dipergunakan secara luas sebagai bagian dari integral untuk monitoring kualitas air.
2.8.2. Struktur Komunitas Makrozoobentos
Komunitas biotik adalah kumpulan populasi yang hidup di daerah tertentu atau habitat fisik tertentu dan merupakan satu satuan yang terorganisir dan mempunyai hubungan timbal balik. Konsep komunitas tersebut dapat digunakan dalam menganalisis lingkungan perairan karena komposisi dan karakter organisme di dalam suatu komunitas merupakan indikator yang cukup baik untuk melihat keadaan lingkungan dimana komunitas tersebut berada (Odum, 1971).
Basmi (2000) menyatakan bahwa analisis struktur komunitas biota sebagai indikator biologis tingkat pencemaran perairan dapat bersifat kuantitatif (berupa indeks) melalui kalkulasi terhadap komponen-komponen tertentu dari struktur komunitas yang diamati dan secara kualitatif dengan mengamati komposisi jenis-jenis tertentu yang dominan di dalam suatu komunitas. Krebs (1989) menambahkan bahwa untuk kondisi suatu struktur komunitas terdapat lima karakteristik komunitas yang dapat diukur yaitu: (1) keanekaragaman, (2) dominansi, (3) bentuk dan struktur pertumbuhan, (4) kelimpahan, dan (5) struktur trofik.
Keanekaragaman dapat digunakan untuk melihat pengaruh pencemaran perairan terhadap komunitas perairan (biologi), dalam hal ini keanekaragaman digunakan untuk mengevaluasi akibat yang terjadi pada komunitas bentos dihubungkan dengan kondisi lingkungan. Selain itu keanekaragaman dapat juga digunakan sebagai indikator kualitas perairan, dalam hal ini digunakan untuk menentukan apakah perubahan yang terjadi pada komunitas merupakan hasil dari adanya bahan pencemar (Dennis dan Patil, 1977). Untuk menghitung keanekaragaman jenis makrozoobentos digunakan metode Shannon-Wiener.
Keanekaragaman dari Shannon-Wiener merupakan indeks yang paling umum digunakan bagi manajemen lingkungan dan berfungsi sebagai alat bantu dalam menggambarkan struktur komunitas dan mendeteksi besarnya degradasi pada ekosistem. Indeks keanekaragaman menggabungkan tiga komponen utama dari struktur komunitas yaitu: kelimpahan, jumlah taksa, dan kemerataan distribusi organisme diantara spesies (Krebs, 1989).
Parameter kualitas air mendukung kehidupan bentos antara lain: bahan organik dan detritus sedangkan faktor penghambat adalah bahan-bahan beracun. Oleh karena itu, hanya jenis-jenis bentos tertentu dan derajat keanekaragaman dapat dipergunakan sebagai indikator tingkat pencemaran perairan dimana organisme itu hidup. Bentos merupakan hewan air yang dapat dijadikan indikator untuk menentukan kualitas perairan berdasarkan ketahanannya terhadap pencemaran air dapat dilihat pada Tabel 4.
Tabel 4. Klassifikasi hewan bentos berdasarkan ketahanannya terhadap pencemaran air (Wilhm, 1975)
Kelompok Jenis Hewan Bentos
Jenis organisme sangat tahan terhadap pencemaran
Cacing tubifecid, Lintah, Larva nyamuk, Siput (musculum dan fisidium)
Jenis yang ketahanannya sedang dan lebih menyenangi air yang jernih
Jenis-jenis siput, Serangga dan Crustacea
Jenis yang tidak tahan terhadap bahan pencemar dan hanya menyenangi air bersih
Siput dari famili viviparidae, amnicolidae serangga, nimfa dari ordo Ephemercidae, odonata, hemiptera, neuroptera dan Colenterata
Selanjutnya Wilhm (1975) memberikan kriteria kualitas air berdasarkan penduga keanekaragaman Shannon-Wiener dari hewan bentos makro dapat dilihat pada Tabel 5.
biologi. Faktor-faktor tersebut adalah: suhu, pH, kekeruhan, kecerahan, gas-gas terlarut dan interaksi dengan organisme lain.
Sedangkan organisme yang tidak toleran terhadap zat pencemar kemanpuan kompetisinya menurun dan akhirnya akan punah, sehingga pada daerah tersebut akan di dominasi oleh organisme yang toleran terhadap polutan (Dennis dan Patil, 1977). Keanekaragaman organisme yang rendah mengindikasikan bahwa pada daerah tersebut telah terjadi tekanan lingkungan akibat polusi. Pada saat terjadi tekanan lingkungan, hanya beberapa spesies yang dapat mentelorir dan keanekaragaman menjadi rendah.
Tabel 5. Beberapa kriteria kualitas air berdasarkan indeks keanekaragaman Shannon-Wiener dari hewan bentos makro
Indeks Keanekaragaman Jenis Kualitas Air < 3
1 - 3 < 1
Air bersih
Setengah tercemar Tercemar Berat 3,0 - 4,5
2,0 - 3,0 1,0 - 2,0
< 1,0
Pencemaran sangat ringan Pencemaran ringan Setengah tercemar Tercemar berat > 2,0
2,0 - 1,6 1,5 - 1,0
> 1,0
Pencemaran sangat ringan Pencemaran ringan Pencemaran sedang Tercemar berat
Dari Tabel diatas dapat diambil kesimpulan bahwa apabila Indeks keanekaragaman jenis lebih besar dari tiga, berarti kualitas perairan di tempat tersebut baik dan sebaliknya apabila indeks keanekaragaman jenis lebih kecil dari satu maka kualitas perairan telah tercemar berat.
III.
METODE PENELITIAN
3.1. Tempat dan Waktu Penelitian
Penelitian ini dilakukan di perairan Waduk Cirata dengan 2 tahap. Penelitian Tahap I merupakan penelitian pendahuluan dengan tujuan untuk mengetahui keberadaan makrozoobentos dan jenis kandungan logam berat yang terdapat dalam makrozoobentos. Penelitian Tahap II merupakan kelanjutan dari Penelitian Tahap I. Berdasarkan Penelitian Tahap I ditentukan jenis logam berat yang akan diteliti, yaitu: Timbal (Pb) dan Seng (Zn). Penetapan 2 jenis logam berat tersebut dilakukan berdasarkan nilai konsentrasi yang dominan (tertinggi) dari 4 jenis logam berat yang dianalisis, antara lain: Cr (16,25 mg/kg), Cu (17,99 mg/kg), Pb (38,82 mg/kg), dan Zn (57,10 mg/kg).
Penelitian ini dimulai pada bulan Desember 2006 sampai bulan Maret 2007. Pengambilan contoh air, sedimen, dan makrozoobentos dilakukan di muara sungai atau Waduk Cirata. Adapun Lokasi pengambilan sampel dapat dilihat pada Gambar 2.
3.2. Bahan dan Alat
Bahan-bahan yang digunakan dalam penelitian ini adalah contoh air, sedimen, dan makrozoobentos dari setiap pengamatan penelitian, air destilasi, dan bahan kimia baik untuk analisis logam berat, analisis kualitas air maupun untuk keperluan pengawetan. Sedangkan alat-alat yang digunakan adalah petersen grab, botol sampel, freezer, saringan, peralatan analisis kimia, pH meter, termometer, turbidimeter, spectrofotometer, dan AAS (Atomic Absorbsion Spectrophotometer).
3.3. Prosedur Kerja
Parameter Fisika-Kimia Air
kandungan logam Pb dan Zn dilakukan di laboratorium Proling (Produktifitas dan Lingkungan Perairan), Fakultas Perikanan dan Ilmu Kelautan IPB Bogor.
Parameter Kimia Sedimen
Pengambilan contoh sedimen dilakukan dengan menggunakan petersen grab. Contoh sedimen yang telah diambil, dimasukkan ke dalam kantong plastik dan selanjutnya diukur kandungan logam berat dengan menggunakan AAS di laboratorium Kimia Tanah Kabupaten Bogor.
Parameter Biologi
Pada setiap lokasi penelitian dilakukan pengambilan contoh makrozoobentos dengan menggunakan petersen grab. Selanjutnya dilakukan penyortiran makrozoobentos yang terdapat dalam sedimen atau lumpur dengan menggunakan saringan. Contoh makrozoobentos tersebut dimasukkan ke dalam wadah (plastik) dan ditambahkan larutan formalin 4 % + asam asetat glacial + metil alkohol 70 % dengan perbandingan 2 : 2 : 1 sebagai bahan pengawet dan dibawa ke laboratorium untuk dianalisis kandungan logam berat (Pb dan Zn). Identifikasi berbagai jenis makrozoobentos yang ditemui pada setiap stasiun pengamatan dilakukan dengan menggunakan berbagai buku kunci identifikasi. Identifikasi dilakukan dengan bantuan buku determinasi jenis-jenis bentos seperti: Pennak (1953), Wegner dan Lieftinck (1956). Untuk lebih jelasnya parameter-perameter kualitas air, sedimen, biota yang diamati, dan alat yang digunakan serta tempat dilakukan analisis pada penelitian ini dapat dilihat pada Tabel 6.
Gambar
Garis besar
Dokumen terkait
Pada penelitian ini didapatkan hasil yang tidak signifikan pada analisis bivariat uji chi-square variabel tingkat adiksi media sosial dengan interaksi sosial dengan nilai
dengan locus of control adalah penelitian Dian Agustia (2009) yang mengemukakan di dalam penelitiannya bahwa locus of control memiliki pengaruh yang kuat dan
Kesalahan yang dilakukan oleh notaris dalam Pasal 48 Undang-Undang Jabatan Notaris Nomor 30 Tahun 2014, tentang “perubahan terhadap isi akta dimana jika notaris pada saat membuat
Perbandingan hasil numerik fungsi gelombang keadaan dasar dengan hasil eksak untuk sebuah partikel dalam potensial osilator harmonik 1D dengan LX = 10, NX = 100 dengan spasi grid
hotel Kristal ke Swiss-Belhotel International juga terjadi pada T- More Hotel yang juga sudah beralih manajemen dengan Sahid International Hotel pada 1 April
Data variabel Prestasi Belajar Konstruksi Bangunan I dalam penelitian ini diperoleh dari dokumen yaitu perolehan nilai mahasiswa dalam bentuk Daftar Penetapan Nilai
Beikut ini adalah gambar sederhana dari sebuah jaringan wireless hotspot yang menggunakan billing system yang berfungsi sebagai gateway, dimana terakhir setelah
Dendrogram kekerabatan di antara jenis kemenyan di dapatkan bahwa kemenyan durame dan kemenyan minyak menjadi satu kelompok kecil dengan jarak genetik 0,44, kemudian membentuk