KENDALI MUTU JAHE MENGGUNAKAN SIDIK JARI
KROMATOGRAFI CAIR KINERJA TINGGI
DAN ANALISIS MULTIVARIAT
RESTU WIDYASTUTI
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
ABSTRAK
RESTU WIDYASTUTI. Kendali Mutu Jahe Menggunakan Sidik Jari
Kromatografi Cair Kinerja Tinggi dan Analisis Multivariat. Dibimbing oleh ETI
ROHAETI dan RUDI HERYANTO.
Jahe dikenal memiliki khasiat obat misalnya sebagai antioksidan, antiradang,
dan antikanker. Rimpang jahe banyak digunakan sebagai komponen dalam
berbagai sediaan obat herbal sehingga diperlukan ketersediaan metode untuk
menjamin mutu dan khasiatnya. Penelitian ini bertujuan mengevaluasi mutu
rimpang jahe gajah melalui pengujian aktivitas antioksidan, pemeriksaan pola
sidik jari kromatografi cair kinerja tinggi (KCKT), penetapan kandungan senyawa
utama, serta pembuatan model mutu ekstrak etanol rimpang jahe yang berasal dari
3 daerah, yaitu Ponorogo, Tangerang, dan Bogor. Semua sampel didapati
berpotensi sebagai antioksidan sangat kuat. Hasil analisis KCKT menunjukkan 6-,
8-, dan 10-gingerol, serta 6-shogaol sebagai senyawa dominan. Pengelompokan
berdasarkan kandungan senyawa dominan dan sidik jari KCKT menggunakan
analisis komponen utama menghasilkan kelompok I (Tangerang), kelompok II
(Ponorogo), dan kelompok III (Bogor). Model mutu yang dibentuk menggunakan
analisis diskriminan kuadrat terkecil parsial menunjukkan bahwa aktivitas
antioksidan jahe lebih ditentukan oleh komposisi keseluruhan senyawa
dibandingkan dengan senyawa dominan.
Kata kunci: analisis multivariat, antioksidan, jahe, KCKT, sidik jari
ABSTRACT
RESTU WIDYASTUTI. Quality Control of Ginger Using High Performance
Liquid Chromatography Fingerprint and Multivariate Analysis. Supervised by ETI
ROHAETI and RUDI HERYANTO
Ginger is known to have pharmacology effect such as antioxidant,
antiinflamation, and anticancer. The rhizome of ginger is widely used as
component in various herbal medicine preparations so that needed some methods
to guarantee its quality and pharmacology effect. The aim of this research was to
evaluate the quality of
gajah
ginger rhizome by antioxidant activity assay, high
performance liquid chromatography (HPLC) fingerprint pattern examination,
major compound content determination, and also quality model establishment of
ginger ethanol extracts from 3 areas, that is Ponorogo, Tangerang, and Bogor. All
samples were indeed potential as very strong antioxidant. The result of HPLC
analysis showed 6-, 8-, and 10-gingerol, also 6-shogaol as dominant compounds.
Grouping based on content of dominant compounds and HPLC fingerprint that
used principal component analysis resulted group I (Tangerang), group II
(Ponorogo), and group III (Bogor). The quality model that was formed using
partial least square discriminant analysis showed that antioxidant activity of
ginger was more defined by composition of all compounds than by its dominant
compounds.
KENDALI MUTU JAHE MENGGUNAKAN SIDIK JARI
KROMATOGRAFI CAIR KINERJA TINGGI
DAN ANALISIS MULTIVARIAT
RESTU WIDYASTUTI
Skripsi
sebagai salah satu syarat untuk memperoleh gelar
Sarjana Sains pada
Departemen Kimia
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
Judul Skripsi : Kendali Mutu Jahe Menggunakan Sidik Jari Kromatografi Cair
Kinerja Tinggi dan Analisis Multivariat
Nama
: Restu Widyastuti
NIM
: G44080048
Disetujui
Pembimbing I Pembimbing II
Dr. Eti Rohaeti, M.S.
Rudi Heryanto, S.Si., M.Si.
NIP 19600807 198703 2 001 NIP 19760428 200501 1 002
Diketahui
Ketua Departemen Kimia
Prof. Dr. Ir. Tun Tedja Irawadi, M.S.
NIP 19501227 197603 2 002
PRAKATA
Segala puji syukur penulis ucapkan kepada Allah SWT yang senantiasa
memberikan rahmat, nikmat, dan hidayah-Nya sehingga penulis dapat
menyeleseikan penelitian serta skripsi dari kegiatan tersebut dengan judul
“K
endali Mutu Jahe Menggunakan Sidik Jari Kromatografi Cair Kinerja Tinggi
dan Analisis
Multivariat”.
Shalawat dan salam disampaikan kepada Nabi
Muhammad SAW beserta keluarga, sahabat, dan pengikutnya yang tetap berada di
jalan-Nya hingga akhir zaman.
Skripsi ini tidak terlepas dari bantuan berbagai pihak, baik secara langsung
maupun tidak langsung. Untuk itu, ungkapan terima kasih penulis sampaikan
kepada Ibu Dr. Eti Rohaeti, M.S. dan Bapak Rudi Heryanto, S.Si., M.Si. selaku
pembimbing yang telah membimbing, memberikan arahan, saran, dan dorongan
selama melaksanakan penelitian dan penulisan karya ilmiah ini. Penghargaan
penulis sampaikan kepada Ayahanda, Ibunda, Adik, dan Sahabat tercinta yang
telah memberikan dukungan moral dan material sehingga menjadi motivasi
penulis untuk berbuat yang terbaik. Terima kasih juga kepada Pak Eman, Pak
Kosasih, Pak Dede, Bu Nunung, dan seluruh staf Laboratorium Kimia Analitik,
serta staf Laboratorium Pusat Studi Biofarmaka IPB atas fasilitas dan bantuan
yang diberikan selama penelitian.
Penulis berharap semoga karya ilmiah ini bermanfaat.
Bogor, Januari 2013
RIWAYAT HIDUP
Restu Widyastuti, lahir di Ponorogo pada tanggal 4 Desember 1989. Penulis
merupakan putri pertama dari dua bersaudara dari pasangan Bapak Djaka Santoso
dan Ibu Misratun. Penulis memiliki satu adik perempuan bernama Rista Afina
Widyarkanti.
Penulis memulai pendidikannya di TK PGRI Prayungan (Ponorogo) pada
tahun 1994
–
1996. Kemudian melanjutkan ke SD Negeri 1 Prayungan (Ponorogo)
pada tahun 1996
–
2002, SMP Negeri 1 Jetis (Ponorogo) pada tahun 2002
–
2005,
dan SMA Negeri 2 Ponorogo pada tahun 2005
–
2008. Setelah lulus dari jenjang
pendidikan SMA, penulis melanjutkan studi di Institut Pertanian Bogor (IPB)
pada tahun 2008 melalui jalur Undangan Seleksi Masuk IPB (USMI) dan diterima
di Departemen Kimia, Fakultas Matematika dan Ilmu Pengetahuan Alam.
DAFTAR ISI
Halaman
DAFTAR TABEL ... vi
DAFTAR GAMBAR ... vi
DAFTAR LAMPIRAN ... vii
PENDAHULUAN ... 1
BAHAN DAN METODE
... 2
Bahan dan Alat ... 2
Metode... 2
HASIL DAN PEMBAHASAN
... 4
Deskripsi Karakteristik Kimia Rimpang Jahe ... 4
Aktivitas Antioksidan Ekstrak Kasar Rimpang Jahe ... 5
Analisis Kuantitatif Gingerol dan Shogaol Menggunakan KCKT ... 6
Klasifikasi Rimpang Jahe Menggunakan PCA ... 8
Analisis PLSDA untuk Model Mutu Ekstrak Jahe ... 9
SIMPULAN DAN SARAN
... 11
Simpulan ... 11
Saran ... 11
DAFTAR PUSTAKA ... 11
DAFTAR TABEL
Halaman
1 Komposisi air-asetonitril pada elusi gradien KCKT ... 3
2 Nilai IC
50ekstrak kasar rimpang jahe ... 5
3 Rerata kadar gingerol dan shogaol hasil KCKT dalam simplisia jahe ... 7
4 Model PLSDA antara senyawa dominan dan aktivitas antioksidan ... 10
5 Model PLSDA antara sidik jari KCKT dan aktivitas antioksidan ... 10
DAFTAR GAMBAR
Halaman
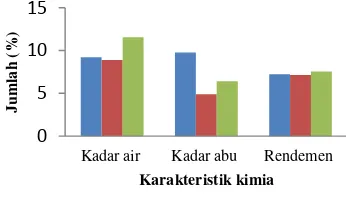
1 Rerata kadar air, kadar abu, dan rendemen sampel rimpang jahe asal
Ponorogo ( ), Tangerang ( ), dan Bogor ( )... 4
2 Plot skor PCA pada pengelompokan jahe berdasarkan aktivitas antioksidan .... 6
3 Kromatogram KCKT standar 6-, 8-, dan 10-gingerol, serta 6-shogaol ... 6
4 Kromatogram KCKT ekstrak kasar jahe Ponorogo 1 ... 6
5 Struktur kimia 6-gingerol (a) dan 6-shogaol (b) ... 7
6 Alur proporsi varians 4 komponen utama ... 8
7 Plot skor dan
loading
PCA pada pengelompokan jahe berdasarkan kadar
senyawa 6-, 8-, dan 10-gingerol, serta 6-shogaol ... 8
8 Alur proporsi varians 7 komponen utama ... 9
DAFTAR LAMPIRAN
Halaman
1 Bagan alir penelitian ... 15
2 Kadar air sampel rimpang jahe ... 16
3 Kadar abu sampel rimpang jahe ... 16
4 Rendemen ekstrak kasar rimpang jahe... 17
5 Kondisi geografis daerah asal jahe... 17
6 Standar mutu simplisia jahe kering berdasarkan SNI 01-7084-2005 ... 18
7 Contoh foto rendemen ekstrak kasar rimpang jahe ... 18
8 Contoh foto uji aktivitas antioksidan ekstrak kasar rimpang jahe ... 18
9 Data uji aktivitas antioksidan ekstrak kasar rimpang jahe ... 19
10 Uji Duncan aktivitas antioksidan ekstrak kasar rimpang jahe ... 26
11 Kromatogram ekstrak kasar rimpang jahe hasil KCKT ... 27
12 Data hasil KCKT ekstrak kasar rimpang jahe ... 30
13 Penentuan kadar 6-, 8-, dan 10-gingerol, serta 6-shogaol dalam simplisia
kering rimpang jahe ... 33
14 Uji Duncan kadar senyawa dominan rimpang jahe ... 35
15 Model PLSDA antara senyawa dominan dan aktivitas antioksidan ... 38
PENDAHULUAN
Obat-obatan herbal telah banyak dimanfaatkan selama ribuan tahun di negara-negara oriental seperti Cina dan Jepang, bahkan saat ini telah menarik perhatian dunia. Obat herbal lebih sering dimanfaatkan sebagai produk jamu dan kosmetik, dikarenakan obat herbal cenderung lebih aman dan memiliki efek samping yang relatif lebih sedikit daripada obat sintetis. Semakin banyaknya penggunaan obat herbal tersebut kurang diimbangi dengan pengawasan yang baik terhadap kualitasnya sehingga menjadi kendala untuk pengembangan dan modernisasi produk jamu.
Belakangan ini, semakin banyak jamu berkualitas rendah dan adanya pemalsuan dengan tanaman lain yang lebih murah dari genus yang sama meskipun tidak diketahui efeknya. Hal tersebut dapat memengaruhi keamanan dan kemanjuran obat-obatan herbal (Jing et al. 2011). Kandungan kimia dalam tanaman herbal juga dapat beragam karena perbedaan musim panen, asal-usul tanaman, proses pengolahan, dan faktor lainnya (Liang et al. 2004). Pembentukan sistem kontrol kualitas tanaman obat yang canggih dan efektif diperlukan untuk menjamin mutu produk jamu yang di antaranya meliputi keaslian, keamanan, dan kemanjuran tanaman obat (Chen 2006).
Jahe termasuk famili Zingiberaceae yang dapat tumbuh di daerah tropis dan subtropis. Jahe memiliki 3 varietas, yaitu jahe gajah, jahe emprit, dan jahe merah. Rimpang jahe gajah lebih besar dan gemuk, berwarna kuning, berserat halus dan sedikit, serta beraroma maupun berasa kurang tajam. Jahe emprit ruasnya lebih kecil, agak rata, berserat halus, serta beraroma dan berasa lebih tajam. Jahe merah rimpangnya berwarna merah dan lebih kecil daripada jahe emprit, berserat kasar, dan beraroma sangat tajam. Jahe memiliki efek farmakologis sebagai obat dan mampu memperkuat khasiat obat lain. Jahe sering digunakan sebagai obat batuk, masuk angin, diare, rematik, anti-mual, radang tenggorokan, menghilangkan rasa sakit, asma, dan lainnya (Harmono dan Andoko 2005).
Komponen senyawa kimia dalam jahe terdiri dari minyak menguap, minyak tidak menguap (oleoresin), dan pati. Minyak menguap merupakan komponen yang memberi bau khas, sedangkan komponen oleoresin dalam minyak tidak menguap memberi rasa pahit dan pedas. Komponen utama dari oleoresin adalah gingerol
(C17H26O4), shogaol (C17H24O3), dan resin
(Chrubasik dan Pitler 2005). Berbagai penelitian membuktikan bahwa jahe mempunyai sifat antioksidan dan antikanker. Oleoresin jahe yang mengandung gingerol, shogaol, dan zingeron memiliki sifat antioksidan melebihi α-tokoferol (Kikuzaki dan Nakatani 1993).
Jahe yang digunakan sebagai bahan baku industri terkadang merupakan jahe berkualitas rendah dan bukan jahe murni, melainkan campuran dari beberapa varietas jahe atau bahkan dengan tanaman lain yang memiliki ciri hampir sama dengan jahe. Untuk menghilangkan masalah tersebut, diperlukan kontrol kualitas jahe yang ditekankan pada kandungan kimianya. Identifikasi morfologi dan mikroskopis dapat digunakan untuk menentukan keaslian tanaman jahe. Selain itu, ciri fisik dan kimia yang ditemukan juga dapat digunakan untuk mengevaluasi kualitas tanaman jahe dari standar kualitas yang ada (Jiang et al. 2006). Penentuan unsur kimia dan senyawa aktif yang penting juga diperlukan untuk mencerminkan kualitas intrinsik tanaman jahe, konsistensi, dan kemanjurannya (Ernst 2002).
Penentuan mutu tanaman obat berdasarkan sidik jari (fingerprint) telah dilakukan dengan berbagai metode seperti kromatografi lapis tipis (TLC), kromatografi cair kinerja tinggi (KCKT), elektroforesis kapiler (CE), spektroskopi inframerah (FTIR), dan spektrometri resonans magnetik inti (NMR). Darusman et al. (2007) pernah menerapkan analisis FTIR untuk mendapatkan sidik jari sediaan ekstrak kunyit, temu lawak, jahe, temu kunci, dan cabe jawa. Metode analisis HPLC digunakan oleh Tao et al. (2011) untuk mendapatkan pola sidik jari dari obat herbal Cina (Gastrodia). Metode analisis yang sama (HPLC) dilakukan oleh Wahyuni (2010) untuk validasi sidik jari ekstrak Phyllanthus niruri L. Umam (2011) juga menerapkan metode FTIR dan HPLC untuk diferensiasi tanaman jahe melalui sidik jari yang diperoleh.
kesamaan sidik jari (Tao et al. 2011). Metode sidik jari KCKT untuk evaluasi kualitas tanaman obat telah digunakan secara luas karena sangat selektif, sensitif, dan memiliki presisi yang bagus sehingga secara kimia dapat mewakili karakteristik dari obat-obatan herbal yang diselidiki (Liang et al. 2004).
Sidik jari KCKT sangat rumit sehingga perbedaan antara kromatogram tidak tampak dengan jelas. Oleh karena itu, diperlukan suatu metode kemometrik untuk mendapatkan informasi tersembunyi yang bersifat kualitatif dan kuantitatif dari daerah sidik jari tersebut. Metode kemometrik yang digunakan ialah analisis multivariat menggunakan principal component analysis (PCA) dan partial least square discriminant analysis (PLSDA). Metode ini memainkan peran penting dalam diskriminasi dan klasifikasi tanaman obat (Jing et al. 2011). Selain itu, metode berbasis sidik jari KCKT ini digunakan parameter lain sebagai indikator baik tidaknya mutu suatu ekstrak, yaitu nilai bioaktivitasnya (aktivitas antioksidan). Penggunaan metode kemometrik tersebut diharapkan mampu mengelompokkan tanaman obat berdasarkan kemiripan pola sidik jarinya dan mengekstrak informasi tersembunyi dari ekstrak yang diuji.
Penelitian ini bertujuan membuat kromatogram sidik jari KCKT, menentukan kandungan senyawa dominan, dan menguji aktivitas antioksidan ekstrak kasar jahe dari 3 daerah, yaitu Ponorogo, Tangerang, dan Bogor. Analisis PCA terhadap sidik jari KCKT dilakukan untuk melihat pengelompokan antardaerah asal jahe. Analisis PLSDA juga dilakukan untuk menduga keterkaitan antara aktivitas antioksidan jahe dengan kandungan senyawa dominan maupun pola sidik jarinya. Jahe yang digunakan dari varietas jahe gajah yang diekstrak menggunakan pelarut etanol dengan cara ekstraksi ultrasonik.
BAHAN DAN METODE
Bahan dan Alat
Bahan-bahan yang digunakan dalam penelitian ini antara lain rimpang jahe gajah yang berasal dari 3 daerah (Bogor, Tangerang, dan Ponorogo) masing-masing 3 sampel dengan rimpang yang berbeda, standar campuran (, 8-, dan 10-gingerol, serta 6-shogaol), etanol 96%, etanol pa, 1.1-difenil-2-pikrilhidrazil (DPPH), metanol pa, dan fase gerak KCKT (air dan asetonitril).
Alat yang digunakan antara lain spektrofotometer Microplate Reader BioRad model 3550; perangkat HPLC Hitachi L-2420 yang dilengkapi dengan detektor ultraviolet (UV), sistem pompa gradien, dan sistem injeksi loop; kolom Shimadzu C18, 4.6 x 250 mm, 5μm, 120 Å; membran filter 0.45 μm; neraca analitik; oven; tanur; perangkat ekstraksi ultrasonik; penguap putar; perangkat keras komputer; serta perangkat lunak The Unscrambler X dan SAS versi 9.0.
Metode
Tahapan Penelitian
Secara umum, penelitian ini terdiri dari tiga tahap. Tahap pertama, yaitu preparasi simplisia dan ekstrak kasar jahe. Pertama-tama, jahe segar dikeringkan, dihaluskan, dan ditentukan kadar air serta abunya. Selanjutnya, simplisia jahe diekstrak menggunakan teknik ekstraksi ultrasonik dengan pelarut etanol. Tahap kedua, yaitu uji aktivitas antioksidan ekstrak jahe menggunakan metode DPPH dan analisis ekstrak jahe menggunakan KCKT. Tahap terakhir, yaitu pengolahan data uji aktivitas antioksidan dan analisis KCKT dengan metode PCA dan PLSDA menggunakan perangkat lunak The Unscrambler X hingga diperoleh kelas jahe dan model mutu ekstrak jahe. Bagan alir penelitian dapat dilihat pada Lampiran 1.
Preparasi Sampel (Daryono 2010)
Jahe segar dibersihkan dari kotoran, kemudian diiris tipis-tipis dan dikeringkan dengan cara dijemur dan diangin-angikan. Setelah kering, jahe kemudian digiling hingga diperoleh simplisia jahe. Simplisia jahe dikeringkan dalam oven pada suhu 40 °C hingga kadar airnya kurang dari 10%.
Penentuan Kadar Air (WHO 1998)
Kadar air simplisia jahe ditentukan dengan gravimetri evolusi tidak langsung. Cawan porselin dikeringkan pada suhu 105 °C selama 30 menit dan didinginkan dalam eksikator. Sampel ditimbang sebanyak 3 gram dan dimasukkan ke dalam cawan porselin yang sudah diketahui bobotnya. Sampel kemudian dikeringkan dalam oven bersuhu 105 °C hingga diperoleh bobot konstan (perbedaan < 5 mg). Kadar air diperoleh dari nisbah selisih bobot awal dengan bobot sampel setelahdikeringkan terhadap bobot sampel sebelum dikeringkan.
Ket:
A = bobot sampel sebelum dikeringkan B = bobot sampel setelah dikeringkan
Penentuan Kadar Abu (WHO 1998) Sampel ditimbang sebanyak 2 gram dan dimasukkan ke dalam cawan porselin yang sudah dikeringkan pada suhu 105 °C selama 30 menit dan diketahui bobotnya. Cawan dipanaskan sampai sampel tidak berasap kemudian dipindahkan ke dalam tanur dan dipanaskan pada suhu 690 °C sampai semua karbon berwarna keabuan hilang. Cawan kemudian didinginkan dan ditimbang. Kadar abu diperoleh dari nisbah bobot abu dengan bobot sampel.
Kadar abu bobot sam elbobot abu 100
Ekstraksi Jahe (BPOM 2005, Anwar 2011) Simplisia jahe dari 3 daerah (Bogor, Tangerang, dan Ponorogo) diekstraksi dengan rasio bahan:pelarut adalah 1:5. Sebanyak 20 g simplisia jahe dicampur dengan 100 mL etanol 96% ke dalam labu erlenmeyer 250 mL. Campuran kemudian diekstraksi pada suhu 40 °C dengan gelombang ultrasonik 42 kHz selama 15 menit. Maserat disaring ke dalam erlenmeyer lain, sedangkan ampas diperlakukan sama sebanyak 2 kali ekstraksi. Hasil ekstraksi kemudian dipekatkan dengan penguap putar pada suhu 40 °C hingga diperoleh ekstrak kental. Ekstrak yang diperoleh ditentukan % rendemennya.
Uji Aktivitas Antioksidan Metode DPPH (Juarez et al. 2011).
Sebanyak 100 µL ekstrak dengan konsentrasi 1.5625, 3.125, 6.25, 12.5, 25, 50, dan 100 µg/mL ditambah dengan 100 µL larutan 1,1-difenil-2-pikrilhidrazil (DPPH) 125 µM dalam etanol pa. Setelah itu larutan diinkubasi selama 30 menit pada suhu 37 °C. Absorbansi sampel dibaca pada panjang gelombang 517 nm menggunakan spektrofotometer UV-Vis. Larutan yang hanya mengandung DPPH digunakan sebagai kontrol negatif. Aktivitas penangkapan DPPH dihitung berdasarkan persamaan:
ktivitas sam el
100
Nilai konsentrasi penghambatan 50% (IC50)
dihitung berdasarkan kurva kalibrasi menggunakan hasil persen aktivitas penangkapan DPPH dan log konsentrasi larutan ekstrak. IC50 menunjukkan nilai
konsentrasi sampel yang diperlukan untuk menghambat 50% radikal bebas DPPH.
Analisis Menggunakan KCKT (Lee et al.
2007)
Larutan standar campuran disiapkan dengan melarutkan masing-masing 10.0 mg senyawa dalam 25 mL metanol pa. Kemudian larutan diencerkan dalam labu takar 5 ml hingga diperoleh konsentrasi 50.0 µg/mL (6-gingerol), 25.0 µg/mL (8-(6-gingerol), 50.0 µg/mL (10-gingerol), dan 50.0 µg/mL (6-shogaol). Selanjutnya larutan standar diambil masing-masing 1 mL untuk dicampur, kemudian disaring melalui membran filter 0.45 µm dan ditempatkan dalam botol kecil. Untuk pembuatan larutan sampel, ekstrak jahe dari 3 daerah (Bogor, Tangerang, dan Ponorogo) ditimbang sebanyak 25 mg lalu dilarutkan dalam 5 mL metanol pa hingga diperoleh konsentrasi 5000 µg/mL. Selanjutnya larutan disaring melalui membran filter 0.45 µm dan ditempatkan dalam botol kecil. Larutan standar dan sampel yang telah disiapkan kemudian dianalisis menggunakan KCKT. Kolom yang digunakan adalah Simadzu C18, 4.6 x 250 mm, 5μm, 120 Å. Suhu kolom dijaga konstan sebesar 40 °C. Detektor yang digunakan adalah UV pada panjang gelombang 280 nm. Laju alir fase gerak 1 mL/menit. Volume larutan yang diinjeksikan adalah 20 µL. Fase gerak yang digunakan adalah air-asetonitril dalam modus gradien seperti disajikan pada Tabel 1. Pertama-tama dilakukan injeksi tunggal dari pelarut ekstrak (metanol), kemudian larutan standar dan sampel. Jumlah puncak yang muncul pada kromatogram setiap ekstrak dihitung. Data sidik jari KCKT masing-masing ekstrak dianalisis dan dibedakan berdasarkan jumlah puncak komponen dan waktu retensinya.
Tabel 1 Komposisi air-asetonitril pada elusi gradien KCKT
Waktu (menit) % air % asetonitril
0 60 40
10 60 40
40 10 90
40.5 0 100
45 0 100
45.5 50 60 60 40 40
Analisis Multivariat (Darusman et al. 2007)
Unscrambler X. Analisis menggunakan PCA berfungsi untuk membuat pola pengelompokan ekstrak berdasarkan kadar senyawa dominan dan sidik jari KCKT yang diperlihatkan pada plot skor dua dimensi. Plot skor untuk dua komponen utama (PC) pertama biasanya paling berguna dalam analisis karena kedua PC ini mengandung paling banyak keragaman dalam data. PLSDA berfungsi untuk membuat model mutu ekstrak. Model ini digunakan untuk menduga keterkaitan antara aktivitas antioksidan dengan senyawa dominan dan sidik jari KCKT dari ekstrak. Dalam PLSDA, data kadar senyawa dominan dan area sidik jari digunakan sebagai peubah bebas, sedangkan untuk data responnya digunakan peubah tak bebas yang berunsurkan 0 dan 1. Peubah tak bebas ini diturunkan dari nilai aktivitas antioksidan ekstrak. Jika nilai IC50 sampel < IC50 standar, maka diberikan
nilai 1, dan sebaliknya diberikan nilai 0. Pemberian nilai 0 dan 1 ini juga bisa dilakukan dari hasil pengelompokan aktivitas antioksidan, yaitu ekstrak dengan kelompok IC50 lebih kecil diberikan nilai 1 dan
sebaliknya diberikan nilai 0. Pemodelan dilakukan dengan memanfaatkan sarana regresi multivariat PLS.
HASIL DAN PEMBAHASAN
Deskripsi Karakteristik Kimia Rimpang Jahe
Analisis karakteristik kimia rimpang jahe gajah meliputi kadar air, kadar abu, dan rendemen ekstrak kasar yang reratanya disajikan pada Gambar 1 dan data lengkapnya berturut-turut pada Lampiran 2–4. Kadar air paling tinggi ditunjukkan oleh jahe asal Bogor, disusul jahe asal Ponorogo, kemudian Tangerang. Perbedaan ini umumnya dipengaruhi oleh proses pascapanen (pencucian, pengeringan, penggilingan, dan penyimpanan) (Rafi et al. 2012). Selain itu, iklim dan curah hujan juga berpengaruh terutama pada jahe segar. Kondisi geografis daerah asal jahe dapat dilihat pada Lampiran 5. Iklim basah dengan curah hujan sangat tinggi seperti daerah Bogor mengakibatkan tanaman jahe memiliki kadar air lebih besar. Sementara iklim dengan 2 musim (penghujan dan kemarau) seperti daerah Ponorogo dan Tangerang mengakibatkan jahe memiliki kadar air lebih kecil.
Kadar air penting untuk proses pengolahan jahe lebih lanjut. Simplisia jahe kering dengan
kadar air kecil akan memiliki masa simpan yang lebih lama. Jika kadar air tinggi, maka akan cepat rusak karena ditumbuhi kapang dan organisme lainnya. Tinggi rendahnya kadar air juga berpengaruh pada proses ekstraksi. Jika kadar air tinggi, maka zat-zat yang larut air seperti karbohidrat, protein, resin, dan gom akan ikut terekstraksi sehingga dapat memengaruhi jumlah dan komposisi komponen kimia dari rendemen yang diperoleh (Daryono 2010). Oleh karena itu, simplisia yang akan diproses lebih lanjut sebaiknya memiliki kadar air lebih kecil daripada standar mutu yang ditetapkan, yaitu SNI 01-7084-2005 (Lampiran 6). Kadar air simplisia jahe asal Ponorogo dan Tangerang telah memenuhi standar mutu tersebut, sehingga memiliki mutu lebih baik daripada simplisia jahe asal Bogor.
Gambar 1 Rerata kadar air, kadar abu, dan rendemen sampel rimpang jahe asal Ponorogo ( ), Tangerang ( ), dan Bogor ( )
Kadar abu menunjukkan kandungan mineral dalam jahe. Kadar abu jahe asal Ponorogo paling tinggi, disusul jahe asal Bogor, kemudian Tangerang. Sampel jahe asal Tangerang memiliki kadar abu lebih kecil daripada standar mutu, sedangkan kadar abu jahe asal Ponorogo dan Bogor lebih besar dari standar mutu yang ada. Perbedaan kadar abu umumnya dipengaruhi oleh jenis tanah dan ketersediaan hara di daerah asal jahe (Rafi et al. 2012). Ponorogo merupakan daerah dengan banyak pegunungan kapur sehingga mengandung banyak mineral terutama kalsium. Oleh karena itu, jahe asal Ponorogo memiliki kadar abu paling tinggi. Kondisi geografis daerah Bogor merupakan pegunungan yang subur dengan jenis tanah latosol, sedangkan daerah Tangerang merupakan dataran rendah juga dengan jenis tanah latosol. Jenis tanah ini tidak banyak mengandung mineral, sehingga kadar abunya lebih rendah.
0 5 10 15
Kadar air Kadar abu Rendemen
Ekstraksi simplisia jahe untuk memperoleh ekstrak kasar berupa oleoresin dipengaruhi oleh beberapa faktor, yaitu penyiapan bahan, jenis pelarut, metode dan kondisi proses ekstraksi, serta proses pemisahan/penguapan pelarut ekstrak (Purseglove et al. 1981).
Dalam penelitian ini digunakan ekstraksi ultrasonik yang memanfaatkan gelombang ultrasonik dengan frekuensi 42 kHz. Keuntungan metode ini antara lain waktu proses lebih singkat, produk lebih banyak, dan kualitas produk lebih baik (Widjanarko et al. 2011).
Pelarut etanol digunakan untuk ekstraksi karena memiliki beberapa keuntungan, yaitu titik didihnya rendah, aman, tidak beracun, dan tidak mudah terbakar. Meskipun demikian, etanol juga memiliki kelemahan, yaitu larut di dalam air sehingga dapat melarutkan komponen larut air seperti karbohidrat, protein, dan gom sehingga kemurnian oleoresin berkurang. Untuk memenuhi standar, ekstrak oleoresin harus diuapkan pelarutnya sampai batas yang tetap untuk setiap jenis pelarut. Pemisahan pelarut dilakukan dengan penguapan vakum pada suhu sekitar 40 °C untuk menghindari kerusakan senyawa dan penguapan minyak atsirinya (Purseglove et al. 1981).
Oleoresin jahe yang diperoleh berbentuk cairan sangat kental dan berwarna cokelat tua atau gelap dengan aroma khas jahe (Lampiran 7). Rendemen yang diperoleh berbeda-beda untuk setiap sampel, tetapi jumlahnya relatif sama untuk setiap daerah. Rendemen yang diperoleh berkisar antara 6.74 sampai 7.81% dan masih memenuhi standar mutu yang ada untuk penggunaan pelarut etanol. Rendemen ini cukup besar, meskipun pada penelitian Daryono (2010), penggunaan pelarut etanol 70% dan waktu ekstraksi 3 jam menghasilkan rendemen yang lebih besar (9.98%). Meskipun demikian, penggunaan ekstraksi ultrasonik dengan pelarut etanol 96% menghasilkan rendemen yang lebih besar dibandingkan dengan pelarut n-heksana yang hanya menghasilkan rendemen 1.58% pada jahe kering dan 1.13% pada jahe basah (Daryono 2010). Rendemen tidak terlalu dipengaruhi oleh kondisi geografis daerah asal jahe karena besarnya relatif sama. Namun, kemiripan jumlah rendemen tidak selalu menunjukkan kemiripan kandungan kimianya, sehingga perlu dilakukan analisis lebih lanjut.
Aktivitas Antioksidan Ekstrak Kasar Rimpang Jahe
Analisis aktivitas antioksidan ekstrak kasar jahe dilakukan menggunakan metode DPPH karena mudah, cepat, dan sensitif. Larutan DPPH berwarna ungu dan mengabsorpsi kuat pada panjang gelombang 517 nm. Antioksidan bereaksi dengan DPPH dengan cara menyumbangkan atom hidrogen atau elektron sehingga mengubah DPPH ke bentuk DPPH-H (hidrazina). Tingkat penghilangan warna menunjukkan potensi peredaman radikal bebas dari senyawa antioksidan. Pada waktu bereaksi, larutan mengalami perubahan warna dari ungu ke kuning (Lampiran 8), dan intensitas warna bergantung pada kemampuan antioksidan (Semuel 2008).
Uji aktivitas antioksidan melalui penentuan nilai IC50 menunjukkan rerata nilai
IC50 jahe asal Bogor lebih besar daripada jahe
asal Ponorogo dan Tangerang (Tabel 2). Data lengkap uji aktivitas antioksidan ini dapat dilihat pada Lampiran 9. Nilai IC50 semua
sampel berkisar antara 9.34 sampai 21.13 µg/mL. Hal ini menunjukkan bahwa ekstrak etanol rimpang jahe berpotensi sebagai antioksidan sangat kuat karena memiliki nilai IC50 di bawah 50 µg/mL (Jun et al. 2003). IC50
merupakan konsentrasi yang dapat menghambat 50% radikal bebas. Semakin kecil nilai IC50, aktivitas penghambatan
radikal bebas dari ekstrak semakin bagus.
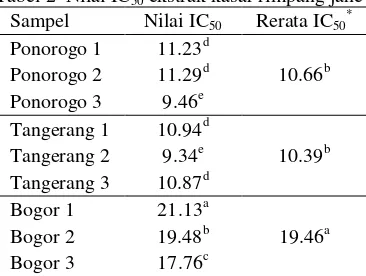
Tabel 2 Nilai IC50 ekstrak kasar rimpang jahe
Sampel Nilai IC50 Rerata IC50 *
Ponorogo 1 11.23d
Ponorogo 2 11.29d 10.66b Ponorogo 3 9.46e
Tangerang 1 10.94d
Tangerang 2 9.34e 10.39b Tangerang 3 10.87d
Bogor 1 21.13a
Bogor 2 19.48b 19.46a Bogor 3 17.76c
*Angka-angka pada kolom yang sama yang diikuti oleh
huruf yang sama tidak berbeda nyata pada taraf uji 5% (uji selang berganda Duncan).
diduga paling aktif sebagai antioksidan adalah 6-gingerol dan 6-shogaol (Suhaj 2004). Antioksidan alami cenderung aman dan juga memiliki potensi sebagai antivirus, antiradang, antikanker, antitumor, dan memiliki sifat hepatoprotektif (Lim dan Murtijaya 2007).
Uji Duncan nilai IC50 digunakan untuk
melihat pengelompokan aktivitas antioksidan di antara ketiga daerah. Hasil uji menunjukkan rerata nilai IC50 berbeda nyata untuk daerah
Bogor dan tidak berbeda nyata untuk daerah Ponorogo dan Tangerang (Lampiran 10). Hasil dikatakan berbeda nyata jika nilai Pr < selisih rata-rata tiap perlakuan. F hitung > F tabel artinya menolak hipotesis bahwa rata-rata antarperlakuan yang dicobakan sama. Nilai 0.05 merupakan taraf signifikansi dan diberi simbol atau α yang dinyatakan dalam proporsi atau persentase, sedangkan nilai (1-α)100 disebut taraf ke ercayaan. Jika α sebesar 0.05 atau 5% berarti sama dengan menentukan taraf kepercayaan sebesar (1-0.05)=0.95 atau 95% (Winer 1971). Uji Duncan menghasilkan 2 kelompok jahe, yaitu kelompok I (Bogor) dan kelompok II (Tangerang dan Ponorogo).
Pengelompokan aktivitas antioksidan menggunakan PCA menghasilkan plot skor 2 dimensi (Gambar 2), yang menunjukkan 2 kelompok aktivitas antioksidan. Kelompok I memiliki nilai IC50 lebih besar, yaitu jahe asal
Bogor dan kelompok II memiliki nilai IC50
lebih kecil, yaitu jahe asal Tangerang dan Ponorogo. Berdasarkan aktivitas antioksidan, jahe kelompok II memiliki mutu lebih baik. Pengelompokan aktivitas antioksidan berdasarkan PCA telah sesuai dengan uji Duncan.
Gambar 2 Plot skor PCA pada pengelompokan jahe
berdasarkan aktivitas antioksidan
Analisis Kuantitatif Gingerol dan Shogaol Menggunakan KCKT
Analisis KCKT dilakukan terhadap seluruh sampel ekstrak kasar jahe menggunakan standar campuran yang berisi 6-, 8-, dan 10-gingerol, serta 6-shogaol dengan konsentrasi
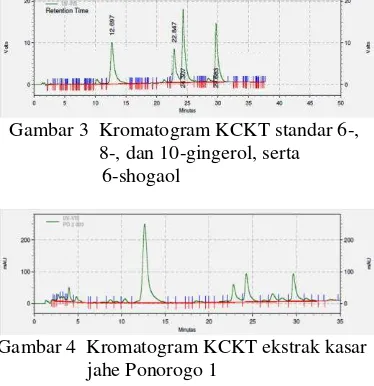
berturut-turut 50, 25, 50, dan 50 µg/mL. Fase diam hidrofobik (C18) digunakan dengan fase gerak air dan asetonitril dalam modus gradien yang mengelusi selama 35 menit. Setiap sampel diukur 1 kali sehingga diperoleh 9 kromatogram (Lampiran 11). Contoh kromatogram standar dan sampel disajikan pada Gambar 3 dan 4. Berdasarkan kromatogram standar, waktu retensi 6-, 8-, dan 10-gingerol, serta 6-shogaol berturut-turut 12.697, 22.847, 29.683, dan 24.307 menit.
Gambar 3 Kromatogram KCKT standar 6-, 8-, dan 10-gingerol, serta
6-shogaol
Gambar 4 Kromatogram KCKT ekstrak kasar jahe Ponorogo 1
Kromatogram seluruh sampel memperlihatkan puncak-puncak yang bentuknya mirip satu sama lain dan hanya berbeda pada besarnya area dan waktu retensi (Lampiran 11). Perbedaan pola sidik jari dari tanaman yang sejenis pada umumnya tidak kasatmata. Dengan alat KCKT, waktu retensi dan area dari puncak-puncak kromatogram dapat direkam sehingga menghasilkan banyak data. Data sidik jari KCKT dapat dilihat pada Lampiran 12. Data yang diperoleh memiliki kisaran waktu retensi dari 2.740 sampai 34.023 menit. Waktu retensi untuk senyawa 6-, 8-6-, dan 10-gingerol6-, serta 6-shogaol pada seluruh sampel berturut-turut berkisar pada 12.6, 22.8, 29.6, dan 24.3 menit. Area sidik jari berjumlah sekitar 87–96% dari total area keseluruhan puncak kromatogram. Senyawa yang mendominasi kromatogram adalah 6-gingerol dengan jumlah sekitar 30–57% dari total area, sedangkan 6-shogaol memiliki jumlah sekitar 9–17% dari total area. Struktur kimia 6-gingerol dan 6-shogaol ditunjukkan oleh Gambar 5 (Chrubasik dan Pitler 2005). I
(a) (b)
Gambar 5 Struktur kimia 6-gingerol (a) dan 6-shogaol (b)
Perbedaan waktu retensi dipengaruhi oleh kepolaran senyawa, struktur kimia senyawa, dan fase gerak KCKT. Pelarut ekstrak untuk analisis KCKT ialah metanol murni, sehingga larutan bersifat polar (Ramadhan dan Phaza 2007). Pada kondisi awal injeksi, komposisi air lebih besar dari asetonitril, sehingga senyawa-senyawa yang bersifat polar seperti 6-gingerol terdeteksi lebih awal. Pada tahap akhir, komposisi asetonitril menjadi lebih besar dari air. Hal ini menyebabkan senyawa-senyawa yang bersifat kurang polar seperti 10-gingerol terdeteksi lebih akhir. Senyawa 8-gingerol dan 6-shogaol memiliki kepolaran yang hampir sama sehingga memiliki waktu retensi yang berdekatan.
Kepolaran keempat senyawa tersebut dipengaruhi oleh jumlah atom oksigen dan panjang rantainya. Semakin banyak atom oksigen pada senyawa, maka kepolaran akan meningkat. Sama dengan senyawa yang berantai pendek dan tidak bercabang, maka akan bersifat lebih polar. Oleh karena itu, senyawa lebih polar akan terdeteksi lebih awal mengikuti komposisi fase gerak, sedangkan senyawa kurang polar akan terdeteksi lebih akhir.
Jahe memiliki kandungan senyawa dalam jumlah tertentu yang dapat menjadi acuan kualitas jahe. Senyawa tersebut dapat merupakan senyawa penanda, senyawa dengan efek farmakologi paling bagus, atau senyawa yang paling berpengaruh terhadap senyawa lain yang dicampurkannya. Sejauh ini, senyawa yang diketahui sebagai komponen utama pada jahe adalah gingerol dan shogaol. Gingerol merupakan senyawa utama pembentuk rasa pedas pada jahe, sedangkan shogaol merupakan senyawa pembentuk rasa pahit pada jahe (Bhattarai et al. 2001). Hasil penentuan kadar 6-, 8-, dan 10-gingerol, serta 6-shogaol menggunakan KCKT disajikan pada Tabel 3 untuk reratanya dan Lampiran 13 untuk data lengkap serta perhitungannya.
Tabel 3 Rerata kadar gingerol dan shogaol hasil KCKT dalam simplisia jahe
Sampel
Rerata jumlah analit dalam simplisia jahe (mg/g)* 6-gingerol 8-gingerol 6-shogaol 10-gingerol Ponorogo 14.92b 2.30a 2.99a 3.95a
Tangerang 22.03a 1.86b 3.02a 0.75b
Bogor 10.23c 1.90ab 3.29a 3.63a *Angka-angka pada kolom yang sama yang diikuti oleh
huruf yang sama tidak berbeda nyata pada taraf uji 5% (uji selang berganda Duncan).
Data memperlihatkan 6-gingerol sebagai senyawa paling dominan, sedangkan 8-gingerol merupakan senyawa dengan jumlah paling kecil dari ekstrak jahe yang dianalisis. Konsentrasi senyawa gingerol dan 6-shogaol sesuai dengan rentang konsentrasi yang dilaporkan oleh Suhaj (2004), yaitu 130– 7138 µg/mL untuk 6-gingerol dan 40–330 µg/mL untuk 6-shogaol. Uji Duncan menunjukkan senyawa 6-gingerol berbeda nyata untuk semua daerah, 8-gingerol dan 6-shogaol tidak berbeda nyata untuk semua daerah, dan 10-gingerol berbeda nyata untuk Tangerang dan tidak berbeda nyata untuk Ponorogo dan Bogor (Lampiran 14). Hal ini menunjukkan bahwa senyawa 6- dan 10-gingerol memiliki jumlah yang lebih bervariasi dibandingkan dengan 8-gingerol dan 6-shogaol.
Variasi kadar senyawa pada jahe umumnya dipengaruhi oleh variasi lingkungan pertumbuhan, kondisi geografis (iklim, jenis tanah, dan ketersediaaan hara), waktu panen, dan proses pengolahan pascapanen (pencucian, pengeringan, penggilingan, penyimpanan, dan ekstraksi) (Rafi et al. 2012). Kondisi lingkungan tumbuh yang menimbulkan stres terhadap suatu tanaman, seperti keterbatasan air dan suhu tinggi akan meningkatkan kandungan senyawa pada jahe.
Berdasarkan hasil analisis, jahe asal Tangerang memiliki kadar gingerol tertinggi, disusul oleh jahe asal Ponorogo, kemudian Bogor. Hal ini sesuai dengan fakta bahwa kondisi iklim dan tanah di daerah Tangerang sangat mendukung untuk pertumbuhan jahe. Jahe asal Ponorogo memiliki kandungan gingerol dengan jumlah terbesar kedua. Hal ini sesuai dengan kondisi iklim yang mirip dengan jahe asal Tangerang. Berbeda dengan daerah Bogor yang memiliki curah hujan sepanjang tahun, sehingga kadar gingerol dalam jahe jumlahnya rendah. Besarnya kandungan senyawa aktif belum tentu memperlihatkan kualitas jahe, sehingga diperlukan analisis lebih lanjut terhadap keseluruhan senyawa pada jahe.
Klasifikasi Rimpang Jahe Menggunakan PCA
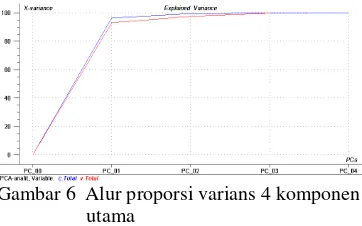
Analisis komponen utama dilakukan terhadap senyawa dominan (6-, 8-, dan 10-gingerol, serta 6-shogaol) dan sidik jari KCKT untuk mengetahui pemisahan antardaerah. Pada analisis senyawa dominan, jenis sampel digunakan sebagai respon dan jenis senyawa sebagai variabel bebasnya. Analisis ini menghasilkan 4 buah PC dengan varians yang berbeda, yaitu PC1 96%, PC2 3%, PC3 1%, dan PC4 0% (Gambar 6). Total nilai varians seluruh PC sebesar 100%. PC1 memiliki nilai varians paling besar karena digunakan untuk memaksimumkan varians data, sedangkan PC selanjutnya digunakan untuk memaksimumkan data sisaan.
Gambar 6 Alur proporsi varians 4 komponen utama
Klasifikasi sampel berdasarkan senyawa dominan menggunakan 2 PC pertama dapat menjelaskan 99% dari total keragaman (PC1: 96%, PC2: 3%). Plot loading menggambarkan besarnya korelasi antara variabel asal dengan komponen utama. Plot loading yang dihasilkan menunjukkan letak 6-, 8-,dan 10-gingerol, serta 6-shogaol yang saling berjauhan (Gambar 7). Hal ini berpengaruh pada letak plot skor yang dihasilkan. Plot skor pada Gambar 7 menghasilkan 3 kelompok jahe, yaitu kelompok I (Tangerang), kelompok II (Ponorogo), dan kelompok III (Bogor). Sampel Ponorogo 2 tidak termasuk ke dalam kelompok karena kadar senyawa yang diperoleh berada di antara Bogor dan Ponorogo. Berkelompoknya plot menunjukkan bahwa komposisi senyawa dominan dalam ekstrak kasar jahe memiliki jumlah yang mirip satu sama lain. Selain itu, plot skor berdasarkan kadar senyawa dominan sudah dapat mengelompokkan jahe berdasarkan daerah asalnya.
Gambar 7 Plot skor dan loading PCA pada pengelompokan jahe berdasarkan kadar senyawa 6-, 8-, dan 10-gingerol, serta 6-shogaol.
Analisis komponen utama terhadap sidik jari KCKT menggunakan jenis sampel sebagai respon dan waktu retensi sebagai variabel bebasnya. Analisis ini menghasilkan 7 buah PC dengan varians yang berbeda, yaitu PC1 89%, PC2 8%, PC3 2%, PC4 0%, PC5 0%,
PC6 0%, dan PC7 0% (Gambar 8). Total nilai varians seluruh PC sebesar 99%.
I
III
Gambar 8 Alur proporsi varians 7 komponen utama
Klasifikasi sampel berdasarkan sidik jari KCKT menggunakan 2 nilai PC pertama dapat menjelaskan 97% dari total keragaman (PC1: 89%, PC2: 8%). Plot loading yang menunjukkan waktu retensi nomor 7, 9, 10, dan 14 dengan senyawa secara berturut-turut 6-gingerol, 8-gingerol, 6-shogaol, dan
10-gingerol memiliki letak yang berjauhan (Gambar 9). Hal ini menunjukkan bahwa senyawa tersebut paling berpengaruh terhadap letak plot skor. Plot skor pada Gambar 9 menghasilkan 3 kelompok jahe, yaitu kelompok I (Tangerang), kelompok II (Ponorogo), dan kelompok III (Bogor). Jahe asal Tangerang dan Ponorogo memiliki pola pengelompokan yang mirip dengan pengelompokan berdasarkan senyawa dominan. Sementara jahe asal Bogor memiliki pola yang lebih acak dibandingkan dengan pengelompokan berdasarkan senyawa dominan. Hal ini menunjukkan bahwa kandungan senyawa pada jahe asal Tangerang dan Ponorogo memiliki konsistensi yang lebih besar daripada jahe asal Bogor.
Gambar 9 Plot skor dan loading PCA pada pengelompokan jahe berdasarkan sidik jari KCKT.
Pengelompokan sampel berdasarkan senyawa dominan maupun sidik jari KCKT memperlihatkan pola yang berbeda dengan pengelompokan berdasarkan aktivitas antioksidan. Pengelompokan berdasarkan aktivitas antioksidan menghasilkan 2 kelompok, sedangkan berdasarkan senyawa dominan maupun sidik jari menghasilkan 3 kelompok berdasarkan asal daerah. Hal ini menunjukkan bahwa pengelompokan sampel menggunakan PCA belum bisa dikaitkan dengan aktivitas antioksidannya. Oleh karena tidak ada kesesuaian pola, maka diperlukan analisis lebih lanjut untuk mengetahui korelasi antara aktivitas antioksidan jahe dengan senyawa dominan maupun sidik jarinya.
Analisis PLSDA untuk Model Mutu Ekstrak Jahe
Pendugaan keterkaitan antara senyawa dominan (, 8-, dan 10-gingerol, serta 6-shogaol) dan sidik jari KCKT dengan aktivitas antioksidan memerlukan metode pemodelan lain, yaitu PLSDA. Metode ini sering digunakan untuk pengenalan pola dan
pembentukan suatu model. Pembuatan model dilakukan dengan cara meregresikan komponen utama dari dua variabel yang digunakan. Dalam kasus dua kelompok, biasanya nilai dari peubah tak bebas diberikan 1 untuk satu kelompok dan 0 atau -1 untuk kelompok lainnya (Hakim 2010). Berbeda dengan metode PCA, kebaikan model klasifikasi pada metode PLSDA cukup dilihat dari nilai determinant coefficient (R2), root mean square error of calibration (RMSEC), dan root mean square error of prediction (RMSEP). Nilai RMSE merupakan galat yang dihasilkan dari model PLSDA (Jing et al. 2011).
PLSDA menggunakan data kadar senyawa dominan dan area sidik jari sebagai peubah bebas, sedangkan untuk data responnya digunakan peubah tak bebas yang bernilai 0 dan 1. Peubah tak bebas ini diturunkan dari nilai aktivitas antioksidan ekstrak. Pemberian nilai 0 dan 1 ini dilakukan dari hasil pengelompokan aktivitas antioksidan, yaitu ekstrak dengan kelompok IC50 lebih kecil
(Tangerang dan Ponorogo) diberikan nilai 1 dan kelompok IC50 lebih besar (Bogor)
III
II
diberikan nilai 0. Masing-masing sampel dianalisis hingga diperoleh slope, RMSE, R2, dan korelasi. Model PLSDA dapat dilihat pada Lampiran 15 dan 16. Y1 merupakan model
untuk sampel yang lebih aktif, sedangkan Y2
merupakan model untuk sampel yang kurang aktif.
Hasil PLSDA antara senyawa dominan dan aktivitas antioksidan disajikan pada Tabel 4. Model kalibrasi dan prediksi untuk Y1 dan Y2
memiliki nilai slope, RMSE, R2, dan korelasi yang sama dan hanya berbeda pada nilai B0. B0 merupakan koefisien regresi, yaitu perkiraan besarnya rata-rata Y ketika kenaikan
nilai X=0. Slope merupakan perkiraan besarnya perubahan nilai variabel Y bila nilai variabel X berubah satu unit pengukuran. Model Y1 menghasilkan nilai B0 negatif,
sedangkan Y2 menghasilkan nilai B0 positif.
Nilai R2 mengindikasikan mutu data antara konsentrasi nyata dan dugaan. Nilai R2 yang mendekati 1 menunjukkan bahwa antara konsentrasi nyata dan dugaan memiliki nilai yang sangat dekat. Nilai R2 yang diperoleh kurang mendekati 1, sehingga konsentrasi nyata dan dugaan memiliki nilai yang kurang dekat.
Tabel 4 Model PLSDA antara senyawa dominan dan aktivitas antioksidan
Model Set Β0 Slope RMSE R2 Korelasi
Y1
kalibrasi -3.139550 0.802999 0.209232 0.802999 0.896102 prediksi -3.139550 0.733709 0.275425 0.730280 0.816717
Y2
kalibrasi 4.139549 0.802999 0.209232 0.802999 0.896102 prediksi 4.139549 0.733709 0.275425 0.730280 0.816717
Nilai RMSEC dan RMSEP secara berurutan menunjukkan kesesuaian jumlah puncak dugaan dengan puncak yang dideteksi pada data yang digunakan untuk membangun model. Semakin kecil nilai RMSEC dan RMSEP, semakin baik model regresi yang dibangun (Naes et al. 2002). Nilai RMSEC yang diperoleh cukup kecil dan lebih kecil dari nilai RMSEP, sehingga model yang dihasilkan sudah cukup baik. Nilai korelasi dari set kalibrasi dan prediksi belum mendekati 1 atau masih lebih kecil dari 95%. Oleh karena itu, penggunaan senyawa dominan belum mampu menduga aktivitas antioksidan pada jahe.
Hasil PLSDA antara sidik jari KCKT dan aktivitas antioksidan disajikan pada Tabel 5.
Model kalibrasi dan prediksi untuk Y1 dan Y2
memiliki nilai slope, RMSE, R2, dan korelasi yang sama dan hanya berbeda pada nilai B0. Model Y1 menghasilkan nilai B0 negatif,
sedangkan Y2 menghasilkan nilai B0 positif.
Nilai R2 kalibrasi yang diperoleh sudah mendekati 1 dan lebih besar dari R2 prediksi, sehingga antara konsentrasi nyata dan dugaan memiliki nilai yang sangat dekat. Nilai RMSEC yang diperoleh sangat kecil dan lebih kecil dari nilai RMSEP, sehingga model yang dihasilkan sudah baik. Nilai korelasi untuk set kalibrasi dan prediksi yang dihasilkan sangat baik karena memiliki rerata lebih besar dari 95%. Oleh karena itu, sidik jari KCKT sudah mengandung informasi penting untuk menduga aktivitas antioksidan pada jahe.
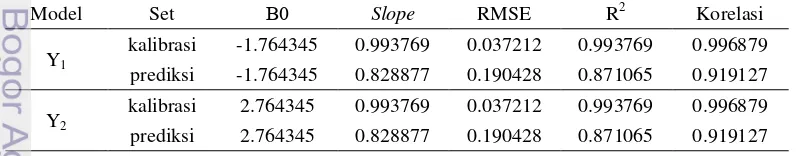
Tabel 5 Model PLSDA antara sidik jari KCKT dan aktivitas antioksidan
Model Set Β0 Slope RMSE R2 Korelasi
Y1
kalibrasi -1.764345 0.993769 0.037212 0.993769 0.996879 prediksi -1.764345 0.828877 0.190428 0.871065 0.919127
Y2
kalibrasi 2.764345 0.993769 0.037212 0.993769 0.996879 prediksi 2.764345 0.828877 0.190428 0.871065 0.919127
Hasil dari kedua model PLSDA menunjukkan korelasi yang lebih besar untuk analisis sidik jari daripada senyawa dominan. Hal ini menunjukkan bahwa aktivitas antioksidan jahe lebih ditentukan oleh keseluruhan senyawa dibandingkan dengan senyawa dominan. Menurut Suhaj (2004), senyawa selain gingerol dan shogaol yang
KCKT dengan aktivitas antioksidan dapat digunakan untuk menentukan aktivitas antioksidan pada sampel jahe yang belum diketahui. Dengan demikian, teknik sidik jari KCKT yang dipadukan dengan PLSDA dapat dimanfaatkan untuk metode cepat dalam menentukan kualitas jahe menggunakan ekstrak kasarnya.
SIMPULAN DAN SARAN
Simpulan
Teknik sidik jari kromatografi cair kinerja tinggi (KCKT) yang dipadukan dengan analisis multivariat berpotensi digunakan untuk kontrol kualitas jahe gajah asal Bogor, Ponorogo, dan Tangerang. Uji aktivitas antioksidan terhadap ekstrak etanol rimpang jahe menunjukkan bahwa semua sampel berpotensi sebagai antioksidan sangat kuat dengan IC50 10.39 µg/mL untuk Tangerang,
10.66 µg/mL untuk Ponorogo, dan 19.46 µg/mL untuk Bogor. Hasil analisis KCKT menunjukkan , 8-, dan 10-gingerol, serta 6-shogaol sebagai senyawa dominan dalam jahe dari ketiga daerah dengan jumlah secara berturut-turut 30.50–56.03%, 5.08–8.95%, 1.76–14.83%, dan 9.17–16.09% dari total area keseluruhan. Pengelompokan menggunakan PCA menghasilkan 2 kelompok berdasarkan aktivitas antioksidan dan 3 kelompok berdasarkan senyawa dominan maupun sidik jari KCKT. Berdasarkan senyawa dominan dan aktivitas antioksidan, jahe asal Tangerang dan Ponorogo memiliki mutu lebih baik daripada jahe asal Bogor. Model mutu yang dibentuk menggunakan PLSDA menghasilkan korelasi lebih kecil dari 95% untuk senyawa dominan dan lebih besar dari 95% untuk sidik jari KCKT. Oleh karena itu, penggunaan senyawa dominan belum mampu menduga aktivitas antioksidan pada jahe, sedangkan sidik jari KCKT sudah mengandung informasi penting untuk menduga aktivitas antioksidan pada jahe. Hal ini menunjukkan bahwa aktivitas antioksidan jahe lebih ditentukan oleh komposisi keseluruhan senyawa dibandingkan dengan senyawa dominan
Saran
Kontrol kualitas tanaman jahe perlu dilakukan pada varietas tanaman jahe lain dan daerah asal jahe dengan kondisi geografis yang lebih beragam. Perlu dilakukan pula analisis diskriminan lebih lanjut dengan
metode diskriminasi lain terhadap sampel yang lebih banyak untuk menghasilkan prediksi mutu yang lebih sahih.
DAFTAR PUSTAKA
[Anonim]. 2012. Pemerintah Kabupaten Ponorogo. [terhubung berkala]. http://www.ponorogo.go.id/ [24 Okt 2012].
[Anonim]. 2012. Pemerintah Kota Bogor.
[terhubung berkala].
http://www.kotabogor.go.id/ [24 Okt 2012].
[Anonim]. 2012. Pemerintah Kota Tangerang Selatan. [terhubung berkala]. http://www.tangerangselatankota.go.id/ [24 Okt 2012].
[BPOM] Badan Pengawas Obat dan Makanan RI. 2005. Monografi Ekstrak Tumbuhan Obat Indonesia Volume 1. Jakarta: BPOM RI.
[SNI] Standar Nasional Indonesia. 2005. Jahe untuk Bahan Baku Obat. Jakarta: Badan Standardisasi Nasional.
[WHO] World Health Organization. 1998. Quality Control Methods for Medicinal Plant Materials. England: WHO. ISBN 92 4 154510 0.
Anwar H. 2011. Pola sidik jari kromatogram KLT untuk identifikasi keragaman kualitas jahe merah [skripsi]. Bogor: Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor.
Bhattarai S, Tran VH, Duke CC. 2001. Stability of gingerol and shogaol in simulated gastric and intestinal fluid. Pharmaceutical and Biomedical Analysis 45: 648–653.
Cai Y, Sun M, Corke H. 2003. Antioxidant activity of betalains from plants of the Amaranthacea. J Agric Food Chem 51: 2288–2294.
Chen YM. 2006. Traditional Chinese medicine industry development and their impact and countermeasures. Mod Chin Med 8: 35–391.
Phytotherapy & Phytopharmacology 12: 684–701.
Darusman LK, Heryanto R, Rafi M, Wahyuni WT. 2007. Potensi daerah sidik jari spektrum inframerah sebagai penanda bioaktivitas ekstrak tanaman obat. Jurnal llmu Pertanian Indonesia 12 (3): 154–162.
Daryono ED. 2010. Oleoresin dari jahe menggunakan proses ekstraksi dengan pelarut etanol. Jurnal Ekstrak 3 (3).
Djubaedah E. 1986. Ekstraksi Oleoresin dari Jahe. Bogor: Balai Besar Penelitian dan Pengembangan Industri Hasil Pertanian.
Ernst E. 2002. Toxic heavy metals and undeclared drugs in Asian herbal medicines. Trends Pharmacol Sci 23: 136– 139.
Hakim F. 2010. Penerapan metode transformasi wavelet diskret dan partial least square discriminant analysis (PLSDA) untuk klasifikasi komponen obat bahan alam [skripsi]. Bogor: Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor.
Harmono dan Andoko. 2005. Budidaya dan Peluang Bisnis Jahe. Jakarta: Agromedia Pustaka.
Jiang B, Kronenberg F, Nuntanakorn P, Qiu MH, Kennelly EJ. 2006. Evaluation of the botanical authenticity and phytochemical profile of black cohosh products by high performance liquid chromatography with selected ion monitoring liquid chromatography-mass spectrometry. J Agric Food Chem 54: 3242–3253.
Jing et al. 2011. Application of chemometrics in quality evaluation of medicinal plants. Journal of Medicinal Plants Research 5 (17): 4001–4008.
Juarez AG, Cavazos LS, Aranda RS, Meseguer JP, Torres NW. 2011. Correlation between chromatographic fingerprint and antioxidant activity of Turnera diffusa (Damiana). Planta Med 77: 958–963
Jun MHY, Yu J, Fong X, Wan CS, Yang CT, Ho. 2003. Comparison of antioxidant activities of isoflavones from kudzu root (Pueraria labata Ohwl.). J. Food Sci 68: 2117–2122.
Kikuzaki K, Nakatani N. 1993. Antioxidant effects of some ginger constituents. Journal of Food Sci 58 (6): 1407–1410. Lee S, Khoo C, Halstead CW, Huynh T,
Bensoussan A. 2007. Liquid chromatographic determination of 6-, 8-, 10-gingerol, and 6-shogaol in ginger (Zingiber officinale) as the raw herb and dried aqueous extract. Journal of AOAC International 90 (5): 1219–1226.
Liang YZ, Xie PS, Chan K. 2004. Quality control of herbal medicines. Chromatogr B 812: 53–70.
Lim YY, Murtijaya J. 2007. Antioxidant properties of Phyllanthus amarus as affected by different drying methods. LebensmWish Technol 40: 1664–1669. Naes T, Isakkson T, Fearn T, Davies T. 2002.
A User-Friendly Guid to Multivariate Calibration and Classification. Chichester: NIR Publication.
Purseglove JW, Brown EG, Green CL, Robbins SRJ. 1981. Spices 2.
Rafi M, Lim LW, Takeuchi T, Darusman LK. 2012. Simultaneous determination of gingerols and shogaol using capillary liquid chromatography and its application in discrimination of three ginger varieties from Indonesia. J Talanta 103: 28–32. Ramadhan E, Phaza AH. 2007. Pengaruh
konsentrasi etanol, suhu, dan jumlah stage pada ekstraksi oleoresin jahe secara batch [skripsi]. Semarang: Fakultas Teknik, Universitas Diponegoro.
Semuel MY. 2008. Aktivitas antioksidan dan antikanker ekstrak kulit batang langsat (Lansium domesticum L.) [tesis]. Bogor: Sekolah Pasca Sarjana, Institut Pertanian Bogor.
Suhaj M. 2004. Spice antioxidants isolation and their antiradical activity: a review. Journal of Food Composition and Analysis 19: 531–537.
Tao et al. 2011. Chemical fingerprint technique and its application in Gastrodia tuber. African Journal of Biotechnology 10 (74): 16746–16756.
Pengetahuan Alam, Institut Pertanian Bogor.
Wahyuni WT. 2010. Pengoptimuman dan validasi sidik jari kromatografi cair kinerja tinggi ekstrak Phyllanthus niruri L [tesis]. Bogor: Sekolah Pasca Sarjana, Institut Pertanian Bogor.
Widjanarko SB, Sutrisno A, Faridah A. 2011. Efek hidrogen peroksida terhadap sifat fisiko-kimia tepung porang (Amorphophallus oncophyllus) dengan metode maserasi dan ultrasonik. Jurnal Teknologi Pertanian 12 (3): 143–152. Winer BJ. 1971. Statistical Principles in
Lampiran 1 Bagan alir penelitian
ekstraksi ultrasonik
Rimpang jahe segar
Tr & area
Simplisia jahe
Ekstrak jahe
Kromatogram
Kelompok
jahe
IC
50Peubah boneka
(0 & 1)
Kadar 6-, 8-,
10-gingerol,
& 6-shogaol
Kelompok
jahe
dikeringkan, dihaluskan
penentuan kadar air & abu
analisis KCKT
PCA
penetuan kadar
senyawa
PCA
uji aktivitas antioksidan
Tr & area
Model (kalibrasi
& prediksi
Lampiran 2 Kadar air sampel rimpang jahe
Asal
daerah Sampel
Bobot sampel awal (a) (g)
Bobot sampel setelah pengeringan (b) (g)
Kadar air (%)
Rerata kadar air (%)
Ponorogo
1 3.0047 2.6931 10.37
2 3.0027 2.7563 8.21 9.22
3 3.0012 2.7287 9.08
Tangerang
1 3.0056 2.7356 8.98
2 3.0068 2.7266 9.32 8.92
3 3.0016 2.7478 8.46
Bogor
1 3.0032 2.6632 11.32
2 3.0049 2.6498 11.82 11.53
3 3.0051 2.6611 11.45
Contoh perhitungan
Penentuan kadar air sampel Ponorogo 1 Kadar air a ba 100
Kadar air .004 g 2.6 1 g
.004 g 100 10.
Lampiran 3 Kadar abu sampel rimpang jahe
Asaldaerah Sampel
Bobot sampel awal (a) (g)
Bobot abu (b) (g)
Kadar abu (%)
Rerata kadar abu (%)
Ponorogo
1 2.0062 0.1971 9.82
2 2.0012 0.1979 9.89 9.78
3 2.0017 0.1927 9.63
Tangerang
1 2.0014 0.0934 4.67
2 2.0034 0.1023 5.11 4.89
3 2.0015 0.0979 4.89
Bogor
1 2.0027 0.1160 5.79
2 2.0024 0.1202 6.00 6.41
3 2.0082 0.1497 7.45
Contoh perhitungan
Penentuan kadar abu sampel Ponorogo 1 Kadar abu a
b 100 Kadar abu 0.1 1 g
Lampiran 4 Rendemen ekstrak kasar rimpang jahe
Asal
daerah Sampel
Bobot sampel awal (g)
Kadar air (%)
Bobot ekstrak (g)
Rendemen (%)
Rerata rendemen (%)
Ponorogo
1 20.0045 10.37 1.3585 7.58
2 20.0008 8.21 1.3003 7.08 7.23
3 20.0044 9.08 1.2766 7.02
Tangerang
1 20.0094 8.98 1.3233 7.27
2 20.0044 9.32 1.2235 6.74 7.14
3 20.0062 8.46 1.3553 7.40
Bogor
1 20.0038 11.32 1.3227 7.46
2 20.0029 11.82 1.2991 7.37 7.55
3 20.0024 11.45 1.3828 7.81
Contoh perhitungan
Penentuan rendemen sampel Ponorogo 1
endemen bobot sam el a al 1 fraksi bobot kadar air bobot ek trak 100
endemen 20.0045 g 1 0.10 )1. 585 g 100 .58
Lampiran 5 Kondisi geografis daerah asal jahe
Daerah Ponorogo Tangerang Bogor
Topografi
92–2.563 mdpl (dataran rendah, dataran tinggi bergelombang, pegunungan)
0–25 mdpl (dataran rendah)
15–2500 mdpl (dataran rendah, dataran rendah bergelombang, pegunungan)
Iklim
tropis dua musim, kemarau dan penghujan
tropis dua musim, kemarau dan penghujan
tropis basah dan sangat basah (penghujan)
Curah hujan ±1500 mm/tahun ±1475 mm/tahun 2500–5.000 mm/tahun
Jenis tanah
podsolik (coklat, kuning, lempung berpasir hingga liat) dan kapur
latosol (merah dan coklat kemerahan)
latosol (merah, coklat kemerahan, coklat sampai kuning)
Lampiran 6 Standar mutu simplisia jahe kering berdasarkan SNI 01-7084-2005
Karakteristik Syarat mutu
Berjamur dan berserangga tidak ada
Bau dan rasa khas jahe
Kadar air (% b/b), maksimum 10
Kadar abu (% b/b), maksimum 5
Benda asing (% b/b), maksimum 2
Kadar minyak atsiri (mL/100g), minimum 1.5 Kadar ekstrak larut etanol (%), minimum 4.3
Lampiran 7 Contoh foto rendemen ekstrak kasar rimpang jahe
Lampiran 8 Contoh foto uji aktivitas antioksidan ekstrak kasar rimpang jahe
cokelat tuaSampel + DPPH
Lampiran 9 Data uji aktivitas antioksidan ekstrak kasar rimpang jahe
Ponorogo
Sampel Ulangan Konsentrasi (µg/mL)
Log
konsentrasi Absorbans % inhibisi
IC50
(µg/mL)
Rerata IC50
(µg/mL)
1
1
1.5625 0.1938 0.459 9.47
11.09
11.23 3.125 0.4949 0.389 23.27
6.25 0.7959 0.318 37.28
12.5 1.0969 0.203 59.96
25 1.3979 0.144 71.60
50 1.699 0.103 79.68
100 2 0.077 84.81
2
1.5625 0.1938 0.463 8.68
11.55 3.125 0.4949 0.401 20.91
6.25 0.7959 0.323 36.29
12.5 1.0969 0.217 57.20
25 1.3979 0.136 73.18
50 1.699 0.100 80.28
100 2 0.079 84.42
3
1.5625 0.1938 0.453 10.65
11.05 3.125 0.4949 0.388 23.47
6.25 0.7959 0.314 38.07
12.5 1.0969 0.223 56.02
25 1.3979 0.137 72.98
50 1.699 0.097 80.87
100 2 0.077 84.81
1
1.5625 0.1938 0.445 12.23
10.80 3.125 0.4949 0.403 20.51
6.25 0.7959 0.318 37.28
12.5 1.0969 0.210 58.58
25 1.3979 0.128 74.75
50 1.699 0.099 80.47
100 2 0.07 86.19
2
1.5625 0.1938 0.439 13.41
11.02 3.125 0.4949 0.404 20.32
6.25 0.7959 0.306 39.64
2 12.5 1.0969 0.232 54.24 11.29
25 1.3979 0.132 73.96
50 1.699 0.107 78.90
Lampiran 9 Lanjutan
3
1.5625 0.1938 0.455 10.26
12.05 3.125 0.4949 0.442 12.82
6.25 0.7959 0.318 37.28
12.5 1.0969 0.226 55.42
25 1.3979 0.137 72.98
50 1.699 0.098 80.67
100 2 0.072 85.80
3
1
1.5625 0.1938 0.421 16.96
9.43
9.46 3.125 0.4949 0.372 26.63
6.25 0.7959 0.313 38.26
12.5 1.0969 0.197 61.40
25 1.3979 0.130 74.36
50 1.699 0.087 82.84
100 2 0.071 86.00
2
1.5625 0.1938 0.433 14.60
10.34 3.125 0.4949 0.384 24.26
6.25 0.7959 0.299 41.03
12.5 1.0969 0.218 57.00
25 1.3979 0.137 72.98
50 1.699 0.087 82.84
100 2 0.080 84.22
3
1.5625 0.1938 0.400 21.10
8.62 3.125 0.4949 0.381 24.85
6.25 0.7959 0.294 42.01
12.5 1.0969 0.185 63.51
25 1.3979 0.118 76.73
50 1.699 0.091 82.05
Lampiran 9 Lanjutan
Tangerang
Sampel Ulangan Konsentrasi (µg/mL)
Log
konsentrasi Absorbans % inhibisi
IC50
(µg/mL)
Rerata IC50
(µg/mL)
1
1
1.5625 0.1938 0.405 12.34
10.00
10.94 3.125 0.4949 0.353 23.59
6.25 0.7959 0.288 37.66
12.5 1.0969 0.206 55.41
25 1.3979 0.125 72.94
50 1.699 0.091 80.30
100 2 0.071 84.63
2
1.5625 0.1938 0.382 17.32
10.55 3.125 0.4949 0.360 22.08
6.25 0.7959 0.284 38.53
12.5 1.0969 0.206 55.41
25 1.3979 0.123 73.38
50 1.699 0.092 80.09
100 2 0.070 84.85
3
1.5625 0.1938 0.405 12.34
11.29 3.125 0.4949 0.364 21.21
6.25 0.7959 0.292 36.80
12.5 1.0969 0.202 56.28
25 1.3979 0.130 71.86
50 1.699 0.091 80.30
100 2 0.070 84.85
1
1.5625 0.1938 0.380 17.75
8.32 3.125 0.4949 0.294 36.36
6.25 0.7959 0.263 43.07
12.5 1.0969 0.183 60.39
25 1.3979 0.119 74.24
50 1.699 0.091 80.30
100 2 0.069 85.06
2
1.5625 0.1938 0.386 16.45
10.13 3.125 0.4949 0.367 20.56
6.25 0.7959 0.272 41.13
2 12.5 1.0969 0.180 61.04 9.34
25 1.3979 0.126 72.73
50 1.699 0.091 80.30
Lampiran 9 Lanjutan
3
1.5625 0.1938 0.386 16.45
9.58 3.125 0.4949 0.336 27.27
6.25 0.7959 0.265 42.64
12.5 1.0969 0.189 59.09
25 1.3979 0.129 72.08
50 1.699 0.091 80.30
100 2 0.070 84.85
3
1
1.5625 0.1938 0.405 12.34
10.99
10.87 3.125 0.4949 0.367 20.56
6.25 0.7959 0.282 38.96
12.5 1.0969 0.199 56.93
25 1.3979 0.127 72.51
50 1.699 0.087 81.17
100 2 0.070 84.85
2
1.5625 0.1938 0.395 14.50
10.10 3.125 0.4949 0.330 28.57
6.25 0.7959 0.281 39.18
12.5 1.0969 0.199 56.93
25 1.3979 0.132 71.43
50 1.699 0.085 81.60
100 2 0.071 84.63
3
1.5625 0.1938 0.403 12.77
11.52 3.125 0.4949 0.395 14.50
6.25 0.7959 0.289 37.45
12.5 1.0969 0.194 58.01
25 1.3979 0.126 72.73
50 1.699 0.086 81.39
Lampiran 9 Lanjutan
Bogor
Sampel Ulangan Konsentrasi (µg/mL)
Log
konsentrasi Absorbans % inhibisi
IC50
(µg/mL)
Rerata IC50
(µg/mL)
1
1
1.5625 0.1938 0.452 6.61
20.88
21.13
3.125 0.4949 0.442 8.68
6.25 0.7959 0.373 22.93
12.5 1.0969 0.311 35.74
25 1.3979 0.215 55.58
50 1.699 0.146 69.83
100 2 0.093 80.79
2
1.5625 0.1938 0.462 4.55
20.60 3.125 0.4949 0.418 13.64
6.25 0.7959 0.366 24.38
12.5 1.0969 0.313 35.33
25 1.3979 0.218 54.96
50 1.699 0.143 70.45
100 2 0.097 79.96
3
1.5625 0.1938 0.472 2.48
21.91
3.125 0.4949 0.445 8.06
6.25 0.7959 0.399 17.56
12.5 1.0969 0.326 32.64
25 1.3979 0.210 56.61
50 1.699 0.135 72.11
100 2 0.098 79.75
1
1.5625 0.1938 0.444 8.26
18.26 3.125 0.4949 0.398 17.77
6.25 0.7959 0.354 26.86
12.5 1.0969 0.290 40.08
25 1.3979 0.203 58.06
50 1.699 0.139 71.28
100 2 0.099 79.55
2
1.5625 0.1938 0.466 3.72
20.07 3.125 0.4949 0.421 13.02
6.25 0.7959 0.370 23.55
2 12.5 1.0969 0.299 38.22 19.48
25 1.3979 0.210 56.61
50 1.699 0.147 69.63
Lampiran 9 Lanjutan
3
1.5625 0.1938 0.458 5.37
20.10 3.125 0.4949 0.426 11.98
6.25 0.7959 0.377 22.11
12.5 1.0969 0.285 41.12
25 1.3979 0.211 56.40
50 1.699 0.150 69.01
100 2 0.096 80.17
3
1
1.5625 0.1938 0.446 7.85
18.21
17.76 3.125 0.4949 0.421 13.02
6.25 0.7959 0.368 23.97
12.5 1.0969 0.270 44.21
25 1.3979 0.189 60.95
50 1.699 0.150 69.01
100 2 0.092 80.99
2
1.5625 0.1938 0.444 8.26
17.63 3.125 0.4949 0.403 16.74
6.25 0.7959 0.354 26.86
12.5 1.0969 0.278 42.56
25 1.3979 0.200 58.68
50 1.699 0.142 70.66
100 2 0.089 81.61
3
1.5625 0.1938 0.453 6.40
17.45 3.125 0.4949 0.383 20.87
6.25 0.7959 0.351 27.48
12.5 1.0969 0.278 42.56
25 1.3979 0.196 59.50
50 1.699 0.149 69.21
Lampiran 9 Lanjutan
Contoh perhitungan
Penentuan IC50 sampel Ponorogo 1 ulangan 1
Kurva kalibrasi log konsentrasi ekstrak vs % inhibisi
y = 44.273x + 3.7326 R2 = 0.9674
IC50 diperoleh saat y = 50
Jadi,
50 = 44.273x + 3.7326 46.2674 = 44.273x x = 1.0450
antilog x = 11.09 µg/mL
y = 44.273x + 3.7326 R² = 0.9674
0.00 20.00 40.00 60.00 80.00 100.00
0 0.5 1 1.5 2 2.5
%
in
h
ib
is
i
Lampiran 10 Uji Duncan aktivitas antioksidan ekstrak kasar rimpang jahe
IC50 semua sampel dengan kelas perlakuan (jenis sampel)
Class Level Information Class Levels Values*
perlakuan 9 B1 B2 B3 P1 P2 P3 T1 T2 T3
Number of observations 27
Source DF Sum of Squares Mean Square F Value Pr > F Model 8 507.4782074 63.4347759 126.25 <.0001
Error 18 9.0439333 0.5024407
Corrected Total 26 516.5221407
R-Square Coeff Var Root MSE respon Mean 0.982491 5.250020 0.708831 13.50148
Alpha 0.05
Error Degrees of Freedom 18 Error Mean Square 0.502441
Number of Means 2 3 4 5 6 7 8 9
Critical Range 1.216 1.276 1.314 1.340 1.359 1.373 1.384 1.393
Means with the same letter are not significantly different.
Duncan Grouping Mean N Perlakuan*
A 21.1300 3 B1
B 19.4767 3 B2
C 17.7633 3 B3
D 11.2900 3 P2
D
D 11.2300 3 P1
D
D 10.9467 3 T1
D
D 10.8700 3 T3
E 9.4633 3 P3
E
E 9.3433 3 T2
Lampiran 10 Lanjutan
Rerata IC50 sampel dengan kelas lokasi (asal daerah)
Class Level Information Class Levels Values
lokasi 3 Bogor Ponorogo Tangerang
Number of observations 9
Source DF Sum of Squares Mean Square