Lampiran 1. Alat Penelitian
a. b. c.
d. e. f.
g. h. i.
Akuarium pH meter Timbangan
Micropipet DO meter Gelas ukur
j. k. l.
Lampiran 2. Bahan Penelitian
a. Pelembut b. c. Pakaian
Lampiran 3. Prosedur Penelitian
a. b.
b. d.
Aklimatisasi Pemberian aerasi
aerasi
Kematian ikan Pemberian
Lampiran 7. Tabel Analisis Sidik Ragam ANOVA Untuk Kelangsungan Hidup Benih Ikan Mas
Ulangan perlakuan (ppm) total
Lampiran 8. Tabel Analisis Sidik Ragam ANOVA Untuk Efisiensi Pakan Benih Ikan Mas
Ulangan perlakuan (ppm) total
Lampiran 9. Tabel Analisis Sidik Ragam ANOVA Untuk Laju Pertumbuhan Benih Ikan Mas
Ulangan perlakuan total
rata-rata
rata=yi 0.2733333 0.146666667 0.07667 0.05 0.27333 0.09111
DAFTAR PUSTAKA
Agusnar, H. 2008. Analisa Pencemaran dan Pengendalian Lingkungan, USU Press.
Connell, D. W. Dan Miller, G. J. 2006. Kimia dan Ekotoksikologi Pencemaran. UI Press, Jakarta.
Darmono. 2001. Lingkungan hidup dan Pencemaran Hubungannya dengan Senyawa Logam. UI press, Jakarta.
Effendi, H. 2003. Telaah Kualitas Air Bagi Pengelolaan Sumber Daya dan Lingkungan Perairan. Kanisius, Yogyakarta.
Ermin, K. W., Winarti, A., Agustin, S. 2006. Distribusi Surfaktan dan Fenol di Perairan Teluk Jakarta.
Halang, B. 2004. Toksisitas Air Limbah Deterjen Terhadap Ikan Mas (Cyprinus carpio). Unlam press. Vol 1, nomor 1, 39-49.
Kordi, M. G. 2010. Panduan Lengkap Memelihara Ikan Tawar di Kolam Terpal. ANDI, Yogyakarta.
Linda, R., Ramadhan, S., Gustina, I. 2012. Pengaruh Limbah Pabrik Karet Terhadap Jumlah Gerakan Operkulum dan Frekuensi Batuk Ikan Mas (Cyprinus carpio L). UNP.
Murtidjo, B. A. 2001. Pedoman Meramu Pakan Ikan. Kanasius, Yogyakarta.
Narantaka, A. 2012. Pembenihan Ikan Mas. Jaralitera, Yogyakarta.
Nida, S. 2004. Pengelolaan Limbah Deterjen Sebagai Upaya Minimalisasi Polutan di Badan Air dalam Rangka Pembangunan Berkelanjutan. Balai Teknologi Lingkungan- BBP, Serpong.
Nugroho, A. 2006. Bioindikator Kualitas Air. Penerbit Universitas Trisakti, Jakarta.
Pribadi, S.T. 2002. Pembesaran Ikan Mas di Kolam Air Deras. Agromedia Pustaka, Jakarta.
Rahardjo, M. F., Sjafei. D. S., Affandi. R dan Sulistiono. 2011. Ikhtiology. Lubuk Agung. Bandung.
Rosina, I. S. 2002. Interaksi Antara Deterjen, Tingkat Stres dan Uji Tantang Bakteri Aeromonas Hydropila pada Ikan Mas (Cyprinus carpio Linn). IPB.
Salmin. 2005. Oksigen Terlarut (DO ) dan Kebutuhan Oksigen Biologi (BOD) Sebagai Salah Satu Indikator untuk Menentukan Kualitas Perairan. Osena, vol. xxx. No.3, 2005 : 21:26.
Septi, P. 2004. Sublasi Surfaktan Kationik dari Larutan Pelembut Pakaian. Universitas Diponegoro, Semarang.
Siti, R dan Astri, D., E. 2009. Pertumbuhan dan Survival Rate Ikan Mas (Cyprinus carpio Linn) pada Berbagai konsentrasi Pestisida Regent 0,3 G. Universitas Diponegoro, Semarang. Jurnal Saintek Perikanan. Vol. 5, No.1, 2009, 49 : 54.
Soemirat, J. 2005. Toksikologi Lingkungan. Gadjah Mada, Yogyakarta.
Suin, N.M. 2002. Metoda Ekologi. Universitas Andalas, Padang.
Supriono, E., Lisnawati, L., Djokosetiyanto, D. 2005. Pengaruh Linear Alkylbenzene Sulfonate terhadap Mortalitas, Daya Tetas Telur dan Abnormalitas Larva Ikan Patin (Pangasius Hypophthalmus sauvage), IPB. Jurnal Akuakultur Indonesia, 4 (1) : 69-78 (2005).
Syahril, N., Thamrin., Huria, M. 2006. Toksisitas Deterjen Terhadap Benih Ikan Kakap Putih (Lates carcarifer, bloch). ISSN 0126-4265. Vol 33 No 2.
Syakti, A. D., Hidayati, N. V., Siregar, A. S. 2012. Agen Pencemaran Laut. IPB Press, Bogor.
Tahir, A. 2012. Ekotoksikologi dalam Perspektif Kesehatan Ekosistem Laut. Karya Putra Darwati, Bandung.
Trievita, A. F., Pamilia, C. 2012. Pengaruh Perbedaan Ukuran Partikel dari Ampas Tebu dan Konsentrasi Natrium Bisulfit (NaHSo3) Pada Proses Pembuatan Surfaktan. Jurnal Tehnik Kimia No.4, Vol. 18.
Ujang, D. 2000. Toksisitas Linear Alkylbenzene Sulfonate Terhadap Embrio Ikan Mas (Cyprinus carpio). IPB.
Yuli, P, sri, S, Winda, F., W. 2012. Uji Toksisitas Limbah Cair Laundry Sebelum dan Sesudah Diolah dengan Tawas dan Karbon Aktif Terhadap Bioindikator (Cyprinus carpio L). Yogyakarta. ISSN : 1979-911X.
BAHAN DAN METODE
Waktu dan Lokasi Penelitian
Penelitian ini dilaksanakan pada bulan Juli sampai November 2013 di
Dinas Pertanian dan Kelautan, Pusat Informasi dan Pengembangan Ikan Hias.
Jl. Karya Wisata, Kec. Medan-Johor. Medan.
Alat dan Bahan
Wadah pemeliharaan yang digunakan pada penelitian ini adalah akuarium
sebanyak 15 unit, dengan ukuran panjang 30 cm, lebar 30 cm, tinggi 30 cm. Bak
fiber ukuran panjang 237 cm, lebar 108 cm dan tinggi 50 cm untuk wadah
penampungan ikan atau aklimatisasi ikan, alat yang digunakan dalam penelitian
adalah aerator, ember, selang sebagai alat siphon pada akuarium, timbangan
analitik model KDE-600, gelas ukur, pipet tetes, gayung, alat tulis, serokan kecil.
Alat pengukuran yang akan digunakan pada penelitian ini termometer, pH meter
dan DO meter (Lampiran 1).
Bahan yang digunakan pada penelitian ini benih ikan mas yang
berukuran 4 - 6 cm sebanyak 600 ekor dimana masing-masing akuarium
berjumlah 10 ekor , pakan pelet, pelembut pakaian, air, kertas label dan tissu.
Metode Penelitian
Penelitian ini dilakukan 3 tahap yaitu uji pendahuluan, uji defenitif, dan uji
subletal. Masing-masing tahap dengan perlakuan dan pengulangan yang berbeda.
Persiapan Penelitian
Bak fiber dibersihkan terlebih dahulu dan dikeringkan selama sehari,
kemudian diisi air setinggi 18 cm, diberi aerasi terus dibiarkan 1 hari untuk
mengendapkan air serta diberi aerasi yang cukup agar dapat mempertahankan
kadar oksigen terlarut selama pengadaptasian, kemudian dimasukan ikan
berukuran 4 – 6 cm kedalam bak fiber dan dipelihara selama 1 minggu untuk
aklimatisasi ikan untuk mengkondisikan hewan uji pada kultur media air dan
memberikan waktu hewan uji beradaptasi dengan lingkungan yang baru, Selama
aklimatisasi ikan uji diberi pakan pelet sebanyak 2 kali sehari yaitu pada pukul
08.00 dan 16.00 WIB, seterusnya mempersiapkan akuarium sebagai media uji
yaitu dengan mencuci akuarium dan dikeringkan selama 1 hari, diisi air sebanyak
10 liter air dan diaerasi selama 1 hari untuk suplai oksigen kemudian ikan yang
sudah siap di aklimatisasi dimasukkan kedalam akuarium sebanyak 10
ekor/akuarium.
Uji Pendahuluan
Uji pendahuluan dilakukan dengan memasukkan bahan pelembut pakaian
untuk menentukan batas kisaran kritis (critical range test) yang menjadi dasar dari
penentuan konsentrasi untuk menentukan ambang batas atas (N) dan ambang
batas bawah (n) yang digunakan dalam uji lanjutan. Konsentrasi ambang batas
atas adalah konsentrasi terendah dari bahan uji yang dapat menyebabkan semua
ikan uji mati pada periode waktu pemaparan 24 jam. Sedangkan konsentrasi
ambang batas bawah adalah kosentrasi tertinggi dari bahan uji yang dapat
Dengan penentuan konsentrasi:
Gambar 4. Bagan peletakan media uji pendahuluan
Perlakuan diatas dengan 2 kali pengulangan, Parameter yang diamati
selama uji pendahuluan adalah mortalitas ikan yang dihitung pada jam ke- 0, 2, 4,
6, 8, 10, 12, 14, 16, 18, 20, 22 dan 24. Sedangkan perhitungan berikutnya
dilakukan setiap 6 jam sekali sampai jam ke- 48 pengukuran kualitas air dilakukan
setiap hari.
Uji Definitif
Konsentrasi perlakuan uji definitif diperoleh dari hasil uji penentuan selang konsentrasi nilai ambang atas dan bawah. Digunakan untuk mengetahui
toksisitas akut, menentukan nilai LC50–96 jam. Nilai LC50 yang dilihat adalah nilai
yang dapat mematikan ikan jam ke 96. Jumlah konsentrasi bahan uji sebanyak 4
buah ditambah 1 kontrol dengan 3 kali pengulangan.
Dengan penentuan konsentrasi menggunakan rumus menurut (Syakti, dkk.
Log N/n = k (log a- log n)
a/n = b/a = c/b = d/c = N/d
Keterangan:
N : Konsentrasi ambang atas
n : Konsentrasi ambang bawah
k : Jumlah konsentrasi yang diuji/banyaknya selang konsentrasi yang
diinginkan (a, b, c, d adalah konsentrasi yang diuji dengan nilai a sebagai
konsentrasi terkecil).
Selama Pengamatan tidak dilakukan pergantian air. Parameter yang diukur
adalah mortalitas ikan yang dihitung pada jam ke- 0, 6, 12, 18, 24 dan selanjutnya
dilakukan perhitungan setiap 12 jam sekali sampai jam ke- 96 Sedangkan
pengukuran Kualitas air dilakukan setiap hari (Suhu, pH, DO). Uji defenitif
terdiri atas 5 perlakuan dan masing-masing perlakuan 3 ulangan yaitu sebagai
berikut :
Perlakuan A : 0 ppm (Kontrol)
Perlakuan B : Konsentrasi 80,35 ppm
Perlakuan C : Konsentrasi 86,09 ppm
Perlakuan D : Konsentrasi 92,25 ppm
Type equation here.
P : Perlakuan P : Perlakuan U : Ulangan
Gambar 5. bagan peletakan media uji defenitif
Analisis Probit
Proses analisis data yang digunakan untuk menentukan nilai LC50 96 jam
pada penelitian ini adalah Analisis Probit. Analisis probit dihitung dengan
menggunakan rumus menurut Hubbert yang diacu oleh Zahri, (2008).
Dengan nilai a dan b diperoleh berdasarkan persamaan sebagai berikut:
Persamaan regresi: Y = a + bx
LC50 96 jam = anti log m, dimana:
Keterangan:
Y : Nilai Probit Mortalitas
X : Logaritma konsentrasi bahan uji
a : Konstanta
b : Slope/kemiringan
m : Nilai X pada Y 50 %
PCU1 PEU1 PDU1 PEU3 PAU3
PAU1 PBU2 PEU2 PBU1 PDU2
Analisa Data Uji Defenitif
Untuk dapat menentukan nilai konsentrasi LC50 dilakukan dengan analisa
probit. Analisa probit adalah suatu cara transformasi statistik dari data presentase
kematian ke dalam varian yang disebut probit dan kemudian digunakan untuk
menentukan fungsi regresi probit dengan log konsentrasi agar dapat mengestimasi
LC50.
Uji Toksisitas subletal
Uji toksisitas subletal dilakukan selama 28 hari, bertujuan untuk
mengetahui pengaruh pelembut pakaian dengan bahan aktif kuaterner amonium
terhadap pertumbuhan dan kelangsungan hidup benih ikan mas. Parameter
pengamatan dilakukan dengan ikan ditimbang sebelum dimasukan ke dalam
akuarium, sebagai data awal, selama pengamatan tetap diberi aerasi. Pemberian
pakan berupa pelet dilakukan 2 kali sehari, yaitu pagi dan sore. Pengamatan
dilakukan 2 kali sehari dengan mengamati tingkah laku ikan dan pengukuran
kualitas air dilakukan setiap hari dan perlakuan pada uji toksisitas subletal adalah
berdasarkan nilai subletal atau setengah nilai LC50-96 jam ke tingkatan
konsentrasi yang lebih rendah. Konsentrasi yang digunakan 0 % sebagai kontrol, 3
%, 6 % dan 9 % dari LC50-96. Pada uji ini menggunakan 3 perlakuan dan kontrol
dimana masing-masing perlakuan 3 ulangan yaitu sebagai berikut :
Perlakuan A : 0 ppm (Kontrol)
Perlakuan B : 2,61 ppm
Perlakuan C : 5,23 ppm
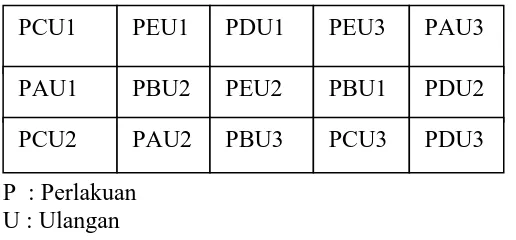
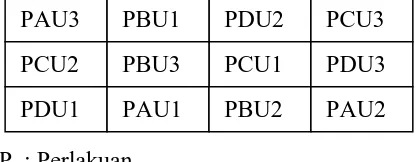
P : Perlakuan U : Ulangan
Gambar 6. Bagan peletakan media uji subletal
Pengumpulan Data Kelangsungan Hidup
Menurut Nugroho (2006) persentase kelangsungan hidup ikan dapat
dihitung dengan rumus sebagai berikut :
Keterangan :
SR : Kelangsungan hidup hewan Uji (%).
Nt : Jumlah ikan uji pada akhir penelitian (ekor).
No : Jumlah ikan uji pada awal penelitian (ekor).
Efisiensi Pakan
Menurut Murtidjo (2001) persentase efisiensi pakan dihitung
menggunakan sebagai berikut :
Keterangan :
Em = Efisiensi makanan ikan
B = Berat tubuh akhir ikan dalam gram
PAU3 PBU1 PDU2
PCU2
PCU3
PCU1 PDU3
PBU3
Bt = Berat mati ikan dalam gram
B0 = Berat tubuh awal dalam gram
Tm = Total makanan yang habis selama pengujian dalam gram
Laju Pertumbuhan
Data laju pertumbuhan ikan uji diperoleh dengan melakukan pengambilan
ikan uji awal dan akhir penelitian, kemudian ditimbang beratnya. Laju
pertumbuhan ikan per hari ini dapat dihitung dengan menggunakan rumus
Murtidjo (2001) :
Keterangan :
Lp = Laju pertumbuhan
W = Waktu yang dibutuhkan dalam pengujian
B = Berat tubuh akhir dalam gram
B0 = Berat tubuh awal dalam gram
Analisis Data Uji Subletal
Data pengaruh konsentrasi pelembut pakaian terhadap perlakuan
pertumbuhan, kelangsungan hidup, efisiensi pakan akan dianalisis menggunakan
sidik ragam (ANOVA) dengan rancangan acak lengkap (RAL). Apabila terdapat
pengaruh nyata maka akan dilanjutkan dengan uji lanjutan. Selanjutnya data
HASIL DAN PEMBAHASAN
Hasil
Uji Pendahuluan
Uji pendahuluan dilakukan untuk menentukan batas kisaran kritis
(critical range test) yang menjadi dasar dari penentuan konsentrasi yang
digunakan dalam uji lanjutan atau uji defenitif dengan 5 perlakuan 2 ulangan yaitu
0 ppm (kontrol), 50 ppm, 75 ppm, 100 ppm dan 125 ppm. Adapun hasil uji
pendahuluan awal disajikan dalam Tabel 1.
Tabel 1. Data Pengamatan Mortalitas Ikan Uji Pendahuluan.
Perlakuan 0 ppm (kontrol), 50 ppm dan 75 ppm tidak ada ikan uji yang
mati pada pemaparan 48 jam sedangkan pada perlakuan 100 ppm dan 125 ppm
semua ikan uji mati selama pemaparan 24 jam, dimana pada konsentrasi 100 ppm
dapat mematikan ikan uji sebanyak 100 % dalam waktu 540 menit (9 jam) dan
konsentrasi 125 ppm mematikan ikan uji 100% dalam waktu 360 menit (6 jam).
Uji Defenitif
Mortalitas ikan uji
Berdasarkan hasil penelitian uji defenitif menunjukkan pada perlakuan 0
ppm (kontrol) dan konsentrasi 80,35 ppm tidak ada ikan uji yang mati sedangkan
pada konsentrasi 86,09 ppm ikan uji mati 40 % dan konsentrasi 92,25 ppm ikan
uji mati 63,3 % kemudian pada konsentrasi 98,85 ppm ikan uji mati 100 %. Hasil
pengamatan mortalitas ikan uji disajikan pada Tabel 2.
Tabel 2. Data pengamatan mortalitas ikan uji defenitif
Konsentrasi 80,35 ppm benih ikan mas masih dapat mentoleransi bahan
toksik pelembut pakaian tersebut sedangkan konsentrasi diatas 86,09 ppm akan
mengalami mortalitas terhadap benih ikan mas dapat dilihat pada Tabel 2. Grafik
pengaruh konsentrasi pelembut pakaian terhadap mortalitas benih ikan dapat
Mortalitas ikan (%)
Gambar 7. Pengaruh Konsentrasi Pelembut Pakaian Terhadap Mortalitas Benih Ikan Mas
Mortalitas paling tinggi terjadi pada perlakuan konsentrasi 98,85 ppm
sedangkan mortalitas terendah pada perlakuan konsentrasi 86,09 ppm, 80,35 ppm
tidak mengalami mortalitas dan pada 0 ppm (Gambar 7).
Analisis Probit Mortalitas
Setelah didapatkan hasil uji defenitif maka dilanjutkan analisis probit
untuk mendapatkan nilai LC50 pada pemaparan 96 jam. Hasil analisis disajikan
pada Tabel 3 dibawah ini.
Hasil penelitian analisis probit LC50 benih ikan mas adalah 87,10 ppm,
dimana pada konsentrasi 87,10 ppm akan mematikan ikan uji 50 % pada waktu 96
jam.
Buka Tutup Operkulum Benih ikan mas
Hasil penelitian uji defenitif pada buka tutup operkulum perlu diamati
untuk melihat tingkah laku ikan uji secara langsung. Adapun hasil pengamatan
buka tutup operkulum dapat dilihat pada Tabel 4.
Tabel 4. Buka tutup operkulum uji defenitif benih ikan mas Konsentrasi
(ppm)
Waktu (menit) Jumlah buka tutup operkulum
0 (Kontrol) 1 45
80,35 1 78
86,09 1 86
92,25 1 106
98,85 1 115
Uji Subletal
Kelangsungan Hidup
Berdasarkan hasil penelitian yang dilakukan pada pemberian bahan toksik
pelembut pakaian berpengaruh nyata terhadap kelangsungan hidup benih ikan
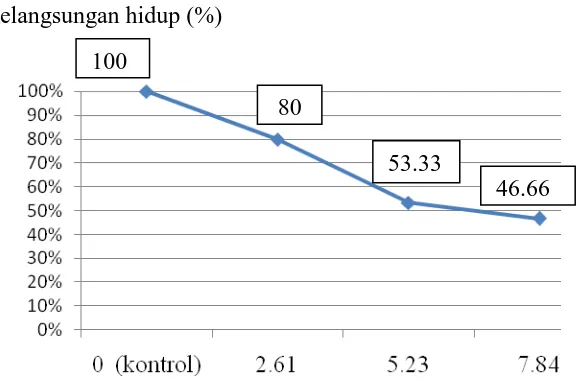
mas. Kelangsungan hidup tertinggi terjadi pada 0 ppm (kontrol) yaitu sebesar
100% dan kelangsungan hidup terendah terjadi pada perlakuan 7,84 ppm yaitu
Kelangsungan hidup (%)
Gambar 9. Efisiensi pakan benih ikan mas yang diberi bahan toksik pelembut pakaian selama 28 hari
Hasil penelitian ini didapatkan bahwa efisiensi pakan berpengaruh nyata
pada benih ikan mas dengan bahan toksik pelembut pakaian didalamnya, adapun
hasil efisiensi pakan tertinggi terdapat pada kontrol yaitu 8,64% sedangkan
efisiensi pakan terendah terdapat pada perlakuan konsentrasi 7,84 ppm yaitu
Laju Pertumbuhan
Hasil pada penelitian ini didapatkan bahwa bahan toksik pelembut pakaian
berpengaruh sangat nyata terhadap laju pertumbuhan terhadap benih ikan mas,
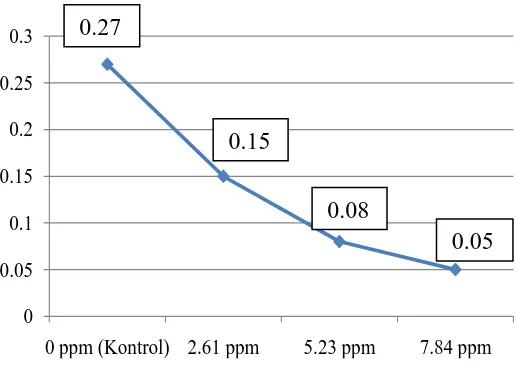
laju pertumbuhan tertinggi terdapat pada kontrol yaitu sebesar 0,27 % sedangkan
laju pertumbuhan terendah terjadi pada konsentrasi 7,84 ppm yaitu sebesar 0,05 %
(Gambar 10).
0 ppm (Kontrol) 2.61 ppm 5.23 ppm 7.84 ppm
Gambar 10. Laju pertumbuhan benih ikan mas yang diberi bahan toksik pelembut pakaian selama 28 hari
Kualitas Air Uji Defenitif
Pengukuran faktor lingkungan sangat penting untuk kehidupan benih ikan
mas, adapun hasil pengukuran faktor lingkungan selama uji defenitif terlihat
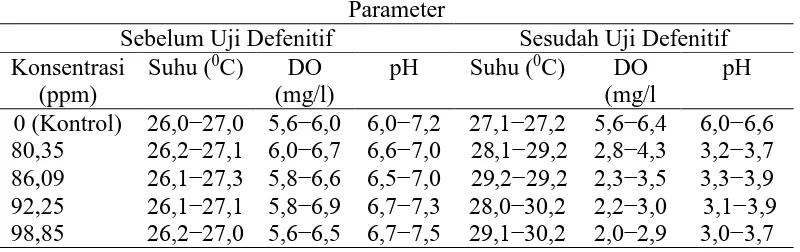
Tabel 5. Hasil Pengukuran kualitas air dengan bahan toksik pelembut pakaian
sebelum dan sesudah uji defenitif
Parameter suhu mengalami kenaikan yaitu sebelum uji defenitif berkisar
26,10C−27,30C sedangkan sesudah uji defenitif suhu berkisar 280C−30,20C,
kemudian pada DO mengalami penurunan drastis yaitu sebelum uji defenitif DO
berkisar 5,6–6,9 mg/l dan sesudah uji defenitif 2,0−6,4 mg/l selanjutnya pH juga
mengalami perubahan yang yaitu pH sebelum uji defenitif berkisar 6,0−7,5 dan
sesudah uji defenitif berkisar 3,0−6,6 sehingga bersifat asam (Tabel 5).
Uji Subletal
Nilai pengukuran kualitas air yang diamati selama penelitian uji subletal
masih layak untuk pemeliharaan benih ikan mas. kisaran Parameter kualitas air
selama penelitian dapat dilihat pada Tabel 6.
Tabel 6. Kualitas Air benih ikan mas yang diberi bahan toksik pelembut pakaian selama 28 hari
Konsentrasi (ppm) Parameter Kualitas Air
Suhu (0C) DO (mg/l) pH
Sebelum Uji Defenitif Sesudah Uji Defenitif
Konsentrasi
0 (Kontrol) 26,0−27,0 5,6−6,0 6,0−7,2 27,1−27,2 5,6−6,4 6,0−6,6
80,35 26,2−27,1 6,0−6,7 6,6−7,0 28,1−29,2 2,8−4,3 3,2−3,7
86,09 26,1−27,3 5,8−6,6 6,5−7,0 29,2−29,2 2,3−3,5 3,3−3,9
92,25 26,1−27,1 5,8−6,9 6,7−7,3 28,0−30,2 2,2−3,0 3,1−3,9
Pembahasan
Uji Pendahuluan
Saat ini tingkat pencemaran di perairan semakin meningkat dengan adanya
bahan pencemar yang berasal dari limbah rumah tangga seperti buangan sisa
pencucian sabun, deterjen, dan pelembut pakaian. Bahan ini bersifat toksik karena
mengandung senyawa kuaterner amonium klorida sesuai dengan pernyataan Nida
(2004) bahwa persenyawaan kimia yang berpotensi bersifat toksik adalah
golongan amonium kuaterner.
Penelitian ini dilakukan uji pendahuluan selama 48 jam, hal ini digunakan
untuk menentukan nilai ambang batas atas dan nilai ambang batas bawah sehingga
akan diperoleh nilai konsentrasi yang digunakan pada uji selanjutnya. Sesuai
dengan pernyataan Syakti, dkk (2012) yaitu Uji toksisitas akut diawali dengan
penentuan kisaran konsentrasi (range finding test) yang menyebabkan kematian
0−100% organisme uji pada uji pendahuluan.
Setiap organisme air memiliki batas toleransi yang berbeda-beda terhadap
suatu bahan pencemar salah satunya pada ikan mas mempunyai batas toleransi
terhadap perbedaan konsentrasi bahan pelembut pakaian. Hasil penelitian ini
menunjukkan bahwa konsentrasi 100 ppm merupakan nilai ambang batas atas
karena pada konsentrasi ini ikan uji mengalami kematian 100 % dalam waktu 24
jam. Sedangkan nilai ambang batas bawahnya berada pada konsentrasi 75 ppm,
karena pada konsentrasi ini semua hewan uji masih mampu bertahan hidup selama
48 jam. Hal ini disebabkan karena bahan pelembut pakaian yang mengandung
terhadap benih ikan mas dimana semakin banyak konsentrasi yang terdapat
didalam akuarium maka semakin tinggi mortalitasnya.
Uji Defenitif Mortalitas ikan uji
Pengaruh konsentrasi pelembut pakaian terhadap mortalitas benih ikan
mas menunjukkan bahwa semakin meningkatnya kecepatan reaksi senyawa kimia
pelembut pakaian yang terkandung didalam air maka semakin tinggi juga nilai
mortalitas atau kematian yang terjadi pada benih ikan mas, hal ini sesuai dengan
pernyataan Septi (2004) bahwa konsentrasi tinggi senyawa-senyawa kuaterner
amonium dapat membahayakan kehidupan lingkungan perairan.
Mortalitas tertinggi pada perlakuan dengan bahan pelembut pakaian
terhadap benih ikan mas terjadi pada konsentrasi 98,85 ppm yaitu sebesar 100%
pada jam ke 18, sedangkan mortalitas terendah terdapat pada konsentrasi 80,35
ppm pada jam ke 96. Kematian ikan disebabkan karena surfaktan yang
menyebabkan keracunan deterjen pada ikan sehingga akan cepat mengalami
kematian dan memberikan respon perubahan tingkah laku sebelum kematian
dengan memperlihatkan ciri-ciri hilangnya keseimbangan, berenang tidak teratur
dan pernafasan terganggu.
Analisis Probit Mortalitas
Berdasarkan data uji toksisitas dari Tabel 3 yang dianalisis dengan
menggunakan rumus analisis probit diperoleh nilai LC50 sebesar 87,10 ppm
menyebabkan kematian 50 % terhadap benih ikan mas selama waktu 96 jam, hal
ini disebabkan karena bahan aktif kuaterner amonium klorida yang terdapat dalam
pelembut pakaian. Kuaterner amonium klorida (NH4C1) yang termasuk kedalam
surfaktan kationik merupakan garam yang berasal dari basa lemah (NH3) dan
asam kuat (HCI) yang kationnya mengalami hidrolisis, sehingga larutan garamnya
bersifat asam, maka dengan konsentrasi yang banyak benih ikan mas mengalami
kematian.
Amonium klorida pada tingkat toksik juga dapat menyebabkan gangguan
osmoregulasi hal ini dimungkinkan adanya tanggapan fisiologi ikan yang sangat
peka pada kondisi awal terhadap bahan aktif kuaterner amonium klorida, Hal ini
sesuai dengan Siti dan Asri (2009) yang menyatakan ikan yang terkena racun
bahan pencemar dapat diketahui dengan gerakan hiperaktif, menggelepar, lumpuh
dan kemudian mati. Nilai LC50 96 jam berada pada 87,10 ppm. Nilai konsentrasi
pelembut pakaian yang aman bagi kehidupan benih ikan mas diperoleh dari 10%
nilai LC50 96 jam yakni 8,71 ppm.
Buka Tutup Operkulum Benih ikan mas
Pelembut pakaian sangat berpengaruh terhadap kecepatan frekuensi buka
tutup operkulum benih ikan mas, apabila konsentrasi semakin banyak dimasukkan
maka ikan uji akan mengalami pergerakan tutup buka operkulum yang semakin
cepat dan diperoleh hasil yang berbeda disebabkan kandungan oksigen terlarut
menurun, sehingga ikan uji kesulitan untuk mendapatkan oksigen.
Pengamatan secara visual gejala yang terlihat adalah perubahan pola
beraturan. Senyawa kuaterner amonium klorida dapat merusak fungsi respirasi
dari insang sehingga proses metabolisme dalam tubuh terganggu. Pemberian
perlakuan pada benih ikan mas juga menyebabkan gerakan renangnya tidak cepat
dan tidak peka terhadap rangsangan.
Hasil penelitian menunjukkan pada perlakuan konsentrasi 80,35 ppm
kecepatan buka tutup operkulumnya berkisar 78 kali permenit merupakan
konsentrasi terendah dan konsentrasi tertinggi yaitu 98,85 ppm buka tutup
operkulum berkisar 115 kali permenit, sesuai dengan pernyataan Linda, dkk
(2012) bahwa penurunan DO air menyebabkan ikan mempercepat gerakan
operkulumnya agar ikan dapat menyuplai oksigen yang dibutuhkan oleh tubuh.
Uji Subletal
Kelangsungan Hidup
Hasil penelitian uji subletal menunjukkan bahwa kelangsungan hidup pada
benih ikan mas semakin menurun seiring dengan bertambahnya konsentrasi bahan
toksik pelembut pakaian. Diperoleh kelangsungan hidup tertinggi sebesar 80 %
pada perlakuan konsentrasi 2,61 ppm, pada konsentrasi ini larutan pelembut
pakaian paling sedikit sehingga pengaruhnya belum terlalu besar terhadap
kelangsungan hidup ikan uji. Sedangkan kelangsungan hidup terendah yaitu pada
perlakuan konsentrasi 7,84 ppm sebesar 46,66% hal ini dikarenakan larutan
pelembut pakaian paling banyak terlihat pada media uji terdapat buih atau busa
sabun yang menutupi permukaan air dengan demikian kandungan oksigen terlarut
Rata-rata kelangsungan hidup dilakukan dengan analisis of varian
(ANOVA) yang menunjukan bahwa pemberian konsentrasi pelembut pakaian
berpengaruh nyata terhadap kelangsungan hidup benih ikan mas (Lampiran 7).
Pada konsentrasi ini benih ikan mas sudah mengalami stres yang ditunjukkan oleh
tingkah laku ikan yang lebih sering berada dipermukaan, tidak mampu beradaptasi
dengan kondisi DO yang semakin berkurang sehingga dapat menyebabkan
kematian. Hal ini didukung oleh pernyataan Siti dan Asri (2009) bahwa Seiring
dengan semakin tingginya konsentrasi yang dilarutkan pada media hidup ikan uji
maka tingkat kelangsungan hidup ikan uji akan semakin rendah.
Efisiensi Pakan
Persentase efisiensi pakan pada benih ikan mas berkurang seiring dengan
bertambahnya konsentrasi pelembut pakaian yang diberikan. Kisaran efisiensi
pakan yang tertinggi diperoleh pada konsentrasi 2,61 ppm sebesar 4,98%
sedangkan efisiensi pakan terendah terdapat pada konsentrasi 7,84 ppm sebesar
1,55% ini terjadi dikarenakan banyaknya pakan yang tidak dimakan oleh benih
ikan mas dan akhirnya mengendap pada dasar media.
Adapun kandungan gizi pakan buatan yang diberikan dapat dilihat Tabel 7
dibawah ini :
Tabel 7. Kandungan Gizi Pada Pakan Buatan untuk Benih Ikan mas dengan perlakuan pelembut pakaian selama 28 hari.
Berdasarkan analis of varian (ANOVA) persentase efisiensi pakan pada
benih ikan mas berkurang seiring dengan bertambahnya konsentrasi pelembut
pakaian yang diberikan, diperoleh bahwa perlakuan pemberian pelembut pakaian
berpengaruh nyata terhadap efisiensi pakan benih ikan mas (Lampiran 8). Bahan
aktif kuarterner amonium klorida mengubah kualitas air sehingga menghambat
proses metabolisme dalam tubuh yang menjadikan ikan stres dan nafsu makan
berkurang, hal ini sesuai dengan penelitian Rosina (2002) menurunnya nafsu
makan ikan, diduga menyebabkan pula turunnya sistem kekebalan tubuh ikan.
Laju Pertumbuhan
Pertumbuhan adalah pertambahan ukuran baik panjang maupun berat. Hal
ini terjadi apabila ada kelebihan input energi dan asam amino (protein) berasal
dari makanan. Laju pertumbuhan tertinggi yang diperoleh konsentrasi 2,61 ppm
sebesar 0,15% sedangkan konsentrasi terendah pada konsentrasi 7,84 ppm sebesar
0,05%, hal ini diduga karena jumlah pelembut pakaian yang terlalu banyak
diberikan sehingga mengakibatkan penurunan nafsu makan pada ikan uji.
Data rata-rata laju pertumbuhan dianalisis dengan analisis of varian
(ANOVA) yang menunjukkan pemberian perlakuan konsentrasi bahan pelembut
pakaian berpengaruh sangat nyata terhadap laju pertumbuhan benih ikan mas
(Lampiran 9), terjadi pertumbuhan yang terhambat ini menunjukkan gangguan
pada fungsi organ tubuh benih ikan uji, sehingga energi yang digunakan untuk
pertumbuhan digunakan untuk melakukan adaptasi terhadap lingkungan yang
mengandung bahan aktif kuaterner amonium klorida dalam pelembut pakaian. Hal
bisa jadi tidak signifikan dimana organisme perairan dapat melakukan seluruh
aktivitasnya secara normal, dan hanya dengan keberadaan stres lingkungan
(contoh : perubahan dalam pH, DO dan suhu) bahan kimia tersebut menimbulkan
dampak buruk yang terdeteksi dengan baik.
Kualitas Air
Uji defenitif
Perubahan kualitas air sangat mempengaruhi pertumbuhan dan
perkembangan organisme air. Menurut Effendi (2003) salah satu tujuan
pemantauan kualitas air untuk mengetahui sebab akibat antara perubahan
variabel-variabel ekologi perairan dengan parameter fisika dan kimia.
Parameter kualitas air yang diukur pada uji defenitif meliputi suhu, DO
dan pH. Kisaran suhu yang diperoleh sebelum uji defenitif adalah 260C−27,30C,
kisaran ini masih keadaan optimal bagi pertumbuhan ikan sesuai dengan
pernyataan Nugroho (2006) suhu optimal untuk ikan berkisar antara 200C−280C.
Sedangkan sesudah uji defenitif suhu berkisar 27,10 C−30,20 C dengan demikian
terlihat peningkatan suhu sehingga diduga menyebabkan mortalitas ikan uji.
Hasil pengamatan DO pada saat penelitian mengalami penurunan yang
drastis yaitu sebelum uji defenitif kisaran DO adalah 5,6−6,9 mg/l sedangkan
sesudah uji defenitif DO menurun hingga kisaran 2,0−6,4 mg/l. Menurut Nugroho DO dari 3−6 mg/l tidak cocok untuk kehidupan ikan sementara DO diatas 6 mg/l
cukup cocok untuk kehidupan ikan. Hal ini dapat dibuktikan dari hasil penelitian
Senyawa amonium kuaterner merupakan garam amonium (NH4+) yang
beberapa atau keseluruhan atom H dari ion NH4+nya memiliki agen aktif
permukaan yang mengandung kation rantai panjang. Kation dari garam-garam
klorida dalam air mudah larut, secara umum ion klorida membentuk senyawa
kompleks dengan ion-ion logam. Ion ini juga tidak dapat dioksidasi dalam
keadaan normal tetapi kelebihan garam-garam klorida dapat menyebabkan
penurunan kualitas air.
Penyebab penurunan DO karena adanya tegangan permukaan yang
mengakibatkan oksigen susah masuk kedalam media uji dan karena adanya busa
yang menutupi permukaan air, hal ini sesuai dengan pernyataan Septi (2004)
bahwa secara umum sifat-sifat fisik yang dimiliki surfaktan yaitu mempunyai
konsentrasi lebih besar pada permukaan dan menurunkan tegangan permukaan
yang bersifat koloid yang memiliki daya busa atau emulsi.
Nilai pH pada saat penelitian juga mengalami perubahan yaitu sebelum uji
defenitif pH berkisar 6 −7,5 sedangkan sesudah uji defenitif pH menurun hingga
3-6,6. Kisaran ini masih baik untuk pertumbuhan ikan didukung oleh pernyataan
Nugroho (2006) ikan tumbuh dengan baik pada pH 5−9. Dibawah 4 dan diatas 10
dapat menghambat pertumbuhan bahkan menyebabkan kematian.
Uji subletal
Konsentrasi uji subletal pada penelitian ini diambil dari konsentrasi uji
defenitif sebanyak 3 perlakuan yakni 3 %, 6 %, dan 9 % dari konsentrasi LC50.
Pada uji subletal terjadi perubahan dan perbedaan kualitas air yang diukur selama
270C−290C. Walaupun terjadi peningkatan suhu pada uji ini masih merupakan
kisaran suhu yang baik untuk pertumbuhan ikan karena menurut Nugroho (2006)
mengatakan bahwa suhu optimal untuk ikan berkisar antara 200C−280C.
Hasil pengukuran DO pada uji subletal mengalami penurunan
dibandingkan dengan DO pada uji defenitif meskipun penurunannya relatif kecil.
Kisaran pH yang diperoleh yaitu 5,2−7,6 mg/l, dimana pada penelitian ini
menunjukkan DO menurun seiring bertambahnya nilai konsentrasi bahan toksik
pelembut pakaian. Rahajo, dkk (2011) mengatakan bahwa oksigen terlarut
merupakan faktor penting pengendali laju pertumbuhan ikan. Kebutuhan minimal
ikan terhadap oksigen terlarut untuk dapat tumbuh dah berkembang umumnya 3
mg/l, dan akan lebih baik bila diatas 5 mg/l.
Hasil uji subletal diperoleh kisaran pH yakni berkisar 3,4−7,5 penurunan
ini diakibatkan karena bahan aktif kuaterner amonium klorida yang bersifat asam.
Menurut Nugroho (2006) ikan tumbuh dengan baik pada pH 5−9 sedangkan pH
dibawah 4 dan diatas 10 dapat menghambat bahkan menyebabkan kematian ikan
KESIMPULAN DAN SARAN
Kesimpulan
Dari hasil penelitian ini dapat disimpulkan bahwa :
1. Nilai ambang batas atas (N) pada penelitian ini sebesar 100 ppm sedangkan
nilai ambang batas bawah (n) sebesar 75 ppm, dan uji defenitif didapatkan
mortalitas terbanyak pada konsentrasi 98,85 ppm sebesar 100 %. Nilai LC50
96 jam yang diperoleh pada penelitian ini sebesar 87,10 ppm. Perlakuan 7,84
ppm memberikan kelangsungan hidup terendah yaitu 46.66%, efisiensi pakan
terendah yaitu sebesar 1.55% dan laju pertumbuhan terendah 0.05%.
2. Pemberian bahan toksik pelembut pakaian bepengaruh nyata terhadap
kelangsungan hidup dan efisiensi pakan, sedangkan laju pertumbuhan
berpengaruh sangat nyata terhadap benih ikan mas. Pengamatan secara visual
gejala yang terlihat adalah perubahan pola renang ikan yang lebih sering
berada dipermukaan, dan gerakan renang yang tidak beraturan.
Saran
Perlu dilakukan uji lanjutan secara histologi agar mengetahui organ-organ
TINJAUAN PUSTAKA
Klasifikasi Ikan Mas
Ikan mas sebagai ikan yang hidup di dalam air tawar memiliki sifat yang
sangat adaptif terhadap lingkungan hidup yang baru. Sifat yang adaptif dari ikan
mas tersebut membuat ikan mas dengan segala macam varietas (strain) nya dapat
hidup dalam perairan air tawar di segala penjuru dunia, Klasifikasi ikan mas
dimaksudkan untuk memasukkan ikan mas dalam kelompok hewan berdasarkan
bentuk tubuh dan sifat-sifatnya. Cara pengelompokkan hewan demikian dipelajari
dalam cabang ilmu biologi yang disebut ilmu taksonomi hewan. Ikan mas
menurut Narantaka (2012) dalam ilmu taksonomi hewan diklasifikasikan sebagai
berikut:
Phyllum : Chordata
Subpyllum : Vertebrata
Superclass : Pisces
Class : Osteichthyes
Subclass : Actinopterygii
Ordo : Ostariophysi
Sub Ordo : Cyprinoidea
Famili : Cyprinidea
Sub Famili : Cyprininae
Genus : Cyprinus
Morfologi Ikan Mas
Sirip punggung ikan mas memanjang dan bagian permukaannya terletak
berseberangan dengan permukaan sirip perut (vental). Sirip punggungnya (dorsal)
berjari-jari keras, sedangkan dibagian akhir bergerigi. Seperti halnya sirip
punggung, bagian belakang sirip dubur (anal) ikan mas ini pun berjari-jari keras
dan bergerigi pada ujungnya. Sirip ekornya menyerupai cagak memanjang
simetris hingga ke belakang tutup insang. Sisik ikan mas relatif besar dengan tipe
sisik lingkaran (cycloid) yang terletak beraturan. Garis rusuk atau gurat sisi (linea
lateralis) yang lengkap terletak di tengah tubuh dengan posisi melintang dari tutup
insang sampai ke ujung belakang pangkal ekor (Pribadi, 2002).
Morfologi ikan mas dapat dilihat pada Gambar 2 dibawah ini :
Gambar 2. (a) Benih ikan mas (b) Induk ikan mas
Habitat Ikan Mas
Habitat ikan mas adalah dalam air tawar. Namun ikan mas dapat hidup
juga di daerah muara sungai yang airnya payau. Berdasarkan sifat ikan mas ini,
masyarakat di beberapa daerah telah mencoba membudidayakan ikan mas di
dalam tambak yang airnya payau dengan kadar garam atau salinitas payau antara
20-30 permil. Suhu air yang ideal untuk tempat hidup ikan mas adalah terletak
pada kisaran antara 25- 300 C, ikan mas menyantap semua jenis bahan makanan,
baik yang berasal dari tumbuhan maupun binatang renik sehingga hewan ini
digolongkan kedalam hewan pemakan segala atau omnivore (Narantaka, 2012).
Surfaktan (Zat Aktif Permukaan)
Menurut Nida (2004) Surfaktan adalah molekul senyawa organik yang
terdiri atas dua bagian yang mempunyai sifat berbeda, yaitu bersifat hidrofobik
dan bagian yang bersifat hidrofilik.
Ditinjau dari struktur kimianya, surfaktan dibedakan menjadi dua, yaitu
rantai lurus yang dikenal dengan Linear alkil benzeneasulfonat (LAS) dan rantai
bercabang yang dikenal dengan alkilbenzenasulfonat (ABS) dapat dilihat pada
Gambar 3 di bawah ini :
a. Liniear alkil sulfonat (LAS)
b. Alkil benzen sulfonat (ABS)
Gambar 3. (a) Struktur kimia Linear alkil benzeneasulfonat (LAS), (b) bentuk struktur alkilbenzenasulfonat (ABS).
Surfaktan sintetik yang biasa digunakan dalam deterjen dibagi menjadi 3 macam
a. surfaktan anionik adalah garam-garam Na dan terionisasi untuk
menghasilkan Na+ dan ion aktif permukaan (surface active ion) yang
bermuatan negatif. Kelompok ini merupakan jumlah yang terbesar yang
beredar di pasaran karena banyak dipakai untuk tujuan domestik.
b. Surfaktan sintetis nonionik tidak terionisasi dalam air, kemampuan
deterjen ini untuk larut dalam air tergantung pada kelompok-kelompok
dalam molekul deterjen. Etoksilat, tidak berubah menjadi partikel yang
bermuatan, busa yang dihasilkan sedikit, tapi dapat bekerja di air sadah
dan dapat mencuci dengan baik untuk hampir semua jenis kotoran.
c. Surfaktan sintetis kationik adalah garam-garam amonium hidroksida
(NH4OH) kuaterner. Senyawa-senyawa amonium kuaterner, berubah
menjadi partikel bermuatan positif bila dilarutkan dalam air, surfaktan ini
biasanya digunakan untuk pelembut (Ermin dkk, 2006).
Nilai Ambang Batas
Daya racun tergantung pada kualitas dan kuantitas bahan tersebut. Dengan
jumlah sedikit sudah membahayakan manusia itu tidak lain karena kualitasnya
cukup memadai untuk membunuh. Untuk menghindari dampak yang diakibatkan
limbah melalui udara selain menghilangkan sumbernya juga dilakukan
pengendalian dengan penetapan nilai ambang batas. Nilai ambang batas adalah
kadar tertinggi suatu zat di dalam udara yang diperkenankan, sehingga manusia
dan makhluk hidup lainnya tidak mengalami gangguan penyakit atau menderita
Dosis Versus Konsentrasi
Dosis sangat menentukan efek biologis yang bakal timbul. Oleh karena itu
dikenal berbagai dosis yang berhubungan dengan efek tersebut, seperti : dosis
letal (LD), misalnya LD10 ( mematikan 10 % dari hewan percobaan), LD50, LD100,
min LD dosis terapeutik, dosis efektif, dosis toksik. Saat ini orang seringkali ingin
mengetahui LD50 (dosis letal) ataupun LC50 (konsentrasi letal) dari suatu zat, yaitu
dosis/konsentrasi yang mematikan 50% dari populasi percobaan (Soemirat, 2005).
Toksisitas Akut
LC50 96 jam berarti nilai yang menyebabkan 50% organisme mengalami
kematian dalam waktu 96 jam. Pada lingkungan perairan, uji toksisitas akut
dilaksanakan untuk mengestimasi konsentrasi medium letal (LC50 ) suatu bahan
kimia dalam air, yaitu perkiraan konsentrasi bahan kimia yang menghasilkan efek
50% populasi jumlah hewan uji yang yang diuji pada kondisi tetap
(Syakti dkk, 2012).
Uji Toksisitas Kronik
Kenyataan dari hasil uji toksisitas akut yang tidak menunjukkan dampak
buruk dan membahayakan pada organisme uji tidak menjamin bahwa bahan kimia
uji tersebut tidak bersifat toksik. Uji toksisitas kronik memungkinkan untuk
melakukan evaluasi tentang kemungkinan efek buruk dan membahayakan dari
bahan kimia, yang dilakukan dalam kondisi uji jangka panjang menggunakan
konsentrasi subletal. Dalam suatu uji toksisitas kronik, organisme uji dipapar
uji. Uji toksisitas siklus hidup parsial (kronik parsial) melibatkan hanya sebagian
siklus hidup, meliputi beberapa stadia hidup sensitif (Tahir, 2012).
Penentuan Nilai Toksisitas (LC50)
Untuk pengolahan data hasil pengujian toksisitas, atau untuk menentukan
nilai LC50 digunakan metode analisis probit. Toksisitas letal dinyatakan dalam
nilai median lethal consentration (LC50) yakni konsentrasi bahan uji yang dapat
mematikan 50% ikan uji pada waktu pemaparan tertentu(Nugroho, 2006)
Pengaruh Letal dan Subletal
Secara kualitatif, pengaruh letal dapat didefenisikan sebagai tanggapan
yang terjadi pada zat-zat fisika atau kimia mengganggu proses sel atau subsel
dalam makhluk hidup sampai suatu batas bahwa kematian mengikuti secara
langsung. Sebagai perbandingan, pengaruh subletal adalah pengaruh yang
merusak kegiatan fisiologis atau perilaku tetapi tidak menyebabkan kematian
langsung meskipun kematian dapat terjadi karena gangguan proses makan,
pertumbuhan atau perilaku yang tidak normal, lebih mudah ditangkap kurangnya
kemampuan mengkoloni, atau sebab-sebab lain yang tidak langsung. Hubungan
antara toksisitas subletal (belum mematikan) dan letal mematikan berlanjut
menjadi penting. Pengukuran kematian (letalitas seringkali digunakan untuk mencari tingkatan “aman” dari kontak dengan racun. Ini mencakup sebagai
contoh, penggunaan “faktor-faktor pemakaian” (misalnya, 1 % atau 0,01 selama
96 jam LC50 ) untuk menghitung tingkatan “aman” yang dapat juga berfungsi
Dampak Deterjen Terhadap Kehidupan Ikan di Perairan
Penelitian Halang (2004) pada limbah deterjen konsentrasi 36 mg/L dapat
mengakibatkan kematian ikan uji 50 % dalam waktu 96 jam. Berdasarkan
kenyatan ini didapatkan bahwa limbah deterjen (jenis anti noda) merupakan zat
toksikan yang mempunyai efek akut terhadap suatu biota yang hidup di perairan.
Penelitian Supriono, dkk (2005) pengaruh akut surfaktan linier
Alkylbenzene sulfonat (LAS) menyebabkan mortalitas, keabnormalan telur dan
larva serta penurunan daya tetas telur ikan patin (Pangasius hypophthalmus
sauvage). Nilai LC50-24 jam surfaktan LAS terhadap telur ikan patin adalah
sebesar 1,8 mg/l, namun sudah mulai berpengaruh terhadap mortalitasnya pada
konsentrasi 0,5 mg/l dan bersifat mematikan pada konsentrasi 9,0 mg/l.
Pada penelitian Priyanto (2006) laju pertumbuhan biakan Lemna sp pada
perlakuan LAS dan ABS terlihat sangat baik hingga konsentrasi surfaktan
masing-masing 13 ppm dan 10 ppm. Tetapi pada konsentrasi surfaktan 13 ppm atau lebih,
pertumbuhan tertekan dan lambat. Pada konsentrasi deterjen sebesar 25 ppm yang
setara dengan 7,25 LAS, laju pertumbuhan sangat lambat dengan waktu ganda
sebesar 3,16 hari.
Dalam penelitian Syahril, dkk (2006) pada konsentrasi 22,52 ppm belum
terjadi kematian hingga waktu 96 jam, sedangkan tingkat mortalitas ikan kakap
putih pada konsentrasi 63,39 ppm deterjen telah memberikan pengaruh kematian
terhadap benih ikan kakap putih, kenaikan tingkat kematian terjadi pada kurun
waktu 96 jam yaitu dari 6,67% menjadi 26,67%. Hal ini menunjukkan bahwa
kemampuan biota uji untuk mentolerir bahan toksikan juga dipengaruhi oleh
Menurut Effendi (2003) kadar surfaktan kationik 0,1 - 10 mg/liter dan
surfaktan non ionik 1 – 10.000 mg/liter dapat menghambat pertumbuhan algae.
Kualitas Air
Dalam budidaya ikan, beberapa parameter/indikator kualitas air perlu
diketahui karena sangat berpengaruh terhadap ikan budidaya. Sekalipun ikan yang
dibudidayakan adalah ikan-ikan yang tahan pada kualitas air yang ekstrim.
Suhu
Perubahan suhu air yang drastis dapat mematikan biota air karena terjadi
perubahan daya angkut darah. Suhu berkaitan dengan konsentrasi oksigen terlarut
dalam air dan konsumsi oksigen hewan air. Pertumbuhan dan kehidupan biota air
sangat dipengaruhi suhu air. Kisaran suhu optimal bagi kehidupan di perairan
tropis adalah antara 28−320 C. Pada kisaran tersebut konsumsi oksigen mencapai
2,2 mg/l berat tubuh-jam. Dibawah suhu 250 C, konsumsi oksigen mencapai 1,2
mg/l berat tubuh-jam. Pada suhu 18−250 C, ikan masih dapat bertahan hidup tetapi
nafsu makannya mulai nurun. Suhu air 12−180C mulai membahayakan ikan,
sedangkan suhu dibawah 120 C akan menyebabkan ikan tropis mati kedinginan
(Kordi, 2010).
Oksigen terlarut (DO)
Di perairan tawar, kadar oksigen terlarut berkisar antara 15 mg/liter pada
suhu 00 C dan 8 mg/liter pada suhu 250 C. kadar oksigen terlarut juga berfluktuasi
secara harian (diurnal) dan musiman, tergantung pada percampuran (mixing) dan
pergerakan (turbulence) massa air, aktivitas fotosintesis, respirasi, dan limbah
serta semakin kecil tekanan atmosfer, kadar oksigen terlarut semakin kecil
(Effendi, 2003).
Biota air membutuhkan oksigen guna pembakaran bahan bakarnya
(makanan) untuk menghasilkan aktivitas, seperti aktivitas berenang, pertumbuhan,
reproduksi. Oleh karena itu, ketersedian oksigen bagi biota air menentukan
lingkaran aktivitas dan konversi pakannya (Kordi, 2010).
Naik turunnya kadar oksigen terlarut dalam air itu disebut fluktuasi
oksigen (oxygen pulse). Besarnya fluktuasi oksigen dalam suatu badan air sangat
menentukan kehidupan hewan air. Hewan air yang kurang tahan pada air yang
kadar oksigennya rendah, titik kritis baginya adalah pada saat kadar oksigen di
malam hari (Suin, 2002).
Sebagaimana diketahui bahwa oksigen berperan sebagai pengoksidasi dan
pereduksi bahan kimia beracun menjadi senyawa lain yang lebih sederhana dan
tidak beracun. Disamping itu, oksigen juga sangat dibutuhkan oleh
mikroorganisme untuk pernapasan. Organisme tertentu, seperti mikroorganisme,
sangat berperan dalam menguraikan senyawa kimia beracun rnenjadi senyawa lain
yang lebih sederhana dan tidak beracun. Karena peranannya yang penting ini, air
buangan industri dan limbah sebelum dibuang ke lingkungan umum terlebih
dahulu diperkaya kadar oksigennya (Salmin, 2005).
Oksigen terlarut (DO) merupakan parameter mutu air yang penting karena
nilai oksigen terlarut dapat menunjukkan tingkat pencemaran atau tingkat
pengolahan air limbah. Kelarutan oksigen dalam air dapat dipengaruhi oleh suhu.
Derajat keasaman (pH)
pH air mempengaruhi tingkat kesuburan perairan karena memengaruhi
kehidupan jasad renik. Perairan asam akan kurang produktif, malah dapat
membunuh ikan budidaya. Pada pH rendah (keasaman yang tinggi), kandungan
oksigen terlarut akan berkurang. Akibatnya, konsumsi oksigen menurun, aktivitas
pernafasan naik, dan selera makan berkurang. Hal yang sebaliknya terjadi pada
suasana basa. Sebagian besar biota akuatik sensitif terhadap perubahan pH dan
menyukai pH sekitar 7- 8,5. Nilai pH sangat memengaruhi proses biokimiawi
PENDAHULUAN
Latar Belakang
Air salah satu sumber kehidupan bagi umat manusia. Apabila air telah
tercemar maka kehidupan manusia akan terganggu. Ini merupakan bencana besar.
Hampir semua makhluk hidup di muka bumi ini memerlukan air, dari
mikroorganisme sampai dengan mamalia. Tanpa air tiada kehidupan di muka
bumi. Jumlah air di muka bumi ini cukup banyak. Sekitar 71% dari luas
permukaan bumi ini terdiri atas air (Wardhana, 2004).
Pencemaran air dapat merupakan masalah regional, maupun lingkungan
global, dan sangat berhubungan dengan pencemaran udara serta penggunaan lahan
atau daratan. Pada saat udara yang tercemar jatuh ke bumi bersama air hujan,
maka air tersebut sudah tercemar. Beberapa jenis bahan kimia akan terbawa air ke
daerah sekitarnya sehingga mencemari air pada permukaan lokasi yang
bersangkutan (Darmono, 2001).
Surfaktan atau surface active agents atau wetting agents merupakan bahan
organik yang berperan sebagai bahan aktif pada deterjen, sabun, dan shampoo.
Surfaktan dapat menurunkan tegangan permukaan sehingga memungkinkan
partikel-partikel yang menempel pada bahan-bahan yang dicuci terlepas dan
mengapung atau terlarut dalam air. Surfaktan dikelompokkan menjadi empat,
yaitu surfaktan kationik, surfaktan anionik, surfaktan nonion dan surfaktan
amphoteric (zwitterionic). Keberadaan surfaktan dapat menimbulkan rasa pada air
Pelembut pakaian merupakan salah satu produk rumah tangga yang
berfungsi mencegah kain kehilangan bentuk dan dapat mengembalikan bentuk
kain. Larutan pelembut pakaian terdapat surfaktan kationik jenis senyawa
kuaterner amonium klorida yang membahayakan kehidupan lingkungan perairan.
Surfaktan kationik merupakan senyawa aktif permukaan dengan sedikit rantai
alkil hidrofobik dan gugus hidrofilik yang membawa muatan positif. Bahan
bakunya diambil dari minyak alam dengan campuran homolog dari surfaktan
(Septi, 2004).
Ikan mas hidup di air tawar yang mempunyai nilai ekonomis penting,
sehingga ikan ini banyak dibudidayakan. Lingkungan perairan yang tercemar
limbah deterjen kategori keras dalam konsentrasi tinggi akan mengancam dan
membahayakan kehidupan biota air dan manusia yang mengkonsumsi biota
tersebut (Halang, 2004).
Kerusakan organ ikan yang cukup nyata disebabkan oleh surfaktan yaitu
kerusakan epitel pernapasan ikan. Deterjen merusak indera perasa ikan, sehingga
menyulitkan ikan dalam mencari makan, surfaktan dalam bentuk phenol
merupakan senyawa bahan kimia yang bersifat toksik ketika terurai dan
membahayakan ikan. Semakin besar kadar surfaktan maka semakin besar pula
kerusakan epitel ikan (Ujang, 2000).
Untuk mengetahui efek zat pencemar terhadap biota dalam suatu perairan
perlu dilakukan suatu uji toksisitas zat pencemar terhadap biota dalam bentuk letal
concentration (LC50 ). Jadi uji toksisitas digunakan untuk mengevaluasi besarnya
konsentrasi toksikan dan durasi pemaparan yang dapat menimbulkan efek toksik
adalah ikan, dengan syarat harus mempunyai kepekaan tinggi, memenuhi syarat
umur, berat, dan panjang serta sesuai dengan ikan yang hidup di perairan
tercemar. Ikan mas adalah salah satu jenis ikan yang memenuhi persyaratan
tersebut karena ikan ini sangat peka, mudah dipelihara, penyebarannya merata,
mudah ditemukan, dan memenuhi syarat untuk uji toksisitas (Yuli dkk, 2012).
Limbah deterjen yang dibuang ke badan air akan menimbulkan masalah
pendangkalan perairan, terhambatnya difusi oksigen, sehingga proses penguraian
secara aerobik terganggu akibatnya terjadi kematian organisme akuatik serta
menurunnya estetika lingkungan yang disebabkan timbulnya bau dan busa.
Antisipasi dari semua pihak perlu dilakukan untuk meminimalisasi dampak
lingkungan, karena surfaktan dari golongan kuaterner amonium klorida dapat
membentuk senyawa nitrosamin dan gugus aromatik dari surfaktan bersifat
karsinogenik. Di bidang lingkungan, masalah yang timbul adalah terjadinya
eutrofikasi di perairan karena penggunaan deterjen (Nida, 2004).
Masalah yang ditimbulkan dari deterjen ini adalah terhambatnya proses
difusi oksigen dari udara yang akan menyebabkan biota dalam perairan
mengalami gangguan. Gangguan yang terjadi yaitu kekurangan oksigen yang bisa
menyebabkan terjadinya kerusakan jaringan insang. Kondisi yang seperti ini
apabila terjadi terus menerus akan menyebabkan ikan mengalami stres dan nafsu
makan menurun, akhirnya ikan mengalami kematian. Selain itu, bahan aktif
(surfaktan) yang banyak terdapat dalam deterjen akan mudah larut dan terserap
oleh makanan sehingga merubah bau dan rasa pelet yang akan menyebabkan
nafsu makan berkurang, dengan menurunnya nafsu makan ikan, diduga
Diketahui bahwa terdapat ragam diantara spesies dalam hal sensitivitas
terhadap bahan kimia, maka kisaran dan tingkatan efek yang berbeda sudah
selayaknya terjadi apabila dilakukan pemaparan suatu kisaran konsentrasi bahan
kimia yang sama terhadap spesies organisme yang berbeda. Oleh karena itu,
penting untuk melakukan uji toksisitas terhadap beberapa spesies organisme yang
berbeda untuk mendapatkan indikasi keragaman di alam (Tahir, 2012).
Perumusan Masalah
Pelembut pakaian dalam jumlah banyak dapat mematikan ikan atau biota
air lainnya, sehingga menghambat kelangsungan hidup dan pertumbuhan ikan
atau biota, sehingga diperlukan sebuah penelitian berapa konsentrasi yang bisa
terdegradasi dalam lingkungannya agar ikan bisa terus bertahan hidup, maka
dirumuskan beberapa permasalahan sebagai berikut :
1. Berapa nilai konsentrasi yang aman terhadap kelangsungan dan pertumbuhan
benih ikan mas ?
2. Bagaimana pengaruh toksisitas pelembut pakaian terhadap kelangsungan hidup,
efisiensi pakan dan laju pertumbuhan benih ikan mas ?
Tujuan Penelitian
1. Untuk menentukan tingkat daya serang pelembut pakaian terhadap benih ikan
mas.
2. Mengetahui pengaruh toksisitas pelembut pakaian dalam berbagai konsentrasi
Hipotesis
Pelembut pakaian bersifat toksik terhadap pertumbuhan dan hidup benih
ikan Mas.
Manfaat Penelitian
Sebagai bahan informasi bagi masyarakat, khususnya bagi pembudidaya
ikan mas tentang pengaruh pelembut pakaian terhadap pencemaran perairan. Serta
pihak-pihak yang terkait, berkompeten dan peduli di bidang lingkungan.
Kerangka Pemikiran Penelitian
Air merupakan kebutuhan pokok makhluk hidup untuk dapat menjalankan
segala aktivitasnya, apabila air tercemar akan mengganggu kehidupan makhluk
hidup, sehingga dibutuhkan benih ikan mas untuk mendeteksi keadaan
pencemaran atau menentukan potensi suatu zat racun di suatu perairan dan
pelembut pakaian salah satu bahan kimia yang sering digunakan masyarakat
sehingga bisa menimbulkan dampak letal dan subletal pada ikan, dimana efek
letal menyebabkan mortalitas dan perubahan tingkah laku ikan serta efek subletal
dilihat pada perubahan laju pertumbuhan, efisiensi pakan dan kelangsungan hidup
yang menyebabkan produksi ikan menurun. Secara singkat kerangka pemikiran
Gambar 1. Bagan alir kerangka pemikiran uji toksisitas pelembut pakaian terhadap benih ikan mas
Benih Ikan Mas Pelembut Pakaian
Air
Letal Subletal
Laju Pertumbuhan
Efisiensi Pakan
Kelangsungan hidup Tingkah laku
benih ikan mas Mortalitas
ABSTRAK
SHUSI NOVITA SIREGAR. Uji Toksisitas Pelembut Pakaian Terhadap Benih Ikan Mas (Cyprinus carpio L). Dibimbing oleh IRWANMAY dan RUSDI LEIDONALD.
Larutan pelembut pakaian mengandung bahan surfaktan jenis kationik dengan senyawa amonium kuaterner klorida yang membahayakan kehidupan lingkungan perairan dan menyebabkan kematian ikan. Penelitian ini bertujuan untuk mengetahui tingkat daya serang dan pengaruh toksisitas pelembut pakaian terhadap benih ikan mas, penelitian ini dilaksanakan pada bulan Juli sampai November 2013 di Dinas Pertanian dan Kelautan Kota Medan.
Tahapan pengujian meliputi : uji pendahuluan, uji definitif untuk menentukan LC50 96 jam dan uji subletal dengan berbagai konsentrasi. Hasil penelitian uji pendahuluan mempunyai nilai ambang batas atas (N) 100 ppm dan nilai ambang batas bawah (n) 75 ppm. Hasil Uji defenitif didapatkan nilai LC50 96 jam 87,10 ppm. Hasil uji subletal kelangsungan hidup tertinggi pada perlakuan konsentrasi 2.61 ppm yaitu sebesar 80% sedangkan kelangsungan hidup terendah pada perlakuan konsentrasi 7.84 ppm 46.66%, efisiensi pakan tertinggi pada perlakuan konsentrasi 2.61 ppm yaitu sebesar 4.98% sedangkan yang terendah pada perlakuan 7.84 sebesar 1.55%, dan terhadap laju pertumbuhan tertinggi pada perlakuan konsentrasi 2.61 ppm yaitu sebesar 0.15% sedangkan terendah pada perlakuan konsentrasi 7.84 ppm sebesar 0.05%. Parameter kualitas air yang diamati selama uji defenitif terjadi penurunan DO 2.0−6.4 mg/l, suhu semakin meningkat 27.1−30.20C dan pH semakin menurun pada tiap perlakuan konsentrasi 3−6.6. Parameter kualitas air pada uji subletal terjadi penurunan DO yang tidak drastis berkisar 5.2−7.6 mg/l, suhu berkisar 27−290C dan kisaran pH 3.4−7.5.
ABSTRACK
SHUSI NOVITA SIREGAR. Fabric Softener Toxicity Test Against Goldfish Seed (Cyprinus carpio L) This research was supervised by IRWANMAY and RUSDI LEIDONALD.
Solution of fabric softener contained cationic surfactant by type quaternary ammonium chloride compounds that harm aquatic life and the environment led to the death of fish . This reaserch intend to determine the level of attack power and influence of fabric softener toxicity to carp seed , this research had been on July - November 2013 in the Department of Agriculture and Marine Medan .
Stages of testing include : a preliminary test , a definitive test to determine the LC50 until 96 hours and sublethal tests with various concentrations . The results showed of the preliminary test studies have upper threshold value ( N ) of 100 ppm and below the threshold value ( n ) 75 ppm . Test results obtained definitive 96 -hour LC50 value of 87.10 ppm . The test results on the highest survival sublethal concentration of 2.61 ppm treatment that is equal to 80 % while the lowest survival at 7.84 ppm concentration and 46.66 % , the highest feed efficiency at treatment concentrations of 2.61 ppm is equal to 4.98 % and the lowest in the treatment of 1:55 7.84 % , and the highest growth rate in the treatment concentration of 2.61 ppm is 0.15 % while the lowest at treatment concentrations of 7.84 ppm at 0.05% . Water quality parameters were observed during the definitive test decreased DO 2.0-6.4 mg / l , the temperature increased 27.1 - 30.20C and pH decrease during each treatment concentration of 3-6.6 . Water quality parameters at sublethal test that does not decrease drastically DO range 5.2-7.6 mg / l , temperature range 27 - 290C and a pH range of 3.4-7.5 .
UJI TOKSISITAS PELEMBUT PAKAIAN TERHADAP BENIH
IKAN MAS (Cyprinus carpio L)
SHUSI NOVITA SIREGAR
090302001
PROGRAM STUDI MANAJEMEN SUMBERDAYA PERAIRAN
FAKULTAS PERTANIAN
UJI TOKSISITAS PELEMBUT PAKAIAN TERHADAP BENIH
IKAN MAS (Cyprinus carpio L)
SKRIPSI
SHUSI NOVITA SIREGAR
090302001
PROGRAM STUDI MANAJEMEN SUMBERDAYA PERAIRAN
FAKULTAS PERTANIAN
UJI TOKSISITAS PELEMBUT PAKAIAN TERHADAP BENIH
IKAN MAS (Cyprinus carpio L)
SKRIPSI
SHUSI NOVITA SIREGAR
090302001Skripsi sebagai satu diantara beberapa syarat untuk dapat memperoleh gelar Sarjana Perikanan Pada Program Studi Manajemen Sumberdaya Perairan
Fakultas Pertanian Universitas Sumatera Utara
PROGRAM STUDI MANAJEMEN SUMBERDAYA PERAIRAN
FAKULTAS PERTANIAN
LEMBAR PENGESAHAN
Judul Penelitian : Uji Toksisitas Pelembut Pakaian Terhadap Benih Ikan
Mas (Cyprinus carpio L)
Nama : Shusi Novita Siregar
Nim : 090302001
Program Studi : Manajemen Sumberdaya Perairan
Disetujui Oleh Komisi Pembimbing
Ir. Irwanmay, M. Si Rusdi Leidonald, SP., M. Sc
Ketua Anggota
Mengetahui
Dr. Ir. Yunasfi, M. Si
PERNYATAAN MENGENAI SKRIPSI
DAN SUMBER INFORMASI
Yang bertanda tangan di bawah ini :
Nama : Shusi Novita Siregar
NIM : 090302001
Menyatakan bahwa skripsi yang berjudul “Uji Toksisitas Pelembut Pakaian
Terhadap Benih Ikan Mas (Cyprinus carpio L)” benar merupakan hasil karya sendiri dan belum diajukan dalam bentuk apapun kepada perguruan tinggi
manapun. Semua sumber dan data informasi yang berasal atau dikutip dari karya
yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam
teks dan dicantumkan dalam daftar pustaka di akhir skripsi ini.
Medan, Mei 2014
Shusi Novita Siregar
ABSTRAK
SHUSI NOVITA SIREGAR. Uji Toksisitas Pelembut Pakaian Terhadap Benih Ikan Mas (Cyprinus carpio L). Dibimbing oleh IRWANMAY dan RUSDI LEIDONALD.
Larutan pelembut pakaian mengandung bahan surfaktan jenis kationik dengan senyawa amonium kuaterner klorida yang membahayakan kehidupan lingkungan perairan dan menyebabkan kematian ikan. Penelitian ini bertujuan untuk mengetahui tingkat daya serang dan pengaruh toksisitas pelembut pakaian terhadap benih ikan mas, penelitian ini dilaksanakan pada bulan Juli sampai November 2013 di Dinas Pertanian dan Kelautan Kota Medan.
Tahapan pengujian meliputi : uji pendahuluan, uji definitif untuk menentukan LC50 96 jam dan uji subletal dengan berbagai konsentrasi. Hasil penelitian uji pendahuluan mempunyai nilai ambang batas atas (N) 100 ppm dan nilai ambang batas bawah (n) 75 ppm. Hasil Uji defenitif didapatkan nilai LC50 96 jam 87,10 ppm. Hasil uji subletal kelangsungan hidup tertinggi pada perlakuan konsentrasi 2.61 ppm yaitu sebesar 80% sedangkan kelangsungan hidup terendah pada perlakuan konsentrasi 7.84 ppm 46.66%, efisiensi pakan tertinggi pada perlakuan konsentrasi 2.61 ppm yaitu sebesar 4.98% sedangkan yang terendah pada perlakuan 7.84 sebesar 1.55%, dan terhadap laju pertumbuhan tertinggi pada perlakuan konsentrasi 2.61 ppm yaitu sebesar 0.15% sedangkan terendah pada perlakuan konsentrasi 7.84 ppm sebesar 0.05%. Parameter kualitas air yang diamati selama uji defenitif terjadi penurunan DO 2.0−6.4 mg/l, suhu semakin
meningkat 27.1−30.20C dan pH semakin menurun pada tiap perlakuan konsentrasi
3−6.6. Parameter kualitas air pada uji subletal terjadi penurunan DO yang tidak drastis berkisar 5.2−7.6 mg/l, suhu berkisar 27−290C dan kisaran pH 3.4−7.5.
ABSTRACK
SHUSI NOVITA SIREGAR. Fabric Softener Toxicity Test Against Goldfish Seed (Cyprinus carpio L) This research was supervised by IRWANMAY and RUSDI LEIDONALD.
Solution of fabric softener contained cationic surfactant by type quaternary ammonium chloride compounds that harm aquatic life and the environment led to the death of fish . This reaserch intend to determine the level of attack power and influence of fabric softener toxicity to carp seed , this research had been on July - November 2013 in the Department of Agriculture and Marine Medan .
Stages of testing include : a preliminary test , a definitive test to determine the LC50 until 96 hours and sublethal tests with various concentrations . The results showed of the preliminary test studies have upper threshold value ( N ) of 100 ppm and below the threshold value ( n ) 75 ppm . Test results obtained definitive 96 -hour LC50 value of 87.10 ppm . The test results on the highest survival sublethal concentration of 2.61 ppm treatment that is equal to 80 % while the lowest survival at 7.84 ppm concentration and 46.66 % , the highest feed efficiency at treatment concentrations of 2.61 ppm is equal to 4.98 % and the lowest in the treatment of 1:55 7.84 % , and the highest growth rate in the treatment concentration of 2.61 ppm is 0.15 % while the lowest at treatment concentrations of 7.84 ppm at 0.05% . Water quality parameters were observed during the definitive test decreased DO 2.0-6.4 mg / l , the temperature increased 27.1 - 30.20C and pH decrease during each treatment concentration of 3-6.6 . Water quality parameters at sublethal test that does not decrease drastically DO range 5.2-7.6 mg / l , temperature range 27 - 290C and a pH range of 3.4-7.5 .