ABSTRACT
INFLUENCE OF TREATMENT EARLY TO CHEMICAL
CHARACTERISTIC AND ORGANOLEPTIK
MUSHROOM OYSTER FLOUR (
PLEUROTUS OSTREATUS
)
By
Ardiansyah
Oyster mushroom (Pleurotus ostreatus) is one of the healthy vegetables and consumed by many people. Oyster mushroom was perishable foodstuffs, like other vegetables. Storage in a cool temperatur, oyster mushroom only last for 3-5 days. To extend the shelf life of the oyster mushroom can be made into flour. This study aims to find treatment that produced oyster mushroom flour with the best chemical and organoleptic properties.
properties colour. Obtained data were analysed with Honestly Significant Difference test (HSD) at the 5% level.
The results showed that pretreatment significantly affect the moisture content, protein content, ash content, carbohydrate content and colour oyster mushroom flour. The best oyster mushroom flour wast control (with no pre-treatment) with chemical characteristics: water content 7.29%, ash content 8.01%, protein content 17.50%, and carbohydrate content of 73.68%., and organoleptic characteristics (colour) was white score (4.34).
ABSTRAK
PENGARUH PERLAKUAN AWAL TERHADAP
KARAKTERISTIK KIMIA DAN ORGANOLEPTIK
TEPUNG JAMUR TIRAM (
PLEUROTUS OSTREATUS
)
Oleh
Ardiansyah
Jamur tiram (Pleurotus ostreatus) merupakan salah satu jenis sayuran sehat yang memiliki manfaat bagi tubuh. Jamur tiram termasuk bahan pangan yang mudah rusak. Penyimpanan jamur tiram pada suhu 15-200C hanya dapat bertahan selama 3-5 hari. Untuk memperpanjang masa simpan, jamur tiram dapat diolah menjadi tepung jamur tiram. Penelitian ini bertujuan untuk mendapatkan perlakuan awal yang menghasilkan tepung jamur tiram dengan sifat kimia dan organoleptik terbaik.
sifat fungsional dilakukan pada tepung jamur tiram terbaik. Data dianalisis dengan sidik ragam dan uji lanjut dengan Beda Nyata Jujur (BNJ) pada taraf 5%.
Hasil penelitian menunjukkan bahwa perlakuan awal berpengaruh nyata terhadap kadar air, protein, abu, karbohidrat dan warna tepung jamur tiram.Tepung jamur tiram tanpa perlakuan awal/kontrol memiliki kadar air sebesar 7,29 %, kadar abu sebesar 8,01%, kadar protein sebesar 17,50%, kadar karbohidrat sebesar 73,68%, dan warna putih dengan skor 4,34.
I. PENDAHULUAN
1.1 Latar Belakang dan Masalah
Jamur tiram (Pleurotus ostreatus) merupakan salah satu jenis sayuran sehat yang dewasa ini sudah banyak dikenal dan dikonsumsi oleh berbagai kalangan
masyarakat. Jamur tiram memiliki manfaat dalam tubuh karena jamur tiram putih mempunyai kadar serat yang tinggi sehingga baik untuk membantu proses
pencernaan dalam usus, menurunkan kadar gula darah penderita diabetes dan membantu menurunkan berat badan (Cahyana dan Mucrodji, 1999).
Jamur tiram termasuk bahan pangan yang mudah rusak, seperti jenis sayuran lainnya. Beberapa hari setelah panen, mutu jamur tiram turun dengan cepat sampai tidak layak dikonsumsi. Perubahan mutu jamur tiram antara lain layu, warna menjadi coklat, lunak dan cita rasanya berubah. Di Indonesia pengawetan jamur pangan komersial belum banyak dilakukan. Di pasar swalayan, jamur biasanya disimpan pada suhu dingin yaitu 15-200C. Pada suhu tersebut, jamur hanya dapat bertahan (masih layak dikonsumsi) selama 3-5 hari, meskipun telah dikemas dengan plastik polietilen (Koesnandar, 2005 dalam Hayyuningsih, 2009).
Untuk mengatasi masalah tersebut, diperlukan pengolahan lebih lanjut sehingga umur simpan jamur tiram dapat diperpanjang. Salah satu cara untuk
upaya untuk memperpanjang masa simpan, memperbaiki mutu bahan pangan, memberikan kemudahan dalam penanganan, dan memperluas aplikasi jamur tiram dalam penganekaragaman produk.
Salah satu masalah dalam proses pembuatan tepung jamur tiram adalah warna tepung yang cenderung coklat. Pencoklatan tepung jamur tiram diduga terjadi akibat reaksi pencoklatan enzimatis dan non-enzimatis. Reaksi pencoklatan enzimatis maupun non-enzimatis dapat dihambat melalui beberapa perlakuan pendahuluan seperti, blanching, perendaman natrium bisulfit, perendaman asam sitrat, blanching + perendaman natrium bisulfit dan blanching + perendaman asam sitrat. Oleh karena itu dalam penelitian ini dilakukan beberapa perlakuan awal terhadap jamur tiram untuk memperoleh tepung jamur tiram dengan sifat kimia dan organoleptik (warna) terbaik.
1.2 Tujuan Penelitian
Penelitian ini bertujuan untuk mendapatkan perlakuan awal yang menghasilkan tepung jamur tiram dengan sifat kimia dan organoleptik terbaik, serta mengetahui sifat fungsionalnya.
1.3 Kerangka Pemikiran
Jamur tiram (Pleurotus sp) merupakan jamur konsumsi dari jenis jamur kayu yang memiliki nilai gizi tinggi dan salah satu dari jamur konsumsi yang bernilai
dibandingkan dengan jenis jamur lainnya. Berdasarkan berat kering, kandungan nutrisi 100 g jamur tiram adalah kalori (367 kkal), protein (10,5-30,4%),
karbohidrat (56,6%), lemak (1,7-2,2%), tiamin (0,20 mg), riboflavin (4,7-4,9 mg), niasin (77,2 mg), dan kalsium (314,0 mg), (Koesnandar, 2005 dalam
Hayyuningsih, 2009).
Proses pengolahan tepung jamur tiram mengakibatkan terjadinya reaksi pencoklatan, baik pencoklatan enzimatis maupun non-enzimatis. Reaksi
pencoklatan enzimatis biasa terjadi pada buah – buahan dan sayur – sayuran yang memilki senyawa fenolik. Senyawa ini berfungsi sebagai substrat bagi enzim polifenoloksidase (PPO/1,2-benzenidiol/oksigen oxidoreduktase;EC 1.10.3.1). Proses pencoklatan enzimatis memerlukan enzim polifenoloksidase dan oksigen untuk berhubungan dengan substrat. Enzim – enzim yang dikenal yaitu fenol oksidase, polifenoloksidase, fenolase/polifenolase, enzim – enzim ini berkerja secara spesifik untuk substrat tertentu. Untuk memicu terjadinya reaksi pencoklatan, harus ada reaksi antara enzim polifenoloksidase, substrat fenolik, serta oksigen. Reaksi pencoklatan akan mengubah struktur kuinol menjadi subtrat kuinon (Winarno, 1997).
Pada penelitian ini dilakukan penelitian bertujuan untuk mengetahui waktu terjadinya reaksi pencoklatan enzimatis pada jamur tiram, dengan menggunakan uji sensori metode uji duo trio (Mailgaard et al. 1999). Pada dasarnya
perubahan fenol menjadi o-quinon yang dalam tahap oksidasi selanjutnya menghasilkan produk berwarna coklat (Senterre et al. 1991).
Reaksi pencoklatan non-enzimatis (Reaksi Maillard) meliputi reaksi yang terjadi antara gula pereduksi (melalui sisi keton dan aldehid yang reaktif) dengan asam amino (melalui gugus amina). Reaksi ini banyak terjadi selama penyimpanan bahan pangan pada pemanasan di atas suhu 450C (Mardinah, 1996).
Untuk mencegah terjadinya reaksi pencoklatan secara umum dapat dilakukan dengan beberapa perlakuan awal yaitu dengan perlakuan blanching, perendaman asam sitrat, dan perendaman larutan sulfit. Blanching merupakan proses panas yang pengoperasiannya menggunakan air panas atau uap air. Pemanasan ini umumnya berlangsung pada suhu 850C selama 3-5 menit. Pada industri
pengolahan pangan, proses blanching selalu digunakan sebagai proses pemanasan pendahuluan. Tujuan utama blanching adalah untuk inaktifasi enzim dalam bahan pangan sehingga akan mengurangi resiko terjadinya pencoklatan pada tepung jamur tiram. Blanching juga berguna untuk mengurangi jumlah mikroorganisme, mengeluarkan udara, perbaikan warna, kerenyahan, pelayuan dan perlakuan pendahuluan sebelum pengolahan lanjutan (Winarno, 1997).
Menurut Susanto (1994), sulfit biasanya ditambahkan dalam makanan pada konsentrasi 500-1000 ppm, tergantung tujuan penambahan dan jenis makanan. Desrosier (1988) menyatakan bahwa batas maksimum penambahan sulfit dalam makanan adalah pada konsentrasi 3000 ppm. Batas residu sulfit yang
diperbolehkan dalam bahan pangan kering adalah 500 ppm.
Mekanisme sulfit dalam mencegah reaksi pencoklatan enzimatis adalah
menghambat aktivitas enzim fenolase dengan cara mengikat logam yang menjadi kofaktor enzim seperti Cu. Penggunaan sulfit dalam mencegah reaksi pencoklatan mempunyai keuntungan dan kerugian. Keuntungan penggunaan sulfit adalah dapat menginaktivasi enzim fenolase dan melindungi vitamin C dari kerusakan, namun penggunaan sulfit harus dibatasi karena penggunaan sulfit yang berlebihan dapat menimbulkan rasa dan bau sulfur pada bahan pangan, selain itu konsentrasi tinggi akan bersifat racun (Eskin, et al.,1971). Hasil penelitian Triono (2006) menunjukkan bahwa penggunaan konsentrasi natrium bisulfit 2500 ppm selama 10 menit dengan cara perendaman ternyata menghasilkan tepung pati kentang terbaik, yaitu berwarna putih, residu sulfit 91,974 ppm, kadar abu 1,904%, kadar air 8,713% dan pH 6,67.
reaktivitasnya sehingga tidak mampu menginisiasi oksidasi sehingga reaksi pencoklatan tidak terjadi (Belitz dan Grosch, 1999).
Tepung merupakan salah satu bentuk alternatif produk setengah jadi yang
dianjurkan, karena lebih tahan simpan, mudah dicampur, dibentuk, dan lebih cepat dimasak sesuai tuntutan kehidupan modern yang serba praktis (Winarno, 2000). Pembuatan tepung jamur tiram ditujukan untuk memperpanjang masa simpan dan diversifikasi produk olahan pangan dengan mengunakan tepung jamur tiram. Tepung jamur tiram dapat digunakan dalam berbagai macam produk olahan seperti mie basah, nugget dan sosis ayam.
Untuk memudahkan aplikasi serta mendapatkan sifat spesifikasi produk olahan seperti yang diharapkan, diperlukan informasi mengenai sifat fungsional dari tepung jamur tiram tersebut. Sifat fungsional didefinisikan sebagai sifat – sifat bahan pangan atau komponen bahan pangan, kecuali nilai gizinya, yang dapat mempengaruhi pemanfaatannya (Yunus, 2003). Murdefi (1992) meyatakan bahwa faktor – faktor pengolahan yang mempengaruhi sifat fungsional protein adalah sumber dan varietas protein, ekstraksi, suhu, pengeringan, kekuatan
1.4 Hipotesis
II. TINJAUAN PUSTAKA
2.1 Jamur Tiram
Jamur tiram putih (Pleurotus ostreatus) merupakan salah satu jamur konsumsi, berwarna putih dengan tudung bulat berdiameter 3-15 cm. Kandungan protein jamur tiram putih rata – rata 3,5 – 4% dari berat basah, protein ini dua kali lipat lebih tinggi dibandingkan asparagus dan kubis. Bila dihitung dari berat kering, kandungan protein jamur tiram putih adalah 19 – 35%, sementara beras 7,3%, gandum 13,2%, kedelai 39,1%, dan susu sapi 25,2%. Jamur tiram putih juga mengandung 9 asam amino esinsial yang tidak bias disentesis dalam tubuh yaitu lisin, metionin, triptofan, threonin, valin, leusin, isoleusin, histidin dan fenilalanin (Cahyana dan Muchrodji, 1999).
Gambar 1. Jamur tiram putih (Anonima, 2011).
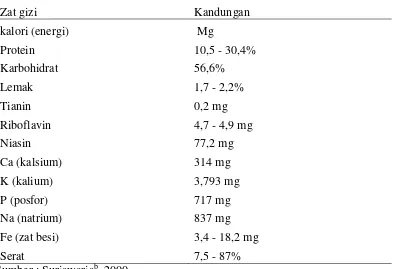
sejumlah vitamin yang penting terutama kelompok vitamin B, sperti vitamin B1 (tiamin), B2 (riboflavin) dan vitamin C, jamur tiram putih merupakan sumber mineral yang baik, kandungan mineral utama adalah kalium (K), kemudian natrium (Na), fosfor (P), kalsium (Ca), dan (Fe). Jamur tiram juga dipercaya berhasiat menurunkan kadar kolestrol, mencega diabetes, mencegah anemia, dan berperan sebagai anti kanker. Komposisi gizi jamur tiram putih dapat dilihat pada Tabel 1.
Tabel 1. Komposisi dan kandungan nutrisi jamur tiram per 100 g
Zat gizi Kandungan
kalori (energi) Mg
Protein 10,5 - 30,4%
Karbohidrat 56,6%
Lemak 1,7 - 2,2%
Tianin 0,2 mg
Riboflavin 4,7 - 4,9 mg
Niasin 77,2 mg
Ca (kalsium) 314 mg K (kalium) 3,793 mg
P (posfor) 717 mg
Na (natrium) 837 mg Fe (zat besi) 3,4 - 18,2 mg
Serat 7,5 - 87%
Sumber : Suriawariab, 2000.
semacam polisakarida kitin di dalam jamur tiram diduga menimbulkan rasa enak. Jamur tiram juga mengandung vitamin penting, terutama, B, C dan D. Vitamin B1 (tiamin), vitamin B2 (riboflavin), niasin dan provitamin D2 (ergosterol) dalam jamur tiram cukup tinggi. Mineral utama tertinggi adalah kalium, fosfor, natrium, kalsium, dan magnesium. Mineral utama tertinggi adalah : Zn, Fe, Mn, Mo, Co, Pb. Konsentrasi K, P, Na, Ca, dan Me mencapai 56 – 70% dari total abu dengan kadar K mencapai 45%. Mineral mikroelemen yang bersifat logam dalam jamur tiram kandungannya rendah, sehingga jamur ini aman dikonsumsi setiap hari (Winarno, 2000).
2.2 Pencoklatan Enzimatis dan Non-Enzimatis
2.2.1 Pencoklatan Enzimatis
Reaksi pencoklatan dapat dialami oleh buah – buahan dan sayur – sayuran yang tidak berwarna. Reaksi ini disebut reaksi pencoklatan karena menyebabkan warna makanan berubah menjadi coklat. Ada beberapa hal yang menyebabkan
terjadinya reaksi pencoklatan, salah satunya adalah keberadaan enzim. Reaksi pencoklatan ini dapat diklasifikasikan menjadi dua yaitu reaksi pencoklatan enzimatis dan reaksi pencoklatan non- enzimatis.
Reaksi pencoklatan enzimatis adalah proses kimia yang terjadi pada sayuran dan buah – buahan oleh enzim polifenol oksidase yang menghasilkan pigmen warna coklat (melanin). Proses pencoklatan enzimatis memerlukan enzim polifenol oksidase dan oksigen untuk berhubungan dengan substrat tersebut. Enzim – enzim yang dikenal yaitu fenol oksidase, polifenol oksidase,
fenolase/polifenolase, enzim – enzim ini berkerja secara spesifik untuk substrat tertentu (Winarno, 1997).
karakteristik warna coklat keemasan pada buah – buahan yang dikeringkan seperti kismis, buah prem, dan buah ara.
Reaksi pencoklatan enzimatis ini juga memiliki kerugian yaitu hilangnya nilai gizi pada produk pangan dan dapat merusak flavor dari bahan pangan itu sendiri. Dalam industri pangan perlu dilakukan langkah – langkah untuk meminimalisasi adanya penurunan mutu produk yaitu dengan mengendalikan reaksi pencoklatan enzimatis. Ada beberapa cara yang dapat dilakukan yakni blanching,
pendinginan, pembekuan, mengubah pH, dehidrasi, iradiasi, HHP (High Pressure Processing), penambahan inhibitor, ultrafiltrasi, dan juga ultrasonikasi.
Pencoklatan enzimatis melibatkan enzim polifenol oksidase ini membentuk melanin sehingga menyebabkan warna coklat. Reaksi yang menyebabkan warna coklat ini merupakan suatu reaksi kimia yang dikenal sebagai oksidatif enzimatik dengan oksigen sebagai katalisator dalam reaksi tersebut. Jadi reaksi pencoklatan enzimatik ini membutuhkan tiga agen yaitu oksigen (dibantu katalis Cu+ ),enzim (polifenolase/PPO) serta komponen fenolik. Secara normal, sel memisahkan enzim dari komponen fenolik, tapi ketika buah atau sayuran dipotong atau memar, enzim dan fenol bereaksi dengan kehadiran oksigen membentuk produk yang kecoklatan.
cathecol menjadi o-benzoquinone. Hasilnya yaitu o-benzoquinone beraksi dengan group amino dari residu lisin protein (Winarno, 1997).
2.2.2 Pencoklatan Non-Enzimatis
Pada setiap proses pengolahan bahan pangan dengan mneggunakan media
pemanas, akan terjadi reaksi pencoklatan pada bahan pangan. Reaksi pencoklatan non-enzimatis disebabkan oleh adanya reaksi Maillard, karamerisasi dan
pencoklatan akibat vitamin C (Winarno, 1997).
Reaksi Maillard merupakan reaksi yang terjadi antara karbohidrat khususnya gula pereduksi dengan gugus amina primer. Hasil reaksi tersebut menghasilkan bahan berwarna coklat (Winarno, 1997). Menurut de Man (1997), reaksi pencoklatan dapat didefinisikan sebagai urutan peristiwa yang dimulai dengan gugus amino, peptida, atau protein dengan hidroksil glikosidik pada gula, diakhiri dengan pembentukan polimer nitrogen berwarna coklat atau melanoidin.
Reaksi non-enzimatis (Maillard) adalah reaksi yang terjadi karena adanya reaksi antara gula pereduksi dengan gugus amin beba dari asam amino dan protein. Reaksi ini banyak terjadi pada produk pangan. Reaksi pencoklatan non-enzimatis adalah reaksi pencoklatan yang bukan diakibatkan oleh aktivitas enzim. Reaksi ini meliputi reaksi Maillard, reaksi karemelisasi, dan reaksi oksidasi asam
Mekanisme reaksi Maillard sangat komplek, di mana gula amin akan mengalami denaturasi, siklitasi, fragmentasi, dan polimerisasi sehingga terbentuk komplek pigmen yang disebut melanoidin. Hasil reaksi Maillard mungkin dikehendaki misalnya, pada pembentukan kulit luar coklat pada roti, dan mungkin juga tidak dikehendaki, seperti pelenturan susu yang diuapkan dan disterilkan. Selain itu reaksi Maillard juga dapat memicu daya cerna pada protein (Prangdimurti, et al., 2007).
Mekanisme reaksi maillard terdiri dari 3 tahapan yaitu, reaksi tahapan awal (initial stage), reaksi intermediate, dan reaksi tahap ahir (final stage). Reaksi tahap awal meliputi reaksi pembentukan glikosilamin dan Amadori
rearrangement. Tahap reaksi intermediate yaitu reaksi dehidrasi, fission, dan degradasi stecker. Reaksi tahap ahir terdiri dari kondensasi aldol dan polimerisasi aldehid amin yaitu pembentukan komponen nitrogen heterosiklik (Batles, 1999).
2.3 Pencegahan Pencoklatan Enzimatis dan Non-Enzimatis
Reaksi pencoklatan enzimatis pada bahan pangan memilki dua macam dampak yaitu dampak menguntungkan dan merugikan. Reaksi enzimatis dapat dicegah dengan beberapa perlakuan yaitu :
2.3.1 Sulfit
pembakaran belerang akan mengandung gas belerang dioksidasi (SO2), yang
kemudian akan larut dalam air membentuk asam sulfit. Kemudian penggunannya berkembang, dan sulfit digunakan untuk mengawetkan sayuran dan buah – buahan kering, daging serta ikan. Senyawa – senyawa sulfit biasa digunakan berbentuk bubuk kering, seperti natrium atau kalium sulfit, natrium atau kalium bisulfit dan kalium metabisulfit. Ada dua tujuan yang diinginkan dari penggunaan sulfit yaitu: (1) untuk mengawetkan (sebagai senyawa anti mikroba), dan (2) untuk mencegah perubahan warna bahan makanan menjadi kecoklatan.
Umunya, senyawa sulfit hanya efektif untuk mengawetkan bahan makanan bersifat asam, dan tidak efektif untuk bahan makanan yang bersifat netral atau alkalis. Sulfit dapat menghambat pertumbuhan mikroba yang dapat merusak atau membusukkan bahan makanan dengan tiga macam mekenisme yang berbeda, tetapi pada dasarnya adalah menginaktifkan enzim – enzim yang terkandung dalam mikroba.
Sulfit dapat mencegah timbulnya reaksi pencoklatan enzimatis dan non-enzimatis. Kemampuan sulfit dalam mencegah reaksi pencoklatan dan sekaligus
mengawetkan belum dapat disaingi oleh bahan kimia lain. Itulah sebabnya mengapa sulfit luas sekali pemakainnya. Misalnya untuk sayuran dan buah – buahan kering, asinan, manisan, sari buah, konsentrat, pure, sirup, anggur minuman dan bahkan untuk produk daging serta ikan yang dikeringkan.
ahirnya akan bereaksi dengan komponen sulfit membentuk hidroksi sulfonat yang stabil. Dengan demikian tidak akan terjadi reaksi antara komponen gula dengan komponen asam amino yang menyebabkan pembentukan melanoidin (Evily, 1992). Menurut Fennema (1996), ion sulfit akan bereaksi dengan group karboksil dari gula pereduksi membentuk α- hidroksi sulfonat. Senyawa ini tidak bereaksi dengan gugus amino dari protein, sehingga reaksi Maillard tidak terjadi.
Sedangkan Braverman (1963) menyatakan bahwa natrium bisulfit (NaHSO3)
dapat mencegah terjadinya reaksi Maillard karena NaHSO3 akan bereaksi dengan
gugus karbonil bebas sehingga gugus karbonil tersebut tidak dapat bereaksi dengan asam amino.
2.3.2 Keamanan Sulfit
Gas belerang dioksidasi dan sulfit dalam tubuh akan dioksidasi menjadi senyawa sulfat yang tidak berbahaya, yang kemudian akan dikeluarkan melalui urine. Mekanisme detoksifikasi ini cukup mampu untuk menangani jumlah sulfit yang termakan. Itulah sebabnya dalam daftar bahan aditif makanan, sulfit digolongkan sebagai senyawa GRAS (generally recognaized as safe) yang berarti aman untuk dikonsumsi.
menimbulkan asma pada orang – orang tertentu. Senyawa aktif yang dapat menyebabkan asma tersebut adalah gas belerang dioksidasi yang terhirup pada waktu mengkonsumsi makanan yang diawetkan dengan sulfit.
Hasil penelitian di Australia menunjukan bahwa sekitar 30-40% anak – anak mempunyai gejala asma, sedangkan pada orang tua angkanya lebih kecil yaitu sekitar 1- 5%. Dari jumlah ini, sekitar 25% sensitif terhadap sulfit. Kemampuan sulfit untuk mencegah reaksi pencoklatan dan sekaligus mengawetkan bahan makanan belum dapat digantikan oleh senyawa kimia lainya. Tetapi mengingat efek negatif yang dapat ditimbulkan bagi kesehatan tubuh, adalah kebijaksanaan untuk mengurang atau jumlah penggunaannya. Di negara barat (terutama Eropa) hal ini telah lama dilakukan. Pencegahan reaksi pencoklatan dapat dilakukan dengan menggunakan senyawa eritrobat atau vitamin C yang lebih aman, yang digabungkan dengan penggunaan bahan pengawet lainnya, misalnya asam atau garam sorbat (Desrosier, 1988).
2.3.3 Blanching
Menurut Winarno (1980), blanching adalah pemanasan pendahuluan dalam pengolahan pangan. Blanching merupakan tahapan pra proses pengolahan bahan pangan yang biasa dilakukan dalam proses pengalengan, pengeringan sayuran dan buah – buahan.
kekurangan yang berbeda. Tetapi pada umunya yang lebih sering digunakan adalah blanching dengan uap panas (steam blanching) karena dengan cara ini lebih sedikit kehilangan air untuk bahan yang mudah larut dalam air (Desrosier, 1988).
Proses thermal dalam pengolahan merupakan suatu cara untuk menghilangkan aktivitas biologi yang tidak diinginkan. Keuntungan yang diperoleh dari proses ini adalah mampu memperpanjang umur simpan bahan pangan dalam wadah tertutup, mempertahankan nutrisi dan mempertahankan mutu bahan.
Blanching dapat dilakukan dengan tiga cara , yaitu blanching dengan air panas (hot water blanching), blanching dengan uap air (steam blanching) dan blanching dengan microwave. Ketiga cara ini masing – masing memiliki kelebihan dan kekurangan yang berbeda. Tetapi pada umunya yang lebih sering digunakan adalah blanching dengan uap panas (steam blanching) karena dengan cara ini lebih sedikit kehilangan air untuk bahan yang mudah larut dalam air (Desrosier, 1988).
1. Blanching menggunakan air panas (hot water blanching). Pada cara ini bahan kontak langsung dengan air panas sehingga bahan akan banyak kehilangan
komponen – komponen yang bersifat larut dalam air. Suhu yang digunakan sekitar 75 – 1000C.
3. Blanching dengan microwave. Cara ini dilakukan dengan meletakkan bahan dan didiamkan dalam microwave, dengan keadaan bahan yang dikemas dalam wadah tipis (film bag). Kelebihan dari cara ini adalah dapat menurunkan kandungan mikroba dan sedikit kehilangan nutrisi, tetapi cara ini sangat mahal harganya.
Menurut Praptiningsih (1999) blanching bertujuan untuk inaktivasi enzim, pembersihan bahan – bahan mentah dan mengurangi kadar bakterinya, membuat jaringan berkerut, membuat pengisian bahan mentah menjadi mudah,
mempertahankan dan memperbaiki warna serta memperbaiki tekstur.
Blanching dapat menyebabkan kerugian pada bahan, yaitu kehilangan gizi yang larut dalam air dan peka terhadap panas, menghambat proses pengeringan bahan – bahan yang mengandung pati dan menyebabkan kerusakan tekstur bila waktu blanching terlalu lama.
Proses blanching paling optimum dilakukan dengan proses High Temperature short time dimana blanching dilakukan dalam waktu yang cepat dengan metode Stem Blanching, karena pada proses ini pelarutan zat nutrisi yang disebabkan karena bahan yang tidak tahan terhadap panas dan mudah terlarut dalam air dapat dikurangi.
enzim- enzim yang tahan panas yang terdapat dalam sayuran dan buah – buahan (Buckle, 1987).
Tujuan dilakukannya blanching adalah :
1. Menginaktivasi ataupun merusak enzim untuk menghindari terjadinya perubahan yang tidak diinginkan
2. Mempertahankan maupun memperbaiki warna dan kenampakan 3. Mengurangi kandungan mikroba
4. Memperlunak jaringan sehingga mempermudah proses berikutnya
5. Mengeluarkan gas – gas seluler dari jaringan sehingga mengurangi terjadinya korosi
6. Memperbaiki tekstur, terutama untuk bahan yang dikeringkan
2.3.4 Peranan Asam Sitrat Pada Reaksi Pencoklatan
Asam sitrat merupakan asam organik lemah yang ditemukan pada daun dan buah tumbuhan genus citrus (jeruk – jerukan). Senyawa ini merupakan bahan pengawet yang baik dan alami, selain digunakan sebagai penambah rasa asam pada
makanan dan minuman ringan. Asam sitrat terdapat pada berbagai jenis sayuran dan buah, namun ditemukan pada konsentrasi tinggi, yang dapat mencapai 8% bobot kering , pada jeruk lemon dan limau (misalnya jeruk nipis dan jeruk purut). Rumus kimia asam sitrat adalah C6H8O7. Struktur asam ini tercermin pada nama
mengkelat logam yang berbahaya yang dapat mepercepat perubahan warna dan flvour, memperbaiki tekstur pada bahan, meningkatkan intensitas pada flavour secara nyata, membentu ekstraksi pektin dan pigmen pada buah dan sayur. Selain itu asam sitrat juga berfungsi mengatur pH karena kelarutan asam sitrat didalam air tinggi (Furia, 1975).
Asam sitrat berperan dalam menurunkan pH jaringan, sehingga menurunkan kecepatan pencoklatan enzimatis. Terjadinya browning akibat fenolase dapat dihambat dengan menurunkan pH larutan sampai 3,0 sebab pH optimum fenolase 6-7. Pengendalian pH sangat diperlukan dalam praktek teknologi pangan. Dalam industri pangan di mana penggunaan enzim mempunyai peranan penting,
pengaturan pH harus ditujukan untuk mendapatkan keefektifan enzim maksimal. Sebaliknya, dalam proses pengolahan pangan, keaktifan enzim tertentu tidak dikehendaki sehingga harus dicegah dan dihambat. Asam sitrat mempunyai efek ganda terhadap pencegahan fenolase, yaitu disamping menurunkan pH medium juga terjadi ikatan dengan Cu2+(efek chelating unsure Cu) dalam enzim (Winarno, 1980).
2.4 Sifat Fungsional Tepung Jamur Tiram
Sifat fungsional merupakan sifat – sifat bahan pangan atau komponen bahan pangan, kecuali nilai gizinya yang dapat mempengaruhi pemanfaatannya (Yunus, 2003). Sifat fungsional yang penting pada tepung adalah kelarutan, viskositas, kapasitas rehidrasi, dan daya emulsi (Kensella, 1976).
2.4.1 Kelarutan
Kelarutan protein dipengaruhi oleh jumlah gugus polar dan non-polar serta susunan molekul tersebut. Kelarutan dalam air kurang baik jika mengandung asam amino dengan gugus hidrofobik lebih banyak dibanding dengan gugus hidrofilik. Umumnya, protein larut di dalam air, gliserol atau asam format. Kelarutan di dalam air juga dipengaruhi oleh pH dan konsentrasi garam. Protein yang terdenaturasi berkurang larutannya. Lapisan molekul protein bagian dalam yang bersifat hidrofobik berbalik keluar, demikian sebaliknya bagian luar yang bersifat hidrofilik berbalik ke dalam. Akibatnya protein menggumpal dan mengendap, sehingga kelarutannya menurun (Winarno, 1997).
menyebabkan keragaman sifat tepung yang dihasilkan. Pada produk yang berbentuk tepung konsentrat (instant), semakin tinggi kadar air produk semakin sulit produk dilatutkan dalam air, karena produk cendrung membentuk butiran
yang lebih besar tetapi tidak “porous” (Masters, 1979 dalam Agung, 1987).
2.4.2 Viskositas
Viskositas berhubungan dengan resistensi granula pati yang mengembang akibat penetrasi air ke dalam granula. Semakin mudah granula mengembang maka semakin cepat terjadinya peningkatan kekentalan selama proses gelatinisasi. Kandunggan amelopektin yang tinggi pada garanula pati meneybabkan daya intermolekul dalam granula semakin lemah sehingga air mudah masuk dalam celah – celah Kristal. Winarno (1997), menjelaskan bahwa molekul pati mempunyai jumlah gugus hidroksil yang sangat besar. Hal ini menyebabkan molekul pati memiliki kemampuan menyerap air sangat besar. Kekentalan meningkat bila air terserap dalam molekul – molekul pati sehingga tidak dapat bergerak dengan bebas.
Menurut Branen et al. (1990) yang dikutip oleh Prangkongpan et al (2002), viskositas dari suatu suspensi tergantung pada bentuk molekul, ukuran, dan muatan. Viskositas atau biasa dikenal dengan kekentalan atau penolakan terhadap penuangan menggambarkan penolakan dalam zat cair kepada aliran dan dapat diperkirakan sebagai cara untuk mengukur gesekan zat cair. Viskositas
terjadinya peningkatan kekentalan selama proses gelatinasi. Winarno (1997) menerangkan bahwa molekul pati mempunyai jumlah gugus hidroksil yang sangat besar. Kekentalan meningkat bila air terserap ke dalam molekul – molekul pati sehingga tidak dapat bergerak dengan bebas.
2.4.3 Kapasitas Rehidrasi
Kapasitas rehidrasi adalah jumlah air yang dapat diikat atau diterima oleh metrik protein pada kondisi tertentu (Rey et al., 1981). Kapasitas rehidrasi protein berhubungan dengan komposisi asam amino bahan itu sendiri. Semakin banyak jumlah residu asam amino yang bermuatan maka kapasitas rehidrasi juga semakin besar. Kapasitas rehidrasi dipengaruhi oleh bebrapa faktor intrinsik pada bahan, antara lain pH, kekuatan ion, garam, temperature, dan konformasi protein. Nilai pH yang tinggi pada bahan akan memperbesar kapasitas rehidrasi . Beberapa zat tambahan terutama garam dan kondensat polyphosphate dapat pula meningkatkan kapasita rehidrasi (Nidhi, 2003).
Kapasitas rehidrasi adalah jumlah air yang dapat diikat atau diterima oleh matrix protein pada kondisi tertentu ( Rey dan Labuza, 1981). Kapasitas rehidrasi dipengaruhi oleh beberapa faktor intrinsik pada bahan, yaitu antara lain kandungan protein dan pH.
Nilai kapasitas rehidrasi adalah fungsi dari ukuran, bentuk, interaksi hidrofobik-hidrofobik dan adanya lipida, karbohidrat dan residu asam amino karena
Protein tepung jamur tiram mengandung asam amino yang mangandung gugus polar tetapi tidak memiliki muatan. Molekul polar ini merupakan dipolar yang dapat berinteraksi dengan air. Pemanasan akan mengakibatkan protein bahan terdenaturasi sehingga kemampuan mengikat air menurun. Hal ini terjadi karena energi panas akan mengakibatkan terputusnya interaksi non-kovalen yang ada pada struktur alami protein tapi tidak memutuskan ikatan kovalen yang berupa ikatan peptida (Ophart, 2003).
Polisakarida mempunyai unit glikosil yang mengandung hidroksil yang dapat membentuk ikatan hidrogen dengan satu atau lebih molekul air. Selain itu, cincin atom oksigen glikosida yang membuat satu gula membentuk rantai dengan gula lainnya juga dapat memebentuk ikatan hidrogen dengan air. Oleh karena itu,
polisakarida mempunyai kemampuan untuk mengikat dan menahan air (Fennama, 1996).
2.4.4 Daya emulsi
Daya emulsi adalah kemampuan suatu bahan untuk membentuk emulsi. Menurut Winarno (1997), emulsi adalah sesuatu dispersi atau suspensi suatu cairan yang lain, dimana molekul – molekul kedua cairan tersebut tidak saling berbaur tetapi saling antagonistik. Pada suatu emulsi biasanya terdapat tiga bagian utama yaitu bagian yang terdispersi terdiri dri butiran – butiran yang biasanya terdiri dari lemak, bagian kedua disebut media pendipersi yang juga dikenal sebagai
pendispersi. Molekul senyawa ini mempunyai afinitas terhadap kedua cairan tersebut.
Dalam emulsi, salah satu cairan (fase terdispersi) terpecah kecil – kecil dan tersuspensi dalam cairan kedua (fase pendispersi) sebagai tetesan – tetesan lembut. Salah satu bagian molekul emulsifier bersifat hidrofilik dan mempunyai daya tarik terhadap air, sedangkan bagian lainnya bersifat hidrofobik dan memiliki afinitas yang kecil terhadap air. Dalam suatu emulsi, molekul emulsifier
mengurung tetesan – tetesan fase terdispersi sehingga molekulnya yang hidrofilik berada dalam air. Hampir semua bahan pangan mengandung partikel dengan ukuran koloid seperti protein, karbohidrat, dan lemak.
Salah satu faktor yang mempengaruhi stabilitas koloid adalah muatan permukaan koloid tersebut. Dengan adanya muatan ini, maka partikel – partikel tersebut akan tolak menolak dan mencegah terjadinya agregasi yang dapat menyebabkan
pengendapan (Bird, 1993). Emulsi dikatagorikan menjadi dua, yaitu emulsi yang terbentuk dari minyak dalam air (o/w) dan emulsi air dalam minyak (w/o). Dalam emulsi minyak dalam air, air berfungsi sebagai medium pendispersi dan minyak sebagai medium terdispersi dalam bentuk globula – globula kecil. Sedangkan pada emulsi air dalam minyak, minyak merupakan medium pendispersi dan air sebagai media terdispersi (Bird, 1993).
2.4.5 Densitas
bahan hasil pertanian dipengaruhi oleh ukuran partikel, kekerasan permukaan dan metode pengukuran. Suatu bahan pangan memiliki densitas yang baik jika nilai densitas kecil, yang berarti untuk berat yang ringan dibutuhkan ruang (volume) yang besar (Anwar, 2000). Suatu produk tepung – tepungan yang diinginkan adalah yang memiliki densitas kecil maka dengan massa yang kecil dapat memenuhi ruang yang besar.
Menurut Winarno (1997), adanya panas menyebabkan energi kinetik air lebih besar dari pada gaya tarik menarik antar molekul pati di dalam granula, sehingga akan terjadi pengembangan granula pati. Granula – granula yang telah
membengkak setelah dikeringkan akan menghasilkan tepung yang mempunyai ukuran lebih besar tetapi rapuh. Ukuran partikel yang lebih besar menyebabkan perbandingan berat dengan volumenya semakin kecil, sehingga densitasnya juga menurun.
Nilai densitas menunjukkan porositas dari bahan, yaitu jumlah rongga yang terdapat diantara partikel- partikel bahan. Ukuran partikel yang lebih kecil menyebabkan perbandingan berat dengan volumenya semakin besar, sehingga densitas kembangnya juga meningkat.
III. BAHAN DAN METODE
3.1 Tempat dan Waktu Penelitian
Penelitian ini dilakukan di Laboratorium Pengolahan Hasil Pertanian dan
Biomassa serta Laboratorium Analisis Kimia Hasil Pertanian Jurusan Teknologi Hasil Pertanian Universitas Lampung Pada bulan Februari 2012 sampai April 2012.
3.2. Bahan dan Alat
Bahan baku utama yang digunakan dalam penelitian ini adalah jamur tiram segar (Pleurotus ostreatus) yang langsung dipanen dari salah satu pengusaha jamur tiram di Kecamatan Kemiling, Bandar Lampung. Bahan lain yang digunakan adalah asam sitrat, sulfit, air, aquades, dan bahan – bahan kimia untuk analisis. Alat – alat yang digunakan pada penelitian ini adalah oven, ayakan, loyang, mixer, pisau, sendok, gelas ukur, timbangan, desikator,cawan porselen, nampan, dan peralatan lainnya.
3.3 Metode Penelitian
menit, blanching + perendaman asam sitrat 0,5% selama 10 menit, perndaman natrium bisulfit 2500 ppm selama 10 menit, dan blanching + perendaman natrium bisulfit 2500 ppm selama 10 menit. Data yang diperoleh diuji kesamaan
ragamnya dengan uji Bartlet dan kenambahan data diuji dengan uji Tuckey.
Analisis data dilanjutkan menggunakan uji Beda Nyata Jujur (BNJ) pada taraf 5%. Tepung jamur dengan enam taraf perlakuan diamati karakteristik kimia dan
organoleptiknya, sedangkan analisis sifat fungsionalnya dilakukan pada tepung jamur dengan perlakuan awal terbaik.
3.4 Pelaksanaan Penelitian
3.4.1 Penelitian Pendahuluan
Penelitian dilakukan dalam dua tahap yaitu penelitian pendahuluan dan penelitian utama. Penelitian pendahuluan dilakukan untuk mengetahui waktu terjadinya pencoklatan pada jamur tiram, yang menunjukan terjadinya reaksi pencoklatan enzimatis.
benar selanjutnya dianalisis dengan tabel duo trio (Meilgaard, 1999). Kuesioner pengujian duo trio disajikan pada Tabel 2.
Tabel 2. Kuesioner Metode Duo Trio
3.4.2 Penelitian Utama
Penelitian utama dilakukan dalam Rancangan Acak Kelompok Lengkap (RAKL) dengan empat ulangan (ulangan sebagai kelompok). Setiap ulangan melibatkan tahap proses pembuatan tepung jamur tiram dengan keenam taraf perlakuan awal yang dicobakan. Ulangan kedua, ketiga, dan keempat dilakukan sama seperti ulangan pertama namun pembuatan tepung jamur tiram dilakukan pada hari yang berbeda.
Pembuatan tepung jamur tiram pada penelitian ini memodifikasi metode yang digunakan oleh Widyastuti dan Istini (2004). Pada proses pengolahan tepung jamur tiram, mula – mula jamur tiram segar dicuci hingga bersih yang bertujuan untuk memisahkan kotoran yang masih menempel pada jamur tiram. Selanjutnya 200 g jamur tiram ditimbang dan dipotong – potong memanjang dengan ukuran
2-Kuesioner Uji Duo Trio
Nama : NPM : Sampel :
Dihadapan anda disajikan 3 sampel jamur tiram, salah satunya adalah “R”. Anda diminta menilai warnanya. Berikan tanda (X) pada kolom yang telah
disediakan untuk sampel berkode yang warnanya berbeda dengan “R” Kode Sampel Sampel yang berbeda dengan R
3 cm. Pemotongan bertujan untuk memoercepat proses pengeringan. Jamur tiram yang telah dipotong – potong kemudian mendapat perlakuan awal sesuai dengan keenam taraf perlakuan yang dicobakan yaitu : kontrol, blanching, perendaman asam sitrat 0,5% selama 10 menit, perendaman natrium bisulfit 2500 ppm selama 10 menit, blanching + perendaman asam sitrat 0,5% selama 10 menit, dan
blanching + perendaman natrium bisulfit 2500 ppm selam 10 menit. Setelah mendapat perlakuan awal jamur tiram dikeringkan dengan oven pada suhu 450C selama 24 jam, lalu digiling sampai halus dengan blender dan diayak
menggunakan ayakan ukuran 80 mesh. Tepung jamur tiram dianalisis sifat kimia dan organoleptiknya.
3.5 Pengamatan
Pengamatan dilakukan terhadap karakteristik kimia dan organoleptik (warna) tepung jamur tiram yang dihasilkan. Pengamatan terhadap karakteristik kimia pada tepung jamur tiram dengan enam taraf perlakuan awal meliputi: kadar air, kadar protein, kadar abu, dan kadar karbohidrat, sedangkan pengamatan
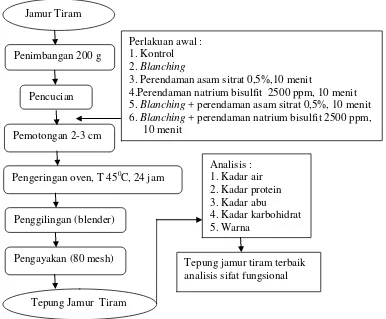
Diagram alir proses pembuatan tepung jamur tiram dapat dilihat pada Gambar 2.
Gambar 2. Diagram alir pembuatan tepung jamur tiram (Widyastuti dan Istini, 2004) yang dimodifikasi
3.5.1 Sifat Kimia Tepung Jamur Tiram 3.5.1.1 Kadar Air
Kadar air dilakukan dengan menggunakan metode gravimetric (AOAC, 1995). Cawan porselen dikeringkan dalam oven selama 30 menit, lalu didinginkan di dalam desikator dan ditimbang. Sebanyak 5 g sampel ditimbang lalu dimasukkan dalam cawan porselen dan dikeringkan dalam oven pada suhu 105 – 1100C selama 3 jam, didinginkan dalam desikator selama 15 menit kemudian ditimbang setelah diperoleh hasil penimbangan pertama, cawan yang berisi sampel tersebut
Penimbangan 200 g
Pencucian
Pemotongan 2-3 cm
Pengeringan oven, T 450C, 24 jam
Penggilingan (blender)
Pengayakan (80 mesh)
Tepung Jamur Tiram
Perlakuan awal : 1. Kontrol 2. Blanching
3. Perendaman asam sitrat 0,5%,10 menit
4.Perendaman natrium bisulfit 2500 ppm, 10 menit 5. Blanching + perendaman asam sitrat 0,5%, 10 menit 6. Blanching + perendaman natrium bisulfit 2500 ppm,
10 menit
Analisis : 1. Kadar air 2. Kadar protein 3. Kadar abu
4. Kadar karbohidrat 5. Warna
dikeringkan kembali selama 30 menit, setelah itu didinginkan dalam desikator selama 15 menit kemudian ditimbang.
Bila penimbangan kedua mencapai bobot tidak lebih dari 0.001 g dari
penimbangan pertama maka dianggap konstan. Akan tetapi apabila tidak maka dilakukan penimbangan kembali sampai diperoleh pengurangan bobot dua penimbangan berturut – turut. Kemudian cawan dan sampel ditimbang.
3.5.1.2 Kadar Protein
Penentuan kadar protein dilakukan dengan metode semimikro kjeldhal (AOAC, 1995). Sampel yang telah dihancurkan ditimbang sebanyak 0,1 – 0,2 g kemudian dimasukkan kedalam labu kjeldhal ukuran 20 ml, labu ditambahkan K2SO4 dan 40
ml HgO serta 2 ml H2SO4 pekat, kemudian didestruksi selama 30 – 60 menit
sampai cairan berwarna jernih. Cairan dibiarkan dalam labu hingga dingin lalu ditambahkan 1-2 ml aqudes secara perlahan, lalu isi labu dipindahkan kedalam alat destilasi dan ditambahkan 8-10 ml NaOH dan Na2S2O3 sampai berbentuk
warna coklat kehitaman. Lalu dilakukan proses destilasi dan hasil destilasi ditampung dalam erlenmeyer 125 ml yang berisi 5 ml H2BO2 dan 2-5 tetes
indikator Phenol Ptalien sampai tertampung kira – kira 15 ml. Hasil destilasi ditampung dan diencerkan dengan aquades kemudian dititrasi dengan HCl 0,0 N sampai berbentuk warna abu kecoklatan. Analisis juga dilakukan terhadap blanko dengan menggunakan air destilasi.
Kadar air (%) =
Berat awal sampel (g)
Berat awal sampel (g) – berat ahir sampel (g)
Keterangan :
A = Jumlah larutan HCl untuk titrasi sampel (ml) B = Jumlah HCl untuk titrasi blanko (ml)
C = Jumlah HCl yang digunakan
3.5.1.3 Kadar Abu
Kadar abu dilakukan dengan memijarkan sampel dalam tanur pada suhu tinggi (AOAC, 1995). Sebanyak 5 g sampel dipijarkan dalam tanur pada suhu 5500C sampai mencapai bobot konstan selama kurang lebih 2 jam. Kemudian sampel didinginkan ke dalam desikator hingga mencapai suhu kamar selama 30 menit, lalu ditimbang. Kadar abu dapt ditentukan dengan rumus :
Keterengan :
A. berat cawan + sampel B. berat cawan kosong C. berat sampel awal
3.5.1.4 Kadar Karbohirat
Penentuan kadar karbohidrat dengan cara perhitungan kasar disebut juga Carbohydrate by difference yaitu penentuan karbohidrat dengan menggunakan perhitungan dan bukan analisis (Winarno, 1992).
Kadar protein (%) =
(A-B) X N HCl X 14,008
Berat awal sampel (mg)
X 100%
Kadar abu (%) =
(A-B)
C
Karbohidrat ( %) = 100% - % ( air + abu + protein)
3.5.2 Uji Organoleptik Tepung Jamur Tiram
[image:39.595.109.506.309.523.2]Uji organoleptik dilakukan terhadap warna tepung jamur tiram menggunakan uji skoring. Sampel diberi kode angka tertentu dan disajikan secara acak kepada 20 orang panelis. Panelis diminta pendapatnya secara tertulis pada blanko atau formulir yang disediakan. Kuisioner uji organoleptik dapat dilihat pada Tabel 3.
Tabel 3. Kuisioner uji organoleptik metode skoring
3.5.3 Sifat Fungsional Tepung Jamur Tiram
Pengamatan yang dilakukan terhadap sifat fungsional tepung jamur tiram terbaik meliputi : kelarutan, viskositas, kapasitas rehidrasi, daya emulsi, dan densitas.
3.5.3.1 Kelarutan
Pengamatan yang dilakukan menggunakan metode Sathe dan Salunke (1981). Sejumlah 0,75 g sampel tepung jamur tiram dilarutkan dalam 150 ml air,
Nama : Produk : Tepung jamur tiram Tanggal :
Dihadapan anda disajikan sampel tepung jamur tiram. Anda diminta untuk mengevaluasi sampel satu – persatu, yaitu warna. Berikan penilaian anda dengan cara menuliskan skor dibawah kode sampel pada tabel penilaian berikut :
Penilaian 289 115 254 388 513 Warna
Keterangan skor mutu uji skoring warna tepung jamur tiram : Sangat putih : 5
kemudian disaring dengan bantuan corong Buncher. Sebelumnya kertas saring yang berukuran 41 µm dikeringkan terlebih dahulu dalam oven 1000C selama 30 menit dan ditimbang. Kertas saring dan endapan yang tersisa dikeringkan dalam oven 1000C selama 3 jam, kemudian didinginkan dalam desikator dan ditimbang.
Keterangan :
a. berat kering sampel (g)
b. berat endapan dan kertas saring (g) c. berat kertas saring (g)
3.5.3.2 Viskositas
Penetuan viskositas dilakukan dengan menggunakan metode (AOAC, 1995) dengan menggunakan viskometer. Sampel tepung jamur tiram sebanyak 1,2 g dimasukan ke dalam tabung dan dilarutkan dengan aquades 25 ml dan divorteks sampai terlarut sempurna. Pada viskometer dipasang pengaduk (spindle) 1 dengan kecepatan 6, selanjutnya alat dihidupkan selama 5 menit. Kekentalan dibaca pada skala centipoises.Metode ini dilakukan berdasarkan petunjuk alat penggunaan viskometer.
Viskometer (centipoises) = (dial reading x faktor)
3.5.3.3 Kapasitas Rehidrasi
Sampel tepung jamur tiram sebanyak 10 g dimasukan kedalam botol sentrifius, kemudian ditambahkan 40 g air suling lalu botol ditimbang. Botol diletakkan
a X 100%
Kelarutan (%) =
dalam shaker dan kocok selama 5 menit pada 330 getaran/menit. Kekuatan sentrifugal disetting pada 3000 dan diputar selama 20 menit. Kemudian buang cairan yang tidak terserap pada sampel secara perlahan – lahan, kemudian botol yang berisi sampel dihitung, selanjutnya ditimbang.
3.5.3.4 Emulsi
Daya emulsi ditetapkkan menggunakan prosedur yang dilakukan oleh Sathe dan Salunke (1981). Sebanyak 10 g sampel tepung jamur tiram disuspensikan didalam 100 g air distilata. Nilai pH diatur mencapai 7,5. Air ditambahkan ke dalam suspense hingga mencapai volume 150 ml dan ditambahkan minyak sawit sebanyak 150 ml. Campuran tersebut diaduk menggunakan homogenizer selama 2 menit dengan kecepatan tinggi. Sebanyak 50 ml emulsi disentrifius pada suhu 250C selama 30 menit pada kecepatan 1450 rpm. Aktivitas emulsi dinyatakan dalam persen total volume.
3.5.3.5 Densitas
Densitas diihitung dengan metode yang ditetapkan AOAC (1990). Tepung jamur tiram dituang ke dalam wadah yang telah diketahui volumenya dari ketinggian 10 sampai 15 cm, kemudian diratakan dari satu arah lalu ditimbang. Densitas
dihitung berat tepung per volume wadah dan dinyatakan dalam g/ml. Bobot botol + sampel terehidrasi setelah sentrifius
=
Daya emulsi
Volume krim yang dihasilkan (ml) Volume keseluruhan (ml)
X 100% =
Bobot botol + sampel + air sebelum sentrifius (g) Kapasitas
Keterangan :
a = berat tepung jamur tiram (g) b = volume wadah (ml)
V. SIMPULAN DAN SARAN
5.1 Simpulan
Berdasarkan hasil penelitian yang telah dilakukan, maka simpulan yang dapat diambil adalah 1. Dalam pembuatan tepung jamur tiram tidak diperlukan perlakuan awal dengan proses
perendaman dalam natrium bisulfit, asam sitrat maupun blanching.
2. Tepung jamur tiram tanpa perlakuan awal/ kontrol memiliki karakteristik sebagai berikut : kadar air 7,29%, kadar protein 17,75%, kadar abu 8,26%, dan kadar karbohidrat 71,68%, dengan warna putih (4.34).
5.2 Saran
PENGARUH PERLAKUAN AWAL TERHADAP KARAKTERISTIK
KIMIA DAN ORGANOLEPTIK
TEPUNG JAMUR TIRAM (
Pleurotus ostreatus
)
Oleh
Ardiansyah
Skripsi
Sebagai Salah Satu Syarat untuk Mencapai Gelar
SARJANA TEKNOLOGI PERTANIAN
Pada
Jurusan Teknologi Hasil Pertanian
Fakultas Pertanian Universitas Lampung
FAKULTAS PERTANIAN
UNIVERSITAS LAMPUNG
PENGARUH PERLAKUAN AWAL TERHADAP
KARAKTERISTIK KIMIA DAN ORGANOLEPTIK
TEPUNG JAMUR TIRAM (
Pleurotus ostreatus
)
Skripsi
Oleh
Ardiansyah
0714051035
FAKULTAS PERTANIAN
UNIVERSITAS LAMPUNG
DAFTAR GAMBAR
DAFTAR ISI
Halaman
KATA PENGANTAR ... ix
DAFTAR ISI ... xi
DAFTAR TABEL ... xii
DAFTAR GAMBAR ... xiii
DAFTAR LAMPIRAN ... xiv
I. PENDAHULUAN 1.1 Latar Belakang dan Masalah ... 1
1.2 Tujuan Penelitian ... 2
1.3 Kerangka Pemikiran ... 2
1.4 Hipotesis ... 7
II. TINJAUAN PUSTAKA 2.1 Jamur Tiram ... 8
2.2 Pencoklatan Enzimatis dan Non-enzimatis ... 11
2.2.1 Pencoklatan Enzimatis ... 11
2.2.2 Pencoklatan Non-enzimatis ... 13
2.3 Pencegahan Pencoklatan Enzimatis dan Non-enzimatis ... 14
2.3.1 Sulfit ... 14
2.3.2 Keamanan Sulfit ... 16
2.3.3 Blanching ... 17
2.4.3 Kapasitas Rehidrasi ... 24
2.4.4 Daya Emulsi ... 25
2.4.5 Densitas ... 26
III. BAHAN DAN METODE 3.1 Tempat dan Waktu Penelitian ... 28
3.2 Bahan dan Alat ... 28
3.3 Metode Penelitian ... 28
3.4 Pelaksanaan Penelitian ... 29
3.4.1 Penelitian Pendahuluan ... 29
3.4.2 Penelitian Utama ... 30
3.5 Pengamatan ... 31
3.5.1 Sifat Kimia Tepung Jamur Tiram ... 32
3.5.1.1 Kadar Air ... 32
3.5.1.2 Kadar Protein ... 33
3.5.1.3 Kadar Abu ... 34
3.5.1.4 Kadar Karbohidrat ... 34
3.5.2 Uji Organoleptik Tepung Jamur Tiram ... 35
3.5.3 Sifat Fungsional Tepung Jamur Tiram ... 36
3.5.3.1 Kelarutan ... 36
3.5.3.2 Viskositas ... 37
3.5.3.3 Kapasitas Rehidrasi ... 37
3.5.3.4 Emulsi ... 38
3.5.3.5 Densitas ... 38
IV. HASIL DAN PEMBAHASAN 4.1 Penelitian Pendahuluan ... 39
4.2 Penelitian Utama ... 40
4.2.1 Kadar Air ... 40
4.2.2 Kadar Protein ... 41
4.2.3 Kadar Abu ... 44
4.2.4 Kadar Karbohidrat ... 45
4.3 Uji Organoleptik ... 47
V. PENUTUP
5.1 Simpulan ... 53
5.2 Saran ... 53
DAFTAR PUSTAKA ... 54
DAFTAR PUSTAKA
Anonim(a). 2011. Jamur Tiram. http://id.wikipedia.org/wiki/jamur_tiram. [ 22 Februari 2011.]
Anonim (b). 2012. Hortikultura.go.id.Jamur Tiram Direktorat Jenderal Bina Produksi Hortikultura. [ 30 Maret 2012.]
Apandi, M. 1984. Teknologi Buah dan Sayur. Alumni, Bandung.
AOAC. 1995. Official Metode of Analisis of the Associates of Official Analytical Chemist. AOAC. Inc, New York.
Belitz, H. D. dan W. Grosch. 1999. Food Chemist. Springer. New York.
Birt, T. 1993. Kimia Fisik Untuk Universitas. Diterjemahkan Oleh Kwee Le Tjien. Gramedia. Jakarta.
Buckle, K. A., R. A Edwards, G. H. Fleet, dan M. Wooton. 1987. Ilmu Pangan. Terjemahan Oleh Adi Purnomo. UI Press, Jakarta.
Braverman, G. G. dan M. G. Cindly. 1963. Intruduction to the Biochemistry of Food. Elsevier, Amsterdam.
Cahyana dan B. Mucrodji. 1999. Jamur Tiram, Pembibitan, Pembudidayaan, Analisis Usaha. Penebar Swadaya. Jakarta.
Cahyadi, W. 2005. Analisis Aspek Kesehatan Bahan Tambahan Pangan. Bumi Aksara. Jakarta.
Desrosier, N. W. 1988. Teknologi Pengawetan Makanan. UI Press. Jakarta. De Man, J. M. 1989. Kimia Makanan. Edisi Kedua. ITB, Bandung.
Damodaran, S dan A. Paraf, 1997. Food Protein and Their Application. Marcel Dekker Inc. New York
Eriksson, C. 1981. Maillard Reaction in Food:Chemical Physiological and Technological Aspects. Pergamon Press, Exford.
Evily, A.J., R. Eyengar., dan W. S. Otwell, 1992. Inhabition on enzimatis browning in food and baverage. Crit. Rev. Food Sci. Nutr. 32: 253-273. Fellows, P. 2000. Food Processing Technology Principles and Practices.
Second Edition. Woodhead Publishingunited. England.
Furia, T. E. 1975. Handbook of Food Additives. The Chemical Rubber Co. Ohio. Fennema, O.R. 1996. Principle Of Food Science. In Food Chemistry (3rd Ed).
Marcel Dekker. Inc. New York.
Harris, O. R. dan E. Karmas. 1975. Nutrional Evaluation of Food Processing. The Avi Publishing Co., Wesport, Connecticut.
Hayyuningsih, D. R. W. 2009. Perbedaan Kandungan Protein, Zat Besi dan Daya Terima pada Pembuatan Bakso dengan Perbandingan Jamur Tiram (Pleurotus sp) dan Daging Sapi yang Berbeda. (Skripsi). Universitas Muhamadiyah Surakarta.
Kinsella, J. E. 1976. Functional properties of soy protein. J. Am. Oil Chem.Soc. 56(3): 242-250.
Koswara, S. 1995. Teknologi Pengolahan Kedelai Menjadi Makanan Bermutu. Pustaka Sinar Harapan. Jakarta.
Kotwaliwale. N., P. Bakane. dan A. Verma. 2005. Change in textural and optical properties of oyster mushroom during hot water air drying. J. of Food Eng. 78(4):1207-1211
Lindsay, R. R. 1976. Other Desirable Of Food. Dalam O.R. Fennama (ed). Principle Of Food Science. Marcel Dekker, Inc. New York.
Luh, B.S. and J.G. Woodroof. 1988. Commercial Vegetables Processing .2nd Edition Avi Book. New York.
Meilgaard, M., E. V. Civille and B. T. Car. 1999. Sensory Evaluation Technique. S rd Ed. CRC. Press. New York.
Muchtadi, T. R dan Sugiyono. 1992. Ilmu Pengetahuan Bahan. Depdikbud PAU-Pangan dan Gizi IPB, Bogor.
Murdefi, Y. 1992. Sifat Fungsional dan Nilai Gizi Tepung Tempe Serta
Pemanfaatannya dalam Pembuatan Biskuit untuk Anak Balita. (Skripsi) Fateta IPB. Bogor.
Naik, S. M.. K.S. Ramachandra dan T. N. Tulasidas. 2006. Drying of oyster mushroom (pleurotus florida) in defferent dryers. J. Dairying Food dan H.S.25(2) : 79-86.
Nakai, S. dan H.W. Modler. 1996. Food Protein Properties and Characterization. VCH Publisher, Inc. New York. Ophart, C.E. 2003. Virtual Chembook. Elmhurst College.
Prangdimurti E, Koswara S, dan A. Hartoyo. 2010. Penuntun Praktikum Evaluasi Biologis Komponen Pangan. Bogor: Departemen Ilmu dan Teknologi Pangan, Fakultas Teknologi Pertanian, IPB.
Pratiningsih, Y. 1999. Buku Ajar Teknologi Pengolahan. Universitas Jember. Prayudi, R.J. 1988. Pengaruh Perlakuan Perendaman NaHSO3 dan Vitamin C
dalam Mencegah Pencoklatan Selama Ekstraksi Pati Sagu. (Skripsi). Skripsi FATETA IPB. Bogor.
Rey, D. K dan T. P. Labuza. 1981. Characterization of The Effect of Solutes the Water- Banding and Gel Strength Properties of Carragenan. J. Food Sci. 46:786-791.
Sathe, S.K., dan Salunke. 1981. Functional Properties of The Great Northern Bean (Phaseolus vulgaris L) Protein : Emulsi, Foaming, Viscosity, and Gelation Properties. J. 2 of Food Science Vol 46 : 82-96.
Senterre, C. R., Leach, T. F., dan J. N. Cash,. 1991. Bisulfite Alternatif in Processing Abration, Antioxidan and Other Mean. J. Food Technol. 47(10): 75-84.
Sriwahyuni, B. (1992). Mempelajari Pengaruh Penggunaan Natrium Bisulfit dan Sendawa terhadap Mutu Dendeng Sapi Selama Penyimpanan. (Skripsi). IPB. Bogor.
Steel dan Torie. 1991. Prinsip dan Prosedur Statistik. Gramedia Utama, Jakarta. Suriawaria(a), H. U. 2000. Sukses Beragrobisnis Jamur Kayu Shitake, Kuping,
Tiram. Penebar Swadaya, Jakarta.
Susanto dan Suseno. 1994. Teknologi Pengolahan Hasil Pertanian. PT. Bina Ilmu, Surabaya
Susilawati. 2000. Kajian Karakteristik dan Sifat – Sifat Fungsional Tepung Ketan. (Skripsi) Fateta IPB, Bogor.
Tolani, E. 1993. Pengaruh Konsentrasi dan Lama Perendaman Dalam Natirum Bisulfit Terhadap Sifat Fisik Kimia dan Organoleptik Pati Sagu. (Skripsi) Universitas Lampung, Bandar Lampung.
Triono, J. 2006. Pengaruh Konsentrasi Natrium Bisulfit Terhadap Sifat Kimia Warna dan Aroma Tepung Pati Kentang (Solanum tuberosum L). (Skripsi). Universitas Lampung. Bandar Lampung.
Vera, F. 2005. Pengaruh Natrium Metabisulfit dan Suhu Pengeringan Terhadap Karateristik Fisik dan Kimia Ubi Jalar Jepang (Shiroyutaka). (Skripsi) Unila. Bandar Lampung.
Winarno, F. G. 1980. Pengantar Teknologi Pengolahan. Jakarta. PT. Gramedia Pustaka Utama, Jakarta.
Winarno, F. G. 1997. Kimia Pangan dan Gizi. Gramedia. Jakarta.
Winarno, F. G. 2000. Kimia Pangan dan Gizi. PT.Gramedia Pustaka Utama. Jakarta.
Widayastuti, N. dan S.,Istini. 2004. Optomasi Proses Pengeringan Tepung Jamur Tiram Putih. (Skripsi). IPB.
Dengan Ilmu kehidupan menjadi mudah, dengan
seni kehidupan menjadi halus, dengan agama
kehidupan menjadi terarah dan bermakna, dengan
iman dan takwa kehidupan menjadi kuat…
(Prof. Dr. Hi. Mukti Ali)
Semakin aku Tahu, sebenarnya aku tahu bahwa aku
tidak tahu apa
–
apa
Hidup Akan Terasa Berarti Jika Kita
Berarti Bagi Orang
lain…
KATA PENGANTAR
Puji syukur penulis panjatkan kehadirat Allah SWT, yang telah memberikan nikmat, rahmat, hidayah serta inayah-Nya kepada penulis sehingga penulis dapat menyelesaikan skripsi ini. Shalawat serta salam semoga tetap tercurah kepada junjungan kita Nabi besar Muhammad SAW beserta keluarga, sahabat, serta para penerus perjuangan-Nya.
Teriring syukur serta harap, penulis telah menyelesaikan sebuah skripsi yang berjudul Pengaruh Perlakuan Awal Terhadap Karakteristik Kimia dan Organoleptik Tepung Jamur Tiram (Pleurotus ostreatus), semoga bermanfaat bagi kita semua. Dalam menyelesaikan karya tulis ini, bimbingan serta dukungan dari beberapa pihak sangat membantu penulis. Oleh karena itu, penulis ingin mengucapkan terimakasih kepada :
1. Ibu Ir. Fibra Nurainy, M.T.A., selaku pembimbing pertama atas bimbingan, saran dan arahan selama pelaksanaan penelitian dan penulisan skripsi ini. 2. Ibu Dr. Ir. Sussi Astuti, M.Si., selaku pembimbing kedua atas bimbingan,
saran serta arahan selama penelitian dan pembuatan skripsi ini.
5. Ibu Ir. Marniza selaku Pembimbing Akademik atas bantuan dan bimbingannya dalam perencanaan studi.
6. Bapak dan Ibuku tersayang serta kakak – kakakku, adik – adikku serta istri dan anakku tersayang yang telah memberikan dorongan moril dan material, semangat serta do’a.
7. Mas Joko, Mbak Untari, Mbak Desi, Mas Khanafi, Mas Midi dan Pak Mul atas bantuan yang diberikan selama penelitian.
8. Sahabatku Aditia Kurniawan, Suhendrik dan Dias atas persahabatan, kebersamaan, keceriahan, bantuan dan motivasi.
9. Seluruh teman – teman angkatan 2007, serta angkatan 2006, 2008 - 2012 atas bantuan dan saran yang diberikan selama penelitian.
Semoga Allah SWT membalas semua kebaikan mereka dan semoga skripsi ini bermanfaat bagi kita semua. Amin.
Bandar Lampung, Maret 2013
Judul Skripsi : PENGARUH PERLAKUAN AWAL
TERHADAP KARAKTERISTIK KIMIA DAN ORGANOLEPTIK TEPUNG JAMUR TIRAM (PLEUROTUS OSTREATUS)
Nama Mahasiswa : Ardiansyah
Nomor Pokok Mahasiswa : 0714051035
Jurusan : Teknologi Hasil Pertanian Fakultas : Pertanian
MENYETUJUI
1. Komisi Pembimbing
Ir. Fibra Nurainy, M.T.A.
Dr. Ir. Sussi Astuti, M.Si.
NIP. 19680225 199603 2 001 NIP.19670824 199303 2 002
2. Ketua Jurusan Taknologi Hasil Pertanian
Ir. Susilawati, M.Si.
MENGESAHKAN
1. Tim Penguji
Ketua
:
Ir. Fibra Nurainy, M.T.A....
…………..
Sekretaris
:
Dr. Ir. Sussi Astuti, M.Si. ..……….
.
Penguji
Bukan Pembimbing :
Ir. Susilawati, M.S. ...………..………
2. Dekan Fakultas Pertanian
Prof. Dr. Ir. Wan Abbas Zakaria, M.S.
NIP 19610826 198702 1 001
Dengan Rasa Syukur Kepada Allah SWT
Kupersembahkan Karya Kecilku ini Kepada
Ayah, Ibu, Kakak - kakakku
Adik - adikku, keponakanku
RIWAYAT HIDUP
Penulis dilahirkan di Padang Cermin pada Tanggal 27 Desember 1987,
merupakan anak ke 5 dari pasangan Muhdi dan Nasmiati. Pendidikan Sekolah Dasar Negeri 1 Kota Bumi diselesaikan pada tahun 1999. Pendidikan Sekolah Madrasah Tsanawiah Negeri 2 Kota Bumi diselesaikan pada tahun 2002.
Pendidikan Sekolah Menengah Atas Negeri 1 Kota Bumi diselesaikan pada tahun 2005.
Pada tahun 2007, penulis terdaftar sebagai mahasiswa di Fakultas Pertanian Universitas Lampung Jurusan Teknologi Hasil Pertanian melalui Seleksi Penerimaan Mahasiswa Baru (SPMB). Pada tahun 2010, penulis melaksanakan Praktik Umum di PT. Bogasari Baking Center Palembang Sumatera Selatan.