SINTESIS ZINK DIISOAMILDITIOFOSFAT PADA MEDIUM
HEPTANA DAN KARAKTERISASI KINERJA INHIBISINYA
TERHADAP KOROSI LOGAM TEMBAGA YANG DIUKUR
SECARA POLARISASI POTENSIODINAMIK
YUNITA PRIMASANTI
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM INSTITUT PERTANIAN BOGOR
PERNYATAAN MENGENAI SKRIPSI DAN
SUMBER INFORMASI SERTA PELIMPAHAN HAK CIPTA
Dengan ini saya menyatakan bahwa skripsi berjudul Sintesis Zink Diisoamilditiofosfat pada Medium Heptana dan Karakterisasi Kinerja Inhibisinya terhadap Korosi Logam Tembaga yang Diukur secara Polarisasi Potensiodinamik adalah benar karya saya dengan arahan dari komisi pembimbing dan belum diajukan dalam bentuk apa pun kepada perguruan tinggi mana pun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir skripsi ini.
Dengan ini saya melimpahkan hak cipta dari karya tulis saya kepada Institut Pertanian Bogor.
ABSTRAK
YUNITA PRIMASANTI. Sintesis Zink Diisoamilditiofosfat pada Medium Heptana dan Karakterisasi Kinerja Inhibisinya terhadap Korosi Logam Tembaga yang Diukur secara Polarisasi Potensiodinamik. Dibimbing oleh KOMAR SUTRIAH dan MOHAMMAD KHOTIB.
Senyawa zink dialkilditiofosfat (ZDTP) telah dikenal sebagai aditif dalam pelumas memiliki berbagai fungsi, salah satunya adalah antikorosi. ZDTPi dapat disintesis melalui 2 tahapan, yang pertama adalah pembentukan zat antara, yaitu asam dialkilditiofosfat (ADTP) dari reaksi antara difosforus pentasulfida (P2S5) dengan isoamil alkohol. Tahap kedua
adalah penambahan oksida logam, yaitu ZnO. Kinerja ZDTPi sebagai antikorosi diukur menggunakan teknik polarisasi potensiodinamik. Efektivitas inhibisi ZDTPi pada logam Cu mencapai 98.77% pada konsentrasi larutan inhibitor 3%. Parameter termodinamika menunjukkan spontanitas reaksi korosi berkurang dengan kehadiran inhibitor. Energi aktivasi meningkat setelah penambahan inhibitor karena meningkatnya energi minimum reaksi.
Kata kunci: antikorosi, asam dialkilditiofosfat, polarisasi potensiodinamik, termodinamika, zink dialkilditiofosfat
ABSTRACT
YUNITA PRIMASANTI. Zinc Diisoamyldithiophosphate Synthesis in Heptane Medium and Inhibition Performance Characterization of Copper Metal Corrosion Using Potentiodynamic Polarization Technique. Supervised by KOMAR SUTRIAH and MOHAMMAD KHOTIB.
Zinc dialkyldithiophosphates (ZDTP) compound is known as a lubricant additive and has many functions, one of which is as anti-corrosion. ZDTPi was synthesized in 2 steps. The first step was formation of intermediates so called dialkyldithiophosphates acid (ADTP) as resulted from the reaction between diphosphorus pentasulfide (P2S5) and isoamyl
alcohol. The second step was addition of metal oxide, ZnO. ZDTPi performance as an anti-corrosion was measured by potentiodynamic polarization technique. The inhibiton effectiveness of ZDTPi to metal Cu reached 98.77% in the 3% concentration of inhibitor solution. Thermodynamic parameter showed a decreasing spontaneity reaction in the presence of inhibitor. The activation energy increased due to the increasing inhibitor addition as indicated by the increasing minimum energy of reaction.
Skripsi
sebagai salah satu syarat untuk memperoleh gelar Sarjana Sains
pada
Departemen Kimia
SINTESIS ZINK DIISOAMILDITIOFOSFAT PADA MEDIUM
HEPTANA DAN KARAKTERISASI KINERJA INHIBISINYA
TERHADAP KOROSI LOGAM TEMBAGA YANG DIUKUR
SECARA POLARISASI POTENSIODINAMIK
YUNITA PRIMASANTI
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM INSTITUT PERTANIAN BOGOR
Judul Skripsi : Sintesis Zink Diisoamilditiofosfat pada Medium Heptana dan Karakterisasi Kinerja Inhibisinya terhadap Korosi Logam Tembaga yang Diukur secara Polarisasi
Potensiodinamik Nama : Yunita Primasanti NIM : G44100032
Disetujui oleh
Dr Komar Sutriah, MS Pembimbing I
Mohammad Khotib, SSi MSi Pembimbing II
Diketahui oleh
Prof Dr Dra Purwantiningsih Sugita, MS Ketua Departemen
PRAKATA
Puji dan syukur penulis panjatkan kepada Allah subhanahu wa ta’ala atas segala karunia-Nya sehingga karya ilmiah ini berhasil diselesaikan. Tema yang dipilih dalam penelitian yang dilaksanakan sejak bulan Maret 2014 ini ialah inhibitor korosi, dengan judul Sintesis Zink Diisoamilditiofosfat pada Medium Heptana dan Karakterisasi Kinerja Inhibisinya terhadap Korosi Logam Tembaga yang Diukur secara Polarisasi Potensiodinamik.
Terima kasih penulis ucapkan kepada Bapak Dr Komar Sutriah, MS dan Bapak Mohammad Khotib, SSi MSi selaku pembimbing. Penghargaan penulis sampaikan kepada Denar Zuliandanu, SSi, Nofianita Khoirunnisa, SSi, Maulana Septiana, SSi, dan Faisal Rizki Gumelar, SSi yang telah membantu selama penelitian. Terima kasih juga untuk staf analis Laboratorium Terpadu IPB yang telah membantu selama pengumpulan data penelitian.
Ungkapan terima kasih juga disampaikan kepada ayah, ibu, adik, serta seluruh keluarga, atas segala doa dan kasih sayangnya. Terima kasih juga disampaikan kepada sahabat-sahabat saya (Mulyati, Mega, Eva, Wulan, Vicky, Rosalina, Fitha, Tazkiya, Aris, dan Dita), mahasiswa penelitian di Laboratorium Terpadu IPB, teman-teman mahasiswa Laboratorium Fisik dan Lingkungan, dan teman-teman Kimia 47 atas doa dan dukungannya.
Semoga karya ilmiah ini bermanfaat.
DAFTAR ISI
DAFTAR TABEL vi
DAFTAR GAMBAR vi
DAFTAR LAMPIRAN vi
PENDAHULUAN 13
Latar Belakang 13
Tujuan Penelitian 2
Waktu dan Lokasi 2
METODE 2
Bahan dan Alat 2
Prosedur 3
HASIL DAN PEMBAHASAN 5
Hasil Sintesis ZDTPi dan Penciriannya 5
Pencirian Produk ZDTPi 6
Pengaruh Konsentrasi ZDTPi terhadap Arus Korosi 7
Pengaruh Suhu pada Efektivitas Inhibisi Korosi ZDTPi 9
Parameter Termodinamika dan Kinetika Korosi 10
SIMPULAN DAN SARAN 12
Simpulan 12
Saran 12
DAFTAR PUSTAKA 12
LAMPIRAN 13
DAFTAR TABEL
1 Rendemen sintesis ZDTPi 6
2 Analisis kadar logam Zn pada produk ZDTPi 7
3 Parameter korosi dan efektivitas inhibisi korosi larutan ZDTPi 8
4 Pengaruh suhu pada arus korosi 9
5 Parameter termodinamika dan kinetika korosi 10
DAFTAR GAMBAR
1 Rute sintesis ZDTPi 6
2 Spektrum inframerah produk ZDTPi 7
3 Hubungan konsentrasi inhibitor dengan efektivitas inhibitor 9 4 Aluran kurva persamaan Arrhenius keadaan transisi 10
5 Aluran kurva persamaan Arrhenius 11
DAFTAR LAMPIRAN
1 Bagan alir sintesis 14
2 Rangkaian alat sintesis 15
3 Elektrode Cu, reservoir, dan Potensiostat 16
4 Bobot dan perhitungan sintesis 17
5 Data hasil analisis kadar Zn 18
6 Data arus korosi 19
PENDAHULUAN
Latar Belakang
Penggunaan berbagai logam dalam berbagai aspek kehidupan semakin meningkat dari tahun ke tahun. Hal tersebut dipicu oleh adanya perkembangan teknologi, pertumbuhan ekonomi, dan pembangunan nasional. Logam-logam seperti baja, besi, aluminium, perak, dan tembaga digunakan di berbagai industri baik sebagai komponen utama maupun komponen tambahan. Terdapat banyak faktor yang menyebabkan turunnya daya guna dari logam tersebut. Salah satu penyebabnya adalah terjadinya korosi atau proses pengaratan logam (Irianty dan Khairat 2013). Korosi menjadi salah satu masalah penting yang dihadapi oleh kelompok industri maju. Kerugian yang dialami industri akibat peristiwa korosi, yaitu adanya gangguan saat proses produksi, operasi berjalan tidak efisien, dan tingginya harga pemeliharaan akibat penambahan ongkos pengontrolan korosi pada mesin (Malik et al. 2011).
Proses terjadinya korosi dapat dikendalikan atau diperlambat lajunya dengan pelapisan pada permukaan logam, perlindungan katodik, dan penambahan inhibitor korosi (Irianty dan Khairat 2013). Penggunaan inhibitor korosi memiliki banyak keuntungan, yaitu tingginya efektivitas inhibisi, harga yang murah, rendahnya toksisitas, dan mudah diproduksi (Malik et al. 2011). Istilah pelumasan dikenal di industri sebagai salah satu upaya untuk menghambat terjadinya korosi. Permukaan logam dilindungi sehingga dapat mencegah keausan dan gesekan mesin yang menjadi penyebab korosi. Penambahan aditif inhibitor korosi dapat meningkatkan kinerja dari pelumas sebagai antikorosi (Dinoiu et al. 2007).
Senyawa zink dialkilditiofosfat (ZDTP) telah dikenal selama empat puluh tahun sebagai aditif dalam pelumas dengan konsentrasi kurang dari 1.5% dari bobot total pelumas (Dinoiu et al. 2007). Senyawa ini mengandung gugus fosfor dan sulfur sehingga memiliki sifat antioksidan yang kuat. Struktur ZDTP dapat teradsorpsi pada permukaan logam dan membentuk lapisan pasif sehingga permukaan menjadi tidak terlalu aktif terkorosi. Atom sulfur, fosfor, dan zink berperan dalam proses adsorpsi sedangkan rantai alkil bertindak sebagai penghalang (barrier) yang melindungi permukaan logam dari serangan oksidasi dari luar (Zuliandanu 2013).
Sintesis ZDTP dapat dilakukan melalui 2 tahapan, yang pertama adalah pembentukan zat antara, yaitu asam dialkilditiofosfat (ADTP) dari reaksi antara difosforus pentasulfida (P2S5) dengan alkohol. Tahap kedua
2
stabilitas termal yang tinggi pada produk ZDTP yang dihasilkan. ZDTP dengan alkil primer memiliki kestabilan termal, kestabilan hidrolitik, antiaus, dan antioksidan yang baik (Rudnick 2009). Halangan sterik yang besar dapat mengurangi kemudahan molekul ZDTP untuk teradsorpsi pada permukaan logam (Zuliandanu 2013).
Pengukuran kinerja antikorosi dari ZDTP dapat dilakukan menggunakan teknik polarisasi potensiodinamik. Teknik elektrokimia ini banyak digunakan untuk mengukur kinerja antikorosi berdasarkan pantauan arus korosi. Parameter polarisasi yang digunakan untuk menjadi parameter pengukur kinerja antikorosi tersebut yaitu arus korosi, potensial korosi, dan kemiringan Tafel (Zuliandanu 2013). Selain itu perlu digunakan juga besaran termodinamika untuk mengukur kemudahan terjadinya reaksi korosi. Akan tetapi, pembahasan termodinamika tentang korosi hanya menunjukkan ada tidaknya kecenderungan korosi. Perlu dipelajari kinetika proses korosi untuk menentukan kecepatan terjadinya reaksi korosi tersebut (Atkins dan Paula 2012).
Tujuan Penelitian
Penelitian ini bertujuan melakukan sintesis dalam medium heptana dan karakterisasi senyawa Zink (diisoamil ditiofosfat) serta menguji kinerjanya sebagai antikorosi pada logam tembaga dengan teknik polarisasi potensiodinamik.
Waktu dan Lokasi
Penelitian ini akan dilaksanakan dari bulan Maret hingga Juli 2014 di Laboratorium Terpadu, Kampus IPB Baranangsiang Bogor.
METODE
Bahan dan Alat
Penelitian ini terdiri atas 2 bagian. Bagian pertama adalah sintesis ZDTPi serta penciriannya dan bagian kedua adalah pengujian antikorosi dengan teknik polarisasi potensiodinamik. Bahan-bahan yang digunakan untuk sintesis dan pencirian ZDTPi adalah P2S5 (Merck), isoamil alkohol,
ZnO (teknis), n-heptana, HNO3 pekat, HCl 37%, KBr, dan akuades.
Pengujian antikorosi dengan teknik polarisasi potensiodinamik menggunakan bahan-bahan yaitu aseton, ampelas silikon karbida 100 CW, HCl 5%, larutan NaCl 1%, dan kupon tembaga (elektrode kerja).
3 Shimadzu, dan spektrofotometer inframerah transformasi Fourier (FTIR) Prestige-21 Shimadzu.
Prosedur
Sintesis Zink Diisoamilditiofosfat (ZDTPi) (Dinoiu et al. 2007)
Bagan alir dari sintesis dijelaskan pada Lampiran 1. Tahap pertama adalah sintesis ADTP terlebih dahulu. P2S5 dan isoamil alkohol direaksikan
dengan nisbah mol 1:4 dalam pelarut n-heptana selama 12 jam di dalam labu didih. Pemanasan dan pengadukan dilakukan pada suhu 70 oC pada penangas air. Rangkaian alat untuk sintesis tahap pertama ditunjukkan pada Lampiran 2. Produk dari hasil reaksi ini adalah asam diisoamilditiofosfat (ADTPi). Sebanyak 1 mol ZnO ditambahkan pada wadah ADTPi lalu dilakukan pengadukan tanpa pemanasan selama 12 jam untuk membentuk ZDTPi. Produk diekstraksi dengan 20 mL n-heptana dan dicuci dengan 20 mL air. Fase organik yang diambil lalu diuapkan pelarutnya. Selanjutnya bobot ZDTPi ditimbang untuk mendapatkan rendemennya.
Pencirian Gugus Fungsi dengan FTIR
ZDTPi hasil sintesis dicirikan dengan menggunakan tipe FTIR Prestige-21 Shimadzu untuk menentukan gugus fungsi atau ikatan kimia pada produk. Pengukuran dilakukan dengan menggerus produk dengan KBr kemudian dibuat pelet dan diukur pada panjang gelombang 400-5000 cm-1. Penetapan Kadar Zn dengan AAS
Sampel Zink (diisoamil ditiofosfat) ditimbang sebanyak 0.5 g dan ditambahkan 10 mL HNO3 pekat. Campuran didestruksi hingga asap
menghilang dan ditambahkan 10 mL HCl 37%. Larutan hasil destruksi disaring ke labu takar 100 mL lalu ditera dengan akuades. Larutan ini kemudian diukur kadar Zn-nya dengan AAS Shimadzu AA-6300 pada panjang gelombang 213.9 nm dengan lebar celah 0.7 nm.
Pengukuran dengan Teknik Polarisasi Potensiodinamik
Elektrode kerja tembaga (Cu) dipreparasi dengan cara diampelas permukaannya kemudian dibilas dengan akuades dan aseton. Setelah itu, elektrode Cu dimasukkan ke dalam reservoir yang berisi larutan uji NaCl 1%. Reservoir diberikan sirkulasi air pada dindingnya untuk memelihara kestabilan suhu. Elektrode Ag/AgCl dan kawat Pt berturut-turut dipasang sebagai elektrode pembanding dan elektrode pembantu. Kabel warna hitam, putih, dan merah dari potensiostat DY2300 berturut-turut disambungkan pada elektrode kerja, pembanding, dan pembantu. Gambar dan rangkaian alat ditunjukkan pada Lampiran 3.
4
mV/s. Setelah pengukuran blanko selesai, elektrode Cu dibersihkan kembali dengan cara dibilas HCl 5% kemudian dicuci dengan akuades dan diampelas kembali. Setelah itu, dicuci kembali menggunakan akuades dan aseton.
Elektrode Cu yang telah dibersihkan kemudian dicelupkan ke dalam larutan ZDTPi dengan konsentrasi 0.5%, 1%, 2%, dan 3% selama 15 detik dan ditiriskan beberapa saat. Elektrode kerja kemudian dirangkaikan kembali pada reservoir dan dilakukan lagi pengondisian secara 2 menit. Setelah pengondisian selesai, sampel diukur pada rentang potensial yang sama baik untuk anode maupun katode. Data yang didapatkan kemudian diproses menggunakan perangkat lunak Microsoft Excel sehingga didapat kurva polarisasi. Dari kurva tersebut, diperoleh informasi berupa potensial korosi (Ecorr), tetapan Tafel anode (a) dan katode (c), serta arus korosi
(icorr). Efektivitas inhibitor dan derajat penutupan permukaan () dihitung sesuai persamaan berikut.
Parameter Termodinamika Proses Korosi
Parameter termodinamika ditentukan berdasarkan persamaan Arrhenius keadaan transisi:
Pengukuran dilakukan pada suhu 30, 40, 50, dan 60 oC. Parameter ΔH* dan
ΔS* berturut-turut merupakan perubahan entalpi dan entropi keadaan transisi, sedangkan NAh adalah tetapan Planck Molar (3.99 × 10-10 JSmol-1). Dengan memvariasikan suhu (T), maka ΔH* dan ΔS* dapat ditentukan dari kurva ln (icorr/T) vs 1/T, sedangkan perubahan energy bebas Gibbs transisi
(ΔG*) dihitung dengan persamaan berikut:
ΔG* = ΔH*– TΔS*
Kinetika Laju Korosi dengan Tinjauan Energi Aktivasi
5
dengan A merupakan tetapan Arrhenius yang ditentukan secara empirik, Ea
adalah energi aktivasi proses korosi (kJ mol-1), R adalah tetapan gas ideal (8.314 J mol-1K-1), dan T adalah suhu (K) (Atkins dan Paula 2012). Pengukuran dilakukan pada suhu 30, 40, dan 50oC.
HASIL DAN PEMBAHASAN
Hasil Sintesis ZDTPi dan Penciriannya
Sintesis ZDTPi dilakukan melalui dua tahapan, yaitu dengan mencampurkan difosforus pentasulfida (P2S5) dengan isoamil alkohol dalam
pelarut n-heptana sehingga dihasilkan zat antara, yaitu asam dialkilditiofosfat (ADTP). Pelarut n-heptana memiliki sifat nonpolar sehingga dapat memudahkan reaksi antara P2S5 yang bersifat nonpolar
dengan alkohol yang bersifat polar. Oleh karena itu, n-heptana dapat melarutkan kedua reaktan dengan baik (Hayati 2013).
Unsur Fosfor (P) memiliki peranan penting sebagai antikorosi. Oleh sebab itu P2S5 yang direaksikan dibuat berlebih agar didapat konsentrasi
fosfor yang lebih tinggi. Konsentrasi P yang tinggi dapat meningkatkan peluang terbentuknya ZDTP yang akan dihasilkan (Dinoiu et al. 2007). Selain itu untuk memastikan bahwa isoamil alkohol habis terpakai saat reaksi karena alkohol yang tersisa akan mengganggu adisi ZnO terhadap ADTP pada tahap 2 sintesis (Zuliandanu 2013).
Pemanasan pada tahap pertama sangat dibutuhkan untuk menghilangkan hasil samping yaitu gas H2S yang dapat mengganggu
jalannya reaksi. Namun apabila suhu terlalu tinggi maka produk ADTP akan terdekomposisi dan rendemen yang dihasilkan akan rendah (Rismawati 2013). Pembentukan ADTP harus dalam kondisi tertutup sebagai upaya pencegahan terjadinya oksidasi pada ADTP yang dihasilkan (Hayati 2013).
6
Tabel 1 Rendemen sintesis ZDTPi
Sampel Bobot ZDTPi (g) Rendemen (%)
Ulangan 1 20.3320 93.54
Ulangan 2 20.2823 93.31
Pencirian Produk ZDTPi
Analisis Gugus Fungsi dengan FTIR
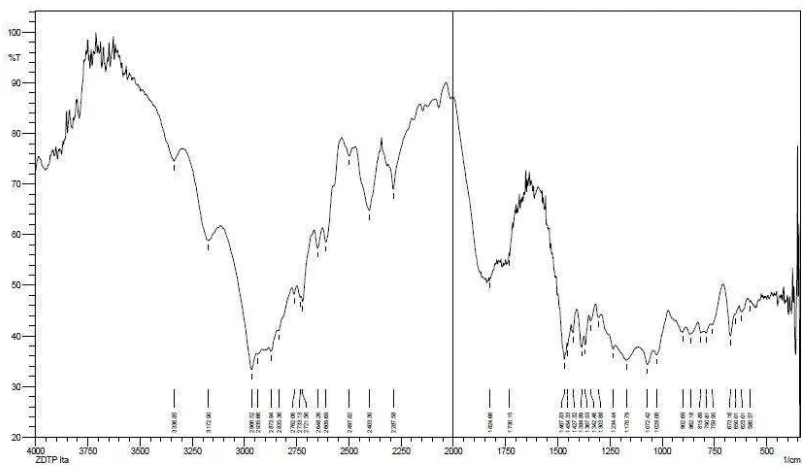
Spektrofotometer inframerah transformasi fourier (FTIR) digunakan untuk mendeteksi gugus fungsi dari senyawa ZDTPi yang dihasilkan. Spektrum yang dihasilkan pada Gambar 2 menunjukkan adanya puncak serapan pada bilangan gelombang 3000-2750 cm-1 regang C-H, 1467 cm-1 regang –CH2-, dan 1384 cm-1 regang –CH3. Bilangan gelombang di daerah
1072 cm-1 menunjukkan adanya ikatan P-O-C dan 673-590 cm-1 menunjukkan adanya ikatan P-S (Hayati 2013). Sementara itu, serapan Zn-S pada daerah 400-300 cm-1 tidak dapat diukur. Dari hasil interpretasi ini dapat diduga bahwa produk ZDTPi telah terbentuk, diantaranya dengan ditandai hilangnya alkohol yang habis bereaksi pada daerah bilangan gelombang 3500-3200 cm-1.
Gambar 1 Rute sintesis ZDTPi ADTP
ZDTPi
7
Gambar 2 Spektrum inframerah produk ZDTPi
Analisis Kadar Zn dengan AAS
Alat yang banyak digunakan untuk analisis logam adalah atomic absorption spectroscopy (AAS) atau spektroskopi serapan atom (SSA). Sampel yang telah dipreparasi kemudian diatomisasi dari atom pada keadaan dasar. Logam yang terkandung dalam sampel akan menyerap sinar elektromagentik sehingga tereksitasi. Rasio sinar yang terserap dengan yang diteruskan dapat dibaca oleh alat sebagai konsentrasi dari logam Zn (Dewi 2009). Kadar Zn yang didapat dari percobaan relatif sama dengan kadar Zn teoritis. Hasil analisis logam Zn yang terukur ditunjukkan pada Tabel 2 dan Lampiran 5.
Tabel 2 Analisis kadar logam Zn pada produk ZDTPi
Ulangan Kadar (%) Zn hasil
percobaan Kadar (%) Zn teoritis
1 12.08
10.83
2 11.79
Pengaruh Konsentrasi ZDTPi terhadap Arus Korosi
8
memiliki sifat agresif dari golongan asam kuat sehingga dapat merusak lapisan oksida logam. Produk ZDTPi sebagai inhibitor akan mengurangi kemungkinan permukaan logam kontak langsung dengan lingkungan (Tjitro et al. 2000). Proses pengendalian ini dapat memperlambat kecepatan korosi karena inhibitor secara kimia berinteraksi dengan permukaan logam untuk memberi tingkat perlindungan tertentu terhadap logam (Djatmiko dan Budiarto 2009).
Arus korosi dapat ditentukan berdasarkan polarisasi potensiodinamik. Pengukuran dilakukan dengan menggunakan metode Tafel sehingga didapat kurva polarisasi anodik dan katodik (Sunarya et al. 2008). Arus korosi kemudian didapat dari perpotongan antara kurva Tafel anode dan katode. Peningkatan konsentrasi larutan ZDTPi menyebabkan arus korosi akan mengalami penurunan dan adanya peningkatan efektivitas inhibisi. Hasil pengukuran dengan menggunakan metode polarisasi potensiodinamik ditunjukkan pada Tabel 3 dan Lampiran 6.
Konsentrasi ZDTP yang memberikan laju korosi (CR) paling kecil,
derajat penutupan permukaan () yang besar, dan daya inhibisi paling besar, yaitu pada konsentrasi 3%. Nilai yang besar mengakibatkan permukaan logam tertutupi penuh oleh inhibitor (Zuliandanu 2013). Peningkatan permukaan logam yang terlindungi ini menyebabkan difusi ion-ion dan elektron yang terlepas dari permukaan logam akan sulit terlepas sehingga arus yang dihasilkan kecil dan laju korosi akan berkurang (Djatmiko dan Budiarto 2009).
Tabel 3 Parameter korosi dan efektivitas inhibisi korosi larutan ZDTPi Konsentrasi (%) Arus korosi
(mA)
9
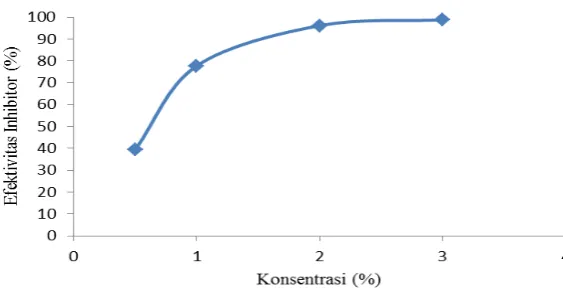
Gambar 3 Hubungan konsentrasi inhibitor dengan efektivitas inhibitor
Pengaruh Suhu pada Efektivitas Inhibisi Korosi ZDTPi
Kenaikan suhu lingkungan yang terlalu tinggi dapat menyebabkan adanya serangan oksidasi yang cepat pada permukaan logam. Peningkatan ini memicu bertambahnya energi pada sistem yang dapat meningkatkan keaktifan dari gerakan ion klorida dalam reservoir. Ion klorida yang bersifat agresif ini dapat mengikis lapisan logam tembaga. Akibatnya terjadi penurunan polarisasi anodik dan bertambah negatifnya potensial anoda sebagai tanda terjadinya korosi. Penambahan inhibitor ZDTPi dapat melindungi lapisan logam tembaga sehingga terbentuk lapisan tipis (Soedarsono 2004).
Data pada Tabel 4 menunjukkan bahwa laju korosi semakin meningkat karena adanya kenaikan suhu. Penambahan ZDTPi sebagai inhibitor menyebabkan laju korosi menurun dibandingkan blangko. Penurunan persen efektivitas inhibisi (EI%) akibat bertambahnya suhu menunjukkan adanya mekanisme adsorpsi secara fisik atau fisisorpsi. Menurut Ebenso et al. (2008) mekanisme fisisorpsi ditunjukkan oleh adanya penurunan %EI dengan kenaikan suhu sedangkan untuk mekanisme kimisorpsi, nilai %EI meningkat dengan kenaikan suhu.
Tabel 4 Pengaruh suhu pada arus korosi Suhu
(oC) Larutan
Garis Tafel
Anode Katode Arus korosi
10
Parameter Termodinamika dan Kinetika Korosi
Besaran termodinamika dan kinetika digunakan untuk mengukur kemudahan suatu reaksi korosi dapat terjadi. Derajat ketidakteraturan sistem dijelaskan dengan perubahan entropi (ΔS) dan kespontanan suatu reaksi
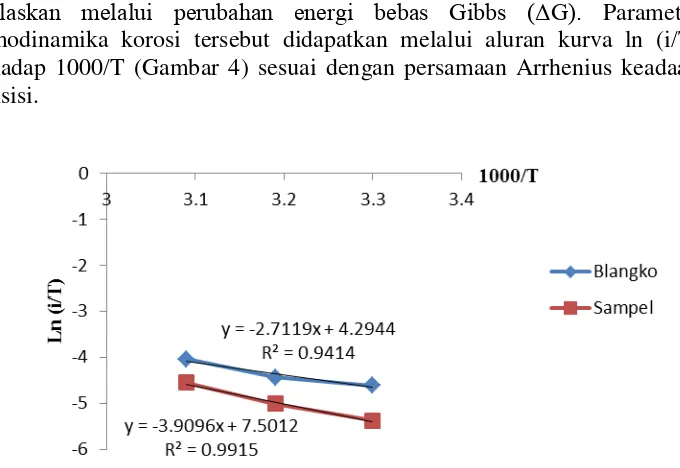
dijelaskan melalui perubahan energi bebas Gibbs (ΔG). Parameter
termodinamika korosi tersebut didapatkan melalui aluran kurva ln (i/T) terhadap 1000/T (Gambar 4) sesuai dengan persamaan Arrhenius keadaan transisi.
Gambar 4 Aluran kurva persamaan Arrhenius keadaan transisi
Tabel 5 menunjukkan bahwa nilai H* sampel lebih besar dari blangko. Hal ini dapat menunjukkan bahwa dengan penambahan inhibitor ZDTPi akan menyebabkan reaksi korosi yang terjadi membutuhkan energi yang lebih besar dibandingkan blanko. Nilai S* yang meningkat mengindikasikan adanya kenaikan derajat ketidakaturan sistem saat reaktan berubah menjadi kompleks teraktifkan (Zarrouk et al. 2011). Nilai G* menjelaskan spontanitas suatu reaksi. Reaksi kimia berjalan spontan dengan adanya arah penurunan nilai G*. Jika nilai G* berkurang maka reaksi korosi mempunyai kecenderungan untuk lebih mudah terjadi (Atkins dan Paula 2012). Nilai G* pada Tabel 5 menunjukkan bahwa dengan penambahan inhibitor ZDTPi terjadi peningkatan nilai G*
sehingga reaksi korosi berjalan tidak spontan.
11
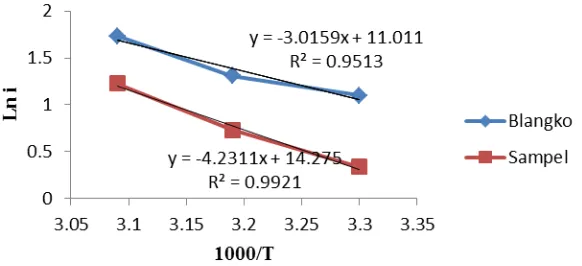
Aspek kinetika dapat digunakan untuk melihat mekanisme inhibisi dari ZDTPi dengan melihat kecepatan dari reaksi korosi. Tinjauan mengenai kinetika korosi dapat dijelaskan berdasarkan nilai energi aktivasi (Ea) proses
korosi. Nilai Ea didapat melalui persamaan Arrhenius (Gambar 5). Gradien
kurva dikalikan dengan tetapan gas ideal (R) merupakan nilai Ea dari reaksi yang terjadi (Zarrouk et al. 2011). Nilai Ea didefinisikan sebagai energi minimum yang harus dimiliki agar suatu reaksi bisa terjadi (Atkins dan Paula 2012). Semakin meningkatnya nilai Ea maka energi minimum yang
dibutuhkan untuk terjadinya proses korosi akan semakin besar sehingga laju korosi akan menurun (Zarrouk et al. 2011).
Data pada Tabel 5 menunjukkan dengan adanya penambahan ZDTPi, nilai Ea semakin meningkat. Hal ini menunjukkan bahwa dengan adanya penambahan ZDTPi, dibutuhkan energi yang lebih besar agar reaksi korosi dapat terjadi. Peningkatan nilai Ea akibat penambahan inhibitor diduga membuktikan adanya mekanisme fisisorpsi (Zarrouk et al. 2011). Adanya interaksi daya tarik elektrostatik antara muatan gugus hidrofilik dan muatan gugus permukaan atom logam menunjukkan mekanisme fisisorpsi (Malik et al. 2011).
12
SIMPULAN DAN SARAN
Simpulan
Sintesis Zink Diisoamilditiofosfat pada medium n-heptana telah berhasil dilakukan dengan rendemen yang tinggi sebesar 93.54% dan 93.31%. Hal ini dibuktikan oleh pencirian gugus fungsi menggunakan FTIR yang menunjukkan adanya pita-pita serapan yang khas untuk ZDTP. Kinerja antikorosi ZDTP telah berhasil ditentukan dengan teknik polarisasi potensiodinamik. Efektivitas inhibisi korosi semakin meningkat seiring meningkatnya konsentrasi ZDTP yang ditambahkan. ZDTP mampu menurunkan spontanitas reaksi korosi yang terukur berdasarkan peningkatan G dari 71.5825 kJmol-1
menjadi 73.4628 kJmol-1. Nilai Ea yang didapat dengan penambahan inhibitor lebih besar dibanding blangko. Hal ini mengindikasikan bahwa reaksi korosi yang terjadi membutuhkan energi minimum yang lebih besar sehingga laju korosi pun menurun dengan adanya penambahan ZDTP.
Saran
Adanya penelitian lebih lanjut dengan memvariasikan logam pusat yang digunakan dengan logam lain yang memiliki kinerja yang baik sebagai antikorosi. Selain itu perlu dilakukan penelitian menggunakan alkohol dengan rantai alkil lainnya.
DAFTAR PUSTAKA
Atkins PW, Paula JD. 2012. Physical Chemistry Sixth Edition. New York (US): WH Freeman.
Dewi KSP. 2009. Kemampuan adsorpsi batu pasir yang dilapisi besi oksida (Fe2O3) untuk menurunkan kadar Pb dalam larutan. J Bumi Lestari.
9(2):254-262.
Dinoiu V, Florescu D, Bogatu L. 2007. The influence of synthesis method of zinc dialkyldithiophosphates on the process of additivation. Rev Chim. 58(2):183-185.
Djatmiko E, Budiarto. 2009. Analisis laju korosi dengan metode polarisasi dan potensiodinamik bahan baja SS 304l. Seminar Nasional ke- 15 Teknologi dan Keselamatan PLTN serta Fasilitas Nuklir; 2009 Oktober 17; Surakarta, Indonesia. Surakarta (ID): Universitas Pancasila. hlm 182-194.
Ebenso EE, Eddy NO, Odiongenyi AO. 2008. Corrosion inhibitive properties and adsorption behavior of ethanol extract of Piper guinensis as a green corrosion inhibitor for mild steel in H2SO4. Afr J
Pure Appl Chem. 2(11):107-115.
13 Irianty RS, Khairat. 2013. Ekstrak daun papaya sebagai inhibitor korosi pada baja AISI 4140 dalam medium air laut. J. Ilmiah Sains Terapan. 4(2):77-82.
Ketis NK, Wahyuningrum D, Achmad S, Bundjah B. 2010. Efektifitas asam glutamat sebagai inhibitor korosi pada baja karbon dalam larutan NaCl 1%. J. Matematika dan Sains. 15(1):1-8.
Malik MA, Hashim MA, Nabi F, Al-Thabairi AS. 2011. Anti-corrosion ability of surfactans: a review. Int J Electrochem Sci. 6:1927-1948. Perez N. 2004. Electrochemistry and Corrosion Science. Boston (USA):
Kluwer Academic Publishers.
Rismawati. 2013. Pengaruh jenis alkohol pada rendemen sintesis zink dialkilditiofosfat [skripsi]. Bogor (ID): Institut Pertanian Bogor. Rudnick LR. 2009. Lubricant Additives Chemistry and Applications Second
Edition. Prancis (FR): CRC Press.
Soedarsono BSA. 2004. Korelasi efisiensi anoda korban Al-Azn-In terhadap perubahan kurva polarisasi dengan menggunakan metode potensiodinamik [tesis]. Jakarta (ID): Universitas Indonesia.
Sunarya Y, Radiman CL, Achmad S, Bundjali B. 2008. Pengaruh temperatur terhadap mekanisme inhibisi oleh sistein pada korosi baja karbon dalam larutan NaCl jenuh CO2. J Matematika dan Sains. 13
(3):90-96.
Sutrisno, E. 2012. Laju korosi lapisan krom pada knalpot berbahan baja karbon AISI 1010 [skripsi]. Depok (ID): Universitas Gunadarma. Utomo B. 2009. Jenis korosi dan penanggulangannya. Kapal. 6(2):138-141. Zarrouk A, Hammouti B, Zarrok H, Al-Dayab SS, Messali M. 2011.
Temperature effect, activation energies and thermodynamic adsorption studies of l-cysteine methyl ester hydrochloride as copper corrosion inhibitor in nitric acid 2M. Int J Electrochem Sci. 6:6261-6274.
14
Lampiran 1 Bagan alir sintesis
Isoamil alkohol + P2S5
ADTP ZnO
Pemisahan Produk
Produk sintesis
Pemanasan dan pengadukan
Pengadukan tanpa pemanasan
Pemisahan dan pencucian
Pencirian dengan FTIR
Uji kinerja korosi (Potensiostat EA160) Penetapan kadar
15 Lampiran 2 Rangkaian alat sintesis
(Sumber: Hayati 2013) Keterangan:
a. campuran pereaksi b. penangas air
16
Lampiran 3 Elektrode Cu, reservoir, dan Potensiostat
Elektrode Cu
Reservoir
17
Lampiran 4 Bobot dan perhitungan sintesis
Sampel Bobot reaktan yang ditimbang (g) Bobot ZDTP (g)
Rendemen (%) P2S5 Alkohol ZnO
Ulangan 1 8.0127 12.7233 2.9313 20.3320 93.54 Ulangan 2 8.0047 12.8043 2.9316 20.2823 93.31
Contoh perhitungan rendemen (Ulangan 1): Mol isoamil alkohol =
Mol produk =
Bobot teoritis ZDTP = mol teoritis Mr ZDTP = 0.036 mol 603.8 g/mol = 21.7368 gram
18
Lampiran 5 Data hasil analisis kadar Zn
Ulangan bobot Konsentrasi Kadar (%)
Zn Rerata kadar (%) Zn hasil percobaan
Kadar (%) Zn teoritis sampel
(g)
terbaca AAS (mg/L)
hasil percobaan
1 0.5129 620.5793 12.08
11.94 10,83
2 0,5187 611.6968 11.79
Contoh perhitungan :
Kadar Zn hasil percobaan (%) × 100%
× 100%
12,08 %
Kadar Zn teoritis (%)
10,83 %
19 Lampiran 6 Data arus korosi
Konsentrasi (%)
Garis Tafel Arus
korosi (mA)
%EI
anode katode
Blanko y=-6.650x+0.039 y=16.82x+0.1167 3.3000 - - 0.5 y=-9.853x+0.037 y=11.923x+0.082 2 39.39 0.39
1 y=-24.662x+0.027 y=47.126x+0.0803 0.7350 77.71 0.77 2 y=-24.678x+0.047 y=92.007x+0.0677 0.1280 96.12 0.96 3 y=-515.13x+0.036 y=367.11x+0.0722 0.0400 98.77 0.98
Perhitungan Ekstrapolasi Tafel 1. Arus blangko
Persamaan garis Tafel anode: y=-6.650x + 0.039 Persamaan garis Tafel katode: y=16.82x + 0.1167 Arus korosi (x) saat terjadi perpotongan (y1= y2)
maka y1= y2
-6.650x + 0.039 = 16.82x + 0.1167 -0.0777 = 10.17x
x = 3.300 mA
2. Efektivitas Inhibisi
=
20
3.
Derajat penutupan permukaan
=
= 0.39
4.
Laju korosi (C
R)
C
R=
C
R=
C
R =C
R = 14.92 mm y-121 Lampiran 7 Data variasi suhu
Larutan Suhu 1000/T I (mA) Ln i i/T Ln (i/T) Blanko 303 3.30 2.9983 1.0980 0.0098 -4.6157
313 3.19 3.6975 1.3076 0.0118 -4.4385 323 3.09 5.6708 1.7353 0.0175 -4.0423 1%
22
RIWAYAT HIDUP
Penulis dilahirkan di Bogor pada tanggal 30 Juni 1993. Penulis sebagai anak dari pasangan Teguh Dwi Santono, SE dan Ninik Martuti merupakan anak pertama dari dua bersaudara. Tahun 2010 penulis lulus dari SMA Negeri 6 Bogor dan pada tahun yang sama diterima di Departemen Kimia, Institut Pertanian Bogor melalui jalur USMI.