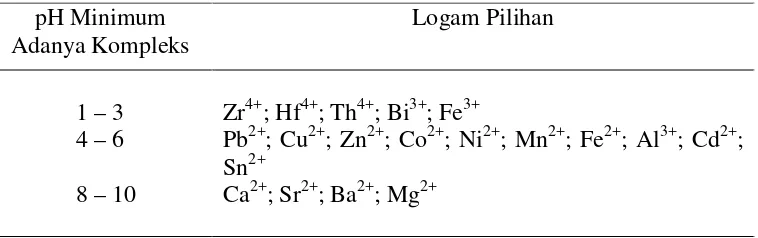PEMERIKSAAN MUTU TABLET KUNYAH ANTASIDA
YANG MENGANDUNG MAGNESIUM HIDROKSIDA
YANG BEREDAR DI APOTEK KOTA MEDAN
SKRIPSI
Diajukan sebagai salah satu syarat untuk memperoleh Gelar Sarjana Farmasi pada Fakultas Farmasi
Universitas Sumatera Utara OLEH:
SYAHRI SEPTIANA NIM 111524063
m
PROGRAM EKSTENSI SARJANA FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
PEMERIKSAAN MUTU TABLET KUNYAH ANTASIDA
YANG MENGANDUNG MAGNESIUM HIDROKSIDA
YANG BEREDAR DI APOTEK KOTA MEDAN
SKRIPSI
Diajukan sebagai salah satu syarat untuk memperoleh Gelar Sarjana Farmasi pada Fakultas Farmasi
Universitas Sumatera Utara OLEH:
SYAHRI SEPTIANA NIM 111524063
m
PROGRAM EKSTENSI SARJANA FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
PENGESAHAN SKRIPSI
PEMERIKSAAN MUTU TABLET KUNYAH ANTASIDA YANG MENGANDUNG MAGNESIUM HIDROKSIDA
YANG BEREDAR DI APOTEK KOTA MEDAN OLEH:
SYAHRI SEPTIANA NIM 111524063
Dipertahankan di Hadapan Panitia Penguji Skripsi Fakultas Farmasi Universitas Sumatera Utara
Pada Tanggal: 6 Februari 2015
Disetujui Oleh :
Pembimbing I, Panitia Penguji:
Drs. Agusmal Dalimunthe, M.S., Apt. Drs. Fathur Rahman Harun. M.Si., Apt. NIP 195406081983031005 NIP 195201041980033002
Pembimbing II, Drs. Agusmal dalimunthe, M.S., Apt.
NIP 195406081983031005
Dra. Sudarmi, M.Si., Apt. Dra. Fat Aminah, M.Sc., Apt. NIP 195409101983032001 NIP 195011171980022001
Dr. Wiryanto, M.S., Apt. NIP 195110251980021001
Medan, April 2015 Fakultas Farmasi
Universitas Sumatera Utara Wakil Dekan I,
i
KATA PENGANTAR
Puji syukur penulis ucapkan kepada Allah SWT atas segala Rahmat dan
KaruniaNya, sehingga penulis dapat menyelesaikan penelitian dan penyusunan
skripsi ini. Skripsi ini disusun untuk melengkapi salah satu syarat mencapai
gelar Sarjana Farmasi pada Fakultas Farmasi Universitas Sumatera Utara,
dengan judul “Pemeriksaan Mutu Tablet Kunyah Antasida Yang Mengandung
Magnesium Hidroksida Yang Beredar Di Apotek Kota Medan”.
Pada kesempatan ini dengan segala kerendahan hati penulis
mengucapkan terima kasih yang sebesar-besarnya kepada Bapak Drs. Agusmal
Dalimunthe, M.S., Apt., dan Ibu Dra. Sudarmi, M.Si., Apt., selaku dosen
pembimbing yang telah membimbing penulis dengan penuh kesabaran dan
tanggung jawab selama penelitian hingga selesainya penulisan skripsi ini,
Bapak Prof. Dr. Sumadio Hadisahputra, Apt., selaku Dekan Fakultas Farmasi
Universitas Sumatera Utara yang telah memberikan fasilitas selama masa
pendidikan, Bapak Dr. Muchlisyam, M.Si., Apt., selaku ketua program studyi
ekstensi farmasi, Bapak Drs. Fathur Rahman Harun, M.Si., Apt., Ibu Dra. Fat
Aminah, M.Sc., Apt., dan Bapak Dr. Wiryanto, M.S., Apt., selaku dosen
penguji yang telah memberikan kritik dan saran yang membangun kepada
penulis dalam penulisan skripsi ini, Ibu Dra. Lely Sari Lubis, M.Si., Apt.,
selaku dosen penasehat akademik yang telah memberikan nasehat dan arahan
yang baik kepada penulis selama masa perkuliahan, Keluarga saya tercinta,
Ayahanda Sumarwan Hutabarat, M. Dori Lubis, Ibunda Halimatussa’diah,
ii
S.Pd, Habibi Nurhayana, Abang Hadi Ismanto, SE, Bachtiar Muhammad, Riza
Pahlevi, SE, Adik Fitri wahyuni Lubis, S.sos., yang telah memberikan cinta
dan kasih sayang yang tidak ternilai dengan apapun, pengorbanan baik materi
maupun motivasi beserta doa yang tulus yang tidak pernah berhenti,
Sahabat-sahabatku Program Farmasi Ekstensi Angkatan 2011, Abang Subhan Ahbar
Lubis, S.farm., Apt., serta seluruh pihak yang telah ikut membantu penulis
namun tidak tercantum namanya terima kasih untuk perhatian, semangat, doa,
dan kebersamaannya selama ini.
Penulis menyadari sepenuhnya bahwa dalam penulisan skripsi ini masih
jauh dari kesempurnaan, oleh karena itu dengan segala kerendahan hati, penulis
menerima kritik dan saran demi kesempurnaan skripsi ini. Akhirnya, penulis
berharap semoga skripsi ini dapat memberi manfaat bagi kita semua.
Medan, April 2015
Penulis,
iii
PEMERIKSAAN MUTU TABLET KUNYAH ANTASIDA YANG MENGANDUNG MAGNESIUM HIDROKSIDA
YANG BEREDAR DI APOTEK KOTA MEDAN
ABSTRAK
Latar belakang: Tablet kunyah merupakan tablet yang banyak beredar di apotek kota Medan pada saat ini, salah satunya digunakan untuk obat antasida, yang dapat membantu untuk mengatasi penyakit maag, dan tablet kunyah antasida dapat diperoleh tanpa resep dokter.
Tujuan: Tujuan dari penelitian ini adalah untuk mengetahui mutu tablet kunyah yang mengandung magnesium hidroksida yang beredar di apotek kota Medan.
Metode: Pemeriksaan mutu tablet ini diambil empat tablet kunyah antasida dari salah satu apotek di kota Medan. Empat tablet kunyah antasida tersebut yaitu Acitral (Interbat), Dexanta (Dexa medica), Magtral (Otto), Mylanta (Bayer Indonesia). Pengujian mutu dilakukan berdasarkan parameter mutu tablet meliputi kekerasan tablet dengan alat strong cobb hardness tester, friabilitas dengan alat friabilator, waktu hancur, dengan alat disintegration tester, keragaman bobot dan penetapan kadar dilakukan secara titrasi kompleksometri.
Hasil: Hasil uji menunjukkan bahwa hasil kekerasan tablet berkisar antara 6,41 s/d 11,07 kg, sedangkan friabilitas diperoleh berkisar antara 0,13 s/d 0,69% dengan waktu hancur berkisar 8,32 menit s/d 12,17 menit, pada uji keragaman bobot berkisar antara 96,38% s/d 99,27% dan pada penetapan kadar yang diperoleh berkisar antara 96,4% s/d 99,42%.
Kesimpulan: Berdasarkan hasil penelitian dapat disimpulkan bahwa seluruh tablet kunyah antasida yang mengandung magnesium hidroksida yang beredar di apotek kota Medan yang diuji berdasarkan kekerasan, friabilitas, waktu hancur, keragaman bobot dan penetapan kadar memenuhi persyaratan.
iv
QUALITY CONTROL OF CHEWING ANTACID TABLETS CONTAINING MAGNESIUM HIDROXIDA WHICH
CIRCULATEIN DRUGSTORE OF MEDAN CITY
ABSTRACT
Background: Chewing tablets are tablets that many circulating in drugstore of Medan city at this time, which can help for gastric pains, and chewing antacid tablets easily obtained without a doctor’s prescription..
Objective: The purpose of this study was to know the quality of chewing antacid tablets containing magnesium hidroxida which circulate in drugstore of Medan city.
Methods: This quality control of chewing tablets taken four chewing antacid tablets from one of the drugstore in Medan city, four chewing antacid tablets that were Acitral (Interbat), Dexanta (Dexa medika), Magtral (Otto), Mylanta (Bayer Indonesia). The quality control of chewing antacid tablets tested by standart tablet quality covered tablet hardness by using device strong cobb hardness tester, Friability by using device Friabilator, disintegration time by using device Disintegration tester, diversity weights and assay tested by titration of complexometri.
Results: The test results showed that the tablet hardness results ranged from 6.41 to 11.07 kg, while friability obtained ranged between 0.13 to 0.69% with a disintegration time ranged between 8.32 minuts to 12.17 minuts, diversity weights results ranged from 96.38% to 99.27%, and the essay was obtained ranged between 96.4% to 99.42%.
Conclusion: Based on the result of this study concluded that the entire chewing antacid tablets containing magnesium hidroxide which circulate in drugstore of Medan city were tested include : hardness test, friability, disintegration time , diversity weight and assay qualified.
v DAFTAR ISI
Halaman
JUDUL ... i
HALAMAN JUDUL ... ii
KATA PENGANTAR ... iii
ABSTRACT ... iv
DAFTAR ISI ... vi
DAFTAR TABEL ... vii
DAFTAR GAMBAR ... xii
DAFTAR LAMPIRAN ... xiii
BAB I PENDAHULUAN ... 1
1.1 Latar belakang ... 1
1.2 Perumusan masalah ... 2
1.3 Hipotesa ... 3
1.4 Tujuan penelitian ... 3
1.5 Manfaat penelitian ... 3
BAB II TINJAUAN PUSTAKA ... 4
2.1 Tablet ... 4
2.2 Antasida ... 4
2.2.1 Penggolongan sediaan ... 5
2.2.2 Sediaan antasida ... 5
vi
2.3.1 Uji kekerasan tablet ... 6
2.3.2 Uji kerapuhan tablet ... 6
2.3.3 Uji waktu hancur ... 6
2.3.4 Uji keragaman bobot ... 7
2.3.5 Uji kadar magnesium hidroksida ... 7
2.4 Magnesium hidroksida ... 8
2.4.1 Teori kompleksometri ... 8
2.4.2 Metode kompleksometri ... 11
2.4.3 Indikator ion logam ... 13
BAB III METODE PENELITIAN ... 15
3.1 Waktu dan tempat penelitian ... 15
3.2 Alat ... 15
3.3 Bahan ... 15
3.4 Pengambilan sampel ... 16
3.5 Pembuatan pereaksi ... 16
3.5.1 Pembakuan Na2EDTA ... 16
3.5.2 Larutan ZnSO4 7H2O 0,05 M(BM=287,54) ... 17
3.5.3 Larutan Na2EDTA 0,05 M (BM=372,24) ... 16
3.5.4 Buffer salmiak / ammonia pH 10 ... 17
3.5.5 HCl 2 N ... 17
3.5.6 Indikator Hitam Eriokhrom ... 17
3.5.7 NaOH 1 N ... 17
vii
3.6.1 Uji kekerasan tablet ... 18
3.6.2 Uji kerapuhan tablet ... 18
3.6.3 Uji waktu hancur ... 18
3.6.4 Uji keragaman bobot ... 19
3.6.5 Uji kadar magnesium hidroksida ... 19
3.7 Analisis data secara statistik ... 20
BAB IV HASIL DAN PEMBAHASAN ... 22
4.1 Hasil uji kekerasan tablet ... 22
4.2 Hasil uji friabilitas tablet ... 23
4.3 Hasil uji waktu hancur tablet ... 24
4.4 Hasil uji keragaman bobot tablet ... 25
4.5 Hasil kadar magnesium hidroksida ... 27
BAB V KESIMPULAN DAN SARAN ... 29
5.1 Kesimpulan ... 29
5.2 Saran ... 29
DAFTAR PUSTAKA ... 30
viii
DAFTAR TABEL
Halaman
Tabel 4.1 Hasil uji kekerasan tablet ... 22
Tabel 4.2 Hasil uji friabilitas tablet ... 23
Tabel 4.3 Hasil uji waktu hancur tablet ... 24
Tabel 4.4 Hasil uji keragaman bobot ... 26
ix
DAFTAR GAMBAR
Halaman
Gambar 4.1 Diagram tabel uji kekerasan tablet ... 23
Gambar 4.2 Diagram tabel uji friabilas tablet ... 24
Gambar 4.3 Diagram tabel uji waktu hancur tablet ... 25
Gambar 4.4 Diagram tabel uji keragaman bobot tablet ... 26
x
DAFTAR LAMPIRAN
Halaman
Lampiran 1. Contoh perhitungan data pengambilan sampel ... 32
Lampiran 2. Hasil uji kekerasan tablet ... 35
Lampiran 3. Hasil uji friabilitas tablet ... 36
Lampiran 4. Hasil uji waktu hancur tablet ... 37
Lampiran 5. Hasil uji keragaman bobot ... 38
Lampiran 6. Perhitungan keragaman bobot tablet acitral ... 39
Lampiran 7. Perhitungan keragaman bobot tablet dexanta ... 42
Lampiran 8. Perhitungan keragaman bobot tablet magtral ... 45
Lampiran 9. Perhitungan keragaman bobot tablet mylanta ... 48
Lampiran 10. Data kadar magnesium hidroksida ... 51
Lampiran 11. Perhitungan penetapan kadar tablet acitral ... 53
Lampiran 12. Perhitungan peneapan kadar tablet dexanta ... 57
Lampiran 13. Perhitungan penetapan kadar tablet magtral ... 61
Lampiran 14. Perhitungan penetapan kadar tablet mylanta ... 65
Lampiran 15. Daftar spesifikasi sampel ... 69
Lampiran 16. Gambar alat Disentagration Tester (Erweka) ... 71
Lampiran 17. Gambar alat Strong Cobb Hardness Tester (Erweka) ... 72
Lampiran 18. Gambar alat Friabilator (Roche) ... 73
Lampiran 19. Gambar Buret ... 74
Lampiran 20. Gambar hasil pembakuan ... 75
iii
PEMERIKSAAN MUTU TABLET KUNYAH ANTASIDA YANG MENGANDUNG MAGNESIUM HIDROKSIDA
YANG BEREDAR DI APOTEK KOTA MEDAN
ABSTRAK
Latar belakang: Tablet kunyah merupakan tablet yang banyak beredar di apotek kota Medan pada saat ini, salah satunya digunakan untuk obat antasida, yang dapat membantu untuk mengatasi penyakit maag, dan tablet kunyah antasida dapat diperoleh tanpa resep dokter.
Tujuan: Tujuan dari penelitian ini adalah untuk mengetahui mutu tablet kunyah yang mengandung magnesium hidroksida yang beredar di apotek kota Medan.
Metode: Pemeriksaan mutu tablet ini diambil empat tablet kunyah antasida dari salah satu apotek di kota Medan. Empat tablet kunyah antasida tersebut yaitu Acitral (Interbat), Dexanta (Dexa medica), Magtral (Otto), Mylanta (Bayer Indonesia). Pengujian mutu dilakukan berdasarkan parameter mutu tablet meliputi kekerasan tablet dengan alat strong cobb hardness tester, friabilitas dengan alat friabilator, waktu hancur, dengan alat disintegration tester, keragaman bobot dan penetapan kadar dilakukan secara titrasi kompleksometri.
Hasil: Hasil uji menunjukkan bahwa hasil kekerasan tablet berkisar antara 6,41 s/d 11,07 kg, sedangkan friabilitas diperoleh berkisar antara 0,13 s/d 0,69% dengan waktu hancur berkisar 8,32 menit s/d 12,17 menit, pada uji keragaman bobot berkisar antara 96,38% s/d 99,27% dan pada penetapan kadar yang diperoleh berkisar antara 96,4% s/d 99,42%.
Kesimpulan: Berdasarkan hasil penelitian dapat disimpulkan bahwa seluruh tablet kunyah antasida yang mengandung magnesium hidroksida yang beredar di apotek kota Medan yang diuji berdasarkan kekerasan, friabilitas, waktu hancur, keragaman bobot dan penetapan kadar memenuhi persyaratan.
iv
QUALITY CONTROL OF CHEWING ANTACID TABLETS CONTAINING MAGNESIUM HIDROXIDA WHICH
CIRCULATEIN DRUGSTORE OF MEDAN CITY
ABSTRACT
Background: Chewing tablets are tablets that many circulating in drugstore of Medan city at this time, which can help for gastric pains, and chewing antacid tablets easily obtained without a doctor’s prescription..
Objective: The purpose of this study was to know the quality of chewing antacid tablets containing magnesium hidroxida which circulate in drugstore of Medan city.
Methods: This quality control of chewing tablets taken four chewing antacid tablets from one of the drugstore in Medan city, four chewing antacid tablets that were Acitral (Interbat), Dexanta (Dexa medika), Magtral (Otto), Mylanta (Bayer Indonesia). The quality control of chewing antacid tablets tested by standart tablet quality covered tablet hardness by using device strong cobb hardness tester, Friability by using device Friabilator, disintegration time by using device Disintegration tester, diversity weights and assay tested by titration of complexometri.
Results: The test results showed that the tablet hardness results ranged from 6.41 to 11.07 kg, while friability obtained ranged between 0.13 to 0.69% with a disintegration time ranged between 8.32 minuts to 12.17 minuts, diversity weights results ranged from 96.38% to 99.27%, and the essay was obtained ranged between 96.4% to 99.42%.
Conclusion: Based on the result of this study concluded that the entire chewing antacid tablets containing magnesium hidroxide which circulate in drugstore of Medan city were tested include : hardness test, friability, disintegration time , diversity weight and assay qualified.
1
BAB I
PENDAHULUAN
1.1Latar Belakang
Tablet kunyah merupakan tablet yang banyak beredar di apotek kota
Medan pada saat ini. Tablet kunyah merupakan tablet untuk dikunyah dan
memberikan rasa yang enak dalam rongga mulut, mudah ditelan dan tidak
meninggalkan rasa pahit. Salah satu pembuatan tablet kunyah ini digunakan
untuk obat antasida (Ditjen POM, 1995).
Menurut Keputusan Menteri Kesehatan RI Nomor 2500/MENKES/SK/XII/
2011 tentang Daftar Obat Esensial Nasional (DOEN) menyatakan bahwa obat
antasida masih termasuk dalam daftar obat esensial nasional karena dinilai
masih sangat efektif dan aman untuk penyakit maag serta harganya terjangkau,
sehingga hal ini menjadi perhatian bagi para produsen obat untuk memproduksi
obat antasida dengan merek dagang (Tampubolon, 1990).
Antasida adalah obat yang menetralkan asam lambung sehingga berguna
untuk menghilangkan nyeri tukak peptik. Antasida tidak mengurangi volume
HCl yang dikeluarkan lambung, tetapi peninggian pH akan menurunkan
aktivitas pepsin. Beberapa antasida, misalnya magnesium hidroksida diduga
menghambat pepsin secara langsung. Kapasitas menetralkan asam dari
berbagai antasida pada dosis terapi bervariasi, tetapi umumnya pH lambung
2
Magnesium hidroksida merupakan salah satu golongan antasida yang
dapat membantu dalam mengatasi penyakit maag. Berdasarkan riset Brain dan
Co bahwa 5 dari 10 pekerja di Indonesia khususnya di kota Medan mengalami
penyakit maag dan jumlah penderita penyakit maag tiap tahunnya mengalami
peningkatan (Anief, 1991).
Magnesium hidroksida yang digunakan sebagai antasida ini praktis tidak
larut dan tidak efektif sebelum obat ini bereaksi dengan HCl. Magnesium
hidroksida yang tidak bereaksi akan tetap berada dalam lambung dan akan
menetralkan HCl yang disekresi belakangan sehingga masa kerjanya lama.
Oleh karena itu Magnesium hidroksida banyak digunakan dalam sediaan
terhadap gangguan lambung (Tjay dan Kirana, 2007).
Berdasarkan uraian di atas, maka Penulis tertarik untuk memeriksa mutu
tablet kunyah antasida yang mengandung magnesium hidroksida yang beredar
di apotek kota Medan dengan melakukan pembuktian dari segi uji keragaman
bobot, uji friabilitas, uji kekerasan, waktu hancur dan penetapan kadar zat
berkhasiat.
1.2Perumusan Masalah
Apakah mutu tablet kunyah antasida yang mengandung Magnesium
hidroksida yang beredar di apotek kota Medan memenuhi persyaratan mutu
yang meliputi kekerasan tablet (Soekemi, 1987), friabilitas (Voigt, 1994),
waktu hancur dan keragaman bobot (Ditjen POM, 1995), dan penetapan kadar
3 1.3 Hipotesa
Tablet kunyah antasida yang mengandung Magnesium hidroksida yang
beredar di apotek kota Medan memenuhi persyaratan mutu meliputi kekerasan
tablet (Soekemi, 1987), friabilitas (Voigt, 1994), waktu hancur dan keragaman
bobot (Ditjen POM, 1995), dan penetapan kadar (USP, 2009).
1.4 Tujuan Penelitian
Untuk mengetahui mutu dari tablet kunyah antasida yang mengandung
Magnesium hidroksida yang beredar di apotek kota Medan meliputi kekerasan
tablet(Soekemi, 1987), friabilitas (Voigt, 1994), waktu hancur dan keragaman
bobot (Ditjen POM 1995), dan penetapan kadar (USP, 2009).
1.5Manfaat Penelitian
Penelitian ini diharapkan dapat bermanfaat untuk memberikan
informasi kepada masyarakat dan instansi terkait, terutama bagi pelayanan
kesehatan mengenai mutu tablet kunyah antasida yang mengandung
4 BAB II
TINJAUAN PUSTAKA
2.1 Tablet
Tablet adalah sediaan padat mengandung bahan obat dengan atau tanpa
bahan pengisi. Berdasarkan metode pembuatan, dapat digolongkan sebagai
tablet cetak dan tablet kempa. Selain bahan pengisi digunakan juga zat
tambahan lain yang berfungsi sebagai bahan tambahan, pengikat, pelicin,
pembasah atau zat lain yang cocok (Ditjen POM, 1995).
Tablet kunyah dimaksudkan untuk dikunyah memberikan rasa yang
enak dalam rongga mulut, mudah ditelan dan tidak meninggalkan rasa pahit
atau tidak enak. Jenis tablet ini digunakan dalam formulasi tablet untuk anak,
terutama formulasi multivitamin, antasida dan antibiotik tertentu. Tablet
kunyah dibuat dengan cara dikempa, umumnya menggunakan manithol,
sorbitol atau sukrosa sebagai bahan pengikat dan bahan pengisi, mengandung
bahan pewarna dan bahan pengaroma untuk meningkatkan penampilan dan
rasa (Ditjen POM, 1995).
2.2 Antasida
Antasida adalah obat yang menetralkan asam lambung sehingga berguna
untuk menghilangkan nyeri tukak peptik. Antasida tidak mengurangi volume
HCl yang dikeluarkan lambung, tetapi peninggian pH akan menurunkan
5
menghambat pepsin secara langsung. Kapasitas menetralkan asam dari
berbagai antasida pada dosis terapi bervariasi, tetapi umumnya pH lambung
tidak sampai diatas 4 (Estuningtyas dan Arif, 2007).
2.2.1 Penggolongan antasida
Antasida dibagi dalam 2 golongan yaitu antasida sistemik dan antasida
nonsistemik. Antasida sistemik, misalnya natrium bikarbonat, diabsorpsi dalam
usus halus sehingga menyebabkan urin bersifat alkalis. Pada pasien dengan
kelainan ginjal dapat terjadi alkalosis metabolik (Estuningtyas dan Arif, 2007).
Antasida nonsistemik hampir tidak diabsorpsi dalam usus sehingga tidak
menimbulkan alkalosis metabolik. Contoh antasida nonsistemik adalah sediaan
magnesium, aluminium, dan kalsium (Estuningtyas dan Arif, 2007).
2.2.2 Sediaan antasida
Antasida tersedia dalam sediaan sirup maupun tablet, antasida juga
tersedia sebagai obat generik maupun obat paten (Anief, 1991).
Kandungan dari sediaan antasida yaitu: kandungan aluminium dan
magnesium, kandungan natrium bikarbonat, serta kandungan kalsium karbonat.
Simeticone diberikan sendiri atau ditambahkan pada antasida sebagai anti buih
untuk meringankan kembung (flatulen) (Sukandar, dkk., 2008).
2.3 Pemeriksaa Mutu Tablet
Pemeriksaan mutu tablet dilakukan dengan uji kekerasan tablet,
6
2.3.1 Uji kekerasan tablet
Masing-masing sediaan diletakkan pada tempat yang tersedia pada alat
Hardness tester (Coplay) dengan posisi tidur, alat diatur, kemudian ditekan
tombol start, pada saat sediaan pecah dicatat angka yang tertera pada layar
digital.
Syarat : Kekerasan tablet secara umum 4 s/d 8 dan 7 s/d 12 untuk tablet kunyah
(Soekemi, 1987).
2.3.2 Uji kerapuhan tablet
Alat : Friabilator (Roche)
Cara : ditimbang 20 tablet yang dibersihkan dari debu, dicatat beratnya (a
gram), dimasukkan ke dalam alat, lalu alat dijalankan selama 4 menit (100
kaliputaran), setelah batas waktu yang ditentukan, tablet dikeluarkan dan
dibersihkan dari debu, lalu ditimbang lagi (b gram), maka friabilitas (F)= (a-b)/
a x 100%
Syarat : Kehilangan berat ≤ 0,8% (Voigt, 1994).
2.3.3 Waktu hancur
Alat : Disintegration Tester ( Erweka).
Cara : Dilakukan pada 6 tablet. Dimasukkan 1 tablet pada masing-masing
tabung darikeranjang, dimasukkan 1 cakram pada tiap tabung. Digunakan air
bersuhu ± 370 sebagai media kemudian alat dijalankan. Waktu hancur tablet
dicatat yaitu sejak tablet dinaik turunkan sampai tablet hancur. Tablet
7
Persyaratan : Menurut Farmakope Indonesia edisi III tahun 1979 tablet
memenuhi syarat jika waktu hancur tablet tidak lebih dari 15 menit. Bila 1
tablet atau 2 tablet tidak hancur sempurna ulangi pengujian dengan 12 tablet
lainnya : tidak kurang 16 tablet dari 18 tablet yang di uji harus hancur semua
(Ditjen POM, 1995).
2.3.4 Uji kergaman bobot
Menurut Farmakope Indonesia edisi IV bahwa kadar zat aktif 50 mg
atau lebih besar dari 50 mg yang merupakan 50% atau lebih dari bobot satuan
sediaan, maka uji keseragaman sediaan dilakukan dengan cara keragaman
bobot.
Cara : Pilih tidak kurang dari 30 tablet dan timbang seksama 10 tablet, satu
persatu dan dihitung bobot rata-rata kemudian ditentukan kadarnya. Dari hasil
penetapan kadar dihitung jumlah zat aktif dari masing-masing 10 tablet dengan
anggapan zat aktif terdistribusi homogen (Ditjen POM, 1995).
2.3.5 Uji kadar magnesium hidroksida
Menurut USP Vol III tahun 2009, timbang seksama 20 tablet sampel,
gerus, timbang serbuk setara dengan 75 mg magnesium hidroksida,
dimasukkan kedalam erlenmeyer, ditambahkan 2 ml asam klorida 2 N,
ditambahkan 100 ml air, ditambahkan natrium hidroksida 1 N , cek pH hingga
mencapai 10 dengan menggunakan indikator universal, ditambahkan 5 ml
ammonium klorida dan 50 mg indikator eriochrom black dan titrasi dengan
dinatrium EDTA 0,05 M hingga terjadi warna biru.
8
2.4 Magnesium Hidroksida
Rumus Molekul : Mg(OH)2
Berat Molekul : 78,00
Magnesium hidroksida yang telah dikeringkan pada suhu 1050 selama 2 jam
mengandung tidak kurang dari 95,0% dan tidak lebih dari 100,5% Mg(OH)2
(Ditjen POM, 1995).
2.4.1. Teori kompleksometri
Reaksi pembentukan kompleks dianggap sebagai reaksi asam-basa Lewis
dengan ligan bekerja sebagai basa dengan memberikan sepasang elektron
kepada kation yang merupakan suatu asam (Day dan Underwood, 1981).
Ligan dari kata Latin ligare, yang berarti “mengikat”. Atom pada ligan
yang memberikan pasangan elektron pada ion logam dinamakan atom donor
sedangkan ion logamnya disebut akseptor. Ligan dalam kompleks dapat berupa
anion atau molekul netral yang mengandung sebuah atom atau lebih dengan
paling sedikit mempunyai sepasang elektron yang dapat diberikan pada ion
logam (Brady, 1999).
Ligan diklasifikasikan atas dasar banyaknya titik lekat kepada ion logam.
Ligan monodentat, yaitu ligan itu terikat pada ion logam hanya pada satu titik
oleh penyumbangan satu pasangan elektron menyendiri kepada logam. Ligan
multidentat mengandung lebih dari dua atom koordinasi per molekul, misalnya
asam 1,2-diaminoetanatetraasetat (EDTA) yang mempunyai dua atom nitrogen
penyumbang dan empat atom oksigen penyumbang dalam molekul yang
9
Schwarzenbach menyatakan bahwa ion asetat mampu membentuk
kompleks-kompleks asetat yang rendah kestabilannya dengan hampir semua
kation polivalen dan sifat ini diperkuat dengan efek sepit, maka
kompleks-kompleks yang jauh lebih kuat akan terbentuk oleh kation ion logam. Ia
menemukan asam-asam aminopolikarboksilat merupakan zat-zat
pengkompleks yang baik (Basset, dkk., 1991).
Berbagai nama trivial (nama khusus) digunakan untuk asam
etilenadiaminatetraasetat dan garam natriumnya meliputi: Trilon B,
Komplekson III, Sekuestrena, Versena, dan Khelaton 3 (Basset, dkk., 1991).
EDTA mendapat aplikasi umum yang paling luas dalam analisis karena
aksi mengkompleksnya yang sangat kuat dan tersedia secara komersial (Basset,
dkk., 1991). Dalam perdagangan yang sering digunakan bentuk garamnya yaitu
dinatrium edetat dengan struktur kimia dibawah ini.
Struktur ruang anionnya yang mempunyai enam atom penyumbang
memungkinkan untuk memenuhi bilangan koordinasi enam yang sering
dijumpai diantara ion-ion logam. Kompleks-kompleks yang dihasilkan
10
yang dibawa. Satu struktur kompleks dengan suatu ion divalen dapat dilihat
pada gambar berikut ini.
CO CH2
O CH2
CO
(Basset, dkk., 1991).
Untuk menyerdehanakan pembahasan berikut, EDTA diberi rumus H4Y;
maka garam dinatriumnya adalah Na2H2Y, dan memberi ion pembentuk
kompleks H4Y2- dalam larutan air; ia bereaksi dengan semua logam dalam
rasio 1:1. Reaksi dengan kation dapat ditulis sebagai:
M2+ + H2Y2-↔ MY2- + 2H+ (1)
M3+ + H2Y2-↔ MY- + 2H+ (2)
M4+ + H2Y2-↔ MY + 2H+ (3)
Rumus Umum: Mn+ + H2Y2-↔ (MY)(n-4)+ + 2H+ (4) (Basset, dkk., 1991).
Dalam semua kasus satu mol H2Y2- yang membentuk kompleks akan
bereaksi dengan satu mol ion logam, dan selalu terbentuk dua mol ion
hidrogen. Nampak dari persamaan (4) bahwa disosiasi kompleks akan
ditentukan oleh pH larutan; menurunkan pH akan mengurangi kestabilan
11
mana suatu titrasi EDTA dari ion logam bersangkutan dapat dilaksanakan
(Basset, dkk., 1991).
Tabel di bawah ini menunjukkan nilai pH minimum untuk eksistensi
kompleks EDTA dari beberapa logam pilihan.
pH Minimum Adanya Kompleks
Logam Pilihan
1 – 3 4 – 6
8 – 10
Zr4+; Hf4+; Th4+; Bi3+; Fe3+
Pb2+; Cu2+; Zn2+; Co2+; Ni2+; Mn2+; Fe2+; Al3+; Cd2+; Sn2+
Ca2+; Sr2+; Ba2+; Mg2+
Jadi terlihat bahwa pada umumnya kompleks EDTA dengan ion logam
divalen stabil dalam larutan basa atau sedikit asam, sementara kompleks
dengan ion logam tri dan tetravalen terjadi dalam larutan-larutan dengan
keasaman yang jauh lebih tinggi (Basset, dkk., 1991).
2.4.2 Metode kompleksometri 1. Titrasi langsung
Larutan yang mengandung ion logam yang akan ditetapkan, dibuferkan
sampai pH yang dikehendaki dan titrasi langsung dengan larutan baku EDTA.
Untuk mencegah pengendapan hidroksida logam (garam basa) dengan
menambahkan sedikit zat pengkompleks pembantu seperti tartrat atau sitrat
atau trietanolamina. Pada titik ekuivalen, besarnya konsentrasi ion logam yang
sedang ditetapkan turun mendadak. Ini umumnya ditetapkan dari perubahan
12 2. Titrasi balik (Tidak Langsung)
Karena berbagai alasan, banyak logam tak dapat dititrasi langsung;
mungkin mengendap dari dalam larutan dalam jangkau pH yang perlu untuk
dititrasi, atau mungkin membentuk kompleks-kompleks yang inert, atau
indikator logam yang sesuai tidak tersedia. Dalam hal ini ditambahkan larutan
baku EDTA berlebih, kemudian larutan di buffer pada pH yang diinginkan, dan
kelebihan pereaksi dititrasi kembali dengan larutan baku ion logam; yaitu
larutan ZnCl2 / ZnSO4 atau MgCl2 / MgSO4. Titik akhir titrasi dideteksi dengan
bantuan indikator logam yang memberi respon terhadap ion logam yang
terdapat dalam titrasi kembali (Basset, dkk., 1991).
3. Titrasi penggantian (Substitusi)
Titrasi substitusi dapat digunakan untuk ion logam yang tidak bereaksi
(bereaksi dengan tak memuaskan) dengan indikator logam, atau untuk ion
logam yang membentuk kompleks EDTA yang lebih stabil dari pada kompleks
EDTA dari logam-logam lainya seperti magnesium dan kalsium. Kation logam
Mn+ yang akan ditetapkan dapat diolah dengan kompleks magnesium EDTA,
pada mana reaksi berikut terjadi:
Mn+ + MgY2-↔ (MY)(n-4)+ + Mg2+
Jumlah ion magnesium yang dibebaskan ekuivalen dengan kation-kation
yang berada disitu, dapat dititrasi dengan suatu larutan baku EDTA dan
13 4. Titrasi alkalimetri
Bila suatu larutan dinatrium etilenadiaminatetraasetat (Na2H2Y), ditambahkan
pada larutan yang mengandung ion-ion logam, terbentuklah
kompleks-kompleks dengan disertai pembebasan dua ekuivalen ion hidrogen:
Mn+ + H2Y2-↔ (MY)(n-4)+ + 2H+
Ion hidrogen yang dibebaskan dapat dititrasi dengan larutan baku natrium
hidroksida dengan menggunakan indikator asam-basa. Pilihan lain, suatu
campuran iodat-iodida ditambahkan disamping larutan EDTA, dan iod yang
dibebaskan dititrasi dengan larutan baku tiosulfat. Larutan logam yang akan
ditetapkan harus dinetralkan dengan tepat sebelum dititrasi; ini hal yang sukar
yang disebabkan oleh hidrolisis banyak garam, dan merupakan segi lemah dari
titrasi alkalimetri (Basset, dkk., 1991).
2.4.3 Indikator ion logam
Keberhasilan suatu titrasi EDTA bergantung pada penetapan titik akhir
secara cermat. Persyaratan bagi sebuah indikator ion logam untuk digunakan
pada pendeteksian visual dari titik-titik akhir meliputi:
1. Reaksi warna harus sedemikian sehingga sebelum titik akhir, bila hampir
semua ion logam telah berkompleks dengan EDTA, larutan akan berwarna
jelas.
2. Reaksi warna itu haruslah spesifik (khusus), atau sedikitnya selektif.
3. Kompleks indikator-logam harus memiliki kestabilan yang cukup, jika
tidak, tak akan diperoleh perubahan warna yang tajam. Namun kompleks
14
untuk menjamin pada titik-akhir, EDTA melepaskan ion-ion logam dari
kompleks indikator-logam. Perubahan dalam kesetimbangan dari kompleks
indikator-logam ke kompleks logam-EDTA harus tajam dan cepat.
4. Warna yang kontras antara indikator bebas dan kompleks indikator-logam
harus sedemikian sehingga mudah diamati.
5. Indikator harus sangat peka terhadap ion logam sehingga perubahan warna
terjadi sedekat mungkin dengan titik ekuivalen.
6. Persyaratan diatas harus dipenuhi dalam jangkau pH pada mana titrasi
15
BAB III
METODE PENELITIAN
3.1 Waktu dan Tempat penelitian
Penelitian dilakukan di Laboraturium Teknologi Sediaan Farmasi II
fakultas Farmasi USU dari bulan Juni 2013 - September 2013, dan di
Laboraturium Kimia Farmasi Kuantitatif Fakultas Farmasi USU dari bulan
September 2013- Desember 2013.
3.2 Alat
Alat yang digunakan dalam penelitian ini adalah neraca listrik (Dj-
Series), timbangan, anak timbangan, mortir, stamfer, Roche Friabilator
(Copley), Hardness Tester (Copley), Disintegratin Tester (Erweka), buret,
statif dan klem, kertas indikator universal dan alat- alat gelas laboratorium.
3.3 Bahan
Asam klorida 2N, Natrium hidroksida 1N, Ammonium chlorida,
dinatrium etilendiaminatetraasetat P, zink sulfat LV, indikator eriochrom
black,. Sampel yang digunakan adalah Tablet Acitral (PT. Interbat), Tablet
Dexanta (PT. Dexa Medica), Magtral (PT. Otto), Mylanta (PT. Bayer
16 3.4 Pengambilan Sampel
Metode pengambilan sampel yang digunakan adalah secara simple
random sampling dengan rumus n +1 yaitu sampel yang terpilih diambil
dari akar jumlah sampel + 1 dari tiap populasi dengan maksud untuk
memperkecil jumlah sampel namun masih mewakili populasi. Adapun batasan
sampel merek dagang tablet antasida yang mengandung alumunium hidroksida,
magnesium hidroksida, dan simeticone yang beredar di kota Medan dengan
anggapan sampel homogen dari masing – masing industri obat untuk tiap
daerah di kota Medan berdasarkan literatur ISO (Informasi Spesialite Obat
Indonesia) volume 47, 2012 - 2013. Sampel diambil dari apotek Samudra 2 Jl.
Kapten muslim No 55 Medan, Dikatakan simple random sampling karena
pengambilan anggota sampel dari populasi dilakukan secara acak tanpa
memperhatikan strata yang ada dalam populasi itu. Cara demikian dilakukan
bila anggota populasi dianggap homogen. (Sugiyono, 2010).
3.5 Pembuatan Pereaksi 3.5.1 Pembakuan Na2EDTA
Dipipet 10 ml larutan dinatrium etilen diaminatetraasetat 0,05 M
tambahkan 3 ml larutan dapar ammonium klorida pH 10 dan 50 mg hitam
eriokrom T. Titrasi dengan larutan baku Zink sulfat 0,05 M sampai terjadi
17
3.5.2 Larutan ZnSO4 7H2O 0,05 M (BM=287,54)
Ditimbang seksama 0,7188 g ZnSO4, dimasukkan kedalam labu
tentukur 50 ml, larutkan dengan aquadest, kocok lalu tambahkan lagi aquadest
sampai 50 ml (Ditjen POM, 1995).
3.5.3 Larutan Na2EDTA 0,05 M (BM=372,24)
Larutkan 18,6 g dinatrium edetat P dalam air suling hingga 1000 ml
(Ditjen POM, 1995).
3.5.4 Buffer salmiak / ammonia pH 10
Ditimbang 17,5 g NH4Cl tambahkan NH4OH 25% sebanyak 15 ml,
encerkan dengan air sampai 35 ml, aduk dan tambahkan lagi NH4OH sampai
pH 10, encerkan dengan aquadest sampai 50 ml (Ditjen POM, 1995).
3.5.5 HCl 2N
Diambil 14,6 ml HCl p masukkan kedalam beaker gelas yang telah
dikalibrasi, encerkan dengan aquadest sampai 200 ml (Ditjen POM, 1995).
3.5.6 Indikator hitam eriokhrom
Dalam 5 g campuran EBT terdapat 50 mg EBT dan 4950 mg NaCl
anhidrat, diambil 50 mg campuran EBT untuk setiap titrasi (Ditjen POM,
1995).
3.5.7 NaOH 1 N
Dilarutkan 5 g NaOH dalam air bebas CO2 sampai 250 ml (Ditjen
18 3.6 Evaluasi Tablet
3.6.1 Uji kekerasan tablet
Masing-masing sediaan diletakkan pada tempat yang tersedia pada alat
Hardness tester (Coplay) dengan posisi tidur, alat diatur, kemudian ditekan
tombol start, pada saat sediaan pecah dicatat angka yang tertera pada layar
digital.
Syarat : Kekerasan tablet secara umum 4 s/d 8 dan 7 s/d 12 untuk tablet kunyah
(Soekemi, 1987).
3.6.2 Uji kerapuhan tablet Alat : Friabilator (Roche)
Cara: Ditimbang 20 tablet yang dibersihkan dari debu, dicatat beratnya (a
gram), dimasukkan ke dalam alat, lalu alat di jalankan selama 4 menit (100 kali
putaran), setelah batas waktu yang ditentukan tablet dikeluarkan dan
dibersihkan dari debu, lalu ditimbang lagi (b gram), maka friabilitas (F)= (a-b)/
a x 100%
Syarat : Kehilangan berat ≤ 0,8%. (Voigt, 1994).
3.6.3 Waktu hancur
Alat: Disintegration Tester (Erweka).
Cara : Dilakukan pada 6 tablet. Dimasukkan 1 tablet pada masing-masing
tabung dari keranjang, dimasukkan 1 cakram pada tiap tabung. Digunakan air
bersuhu ± 370 sebagai media kemudian alat dijalankan. Waktu hancur tablet
dicatat yaitu sejak tablet dinaik turunkan sampai tablet hancur. Tablet
19
Persyaratan : Menurut Farmakope Indonesia edisi III tahun 1979 tablet
memenuhi syarat jika waktu hancur tablet tidak lebih dari 15 menit. Bila 1
tablet atau 2 tablet tidak hancur sempurna ulangi pengujian dengan 12 tablet
lainnya : tidak kurang 16 tablet dari 18 tablet yang di uji harus hancur semua
(Ditjen POM, 1995).
3.6.4 Uji keragaman bobot
Menurut Farmakope Indonesia edisi IV bahwa kadar zat aktif 50 mg atau
lebih besar dari 50 mg yang merupakan 50% atau lebih dari bobot satuan
sediaan, maka uji keseragaman sediaan dilakukan dengan cara keragaman
bobot.
Cara: Pilih tidak kurang dari 30 tablet dan timbang seksama 10 tablet, satu
persatu dan dihitung bobot rata rata kemudian ditentukan kadarnya. Dari hasil
penetapan kadar dihitung jumlah zat aktif dari masing-masing 10 tablet dengan
anggapan zat aktif terdistribusi homogen (Ditjen POM, 1995).
3.6.5 Uji kadar magnesium hidroksida
Menurut USP Vol III tahun 2009, timbang seksama 20 tablet sampel,
gerus, timbang serbuk setara dengan 75 mg magnesium hidroksida.
Dimasukkan kedalam erlenmeyer, ditambahkan 2 ml asam klorida 2 N,
ditambahkan 100 ml air, ditambahkan natrium hidroksida 1N cek pH hingga
mencapai 10 dengan menggunakan indikator eriochrom black dan titrasi
dengan dinatrium EDTA 0,05 M hingga terjadi warna biru.
20
3.7 Analisis Data Secara Statistik
Untuk mengetahui diterima atau ditolaknya data penelitian, maka data
yang diperoleh dianalisis secara statistik dengan uji t. Menurut Day dan
Underwood (1981), pada interval kepercayaan 95% dengan nilai α = 0,05,
maka data diterima jika t hitung < t tabel.
Untuk mencari t hitung digunakan rumus:
t
hitung = n = Jumlah pengulangan x = Kadar rata–rata sampelUntuk mencari SD (Standar Deviasi) digunakan rumus:
SD =
( )
Menurut Day dan Underwood (1981), maka menghitung kadar rata–rata
digunakan rumus sebagai berikut:
μ = Interval kepercayaan x = Kadar rata–rata sampel
21 dk = Derajat kebebasan
22 BAB IV
HASIL DAN PEMBAHASAN
4.1 Hasil Uji Kekerasan Tablet Kunyah Antasida yang Mengandung Magnesium Hidroksida
Berdasarkan Tabel 4.1 di bawah dapat dilihat bahwa kekerasan rata-rata
tablet kunyah antasida yang mengandung Magnesium hidroksida berkisar
antara 4 s/d 8 kg, sedangkan 7 s/d 12 kg untuk tablet kunyah (Soekemi, 1987).
Tabel 4.1. Hasil uji kekerasan tablet kunyah antasida yang mengandung magnesium hidroksida
No Nama Obat Kekerasan Rata-rata
(kg)
1. Acitral® (Interbat) 11,07
2. Dexanta® (Dexa Medica) 6,70
3. Magtral® (Otto Pharmaceutical Industries)
6,41
4. Mylanta® (Bayer indonesia) 6,92
Untuk tablet Acitral® (Interbat) dengan berat rata-rata 11,07 kg, untuk tablet
Dexanta® (Dexa Medica) dengan berat rata-rata 6,70 kg, tablet Magtral® (Otto)
dengan berat rata-rata 6,41 kg, dan untuk tablet Mylanta® (Bayer Indonesia)
dengan berat rata-rata 6,92 kg, keempat tablet yang di uji kekerasannya
memenuhi persyaratan. Adanya perbedaan kekerasan ini dapat disebabkan
23
tekanan maka kekerasan tablet akan semakin meningkat. Selain itu perbedaan
kekerasan juga dapat disebabkan oleh adanya perbedaan bahan tambahan
maupun jumlahnya dalam formulasi (Lachman, dkk., 1994).
Gambar 4.1. Diagram tabel uji kekerasan tablet.
Tabel 4.2. Hasil uji friabilitas tablet kunyah antasida yang mengandung magnesium hidroksida
4.2 Hasil Uji Friabilitas Tablet Kunyah Antasida yang Mengandung Magnesium hidroksida
Pada Tabel 4.2 dapat dilihat bahwa tablet kunyah antasida yang
mengandung Magnesiun hidroksida memenuhi persyaratan uji friabilitas. Hal
ini sesuai dengan persyaratan bahwa kehilangan berat pada uji friabilitas tidak
lebih dari 0,8%. Friabilitas berhubungan dengan kekerasan. Semakin besar
24
kekerasan suatu tablet maka semakin kecil friabilitasnya (Lachman, dkk.,
1994).
Gambar 4.2 Diagram tabel uji friabilitas tablet
Tabel 4.3. Hasil uji waktu hancur tablet kunyah antasida yang mengandung magnesium hidroksida
No Nama Obat Waktu Hancur Rata-rata
(menit)
4. Mylanta® (Bayer Indonesia) 10'08"
4.3 Hasil Uji Waktu Hancur Tablet Kunyah Antasida yang Mengandung Magnesium hidroksida
Waktu hancur suatu tablet dipengaruhi oleh kekerasan tablet. Semakin
keras suatu tablet maka waktu hancur tablet semakin lama, seperti yang
dikatakan oleh Aiache (1993), bahwa semakin keras suatu tablet maka ikatan
antar partikelnya semakin kuat dan jumlah pori-pori semakin sedikit. Dengan
berkurangnya jumlah pori-pori tablet, bila tablet diletakkan dalam medium air
25
akan sulit masuk ke dalam tablet sehingga waktu hancurnya semakin lama.
Hasil uji waktu hancur tablet kunyah antasida yang mengandung Magnesium
hidroksida dapat dilihat pada Tabel 4.3.
Gambar 4.3 Diagram tabel uji waktu hancur tablet
Dari Tabel 4.3, dapat dilihat bahwa semua tablet kunyah antasida yang
mengandung Magnesium hidroksida mempunyai waktu hancur 7 menit 52
detik sampai dengan 12 menit 29 detik, ini menunjukkan bahwa semua tablet
memenuhi syarat waktu hancur berdasarkan Farmakope Indonesia edisi III
(1979) yaitu tidak lebih dari 15 menit.
4.4 Hasil Uji Keragaman Bobot
Menurut Farmakope Indonesia edisi IV (1995) bahwa persyaratan
keseragaman bobot dipenuhi jika jumlah zat aktif dalam masing-masing dari 10
satuan sediaan terlatak antara 85,0% - 115,0% dari yang tertera di etiket dan
simpangan baku relatif kurang dari atau sama dengan 6%. Dari hasil pengujian
yang dilakukan, tablet kunyah antasida yang mengandung Magnesium
0 5 10 15
Acitral® Dexanta® Magtral® Mylanta®
Waktu hancur rata rata
26
hidroksida memenuhi persyaratan keseragaman bobot sebagaimana terlihat
pada Tabel 4.4.
Tabel 4.4. Hasil uji keragaman bobot tablet kunyah antasida yang mengandung magnesium hidroksida
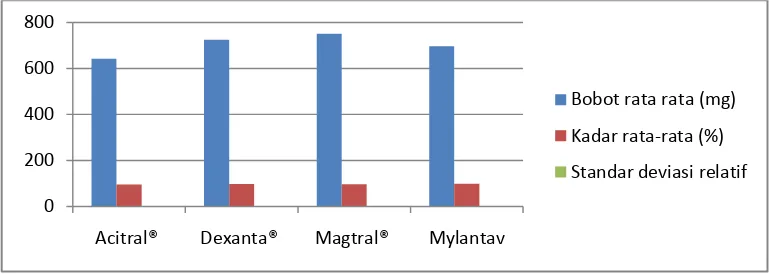
Gambar 4.4 Diagram tabel uji keragaman bobot tablet
Dari Tabel 4.4 dapat dilihat keseragaman bobot tablet kunyah antasida
yang mengandung magnesium hidroksida berkisar antara 96,38 ± 1,08%
sampai 99,27 ± 0,96% dimana dengan kadar yang sedemikian masih memenuhi
syarat menurut Farmakope Indonesia edisi IV (1995) yaitu kadar dari 10 tablet
0 200 400 600 800
Acitral® Dexanta® Magtral® Mylantav
Bobot rata rata (mg)
Kadar rata-rata (%)
27
masing-masing tidak kurang dari 85,0% dan tidak lebih dari 115,0% dan
mempunyai simpangan baku relatif kurang dari 6%.
4.5 Hasil Penetapan kadar Magnesium Hidroksida
Menurut USP Vol III tahun 2009, bahwa persyaratan kadar magnesium
hidroksida mengandung tidak kurang dari 95,0% dan tidak lebih dari 100,5%
magnesium hidroksida.
Tabel 4.5. Hasil pengolahan data penetapan kadar magnesium hidroksida dalam Sediaan
No Nama Sediaan
Kadar yang diperoleh
(%)
1. Acitral® (Interbat) 96,09 ± 0,19
2. Dexanta® (Dexa Medica) 98,09 ± 0,33
3. Magtral® (Otto) 96,4 ± 0,13
4 Mylanta® (Bayer Indonesia) 99,42 ± 0,56
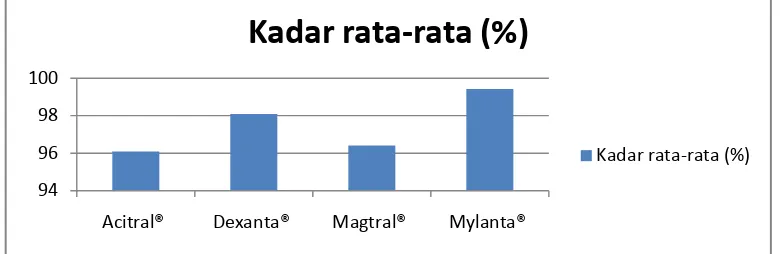
Gambar 4.5 Diagram uji penetapan kadar tablet
94 96 98 100
Acitral® Dexanta® Magtral® Mylanta®
Kadar rata-rata (%)
28
Dari Tabel 4.5 menunjukkan kadar magnesium hidroksida dalam
sediaan tablet yang beredar di apotek kota Medan memenuhi persyaratan yang
tertera dalam USP Vol III (2009) yaitu tidak kurang dari 95,0% - 100,5% dari
29 BAB V
KESIMPULAN DAN SARAN
5.1 Kesimpulan
Hasil kekerasan berkisar antara 6,41 s/d 11,07 kg , sedangkan friabilitas
diperoleh berkisar antara 0,13 s/d 0,69% dengan waktu hancur berkisar antara
7'52" s/d 12'29". Pada uji keragaman bobot diperoleh rentang kadar rata-rata
zat aktif per unit sediaan berkisar antara 96,38% s/d 99,27% dan pada
penetapan kadar yang diperoleh berkisar antara 96,4% - 99,42%.
Berdasarkan hasil penelitian dapat disimpulkan bahwa seluruh tablet
kunyah antasida yang mengandung Magnesium hidroksida yang di uji
memenuhi persyaratan uji untuk sediaan tablet.
5.2 Saran
Disarankan kepada peneliti lainnya agar melakukan pemeriksaan mutu
30
DAFTAR PUSTAKA
Aiache, J.M. (1993). Farmasetika 2 Biofarmasetika Sediaan Per Oral. Edisi Kedua. Surabaya: Airlangga University Press. Hal. 301-303.
Alamsyah, A. (1994). Analisa Kuantitatif Beberapa Senyawa Farmasi. Medan: FMIPA USU. Hal. 19-20.
Anief, M. (1991). Apa yang Perlu Diketahui Tentang Obat. Yogyakarta: Universitas Gajah Mada Press. Hal. 140, 144.
Basset, J., Denny, R.C., Jeffrey, G.H., dan Mendham, J. (1991). Vogel’s Textbook of Quantitative Inorganic Analysis Including Elementary Instrumental Analysis. Edisi Keempat. Alih Bahasa Hadyana Pudjaatmaka dan Setiono. Jakarta: Kalman Media Pustaka. Hal. 299-315.
Brady, J.E. (1999). Kimia Universitas Asas & Struktur. Edisi kelima. Jilid Satu Alih Bahasa Sukmariah Maun, Kamianti Anas dan Tilda Sally. Jakarta: UI Press. Hal. 478.
Day, R.A., dan Underwood, A.L. (1981). Analisa Kimia Kuantitatif. Diterjemahkan oleh: Soendoro, Widianingsih, Sri Rahadjeng. Surabaya: Erlangga. Hal. 21-24.
Ditjen POM. (1979). Farmakope Indonesia. Edisi III. Jakarta: Departemen Kesehatan RI. Hal: 6.
Ditjen POM. (1995). Farmakope Indonesia. Edisi IV. Jakarta : Departemen Kesehatan RI. Hal. 1083.
Estuningtyas, A., dan Arif, A. (2007). Obat Lokal. Dalam Buku Farmakologi dan Terapi. Editor Sulistia Gan Gunawan, Rianto Setiabudy, Nafrialdi dan Elysabeth. Edisi Kelima. Jakarta: Departemen Farmakologi dan Terapi Fakultas Kedokteran Universitas Indonesia. Hal. 518-519.
Lachman, L., Lieberman, H.A., Kanig J.L., (1994). Teori dan Praktek Farmasi Industri. Edisi Kedua. Jakarta: UI Press. Hal. 647-662.
Soekemi, R. A., Yuanita, T., Fat Aminah., dan Usman. (1987). Tablet. Medan: PT. Mayang Kencana. Hal. 25.
31
Sukandar, E.Y., Andrajati, R., Sigit, J.I, Adnyana, I.K., Setiadi, A.A.P., dan Kusnandar. (2008). ISO Farmakoterapi. Cetakan Pertama. Jakarta: Penerbit PT. ISFI Penerbitan. Hal. 433-435.
Tampubolon, O. (1990). Panduan Pelayanan Informasi Obat. Edisi obat essensial. Jakarta: Kimia Farma Press. Hal. 5-6.
Tan, H. T., dan Raharja, K. (2002). Obat-Obat Penting. Edisi ke V. Jakarta: PT. Alex Media Komputindo. Hal. 102-103.
USP Pharmacopiea, (2009). The national Formulary. Edisi 30. The United States Pharmacopiea Convention. Hal. 2834-2835.
Voigt. R., (1994). Buku Pelajaran Teknologi Farmasi. Penerjemah Dr. Soendani Noerono. Edisi Kelima. Yogyakarta: Gadjah Mada University Press. Hal. 165.
32
Lampiran 1. Contoh perhitungan data pengambilan sampel
Sampel disurvey di beberapa Apotek yang beredar di Kota Medan. Lalu
digunakan metode n+1 yaitu sampel yang terpilih diambil dari akar jumlah
sampel + 1 dengan maksud untuk memperkecil jumlah sampel namun masih
mewakili populasi.
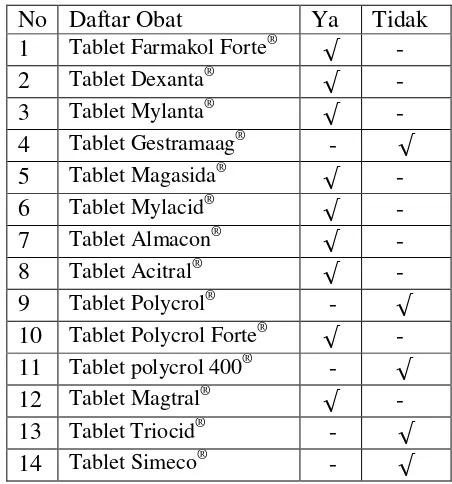
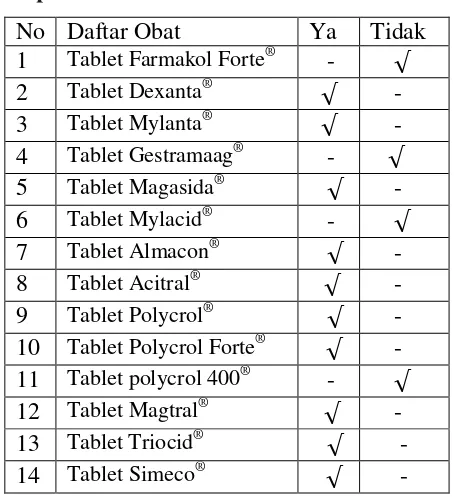
1. Apotek Samudra 2 Jl. Kapten muslim No. 55 Medan
No Daftar Obat Ya Tidak
Jumlah (n) = 10 sampel, maka jumlah sampel yang di sampling adalah
1
10+ = 4 sampel.
2. Apotek Kalimas Jl. Setia budi No. 133 Medan
33 11 Tablet polycrol 400® - √ 12 Tablet Magtral® - √ 13 Tablet Triocid® √ - 14 Tablet Simeco® √ -
Jumlah (n) = 9 sampel, maka jumlah sampel yang di sampling adalah
1
9+ = 4 sampel,
3. Apotek Iskandar muda Jl. Iskandar muda No.83 Medan
34
Keterangan : jumlah sampel yang digunakan dalam penelitian adalah 4 sampel yaitu tablet Acitral® , tablet Dexanta®, tablet Magtral® dan tablet Mylanta® karena keempat tablet kunyah antasida tersebut terdapat di semua Apotek yang penulis survey.
35
Lampiran 2. Hasil uji kekerasan tablet kunyah antasida yang mengandung magnesium hidroksida.
Nama Obat Kekerasan Tablet (Kg)
Acitral®
Mylanta® (Bayer Indonesia) 6,66
36
Lampiran 3. Hasil uji friabilitas tablet kunyah antasida yang mengandung magnesium hidroksida.
Friabilitas ( F ) = �−�
�
x
100 %Dimana : a = bobot 20 tablet sebelum diputar dengan friabilator (gram) b = bobot 20 tablet setelah diputar dengan friabilator (gram) F = friabilitas (%)
- Tablet Mylanta® PT. Bayer Indonesia
F= 13,88−13,83
37
Lampiran 4. Hasil uji waktu hancur tablet kunyah antasida yang mengandung magnesium hidroksida.
Nama Obat Waktu Hancur (menit:detik)
Acitra® (Interbat) 12'11" Mylanta® (Bayer Indonesia) 9'26"
38
Lampiran 5. Hasil uji keragaman bobot tablet kunyah antasida yang mengandung magnesium hidroksida
Acitral® (Interbat)
Dexanta®
Simpangan baku relatif : ≤ 6%
Keterangan :
A : bobot tablet (gram)
B : Kandungan zat berkhasiat (miligram) C : Penyimpangan (%)
Wr : bobot rata-rata tablet (miligram X : kadar (%)
SD : Standard Deviasi
39
Lampiran 6. Perhitungan keragaman bobot tablet acitral PT Interbat.
Ditimbang 10 tablet satu per satu masing-masing tablet :
1. 640 mg 6. 640 mg
Tiap tablet mengandung 200 mg Magnesium hidroksida
Berat Magnesium hidroksida dalam 10 tablet = 10 x 200 mg = 2000 mg
Berat serbuk setara 75 mg Magnesium hidroksida= 75 ��
2000 �� x 6495 mg = 243,56
mg
Ditimbang sebanyak 6 kali, kemudian dilakukan pengujian sesuai dengan
prosedur.
Data penimbangan serbuk setara 75 mg Magnesium hidroksida.
40
Lampiran 6. (lanjutan)
Perhitungan kesetaraan serbuk
Serbuk ditimbang = 243,6 mg
Berat kesetaraan = 243,6 ���2000��
6495�� = 75,0115 mg
Perhitungan kadar tablet acitral dalam sampel :
% kadar = �����.������
Dengan cara yang sama, dihitung kadar tablet lainnya
Perhitungan % penyimpangan berat tablet :
Rata-rata hasilpenetapan kadar = 96,38% x 200 mg
= 192,76 mg zat berkhasiat/tablet
Contoh : Berat tablet 1 = 640 mg, maka zat berkhasiatnya
= 640 ��
649,5 �� x 192,76 mg = 189,9405 mg
41 Lampiran 6. (lanjutan)
= 189,9405−192,76
192,76 x 100% = 1,46%
Tabel hasil keragaman bobot tablet acitral® PT. Interbat Tablet Berat tablet
(mg)
Perhitungan Standar Deviasi Relatif :
SD =
�
Σ (X−X�)2
n−1
=
�
53,73569 = 2,4434
Maka perhitungan standar deviasi relatif ;
RSD = ��
� x 100%
= 2,0776
42
Lampiran 7. Contoh perhitungan keragaman bobot tablet dexanta PT. Dexa Medika
Ditimbang 10 tablet satu per satu masing-masing tablet :
1. 720 mg 6. 750 mg
Berat rata-rata = 7220 mg / 10 tablet = 720 mg/tablet
Tiap tablet mengandung 200 mg Magnesium hidroksida
Berat Magnesium hidroksida dalam 10 tablet = 10 x 200 mg = 2000 mg
Berat serbuk setara 75 mg Magnesium hidroksida= 75 ��
2000 �� x 7220 mg = 270,75
mg
Ditimbang sebanyak 6 kali, kemudian dilakukan pengujian sesuai dengan
prosedur.
Data penimbangan serbuk setara 75 mg Magnesium hidroksida.
43
Lampiran 7. (lanjutan)
Contoh Perhitungan kesetaraan serbuk
Serbuk ditimbang = 271,2 mg
Berat kesetaraan = 271,2���2000��
7220�� = 75,1246 mg
Perhitungan kadar tablet acitral dalam sampel :
% kadar = �����.������
Dengan cara yang sama, dihitung kadar tablet lainnya
Perhitungan % penyimpangan berat tablet :
Rata-rata hasilpenetapan kadar = 97,91% x 200 mg
= 195,82 mg zat berkhasiat/tablet
Berat tablet 1 = 720 mg, maka zat berkhasiatnya
= 720 ��
722 �� x 195,82 mg = 195,2775 mg
44 Lampiran 7. (lanjutan)
= 195,2775−195,82
195,82 x 100% = 0,27%
Tabel hasil keragaman bobot tablet dexanta PT. Dexa Medika
Tablet Berat tablet (mg)
Perhitungan Standar Deviasi Relatif :
SD =
�
Σ (X−X�)2
n−1
=
�
91,94479 = 3,1962
Maka perhitungan standar deviasi relatif ;
RSD = ��
� x 100%
= 3,1962
45
Lampiran 8. Contoh perhitungan keragaman bobot tablet magtral PT. Otto
Ditimbang 10 tablet satu per satu masing-masing tablet :
Berat rata-rata = 7525 mg / 10 tablet = 752,5 mg/tablet
Tiap tablet mengandung 250 mg Magnesium hidroksida
Berat Magnesium hidroksida dalam 10 tablet = 10 x 250 mg = 2500 mg
Berat serbuk setara 75 mg Magnesium hidroksida= 75 ��
2500 �� x 7525 mg = 225,75
mg
Ditimbang sebanyak 6 kali, kemudian dilakukan pengujian sesuai dengan
prosedur.
Tabel data penimbangan serbuk setara 75 mg Magnesium hidroksida.
46
Lampiran 8. (lanjutan)
Contoh Perhitungan kesetaraan serbuk
Serbuk ditimbang = 226,2 mg
Berat kesetaraan = 226,2���2500��
7525�� = 75,1495 mg
Perhitungan kadar tablet acitral dalam sampel :
% kadar = �����.������
Dengan cara yang sama, dihitung kadar tablet lainnya
Perhitungan % penyimpangan berat tablet :
Rata-rata hasilpenetapan kadar = 96,61% x 250 mg
= 241,525 mg zat berkhasiat/tablet
Berat tablet 1 = 750 mg, maka zat berkhasiatnya
= 750 ��
752,5�� x 241,525 mg = 240,7225 mg
47 Lampiran 8. (lanjutan)
= 240,7231−241,525
241,525 x 100% = 0,33%
Tabel hasil keragaman bobot tablet magtral PT.Otto
Tablet Berat tablet (mg)
Perhitungan Standar Deviasi Relatif :
SD =
�
Σ (X−X�)2
n−1
=
�
50,48649 = 2,3684
Maka perhitungan standar deviasi relatif ;
RSD = ��
� x 100%
= 2,3684
48
Lampiran 9. Contoh perhitungan keragaman bobot tablet mylanta PT. Bayer Indonesia
Ditimbang 10 tablet satu per satu masing-masing tablet :
1. 700 mg 6. 700 mg
Berat rata-rata = 6940 mg / 10 tablet = 694 mg/tablet
Tiap tablet mengandung 200 mg Magnesium hidroksida
Berat Magnesium hidroksida dalam 10 tablet = 10 x 200 mg = 2000 mg
Berat serbuk setara 75 mg Magnesium hidroksida= 75 ��
2000 �� x 6940 mg = 260,25
mg
Ditimbang sebanyak 6 kali, kemudian dilakukan pengujian sesuai dengan
prosedur.
Data penimbangan serbuk setara 75 mg Magnesium hidroksida.
49
Lampiran 9. (lanjutan)
Contoh Perhitungan kesetaraan serbuk
Serbuk ditimbang = 261,2 mg
Berat kesetaraan = 261,2���2000��
6940 �� = 75,2737 mg
Perhitungan kadar tablet acitral dalam sampel :
% kadar = �����.������
Dengan cara yang sama, dihitung kadar tablet lainnya
Perhitungan % penyimpangan berat tablet :
Rata-rata hasilpenetapan kadar = 99,27% x 200 mg
= 198,54 mg zat berkhasiat/tablet
Berat tablet 1 = 700 mg, maka zat berkhasiatnya
= 700 ��
694 �� x 198,54 mg = 200,2564 mg
50 Lampiran 9. (lanjutan)
= 200,2573−198,54
198,54 x 100% = 0,86%
Tabel hasil keragaman bobot tabel mylanta PT. Bayer Tablet Berat tablet
(mg)
Perhitungan Standar Deviasi Relatif :
SD =
�
Σ (X−X�)2
n−1
=
�
33,54239 = 1,9305
Maka perhitungan standar deviasi relatif ;
RSD = ��
� x 100%
= 1,9305
51
Lampiran 10. Data kadar magnesium hidroksida dalam sediaan tablet
No Nama obat Berat yang
Tabel Hasil Pembakuan
No Volume EDTA
52 M EDTA = 0,05 M
Titrasi 2 : V ZnSO4 x M ZnSO4 = V EDTA x M EDTA 9,50 x 0,05 = 10 x M EDTA
M EDTA = 0,0475 M
Titrasi 3 : V ZnSO4 x M ZnSO4 = V EDTA x M EDTA 9,90 x 0,05 = 10 x M EDTA
M EDTA = 0,0495 M
M EDTA rata-rata = 0,05+0,0475 +0,0495
53
Lampiran 11. Perhitungan kadar magnesium hidroksida pada tablet acitral Cara perhitungan kadar Magnesium hidroksida
% Kadar Mg(OH)2 =
������������
0,05 ��� x 100%
Keterangan :
Vs : Volume titrasi sampel
M : Molaritas EDTA yang digunakan
Bsetara: 1 ml dinatrium edetat 0,05 M setara dengan 2,916 Mg(OH)2
BS : Bobot Mg(OH)2 dalam sampel yang digunakan dalam mg
Bobot 20 tablet = 12,9014 gram = 12901,4 mg
Ditimbang setara 75 Magnesium hidroksida
Berat Magnesium hidroksida dalam tablet Acitral 200 mg x20 tablet = 4000 mg
Massa berat sampel yang ditimbang
54 Lampiran 11. (lanjutan)
K1 = 25,3 � 0,049 � 2,916
Perhitungan statistik kadar magnesium hidroksida (Acitral® Interbat)
55
Lampiran 11. (lanjutan)
Data ditolak apabila thitung≥ ttabel
thitung = |�−��|
Karena thitung ≤ -ttabel maka data ditolak, selanjutnya dilakukan pengujian
terhadap data yang dianggap tidak menyimpang.
56
Lampiran 11. (lanjutan)
Pada tingkat kepercayaan 95% dengan nilai α = 0,01, dk = n – 1 = 5 – 1 = 4
Diperoleh ttabel = 2,776
Data ditolak apabila thitung≥ ttable atau thitung≤ - ttabel
thitung = |�−��| �� √�⁄
thitung data 1 =
0,19
0,1531 √5 = 2,7766
thitung data 2 =
0,12
0,1531 √5 = 1,7543
thitung data 3 =
0,08
0,1531 √5 = 1,1695
thitung data 4 =
0,12
0,1531 √5 = 1,7543
thitung data 5 =
0,15
0,1531 √5 = 2,1929
Karena thitung≥ ttabel maka data diterima, maka kadar sebenarnya terletak antara:
μ =X ± t(1-1/2α)dk x ��√�
= 96,09 ± 2,776 x 0,1531 �5
57
Lampiran 12. Perhitungan kadar magnesium hidroksida pada tablet dexanta Bobot 20 tablet 14,4314 gram = 14431,4 mg
Ditimbang setara 75 Magnesium hidroksida
Berat Magnesium hidroksida dalam tablet Acitral 200 mg x20 tablet = 4000 mg
Massa berat sampel yang ditimbang
58 Lampiran 12. (lanjutan)
K5 = 25,6 � 0,049 � 2,916
0,05 � 75,0031 x 100% = 97,53%
K6 = 25,9 � 0,049 � 2,916
0,05 � 75,3911 x 100% = 98,17%
Perhitungan statistik kadar magnesium hidroksida (Dexanta, Dexa Medica)
59 Lampiran 12. (lanjutan)
thitung data 3 = 0,39
Karena thitung ≤ -ttabel maka data ditolak, selanjutnya dilakukan pengujian
terhadap data yang dianggap tidak menyimpang.
60
Lampiran 12. (lanjutan)
thitung data 1 =
0,07
0,1358 √3 = 0,8928
thitung data 4 =
0,16
0,1358 √3 = 2,0408
thitung data 6 =
0,08
0,1358 √3 = 1,0204
Karena thitung≥ ttabel maka data diterima, maka kadar sebenarnya terletak antara:
μ =X ± t(1-1/2α)dk x ��√�
= 98,09 ± 4,303 x 0,1358 �3
61
Lampiran 13. Perhitungan kadar magnesium hidroksida pada tablet magtral Bobot 20 tablet 15,0118 gram = 15011,8 mg
Ditimbang setara 75 Magnesium hidroksida
Berat Magnesium hidroksida dalam tablet Acitral 250 mg x20 tablet = 5000 mg
Massa berat sampel yang ditimbang
62 Lampiran 13. (lanjutan)
K5 = 25,4 � 0,049 � 2,916
0,05 � 75,2741 x 100% = 96,42%
K6 = 25,5 � 0,049 � 2,916
0,05 � 75,1742 x 100% = 96,93%
Perhitungan statistik kadar magnesium hidroksida (Magtral® Otto)
63 Lampiran 13. (lanjutan)
thitung data 3 = 0,27
Karena thitung ≤ -ttabel maka data ditolak, selanjutnya dilakukan pengujian
terhadap data yang dianggap tidak menyimpang.
64
Lampiran 13. (lnjutan)
thitung data 3 =
0,1
0,0832√4 = 2,4038
thitung data 4 =
0,02
0,0832√4 = 0,4807
thitung data 5 =
0,02
0,0832√4 = 0,4807
Karena thitung≥ ttabel maka data diterima, maka kadar sebenarnya terletak antara:
μ =X ± t(1-1/2α)dk x ��√�
= 96,4 ± 3,182 x 0,0832 �4
65
Lampiran 14. Perhitungan kadar magnesium hidroksida pada tablet mylanta Bobot 20 tablet 13,8503 gram = 13850,3 mg
Ditimbang setara 75 Magnesium hidroksida
Berat Magnesium hidroksida dalam tablet Acitral 200 mg x20 tablet = 4000 mg
Massa berat sampel yang ditimbang
66 Lampiran 14. (lanjutan)
K5 = 26,2 � 0,049 � 2,916
0,05 � 75,0019 x 100% = 99,82%
K6 = 26,2 � 0,049 � 2,916
0,05 � 75,2619 x 100% = 96,48%
Perhitungan statistik kadar magnesium hidroksida (Mylanta®Bayer Indonesia) No Kadar [X]
Data ditolak apabila thitung≥ ttabel
67 Lampiran 14. (lanjutan)
thitung data 4 = 0,52
Karena thitung ≤ -ttabel maka data ditolak, selanjutnya dilakukan pengujian
terhadap data yang dianggap tidak menyimpang.
68
Lampiran 14. (lanjutan)
Karena thitung≥ ttabel maka data diterima, maka kadar sebenarnya terletak antara:
μ =X ± t(1-1/2α)dk x ��√�
= 99,42 ± 4,303 x 0,2282 �3
69 Lampiran 15. Daftar spesifikasi sampel.
1.Acitral® (Interbat)
No. Batch : T017B017
No. Reg : DBL851760301A1
Expire Date : Mar 2016
Komposisi : Aluminium hidroxide 200 mg
Magnesium hidroxide 200 mg
Simethicone 20 mg
2.Dexanta® (Dexa Medica)
No. Batch : 4309107
No. Reg : DBL7605006363A1
Expire Date : September 2016
Komposisi : Aluminium hidroxide 200 mg
Magnesium hidroxide 200 mg
Simethicone 50 mg
3. Magtral® ( Otto)
No. Batch : C2F7562
No. Reg : DBL8818804663A1
Expire Date : Desember 2015
Komposisi : Aluminium hidroxide 250 mg
Manesium hidroxide 250 mg
70 Lampiran 15. (lanjutan)
4. Mylanta® (Bayer Indonesia)
No. Batch : CR09968
No. Reg : DBL0802007363A1
Expire Date : November 2014
Komposisi : Aluminium hidroxide 200 mg
Magnesium hidrixide 200 mg
71 Lampiran 16. Gambar alat uji waktu hancur
Disintegration Tester (erweka)
72 Lampiran 17. Gambar alat uji kekerasan
73 Lampiran 18. Gambar alat uji kerapuhan
74 Lampiran 19. Gambar alat uji penetapan kadar
75 Lampiran 20. Gammbar hasil pembakuan
Warna sebelum titrasi
76 Lampiran 21. Gambar penetapan kadar
Warna sebelum titrasi
Warna sesudah titrasi