PRODUCTION CHITOSAN FROM RAW MATERIALS SHRIMP SHELLS USES THE METHOD OF CHEMICAL AND OF ENZYMATIC WITH ENZIM CHITIN
DEACETILASE
By
WINDA RAHMAWATI
Has been conducted research on the production of chitosan shrimp shells with two methods. Test a method of chemical deproteinasi, covering demineralisasi, deasetilasi and methods of enzymatic with deasetilasi chemical partly followed by the addition of an enzyme chitin deasetilase. Characterization chitosan produced covering the water level, levels of ashes levels of nitrogen and degrees deasetilasi. The result showed that kitosan resulting from a method of chemical having the water level, levels of ashes levels of nitrogen and degrees deasetilasi successive also 7.39 %; 2,10 %; 7,59 % and 71 %. While in deasetilasi of enzymatic, the result analysis deasetilasi chemical partly use of the spectrophotometer fourier transform infrared (FTIR) produces chitosan deasetilasi 46,68 %, with degrees followed by the addition of an enzyme CDA ( chitin deacetilase ) produces chitosan with degrees deasetilasi 75,91 %.
PRODUKSI KITOSAN DARI BAHAN BAKU CANGKANG UDANG MENGGUNAKAN METODE KIMIA DAN ENZIMATIS DENGAN ENZIM
KITIN DEASETILASE
Oleh
WINDA RAHMAWATI
Telah dilakukan penelitian mengenai produksi kitosan dari cangkang udang dengan dua metode. Uji metode kimia meliputi deproteinasi, demineralisasi, deasetilasi dan metode enzimatis dengan deasetilasi kimia sebagian diikuti dengan penambahan enzim kitin deasetilase. Karakterisasi kitosan yang dihasilkan meliputi kadar air, kadar abu, kadar nitrogen dan derajat deasetilasi. Hasil penelitian menunjukkan bahwa kitosan yang dihasilkan dari metode kimia memiliki kadar air, kadar abu, kadar nitrogen dan derajat deasetilasi berturut–
turut 7,39%; 2,10%; 7,59% dan 71%. Sedangkan pada deasetilasi enzimatis, hasil analisis derajat deasetilasi kimia sebagian menggunakan spektrofotometer fourier transform infrared (FTIR) menghasilkan kitosan dengan derajat deasetilasi 46,68 %, diikuti dengan penambahan enzim CDA (Kitin Deasetilase) menghasilkan kitosan dengan derajat deasetilasi 75,91%.
A. Latar Belakang
Indonesia adalah negara maritim dengan potensi hasil laut dan perikanan yang sangat melimpah. Udang merupakan salah satu komoditas ekspor non migas Indonesia dan biota laut yang bernilai ekonomis tinggi. Pada umumnya udang diekspor dalam bentuk daging beku dimana hasil samping pengolahan daging udang berupa limbah cangkang yang terdiri dari (kepala, ekor, dan kulit). Limbah ini belum termanfaatkan secara baik, bahkan sebagian besar juga merupakan buangan yang turut mencemari lingkungan. Limbah cangkang udang memilki kandungan kitin 15-20% (Marganov, 2003). Kitin adalah salah satu polisakarida yang melimpah di bumi selain selulosa dan pati. Kitin merupakan polimer dari N-asetilglukosamin yang terikat melalui ikatan ß-(1,4) (Tsigos dan Bouriotis, 1995). Kitin merupakan zat padat kristalin, tidak larut dalam air, asam anorganik encer, alkali, alkohol, dan pelarut organik lainnya, tetapi larut dalam asam-asam mineral yang pekat (Austin, 1981).
berkonsentrasi tinggi (No and Meyer, 1997). Kitosan tidak larut dalam air dan asam sulfat, sedikit larut dalam asam klorida dan asam nitrat. Adanya gugus amino pada kitosan, menyebabkan kitosan bersifat polielektrolitik (Hirano, 1986).
Kitin dan kitosan digunakan secara luas dalam dunia industri terutama sebagai bahan baku kosmetik dan obat-obatan serta zat aditif pada kertas. Dalam hal ini, kitosan lebih luas digunakan karena sifatnya yang lebih larut dalam asam-asam organik sehingga dapat dimodifikasi dalam bentuk larutan, gel, membran, dan krim (Peter, 1995). Deasetilasi kitin menjadi kitosan dapat dilakukan dengan dua metode yaitu metode konvensional (cara kimia) dan metode enzimatis (Gooday, 1994). Metode kimia seringkali menyisakan limbah berbahaya, namun metode ini lebih mudah dan cepat. Sedangkan pada metode enzimatis digunakan enzim spesifik (misal: kitin deasetilase). Enzim ini bekerja spesifik memotong gugus asetil dari kitin menjadi kitosan. sehingga tidak menyisakan limbah berbahaya. Jadi metode enzimatis ini lebih aman dan efektif dibandingkan metode
konvensional (Jayanti, 2002).
Berdasarkan uraian diatas, maka dalam penelitian ini akan dilakukan pembuatan kitosan dengan metode kimia dan secara enzimatis menggunakan enzim kitin deasetilase dari penelitian pendahuluan mengenai isolasi enzim kitin deasetilase dari isolat tanah humusAspergillus Aculeatusdan identifikasi enzim tersebut dalam produksi kitosan (Husniati dkk., 2012). Menurut Kafetzopoulos (1993), bahwa enzim kitin deasetilase dapat mengubah kitin menjadi kitosan melalui pemutusan ikatan N-asetamido pada kitin. Kitosan hasil penelitian dikarakterisasi menggunakan Spektrofotometer Fourir Transform Infrared (FTIR) untuk
B. Tujuan Penelitian
Tujuan dari penelitian ini adalah:
1. Mengetahui langkah-langkah pembuatan kitosan dari cangkang udang melalui metode kimia dan enzimatis.
2. Mengkarakterisasi produk kitosan dari metode kimia dan enzimatis.
C. Manfaat Penelitian
II. TINJAUAN PUSTAKA
A. Udang
Udang merupakan salah satu golongan binatang air yang termasuk dalam arthopoda(binatang berbuku-buku). Seluruh tubuh terdiri dari ruas-ruas yang terbungkus oleh kerangka luar ataueksoskeletondari zat tanduk atau kitin dan diperkuat oleh bahan kapur kalsium karbonat (Soetomo, 1990).
Klasifikasi udang diperlihatkan pada Tabel 1. Spesies Morfologi
Kelas Crustacea(binatang berkulit keras)
Sub Kelas Malacrostraca(udang-udangan tingkat tinggi) Super Ordo Eucarida
Ordo Decapoda
Sub Ordo Natantia(kaki digunakan untuk berenang) Famili Palaemonidae, Penaidae
(Departemen Kelautan dan Perikanan 2003 dalam Siregar, 2009)
Produksi tambak udang meningkat seiring dengan meningkatnya permintaan ekspor. Udang yang diekspor diantaranya dalam bentuk beku (block frozen) yang terdiri dari produkhead on(utuh),headless(tanpa kepala) danpeeled(tanpa kepala dan kulit). Usaha tersebut menghasilkan limbah udang dalam jumlah cukup besar yang terdiri dari bagian kepala, kulit, dan ekor. Kepala udang
merupakan salah satu hasil proses pengolahan produk perikanan yang dapat dibuat menjadi silase. Selain menghasilkan produk berupa filtrat, silase kepala udang juga menghasilkan limbah berupa ampas silase. Yang dapat dimanfaatkan sebagai bahan baku kitosan (Zahiruddinet al., 2008).
B. Kitin
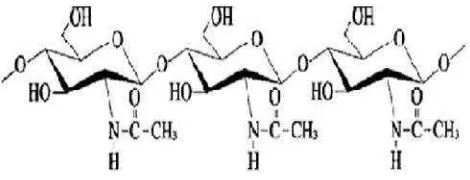
Kitin termasuk golongan polisakarida yang mempunyai berat molekul tinggi dan merupakan molekul polimer berantai lurus dengan nama lain ß-(1,4)-2-asetamida-2-dioksi-D-glukosa (N-asetil-D-glukosamin). Struktur kitin sama dengan selulosa dimana ikatan yang terjadi antara monomernya terangkai dengan ikatan glikosida pada posisi ß-(1,4). Perbedaannya dengan selulosa adalah gugus hidroksil yang terikat pada atom karbon yang kedua pada kitin diganti oleh gugus asetamida (NHCOCH2) sehingga kitin menjadi sebuah polimer berunit N-asetilglukosamin (Muzzarelli, 1985). Adapun struktur kitin ditunjukkan pada Gambar 1.
Gambar 1. Struktur Kitin (Kaban, 2009)
protein (deproteinasi) dan pemisahan mineral (demineralisasi). Sedangkan untuk mendapatkan kitosan dilanjutkan dengan proses deasetilasi (Wardaniati dan Setyaningsih, 1999). Kandungan kitin dan protein pada limbahcrustaceaedapat dilihat pada Tabel 2.
Tabel 2: Kandungan Kitin dan Protein pada limbahcrustaceae Sumber Kitin Protein (%) Kitin (%) KepitingCollnectes sapidus 21,5 13,5 Chinocetes opillo 29,2 26,6 UdangPandanus borealis 41,9 17,0
Crangon crangon 40,6 17,8
Penaeus monodon 47,4 40,4
Udang karangPrtocamborus clarkii 29,8 13,2 KrillEuphausia superb 41,0 24,0
Udang biasa 61,6 33,0
(Synowiecky dan Al-Khateeb, 2003)
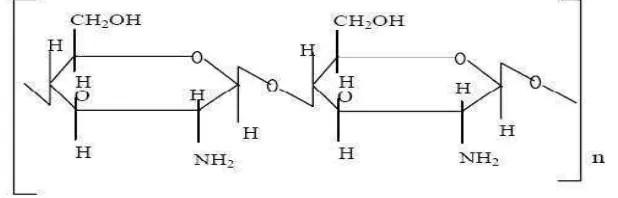
C. Kitosan
kreatifitas kimia yang tinggi (Tokura, 1995).
Gambar 2. Struktur Kitosan
D. Sifat Fisika-Kimia Kitin dan Kitosan
Kitin tidak larut dalam air maupun pelarut organik, pelarut yang umum digunakan untuk kitin adalah campuran N,N-dimetilasetamida dan LiCl 5%,
metil-2-pirolidine (Rutherford dan Austin, 1977) dan juga dalam asam mineral pekat (Alexander, 1977). Berbeda dengan polisakarida lainnya yang umumnya bersifat netral atau sedikit asam, kitin dan kitosan bersifat basa karena adanya gugus asetamida pada kitin dan gugus amino pada kitosan. Kitosan dapat larut dalam pelarut organik seperti asam asetat encer, asam sitrat, asam piruvat, dan asam laktat, tidak larut dalam basa maupun asam mineral (Kaban, 2009).
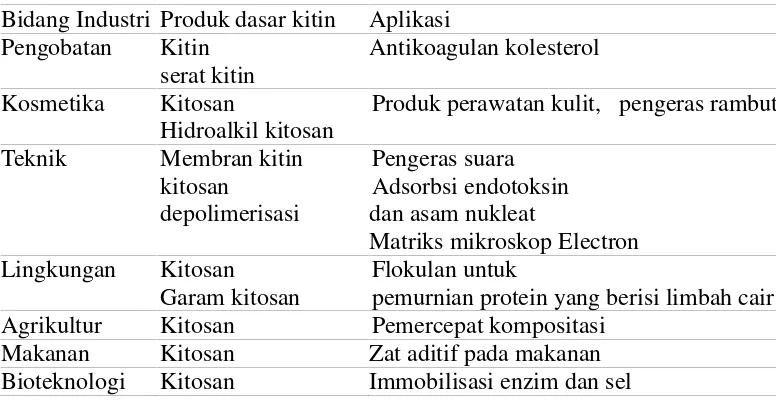
E. Kegunaan Kitin dan Kitosan
Tabel 3.Kegunaan kitin dan kitosan dalam bidang industri Bidang Industri Produk dasar kitin Aplikasi
Pengobatan Kitin serat kitin
Antikoagulan kolesterol Kosmetika Kitosan
Hidroalkil kitosan
Produk perawatan kulit, pengeras rambut Teknik Membran kitin
kitosan
depolimerisasi
Pengeras suara Adsorbsi endotoksin dan asam nukleat
Matriks mikroskop Electron Lingkungan Kitosan
Garam kitosan
Flokulan untuk
pemurnian protein yang berisi limbah cair Agrikultur Kitosan Pemercepat kompositasi
Makanan Kitosan Zat aditif pada makanan Bioteknologi Kitosan Immobilisasi enzim dan sel
F. Pembuatan Kitin Dan Kitosan
Kitosan yang disebut juga dengan β-1,4-2 amino-2-dioksi-D-glukosa merupakan turunan dari kitin melalui proses deasetilasi, pencucian, pengeringan dan
penepungan. Deasetilasi atau penghilangan gugus asetil biasanya dilakukan dengan menggunakan basa kuat berkonsentrasi tinggi (NaOH). Sedangkan proses isolasi kitin dari cangkang udang meliputi dua tahap, yaitu deproteinasi dan demineralisasi.
a. Deproteinasi
protein menggunakan NaOH, protein diekstraksi sebagai Na-proteinat yang larut, dan jika menggunakan KOH akan diperoleh K-proteinat yang mengendap (Knorr, 1984), sedangkan enzim proteolitik akan mendegradasi protein sehingga terpisah dari kitin (Muzzarelli, 1984).
b. Demineralisasi
Demineralisasi merupakan proses pemisahan mineral atau senyawa anorganik yang ada pada cangkang udang dari kitin. Mineral utama yang terkandung dalam cangkang udang adalah kalsium karbonat (CaCO3) dan kalsium fosfat
(Ca3(PO4)2). Proses demineralisasi ini biasanya dilakukan dengan merendam bahan hasil deproteinasi dalam larutan asam klorida (Austin, 1988 dalam Theresia, 2004)
Menurut Shimahara dan Takiguchi (1988), asam klorida efektif untuk melarutkan kalsium menjadi kalsium klorida, namun asam klorida juga menyebabkan kitin mengalami depolimerisasi (Shimahara dan Takiguchi, 1988 dalam Theresia 2004)
c. Deasetilasi
G. Enzim
Enzim adalah golongan protein yang paling banyak terdapat dalam sel hidup dengan berat molekul antara 15.000 - 1.000.000, berfungsi mengkatalis reaksi-reaksi kimia baik dalam sel ataupun di luar sel. Daya katalitiknya bersifat spesifik, artinya hanya mampu mengkatalisis satu jenis reaksi atau substrat
tertentu. Enzim mampu mempercepat reaksi 1012- 1020kali lebih cepat dari reaksi kimia biasa yang tidak menggunakan enzim serta mempunyai efisiensi katalisis yang tinggi. Sebuah molekul enzim mampu menguraikan 10.000–
1.000.000 substrat per menit (Poedjiadi, 1994).
Enzim adalah protein yang berfungsi sebagai katalisator, senyawa yang meningkatkan kecepatan reaksi kimia. Enzim katalisator berkaitan dengan reaktan yang disebut substrat. Mengubah reaktan menjadi produk, lalu
melepaskan produk. Walaupun enzim dapat mengalami modifikasi selama urutan tersebut, pada akhir reaksi, enzim kembali ke bentuk asalnya (Marks, 2000). Enzim memiliki kelebihan jika dibandingkan dengan katalis biasa, antara lain; enzim bekerja secara spesifik, enzim bekerja pada suhu biasa dan pH mendekati netral, serta dapat mengurangi polutan yang dihasilkan. Karena kespesifikan enzim yang sangat tinggi, maka hanya dapat memecah atau mensintesis senyawa tertentu (Page, 1997). Hubungan atau kontak antara enzim dengan substrat menyebabkan terjadinya kompleks Enzim-Substrat (ES). Kompleks ini
H. Kitin Deasetilase
Enzim kitin deasetilase merupakan enzim yang bekerja mengkatalisis konversi kitin menjadi kitosan dalam proses deasetilase N-asetilglukosamin. Enzim kitin deasetilase dikandung oleh mikroorganisme yang dinding selnya tersusun dari kitosan. Kitin deasetilase mampu mengubah sebagian gugus asetamida pada kitin menjadi gugus amino dengan melepaskan gugus asetil, sehingga diperoleh kitosan dengan derajat deasetilasi yang seragam. Enzim kitin deasetilase mengkatalisis reaksi deasetilasi kitin dengan bantuan air menghasilkan asetat dan kitosan. Reaksi tersebut diinhibisi oleh adanya asetat, glikol kitosan, EDTA, dan katio-kation seperti Mn2+, CO2+, dan Na2+, dengan range pH inkubasi antara 4,5-8,5 (Schomburg dan Salzmann, 1991 dalam Sunardi 2011).
I.Spektrofotometer Fourier Transform Infrared(FTIR)
Spektroskopi adalah ilmu yang mempelajari segala sesuatu tentang interaksi antara materi dengan dengan radiasi elektromagnetik (REM). Spektrofotometer FTIR dapat digunakan untuk menganalisa kualitatif maupun kuantitatif. Analisa kualitatif spektroskopi FTIR secara umum dipergunakan untuk identifikasi gugus-gugus fungsional yang terdapat dalam suatu senyawa yang dianalisa.
Spektrofotometer FTIR pada prinsipnya sama dengan spektroskopi inframerah, hanya saja spektroskopi FTIR ditambahkan alat optik (Fourier Transform) untuk menghasilkan spektra yang lebih baik, sehingga spektroskopi FTIR dapat
menghasilkan data dimana dengan spektroskopi inframerah puncak yang
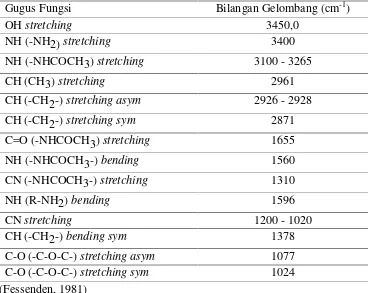
spektrum IR antara 4000-400 cm-1(2.5 sampai 25 µm) (Silverstein dkk, 1986). Sebagai contoh senyawa kitosan memberikan data serapan IR yang dapat dilihat pada Tabel 4.
Tabel 4.Gugus fungsi IR dari senyawa kitosan.
Gugus Fungsi Bilangan Gelombang (cm-1)
OHstretching 3450,0
NH (-NH2)stretching 3400
NH (-NHCOCH3)stretching 3100 - 3265
CH (CH3)stretching 2961
CH (-CH2-)stretching asym 2926 - 2928
CH (-CH2-)stretching sym 2871
C=O (-NHCOCH3)stretching 1655
NH (-NHCOCH3-)bending 1560
CN (-NHCOCH3-)stretching 1310
NH (R-NH2)bending 1596
CNstretching 1200 - 1020
CH (-CH2-)bending sym 1378
A. Waktu dan Tempat
Penelitian ini telah dilaksanakan dari bulan juni 2011 sampai Desember 2011, dengan tahapan kegiatan, yaitu: pengambilan sampel cangkang udang di PT. Indokom Samudra Persada, Lampung Selatan. Persiapan cangkang udang,
pembuatan kitin dan kitosan serta karakterisasi kitosan dilakukan di Laboratorium Balai Riset dan Standardisasi Industri Perdagangan (BARISTAND) Bandar Lampung. Analisis spektroskopi IR dilakukan di Laboratorium LIPI dan Laboratorium Biomassa Universitas Lampung.
B. Alat dan Bahan
Adapun bahan-bahan yang digunakan yaitu cangkang udang, tepung kitin komersial, ekstrak kasar enzim kitin deasetilase (CDA) dari penelitian
pendahuluan (Isolasi enzim kitin deasetilase dari isolat tanah humusAspergillus Aculeatusdan identifikasi enzim tersebut dalam produksi kitosan, Husniati dkk., 2012), asam klorida, natrium hidroksida, asam asetat, selenium, K2SO4, asam sulfat,H2O2,asam borat 4%, indikator metil merah, HCl 0,2 N, akuades, indikator universal, dan kertas saring.
C. Prosedur Penelitian
1. Persiapan Sampel
Cangkang udang dibersihkan, kemudian dipotong-potong yang selanjutnya disebut sampel.
2. Pembuatan Kitosan Dengan Metode Kimia Murni
Proses pembuatan kitosan umumnya terdiri dari tiga tahap yaitu deproteinasi, demineralisasi dan deasetilasi, tetapi proses pembuatan kitin dari cangkang udang sendiri terdiri atas dua tahap, yaitu: deproteinasi yang merupakan proses
pemisahan protein dari cangkang udang dan demineralisasi yang merupakan proses pemisahan mineral.
2.1. Deproteinasi (Modifikasi Muzzarelly, 1984)
NaOH 3 M dengan perbandingan (1:10). Kemudian sampel diletakkan dalam
penangas air dan didiamkan selama 1 jam pada suhu 900C, sambil dilakukan pengadukan. Setelah itu, dilakukan penyaringan sehingga diperoleh padatan dan filtrat. Padatannya dicuci dengan akuades hingga pH netral, kemudian
dikeringkan menggunakan oven dengan suhu 600C selama 24 jam atau sampai kering. Sehingga diperoleh kitin kasar yang berwarna kuning kemerahan.
2.2. Demineralisasi (Modifikasi Muzzarelly, 1984)
Kitin kasar hasil deproteinasi dimasukkan dalam bejana tahan asam dan basa yang dilengkapi dengan pengaduk dan termometer. Kemudian sampel ditambahkan larutan HCl 2 N dengan perbandingan 1:7 (w/v) dan diletakkan dalam penangas
air selama 2 jam pada suhu 25-300C . Setelah itu, dilakukan penyaringan
sehingga diperoleh padatan dan filtrat. Padatannya dicuci dengan akuades sampai
pH netral, kemudian diletakkan dalam oven pada suhu 600C selama 24 jam atau sampai kering. Sehingga diperoleh kitin.
2.3 Deasetilasi (Modifikasi Muzzarelly, 1984)
Kitin direndam dengan larutan NaOH 20% dengan perbandingan (1:5) selama 1
jam pada suhu 900C, sambil diaduk konstan. Setelah itu dilakukan penyaringan untuk memisahkan padatan dan filtrat. Padatannya dicuci dengan akuades sampai pH netral. Padatan dikeringkan dalam oven dengan suhu 60°C selama 24 jam atau sampai kering. Sehingga diperoleh kitosan. Kitosan yang diperoleh
3. Pembuatan Kitosan Dengan Metode Enzimatis 3.1. Deasetilasi Kimia Sebagian (Emmawati, 2004)
Sebanyak 20 gram tepung kitin komersial direndam dalam NaOH 60% selama 24 jam, kemudian dipanaskan selama 2 jam pada suhu 60°C. Setelah itu dilakukan penyaringan untuk memisahkan padatan dan filtrat. Padatannya dicuci dengan akuades sampai pH netral. Kemudian padatan dikeringkan dalam oven dengan suhu 60°C selama 24 jam atau sampai kering.
3.2. Deasetilasi Enzimatis (Rochima, 2007)
Kitin hasil deasetilasi kimia dilarutkan dalam asam asetat 0,1 M , selanjutnya dicampurkan dengan ekstrak kasar enzim kitin deasetilase sebanyak 100μ L dalam
larutan kitosan 1%. Kemudian di inkubasi pada suhu 55°C selama 24 jam. Serapan dianalisis menggunakan spektrofotometer IR dan ditentukan derajat deasetilasinya.
4. Karakterisasi Kitosan
4.1 Karakterisasi Kitosan dengan Spektrofotometer FTIR
Kitosan yang diperoleh dibaca dengan Spektrofotometer IR. Kitosan dibuat pelet dengan KBr, kemudian dilakukanscanningpada daerah frekuensi antara 4000
cm-1sampai dengan 400 cm-1.
A = log Po/P Dengan : Po = % transmitansi pada garis dasar
P = % transmitansi pada puncak minimum
Perbandingan antara absorbansi pada ν = 1655 cm-1(serapan pita amina) dengan absorbansi ν = 3450 cm-1(serapan pita hidroksi) dihitung untuk N-deasetilasi kitin
yang sempurna (100%) diperoleh A1655 = 1,33. Penggunaan nilai absorbansi puncak yang terkait derajat deasetilasi dapat dihitung dengan cara :
N- deasetilasi = 1- (A1655/A3450 x 1/1,33) x 100% (Bastaman, 1989 dalam Haryanto 1995).
4.2 Kadar Air (AOAC, 1999)
Pengukuran kadar air dilakukan dengan menimbang cawan yang akan digunakan, kemudian dimasukkan sebanyak 1 gram sampel. Selanjutnya dikeringkan dalam oven pada suhu 105°C. Kemudian didinginkan dalam desikator dan ditimbang hingga berat konstan.
Perhitungan :
Kadar air = b–a x 100%
b
4.3 Kadar Abu (AOAC, 1999)
Krus porselin untuk pengabuan ditimbang, kemudian dimasukkan sampel
sebanyak 1 gram dibakar dalam tanur pada suhu 600°C selama 3 jam, selanjutnya didinginkan dalam desikator dan ditimbang setelah mencapai suhu konstan. Perhitungan
Kadar abu = b–a x 100% b
a = berat sampel sesudah dikeringkan b = berat awal sampel
4.4. Kadar Nitrogen (SNI, 1996)
Sebanyak 1 gram kitosan dimasukkan dalam labu kjeldal, kemudian ditambahkan dengan 7 g K2SO4, 0,005 g selenium, 12 ml H2SO4, dan 5 ml H2O2. Kemudian campuran dipanaskan dalam labu kjeldal selama 2 jam pada suhu 4000C dalam lemari asam sampai berhenti mengeluarkan asap, dan cairan menjadi jernih, cairan didinginkan lalu didestilasi dengan penambahan indikator metil merah sebanyak 4 tetes, dan sebagai blangko sebanyak 40 mL asam borat 4% ditambahkan indikator metil merah. Selanjutnya destilat dan blangko dititrasi dengan HCl 0,2 N.
Perhitungan :
A. Simpulan
Berdasarkan hasil dari penelitian, maka dapat diambil kesimpulan bahwa :
1. Kitosan yang diperoleh dari metode kimia memilki kadar air, kadar abu, kadar nitrogen dan derajat deasetilasi berturut - turut 7,39%; 2,10%, 7,%59 dan 71%. 2. Produksi kitosan dari metode enzimatis melalui deasetilasi kimia sebagian
diperoleh derajat deasetilasi 46,68% dan diikuti dengan penambahan enzim CDA memberikan peningkatan derajat deasetilasi menjadi 75,91%.
B. Saran
Winda Rahmawati1, Dian Herasari1, Husniati2
Jurusan Kimia Fakultas Matematika Dan Ilmu Pengetahuan Alam Universitas Lampung1
Baristand Industri Bandar Lampung2 email: ewindathestorm@gmail.com
Abstrak
Telah dilakukan penelitian mengenai produksi kitosan dari cangkang udang dengan dua metode. Uji metode kimia meliputi deproteinasi, demineralisasi, deasetilasi dan metode enzimatis dengan deasetilasi kimia sebagian diikuti dengan penambahan enzim kitin deasetilase. Karakterisasi kitosan yang dihasilkan meliputi kadar air, kadar abu, kadar nitrogen dan derajat deasetilasi. Hasil penelitian menunjukkan bahwa kitosan yang dihasilkan dari metode kimia memiliki kadar air, kadar abu, kadar nitrogen dan derajat deasetilasi berturut– turut 7,39%; 2,10%; 7,59% dan 71%. Sedangkan pada deasetilasi enzimatis, hasil analisis derajat deasetilasi kimia sebagian menggunakan spektrofotometer fourier transform infrared (FTIR) menghasilkan kitosan dengan derajat deasetilasi 46,68 %, diikuti dengan penambahan enzim CDA (Kitin Deasetilase) menghasilkan kitosan dengan derajat deasetilasi 75,91%.
Kata Kunci: derajat deasetilasi, kitosan, kitin deasetilase.
1. Pendahuluan
Indonesia merupakan negara maritim yang kaya akan potensi perikanan seperti udang. Pemanfaatan udang untuk keperluan konsumsi menghasilkan limbah dalam jumlah besar yang belum dimanfaatkan secara komersial.
Sekitar 35% dari cangkang kering udang mengandung kitin. Dari kitin udang dapat dihasilkan sekitar 80% kitosan (No dan Meyer, 1997). Kitin
polielektrolit (Hirano, 1986). Deasetilasi kitin menjadi kitosan dapat dilakukan dengan dua metode, yaitu metode kimia dan enzimatis. Metode kimia lebih mudah dan cepat. Sedangkan pada metode enzimatik digunakan enzim spesifik (misal: enzimkitin deasetilase). Dalam sebuah penelitian pendahuluan dilakukan isolasi enzim kitin deasetilase dari mikroba Aspergillus Aculeatus. Enzim ini bekerja spesifik memotong gugus asetil dari kitin menjadi kitosan, melalui pemutusan ikatan N-asetamido pada kitin dan merubahnya menjadi kitosan (Kafetzopouloset al., 1993).
Berdasarkan uraian diatas, maka dalam penelitian ini akan dilakukan pembuatan kitin dengan metode kimia yang meliputi tahap deproteinasi, demineralisasi dan deasetilasi kitin untuk menghasilkan kitosan. Sedangkan deasetilasi secara enzimatis menggunakan enzim kitin deasetilase, proses deasetilasi enzimatis bersifat selektif dan tidak merusak struktur rantai kitosan, sehingga menghasilkan kitosan dengan karakteristik yang lebih seragam (Tokoyasu et al., 1997) Kitosan yang diperoleh kemudian dikarakterisasi menggunakan Fourier Transform Infrared (FTIR) untuk menganalisis gugus fungsinya.
2. Metode Penelitian 2.1 Bahan dan Alat
Bahan-bahan yang digunakan adalah cangkang udang dari PT. Indokom Samudra Persada, kitin komersial dari PT. Biotech Sukofindo, crude enzim kitin deasetilase dari penelitian pendahuluan mengenai (Isolasi Enzim Kitin Deasetilase Dari Isolat Tanah Humus Aspergillus Aculeatus Dan Identifikasi Enzim Tersebut Dalam Produksi Kitosan, Husniati., dkk), asam klorida pekat (HCl), natrium hidroksida (NaOH), asam asetat (CH3COOH), indikator universal, akuades,
Alat-alat yang digunakan adalah alat gelas, orbital shaker (Memmert),
tabung sentrifuga (eppendorf), autoclave (Sturdy), oven (Memmert), kertas saring, statif, penangas air (Stuart Scientific), batang pengaduk, pipet ukur, pipet volum, tanur, corong, , desikator, bola hisap, neraca analitik, penangas minyak, cawan pengabuan, spektrofotometer fourier transform inframerah (FTIR) merk varian 2000 Scimitar Series , dan spektrofotometetr
fourier transform inframerahShimadzu FTIR -8010PC).
2.2 Preosedur Penelitian
2.2.1 Pembuatan Kitosan Dengan Metode Kimia
Proses pembuatan kitosan terdiri atas tiga tahap yaitu deproteinasi merupakan tahap pemisahan protein, demineralisasi yaitu tahap pemisahan mineral. Dan deasetilasi kitin untuk memperoleh kitosan.
2.2.2 Deproteinasi
Sebanyak 40 gram cangkang udang ditempatkan dalam bejana tahan asam basa yang dilengkapi dengan pengaduk, penangas air dan termometer. Kemudian ditambahkan NaOH 3 M sebanyak 400 ml dengan perbandingan 1:10 (b/v) dan dipanaskan selama 60 menit pada suhu 90 0C sambil di aduk konstan.. Endapan yang diperoleh dicuci dengan menggunakan akuades sampai pH netral. Endapan dikeringkan dalam oven dengan suhu 60 0C selama 24 jam. Kitin kasar yang diperoleh berwarna kuning kemerahan.
2.2.3 Demineralisasi
oven dengan suhu 60 0C selama 24 jam, sehingga diperoleh kitin berwarna kuning kemerahan.
2.2.4 Deasetilasi Kitin
Kemudian kitin dimasukkan dalam larutan NaOH 20 %, lalu dipanaskan pada suhu 90-100 0C sambil diaduk konstan selama 60 menit. Setelah itu didinginkan selama 3 jam pada suhu ruang dan dilakukan penyaringan untuk memisahkan padatan dan cairannya. Padatannya dicuci dengan akuades sampai pH netral. Selanjutnya padatan dikeringkan dalam oven dengan suhu 60 0C selama 24 jam. Hasil yang diperoleh disebut kitosan. Kitosan yang diperoleh di ukur menggunakan spektrofotometer IR.
2.3 Pembuatan Kitosan Dengan Metode Enzimatis
2.3.1 Deasetilasi Kimia sebagian
Sebanyak 20 gram tepung kitin komersial direndam dalam larutan NaOH 60% selama 24 jam, kemudian dipanaskan pada suhu 60 0C selama 2 jam. Kemudian kitin yang diperoleh dicuci dengan akuades hingga pH netral, dan dikeringkan dalam oven dengan suhu 60 0C selama 24 jam.
2.3.2 Deasetilasi Enzimatis
Kitosan hasil deasetilasi kimia sebagian dilarutkan dalam asam asetat 0,1 M. Kemudian dicampurkan enzim CDA sebanyak100 μ L dalam 10 ml larutan kitosan 1% kemudian di inkubasi pada suhu 55 0C selama 24 jam.
2.4 Karakterisasi Kitosan
2.4.1 Pengukuran Spektroskopi IR
Kitosan yang diperoleh dibaca dengan spektrofotometer IR. Kitosan dibuat pelet dengan KBr, kemudian dilakukan scanning pada daerah frekuensi antara 4000 cm-1 sampai
2.4.2 Kadar Air (AOAC 1999)
Dilakukan penimbangan terhadap cawan yang hendak dipakai, kemudian dimasukkan sampel cangkang udang sebanyak 1 gram. Sampel lalu dimasukkan dalam oven pada suhu 1050C selama 3 jam sampai diperoleh berat yang tetap, didinginkan dalam desikator lalu ditimbang. Kadar air dihitung dengan persamaan sebagai berikut:
Perhitungan :
Kadar Air = b- a x 100%
b
a = berat sampel sesudah dikeringkan b = berat awal sampel
2.4.2 Kadar Abu (AOAC 1999)
Krus porselin untuk pengabuan ditimbang, lalu dibakar dalam tanur pada suhu 6000C selama 3 jam, didinginkan dalam desikator lalu ditimbang. Dimasukkan sampel cangkang udang sebanyak 1 gram, lalu dibakar dalam tanur selama 6 jam pada suhu 6000C sampai diperoleh abu berwarna putih.
Perhitungan:
Kadar abu =berat abu(g) x 100%
berat sampel (g)
2.4.3 Derajat Deasetilasi
Derajat deasetilasi ditentukan dari spektrum serapan spektrofotometer IR dengan metode garis dasar. Puncak tertinggi dicatat dan diukur dari garis dasar yang dipilih. Nilai absorbansi dihitung dengan rumus :
A = log P0/P Keterangan;
P0= % transmitansi pada garis dasar P=% transmitansi pada puncak
minimum
Perbandingan antara absorbansi pada
Ѵ= 1655 cm-1 (serapan pita amina)
dengan absorbansi Ѵ= 3450 cm-1
dihitung dengan cara : N-deasetilasi = 1- (A1655/A3450 x 1/1,33) x 100% (Bastaman, 1989, dalam Haryanto, 1955).
3. Hasil dan Pembahasan 3.1 Pembuatan Kitin
Penelitian utama dilakukan untuk mengekstraksi kitin dari cangkang udang melalui proses deproteinasi
menggunakan NaOH dengan
pemanasan tinggi. Deproteinasi bertujuan untuk memutuskan ikatan antara protein dan kitin, dengan cara
menambahkan NaOH. Selama
perendaman, protein terekstrak dalam bentuk Na-asam lemak ( Na-proteinat) akibat reaksi saponifikasi antara lemak yang terkandung dalam cangkang udang dengan larutan NaOH panas, dimana ion Na+ akan mengikat ujung rantai protein yang bermuatan negatif dan mengendap (Suhartono,2000). Deproteinasi dalam penelitian ini dilakukan dengan menggunakan NaOH 3 M dalam waktu 60 menit dan suhu ± 900C.
Setelah dilakukan tahap deproteinasi, endapan yang diperoleh dicuci dengan akuades sampai pH netral, sebagai indikator digunakan pH universal. Pencucian ini dimaksudkan untuk mencegah terjadinya degradasi produk selama proses pengeringan.
Pada tahap demineralisasi, senyawa kalsium akan bereaksi dengan asam klorida yang larut dalam air (Bastaman, 1989) Protein, lemak, fosfor, magnesium, dan besi turut terbuang dalam proses ini. Dalam penelitian ini, demineralisasi dilakukan pada temperatur 25-300C dengan larutan asam klorida 2 M dengan perbandingan (1:7).
Kitosan dihasilkan melalui tahap deasetilasi. Deasetilasi bertujuan untuk memutuskan gugus asetil (−COCH3) yang terdapat pada kitin. Pada penelitian ini, deasetilasi kitin dilakukan dengan merendam kitin selama 60 menit pada suhu 900C menggunakan
Oleh karena itu pada proses deasetilasi digunakan larutan NaOH dengan konsentrasi tinggi (40-60%) untuk mendapatkan kitosan dari kitin.
Berdasarkan hal di atas, deasetilasi kitin menggunakan metode kimia dengan perlakuan suhu 90-100 0C selama 60 menit diperoleh derajat deasetilasi sebesar 71%.
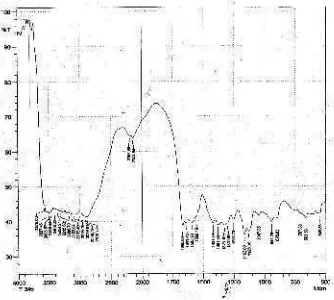
3.2 Penafsiran Spektrum IR kitosan
Gambar 1 menunjukkan hasil identifikasi kitosan menggunakan metode kimia murni dengan pengukuran spektrofotometer FTIR Varian 2000. Hasil identifikasi gugus fungsi terlihat adanya serapan pada bilangan gelombang 3452, 49 cm-1 yang merupakan serapan dari gugus -OH. Gugus –OH digunakan sebagai standar internal dalam kitosan (Mario
et., al2008) sedangkan serapan khas kitosan terlihat pada bilangan gelombang 1666, 50 cm-1 yang merupakan geseran tekuk N-H yang menunjukkan keberadaan amina primer (NH
2). Berikut adalah spektrum IR dari kitosan menggunakan metode kimia murni.
3.3 Deasetilasi Enzimatis
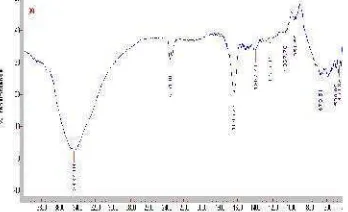
Proses deasetilasi enzimatis dapat meningkatkan derajat deasetilasi 5-30%, tergantung pada derajat deasetilasi awal. Semakin tinggi derajat deasetilasi awal, semakin kecil peningkatan derajat deasetilasi yang terjadi. Sebelumnya kitin dalam bentuk tepung direndam dalam NaOH 60% selama 24 jam, kemudian di panaskan pada suhu 600C selama 2 jam. Penepungan dilakukan agar proses deasetilasi dapat berlangsung lebih cepat dan sempurna, karena semakin luasnya permukaan yang dapat diakses oleh larutan alkali (No dan Meyers, 1997). Hasil pengukuran derajat deasetilasi kitosan kimiawi dengan spektrofotometer IR disajikan pada gambar 2.
Gambar 2. Spektra IR kitosan hasil deasetilasi kimia sebagian hasil pengukuran
spektrofotometer FTIR (-8010PC)
Derajat deasetilasi awal yang rendah menunjukkan banyaknya jumlah residu asetil yang belum terpotong. Lebih banyak residu asetil menunjukkan lebih banyak substrat yang tersedia untuk reaksi enzim. Sesuai dengan kinetika enzim, semakin banyak substrat yang tersedia, laju reaksi akan semakin cepat dan akan menurun jika jumlah substrat berkurang (Suhartono 1989).
Kitin hasil deasetilasi sebagian dilarutkan dalam asam asetat 0,1 M.
pengukuran derajat deasetilasi kitosan enzimatis dengan spektrofotometer IR disajikan pada gambar 3.
Gambar 3. Spektra IR kitosan hasil deasetilasi enzimatis hasil
Pengukuran
spektrofotometer FTIR (-8010PC)
3.4 Kadar Air
Berdasarkan hasil penelitian telah diketahui bahwa kadar air kitosan sebesar 7,59%. Hal ini menunjukkan bahwa kitosan yang dihasilkan memenuhi standar mutu kadar abu yang ditetapkan Spesifikasi Kitosan Niaga (Anonim, 1987) yakni sebesar < 10%. Kadar air tidak dipengaruhi oleh konsentrasi NaOH serta suhu deasetilasi yang digunakan. Hal ini disebabkan kadar air yang terkandung pada kitosan dipengaruhi oleh proses pengeringan, lama pengeringan yang dilakukan, jumlah kitosan yang dikeringkan dan luas permukaan tempat kitosan dikeringkan (Saleh et al., 1994).
3.5 Kadar Abu
pelarut asam klorida (HCl) dapat mengikat mineral secara sempurna. Jika pengadukan yang dilakukan tidak konstan maka panas yang dihasilkan tidak merata, sehingga reaksi pengikatan mineral oleh pelarut juga akan tidam sempurna (Hartati FK et al., 2002). Selain itu proses pencucian yang baik hingga diperoleh pH netral juga berpengaruh terhadap kadar abu. Mineral yang terlepas dari sampel akan berikatan dengan pelarut dapat terbuang dan larut bersama air (Angka dan Suhartono, 2000).
4. Simpulan
Berdasarkan hasil penelitian dapat disimpulkan bahwa karakteristik kitosan yang meliputi kadar air, kadar abu, dan derajat deasetilasi masing-masing adalah 7,39%, 2,10%, dan derajat deasetilasi kimia murni sebesar 71%. Berdasarkan pengamatan spektrofotometer IR menunjukkan adanya kitosan hasil deasetilasi sebagian yang terdeteksi pada daerah serapan amina primer dengan bilangan gelombang 1645,77 cm-1, dan setelah penambahan enzim CDA menghasilkan kitosan yang terdeteksi pada daerah serapan 1636,50 cm-1.
5. Ucapan Terima Kasih
Penulis mengucapkan terima kasih atas dukungan dana penelitian dari Program Kegiatan Insentif PKPP 2011 Kementrian Riset dan Teknologi melalui penelitian pembuatan kitosan dan nano partikel kitosan dengan tripoli fosfat dari limbah cangkang udang (crustaceae) dan aplikasinya sebagai bahan memperpanjang shelf-life produk buah segar dan buah kaleng dengan No. Kontrak 12/SPK/RISTEK/BPKIMI/03/2011 tanggal 3 Maret 2011.
Angka, S.L. dan M.T. Suhartono, 2000. Pemanfaatan Limbah Hasil Laut. IPB.Bogor
AOAC. 1999. Official Methods of Analysis of AOAC International. 5th Revision. Volume 2. Cunnif P(Editor). Maryland : AOAC International.
Bastaman S. 1989. Studies On Degradation and Extraction of Chitin and Chitosan From Prawn Shells. Belfast: The Departement Of Mechanical Manufacturing , Aeronautical and Chemical Engineering. The Queen’s University
Hartati FK, Susanto.T, Rakhmadiono S, Adi Loekito S. 2002. Faktor-faktor yang berpengaruh terhadap tahap deproteinasi Menggunakan Enzim Protease dalam Pembuatan Kitin dan Kitosan dari cangkang Rajungan (Portunus Pelagius). Jurnal Biosain. Vol 2:1
Hirano, S. 1986. Chitin and Chitosan. Ulmann’s Encyclopedia of Industrial Chemistry.Republicka of Germany. 5th . ed. A 6: 231 – 232.
Kafetzhopoulos D, Martinou A, Bouriotis V. 1993. Bioconversion of chitin to chitosan: purification and characterization of chitin deacetylase from Mucor Rouxii.
Proc Natl Acad Scii USA 90:2564-2568.
Mario, F. D., P. Rapan’a, U. Tomati, E. Galli.2008. Chitin and Chitosan from Basidomycetes. Intern.
Journal of Biological Macromolecules,4:8-12
No, H.K., S.P. Meyers, K.S. Lee, 1989. Isolation abd Characterization of chitin frow Crawfish Shell Waste,J. Agri. Food Chem., 37:575-579
Saleh MR, Abdillah, Suerman E, Basmal J, Indriati N.1994. Pengaruh Suhu, waktu dan konsentrasi pelarut pada Ekstraksi Kitosan dari Limbah Pengolahan Udang Beku Terhadap Beberapa Parameter Mutu Kitosan. Jurnal Pasca Panen Perikanan 81:30-43
Tsigos I, Bouriotis V. 1995. Purification and Characterization of Chitin Deacetylase fromColletotrichum Lindemuthianum.The Journal Of Biological Chemistry270: 26286-26291.
Tsigos, I., A. Martinou, Kafetzopoulos and V. Bouriotis. 2000. Chitin deacetylases: New versatile tools in biotechnology.TIBTECH Rev,18: 305-312.
Tokuyasu K, Ono H, Kameyama MO, Hayashi K, Moil Y. 1997. Deacetylation of Chitin Oligosaccharides of dp 2-4 by Chitin Deascetylase from
Colletotrichum Lindemuthianum. Carbohydrate Research
Sesungguhnya bersama kesulitan ada kemudahan (Q.S.
Al-insyirah ayat 8)
Barangsiapa yang menempuh perjalanan dengan tujuan untuk menuntut ilmu, niscaya Allah akan memudahkan jalan ke surga
(HR Muslim)
Berani hidup berarti berani menderita. Bila takut menderita, sebaiknya batalkan hidupmu sekarang juga. Ketahuilah bahwa tidak
ada tempat lagi bagi orang yang takut menderita di dunia ini karena penderitaan adalah syarat dari kehidupan
(Fidi Mahendra)
Sesungguhnya kamu melalui tingkat demi tingkat dalam kehidupan (QS Al Insyiqaaq : 19)
Syukuri apa yang ada hidup adalah anugerah, tetap jalani hidup ini melakukan yang terbaik
(D'Masiv)
Kupersembahkan karya sederhana ini kepada :
Kedua orang tuaku Markum dan Mariyem yang selalu menjadi motivator utamaku, terima kasih atas doa, nasihat
dan kasih sayang tulus yang kau berikan sehingga mampu
menguatkan aku di saat-saat sulit
.
Kakak dan mbak ku tersayang
Yuli Efendi,Subiyanto, Sukron, Sofardana Ganda Herlani, Siti Kholifah, Siti Nurul Khamimah, Siti Nur Halimah, dan Heridini Harianti. Serta Ponakanku tersayang Sayyidati Nur Aulia Rahma, Nur Muhammad Nabil Al Qarni, Helga
Muharani Irbah Efendi, dan Muhammad Haziq Faizi.
Dian Herasari, M.Si, Husniati, M.S.i., dan Prof. Dr. John Hendri, M.S. terima kasih untuk bimbingannya selama ini.
Segenap Keluarga besarku yang selalu menyemangati dan mendoakan keberhasilanku.
Sahabat ku 2007 yang selalu berbagi kebahagiaan.
Seseorang yang kelak akan mendampingiku,
Assalamu'alaikum Wr.Wb
Segala puja dan puji syukur hanyalah milik Allah SWT, karena atas rahmat, hidayah, dan kehendak-Nya skripsi ini dapat diselesaikan.
Skripsi dengan judul“Produksi Kitosan Dari Bahan Baku Cangkang
Udang Menggunakan Metode Kimia Dan Enzimatis Dengan Enzim
Kitin Deasetilase . Shalawat teriring salam selalu tercurah kepada Nabi
2. Ibu Dian Herasari, M.Si., selaku Pembimbing Utama yang telah banyak memberikan ilmu pengetahuan, bimbingan, gagasan, kritik dan saran dalam proses penyelesaian skripsi ini.
3. Ibu Husniati, M.Si., selaku Pembimbing Kedua yang telah memberikan bimbingan, masukan dan kritikan, serta arahan yang diberikan kepada penulis sehingga skripsi ini terselesaikan dengan baik.
4. Bapak Prof. Dr. John Hendri, M.S., selaku pembahas yang telah banyak memberi kritikan, masukan, dan saran sehingga skripsi ini dapat terselesaikan dengan baik.
5. Bapak Prof. Suharso, Ph.D. selaku Pembimbing Akademik atas kesediaannya untuk memberikan bimbingan, bantuan, nasehat dan informasi dalam penyelesaian studi.
6. Bapak Andi Setiawan, Ph.D., selaku Ketua Jurusan Kimia Fakultas MIPA Universitas Lampung.
7. Seluruh dosen FMIPA Unila yang telah mendidik dan memberikan ilmu pengetahuan yang sangat bermanfaat kepada penulis selama masa kuliah. 8. Kedua orang tuaku yang sangat aku sayangi dan cintai. Ibu dan Bapak yang
yang telah diberikan kepadaku yang takkan bisa aku ganti dengan apapun. 9. Kepada kakak ku Subiyanto, Yuli Efendi, Sukron, Sofardana Ganda Herlani,
dan Mbak ku Siti Kholifah, Heridini Harianti, Siti Nurul Khamimah, Siti Nur Halimah yang selalu mendorongku untuk terus maju, dan selalu mendoakan keberhasilnku, semoga amal baikmu dapat menjadi cahaya yang menerangi setiap langkahku. Tak lupa kepada keponakanku yang aku sayangi Sayyidati Nur Aulia Rahma, Nur Muhammad Nabil AL Qarni, Helga Muharani Irbah Efendi, dan Muhammad Haziq Faizi. Terima kasih atas senyum tulus kalian yang diberikan kepada penulis, dan motivasi kalian semua, kehadiran kalian adalah hal yang tidak ternilai harganya dalam hidupku. Semoga Allah yang memberikan balasanny.
10. Keluarga besarku yang selalu memberikan motivasi, dukungan.dan doa untuk keberhasilanku.
Karlin S.Si, Mb Uyun S.Si, Mb Okta 05, Kak Eko S.Si, Gunadi S.Si, Dwi Fitrian S.Si, Astri Rahayu terima kasih atas kebersamaan, dukungan, dan segala bantuannya. Tetap semangat dan jangan menyerah, perjuangan kita masih panjang, dan sukses selalu untuk kita.
13. Teman – teman kimia 2008 Albert S. Si, Eli S.Si, Ani S.Si, Sundari S.Si, Ade S.Si, Putu, S.Si, Ramdan S.Si, Riki, Majid, Sri, Ayu, Novi, Nanda, Puji. 14. Teman- teman kimia 2008, 2009, 2010, 2011 dan seluruh orang yang telah membantu dalam proses penyelesaian skripsi ini, serta teman-teman yang tidak dapat disebutkan satu per satu, terima kasih atas dukungannya dan segala bantuannya.
15. Almamater tercinta.
Akhir kata, penulis menyadari bahwa skripsi ini masih jauh dari kesempurnaan, akan tetapi sedikit harapan semoga skripsi yang sederhana ini dapat berguna dan bermanfaat bagi kita semua. Amiin.
Bandar Lampung, 8 Agustus 2012 Penulis