VARIASI SPASIAL DAN TEMPORAL KUALITAS AIR
DALAM WILAYAH PELABUHAN TANJUNG PRIOK
DAN PERAIRAN MUARA GEMBONG (Dumping Site)
TAHUN 2005
IRMA HARDIANI
DEPARTEMEN MANAJEMEN SUMBERDAYA PERAIRAN
FAKULTAS PERIKANAN DAN ILMU KELAUTAN
INSTITUT PERTANIAN BOGOR
BOGOR
PERNYATAAN MENGENAI SKRIPSI DAN
SUMBER INFORMASI
Dengan ini saya menyatakan bahwa skripsi Variasi Spasial dan Temporal Kualitas Air Dalam Wilayah Pelabuhan Tanjung Priok dan Perairan Muara Gembong (Dumping Site) Tahun 2005 adalah benar merupakan hasil karya saya sendiri dan belum diajukan dalam bentuk apapun kepada perguruan tinggi manapun. Semua sumber data dan informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir skripsi ini.
Bogor, Agustus 2006
ABSTRAK
IRMA HARDIANI. Variasi Spasial dan Temporal Kualitas Air Dalam Wilayah Pelabuhan Tanjung Priok dan Perairan Muara Gembong (Dumping Site) Tahun 2005. Dibimbing oleh ARIO DAMAR dan M.MUKHLIS KAMAL.
Tujuan penelitian ini untuk mengetahui kondisi kualitas air pada wilayah pelabuhan Tanjung Priok dan perairan Muara Gembong (Dumping Site) secara spasial dan temporal berdasarkan parameter fisika, kimia dan biologi.
Pengambilan sampel oleh JICA Study Team, dilakukan pada bulan Juni dan Oktober 2005. Parameter kualitas air meliputi: parameter físika (suhu, salinitas, dan total suspensi), kimia (minyak, derajat keasaman, oksigen terlarut,
Biochemical Oxygen Demand, Chemical Oxygen Demand, total nitrogen,
ammonium, total fosfat, kadmium, kromium, timbal, arsen, merkuri dan sianida) dan biologi (total coliform). Analisis data meliputi analisis deskriptif kualitas air; Indeks STORET; hubungan antar parameter físika, kimia dan biologi; uji nilai tengah; dan Indeks Similaritas Canberra.
Parameter DO dengan kisaran 0,00-1,77 mg/l (permukaan); 0,40-1,32 mg/l (tengah); 0,00-1,24 mg/l (dasar), total fosfat dengan kisaran 0,0009-1,6892 mg/l (permukaan); 0,0210-1,6010 mg/l (tengah); 0,0390-1,7970 mg/l (dasar) dan total coliform dengan kisaran 1600-1601 MPN/100ml (permukaan); 900-1601 MPN/100ml (tengah dan dasar) pada perairan pelabuhan Tanjung Priok di bulan Juni 2005 tidak sesuai dengan baku mutu untuk biota laut. Pada perairan Muara Gembong, parameter yang melampaui baku mutu biota laut adalah total fosfat di tiap lapisan dan total coliform di lapisan tengah dan dasar.
VARIASI SPASIAL DAN TEMPORAL KUALITAS AIR
DALAM WILAYAH PELABUHAN TANJUNG PRIOK
DAN PERAIRAN MUARA GEMBONG (Dumping Site)
TAHUN 2005
IRMA HARDIANI
SKRIPSI
Sebagai salah satu syarat untuk memperoleh gelar Sarjana Perikanan pada
Departemen Manajemen Sumberdaya Perairan
DEPARTEMEN MANAJEMEN SUMBERDAYA PERAIRAN
FAKULTAS PERIKANAN DAN ILMU KELAUTAN
INSTITUT PERTANIAN BOGOR
BOGOR
LEMBAR PENGESAHAN
Judul Proposal : Variasi Spasial dan Temporal Kualitas Air Dalam Wilayah Pelabuhan Tanjung Priok dan Perairan Muara Gembong (Dumping Site) Tahun 2005
Nama mahasiswa : Irma Hardiani
NIM : C 24102078
Disetujui,
Pembimbing I Pembimbing II
Dr. Ir. Ario Damar, M.Si Dr. Ir. M. Mukhlis Kamal, M.Sc NIP. 131 878 933 NIP. 132 084 932
Mengetahui
Dekan Fakultas Perikanan dan Ilmu Kelautan
Dr. Ir. Kadarwan Soewardi NIP. 130 805 031
PRAKATA
Segala puji syukur dipanjatkan kehadirat Allah SWT yang telah memberikan berkah, rahmat serta karunia-Nya sehingga skripsi dengan judul “Variasi Spasial dan Temporal Kualitas Air Dalam Wilayah Pelabuhan Tanjung Priok dan
Perairan Muara Gembong (Dumping Site) Tahun 2005” ini dapat diselesaikan oleh penulis.
Penulis mengucapkan terima kasih kepada :
1. Dr. Ir. Ario Damar, M.Si dan Dr. Ir. M. Mukhlis Kamal, M.Sc, selaku komisi pembimbing yang telah memberikan masukan, arahan dan bimbingan selama penyusunan skripsi ini.
2. Dr. Ir. Yusli Wardiatno, M.Sc selaku pembimbing akademik yang telah memberikan arahan dan bimbingan selama penulis menjalani studi.
3. Keluargaku (papah, mamah dan kakak) yang selalu memberikan kasih sayang, doa serta dukungannya kepada penulis.
4. Wahyu Hidayati, atas kerja sama, kesabaran dan bantuannya.
5. Teman-teman MSP’39 atas kasih sayang dan bantuannya. Kalian merupakan teman dan keluarga yang sangat berarti bagi penulis.
6. Kakak kelas MSP’37 dan MSP’38 serta adik-adik kelasku MSP’40 dan MSP’41 atas bantuanya.
7. Semua pihak yang telah membant u penulis dan tidak dapat disebutkan satu persatu.
Bogor, Agustus 2006
DAFTAR ISI
3.4.1. Analisis Deskriptif Kualitas Air ... 23
3.4.2. Indeks STORET ... 23
3.4.3. Hubungan Antar Parameter Fisika, Kimia dan Biologi ... 25
3.4.4. Uji Nilai Tengah ... 25
IV. HASIL DAN PEMBAHASAN ... 27
4.1. Kondisi Fisika, Kimia dan Biologi Perairan ... 27
4.1.1. Suhu... 27
4.2. Evaluasi Kualitas Air Perairan Pelabuhan Tanjung Priok dan Perairan Muara Gembong dengan Indeks STORET ... 63
4.3. Kesamaan Antar Stasiun Berdasarkan Parameter Fisika-Kimia ... 65
4.3.1. Kesamaan antar stasiun pada bulan Juni 2005 ... 65
4.3.1.1. Kesamaan antar stasiun pada perairan pelabuhan Tanjung Priok ... 65
4.3.1.2. Kesamaan antar stasiun pada perairan Muara Gembong... 69
4.3.2. Kesamaan antar stasiun pada bulan Oktober 2005... 72
4.3.2.1. Kesamaan antar stasiun pada perairan pelabuhan Tanjung Priok ... 72
4.3.2.2. Kesamaan antar stasiun pada perairan Muara Gembong... 76
DAFTAR TABEL
Halaman
1. Koordinat titik pengambilan sampel ... 18
3. Parameter kualitas air yang diamati ... 22
4. Penentuan sistem nilai untuk menentukan status mutu air... 24
DAFTAR GAMBAR
Halaman
1. Skema perumusan masalah ... 3 2. Lokasi pengambilan sampel perairan pelabuhan Tanjung Priok ... 19 3. Lokasi pengambilan sampel perairan Muara Gembong... 20 4. Suhu di tiap lapisan perairan pelabuha n Tanjung Priok
(stasiun 6-25) dan perairan Muara Gembong (stasiun 1-5) pada
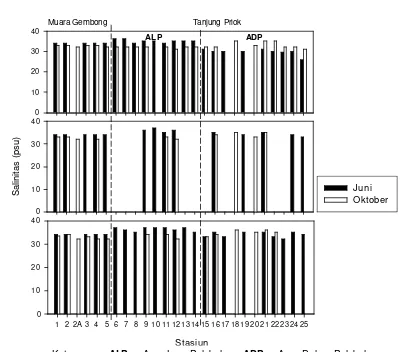
bulan Juni dan Oktober 2005 ... 28 5. Salinitas di tiap lapisan perairan pelabuhan Tanjung Priok
(stasiun 6-25) dan perairan Muara Gembong (stasiun 1-5) pada
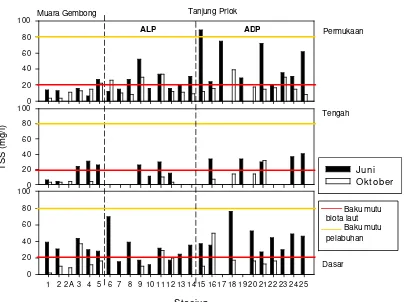
bulan Juni dan Oktober 2005 ... 30 6. Konsentrasi TSS di tiap lapisan perairan pelabuhan Tanjung Priok
(stasiun 6-25) dan perairan Muara Gembong (stasiun 1-5) pada
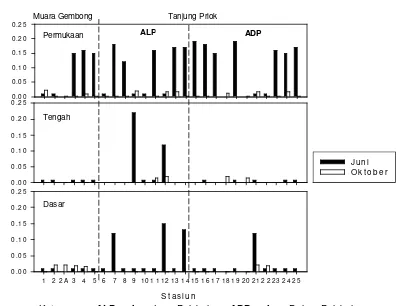
bulan Juni dan Oktober 2005 ... 32 7. Konsentasi minyak di tiap lapisan perairan pelabuhan Tanjung Priok
(stasiun 6-25) dan perairan Muara Gembong (stasiun 1-5) pada
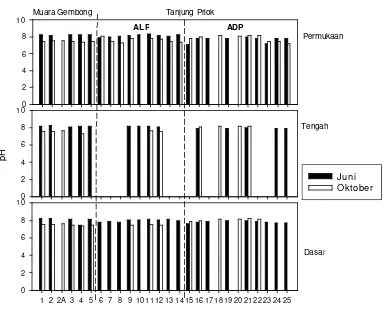
bulan Juni dan Oktober 2005 ... 32 8. Nilai pH di tiap lapisan perairan pelabuhan Tanjung Priok
(stasiun 6-25) dan perairan Muara Gembong (stasiun 1-5) pada
bulan Juni dan Oktober 2005 ... 36 9. Konsentrasi DO di tiap lapisan perairan pelabuhan Tanjung Priok
(stasiun 6-25) dan perairan Muara Gembong (stasiun 1-5) pada
bulan Juni dan Oktober 2005... 38 10. Konsentrasi BOD di tiap lapisan perairan pelabuhan Tanjung Priok
(stasiun 6-25) dan perairan Muara Gembong (stasiun 1-5) pada
bulan Juni dan Oktober 2005 ... 40 11. Konsentrasi COD di tiap lapisan perairan pelabuhan Tanjung Priok
(stasiun 6-25) dan perairan Muara Gembong (stasiun 1-5) pada
bulan Juni dan Oktober 2005 ... 43 12. Konsentrasi total nitrogen di tiap lapisan perairan pelabuhan
Tanjung Priok(stasiun 6-25) dan perairan Muara Gembong
(stasiun 1-5) pada bulan Juni dan Oktober 2005... 45 13. Konsentrasi ammonium di tiap lapisan perairan pelabuhan
Tanjung Priok(stasiun 6-25) dan perairan Muara Gembong
(stasiun 1-5) pada bulan Juni dan Oktober 2005... 47 14. Konsentrasi total fosfat di tiap lapisan perairan pelabuhan
Tanjung Priok(stasiun 6-25) dan perairan Muara Gembong
(stasiun 1-5) pada bulan Juni dan Oktober 2005... 49 15. Konsentrasi kadmium di tiap lapisan perairan pelabuhan
(stasiun 1-5) pada bulan Juni dan Oktober 2005 ... 51 16. Konsentrasi kromium di tiap lapisan perairan pelabuhan
Tanjung Priok(stasiun 6-25) dan perairan Muara Gembong
(stasiun 1-5) pada bulan Juni dan Oktober 2005... 53 17. Konsentrasi Arsen di tiap lapisan perairan pelabuhan
Tanjung Priok(stasiun 6-25) dan perairan Muara Gembong
(stasiun 1-5) pada bulan Juni dan Oktober 2005... 56 18. Konsentrasi Merkuri di tiap lapisan perairan pelabuhan
Tanjung Priok(stasiun 6-25) dan perairan Muara Gembong
(stasiun 1-5) pada bulan Juni dan Oktober 2005... 58 19. Konsentrasi Sianida di tiap lapisan perairan pelabuhan
Tanjung Priok(stasiun 6-25) dan perairan Muara Gembong
(stasiun 1-5) pada bulan Juni dan Oktober 2005... 59 20. Total coliform di tiap lapisan perairan pelabuhan
Tanjung Priok(stasiun 6-25) dan perairan Muara Gembong
(stasiun 1-5) pada bulan Juni dan Oktober 2005... 61 21. Evaluasi kualitas air di perairan pelabuhan Tanjung Priok dan
perairan Muara Gembong pada bulan Juni dan Oktober 2005... 63 22. Dendrogram kesamaan antar stasiun di lapisan permukaan perairan
pelabuhan Tanjung Priok pada bulan Juni 2005 ... 66 23. Dendrogram kesamaan antar stasiun di lapisan tengah perairan
pelabuhan Tanjung Priok pada bulan Juni 2005 ... 67 24. Dendrogram kesamaan antar stasiun di lapisan dasar perairan
pelabuhan Tanjung Priok pada bulan Juni 2005 ... 68 25. Dendrogram kesamaan antar stasiun di lapisan permukaan perairan
Muara Gembong pada bulan Juni 2005... 70 26. Dendrogram kesamaan antar stasiun di lapisan tengah perairan
Muara Gembong pada bulan Juni 2005... 71 27. Dendrogram kesamaan antar stasiun di lapisan dasar perairan
Muara Gembong pada bulan Juni 2005... 72 28. Dendrogram kesamaan antar stasiun di lapisan permukaan perairan
pelabuhan Tanjung Priok pada bulan Oktober 2005 ... 73 29. Dendrogram kesamaan antar stasiun di lapisan tengah perairan
pelabuhan Tanjung Priok pada bulan Oktober 2005 ... 74 30. Dendrogram kesamaan antar stasiun di lapisan dasar perairan
pelabuhan Tanjung Priok pada bulan Oktober 2005 ... 75 31. Dendrogram kesamaan antar stasiun di lapisan permukaan perairan
32. Dendrogram kesamaan antar stasiun di lapisan tengah perairan
Muara Gembong pada bulan Oktober 2005 ... 77 33. Dendrogram kesamaan antar stasiun di lapisan dasar perairan
DAFTAR LAMPIRAN
Halaman
1. Data pasang surut pada bulan Juni dan Oktober 2005 ... 86
2. Kep. Men. LH No.51 Tahun 2004 ... 87
3. Contoh analisis uji nilai tengah ... 88
4. Hubungan antar parameter ... 90
5. Kandungan bahan organik dalam sedimen pada bulan Juni dan Oktober 2005 ... 96
6. Jenis kegiatan industri di sekitar sungai Ancol dan Sunter yang bermuara ke perairan pelabuhan Tanjung Pirok ... 98
7. Analisis Indeks STORET ... 99
I. PENDAHULUAN
1.1. Latar Belakang
Perairan pelabuhan Tanjung Priok merupakan pelabuhan terbesar di Indonesia yang terletak di pantai utara Pula u Jawa, tepatnya di Daerah Khusus Ibukota Jakarta, dengan posisi geografis 1060 52’ BT dan 60 6’ LS (Latif 2003). Pelabuhan ini sebagai tempat keluar masuknya kapal-kapal internasional dan domestik, sehingga potensi pencemaran di perairan pelabuhan ini cukup tinggi. Sumber pencemaran dapat berasal dari kegiatan industri, kegiatan pelabuhan (transportasi laut, bongkar muat kapal, pembuangan jangkar dan pembuangan air
ballast) dan kegiatan pengerukkan sedimen kolam pelabuhan yang kemudian membuang hasil pengerukkan ke perairan Muara Gembong. Selain itu, pencemaran juga dapat berasal dari sungai-sungai yang bermuara ke perairan pelabuhan Tanjung Priok. Karena pada umumnya, air sungai banyak sekali mengangkut cemaran hasil berbagai aktivitas manusia di darat. Selain itu, faktor alam seperti musim dan arus dapat mempengaruhi kondisi suatu perairan. Hal ini dikarenakan musim dapat mempengaruhi masuknya bahan-bahan pencemar baik yang berasal dari daratan maupun dari udara. Berdasarkan LAPI ITB (2001) bahwa pola arus di perairan pelabuhan Tanjung Priok bergerak dari dalam kolom pelabuhan menuju ke luar pelabuhan.
Peristiwa pencemaran perairan di wilayah pelabuhan Tanjung Priok tidak hanya terjadi pada saat ini, melainkan diindikasikan telah terjadi sejak tahun 1993. Hal ini ditunjang dengan penelitian yang dilakukan oleh Ciptaningtyas (1993), bahwa pada saat penelitian dilakukan, kondisi perairan wilayah Tanjung Priok telah mengalami pencemaran tinggi. Hal ini dapat terlihat dari tingkat kecerahan yang rendah, kadar TSS, DO, COD, BOD5, deterjen serta kandungan minyak yang
telah melewati ambang batas yang telah ditetapkan. Selain itu, ditemukan pula adanya logam berat dalam jumlah yang tinggi.
berpotensi mencemari perairan Muara Gembong adalah sedimen atau lumpur dari hasil pengerukan kolam pelabuhan Tanjung Priok, karena sedimen atau lumpur yang dibuang ini dilaporkan mengandung logam berat dengan kadar ya ng cukup tinggi (Perumpel 1990, dalam Bengen et al., 1994).
Pencemaran yang terjadi di perairan pelabuhan Tanjung Priok dan perairan Muara Gembong dapat menyebabkan terjadinya penurunan kualitas air sehingga akan memberikan dampak negatif baik bagi ekologi maupun bagi manusia yang memanfaatkan air tersebut dalam kehidupan sehari-hari. Jumlah bahan organik yang tinggi menyebabkan bakteri dan spesies invertebrata dalam jumlah terbatas, akumulasi logam berat dalam tubuh ikan menyebabkan kematian pada ikan dan kematian pada manusia yang mengkonsumsi ikan tersebut, juga dapat terjadinya
blooming algae.
Untuk dapat terus menunjang kegiatan pelabuhan di wilayah perairan Tanjung Priok, dalam waktu dekat ini pelabuhan Tanjung Priok akan mengalami rehabilitasi, seperti: pembongkaran dan relokasi breakwater, pembuang sedimen hasil pengerukan kolam pelabuhan ke perairan Muara Gembong (dumping site)
dan pemindahan dumping site dari perairan Muara Gembong ke perairan Tanjung Karawang. Dari kegiatan-kegiatan tersebut dapat menyebabkan perubahan kualitas perairan dan pencemaran perairan. Untuk itu perlu adanya upaya pengelolaan lingkungan perairan yaitu dengan memperkecil pengaruh atau dampak negatif dari pencemaran tersebut agar masyarakat dapat memanfaatkan perairan tersebut secara berkesinambungan. Hal yang mendasar dalam menunjang upaya tersebut adalah dengan adanya pengetahuan mengenai kondisi kualitas air pada wilayah pelabuhan Tanjung Priok dan perairan Muara Gembong.
1.2. Perumusan Masalah
bahan-bahan pencemar ke perairan berupa minyak, limbah domestik dan industri serta logam berat. Pengetahuan mengenai kondisi kualitas perairan sebagai faktor penunjang dalam melakukan upaya pengelolaan lingkungan perairan pelabuhan Tanjung Priok dan perairan Muara Gembong.
Gambar 1. Skema perumusan masalah
1.3. Tujuan dan Manfaat
Penelitian ini bertujuan untuk mengetahui kondisi kualitas air pada wilayah pelabuhan Tanjung Priok dan perairan Muara Gembong (dumping site) secara spasial dan temporal berdasarkan parameter fisika, kimia dan biologi. Dari hasil penelitian ini, diharapkan dapat dijadikan bahan pertimbangan dalam pengelolaan sumberdaya perairan di pelabuhan Tanjung Priok dan perairan Muara Gembong.
Perubahan kualitas air Anthropogenik :
- Kegiatan industri - Kegiatan pelabuhan (transportasi laut, bongkar muat kapal, pembuangan jangkar dan air ballast serta pengerukkan pelabuhan
Fisika Kimia Biologi Faktor alam:
- Arus - Musim
II. TINJAUAN PUSTAKA
2.1. Parameter Fisika
2.1.1. Pasang Surut
Air pada bagian ujung pantai yang berbatasan dengan lautan tidak pernah diam pada suatu ketinggian yang tetap, tetapi selalu bergerak naik dan turun sesuai dengan siklus pasang. Fenomena pasang surut itu sendiri merupakan suatu fenomena naik turunnya paras laut (sea-level) secara berkala akibat gaya tarik benda-benda angkasa, terutama oleh bulan dan matahari (Pariwono 1989). Peristiwa dari adanya pasang surut ini merupakan salah satu proses sirkulasi air di lautan. Permukaan air laut yang perlahan- lahan naik sampai pada ketinggian maksimum, peristiwa ini dinamakan pasang tinggi (high water), kemudian permukaan air laut tersebut turun sampai kepada suatu ketinggian minimum yang disebut dengan pasang rendah (low water). Menurut Rustandi (1993) bahwa pada kurun waktu antara air surut dan air pasang (berkisar antara 6-12 jam), massa air laut mengalir dari laut lepas ke muara sungai. Begitu pula sebaliknya, pada kurun waktu antara air pasang dan air surut massa air laut akan mengalir kembali ke laut.
Kondisi pasang surut di perairan pelabuhan Tanjung Priok pada umumnya bersifat harian tunggal, yaitu satu kali pasang dan satu kali surut dalam satu hari. Rata-rata naik turun tinggi gelombang yaitu sebesar 1 meter (Ciptaningtyas 1993). Kondisi pasang surut perairan pelabuhan Tanjung Priok pada bulan Juni dan Oktober 2005 berdasarkan Dinas Oseanografi TNI-AL (2005) terlampir dalam Lampiran 1.
2.1.2. Suhu
Suhu merupakan energi panas yang dihasilkan dari proses penyerapan cahaya matahari yang biasa dinyatakan dalam satuan derajat Celcius (oC). Proses penyerapan ini berlangsung intensif pada bagian permukaan air, dengan demikian suhu pada bagian permukaan air lebih panas dibandingkan pada bagian bawah air. Berdasarkan Nontji (2005) bahwa suhu air permukaan di perairan Nusantara Indonesia umumnya berkisar antara 28–31 oC, dan suhu di lapisan permukaan hangat akibat dari kerja angin sehingga lapisan teratas sampai kedalaman kira-kira 50-70 m terjadi pengadukan yang kemudian bersifat homogen. Selain angin, faktor- faktor lain yang dapat mempengaruhi suhu di suatu perairan adalah musim, lintang, waktu dalam satu hari, penutupan awan dan aliran serta kedala man dari badan air (Effendi 2003).
Keberadaan suhu di suatu perairan dapat mempengaruhi kehidupan (metabolisme) dan penyebaran organisme akuatik, selain itu suhu juga dapat mempengaruhi kelarutan gas-gas dalam air terutama oksigen. Proses metabolisme suatu organisme akan meningkat dengan meningkatnya suhu sebesar 10 oC (Nybakken 1992). Effendi (2003) menyatakan bahwa kelarutan gas- gas H2, N2,
CO2 dan O2 akan menurun dengan meningkatnya suhu di perairan.
2.1.3. Salinitas
Salinitas pada berbagai tempat di lautan terbuka yang jauh dari daerah pantai variasinya sempit, biasanya berkisar antara 34-37 ‰. Namun pada umumnya salinitas pada perairan laut adalah sebesar 35 ‰ (Nybakken 1992). Salinitas pada perairan laut dapat dipengaruhi oleh penguapan, presipitasi dan run off dari tanah-tanah di daratan. Menurut Sedyowati (2005), faktor yang menyebabkan salinitas berfluktuasi adalah topografi pasang surut, serta jumlah air tawar yang masuk ke perairan laut. Air tawar yang masuk ke perairan laut dapat berasal dari air sungai dan hujan, pada musim peralihan dari musim kemarau ke musim hujan memiliki curah hujan lebih tinggi dibandingkan dengan musim kemarau, namun kedua musim ini cenderung memiliki karakteristik yang sama (Tomascik et al., 1997).
2.1.4. Total Suspended Solid (TSS)
Padatan tersuspensi total (Total Suspended Solid/TSS) adalah bahan-bahan tersuspensi (diameter > 1 µ m) yang tertahan pada saringan millipore dengan diameter pori 0,45 µ m. TSS terdiri dari lumpur dan pasir halus serta jasad-jasad renik. Penyebab nilai TSS yang utama adalah dari kikisan tanah atau erosi tanah yang terbawa ke badan air (Effendi 2003) . Pada umumnya nilai TSS akan berbanding lurus dengan kekeruhan, oleh sebab itu nilai TSS yang tinggi akan menghalangi penetrasi cahaya ke dalam perairan sehingga dapat mempengaruhi proses fotosintesis. Pada air laut TSS biasanya cenderung tinggi karena banyaknya jumlah padatan total seperti kandungan garam- garam pada air laut. Berdasarkan Keputusan Menteri Lingkungan Hidup No. 51 tahun 2004 bahwa perairan laut yang diperuntukan bagi kehidupan biota laut dan kegiatan pelabuhan adalah masing- masing sebesar 20 mg/l dan 80 mg/l
2.2. Parameter Kimia
2.2.1. Minyak
senyawa-senyawa volatile yang segera dapat menguap dan setelah beberapa hari sebanyak 25 % dari volume minyak akan hilang karena menguap. Tetapi sisa minyak yang tidak menguap akan mengalami emulsifikasi yang mengakibatkan air dan minyak dapat bercampur (Fardiaz 1992).
Minyak tersebar di perairan dalam bentuk terlarut, lapisan film yang tipis di permukaan, emulsi dan fraksi terserap. Minyak dengan massa yang rendah cenderung untuk diserap oleh partikel pasir, lumpur, tanah liat, organisme laut serta baha n-bahan tersuspensi yang ada di laut (Barnes 1975).
Pencemaran minyak yang terjadi pada perairan laut secara langsung berasal dari kapal-kapal yang ada di pelabuhan. Kapal-kapal yang ada di pelabuhan biasanya mengangkut minyak dan menggunakan minyak sebagai bahan bakar atau pelumas (William 1979). Air ballast yang dihasilkan dari kapal-kapal tersebut juga mengandung minyak. Keberadaan minyak pada perairan laut dapat mengganggu proses-proses kimia dalam ekologi dan merusak ekosistem laut itu sendiri, bahkan dapat menyebabkan kematian bagi organisme dan manusia yang mengkonsumsi ikan atau biota laut yang telah terkontaminasi oleh minyak. Oleh sebab itu, konsentrasi minyak pada perairan yang layak bagi kehidupan biota laut dan kegiatan pelabuhan adalah masing- masing tidak lebih dari 1 mg/l dan 5 mg/l (Kep. Men. LH No.51 Tahun 2004). Perpindahan serta lamanya minyak dalam air laut dapat dipengaruhi oleh adanya arus laut, selain itu angin juga dapat memindahkan minyak yang mengapung di permukaan ke tempat lain (Barnes 1975).
2.2.2. Derajat Keasaman (pH)
penurunan di daerah dekat dengan dasar perairan terutama pada kondisi yang miskin akan oksigen dan pada saat memproduksi H2S.
pH dapat mempengaruhi jenis dan susunan zat dalam lingkungan perairan dan mempengaruhi tersedianya unsur hara serta toksisitas dari unsur-unsur renik, selain itu pH dapat mempengaruhi kehidupan biota air. Menurut Novotny dan Olem (1994) kebanyakan dari biota air lebih menyukai pH yang netral atau pada kisaran 6–8,5. Daya larut dan sifat toksik suatu logam dipengaruhi oleh pH, dan logam akan semakin toksik dengan kisaran pH yang rendah. Keasaman pH akan menyebabkan logam- logam larut dalam air (Palmer 2001, dalam Anggraeni 2002).
2.2.3. Oksigen Terlaut (DO)
Oksigen terlarut (DO) adalah jumlah mg/l gas oksigen yang terlarut dalam air (Hariyadi et al., 1992). Faktor yang mempengaruhi kelarutan oksigen dalam air yaitu temperatur dan salinitas, oleh sebab itu oksigen terlarut dalam air laut lebih rendah dibandingkan pada air tawar. Selain itu, oksigen terlarut lebih mudah larut pada temperatur yang rendah, dengan demikian oksigen lebih banyak ditemukan pada kedalaman yang tinggi walaupun konsentrasinya lebih rendah dibandingkan pada permukaan laut (kedalaman rendah). Kadar oksigen terlarut akan selalu mengalami fluktuasi setiap hari dan musimnya, berfluktuasinya kadar oksigen ini bergantung pada percampuran dan pergerakan massa air, aktivitas fotosintesis, respirasi dan limbah yang masuk ke perairan (Effendi 2003).
Sumber oksigen yang berada di dalam air 35 % berasal dari difusi atmosfer dan sisanya berasal dari hasil proses fotosintesis oleh tumbuhan air dan fitoplankton (Wetzel 1983). Penyebaran oksigen di dalam lautan bervariasi menurut kedalaman. Pada kedalaman 5-20 m, oksigen akan maksimum karena pada kedalaman tersebut proses fotosintesis berlangsung maksimum sedangkan minimumnya kadar oksigen terla rut dalam air merupakan pertanda bahwa kegiatan biologik telah menghabiskan oksigen (Nybakken 1992).
(Duxbury dan Duxbury 1991). Kurangnya oksigen di perairan selain digunakan untuk respirasi bagi biota akuatik juga dimanfaatkan dalam menghancurkan bahan pencemar, oleh sebab itu terkadang kematian ikan yang terjadi bukan hanya karena toksisitas dari bahan-bahan pencemar melainkan secara tidak langsung karena kekurangan oksigen sebagai akibat dari pemakaiannya untuk menghancurkan bahan-bahan pencemar. Berdasarkan Kep. Men. LH No.51 Tahun 2004, oksigen terlarut pada perairan laut tidak boleh kurang dari 5 mg/l.
2.2.4. Biochemical Oxygen Demand/BOD5
BOD menggambarkan jumlah oksigen yang dibutuhkan oleh mikroba aerob dalam mengoksidasi bahan organik menjadi karbondioksida dan air (Davis dan Cornwell 1991, dalam Effendi 2003). Dalam BOD5, bahan organik yang dapat
terdekomposisi adalah bahan organik yang hanya dapat terurai secara biologi dan yang terurai sekitar 75 %.
Nilai BOD5 perairan dipengaruhi oleh suhu, oksigen, densitas plankton dan
keberadaan mikroba, serta jenis dan kandungan bahan organik. Bahan organik ini berupa lemak, protein, kanji, glukosa, aldehida dan ester (Effendi 2003). Air dengan kadar BOD5 tinggi dan tidak mempunyai kemampuan menambah kadar
oksigennya, tidak dapat mendukung kehidupan organisme yang membutuhkan oksigen. Suatu perairan laut yang layak bagi kehidupan biota laut harus memiliki kadar BOD5 kurang dari 20 mg/l (Kep. Men. LH No.51 Tahun 2004).
2.2.5. Chemical Oxygen Demand/COD
COD menyatakan jumlah total oksigen yang dibutuhkan untuk mengoksidasi semua bahan organik yang terdapat di perairan, menjadi CO2 dan
H2O (Hariyadi et al., 1992). Untuk menentukan kadar bahan organik pada suatu
menggunakan oksidator kuat ini, diperkirakan sekitar 95–100 % bahan organik dapat dioksidasi.
Bahan organik yang diukur dalam COD dapat berasal dari alam, aktivitas rumah tangga dan industri seperti pabrik pulp dan kertas serta industri makanan. Perairan yang memiliki kadar COD tinggi tidak diinginkan bagi kehidupan biota. Berdasarkan UNESCO/WHO/UNEP (1992), dalam Effendi (2003) nilai COD pada perairan yang tidak tercemar biasanya memiliki kadar COD < 20 mg/l, pada perairan tercemar dapat melebihi 200 mg/l.
2.2.6. Total Nitrogen (T-N)
Lapisan atmosfer mengandung sekitar 78% gas nitrogen. Bebatuan juga mengandung nitrogen. Keberadaan nitrogen yang didukung dengan keberadaan fosfat di dalam air dapat merangsang pertumbuhan fitoplankton menjadi berlimpah (blooming algae). Nitrogen di perairan terdapat dalam berbagai bentuk seperti: gas N2, Nitrit (NO2-), Nitrat (NO3-), Ammonia (NH3) dan Ammonium
(NH4+) serta sejumlah besar N yang berikatan dalam organik kompleks. Namun
yang paling sering ditemukan pada perairan laut adalah nitrogen dalam bentuk molekuler nitrogen, tetapi nitrogen dalam bentuk ini tidak dapat dimanfaatkan secara langsung oleh organisme, melainkan harus difiksasi terlebih dahulu menjadi ammonia, nitrit dan nitrat (Davis 1991).
Sumber-sumber nitrogen dalam air dapat bermacam- macam, meliputi hancuran bahan organik, buangan domestik, limbah industri, limbah peternakan dan pupuk (Saeni 1989). Barnes (1975) menyatakan bahwa dalam sampah domestik dan limbah industri yang masuk ke laut mengandung nitrogen yang kemudian dapat dioksidasi menjadi ammonia, nitrat dan nitrit. Sumber nitrogen terbesar adalah difusi dari atmosfer, sehubungan dengan jumlah yang besar di atmosfer (78 %) (Hariyadi et al., 1992). Menurut Moore (1962) keberadaan nitrogen di dalam perairan tidak sebanyak keberadaannya di dalam tanah, hal ini disebabkan karena terlepasnya gas nitrogen dari perairan ke atmosfer akibat proses reduksi dari nitrat menjadi N2 oleh bakteri denitrifikasi, adanya proses
2.2.7. Ammonium
Ammonium merupakan salah satu bentuk nitrogen di perairan dan merupakan bentuk transisi dari ammonia. Ammonium masuk ke perairan melalui
run off dari lahan pertanian yang menggunakan pupuk urea, sebab urea merupakan contoh pupuk yang mengandung ammonium dan berfungsi untuk menambah pasokan nitrogen ke dalam tanah yang dimanfaatkan secara langs ung oleh tumbuhan (Effendi 2003). Ammonia ataupun ammonium dapat dimanfaatkan oleh tumbuhan akuatik atau mengalami nitrifikasi membentuk nitrat (Hariyadi et al., 1992). Ammonium akan bersifat toksik apabila mengalami ionisasi, sifat toksik ini dipengaruhi oleh pH dan suhu. Sedangkan ammonium yang tidak terionisasi akan mudah menguap dari air (Novotny dan Olem 1994).
2.2.8. Total Fosfat
Total fosfat menunjukkan kandungan P (fosfor) baik yang berupa senyawa organik maupun anorganik (Hariyadi et al., 1992). Fosfat dalam bentuk organik cenderung banyak terdapat pada perairan yang banyak mengandung bahan organik (Effendi 2000). Fosfat yang masuk ke dalam perairan berasal dari batuan dan tanah yang masuk ke perairan melalui run off dan juga berasal dari partikel-partikel organik yang telah mati, namun jumlahnya dalam perairan sangatlah sedikit.
Kadar fosfat yang berlebihan di dalam air dapat mengakibatkan terjadinya
eutrofikasi. Selain itu menurut Saeni (1989), kenaikan konsentrasi fosfat menyatakan adanya zat pencemar, karena sejumlah industri dapat membuang polyphosphate berupa bahan pencuci yang mengapung di atas permukaan air. Berdasarkan Kep. Men. LH No.51 Tahun 2004 kandungan total fosfat pada perairan laut yang layak bagi kehidupan biota laut tidak lebih dari 0,015 mg/l.
2.2.9. Logam Berat
beratnya lima kali dari berat air. Sedangkan logam ringan adalah logam yang memiliki berat kurang dari 5 gram (Darmono 1995). Namun Palar (2004) menyatakan bahwa perbedaan antara logam berat dengan logam ringan bukan dilihat dari beratnya melainkan dari pengaruh yang dihasilkan bila logam ini berikatan dan atau masuk ke dalam tubuh organisme hidup.
Logam yang berada di perairan dapat berasal dari pelapukan batuan dan tanah, aktivitas gunung berapi dan beberapa aktivitas ant hropogenik seperti kegiatan pertambangan, proses produksi dan aktivitas yang menggunakan logam secara langsung ataupun penggunaan bahan-bahan lain yang mengandung logam berat (Sualia 2005). Pada umumnya daerah pantai memiliki kandungan logam lebih besar karena kebanyakan berasal dari mulut- mulut sungai yang terkontaminasi oleh limbah buangan industri/pertambangan.
Beberapa logam baik logam berat maupun logam ringan memiliki jumlah yang sangat sedikit di perairan, karena logam- logam tersebut mengendap pada sedimen. Berdasarkan Diniah (1995) logam berat di perairan laut akan disebarkan oleh turbulensi dan arus laut serta akan dibawa oleh arus dan biota yang beruaya. Daya racun dari logam dipengaruhi oleh pH, semakin rendah pH maka daya racun dari logam akan meningkat.
2.2.9.1. Kadmium (Cd)
Kadmium merupakan logam lunak berwarna putih perak (Palar 2004). Walaupun kadmium tersebar luas di alam, tetapi biasanya sering ditemukan dalam konsentrasi rendah dalam tanah dan bebatuan (100–300 ppb). Kadmium bersifat mudah menguap dan tidak larut dalam air. Menurut Effendi (2003) pada pH yang tinggi kadmium akan mengalami pengendapan.
oleh pH dan kesadahan, kadmium akan semakin beracun dengan adanya zinc dan timbal (Effendi 2003). Oleh sebab itu keberadaan kadmium di perairan laut tidak boleh melebihi 0,0001 mg/l (MecNeely et al., 1979, dalam Effendi 2003), sedangkan berdasarkan Kep. Men. LH No.51 Tahun 2004 perairan laut yang layak bagi kehidupan biota laut dan kegiatan pelabuhan masing- masing sebesar 0,001 mg/l dan 0,01 mg/l.
2.2.9.2. Kromium Heksavalen (Cr6+)
Kromium (Cr6+) merupakan unsur yang paling jarang ditemukan pada perairan alami (Effendi 2003). Di alam, kromium ditemukan dalam bentuk persenyawaan padat atau mineral dengan unsur-unsur lain. Pada suatu perairan, kromium ditemukan dalam bentuk kromium trivalen dan kromium heksavalen. Namun yang paling beracun bagi organisme dan manusia adalah kromium heksavalen, hal ini dilihat dari ion valensinya yang lebih tinggi sehingga kemampuannya untuk berikatan dengan ion lain lebih tinggi pula. Sumber-sumber masukan logam kromium ke dalam lingkungan diduga paling banyak dari kegiatan industri, kegiatan rumah tangga, serta pembakaran dan mobilisasi bahan bakar. Kromium dalam badan perairan dapat masuk melalui dua cara, yaitu secara alamiah dan nonalamiah. Masuknya kromium secara alamiah berasal dari peristiwa erosi pada batuan mineral, disamping itu debu-debu dan partikel-partikel Cr6+ yang di udara akan dibawa turun oleh air hujan. Masukkan Cr6+ secara nonalamiah lebih merupakan dampak dari aktivitas yang dilakukan oleh manusia seperti buangan industri (Palar 2004).
Telah dikatakan bahwa kromium heksavalen lebih beracun dan daya racunnya dipengaruhi oleh suhu dan pH. Keracunan dari kromium ini dapat mengganggu fungsi hati, ginjal, pernafasan dan mengakibatkan kerusakan pada kulit. Kadar kromium di perairan yang diperkenankan bagi kehidupan biota laut adalah 0,005 mg/l (Kep. Men. LH No.51 Tahun 2004).
2.2.9.3. Timbal (Pb)
pertambangan logam ini berbentuk sulfide logam (PbS), yang sering disebut galena (Darmono 1995). Kelarutan timbal yang cukup rendah mengakibatkan konsentrasi di perairan relatif sedikit, selain itu timbal diserap dengan baik oleh tanah sehingga pengaruhnya terhadap tanaman relatif sedikit (Effendi 2003).
Penggunaan timbal yang sangat dikenal adalah pada pembuatan baterai, tidak sedikit pula digunakan sebagai pelapis logam untuk mencegah perkaratan, karena timbal sendiri mempunyai sifat tahan korosi. Masuknya timbal di perairan melalui pengkristalan Pb di udara dengan bantuan air hujan. Disamping itu, proses korosifikasi dari batuan mineral akibat he mpasan gelombang dan angin, juga merupakan salah satu jalur sumber Pb yang akan masuk ke dalam badan perairan (Palar 2004). Walaupun timbal sering dimanfaatkan untuk berbagai produk industri, pada dasarnya timbal juga dapat memberikan dampak keracunan khususnya bagi manusia, tetapi daya racun dari timbal tidak sebesar unsur lainnya (Cd, Hg, Cu). Kadar dan daya racun dari timbal dipengaruhi oleh kesadahan, pH, alkalinitas dan oksigen (Effendi 2003). Perairan laut yang layak bagi kehidupan biota laut dan kegiatan pelabuhan memiliki konsentrasi timbal masing- masing sebesar 0,008 mg/l dan 0,05 mg/l (Kep. Men. LH No.51 Tahun 2004).
2.2.9.4. Arsen (As)
2.2.9.5. Merkuri (Hg)
Merkuri (Hg) merupakan butiran berwarna perak putih, tebal dan akan membentuk zat cair pada suhu kamar 25 oC dan membeku pada suhu 38.9 oC. Merkuri merupakan logam yang mudah menguap, tetapi tentu saja pada suhu tertentu. Karena sifatnya yang mudah menguap, pada umumnya keberadaannya pada perairan alami sedikit (Novotny dan Olem 1994). Menurut Effendi (2003) merkuri dapat terserap pada bahan-bahan partikulat dan mengalami presipitasi.
Merkuri masuk ke lingkungan dapat melalui berbagai sumber. Bila zat ini tidak masuk secara langsung ke ekosistem perairan, zat ini dapat masuk melalui air hujan dari atmosfir atau pencucian tanah (Saeni 1989). Keberadaan merkuri yang berlebihan di dalam perairan dapat menyebabkan toksik bagi biota akuatik dan juga manusia. Masuknya merkuri ke dalam tubuh manusia dapat melalui debu, makanan dan air. Pada umumnya racun dari merkuri ini lebih besar pada konsumen tingkat akhir yang mengkonsumsi makanan yang telah terkontaminasi oleh merkuri, contohnya memakan ikan. Untuk itu, Menteri Lingkungan Hidup menyatakan bahwa perairan laut yang layak bagi kehidupan biota laut dan kegiatan pelabuhan memiliki konsentrasi merkuri masing- masing 0,001 mg/l dan 0,003 mg/l (Kep. Men. LH No.51 Tahun 2004).
2.2.9.6. Sianida (CN)
2.3. Parameter Biologi
2.3.1. Total Coliform
Patogen merupakan organisme yang hidupnya dapat menimbulkan suatu penyakit bagi tana man ataupun hewan dan juga bagi manusia yang melakukan kontak langsung dengan air dimana organisme tersebut hidup atau bahkan dengan mengkonsumsi ikan yang ditangkap pada perairan tersebut (William 1979). Bakteri patogen biasanya selalu ada dalam lingkungan terutama lingkungan yang tidak bersih atau tercemar, oleh sebab itu bakteri patogen dapat dijadikan sebagai indikator terjadinya pencemaran pada suatu perairan. Keberadaan bakteri patogen di lingkungan biasanya ada pada saluran-saluran kotoran manusia dan juga genangan- genangan air (Laws 1993).
Salah satu tipe dari bakteri patogen adalah Escherichia coli, bakteri jenis ini biasanya ditemukan di dalam usus semua hewan berdarah panas termasuk manusia. Pada kenyataannya, semua feses manusia mengandung 5-50 % E.coli.
III. METODE PENELITIAN
3.1. Tempat dan Waktu Penelitian
Penelitian ini dilakukan di perairan pelabuhan Tanjung Priok Propinsi Daerah Khusus Ibukota Jakarta dan perairan Muara Gembong yang merupakan tempat pembuangan sedimen dari hasil pengerukan kolam pelabuhan Tanjung Priok (dumping site). Penelitian menggunakan data dari JICA (Japan International Cooperation Agency) Study Team yang dilaksanakan pada bulan Juni 2005 (tanggal 15-17) dan penulis membantu pengambilan sampel pada bulan Oktober 2005 (tanggal 12-14). Pengambilan sampel dilakukan selama tiga hari pada tiap bulannya dan dimulai pada pukul 06.00–12.00 WIB. Kegiatan analisis sampel untuk kualitas air dilakukan di Laboratorium Produktivitas dan Lingkungan Perairan, Fakultas Perikanan dan Ilmu Kelautan, Institut Pertanian Bogor.
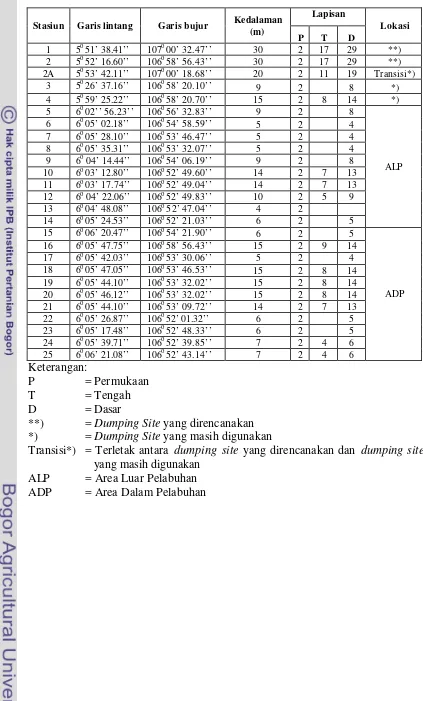
Titik sampel yang diamati berjumlah 26 stasiun, 20 stasiun berada di perairan pelabuhan Tanjung Priok dan 6 stasiun berada di perairan Muara Gembong. Penentuan titik sampel didasarkan pada pertimbangan lokasi yang aktif akan kegiatan pelabuhan dan dumping site, sedangkan waktu pengamatan didasarkan pada pertimbangan dua musim yaitu musim kemarau (Juni) dan musim peralihan dari musim kemarau ke musim hujan (Oktober). Koordinat titik sampel, kedalaman serta lokasi pengambilan contoh air dapat terlihat pada Tabel 1.
3.2. Alat dan Bahan
Alat-alat yang digunakan dalam pengamatan adalah Van Dorn Water Sampler dengan volume 2,5 liter (Merk: Wildco), botol sampel yang terbuat dari bahan polyethilene dan kaca, spektrofotometer (Merk: Atogo), botol BOD, ice box, pH meter (Merk: Double Juction), Atomic Absorbtion Spectroscopy (AAS), oven, kertas millipore pori 0,45 µm, vacum pump, titrasi set, MPN table, counting cell dan peralatan analisis kimia di laboratorium. Sedangkan bahan-bahan yang digunakan adalah contoh air, es, bahan pengawet (HNO3 dan H2SO4) serta
Tabel 1. Koordinat titik pengambilan sampel
Stasiun Garis lintang Garis bujur Kedalaman (m)
Transisi*) = Terletak antara dumping site yang direncanakan dan dumping site
yang masih digunakan ALP = Area Luar Pelabuhan ADP = Area Dalam Pelabuhan
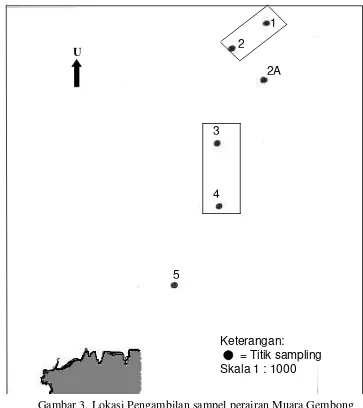
Gambar 3. Lokasi Pengambilan sampel perairan Muara Gembong
Keterangan:
Stasiun 1 dan 2: Dumping site yang direncanakan Stasiun 3 dan 4: Dumping site yang masih digunakan
3.3. Prosedur Kerja
Contoh air diambil pada kedalaman yang berbeda untuk tiap stasiun, yaitu kira-kira 1 m dari permukaan, lapisan tengah dan kira-kira 1 m dari dasar perairan (Tabel 1). Pengambilan contoh air dilakukan dengan menggunakan Van Dorn Water Sampler (merk: Wildco)dengan volume 2,5 liter.
Penanganan air sampel yang dianalisis di laboratorium diawetkan dengan memberikan H2SO4 dan HNO3 masing- masing sebanyak 5 tetes. Bahan pengawet
H2SO4 digunakan untuk mengawetkan air sampel dalam pengukuran parameter
COD. Sedangkan bahan pengawet HNO3 digunakan untuk mengawetkan air 1
2A 2
3
4
5 U
Keterangan:
sampel dalam pengukuran parameter logam berat, seperti: kadmium, kromium, arsen, timbal, merkuri dan sianida. Setelah penanganan, air sampel dimasukkan ke dalam ice box dan dibawa ke laboratorium untuk dianalisis leboh lanjut.
3.3.1. Parameter Fisika
Parameter fisika kualitas air yang diamati terdiri dari parameter suhu, salinitas dan TSS (Tabel 2). Parameter suhu dan salinitas dilakukan di lapang (insitu), dalam pengukuran parameter suhu menggunakan alat termometer raksa, sedangkan pengukuran salinitas menggunakan alat refraktometer (merk: Atogo). Pengukuran parameter fisika lainnya seperti TSS dilakukan di laboratorium. Sebelum dilakukan pengukuran di laboratorium, air sampel yang telah diambil dimasukkan ke dalam botol sampel yang terbuat dari bahan polyethilene
bervolume 250 ml dan tanpa diberi bahan pengawet.
3.3.2. Parameter Kimia
Parameter kimia kualitas air yang diamati dapat terlihat pada Tabel 2. Beberapa parameter kimia seperti pH dan DO dilakukan di lapang (insitu), dalam pengukuran parameter pH dilakukan dengan menggunakan alat pH meter (merk:
Double Junction) dan pengukuran DO dilakukan dengan menggunakan metode modifikasi Winkler. Untuk pengukuran DO, air sampel dimasukkan ke dalam botol BOD dengan volume 300 ml. Pengukuran parameter kimia lainnya, seperti minyak, BOD5, COD, total nitrogen, total fosfat, ammonium dan logam berat (Cd,
Cr6+, As, Hg, Pb dan CN) dilakukan di laboratorium. Sebelum dilakukan pengukuran di laboratorium, air sampel yang digunakan dalam pengukuran parameter minyak, total nitrogen, total fosfat dan ammonium dimasukkan ke dalam botol sampel terbuat dari bahan polyethilene bervolume 250 ml tanpa diberi bahan pengawet; air sampel dalam pengukuran parameter logam berat dimasukkan ke dalam botol sampel terbuat dari bahan polyethilene bervolume 500 ml dan ditambahkan bahan pengawet HNO3 sebanyak 5 tetes; air sampel yang
digunakan dalam pengukuran parameter BOD5 dimasukkan ke dalam botol BOD
dalam botol sampel terbuat dari bahan polyethilene bervolume 100 ml dan diberi bahan pengawet H2SO4 sebanyak 5 tetes.
3.3.3. Parameter Biologi
Parameter biologi yang diamati dapat terlihat pada Tabel 2. Analisis kualitas air untuk parameter biologi (total coliform) dilakukan di laboratorium. Sebelum dilakukan pengukuran di laboratorium, air sampel dalam pengukuran total coliform dimasukkan ke dalam botol kaca dengan volume 100 ml yang telah disterilkan. Setelah air sampel dimasukkan, botol sampel ditutup dengan
alumunium foil kemudian ditutup kembali dengan penutup botol sampel. Penggunaan alumuniun foil bertujuan untuk menghindari terjadinya kontaminasi oleh bakteri lain selain bakteri yang ada dalam air sampel.
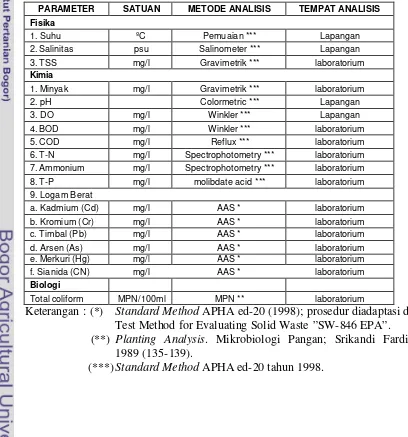
Tabel 2. Parameter kualitas air yang diamati
PARAMETER SATUAN METODE ANALISIS TEMPAT ANALISIS
Fisika
1. Suhu ºC Pemuaian *** Lapangan
2. Salinitas psu Salinometer *** Lapangan
3. TSS mg/l Gravimetrik *** laboratorium
Kimia
1. Minyak mg/l Gravimetrik *** laboratorium
2. pH Colormetric *** Lapangan
3. DO mg/l Winkler *** Lapangan
4. BOD mg/l Winkler *** laboratorium
5. COD mg/l Reflux *** laboratorium
6. T-N mg/l Spectrophotometry *** laboratorium
7. Ammonium mg/l Spectrophotometry *** laboratorium
8. T-P mg/l molibdate acid *** laboratorium
Total coliform MPN/100ml MPN ** laboratorium
Keterangan : (*) Standard Method APHA ed-20 (1998); prosedur diadaptasi dari Test Method for Evaluating Solid Waste ”SW-846 EPA”.
(**) Planting Analysis. Mikrobiologi Pangan; Srikandi Fardiaz, 1989 (135-139).
3.4. Analisis Data
Dalam penelitian, data diolah secara spasial dan temporal. Secara spasial, data diperoleh dari pengambilan sampel di tiap lapisan perairan pelabuhan Tanjung Priok dan perairan Muara Gembong. Secara temporal, data diperoleh dari pengambilan sampel pada musim kemarau (Juni 2005) dan musim peralihan (Oktober 2005). Analisis data yang dilakukan dengan menggunakan analisis deskriptif kualitas air, Indeks STORET, hubungan antara parameter fisika, kimia dan biologi, Uji Nilai Tengah dan Indeks Similaritas Canberra.
3.4.1. Analisis Deskriptif Kualitas Air
Analisis deskriptif kualitas air dengan cara membandingkan nilai dari masing- masing parameter fisika, kimia dan biologi dengan literatur yang ada dan Kep. Men. LH No.51 Tahun 2004 bagi kehidupan biota laut dan kegiatan pelabuhan untuk melihat kualitas perairan. Tahapan dalam analisis deskriptif kualitas air adalah:
- Menyajikan data tiap stasiun dalam bentuk grafik untuk distribusi secara spasial dan temporal.
- Membandingkan data dengan baku mutu kualitas air berdasarkan Kep. Men. LH No.51 Tahun 2004 bagi biota laut dan kegiatan pelabuhan (Lampiran 2) dan literatur untuk melihat kualitas perairan, serta membandingkan kualitas perairan tersebut pada kedua musim yaitu pada musim kemarau (Juni) dan musim peralihan (Oktober).
3.4.2. Indeks STORET
Penggunaan Indeks STORET bertujuan untuk mengetahui kondisi kualitas air suatu perairan serta dapat mengetahui parameter-parameter yang telah melampaui batas baku mutu berdasarkan Kep. Men. LH No.51 Tahun 2004 bagi kehidupan biota laut dan kegiatan pelabuhan. Untuk kepentingan analisis dengan menggunakan Indeks STORET, parameter yang digunakan berdasarkan baku mutu biota laut adalah parameter TSS, pH, minyak, DO, BOD5, total fosfat, arsen,
adalah TSS, pH, minyak, timbal, kadmium, merkuri dan total coliform. Tahapan dalam analisis Indeks STORET adalah sebagai berikut :
1. Menyajikan tabel analisis kualitas air yang memuat semua nilai-nilai hasil pengukuran dari tiap parameter, yaitu parameter fisika, kimia dan biologi perairan. Kemudian mencantumkan nilai minimal, maksimal dan rata-rata dari hasil pengukuran tersebut.
2. Pada tabel yang sama, dicantumkan pula nilai baku mutu untuk masing- masing parameter.
3. Membandingkan nilai minimum, maksimum dan rata-rata hasil pengukuran dari masing- masing parameter terhadap baku mutu yang telah ditetapkan.
4. Kemudian memberikan skor pada tiap nilai minimum, maksimum dan rata-rata dari tiap parameter. Penentuan skor dapat terlihat pada Tabel 3.
Tabel 3. Penentuan sistem nilai untuk menentukan status mutu air (Canter 1977).
Jumlah Nilai Parameter
Contoh Fisika Kimia Biologi
Minimum -1 -2 -3
< 10 Maksimum -1 -2 -3
Rata-rata -3 -6 -9
Minimum -2 -4 -6
= 10 Maksimum -2 -4 -6
Rata-rata -6 -12 -18
5. Pemberian skor, yaitu apabila nilai dari hasil pengukuran berada di luar baku mutu yang telah ditetapkan, maka pemberian skor sesuai dengan Tabel 3. Tetapi jika nilai hasil pengukuran memenuhi nilai baku mutu maka diberi skor 0.
6. Setelah diketahui jumlah skor seluruh parameter, maka dapat diketahui status mutu perairan yang diamati. Penentuan status mutu air dapat terlihat pada Tabel 4.
Tabel 4. Penentuan status mutu perairan (Kep. Men. LH No.115 Tahun 2003)
Kriteria Skor
Baik sekali 0
Baik -1 s/d -10
Sedang -11 s/d -30
3.4.3. Hubungan Antar Parameter Fisika, Kimia dan Biologi
Untuk melihat hubungan antar parameter fisika, kimia dan biologi yang diamati, dapat diketahui melalui perhitungan nilai korelasi antar parameter tersebut. Analisis data untuk mengetahui nilai korelasi dilakukan dengan menggunakan sofware SPSS versi 11,5.
3.4.4. Uji Nilai Tengah
Analisis data dengan menggunakan uji nilai tengah untuk mengetahui perbedaan yang terjadi antar lapisan perairan dan waktu yang diamati. Uji nilai tengah dilakukan dengan asumsi bahwa ragam populasi adalah sama, dengan menggunakan rumus sebagai berikut (Walpole 1992).
t =
Dasar pengambilan keputusan dalam uji nilai tengah, berdasarkan nilai probabilitas (tingkat signifikan) dari hasil nilai t, pada selang kepercayaan sebesar 95 %. Hipotesis yang digunakan adalah :
Ho : µ1 = µo
H1 : µ1 ? µo
- Jika probabilitas p > 0,05, maka Ho diterima - Jika probabilitas p < 0,005, maka Ho ditolak
3.4.5. Indeks Similaritas Canberra
Untuk melihat kesamaan antar stasiun pengamatan berdasarkan parameter fisika-kimia air dengan menggunakan Indeks Similaritas Canberra, rumus yang digunakan adalah sebagai berikut (Field 1971, dalam Abdurochman 2005) :
Keteragan : Ic = Nilai kesamaan Indeks Canberra
n = Jumlah parameter yang diperbandingkan
Xij,Xik = Nilai parameter fisika-kimia ke-i pada dua tempat yang
berbeda.
IV. HASIL DAN PEMBAHASAN
4.1. Kondisi Fisika, Kimia dan Biologi Perairan
Berdasarkan pengamatan yang dilakukan, perairan Pelabuhan Tanjung Priok dan perairan Muara Gembong di bulan Juni dan Oktober 2005 terdapat perbedaan kondisi parameter fisika, kimia dan biologi baik secara spasial maupun temporal. Walaupun perairan Muara Gembong sebagai dumping site, namun pada umumnya perairan Muara Gembong memiliki kondisi parameter fisika, kimia dan biologi lebih baik jika dibandingkan dengan perairan pelabuhan Tanjung Priok baik pada bulan Juni maupun bulan Oktober 2005.
4.1.1. Suhu
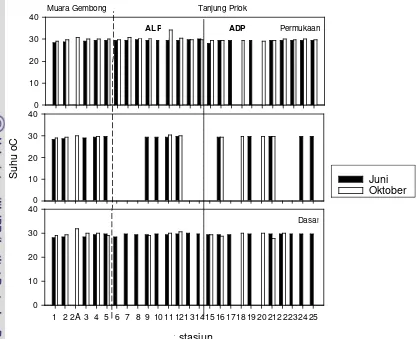
Hasil analisis menunjukkan kondisi suhu pada perairan pelabuhan Tanjung Priok dengan perairan Muara Gembong baik pada pengamatan bulan Juni 2005 maupun bulan Oktober 2005 relatif seragam di tiap lapisan perairan (Gambar 4). Kisaran suhu di lapisan permukaan, tengah dan dasar pada perairan pelabuhan Tanjung Priok masing- masing antara 28,1–30,1 0C; 29,2–29,6 0C dan 28,4–29,8 0C (Gambar 4). Dilihat secara spasial bahwa suhu di perairan pelabuhan Tanjung Priok pada bulan Juni 2005 tidak terdapat perbedaan yang nyata antar lapisan perairan (p>0,05).
Gambar 4. Suhu di tiap lapisan perairan pelabuhan Tanjung Priok (stasiun 6-25) dan perairan Muara Gembong (stasiun 1-5) pada bulan Juni dan Oktober 2005
Secara umum, kondisi suhu antar waktu pengamatan pada tiap lapisan perairan pelabuhan Tanjung Priok dan perairan Muara Gembong tidak berbeda nyata, kecuali pada lapisan permukaan (Lampiran 3). Perbedaan kondisi suhu yang terjadi pada lapisan permukaan antar waktu pengamatan, diduga dipengaruhi oleh adanya perbedaan intensitas cahaya matahari, sirkulasi udara dan cuaca pada saat pengamatan. Perairan pelabuhan Tanjung Priok pada pengamatan bulan Oktober 2005, memiliki kisaran suhu di tiap lapisan perairan antara 29,2-34,4 oC di lapisan permukaan; 29,2-30,2 oC di lapisan tengah; dan 27,7-30,4 oC di lapisan dasar. Berdasarkan uji nilai tengah menunjukkan tidak adanya perbedaan yang nyata antar lapisan perairan (p>0,05), hal ini dapat terlihat pula pada gambar (Gambar 4).
Muara Gembong Tanjung Priok
ALP ADP
Kisaran suhu di tiap lapisan perairan Muara Gembong antara 29,1-30,7 oC di lapisan permukaan; 29,1-30,0 oC di lapisan tengah; dan 29,0-31,9 oC di lapisan dasar (Gambar 4). Berdasarkan hasil uji nilai tengah, tidak terdapat perbedaan yang nyata antar lapisan perairan (p>0,05). Kondisi suhu di perairan pelabuhan Tanjung Priok dan perairan Muara Gembong pada bulan Oktober 2005 tergolong alami dan dalam keadaan baik untuk kehidupan biota laut.
4.1.2. Salinitas
Hasil pengamatan pada bulan Juni 2005 menunjukkan bahwa kondisi salinitas pada perairan pelabuhan Tanjung Priok dan perairan Muara Gembong memiliki nilai yang cukup tinggi. Kondisi ini relatif seragam di tiap stasiun (Gambar 5). Pada lapisan permukaan, tengah dan dasar perairan pelabuhan Tanjung Priok memiliki kisaran salinitas, masing- masing antara 26,0-36,0 psu; 33,0-37,0 psu; dan 32,0-37,0 psu. Perbedaan salinitas pada tiap lapisan dapat terlihat pada uji nilai tengah dengan taraf kepercayaan sebesar 0,05 bahwa salinitas antar lapisan tidak berbeda nyata.
Perairan Muara Gembong memiliki salinitas sebesar 34,0 psu pada tiap lapisannya (Gambar 5). Keseragaman salinitas pada tiap lapisan perairan dapat terlihat pula dari hasil uji nilai tengah, yang menunjukkan tidak terdapat perbedaaan yang nyata antar lapisan perairan (p>0,05). Berdasarkan hasil analisis, salinitas antara perairan pelabuhan Tanjung Priok dengan perairan Muara Gembong pada bulan Juni 2005 berada dalam kondisi alami.
perairan pelabuhan Tanjung Priok berkisar antara 31,0-35,0 psu pada lapisan permukaan; 32,0-35,0 psu pada lapisan tengah; dan 32,0-36,0 psu pada lapisan dasar (Gambar 5). Berdasarkan hasil uji nilai tengah, kondisi salinitas antar lapisan perairan pelabuhan Ta njung Priok terdapat perbedaan yang nyata (p<0,05).
Gambar 5. Salinitas di tiap lapisan perairan pelabuhahan Tanjung Priok (stasiun 6-25) dan perairan Muara Gembong (stasiun 1-5) pada bulan Juni dan Oktober 2005
Berbeda dengan perairan pelabuhan Tanjung Priok, salinitas di tiap lapisan perairan Muara Gembong antar waktu pengamatan tidak berbeda nyata. Kisaran salinitas di tiap lapisan perairan antara 33,0 psu di lapisan permukaan; 32,0-33,0 psu di lapisan tengah; dan 32,0-34,0 psu di lapisan dasar (Gambar 5). Hasil uji nilai tengah menunjukkan salinitas antar lapisan perairan di bulan Oktober 2005 tidak memiliki perbedaan yang nyata (p>0,05). Kondisi salinitas di perairan
0 10 20 30 40
Salinitas (psu)
0 1 0 2 0 3 0 4 0
Juni Oktober
Stasiun
1 2 2A 3 4 5 6 7 8 9 1 0 11 12 13 14 15 16 17 18 19 20 2 1 22 23 24 25 0
1 0 2 0 3 0 4 0
Muara Gembong Tanjung Priok
ALP ADP
pelabuhan Tanjung Priok dan perairan Muara Gembong masih berada dalam kondisi yang alami.
4.1.3. Total Suspended Solid (TSS)
Kondisi TSS pada bulan Juni 2005 di perairan pelabuhan Tanjung priok lebih tinggi dibandingkan dengan perairan Muara Gembong (Gambar 6). Hal ini diduga karena perairan pelabuhan Tanjung Priok merupakan tempat bermuaranya sungai Sunter dan sungai Ancol yang dapat membawa sedimen ataupun lumpur ke perairan laut. Kisaran TSS pada tiap lapisan perairan pelabuhan Tanjung Priok antara 12-89 mg/l pada lapisan permukaan; 11-41 mg/l pada lapisan tengah; dan 12-76 mg/l pada lapisan dasar (Gambar 6). Berdasarkan hasil uji nilai tengah menunjukkan bahwa kondisi TSS antar lapisan perairan tidak terdapat perbedaan yang nyata (p>0,05). Lapisan permukaan pada stasiun 15 memiliki TSS lebih tinggi dibandingkan dengan stasiun lainnya yaitu mencapai 89 mg/l (Gambar 6). Hal ini diduga karena stasiun 15 merupakan stasiun yang dekat dengan daratan, sehingga akibat dari pengikisan tanah dapat mempengaruhi nilai TSS pada stasiun 15.
Berdasarkan Kep. Men. LH No.51 Tahun 2004, kondisi perairan pelabuhan Tanjung Priok pada bulan Juni 2005 tidak baik bagi kehidupan biota laut. Namun masih dalam kondisi yang baik bagi perairan pelabuhan. Karena perairan yang layak bagi kehidupan biota laut dan kegiatan pelabuhan masing- masing sebesar 20 mg/l dan 80 mg/l.
Muara Gembong Tanjung Priok
stasiun yang memiliki kadar TSS tinggi pada perairan Muara Gembong, pada umumnya TSS di perairan ini berada dalam kondisi yang layak bagi kehidupan biota laut dan kegiatan pelabuhan..
Gambar 6. Konsentrasi TSS di tiap lapisan perairan pelabuhan Tanjung Priok (stasiun 6-25) dan perairan Muara Gembong (stasiun 1-5) pada bulan Juni dan Oktober 2005
Kondisi TSS antar waktu pengamatan pada tiap lapisan perairan pelabuhan Tanjung Priok berbeda nyata, pada bulan Oktober 2005 konsentrasi TSS lebih rendah dibandingkan pada bulan Juni 2005 (Gambar 6). Hal ini diduga karena adanya aktivitas pengerukan sedimen di kolam pelabuhan Tanjung Priok pada musim kemarau (Juni 2005). Aktivitas ini dapat mempengaruhi terjadinya peningkatan parameter TSS di perairan pelabuhan Tanjung Priok. Kisaran TSS pada tiap lapisan perairan pelabuhan Tanjung Priok antara 8-39 mg/l pada lapisan permukaan; 3-32 mg/l pada lapisan tengah; dan 10-50 mg/l pada lapisan dasar (Gambar 6). Berdasarkan hasil uji nilai tengah, kondisi TSS di perairan
Permukaan
Muara Gembong Tanjung Priok
ALP ADP
pelabuhan Tanjung Priok pada bulan Oktober 2005 tidak memiliki perbedaan yang nyata antar lapisan perairan (p>0,05).
Untuk perairan Muara Gembong, kondisi TSS antar waktu pengamatan di tiap lapisan secara umum berbeda nyata kecuali pada lapisan permukaan (Lampiran 3). Kisaran TSS di tiap lapisan perairan pada bulan Oktober 2005 antara 44-22 mg/l di lapisan permukaan; 3-4 mg/l di lapisan tengah; dan 2-37 mg/l di lapisan dasar (Gambar 6). Kondisi TSS antar lapisan perairan Muara Gembong terdapat perbedaaan yang nyata (p<0,05). Walaupun terjadi perbedaan kondisi TSS antara perairan pelabuhan Tanjung priok dan perairan Muara Gembong, namun pada pengamatan bulan Oktober 2005, kedua perairan ini berada dalam kondisi yang baik bagi kehidupan biota laut dan kegiatan pelabuhan.
4.1.4. Minyak
Gambar 7. Konsentrasi minyak di tiap lapisan perairan pelabuhan Tanjung Priok (stasiun 6-25) dan perairan Muara Gembong (stasiun 1-5) pada bulan Juni dan Oktober 2005
Secara temporal, pada umumnya keberadaan minyak di perairan pelabuhan Tanjung Priok berbeda nyata, yaitu pada pengamatan bulan Oktober 2005 berada dalam kondisi yang lebih rendah dibandingkan dengan bulan Juni 2005 (Gambar 7). Perubahan konsentrasi minyak yang terjadi pada bulan Oktober 2005 dapat dipengaruhi oleh faktor angin dan arus yang dapat memindahkan minyak pada permukaan ke tempat lain. Selain itu, berkurangnya keberadaan minyak di perairan laut diduga karena adanya proses dekomposisi oleh mikroorganisme.
Konsentrasi minyak pada tiap lapisan perairan pelabuhan Tanjung Priok berkisar antara 0,0009-0,0190 mg/l pada lapisan permukaan serta 0,0009-0,0210 mg/l pada lapisan tengah dan dasar (Gambar 7). Berdasarkan uji nilai tengah, keberadaan minyak pada perairan pelabuhan Tanjung Priok di bulan Oktober 2005 tidak terdapat perbedaan yang nyata antar lapisan perairan (p>0,05).
Kadar minyak antar waktu pengamatan di tiap lapisan perairan Muara Gembong secara umum berbeda nyata, kondisi ini tidak berbeda dengan perairan
ADP
Muara Gembong Tanjung Priok
ALP
Keterangan: ALP = Area Luar Pelabuhan, ADP = Area Dalam Pelabuhan
pelabuhan Tanjung Priok. Kisaran minyak pada tiap lapisan perairan Muara Gembong pada bulan Oktober 2005 antara 0,0009-0,0230 mg/l pada lapisan permukaan; 0,0009 mg/l pada lapisan tengah; dan 0,0009-0,0220 mg/l pada lapisan dasar (Gambar 7). Berdasarkan hasil uji nilai tengah, konsentrasi minyak antar lapisan menunjukkan adanya perbedaan yang nyata (p<0,05). Hasil pengamatan bulan Juni dan Oktober 2005, menunjukkan perairan pelabuhan Tanjung Priok dan perairan Muara Gembong berada dalam kondisi yang layak bagi kehidupan biota laut dan kegiatan pelabuhan. Karena memiliki konsentrasi kurang dari 1 mg/l (baku mutu biota laut) dan 5 mg/l (baku mutu pelabuhan) (Kep.Men. LH No.51 Tahun 2004).
4.1.5. Derajat Keasaman (pH)
Hasil pengamatan pada bulan Juni 2005, bahwa nilai pH di perairan pelabuhan Tanjung Priok dan perairan Muara Gembong relatif seragam antar stasiun di tiap lapisan perairan (Gambar 8). Kisaran pH pada tiap lapisan perairan pelabuhan Tanjung Priok antara 7,09-8,31 pada lapisan permukaan; 7,90-8,18 pada lapisan tengah; dan 7,61-8,15 pada lapisan dasar (Gambar 8). Berdasarkan hasil uji nilai tengah, nilai pH antar lapisan perairan memiliki perbedaan yang nyata (p<0,05).
Gambar 8. Nilai pH di tiap lapisan perairan pelabuhan Tanjung Priok (stasiun 6-25) dan perairan Muara Gembong (stasiun 1-5) pada bulan Juni dan Oktober 2005
Nilai pH antar waktu pengamatan di tiap lapisan perairan pelabuhan Tanjung Priok tidak berbeda nyata. Kisaran pH di tiap lapisan perairan pelabuhan Tanjung Priok pada bulan Oktober 2005, antara 7,22-8,20 di lapisan permukaan; 7,52-8,18 di lapisan tengah; dan 7,45-8,19 di lapisan dasar (Gambar 8). Hasil pengamatan pada bulan Oktober 2005 menunjukan bahwa pH di perairan pelabuhan Tanjung Priok tidak terdapat perbedaan yang nyata antar lapisan (p>0,05).
Nilai pH antar waktu pengamatan di tiap lapisan perairan Muara Gembong berbeda nyata, dengan kisaran pH antara 7,33-7,54 di lapisan permukaan; 7,31-7,63 di lapisan tengah; dan 7,33-7,61 di lapisan dasar (Gambar 8). Berdasarkan hasil uji nilai tengah, nilai pH pada perairan Muara Gembong tidak terdapat perbedaan yang nyata antar lapisan perairan (p>0,05). Kondisi ini tidak berbeda dengan pengamatan pada bulan Juni 2005 (Gambar 8). Hasil pengamatan pada
0
Muara Gembong Tanjung Priok
ALP ADP
bulan Oktober 2005 menunjukan perairan pelabuhan Tanjung Priok dan perairan Muara Gembong berada dalam kisaran pH bagi perairan pelabuhan dan kehidupan biota laut.
Berdasarkan nilai korelasi bahwa pH berhubungan erat dengan DO, BOD, COD dan beberapa unsur hara seperti fosfat dan nitrogen (Lampiran 4). Nilai pH biasanya akan mengalami penurunan di daerah dekat dengan dasar perairan terutama pada kondisi yang miskin akan oksigen dan pada saat memproduksi H2S.
Selain itu, tingginya nilai pH pada perairan diduga karena proses fotosintesis berlangsung lebih aktif (Davis 1991).
4.1.6. Oksigen Terlarut (DO)
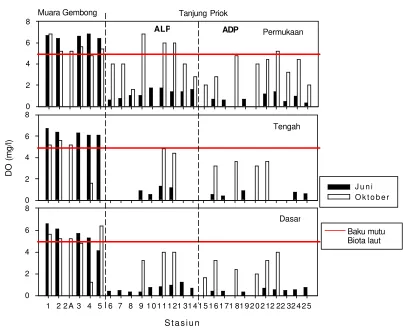
Hasil pengamatan bulan Juni 2005, secara umum menunjukkan konsentrasi DO di perairan pelabuhan Tanjung Priok lebih rendah dari konsentrasi DO di perairan Muara Gembong (Gambar 9). Hal ini diduga karena perairan pelabuhan Tanjung Priok mendapat masukkan bahan organik lebih banyak dibandingkan dengan perairan Muara Gembong. Masukkan bahan organik selain berasal dari kegiatan pelabuhan juga berasal dari dua sungai yang bermuara ke perairan pelabuhan Tanjung Priok, yaitu sungai Ancol dan sungai Sunter. Konsentrasi DO di tiap lapisan perairan pelabuhan Tanjung Priok, berkisar antara 0,00-1,77 mg/l di lapisan permukaan; 0,40-1,32 mg/l di lapisan tengah; dan 0,00-1,24 mg/l di lapisan dasar (Gambar 9). Dari hasil pengamatan terlihat bahwa konsentrasi DO cenderung akan semakin menurun dengan meningkatnya kedalaman (Gambar 9). Berdasarkan hasil uji nilai tengah, konsentrasi DO antar lapisan perairan terdapat perbedaaan yang nyata (p>0,05).
Gambar 9. Konsentrasi DO di tiap lapisan perairan pelabuhan Tanjung Priok (stasiun 6-25) dan perairan Muara Gembong (stasiun 1-5) pada bulan Juni dan Oktober 2005
Kisaran DO di tiap lapisan perairan Muara Gembong, antara 6,40-6,80 mg/l di lapisan permukaan; 6,10-6,70 mg/l di lapisan tengah; dan 4,10-6,60 mg/l di lapisan dasar (Gambar 9). Konsentrasi DO pada perairan Muara Gembong tertinggi pada lapisan permukaan dan menurun dengan meningkatnya kedalaman, kondisi ini tidak berbeda dengan perairan pelabuhan Tanjung Priok (Gambar 9). Meningkatnya konsentrasi DO pada lapisan permukaan dapat disebabkan karena adanya difusi oksigen dari udara dan proses fotosintesis berlangsung maksimum pada lapisan ini dibandingkan dengan lapisan di bawahnya. Berdasarkan hasil uji nilai tengah, konsentrasi DO pada perairan Muara Gembong terdapat perbedaan yang nyata antar lapisan perairan (p>0,05). Tingginya kisaran DO di tiap lapisan perairan Muara Gembong dibulan Juni 2005, menunjukan perairan ini dapat menunjang bagi kehidupan biota laut.
0
Muara Gembong Tanjung Priok
ALP ADP
Kadar DO pada tiap lapisan perairan pelabuhan Tanjung Priok berbeda nyata antar waktu pengamatan, yaitu pada bulan Oktober 2005 kadar DO lebih tinggi. Kisaran DO di tiap lapisan perairan pelabuhan Tanjung Priok pada bulan Oktober 2005, antara 1,60-6,80 mg/l di lapisan permukaan; 3,20-4,80 mg/l di lapisan tengah; dan 1,60-4,00 mg/l di lapisan dasar (Gambar 9). Berdasarkan hasil uji nilai tengah, konsentrasi DO pada perairan pelabuhan Tanjung Priok tidak terdapat perbedaan yang nyata antar lapisan perairan (p>0,05). Dengan kisaran DO yang rendah, menunjukkan perairan pelabuhan Tanjung Priok di tiap lapisan perairan pada bulan Oktober 2005 tidak layak bagi kehidupan biota laut.
Secara umum, kadar DO pada tiap lapisan perairan Muara Gembong berbeda nyata antar waktu, kecuali pada lapisan dasar. Kadar DO pada tiap lapisan perairan Muara Gembong di bulan Oktober 2005 lebih rendah dibandingkan dengan pengamatan sebelumnya, yaitu berkisar antara 4,80-6,80 mg/l di lapisan permukaan; 1,60-5,60 mg/l di lapisan tengah; dan 1,20-6,40 mg/l di lapisan dasar (Gambar 9). Berdasarkan hasil uji nilai tengah, konsentrasi DO pada perairan Muara Gembong tidak terdapat perbedaan yang nyata antar lapisan perairan (p>0,05). Kondisi perairan Muara Gembong di bulan Oktober 2005 pada lapisan tengah dan dasar menunjukan kurang layak bagi kehidupan biota laut karena tidak sesuai dengan baku mutu. Perbedaan konsentrasi DO yang terjadi secara temporal, dapat diduga karena adanya perbedaan bahan organik yang terdapat di perairan. Kondisi ini dapat terlihat dari hubungan antar parameter, bahwa pada saat bahan organik di perairan tinggi dapat mempengaruhi kelarutan oksigen yang ada di perairan karena oksigen digunakan untuk mendekomposisi bahan organik (Lampiran 4).
4.1.7. Biochemical Oxygen Demand (BOD5)
Kadar BOD5 secara tidak langsung menunjukkan kandungan bahan organik
yang ada di perairan. Berdasarkan hasil pengamatan pada bulan Juni 2005, terjadi perbedaan konsentrasi BOD5 yang relatif tinggi antara perairan pelabuhan
Tanjung Priok dengan perairan Muara Gembong. Pada perairan pelabuhan Tanjung Priok memiliki konsentrasi BOD5 lebih tinggi dibandingkan dengan
perairan pelabuhan Tanjung Priok, berkisar antara 2,50-20,50 mg/l di lapisan permukaan; 4,70-15,37 mg/l di lapisan tengah; dan 2,90-17,20 mg/l di lapisan dasar (Gambar 10). Berdasarkan hasil uji nilai tengah, BOD5 antar lapisan
perairan terdapat perbedaan yang nyata (p<0,05). Konsentrasi BOD5 tertinggi
terjadi pada lapisan permukaan yaitu pada stasiun 15 (Gambar 10). Hal ini diduga karena stasiun 15 mendapat limpasan bahan organik dari daratan. Kondisi perairan pelabuhan Tanjung Priok pada bulan Juni 2005 di tiap lapisan perairan menunjukkan masih dalam kondisi yang baik bagi kehidupan biota laut, karena memiliki konsentrasi BOD5 kurang dari 20 mg/l (Kep. Men. LH No.51 Tahun
2004).
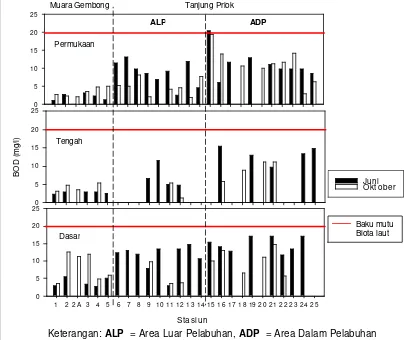
Gambar 10. Konsentrasi BOD di tiap lapisan perairan pelabuhan Tanjung Priok (stasiun 6-25) dan perairan Muara Gembong (stasiun 1-5) pada bulan Juni dan Oktober 2005
Kisaran BOD5 pada perairan Muara Gembong di tiap lapisan perairan,
antara 1,10-3,10 mg/l di lapisan permukaan; 2,26-2,87 mg/l di lapisan tengah; dan
0
Muara Gembong Tanjung Priok
ALP ADP
2,67-5,54 mg/l di lapisan dasar (Gambar 10). Berdasarkan hasil uji nilai tengah, BOD5 antar lapisan terdapat perbedaan yang nyata (p<0.05). Gambar 10
menunjukkan konsentrasi BOD5 tertinggi terdapat pada stasiun 2, sedangkan
stasiun yang berperan sebagai dumping site (stasiun 3 dan 4) memiliki konsentrasi BOD5 yang lebih rendah dari stasiun 2. Meskipun konsentrasi BOD5 pada
perairan Muara Gembong di bulan Juni 2005 rendah, namun kondisinya masih baik bagi kehidupan biota laut.
Hasil pengamatan pada bulan Oktober 2005, menunjukkan adanya perubahan nilai BOD5 baik pada perairan pelabuhan Tanjung Priok maupun
perairan Muara Gembong (Gambar 10). Secara umum, kadar BOD5 pada tiap
lapisan perairan pelabuhan Tanjung Priok berbeda nyata antar waktu, kecuali pada lapisan dasar. Konsentrasi BOD5 pada perairan pelabuhan Tanjung Priok dibulan
Oktober 2005 mengalami penurunan dengan kisaran konsentrasi di tiap lapisan perairan, antara 1,95-19,38 mg/l di lapisan permukaan; 1,38-11,19 mg/l di lapisan tengah; dan 3,64-14,70 mg/l di lapisan dasar (Gambar 10). Perubahan konsent rasi BOD5 antara bulan Juni dengan Oktober 2005 diduga karena aliran sungai yang
membawa bahan organik ke perairan pelabuhan Tanjung Priok pada bulan Juni 2005 lebih banyak dibandingkan pada bulan Oktober 2005. Kondisi ini dapat ditunjang dari hasil penga matan Hidayati (2006) bahwa kandungan bahan organik dalam sedimen pada bulan Juni 2005 lebih banyak dibandingkan pada bulan Oktober 2005 (Lampiran 5). Walaupun terjadi perbedaan konsentrasi BOD5 di
tiap lapisan, namun berdasarkan hasil uji nilai tengah me nunjukkan tidak terdapat perbedaan yang nyata antar lapisan (p>0,05). Kondisi perairan pelabuhan Tanjung Priok pada bulan Oktober 2005 tidak berbeda dengan pengamatan sebelumnya yaitu berada dalam kondisi baik bagi kehidupan biota laut.
Konsentrasi BOD5 pada tiap lapisan perairan Muara Gembong berbeda
nyata antar waktu, yaitu mengalami peningkatan pada bulan Oktober 2005 (Gambar 10). Konsentrasi BOD5 di tiap lapisan perairan, berkisar antara
2,00-4,96 mg/l di lapisan permukaan; 3,20-5,40 mg/l di lapisan tengah; dan 3,60-12,60 mg/l di lapisan dasar. Walaupun terjadi peningkatan konsentrasi BOD5 pada