ISOLASI GOLONGAN BENZOFENON DARI EKSTRAK
METANOL DAGING BUAH MAHKOTA DEWA
[
Phaleria macrocarpa
(Sheff). Boerl.]
YENTI HARIYANI
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
PERNYATAAN MENGENAI TESIS DAN
SUMBER INFORMASI
Dengan ini saya menyatakan bahwa tesis Isolasi Golongan Benzofenon dari Ekstrak Metanol Daging Buah Mahkota Dewa [Phaleria macrocarpa (Sheff). Boerl.] adalah karya saya dengan arahan komisi pembimbing dan belum diajukan dalam bentuk apapun kepada perguruan tinggi manapun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam daftar pustaka di bagian akhir tesis ini.
Bogor, Juli 2011
ABSTRACT
YENTI HARIYANI. Isolation of Benzophenone Group from the Methanolic Extract of Mahkota Dewa [Phaleria macrocarpa (Scheff.) Boerl. Pulp. Under direction of LATIFAH K. DARUSMAN and IRMANIDA BATUBARA
Traditionally, mahkota dewa plant [Phaleria macrocarpa (Scheff.) Boerl.] is used to treat various diseases in Indonesia, including cancer. In developing the mahkota dewa plant as material for cancer therapy, it requires for quality control that responsible for its activity. Quality control can be determined through marker compound. This study aimed to isolate marker compound benzophenone compound, from the methanol extract of mahkota dewa pulp. Isolation was done using column chromatography and preparative thin layer chromatography (TLC) guided by BSLT activity and benzophenone coloring reagent. Mahkota dewa pulp methanol extract was fractionated with silica gel. The fraction 4 column chromatography resulted had a LC50 value of 30.90 µg/ml. Based on TLC on fraction 4, fraction 4 consisted of benzophenone on Rf 0.37. Separation of fraction 4 using preparative TLC with eluent chloroform-methanol-water (70:20:2) yielded eight fractions. The benzophenone compound could be detected at fraction 45 with the Rf of value 0.37 and gave the LC50 value 899.28 µg/ml. Identification of fraction 45 by UV-Vis spectrometer showed UV absorption at 200 nm and 264 nm. IR spectra indicated that the fraction 45 has an aromatic compound and have the same pattern with phalerin.
RINGKASAN
YENTI HARIYANI. Isolasi Golongan Benzofenon dari Ekstrak Metanol Daging
Buah Mahkota Dewa [Phaleria macrocarpa (Sheff.) Boerl.]. Dibimbing oleh
LATIFAH K. DARUSMAN dan IRMANIDA BATUBARA.
Tanaman mahkota dewa (Phaleria macrocarpa) secara luas di Indonesia telah
digunakan sebagai obat berbagai penyakit, diantaranya kanker. Di dalam pengembangan mahkota dewa sebagai obat penyakit kanker diperlukan kontrol kualitas yang bertanggung jawab terhadap aktivitasnya sebagai antikanker. Kontrol kualitas dapat ditentukan antara lain melalui senyawa penciri. Salah satu senyawa yang berperan sebagai antikanker pada tanaman mahkota dewa adalah senyawa benzofenon. Bertolak dari hal tersebut maka penelitian ini bertujuan untuk memperoleh senyawa penciri golongan benzofenon dari ekstrak metanol buah
mahkota dewa melalui pemisahan, uji Brine Shrimp Lethality Test (BSLT) dan uji
kualitatif benzofenon.
Metode ektraksi sampel dilakukan dengan cara refluks menggunakan pelarut metanol. Selanjutnya ekstrak metanol dipartisi menggunakan kloroform untuk memisahkan komponen yang bersifat semipolar, fraksi metanol dan fraksi kloroform yang diperoleh diuji fitokimia. Fraksinasi pada fraksi metanol dilakukan menggunakan kromatografi kolom dengan fase diam berupa silika gel dan fase gerak berupa n-heksana, etil asetat, metanol dengan peningkatan kepolaran. Fraksi-fraksi hasil kolom yang diduga mengandung golongan benzofenon diuji toksisitas melalui uji BSLT. Selanjutnya fraksi yang paling toksik difraksinasi dengan KLT preparatif. Fraksi hasil KLT preparatif diuji BSLT dan uji kualitatif golongan benzofenon, fraksi yang paling toksik dan positif mengandung benzofenon diidentifikasi menggunakan spektrofotometer UV-Vis dan IR.
Ekstraksi sampel sebanyak 200 g secara refluks menggunakan pelarut metanol menghasilkan rendemen 20.85%. Hasil partisi dengan kloroform diperoleh fraksi metanol dengan rendemen 72.25% dan fraksi kloroform 24.98% dari ekstrak kasar metanol. Hasil uji fitokimia pada fraksi metanol dan fraksi kloroform diperoleh data bahwa kandungan golongan benzofenon terbanyak terdapat pada fraksi metanol. Fraksinasi selanjutnya menggunakan kromatografi kolom dilakukan pada fraksi metanol. Pencarian eluen terbaik untuk penggabungan fraksi hasil kromatografi kolom menggunakan pelat kromatografi lapis tipis (KLT), fraksi yang memiliki nilai
Rf yang sama atau hampir sama akan digabung. Fraksinasi yang dilakukan terhadap
fraksi metanol menghasilkan 167 tabung yang digabung berdasarkan pola KLT dengan eluen campuran n-heksana:etil asetat:metanol (7:14:3) dan diperoleh 12 fraksi gabungan (fraksi 1-12).
BSLT menunjukkan 3 fraksi terbaik yang memiliki toksisitas yaitu fraksi 4, 10, dan
11. Fraksi 4 merupakan yang paling baik dengan nilai LC50 yang paling rendah.
Fraksinasi golongan benzofenon pada fraksi 4 dilakukan dengan menggunakan KLTP, dengan eluen campuran antara kloroform:metanol:air, perbandingan 70:20:2. Proses pemurnian fraksi 4 dengan KLTP diperoleh 8 fraksi
(fraksi 41-48). Hasil fraksinasi menggunakan KLTP ini diuji toksisitas BSLT-nya
untuk mendapatkan fraksi yang berpotensi sitotoksik. Fraksi hasil KLTP yang
memiliki potensi sitotoksik yang paling baik dengan nilai LC50 paling rendah adalah
fraksi 47 dengan nilai LC50 100 g/ml, akan tetapi nilai ini tidak sebaik nilai LC50
fraksi 4 hasil kromatografi kolom, yaitu sebesar 30.90 g/ml. Hal ini diduga karena komponen aktif tidak terpisah dengan baik pada KLTP atau disebabkan oleh komponen yang bekerja secara sinergis pada fraksi 4 menjadi berkurang setelah
difraksinasi menggunakan KLTP. Sementara itu fraksi 45 menunjukkan nilai LC50 di
bawah 1000 g/ml, yaitu 899.28 g/ml, yang berpotensi sitotoksik.
Uji kualitatif golongan benzofenon dilakukan terhadap fraksi hasil kolom,
yaitu fraksi 4-12 dan fraksi hasil KLTP, yaitu fraksi 41-48 untuk mengetahui yang
yang bersifat sitotoksik termasuk golongan benzofenon. Uji kualitatif dilakukan
dengan cara menyemprotkan reagen pendeteksi golongan benzofenon Fast Blue Salt
B 1% dalam metanol air 1:1 pada plat KLT yang telah dielusi dengan eluen terbaik
yaitu campuran kloroform:metanol:air (70:20:2). Hasil uji kualitatif menunjukkan fraksi yang diduga positif mengandung benzofenon yaitu fraksi 4, 5, 6, 10, dan 11. Hal ini terlihat dari perubahan warna spot pada plat KLT menjadi merah ungu terang sesaat setelah disemprot dengan reagen pendeteksi dan merah kecoklatan setelah
teroksidasi. Pada fraksi 4 dengan Rf 0,37 warna merah ungu sangat kontras, pada
fraksi 5 terdapat 2 spot yang positif benzofenon yaitu pada spot ke-5 dengan Rf 0,37
warna merah ungu juga sangat kontras dan pada spot ke-4 dengan Rf 0.30. Hasil uji
kualitatif fraksi hasil KLTP diperoleh fraksi 44 dan 45 yang diduga positif
mengandung golongan benzofenon. Pada fraksi 45 spot dengan nilai Rf 0.37
warnanya terlihat sangat kontras dibanding fraksi 44 yaitu merah ungu setelah
disemprot menggunakan Fast Blue Salt B dan menjadi coklat kemerahan setelah
teroksidasi. Sementara itu fraksi 44 pada uji toksisitas BSLT tidak menunjukkan
aktivitas yang baik, fraksi 45 menunjukkan aktivitas yang cukup baik walaupun tidak
sebaik aktivitas fraksi 47, tetapi pada uji kualitatif fraksi 47 tidak terdeteksi
mengandung golongan benzofenon.
Fraksi 45 hasil KLTP yang diduga merupakan golongan benzofenon dianalisis
menggunakan spektrofotometer UV-Vis. Hasil analisis menunjukkan fraksi 45
memiliki panjang gelombang maksimum ( max) dalam MeOH pada 200 nm dan
serapan lainnya pada 264 nm. Serapan pada panjang gelombang maksimum 200 nm
dan 264 nm menunjukkan adanya transisi elektron dari π ke π* yang merupakan ciri
khas untuk sistem ikatan rangkap terkonjugasi dari suatu cincin aromatik yaitu
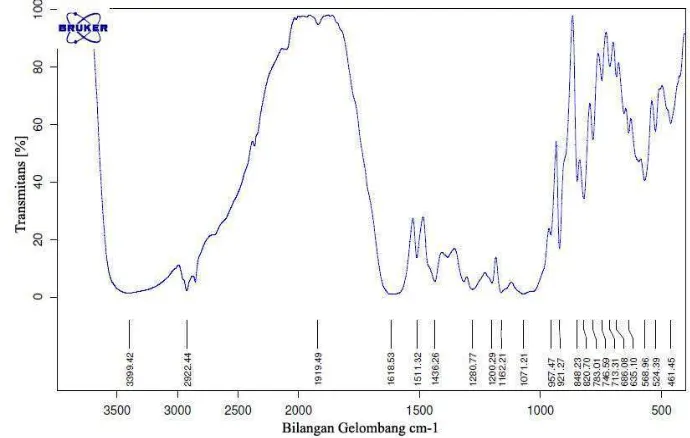
kromofor C=C aromatik dan C=O. Analisis spektrum IR fraksi 45 hasil KLTP
menunjukkan uluran pada bilangan gelombang 3399, 2922, 1919, 1618, 1511, dan
1436 cm-1. Vibrasi regang pada bilangan gelombang 3399 cm-1 dengan bentuk pita
lebar menunjukkan adanya gugus OH, vibrasi regang pada 2922 cm-1 menunjukkan
secara kuat mengindikasikan keberadaan αβ C=O tak jenuh dan vibrasi regang pada
1511 dan 1436 cm-1 mengindikasikan keberadaan cincin aromatik. Fraksi 45 hasil
KLTP yang diduga golongan benzofenon terbukti memiliki serapan pada panjang gelombang yang mirip dengan phalerin (glikosida benzofenon) yang diisolasi dari ekstrak metanol daun mahkota dewa.
Fraksi 47 hasil KLTP dari analisis spektrometer UV-Vis memiliki serapan
maksimum pada panjang gelombang 249 dan 341 nm. Kisaran panjang gelombang 250-280 nm dan 310-350 nm tergolong flavonoid yaitu jenis flavon. Sementara itu
analisis spektrum fraksi 47 hasil KLTP terdapat uluran pada bilangan gelombang
3399, 2927, 2855, 1706, 1609, 1469, 1283 cm-1 dengan uluran khas pada bilangan
gelombang 3399 cm-1 yang menunjukkan gugus OH, 2927 dan 2852 cm-1 yang
menunjukkan gugus CH2, vibrasi regang pada bilangan gelombang 1706 cm-1 yang
menandakan adanya gugus karbonil. Sedangkan pada bilangan gelombang 1609 dan
1465 cm-1 mengindikasikan keberadaan cincin aromatik. Dari data UV-Vis dan IR
fraksi 47 diduga merupakan golongan flavonoid, yaitu flavon.
Fraksi 4 yang mengandung benzofenon dan terdeteksi pada fraksi 44 dan 45,
© Hak Cipta Milik IPB, Tahun 2011 Hak Cipta dilindungi Undang-Undang
1. Dilarang mengutip sebagian atau seluruh karya tulis ini tanpa mencamtumkan
atau menyebutkan sumbernya.
a. Pengutipan hanya untuk kepentingan pendidikan, penelitian, penulisan
karya ilmiah, penyusunan laporan, penulisan kritik, atau tinjauan masalah
b. pengutipan tersebut tidak merugikan kepentingan yang wajar IPB
2. Dilarang mengumumkan dan memperbanyak sebagian atau seluruh karya tulis
ISOLASI GOLONGAN BENZOFENON DARI EKSTRAK
METANOL DAGING BUAH MAHKOTA DEWA
[
Phaleria macrocarpa
(Sheff). Boerl.]
YENTI HARIYANI
Tesis
sebagai salah satu syarat untuk memperoleh gelar Magister Sains pada
Program Studi Kimia
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
Judul Tesis : Isolasi Golongan Benzofenon Dari Ekstrak Metanol Daging Buah Mahkota Dewa [Phaleria macrocarpa (Sheff.) Boerl.]
Nama : Yenti Hariyani
NIM : G451090071
Disetujui
Komisi Pembimbing
Prof. Dr. Ir. Latifah K. Darusman, M.S. Dr. Irmanida Batubara, S.Si, M.Si
Ketua Anggota
Diketahui
Ketua Program Mayor Kimia Dekan Sekolah Pascasarjana
Prof. Dr. Purwantiningsih Sugita, M.S. Dr. Ir. Dahrul Syah, M.Sc. Agr
PRAKATA
Puji dan syukur saya panjatkan ke hadirat Allah SWT atas rahmat dan karunia-Nya sehingga karya ilmiah ini dapat diselesaikan. Tema yang dipilih dalam penelitian yang dilaksanakan sejak bulan Februari sampai Juni 2011 ini ialah Isolasi Golongan Benzofenon Dari Ekstrak Metanol Daging Buah Mahkota Dewa [Phaleria macrocarpa (Sheff.) Boerl.].
Ucapan terima kasih yang tak terhingga kepada Prof. Dr. Ir. Latifah K. Darusman, M.S. selaku Ketua Komisi Pembimbing, dan Dr. Irmanida Batubara, S.Si, M.Si. selaku Anggota Komisi Pembimbing atas segala curahan waktu, bimbingan dan dorongan moral kepada saya, serta kepada Dr. dr. Irma Herawati Suparto, M.S. selaku penguji luar komisi yang telah memberikan banyak saran untuk perbaikan tesis saya. Serta ucapan terima kasih saya kepada Kementrian Agama atas pemberian beasiswa dan biaya penelitian, dan teman-teman BUD Kemenag 2009, juga kepada staf Laboratorium Kimia Analitik Departemen Kimia IPB dan Pusat Studi Biofarmaka IPB yang telah membantu kelancaran penelitian Isolasi Golongan Benzofenon dari Ekstrak Metanol Daging Buah Mahkota Dewa ini. Ucapan terima kasih juga disampaikan kepada ibu, ayah (alm.), mas Agus, Kurnia Rizki Gusti Putra, Citra Kartika Gusti Putri atas segala doa dan kasih sayangnya.
Semoga karya ilmiah ini bermanfaat.
Bogor, Juli 2011
RIWAYAT HIDUP
Penulis dilahirkan di Sungai Penuh Kabupaten Kerinci Jambi pada tanggal 12 Januari 1971 dari ayah Hadis Rais dan ibu Mariana Syarif. Penulis merupakan putri ketiga dari empat bersaudara.
Tahun 1989, penulis lulus dari SMA DB I dan pada tahun yang sama lulus seleksi masuk Universitas Jambi melalui jalur seleksi penerimaan mahasiswa baru (sipenmaru). Penulis memilih jurusan Pendidikan Kimia Strata I, Fakultas Pendidikan Matematika dan Ilmu Pengetahuan Alam, lulus pada tahun 1994. Dan pada tahun 2009, penulis mendapatkan Beasiswa Utusan Daerah (BUD) dari Kementrian Agama Republik Indonesia untuk melanjutkan studi Magister Sains pada Program Studi Kimia, Sekolah Pascasarjana Institut Pertanian Bogor.
DAFTAR ISI
Identifikasi Golongan Benzofenon dengan Spektrofotometer UV-Vis ……….
Identifikasi Golongan Benzofenon dengan Spektrofotometer IR...
10
HASIL DAN PEMBAHASAN
Ekstraksi dan Fraksinasi ……… Toksisitas Brine Shrimp Lethality Test (BSLT) Fraksi Hasil
Kromatografi Kolom ……….
Kromatografi Lapis Tipis Preparatif (KLTP) ……… Toksisitas Brine Shrimp Lethality Test (BSLT)Fraksi Hasil
Kromatografi Lapis Tipis Preparatif (KLTP) ………
Keberadaan Golongan Benzofenon Hasil Kromatografi Kolom dan Kromatografi Lapis Tipis Preparatif (KLTP) ...
xiv
DAFTAR TABEL
Halaman
1 2
Senyawa glikosida benzofenon dari Phaleria macrocarpa ……... Hasil uji fitokimia fraksi metanol dan fraksi kloroform buah mahkota dewa ………
Hasil uji toksisitas BSLT fraksi hasil kolom ……….. Hasil uji toksisitas BSLT fraksi hasil KLTP ……….. Jumlah spot dan nilai Rf dari fraksi yang diduga positif
mengandung senyawa benzofenon ………
Hasil fraksinasi kromatografi kolom dan KLTP, toksisitas BSLT dan keberadaan benzofenon...
Absorpsi IR gugus-gugus fungsi fraksi 45 dan 47 hasil
xv
DAFTAR GAMBAR
Halaman
1 Buah muda dan tua tanaman mahkota dewa ………... 4 2 Struktur kimia senyawa turunan benzofenon ……… 6 3 Pola KLT eluen terbaik eluen n-heksana:etil asetat: metanol
(7:14:3) ………..……... 14 4 Pola KLT penggabungan fraksi hasil kromatografi kolom .…….. 15 5 Pola KLT preparatif fraksi 4 hasil kromatografi kolom ...…….. 17 6 Pola KLT hasil KLTP fraksi 4 ..……… 17
xvi
DAFTAR LAMPIRAN
Halaman
1 Bagan alir penelitian ………….………... 30 2 Hasil pencarian eluen terbaik dengan penggabungan 2 eluen ….. 31 3
4 5
Pengelompokan fraksi hasil kromatografi kolom …...………….. Contoh perhitungan LC50 fraksi 4 hasil kolom ……… Nilai Rf fraksi hasil KLTP ………
1
PENDAHULUAN
Latar BelakangTanaman mahkota dewa (Phaleria macrocarpa) secara luas di Indonesia telah digunakan sebagai obat alternatif kanker. Secara empirik, mahkota dewa digunakan untuk pengobatan medis. Batangnya digunakan untuk pengobatan kanker tulang, daunnya digunakan untuk pengobatan impotensi, alergi, diabetes mellitus, dan tumor. Cangkang biji buah mahkota dewa digunakan untuk penyakit kanker payudara, kanker rahim, penyakit paru-paru, dan penyakit hati (Aditama 2001).
Dari hasil evaluasi fitokimia, simplisia buah mahkota dewa mengandung alkaloid, flavonoid, fenol/polifenol, tanin, saponin, terpenoid/sterol (Lisdawati 2002). Hasil identifikasi senyawa kimia dari buah mahkota dewa diperoleh kandungan asam lemak, steroid, benzofenon glikosida dan karbohidrat (Simanjuntak 2008). Hartati et al. (2005) melaporkan suatu senyawa glikosida benzofenon baru (phalerin) dari daun mahkota dewa yang bersifat sitotoksik terhadap sel myeloma (NS-1) dan uji aktivitas biologi pada phalerin menunjukkan bahwa senyawa ini bersifat non-toksik dan memiliki potensi imunostimulan. Penelitian yang dilakukan oleh Oshimi et al. (2008) pada buah mahkota dewa dilaporkan senyawa turunan glikosida benzofenon yang berbeda dari phalerin yaitu 2,4’,6-trihidroksi-4-metoksibenzofenon-2-O-β-D-glukosida yang sebelumnya telah diisolasi dari tanaman Gnidia involucrate yang juga termasuk genus Thymelaeaceae. Senyawa ini juga telah diisolasi oleh Tambunan dan Simanjuntak (2006) dari ekstrak n-butanol buah mahkota dewa yang dihidrolisis dengan HCl 9% dalam metanol.
Di dalam pengembangan mahkota dewa sebagai obat berbagai jenis penyakit terutama kanker diperlukan kontrol kualitas yang bertanggung jawab terhadap aktivitasnya sebagai antikanker. Kontrol kualitas dapat ditentukan antara lain melalui senyawa penciri.
2
ditemukan untuk mendapatkan suatu senyawa metabolit sekunder dari tumbuhan obat diperoleh rendemen dan kemurnian relatif kecil dan sulit untuk dijadikan standar karena kurang tepatnya pelarut atau eluen, teknik ekstraksi dan teknik pemisahan yang digunakan.
Tujuan Penelitian
Penelitian ini bertujuan untuk memperoleh senyawa penciri golongan benzofenon dari ekstrak metanol buah mahkota dewa melalui pemisahan, uji
Brine Shrimp Lethality Test (BSLT) dan uji kualitatif benzofenon.
Manfaat Penelitian
TINJAUAN PUSTAKA
Mahkota Dewa
Phaleria macrocarpa (Scheff.) Boerl atau yang dikenal dengan nama mahkota dewa merupakan tanaman asli Indonesia yang berasal dari Papua. Umumnya tanaman ini dibudidayakan sebagai tanaman hias atau tanaman peneduh, tetapi terkadang masih dapat dijumpai tumbuh liar di hutan pada ketinggian 10-1.200 m di atas permukaan laut dengan curah hujan rata-rata 1.000-2.500 mm/tahun. Dari segi taksonomi tanaman ini dikelompokkan ke dalam divisi Spermathophyta, filum Angiospermae, kelas Dycotyledoneae, ordo Tymelaeales, famili Tymelaeaceae, genus Phaleria dan spesies Phaleria macrocarpa (Scheff.) Boerl.
4
Gambar 1. Buah muda (hijau) dan buah tua (merah) mahkota dewa
Phaleria macrocarpa (Scheff.) Boerl, yang dikenal dengan nama mahkota dewa telah cukup lama dimanfaatkan oleh masyarakat Indonesia untuk mengobati berbagai penyakit, seperti diabetes melitus, kanker, hati, jantung, asam urat, rematik, ginjal, tekanan darah tinggi, eksim, jerawat, dan luka gigitan serangga (Lisdawati 2002). Penelitian yang dilakukan oleh Sugiwati (2005) diperoleh bahwa ekstrak kasar buah mahkota dewa pada fraksi etil asetat, butanol dan air berhasil menghambat aktivitas α-glukosidase secara in vitro berturut-turut sebesar 69.90 %, 42.27 %, dan 33.01 %.
Penapisan farmakologi untuk aktivitas antikanker secara in vitro dari ekstrak kasar fraksi non polar, semipolar dan polar daging buah serta cangkang biji mahkota dewa telah diujikan terhadap sel leukemia L1210. Fraksi semipolar (etil asetat) merupakan fraksi yang memiliki aktivitas inhibisi paling tinggi terhadap perkembangbiakan sel leukemia L1210 dengan nilai IC50 5.76 µg/ml
5
Glikosida benzofenon
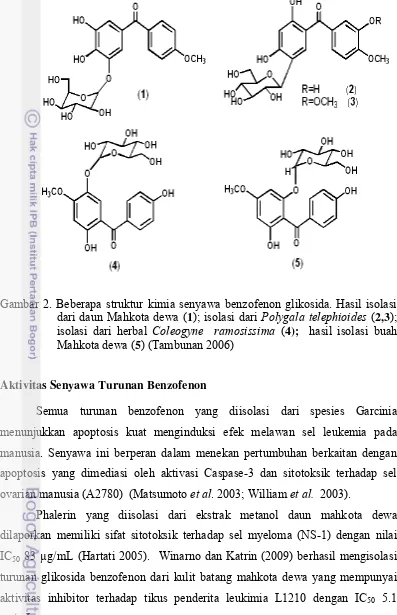
Glikosida benzofenon merupakan senyawa turunan benzofenon yang satu atau lebih gugus hidroksilnya terikat pada satu gula atau lebih. Beberapa senyawa glikosida benzofenon yang terdapat dalam tanaman mahkota dewa ditunjukkan dalam Tabel 1.
Tabel 1 Senyawa glikosida benzofenon dari Phaleria macrocarpa
Bagian tumbuhan Nama Senyawa glikosida benzofenon Peneliti
Daun
4,5-dihidroksi-4-metoksibenzofenon-Kulit kayu 6,4’-dihidroksi-4-metoksi benzofenon-2-O-β
6
Gambar 2. Beberapa struktur kimia senyawa benzofenon glikosida. Hasil isolasi dari daun Mahkota dewa (1); isolasi dari Polygala telephioides (2,3); isolasi dari herbal Coleogyne ramosissima (4); hasil isolasi buah Mahkota dewa (5) (Tambunan 2006)
Aktivitas Senyawa Turunan Benzofenon
Semua turunan benzofenon yang diisolasi dari spesies Garcinia menunjukkan apoptosis kuat menginduksi efek melawan sel leukemia pada manusia. Senyawa ini berperan dalam menekan pertumbuhan berkaitan dengan apoptosis yang dimediasi oleh aktivasi Caspase-3 dan sitotoksik terhadap sel ovarian manusia (A2780) (Matsumoto et al. 2003; William et al. 2003).
Phalerin yang diisolasi dari ekstrak metanol daun mahkota dewa dilaporkan memiliki sifat sitotoksik terhadap sel myeloma (NS-1) dengan nilai IC50 83 µg/mL (Hartati 2005). Winarno dan Katrin (2009) berhasil mengisolasi
turunan glikosida benzofenon dari kulit batang mahkota dewa yang mempunyai aktivitas inhibitor terhadap tikus penderita leukimia L1210 dengan IC50 5.1
7
Uji Toksisitas Brine Shrimp Lethality Test (BSLT)
Uji toksisitas BSLT merupakan deteksi awal untuk mengetahui potensi bioaktivitas dan toksisitas dari sampel sehingga dapat ditentukan konsentrasi ekstrak yang aman untuk pengujian. Uji dilakukan untuk mengamati tingkat kematian larva udang Artemia salina Leach yang disebabkan oleh ekstrak metabolit sekunder, tingkat kematian atau mortalitas selanjutnya dianalisis dengan menggunakan analisis probit untuk menentukan konsentrasi LC50 (lethal
concentration) 50%, yaitu konsentrasi yang menyebabkan kematian populasi larva udang sebesar 50% dari populasi total. Senyawa yang mempunyai LC50
lebih kecil dari 1000 ppm dikatakan memiliki potensi bioaktivitas (Meyer et al.
1982).
Lisdawati (2002) telah melakukan pengujian BSLT terhadap kadar toksisitas ekstrak daging buah mahkota dewa dan kulit bijinya dengan melihat tingkat kematian larva A. Salina setelah diinkubasi selama 24 jam. Hasilnya menunjukkan toksisitas yang sangat tinggi yang menyebabkan kematian 50% larva udang (LC50) yang berkisar antara 0.1615-11.8351 µg/ml.
9
METODE PENELITIAN
Alat dan Bahan
Alat-alat yang digunakan adalah Spektrofotometer UV-Vis (Shimadzu), dan IR (Brucker), multiwell plates, evaporator, pelat KLT silika gel GF254 dan
pelat KLT preparatif, kolom kromatografi silika gel (Merck; 70-230 mesh; 1x25 cm), pipet mikro, tip pipet mikro, pipet Mohr.
Bahan yang digunakan adalah buah mahkota dewa yang diperoleh dari kebun percobaan Pusat Studi Biofarmaka (PSB), pelarut MeOH, CHCl3, EtOAc, Artemia salina Leach, dan air laut.
Preparasi dan Ekstraksi Sampel (Hartati et al. 2005)
Preparasi sampel ekstrak buah mahkota dewa dilakukan dengan cara mengeringanginkan daging buah mahkota dewa yang telah diiris tipis, kemudian dibuat serbuk berukuran 80 mesh. Sampel serbuk kering ditentukan kadar airnya. Sampel diekstraksi dengan cara refluks menggunakan pelarut metanol pada suhu 600C. Semua ekstrak yang diperoleh disaring dengan menggunakan kertas saring Whatman no. 1 dan dipekatkan dengan penguap putar pada suhu 300C kemudian dihitung rendemennya. Selanjutnya ekstrak metanol dipartisi menggunakan kloroform untuk memisahkan komponen yang bersifat semipolar, masing-masing ekstrak diuji flavonoid, fenol, dan triterpenoid dan steroid.
Penentuan Kadar Air (AOAC 2006)
Cawan dikeringkan terlebih dahulu selama 30 menit dalam oven pada suhu 1050C, lalu didinginkan dalam eksikator kemudian beratnya ditimbang. Sampel ditimbang seberat 5 gram dan dimasukkan ke dalam cawan, kemudian sampel dimasukkan kedalam oven selama 3 jam pada suhu 1050C, lalu didinginkan dalam eksikator selama 30 menit kemudian ditimbang kembali sampai diperoleh bobot yang konstan (AOAC 2006).Persen kadar air dihitung dengan persamaan:
Kadar air (%) : a-b x 100 %
a
a adalah bobot sebelum dikeringkan (g)
10
Uji Fitokimia (Harborne 1987)
Uji Flavonoid. Sebanyak 1 gram ekstrak ditambah 100 ml air panas kemudian dididihkan selama 5 menit dan disaring. Filtrat yang diperoleh diambil sebanyak 5 ml ditambah 0,05 g serbuk magnesium, 1 ml HCl pekat dan 1 ml amil alkohol kemudian dikocok kuat-kuat, terbentuknya warna merah, kuning dan jingga pada lapisan amil akohol menunjukkan adanya flavonoid.
Uji Triterpenoid dan Steroid. Ekstrak mahkota dewa dilarutkan dalam 25 ml etanol panas (500C) kemudian disaring dalam cawan porselin dan diuapkan sampai kering. Residu ditambahkan eter dan ekstrak eter dipindahkan ke dalam lempeng, lalu ditambahkan 3 tetes anhidrida asam asetat dan 1 tetes H2SO4 pekat
(uji Lieberman-Burchard), warna merah atau ungu menunjukkan adanya triterpenoid dan warna hijau atau biru menunjukkan adanya steroid.
Uji Fenol. Ekstrak mahkota dewa dengan bobot tertentu dimasukkan ke dalam tabung reaksi. Kemudian ditambahkan FeCl3 dan bila terbentuk warna ungu, biru
atau hijau menunjukkan adanya senyawa golongan fenol.
Penentuan Eluen Terbaik pada KLT
Ekstrak pekat dari sampel ditotolkan pada pelat KLT. Setelah kering langsung dielusi dalam ruang elusi yang telah dijenuhkan oleh uap eluen pengembang. Eluen yang digunakan adalah metanol, etil asetat, kloroform, aseton butanol, diklorometana,dan n-heksana, lalu dilakukan perbandingan pada eluen yang menghasilkan spot yang banyak dan terpisah. Eluen akan diperbaiki lebih lanjut apabila pemisahan belum baik. Noda hasil elusi diamati di bawah lampu UV pada panjang gelombang 254 dan 366 nm.
Fraksinasi dengan Kromatografi Kolom (Rouessac & Rouessac 2007)
Fraksinasi dilakukan menggunakan kromatografi kolom dengan fase diam berupa silika gel Merck dengan ukuran 70-230 mesh dan fase gerak berupa n-heksana, etil asetat, metanol dengan peningkatan kepolaran. Eluat ditampung setiap 5 ml dalam tabung reaksi, kemudian eluat diuji dengan KLT. Eluat yang memiliki jumlah bercak dan nilai Rf yang sama atau hampir sama digabung
11
Fraksi-fraksi hasil kolom yang diduga mengandung senyawa golongan benzofenon diuji toksisitas melalui uji BSLT. Selanjutnya fraksi yang paling toksik difraksinasi dengan KLT preparatif, noda yang diperoleh kemudian dideteksi di bawah lampu UV 254 nm dan 366 nm. Fraksi hasil KLT preparatif diuji BSLT dan uji kualitatif senyawa golongan benzofenon, fraksi yang paling toksik dan positif mengandung benzofenon diidentifikasi menggunakan spektrofotometer UV-Vis dan IR. Diagram alir penelitian dapat dilihat pada Lampiran 1.
Uji Toksisitas Brine Shrimp Lethality Test (BSLT) (Meyer et al. 1982)
Uji toksisitas dilakukan dengan menentukan nilai Lethal Concentration
(LC50) menngunakan larva udang Artemia salina L. Telur udang ditetaskan dalam
gelas piala yang berisi air laut, penetasan dilakukan selama 48 jam dan diaerasi agar kadar oksigen tercukupi sehingga telur udang menetas menjadi larva. Ke dalam masing-masing sumur dimasukkan 10 ekor larva udang dan larutan fraksi yang akan diuji dengan konsentrasi 10 sampai 1.000 ppm (masing-masing 3 kali ulangan), diinkubasi selama 24 jam dan dihitung jumlah larva yang mati. LC50
ditentukan dengan membuat kurva hubungan antara % kematian larva dan log konsentrasi ekstrak. Apabila pada kontrol ada larva yang mati maka % kematian larva udang ditentukan dengan rumus Abbot.
% kematian larva : T – K x 100 % S
Keterangan : T : jumlah larva uji yang mati K : jumlah larva kontrol yang mati S : jumlah larva uji
Uji Kualitatif Golongan Benzofenon (Nedialkov P & Kitanov G 2001)
Untuk mendeteksi adanya senyawa benzofenon dalam suatu sampel dapat dilakukan dengan cara menyemprotkan reagen Fast Blue Salt B dalam MeOH:H2O (1:1). Bila terjadi perubahan warna spot pada plat KLT menjadi ungu
12
Identifikasi Senyawa Benzofenon dengan Spektrofotometer UV-Vis
Identifikasi dengan spektrofotometer UV-Vis dilakukan dengan mengukur spektrum serapan dalam larutan blanko yang sangat encer dengan pembanding blanko pelarut, pelarut yang digunakan dalam pengukuran adalah pelarut sampel yaitu metanol (Harborne, 1987). Senyawa dalam sampel diukur pada panjang gelombang 200-800 nm. Analisis dilakukan dengan metode baku di Laboratorium Pusat Studi Biofarmaka, IPB.
Identifikasi Senyawa Benzofenon dengan Spektrofotometer IR
13
HASIL DAN PEMBAHASAN
Ekstraksi dan Fraksinasi
Sampel buah mahkota dewa yang digunakan pada penelitian ini diperoleh dari kebun percobaan Pusat Studi Biofarmaka, Institut Pertanian Bogor dalam bentuk simplisia yang kemudian dijadikan serbuk dengan ukuran 80 mesh. Kadar air serbuk mahkota dewa yang diperoleh sebesar 2.12%. Kadar air yang diperoleh kurang dari 10% merupakan kadar air yang baik karena pada tingkat kadar air tersebut waktu simpan sampel akan relatif lebih lama dan terhindar dari pencemaran yang disebabkan oleh mikroba dan memenuhi syarat sebagai bahan baku herbal (Winarno 1992; BPOM 2004).
Ekstraksi serbuk buah mahkota dewa sebanyak 200 g dilakukan dengan cara refluks menggunakan pelarut metanol, disaring dan diuapkan dengan rotary evaporator pada suhu 30oC. Ekstrak pekat yang diperoleh sebanyak 39.0776 g dengan rendemen 20.85%. Selanjutnya ekstrak metanol yang diperoleh dipartisi menggunakan kloroform. Hasil partisi dengan kloroform diperoleh fraksi metanol dengan rendemen 72.25% dan fraksi kloroform 24.98% dari ekstrak kasar metanol.
Untuk mengetahui kandungan kimia dari fraksi metanol dan fraksi kloroform dilakukan uji fitokimia antara lain uji flavonoid, triterpenoid, steroid dan uji fenol. Hasil pengujian fitokimia fraksi metanol dan fraksi kloroformbuah mahkota dewa dapat dilihat pada Tabel 2.
Tabel 2 Hasil uji fitokimia fraksi metanol dan fraksi kloroform buah mahkota dewa
Golongan Senyawa Fraksi Metanol Fraksi Kloroform
14
Hasil uji fitokimia pada Tabel 2 menunjukkan bahwa pada fraksi metanol golongan triterpenoid memperlihatkan warna ungu yang tidak terlalu kuat, sedangkan pada fraksi kloroform warna ungu terlihat pekat sehingga diduga triterpenoid terpisahkan pada partisi dengan kloroform. Sementara itu steroid pada kedua fraksi baik fraksi metanol maupun kloroform menunjukkan intensitas warna hijau yang kuat, yang menunjukkan keberadaan golongan steroid. Flavonoid pada fraksi metanol lebih kuat intensitas warnanya dibanding pada fraksi kloroform, hal itu terlihat dari warna merah yang kuat pada lapisan amil alkohol dari fraksi metanol.
Pada uji fenol, fraksi metanol menunjukkan intensitas warna hijau yang lebih kuat dibanding fraksi kloroform. Oleh karena itu pada penelitian ini tujuan utamanya adalah untuk memperoleh golongan benzofenon yang merupakan bagian dari fenol, maka fraksinasi selanjutnya dilakukan pada fraksi metanol.
Pencarian eluen terbaik untuk penggabungan fraksi hasil kromatografi kolom menggunakan pelat kromatografi lapis tipis (KLT), fraksi yang memiliki nilai Rf yang sama atau hampir sama akan digabung. Pencarian eluen dimulai dari
15
Gambar 3 Pola KLT eluen terbaik eluen n-heksana:etil asetat: metanol (7:14:3)
Fraksinasi dilakukan untuk memurnikan fraksi metanol sehingga diperoleh senyawa golongan benzofenon yang bersifat sitotoksik melalui uji toksisitas Brine Shrimp Lethality Test (BSLT). Fraksinasi dilakukan menggunakan kromatografi kolom dengan fase diam silika gel dengan metode step gradient (peningkatan kepolaran) dimulai dari eluen n-heksana, etil asetat, dan metanol. Tujuan peningkatan polaritas sistem eluen agar semua komponen yang terlarut dalam fraksi metanol akan terbawa lebih cepat dan pemisahan dapat berlangsung dengan baik.
Fraksinasi yang dilakukan terhadap fraksi metanol menghasilkan 167 tabung yang digabung berdasarkan pola KLT dengan eluen campuran n-heksana:etil asetat:metanol (7:14:3) sehingga diperoleh 12 fraksi (fraksi 1-12) seperti yang ditunjukkan pada Gambar 4. Harga Rf dan jumlah spot
16
E F1 F2 F3 F4 F5 F6 F7 F8 F9 F10 F11 F12
Gambar 4 Pola KLT penggabungan fraksi hasil kromatografi kolom dengan eluen terbaik eluen n-heksana:etil asetat: metanol (7:14:3)
Uji Toksisitas Brine Shrimp Lethality Test (BSLT) Fraksi Hasil Kromatografi
Kolom
Uji toksisitas dilakukan pada fraksi 4-12 yang diduga mengandung senyawa golongan benzofenon. Terhadap fraksi 1-3 tidak dilakukan uji toksisitas karena diduga kuat tidak terdapat senyawa golongan benzofenon yang bersifat polar, sementara itu fraksi 1-3 diduga merupakan kelompok senyawa nonpolar karena fraksi 1-3 diperoleh setelah dielusi dengan eluen nonpolar.
Nilai LC50 fraksi 4-12 dapat dilihat pada Tabel 3. Dari hasil uji toksisitas
BSLT (Tabel 3) diperoleh 3 fraksi terbaik yang memiliki toksisitas yaitu fraksi 4, 10, dan 11. Contoh perhitungan nilai LC50 dapat dilihat pada Lampiran 4. Fraksi
4 merupakan yang paling baik dengan nilai LC50 yang paling rendah. Hasil yang
17
(2002) terhadap ekstrak kasar metanol mahkota dewa (LC50 berkisar antara
0.1615-11.8351 g/ml). Diduga hal tersebut disebabkan oleh perbedaan lokasi tanam, iklim, dan waktu simpan yang membuat kandungan metabolit sekundernya berbeda.
Tabel 3 Toksisitas BSLT fraksi hasil kolom (fraksi 4-12) fraksi metanol buah mahkota dewa
Kromatografi Lapis Tipis Preparatif (KLTP)
18
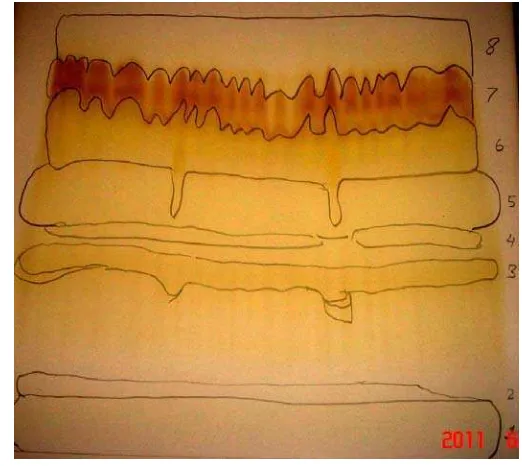
Gambar 5 Pola KLT preparatif fraksi 4 hasil kromatografi kolom, eluen kloroform:metanol:air (70:20:2)
Proses pemurnian fraksi 4 dengan KLTP menggunakan adsorben silika gel. Berdasarkan pemisahan yang dilakukan diperoleh 8 fraksi (fraksi 41-48).
Noda yang terbentuk dapat dilihat dari pola KLT fraksi 4 hasil KLTP pada Gambar 6. Nilai Rf ke-8 fraksi hasil KLTP ini dapat dilihat pada Lampiran 5.
F4 F41 F42 F43 F44 F45 F46 F47 F48
19
Toksisitas Brine Shrimp Lethality Test (BSLT) Fraksi Hasil Kromatografi
Lapis Tipis Preparatif (KLTP)
Hasil fraksinasi menggunakan KLTP ini diuji toksisitas BSLT-nya untuk mendapatkan fraksi yang berpotensi sitotoksik. Adapun hasil pengujian aktivitas toksisitas BSLT terhadap 8 fraksi KLTP yang diperoleh ditunjukkan pada Tabel 4.
Tabel 4. Toksisitas BSLT fraksi hasil KLTP (fraksi41-48)
Fraksi hasil
Data pada Tabel 4 menunjukkan bahwa fraksi hasil KLTP yang memiliki potensi sitotoksik yang paling baik dengan nilai LC50 paling rendah adalah fraksi
47 dengan nilai LC50 100 g/ml, akan tetapi nilai ini tidak sebaik nilai LC50 fraksi
4 hasil kromatografi kolom yaitu sebesar 30.90 g/ml. Hal ini diduga karena komponen aktif tidak terpisah dengan baik pada KLTP atau disebabkan oleh komponen yang bekerja secara sinergis pada fraksi 4 menjadi berkurang setelah difraksinasi menggunakan KLTP. Sementara itu fraksi 45 menunjukkan nilai
LC50 di bawah 1000 g/ml, yaitu 899.28 g/ml, yang berpotensi sitotoksik.
Keberadaan Golongan Benzofenon pada Fraksi Hasil Kromatografi Kolom
dan Kromatografi Lapis Tipis Preparatif (KLTP)
Uji kualitatif golongan benzofenon dilakukan terhadap fraksi-fraksi hasil kromatografi kolom dan KLTP yang telah diuji toksisitas BSLTnya. Uji kualitatif ini dilakukan untuk mengetahui senyawa yang bersifat sitotoksik termasuk senyawa golongan benzofenon. Uji kualitatif fraksi hasil kolom, yaitu fraksi 4-12 dan fraksi hasil KLTP, yaitu fraksi 41-48. Uji kualitatif dilakukan dengan cara
20
dalam metanol air 1:1 pada plat KLT yang telah dielusi dengan eluen terbaik yaitu campuran kloroform:metanol:air (70:20:2). Hasil uji kualitatif fraksi-fraksi hasil kolom ditunjukkan pada Gambar 7.
E F4 F5 F6 F7 F8 F9 F10 F11 F12
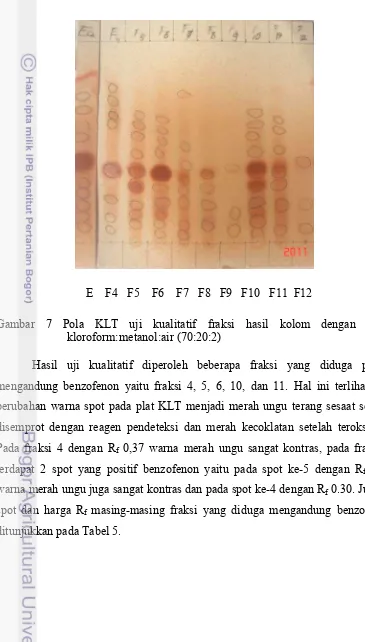
Gambar 7 Pola KLT uji kualitatif fraksi hasil kolom dengan eluen kloroform:metanol:air (70:20:2)
Hasil uji kualitatif diperoleh beberapa fraksi yang diduga positif mengandung benzofenon yaitu fraksi 4, 5, 6, 10, dan 11. Hal ini terlihat dari perubahan warna spot pada plat KLT menjadi merah ungu terang sesaat setelah disemprot dengan reagen pendeteksi dan merah kecoklatan setelah teroksidasi. Pada fraksi 4 dengan Rf 0,37 warna merah ungu sangat kontras, pada fraksi 5
terdapat 2 spot yang positif benzofenon yaitu pada spot ke-5 dengan Rf 0,37
warna merah ungu juga sangat kontras dan pada spot ke-4 dengan Rf 0.30. Jumlah
spot dan harga Rf masing-masing fraksi yang diduga mengandung benzofenon
21
Tabel 5 Jumlah spot dan nilai Rf dari fraksi yang diduga positif mengandung
senyawa benzofenon
Fraksi hasil kolom Jumlah spot Nilai Rf
4 1 0.37
5 2 0.30;0.37
6 2 0.15;0,37
10 3 0.15;0.30;0.37
11 2 0.30;0.37
Selanjutnya dilakukan uji kualitatif terhadap fraksi hasil KLTP yaitu fraksi 41-48 melalui cara yang sama dengan yang dilakukan pada fraksi-fraksi hasil
kromatografi kolom. Hasil uji kualitatif fraksi hasil KLTP ditunjukkan pada Gambar 8.
F4 F41 F42 F43 F44 F45 F46 F47 F48
Gambar 8 Pola KLT uji kualitatif fraksi 4 hasil KLTP dengan eluen kloroform:metanol:air (70:20:2).
Dari hasil uji kualitatif fraksi hasil KLTP diperoleh fraksi 44 dan 45 yang
diduga positif mengandung senyawa benzofenon. Pada fraksi 45 spot dengan nilai
Rf 0.37 warnanya terlihat sangat kontras dibanding fraksi 44 yaitu merah ungu
setelah disemprot menggunakan Fast Blue Salt B dan menjadi coklat kemerahan setelah teroksidasi. Sementara itu fraksi 44 pada uji toksisitas BSLT tidak
menunjukkan aktivitas yang baik, fraksi 45 menunjukkan aktivitas yang cukup
baik walaupun tidak sebaik aktivitas fraksi 47, tetapi pada uji kualitatif fraksi 47
22
dan memiliki potensi sitotoksik terbaik dibanding fraksi hasil KLTP lainnya, diduga fraksi 47 merupakan senyawa turunan fenolat lain. Untuk mengidentifikasi
golongan senyawa dideteksi menggunakan spektrofotometer UV-Vis dan IR. Rangkuman hasil fraksinasi, uji toksisitas dan uji kualitatif yang telah dilakukan selengkapnya ditunjukkan pada Tabel 6.
Tabel 6 Hasil fraksinasi kromatografi kolom dan KLTP, toksisitas BSLT dan keberadaan benzofenon
Keterangan : pada uji kualitatif : (-): tidak terdeteksi; (+): intensitas warna cukup kuat; (++): intensitas warna kuat; pada LC50 : (-): tidak toksik
Dari data pada Tabel 6 terlihat bahwa fraksi 4 hasil kolom dari fraksi metanol selain memiliki rendemen terbanyak, juga paling toksik pada uji BSLT dan positif mengandung benzofenon pada uji kualitatif. Dari data tersebut diduga bahwa pada fraksi 4 yang bersifat sitotoksik adalah senyawa benzofenon. Sementara itu fraksi 47 hasil KLTP yang tidak terdeteksi mengandung benzofenon
dari uji BSLT ternyata memiliki toksisitas yang tinggi, sedangkan fraksi 45 yang
23
diduga pada fraksinasi menggunakan KLTP senyawa aktif belum terpisah dengan baik sehingga efek toksisitasnya menurun.
Fraksi 47 merupakan fraksi hasil pemisahan dari fraksi metanol yang pada
uji fitokimia terdeteksi memiliki kandungan flavonoid yang tinggi sehingga diduga senyawa yang bersifat sitotoksik pada fraksi 47 merupakan senyawa
golongan flavonoid. Untuk mengetahui golongan senyawa dari fraksi 45 dan 47
maka dilakukan identifikasi menggunakan spektrofotometer UV-Vis dan IR.
Analisis Spektrofotometer UV-Vis Fraksi Hasil KLTP
Fraksi 45 hasil KLTP yang dari uji kualitatif diduga merupakan senyawa
golongan benzofenon dianalisis menggunakan spektrofotometer UV-Vis. Hasil analisis menunjukkan fraksi 45 memiliki panjang gelombang maksimum ( max)
dalam MeOH pada 200 nm dan serapan lainnya pada 264 nm (Gambar 9).
Gambar 9 Spektrum UV-Vis Fraksi 45 hasil KLTP
24
berada pada kisaran panjang gelombang senyawa benzofenon yang telah dilaporkan oleh Bernardi et al. (2004).
Sementara itu pada fraksi 47 hasil KLTP yang pada uji kualitatif tidak
mengandung senyawa benzofenon, tetapi melalui uji sitotoksik BSLT memiliki nilai LC50 paling rendah, memiliki serapan maksimum pada panjang gelombang
249 dan 341 nm (Gambar 10), menurut Markham (1988) kisaran panjang gelombang 250-280 nm dan 310-350 nm tergolong flavonoid yaitu jenis flavon,
maks 250-270 nm menurut Harborne (1982) merupakan golongan flavon.
Gambar 10 Spektrum UV-Vis Fraksi 47 hasil KLTP
Analisis Spektrofotometer IR Fraksi Hasil KLTP
Analisis spektrum IR fraksi 45 hasil KLTP (Gambar 11) menunjukkan
uluran pada bilangan gelombang 3399, 2922, 1919, 1618, 1511, dan 1436 cm-1. Vibrasi regang pada bilangan gelombang 3399 cm-1 dengan bentuk pita lebar menunjukkan adanya gugus OH, vibrasi regang pada 2922 cm-1 menunjukkan grup C-H jenuh atau metil (-CH3), serapan pada bilangan gelombang 1618 cm-1
25
Gambar 11 Spektrum IR fraksi 45 hasil KLTP
Sementara itu analisis spektrum fraksi 47 (Gambar 12) hasil KLTP
terdapat uluran pada bilangan gelombang 3399, 2927, 2855, 1706, 1609, 1469, 1283 cm-1 dimana pada bilangan gelombang 3399 cm-1 menunjukkan gugus OH, 2927 dan 2852 cm-1 menunjukkan gugus CH2, vibrasi regang pada bilangan
gelombang 1706 cm-1 menandakan adanya gugus karbonil. Sedangkan pada bilangan gelombang 1609 dan 1465 cm-1 mengindikasikan keberadaan cincin aromatik. Dari data UV-Vis dan IR fraksi 47 diduga merupakan golongan
flavonoid yaitu flavon.
26
Berdasarkan dugaan gugus fungsi yang didapatkan, terbukti adanya senyawa golongan benzofenon pada fraksi 45 hasil kLTP dan golongan flavonoid
yaitu flavon pada fraksi 47 hasil KLTP yang dapat dilihat pada Tabel 7.
Tabel 7 Absorpsi IR gugus-gugus fungsi fraksi 45 dan 47 hasil KLTP
Bilangan gelombang (cm-1) Dugaan
Keterangan: *)Hartati et al. 2005; **)Fessenden & Fessenden J.S 1986; ***)Colthup et al. 1975
Fraksi 45 hasil KLTP yang diduga senyawa golongan benzofenon terbukti
27
SIMPULAN DAN SARAN
Simpulan
Fraksi 4 hasil pemisahan ekstrak metanol mahkota dewa menggunakan kromatografi kolom mengandung senyawa benzofenon dan berpotensi sitotoksik dengan nilai LC50 sebesar 30.90 µg/ml. Fraksi 45 hasil KLTP dari analisis
UV-Vis dan IR diduga merupakan senyawa benzofenon dari data spektrum IR yang menunjukkan kemiripan dengan spektrum IR phalerin yang merupakan senyawa golongan benzofenon glikosida, dengan LC50 sebesar 899.28 µg/ml. Sementara
itu dari fraksi 4 diperoleh fraksi 47 hasil KLTP yang bersifat lebih sitotoksik dari
fraksi 45 dengan nilai LC50 sebesar 100 µg/ml yang diduga merupakan golongan
flavonoid yaitu flavon.
Saran
29
DAFTAR PUSTAKA
Aditama, T.Y. Kanker, 2001. Medisinal Jurnal Kedokteran, 2. 1-5
[AOAC] Association of Official Analytical Chemist. 2006. Official Methods of Analysis of the Association of Official Analytical Chemist. Edisi ke-18. Washington DC: AOAC.
(BPOM) Badan Pengawas Obat dan Makanan, 2004. Monografi Ekstrak Tumbuhan Indonesia. Volume 1. Jakarta: Direktorat Jendral Pengawasan Obat dan Makanan.
Bernardi APM, Ferraz ABF, Albring DV, Bordignon SAL, Schripsema J, Bridi R, Dultra-Filho CS, Henriques AT, von Poser GL. 2004. Benzophenone from
Hypericum carinatum. American Chemical Society and American Society of Pharmacognosy.
Colthup NB, Daly LD, Wilberly SE. 1975. Introduction to Infrared and Raman Spectroscopy. 2nd edition. New York: Academic Press.
Fessenden R.J dan Fessenden J.S. 1986. Kimia Organik. Jilid I. Aloysius Hadyana Pudjaatmaka, penerjemah. Jakarta: Erlangga. Terjemahan dari: Organic Chemistry
Harborne JB. 1987. Metode Fitokimia:Penuntun Cara Modern Menganalisis Tumbuhan. Terbitan ke-2. K. Padmawinata dan I Soediro, Penerjemah; Bandung ITB. Terjemahan dari: Phytochemical Methods
Harmanto N. 2003. Mahkota Dewa Obat Pusaka Para Dewa. Jakarta: Agromedia Pustaka.
Hartati WMS, Mubarika S, Gandjar IG, Hamann MT, Rao KV, Wahyuono S. 2005. Phalerin, a new benzhopenoic glucoside isolated from the methanolic extract of Mahkota Dewa [Phaleria macrocarpa (scheff). Boerl.]. Majalah Farmasi Indonesia. 16 (1), 51- 57.
Ito H, Nishitani E, Konoshima T, Takasaki M, Kozuka M, Yoshida T. 2000. Flavonoid and benzophenone glycosides from Coleogyne ramosiisima. Phytochem. 54. h. 695-700.
Li, J. & T. Nohara (2000). Benzophenone C-glucosides from Polygala telephioides, chem.. Pharm. Bull. 48 (9), h. 1354-1355.
30
Markham K.R, 1988. Cara Mengidentifikasi Flavonoid. K. Padmawinata Penerjemah; Bandung ITB. Terjemahan dari : Techniques of Flavonoid Identification.
Matsumoto K, Akao Y, Kobayashi E, Ito T, Ohguchi K, Iinuma M, dan Nozawa Y. 2003. Cytotoxic benzophenone derivates from Garcinia sp. Display a strong apoptosis inducing effect against human leukemia cell line. Biol. Pharm. Bull. April;26(4):569-71
Meyer BN, Feerigni NR, Putnam JE, Jacobson LB, Nicholas DE, Mclaughlin JL. 1982. Brine Shrimp: a comvenient general bioassay for active plant constituents. Planta Medica 45: 31-34
Nawawi A. 2004, Isolasi benzofenon dari daun mahkota dewa [Phaleria macrocarpa (scheff). Boerl.], Acta Pharmaceutika Indonesia.
Nedialkov P, Kitanov G. 2001. Two benzophenone O-arabinosides and a chromone from Hypericum annalatum. Phytochemistry 59 (2002) 867-871
Oshimi S, Zaima K, Matsuno Y, Hirasawa Y, Iizuka T, Studiawan H, Indrayanto G, Zaini NC, Morita H. 2008. Studies on the constituens from the fruits of Phaleria macrocarpa. J Nat Med 62: 207-210.
Simanjuntak P. 2008 Identifikasi senyawa kimia dalam buah Mahkota Dewa
(Phaleria macrocarpa) Thymelaceae. Jurnal Ilmu Kefarmasian Indonesia Vol. 6 No.1 Hal 23-28 ISSN 1693-1841.
Sinambela JM. 2003. Standarisasi sediaan obat herba, Prosiding Seminar dan Pameran Nasional Tumbuhan Obat Indonesia ke XXIII, 25-26 Maret, Jakarta: Fakultas Farmasi, Universitas Pancasila
Sugiwati S. 2005. Aktivitas Antihiperglikemik dari Ekstrak Buah Mahkota Dewa [Phaleria macrocarpa (scheff). Boerl.] Sebagai Inhibitor α-Glukosidase
In vitro an In vivo pada Tikus Putih [Tesis]. Bogor. Program Pascasarjana Institut Pertanian Bogor.
Tambunan RM dan Simanjuntak P. 2006. Penentuan struktur kimia antioksidan benzofenon glikosida dari ekstrak n-butanol buah Mahkota Dewa [Phaleria macrocarpa (Sceff) Boerl.] Majalah Farmasi Indonesia, 17(4), 184-189, 2006.
William R.B, Hoch J, Glass T.E, Evans R, Miller J.S, Wisse J.H, Kingston D.G, 2003. A novel cytotoxic guttiferone analogue from Garcinia macrophylla
31
Winarno H, Katrin E. 2009. Benzophenone Glucoside isolated from the ethyl Acetate extract of the bark of Mahkota Dewa [Phaleria macrocarpa
(Sceff) Boerl.] and its inhibitory activity on Leukemia L1210 cell line.
32
34
Lampiran 1 Bagan alir penelitian
Direfluks dengan metanol (suhu 60oC) sebanyak 3 kali, disaring
35
Lampiran 2 Hasil pencarian eluen terbaik dengan penggabungan 2 eluen (etil asetat:metanol) dengan berbagai perbandingan
Keterangan: eluen etil asetat:metanol
Jenis eluen Perbandingan Jumlah spot
Nilai Rf
Etil asetat : metanol 9:1 4 0.25,0.37,0.47.0.87 Etil asetat : metanol 8:2 4 0.13,0.23,0.52,0.75 Etil asetat : metanol 7:3 4 0.23,0.57,0.75,0.87
Etil asetat : metanol 6:4 2 0.25,0.75
Etil asetat : metanol 5:5 5 0.13,0.23,0.35,0.520.75 Etil asetat : metanol 6:4 4 0.13,0.37,0.57,0.83 Etil asetat : metanol 3:7 4 0.23,0.52,0.75,0.87
Etil asetat : metanol 2:8 2 0.58,0.75
36
Lampiran 3 Pengelompokan fraksi hasil kromatografi kolom dengan eluen n-heksana:kloroform:metanol (7:14:3)
Fraksi hasil kolom Jumlah spot Nilai Rf
37
Lampiran 4 Contoh Perhitungan LC50 fraksi 4 hasil kolom
Konsentrasi ( gmL-1) % kematian larva udang
1000 93.3 100 63.3
10 36.7
Kurva persamaan garis antara konsentrasi fraksi hasil kolom ( gmL-1) sebagai sumbu X dan % kematian larva udang sebagai sumbu Y sebagai berikut:
Diperoleh persamaan garis sebagai berikut :
38
Lampiran 5 Nilai Rf fraksi hasil KLTP dengan eluen kloroform:metanol:air (70:20:2)
Fraksi hasil KLTP Nilai Rf
41
42
43
44
45
46
47
48
0.08 0.087,0.14 0.08,0.14,0.24
0.37,0.45 0.37,0.55 0.61,0.66 0.65,0.75,0.8
ABSTRACT
YENTI HARIYANI. Isolation of Benzophenone Group from the Methanolic Extract of Mahkota Dewa [Phaleria macrocarpa (Scheff.) Boerl. Pulp. Under direction of LATIFAH K. DARUSMAN and IRMANIDA BATUBARA
Traditionally, mahkota dewa plant [Phaleria macrocarpa (Scheff.) Boerl.] is used to treat various diseases in Indonesia, including cancer. In developing the mahkota dewa plant as material for cancer therapy, it requires for quality control that responsible for its activity. Quality control can be determined through marker compound. This study aimed to isolate marker compound benzophenone compound, from the methanol extract of mahkota dewa pulp. Isolation was done using column chromatography and preparative thin layer chromatography (TLC) guided by BSLT activity and benzophenone coloring reagent. Mahkota dewa pulp methanol extract was fractionated with silica gel. The fraction 4 column chromatography resulted had a LC50 value of 30.90 µg/ml. Based on TLC on fraction 4, fraction 4 consisted of benzophenone on Rf 0.37. Separation of fraction 4 using preparative TLC with eluent chloroform-methanol-water (70:20:2) yielded eight fractions. The benzophenone compound could be detected at fraction 45 with the Rf of value 0.37 and gave the LC50 value 899.28 µg/ml. Identification of fraction 45 by UV-Vis spectrometer showed UV absorption at 200 nm and 264 nm. IR spectra indicated that the fraction 45 has an aromatic compound and have the same pattern with phalerin.
1
PENDAHULUAN
Latar BelakangTanaman mahkota dewa (Phaleria macrocarpa) secara luas di Indonesia telah digunakan sebagai obat alternatif kanker. Secara empirik, mahkota dewa digunakan untuk pengobatan medis. Batangnya digunakan untuk pengobatan kanker tulang, daunnya digunakan untuk pengobatan impotensi, alergi, diabetes mellitus, dan tumor. Cangkang biji buah mahkota dewa digunakan untuk penyakit kanker payudara, kanker rahim, penyakit paru-paru, dan penyakit hati (Aditama 2001).
Dari hasil evaluasi fitokimia, simplisia buah mahkota dewa mengandung alkaloid, flavonoid, fenol/polifenol, tanin, saponin, terpenoid/sterol (Lisdawati 2002). Hasil identifikasi senyawa kimia dari buah mahkota dewa diperoleh kandungan asam lemak, steroid, benzofenon glikosida dan karbohidrat (Simanjuntak 2008). Hartati et al. (2005) melaporkan suatu senyawa glikosida benzofenon baru (phalerin) dari daun mahkota dewa yang bersifat sitotoksik terhadap sel myeloma (NS-1) dan uji aktivitas biologi pada phalerin menunjukkan bahwa senyawa ini bersifat non-toksik dan memiliki potensi imunostimulan. Penelitian yang dilakukan oleh Oshimi et al. (2008) pada buah mahkota dewa dilaporkan senyawa turunan glikosida benzofenon yang berbeda dari phalerin yaitu 2,4’,6-trihidroksi-4-metoksibenzofenon-2-O-β-D-glukosida yang sebelumnya telah diisolasi dari tanaman Gnidia involucrate yang juga termasuk genus Thymelaeaceae. Senyawa ini juga telah diisolasi oleh Tambunan dan Simanjuntak (2006) dari ekstrak n-butanol buah mahkota dewa yang dihidrolisis dengan HCl 9% dalam metanol.
Di dalam pengembangan mahkota dewa sebagai obat berbagai jenis penyakit terutama kanker diperlukan kontrol kualitas yang bertanggung jawab terhadap aktivitasnya sebagai antikanker. Kontrol kualitas dapat ditentukan antara lain melalui senyawa penciri.
2
ditemukan untuk mendapatkan suatu senyawa metabolit sekunder dari tumbuhan obat diperoleh rendemen dan kemurnian relatif kecil dan sulit untuk dijadikan standar karena kurang tepatnya pelarut atau eluen, teknik ekstraksi dan teknik pemisahan yang digunakan.
Tujuan Penelitian
Penelitian ini bertujuan untuk memperoleh senyawa penciri golongan benzofenon dari ekstrak metanol buah mahkota dewa melalui pemisahan, uji
Brine Shrimp Lethality Test (BSLT) dan uji kualitatif benzofenon.
Manfaat Penelitian
TINJAUAN PUSTAKA
Mahkota Dewa
Phaleria macrocarpa (Scheff.) Boerl atau yang dikenal dengan nama mahkota dewa merupakan tanaman asli Indonesia yang berasal dari Papua. Umumnya tanaman ini dibudidayakan sebagai tanaman hias atau tanaman peneduh, tetapi terkadang masih dapat dijumpai tumbuh liar di hutan pada ketinggian 10-1.200 m di atas permukaan laut dengan curah hujan rata-rata 1.000-2.500 mm/tahun. Dari segi taksonomi tanaman ini dikelompokkan ke dalam divisi Spermathophyta, filum Angiospermae, kelas Dycotyledoneae, ordo Tymelaeales, famili Tymelaeaceae, genus Phaleria dan spesies Phaleria macrocarpa (Scheff.) Boerl.
4
Gambar 1. Buah muda (hijau) dan buah tua (merah) mahkota dewa
Phaleria macrocarpa (Scheff.) Boerl, yang dikenal dengan nama mahkota dewa telah cukup lama dimanfaatkan oleh masyarakat Indonesia untuk mengobati berbagai penyakit, seperti diabetes melitus, kanker, hati, jantung, asam urat, rematik, ginjal, tekanan darah tinggi, eksim, jerawat, dan luka gigitan serangga (Lisdawati 2002). Penelitian yang dilakukan oleh Sugiwati (2005) diperoleh bahwa ekstrak kasar buah mahkota dewa pada fraksi etil asetat, butanol dan air berhasil menghambat aktivitas α-glukosidase secara in vitro berturut-turut sebesar 69.90 %, 42.27 %, dan 33.01 %.
Penapisan farmakologi untuk aktivitas antikanker secara in vitro dari ekstrak kasar fraksi non polar, semipolar dan polar daging buah serta cangkang biji mahkota dewa telah diujikan terhadap sel leukemia L1210. Fraksi semipolar (etil asetat) merupakan fraksi yang memiliki aktivitas inhibisi paling tinggi terhadap perkembangbiakan sel leukemia L1210 dengan nilai IC50 5.76 µg/ml
5
Glikosida benzofenon
Glikosida benzofenon merupakan senyawa turunan benzofenon yang satu atau lebih gugus hidroksilnya terikat pada satu gula atau lebih. Beberapa senyawa glikosida benzofenon yang terdapat dalam tanaman mahkota dewa ditunjukkan dalam Tabel 1.
Tabel 1 Senyawa glikosida benzofenon dari Phaleria macrocarpa
Bagian tumbuhan Nama Senyawa glikosida benzofenon Peneliti
Daun
4,5-dihidroksi-4-metoksibenzofenon-Kulit kayu 6,4’-dihidroksi-4-metoksi benzofenon-2-O-β
6
Gambar 2. Beberapa struktur kimia senyawa benzofenon glikosida. Hasil isolasi dari daun Mahkota dewa (1); isolasi dari Polygala telephioides (2,3); isolasi dari herbal Coleogyne ramosissima (4); hasil isolasi buah Mahkota dewa (5) (Tambunan 2006)
Aktivitas Senyawa Turunan Benzofenon
Semua turunan benzofenon yang diisolasi dari spesies Garcinia menunjukkan apoptosis kuat menginduksi efek melawan sel leukemia pada manusia. Senyawa ini berperan dalam menekan pertumbuhan berkaitan dengan apoptosis yang dimediasi oleh aktivasi Caspase-3 dan sitotoksik terhadap sel ovarian manusia (A2780) (Matsumoto et al. 2003; William et al. 2003).
Phalerin yang diisolasi dari ekstrak metanol daun mahkota dewa dilaporkan memiliki sifat sitotoksik terhadap sel myeloma (NS-1) dengan nilai IC50 83 µg/mL (Hartati 2005). Winarno dan Katrin (2009) berhasil mengisolasi
turunan glikosida benzofenon dari kulit batang mahkota dewa yang mempunyai aktivitas inhibitor terhadap tikus penderita leukimia L1210 dengan IC50 5.1
7
Uji Toksisitas Brine Shrimp Lethality Test (BSLT)
Uji toksisitas BSLT merupakan deteksi awal untuk mengetahui potensi bioaktivitas dan toksisitas dari sampel sehingga dapat ditentukan konsentrasi ekstrak yang aman untuk pengujian. Uji dilakukan untuk mengamati tingkat kematian larva udang Artemia salina Leach yang disebabkan oleh ekstrak metabolit sekunder, tingkat kematian atau mortalitas selanjutnya dianalisis dengan menggunakan analisis probit untuk menentukan konsentrasi LC50 (lethal
concentration) 50%, yaitu konsentrasi yang menyebabkan kematian populasi larva udang sebesar 50% dari populasi total. Senyawa yang mempunyai LC50
lebih kecil dari 1000 ppm dikatakan memiliki potensi bioaktivitas (Meyer et al.
1982).
Lisdawati (2002) telah melakukan pengujian BSLT terhadap kadar toksisitas ekstrak daging buah mahkota dewa dan kulit bijinya dengan melihat tingkat kematian larva A. Salina setelah diinkubasi selama 24 jam. Hasilnya menunjukkan toksisitas yang sangat tinggi yang menyebabkan kematian 50% larva udang (LC50) yang berkisar antara 0.1615-11.8351 µg/ml.
9
METODE PENELITIAN
Alat dan Bahan
Alat-alat yang digunakan adalah Spektrofotometer UV-Vis (Shimadzu), dan IR (Brucker), multiwell plates, evaporator, pelat KLT silika gel GF254 dan
pelat KLT preparatif, kolom kromatografi silika gel (Merck; 70-230 mesh; 1x25 cm), pipet mikro, tip pipet mikro, pipet Mohr.
Bahan yang digunakan adalah buah mahkota dewa yang diperoleh dari kebun percobaan Pusat Studi Biofarmaka (PSB), pelarut MeOH, CHCl3, EtOAc, Artemia salina Leach, dan air laut.
Preparasi dan Ekstraksi Sampel (Hartati et al. 2005)
Preparasi sampel ekstrak buah mahkota dewa dilakukan dengan cara mengeringanginkan daging buah mahkota dewa yang telah diiris tipis, kemudian dibuat serbuk berukuran 80 mesh. Sampel serbuk kering ditentukan kadar airnya. Sampel diekstraksi dengan cara refluks menggunakan pelarut metanol pada suhu 600C. Semua ekstrak yang diperoleh disaring dengan menggunakan kertas saring Whatman no. 1 dan dipekatkan dengan penguap putar pada suhu 300C kemudian dihitung rendemennya. Selanjutnya ekstrak metanol dipartisi menggunakan kloroform untuk memisahkan komponen yang bersifat semipolar, masing-masing ekstrak diuji flavonoid, fenol, dan triterpenoid dan steroid.
Penentuan Kadar Air (AOAC 2006)
Cawan dikeringkan terlebih dahulu selama 30 menit dalam oven pada suhu 1050C, lalu didinginkan dalam eksikator kemudian beratnya ditimbang. Sampel ditimbang seberat 5 gram dan dimasukkan ke dalam cawan, kemudian sampel dimasukkan kedalam oven selama 3 jam pada suhu 1050C, lalu didinginkan dalam eksikator selama 30 menit kemudian ditimbang kembali sampai diperoleh bobot yang konstan (AOAC 2006).Persen kadar air dihitung dengan persamaan:
Kadar air (%) : a-b x 100 %
a
a adalah bobot sebelum dikeringkan (g)
10
Uji Fitokimia (Harborne 1987)
Uji Flavonoid. Sebanyak 1 gram ekstrak ditambah 100 ml air panas kemudian dididihkan selama 5 menit dan disaring. Filtrat yang diperoleh diambil sebanyak 5 ml ditambah 0,05 g serbuk magnesium, 1 ml HCl pekat dan 1 ml amil alkohol kemudian dikocok kuat-kuat, terbentuknya warna merah, kuning dan jingga pada lapisan amil akohol menunjukkan adanya flavonoid.
Uji Triterpenoid dan Steroid. Ekstrak mahkota dewa dilarutkan dalam 25 ml etanol panas (500C) kemudian disaring dalam cawan porselin dan diuapkan sampai kering. Residu ditambahkan eter dan ekstrak eter dipindahkan ke dalam lempeng, lalu ditambahkan 3 tetes anhidrida asam asetat dan 1 tetes H2SO4 pekat
(uji Lieberman-Burchard), warna merah atau ungu menunjukkan adanya triterpenoid dan warna hijau atau biru menunjukkan adanya steroid.
Uji Fenol. Ekstrak mahkota dewa dengan bobot tertentu dimasukkan ke dalam tabung reaksi. Kemudian ditambahkan FeCl3 dan bila terbentuk warna ungu, biru
atau hijau menunjukkan adanya senyawa golongan fenol.
Penentuan Eluen Terbaik pada KLT
Ekstrak pekat dari sampel ditotolkan pada pelat KLT. Setelah kering langsung dielusi dalam ruang elusi yang telah dijenuhkan oleh uap eluen pengembang. Eluen yang digunakan adalah metanol, etil asetat, kloroform, aseton butanol, diklorometana,dan n-heksana, lalu dilakukan perbandingan pada eluen yang menghasilkan spot yang banyak dan terpisah. Eluen akan diperbaiki lebih lanjut apabila pemisahan belum baik. Noda hasil elusi diamati di bawah lampu UV pada panjang gelombang 254 dan 366 nm.
Fraksinasi dengan Kromatografi Kolom (Rouessac & Rouessac 2007)
Fraksinasi dilakukan menggunakan kromatografi kolom dengan fase diam berupa silika gel Merck dengan ukuran 70-230 mesh dan fase gerak berupa n-heksana, etil asetat, metanol dengan peningkatan kepolaran. Eluat ditampung setiap 5 ml dalam tabung reaksi, kemudian eluat diuji dengan KLT. Eluat yang memiliki jumlah bercak dan nilai Rf yang sama atau hampir sama digabung
11
Fraksi-fraksi hasil kolom yang diduga mengandung senyawa golongan benzofenon diuji toksisitas melalui uji BSLT. Selanjutnya fraksi yang paling toksik difraksinasi dengan KLT preparatif, noda yang diperoleh kemudian dideteksi di bawah lampu UV 254 nm dan 366 nm. Fraksi hasil KLT preparatif diuji BSLT dan uji kualitatif senyawa golongan benzofenon, fraksi yang paling toksik dan positif mengandung benzofenon diidentifikasi menggunakan spektrofotometer UV-Vis dan IR. Diagram alir penelitian dapat dilihat pada Lampiran 1.
Uji Toksisitas Brine Shrimp Lethality Test (BSLT) (Meyer et al. 1982)
Uji toksisitas dilakukan dengan menentukan nilai Lethal Concentration
(LC50) menngunakan larva udang Artemia salina L. Telur udang ditetaskan dalam
gelas piala yang berisi air laut, penetasan dilakukan selama 48 jam dan diaerasi agar kadar oksigen tercukupi sehingga telur udang menetas menjadi larva. Ke dalam masing-masing sumur dimasukkan 10 ekor larva udang dan larutan fraksi yang akan diuji dengan konsentrasi 10 sampai 1.000 ppm (masing-masing 3 kali ulangan), diinkubasi selama 24 jam dan dihitung jumlah larva yang mati. LC50
ditentukan dengan membuat kurva hubungan antara % kematian larva dan log konsentrasi ekstrak. Apabila pada kontrol ada larva yang mati maka % kematian larva udang ditentukan dengan rumus Abbot.
% kematian larva : T – K x 100 % S
Keterangan : T : jumlah larva uji yang mati K : jumlah larva kontrol yang mati S : jumlah larva uji
Uji Kualitatif Golongan Benzofenon (Nedialkov P & Kitanov G 2001)
Untuk mendeteksi adanya senyawa benzofenon dalam suatu sampel dapat dilakukan dengan cara menyemprotkan reagen Fast Blue Salt B dalam MeOH:H2O (1:1). Bila terjadi perubahan warna spot pada plat KLT menjadi ungu
12
Identifikasi Senyawa Benzofenon dengan Spektrofotometer UV-Vis
Identifikasi dengan spektrofotometer UV-Vis dilakukan dengan mengukur spektrum serapan dalam larutan blanko yang sangat encer dengan pembanding blanko pelarut, pelarut yang digunakan dalam pengukuran adalah pelarut sampel yaitu metanol (Harborne, 1987). Senyawa dalam sampel diukur pada panjang gelombang 200-800 nm. Analisis dilakukan dengan metode baku di Laboratorium Pusat Studi Biofarmaka, IPB.
Identifikasi Senyawa Benzofenon dengan Spektrofotometer IR
13
HASIL DAN PEMBAHASAN
Ekstraksi dan Fraksinasi
Sampel buah mahkota dewa yang digunakan pada penelitian ini diperoleh dari kebun percobaan Pusat Studi Biofarmaka, Institut Pertanian Bogor dalam bentuk simplisia yang kemudian dijadikan serbuk dengan ukuran 80 mesh. Kadar air serbuk mahkota dewa yang diperoleh sebesar 2.12%. Kadar air yang diperoleh kurang dari 10% merupakan kadar air yang baik karena pada tingkat kadar air tersebut waktu simpan sampel akan relatif lebih lama dan terhindar dari pencemaran yang disebabkan oleh mikroba dan memenuhi syarat sebagai bahan baku herbal (Winarno 1992; BPOM 2004).
Ekstraksi serbuk buah mahkota dewa sebanyak 200 g dilakukan dengan cara refluks menggunakan pelarut metanol, disaring dan diuapkan dengan rotary evaporator pada suhu 30oC. Ekstrak pekat yang diperoleh sebanyak 39.0776 g dengan rendemen 20.85%. Selanjutnya ekstrak metanol yang diperoleh dipartisi menggunakan kloroform. Hasil partisi dengan kloroform diperoleh fraksi metanol dengan rendemen 72.25% dan fraksi kloroform 24.98% dari ekstrak kasar metanol.
Untuk mengetahui kandungan kimia dari fraksi metanol dan fraksi kloroform dilakukan uji fitokimia antara lain uji flavonoid, triterpenoid, steroid dan uji fenol. Hasil pengujian fitokimia fraksi metanol dan fraksi kloroformbuah mahkota dewa dapat dilihat pada Tabel 2.
Tabel 2 Hasil uji fitokimia fraksi metanol dan fraksi kloroform buah mahkota dewa
Golongan Senyawa Fraksi Metanol Fraksi Kloroform
14
Hasil uji fitokimia pada Tabel 2 menunjukkan bahwa pada fraksi metanol golongan triterpenoid memperlihatkan warna ungu yang tidak terlalu kuat, sedangkan pada fraksi kloroform warna ungu terlihat pekat sehingga diduga triterpenoid terpisahkan pada partisi dengan kloroform. Sementara itu steroid pada kedua fraksi baik fraksi metanol maupun kloroform menunjukkan intensitas warna hijau yang kuat, yang menunjukkan keberadaan golongan steroid. Flavonoid pada fraksi metanol lebih kuat intensitas warnanya dibanding pada fraksi kloroform, hal itu terlihat dari warna merah yang kuat pada lapisan amil alkohol dari fraksi metanol.
Pada uji fenol, fraksi metanol menunjukkan intensitas warna hijau yang lebih kuat dibanding fraksi kloroform. Oleh karena itu pada penelitian ini tujuan utamanya adalah untuk memperoleh golongan benzofenon yang merupakan bagian dari fenol, maka fraksinasi selanjutnya dilakukan pada fraksi metanol.
Pencarian eluen terbaik untuk penggabungan fraksi hasil kromatografi kolom menggunakan pelat kromatografi lapis tipis (KLT), fraksi yang memiliki nilai Rf yang sama atau hampir sama akan digabung. Pencarian eluen dimulai dari
15
Gambar 3 Pola KLT eluen terbaik eluen n-heksana:etil asetat: metanol (7:14:3)
Fraksinasi dilakukan untuk memurnikan fraksi metanol sehingga diperoleh senyawa golongan benzofenon yang bersifat sitotoksik melalui uji toksisitas Brine Shrimp Lethality Test (BSLT). Fraksinasi dilakukan menggunakan kromatografi kolom dengan fase diam silika gel dengan metode step gradient (peningkatan kepolaran) dimulai dari eluen n-heksana, etil asetat, dan metanol. Tujuan peningkatan polaritas sistem eluen agar semua komponen yang terlarut dalam fraksi metanol akan terbawa lebih cepat dan pemisahan dapat berlangsung dengan baik.
Fraksinasi yang dilakukan terhadap fraksi metanol menghasilkan 167 tabung yang digabung berdasarkan pola KLT dengan eluen campuran n-heksana:etil asetat:metanol (7:14:3) sehingga diperoleh 12 fraksi (fraksi 1-12) seperti yang ditunjukkan pada Gambar 4. Harga Rf dan jumlah spot