ISOLASI SENYAWA FLAVONOIDA DARI BUAH MAHKOTA DEWA (Phaleria macrocarpa Boerl.)
SKRIPSI
ALBINUR P. S 050802058
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGENTAHUAN ALAM UNIVERSITAS SUMATERA UTARA
ISOLASI SENYAWA FLAVONOIDA DARI BUAH MAHKOTA DEWA
(Phaleria Macrocarpa Boerl.)
SKRIPSI
Diajukan untuk melengkapi tugas dan memenuhi syarat mencapai gelar Sarjana Sains
ALBINUR P. S 050802058
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS SUMATERA UTARA
PERSETUJUAN
JUDUL : ISOLASI SENYAWA FLAVONOIDA
DARI BUAH MAHKOTA DEWA (Phaleria macrocarpa Boerl.)
Kategori : SKRIPSI
Nama Mahasiswa : Albinur P. S
Nomor Induk Mahasiswa : 050802058
Program Studi : SARJANA (S1) KIMIA
Departemen : KIMIA
Fakultas : MATEMATIKA DAN ILMU
PENGETAHUAN ALAM (FMIPA) UNIVERSITAS SUMATERA UTARA
Disetujui di
Medan, Mei 2011
Komisi Pembimbing :
Pembimbing 2 Pembimbing 1
Drs.Philipus H. Siregar, MSi Lamek Marpaung, M.Phil, Ph.D NIP: 1958 0504 1986 011002 NIP: 1952 0828 1982 031001
Diketahui oleh
Departemen Kimia FMIPA USU Ketua,
PERNYATAAN
ISOLASI SENYAWA FLAVONOIDA DARI BUAH MAHKOTA DEWA (Phaleria macrocarpa Boerl.)
SKRIPSI
Saya mengakui bahwa skripsi ini adalah hasil kerja Saya sendiri, kecuali beberapa kutipan dan ringkasan yang masing-masing disebutkan sumbernya.
Medan, Mei 2011
ABSTRAK
ISOLATION OF FLAVONOID COMPOUNDS FROM MAHKOTA DEWA FRUITS (Phaleria macrocarpa Boerl.)
ABSTRACT
DAFTAR ISI
Daftar lampiran ix
Daftar tabel x
Bab 1 Pendahuluan
1.1Latar belakang 1
1.2Permasalahan 2
1.3Tujuan Penelitian 3
1.4Manfaat Penelitian 3
1.5Lokasi Penelitian 3
1.6Metode Penelitian 3
Bab 2 Tinjauan Pustaka 5
2.1 Tumbuhan Mahkota Dewa 5
2.1.1 Morfologi Tumbuhan Mahkota Dewa 5
2.1.2 Sistematika Tumbuhan Mahkota Dewa 5
2.1.3 Kandungan Tumbuhan Mahkota Dewa 6
2.1.4 Manfaat Tumbuhan Mahkota Dewa 6
2.2 Senyawa Flavonoida 7
2.2.1 Struktur Dasar Senyawa Flavonoida 7
2.2.2 Klasifikasi Senyawa Flavonoida 8
2.2.3 Metode Isolasi Senyawa Flavonoida 14
2.2.4 Sifat Kelarutan Flavonoida 14
2.3 Teknik Pemisahan 15
2.3.1 Kromatografi 15
2.3.1.1 Kromatografi Lapis Tipis 16
2.3.1.2 Kromatografi Kolom 17
2.3.1.3 Harga Rf (Reterdation Factor) 17
2.3.2 Kristalisasi 18
2.3.3 Ekstraksi 18
2.4 Teknik Spektroskopi 19
2.4.1 Spektrofotometer Ultraviolet (UV-Visible) 19
2.4.2 Spektrofotometer Infra Merah (FT-IR) 20
Bab 3 Metodologi Penelitian
3.1 Alat-alat 22
3.2 Bahan 23
3.3 Prosedur Penelitian 23
3.3.1 Penyediaan Sampel 23
3.3.2.1 Uji Busa 24
3.3.2.2 Skrining Fitokimia 24
3.3.2.3Kromatografi Lapis Tipis 25
3.3.3Prosedur Untuk Memperoleh Senyawa Kimia dari Ekstrak Buah
Mahkota Dewa 25
3.3.4Isolasi Senyawa Flavonoida dengan Kromatografi Kolom 26
3.3.5Pemurnian 26
3.3.6Uji Kemurnian Hasil Isolasi dengan Kromatografi Lapis Tipis 26 3.3.7Analisis Spektroskopi Senyawa Hasil Isolasi 27
3.3.7.1 Pengukuran Titik Lebur 27
3.3.7.2 Analisis Senyawa Hasil Isolasi dengan Spektrofotometer
Ultraviolet (UV-Visible) 27
3.3.7.3 Analisis Senyawa Hasil Isolasi dengan Spektrofotometer
Infra Merah (FT-IR) 28
3.3.7.4 Analisis Senyawa Hasil Isolasi dengan Spektrofotometer
Resonansi Magnetik Inti (1H-NMR) 28
3.4 Bagan Skrining Fitokimia 29
3.4.1 Bagan Penelitian 30
Bab 4 Hasil dan Pembahasan
4.1 Hasil Penelitian 31
4.2 Pembahasan 33
Bab 5 Kesimpulan dan Saran
5.1 Kesimpulan 36
5.2 Saran 36
DAFTAR LAMPIRAN
Halaman
Lampiran A. Gambar Buah Mahkota Dewa 40
Lampiran B. Hasil Determinasi Buah Mahkota Dewa 41
Lampiran C. Kromatografi Lapis Tipis Ekstrak Klorofom Buah Mahkota Dewa dengan Penampakan Noda dibawah Sinar Ultraviolet dengan
λ= 254 nm 42
Lampiran D. Kromatografi Lapis Tipis Senyawa Hasil Isolasi Melalui Penampakan
Noda dengan Penambahan Pereaksi 43
DAFTAR TABEL
Halaman
Tabel 1. Golongan - golongan Flavonoida menurut Harbone 13 Tabel 2. Rentang Serapan Spektrum UV-Visible Golongan Flavonoida 21 Tabel 3. Gugus Fungsi dan Pita Serapan Hasil analisis FT-IR senyawa
ABSTRAK
ISOLATION OF FLAVONOID COMPOUNDS FROM MAHKOTA DEWA FRUITS (Phaleria macrocarpa Boerl.)
ABSTRACT
BAB 1
PENDAHULUAN
1.1 Latar Belakang
Flavonoid merupakan kandungan khas tumbuhan hijau dengan mengecualikan
alga dan hornwort, Flavonoid sebenarnya terdapat pada semua bagian tumbuhan
termasuk daun, akar, kayu, kulit, tepung sari, nectar, bunga, buah buni, dan biji.
Hanya sedikit saja catatan yang melaporkan adanya flavonoid pada hewan, misalnya
dalam kelenjar bau berang-berang, ‘propolis’ (sekresi lebah), dan di dalam sayap
kupu-kupu; itu pun dengan anggapan bahwa flavonoid tersebut berasal dari tumbuhan
yang menjadi makanan hewan tersebut dan tidak disimbiosis di dalam tubuh mereka.
Indonesia juga diketahui memiliki kekayaan keanekaragaman hayati terbesar
di dunia dengan lebih kurang 30.000 jenis tumbuh-tumbuhan berikut biota lautnya.
Dari sekian besar jumlah tersebut baru sekitar 940 species yang diketahui berkhasiat
terapautik (mengobati) melalui penelitian ilmiah dan hanya sekitar 180 spesies
diantaranya yang dimanfaatkan dalam temuan obat tradisional oleh industri obat
tradisional Indonesia. (Arif, Hariana, 2004).
Hal ini disebabkan karena pemanfaatan tumbuhan di Indonesia untuk
mengobati suatu penyakit biasanya hanya berdasarkan pengalaman empiris yang
diwariskan secara turun-menurun tanpa disertai data penunjang yang memenuhi
persyaratan. (Harmanto, 2001).
Bertitik tolak dari sumber bahan alam hayati ini, yang mempunyai peranan
penting didalam penyediaan senyawa-senyawa kimia dalam bidang obat-obatan maka
pemerintah menghimbau para ahli untuk meningkatkan penelitiannya dalam bidang
tersebut, hal ini merupakan suatu tantangan bagi para ahli untuk melibatkan diri
dalam penelitian senyawa-senyawa baru yang dihasilkan dari tumbuh-tumbuhan
Salah satu tumbuhan yang digunakan sebagai tumbuhan obat adalah tumbuhan
mahkota dewa (P. macrocarpa Boerl.). Tanaman ini merupakan salah satu tanaman
tradisional Indonesia yang masih belum memiliki acuan informasi yang lengkap, baik
dari segi fitokimia maupun dari segi farmakologi guna dapat dimanfaatkan secara
optimal sebagai salah satu bentuk pengobatan alternatif. (Harmanto, 2001). Mahkota
dewa mengandung antihistamin alkaloida, sebab daun maupun buahnya agak pahit, mengandung senyawa triterpen, saponin dan polifenol (lignan). Kulit buahnya juga
mengandung alkaloida, triterpen, saponin dan flavonoida. (Gotama, dkk, 1999).
Tumbuhan mahkota dewa (P. macrocarpa Boerl.) tumbuh tegak dengan tinggi
1-2,5 m, tanaman ini bisa ditemukan ditanam di pekarangan sebagai tanaman hias atau
di kebun-kebun sebagai tanaman peneduh. Bagian tanaman yang digunakan sebagai
obat adalah daun, daging, dan kulit buahnya (Dalimartha, 2004).
Manfaat buah mahkota dewa telah diketahui oleh sebagian masyarakat, tetapi
belum banyak yang mengetahui kegunaan dari daunnya, padahal daun mahkota dewa
dapat dihasilkan sepanjang tahun sedangkan buahnya tidak berbuah sepanjang tahun
dan buahnya dapat digunakan setelah masak atau berwarna merah. Khasiat dari daun
tumbuhan mahkota dewa dapat mengobati penyakit seperti: kanker, tumor, diabetes
(kencing manis), pembengkakan prostad, asam urat, darah tinggi (hypertensi),
reumatik, batu ginjal, hepatitis, dan penyakit jantung. (Harmanto, 2001).
Dari uraian diatas dan berdasarkan literatur mengenai fungsi buah tumbuhan
mahkota dewa sebagai obat tradisional dari berbagai penyakit maka penulis merasa
tertarik untuk mengisolasi senyawa flavonoida dari buah tumbuhan mahkota dewa.
1.2Permasalahan
Permasalahan dalam penelitan ini adalah bagaimana cara mengisolasi senyawa
1.3Tujuan penelitian
Tujuan dari penelitian ini adalah untuk mengisolasi senyawa flavonoida dari daging
buah mahkota dewa (P. macrocarpa Boerl.).
1.4Manfaat penelitian
Hasil dari penelitian ini diharapkan dapat memberikan informasi ilmiah dalam bidang
kimia bahan alam hayati dan farmasi dalam upaya pemanfaatan senyawa flavonoida
dari daging buah mahkota dewa ( P. macrocarpa Boerl.)
1.5Lokasi penelitian
Buah mahkota dewa diperoleh dari daerah Perumnas Simalingkar Medan, Sumatera
Utara. Penelitian dilakukan di laboratorium Kimia Organik Bahan Alam FMIPA USU.
Analis Spektrofotometer UV-Visible, Spektrofotometer Infra Merah (FT-IR), dan
Spektrofotometer Resonansi Magnetik Inti Proton (1H-NMR), dilakukan di Pusat
Penelitian Kimia LIPI, Serpong-Tangerang.
1.6 Metode Penelitian
Dalam penelitian ini, isolasi senyawa flavonoida dilakukan terhadap daging buah
mahkota dewa berupa serbuk halus yang kering sebanyak 1170 g. Tahap awal dilakukan uji skrining fitokimia untuk senyawa flavonoida, yaitu dengan
menggunakan pereaksi FeCl3 1%, NaOH 10%, Mg-HCl dan H2SO4(p).
Tahap isolasi yang dilakukan :
- Ekstraksi Maserasi
- Ekstraksi Partisi
- Analisis Kromatografi Lapis Tipis
- Rekristalisasi
- Analisis Kristal Hasil Isolasi
Analisis kristal mencakup Kromatografi Lapis Tipis, Pengukuran titik lebur
dan identifikasi dengan menggunakan Spektrofotometer UV-Visible,
Spektrofotometer Infra Merah (FT-IR), dan Spektrofotometer Resonansi Magnetik Inti
BAB 2
TINJAUAN PUSTAKA
2.1. Tumbuhan Mahkota Dewa
2.1.1 Morfologi Tumbuhan Mahkota Dewa
Tumbuhan Mahkota dewa merupakan tumbuhan yang hidup di daerah tropis, juga bisa
ditemukan di pekarangan rumah sebagai tanaman hias atau di kebun-kebun sebagai
tanaman peneduh. Perdu ini tumbuh tegak dengan tinggi 1-2,5 m. Daun mahkota dewa
dapat dihasilkan sepanjang tahun sedangkan buahnya tidak berbuah sepanjang tahun
dan buah tumbuhan ini dapat digunakan setelah masak atau berwarna merah. Daun
dan buah tumbuhan mahkota dewa merupakan tanaman obat. (Dalimartha, 2004).
2.1.2 Sistematika Tumbuhan Mahkota Dewa
Sistematika tumbuhan mahkota dewa adalah sebagai berikut:
Kingdom : Plantae
Divisi : Spermatophyta
Sub divisi : Dicotyledon
Kelas : Thymelaeales
Famili : Thymelaeaceae
Marga : Phaleria
Spesies : Phaleria macrocarpa
Nama Daerah
Melayu : Simalakama
Jawa : Makuto rojo
Pohon : Tinggi 1 – 2.5 meter.
Daun : Bulat panjang, daun tunggal, bertangkai pendek ,
runcing, pertulangan menyirip dan rata, berwarna
hijau tua, panjang daun 7– 10 cm, lebar daun 2 – 5 cm.
Bunga : Muncul sepanjang tahun, tersebar dibatang atau ketiak
daun, berwarna putih.
Buah : Berbentuk bulat, permukaan licin serta beralur, saat masih muda berwarna hijau dan bila sudah masak
bewarna merah dan daging buah bewarna putih,
berserat dan berair.
Akar : Berjenis tunggang.
(Hartono, H. Soesanti, 2004).
2.1.3 Kandungan Kimia Tumbuhan Mahkota Dewa
Tumbuhan mahkota dewa adalah termasuk dari salah satu famili Thymelaeaceae dan
spesies Phaleria macrocarpa. Dari sumber literatur, mahkota dewa mengandung
antihistamin alkaloida, sebab daun maupun buahnya agak pahit, mengandung senyawa
triterpen, saponin dan polifenol (lignan). Kulit buahnya juga mengandung alkaloida,
triterpen, saponin dan flavonoida. (Gotama, dkk, 1999).
2.1.4 Manfaat Tumbuhan Mahkota Dewa
Sebagian masyarakat telah mengetahui manfaat buah mahkota dewa, tetapi belum
mengetahui kegunaan dari daunnya. Khasiat dari daun tumbuhan mahkota dewa dapat mengobati penyakit seperti: kanker, tumor, diabetes (kencing manis), pembengkakan
prostad, asam urat, darah tinggi (hipertensi), reumatik, batu ginjal, hepatitis, dan
penyakit jantung. (Harmanto, 2001).
Dosis efektif yang aman dan bermanfaat belum diketahui secara tepat. Untuk
obat yang diminum biasanya digunakan beberapa irisan buah kering (tanpa biji).
Selama beberapa hari baru dosis ditingkatkan sedikit demi sedikit, sampai dirasakan
kadang harus lebih besar agar mendapat manfaat perbaikan. Efek samping yang
timbul harus diperhatikan. (Dalimartha, 2004).
2.2 Senyawa Flavonoida
Senyawa-senyawa flavonoida adalah senyawa-senyawa polifenol yang mempunyai 15
atom karbon, terdiri dari dua cincin benzena yang dihubungkan menjadi satu oleh
rantai linier yang terdiri dari tiga atom karbon. Senyawa-senyawa flavonoida adalah
senyawa 1,3 diaril propana, senyawa isoflavonoida adalah senyawa 1,2 diaril propana,
sedangkan senyawa-senyawa neoflavonoida adalah 1,1 diaril propana.
Istilah flavonoida diberikan pada suatu golongan besar senyawa yang berasal
dari kelompok senyawa yang paling umum, yaitu senyawa flavon; suatu jembatan
oksigen terdapat diantara cincin A dalam kedudukan orto, dan atom karbon benzil
yang terletak disebelah cincin B. Senyawa heterosoklik ini, pada tingkat oksidasi yang
berbeda terdapat dalam kebanyakan tumbuhan. Flavon adalah bentuk yang
mempunyai cincin C dengan tingkat oksidasi paling rendah dan dianggap sebagai
struktur induk dalam nomenklatur kelompok senyawa-senyawa ini. (Manitto, 1981)
Senyawa flavonoida sebenarnya terdapat pada semua bagian tumbuhan
termasuk daun, akar, kayu, kulit, tepung sari, bunga, buah, dan biji. Kebanyakan
flavonoida ini berada di dalam tumbuh-tumbuhan, kecuali alga. Namun ada juga
flavonoida yng terdapat pada hewan, misalnya dalam kelenjar bau berang-berang dan
sekresi lebah. Dalam sayap kupu - kupu dengan anggapan bahwa flavonoida berasal
dari tumbuh-tumbuhan yang menjadi makanan hewan tersebut dan tidak dibiosintesis
di dalam tubuh mereka. Penyebaran jenis flavonoida pada golongan tumbuhan yang tersebar yaitu angiospermae, klorofita, fungi, briofita. (Markham, 1988)
2.2.1 Struktur dasar senyawa flavonoida
Senyawa flavonoida adalah senyawa yang mengandung C15 terdiri atas dua inti
fenolat yang dihubungkan dengan tiga satuan karbon. Struktur dasar flavonoida dapat
C C C
A B
Kerangka dasar senyawa flavonoida
Cincin A adalah karakteristik phloroglusinol atau bentuk resorsinol tersubstitusi.
Namun sering terhidroksilasi lebih lanjut :
Cincin B adalah karakteristik 4-, 3,4-, 3,4,5- terhidroksilasi
C3
2.2.2 Klasifikasi Senyawa Flavonoida
Flavonoida mengandung sistem aromatik yang terkonjugasi sehingga menunjukkan
pita serapan kuat pada daerah spektrum sinar ultraviolet dan spektrum sinar tampak,
umumnya dalam tumbuhan terikat pada gula yang disebut dengan glikosida. (Harborne, 1996)
A A A
Pada flavonoida O-glikosida, satu gugus hidroksil flavonoida (atau lebih)
terikat pada satu gula (lebih) dengan ikatan yang tahan asam. Glukosa merupakan gula
yang paling umum terlibat dan gula lain yang sering juga terdapat adalah galaktosa,
ramnosa, silosa, arabinosa, dan rutinosa. Waktu yang diperlukan untuk memutuskan
suatu gula dari suatu flavonoida O-glukosida dengan hidrolisis asam ditentukan oleh
sifat gula tersebut.
Pada flavonoida C-glikosida, gula terikat pada atom karbon flavonoida dan
dalam hal ini gula tersebut terikat langsung pada inti benzena dengan suatu ikatan
karbon-karbon yang tahan asam. Gula yang terikat pada atom C hanya ditemukan
pada atom C nomor 6 dan 8 dalam inti flavonoida, misalnya pada orientin. (Markham,
1988)
Menurut Robinson (1995), flavonoida dapat dikelompokkan berdasarkan
keragaman pada rantai C3 yaitu :
1. Flavonol
Flavonol paling sering terdapat sebagai glikosida, biasanya 3-glikosida, dan aglikon
flavonol yang umum yaitu kamferol, kuersetin, dan mirisetin yang berkhasiat sebagai
antioksidan dan antiimflamasi. Flavonol lain yang terdapat di alam bebas kebanyakan
merupakan variasi struktur sederhana dari flavonol. Larutan flavonol dalam suasana
basa dioksidasi oleh udara tetapi tidak begitu cepat sehingga penggunaan basa pada
pengerjaannya masih dapat dilakukan.
O
OH O
2. Flavon
Flavon berbeda dengan flavonol dimana pada flavon tidak terdapat gugusan
3-hidroksi. Hal ini mempunyai serapan UV-nya, gerakan kromatografi, serta reaksi
warnanya. Flavon terdapat juga sebagai glikosidanya lebih sedikit daripada jenis
glikosida pada flavonol. Flavon yang paling umum dijumpai adalah apigenin dan
luteolin. Luteolin merupakan zat warna yang pertama kali dipakai di Eropa. Jenis yang paling umum adalah 7-glukosida dan terdapat juga flavon yang terikat pada gula
melalui ikatan karbon-karbon. Contohnya luteolin 8-C-glikosida. Flavon dianggap
sebagai induk dalam nomenklatur kelompok senyawa flavonoida.
Isoflavon merupakan isomer flavon, tetapi jumlahnya sangat sedikit dan sebagai
fitoaleksin yaitu senyawa pelindung yang terbentuk dalam tumbuhan sebagai
pertahanan terhadap serangan penyakit. Isoflavon sukar dicirikan karena reaksinya
tidak khas dengan pereaksi warna manapun. Beberapa isoflavon (misalnya daidzein)
memberikan warna biru muda cemerlang dengan sinar UV bila diuapi amonia, tetapi kebanyakan yang lain tampak sebagai bercak lembayung yang pudar dengan amonia
berubah menjadi coklat.
O
O
4. Flavanon
Flavanon terdistribusi luas di alam. Flavanon terdapat di dalam kayu, daun dan bunga.
Flavanon glikosida merupakan konstituen utama dari tanaman genus prenus dan buah
jeruk ; dua glikosida yang paling lazim adalah neringenin dan hesperitin, terdapat
dalam buah anggur dan jeruk.
O
O
Struktur Flavanon
5. Flavanonol
Senyawa ini berkhasiat sebagai antioksidan dan hanya terdapat sedikit sekali jika
dibandingkan dengan flavonoida lain. Sebagian besar senyawa ini diabaikan karena
konsentrasinya rendah dan tidak berwarna.
O
O
OH
Struktur Flavanonol
6. Katekin
Katekin terdapat pada seluruh dunia tumbuhan, terutama pada tumbuhan berkayu.
Senyawa ini mudah diperoleh dalam jumlah besar dari ekstrak kental Uncaria gambir
dan daun teh kering yang mengandung kira-kira 30% senyawa ini. Katekin berkhasiat
7. Leukoantosianidin
Leukoantosianidin merupakan senyawa tan warna, terutama terdapat pada tumbuhan
berkayu. Senyawa ini jarang terdapat sebagai glikosida, contohnya melaksidin,
apiferol.
Antosianin merupakan pewarna yang paling penting dan paling tersebar luas dalam
tumbuhan. Pigmen yang berwarna kuat dan larut dalam air ini adalah penyebab
hampir semua warna merah jambu, merah marak , ungu, dan biru dalam daun, bunga,
dan buah pada tumbuhan tinggi. Secara kimia semua antosianin merupakan turunan
suatu struktur aromatik tunggal yaitu sianidin, dan semuanya terbentuk dari pigmen
sianidin ini dengan penambahan atau pengurangan gugus hidroksil atau dengan
metilasi atau glikosilasi.
O
OH
Struktur Antosianin
9.Khalkon
Khalkon adalah pigmen fenol kuning yang berwarna coklat kuat dengan sinar UV bila
dikromatografi kertas. Aglikon flavon dapat dibedakan dari glikosidanya, karena
hanya pigmen dalam bentuk glikosida yang dapat bergerak pada kromatografi kertas
dalam pengembang air. (Harborne, 1996)
O
10. Auron
Auron berupa pigmen kuning emas yang terdapat dalam bunga tertentu dan briofita.
Dalam larutan basa senyawa ini berwarna merah ros dan tampak pada kromatografi
kertas berupa bercak kuning, dengan sinar ultraviolet warna kuning kuat berubah
menjadi merah jingga bila diberi uap amonia. (Robinson, 1995)
HC O
O
Struktur Auron
Menurut Harborne (1996), dikenal sekitar sepuluh kelas flavonoida dimana semua
flavonoida, menurut strukturnya, merupakan turunan senyawa induk flavon dan
semuanya mempunyai sejumlah sifat yang sama yakni:
Golongan flavonoida Penyebaran Ciri khas
Antosianin
Proantosianidin
Flavonol
Flavon
Glikoflavon
pigmen bunga merah
marak,dan biru juga dalam
daun dan jaringan lain.
terutama tan warna, dalam
daun tumbuhan berkayu.
terutama ko-pigmen
tanwarna dalam bunga
sianik dan asianik;
tersebar luas dalam daun.
seperti flavonol
seperti flavonol
larut dalam air, λmaks 515-545 nm, bergerak dengan BAA pada kertas.
menghasilkan antosianidin (warna
dapat diekstraksi dengan amil alkohol ) bila jaringan dipanaskan dalam HCl
2M selama setengah jam.
setelah hidrolisis, berupa bercak
kuning murup pada kromatogram
Forestal bila disinari dengan sinar UV;
maksimal spektrum pada 330 – 350
setelah hidrolisis, berupa bercak coklat
redup pada kromatogram Forestal;
maksimal spektrum pada 330-350 nm.
mengandung gula yang terikat melalui
ikatan C-C; bergerak dengan
pengembang air, tidak seperti flavon
Biflavonil
pigmen bunga kuning,
kadang-kadang terdapat
juga dalam jaringan lain
tanwarna; dalam daun dan
buah
( terutama dalam Citrus )
tanwarna; sering kali
dalam akar; hanya terdapat
dalam satu suku,
Leguminosae
pada kromatogram BAA beupa bercak
redup dengan RF tinggi .
dengan amonia berwarna merah
; maksimal spektrum 370-410 nm.
berwarna merah kuat dengan Mg /
HCl; kadang – kadang sangat pahit . bergerak pada kertas dengan
pengembang air; tak ada uji warna
yang khas.
2.2.3 Metoda isolasi senyawa flavonoida
Metoda Isolasi Senyawa Flavonoida oleh Harborne
Dalam metoda ini, daun yang segar dimaserasi dengan MeOH, lalu disaring. Ekstrak
MeOH dipekatkan dengan rotari evaporator. Lalu ekstrak pekat yang dihasilkan,
diasamkan dengan H2SO4 2M, didiamkan, lalu diesktraksi dengan Kloroform. Lapisan
Kloroform diambil, lalu diuapkan, sehingga dihasilkan ekstrak polar pertengahan
(Terpenoida atau senyawa Fenol). (Harborne, 1996)
2.2.4 Sifat kelarutan flavonoida
Aglikon flavonoida adalah polifenol dan karena itu mempunyai sifat kimia senyawa
fenol, yaitu bersifat agak asam sehingga dapat larut dalam basa. Tetapi harus diingat,
bila dibiarkan dalam larutan basa, dan disamping itu terdapat oksigen, banyak yang
akan terurai. Karena mempunyai sejumlah gugus hidroksil, atau suatu gula,flavonoida
merupakan senyawa polar, maka umumnya flavonoida cukup larut dalam pelarut polar
(DMSO), Dimetilformamida (DMF), Air dan lain-lain. Adanya gula yang terikat pada
flavonoida (bentuk yang umum ditemukan) cenderung menyebabkan flavonoida lebih
mudah larut dalam air dan dengan demikian campuran pelarut yang disebut diatas
dengan air merupakan pelarut yang lebih baik untuk glikosida. Sebaliknya, aglikon
yang kurang polar seperti isoflavon, flavanon dan flavon serta flavonol yang
termetoksilasi cenderung lebih mudah larut dalam pelarut seperti Eter dan Kloroform. (Markham, 1988)
2.3 Teknik Pemisahan
Tujuan dari teknik pemisahan adalah untuk memisahkan komponen yang akan
ditentukan berada dalam keadaan murni, tidak tercampur dengan
komponen-komponen lainnya. Ada 2 jenis teknik pemisahan:
1. Pemisahan kimia adalah suatu teknik pemisahan yang berdasarkan adanya
perbedaan yang besar dari sifat-sifat fisika komponen dalam campuran yang
akan dipisahkan.
2. Pemisahan fisika adalah suatu teknik pemisahan yang didasarkan pada
perbedaan-perbedaan kecil dari sifat-sifat fisik antara senyawa-senyawa yang
termasuk dalam suatu golongan. (Muldja, 1995)
2.3.1 Kromatografi
Kromatografi merupakan suatu cara pemisahan fisik dengan unsur-unsur yang akan
dipisahkan terdistribusikan antara dua fasa, satu dari fasa-fasa ini membentuk lapisan stasioner denagn luas permukaan yang besar dan yang lainnya merupakan cairan yang
merembes lewat.
Fasa stasioner mungkin suatu zat padat atau suatu cairan dan fase yang
bergerak mungkin suatu cairan atau suatu gas. (Underwood, 1981)
Cara-cara kromatografi dapat digolongkan sesuai dengan sifat – sifat dari fasa diam,
yang dapat berupa zat padat atau zat cair. Jika fasa diam berupa zat padat disebut
gerak dapat berupa zat cair atau gas maka ada empat macam sistem kromatografi
yaitu:
1. Fasa gerak cair–fasa diam padat (kromatografi serapan):
a. kromatografi lapis tipis
b. kromatografi penukar ion
2. Fasa gerak gas–fasa diam padat, yakni kromatografi gas padat.
3. Fasa gerak cair–fasa diam cair (kromatografi partisi), yakni kromatografi kertas.
4. Fasa gerak gas–fasa diam zat cair, yakni :
a. kromatografi gas–cair
b. kromatografi kolom kapiler
Semua pemisahan dengan kromatografi tergantung pada kenyataan bahwa senyawa –
senyawa yang dipisahkan terdistribusi diantara fasa gerak dan fasa diam dalam
perbandingan yang sangat berbeda – beda dari satu senyawa terhadap senyawa yang
lain (Sastrohamidjojo, 1991).
2.3.1.1 Kromatografi Lapis Tipis
Kromatografi Lapis Tipis pada plat berlapis yang berukuran lebih besar, biasanya
5x20 cm, 10x20 cm, atau 20x20 cm. Biasanya memerlukan waktu pengembangan 30
menit sampai satu jam. Pada hakikatnya KLT melibatkan dua fase yaitu fase diam
atau sifat lapisan, dan fase gerak atau campuran pelarut pengembang. Fase diam dapat
berupa serbuk halus yang berfungsi sebagai permukaan penyerap atau penyangga
untuk lapisan zat cair. Fase gerak dapat berupa hampir segala macam pelarut atau
campuran pelarut. (Sudjadi, 1986)
Pemisahan senyawa dengan Kromatografi Lapis Tipis seperti senyawa organik alam dan senyawa organik sintetik dapat dilakukan dalam beberapa menit dengan alat
yang harganya tidak terlalu mahal. Jumlah cuplikan beberapa mikrogram atau
sebanyak 5g dapat ditangani. Kelebihan KLT yang lain ialah pemakaian jumlah
pelarut dan jumlah cuplikan yang sedikit. Kromatografi Lapis Tipis (KLT) merupakan
salah satu metode pemisahan yang cukup sederhana yaitu dengan menggunakan plat
Nilai utama Kromatografi Lapis Tipis pada penelitian senyawa flavonoida
ialah sebagai cara analisis cepat yang memerlukan bahan sangat sedikit. Menurut
Markham, Kromatografi Lapis Tipis terutama berguna untuk tujuan berikut:
1. Mencari pelarut untuk kromatografi kolom
2. Analisis fraksi yang diperoleh dari kromatografi kolom
3. Identifikasi flavonoida secara ko-kromatografi. 4. Isolasi flavonoida murni skala kecil
5. Penyerap dan pengembang yang digunakan umumnya sama dengan penyerap
dan pengembang pada kromatografi kolom dan kromatografi kertas.
(Markham, 1988)
2.3.1.2 Kromatografi Kolom
Kromatografi cair yang dilakukan dalam kolom besar merupakan metode
kromatografi terbaik untuk pemisahan dalam jumlah besar (lebih dari 1 g). Pada
kromatografi kolom, campuran yang akan dipisahkan diletakkan berupa pita pada
bagian atas kolom penyerap yang berada dalam tabung kaca, tabung logam, dan
tabung plastik. Pelarut atau fasa gerak dibiarkan mengalir melalui kolom karena
aliran yang disebabkan oleh gaya berat atau didorong dengan tekanan. Pita senyawa
linarut bergerak melalui kolom dengan laju yang berbeda, memisah, dan dikumpulkan
berupa fraksi ketika keluar dari atas kolom (Gritter, 1991).
Dengan menggunakan cara ini, skala isolasi flavonoida dapat ditingkatkan
hampir ke skala industri. Pada dasarnya, cara ini meliputi penempatan campuran
flavonoida (berupa larutan) diatas kolom yang berisi serbuk penyerap (seperti
selulose, silika atau poliamida), dilanjutkan dengan elusi beruntun setiap komponen
memakai pelarut yang cocok. Kolom hanya berupa tabung kaca yang dilengkapi
dengan keran pada salah satu ujung. (Markham, 1988)
2.3.1.3 Harga Rf (Reterdation Factor)
Mengidentifikasi noda-noda dalam lapisan tipis lazim menggunakan harga Rf yang
diidentifikasikan sebagai perbandingan antara jarak perambatan suatu zat dengan
ditempuh oleh tiap bercak dari titik penotolan diukur dari pusat bercak. Untuk
mengidentifikasi suatu senyawa, maka harga Rf senyawa tersebut dapat dibandingkan
dengan harga Rf senyawa pembanding.
Jarak perambatan bercak dari titik penotolan
Rf =
Jarak perambatan pelarut dari titik penotolan (Sastrohamidjojo, 1991).
2.3.2 Kristalisasi
Kristalisasi adalah pengendapan kristal dari larutan yang terbuat dari bahan
tertentu. selama proses pembentukan kristal, molekul akan cenderung menjadi melekat
kristal tumbuh terdiri dari jenis yang sama molekul karena lebih cocok dalam kisi
kristal untuk molekul struktur yang sama daripada molekul lain. Jika proses
kristalisasi diperbolehkan untuk terjadi dalam dekat - kondisi kesetimbangan,
preferensi molekul untuk deposit pada permukaan terdiri dari molekul seperti akan
menyebabkan peningkatan dalam kemurnian bahan kristal. Sehingga proses
rekristalisasi adalah salah satu metode yang paling penting tersedia bagi ahli kimia
untuk pemurnian padatan. Prosedur tambahan dapat dimasukkan ke dalam proses
kristalisasi untuk menghilangkan kotoran. Ini termasuk filtrasi untuk menghilangkan
padatan undissolved dan adsorpsi untuk menghilangkan kotoran yang sangat
polar.(Daniel J.Pasto,1992)
2.3.3 Ekstraksi
Ekstraksi dapat dilakukan dengan metoda maserasi, sokletasi, dan perkolasi. Sebelum
ekstraksi dilakukan, biasanya serbuk tumbuhan dikeringkan lalu dihaluskan dengan
derajat kehalusan tertentu, kemudian diekstraksi dengan salah satu cara di atas. Ekstraksi dengan metoda sokletasi dapat dilakukan secara bertingkat dengan berbagai
pelarut berdasarkan kepolarannya, misalnya n-heksana, Eter, Benzena, Kloroform, Etil
asetat, Etanol, Metanol, dan Air.
Ekstraksi dianggap selesai bila tetesan terakhir memberikan reaksi negatif
terhadap senyawa yang diekstraksi. Untuk mendapatkan larutan ekstrak yang pekat
biasanya pelarut ekstrak diuapkan dengan menggunakan alat rotari evaporator.
2.4 Teknik Spektroskopi
Teknik spektroskopi adalah salah satu teknik analisis kimia–fisika yang mengamati
tentang interaksi atom atau molekul dengan radiasi elektromagnetik.
Ada dua macam instrumen pada teknik spektroskopi yaitu spektrometer dan spektrofotometer. Instrumen yang memakai monokromator celah tetap pada bidang
fokus disebut sebagai spektrometer. Apabila spektrometer tersebut dilengkapi dengan
detektor yang bersifat fotoelektrik maka disebut spektrofotometer (Muldja, 1955).
Informasi Spektroskopi Inframerah menunjukkan tipe – tipe dari adanya gugus
fungsi dalam satu molekul dan Resonansi Magnetik Inti yang memberikan informasi
tentang bilangan dari setiap tipe dari atom hidrogen dan juga memberikan informasi
yang menyatakan tentang lingkungan dari setiap tipe dari atom hidrogen.
Kombinasinya dan data yang ada kadang – kadang menentukan struktur yang lengkap
dari molekul yang tidak diketahui. (Pavia, 1979).
2.4.1 Spektrofotometri Ultra Violet
Serapan molekul di dalam derah ultra violet dan terlihat dari spektrum bergantung
pada struktur ultra elektronik dari molekul. Penyerapan sejumlah energi,
menghasilkan percepatan dari elektron dalam orbital tingkat dasar ke orbital yang
berenergi lebih tinggi di dalam keadaan tereksitasi (Silverstein, 1986).
Spektrum Flavonoida biasanya ditentukan dalam larutan dengan pelarut Metanol
(MeOH) atau Etanol (EtOH). Spektrum khas terdiri atas dua maksima pada rentang 240-285 nm (pita II) dan 300-550 nm (pita I). Kedudukan yang tepat dan kekuatan
nisbi maksima tersebut memberikan informasi yang berharga mengenai sifat
flavonoida dan pola oksigenasinya. Ciri khas spektrum tersebut ialah kekuatan nisbi
yang rendah pada pita I dalam dihidroflavon, dihidroflavonol, dan isoflavon serta
kedudukan pita I pada spektrum khalkon, auron dan antosianin yang terdapat pada
Ciri spektrum golongan flavonoida utama dapat ditunjukkan sebagai berikut:
2.4.2 Spektrofotometri infra merah (FT-IR)
Spektrum inframerah suatu molekul adalah hasil transisi antara tingkat energi getaran
yang berlainan. Pancaran inframerah yang kerapatannya kurang dari 100 cm -1
(panjang gelombang lebih daripada 100 µm) diserap oleh sebuah molekul organik dan diubah menjadi putaran energi molekul.
Penyerapan ini tercantum, namun spektrum getaran terlihat bukan sebagai
garis – garis melainkan berupa pita – pita. Hal ini disebabkan perubahan energi
getaran tunggal selalu disertai sejumlah perubahan energi putaran (Silverstein, 1986).
Dalam molekul sederhana beratom dua atau beratom tiga tidak sukar untuk
menentukan jumlah dan jenis vibrasinya dan menghubungkan vibrasi-vibrasi tersebut
dengan energi serapan. Tetapi untuk molekul-molekul beratom banyak, analisis
jumlah dan jenis vibrasi itu menjadi sukar sekali atau tidak mungkin sama sekali,
karena juga harus diperhitungkan terjadinya saling mempengaruhi (inter-aksi)
beberapa pusat vibrasi.
Vibrasi molekul dapat dibagi dalam dua golongan , yaitu vibrasi regang dan vibrasi
lentur.
1. Vibrasi regang
Di sini terjadi terus menerus perubahan jarak antara dua atom di didalam suatu
molekul. Vibrasi regang ini ada dua macam yaitu vibrasi regang simetris dan tak
simetri.
2.Vibrasi lentur
Di sini terjadi perubahan sudut antara dua ikatan kimia. Ada empat macam vibrasi
lentur yaitu vibrasi lentur dalam bidang yang dapat berupa vibrasi scissoring atau
vibrasi rocking dan vibrasi keluar bidang yang dapat berupa waging atau berupa
BAB 3
8. Neraca Analitis Mettler PM 480
9. Alat pengering Memmers
10.Rotari evaporator Buchi B-480
11.Labu alas 500 ml Pyrex
12.Alat pengukut titik lebur Fisher-Jhons
13.Statif dan klem
14.Lampu UV 254 nm
15.Spatula
16.Batang pengaduk
17.Pipet tetes
18.Botol vial
19.Bejana Kromatografi Lapis Tipis
20.Spektrofotometer FT-IR Jasco
21.Spektrofotometer UV-Visible
22.Kertas Saring
3.2. Bahan
1. Buah Mahkota Dewa (P. macrocarpa Boerl.)
2. Etil Asetat Teknis
3. Kloroform p.a Merck
4. Metanol Destilasi
5. HCl 6%
6. n-heksana Teknis
7. FeCl 5%
8. NaOH 10%
9. Mg-HCl
10.H2SO4(p)
11.Aquades
12.Silika Gel 40 (70-230 Mesh) ASTM E.Merck.KgaA
3.3. Prosedur Penelitian
3.3.1 Penyediaan sampel
Sampel yang diteliti adalah buah mahkota dewa yang diperoleh dari Perumnas
Simalingkar Medan, Sumatera Utara. Buah mahkota dewa dihaluskan dengan cara
dipotong kecil-kecil kemudian dikeringkan di udara terbuka hingga diperoleh
potongan daging buah mahkota dewa kering sebanyak 1170 g.
3.3.2 Uji Pendahuluan Terhadap Ekstrak Daging Buah Mahkota Dewa
Serbuk kering buah mahkota dewa diidentifikasi dengan menggunakan cara:
1. Uji Busa
2. Skrining Fitokimia
3.3.2.1Uji Busa
Ekstrak metanol daging buah mahkota dewa sebanyak 5 ml dimasukkan kedalam
tabung reaksi. Kemudian ditambahkan 10 ml Aquades, lalu dikocok-kocok dengan
kuat hingga terbentuk busa dan didiamkan selama 5 menit. Melalui perlakuan tersebut
dalam sampel terdapat senyawa glikosida.
3.3.2.2Skrining Fitokimia
Untuk mengetahui adanya senyawa Flavonoida yang terdapat dalam buah mahkota
dewa (P. macrocarpa Boerl.) maka dilakukan uji pendahuluan secara kualitatif
dengan reaksi warna sebagai berikut :
Prosedur :
- Dimasukkan 10 gram serbuk kering daging buah mahkota dewa (P.
macrocarpa Boerl.)
- Ditambahkan 100 ml metanol
- Didiamkan selama 1 malam
- Disaring
- Dibagi ekstrak metanol kedalam 4 tabung reaksi
- Ditambahkan masing-masing pereaksi
a) Tabung I : dengan FeCl3 1% menghasilkan larutan berwarna hitam
b) Tabung II : dengan H2SO4(p) menghasilkan larutan berwarna orange
kekuningan
c) Tabung III : dengan Mg-HCl menghasilkan larutan berwarna merah muda
3.3.2.3Analisis Kromatografi Lapis Tipis (KLT)
Analisis Kromatografi Lapis Tipis dilakukan terhadap Ekstrak Kloroform dengan
menggunakan fase diam silika gel 60F254. Analisis ini dimaksudkan untuk mencari
pelarut yang sesuai didalam analisis kromatografi kolom. Pelarut yg digunakan adalah
campuran pelarut n-heksana: etil asetat (90:10 ; 80:20 ; 70:30 ; 60:40) v/v, sehingga diperoleh perbandingan pelarut n-heksana: etil asetat yang sesuai untuk kromatografi
kolom. Pelarut yang digunakan berdasarkan pada jumlah bercak atau noda yang
terpisah dengan baik dalam kromatografi lapis tipis.
Prosedur Analisis Kromatografi Lapis Tipis :
Kedalam bejana kromatografi lapis tipis dimasukkan larutan fase gerak yaitu
campuran n-heksana: etil asetat dengan campuran ( 90:10 ; 80:20 ; 70:30 ; 60:40 ) v/v.
Kemudian ekstrak kloroform di totolkan pada plat KLT. Lalu plat dimasukkan
kedalam bejana yang berisi pelarut yang dijenuhkan. Setelah dielusi, dikeluarkan dari
bejana dan dikeringkan. Noda terbentuk diamati dengan sinar Ultra Violet dan
difiksasi dengan pereaksi FeCl3 1%. Kemudian dihitung dan dicatat harga Rf. Yang
memberikan pemisahan bercak noda yang baik adalah perbandingan perlarut
n-heksana: etil asetat ( 70:30) v/v yang memberikan 3 noda dengan harga Rf yaitu 0,55 ;
0,42 dan 0,33.
3.3.3 Prosedur Untuk Memperoleh Senyawa Kimia Dari Ekstrak Buah Mahkota Dewa
Serbuk dari daging buah mahkota dewa ditimbang sebanyak 1170 g, dimasukkan kedalam ekstraktor kemudian ditambahkan dengan pelarut metanol sampai semua
sampel terendam oleh pelarut dan dibiarkan selama ± 72 jam dan sesekali diaduk.
Ekstrak disaring dan diperoleh ekstrak berwarna merah kecoklatan. Maserasi
dilakukan secara berulang kali dengan menggunakan pelarut metanol hingga ekstrak
metanol yang diperoleh memberikan hasil uji yang negatif pada pereaksi untuk
identifikasi senyawa Flavonoida. Ekstrak metanol yang diperoleh dipekatkan dengan
metanol, kemudian di ekstraksi partisi dengan menggunakan pelarut n-heksana,
sehingga terbentuk 2 lapisan n-heksana dan lapisan metanol. Kemudian fraksi metanol
ditampung dan dipekatkan dan kemudian dihidrolisa dengan menggunakan HCl 6%.
Kemudian disaring dan fitrat yang diperoleh diekstraksi partisi dengan kloroform
secara berulang-ulang. Ekstrak kloroform dipekatkan kembali dengan menggunakan
alat rotari-evaporator sehingga diperoleh ekstrak pekat kloroform sebanyak 14,62 g.
3.3.4 Isolasi Senyawa Flavonoida Dengan Kromatografi Kolom
Isolasi senyawa flavonoida secara kromatografi kolom dilakukan terhadap ekstrak
pekat klorofom dari buah mahkota dewa yang diperoleh. Fasa diam yang digunakan
adalah silika gel 40 (70-230 mesh) ASTM dan fase gerak yaitu n-heksana 100% dan
campuran pelarut n-heksana : etil asetat (90:10 ; 80:20 ; 70:30 ) v/v.
Prosedur Isolasi Senyawa Flavonoida Dengan Kromatografi Kolom :
Dirangkai alat kolom kromatografi, dimana terlebih dahulu dibuburkan silika gel 40
(70-230 mesh) ASTM dengan menggunakan n-heksana. Diaduk-aduk hingga
homogen lalu dimasukkan kedalam kolom kromatografi. Kemudian di elusi dengan
menggunakan n-heksana 100% hingga silika gel dalam kolom padat dan homogen.
Dimasukkan 14,62g ekstrak klorofom buah mahkota dewa kedalam kolom
kromatografi yang telah diisi dengan bubur silika gel yang telah dielusi. Kemudian
ditambahkan fasa gerak n-heksana: etil asetat dengan perbandingan mulai dari
(90:10)v/v; (80:20)v/v; (70:30)v/v, secara perlahan-lahan dan diatur sehingga aliran
fasa gerak yang keluar dari Kolom Kromatografi sama banyaknya dengan jumlah fasa
gerak yang ditambahkan. Hasil yang diperoleh ditampung dalam botol vial setiap 8 ml. Kemudian di KLT dan digabung fraksi yang berharga Rf sama. Setelah itu
dilakukan uji Flavonoida dan diuapkan pelarutnya.
3.3.5 Pemurnian
Prosedur
Senyawa hasil isolasi di rekristalisasi, dengan cara melarutkan kembali dengan Aseton
dan kemudian diuapkan di udara terbuka hingga diperoleh kristal murni sebanyak
80mg.
3.3.6 Uji Kemurnian Hasil Isolasi dengan Kromatografi Lapis Tipis (KLT)
Uji kemurnian senyawa hasil isolasi dilakukan dengan kromatografi lapis tipis dengan
menggunakan fasa diam silika gel 60 F254 dengan fasa gerak n-heksana: etil asetat
dengan perbadingan (70:30) v/v.
Prosedur uji kemurnian hasil isolasi dengan kromatografi lapis tipis.
Dimasukkan 10 ml larutan fasa gerak n-heksana: etil asetat kedalam bejana
kromatografi, kemudian dijenuhkan. Ditotolkan kristal yang sebelumnya telah
dilarutkan dengan klorofom pada plat KLT. Dimasukkan plat KLT yang telah
ditotolkan tersebut kedalam bejana kromatografi yang telah jenuh. Setelah pelarut fasa
gerak merembes hingga batas atas plat KLT dikeluarkan dari bejana kemudian
dikeringkan, dan difiksasi dengan menggunakan FeCl3 5% menghasilkan bercak
berwarna hitam yang menunjukkan adanya senyawa flavonoida. Perlakuan yang sama
dilakukan dan difiksasi dengan NaOH 10% yang menghasilkan bercak berwarna biru
violet.
3.3.7 Analisis Senyawa Hasil Isolasi
3.3.7.1 Pengukuran Titik Lebur Senyawa hasil Isolasi
Senyawa hasil isolasi memiliki rentangan titik lebur 172 – 174oC
3.3.7.2Analisis senyawa hasil isolasi dengan Spektrofotometer UV-Visible
Analasis spektrofotometer UV-Visible dilakukan di Pusat Penelitian LIPI, Serpong -
3.3.7.3 Analisis Senyawa Hasil Isolasi Dengan Spektrofotometer Infra Merah Analasis spektrofotometer FT-IR dilakukan di Pusat Penelitian LIPI, Serpong -
Tangerang.
3.3.7.4 Analsis Senyawa Hasil Isolasi Dengan Spektrofotometer Resonansi Magnetik Inti Proton (1H-NMR)
Analasis dengan spektrofotometer Resonansi Magnetik Inti Proton (1H-NMR)
dilakukan di Pusat Penelitian LIPI, Serpong Tangerang. Dengan menggunakan Aseton
3.4 Bagan Skrining Fitokimia
diekstraksi maserasi dengan metanol
disaring
ditambahkan ditambahkan ditambahkan ditambahkan pereaksi FeCl3 1% pereaksi NaOH 10% pereaksi Mg-HCl pereaksi H2SO4(p)
Larutan Biru Violet
Larutan Merah Muda
Larutan Orange Kekuningan Larutan
Hitam
3.4.1 Bagan Penelitian
Dimaserasi dengan metanol selama ±72 jam Diulangi sebanyak 3 kali
Disaring
diskrining Fitokimia
dipekatkan dengan rotari-evaporator
diekstraksi partisi dengan n-heksana
diuapkan sampai larutan metanolnya menguap semua
dilakukan uji kandungan glukosa dengan menggunakan pereaksi Millon (+) dihidrolisa dengan menggunakan HCl 6% sambil dipanaskan selama ± 40 menit
didinginkan kemudian disaring
diekstraksi partisi dengan Klorofom sebanyak 3 kali
diuapkan hingga pekat
diskrining fitokimia
diuji KLT dengan menggunakan n-heksana : etil asetat (90:10;80:20;70:30;60:40)v/v
dikolom kromatografi dengan fase diam silica gel dan fase gerak n-heksana : etil asetat (90:10 ;80:20 ;70:30 ; 60:40)v/v
ditampung tiap fraksi sebanyak 8ml dalam botol vial
diuji FeCl3 1% diuji FeCl3 1% diuji FeCl3 1% diuji FeCl3 1% diuji FeCl3 1%
di KLT
digabung fraksi dengan harga Rf sama diuapkan spektrofotometer 1H-NMR 1170g daging buah mahkota dewa
( P. Macrocarpa Boerl.)
residu
Ekstrak Klorofom
Lapisan metanol-asam residu
Lapisan metanol Lapisan n-heksana ( negatif
terhadap pereaksi Flavonoida Ekstrak pekat metanol
Hasil negatif Hasil negatif Hasil positif Hasil positif
Senyawa murni
BAB 4
HASIL DAN PEMBAHASAN
5.1. Hasil Penelitian
Dari hasil skrining fitokimia terhadap ekstrak dari buah mahkota dewa dengan
menambahkan pereaksi - pereaksi warna untuk menentukan golongan senyawa kimia
yang dikandung dengan menggunakan pereaksi Flavonoida yaitu:
1. H2SO4(p) memberikan warnaorange kekuningan
2. NaOH 10% memberikan warna biru violet
3. FeCl3 1% memberikan warna hitam
4. Mg-HCl memberikan warna merah muda
Hasil isolasi senyawa flavonoida dari ekstrak buah mahkota dewa (P. macrocarpa
Boerl.), diperoleh dengan menggunakan fase gerak n-heksana: etil asetat (70:30)v/v yang menghasilkan kristal berwarna kuning kecoklatan sebanyak 80 mg dan
memiliki rentangan titik lebur antara 172 – 174oC.
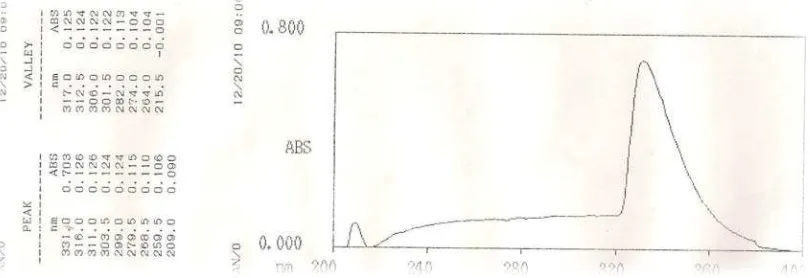
Dari hasil analisis Spektrofotometer Ultra Violet Visible (UV-Visible)
memberikan 2 peak dengan panjang gelombang 209,0 nm dan 331,0 nm
Hasil analisis Spektrofotometer Infra Merah (FT-IR) dari kristal hasil isolasi
memberikan pita-pita serapan pada daerah bilangan gelombang (cm-1) sebagai berikut
Gambar : Spektrum Hasil Analisis Infra Merah
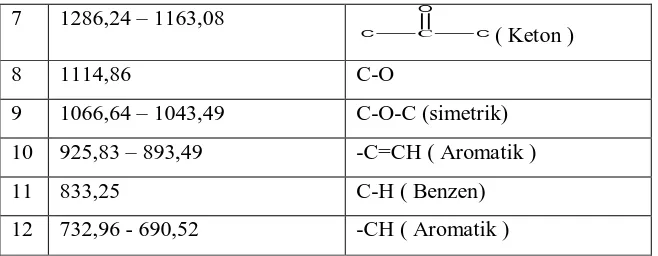
Tabel. Gugus Fungsi dan Pita Serapan Hasil analisis FT-IR senyawa hasil isolasi
No Rentangan Pita Serapan Gugus Fungsi
1 3211,48 – 3122,75 cm-1 C-H ( aromatik )
2 2985,81 – 2800,64 CH2 dan CH3
3 1604,77 C=O ( Keton )
4 1587,42 C=C (Aromatik dan Alifatik )
5 1446,96 CH2
7 1286,24 – 1163,08
C O
C C( Keton )
8 1114,86 C-O
9 1066,64 – 1043,49 C-O-C (simetrik)
10 925,83 – 893,49 -C=CH ( Aromatik )
11 833,25 C-H ( Benzen)
12 732,96 - 690,52 -CH ( Aromatik )
Hasil analisis spektrofotometer Resonansi Magnetik Inti Proton (1H-NMR)
memberikan pergeseran kimia pada daerah (ppm) sebagai berikut
Gambar : Spektrum Magnetik Inti Proton (1H-NMR) Senyawa Hasil Isolasi
2. Pergeseran kimia pada daerah δ= 6,0480 ppm dengan puncak singlet menunjukkan proton yang terdapat pada C6 dan C8 pada cincin A
dan C3 pada cincin C (Marby,T.J 1970)
3. Pergeseran kimia pada daerah δ= 6,8596 – 6,8764 ppm dengan puncak doublet menunjukkan C-CH=CH-C pada posisi C3’ dan C5’
4. Pergeseran kimia pada daerah δ= 7,6299 – 7,6483 ppm dengan puncak doublet menunjukkan C-CH=CH-C pada posisi C2’ dan C6’
4.2 Pembahasan
Dari hasil kromatografi lapis tipis, diketahui bahwa perbandigan pelarut yang baik
digunakan untuk mengisolasi senyawa flavonoida dari buah mahkota dewa adalah
n-heksana: etil asetat (70:30 v/v) yang menunjukkan pemisahan yang lebih baik dari
noda yang di hasilkan. Hal ini juga didukung oleh dengan analisi KLT yang dilakukan
pada kristal menghasilkan noda tunggal.
Berdasarkan spektrum UV-Visible dari senyawa flavonoida yang di isolasi memberikan panjang gelombang I ( λI ) 331,0 nm dan λII 209,0 nm dengan pelarut aseton. Dan pada literatur dengan panjang gelombang 250 – 280 nm pada λII dan 310 – 350 nm pada λI yaitu senyawa flavonoida dengan jenis Flavon ( Markham, 1988 )
Dari hasil interpretasi Spektrum Infra Merah dan Spektrum Resonansi
Magnetik Inti Proton (1H-NMR), senyawa hasil isolasi dengan pelarut aseton
diperoleh sebagai berikut:
1. Pergeseran kimia pada daerah δ = 3,7889 ppm dengan puncak singlet menunjukkan proton-proton dari gugus metoksi O-CH3, hal ini didukung oleh spektrum inframerah pada bilangan
gelombang 2985,81 – 2800,64 cm-1 dengan puncak lemah
menunjukkan vibrasi ulur C-H. Hal ini juga didukung pita pada
bilangan gelombang 1446,61 cm-1 dengan puncak kuat
menunjukkan adanya vibrasi regang CH2, dan pada bilangan
gelombang 1382,96 cm-1 menunjukkan adanya vibrasi ulur metil
sedang menunjukkan adanya vibrasi ulur C-O dan 1066,64 –
1043,49 cm-1 dengan puncak kuat menunjukkan adanya serapan
C-O-C simetrik
2. Pergeseran kimia pada daerah δ= 6,0480 ppm dengan puncak singlet menunjukkan proton pada C6 dan C8 yang terdapat pada
cincin A dan C3 pada cincin C. Hal ini didukung oleh pita pada bilangan gelombang 925,83 – 893,49 cm-1 dengan puncak kuat
menunjukkan adanya vibrasi –C=CH dari cincin aromatik dan
pada bilangan gelombang 833,25 cm-1 dengan puncak kuat
menunjukan adanya vibrasi C-H dari sistem benzen dan pada
bilangan gelombang 732,96 – 690,52 dengan puncak kuat
menunjukkan adanya vibrasi –CH pada cincin aromatik
3. Pergeseran kimia pada daerah δ= 6,8596 – 6,8764 ppm dengan puncak doublet menunjukkan C-CH=CH-C pada posisi C3’ dan
C5’ dan pada C2’ dan C6’ juga menunjukkan puncak doublet
C-CH=CH-C pada daerah δ= 7,6299 – 7,6483 ppm. Hal ini didukung oleh pita pada bilangan gelombang 1604,77 cm-1
menunjukkan vibrasi ulur C=C dari sistem aromatik dan alifatik
dan pada bilangan gelombang 925,83 – 893,49 cm-1 dengan
puncak kuat menunjukkan adanya vibrasi –C=CH dari cincin
aromatik
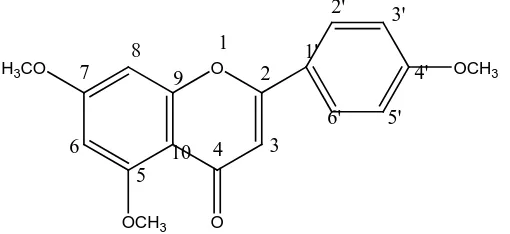
Dari data spektrum UV-Visible, FT-IR, dan 1H-NMR dapat
disimpulkan bahwa kemungkinan senyawa yg diisolasi adalah senyawa
Flavonoida jenis Flavon dengan struktur sebagai berikut:
BAB 5
KESIMPULAN DAN SARAN
5.1 Kesimpulan
1. Dari hasil uji skrining fitokimia dengan pereaksi flavonoida menunjukkan
bahwa buah mahkota dewa (P. macrocaarpa Boerl.) mengandung senyawa
flavonoida. Isolasi senyawa flavonoida dari buah mahkota dewa (P.
macrocarpa Boerl.) sebanyak 1170g yang di ekstraksi dengan menggunakan
klorofom kemudian direkristalisasi dengan aseton menghasilkan kristal
berwarna kuning kecoklatan sebanyak 80 mg dengan rentangan titik lebur 172
– 174oC.
2. Dari data analisis sepektrofotometer UV-Visible, spektrofotometer Infra
Merah (FT-IR) dan sepktrofotometer Magnetik Inti Proton (1H-NMR)
menunjukkan senyawa yang diperoleh adalah senyawa flavonoida golongan
flavon.
5.2 Saran
1. Untuk lebih mendukung struktur senyawa flavonoida hasil isolasi sebaiknya
perlu dilakukan analisis spektroskopi karbon (13C-NMR) dan Spektroskopi
Massa (MS).
Arif, H. H. 2004. Tumbuhan Obat dan Khasiatnya (Seri Agri Sehat). Seri Pertama Jakarta : Penerbit Penebar swadaya.
Dalimartha, Setiawan. 2004. Atlas Tumbuhan Obat Indonesia. Jilid 4. Jakarta : Puspa Swara.
Dreyer,L.D.1986.Chemataxonomy of The Rutaceae ,Constituent of
Murrayapaniculata(Linn.)Jack.The Journal of Organic Chemistry .33(3658) : halaman. 3575
Gritter, R. J. 1991. Pengantar Kromatografi. Terbitan ke-2. Terjemahan Kosasih Padmawinata. ITB. Bandung
Gotama. I. B .I dkk. 1999. Inventaris Tanaman Obat Indonesia, Jilid 4. Jakarta : Departemen Kes. Badan Penelitian dan Pengembangan Kesehatan.
Harmanto, N. 2001. Sehat Dengan Ramuan Tradisional Mahkota Dewa. Cetakan Pertama. Tangerang : PT. Agromedia Pustaka.
Hartono, H. Soesanti. 2004. Tanaman Obat Keluarga 3. Cetakan Pertama. Jakarta : Penerbit Inti Sari Mediatama
Harborne, J. B. 1996. Metoda Fitokimia, Penuntun Cara Modern Menganalisa Tumbuhan. Terbitan ke-2. Terjemahan Kosasih Padmawinata dan Iwang Soediro. ITB. Bandung
Joshi,B.S.1969 .Structure of Exoticin ,a Flavone from the Leaves of Murraya exotica (Linn.). Journal Indian Chem .7, halaman. 636
Manito, P. 1992. Biosintesis Produk Alami. Cetakan ke-1. Terjemahan Koensoemardiyah. IKIP Press. Semarang
Markham, K. R. 1988. Cara Mengidentifikasi Flavonoida. Terjemahan Kosasih Padmawinata. ITB. Bandung
Marby,T.J dkk.1970.The Systematic identification of flavoniods.Springer-verlag, Heidelberg.New York
Muldja, M.H.1995 .Analisis Instrumental.Cetakan ke-1. Airlangga Universitas Press. Surabaya
Noerdin,D.1985.Elusidasi Struktur Senyawa Organik dengan Cara Spektroskopi Ultra Lembayung dan Inframerah .Edisi ke-1. Penerbit Angkasa. Bandung
Pavia, L. D. 1979. Introduction to Spectroscopy a Guide for Students of Organic Chemistry. Philladelphia: Saunders College.
Robinson, T. 1995. Kandungan Organik Tumbuhan Tinggi. Edisi ke-4. Terjemahan Kosasih Padmawinata. ITB Press. Bandung
Sastrohamidjojo, H. 1991. Kromatografi . Edisi ke-1.Yogyakarta:Penerbit Liberty
Silverstein, R. M. 1986. Penyidikan Spektrometrik Senyawa Organik. Edisi ke-4. Terjemahan A. J. Hartomo dan Anny Victor Purba. Erlangga. Jakarta
Lampiran C. Kromatografi Lapis Tipis Ekstrak Klorofom buah mahkota dewa (P. macrocarpa Boerl.) dengan penampakan noda dibawah sinar
ultraviolet dengan λ = 254 nm
I II III IV
MD MD MD MD
Keterangan :
Fase diam : Silika gel 60 F254
MD : Ekstrak Klorofom Buah mahkota dewa
I : Fase gerak n-heksana: etil asetat (90:10)v/v
II : Fase gerak n-heksana: etil asetat (80:20)v/v
III : Fase gerak n-heksana: etil asetat (70:30)v/v
IV : Fase gerak n-heksana: etil asetat (60:40)v/v
No Fase Gerak Jumlah
noda
Warna Noda Rf
1 n-heksana: etil asetat (90:10) v/v - - -
2 n-heksana: etil asetat (80:20) v/v 1 Coklat 0,59
3 n-heksana: etil asetat (70:30) v/v 3 Coklat 0,55
0,42
0,33
4 n-heksana: etil asetat (60:40) v/v 2 Coklat 0,3
Lampiran D. Kromatografi Lapis Tipis Senyawa Hasil Isolasi melalui penampakan noda dengan penambahan pereaksi
I II
F F
Keterangan :
Fase diam : Silika gel 60 F254
F : Senyawa hasil isolasi
I : FeCl3 1% ( berwarna hitam)
II : NaOH 10% (berwarna biru violet)
Data harga Rf dari bercak noda :
No Penampakan Bercak Pereaksi Warna noda Rf
1 I FeCl3 Hitam 0,42
Lampiran I. Spektrum 1H-NMR Pembanding Untuk Senyawa Flavonoida a. Spektrum RMI-1H apigenin (eter TMS) dalam CCl4