ABSTRAK
ISOLASI DAN IDENTIFIKASI SENYAWA STEROID DARI BUAH MAHKOTA DEWA (Phaleria macrocarpa)
Oleh
Astri Rahayu
Pada penelitian ini telah dilakukan isolasi dan identifikasi senyawa steroid dari buah mahkota dewa (Phaleria macrocarpa). Tahapan penelitian yang dilakukan meliputi pengumpulan, persiapan sampel, dan ekstraksi. Identifikasi senyawa steroid dilakukan menggunakan KLT dengan berbagai eluen, pereaksi Liebermann-Burchard, dan uji titik leleh. Penentuan struktur senyawa yang dilakukan meliputi spektrofotometer ultraungu-tampak (UV-Vis),
spektrofotometer FT-IR, spektrofotometer NMR, dan spektrofotometer massa (MS). Hasil penelitian menunjukkan bahwa berdasarkan identifikasi dengan KLT, pereaksi Liebermann-Burchard, uji titik eleh, data spektrum FT-IR, ultraungu-tampak, NMR, dan massa senyawa hasil isolasi tersebut merupakan senyawa steroid yang bernama stigmast5en3 ol ( -sitosterol) sebanyak 10 mg yang berupa kristal murni berbentuk jarum berwarna putih dengan titik leleh 135o-137oC.
ABSTRACT
ISOLATION AND IDENTIFICATION OF STEROID FROM THE FRUIT OF MAHKOTA DEWA (Phaleria macrocarpa)
By Astri Rahayu
This research had done the isolation and identification of steroid from the fruit of mahkota dewa (Phaleria macrocarpa). Research phase conducted include the collection and
preparation samples, extraction, isolation. Identification of steroid compound is carried out using TLC with various eluen, reagent Liebermann-Burchard, and melting point test. Determining of structure using UV-Vis spectrophotometer, FT-IR spectrophotometer, NMR, and mass spectrophotometer (MS). The result showed that based on identification by TLC, reagent Liebermann-Burchard, melting point test, FT-IR spectrum data, UV-Vis spectra, NMR and MS, indicate that had formed a steroid compound called stigmast5en3 ol ( -sitosterol) as much as 10 mg as a pure crystal needle-shaped with the melting point ca 135o -137 oC.
i
DAFTAR ISI
Halaman
DAFTAR ISI ... i
DAFTAR TABEL ... iv
DAFTAR GAMBAR ... v
I. PENDAHULUAN ... 1
A. Latar Belakang ... 1
B. Tujuan Penelitian ... 3
C. Manfaat Penelitian ... 3
II. TINJAUAN PUSTAKA ... 4
A. Tymelaceae ... 4
B. Mahkota Dewa (Phaleria macrocarpa) ... 4
1. Kandungan kimia mahkota dewa ... 6
2. Manfaat mahkota dewa ... 7
C. Senyawa steroid ... 8
1. Manfaat steroid... 12
2. Ekstraksi dan isolasi steroid ... 13
D. Pemisahan Senyawa Secara Kromatografi ... 16
1. Kromatografi lapis tipis (KLT) ... 17
ii
3. Kromatografi cair vakum (KCV) ... 19
4. Kromatotron ... 19
5. Analisis kemurnian ... 21
E. Penentuan Struktur Senyawa Organik ... 22
1. Identifikasi Senyawa Organik Secara Spektroskopi ... 22
1.1. Fourier transform infrared spectroscopy (FT-IR) ... 22
1.2. Spektroskopi ultraungu-tampak (UV-VIS) ... 24
1.3. Spektroskopi resonansi magnetik nuklir (NMR) ... 25
1.4. Spektroskopi GC-massa (MS)... 26
1.5. Spektroskopi massa (MS) ... 26
III. METODOLOGI PENELITIAN ... 27
A. Waktu dan Tempat Penelitian ... 27
B. Alat dan Bahan ... 27
1. Alat-alat yang digunakan ... 27
2. Bahan-bahan yang digunakan ... 28
C. Prosedur Penelitian ... 28
1. Pengumpulan dan penyiapan sampel ... 28
2. Ekstraksi dengan etil asetat ... 29
3. Kromatografi cair vakum (KCV) ... 29
4. Kromatografi lapis tipis (KLT) ... 30
5. Kromatotron ... 30
6. Kromatografi kolom (KK) ... 31
7. Analisis kemurnian ... 31
iii
9. Fourier transform infrared spectroscopy (FTIR) ... 32
10. Spektroskopi resonansi magnetik nuklir (NMR) ... 33
11. Spektroskopi GC-massa (MS) ... 33
12. Spektroskopi massa ... 34
IV. HASIL DAN PEMBAHASAN ... 35
A. Isolasi senyawa steroid ... 35
B. Penentuan titik leleh ... 41
C. Penentuan struktur senyawa organik ... 42
1. Identifikasi senyawa organik secara spektroskopi ... 42
1.1. Spektroskopi ultraungu-tampak (UV-Vis) ... 42
2. Analisis fourier transform infrared spectroscopy (FT-IR) ... 43
3. Spektroskopi magnetik nuklir (NMR) ... 45
3.1. Spektroskopi NMR karbon ... 45
3.2. Spektroskopi DEPT ... 47
4. Spektroskopi GC-massa (MS) ... 49
5. Spektroskopi massa (MS) ... 49
V. SIMPULAN ... 51
A. Simpulan ... 51
I. PENDAHULUAN
A. Latar Belakang
Keragaman jenis tumbuhan menjadi salah satu sumber senyawa organik yang
dapat dimanfaatkan dalam kehidupan, salah satunya digunakan dalam kesehatan.
Dari adanya keragaman jenis tumbuhan dan keragaman jenis senyawa yang
dikandungnya ini, maka sangat diperlukan penelitian-penelitian dalam
pemanfaatannya. Senyawa kimiawi hasil isolasi dari tumbuhan banyak
dimanfaatkan sebagai obat. Di Indonesia spesies tumbuhan yang banyak
dimanfaatkan sebagai obat salah satunya berasal dari famili Tymelaceae yaitu
Phaleria macrocarpa. P. macrocarpa adalah tanaman perdu dari suku
Tymelaceae yang tumbuh subur pada dataran rendah hingga ketinggian 1200
meter di atas permukaan laut (Burkill, 1966).
Pemanfaatan buah tumbuhan mahkota dewa sebagai obat tradisional secara
konvensional telah banyak dilakukan oleh masyarakat untuk mengobati asam urat,
diabetes melitus, hipertensi, dan penyakit ginjal (Wiryowidagdo, 2000).
Phaleria macrocarpa adalah sumber bagi senyawa-senyawa kimia yang berguna,
termasuk senyawa medisinal yang bersifat anti-hipertensi, anti-bakteri, dan
senyawa steroid yang berpotensi sebagai senyawa obat, maka diperlukan
penelitian lebih lanjut dalam rangka untuk mengungkapkan dan menemukan
senyawa-senyawa kimia yang berguna dari tumbuhan mahkota dewa. Tumbuhan
Phaleria macrocarpa dikenal dengan nama mahkota dewa, sudah pernah diteliti
sebelumnya dan diperoleh beberapa senyawa derivat steroid hasil pemurnian
senyawa dari ekstrak etil asetat pada bagian buah memberikan tiga senyawa yaitu:
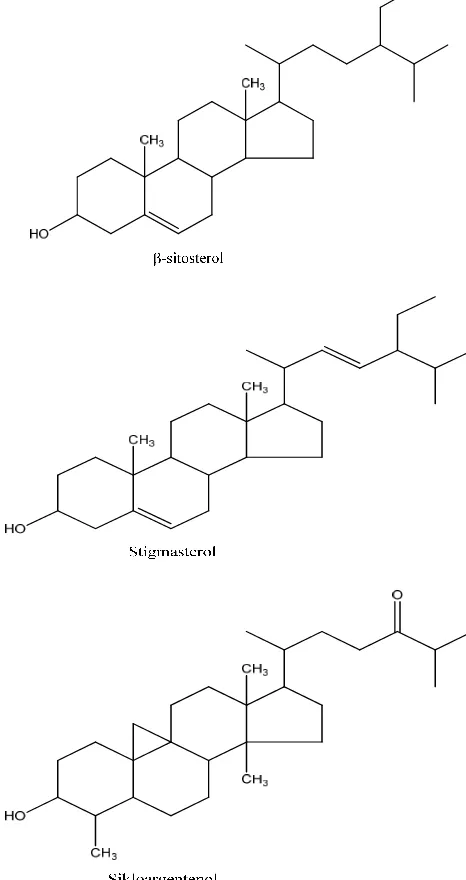
sikloargentenol, -sitosterol, dan stigmasterol (Simanjuntak et al., 2005).
Jumlah kandungan senyawa metabolit sekunder dalam tumbuhan terdistribusi
pada berbagai bagian tumbuhan, dan dalam masing-masing bagian itu mempunyai
jenis dan kuantitas senyawa yang relatif tidak sama. Keadaan geologis yang
berbeda dapat mempengaruhi kandungan senyawa dalam suatu tumbuhan
(Lisdawati, 2002). Lingkungan dengan kondisi yang berbeda suhu, ketersediaan
air, energi surya, mutu atmosfer, struktur dan komposisi udara tanah, reaksi tanah
dan organisme mempengaruhi kehidupan dan perkembangan organisme (Nyapka,
1988). Dengan memperhatikan faktor-faktor di atas, maka perbedaan tempat
pengambilan sampel memungkinkan diperolehnya senyawa hasil isolasi yang
akan berbeda pula. Oleh sebab itu, dilakukan penelitian terhadap tumbuhan
mahkota dewa yang tumbuh di daerah Way Halim Bandar Lampung.
Sampel yang digunakan pada penelitian ini adalah buah mahkota dewa. Bagian
buah dipilih karena bagian tumbuhan ini diperkirakan memiliki senyawa hasil
metabolit sekunder yang bervariasi. Hal ini disebabkan karena bagian buah
merupakan bagian yang digunakan oleh tumbuhan untuk berinteraksi dengan
tersebut mendorong tumbuhan untuk memproduksi senyawa metabolit sekunder
agar dapat mempertahankan diri terhadap perubahan lingkungan yang terjadi.
Metode isolasi senyawa steroid dilakukan dengan cara maserasi menggunakan etil
asetat. Pemisahan dilakukan dengan cara kromatografi cair vakum (KCV),
kromatotron, dan kromatografi kolom (KK). Identifikasi kemurnian dilakukan
menggunakan kromatografi lapis tipis (KLT) dan uji titik leleh. Identifikasi
struktur molekul dilakukan dengan menggunakan spektroskopi ultraungu-tampak
(UV-VIS), Fourier Transform Infrared Spectroscopy (FT-IR), spektroskopi
resonansi magnetik nuklir (NMR), spektroskopi GC-massa (MS), dan
spektroskopi massa (MS).
B. Tujuan Penelitian
Tujuan penelitian ini adalah
1. Mengisolasi senyawa steroid dari buah mahkota dewa dari daerah Way Halim
Kecamatan Kedaton Kelurahan Labuhan Ratu Bandar Lampung.
2. Menentukan struktur molekul senyawa steroid hasil isolasi.
C. Manfaat Penelitian
Penelitian ini diharapkan dapat memberikan informasi mengenai penemuan
senyawa baru hasil isolasi senyawa steroid dari buah mahkota dewa (Phaleria
macrocarpa), dalam rangka penggalian dan pengembangan potensi sumber daya
alam Provinsi Lampung sebagai penghasil senyawa-senyawa berkhasiat sebagai
II. TINJAUAN PUSTAKA
A. Tymelaceae
Tumbuhan yang masuk pada famili Tymelaceae merupakan tanaman perdu
bercabang banyak dengan tinggi 1,5 sampai dengan 2,5 m (Harmanto, 2003).
Famili ini dikenal sebagai sumber utama senyawa fenolat turunan flavonoid,
aril-benzofuran, stilbenoid dan santon turunan flavonoid, terdiri dari 40 genus dan
tidak kurang dari 3000 spesies, dari sejumlah senyawa yang dihasilkan
mempunyai aktivitas biologi, sebagai promotor tumor, bakteri,
anti-kanker dan lain-lain (Achmad et al., 1986).
B. Mahkota Dewa (Phaleria macrocarpa)
Tumbuhan mahkota dewa ini umumnya berupa pohon perdu. Tajuk pohon
bercabang-cabang, ketinggian pohonnya sekitar 1,5 – 2,5 m. Namun, jika
dibiarkan bisa mencapai 5 m. Mahkota dewa bisa sampai berumur puluhan tahun.
Tingkat produktivitasnya mampu dipertahankan sampai usia 10 hingga 20 tahun.
Pohon mahkota dewa terdiri dari akar, batang, daun, bunga dan buah. Akarnya
berupa akar tunggang, panjang akar bisa mencapai 100 cm. Akar ini belum
Kulit dan daging buah
Saat masih muda, kulitnya berwarna hijau. Namun, saat sudah tua warnanya
berubah menjadi merah marun. Ketebalan kulit sekitar 0,1 – 1 mm. Daging buah
berwarna putih. Ketebalan daging bervariasi tergantung pada ukuran buah.
Dalam pengobatan, kulit dan daging buah tidak dipisahkan. Jika dimakan
langsung akan menimbulkan bengkak di mulut, sariawan, mabuk bahkan
keracunan. Pemanfaatan kulit dan daging buah dianjurkan dengan cara
merebusnya terlebih dahulu.
Cangkang buah
Cangkang buah adalah batok pada biji. Jadi, cangkang ini bagian buah yang
paling dekat dengan biji. Cangkang buah berwarna putih, ketebalannya mencapai
2 mm. Rasa cangkang buah juga sepet-sepet pahit, tetapi lebih pahit daripada
kulit dan daging. Pemanfaatannya juga dianjurkan dengan cara merebusnya.
Cangkang ini lebih berkhasiat dibandingkan dengan kulit dan daging buah.
Biji
Seperti bentuk buah, biji juga bulat, warnanya putih dan diameternya mencapai 2
cm. Biji ini sangat beracun, jika tergigit akan menyebabkan lidah kaku, mati rasa
dan meriang. Oleh karena itu biji hanya digunakan untuk obat luar yaitu sebagai
obat oles. Pemanfaatan biji dilakukan dengan cara mengeringkan dan
Dalam taksonomi, tumbuhan ini diklasifikasikan sebagai berikut :
Divisi : Spermathophyta
Sub divisi : Angiospermae
Kelas : Dicotyledoneae
Bangsa : Thymelaeales
Suku : Thymelaeaceae
Marga : Phaleria
Spesies : Phaleria macrocarpa
(Sumber : Winarto, 2003).
Gambar 1. Buah mahkota dewa (Harmanto, 2001).
1. Kandungan Kimia Mahkota Dewa
Di dalam kulit buah mahkota dewa terkandung senyawa alkaloid, saponin,
flavonoid, dan ekstrak kloroformnya juga ditemukan senyawa terpenoid (Gotawa
dkk., 1999). Buah mahkota dewa dilaporkan mengandung anti-histamin
Sedangkan daging buah dan cangkang biji mengandung zat-zat aktif seperti :
Alkaloid : berfungsi sebagai detoksifikasi yang dapat menetralisir
racun-racun di dalam tubuh.
Saponin : – Menjadi sumber anti-bakteri dan anti-virus
– Meningkatkan sistem kekebalan tubuh
– Meningkatkan vitalitas
– Mengurangi kadar gula dalam darah
– Mengurangi penggumpalan darah
Flavanoid : – Melancarkan peredaran darah ke seluruh tubuh dan mencegah
terjadinya penyumbatan pada pembuluh darah.
– Mengurangi kandungan kolesterol serta mengurangi
penimbunan lemak pada dinding pembuluh.
– Mengurangi kadar resiko penyakit jantung koroner.
– Mengandung anti-inflamasi (anti-radang)
• Steroid : Meningkatkan metabolisme hormonal tubuh
Polifenol : Berfungsi sebagai anti-histamin
(Sumber : Lisdawati, 2002).
2. Manfaat Mahkota Dewa
Batang tanaman mahkota dewa yang bergetah digunakan untuk mengobati
penyakit kanker tulang, sehingga mungkin hanya akar dan bunganya saja yang
jarang dipergunakan sebagai obat (Harmanto, 2001). Berdasarkan sejumlah
pengalaman eksperimen, terbukti bahwa sebagian besar tanaman yang memiliki
anti-kanker karena toksisitas yang dimilikinya tersebut dapat bekerja terhadap fase
tertentu dari siklus sel tumor (Lisdawati, 2002). Zat penangkal alergi seperti
biduran, gatal-gatal, dan sesak nafas. Mahkota dewa juga dapat berperan sebagai
oksitoksin yang dapat memacu kerja otot rahim sehingga persalinan berlangsung
lancar (Sumastuti, 2002). Golongan senyawa dalam tanaman yang berkaitan
dengan aktivitas anti-kanker dan anti-oksidan antara lain adalah golongan
alkaloid, steroid, terpenoid, polifenol, dan flavonoid (Wiryowidagdo, 2000).
C. Senyawa Steroid
Steroid adalah sebuah kelas tanaman metabolit sekunder. Steroid merupakan
senyawa organik lemak sterol tidak terhidrolisis yang merupakan hasil reaksi dari
turunan terpena atau skualena (Hanani et al., 2005).
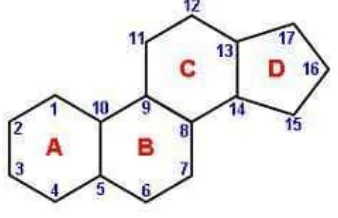
Steroid mempunyai kerangka dasar triterpena asiklik. Ciri umum steroid ialah
sistem empat cincin yang tergabung. Cincin A, B dan C beranggotakan enam
atom karbon, dan cincin D beranggotakan lima. Perhatikan Gambar 2.
L k d p d h s f P b i d s k d u Lemak stero kerangka kol dengan mini
penting di da
disebut zoos
hormon stero
stigmasterol
fungi yang b
Pada tanama
bentuk utam
itu terdapat p
dan metil ste
sangatlah ren
kampesterol.
dibandingka
untuk dapat
rol (bahasa Yu
kolestana yang
inimal 8 atom
dalam steroid
osterol. Jenis
eroid. Sedang
ol. Ergosterol
berfungsi lay
an terdapat le
ma fitosterol,
t pula sitoasta
sterol. Tingka
rendah, yaitu s
ol. Selain itu,
kan kolesterol,
at memenuhi k
Yunani: stereo
ng mengandun
karbon yang
id. Lemak ste
is zoosterol ya
ngkan pada fit
rol adalah lema
ayaknya koles
Gambar
t lebih dari 40
, yaitu: -sito
tanol yang me
kat absorbsi fi
u sekitar 5-10%
u, fitosterol ju
ol, sehingga ju
i kebutuhan tu
eos, padat) ad
ung gugus hid
ng terikat. Le
sterol nabati di
yang penting a
fitosterol diken
mak sterol yan
lesterol pada h
ar 3. Struktur
0 senyawa ste
itosterol, kamp
merupakan kom
fitosterol dari
0% untuk -si
juga lebih cep
jumlah konsu
tubuh (Yuk et
adalah steroid
idroksil-3 da
Lemak sterol m
disebut fitoste
g antara lain a
kenal kampest
ang ditemuka
hewan (Atun,
ur sterol
sterol yang did
mpesterol, dan
omponen cam
ari jumlah yan
sitosterol dan
epat dielimina
umsi fitostero
et al., 2007).
tak jenuh de
dan rantai sisi
l merupakan k
sterol dan yan
adalah kolest
sterol, sitoster
kan pada mem
n, 2005).
idominasi ole
an stigmastero
ampuran kamp
ang dikonsum
an 15% untuk
nasi dari dalam
erol dianjurkan dengan isi alifatik kelompok ang hewani sterol dan terol dan mbran sel leh tiga
rol. Selain
mpesterol
msi
k
lam tubuh
Perlu diketahui bahwa senyawa -sitosterol mampu menghambat kerja enzim
yang mengkonversi testosteron menjadi dehidrotestosteron (DHT) yang
merupakan penyebab terjadinya kanker prostat (Salempa et al., 2009).
-sitosterol merupakan senyawa yang efektif digunakan dalam penyembuhan
penyakit asma, sehingga memungkinkan senyawa ini untuk dikembangkan
sebagai obat terapi penyakit alergi (Yuk et al., 2007).
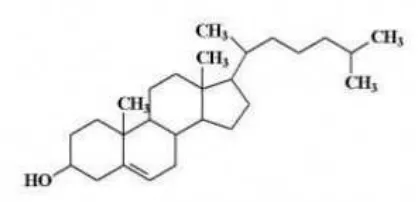
Senyawa yang termasuk turunan steroid, misalnya kolesterol, ergosterol,
progesteron, dan estrogen. Kolestrol memiliki struktur dasar inti steroid yang
mengandung gugus metil, gugus hidroksi yang terikat pada cincin pertama, dan
rantai alkil. Kolestrol merupakan steroid yang terbanyak di dalam tubuh manusia.
Kandungan kolestrol dalam darah berkisar 200-220 mg/dL, meningkatnya kadar
kolestrol dalam darah dapat menyempitkan pembuluh darah di jantung, sehingga
terjadi gangguan jantung koroner. Pengobatan yang sering dilakukan adalah
melebarkan pembuluh darah seperti, memasang ring atau melakukan operasi.
Kolestrol dalam tubuh dibentuk di dalam liver dari makanan. Struktur kolestrol
dapat dilihat pada Gambar 4.
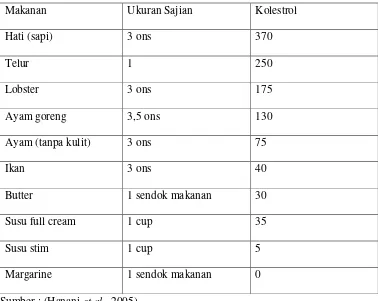
Kolestrol dalam makanan yang perlu kita waspadai mengingat tren penyakit
jantung cukup tinggi di Indonesia. Beberapa makanan yang banyak mengandung
kolestrol disajikan dalam Tabel 1.
Tabel 1. Sumber makanan dan ukuran sajian serta kandungan kolestrolnya.
Makanan Ukuran Sajian Kolestrol
Hati (sapi) 3 ons 370
Telur 1 250
Lobster 3 ons 175
Ayam goreng 3,5 ons 130
Ayam (tanpa kulit) 3 ons 75
Ikan 3 ons 40
Butter 1 sendok makanan 30
Susu full cream 1 cup 35
Susu stim 1 cup 5
Margarine 1 sendok makanan 0
Sumber : (Hanani et al., 2005).
Garam empedu merupakan hasil sintesis kolestrol dan disimpan dalam bladder,
peran senyawa ini adalah untuk mengemulsikan asam lemak dan minyak sehingga
memperluas permukaan lipida yang akan dibongkar secara enzimatik. Struktur
Gambar 5. Struktur molekul garam empedu (Hanani et al., 2005).
1. Manfaat Steroid
Steroid terdistribusi secara luas dalam tanaman dan memiliki berbagai fungsi.
Pada umunya steroid berfungsi sebagai hormon (Hanani et al., 2005).
Secara rinci beberapa fungsi steroid adalah sebagai berikut :
- Meningkatkan laju perpanjangan sel tumbuhan
- Menghambat penuaan daun (senescence)
- Mengakibatkan lengkuk pada daun rumput-rumputan
- Menghambat proses gugurnya daun
- Menghambat pertumbuhan akar tumbuhan
- Meningkatkan resistensi pucuk tumbuhan kepada stress lingkungan
- Menstimulasi perpanjangan sel di pucuk tumbuhan
- Merangsang pertumbuhan pucuk tumbuhan
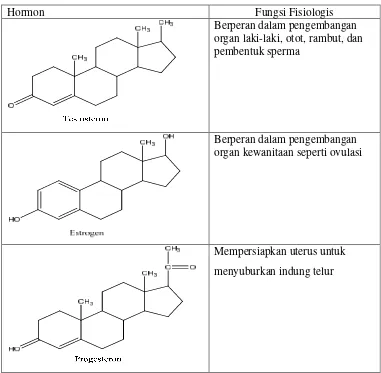
Contoh jenis hormon steroid pada manusia adalah hormon seks bagi kaum
laki-laki dan perempuan seperti testosteron, estradiol dan progesteron. Struktur
molekul dan fungsinya dapat dilihat dalam Tabel 2.
Tabel 2. Jenis hormon dan fungsi fisiologisnya.
Hormon Fungsi Fisiologis
Berperan dalam pengembangan organ laki-laki, otot, rambut, dan pembentuk sperma
Berperan dalam pengembangan organ kewanitaan seperti ovulasi
Mempersiapkan uterus untuk
menyuburkan indung telur
Sumber : (Hanani et al., 2005).
2. Ekstraksi dan Isolasi Steroid
Ekstraksi dilakukan menggunakan metode maserasi. Maserasi merupakan proses
perendaman sampel dengan pelarut organik yang digunakan pada temperatur
karena dengan perendaman sampel tumbuhan akan terjadi pemecahan dinding dan
membran sel akibat perbedaan tekanan antara di dalam dan di luar sel sehingga
senyawa metabolit sekunder yang ada dalam sitoplasma akan terlarut dalam
pelarut organik dan ekstrasi senyawa akan sempurna karena dapat diatur lama
perendaman yang dilakukan (Lenny, 2006). Proses ini dilakukan beberapa kali
dan ekstrak kemudian disatukan lalu diuapkan dengan menggunakan
penguap-putar vakum (Markham, 1988). Setelah dilakukan proses ekstraksi, tahap isolasi
selanjutnya adalah analisis senyawa dengan menggunakan beberapa jenis
kromatografi.
Hasil isolasi dari buah mahkota dewa mengandung senyawa lignan C19H20O6:
5-[4(4-metoksi-fenil)-tetrahidrofuro[3,4-c]furan-1-il]-benzena-1,2,3-triol. Struktur
molekulnya seperti ditunjukkan pada Gambar 6.
Hasil isolasi dan pemurnian senyawa ekstrak etil asetat dari buah mahkota dewa
memberikan tiga senyawa yaitu: -sitosterol, stigmasterol, dan sikloargentenol.
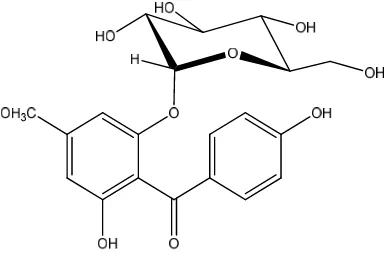
Hasil isolasi dan identifikasi dari ekstrak n-butanol buah mahkota dewa yang
mempunyai daya aktivitas sebagai senyawa anti-oksidan yaitu senyawa
6,4’-dihidroksi-4-metoksibenzofenon-2-O- -D-glukopiranosida.
Gambar 8. Struktur molekul senyawa 6,4’-dihidroksi-4-metoksibenzofenon-2-O- -D-glukopiranosida (Hartati et al., 2005).
D. Pemisahan Senyawa secara Kromatografi
Kromatografi merupakan pemisahan suatu senyawa yang didasarkan atas
perbedaan laju perpindahan dari komponen-komponen dalam campuran.
Pemisahan dengan metode kromatografi dilakukan dengan cara memanfaatkan
sifat-sifat fisik dari sampel, seperti kelarutan, adsorbsi, keatsirian dan kepolaran.
Kelarutan merupakan kecenderungan molekul untuk melarut dalam cairan.
Adsorpsi penjerapan adalah kecenderungan molekul untuk melekat pada
permukaan serbuk halus (Johnson dan Stevenson, 1991).
Berdasarkan jenis fasa diam dan fasa gerak yang dipartisi, kromatografi dapat
Tabel 3. Penggolongan kromatografi berdasarkan fasa diam dan fasa gerak.
Fasa Diam Fasa Gerak Sistem kromatogafi
Padat
Padat
Cair
Cair
Cair
Gas
Cair
Gas
Cair- adsorbsi
Gas-adsorbsi
Cair-partisi
Gas-partisi
Sumber : Johnson dan Stevenson (1991).
1. Kromatografi Lapis Tipis (KLT)
Kromatografi Lapis Tipis ialah metode pemisahan fisikokimia yang terdiri atas
bahan berbutir-butir (fase diam), ditempatkan pada penyangga berupa pelat gelas,
logam, atau lapisan yang cocok. Campuran yang akan dipisah, berupa larutan,
ditotolkan berupa bercak atau pita. Setelah pelat atau lapisan diletakkan di dalam
bejana tertutup rapat yang berisi larutan pengembang yang cocok (fase gerak),
pemisahan terjadi selama perambatan kapiler (pengembangan). Selanjutnya,
senyawa yang tidak berwarna harus ditampakkan (dideteksi) (Stahl, 1985).
Kromatogarafi Lapis Tipis merupakan cara analisis cepat yang memerlukan bahan
yang sedikit. Untuk peneliti pendahuluan kandungan flavonoid suatu ekstrak,
sudah menjadi kebiasaan umum untuk menggunakan pengembang beralkohol
pada pengembangan pertama dengan kromatografi lapis tipis, misalnya
butanol-asam asetat-air (Markham, 1988).
Kromatografi Lapis Tipis digunakan untuk memisahkan senyawa-senyawa
yang sifatnya hidrofob seperti lipida-lipida dan hidrokarbon. Sebagai fase diam
biasa diberi pengikat yang dimaksudkan untuk memberikan kekuatan pada lapisan
dan menambah adesi pada gelas penyokong. Pengikat yang biasa digunakan
adalah kalsium sulfat (Sastrohamidjojo, 2002).
Metode dalam KLT dapat dihitung nilai Retention factor (Rf) dengan persamaan :
Tetapi pada gugus-gugus yang besar dari senyawa-senyawa yang susunannya
mirip, sering kali harga Rf berdekatan satu sama lainnya (Sastrohamidjojo, 2002).
2. Kromatogafi Kolom (KK)
Pada prinsipnya Kromatografi Kolom (KK) digunakan untuk pemisahan
campuran beberapa senyawa yang diperoleh dari isolasi tumbuhan. Dengan
menggunakan fase padat dan fasa cair maka fraksi-fraksi senyawa akan
menghasilkan kemurnian yang cukup tinggi.
Teknik KK pada dasarnya sama dengan KCV, yaitu merupakan kromatografi
cair-adsorpsi, hanya saja KK dilakukan pada sistem yang bekerja pada kondisi normal
tanpa vakum. Waktu yang dibutuhkan dalam pelaksanaannya lebih lama, namun
diharapkan akan mendapat hasil dengan pemisahan yang lebih baik dan lebih
3.Kromatografi Cair Vakum (KCV)
Teknik KCV dilakukan dengan suatu sistem yang bekerja pada kondisi vakum
secara terus-menerus sehingga diperoleh kerapatan kemasan yang maksimum atau
menggunakan tekanan rendah untuk meningkatkan laju alir fasa gerak. Urutan
eluen yang digunakan dalam kromatografi cair diawali dari eluen yang
mempunyai tingkat kepolaran rendah kemudian kepolarannya ditingkatkan secara
perlahan-lahan. Urutan eluen yang digunakan dalam kromatografi diawali dari
eluen yang mempunyai tingkat kepolaran rendah kemudian kepolarannya
ditingkatkan secara perlahan-lahan (Hosstetmann et al., 1995).
Berikut ini merupakan urutan eluen pada kromatografi berdasarkan kenaikan
tingkat kepolarannya :
n-heksana Non polar Sikloheksana
Karbon tetraklorida Benzena
Toluena
Metilen klorida Kloroform Etil asetat Aseton
n-propanol Etanol Asetonitril
Metanol
Air Polar
(Sumber: Gritter dkk., 1991).
4. Kromatotron
Kromatografi digunakan pada beberapa teknik pemisahan berdasarkan pada
fase gerak. Terdapat 3 hal yang wajib ada pada teknik ini, yang pertama yaitu
harus terdapat medium perpindahan tempat, yaitu tempat terjadinya pemisahan.
Kedua harus terdapat gaya dorong agar spesies dapat berpisah sepanjang
“migration medium“. Ketiga harus terdapat gaya tolakan selektif. Gaya yang
terakhir ini dapat menyebabkan pemisahan dari bahan kimia yang
dipertimbangkan (Sienko et al., 1984).
Kromatografi Lapis Tipis merupakan teknik pemisahan cara lama yang digunakan
secara luas, terutama dalam analisis campuran yang rumit dari sumber alam.
Tetapi dalam kuantisasi belakangan ini kromatografi lapis tipis digantikan oleh
“HPLC” (High Performance Thin-layer Chromatography) atau Kromatografi
Lapis Tipis Kinerja Tinggi (Munson, 1991).
Kromatotron memiliki prinsip sama seperti kromatografi klasik dengan aliran fase
gerak yang dipercepatoleh gayasentrifugal. Kromatografi jenis ini menggunakan
rotor yang dimiringkan dan terdapat dalam ruang tertutup oleh plat kaca kuarsa,
sedangkan lapisan penyerapnya berupa plat kaca yang dilapisi oleh silika gel. Plat
tersebut dipasang pada motor listrik dan diputar dengan kecepatan 800 rpm.
Pelarut pengelusi dimasukkan kebagian tengah pelarut melalui pompa torak
sehingga dapat mengalir dan merambat melalui lapis tipis karena gaya sentrifugal.
Untuk mengetahui jalannya proses elusi dimonitor dengan lampu UV. Gas
nitrogen dialirkan kedalam ruang plat untuk mencegah pengembunan pelarut
pengelusi dan mencegah oksidasi sampel. Pemasukan sampel itu diikuti dengan
tepi plat, pita-pita akan terputar keluar dengan gaya sentrifugal dan di tampung
dalam botol fraksi, diidentifikasi dengan KLT (Hostettmann et al., 1995).
5. Analisis Kemurnian
Analisis kemurnian senyawa hasil isolasi dilakukan dengan kromatografi lapis
tipis (KLT) dan uji titik leleh. KLT dilakukan dengan mengelusi larutan sampel
yang ditotolkan pada lempeng silika gel60 F254 dengan fase gerak berupa eluen
etil asetat-heksana (4 : 6). Bercak yang ada diamati dengan sinar tampak, UV 254
nm dan UV 366 nm kemurnian senyawa ditetapkan secara semi kuantitatif dengan
densitometer pada maks = 347 nm (Margono dan Zendrato, 2006). Senyawa
hasil analisis dikatakan murni apabila memberikan noda tunggal pada KLT
dengan berbagai fase gerak (Setyowati et al., 2007).
Sedangkan titik leleh merupakan ciri penting senyawa organik padat. Titik leleh
memiliki arti penting dalam identifikasi dan pengukuran kemurnian. Penggunaan
untuk identifikasi didasarkan pada fakta bahwa semua senyawa murni mempunyai
titik leleh yang tajam ketika berubah sempurna dari padat ke cair. Selain itu,
penggunaan titik leleh untuk identifikasi juga didasarkan pada fakta bahwa
senyawa yang tidak murni menunjukkan 2 fenomena, pertama yaitu suhu leleh
yang lebih rendah, dan kedua memiliki jarak leleh yang lebih lebar. Alat yang
digunakan untuk menguji titik leleh suatu senyawa adalah termopan. Untuk
identifikasi kualitatif, titik leleh merupakan tetapan fisika yang penting terutama
untuk suatu senyawa hasil sintesis, isolasi, maupun kristalisasi. Titik leleh suatu
tekanan udara 1 atm. Jika suhu dinaikkan, molekul senyawa akan menyerap
energi. Semakin tinggi suhu maka akan semakin banyak energi yang diserap
sehingga akan menaikkan gerakkan vibrasi dan rotasi molekul (Hadiprabowo,
2009).
E. Penentuan Struktur Senyawa Organik
Suatu senyawa bahan alam hasil isolasi akan diidentifikasi berdasarkan sifat
fisika, sifat kimia dan identifikasi dengan spektroskopi (Achmad et al., 2006).
1. Identifikasi Senyawa Organik Secara Spektroskopi
Spektroskopi merupakan ilmu yang mempelajari tentang cara menganalisis
spektrum suatu senyawa dan interaksi antara radiasi elektromagnetik. Teknik
spektroskopi dapat digunakan untuk menentukan struktur dari senyawa organik
tersebut (Fessenden dan Fessenden, 1999). Metode spektroskopi yang dipakai
pada penelitian ini antara lain, Fourier Transform Infrared Spectroscopy (FTIR),
spektroskopi ultraungu-tampak (UV-VIS), spektroskopi resonansi magnetik nuklir
(NMR), spektroskopi GC-massa (MS), dan spektroskopi massa (MS).
1.1 Fourier Transform Infrared Spectroscopy (FT-IR)
Pada spektroskopi inframerah (IR), senyawa organik akan menyerap berbagai
frekuensi radiasi elektromagnetik inframerah. Molekul-molekul senyawa akan
menyerap sebagian atau seluruh radiasinya. Penyerapan ini berhubungan dengan
kovalen pada molekul-molekul itu. Penyerapan ini juga berhubungan dengan
adanya perubahan momen dipol dari ikatan kovalen pada waktu terjadinya vibrasi
(Supriyanto, 1999). Pada dasarnya spektrofotometer FT-IR (Fourier Trasform
Infra Red) adalah sama dengan spektrofotometer IR dispersi, yang
membedakannya adalah pengembangan pada sistim optiknya sebelum berkas
sinar infra merah melewati contoh. Pada sistem optik FT-IR digunakan radiasi
LASER (Light Amplification by Stimulated Emmission of Radiation) yang
berfungsi sebagai radiasi yang diinterferensikan dengan radiasi infra merah agar
sinyal radiasi infra merah yang diterima oleh detektor secara utuh dan lebih baik.
[image:31.612.135.492.375.701.2]Karakteristik frekuensi uluran beberapa gugus molekul ditunjukkan pada Tabel 4.
Tabel 4. Karakteristik frekuensi uluran beberapa gugus fungsi.
Gugus Serapan (cm-1) Gugus Serapan(cm-1)
OH 3600
CH2
2930
2860
1470
NH2 3400
CH 3300
H
Ar 3060 C O 1200-1000
CH 2
3030
2870
1460
1375
C C 1650
C N 1600
C N 1200-1000 C C 1200-1000
C O 1750-1600
Daerah panjang gelombang yang digunakan pada alat spektroskopi inframerah
adalah pada daerah inframerah pertengahan, yaitu pada panjang gelombang 2,5 –
50 µm atau pada bilangan gelombang 4.000 – 200 cm-1 . Daerah tersebut adalah
cocok untuk perubahan energi vibrasi dalam molekul. Daerah inframerah yang
jauh (400-10 cm-1), berguna untuk molekul yang mengandung atom berat, seperti
senyawa anorganik tetapi lebih memerlukan teknik khusus percobaan (Silverstein,
1986).
Penggunaan spektrum inframerah dalam menentukan struktur senyawa organik
berada antara 650-4000 cm-1. Daerah di bawah frekuensi 650 cm -1 dinamakan
daerah infra merah jauh dan daerah di atas frekuensi 4000 cm -1 dinamakan infra
merah dekat (Sudjadi, 1983). Daerah antara 1400-4000 cm -1 merupakan daerah
khusus yang berguna untuk identifikasi gugus fungsional. Daerah ini
menunjukkan absorpsi yang disebabkan oleh vibrasi uluran. Daerah antara
1400-700 cm -1 (daerah sidik jari) seringkali sangat rumit karena menunjukkan absorpsi
yang disebabkan oleh vibrasi uluran dan tekukan (Fessenden dan Fessenden,
1999).
1.2 Spektroskopi Ultraungu-Tampak (UV-VIS)
Dalam spektoskopi UV-VIS penyerapan sinar tampak dan ultraviolet oleh suatu
molekul akan menghasilkan transisi di antara tingkat energi elektronik molekul
tersebut. Transisi tersebut pada umumnya antara orbital ikatan, orbital non-ikatan
atau orbital anti-ikatan. Panjang gelombang serapan yang muncul merupakan
ukuran perbedaan tingkat-tingkat energi dari orbital suatu molekul (Sudjadi,
1.3 Spektroskopi Resonansi Magnetik Nuklir (NMR)
Analisis spektroskopi NMR akan memberikan informasi tentang posisi atom-atom
karbon yang memiliki proton atau yang tidak memiliki proton. Selain itu juga
untuk mengenali atom-atom lainnya yang berkaitan dengan proton. Spektroskopi
NMR juga dapat memberikan informasi tentang jumlah dan jenis atom karbon
yang ada pada struktur senyawa organik. Teknik spektroskopi ini didasarkan pada
penyerapan gelombang radio elektromagnetik oleh inti atom hidrogen atau karbon
(Silverstein et al., 1986). Letak pergeseran kimia untuk proton pada beberapa
[image:33.612.164.475.352.697.2]molekul organik dapat dilihat pada Tabel 5.
Tabel 5. Letak pergeseran kimia untuk proton dalam molekul organik.
Jenis Senyawa JenisProton 1H ( ) ppm
Alkana Alkuna Eter Alkena Fenol Alkohol Aromatik Aldehid Karboksilat
C CH3
C C H
H3C O
H2C C
Ar OH
R OH
Ar H
O
C H
O
C OH
0,5 – 2
2,5 - 3,5
3,5 - 3,8
4,5 - 7,5
4 - 8
5 - 5,5
6 - 9
9,8 - 10,5
11,5 - 12,5
1.4. Spektroskopi GC-Massa (MS)
GC-MS merupakan metode pemisahan senyawa organik yang menggunakan dua
metode analisis senyawa yaitu kromatografi gas (GC) untuk menganalisis jumlah
senyawa secara kuantitatif dan spektrometri massa (MS) untuk menganalisis
struktur molekul senyawa analit (Fowlis, 1998).
Gas kromatografi merupakan salah satu teknik spektroskopi yang menggunakan
prinsip pemisahan campuran berdasarkan perbedaan kecepatan migrasi
komponen-komponen penyusunnya. Gas kromatografi biasa digunakan untuk
mengidentifikasi suatu senyawa yang terdapat pada campuran gas dan juga
menentukan konsentrasi suatu senyawa dalam fase gas (Fowlis, 1998).
1.5. Spektroskopi Massa (MS)
Spektroskopi massa (MS) akan melengkapi pelacakan struktur untuk suatu
molekul yang belum diketahui berat molekulnya (g/mol) dan bagaimana pola
pemecahan (fragmentasi) dari suatu molekul organik. Rekonstruksi terhadap
pemecahan dan dipandu dengan interpretasi data spektra FT-IR dan H1-NMR
akan dapat mengelusidasi struktur molekul organik yang belum diketahui (Sitorus,
2009).
Analisis spektroskopi massa berfungsi untuk menghasilkan berkas sinar kation
dari zat, berkas kation menjadi bentuk spektrum massa (m/z), mendeteksi dan
mencatat nilai massa relatif (m/z) atau menentukan bobot molekul suatu senyawa
III. METODOLOGI PENELITIAN
A. Waktu dan Tempat Penelitian
Penelitian ini akan dilakukan pada bulan Agustus 2012 -April 2013, bertempat di
Laboratorium Kimia Organik Jurusan Kimia Fakultas MIPA Universitas
Lampung. Analisis spektroskopi yang digunakan adalah spektroskopi
ultraungu-tampak (UV-Vis), Fourier Trasform Infra Red (FT-IR) dilakukan di Laboratorium
Biomassa, spektroskopi resonansi magnetik nuklir (NMR) di Laboratorium
NMR-LIPI Serpong, spektroskopi GC-massa (MS) dan spektroskopi massa (MS) di
Laboratorium Kimia Organik Jurusan Kimia Fakultas MIPA Universitas Gajah
Mada, Yogyakarta.
B. Alat dan Bahan
1. Alat-alat yang digunakan
Alat-alat yang digunakan dalam penelitian ini meliputi alat-alat gelas, penguap
putar vakum, satu set alat kromatografi cair vakum (KCV), kromatotron, satu set
alat kromatografi kolom (KK), pengukur titik leleh, lampu UV, pipet kapiler,
penguap putar vakum, spektrofotometer FT-IR merk Scimitar 2000,
NMR, spektrofotometer GC-massa (MS) merk Shimadzu QP-2010, dan
spektofotometer massa (MS) merk Shimadzu QP-2010.
2. Bahan-bahan yang digunakan
Bahan yang digunakan adalah buah mahkota dewa yang telah dikeringkan dan
dihaluskan, diperoleh dari daerah Way Halim Kecamatan Kedaton Kelurahan
Labuhan Ratu Bandar Lampung. Pelarut yang digunakan untuk ekstraksi dan
kromatografi berkualitas teknis yang telah didestilasi sedangkan untuk analisis
spektrofotometer berkualitas pro-analisis (p.a). Bahan kimia yang dipakai
meliputi etil asetat (EtOAc), metanol (MeOH), n-heksana (n-C6H14), aseton
(C3H6O2), akuades (H2O), serium sulfat 1,5% dalam asam sulfat (H2SO4) 2N,
benzena (C6H6), kloroform (CH3Cl), diklorometana (CH2Cl2), silika gel Merck G
60 untuk impregnasi, silika gel Merck 60 (35-70 Mesh) untuk KCV dan KK,
untuk KLT digunakan plat KLT silika gel Merck kiesegal 60 F254 0,25 mm, silika
gel 60 PF254 untuk plat kromatotron.
C. Prosedur Penelitian
1. Pengumpulan dan Persiapan Sampel
Sampel berupa buah mahkota dewa yang dipisahkan bijinya kemudian buah
dibersihkan dan di potong kecil-kecil. Sampel buah yang telah dipotong kemudian
2. Ekstraksi dengan Etil Asetat
Sebanyak 1500 gram buah mahkota dewa yang telah dihaluskan,dimaserasi 3 kali
dengan menggunakan etil asetat (EtOAc) masing-masing selama 1x24 jam.
Ekstrak etil asetat yang diperoleh disaring kemudian dipekatkan dengan
menggunakan penguap putar vakum pada suhu 45o-50oC dengan laju putaran
120-150 rpm.
3. Kromatografi Cair Vakum (KCV)
Ekstrak kasar kemudian difraksinasi dengan KCV. Terlebih dahulu fasa diam
silika gel halus sebanyak 3 kali berat sampel dimasukkan ke dalam kolom.
Kemudian kolom dikemas kering dalam keadaan vakum menggunakan alat
vakum. Eluen yang kepolarannya rendah, dimasukkan ke permukaan silikagel
halus terlebih dahulu kemudian divakum kembali. Kolom dihisap sampai kering
dengan alat vakum dan siap digunakan.
Ekstrak kasar yang telah dilarutkan dalam aseton dan diimpregnasikan kepada
silika gel kasar, kemudian dimasukkan pada bagian atas kolom yang telah berisi
fasa diam dan kemudian dihisap secara perlahan-lahan ke dalam kemasan dengan
cara memvakumkannya. Setelah itu kolom dielusi dengan etil asetat/n-heksan 0%
sampai dengan etil asetat 100%. Kolom dihisap dengan vakum sampai kering
pada setiap penambahan eluen (tiap kali elusi dilakukan). Kemudian fraksi-fraksi
yang terbentuk dikumpulkan berdasarkan pola fraksinasinya. Fraksinasi sampel
dengan teknik KCV dilakukan berulang kali dengan perlakuan yang sama seperti
4. Kromatografi Lapis Tipis (KLT)
Sebelum difraksinasi, terlebih dahulu dilakukan uji KLT untuk melihat pola
pemisahan komponen-komponen senyawa yang terdapat dalam ekstrak kasar. Uji
KLT juga dilakukan terhadap fraksi yang akan difraksinasi dan juga
fraksi-fraksi yang didapat setelah perlakuan fraksi-fraksinasi. Uji KLT dilakukan
menggunakan sistem campuran eluen menggunakan pelarut n-heksana, etilasetat,
kloroform, benzena, metanol, dan diklorometana. Hasil kromatogram tersebut
kemudian disemprot menggunakan larutan serium sulfat untuk menampakkan
bercak/noda dari komponen senyawa tersebut. Ketika diperoleh fraksi yang lebih
sedikit bercak/noda dilihat dibawah lampu UV setelah dilakukan elusi terhadap
plat KLT. Setiap fraksi yang menghasilkan pola pemisahan dengan Rf (Retention
factor) yang sama pada kromatogram, digabung dan dipekatkan sehingga
diperoleh beberapa fraksi gabungan yang akan difraksinasi lebih lanjut.
5. Kromatotron
Setelah sampel diidentifikasi dengan menggunakan Kromatografi Lapis Tipis
(KLT), kemudian difraksinasi menggunakan kromatotron dengan menggunakan
plat silika 2 mm dan menggunakan eluen diklorometana/n-heksana. Sebelum
digunakan plat silika diaktifkan terlebih dahulu dengan pemanasan lampu pijar
selama 20 jam. Plat silika yang sudah aktif kemudian dipasang pada kromatotron
dan dibasahi perlahan dengan pelarut n-heksana sampai menetes, kemudian
sampel diteteskan perlahan ke dalam plat silika selagi basah. Setelah sampel
Setelah sampel kering, kemudian dialirkan 100 mL n-heksana dilanjutkan dengan
mengalirkan eluen diklorometana/n-heksana 1%, 2%, 3%, 4%, 5%, dan 100%
masing-masing sebanyak 100 mL. Hasil fraksinasi kemudian ditampung dalam
botol-botol kecil berukuran ±10 mL. Setelah selesai fraksinasi, plat silika
kemudian dicuci dengan mengalirkan aseton sebanyak 100 mL dilanjutkan
dengan mengalirkan air-metanol 5% sebanyak 100 mL.
6. Kromatografi Kolom (KK)
Setelah dihasilkan fraksi-fraksi dengan jumlah yang lebih sedikit, tahapan
fraksinasi selanjutnya dilakukan menggunakan teknik kromatografi kolom.
Adsorben silika gel Merck (35-70 Mesh) dilarutkan dalam pelarut yang akan
digunakan dalam proses pengelusian. Slurry dari silika gel dimasukkan terlebih
dahulu ke dalam kolom, atur fasa diam hingga rapat (tidak berongga) dan rata.
Selanjutnya masukkan sampel yang telah diimpregnasi pada silika gel ke dalam
kolom yang telah berisi fasa diam. Pada saat sampel dimasukkan, usahakan agar
kolom tidak kering/kehabisan pelarut karena akan mengganggu fasa diam yang
telah dikemas rapat, sehingga proses elusi tidak akan terganggu.
7. Analisis Kemurnian
Uji kemurnian dilakukan dengan metode KLT dan uji titik leleh. Uji kemurnian
secara KLT menggunakan beberapa campuran eluen. Kemurnian suatu senyawa
ditunjukkan dengan timbulnya satu noda dengan berbagai campuran eluen yang
menampakkan bercak/noda dari komponen senyawa tersebut dan pereaksi
Liebermann-Burchard untuk identifikasi senyawa steroid.
Untuk kristal yang berukuran besar, kristal terlebih dahulu digerus hingga
berbentuk serbuk kemudian kristal yang akan ditentukan titik lelehnya diletakkan
pada lempeng kaca, diambil sedikit dengan menggunakan pipet kapiler, alat
dihidupkan dan titik leleh diamati dengan bantuan kaca pembesar. Suhu pada saat
kristal pertama kali mulai meleleh sampai semua zat meleleh, itulah titik leleh dari
senyawa tersebut.
8. Spektroskopi Ultraungu–tampak (UV-VIS)
Sampel berupa kristal murni sebanyak 0,001 gram dilarutkan dalam 10 mL etil
asetat. Larutan ini digunakan sebagai persediaan untuk beberapa kali pengukuran.
Pertama, sampel diukur serapan maksimumnya dalam etil asetat lalu sampel
kristal tersebut dilarutkan dalam 10 mL etil asetat kemudian larutan diukur
serapan maksimumnya.
9. Fourier Transform Infrared Spectroscopy (FT-IR)
Sampel kristal hasil isolasi yang telah murni dianalisis menggunakan
spektrofotometer inframerah. Kristal yang telah murni dibebaskan dari air
kemudian digerus bersama-sama dengan halida anorganik, KBr. Gerusan kristal
murni dengan KBr dibentuk menjadi lempeng tipis atau pelet dengan bantuan alat
penekan berkekuatan 8-10 ton per satuan luas kemudian pelet tersebut diukur
10. Spektroskopi Resonansi Magnetik Nuklir (NMR)
Sampel berupa kristal murni yang akan diidentifikasi dilarutkan ke dalam pelarut
inert yang tidak mengandung proton seperti CCl4 dan CDCl3, kemudian
ditambahkan sedikit senyawa acuan. Larutan ini ditempatkan dalam tabung gelas
tipis dengan tebal 5 mm di tengah-tengah kumparan frekuensi radio (rf) di antara
dua kutub magnet yang sangat kuat kemudian energi dari kumparan rf ditambah
secara terus-menerus. Energi pada frekuensi terpasang dari kumparan rf yang
diserap cuplikan direkam dan memberikan spektrum NMR (Silverstein et
al.,1986).
11. Spektroskopi GC-Massa (MS)
Spektroskopi GC-MS merupakan jenis kromatografi yang digunakan dalam kimia
organik untuk pemisahan dan analisis. GC dapat digunakan untuk menguji
kemurnian dari bahan tertentu atau memisahkan berbagai komponen dari
campuran. Dalam beberapa situasi, GC dapat membantu dalam mengidentifikasi
sebuah senyawa kompleks. Dalam kromatografi gas, fase yang bergerak atau
mobile phase adalah sebuah operator gas yang biasanya gas murni seperti helium
atau yang tidak reactive seperti gas nitrogen. Stationary atau fasa diam
merupakan tahap mikroskopis lapisan cair atau polimer yang mendukung gas
murni di dalam bagian dari sistem pipa-pipa kaca atau logam yang disebut kolom.
Instrumen yang digunakan untuk melakukan kromatografi gas disebut gas
12. Spektroskopi Massa (MS)
Sampel diuapkan di bawah vakum dan diionkan menggunakan berkas elektron.
Ion sampel dipercepat menggunakan medan listrik memasuki tabung penganalisis
dan dilalukan dalam medan magnet. Dalam kekuatan medan magnet yang
diberikan, hanya ion-ion positif dan radikal positif akan difokuskan ke detektor,
sedang ion-ion yang lain (radikal netral) akan dibelokkan ke dinding tabung. Ion
dengan m/z lebih besar akan mencapai detektor lebih dulu diikuti m/z yang lebih
kecil. Arus listrik yang diterima detektor akan diperkuat dan spektrum massa dari
49
V. SIMPULAN DAN SARAN
A. Simpulan
Berdasarkan pembahasan hasil penelitian yang telah dilakukan, maka diperoleh simpulan sebagai berikut:
1. Pada penelitian ini telah berhasil diisolasi dan diidentifikasi senyawa steroid dari buah mahkota dewa (Phaleria macrocarpa).
2. Senyawa steroid yang didapatkan memiliki sifat fisik berupa padatan berwarna putih dengan titik leleh 135o-137oC.
3. Senyawa steroid yang dikenal dengan nama stigmast-5-en-3 -ol ( -sitosterol) sebanyak 10 mg.
B. Saran
1. Penelitian lebih lanjut terhadap sampel buah mahkota dewa perlu dilakukan sehingga memperoleh informasi lebih tentang jenis senyawa steroid yang terkandung.
2. Penggunaan pelarut yang berbeda pada saat maserasi atau partisi sehingga diharapkan memperoleh senyawa steroid dari jenis yang berbeda.
DAFTAR PUSTAKA
Achmad, S.A. 1986. Kimia Organik Bahan Alam, Materi 4: Ilmu Kimia Flavonoid. Karunia Universitas Terbuka. Jakarta. Hlm 39.
Achmad, S.A., E.H. Hakim, L.J. Dewi, L. Makmur, dan Y.A. Maolana. 2006. Hakekat Perkembangan kimia Organik Bahan Alam Dari Tradisional ke Moderen dan Contoh terkait Dengan Tumbuhan Lauraceae, Moraceae, dan Dipterocarpaceae Indonesia.Akta Kimindo. 1 (2). Hlm 55-66.
Atun, S. 2005. Pengembagan Potensi Bahan Alam sebagai Sumber Penemuan Obat Baru, Makalah disajikan dalam Seminar Nasional Kimia. Universitas Negeri Yogyakarta.
Banwell, C.N. and E.M. McCash. 1994. Fundamental of Molecular Spectroscopy. Mc Graw-Hill Book Company. London.
Burkill, I.H. 1966. A Dictionary of the Economic Products of the Malay Penninsula. Vol II. Ministry of Agriculture and Co-operatives. Kuala Lumpur. Hlm 1732.
Ersam, T. 2004. Keunggulan Biodiversitas Hutan Tropika Indonesia Dalam Merekayasa Model Molekul Alami. Prosiding Seminar Nasional Kimia VI. ITS. Surabaya. Hlm 4-12.
Fessenden, R.J. dan J. S. Fessenden. 1999. Kimia Organik Jilid I. Alih Bahasa Hadyana Pujaatmaka. Erlangga. Jakarta. Hlm 525.
Fowlis, Ian A.,1998. Gas Chromatography Analytical Chemistry by Open Learning. John Wiley & Sons Ltd: Chichester.
Gotawa, I. B. I. , Sugiarto, S. , Nurhadi, M. , Widiyastuti, Y. Wahyono, S. , Prapti, I. J. 1999. Inventaris Tanaman Obat Indonesia. Jilid V. Departemen Kes. Badan Penelitian dan Pengembangan Kesehatan. Jakarta. Hal. 147-148.
Hadiprabowo, T. 2009. Optimasi Sintesis Analog Kurkumarin 1,3-Bis- (4-Hidroksi-3-Metoksi Benzilidin) Urea pada Rentang pH 3-4. (Skripsi). Universitas Muhammadiyah Surakarta. Surakarta. Hlm 10-11.
Hanani, E, Mun’im A, Sekarini, R. 2005. Identifikasi Senyawa Antioksidan Dalam Spons Callyspongia Sp. Dari Kepulauan Seribu. Majalah Ilmu Kefarmasian, vol. II, No.3. Departemen Farmasi, FMIPA-UI,
Kampus UI Depok. Hlm 127-133.
Harmanto, N. 2001. Mahkota Dewa: Obat Pusaka Para Dewa. Agromedia Pustaka. Jakarta.
Harmanto, N. 2003. Sehat dengan Ramuan Tradisional Mahkota Dewa. Cetakan empat. PT. Agromedia Pustaka. Tangerang. Hlm 5.
Harborne, J.B. 1996. Metode Fitokimia. Penuntun Cara Modern Menganalisis Tumbuhan. Alih bahasa Kosasih Padmawinata. ITB Bandung. Hlm 151. Hartati, S. M., S. Mubarika, I. G. Gandjar, M. T. Harmann, K.V. Rao dan S.
Wahyuno. 2005. Phalerin, Glukosida Benzofenon Baru Diisolasi dari Ekstrak Metanolik dan Mahkota DewaPhaleria macrpcarpa (Scheff) Boerl. (Tymelaceae). Majalah Farmasi Indonesia. Hlm 51-57.
Hostettman, K., M. Hostettman, dan A. Manson. 1995. Cara kromatografi Preparatif Penggunaan pada Senyawa Bahan Alam. Alih bahasa Kosasih Padmawinata. Institut Teknologi Bandung. Bandung. Hlm 27-34.
Johnson, L.E. dan R. Stevenson. 1991. Dasar Kromatografi Cair. Alih bahasa Kosasih Padmawinata. Institut Teknologi Bandung. Bandung. Hlm 365.
Lenny, S. 2006. Senyawa Flavonoida, Fenilpropanoida, dan alkaloid. Karya ilmiah.Departemen Kimia. FMIPA. Universitas Sumatera Utara. Medan. Hlm 7.
Lisdawati, V. 2002. Buah Mahkota Dewa-Toksisitas, Efek Antioksidan, dan Efek Anti Kanker Berdasarkan Uji Penapisan Farmakologi.
http://www.mahkotadewa.com/ 7 Februari 2011 pukul 13:00
Manitto, P. 1992. Biosintesis Produk Alami. Alih Bahasa Koensoemardiyah. IKIP Semarang Press. Semarang. Hlm 235.
Margono, S.A., dan R.N. Zendrato. 2006. Sintesis Diasetil Gamavuton-0 dengan menggunakan Asetil Klorida sebagai Acylating agent. M. Far. Indo. 17. (1). Hlm 25-31.
Munson, J. W. 1991. Analisis Farmasi Metode Modern.Airlangga University Press. Surabaya.
Nyapka, Y., A. M. Lubis, M. Pulung, G. Amrah, A. Munandar, G. B. Hong, N. Hakimi. 1988. Kesuburan Tanah. Penerbit Unila. Bandar Lampung. Hlm 117.
Padua, D., L.S, N. Bunyapraphatsara dan R.H.M.S Lemmens. 1999. Plant Resources of South East Asia. Medical and Poisonous Plants in Bogor Indonesia (PROSEA). Bakhuys Publishers, Leiden, the Neaderlands. Hlm 36.
Patra, A., S. Jha, P.N Murthy, Manik, A. Sharone. 2010. Isolation And
Characterization Of Stigmast-5-en-3 -ol ( -sitosterol) From The Leave Of Hygrophila spinosa T. Anders. International Journal of Pharma Sciences and Research (IJPSR) vol.1 (2). Hlm 95-100.
Pavia, Donald L., Gary M. Lampman, George S. Kritz, Randall G. Engel.
2006. Introduction to Organic Laboratory Techniques (4th Ed.). Thomson Brooks/Cole. pp. 797–817.
Rohyami, Y. 2007. Identifikasi Flavonoid dari Ekstrak Metanol Daging Buah Mahkota Dewa (Phaleria macrocarpa Boerl) Menggunakan
Spektrofotometer UV-Vi dan FT-IR, Laporan Penelitian PDM DIKTI. Jakarta.
Saleh, Chairul. 2008. Isolasi dan Penentuan Struktur Senyawa Steroid Dari Akar Tumbuhan Cendan (Santalum Album Linn), USU e-Reposetory.
Salempa, P., Noor, A., Soekamto, N.H. dan Harlim, T. 2009. Bioaktivitas Fraksi n-heksan dan Senyawa -sitosterol dari Kayu Akar Pterospermum subpeltatum C.B.Rob, Farmakologi 4 (2), Hlm 45-50.
Sastrohamidjojo, H. 2002. Kromatografi. Liberty. Yogyakarta. Hlm 35-36. Setyowati, E. P., U. A. Jenie, Sudarsono, B. Kardono, R. Rahmat, dan E.
Meiyanto. 2007. Isolasi Senyawa Sitotoksik Spons Kaliasis.M. Far. Indo. 18 (4). Hlm 183-189.
Simanjuntak, P. 2005. Report On Research Centre For Green Sciences, Fukuyama University in post doctoral program. Fukuyama, Japan.
Sienko, Plane and Marcus. 1984. Experimental Chemistry 6th Edition. Mc Graw Hill Book Co. Singapore.
Sitorus, M. 2009. Spektroskopi ( Elusidasi Struktur Molekul Organik). Graha Ilmu. Yogyakarta. Hlm 78.
Stahl, E. 1985. Analisis Obat Secara kromatografi dan Mikroskopi. diterjemahkan oleh Kosasih Padmawinata dan Iwang Soediro. Institut Teknologi
Bandung. Bandung. Hlm 3-17.
Sudjadi. 1983. Penentuan Struktur Senyawa Organik. Ghalia Indonesia. Jakarta. Hlm 283.
Soeksmanto, A., Y. Hapsari, dan P. Simanjuntak. 2007. Analisis Antioksidan Beberapa Bagian Tanaman Mahkota Dewa, Phaleria macrpcarpa (Scheff) Boerl. (Tymelaceae). Jurnal Ilmu Kefarmasian. In Press. Jakarta.
Sumastuti. 2002. Efek Antihistamin Ekstrak Daun dan Buah Mahkota Dewa pada Ileum Marmot Terpisah.
http://www.mahkotadewa.com/ 7 Februari 2011 pukul 14:00
Supriyanto, R. 1999. Buku Ajar Kimia Analitik III. FMIPA Universitas Lampung. Bandar Lampung. Hlm 2-3.
Tim Penyusun. 2007. Modul Kuliah Spektroskopi. Fakultas Farmasi Universitas Sanata Dharma. Yogyakarta. Hlm 58-62.
Venkata Sai Prakash Chaturvedula, Indra Prakash. 2012. Isolation of Stigmasterol and -sitosterol From The Dichloromethane Extract Of Rubus
suavissimus. International Current Pharmaceutical Journal. Hlm 239-242. Winarto, WP. 2003. Mahkota Dewa, budidaya dan pemanfaatan untuk obat. PenebarSwadana. Jakarta.
Wiryowidagdo, Sumali. 2000. Kimia dan Farmakologi Bahan Alam. Dirjen Dikti-Universitas Indonesia. Jakarta. Hlm 339.
Yuk, J.K., Woo, J.S., Yun, C.Y., Lee, J.S., Kim, J.H., Song, G.Y., Yang, E.J., Hur, I.K. and Kim, I.S. 2007. Effects of Lactose- -sitosterol and


![Gambar 6. Struktur molekul senyawa C19H20O6: 5-[4(4-metoksi-fenil) tetrahidrofuro[3,4-c] furan-1-il]-benzena-1,2,3-triol (Lisdawati, 2002)](https://thumb-ap.123doks.com/thumbv2/123dok/469110.134755/22.612.180.460.419.524/gambar-struktur-molekul-senyawa-metoksi-tetrahidrofuro-benzena-lisdawati.webp)