FRAKSINASI SENYAWA AKTIF MINYAK ATSIRI KENCUR
(Kaempferia galanga L) SEBAGAI PELANGSING
AROMATERAPI SECARA IN VIVO
LUSIANI DEWI ASSAAT
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
Dengan ini saya menyatakan bahwa tesis Fraksinasi Senyawa Aktif Minyak Atsiri Kencur (Kaempferia galanga L) Sebagai Pelangsing Aromaterapi Secara In Vivo adalah karya saya dengan arahan dari komisi pembimbing dan belum diajukan dalam bentuk apa pun kepada perguruan tinggi mana pun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir tesis ini.
Bogor, Juni 2011
Kaempferia galanga L Essential oil as Aromatherapy for Antiobesity using In Vivo Analysis. Under direction of TUN TEDJA IRAWADI and IRMANIDA BATUBARA
The purposes of this research were to separate constituents of kencur (Kaempferia galanga L) essential oil and to evaluate their active components as aromatherapy for antiobesity using in vivo analysis to the male Sprague-dawley rats. Volatile oil of dried rhizome of K. galanga L obtained by water distillation. Its chemical components determined using gas chromatography and mass spectrometry (GC-MS). The main components of volatile oil isolated were α-pinene, camphene, δ -3-carene, α-phellandrene, limonene, p-cymene 4-isopropyltoluene, 7,8-epoxytricyclo dodecana, 5-methyltricyclo undec-2-en-4-one, 2-propenoic methoxyphenyl)-, ethyl ester. Pure compound (2-propenoic acid,3-(4-methoxyphenyl)-, ethyl ester) was determined the structure by GC-MS and NMR analysis. A total of forty male Sprague-dawley rats were used for this study. They were divided into five groups i.e. (1) a normal control group, without treatment of both high cholesterol diet and inhalation, (2) a negative control group was treated by high cholesterol diet only, without inhalation treatment, (3) treated with high cholesterol diet followed by treatment with inhalation of crude oils, (4) Treated with high cholesterol diet followed by inhalation one of essential oils fraction, and (5) Treated with high cholesterol diet followed inhalation of 2-propenoic acid,3-(4-methoxyphenyl)-, ethyl ester. Treatment condition was achieved by five months. Rat’s weight and stool were weighed every day during the treatment period. Blood cholesterol total (LDL, HDL and Triglyceride) level was determined in the end of treatment period. Duncan test analysis showed that percentage increase in body weight and liver weight has significant difference but fat weight wasn’t significant difference. For blood test analysis HDL, Cholesterol, and Triglyceride level has significant difference. The conclusion were kencur essential oil has ethyl-para-methoxycinnamate as pure compound, based on in vivo test analysis fraction has potentially as antiobesity and crude oils and pure compound has potentially decreased cholesterol and triglyceride using aromatherapy method.
RINGKASAN
LUSIANI DEWI ASSAAT. Fraksinasi Senyawa Aktif Minyak Atsiri Kencur (Kaempferia galanga L) Sebagai Pelangsing Aromaterapi Secara In Vivo. Dibimbing oleh TUN TEDJA IRAWADI dan IRMANIDA BATUBARA.
Lemak merupakan salah satu komponen makanan yang dibutuhkan oleh tubuh. Tetapi jika seseorang mengkonsumsi lemak secara berlebihan akan mengakibatkan terjadi penumpukan lemak tubuh yang disebut dengan kelebihan berat badan atau identik dengan obesitas. Obesitas dapat mengganggu penampilan dan memiliki resiko terhadap berbagai penyakit diantaranya hiperkolesterol, penyempitan pembuluh darah, diabetes, tekanan darah tinggi, dan penyakit jantung koroner (Giannessi et al, 2008). Oleh karena itu, penanganan atau pencegahan terjadinya obesitas sangat diperlukan sehingga dapat mencegah penyakit yang ditimbulkan oleh obesitas seperti tingginya kadar kolesterol darah. Terdapat pengobatan alternatif seperti aromaterapi yang dapat menjadi suatu pilihan. Aromaterapi merupakan pengobatan herba yang menggunakan bau-bauan dari minyak atsiri dari suatu tanaman.
Kencur (Kaempferia galanga L) memiliki kandungan minyak atsiri sebesar 2-7% dari bobotnya (Rostiana dan Djazuli, 2007). Kencur merupakan tanaman tradisional yang lazim digunakan sebagai jamu, bumbu, mengobati bengkak, batuk, menghangatkan badan, dsb. Minyak atsiri dari kencur memiliki aktivitas biologis sebagai antimikroba Tewtrakul (2005). Namun kajian mengenai potensi minyak atsiri kencur sebagai pelangsing aromaterapi belum diamati secara luas. Oleh karena itu tujuan dari penelitian ini adalah untuk memperoleh senyawa aktif minyak atsiri kencur sebagai pelangsing atau penurun kolesterol aromaterapi secara in vivo.
Pada penelitian ini, Sampel kencur segar yang berusia sekitar 1.0-1.5 tahun diperoleh dari pasar induk Kramat Djati. Sampel yang digunakan memiliki kadar air 85.3% dan kadar abu 1,35 % berdasarkan bobot basah. Kencur kemudian didestilasi sehingga diperoleh destilat dan residu. Destilat adalah minyak atsiri kencur (rendemen 0.3% berdasarkan bobot basah). Minyak atsiri kencur memiliki parameter sebagai berikut: berwarna kuning agak keruh pada kondisi panas, indeks bias 1,4958 pada suhu 20ºC diukur menggunakan refraktometer Abbe-Atago NAR-3T. Densitas 0,9433 g/mL yang dibandingkan dengan densitas air 1,043 g/mL. Minyak atsiri kencur setelah dibiarkan lama pada suhu ruang atau semalam pada lemari es, terbentuk padatan berwarna putih seperti kristal yang berada di dasar botol penampung minyak atsiri. Demikian pula pada residu, setelah dibiarkan selama 1 x 24 jam terbentuk padatan berwarna putih seperti kristal yang berada di atas permukaan air. Kedua padatan ini kemudian dipisahkan dari destilat minyak atsiri dan residu kemudian ditampung dalam wadah yang berbeda untuk kemudian diidentifikasi lebih lanjut. Untuk selanjutnya kedua padatan ini diberi nama kristal fase air dan kristal fase minyak.
gerak). Fraksinasi minyak atsiri kencur menghasilkan 11 fraksi. Fraksi 2 memiliki rendemen terbesar yaitu 28.42%. Oleh karena itu fraksi 2 ini dilanjutkan dengan analisis GC-MS untuk mengidentifikasi komponen yang terkandung di dalamnya, dan diuji aktivitasnya sebagai pelangsing aromaterapi secara in vivo.
Hasil kromatogram GC-MS dari sampel minyak atsiri kencur memiliki 3 komponen utama yaitu δ-3-carene, 5-metiltrisiklo undek-2-en-4-one, dan 2-asam propenoat,3-(4-metoksifenil)-,etilester. Begitu pula dengan fraksi 2 hasil pemisahan menggunakan teknik kromatografi kolom, ternyata masih terdapat beberapa komponen di dalamnya dengan δ-3-carene sebagai komponen utamanya. Untuk kedua kristal yang diperoleh dari destilasi, baik kristal di fasa air ataupun kristal di fasa minyak memiliki komponen yang sama, yaitu senyawa 2-asam propenoat,3-(4-metoksifenil)-,etilester atau etil-p-metoksisinamat (nama trivial). Berdasarkan analisis 1H-NMR, COSY, HMQC, dan HMBC menunjukkan bahwa kedua kristal tersebut merupakan senyawa yang sama. Oleh karena itu minyak atsiri kencur, fraksi 2, dan Kristal etil-p-etoksisinamat dilanjutkan dengan uji In Vivo dengan pemberian dengan cara inhalasi kepada hewan uji berupa tikus putih jantan galur Sprague-dawley. Tikus yang digunakan sebanyak 40 ekor yang dibagi menjadi 5 kelompok yaitu kelompok kontrol normal merupakan kelompok yang diberi pakan standar dan tidak diinhalasi. Kelompok kontrol negatif merupakan kelompok yang diberi pakan kolesterol tinggi dan tidak diinhalasi. Kelompok atsiri kasar diberi pakan kolesterol tinggi dan diinhalasi minyak atsiri kasar hasil destilasi uap dari rimpang kencur. Kelompok Fraksi 2 diberi pakan kolesterol tinggi dan diinhalasi menggunakan Fraksi 2 yang merupakan Fraksi dengan randemen terbanyak. Kelompok kristal diberi pakan kolesterol tinggi dan diinhalasi menggunakan Fraksi senyawa murni. Masa adaptasi dilakukan selama 2 minggu sebelum masa perlakuan. Hewan uji ditempatkan pada suatu kandang plastik bertutup kawat dengan 4 ekor tikus untuk setiap kandang. Selama masa adaptasi semua kelompok diberi pakan standar yang sama. Adapun pakan yang diberikan pada tikus adalah 20g/ekor/hari, karena konsumsi pakan tikus hanya 10-20 g/ekor/hari. Selama masa adaptasi dan perlakuan hewan uji diberi minum menggunakan air minum dalam kemasan (AMDK) tanpa dibatasi (ad libitum). Minyak atsiri kasar, fraksi 2, dan kristal diinhalasikan terhadap hewan uji selama masa perlakuan dengan konsentrasi masing-masing 1% dalam aquades. Perlakuan ini dilakukan selama 5 minggu. Pemberian pakan dilakukan setiap hari, sehingga bobot pakan ditimbang setiap hari. Bobot badan tikus ditimbang setiap 1 minggu sekali. Pada akhir masa perlakuan, darah di ambil di bagian ekor tikus sebelum tikus dibius (anastesi) menggunakan eter teknis. Kemudian dibedah dan seluruh organ yang diperlukan ditimbang lalu disimpan di dalam formalin.
Berdasarkan analisis secara fisik, perlakuan selama 5 minggu yang diberikan kepada tiap kelompok Fraksi 2 menunjukkan perbedaan yang signifikan untuk parameter persentase kenaikan bobot badan, bobot hati, dan pakan yang dikonsumsinya. Hanya parameter bobot lemak dan bobot pengeluaran feses dan urin yang tidak menunjukkan perbedaan yang signifikan antara Fraksi 2 dengan kelompok lainnya. Hal ini menunjukkan bahwa terdapat pengaruh perlakuan terhadap perubahan fisik hewan uji. Oleh karena itu, uji in vivo menunjukkan bahwa Fraksi 2 berpotensi sebagai pelangsing aromaterapi.
dianastesi. Darah ditampung pada vial sebanyak 2 mL dan diberi label. Kemudian darah disentrifuga untuk memperoleh serum yang akan di uji HDL, kolesterol, dan trigliseridanya. Kadar kolesterol darah berbeda secara signifikan dengan pemberian perlakuan. Kelompok kontrol normal memiliki kolesterol darah yang terendah, dan kelompok kontrol negatif memiliki kolesterol darah yang tertinggi. Untuk kelompok perlakuan, dengan pemberian pakan lemak tinggi selama 5 minggu, perlakuan inhalasi mampu menurunkan kadar kolesterol darah yang berbeda signifikan dengan kelompok kontrol negatif. Dibandingkan dengan ketiga kelompok perlakuan (Fraksi2, atsiri kasar, dan kristal), perlakuan inhalasi menggunakan kristal kencur (etil-p-metoksisinamat) mampu menurunkan kadar kolesterol paling maksimal sehingga tergolong ke dalam kategori normal. Kadar kolesterol normal untuk hewan uji tikus adalah 47-88 mg/dL (Suckow et al
,2006). Untuk 2 kelompok perlakuan lainnya yaitu kelompok fraksi 2 dan atsiri kasar, walaupun kadar kolesterolnya berbeda nyata dengan kadar kolesterol normal, namun perlakuan tersebut berhasil menurunkan kadar kolesterol dibandingkan dengan kelompok kontrol negatif. Kadar trigliserida normal untuk hewan uji tikus berada pada batas 25-145 mg/dL (Suckow et al ,2006). Data menunjukkan bahwa kadar trigliserida untuk kelima kelompok masih termasuk ke dalam kadar trigliserida normal. Meskipun normal, kelompok kontrol negatif memiliki kadar trigliserida yang berbeda signifikan dengan keempat kelompok lainnya. Kelompok yang diberi perlakuan (fraksi2, atsiri kasar, kristal), mampu menurunkan kadar trigliserida hingga sama dengan kelompok normal dan berbeda secara signifikan dengan kelompok kontrol negatif.
Etil-p-metoksisinamat merupakan senyawa utama (penciri kencur) yang diperoleh dari minyak atsiri kencur. Hasil uji in vivo menunjukkan bahwa, Fraksi 2 berpotensi sebagai pelangsing aromaterapi, sedangkan minyak atsiri kencur dan etil-p-metoksisinamat berpotensi menurunkan kadar kolesterol dan trigliserida darah menggunakan metode aromaterapi.
© Hak Cipta milik IPB, tahun 2011
Hak Cipta dilindungi Undang-Undang
Dilarang mengutip sebagian atau seluruh karya tulis ini tanpa mencantumkan atau menyebutkan sumbernya. Pengutipan hanya untuk kepentingan pendidikan, penelitian, penulisan karya ilmiah, penyusunan laporan, penulisan kritik, atau tinjauan suatu masalah; dan pengutipan tersebut tidak merugikan kepentingan yang wajar IPB
AROMATERAPI SECARA IN VIVO
LUSIANI DEWI ASSAAT
Tesis
sebagai salah satu syarat untuk memperoleh gelar Magister Sains pada
Program Studi Kimia
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
NIM : G451090291
Disetujui
Komisi Pembimbing
Prof. Dr. Ir. Tun Tedja Irawadi, MS Dr. Irmanida Batubara, MSi Ketua Anggota
Diketahui
Ketua Program Studi An. Dekan Sekolah Pascasarjana IPB Kimia Sekretaris Program Magister
Prof. Dr. Purwantiningsih S, M.Si Dr. Ir. Dahrul Syah, M.Sc. Agr
Nya sehingga proposal penelitian ini berhasil diselesaikan. Judul penelitian ini adalah Fraksinasi Senyawa Aktif Minyak Atsiri Kencur (Kaempferia galanga L) Sebagai Pelangsing Aromaterapi Secara In Vivo.
Terima kasih penulis ucapkan kepada Ibu Prof. Dr. Ir. Tun Tedja Irawadi, MS dan Dr. Irmanida Batubara, M.Si selaku pembimbing yang telah banyak memberi saran, arahan dan bimbingan selama penyusunan tesis ini. Ucapan terima kasih juga penulis sampaikan kepada Ibu Dr. dr. Irma H. Suparto, MS selaku penguji luar komisi pembimbing yang telah memberikan saran dan arahan, serta Ibu Prof. Dr. Purwantiningsih S, M.Si selaku ketua program studi Kimia.
Ungkapan terima kasih yang tak terhingga disampaikan kepada suami penulis Soleh atas kesabaran, dukungan moril dan materil serta doanya. Kepada anak-anak ku Khanza dan Rafi, serta kakak, dan adik-adik ku terima kasih atas segala doa dan kasih sayangnya. Untuk semua pihak yang tidak dapat penulis sebutkan satu persatu, terima kasih atas segala bantuannya selama penelitian, semoga jasa dan semua amal kebaikannya mendapat imbalan yang berlipat ganda dari Alloh SWT.
Karya ilmiah ini juga didedikasikan untuk Alm. Ayahanda H. Dudung Djoendulloh dan Alm. Ibunda Hj. Ai Sholihat, semoga Alloh memberikan tempat terindah di sana.
Semoga karya ilmiah ini bermanfaat.
Bogor, Juni 2011
Lusiani Dewi Assaat
Dudung Djoendulloh dan ibu Ai Solihat. Penulis merupakan anak kedua dari tujuh bersaudara.
Tahun 1999 penulis lulus dari SMU Negeri 1 Tasikmalaya Jawa Barat dan pada tahun yang sama lulus seleksi masuk Universitas Pendidikan Indonesia melalui jalur Penelusuran Minat, Bakat, dan Kemampuan (PMDK). Penulis memilih mayor Pendidikan Kimia, Fakultas Pendidikan Matematika dan Ilmu Pengetahuan Alam. Pada tahun 2009, penulis diterima di Program Studi Kimia pada Program Pascasarjana IPB. Beasiswa pendidikan pascasarjana diperoleh dari Pendidikan Perguruan Tinggi (DIKTI).
DAFTAR TABEL ……… vii
Kromatografi Kolom dan Kromatografi Lapis Tipis ……….. 7
GC-MS ……… 8
Metode Analisis Bobot Hati dan Bobot Deposit Lemak pada Hewan Uji ..………. 17
Metode Analisis Data ………. 17
HASIL DAN PEMBAHASAN ………. 19
Kadar Air dan Kadar Abu ……….. 19
Isolasi Minyak Atsiri Kencur Menggunakan Distilasi Uap ………… 19
Penentuan Eluen Terbaik ……… 21
Fraksinasi Minyak Atsiri Kencur ……… 22
Analisis GC-MS Minyak Atsiri Kencur, Fraksi 2, Kristal Fase Air, dan Kristal Fase Minyak ………. 24
Uji In Vivo Minyak Atsiri Kencur, Fraksi 2, dan Kristal …………... 28
Analisis Fisik ……….. 29
Analisis Uji Darah ……….. 32
DAFTAR TABEL
1 Penggolongan bobot badan berdasarkan IMT ………. 4 2 Perbandingan komponen-komponen kencur perolehan
Tewtrakul 2005 dan Sudibyo 2000 ……….…… 7 3 Hasil fraksinasi minyak atsiri kencur dengan
kromatografi kolom (elusi gradien) ………. 23 4 Komponen yang terkandung dalam sampel berdasarkan
1 Alur penelitian ………. 13 2 Metode analisis minyak atsiri yang berpotensi sebagai pelangsing
aromaterapi pada hewan uji ……… 14 3 Minyak dan kristal yang diperoleh dari hasil distilasi ……… 20 4 Profil kromatogram minyak atsiri kencur dengan berbagai
eluen tunggal dan eluen campuran ………. 21 5 Profil kromatogram hasil fraksinasi minyak atsiri kencur ………. 23 6 Kromatogram GC-MS dari sampel minyak atsiri kencur, fraksi 2,
kristal fase air, dan kristal fase minyak ……….. 25 7 Spektrum 1H-NMR kristal fase air dan kristal fase minyak ………... 26 8 Hasil analisis NMR lengkap senyawa etil-p-metoksisinamat …….……… 27 9 Struktur senyawa etil-p-metoksisinamat ……… 28 10 Rangkaian alat inhalator, pengumpulan darah dan organ ……….. 29 11 Persentase kenaikan bobot badan hewan uji tiap minggu
1 Hasil determinasi sampel ……….………. 43
2 Penentuan kadar air dan kadar abu rimpang kencur ………. 44
3 Perhitungan randemen, indeks bias, dan densitas ………. 45
4 Spektrum MS δ-3-carene, etil sinamat, etil-p-metoksisinamat ………. 46
5 Spektrum COSY, HMQC, HMBC dari kristal fase air dan kristal fase minyak ………. 48
6 Komposisi pakan yang diberikan pada hewan uji ……… 50
7 Statistik deskriptif, homogenitas, ANOVA, dan uji Duncan data persentase kenaikan bobot badan, bobot pakan yang dikonsumsi, dan bobot feses dan urin ……….. 51
Latar Belakang
Lemak merupakan salah satu komponen makanan yang dibutuhkan oleh
tubuh. Tetapi jika seseorang mengkonsumsi lemak secara berlebihan akan
mengakibatkan terjadi penumpukan lemak tubuh yang disebut dengan kelebihan
berat badan atau identik dengan obesitas. Obesitas merupakan keadaan
berlebihnya lemak tubuh (Lebenthal & Damayanti 2007). Obesitas dapat
mengganggu penampilan dan memiliki resiko terhadap berbagai penyakit
diantaranya hiperkolesterol, penyempitan pembuluh darah, diabetes, tekanan
darah tinggi, dan penyakit jantung koroner (Giannessi et al. 2008). Selain itu
obesitas juga dapat mengganggu penampilan. WHO menyatakan bahwa obesitas
adalah salah satu dari 10 faktor paling beresiko di seluruh dunia. Bahkan hal ini
mulai mengancam negara-negara di benua Asia. Salah satunya di Indonesia pada
tahun 2000, jumlah penduduk yang mengalami overweight mencapai 17,5 %, dan
pasien obesitas 4,7 %.
Oleh karena itu, penanganan atau pencegahan terjadinya obesitas sangat
diperlukan sehingga dapat mencegah penyakit yang ditimbulkan oleh obesitas.
Terapi non farmakologis seperti diet dan gerak badan lebih diutamakan untuk
pencegahan obesitas, tetapi terapi nonfarmakologis seperti penggunaan obat
sintetik ataupun obat herbal juga dilakukan untuk penanganan obesitas. Obat
antiobesitas atau pelangsing memiliki fungsi mengurangi nafsu makan,
merangsang pembakaran lemak, dan menghambat penyerapan lemak dalam batas
tertentu (Birari & Bhutani 2007). Obat pelangsing yang ada di pasaran terdiri atas
obat pelangsing sintetik dan obat pelangsing alami yang dibuat secara tradisional.
Kedua jenis obat ini biasanya dikonsumsi secara oral. Namun jenis obat
pelangsing yang sedang dikembangkan adalah obat pelangsing aromaterapi dari
tanaman herbal. Kandungan tanaman herbal yang berpotensi sebagai pelangsing
aromaterapi adalah minyak atsirinya (Maniapoto 2002).
Kencur (Kaempferia galanga L) merupakan salah satu jenis rimpang yang
lazim digunakan oleh masyarakat Indonesia. Kencur memiliki kandungan minyak
kencur sebesar 2-7 % dari bobotnya (Rostiana dan Djazuli 2007). Khasiat dari
kencur telah banyak dilaporkan dalam berbagai penelitian. Serbuk kencur
memiliki efek tonik terhadap mencit jantan (Nurhayati 2008) dan minyak atsiri
kencur memiliki aktivitas biologis sebagai antimikroba (Tewtrakul 2005). Namun
kajian mengenai potensi minyak atsiri kencur sebagai pelangsing aromaterapi
belum diamati secara luas. Sebelumnya telah dilakukan kajian mengenai potensi
minyak atsiri temulawak sebagai pelangsing aromaterapi (Anggraeni 2010).
Hasilnya bahwa senyawa -elemenona yang terkandung dalam minyak atsiri
temulawak berpotensi sebagai pelangsing. Oleh karena itu penelitian ini bertujuan
untuk mengidentifikasi senyawa yang terkandung dalam minyak atsiri kencur dan
menganalisis potensi senyawa aktifnya sebagai pelangsing aromaterapi secara in
vivo.
Tujuan
Tujuan dari penelitian ini adalah untuk memperoleh senyawa aktif minyak
atsiri kencur sebagai pelangsing dan penurun kolesterol aromaterapi secara in
vivo.
Hipotesis
Hipotesis penelitian ini adalah minyak atsiri kencur memiliki senyawa aktif
Obesitas
Asupan makanan yang mengandung lemak tinggi memiliki kandungan
trigliserida yang tinggi. Trigliserida di dalam tubuh akan dipecah oleh enzim
lipase menjadi asam lemak dan gliserol. Proses ini dinamakan hidrolisis lemak
yang terjadi di usus. Lemak kemudian diabsorbsi melalui sel-sel mukosa pada
dinding usus dan diubah kembali menjadi lemak dan trigliserida. Lemak ini
memiliki ukuran partikel yang kecil (kilomikron) dan dibawa ke dalam darah
melalui cairan limfa. Dari darah lemak kemudian diangkut ke hati yang kemudian
diangkut ke jaringan organ lainnya dan dimanfaatkan sebagai sumber energi,
pertumbuhan, bahan baku hormon, dan sebagainya. Sisa asam lemak yang tidak
dimanfaatkan oleh tubuh disimpan sebagai deposit lemak yang berfungsi sebagai
cadangan makanan dalam tubuh. Jika deposit lemak di dalam tubuh terlalu
berlebih maka akan menyebabkan obesitas atau identik dengan kegemukan.
Penyebab kegemukan terjadi karena kebiasaan mengkonsumsi makanan siap saji
dengan kandungan lemak dan kalori yang tinggi atau mengkonsumsi makanan
yang kurang berserat, stres yang dilarikan pada makanan, dan faktor keturunan
(Lebenthal & Damayanti 2007).
Terdapat beberapa metode untuk menilai kelebihan berat badan.
Diantaranya adalah metode densitometri, yaitu penentuan berat jenis tubuh
dengan cara menimbang di bawah air, CT-scan dan MRI, yaitu penentuan lemak
tubuh total dan pembagian lemak dalam tubuh, dan yang lebih praktis adalah
Indeks Massa Tubuh (IMT). IMT dapat menentukan besarnya massa lemak tetapi
tidak menerangkan pembagian lemak dalam tubuh. Nilai Indeks Massa Tubuh
(IMT), atau Body Mass Index (BMI), atau Quatelet Index (QI) dapat dihitung
dengan cara membagi bobot badan (kg) terhadap kuadrat tinggi badan (m2).
Berdasarkan harga IMT ini tingkat kegemukan digolongkan ke dalam 6
Tabel 1. Penggolongan bobot badan berdasarkan IMT
Kategori bobot badan IMT
Kurang < 18.5
Normal 18.5 – 24.5
Gemuk, overweight 25 – 29.9
Gemuk, obesitas I 30 – 34.9
Gemuk, obesitas II 35 – 39.9
Obesitas hebat > 39.9
(Tjay dan Rahardja 2003)
Selain menimbulkan permasalahan pada penampilan, obesitas juga sering
menjadi penyebab berbagai penyakit antara lain hiperkolesterol, penyempitan
pembuluh darah, diabetes, tekanan darah tinggi, dan penyakit jantung koroner
(Giannessi et al. 2008). Oleh karena itu pencegahan dan penanganan kegemukan
perlu dilakukan agar penyakit-penyakit yang ditimbulkan karena kegemukan
dapat dihindari.
Pelangsing
Obat antiobesitas atau pelangsing memiliki fungsi mengurangi nafsu makan,
merangsang pembakaran lemak, dan menghambat penyerapan lemak dalam batas
tertentu (Birari & Bhutani 2007). Obat obatan yang biasa digunakan sebagai
pelangsing adalah anoreksansia, yaitu zat-zat yang berdaya menekan nafsu makan
dan digunakan untuk menunjang diet pada penanganan kegemukan. Selain itu
obat-obatan lainnya adalah orlistat, dan hidroksisitrat (HCA). Kedua obat ini
merupakan obat baru yang penggunaannya dimulai tahun 1998. Obat yang
tergolong sintetis ini selain memberikan manfaat dalam penggunaannya juga
memberikan efek samping. Diantaranya memberikan efek samping berupa
gangguan lambung, usus, sakit perut, diare, dan kejang lambung. (Tjay dan
Rahardja 2003).
Selain obat-obatan sintetis juga banyak dikembangkan obat-obatan herba.
polong-polongan Nomame herba dapat dijadikan sebagai antiobesitas karena
menghambat aktivitas kerja enzim lipase.
Aromaterapi
Aromaterapi adalah istilah untuk suatu pengobatan alternatif yang
menggunakan bau-bauan atau wangi-wangian yang berasal dari senyawa-senyawa
aromatik. Hasil penelitian Maniapoto (2002) melaporkan bahwa manfaat dari
aromaterapi umumnya berkaitan dengan kondisi fisik, mental, emosional, dan
spiritual. Sedangkan Hongratanaworakit (2004) melaporkan bahwa aroma
memberikan efek fisiologis dan psikologis bagi manusia. Denyut jantung, tekanan
darah, aktivitas elektrodermal, electroencephalogram, gelombang otak, dan
kedipan mata dapat digunakan sebagai indikasi untuk mengukur pengaruh aroma
terhadap fisiologis manusia.
Bahan yang digunakan untuk aromaterapi biasanya dari cairan tanaman
yang mudah menguap atau disebut sebagai minyak atsiri. Minyak atsiri
merupakan zat yang memberikan aroma pada tanaman dan memiliki komponen
yang mudah menguap (volatil) pada beberapa tanaman dengan karakteristik
tertentu. Setiap senyawa penyusun minyak atsiri memiliki efek tersendiri, dan
campurannya dapat menghasilkan rasa yang berbeda. Secara kimiawi, minyak
atsiri tersusun dari berbagai senyawa, namun suatu senyawa tertentu biasanya
bertanggung jawab atas suatu aroma tertentu. Buchbauer (1993) melaporkan
bahwa minyak atsiri telah digunakan sebagai minyak wangi, kosmetik, bahan
tambahan makanan, dan obat. Penelitian Maniapoto (2002) menyatakan bahwa
minyak atsiri memiliki potensi sebagai obat yang penggunaannya berkaitan
dengan aromaterapi contohnya pelangsing aromaterapi.
Perolehan minyak atsiri temulawak dari rimpang temulawak (berdasarkan
bobot basah) menggunakan destilasi uap sebesar 0,2003%. Kandungan minyak
atsiri temulawak yang dianalisis menggunakan GC-MS adalah xantorizol, kamfor,
borneol, zingiberena, -elemena, germakrena-B, -farnesena, α-kurkumena, α
-cedrena, -seskuifelandrena, -elemenona. Hasil penelitian menunjukkan
melaporkan bahwa senyawa -elemenona yang terkandung dalam minyak atsiri
Kencur
Kencur diklasifikasikan ke dalam kingdom Plantae, divisi Spermatophyta,
subdivisi Angiospermae, kelas Monocotyledonae, ordo Zingiberales, family
Zingiberaceae, genus Kaempferia, dan spesies K. galanga Linn. Sehingga kencur
ini dikenal dengan nama Kaempferia galanga Linn. Kencur merupakan bahan
baku berbagai industri sebagai obat tradisional, obat herbal terstandar, kosmetik,
bumbu, bahan makanan, dan minuman penyegar. Di masyarakat kencur telah
banyak dimanfaatkan untuk mengobati bengkak, reumatik, batuk, sakit perut,
ekspektoran (memperlancar pengeluaran dahak), infeksi bakteri, dan
menghangatkan badan.
Tanaman kencur banyak ditemukan di daerah Jawa, selain itu mulai
dikembangkan pula pembukaan areal tanam di luar Jawa, antara lain di
Kalimantan Selatan. Secara botanis, kencur dapat dikelompokkan ke dalam dua
tipe, yaitu berdaun lebar dan berdaun sempit. Kencur berdaun lebar biasanya
memiliki rimpang yang besar, sedangkan kencur berdaun sempit berimpang kecil.
Kencur berdaun lebar banyak dibudidayakan di Jawa Barat terutama di daerah
Bogor, sedangkan di Jawa Tengah dan Jawa Timur, petani umumnya menanam
kencur berdaun sempit. Kencur berimpang kecil memiliki kandungan minyak
atsiri lebih tinggi daripada kencur berimpang besar (Rostiana dan Djazuli 2007).
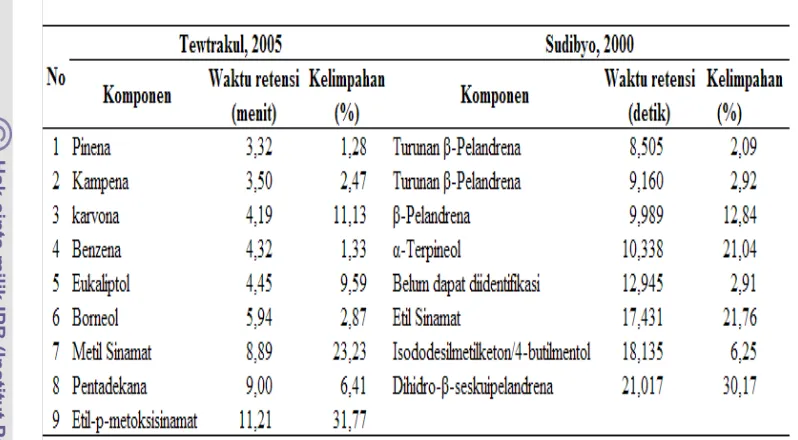
Tewtrakul et al (2005) melaporkan bahwa komponen utama kencur adalah
etil-p-metoksisinamat, metil sinamat, karvona, eukaliptol, dan pentadekana.
Sedangkan sumber lain menyebutkan bahwa komponen utama kencur adalah
-pelandrena, α-terpineol, etilsinamat, dan dihidro- -seskuipelandrena (Sudibyo
2000).
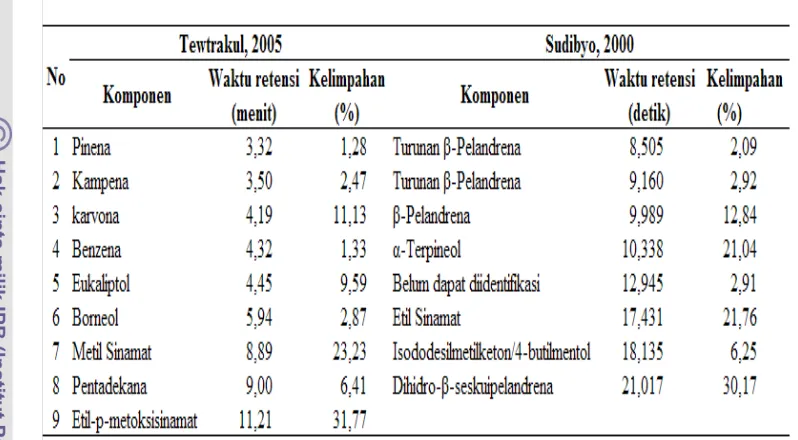
Di bawah ini adalah tabel perbandingan komponen-komponen kencur
Tabel 2. Perbandingan komponen-komponen kencur perolehan Tewtrakul 2005
dan Sudibyo 2000
Dari tabel tersebut terlihat bahwa komponen yang terkandung dalam kencur
berbeda, hal ini disebabkan karena adanya perbedaan iklim dan kondisi geografis
dari area pengambilan sampel yang berbeda sehingga berpengaruh terhadap
produksi dari komponen minyak atsirinya (Tewtrakul et al. 2005).
Kromatografi Kolom dan Kromatografi Lapis Tipis
Kromatografi merupakan suatu metode pemisahan komponen yang
didasarkan pada distribusi diferensial dari komponen sampel diantara 2 fase, yaitu
fase diam dan fase gerak. Dengan adanya fase diam maka campuran pelarut akan
terpisah sepanjang kolom berdasarkan pada perbedaan laju migrasi dari berbagai
macam pelarut. Metode pemisahan yang paling umum digunakan adalah
kromatografi kolom dan kromatografi lapis tipis. Kromatografi kolom merupakan
teknik analisis yang digunakan dalam penentuan jumlah komponen yang terdapat
pada suatu campuran senyawa, pemisahan, dan pemurnian komponen senyawa
pengelusi dialirkan secara kontinu melewati kolom, kemudian
komponen-komponen dari campuran senyawa yang dipisahkan keluar dari kolom,
dikumpulkan, dan difraksinasi. Umumnya, silika gel digunakan sebagai fase diam
kromatografi kolom, karena memiliki luas relatif yang besar. Proses elusinya
dapat berupa elusi isokratik ataupun elusi gradien (Harvey 2000).
Hasil pemisahan dengan kromatografi kolom dapat dianalisis lebih lanjut
menggunakan kromatografi lapis tipis (KLT). Kromatografi Lapis Tipis (KLT)
merupakan jenis kromatografi partisi yang menggunakan sebuah lapis tipis silika
atau alumina yang seragam pada sebuah lempeng gelas atau logam yang keras
sebagai fase diam. Fase diam KLT tersebut seringkali mengandung substansi yang
dapat berpendar dalam sinar ultraviolet. Kemudian fase gerak pada KLT
merupakan pelarut atau campuran pelarut yang sesuai. Pergerakan zat relative
terhadap garis depan pelarut dalam sistem kromatografi lapis tipis dapat
didefinisikan sebagai nilai Rf, yaitu perbandingan jarak tempuh zat dengan jarak
tempuh garis depan pelarut.
Teknik pemisahan kromatografi kolom dan KLT dapat digunakan untuk
memisahkan senyawa yang terkandung dalam minyak atsiri. Identifikasi senyawa
yang terkandung dalam minyak atsiri tersebut dapat dilakukan dengan
menggunakan metode GC-MS.
GC-MS
GC-MS (Gas chromatographic mass spectroscopy) atau kromatografi gas
merupakan instrumen untuk identifikasi senyawa organik yaitu penentuan bobot
molekul dan penentuan rumus molekul. Alat ini merupakan gabungan antara
kromatografi gas dengan spektrometer massa. Komponen dasar dari instrumen
GC-MS berupa gas kromatografi inlet, kamar ionisasi, penganalisa massa,
detektor, dan rekorder. Kromatografi gas (GC) merupakan kromatografi partisi
dari salah satu jenis kromatografi kolom modern yang digunakan untuk
memisahkan senyawa yang mudah menguap (volatil) dan tidak mengalami
dekomposisi akibat pemanasan. Sistem pemisahan pada GC umumnya didasarkan
dipisahkan. Fase diam GC dapat berupa padatan atau cairan. Sedangkan fase
geraknya berupa gas pembawa yang bersifat inert seperti He, N2, dan H2 (Skoog
et al. 2004).
Instrumentasi GC yang menggunakan spektrometer massa (MS) sebagai
detektor dapat digunakan untuk memisahkan campuran komponen dalam suatu
sampel (GC komponen) sekaligus mengidentifikasi komponen-komponen tersebut
pada tingkat molekuler (MS komponen). Oleh karena itu, prinsip kerja GC-MS
lebih baik daripada prinsip kerja dan analisis dari GC.
Senyawa-senyawa yang terpisah dari analisis GC akan keluar dari kolom
dan mengalir ke dalam MS. MS kemudian mengidentifikasi senyawa-senyawa
tersebut berdasarkan bobot molekul senyawanya. Molekul-molekul analat yang
bersifat netral diubah menjdi ion-ion dalam fase gas. Ion-ion yang dihasilkan
kemudian dipisahkan menurut rasio massanya untuk menghitung rasio (m/e) yang
didasarkan pada suatu proses yang analog dengan disperse cahaya oleh prisma
pada panjang gelombang tertentu. Spektrum massa dari analat yang muncul
dibandingkan dengan spectrum pada “library” MS sehingga akan diketahui bobot
molekul dari analat tersebut. Hal ini disebabkan spektrum massa adalah gambaran
antara limpahan relatif lawan perbandingan massa/muatan (m/e atau m/z) (Skoog
et al. 2004).
Spektroskopi NMR (Nuclear Magnetic Resonance)
Spektroskopi nuclear magnetic resonance atau resonansi magnet inti (RMI)
termasuk ke dalam spektroskopi absorpsi seperti halnya dengan spektroskopi
inframerah atau spektroskopi ultraviolet. Dasar dari spektroskopi nmr adalah
absorpsi radiasi elektromagnetik dengan frekuensi radio oleh inti atom. Frekuensi
radio berkisar 0.1 sampai 100 MHz atau sama dengan panjang gelombang antara
3000m dan 3m.
Inti atom hidrogen atau proton mempunyai sifat-sifat magnet. Bila suatu
senyawa mengandung hidrogen diletakkan dalam bidang magnet yang sangat kuat
dan diradiasi dengan radiasi elektromagnetik maka inti atom hidrogen dari
dikenal dengan resonansi magnet. Absorpsi radiasi terjadi bila kekuatan medan
magnet sesuai dengan frekuensi radiasi elektromagnetik.
Spektrometer resolusi tinggi memiliki komponen pokok magnet, tempat
sampel, generator FR, osilator FR, detektor FR, dan rekorder. Adapun prinsip
kerja NMR adalah sampel diletakkan diantara 2 kutub magnet dan disinari denga
gelombang radio. Bila proton-proton membalik dari keadaan paralel ke keadaan
anti paralel, penyerapan energi akan dideteksi oleh suatu indikator daya atau
power. Pada spektrometer nmr frekuensi radionya dibuat tetap pada 60 MHz,
sedangkan medan magnet luar diubah-ubah dalam suatu jangka kecil dan
frekuensi absorpsi energinya direkam. Jadi spektrum nmr ialah grafik dari
benyaknya energi yang diserap dengan kuat medan magnet. Spektrum nmr
merupakan nilai pergeseran kimia dari berbagai tipe proton yang relatif terhadap
kedudukan pembanding tetrametilsilan (TMS). TMS digunakan sebagai
pembanding eksternal karena memiliki beberapa keuntungan tidak mudah ereaksi,
mudah menguap, larut dalam kebanyakan pelarut organik dan memberikan
puncak absorpsi tunggal yang tajam pada pergeseran kimia 0 ppm.
Pengujian In Vivo
Pengujian secara in vivo merupakan model pengujian potensi sampel dalam
tubuh mahluk hidup seperti tikus, mencit, kelinci, dan kera. Yamamoto et al.
(2000) menyatakan bahwa ekstrak herba Nomame dapat menghambat enzim
lipase CT II sehingga efektif untuk mengatasi kegemukan pada tikus Sprague
dawley. Pramono et al. (2000) melakukan pengujian antiobesitas secara in vivo
terhadap Rattus norvegicus (tikus putih) dan menyatakan bahwa lendir daun jati
belanda dapat menghambat aktivitas enzim lipase pankreas. Selain secara oral,
pengujian secara in vivo juga umum digunakan untuk analisis sampel di bidang
aromaterapi.
Pengggunaan hewan model dalam pengujian in vivo harus disesuaikan
dengan tujuan penggunaannya. Hewan model juga harus memiliki karakteristik
mudah diperoleh dan dipelihara, mudah ditangani, mudah direproduksi dalam
baik. Tikus merupakan hewan uji kedua terbesar yang digunakan sebagai hewan
model setelah mencit. Tikus yang biasa dijadikan sebagai hewan model berasal
dari jenis Sprague dawley, Wistar, dan Long evans. Jenis Sprague dawley dan
Wistar merupakan jenis yang lazim digunakan di Indonesia. Jenis kelamin dari
hewan model juga perlu dijadikan pertimbangan. Umumnya, pengujian in vivo
menggunakan hewan uji jantan untuk menghindari adanya pengaruh hormonal
seperti hormon estrogen terhadap kondisi tubuhnya. Karena hormon estrogen
dapat mempengaruhi konsentrasi kolesterol darah dalam tubuh hewan uji yang
Alat-alat dan Bahan
Alat-alat yang digunakan adalah peralatan gelas, neraca analitik, pembakar
Bunsen, rangkaian alat distilasi uap, kolom kromatografi, pipa kapiler, GC-MS,
alat bedah, rangkaian alat inhalasi. Bahan-bahan yang digunakan adalah rimpang
kencur, akuades, n-heksana, metanol, aseton, kloroform, dietil eter, etil asetat,
silika gel, batu didih, pakan standar tikus, pakan kolesterol tinggi tikus, larutan
pereaksi kolesterol, larutan pereaksi trigliserida.
Metode
Metode penelitian yang dilakukan mengikuti Gambar 1:
Pada tahap preparasi sampel, sampel kencur segar yang berusia sekitar
1.0-1.5 tahun diperoleh dari pasar induk Kramat Djati. Sampel dideterminasi di
Herbarium Bogoriense Bidang Botani Pusat Penelitian Biologi LIPI-Bogor
(Lampiran 1), diuji kadar air, dan kadar abu. Isolasi minyak atsiri kencur
dilakukan dengan menggunakan destilasi. Minyak atsiri yang diperoleh disimpan
dalam botol tertutup. Untuk memisahkan senyawa-senyawa yang terkandung
dalam destilat minyak atsiri kencur, terlebih dahulu dilakukan penentuan eluen
terbaik menggunakan KLT. Selanjutnya fraksinasi dilakukan menggunakan
kromatografi kolom. Fraksi-fraksi yang telah diperoleh dianalisis jumlah nodanya.
Fraksi dengan rendemen terbanyak, fraksi murni, dan distilat minyak atsiri kencur
dianalisis menggunakan GC-MS untuk menentukan kandungan senyawanya.
Ketiga sampel ini disimpan di dalam botol untuk kemudian diujikan pada hewan
uji untuk mengetahui potensinya sebagai pelangsing atau penurun kolesterol
aromaterapi.
Metode analisis minyak atsiri yang berpotensi sebagai pelangsing
aromaterapi pada hewan uji digambarkan dalam Gambar 2.
Gambar 2. Metode analisis minyak atsiri yang berpotensi sebagai pelangsing
Hewan uji yang digunakan adalah tikus putih jantan galur Sprague-dawley
(Yamamoto et al. 2000). Tikus yang digunakan sebanyak 40 ekor berusia 8
minggu dengan bobot badan 140-160 gram. Tikus dikelompokkan menjadi 5
kelompok. Setiap kelompok berjumlah 8 ekor yang ditempatkan di dalam kotak
plastik bertutup kawat yang berisi 4 ekor tikus untuk setiap kotak. Jadi setiap
kelompok ditempatkan dalam 2 kotak. Adapun penggolongan kelompoknya yaitu
kelompok kontrol normal, kontrol negatif, atsiri kasar, Fraksi 2, dan kristal.
Kelompok kontrol normal merupakan kelompok yang diberi pakan standar dan
tidak diinhalasi. Kelompok kontrol negatif merupakan kelompok yang diberi
pakan kolesterol tinggi dan tidak diinhalasi. Kelompok atsiri kasar diberi pakan
kolesterol tinggi dan diinhalasi minyak atsiri kasar hasil destilasi uap dari rimpang
kencur. Kelompok Fraksi 2 diberi pakan kolesterol tinggi dan diinhalasi
menggunakan Fraksi 2 yang merupakan Fraksi dengan rendemen terbanyak.
Kelompok kristal diberi pakan kolesterol tinggi dan diinhalasi menggunakan
Fraksi senyawa murni.. Masa perlakuan dilakukan selama 5 minggu. Pemberian
pakan dilakukan setiap hari, sehingga bobot pakan ditimbang setiap hari. Bobot
badan tikus ditimbang setiap 1 minggu sekali. Pada minggu ke-5, setelah
perlakuan selesai, dilakukan analisis secara fisik meliputi parameter persentase
kenaikan bobot badan, bobot lemak dan hati. Adapun analisis uji darah meliputi
kadar kolesterol, trigliserida dan HDL darah hewan uji.
Metode analisis darah
Metode analisis darah diawali dengan pengumpulan darah pada minggu
ke-5 setelah masa perlakuan. Darah diambil di bagian ekor hewan uji. Darah
disentrifuga kemudian dipisahkan serum darahnya (bagian cairan jernih) dan
disimpan dengan baik di lemari pendingin. Uji analisis darah yang dilakukan
adalah analisis profil lipid meliputi pengukuran kadar kolesterol, kadar
trigliserida, kadar high density lipoprotein (HDL). Berikut adalah cara kerja
1. Pengukuran kadar kolesterol total
Serum darah sebanyak 0,01 mL dipipet ke dalam tabung reaksi, kemudian
ditambahkan larutan pereaksi kolesterol sebanyak 1 mL. Serapannya diukur
pada panjang gelombang 500 nm terhadap blanko. Sebagai blanko digunakan
pereaksi kolesterol 1 mL dan akuades 0,01 mL.
Pengukuran serapan standar sama dengan pengukuran serapan sampel,
tetapi serum darah diganti dengan standar kolesterol.
Kadar kolesterol total dihitung menggunakan rumus:
Keterangan : C = kadar kolesterol (mg/dL)
A = serapan
C Standar = kadar kolesterol standar
Larutan pereaksi kolesterol dari PT. Rajawali Nusindo terdiri dari buffer
pH 6.5, fenol, 4-aminofenazon, kolesterol esterase, kolesterol oksidase,
peroksidase, sodium azida, standar kolesterol.
2. Pengukuran Kadar Trigliserida
Serum darah sebanyak 0,01 mL dipipet ke dalam tabung reaksi, kemudian
ditambahkan larutan pereaksi trigliserida sebanyak 1 mL. Serapannya diukur
pada panjang gelombang 500 nm terhadap blanko. Sebagai blanko digunakan
pereaksi trigliserida 1 mL dan akuades 0,01 mL.
Pengukuran serapan standar sama dengan pengukuran serapan sampel,
tetapi serum darah diganti dengan standar trigliserida.
Kadar trigliserida total dihitung menggunakan rumus:
Keterangan : C = kadar trigliserida (mg/dL)
A = serapan
C Standar = kadar trigliserida standar
Larutan pereaksi trigliserida dari PT. Rajawali Nusindo terdiri dari buffer
pH 7.5, klorofenol, gliserolkinase, peroksidase, lipase, ATP,
3. Pengukuran kadar HDL
Serum darah sebanyak 0,02 mL dipipet ke dalam tabung reaksi, kemudian
ditambahkan 0,5 mL larutan pengendap kemudian disentrifuga. Pisahkan
supernatannya sebanyak 0,01 mL, kemudian ditambahkan larutan pereaksi
kolesterol sebanyak 1 mL ke dalam supernatan. Serapannya diukur pada
panjang gelombang 500 nm terhadap blanko. Sebagai blanko digunakan
pereaksi kolesterol 1 mL dan akuades 0,01 mL.
Kadar HDL dihitung menggunakan rumus:
Keterangan : C = kadar HDL (mg/dL)
A = serapan
C Standar = kadar kolesterol standar
Metode analisis bobot hati dan bobot deposit lemak pada hewan uji
Metode analisis bobot hati dan bobot deposit lemak dilakukan pada minggu
ke-5 setelah masa perlakuan. Masing-masing tikus dari setiap kelompok perlakuan
dikeluarkan hati dan deposit lemaknya. Kemudian ditimbang bobot hati dan
deposit lemaknya. Adapun lemak yang diambil adalah lemak pada perut bagian
bawah, dan lemak yang membungkus organ di bagian perut.
Metode analisis data
Data yang diperoleh dari percobaan akan dianalisis dengan metode
rancangan acak lengkap (RAL) dan ANOVA (analysis of variance) pada tingkat
kepercayaan 95% (taraf α 0.05). Nilai P<0.05 menunjukkan bahwa terdapat
perbedaan yang nyata terhadap respon yang diukur. Uji lanjut yang digunakan
Kadar Air dan Kadar Abu
Sampel kencur segar yang berusia sekitar 1.0-1.5 tahun diperoleh dari pasar
induk Kramat Djati. Sampel kemudian ditentukan kadar air dan abunya.
Penentuan kadar air dilakukan untuk mengetahui kandungan air di dalam suatu
sampel. Selain itu kadar air pun berguna untuk mengetahui ketahanan
penyimpanan suatu sampel. Sampel akan relatif lebih tahan lama jika
mengandung kadar air < 10 %, karena pada kadar tersebut sampel terhindar dari
mikroba (Winarno 1995). Pada penelitian ini, sampel yang merupakan rimpang
kencur segar memiliki kadar air 85.3 % (Lampiran 2). Hal ini dikarenakan sampel
selanjutnya akan diproses melalui distilasi uap sehingga diperoleh minyak atsiri
kencur. Maka pemilihan sampel segar merupakan pilihan yang terbaik agar
meminimalkan kerusakan dan kehilangan komponen atsiri yang diperoleh karena
minyak atsiri mengandung komponen yang volatil (mudah menguap).
Penentuan kadar abu juga dilakukan pada sampel. Kadar abu ini berguna
untuk mengidentifikasi kandungan mineral-mineral logam pada sampel. Batas
maksimum kadar abu tanaman herbal yang dapat digunakan sebagai obat adalah
5% (Dalimartha 2005). Kadar abu sampel ini adalah 1,35 % berdasarkan bobot
basah (Lampiran 2). Kadar abu ini masih di bawah batas maksimum kadar abu
tanaman herbal yang dapat digunakan sebagai obat, oleh karena itu sampel ini
dapat digunakan sebagai obat.
Isolasi Minyak Atsiri Kencur Menggunakan Destilasi
Isolasi minyak atsiri dari kencur dilakukan menggunakan destilasi dengan
pelarut akuades. Untuk memperoleh 1,2-1,7 mL minyak atsiri kencur dibutuhkan
500g kencur segar, kemudian kencur didestilasi selama 3 jam. Selama proses
distilasi suhu pelarut diatur pada 95-105 ºC, yaitu suhu pada saat air mendidih.
Ketika mendidih, uap air akan membawa komponen-komponen minyak atsiri
terbentuk 2 lapisan, yaitu destilat dan residu. Destilat adalah minyak atsiri kencur,
sedangkan residu adalah lapisan air yang berada di bawah minyak atsiri kencur.
Oleh karena destilat dan residu ini memiliki perbedaan fase, yaitu fasa minyak
dan air, maka keduanya dapat dengan mudah dipisahkan.
Gambar 3. Minyak(pertama dan kedua dari kiri) dan Kristal (ke-3 dan 4 dari kiri)
yang diperoleh dari hasil distilasi
Rendemen minyak atsiri yang dihasilkan dari sampel ini sebesar 0.3%.
Indeks bias minyak atsiri sebesar 1,4958 pada suhu 20ºC diukur menggunakan
refraktometer Abbe-Atago NAR-3T. Densitas minyak atsiri kencur sebesar 0,9433
g/mL yang dibandingkan dengan densitas air sebesar 1,043 g/mL (Lampiran 3).
Pembandingan minyak atsiri kencur dengan air ini bertujuan sebagai faktor
koreksi.
Minyak atsiri kencur hasil distilasi diidentifikasi lebih lanjut menggunakan
GC-MS (Gas Chromatograph-Mass Spektrometer), kemudian diuji aktivitasnya
sebagai pelangsing aromaterapi secara in vivo. Karena dari hasil distilasi ini
diperoleh kristal dan diduga bahwa kristal tersebut adalah senyawa murni, maka
kedua kristal diidentifikasi lebih lanjut menggunakan GC-MS dan NMR (Nuclear
Magnetic Resonance). Untuk tahapan kerja selanjutnya minyak atsiri kencur yang
diperoleh dari hasil destilasi dilanjutkan ke kromatografi kolom untuk
memperoleh fraksi dengan rendemen terbanyak dimana sebelumnya minyak atsiri
kencur tersebut ditentukan terlebih dahulu eluen terbaik menggunakan KLT.
Penentuan Eluen Terbaik
Penentuan eluen terbaik dilakukan menggunakan Kromatografi Lapis Tipis
(KLT) dengan fase diam silika G60F254 dari Merck dan menggunakan beberapa
pelarut dengan rentang non polar ke semi polar. Di bawah ini adalah profil
kromatogram minyak atsiri kencur setelah dielusi menggunakan beberapa pelarut,
H K DE EA Ac M K:H K:H K:H K:H H:EA H:EA H:M
4:6 1:1 6:4 7:3 1:1 9:1 9:1
Ket : H : n-heksana K : kloroform DE : dietil eter EA : etil asetat Ac : aseton M : metanol
K:H : kloroform:n-heksana H:Ea : n-heksana:etil asetat H:M : n-heksana:methanol (H:M)
Gambar 4. Profil kromatogram minyak atsiri kencur dengan berbagai eluen
tunggal dan eluen campuran.
Gambar di atas adalah profil kromatogram minyak atsiri kencur dengan
berbagai eluen secara berturut-turut dari kiri ke kanan n-heksana (H); kloroform
(K); dietil eter (DE); etil asetat (EA); aseton (Ac); metanol (M); dan eluen
campuran berturut-turut kloroform:n-heksana (K:H); n-heksana:etil asetat (H:EA);
n-heksana:methanol (H:M). Maka dapat diambil suatu kesimpulan bahwa pelarut
tunggal n-heksana menghasilkan jumlah noda terbanyak dan terpisah, yaitu 6
noda dibandingkan dengan pelarut tunggal lain dan campuran 2 pelarut. Oleh
karena itu n-heksana dipilih sebagai eluen terbaik karena menghasilkan jumlah
noda terbanyak dan terpisah (Skoog et al 2004). Maka eluen terbaik ini akan
dijadikan dasar dalam penentuan fraksi hasil pemisahan minyak atsiri kencur
Fraksinasi Minyak Atsiri Kencur
Minyak atsiri kencur dipisahkan menggunakan kromatografi kolom untuk
mengidentifikasi komponen-komponen yang terkandung di dalam minyak atsiri
kencur. Fase diam yang digunakan adalah silika gel dan proses elusinya dilakukan
secara gradien (peningkatan kepolaran), karena dengan menggunakan peningkatan
polaritas sistem eluen, semua komponen dalam sampel tersebut akan terbawa
lebih cepat keluar kolom (Harvey 2000). Sampel sebanyak 2 g dimasukan ke
dalam kolom diameter 2 cm dan panjang 30 cm. Sampel kemudian dielusi
menggunakan dua pelarut n-heksana dan kloroform dengan berbagai
perbandingan. Fraksi yang sudah terpisahkan kemudian ditampung dalam vial
sebanyak 5 mL. Kemudian dianalisis menggunakan teknik KLT dengan silika
G60F254 sebagai fase diam, dan fase gerak berupa eluen terbaik dari hasil analisis
sebelumnya yaitu pelarut tunggal n-heksana. Di bawah ini profil KLT hasil
fraksinasi minyak atsiri kencur menggunakan kromatografi kolom.
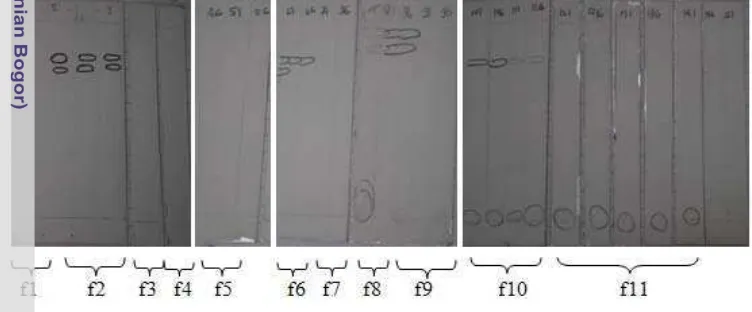
Gambar 5 Profil kromatogram hasil fraksinasi minyak atsiri kencur.
Dengan panduan dari profil KLT di atas, vial-vial yang memiliki noda sama
kemudian digabungkan menjadi satu fraksi, sehingga diperoleh 11 fraksi. Setiap
vial memiliki bau khas yang berbeda-beda. Bau khas tersebut menandakan
senyawa atsiri yang sudah terfraksinasi dan terbawa oleh eluen. Di bawah ini
adalah tabel hasil fraksinasi minyak atsiri kencur menggunakan kromatografi
Tabel 3. Hasil fraksinasi minyak atsiri kencur dengan kromatografi kolom (elusi gradien)
Tabel di atas menunjukkan bahwa fraksinasi minyak atsiri kencur
menghasilkan 11 fraksi. Fraksi 2 memiliki rendemen terbesar yaitu, 28.42%.
Karena Fraksi 2 ini merupakan fraksi dengan rendemen terbanyak, dan memiliki
bau khas yang berbeda dengan minyak atsiri kencur, maka Fraksi 2 dilanjutkan
dengan analisis GC-MS untuk mengidentifikasi komponen yang terkandung di
dalamnya, dan diuji aktivitasnya sebagai pelangsing aromaterapi secara in vivo.
Analisis GC-MS Minyak Atsiri Kencur, Fraksi 2, Kristal Fase Air, dan
Kristal Fase Minyak
Identifikasi minyak atsiri kencur, Fraksi 2, kristal fase air, dan kristal fase
minyak dilakukan dengan menggunakan Agilent Technologies 6890 Gas
Chromatograph with Auto Sampler and 5973 Mass Selective Detector and
Chemstation data system. Dengan parameter operasinya sebagai berikut, gas
pembawa Helium, kolom menggunakan HP WAX 25 (m) X 0.25 (mm) I.D X 0.25 (µm) Film Thickness, temperatur kolom 60-240 ºC, temperatur interface
280ºC , temperatur sumber ion 230 ºC, volume injek 1µL, dan mode laju alir
ionisasinya adalah EI, split ratio: 250:1. Setiap puncak yang muncul dalam
kromatogram ion total diidentifikasi dengan menganalisis dan membandingkan
hasil spektrum massa yang diperoleh dengan spektrum massa pada library index
MS.
Gambar 6 menunjukkan kromatogram GC dari sampel minyak atsiri kencur,
Fraksi 2, kristal fase air, dan kristal fase minyak. Pada kromatogram terlihat
bahwa minyak atsiri kencur memiliki 3 komponen utama yaitu δ-3-carene,
5-metiltrisiklo undek-2-en-4-one atau etil sinamat (nama trivial), dan 2-asam
propenoat,3-(4-metoksifenil)-,etilester atau etil-p-metoksisinamat (nama trivial).
Begitu pula dengan fraksi 2 hasil pemisahan menggunakan teknik kromatografi
kolom, ternyata masih terdapat beberapa komponen di dalamnya dengan δ
-3-carene sebagai komponen utamanya. Untuk kedua kristal yang diperoleh dari
destilasi, baik kristal di fase air ataupun kristal di fase minyak memiliki
komponen yang sama, yaitu senyawa etil-p-metoksisinamat.
Gambar 6. Kromatogram GC-MS dari sampel minyak atsiri kencur, fraksi 2,
kristal fase air, dan kristal fase minyak
Minyak atsiri kencur berdasarkan data GC-MS memiliki komponen etil
p-metoksisinamat dengan kelimpahan yang paling banyak 38,45%. Hal ini sesuai
dengan isolasi minyak atsiri kencur yang dilakukan oleh Tewtrakul (2005) yang
mengandung komponen etil-p-metoksisinamat sebagai komponen terbesarnya
31,77%.
Berikut ini adalah daftar komponen yang terkandung dalam minyak atsiri
kencur, Fraksi 2, kristal fase minyak dan kristal fase air berdasarkan analisis
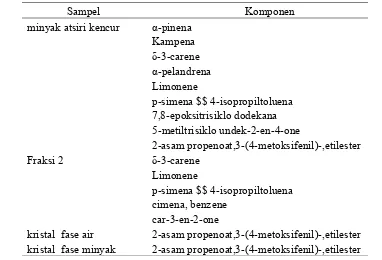
Tabel 4. Komponen yang terkandung dalam sampel berdasarkan analisis GC-MS
Sampel Komponen
minyak atsiri kencur α-pinena
Kampena
δ-3-carene
α-pelandrena
Limonene
p-simena $$ 4-isopropiltoluena
7,8-epoksitrisiklo dodekana
5-metiltrisiklo undek-2-en-4-one
2-asam propenoat,3-(4-metoksifenil)-,etilester Fraksi 2 δ-3-carene
Limonene
p-simena $$ 4-isopropiltoluena
cimena, benzene
car-3-en-2-one
kristal fase air 2-asam propenoat,3-(4-metoksifenil)-,etilester kristal fase minyak 2-asam propenoat,3-(4-metoksifenil)-,etilester
Berdasarkan analisis GC-MS kristal fase air dan fase minyak merupakan
senyawa yang sama walaupun pada saat proses destilasi diperoleh di dua tempat
yang berbeda, yaitu di fase air dan fase minyak. Oleh karena itu, kedua padatan
ini dilanjutkan dengan analisis NMR untuk mengetahui strukturnya. Gambar 7
menunjukkan spektrum hasil analisis 1H-NMR.
Gambar 7. Spektrum 1H-NMR kristal fase air (atas) dan kristal fase minyak
Dari kedua spektrum 1H-NMR di atas terlihat jelas bahwa kedua kristal
memiliki spektrum yang sama. Oleh karena itu kedua kristal tersebut merupakan
senyawa yang sama dengan nama senyawa 2-asam
propenoat,3-(4-metoksifenil)-,etilester atau etil-p-metoksisinamat (nama trivial). Tabel 5 merupakan tabel hasil
analisis spektrum 1H-NMR.
Tabel 5. Hasil analisis spektrum 1H-NMR
No
Hal ini dikuatkan oleh spektrum COSY, HMQC, HMBC (lampiran 5). Adapun
hasil analisis lengkap disajikan pada gambar 8.
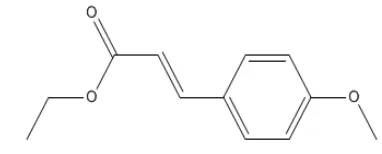
Maka berdasarkan hasil NMR di atas dapat disimpulkan bahwa kristal
kencur merupakan senyawa murni etil-p-metoksisinamat yang memiliki struktur
kimia seperti gambar 9.
Gambar 9. Struktur senyawa etil-p-metoksisinamat (nama trivial)
Uji In Vivo Minyak Atsiri Kencur, Fraksi 2, dan Kristal
Masa adaptasi dilakukan selama 2 minggu sebelum masa perlakuan. Masa
adaptasi ini bertujuan untuk mengkondisikan fisiologis, nutrisi, dan lingkungan
hewan uji. Hewan uji ditempatkan pada suatu kandang plastik bertutup kawat
dengan 4 ekor tikus untuk setiap kandang. Selama masa adaptasi semua kelompok
diberi pakan standar yang sama. Komposisi pakan yang diberikan ke hewan uji
terdiri atas protein, lemak, serat, dsb (lampiran 6). Adapun pakan yang diberikan
pada tikus adalah 20g/ekor/hari, karena konsumsi pakan tikus hanya 10-20
g/ekor/hari (Malole dan Pramono,1989). Selama masa adaptasi dan perlakuan
hewan uji diberi minum menggunakan air minum dalam kemasan tanpa dibatasi
(ad libitum). Sekam diganti setiap 2 kali dalam 1 minggu dan ditimbang bobotnya
untuk melihat pengaruh pemberian perlakuan terhadap pengeluaran feses dan urin.
Hewan uji ditimbang setiap minggu. Masa perlakuan dilakukan selama 5 minggu.
Minyak atsiri kasar, fraksi 2, dan kristal diinhalasikan terhadap hewan uji selama
masa perlakuan dengan konsentrasi masing-masing 1% dalam aquades.
Rangkaian alat inhalasi selama masa perlakuan ditunjukkan pada gambar di
Gambar 10. Rangkaian alat inhalator (kiri), pengumpulan darah (kedua dari kiri)
dan organ (ke-3 dan 4 dari kiri)
Pada akhir masa perlakuan, darah di ambil di bagian ekor tikus sebelum
tikus dibius (anastesi) menggunakan eter teknis. Kemudian tikus dibedah dan
seluruh organ yang diperlukan ditimbang lalu disimpan di dalam formalin.
Analisis Fisik
Data bobot badan, hati, lemak, kolesterol, trigliserida, dan HDL dihitung
dengan metode rancangan acak lengkap (RAL) in time yang dilanjutkan dengan
uji Duncan (Lampiran 7).
Gambar 11 menunjukkan persentase kenaikan bobot badan untuk setiap
kelompok. Di minggu ke 3 hingga akhir masa perlakuan persentase kenaikan
bobot badan menunjukkan perbedaan yang signifikan berdasarkan hasil
perhitungan statistik uji Duncan. Kelompok kristal, Fraksi 2, dan normal memiliki
persentase kenaikan bobot badan yang sama di minggu ke 3 hingga akhir masa
perlakuan. Bahkan kelompok kristal dan Fraksi 2 memiliki persentase kenaikan
terendah dibandingkan kelompok lainnya. Adapun persentase kenaikan bobot
badan kelompok negatif berada jauh di atas ketiga kelompok tadi. Sedangkan
kelompok atsiri kasar mengalami kenaikan bobot badan paling tinggi
dibandingkan dengan kelompok lainnya, bahkan dengan kelompok negatif
sekalipun.
Hal ini dikuatkan oleh data bobot pakan yang dikonsumsi dan bobot feses
dan urin yang dikeluarkan. Pakan yang dikonsumsi oleh ketiga kelompok
perlakuan (atsiri kasar, Fraksi 2, dan kristal) memiliki rata-rata konsumsi pakan
yang lebih rendah dibandingkan kelompok normal dan kelompok negatif. Adapun
kelompok negatif memiliki rata-rata konsumsi pakan yang lebih tinggi daripada
kelompok lainnya, sedangkan bobot feses dan urin kelompok negatif di bawah
kelompok normal. Hal ini kemudian menyebabkan kelompok negatif memiliki
bobot badan yang lebih tinggi dibandingkan kelompok lainnya kecuali kelompok
terendah dibandingkan dengan kelompok lainnya. Begitu pula dengan bobot feses
dan urinnya, kelompok Fraksi 2 memiliki rata-rata bobot feses dan urin terendah.
Oleh karena itu, perlakuan yang diberikan terutama kepada kelompok Fraksi 2
mampu menyebabkan bobot badan paling rendah, menekan nafsu makan hingga
bobot pakan yang dikonsumsinya paling rendah, dan memiliki bobot feses dan
urin yang rendah.
Gambar 11. Persentase kenaikan bobot badan hewan uji tiap minggu (atas) bobot
pakan yang dikonsumsi (kiri bawah), bobot feses dan urin hewan uji
(kanan bawah)
Parameter analisis fisik yang lain adalah bobot lemak dan hati. Untuk data
bobot lemak diperoleh dari lemak yang diambil di perut bagian bawah hingga ke
testis. Berdasarkan hasil perhitungan statistik uji Duncan menunjukkan bobot
Gambar 12. Bobot lemak dan hati hewan uji
Gambar 12 menunjukkan bobot lemak yang tidak memiliki perbedaan yang
signifikan dan bobot hati yang memiliki perbedaan yang signifikan. Berdasarkan
hasil perhitungan statistik uji Duncan kelompok normal memiliki bobot hati yang
terendah dibandingkan kelompok yang lainnya, sedangkan kelompok kristal
memiliki bobot hati yang tertinggi dibandingkan dengan yang lainnya. Adapun
bobot hati kelompok negatif, kelompok minyak atsiri kencur, dan kelompok
fraksi2 dikelompokkan dalam kelompok yang sama dan berada diantara diantara
kelompok normal dan kelompok kristal.
Berdasarkan analisis secara fisik, perlakuan selama 5 minggu yang
diberikan kepada tiap kelompok menunjukkan perbedaan yang signifikan untuk
parameter persentase kenaikan bobot badan, dan bobot hati. Sedangkan parameter
bobot lemak tidak menunjukkan perbedaan yang signifikan antar kelompok. Hal
ini menunjukkan bahwa terdapat pengaruh perlakuan terhadap perubahan fisik
hewan uji. Terutama untuk kelompok perlakuan Fraksi 2 yang memiliki bobot
badan, bobot pakan yang dikonsumsi, dan bobot hati paling rendah diantara
kelompok negatif dan perlakuan lainnya.
Analisis ini dimaksudkan untuk mengetahui profil lipid yang terdapat di darah
setiap kelompok hewan uji. Darah diambil di bagian ekor hewan uji sesaat
sebelum dianastesi. Darah ditampung pada vial sebanyak 2 mL dan diberi label.
Kemudian darah disentrifuga untuk memperoleh serum yang akan di uji HDL,
kolesterol, dan trigliseridanya.
Gambar 13 menunjukkan kadar HDL dan kolesterol hewan uji. Dari data
kadar HDL darah kelompok normal memiliki kadar HDL yang berbeda signifikan
dengan keempat kelompok lainnya. Sedangkan ketiga kelompok perlakuan
memiliki kadar HDL yang tidak berbeda signifikan dengan kelompok negatif. Hal
ini memiliki arti bahwa tidak ada pengaruh pemberian minyak atsiri, Fraksi 2 dan
kristal kencur terhadap kadar HDL hewan uji.
Gambar 13. Kadar HDL dan kolesterol darah hewan uji
Selain kadar HDL dan kadar kolesterol darah, parameter lain yang dijadikan
pengukuran profil lipid darah adalah kadar trigliserida darah. Kadar trigliserida
darah hewan uji disajikan pada gambar 14.
Kadar trigliserida normal untuk hewan uji tikus berada pada batas 25-145
mg/dL (Suckow et al ,2006). Data menunjukkan bahwa kadar trigliserida untuk
kelima kelompok masih termasuk ke dalam kadar trigliserida normal. Meskipun
normal, kelompok kontrol negatif memiliki kadar trigliserida yang berbeda
signifikan dengan keempat kelompok lainnya. Kelompok yang diberi perlakuan
(minyak atsiri kasar, Fraksi2 dan kristal), mampu menurunkan kadar trigliserida
hingga sama dengan kelompok normal dan berbeda secara signifikan dengan
kelompok kontrol negatif. Terutama pemberian inhalasi minyak atsiri kasar
memiliki kadar trigliserida paling rendah dibandingkan dengan kelompok
SIMPULAN
SARAN
Dari penelitian ini perlu diteliti lebih lanjut mengenai konsentrasi optimum
dari minyak atsiri kencur, Fraksi 2, dan kristal kencur untuk mengetahui aktivitas
optimumnya sebagai pelangsing ataupun penurun kadar kolesterol dan trigliserida
darah menggunakan metode aromaterapi dan perlu diteliti lebih lanjut pengaruh
pemberian minyak atsiri kencur, Fraksi2, dan kristal kencur terhadap hati
Anggraeni A. 2010. Fraksinasi senyawa aktif minyak atsiri temulawak sebagai pelangsing aromaterapi secara in vivo. Skripsi: Bogor. Departemen Kimia. Institut Pertanian Bogor.
Birari RB, Bhutani KK. 2007. Pancreatic lipase inhibitors from natural sources: unexplored potential. Drug Discovery Today. 12:379-389.
Buchbauer G. 1993. Biological effects of fragrances and essential oils. Journal Perfumer and Favorist. 18:19-24.
Dachriyanus, Katrin DO, Oktarina R, Ernas O, Suhatri, Mukhtar MH. 2007. Uji efek A-Mangostin terhadap kadar kolesterol total, trigliserida, kolesterol HDL, dan kolesterol LDL darah mencit putih jantan serta penentuan lethal dosis 50 (LD50). J. Sains Tek. Far. 12(2).
Dalimartha S. 2005. Temulawak dalam atlas tumbuhan obat Indonesia. [terhubung berkala]. http://pusdiknakes.or.id/persi-inew/news/content/temulawak_herbal.pdf. [31 Desember 2009].
Giannessi J, Alviar B, Agusta A. 2008. Variously substituted derivatives of guanidine, and their use as medicines with anti-diabetes and/or anti-obesity activity. United States Patents No. 7368605. www.upsto.gov.
Harvey D. 2000. Modern Analytical Chemistry. New York: McGraw-Hill. Hlm 547-549.
Hongratanaworakit, T. 2004. Physiological effects in aromatherapy. Songklanakarin J.Sci. Technol. 26(1): 117-125.
Jirovetz L, Buchbauer G, Jager W, Woidich A, and Nikiforov A. 1992. Analysis of Fragrance Coumpound in Blood Samples of Mice by Gas Chromatography, Mass Spectrometry, GC/FTIR, and GC/AES after inhalation of Sandalwood Oil. J. Bio. Chrrom. 6: 133-134.
Juheini. 2002. Pemanfaatan herba seledri (Apium graveolens L) untuk menurunkan kolesterol dan lipid dalam darah tikus putih yang diberi diit tinggi kolesterol dan lemak. Makara Sains. 6:2.
Lebenthal & Damayanti, 2007. Obesity as a poverty-related emerging nutrition problem in Indonesia. http://ugm.ac.id.
Maniapoto. 2002. Aromatherapy: the language of scent is the sweetest melody. http://nzase.org.nz.
Nurhayati T. 2008. Uji efek sediaan serbuk instan rimpang kencur (Kaempferia galanga L) sebagai tonikum terhadap mencit jantan galur Swiss Webster. Skripsi: Malang. Fakultas Farmasi. Universitas Muhamadiyah Surakarta.
Rostiana O dan Djazuli M. 2007. Varietas unggul kencur. Warta Penelitian dan Perkembangan Pertanian. 29 :2.
Skoog DA, Holler PJ, Nieman TA. 2004. Principles of Instrumental Analysis. Ed ke-5. Philadelphia: Hartcaurt Brace. Hlm 715-730.
Suckow MA., et al. 2006. The Laboratory Rat. 2nd Edition. Elsevier Academic Press.
Sudibyo RS. 2000. The contents of volatile oil isolated from Kaempferia galanga
rhizomes. Mass spectroscopic approach. Majalah Farmasi Indonesia. 11 (3) : 142-149.
Tewtrakul S, Yuenyongsawad S, Kummee S, Atsawajaruwan S. 2005. Chemical components and biological activities of volatile oil of Kaempferia galanga
Linn. Songklanakarin J. Sci. Technol. 27 : 503-506.
Tjay TH, Rahardja K, 2003. Obat-obatan penting khasiat, penggunaan, dan efek-efek sampingnya. PT. Elexmedia Komputindo. Kelompok Gramedia-Jakarta.
Winarno FG. 1995. Kimia Pangan dan Gizi. Jakarta: Gramedia Pustaka Utama. Hlm 81-82.
Yamamoto M, Shimura S, Itoh Y, Ohsaka T, Egawa M, Inoue S. 2000. Anti-obesity effect of lipase inhibitor CT-II, an extract from edible herbs,
Kaempferia galanga L Essential oil as Aromatherapy for Antiobesity using In Vivo Analysis. Under direction of TUN TEDJA IRAWADI and IRMANIDA BATUBARA
The purposes of this research were to separate constituents of kencur (Kaempferia galanga L) essential oil and to evaluate their active components as aromatherapy for antiobesity using in vivo analysis to the male Sprague-dawley rats. Volatile oil of dried rhizome of K. galanga L obtained by water distillation. Its chemical components determined using gas chromatography and mass spectrometry (GC-MS). The main components of volatile oil isolated were α-pinene, camphene, δ -3-carene, α-phellandrene, limonene, p-cymene 4-isopropyltoluene, 7,8-epoxytricyclo dodecana, 5-methyltricyclo undec-2-en-4-one, 2-propenoic methoxyphenyl)-, ethyl ester. Pure compound (2-propenoic acid,3-(4-methoxyphenyl)-, ethyl ester) was determined the structure by GC-MS and NMR analysis. A total of forty male Sprague-dawley rats were used for this study. They were divided into five groups i.e. (1) a normal control group, without treatment of both high cholesterol diet and inhalation, (2) a negative control group was treated by high cholesterol diet only, without inhalation treatment, (3) treated with high cholesterol diet followed by treatment with inhalation of crude oils, (4) Treated with high cholesterol diet followed by inhalation one of essential oils fraction, and (5) Treated with high cholesterol diet followed inhalation of 2-propenoic acid,3-(4-methoxyphenyl)-, ethyl ester. Treatment condition was achieved by five months. Rat’s weight and stool were weighed every day during the treatment period. Blood cholesterol total (LDL, HDL and Triglyceride) level was determined in the end of treatment period. Duncan test analysis showed that percentage increase in body weight and liver weight has significant difference but fat weight wasn’t significant difference. For blood test analysis HDL, Cholesterol, and Triglyceride level has significant difference. The conclusion were kencur essential oil has ethyl-para-methoxycinnamate as pure compound, based on in vivo test analysis fraction has potentially as antiobesity and crude oils and pure compound has potentially decreased cholesterol and triglyceride using aromatherapy method.
Latar Belakang
Lemak merupakan salah satu komponen makanan yang dibutuhkan oleh
tubuh. Tetapi jika seseorang mengkonsumsi lemak secara berlebihan akan
mengakibatkan terjadi penumpukan lemak tubuh yang disebut dengan kelebihan
berat badan atau identik dengan obesitas. Obesitas merupakan keadaan
berlebihnya lemak tubuh (Lebenthal & Damayanti 2007). Obesitas dapat
mengganggu penampilan dan memiliki resiko terhadap berbagai penyakit
diantaranya hiperkolesterol, penyempitan pembuluh darah, diabetes, tekanan
darah tinggi, dan penyakit jantung koroner (Giannessi et al. 2008). Selain itu
obesitas juga dapat mengganggu penampilan. WHO menyatakan bahwa obesitas
adalah salah satu dari 10 faktor paling beresiko di seluruh dunia. Bahkan hal ini
mulai mengancam negara-negara di benua Asia. Salah satunya di Indonesia pada
tahun 2000, jumlah penduduk yang mengalami overweight mencapai 17,5 %, dan
pasien obesitas 4,7 %.
Oleh karena itu, penanganan atau pencegahan terjadinya obesitas sangat
diperlukan sehingga dapat mencegah penyakit yang ditimbulkan oleh obesitas.
Terapi non farmakologis seperti diet dan gerak badan lebih diutamakan untuk
pencegahan obesitas, tetapi terapi nonfarmakologis seperti penggunaan obat
sintetik ataupun obat herbal juga dilakukan untuk penanganan obesitas. Obat
antiobesitas atau pelangsing memiliki fungsi mengurangi nafsu makan,
merangsang pembakaran lemak, dan menghambat penyerapan lemak dalam batas
tertentu (Birari & Bhutani 2007). Obat pelangsing yang ada di pasaran terdiri atas
obat pelangsing sintetik dan obat pelangsing alami yang dibuat secara tradisional.
Kedua jenis obat ini biasanya dikonsumsi secara oral. Namun jenis obat
pelangsing yang sedang dikembangkan adalah obat pelangsing aromaterapi dari
tanaman herbal. Kandungan tanaman herbal yang berpotensi sebagai pelangsing
aromaterapi adalah minyak atsirinya (Maniapoto 2002).
Kencur (Kaempferia galanga L) merupakan salah satu jenis rimpang yang
lazim digunakan oleh masyarakat Indonesia. Kencur memiliki kandungan minyak