ABSTRACT
RAMATINA. Effectiveness of Various Antioxidant Supplements on Reducing Oxidative Status (Level of Plasma Malondialdehid (MDA)) among Extension Students of Bogor Agriculture University. Supervised by LEILY AMALIA and IKEU EKAYANTI.
The objective of this study was to analyze the effectiveness of vitamin C, vitamin E and multivitamin-mineral supplements on level of plasma malondialdehyde (MDA) among extension students of Bogor Agricultural University. The samples were 24 students and divided into 4 groups, namely 1) control group, 2) vitamin C group (given supplement of vitamin C 500 mg), 3) vitamin E group (given supplement of vitamin E 200 IU), 4) multivitamin-mineral group (given supplement consist of vitamin C 500 mg, vitamin E 30 mg, zinc 15 mg and copper 1,5 mg). The interventions of supplements were given for 7 days. In term of intake an adequate level of energy, protein, vitamin and mineral samples. From food, they were no significantly differences among groups. Before the intervention, blood samples were taken for the analysis of early plasma level of MDA. Examination was repeated at the end of treatment. From the results of statistical analysis known that there are significant differences (p <0.05) between plasma MDA levels before and after intervention. There was no significant difference (p> 0.05) between the average reduction in level of MDA plasma in group of vitamin C, vitamin E and multivitamins, but there are significant differences (p <0.05) between the control group of intervention with vitamin C, vitamin E and multivitamin-mineral. Based on this study, it can be concluded that by consuming vitamin C, vitamin E or a multivitamin-mineral supplement every day had relatively similar effects in reducing level of MDA plasma among healthy young women.
PENDAHULUAN
Latar Belakang
Radikal bebas atau sering disebut oksidan merupakan hal yang normal dan terbentuk secara terus menerus dalam tubuh manusia. Tubuh manusia mengonsumsi oksigen sekitar 250 gram setiap hari, dari jumlah tersebut 3-5% diubah menjadi oksigen reaktif. Oksigen reaktif (reactive oxygen species atau ROS) dapat terbentuk secara endogen maupun eksogen, sebagai bagian dari aktivitas metabolik regular, aktivitas fisik, gaya hidup dan diet. Stress oksidatif pada manusia, terutama di perkotaan cenderung meningkat. Stress oksidatif disebabkan oleh paparan seperti radiasi, rokok, polusi udara, logam berat, pestisida dan food additive (Miharja 2005).
Keadaan stress oksidatif biasanya terjadi bila jumlah radikal bebas lebih tinggi dibandingkan jumlah antioksidan dalam tubuh. Stress oksidatif tubuh dapat ditentukan dengan mengukur salah satu parameternya, yaitu kadar malondialdehid (MDA) dalam plasma. Semakin tinggi kadar MDA plasma maka semakin tinggi stress oksidatif yang terjadi dalam sel-sel tubuh (Valko 2006). Konsentrasi MDA dalam material biologi telah digunakan secara luas sebagai indicator kerusakan oksidatif pada lemak tak jenuh sekaligus merupakan indikator keberadaan radikal bebas (Zakaria 1996).
Makhluk hidup memiliki cara untuk melindungi tubuh dari bahaya radikal bebas atau dikenal sebagai spesies oksigen reaktif (Reactive Oxigen Species, ROS) yang terbentuk sebagai hasil dari metabolisme oksidatif yaitu dengan sistem antioksidasi tubuh. Secara alami tubuh dapat menghasilkan antioksidan, seperti superoksida dismutase (SOD), katalase (CAT), glutation peroksidase (GPx), glutation reduktase (GR) dan seruloplasmin dan disebut sebagai antioksidan endogen. Bila sistem antioksidan endogen tidak mencukupi untuk mengatasi radikal bebas, maka sangat dibutuhkan antioksidan dari luar (antioksidan eksogen) seperti vitamin E, vitamin A, vitamin C dan senyawa-senyawa flavonoid untuk mencegah kerusakan oksidatif yang dapat mengakibatkan terjadinya berbagai macam penyakit (Simanjuntak 2007).
peroksidasi lipid melalui penurunan kadar MDA dalam plasma. Penelitian Pironi et al (1998) pada 6 laki-laki dan 6 perempuan yang diberikan formulasi tokoferol, seng (Zn), tembaga (Cu), dan mangan yang direkomendasikan oleh American Medical Association dapat mempertahankan aktivitas SOD dan stress peroksidatif. Meskipun demikian, penelitian yang membandingkan efektivitas antar suplemen vitamin C, vitamin E dan multivitamin-mineral sebagai antioksidan terhadap radikal bebas dalam tubuh masih terbatas. Di samping itu, kebiasaan masyarakat dalam mengonsumsi suplemen antioksidan menjadi fenomena tersendiri.
Mahasiswi alih jenis merupakan salah satu kelompok yang rentan terkena berbagai radikal bebas yang berasal dari aktivitas metabolik regular, aktivitas fisik, gaya hidup maupun diet. Perkuliahan yang dimulai pada sore hari sampai malam, tidur yang terlalu larut menuntut tubuh untuk lebih banyak beraktivitas (stress), Selain itu, polutan yang berasal dari asap kendaran bermotor, rokok (pasif) dan lainnya. Tidak hanya itu, makanan juga dapat menjadi penyebab meningkatnya radikal bebas dalam tubuh. Mahasiswi alih jenis sangat gemar mengonsumsi makanan gorengan seperti tempe, bakwan, molen, pisang, tahu, combro, ubi dan kentang karena harganya yang murah, ataupun pecel ayam dan pecel lele. Baik gorengan maupun pecel ayam ataupun lele yang dijual, digoreng menggunakan minyak yang berwarna keruh hampir berwarna hitam menandakan minyak telah digunakan berulang-ulang oleh penjual. Minyak tersebut memiliki peroksida lipid yang tinggi dan mungkin dapat menjadi penyebab meningkatnya radikal bebas dalam tubuh.
Penelitian Foote et al (2003) menunjukkan bahwa faktor jenis kelamin mempengaruhi konsumsi suplemen makanan, dimana konsumsi suplemen di kalangan perempuan lebih tinggi dibandingkan laki-laki (56% Vs. 48%). Hasil survey Fitriani (2007) konsumen suplemen perempuan Indonesia mencapai 18,9 % dari seluruh populasi perempuan dewasa Indonesia.
mempertimbangkan berbagai hasil penelitian sebelumnya dan fenomena kebisaan mengonsumsi suplemen di kalangan mahasiswi Alih Jenis dinilai perlu dilakukan penelitian untuk membandingkan efektifitas suplemen vitamin C, vitamin E dan multivitamin-mineral terhadap penurunan status oksidatif dengan menggunakan parameter kadar MDA plasma pada mahasiswi alih jenis Institut Pertanian Bogor.
Tujuan
Tujuan Umum
Secara umum penelitian ini bertujuan untuk mengetahui efektivitas suplemen vitamin C, vitamin E dan multivitamin-mineral terhadap penurunan status oksidatif dengan parameter kadar malondialdehid (MDA) plasma mahasiswi alih jenis Institut Pertanian Bogor.
Tujuan Khusus
Secara khusus penelitian ini bertujuan untuk : 1. Mengetahui karakteristik individu sampel.
2. Menganalisis konsumsi pangan sumber vitamin C, vitamin E, seng dan Tembaga sampel.
3. Menganalisis asupan dan tingkat kecukupan energi dan zat gizi rata-rata sampel per hari.
4. Menganalisis kadar MDA plasma sampel sebelum dan setelah pemberian suplemen.
5. Mengetahui perbedaan penurunan kadar MDA plasma sampel antar kelompok yang diberi suplemen vitamin C, vitamin E dan multivitamin-mineral.
Hipotesis
1. Pemberian suplemen vitamin C dapat menurunkan kadar MDA plasma. 2. Pemberian suplemen vitamin E dapat menurunkan kadar MDA plasma. 3. Pemberian suplemen multivitamin-mineral dapat menurunkan kadar MDA
plasma.
Manfaat Penelitian
TINJAUAN PUSTAKA
Radikal Bebas
Radikal bebas dapat didefinisikan sebagai suatu molekul, atom, atau beberapa atom yang mempunyai satu atau lebih elektron tidak berpasangan pada orbit luarnya sehingga bersifat sangat reaktif. Suatu molekul bersifat stabil bila elektronnya berpasangan, tetapi bila tidak berpasangan (single) molekul tersebut menjadi tidak stabil dan memiliki potensi untuk merusak. Bila molekul tidak stabil ini mengambil satu elektron dari senyawa lain maka molekul tersebut menjadi stabil sedangkan molekul yang diambil elektronnya menjadi tidak stabil berubah menjadi radikal dan memicu reaksi pembentukan radikal bebas berikutnya (reaksi berantai) (Yuniastuti 2008).
Menurut Yuniastuti (2008) radikal bebas bersumber dari berbagai hal, antara lain: radiasi sinar X dan sinar ultraviolet, polusi udara akibat asap kendaraan bermotor, gas buang dari pabrik, atau asap rokok. Beberapa kondisi juga bisa memicu terbentuknya radikal bebas di dalam tubuh, misalnya stress, sakit, olah raga berlebihan dan lain-lain. Radikal bebas dapat menyebabkan kerusakan pada sel karena dapat menimbulkan kerusakan pada protein, (aktivitas enzim terganggu) dan asam nukleat (kerusakan DNA, mutasi sel). Sebagai akibatnya. pertumbuhan dan perkembangan sel menjadi tidak wajar, bahkan dapat menyebabkan kematian sel.
Radikal dalam tubuh berasal dari dalam (endogen) atau dari luar tubuh (eksogen). Secara endogen, radikal bebas terbentuk sebagai respon normal dari rantai peristiwa biokimia dalam tubuh. Secara alamiah radikal bebas dibentuk dalam tubuh makhluk hidup termasuk manusia, binatang dan tumbuhan. Dalam kondisi normal jumlah radikal tersebut berada dalam keseimbangan atau terkendali. Sumber radikal bebas endogen tersebut berasal dari proses otooksidasi, oksidasi enzimatik, respiratory burst, reaksi yang dikatalisis ion logam transisi, dan ischemia reperfusion injury (Khachik 2002).
Radikal terpenting yang terdapat dalam tubuh merupakan derivat oksigen atau oksi-radikal yang sering disebut reactive Oxygen Species (ROS). Radikal tersebut terdapat dalam bentuk singlet oxygen (1O2*), anion superoksida (O2*),
radikal hidroksil (OH*), nitrogen oksida (NO*), peroksinitrit (ONOO-), asam hipoklor (HOCl), hydrogen peroksida (H2O2), radikal alkoksil (LO*) dan radikal
Berbagai jenis reactive Oxygen Species (ROS) dalam tubuh diperlihatkan pada Tabel 1, dari tabel tersebut terlihat bahwa diantara berbagai ROS terdapat molekul yang bukan radikal bebas, yaitu 1O2 dan H2O2, namun karena sifatnya
yang sangat reaktif maka dimasukkan ke dalam kelompok ini (Kurnani 2001).
Tabel 1 Jenis-jenis Reactive Oxygen Species (ROS)
ROS Keterangan
Anion superoksida O2* Tidak terlalu merusak, tetapi dapat membentuk
hidrogen peroksida, yang merupakan reduktan logam transisi dalam pembentukan radikal hidroksil
Radikal hidroksil OH* Radikal pengoksidasi yang sangat reaktif dan dapat bereaksi dengan hampir seluruh biomolekul
Radikal peroksil LO2* Dihasilkan antara lain pada proses peroksidasi
lipid Hydrogen
peroksida
H2O2. Hidrogen peroksida bukan radikal bebas tetapi
dikategorikan sebagai ROS. Molekul ini merupakan sumber radikal hidroksil dalam kondisi jenuh ion logam transisi, juga terlibat dalam pembentukan HOCl
Oksigen singlet 1O2 Meskipun bukan radikal bebas, tetapi merupakan
pengoksidasi yang kuat.
Nitrogen oksida NO* Radikal bebas dalam bentuk gas Peroksinitrit ONOO- Terbentuk dari reaksi NO* dengan O2*
Asam hipoklor HOCl Dihasilkan oleh netrofil pada proses inflamasi terbentuk dari H2O2 dan Cl- yang dikatalisis oleh
mieloperoksidase.
Secara eksogen, radikal bebas diperoleh dari bermacam-macam sumber antara lain polutan, makanan dan minuman, radiasi, ozon dan pestisida. Radikal bebas diproduksi di dalam sel oleh mitokondria, lisosom, peroksisom, endoplasmic reticulum dan inti sel. (Muchtadi 2009). Sekitar 90% pencemar udara terdiri atas karbon monoksida, nitrogen oksida, sulfur oksida, dan hidrokarbon (Kurniani 2001).
Secara umum, menurut Winarsi (2011) tahapan reaksi pembentukan radikal bebas melalui tiga tahapan reaksi sebagai berikut :
a. Tahapan inisiasi, yaitu tahapan pembentukan radikal bebas. b. Tahapan propagasi, yaitu pemanjangan rantai radikal.
Antioksidan
Menurut Winarsi (2011) senyawa antioksidan adalah senyawa pemberi elektron (electron donors). Secara biologis, pengertian antioksidan adalah senyawa yang mampu menangkal atau meredam dampak negatif oksidan dalam tubuh. Antioksidan bekerja dengan cara mendonorkan satu elektronnya kepada senyawa yang bersifat oksidan sehingga aktivitas senyawa oksidan tersebut bisa dihambat.
Menurut Kumalaningsih (2007), antioksidan adalah senyawa yang mempunyai struktur molekul yang dapat memberikan elektronnya dengan cuma-cuma kepada molekul radikal bebas tanpa terganggu sama sekali fungsinya dan dapat memutus reaksi berantai dari radikal bebas. Menurut Hillbom dalam Sulistyowati (2006), antioksidan adalah senyawa dalam kadar rendah mampu menghambat oksidasi molekul target sehingga dapat melawan atau menetralisir radikal bebas.
Dikenal ada tiga kelompok antioksidan, yaitu antioksidan enzimatik, antioksidan pemutus rantai dan antioksidan logam transisi terikat protein. Yang termasuk antioksidan enzimatik adalah superoksida dismutase (SOD), katalase (CAT), gluthathion peroksidase (GPx), gluthathion reduktase (GR) seruloplasmin. Mekanisme kerja antioksidan enzimatik adalah mengkatalisir pemusnahan radikal bebas dalam sel. Antioksidan pemutus rantai adalah molekul kecil yang dapat menerima dan memberi elektron dari atau ke radikal bebas, sehingga membentuk senyawa baru yang stabil, contoh antioksidannya adalah vitamin E dan vitamin C. Sedangkan antioksidan logam transisi terikat protein bekerja mengikat ion logam seperti fe2+ dan Cu2+ contohnya Flavonoid dapat mencegah radikal bebas. Antioksidan jenis ini memperbaiki kerusakan sel-sel dan jaringan yang disebabkan radikal bebas(Winarsi 2011).
logam-logam (sequestram). Sebagai contoh, satu molekul asam sitrat akan mengikat prooksidan Fe seperti sering dilakukan pada minyak kacang kedelai.
Mekanisme antioksidan dalam menghambat oksidasi atau menghentikan reaksi berantai pada radikal bebas dari lemak yang teroksidasi dapat disebabkan oleh empat macam mekanisme reaksi, yaitu: 1). Pelepasan hidrogen dari antioksidan, 2) Pelepasan elektron dari antioksidan, 3). Adisi lemak ke dalam cincin aromatik pada antioksidan, 4). Pembentukan senyawa kompleks antara lemak dan cincin aromatik dari antioksidan (Winarti 2010).
Gambar 1 Cara Kerja Antioksidan
RH + O2 R* + OOH
Asam lemak tak jenuh Oksigen Radikal bebas R* + O2 ROO*
Radikal bebas Oksigen Peroksida aktif
Apabila dalam suatu asam lemak yang terdapat dalam minyak tidak mengandung antioksidan, maka peroksida aktif akan bereaksi dengan ikatan rangkap lemak. Apabila ditambah suatu antioksidan, maka peroksida aktif akan bereaksi dengan antioksidan tersebut. Sehingga pembentukan radikal bebas dapat dihentikan dengan penambahan suatu antioksidan.
Vitamin C (Asam Askorbat)
Vitamin C adalah vitamin larut air yang tidak disimpan oleh tubuh, diekresikan melalui urine. Dalam keadaan murni vitamin C berbentuk kristal putih dengan berat molekul 176,13 dan rumus molekul C6H6O6, vitamin C juga mudah
teroksidasi secara reversible membentuk asam dehidro-L askorbat dan kehilangan 2 atom hidrogen. Vitamin C memiliki struktur yang mirip dengan struktur monosakarida, tetapi mengandung gugus enadiol (Zakaria et al 1996).
Vitamin C terdapat dalam dua bentuk di alam, yaitu L-asam askorbat (bentuk tereduksi) dan L-asam dehidro askorbat (bentuk teroksidasi). Oksidasi bolak-balik L-asam askorbat menjadi L-asam dehidro askorbat terjadi bila bersentuhan dengan Cu, panas atau alkali. Kedua bentuk vitamin C aktif secara biologik tetapi bentuk tereduksi adalah yang paling aktif (Almatsier 2004).
Menurut Muchtadi et al (1993) isomer-L. Isomer ini memiliki aktivitas lebih besar di bandingkan dengan bentuk isomer D. Aktivitas vitamin C bentuk D hanya 10% dari aktivitas isomer L.
Vitamin C adalah vitamin yang penting dalam diet manusia. Vitamin ini banyak ditemukan dalam jaringan tanaman, Daun-daunan hijau mengandung vitamin C dalam jumlah yang sama dengan yang dikandung klorofil.
Takaran yang dianjurkan untuk konsumsi vitamin C adalah; anak-anak: 30-45 mg/hari, wanita dewasa: 60 mg/hari, pria dewasa: 60 mg/hari. Pada RDA (Recommended Dietary Allowances), maka anjuran konsumsi vitamin C adalah 60-100 mg/hari. Sementara untuk pengobatan dosisnya bisa mencapai 1000-2000 mg/hari (Winarti 2010).
Board-institute of Medicine (FNB-IOM) (2004) adalah 2000 mg/hari, pada asupan normal dapat diabsorpsi sebesar 90-95%, asupan lebih dari 60 mg akan meningkatkan ekskresi bentuk vitamin C secara proporsional (WNPG 2004). Tubuh dapat menyimpan hingga 1500 mg vitamin C bila konsumsi mencapai 100 mg sehari (Almatsier 2004).
Vitamin C sebagai Antioksidan
Vitamin C atau L-asam askorbat merupakan antioksidan yang larut dalam air (aqueous antioxidant). Senyawa ini, menurut Zakaria et al (1996), merupakan bagian dari sistem pertahanan tubuh terhadap senyawa oksigen rektif dalam plasma dan sel.
Sebagai antioksidan, vitamin C bekerja sebagai donor elektron, dengan cara memindahkan satu elektron ke senyawa logam Tembaga. Selain itu, vitamin C juga dapat menyumbangkan elektron ke dalam reaksi biokimia intraseluler dan ekstraseluler. Vitamin C mampu menghilangkan senyawa oksigen reaktif di dalam sel netrofil, monosit, protein lensa dan retina. Vitamin ini juga dapat bereaksi dengan Fe-ferritin. Di luar sel, vitamin C mampu menghilangkan senyawa oksigen reaktif, mencegah terjadinya LDL teroksidasi, mentransfer elektron ke dalam tokoferol teroksidasi, dan mengabsorpsi logam dalam saluran pencernaan (Levine et al 1995).
Vitamin C mampu mereduksi radikal superoksida, hidroksil, asam hipoklorida, dan oksigen reaktif yang berasal dari netrofil dan monosit yang teraktivasi. Antioksidan vitamin C mampu bereaksi dengan radikal bebas, kemudian mengubahnya menjadi radikal askorbil. Senyawa radikal terakhir ini akan segera berubah menjadi askorbat dan dehidroaskorbat. Asam askorbat dapat bereaksi dengan oksigen teraktivasi, seperti anion superoksida dan radikal hidroksil. Pada konsentrasi rendah, vitamin C bereaksi dengan radikal hidroksil menjadi askorbil yang sedikit reaktif, sementara pada kadar tinggi, asam ini tidak akan bereaksi (Zakaria et al 1996).
komponen cair lainnya. Askorbat juga melindungi makromolekul penting dari kerusakan oksidatif. Reaksinya terhadap radikal hidroksil terbatas hanya melalui proses difusi (winarsi 2011).
CH2OH
Gambar 2 Struktur asam askorbat dan metabolitnya
Sebagai antioksidan, askorbat akan bereaksi dengan radikal superoksida, hidrogen peroksida, maupun radikal tokoferol membentuk asam monodehidro askorbat dan atau asam dehidroaskorbat reduktase, yang ekuivalen dengan NADPH atau glutation tereduksi. Dehidroaskorbat selanjutnya dipecah menjadi tartarat dan oksalat.
meregenerasi bentuk aktif metabolik dari antioksidan lipid vitamin E (α-tocopherol recycling) (Combs dalam Sareharto 2010).
Asam askorbat dapat mendonorkan satu atom hidrogen pada radikal tokoferoksil dengan kecepatan 2x105/M/s. Karena adanya perbedaan potensial reduksi 1 –elektron standar antara asam askorbat (282 mV) dan tokoferol (480 mV) (Muchtadi 2009).
Vitamin E
Vitamin E adalah salah satu fitonutrien penting dalam minyak makan. Vitamin ini secara alami memiliki 8 isomer yang dikelompokkan dalam 4 tokoferol
α, , , dan δ tokotrienol α, , , homolog. Suplemen vitamin E yang ada di
pasaran umumnya tersusun atas tokoferol dan tokotrienol yang diyakini merupakan atioksidan potensial (Winarsi 2011).
Berdasarkan jumlah gugus metil pada inti aromatik tokotrienol, dikenal 6
jenis tokoferol, yaitu α, , , , , dan , di antara keenam bentuk tokoferol
tersebut, yang paling aktif adalah α tokoferol. Oleh sebab itu, aktivitas vitamin E
diukur sebagai α tokoferol.
Menurut Almatsier (2004) ada empat jenis tokoferol yang penting dalam makanan α, , , tokoferol dan tokotreinol. Karakteristik kimia utamanya adalah bertindak sebagai antioksidan. Tokoferol terdiri atas struktur cincin 6-kromanol dengan rantai samping jenuh panjang enam belas karbon fitol. Perbedaan antarjenis tokoferol terletak pada jumlah dan posisi gugus metal struktur cincin.
Tokotrienol mempunyai tiga ikatan rangkap pada rantai samping. Perbedaan struktur ini mempengaruhi tingkat aktivitas enzim vitamin E secara biologik. Tokotrienol tidak banyak terdapat di alam dan kurang aktif secara biologik. Alfa-tokoferol adalah bentuk vitamin E paling aktif, yang digunakan pula sebagai standar pengukuran vitamin E dalam makanan. Jumlah vitamin E dalam bentuk lain disignifikankan dalam bentuk tokoferol ekivalen (TE). Bentuk sintetik vitamin E mempunyai aktivitas biologik 50% daripada alfa-tokoferol yang terdapat di alam (Almatsier 2004).
food and nutrition Board and Institute of medicine (IOM) (2000) adalah 1000 mg/hari, yang di dapatkan dari suplemen.
Vitamin E sebagai Antioksidan
Vitamin E adalah vitamin larut lemak yang sangat berguna selain sebagai antioksidan. Yang terpenting dan paling diakui peran dari vitamin E yaitu melindungi polyunsaturated fatty acids PUFAs) seperti linoleat, linolenic dan arachidonic acids (Pryor dalam B. A. Bowman & R. M. Russell 2001). Selain itu, vitamin E di dalam tubuh sebagai antioksidan alami yang membuang radikal bebas dan molekul oksigen, yang penting dalam mencegah peroksidasi membran asam lemak tak jenuh (Burke 2007).
Sebagai antioksidan, α tokoferol memiliki potensi lebih tinggi daripada tokoferol yang dikenal sebagai vitamin E. Tokoferol, terutama α tokoferol merupakan antioksidan yang mampu mempertahakan integritas membran. Senyawa tersebut dilaporkan bekerja sebagai scavenger radikal bebas oksigen, peroksida lipid, dan oksigen singlet (Winarsi 2011). Menurut Archerio et al (1992)
α tokoferol merupakan bentuk suplemen vitamin E yang paling banyak.
Vitamin E atau α tokoferol merupakan antioksidan yang larut dalam
lemak. Sebagai antioksidan vitamin E berfungsi sebagai donor ion hidrogen yang mampu merubah radikal peroksil (hasil peroksida lipid), menjadi radikal tokoferol yang kurang reaktif, sehingga tidak mampu merusak rantai asam lemak (Winarsi 2011). Di samping itu menurut Salonen et al (1997), vitamin E dan vitamin C dan
karoten atau kombinasinya dapat menghambat peroksida lipid secara in vivo. Sebagai antioksidan vitamin E mampu bereaksi dengan radikal bebas lipid membran membentuk radikal vitamin E yang sedikit reaktif. Menurut Halliwel et al (1992) radikal vitamin E dapat mengalami regenerasi oleh adanya glutation atau asam askorbat.
Tokotrienol telah dibuktikan mempunyai aktivitas anti-kanker, dan mempunyai kemampuan menurunkan kadar kolesterol. Beberapa penelitian in vitro memperlihatkan bahwa tokotrienol dapat menghambat oksidasi terhadap LDL, lebih baik dibandingkan tokoferol.
kroman yang aktif terletak pada permukaan sel. Struktur yang unik tersebut menyebabkan tokoferol dapat bekerja secara efektif sebagai antioksidan, dan dapat diregenerasi melalui reaksi dengan antioksidan lain seperti asam askorbat.
α-tokoferol mempunyai aktivitas vitamin E dan kemampuan inaktivasi singlet oxygen lebih tinggi dibandingka beta-, gamma-, dan delta-tokoferol, sedangkan gamma tokoferol mempunyai kemampuan menangkap nitrogen dioksidan dan radikal peroksinitrit dibandingkan alfa-tokoferol. Efesiensi penangkapan radikal-radikal hidroksil, akoksil dan peroksil oleh alfa-tokoferol berturut-turutadalah sekitar 1010, 108 dan 106/M/s.
Seseorang tidak akan memperoleh cukup vitamin E hanya dari makanan yang dikonsumsi. Agar dapat bertindak sebagai antioksidan, seseorang harus mengonsumsi vitamin E lebih dari AKG, umunya sekitar 100 mg/hari (Muchtadi 2009).
Multivitamin
Suplemen multivitamin adalah multivitamin tambahan pada orang dewasa sebagai pelengkap multivitamin pokok yang berasal dari makanan utama untuk menjaga vitalitas dan kesehatan seseorang. Menurut Ransley et al (2001), Multivitamin merupakan kombinasi dari berbagai vitamin, atau berbagai vitamin dan mineral.
Menurut Ahira (2007), mesignifikankan bahwa suplemen multivitamin adalah vitamin yang diolah sedemikian rupa dan sudah berbentuk pil atau kapsul, yang dapat mengandung berbagai vitamin dan mineral seperti vitamin C, seng (Zn), tembaga (Cu), selenium (Se) dan lain-lain.
Superoksida dismutase (SOD) yang merupakan salah satu antioksidan endogen yang mengandung logam-logam esensial tembaga (Cu) dan seng (Zn) untuk melakukan fungsi katalisasi beberapa reaksi kimia dalam sel. Dalam keadaan bebas, besi dan tembaga adalah promotor berkemampuan sangat besar dalam melakukan reaksi oksidasi yang merusak. Logam-logam ini juga dibutuhkan dalam pertahanan antioksidan. Logam-logam ini berikatan dengan SOD dan mengkatalis reaksi dua molekul superoksida dengan ion H+ untuk membentuk hidrogen peroksida (H2O2) dan O2. SOD yang berikatan dengan
logam dapat mempercepat SOD dilepaskan di darah, sehingga sel darah manusia dapat dilindungi dari serangan radikal bebas.
air. Se berfungsi sebagai bagian integral dari sistem enzim glutation peroxidase, merubah bentuk reaksi glutathin (GSH) menjadi bentuk oksidasi glutation (GSSH) dan GSSH harus dikonversi kembali menjadi GSH. Reaksi konversi ini membutuhkan NADPH sebagai sumber energi reduksi. GSH dibutuhkan untuk menetralkan radikal bebas yang dihasilkan oleh berbagai reaksi di dalam sel. pada waktu bersamaan merusak peroksida dengan cara mengonversi peroksida menjadi bentuk alkohol yang tidak berbahaya. Reaksi sangat penting untuk mencegah terjadinya peroksida terhadap asam-asam lemak tak jenuh (kolesterol jahat).
Peroksida Lipid
Peroksida lipid terbentuk sebagai hasil reaksi antara radikal bebas dengan asam lemak tidak jenuh (PUFA = Poly Unsaturated Fatty Acid) yang merupakan unsur utama dari membran sel. Proses peroksida lipid umumnya dimulai dengan penarikan atom hidrogen yang mengandung satu elektron dari ikatan rangkap PUFA membentuk radikal lipid. Penambahan oksigen akan menyebabkan terbentuknya radikal peroksil lipid yang selanjutnya akan menarik lagi atom hidrogen dari ikatan rangkap PUFA yang lain, sehingga terbentuk radikal lipid berikutnya. Sedangkan radikal peroksil lipid tersebut akan mengalamai dekomposisi menjadi peroksida lipid. Peroksida lipid bersifat tidak stabil dan akan terurai menghasilkan sejumlah senyawa, antara lain MDA (Pendit 1996).
Kadar peroksida lipid dapat digunakan sebagai indikator terjadinya stress oksidatif pada jaringan. Hasil peroksida lipid dapat diperiksa dengan berbagai cara, antara lain dengan pembentukan konjugat MDA dengan asam tiobarbiturat.
Malondialdehid (MDA)
Menurut Pryor et al dalam Winarsi, MDA adalah senyawa aldehida yang merupakan produk akhir peroksida lipid di dalam tubuh. Senyawa ini memiliki tiga rantai karbon, dengan rumus molekul C3H4O2. MDA juga merupakan produk
dekomposisi dari asam amino, karbohidrat kompleks, pentose dan heksosa. Selain itu, MDA juga merupakan produk yang dihasilkan oleh radikal bebas melalui reaksi ionisasi dalam tubuh dan produk sampah biosintesis prostaglandin yang merupakan produk akhir oksidasi lipid membran.
Menurut Helliwell dan Gutteridge (1999), MDA merupakan produk oksidasi asam lemak tidak jenuh oleh radikal bebas. Di samping itu, MDA juga merupakan metabolit komponen sel yang dihasilkan oleh radikal bebas. Konsentrasi MDA yang tinggi menunjukkan adanya proses oksidasi dalam membran sel. Status antioksidan yang tinggi biasanya diikuti oleh penurunan kadar MDA.
Pengukuran MDA mudah dilakukan baik secara spektrofotometrik atau flurometrik. Karena MDA tidak stabil maka cara penyimpanan sampel harus terlindung dari cahaya, dan bila tidak segera diperiksa harus disimpan pada suhu -700C. Penyimpanan -200C tidak memadai (Mates 2000).
HS N OH CHO
2 + CH2
N
CHO OH
Asam Tiobarbiturat Malondialdehid
S N OH HO N SH
N CH CH CH N + 2H2O
OH OH
Produk berwarna merah muda
Gambar 3 Reaksi malondialdehid dengan asam tiobarbiturat Sumber : Helliwell dan Gutteridge 1994
Mahasiswa Alih Jenis Institut Pertanian Bogor
Mahasiswa merupakan orang yang belajar di perguruan tinggi (Kamus Besar Bahasa Indonesia 1988). Menurut Perty yang diacu dalam Deutsch (1993), mahasiswa pada umumnya berusia 17-22 tahun, dan termasuk ke dalam kategori remaja akhir. Jika dilihat dari segi kesehatan, masa remaja merupakan masa yang paling sehat selama kehidupan.
Mahasiswa Alih Jenis Institut Pertanian Bogor berasal dari Program Studi Gizi Masyarakat, Agribisnis, Manajemen dan Kimia. Sebagaian besar mahasiswa alih jenis di IPB sudah bekerja dan berusia antara 21-30 tahun. Jadwal kuliah mahasiswa alih jenis dimulai dari sore hingga malam hari.
pecel ayam dan pecel lele. Baik gorengan maupun pecel ayam ataupun lele yang dijual, digoreng menggunakan minyak yang berwarna keruh hampir berwarna hitam menandakan minyak telah digunakan berulang-ulang oleh penjual. Minyak tersebut memiliki peroksida lipid yang tinggi dan mungkin dapat menjadi penyebab meningkatnya radikal bebas dalam tubuh.
KERANGKA PEMIKIRAN
Radikal bebas dalam tubuh dapat berasal dari dalam (endogen) atau dari luar tubuh (eksogen). Secara endogen, radikal bebas dapat berasal dari makanan sumber lipid yang dapat membentuk peroksidasi lipid di dalam tubuh, selain itu, radikal radikal endogen juga bisa disebabkan oleh kondisi stress, sakit dan olah raga yang berlebihan. Secara eksogen, radikal bebas bersumber dari polutan, sinar X, asap rokok, radiasi dan lain-lain.
Secara alami tubuh dapat menghasilkan antioksidan, yang disebut sebagai antioksidan endogen seperti superoksida dismutase (SOD), katalase (CAT), glutationperoksidase(GPx), glutationreduktase (GR) dan seruloplasmin.
Apabila jumlah radikal bebas lebih tinggi dibandingkan antioksidan endogen dapat menimbulkan stress oksidatif dalam tubuh. Stress oksidatif dalam tubuh menimbulkan kerusakan pada sel. Stress oksidatif dalam tubuh dapat diukur dengan menggunakan salah satu parameternya yaitu kadar MDA plasma. Semakin tinggi stress oksidatif yang terjadi dalam tubuh maka semakin tinggi kadar MDA plasma.
Stress oksidatif dalam tubuh dapat diredam oleh antioksidan eksogen baik yang alami berasal dari bahan pangan ataupun yang berasal dari suplemen seperti suplemen vitamin C, vitamin E dan multivitamin-mineral, sehingga dapat menurunkan kadar MDA plasma.
Keterangan
: Variabel yang diteliti : Variabel yang tidak diteliti : Hubungan yang diteliti : Hubungan yang tidak diteliti
Gambar 4 Kerangka pemikiran hubungan antara konsumsi suplemen vitamin C, vitamin E dan multivitamin-mineral terhadap kadar MDA plasma Radikal Bebas dalam tubuh
Stress Oksidatif
Radikal eksogen Radikal endogen
Antioksidan Radikal Bebas dalam tubuh
Stress Oksidatif
DEFINISI OPERASIONAL
Mahasiswi Alih Jenis adalah kelompok yang rentan terkena radikal bebas baik secara endogen ataupun eksogen.
Radikal bebas adalah suatu molekul, atom atau beberapa atom yang mempunyai satu atau lebih elektron tidak berpasangan pada orbit luarnya sehingga bersifat sangat reaktif yang bersumber dari Polutan, sinar x, sinar ultraviolet, asap rokok, stress, sakit, olah raga berlebihan dan makanan sumber lipid.
Stres oksidatif adalah keadaan di mana kadar radikal bebas dalam tubuh yang meningkat melebihi kemampuan dari jumlah system antioksidan dalam tubuh untuk mengatasinya.
Kerusakan oksidatif sel adalah suatu kerusakan pada sel dikarenakan serangan radikal bebas yang menimbulkan kerusakan pada protein, asam nulkeat (DNA), dan kerusakan pada lipid.
Peroksida Lipid adalah rusaknya asam lemak tidak jenuh ganda teroksidasi oleh radikal bebas yang menyerang membrane sel.
Malondialdehid (MDA) senyawa yang tidak stabil dari penguraian peroksida lipid sebagai akibat dari terjadinya reaksi antara radikal bebas dengan asam lemak tak jenuh dan merupakan salah satu parameter stress oksidatif dalam tubuh.
Suplemen vitamin E adalah antioksidan vitamin E yang diberikan dalam bentuk kapsul dengan dosis 200 IU (8x AKG) selama satu minggu pada sampel untuk menurunkan kadar malondialdehid (MDA) plasma.
Suplemen vitamin C adalah antioksidan vitamin C yang diberikan dalam bentuk tablet dengan dosis 500 mg (8x AKG) selama satu minggu pada sampel untuk menurunkan kadar malondialdehid (MDA) plasma.
Suplemen multivitamin adalah vitamin dan mineral (Vitamin C, Seng dan Se) yang diberikan dalam bentuk tablet dengan dosis vitamin C 500 mg, vitamin E 30 mg, Seng 15 mg, Tembaga 1,5 mg pada sampel untuk menurunkan kadar malondialdehid (MDA) plasma.
Makanan sumber lipid adalah semua pangan maupun olahannya yang mengandung lemak tinggi, seperti kacang-kacangan, daging sapi, keju, gorengan, sate, ayam goreng dan lain-lain
Sumber vitamin C adalah semua pangan yang mengandung tinggi vitamin C, seperti daun singkong, daun katuk, daun melinjo, daun papaya, sawi, jambu biji, papaya, mangga, kedondong, jeruk manis, dan lain-lain.
Sumber vitamin E adalah semua pangan yang mengandung tinggi vitamin E seperti jagung, kacang kedele, kacang tanah, daging, telur, susu dan lain-lain.
Sumber Seng (Zn) adalah semua pangan yang mengandung tinggi seng (Zn) seperti daging, hati, kerang dan telur.
Sumber Selenium (Se) adalah semua pangan yang mengandung tinggi selenium seperti makanan laut, hati, ginjal, daging dan unggas.
METODE PENELITIAN
Desain, Tempat dan Waktu Penelitian
Penelitian ini merupakan jenis penelitian quasi eksperimental dengan pre-post test with control design (Bhisma 2003), karena analisis dilakukan sebelum dan setelah intervensi. Lokasi penelitian yaitu lingkungan Institut Pertanian Bogor. Analisis kadar MDA plasma dilakukan di Laboratorium Biokimia Departemen Gizi Masyarakat Institut Pertanian Bogor (IPB). Penelitian dilakukan dari bulan Mei hingga September 2011. Penelitian ini telah direview oleh tim Komisi Etik Penelitian Kedokteran dan Kesehatan Indonesia dengan dikeluarkannya Ethical Approval atau ethical clearance No. KE.01.07/EC/418/2011 yang diterbitkan di Jakarta pada tanggal 5 Juli 2011 (Lampiran 1).
Jumlah dan Cara Pengambilan Sampel
Populasi dalam penelitian ini adalah mahasiswi Alih Jenis Institut Pertanian Bogor. Teknik pemilihan dan pengambilan sampel dilakukan dengan metode purposive sampling. Semua sampel, baik perlakuan maupun kontrol harus memenuhi persyaratan inklusi maupun eksklusi yang ditetapkan.
Syarat inklusi yang harus dipenuhi oleh sampel adalah: 1. Memiliki rentang umur 16-29 tahun.
2. Belum pernah mendapatkan intervensi suplementasi serupa dalam waktu yang berdekatan, serta
3. Bersedia mengisi informed concent dan berpartisipasi dalam penelitian. 4. IMT tidak lebih dari 25 kg/m2.
Syarat ekslusi yang harus dipenuhi oleh sampel adalah: 1. Hamil atau menyusui.
2. Merokok.
3. Menderita suatu penyakit yang mengharuskannya cek rutin, serta
4. Pindah atau berada di luar lokasi dalam jangka waktu lama, sehingga tidak dapat mengikuti perlakuan.
Jumlah sampel ditetapkan dengan menggunakan rumus berikut (Supranto 2000):
(t-1) (r-1) ≥ 15
Keterangan:
t = banyaknya kelompok
r = jumlah replikasi per kelompok
Berdasarkan rumus tersebut, dengan jumlah 4 kelompok (t=4), maka jumlah sampel minimal setiap kelompok (r) yang diperlukan dalam penelitian ini adalah 6 orang. Dengan demikian jumlah sampel secara keseluruhan adalah 24 orang.
Metode Intervensi
Kelompok perlakuan dibagi menjadi 4, dengan masing-masing kelompok terdiri dari enam sampel. Kelompok perlakuan tersebut adalah :
1. Kelompok yang diberi vitamin C dosis 500 mg.
2. Kelompok yang diberi vitamin E dengan dosis 200IU (setara 133 mg). 3. Kelompok yang diberi multivitamin-mineral, yaitu vitamin C 500 mg,
vitamin E 30 mg, Seng 15 mg, Tembaga 1,5 mg, serta 4. Kelompok kontrol (tidak mendapatkan suplemen).
Dosis diberikan 8 kali dari AKG, untuk vitamin C kebutuhan wanita dewasa adalah 60 mg/orang/hari. Untuk perlakuan diberikan 8 kali AKG yaitu 500 mg. Sedangkan untuk vitamin E kebutuhan wanita dewasa adalah 15 mg/orang /hari, untuk perlakuan diberikan 8 kali AKG yaitu 200 IU, dikonversi dalam mg yaitu menjadi 133mg. Multivitamin-mineral yang digunakan adalah multivitamin dengan komposisi tiap kaplet yaitu vitamin B1 15 mg, vitamin B2 15 mg, vitamin
B3 50 mg, vitamin B5 20 mg, vitamin B6 20 mg, vitamin B12 12 mcg, biotin 45 mcg,
asam folat 400 mcg, vitamin C 500 mg, vitamin D 200 IU, vitamin E 30 mg, seng 15 mg, tembaga 1,5 mg dan calcium 100 mg.
Tolerable Upper Intake Levels (ULs) atau angka tertinggi dari nilai zat gizi yang bila dikonsumsi tiap hati tidak membahayakan kesehatan untuk dewasa ≥ 19 tahun menurut food and nutrition Board-institute of Medicine (FNB-IOM) (2004) adalah 2000 mg/hari (WNPG 2004).
Tolerable Upper Intake Levels (ULs) atau angka tertinggi dari nilai zat gizi yang bila dikonsumsi tiap hari tidak membahayakan kesehatan untuk dewasa
Jenis dan Cara Pengambilan Data
Data yang digunakan dalam penelitian ini adalah data primer yang terdiri dari data karakteristik, data konsumsi dan data kadar MDA plasma.
a. Data Identitas
Data karekteristik keluarga sampel meliputi pendidikan dan pekerjaan. Menurut Depkes 2008 klasifikasi tingkat pendidikan menjadi 6 golongan yaitu tidak pernah sekolah, tidak tamat SD, tamat SMP, tamat SMA dan tamat perguruan tinggi. Sedangkan pekerjaan diklasifikasikan menjadi swasta, PNS, wiraswasta, petani dan Ibu Rumah Tangga.
Data karakteristik sampel meliputi nama, umur, departemen dan riwayat penyakit dilakukan dengan wawancara. Data berat badan, tinggi badan dilakukan dengan penimbangan dan pengukuran, lalu dihitung Indeks Massa Tubuh (IMT) didapatkan dari hasil perhitungan:
IMT= Berat badan (kg) [tinggi badan (cm)]2
b. Data Konsumsi
Data konsumsi didapatkan dari food record selama perlakuan (7 hari) pada sampel dengan menggunakan form food record dengan mencatat jenis dan jumlah bahan makanan yang dikonsumsi setiap hari selama 24 jam, sedangkan untuk mengetahui data frekuensi konsumsi makanan sumber antioksidan selama 1 minggu terakhir sampel digunakan food frequency. Form food record dan food frequency dapat dilihat pada lampiran 4 dan lampiran 3.
c. Data Ketaatan Mengonsumsi Suplemen
Sampel harus mengonsumsi suplemen selama satu minggu berturut-turut. Ketaatan sampel dalam mengonsumsi suplemen diamati dengan mengisi form kepatuhan.
d. Data Kadar Malondialdehid (MDA) Plasma
Prinsip
Penetapan MDA dengan metode uji asam tiobarbiturat (TBA) dapat diukur secara spektrofotometrik berdasarkan prinsip bahwa asam lemak tidak jenuh jamak (PUFA) dapat mengalami proses peroksidasi menjadi peroksida lipid yang kemudian mengalami dekomposisi menjadi malondialdehid (MDA). MDA bila direaksikan dengan asam tiobarbituburat (thiobarbiriuric acid, TBA), akan membentuk senyawa berwarna merah muda yang menyerap cahaya pada panjang gelombang 532 nm. Jumlah MDA yang terbentuk dapat menggambarkan proses peroksidasi lipid (Soewoto et al 2001).
Bahan dan Alat
Bahan yang dibutuhkan untuk analisis: Bahan analisis adalah
Plasma yang diperoleh dari darah vena yang diambil dari vena mediana cubiti sebanyak 5 ml dan pemisahan dengan cara pemusingan menggunakan sentrifuge dengan kecepatan 3000 rpm selama 15 menit. Reagen yang digunakan adalah
a. Larutan asam trikloroasetat (TCA) 20 % ( 20 gram TCA dilarutkan dalam 100 ml Aquades bebas ion)
b. Larutan asam tiobarbiturat (TBA) 0,67% (0,67 gram TBA dilarutkan dalam 100 ml Asam asetat)
c. Larutan standar tetraetoksipropan d. Aquades bebas ion
Alat yang digunakan dalam penelitian: Alat untuk pengambilan darah adalah a. Spuit
b. Jarum suntik ukuran G23 c. Kapas
d. Alkohol
e. Tabung EDTA 5 ml
Alat untuk analisis radikal bebas dengan analisis lemak peroksida (MDA) adalah
a. Tabung reaksi ukuran 5 ml b. Labu ukur
d. Pipet mikro e. Sentrifuge f. Vorteks g. Penangas air h. Spektrofotometer
Prosedur Pengambilan Darah
Darah diambil dari vena cubiti dengan menggunakan spuit ukuran 5 ml dengan menggunakan jarum G 23. Darah dimasukkan ke dalam tabung EDTA agar darah tidak membeku dan ditempatkan dalam cool box sebelum disentrifuge. Darah disentrifugasi pada kecepatan 3000 rpm selama 15 menit. Cairan plasma darah yang telah terpisah dari bagian padat darah segera dipindahkan ke tabung fial kosong, untuk selanjutnya dianalisis MDA. Prosedur Analisis MDA Plasma
Prosedur analisis MDA Plasma
Gambar 5 Diagram alir analisis kadar MDA plasma 1 ml plasma sampel
Ambil supernatan 1 ml
Tambahkan larutan TBA 0,67% sebanyak 2 ml
Masukkan ke penangas mendidih selama ± 15 menit
Dinginkan
Baca serapan pada panjang gelombang 532 nm Disentrifuge selama 10 menit (3000 rpm) Tambahkan Larutan TCA 20%, dingin sebanyak 1 ml
Mengendap Divorteks
Divorteks
Alur Penelitian
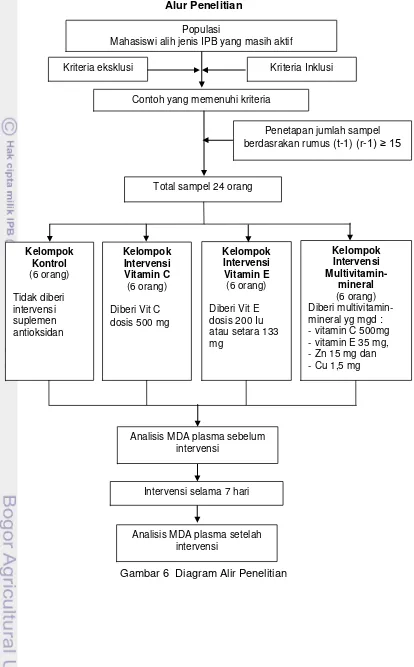
Gambar 6 Diagram Alir Penelitian Contoh yang memenuhi kriteria
Populasi
Mahasiswi alih jenis IPB yang masih aktif
Kriteria Inklusi Kriteria eksklusi
Total sampel 24 orang
Penetapan jumlah sampel berdasrakan rumus (t-1) (r-1) ≥ 15
Analisis MDA plasma sebelum
Intervensi selama 7 hari
Pengolahan Data
Data-data yang dikumpulkan selama penelitian ini disajikan dalam bentuk tabel dan kemudian dianalisis secara deskriptif dan inferensial. Data yang dianalisis secara deskriptif meliputi data karakteristik sampel, data record kebiasaan makan, data food frequency dan Indeks Massa Tubuh (IMT).
Konsumsi
Data konsumsi pangan sumber antioksidan dikumpulkan dengan metode food frequency kemudian diolah untuk mendapatkan data frekuensi konsumsi pangan berapa kali per minggu. Data konsumsi pangan sehari sampel selama 7 hari didapatkan dengan metode food record. Data konsumsi pagan tersebut kemudian diolah dan dikonversi menggunakan nutri-survey menjadi data asupan energi dan zat gizi protein, vitamin A, vitamin C, vitamin E, kalsium, seng dan tembaga.
Data asupan energi tersebut kemudian dibandingkan dengan AKG untuk mendapatkan nilai tingkat kecukupan energi dan zat gizi, dengan menggunakan rumus tingkat kecukupan zat gizi di bawah ini :
TKG = (K/AKGi) x 100% Keterangan :
TKG : Tk. kecukupan zat gizi K : Konsumsi zat gizi
AKGi : Angka kecukupan zat gizi sampel yang dicari
Menurut Supariasa 2002, Kategori tingkat kecukupan untuk Energi dan vitamin di bagi menjadi empat kategori yaitu defisit <70%; kurang 70-80%; sedang 80-99% dan baik ≥ 100%. εenurut Gibson (β005) tingkat kecukupan
vitamin dan mineral dibagi menjadi dua kategori yaitu kurang ≤77% dan cukup
>77%.
Status Gizi
Tabel 2 Kategori indeks massa tubuh menurut Depkes (1999)
Kategori IMT
Kurus Kekurangan BB Tingkat Berat < 17,0 kg/m
2
Kekurangan BB Tingkat Ringan 17,0-18,5 kg/m2
Normal Normal >18,5-25,0 kg/m2
Gemuk Kelebihan BB Tingkat Ringan >25,0-27,0 kg/m
2
Kelebihan BB Tingkat Berat >27,0 kg/m2 Sumber : Depkes (1994) dalam Supariasa et al (2002)
Penetapan MDA
Data kadar MDA plasma sampel diukur sebelum dan setelah 7 hari intervensi, kemudian dihitung perubahan kadar MDA plasma yaitu selisih antara kadar MDA sebelum dan setelah 7 hari intervensi.
Penetapan MDA dengan metode uji asam tiobarbiturat (TBA) diukur dengan spektrofotometer panjang gelombang 532 nm. Hasilnya dihitung dengan rumus Kadar MDA, membandingkan absorbansi dengan kurva standar memakai tetraetoksipropan, menggunakan persamaan Y = aX + b.
Keterangan :
fp Faktor Pengenceran
Penetapan Standar MDA
Mengukur MDA sebagai produk peroksidasi lipid, dalam penelitian ini digunakan tetraetoksipropan (TEP) sebagai prekursor dari MDA, karena MDA merupakan senyawa yang tidak stabil. TEP dihidrolisis oleh air menjadi MDA dan alkohol. Prosedur Penetapan standar tersaji lengkap pada Lampiran 6.
Gambar 7 Kurva standar tetraetoksipropan (TEP)
Analisis Data
Data yang telah terkumpul diolah dan dianalisis secara deskriptif dan inferensial menggunakan Microsoft Excel 2007 dan program SPSS versi 16.0 for Windows. Untuk menganalisis perbedaan sebelum dan setelah intervensi pada setiap kelompok perlakuan dilakukan uji T. Sedangkan untuk melihat perbedaan perubahan kadar MDA plasma (antara setelah dan sebelum intervensi) antar kelompok perlakuan dilakukan uji beda ANOVA. Jika terdapat indikasi perbedaan yang signifikan, maka dilanjutkan dengan uji Beda Duncan dan Least Significant Different (LSD) untuk mengetahui kelompok mana yang sesungguhnya berbeda.
0 0,2 0,4 0,6 0,8 1 1,2
0 200 400 600
A532
nmol/ml Kurva Standar TEP
HASIL DAN PEMBAHASAN
Karakteristik Individu Sampel
Sampel dalam penelitian ini adalah mahasiswi alih jenis Institut Pertanian Bogor, dengan kriteria sampel yang memenuhi syarat inklusi yaitu: (1) IMT tidak lebih dari 25 kg/m2, (2) Memiliki rentang umur 16-29 tahun, (3) Belum pernah mendapatkan intervensi suplementasi serupa dalam waktu yang berdekatan, serta (4) Bersedia mengisi informed concent dan berpartisipasi dalam penelitian. Syarat eksklusi terdiri dari (1) Hamil atau menyusui, (2) Merokok, (3) Menderita suatu penyakit yang mengharuskannya cek rutin, serta (4) Pindah atau berada di luar lokasi dalam jangka waktu lama, sehingga tidak dapat mengikuti perlakuan.
Keseluruhan sampel dalam penelitian ini berpartisipasi dengan baik, sehingga tidak ada sampel yang harus di drop out. Karakteristik sampel yang diamati pada penelitian ini meliputi variabel umur, program studi, tinggi badan, berat badan, indeks massa tubuh (IMT), dan riwayat penyakit.
Penentuan sampel perempuan muda sehat dalam penelitian ini, didasarkan pada penelitian sebelumnya yang dilakukan oleh Lyle et al (1998) bahwa penggunaan suplemen makanan lebih banyak ditemui pada populasi perempuan dari pada laki-laki. Kondisi serupa juga didukung oleh penelitian Greger (2001) bahwa perempuan lebih sering mengonsumsi suplemen, terutama multivitamin, vitamin C dan vitamin E dibandingkan laki-laki.
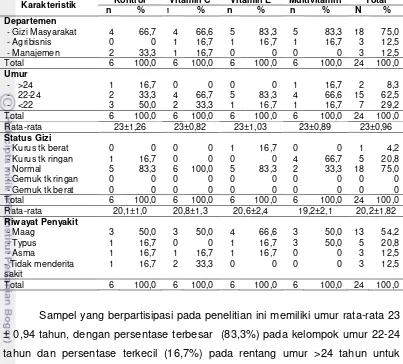
Pada penelitian ini, sampel berasal dari 3 program studi alih jenis yang berbeda yang berada di Institut Pertanian Bogor yaitu program studi Gizi Masyarakat, Agribisnis dan Manajemen, namun sampel terbanyak untuk masing-masing kelompok perlakuan berasal dari program studi Gizi Masyarakat dengan persentase berkisar antara 66,7%-83,3%, sedangkan persentase terendah adalah 16,7% berasal dari program studi Agribisnis dan Manajemen tersebar pada semua kelompok perlakuan. Secara keseluruhan, variabel karakteristik dari sampel penelitian tersaji dalam Tabel 3.
Tabel 3 Sebaran karakteristik individu sampel pada tiap kelompok perlakuan Karakteristik Kontrol Vitamin C Vitamin E Multivitamin Total
n % n % n % n % N %
Sampel yang berpartisipasi pada penelitian ini memiliki umur rata-rata 23 ± 0,94 tahun, dengan persentase terbesar (83,3%) pada kelompok umur 22-24 tahun dan persentase terkecil (16,7%) pada rentang umur >24 tahun untuk kelompok perlakuan kontrol dan multivitamin. Berdasarkan hasil uji statistik tidak terdapat perbedaan signifikan (p>0,05) umur sampel antar kelompok perlakuan. Kemiripan umur menjadi salah satu faktor penting yang dipertimbangkan untuk menjaga validitas internal dari penelitian ini, diharapkan bahwa pada rentang yang tidak terlalu jauh memiliki kemiripan dalam sistem atau proses metabolisme secara umum walaupun tidak menutup kemungkinan variasi setiap individu tetap ada.
Rata-rata IMT sampel tiap kelompok perlakuan berada pada kategori normal (>18,5-25,0) dengan kisaran persentase (33,3-100%). Persentase terendah pada rentang kategori (<17,0) dan (17,0-18,5) yaitu sebesar 16,7%. Hasil uji statistik menunjukkan bahwa tidak terdapat perbedaan yang signifikan (p>0,05) indeks massa tubuh sampel antar kelompok perlakuan.
Penelitian Lee et al (2002) memperlihatkan bahwa terdapat hubungan bermakna antara Indeks Massa tubuh dengan konsumsi suplemen zat gizi. Penelitian lain menyebutkan bahwa pengguna suplemen makanan adalah mereka yang underweight (Messerer 2001). Menurut White et al (2004) semakin rendah IMT seseorang maka semakin tinggi kecenderungan orang untuk mengonsumsi suplemen makanan.
Sampel pada umumnya memiliki riwayat penyakit maag, typus, asma dan hepatitis. Secara keseluruhan rata-rata sampel tiap kelompok perlakuan memiliki riwayat penyakit maag dengan persentase 54,2% . Ini diduga dikarenakan pola makan mahasiswa yang tidak menentu, selain itu mahasiswa kurang memperhatikan jenis makanan yang dikonsumsinya. Hal ini juga diperkirakan yang menyebabkan penyakit selanjutnya yang banyak diderita mahasiswa setelah penyakit maag yaitu tipus. Rata-rata sampel yang menderita penyakit tipus secara keseluruhan kelompok perlakuan adalah 20,8%.
Konsumsi, Frekuensi, Asupan dan Tingkat Kecukupan
Konsumsi Pangan
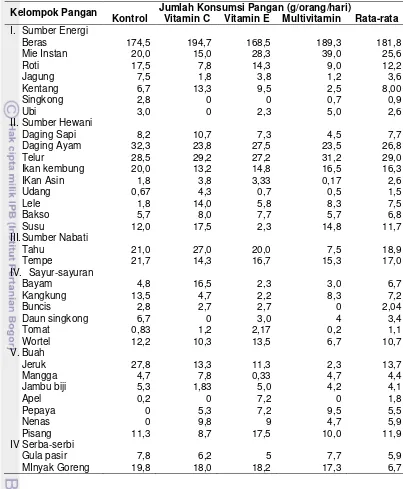
Konsumsi pangan adalah jenis dan jumlah (berat) pangan yang dikonsumsi sampel rata-rata perorang perhari (gram/orang/hari), dapat dilihat pada Tabel 4.
Tabel 4 Rata-rata konsumsi pangan sampel per orang per hari (g/orang/hari)
Kelompok Pangan Jumlah Konsumsi Pangan (g/orang/hari)
Kontrol Vitamin C Vitamin E Multivitamin Rata-rata
I. Sumber Energi disukai dan paling banyak dikonsumsi sampel dengan jumlah rata-rata konsumsi perorang perhari dari semua perlakuan adalah 18,9 g dan 17,0 g. Protein nabati seperti tahu dan tempe pada umumnya berasal dari gorengan yang dibeli oleh sampel. Sehingga konsumsi protein nabati tinggi diikuti dengan konsumsi minyak yang juga tinggi.
vitamin dan mineral. Sayuran yang paling banyak disukai dan banyak dikonsumsi oleh sampel dari tiap kelompok perlakuan adalah wortel, kangkung dan bayam dengan rata-rata konsumsi perorang perhari secara berurutan adalah 10,7 g, 7,2 g dan 6,7 g. Buah-buahan yang dikonsumsi sampel juga bervariasi seperti jeruk, mangga, jambu biji, apel, pepaya, nenas dan pisang. Buah yang paling banyak dikonsumsi sampel adalah pisang dan jeruk dengan rata-rata secara keseluruhan konsumsi perorang perhari secara berurutan adalah 11,9 g dan 13,7 g.
Frekuensi Konsumsi Pangan Sumber Antioksidan
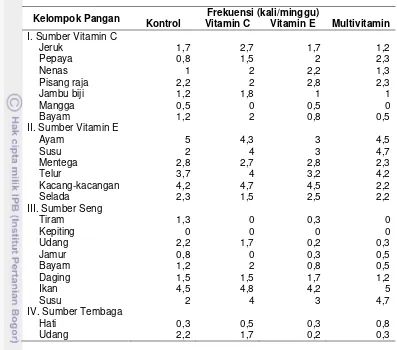
Frekuensi konsumsi pangan dilakukan untuk memperoleh data tentang frekuensi konsumsi sejumlah bahan pangan atau makanan, selama periode tertentu, dalam penelitian ini adalah satu minggu. Frekuensi konsumsi pangan merupakan aspek penting dari kebiasaan konsumsi pangan yang secara kualitatif dapat memberikan gambaran tentang pola konsumsi bahan pangan. Frekuensi konsumsi pangan sumber vitamin C, vitamin E, Seng, Tembaga secara lengkap tersaji pada Tabel 5.
Frekuensi sampel mengonsumsi sumber vitamin dan mineral terutama vitamin C, vitamin E, seng dan tembaga. Secara keseluruhan pangan sumber vitamin C sampel yang paling sering dikonsumsi yaitu pisang, jeruk dan nenas, dengan frekuensi secara berurutan 2-3 kali, 1-2 kali dan 1-3 kali per minggu. Frekuensi konsumsi sumber vitamin E sampel yang sering dikonsumsi berasal dari bahan pangan daging ayam, susu dan telur dengan frekuensi masing-masing 3-5 kali, 2-5 kali, dan 3-4 kali per minggu.
Tabel 5 Rata-rata frekuensi konsumsi pangan sumber vitamin C, vitamin E, seng, dan tembaga antar kelompok perlakuan
Kelompok Pangan Frekuensi (kali/minggu)
Kontrol Vitamin C Vitamin E Multivitamin
I. Sumber Vitamin C
Asupan Energi dan Zat Gizi
Besarnya porsi pangan sampel berdasarkan ukuran rumah tangga (URT) dikonversi ke dalam gram. Jumlah zat gizi yang dikonsumsi dari berbagai jenis dan kelompok pangan diketahui menggunakan nutri survey, sehingga dapat melihat rata-rata asupan masing-masing sampel antar tiap kelompok perlakuan.
Tabel 6 Asupan rata-rata energi dan zat gizi kelompok perlakuan berdasarkan record 7x 24 jam
Zat Gizi Kelompok Perlakuan
Kontrol Vitamin C Vitamin E Multivitamin
Energi (kkal) 1509 1651 1412 1515
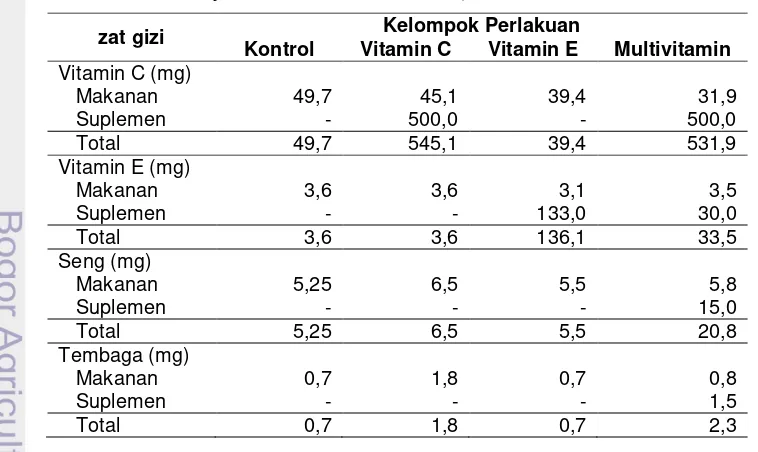
Asupan Vitamin dan Mineral Sampel dari Makanan dan Intervensi
Seseorang tidak akan memperoleh cukup vitamin hanya dari makanan yang dikonsumsi. Agar dapat bertindak sebagai antioksidan, seseorang harus mengonsumsi vitamin E lebih dari AKG, umumnya sekitar 100 mg/hari (Muchtadi 2009). Sedangkan untuk vitamin C seseorang harus mengonsumsi melebihi AKG sehingga dapat berfungsi sebagai antioksidan dalam tubuh. Rata-rata asupan vitamin dan mineral sampel tiap kelompok perlakuan yang berasal dari makanan dan intervensi tersaji pada Tabel 7.
Tabel 7 Asupan rata-rata vitamin dan mineral kelompok perlakuan berdasarkan record 7x 24 jam dari makanan dan suplemen
zat gizi Kelompok Perlakuan
Kontrol Vitamin C Vitamin E Multivitamin
Berdasarkan Tabel 7 terlihat bahwa konsumsi vitamin dan mineral dari tiap kelompok perlakuan kurang dari angka kecukupan yang dianjurkan yaitu vitamin C 75 mg/hari, vitamin E 15 mg/hari, Seng 9,3 mg/hari. Pada kelompok kontrol sumber vitamin C, vitamin E, seng dan Tembaga hanya berasal dari makanan. Sedangkan pada kelompok vitamin C mendapatkan tambahan vitamin C dari intervensi sebesar 500 mg/hari sehingga rata-rata konsumsi vitamin C /orang/hari adalah 545 mg, namun untuk vitamin E, seng dan Tembaga pada kelompok ini masih kurang karena tidak mendapatkan tambahan asupan dari intervensi.
Pada kelompok vitamin E mendapatkan tambahan vitamin E dari intervensi sebesar 133 mg/hari atau setara dengan 200 IU sehingga rata-rata konsumsi vitamin E /orang/hari adalah 136 mg, namun untuk vitamin C, seng dan Tembaga pada kelompok ini masih kurang karena tidak mendapatkan tambahan asupan dari intervensi. Pada kelompok multivitamin-mineral mendapatkan tambahan vitamin C, vitamin E, seng dan Tembaga dari intervensi sebesar 500 mg/ hari untuk vitamin C, 30 mg/ hari untuk vitamin E, 15 mg/hari untuk seng dan 1,5 mg/hari untuk Tembaga. Sehingga rata-rata konsumsi vitamin C, vitamin E, seng dan Tembaga /orang/hari secara berurutan adalah 532 mg, 33,5 mg, 20,8 mg dan 2,3 mg.
Untuk mengonsumsi vitamin E dan vitamin C hingga mencapai nilai yang melebihi AKG dapat diperoleh dengan mengonsumsi suplemen vitamin E dan vitamin C dengan dosis tertentu di samping sumber yang berasal dari makanan.
Tingkat Kecukupan
Angka kecukupan vitamin C, vitamin E, seng, dan tembaga pada kelompok umur 19-29 dengan jenis kelamin perempuan secara berurutan adalah 75 mg, 15 mg, 9,3 mg (WNKPG 2004). Berdasarkan AKG dapat diketahui tingkat kecukupan konsumsi sampel antar tiap kelompok perlakuan. Tingkat kecukupan energi dan zat gizi dapat dilihat pada Tabel 8.
Tingkat kecukupan protein sebagian besar sampel sebagian besar berada pada kategori baik yaitu dengan persentase 54,1%. Tingkat kecukupan protein sampel baik pada kelompok intervensi vitamin C yaitu 66,7%. Hal ini dikarenakan konsumsi protein hewani sampel cukup bervariasi baik jumlah dan frekuensi.
Tingkat kecukupan vitamin C, vitamin E, seng dan sampel tiap kelompok perlakuan masih sangat kurang, yaitu dengan persentase secara berurutan adalah 83%, 100% dan 87,5%. Berdeda dengan vitamin A yang secara keseluruhan sampel memiliki tingkat kecukupan yang baik yaitu dengan persentase 100%. Hal ini dikarenakan konsumsi pangan sumber vitamin C, vitamin E, Seng dan Tembaga yang masih sangat rendah. Terutama pada konsumsi sayuran dan buah. Sedangkan bahan pangan yang banyak menyumbang vitamin A adalah wortel, telur, mangga dan minyak.
Tabel 8 Sebaran sampel berdasarkan tingkat kecukupan energi dan zat gizi yang berasal dari makanan pada tiap kelompok perlakuan
Kategori Kontrol Vitamin C Vitamin E Multivitamin Rata-rata
Berikut adalah tingkat kecukupan vitamin C, vitamin E, Seng, dan Tembaga sampel pada tiap kelompok perlakuan dengan konsumsi dari makanan dan intervensi.
Tingkat kecukupan vitamin C sampel pada kelompok yang tidak mendapatkan intervensi vitamin C yaitu kelompok kontrol dan vitamin E berada pada tingkat kecukupan yang kurang dengan persentase secara berurutan 66,7% dan 100%. Sedangkan kelompok yang mendapatkan intervensi vitamin C, tingkat kecukupan sampel menjadi baik yaitu 100%.
Berbeda dengan kelompok vitamin C dan kontrol, tingkat kecukupan vitamin E pada kelompok intervensi vitamin E dan multivitamin berada pada kategori baik yaitu dengan persentase 100%. dikarenakan multivitamin memberikan sumbangan untuk menambah vitamin C, E, Seng dan Tembaga. Sedangkan tingkat kecukupan sampel pada kelompok vitamin C dan kontrol sangat kurang dengan persentase 100%.
Begitu juga dengan Seng dan Tembaga, pada kelompok multivitamin Seng dan Tembaga berada pada kategori baik dengan persenatse 100%. Sedangkan untuk tiga kelompok lainnya berada pada kategori kurang.
Konsumsi antioksidan dalam jumlah memadai dilaporkan dapat menurunkan kejadian penyakit yang ditimbulkan oleh radikal bebas seperti penyakit degeneratif, kanker. Konsumsi makanan yang mengandung antioksidan dapat meningkatkan status imunologis dan menghambat timbulnya penyakit degeneratif karena penuaan. Oleh sebab itu, kecukupan asupan antioksidan secara optimal diperlukan pada semua kelompok umur (Winarsi 2011).
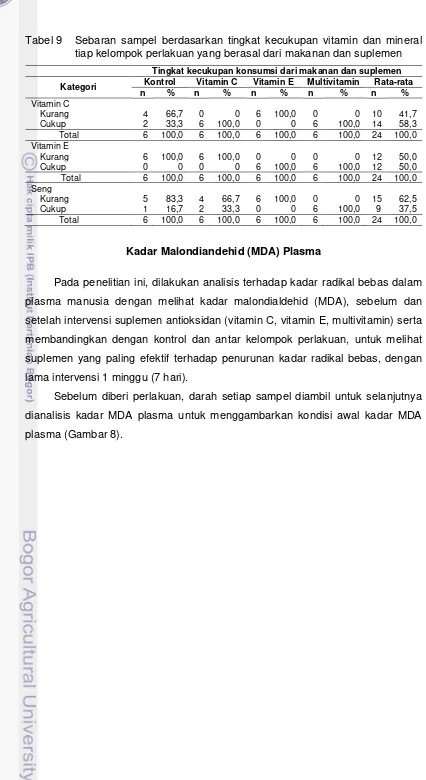
Tabel 9 Sebaran sampel berdasarkan tingkat kecukupan vitamin dan mineral tiap kelompok perlakuan yang berasal dari makanan dan suplemen
Tingkat kecukupan konsumsi dari makanan dan suplemen
Kategori Kontrol Vitamin C Vitamin E Multivitamin Rata-rata
n % n % n % n % n %
Vitamin C
Kurang 4 66,7 0 0 6 100,0 0 0 10 41,7
Cukup 2 33,3 6 100,0 0 0 6 100,0 14 58,3
Total 6 100,0 6 100,0 6 100,0 6 100,0 24 100,0
Vitamin E
Kurang 6 100,0 6 100,0 0 0 0 0 12 50,0
Cukup 0 0 0 0 6 100,0 6 100,0 12 50,0
Total 6 100,0 6 100,0 6 100,0 6 100,0 24 100,0
Seng
Kurang 5 83,3 4 66,7 6 100,0 0 0 15 62,5
Cukup 1 16,7 2 33,3 0 0 6 100,0 9 37,5
Total 6 100,0 6 100,0 6 100,0 6 100,0 24 100,0
Kadar Malondiandehid (MDA) Plasma
Pada penelitian ini, dilakukan analisis terhadap kadar radikal bebas dalam plasma manusia dengan melihat kadar malondialdehid (MDA), sebelum dan setelah intervensi suplemen antioksidan (vitamin C, vitamin E, multivitamin) serta membandingkan dengan kontrol dan antar kelompok perlakuan, untuk melihat suplemen yang paling efektif terhadap penurunan kadar radikal bebas, dengan lama intervensi 1 minggu (7 hari).
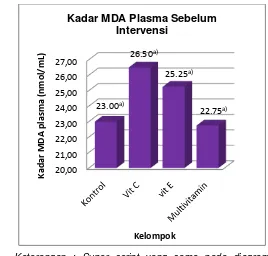
Keterangan : Super script yang sama pada diagram batang menunjukkan nilai yang tidak berbeda signifikan pada taraf uji (p>0,05).
Gambar 8 Grafik kadar MDA plasma sampel sebelum intervensi
Kondisi awal kadar MDA plasma sampel untuk masing-masing kelompok perlakuan dan kontrol cukup homogen karena secara statistik tidak berbeda signifikan (p>0,05) (Lampiran 8).
Hasil penelitian menunjukkan setelah 7 hari intervensi suplemen antioksidan, rata-rata kadar Malondialdehid (MDA) plasma kelompok vitamin E, vitamin C, dan multivitamin, nampak turun jika dibandingkan dengan kadar MDA plasma pada kondisi awal penelitian, sedangkan kadar MDA plasma pada kelompok kontrol terlihat naik pada akhir penelitian jika dibandingkan dengan kadar MDA plasma kelompok kontrol di awal penelitian (Gambar 9)
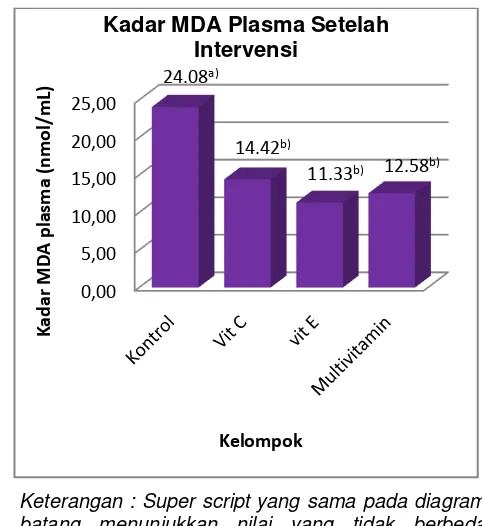
Keterangan : Super script yang sama pada diagram batang menunjukkan nilai yang tidak berbeda signifikan pada taraf uji (p>0,05).
Gambar 9 Grafik kadar MDA plasma setelah intervensi
Pada Gambar 9 menjelaskan bahwa mengonsumsi suplemen antioksidan vitamin E (dosis 8 kali AKG) mampu menurunkan kadar MDA plasma dari 25,25 nmol/mL menjadi 11,33 nmol/mL. Pada kelompok yang diberikan vitamin C (dosis 8 kali AKG), rata-rata kadar MDA juga menurun dari 26,50 nmol/mL menjadi 14,42 nmol/mL, demikian pula dengan kelompok diberikan suplemen multivitamin, rata-rata kadar MDA plasma juga menurun dari 22,75 nmol/mL menjadi 12,08 nmol/mL. Sebaliknya, rata-rata kadar MDA plasma kelompok kontrol meningkat dari 23,00 nmol/mL menjadi 24,08 nmol/mL. Berdasarkan uji T diketahui kelompok perlakuan vitamin C, vitamin E dan multivitamin berbeda secara signifikan (p<0,05) kadar MDA plasma sebelum dan setelah intervensi. Berbeda untuk kelompok kontrol tidak terdapat perdedaan yang signifikan (p>0,05) kadar MDA plasma sebelum dan setelah intervensi.
Penurunan terendah terjadi pada kelompok multivitamin-mineral. Hal ini diduga karena pada kelompok ini, hampir keseluruhan sampel berada pada status gizi kurus tingkat ringan dengan konsumsi pangan sumber antioksidan yang kurang, sehingga diduga asupan vitamin dan mineral yang terkandung dalam suplemen multivitamin-mineral digunakan tubuh untuk melengkapi kebutuhan tubuh akan vitamin dan mineral.
Penurunan kadar MDA plasma pada sampel yang diberi intervensi vitamin C, vitamin E, dan multivitamin, diduga karena efek konsumsi vitamin c, vitamin E dan multivitamin-mineral selama 7 hari. Menurut Bellivelle-Nebet (1996) dan Lunec (1990) bahwa tinggi rendahnya kadar MDA plasma sangat tergantung pada status antioksidan dalam tubuh. Hal ini disebabkan karena radikal bebas akan dinetralkan menjadi produk yang lebih stabil.
Penurunan kadar MDA plasma sesuai juga dengan penelitian yang dilakukan Dewi et al (2009) pada sampel remaja yang mengalami obesitas yang diberikan susu kedelai selama 30 hari menunjukkan bahwa pada awal perlakuan, konsentrasi MDA plasma tidak berbeda signifikan pada semua kelompok, sedangkan pada akhir perlakuan konsentrasi plasma mengalami penurunan dari kadar MDA awal yang berbeda secara sangat signifikan.
Penurunan kadar MDA plasma menunjukkan adanya penghambatan oleh zat antioksidan. Status antioksidan yang tinggi biasanya diikuti oleh penurunan kadar MDA plasma (Zakaria et al 2000).
Berdasarkan uji ANOVA terdapat perbedaan yang signifikan (p<0,05) perubahan penurunan kadar MDA plasma antar kelompok perlakuan. Uji lanjutan Duncan dan uji Least Significant Different (LSD) menunjukkan bahwa tidak ada perbedaan yang signifikan (p>0,05) antara rata-rata penurunan kadar MDA plasma pada kelompok vitamin C, vitamin E dan multivitamin (Tabel 10), tetapi terdapat perbedaan yang sigifikan (p<0,05) antara kontrol dengan kelompok intervensi vitamin C, vitamin E dan multivitamin-mineral. Jadi dapat disimpulkan, ketiga suplemen antioksidan ini memiliki keefektivitasan yang hampir sama.
Tabel 10 Kadar MDA plasma sampel menurut kelompok perlakuan sebelum dan setelah intervensi Setelah 24,1±6,79b) 14,4±3,51a) 11,3±2,86a) 12,6±2,01a) 15,6±6,45 Selisih
(sebelum dan setelah) 1,08±2,73 b)
-12,08±9,47a) -13,9±6,48a) -10,2±4,24a) -8,77±8,35
Keterangan :
Huruf yang berbeda pada baris yang sama menunjukkan adanya perbedaan yang signifikan (p<0.05) antar kelompok perlakuan
antioksidan dari makanan tidak dapat memenuhi kebutuhan tubuh akan antioksidan. Sehingga kurang mampu mencegah proses peroksidasi lipid dibandingkan kelompok yang mendapatkan intervensi suplemen antioksidan.
Winarsi et al (2005) menemukan bahwa dalam tubuh wanita premonopause banyak terbentuk radikal bebas. Ini diketahui melaui kadar MDA plasma. Tingginya produk MDA ini merupakan bukti rendahnya status antioksidan tubuh sehingga tidak dapat mencegah reaktivitas senyawa radikal bebas. Di sisi lain, tingginya kadar MDA plasma membuktikan kerentanan komponen membran sel terhadap reaksi oksidasi (Wijaya 1996).
Konsumsi antioksidan dalam jumlah memadai dapat menurunkan kejadian penyakit yang ditimbulkan oleh radikal bebas seperti penyakit degeneratif, kanker. Konsumsi makanan yang mengandung antioksidan dapat meningkatkan status imunologis dan menghambat timbulnya penyakit degenerative karena penuaan. Oleh sebab itu, kecukupan asupan antioksidan secara optimal diperlukan pada semua kelompok umur (winarsi 2011).
Hasil penelitian ini, mengindikasikan bahwa untuk mencegah terjadinya peningkatan kadar MDA plasma yang bersifat toksik di dalam tubuh dapat dicegah dengan mengonsumsi salah satu suplemen antioksidan seperti vitamin E dosis 200 IU (setara dengan 133 mg), vitamin C dosis 500 mg dan multivitamin-mineral, karena ketiganya memberikan pengaruh yang hampir sama.
Kadar MDA plasma juga menurun pada 40 wanita muda sehat yang berumur 26 tahun setelah mengonsumsi minyak linola nabati yang di dalamnya mengandung alfa dan tokoferol yang bersifat antioksidan (Lemcke-Norojarvi et al 2001). Penurunan radikal bebas juga terjadi pada tikus jantan Fischer 344 yang diberikan Cu dan Zn-SOD (Rao et al 1990).