ISOLASI DAN KARAKTERISASI NATRIUM ALGINAT DARI
ALGA COKLAT Sargassum plagyophyllum (Mertens) J.G.
Agardh SERTA PENGARUH PENAMBAHAN
KONSENTRASI PEMUTIH TERHADAP
VISKOSITAS
SKRIPSI
OLEH:
NINA RIMELDA
NIM 101524048
PROGRAM EKSTENSI SARJANA FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
ISOLASI DAN KARAKTERISASI NATRIUM ALGINAT DARI
ALGA COKLAT Sargassum plagyophyllum (Mertens) J.G.
Agardh SERTA PENGARUH PENAMBAHAN
KONSENTRASI PEMUTIH TERHADAP
VISKOSITAS
SKRIPSI
Diajukan untuk melengkapi salah satu syarat untuk memperoleh
gelar Sarjana Farmasi pada Fakultas Farmasi
Universitas Sumatera Utara
OLEH:
NINA RIMELDA
NIM 101524048
PROGRAM EKSTENSI SARJANA FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
LEMBAR PENGESAHAN
ISOLASI DAN KARAKTERISASI NATRIUM ALGINAT DARI
ALGA COKLAT Sargassum plagyophyllum (Mertens) J.G.
Agardh SERTA PENGARUH PENAMBAHAN
KONSENTRASI PEMUTIH TERHADAP
VISKOSITAS
OLEH: NINA RIMELDANIM 101524048
Dipertahankan di hadapan Panitia Penguji Skripsi Fakultas Farmasi Universitas Sumatera Utara
Pada Tanggal: 04 Mei 2013
Pembimbing I, Panitia Penguji,
Dra. Suwarti Aris, M.Si., Apt. Dra. Aswita Hafni Lubis, M.Si., Apt. NIP 195107231982032001 NIP 195304031983032001
Dra. Suwarti Aris, M.Si., Apt.
Pembimbing II, NIP 195107231982032001
Dra. Djendakita Purba, M.Si., Apt. Drs. Agusmal Dalimunthe, M.S., Apt. NIP 195107031977102001 NIP 195406081983031005
Drs. Suryanto, M.Si., Apt. NIP 196106191991031001 Medan, Juni 2013
Fakultas Farmasi
Universitas Sumatera Utara Dekan,
KATA PENGANTAR
Puji syukur penulis ucapkan kepada Allah SWT atas segala limpahan rahmat dan karuniaNya, sehingga penulis dapat menyelesaikan penelitian dan penyusunan skripsi ini, serta Shalawat dan Salam kepada Nabi Muhammad SAW sebagai suri tauladan dalam kehidupan.
Skripsi ini disusun untuk melengkapi salah satu syarat mencapai gelar Sarjana Farmasi dari Fakultas Farmasi Universitas Sumatera Utara, yang berjudul:
“Isolasi dan Karakterisasi Natrium Alginat dari Alga Coklat Sargassum
plagyophyllum (Mertens) J.G. Agardh Serta Pengaruh Penambahan Konsentrasi
Pemutih Terhadap Viskositas”.
penguji yang memberikan masukan, kritikan, arahan, dan saran dalam penyusunan skripsi ini.
Penulis juga tidak lupa mengucapkan terima kasih dan penghargaan yang tulus kepada orang tua, Ayahanda Darman Nasution dan Ibunda Darwisah Lubis tercinta, atas doa dan dukungan baik moril maupun materil, abang dan adik tersayang, serta teman-teman seperjuangan atas doa, dorongan dan semangat dalam penyelesaian skripsi ini.
Penulis menyadari bahwa skripsi ini masih banyak kekurangan, oleh karena itu sangat diharapkan kritik dan saran yang bersifat membangun dari semua pihak guna perbaikan skripsi ini. Akhir kata penulis berharap semoga skripsi ini bermanfaat bagi ilmu pengetahuan khususnya bidang farmasi.
Medan, Juni 2013 Penulis,
ISOLASI DAN KARAKTERISASI NATRIUM ALGINAT DARI ALGA COKLAT Sargassum plagyophyllum (Mertens) J.G. Agardh SERTA
PENGARUH PENAMBAHAN KONSENTRASI PEMUTIH TERHADAP VISKOSITAS
ABSTRAK
Alga coklat merupakan salah satu sumber produksi alginat yang cukup potensial. Sargassum plagyophyllum (Mertens) J.G. Agardh adalah salah satu jenis alga coklat sebagai penghasil alginat yang belum banyak dimanfaatkan dan terdapat diperairan Indonesia, khususnya Sumatera Utara.
Tujuan penelitian ini untuk mengetahui karakteristik simplisia Sargassum
plagyophyllum (Mertens) J.G. Agardh, isolasi natrium alginat menggunakan
pemutih dengan berbagai konsentrasi yaitu 0,25%; 0,50%; 0,75%; 1,0% dan 1,25%. Identifikasi natrium alginat secara kualitatif, penetapan rendemen, pemeriksaan karakteristik natrium alginat meliputi penetapan susut pengeringan, penetapan viskositas, penetapan kadar abu total, penetapan kadar abu tidak larut asam dan identifikasi gugus fungsi dengan cara spektrofotometri inframerah.
Hasil pemeriksaan makroskopik simplisia bentuk talus menciut, tidak berasa, tidak berbau dan berwarna coklat kehitaman. Pemeriksaan mikroskopik serbuk terlihat adanya sel-sel parenkim yang berisi pigmen berwarna coklat dan terdapat sel propagule yang memiliki dua sel. Kadar air 9,97%, kadar sari larut air 11,78%, kadar sari larut etanol 2,34%, kadar abu total 17,52%, kadar abu tidak larut asam 0,48%. Identifikasi natrium alginat secara kualitatif memberikan hasil yang positif terhadap semua perlakuan, rendemen natrium alginat tertingi adalah 16,63% dengan konsentrasi pemutih 1,25% dan rendemen natrium alginat terendah adalah 9,99% dengan konsentrasi pemutih 0,25%. Penetapan susut pengeringan 6,21%, kadar abu total 9,80%, kadar abu tidak larut asam 0,43%. Penetapan viskositas adalah 24,24 cps yang diperoleh dari konsentrasi pemutih 0,25% dengan warna serbuk coklat tua, sedangkan konsentrasi pemutih 1,25% diperoleh 15,23 cps dengan warna serbuk putih. Hasil spektrofotometri inframerah menunjukkan adanya gugus O-H (3446 cm-1), gugus C-H alifatik (2930 cm-1) gugus C=O (1601 cm-1), ikatan C-O-H (1420 cm-1) dan ikatan C-O-C (1033 cm-1), spektrum natrium alginat hasil isolasi sesuai dengan natrium alginat pembanding.
ISOLATION AND CHARACTERIZATION OF SODIUM ALGINATE FROM BROWN ALGAE Sargassum plagyophyllum (Mertens) J.G.
Agardh AND BLEACH OF EFFECT CONCENTRATION ADDITION ON THE VISCOSITY
ABSTRACT
Brown algae is one a source of alginate production considerable potential.
Sargassum plagyophyllum (Mertens) J.G. Agardh is one type of brown algae as a
producer of alginate and there has not been much exploited waters of Indonesia, especially North Sumatera.
The purpose of this study to investigate the characteristics of crude drugs
Sargassum plagyophyllum (Mertens) J.G. Agardh, isolation of sodium alginate
with various concentrations of bleach that is 0.25%, 0.50%, 0.75%, 1.0% and 1.25%. Sodium alginate are qualitatively identification, determination of yield, the characteristics of sodium alginate examination includes determination of loss on drying, viscosity determination, determination of total ash content, determination of acid insoluble ash content and identification of functional groups by infrared spectrophotometry.
Macroscopic examination crude form of talus wrinkled, tasteless, odorless and blackish brown. Microscopic examination of pollen seen the parenchyma cells containing brown pigment and there propagule cell has two cells. Water content 9.97%, the levels of water-soluble extract 11.78%, levels of ethanol soluble extract 2.34%, 17.52% total ash, acid insoluble ash content of 0.48%. Qualitative identification of sodium alginate yielded positive results for all treatments, sodium alginate highest yield was 16.63% with a 1.25% concentration of bleach and sodium alginate yield the lowest is 9.99% with a 0.25% concentration of bleach. Determination of loss on drying of 6.21%, total ash of 9.80%, acid insoluble ash content of 0.43%. Determination of viscosity is 24.24 cps obtained from a concentration bleach of 0.25% with the color of the powder is dark brown, while a concentration bleach of 1.25% is obtained 15.23 cps with the color of the powder is white. The results of infrared spectrophotometry showed an O-H group (3446 cm-1), aliphatic C-H (2930 cm-1) group C=O (1601 cm-1), C-O-H bond (1420 cm1) and C-O-C bonds (1033 cm-1), spectrum of sodium alginate the isolated according to the comparison of sodium alginate.
DAFTAR ISI
Halaman
JUDUL ... i
HALAMAN PENGESAHAN ... iii
KATA PENGANTAR ... iv
ABSTRAK ... vi
ABSTRACT ... vii
DAFTAR ISI ... viii
DAFTAR TABEL ... xii
DAFTAR GAMBAR ... xiii
DAFTAR LAMPIRAN ... xiv
BAB I PENDAHULUAN ... 1
1.1 Latar Belakang ... 1
1.2 Perumusan Masalah ... 3
1.3 Hipotesis ... 3
1.4 Tujuan Penelitian ... 4
1.5 Manfaat Penelitian ... 4
BAB II TINJAUAN PUSTAKA ... 5
2.1 Uraian Tumbuhan ... 5
2.1.1 Habitat dan sebaran tumbuhan ... 5
2.1.2 Morfologi tumbuhan ... 5
2.1.3 Sistematika tumbuhan ... 6
2.1.5 Perkembangbiakan tumbuhan ... 6
2.1.6 Kandungan kimia tumbuhan ... 7
2.2 Alginat ... 8
2.2.1 Natrium alginat ... 9
2.2.2 Sumber alginat ... 9
2.2.3 Penggunaan alginat ... 9
2.3 Viskositas ... 10
2.3.1 Metode pengukuran viskositas dengan metode Ostwald ... 11
2.4 Spektrofotometri Inframerah ... 12
2.4.1 Spektrofotometri inframerah fourier transform ... 13
2.4.1.1 Vibrasi molekul ... 14
2.4.1.2 Peralatan ... 15
2.4.2 Penanganan sampel ... 16
BAB III METODE PENELITIAN ... 18
3.1 Alat ... 18
3.2 Bahan ... 18
3.3 Pengumpulan dan Pengolahan Bahan Tumbuhan ... 19
3.3.1 Pengumpulan bahan tumbuhan ... 19
3.3.2 Identifikasi bahan tumbuhan ... 19
3.3.3 Pemeriksaan makroskopik tumbuhan segar ... 19
3.3.4 Pengolahan bahan tumbuhan ... 19
3.4 Pembuatan Larutan Pereaksi ... 20
3.4.2 Larutan kalsium klorida 1,0% ... 20
3.4.3 Larutan natrium karbonat 5,0% ... 20
3.4.4 Larutan natrium hipoklorit 0,25% ... 20
3.4.5 Larutan natrium hipoklorit 0,50% ... 20
3.4.6 Larutan natrium hipoklorit 0,75% ... 21
3.4.7 Larutan natrium hipoklorit 1,0% ... 21
3.4.8 Larutan natrium hipoklorit 1,25% ... 21
3.4.9 Larutan hidrogen peroksida 0,25% ... 21
3.4.10 Larutan hidrogen peroksida 0,50% ... 21
3.4.11 Larutan hidrogen peroksida 0,75% ... 21
3.4.12 Larutan hidrogen peroksida 1,0% ... 21
3.4.13 Larutan hidrogen peroksida 1,25% ... 21
3.4.14 Larutan natrium hidroksida 0,1N ... 22
3.4.15 Larutan air kloroform ... 22
3.5 Pemeriksaan Karakteristik Simplisia ... 22
3.5.1 Pemeriksaan makroskopik ... 22
3.5.2 Pemeriksaan mikroskopik ... 22
3.5.3 Penetapan kadar air ... 22
3.5.4 Penetapan kadar sari yang larut dalam air ... 23
3.5.5 Penetapan kadar sari yang larut dalam etanol ... 23
3.5.6 Penetapan kadar abu total ... 24
3.5.7 Penetapan kadar abu yang tidak larut dalam asam ... 24
3.6 Isolasi Natrium Alginat ... 24
3.6.2 Tahap pemutihan ... 25
3.6.3 Tahap ekstraksi ... 25
3.6.4 Tahap pembuatan natrium alginat ... 25
3.7 Pemeriksaan Karakteristik Natrium Alginat ... 26
3.7.1 Identifikasi natrium alginat ... 26
3.7.2 Penetapan susut pengeringan ... 26
3.7.3 Penetapan kadar abu total ... 26
3.7.4 Penetapan kadar abu tidak larut dalam asam ... 26
3.7.5 Penetapan viskositas ... 27
3.7.6 Karakteristik natrium alginat secara spektrofotometri inframerah ... 27
BAB IV HASIL DAN PEMBAHASAN ... 28
4.1 Hasil Identifikasi Tumbuhan ... 28
4.2 Hasil Karakteristik Tumbuhan Segar dan Simplisia ... 28
4.3 Hasil Isolasi Natrium Alginat ... 30
4.4 Hasil Karakteristik Natrium Alginat ... 33
BAB V KESIMPULAN DAN SARAN ... 37
5.1 Kesimpulan ... 37
5.2 Saran ... 38
DAFTAR PUSTAKA ... 39
DAFTAR TABEL
Tabel Halaman 4.1 Hasil Pemeriksaan Karakteristik Simplisia
Sargaasum plagyophyllum (Mertens) J.G. Agardh ... 29
4.2 Hasil Rendemen Natrium Alginat dengan Berbagai Konsentrasi
Pemutih ... 32
4.3 Spesifikasi Natrium Alginat Hasil Isolasi Dibandingkan dengan
Pustaka (Handbook of Pharmaceutical Excipients) ... 33
4.4 Viskositas dan Warna Natrium Alginat dengan Berbagai
Konsentrasi Pemutih ... 34
4.5 Data Spektrum Inframerah Natrium Alginat Hasil Isolasi dan
DAFTAR GAMBAR
Gambar Halaman 2.1 Struktur Asam Alginat ... 8
DAFTAR LAMPIRAN
Lampiran Halaman 1. Hasil Identifikasi Tumbuhan ... 42 2. Gambar Makroskopik Tumbuhan Segar dan Simplisia Sargassum
plagyophyllum (Mertens) J.G. Agardh ... 43
3. Gambar Serbuk Simplisia Sargassum plagyophyllum (Mertens) J.G. Agardh ... 44 4. Gambar Mikroskopik Serbuk Simplisia Sargassum plagyophyllum
(Mertens) J.G. Agardh ... 45 5. Perhitungan Pemeriksaan Karakteristik Simplisia Sargassum
plagyophyllum (Mertens) J.G. Agardh ... 46
6. Bagan Isolasi dan Karakterisasi Natrium Alginat ... 51
7. Perhitungan Karakteristik Natrium Alginat dari Sargassum
plagyophyllum (Mertens) J.G. Agardh ... 52
8. Gambar Spektrum Inframerah Sampel Natrium Alginat dan
ISOLASI DAN KARAKTERISASI NATRIUM ALGINAT DARI ALGA COKLAT Sargassum plagyophyllum (Mertens) J.G. Agardh SERTA
PENGARUH PENAMBAHAN KONSENTRASI PEMUTIH TERHADAP VISKOSITAS
ABSTRAK
Alga coklat merupakan salah satu sumber produksi alginat yang cukup potensial. Sargassum plagyophyllum (Mertens) J.G. Agardh adalah salah satu jenis alga coklat sebagai penghasil alginat yang belum banyak dimanfaatkan dan terdapat diperairan Indonesia, khususnya Sumatera Utara.
Tujuan penelitian ini untuk mengetahui karakteristik simplisia Sargassum
plagyophyllum (Mertens) J.G. Agardh, isolasi natrium alginat menggunakan
pemutih dengan berbagai konsentrasi yaitu 0,25%; 0,50%; 0,75%; 1,0% dan 1,25%. Identifikasi natrium alginat secara kualitatif, penetapan rendemen, pemeriksaan karakteristik natrium alginat meliputi penetapan susut pengeringan, penetapan viskositas, penetapan kadar abu total, penetapan kadar abu tidak larut asam dan identifikasi gugus fungsi dengan cara spektrofotometri inframerah.
Hasil pemeriksaan makroskopik simplisia bentuk talus menciut, tidak berasa, tidak berbau dan berwarna coklat kehitaman. Pemeriksaan mikroskopik serbuk terlihat adanya sel-sel parenkim yang berisi pigmen berwarna coklat dan terdapat sel propagule yang memiliki dua sel. Kadar air 9,97%, kadar sari larut air 11,78%, kadar sari larut etanol 2,34%, kadar abu total 17,52%, kadar abu tidak larut asam 0,48%. Identifikasi natrium alginat secara kualitatif memberikan hasil yang positif terhadap semua perlakuan, rendemen natrium alginat tertingi adalah 16,63% dengan konsentrasi pemutih 1,25% dan rendemen natrium alginat terendah adalah 9,99% dengan konsentrasi pemutih 0,25%. Penetapan susut pengeringan 6,21%, kadar abu total 9,80%, kadar abu tidak larut asam 0,43%. Penetapan viskositas adalah 24,24 cps yang diperoleh dari konsentrasi pemutih 0,25% dengan warna serbuk coklat tua, sedangkan konsentrasi pemutih 1,25% diperoleh 15,23 cps dengan warna serbuk putih. Hasil spektrofotometri inframerah menunjukkan adanya gugus O-H (3446 cm-1), gugus C-H alifatik (2930 cm-1) gugus C=O (1601 cm-1), ikatan C-O-H (1420 cm-1) dan ikatan C-O-C (1033 cm-1), spektrum natrium alginat hasil isolasi sesuai dengan natrium alginat pembanding.
ISOLATION AND CHARACTERIZATION OF SODIUM ALGINATE FROM BROWN ALGAE Sargassum plagyophyllum (Mertens) J.G.
Agardh AND BLEACH OF EFFECT CONCENTRATION ADDITION ON THE VISCOSITY
ABSTRACT
Brown algae is one a source of alginate production considerable potential.
Sargassum plagyophyllum (Mertens) J.G. Agardh is one type of brown algae as a
producer of alginate and there has not been much exploited waters of Indonesia, especially North Sumatera.
The purpose of this study to investigate the characteristics of crude drugs
Sargassum plagyophyllum (Mertens) J.G. Agardh, isolation of sodium alginate
with various concentrations of bleach that is 0.25%, 0.50%, 0.75%, 1.0% and 1.25%. Sodium alginate are qualitatively identification, determination of yield, the characteristics of sodium alginate examination includes determination of loss on drying, viscosity determination, determination of total ash content, determination of acid insoluble ash content and identification of functional groups by infrared spectrophotometry.
Macroscopic examination crude form of talus wrinkled, tasteless, odorless and blackish brown. Microscopic examination of pollen seen the parenchyma cells containing brown pigment and there propagule cell has two cells. Water content 9.97%, the levels of water-soluble extract 11.78%, levels of ethanol soluble extract 2.34%, 17.52% total ash, acid insoluble ash content of 0.48%. Qualitative identification of sodium alginate yielded positive results for all treatments, sodium alginate highest yield was 16.63% with a 1.25% concentration of bleach and sodium alginate yield the lowest is 9.99% with a 0.25% concentration of bleach. Determination of loss on drying of 6.21%, total ash of 9.80%, acid insoluble ash content of 0.43%. Determination of viscosity is 24.24 cps obtained from a concentration bleach of 0.25% with the color of the powder is dark brown, while a concentration bleach of 1.25% is obtained 15.23 cps with the color of the powder is white. The results of infrared spectrophotometry showed an O-H group (3446 cm-1), aliphatic C-H (2930 cm-1) group C=O (1601 cm-1), C-O-H bond (1420 cm1) and C-O-C bonds (1033 cm-1), spectrum of sodium alginate the isolated according to the comparison of sodium alginate.
BAB I
PENDAHULUAN
1.1Latar Belakang
Salah satu sumber daya alam yang cukup potensial dari perairan laut Indonesia adalah rumput laut atau alga dan diperdagangan dikenal dengan nama
seaweed (Sulastri, 2011). Alga yang hidup di perairan Indonesia sangat beragam
sekitar 782 jenis, yaitu 196 alga hijau, 134 alga coklat, dan 452 alga merah. Di Indonesia jenis alga diatas bernilai ekonomis dan telah diperdagangkan sejak dahulu, yaitu dari golongan alga merah Eucheuma sp., Gracillaria sp., Hypnea sp.
dan Gelidium sp., sedangkan golongan alga coklat yaitu Hormophysa sp., Padina
sp., Sargassum sp. dan Turbinaria sp. (Anggadiredja, dkk., 2011; Winarno, 1990)
Alga tumbuh dan tersebar hampir diseluruh perairan Indonesia, dan daerah yang mempunyai potensi sebagai penghasil alga cukup luas antara lain, Sumatera Utara, Sumatera Barat, Riau, Bali, Nusa Tenggara Barat, Nusa Tenggara Timur dan Maluku (Aslan, 1998). Alga coklat (Phaeophyceae) dan alga merah (Rhodophyceae) merupakan sumber alginat, agar-agar dan karagenan. Alga coklat merupakan sumber produksi alginat yaitu kelompok polisakarida yang terdiri dari asam manuronat dan asam guluronat juga mengandung pigmen klorofil a dan c, beta karoten, violasantin dan fukosantin (Lobban dan Wynne, 1981; Marpaung, 2005).
Sargassum plagyophyllum (Mertens) J.G. Agardh adalah salah satu jenis
terdapat di perairan Indonesia, khususnya Propinsi Sumatera Utara yaitu di daerah pantai Poncan, Kota Sibolga Kabupaten Tapanuli Tengah.
Peneliti terdahulu telah melakukan penelitian terhadap enam spesies alga coklat sebagai penghasil alginat yaitu Sargassum crassifolium J.G. Agardh dan
Turbinaria conoides J.G. Agardh (Supomo, 2002), Hormophysa triquetra (L) J.
Agardh (Susanti, 2003), Turbinaria decurrens Bory (Marpaung, 2005),
Sargassum ilicifolium (Turner) C. Agardh (Aris, dkk., 2012) dan Sargassum
polycystum C. Agardh (Aryani, 2004).
Alginat dalam pemanfaatannya berupa natrium alginat yaitu suatu garam alginat yang larut dalam air. Natrium alginat banyak digunakan untuk kebutuhan industri misalnya industri farmasi, makanan, tekstil, cat dan beberapa industri lainnya (Rasyid, 2005). Diperdagangan warna dan viskositas natrium alginat merupakan persyaratan kualitas yang telah ditetapkan, yaitu persyaratan warna serbuk natrium alginat adalah berwarna putih kekuningan sampai putih, sedangkan viskositas natrium alginat adalah 20-400 cps (Anggadiredja, dkk., 2011; Rowe, dkk., 2009).
penetapan kadar abu total, penetapan kadar abu tidak larut asam serta identifikasi gugus fungsi dengan cara spektrofotometri inframerah.
1.2Perumusan Masalah
Perumusan masalah pada penelitian ini adalah:
a. apakah karakteristik simplisia yang diperoleh dari Sargassum
plagyophyllum (Mertens) J.G. Agardh dapat digunakan sebagai acuan?
b. apakah rendemen natrium alginat yang diperoleh dari Sargassum
plagyophyllum (Mertens) J.G. Agardh memenuhi persyaratan yang
ditetapkan?
c. apakah penambahan konsentrasi pemutih dapat mempengaruhi warna dan nilai viskositas natrium alginat?
1.3Hipotesis
Hipotesis pada penelitian ini adalah:
a. karakteristik simplisia yang diperoleh dari Sargassum plagyophyllum
(Mertens) J.G. Agardh dapat digunakan sebagai acuan.
b. rendemen natrium alginat yang diperoleh dari Sargassum plagyophyllum
(Mertens) J.G. Agardh memenuhi persyaratan yang ditetapkan.
1.4Tujuan Penelitian
Tujuan pada penelitian ini adalah:
a. untuk memperoleh informasi mengenai karakteristik simplisia dari
Sargassum plagyophyllum (Mertens) J.G. Agardh agar nantinya digunakan
sebagai acuan.
b. untuk memperoleh informasi mengenai rendemen natrium alginat yang diperoleh dari Sargassum plagyophyllum (Mertens) J.G. Agardh.
c. untuk memperoleh informasi mengenai pengaruh penambahan konsentrasi pemutih terhadap warna dan nilai viskositas natrium alginat hasil isolasi.
1.5 Manfaat Penelitian
BAB II
TINJAUAN PUSTAKA
2.1 Uraian Tumbuhan
Uraian tumbuhan meliputi habitat dan sebaran tumbuhan, morfologi tumbuhan, sistematika tumbuhan, nama daerah, perkembangbiakan tumbuhan, kandungan kimia tumbuhan.
2.1.1 Habitat dan sebaran tumbuhan
Daerah sebaran beberapa jenis alga di Indonesia sangat luas, baik yang tumbuh secara alami maupun yang dibudidayakan. Wilayah sebaran alga yang tumbuh alami terdapat hampir diseluruh perairan dangkal laut Indonesia (Anggadiredja, dkk., 2011).
Habitat dan sebaran Sargassum sp. di Indonesia pada umumnya tumbuh di perairan yang terlindung maupun yang berombak besar pada habitat batu (Indriani dan Sumiarsih, 2001). Pengaruh alam yang banyak menentukan sebarannya adalah jenis substrat, cahaya matahari, kadar garam (salinitas), ombak arus dan pasang surut. Substrat dasar tempat melekat biasanya berupa karang, batu, lumpur, pasir, kerang, atau kayu. Penyebaran jenis Sargassum plagyophyllum
(Mertens) J.G. Agardh banyak tumbuh pada substrat batu di daerah rataan terumbu karang khususnya di perairan Propinsi Sumatera Utara (Atmadja, dkk., 1996).
2.1.2 Morfologi tumbuhan
Sargassum plagyophyllum (Mertens) J.G. Agardh mempunyai percabangan utama bagian bawah gepeng tetapi agak membulat pada bagian atas. Batang utama agak silindris, pendek sekitar 1,5 cm. Tinggi rumpun dapat mencapai 60 cm, “daun” oval sampai lonjong, panjang sekitar 4 cm, lebar 1,4 cm, pinggir bergerigi, ujung runcing dan kebagian atas mengecil, bentuk holdfast menggarpu ( Atmadja, dkk., 1996).
2.1.3 Sistematika tumbuhan
Berdasarkan hasil identifikasi yang diteliti di Lembaga Ilmu Pengetahuan Indonesia Pusat Penelitian Oseanografi Jakarta, taksonomi alga coklat diklasifikasikan sebagai berikut:
Filum / Divisio : Phaeophyta Kelas / Class : Phaeophyceae Bangsa / Order : Fucales Suku / Family : Sargassaceae Marga / Genus : Sargassum
Jenis / Species : Sargassum plagyophyllum (Mertens) J.G. Agardh
2.1.4 Nama daerah
Nama daerah Sargassum plagyophyllum (Mertens) J.G. Agardh di daerah Pantai Poncan Kota Sibolga Kabupaten Tapanuli Tengah Propinsi Sumatera Utara,dikenal dengan nama Jariango.
2.1.5 Perkembangbiakan tumbuhan
tumbuh menjadi tanaman baru. Sementara perbanyakan secara generatif dikembangkan melalui spora, baik alamiah maupun melalui budidaya. Pertemuan dua gamet membentuk zygot yang selanjutnya berkembang menjadi sporofit. Individu baru inilah yang mengeluarkan spora dan berkembang melalui pembelahan dalam sporogenesis menjadi gametofit (Anggadiredja, dkk., 2011).
Faktor biologi utama yang menjadi pembatas produktivitas alga yaitu faktor persaingan dan pemangsa dari hewan herbivora. Selain itu, dapat juga dihambat oleh faktor morbiditas dan mortalitas alga itu sendiri. Morbiditas disebabkan oleh penyakit dari infeksi mikroorganisme, tekanan lingkungan perairan (fisika dan kimia perairan) yang buruk, serta tumbuhnya tanaman penempel (parasit). Sementara, mortalitas dapat disebabkan oleh pemangsaan hewan-hewan herbivora (Aslan, 1998).
2.1.6 Kandungan kimia tumbuhan
Sargassum plagyophyllum (Mertens) J.G. Agardh merupakan jenis Alga
2.2 Alginat
Alginat merupakan hidrokoloid yang diekstraksi dari Phaeophyceae (alga coklat), terutama jenis Sargassum plagyophyllum (Mertens) J.G. Agardh (Anggadiredja, dkk., 2011). Alginat juga merupakan kelompok polisakarida yang terbentuk dalam dinding sel alga coklat dengan kadar mencapai 40% dari total berat kering. Alginat tersusun atas asam guluronat dan manuronat, dengan ikatan 1,4 β-D-asam manuronat dan α-L-guluronat (Rasyid, 2003).
Alginat pertama kali ditemukan oleh Stanford pada awal tahun 1880-an, ketika diisolasinya alginat ini tidak berhasil diperoleh dalam keadaan murni. Peneliti selanjutnya yaitu Krefting mengisolasi alginat dalam keadaan murni, dia menganggap alginat memiliki bahan baru yang disebut tangsaure ataupun asam alginat. Alginat di dalam perdagangan ditemukan sebagai campuran garam natrium, kalium, kalsium dan magnesium (Chapman dan Chapman, 1980; Rachmat, 2012). Struktur asam alginat dapat dilihat pada Gambar 2.1 berikut:
Gambar 2.1 Struktur Asam Alginat Keterangan: M = β-D asam manuronat
G = α-L asam guluronat
2.2.1 Natrium alginat
dalam air dengan membentuk larutan koloid, kental, tidak larut dalam alkohol, kloroform, eter dan larutan asam jika pH dibawah 3, menurut Ekstra Farmakope Indonesia (1974) kadar natrium alginat yaitu >18% dari total berat kering. Asam alginat tidak larut dalam air, karena itu yang digunakan dalam industri adalah dalam bentuk garam natrium (Belitz dan Grosch, 1987).
2.2.2 Sumber Alginat
Umumnya alginat terdapat dalam semua jenis alga yang tergolong dalam kelas Phaeophyceae dengan kadar yang berbeda-beda. Secara komersial sebagian besar alginat diproduksi hanya dari jenis Macrocystis pyrifera, Laminaria byperborea, Laminaria digitata, Laminaria japonica, Ascophyllum nodosum,
Ecklonia maxima, Eisenia bycyclis (Rasyid, 2003). Jumlah polisakarida yang
terdapat pada masing-masing alga coklat berbeda-beda tergantung dari spesies, tempat tumbuh, dan iklim, yaitu antara 15 – 40% terhadap berat kering (Winarno, 1990).
2.2.3Penggunaan Alginat
1. Bidang farmasi dan kosmetika
Dalam bidang farmasi alginat digunakan sebagai suspending agent (stabilisasi untuk emulsi dan suspensi) misalnya dalam sediaan antasida untuk pengobatan lambung, bahan pengental, pengikat, sebagai bahan penghancur pada sediaan tablet dan alginat juga dapat digunakan sebagai gel untuk sediaan obat luar.
misalnya pada pembuatan shampoo cair karena dapat meningkatkan viskositas dan pensuspensi bahan padat sehingga digunakan sebagai koloid pelindung.
2. Bidang industri makanan
Alginat dikenal tidak memiliki toksisitas jangka pendek dan jangka panjang dan tidak menyebabkan alergi sehingga digunakan sebagai zat tambahan makanan. Pada industri makanan digunakan sebagai bahan pembentuk gel, pengental, bahan pengemulsi, dan bahan penahan air dalam industri hasil olahan susu, roti, kue, dan makanan lain.
3. Bidang industri lain
Pada industri cat digunakan sebagai pengental cat (dye thickener) dan bahan perekat (adhesive) (Brunetton, 1995; Yulianto, 2007).
2.3 Viskositas
Viskositas adalah suatu sifat dari cairan yang lebih bertahan untuk mengalir (Martin, dkk., 1993). Viskositas dapat dianggap sebagai suatu sifat yang relatif dengan air sebagai bahan rujukan dan semua viskositas dinyatakan dalam istilah-istilah viskositas air murni pada suhu 20oC. Viskositas air yaitu 1,0050 centipoise disingkat dengan cps. Makin kental suatu cairan, makin besar kekuatan yang diperlukan agar cairan tersebut mengalir dengan laju tertentu (Lachman, dkk., 1989; Yulianto, 2007).
Faktor-faktor yang mempengaruhi viskositas larutan adalah sebagai berikut:
2. Konsentrasi larutan, bertambahnya konsentrasi larutan akan meningkatkan viskositas.
3. Temperatur, viskositas akan turun dengan naiknya suhu. 4. Tekanan, viskositas cairan akan naik dengan naiknya tekanan.
2.3.1 Metode pengukuran viskositas dengan metode Ostwald
Metode ini ditentukan berdasarkan hukum Poiseuille menggunakan alat viskometer Ostwald seperti yang terlihat pada Gambar 2.2 berikut ini:
Gambar 2.2 Viskometer Ostwald
Penetapannya dilakukan dengan jalan mengukur waktu yang diperlukan untuk mengalirkan cairan dalam pipa kapiler dari A ke C.
Sejumlah cairan yang akan diukur viskositasnya dimasukkan ke dalam viskometer yang diletakkan pada thermostat. Cairan kemudian dihisap dengan pompa dari bagian yang menggembung (E) ke dalam bagian yang menggembung di atas tanda A, dan waktu jatuhnya miniskus atas dari garis A ke garis C dari zat cair yang berisi di dalam B dihitung dengan menggunakan stopwatch, garis tengah dan panjang kapiler (D). Pada metode Ostwald yang diukur adalah waktu yang diperlukan oleh sejumlah cairan tertentu untuk mengalir melalui pipa kapiler
E A
C B
dengan gaya yang disebabkan oleh berat cairan itu sendiri (Lachman, dkk., 1989; Sukardjo, 2003).
2.4 Spektrofotometri Inframerah
Alat yang dapat menentukan spektrum serapan suatu senyawa disebut spektrofotometer inframerah. Spektrofotometer menentukan kekuatan dan kedudukan relatif dari semua serapan dalam daerah inframerah dan menggambarkannya pada kertas grafik yang sudah dikalibrasi (Supratman, 2010). Pancaran inframerah pada umumnya mengacu pada bagian spektrum elektromagnet yang terletak diantara daerah tampak dan daerah gelombang mikro. Spektrum inframerah suatu molekul adalah hasil transisi antara tingkat energi getaran (vibrasi) yang berlainan. Inti-inti atom yang terikat oleh ikatan kovalen mengalami getaran (vibrasi) atau osilasi (oscillation). Bila molekul menyerap inframerah, energi yang diserap menyebabkan kenaikan dalam amplitudo getaran atom-atom yang terikat. Jadi molekul ini berada dalam keadaan vibrasi tereksitasi
(excited vibrational state), energi yang diserap ini akan dibuang dalam bentuk
panas bila molekul itu kembali lagi (Sastrohamidjojo, 1992).
Spektrum inframerah suatu senyawa adalah grafik dari bilangan gelombang yang secara berkesinambungan berubah sepanjang suatu daerah sempit dari spektrum elektromagnetik, versus transmitan-persen atau pada absorbans (A). Kebanyakan spektrum inframerah merekam bilangan gelombang versus %T.
Bila suatu senyawa menyerap radiasi pada suatu panjang gelombang tertentu, intensitas radiasi yang diteruskan oleh contoh berkurang. Ini mengakibatkan suatu penurunan dalam %T dan terlihat pada spektrum sebagai suatu sumur (deep) yang disebut puncak absorpsi atau pita absorpsi. Bagian spektrum dimana %T menunjukkan angka 100 (atau hampir 100) disebut garis dasar (base line) yang direkam pada spektrum inframerah pada bagian atas (Supratman, 2010).
2.4.1 Spektrofotometri inframerah fourier transform
Radiasi inframerah dapat dianalisis dengan spektroskopi FTIR yang bagiannya terdiri dari cermin gerak, cermin statik, dan pembagi berkas radiasi. Radiasi yang berasal dari sumber radiasi inframerah dikolimasikan oleh sebuah cermin cekung ke pembagi berkas radiasi, setengah berkas dilewatkan cermin statik dan setengah berkas lainnya ke cermin gerak. Pergerakan cermin memodulasi semua bilangan gelombang dalam berkas radiasi. Setelah terjadi refleksi pada kedua cermin, kedua berkas tersebut bergabung kembali pada pembagi berkas radiasi.
gelombangnya dapat berinteferensi dengan kadar yang berbeda. Berkas gabungan lewat melalui sel sampel dan sampai ke detektor yang memberikan keuntungan dibandingkan dengan metode dispersi. Tiap bilangan gelombang dimodulasi dan dideteksi pada frekuensi yang berbeda, akan terjadi gangguan noise hanya pada lebar pitanya yang sempit. Sebagai hasilnya betul-betul tidak ada radiasi baur yang menyertai pengukuran fourier transform.
Bebasnya dari radiasi baur merupakan salah satu keuntungan Spektroskopi Inframerah Fourier Transform (FTIR). Sinyal analisis yang dihasilkan pada FTIR sangat kompleks dan memerlukan perubahan dengan transformasi Fourier dari bidang kekuasaan waktu (time domain) ke bidang kekuasaan frekuensi (frequency
domain) agar diperoleh spketrum inframerah biasa. Salah satu keuntungan FTIR
adalah perekaman spektrum inframerah yang sangat tepat, sehingga memungkinkan merekam komponen senyawa yang dipisahkan pada kromatografi gas (Satiadarma, dkk., 2004).
2.4.1.1 Vibrasi molekul
Suatu ikatan dalam sebuah molekul dapat mengalami berbagai vibrasi molekul. Secara umum terdapat dua tipe vibrasi molekul:
a. Stretching (vibrasi regang/ulur): vibrasi sepanjang ikatan sehingga terjadi
perpanjangan atau pemendekan ikatan.
b. Bending (vibrasi lentur/tekuk): vibrasi yang disebabkan oleh sudut ikatan
2.4.1.2 Peralatan
Spektrum inframerah umumnya merupakan spektrometer double-beam
(berkas ganda) dan terdiri dari: sumber radiasi, monokromator dan detektor. a. Sumber radiasi
Radiasi inframerah biasanya dihasilkan oleh pemijar Nernst dan Globar. Pemijar Nerst merupakan batang cekung dari Zirkunium dan Ytrium oksida yang dipanaskan hingga 1200oC dengan arus listrik. Pemijar Globar merupakan batang silikon karbida yang dipanaskan hingga 12000C dengan arus listrik.
b. Monokromator
Terdiri dari sistem celah masuk dan celah keluar, alat pendispersi yang berupa kisi difraksi atau prisma, dan cermin untuk memantulkan dan menfokuskan sinar. Bahan prisma adalah natrium klorida, kalium bromida, sesium bromida, litium fluorida. Prisma natrium klorida paling banyak digunakan, karena natrium klorida hanya transparan dibawah 625 cm-1, sedangkan halida logam lainnya harus digunakan dengan frekuensi yang rendah.
c. Detektor
2.4.2 Penanganan sampel
Bila sinar inframerah dilewatkan melalui cuplikan, maka sejumlah frekuensi diserap sedangkan frekuensi yang lain diteruskan/ditransmisikan tanpa diserap. Jika kita menggambar antara persen absorbansi atau persen transmitansi dengan bilangan gelombang maka akan dihasilkan spektrum inframerah. Cara penanganan sampel, tergantung dari jenis sampelnya (padat dan cair). Spektrum inframerah biasanya menunjukkan pengaruh dari perbedaan penanganan sampel dalam bentuk pergeseran frekuensi atau pita serapan.
a. Cairan
Cara yang paling mudah dalam penanganan sampel bentuk cairan adalah menempatkan cuplikan tersebut sebagai film yang tipis diantara lapis natrium klorida yang transparan terhadap inframerah.
b. Padatan
Ada dua cara untuk penanganan sampel padatan:
1. Mull atau pasta, sampel padat digerus hingga halus dalam mortar dengan meneteskan hidrokarbon cair (Nujol, Kaydol) hingga diperoleh pasta yang halus, selanjutnya pasta ditekan antara dua plat natrium klorida hingga diperoleh film yang tipis.
BAB III
METODE PENELITIAN
Penelitian ini dilakukan secara eksperimental yang meliputi pengumpulan dan pengolahan bahan tumbuhan, pemeriksaan karakteristik simplisia, isolasi natrium alginat menggunakan pemutih dengan berbagai konsentrasi yaitu 0,25%; 0,50%; 0,75%; 1,0% dan 1,25%. Identifikasi natrium alginat dilakukan secara kualitatif, penetapan rendemen, karakterisasi natrium alginat meliputi penetapan susut pengeringan, penetapan viskositas, penetapan kadar abu total, penetapan kadar abu tidak larut asam, dan identifikasi gugus fungsi dengan cara spektrofotometri inframerah.
3.1 Alat
3.2Bahan
Bahan-bahan yang digunakan pada penelitian ini adalah alga coklat
Sargassum plagyophyllum (Mertens) J.G. Agardh. Bahan-bahan kimia yang
digunakan adalah berkualitas pro analisis (E. Merck) yaitu toluen, asam klorida, etanol 96%, asam sulfat, natrium hidroksida, kloralhidrat, kalsium klorida, hidrogen peroksida, kloroform, natrium karbonat, isopropanol, kecuali natrium hipoklorit dan air suling.
3.3Pengumpulan dan Pengolahan Bahan Tumbuhan
3.3.1 Pengumpulan bahan tumbuhan
Pengumpulan bahan tumbuhan dilakukan secara purposif yaitu tanpa membandingkan dengan tumbuhan dari daerah lain. Bahan tumbuhan yang digunakan adalah alga coklat jenis Sargassum plagyophyllum (Mertens) J.G. Agardh yang diperoleh dari Pantai Poncan Kota Sibolga Kabupaten Tapanuli Tengah Propinsi Sumatera Utara pada bulan Juli 2012.
3.3.2 Identifikasi bahan tumbuhan
Identifikasi bahan tumbuhan dilakukan di Lembaga Ilmu Pengetahuan Indonesia Pusat Penelitian Oseanografi, Jakarta. Hasil identifikasi tumbuhan dapat dilihat pada Lampiran 1, halaman 42.
3.3.3 Pemeriksaan makroskopik tumbuhan segar
3.3.4 Pengolahan bahan tumbuhan
Bahan tumbuhan yang telah dikumpulkan, direndam dalam air ledeng kemudian dibersihkan dari kotoran-kotoran dan sisa karang yang melekat. Dicuci berkali-kali dengan air mengalir sampai bersih, ditiriskan dan ditimbang beratnya. Berat bahan basah adalah 28,20 kg, bahan tumbuhan disebarkan diatas kertas lalu dikeringkan dengan cara diangin-anginkan dan dimasukkan ke dalam lemari pengering hingga kering sampai simplisia tersebut jika diremas akan hancur. Berat bahan kering adalah 2,38 kg. Selanjutnya simplisia diblender sampai menjadi serbuk, kemudian serbuk simplisia disimpan dalam kantung plastik. Gambar serbuk simplisia dapat dilihat pada Lampiran 3, halaman 44.
3.4 Pembuatan Larutan Pereaksi (Ditjen POM, 1995)
3.4.1 Larutan asam klorida 5,0% (v/v)
Asam klorida pekat sebanyak 13,51 ml diencerkan dengan air suling hingga volumenya 100 ml.
3.4.2 Larutan kalsium klorida 1,0% (b/v)
Kalsium klorida sebanyak 1 g dilarutkan dalam air suling hingga volumenya 100 ml.
3.4.3 Larutan natrium karbonat 5,0% (b/v)
Natrium karbonat sebanyak 5 g dilarutkan dalam air suling hingga volumenya 100 ml.
3.4.4 Larutan natrium hipoklorit 0,25% (v/v)
3.4.5 Larutan natrium hipoklorit 0,50% (v/v)
Natrium hipoklorit 5,25% sebanyak 9,52 ml diencerkan dengan air suling hingga volumenya 100 ml.
3.4.6 Larutan natrium hipoklorit 0,75% (v/v)
Natrium hipoklorit 5,25% sebanyak 14,28 ml diencerkan dengan air suling hingga volumenya 100 ml.
3.4.7 Larutan natrium hipoklorit 1,0% (v/v)
Natrium hipoklorit 5,25% sebanyak 19,04 ml diencerkan dengan air suling hingga volumenya 100 ml.
3.4.8 Larutan natrium hipoklorit 1,25% (v/v)
Natrium hipoklorit 5,25% sebanyak 23,80 ml diencerkan dengan air suling hingga volumenya 100 ml.
3.4.9 Larutan hidrogen peroksida 0,25% (v/v)
Hidrogen peroksida 30% sebanyak 0,83 ml diencerkandengan air suling hingga volumenya 100 ml
3.4.10 Larutan hidrogen peroksida 0,50% (v/v)
Hidrogen peroksida 30% sebanyak 1,67 ml diencerkankan dengan air suling hingga volumenya 100 ml.
3.4.11 Larutan hidrogen peroksida 0,75% (v/v)
Hidrogen peroksida 30% sebanyak 2,50 ml diencerkan dengan air suling hingga volumenya 100 ml.
3.4.12 Larutan hidrogen peroksida 1,0% (v/v)
3.4.13 Larutan hidrogen peroksida 1,25% (v/v)
Hidrogen peroksida 30% sebanyak 4,16 ml diencerkan dengan air suling hingga volumenya 100 ml.
3.4.14 Larutan natrium hidroksida 0,1 N (b/v)
Natrium hidroksida sebanyak 0,40 g dilarutkan dalam air suling hingga volumenya 100 ml.
3.4.15 Air kloroform
Kloroform sebanyak 2,50 ml dicampurkan dalam air suling hingga volumenya 1000 ml.
3.5 Pemeriksaan Karakteristik Simplisia
3.5.1 Pemeriksaan makroskopik
Pemeriksaan makroskopik simplisia dilakukan terhadap bentuk “batang” dan “daun”, rasa, bau dan warna simplisia. Gambar makroskopik simplisia dapat dilihat pada Lampiran 2, halaman 43.
3.5.2 Pemeriksaan mikroskopik
Pemeriksaan mikroskopik dilakukan terhadap serbuk simplisia alga coklat yang dikeringkan. Serbuk simplisia ditaburkan di atas kaca objek yang telah ditetesi larutan kloralhidrat, kemudian ditutup dengan kaca penutup lalu diamati di bawah mikroskop. Gambar mikroskopik dapat dilihat pada Lampiran 4, halaman 45.
3.5.3 Penetapan kadar air
Cara kerja:
Ke dalam labu alas bulat dimasukkan 200 ml toluen dan 2 ml air, dipasang alat penampung dan pendingin, kemudian didestilasi selama 2 jam. Destilasi dihentikan dan toluen didinginkan selama 30 menit, dan dibaca volume air pada tabung penerima dengan ketelitian 0,05 ml. Kemudian ke dalam labu tersebut dimasukkan 5 g serbuk simplisia yang telah ditimbang seksama, labu dipanaskan hati-hati selama 15 menit. Setelah toluen mendidih, kecepatan tetesan diatur 2 tetes untuk tiap detik sampai sebagian besar air terdestilasi, kemudian kecepatan destilasi dinaikkan sampai 4 tetes tiap detik. Setelah semua air terdestilasi, bagian dalam pendingin dibilas dengan toluen yang telah dijenuhkan. Destilasi dilanjutkan selama 5 menit, kemudian tabung penerima dibiarkan mendingin pada suhu kamar. Setelah air dan toluen memisah sempurna, volume air dibaca dengan ketelitian 0,05 ml. Selisih kedua volume air yang dibaca sesuai dengan kandungan air yang terdapat dalam bahan yang diperiksa. Kadar air dihitung dalam persen.
3.5.4 Penetapan kadar sari yang larut dalam air
3.5.5 Penetapan kadar sari yang larut dalam etanol
Sebanyak 5 g serbuk yang telah dikeringkan, dimaserasi selama 24 jam dalam 100 ml etanol 96% dalam labu bersumbat sambil dikocok sesekali selama 6 jam pertama, kemudian dibiarkan selama 18 jam. Kemudian disaring cepat untuk menghindari penguapan etanol. Sejumlah 20 ml filtrat diuapkan sampai kering dalam cawan penguap yang berdasar rata yang telah dipanaskan dan ditara. Sisa dipanaskan pada suhu 105oC sampai bobot tetap. Kadar dalam persen sari yang larut dalam etanol 96% dihitung terhadap bahan yang telah dikeringkan (Depkes, 1980).
3.5.6 Penetapan kadar abu total
Sebanyak 2 g serbuk yang telah digerus dan ditimbang seksama dimasukkan dalam krus porselin yang telah dipijar dan ditara, kemudian diratakan. Krus dipijar perlahan-lahan sampai arang habis, pijaran dilakukan pada suhu 600oC selama 6 jam kemudian didinginkan dan ditimbang sampel sampai diperoleh bobot tetap. Kadar abu dihitung terhadap bahan yang telah dikeringkan (Depkes, 1980).
3.5.7 Penetapan kadar abu tidak larut dalam asam
Abu yang diperoleh dalam penetapan kadar abu total dididihkan dalam 25 ml asam klorida encer selama 5 menit, bagian yang tidak larut dalam asam dikumpulkan, disaring melalui kertas saring dipijar sampai bobot tetap, kemudian didinginkan dan ditimbang. Kadar abu yang tidak larut dalam asam dihitung terhadap bahan yang telah dikeringkan (Depkes, 1980).
3.6 Isolasi Natrium Alginat
Proses isolasi alginat dibagi dalam empat tahap, yaitu tahap praekstraksi, pemutihan, isolasi dan pemurnian, serta pembuatan natrium alginat.
3.6.1 Tahap praekstraksi
Sebanyak 100 gram serbuk kering simplisia direndam dengan larutan asam klorida 5% selama 2 jam, disaring dan residu dicuci dengan air suling sampai netral yaitu pH 7 (Rasyid, 2003).
3.6.2 Tahap pemutihan
Residu yang telah netral yaitu pH 7 diputihkan dengan larutan natrium hipoklorit masing-masing dengan konsentrasi 0,25%, 0,50%, 0,75%, 1,0% dan 1,25% selama 2,5 jam, kemudian disaring dan residu dicuci dengan air suling sampai netral yaitu pH 7 (Rasyid, 2003).
3.6.3 Tahap ekstraksi
3.6.4 Tahap pembuatan natrium alginat
Asam alginat yang berbentuk gel dilarutkan dalam larutan natrium karbonat 5% dan diendapkan dengan larutan isopropanol 95%. Natrium alginat yang diperoleh dikeringkan, kemudian dihaluskan. Bagan isolasi dan karakterisasi natrium alginat dapat dilihat pada Lampiran 6, halaman 51.
3.7 Pemeriksaan Karakteristik Natrium Alginat
3.7.1 Identifikasi natrium alginat secara kualitatif (Ditjen POM, 1995)
a. Pada 5 ml larutan dalam natrium hidroksida 0,1 N ditambahkan 1 ml kalsium klorida, terbentuk endapan ruah menyerupai jeli.
b. Pada 5 ml larutan dalam natrium hidtroksida 0,1 N, ditambahkan 1 ml asam sulfat 4 N, terbentuk endapan berat menyerupai jeli.
3.7.2 Penetapan susut pengeringan
Susut pengeringan adalah kadar bagian yang menguap dari suatu zat. Sebanyak 1 gram serbuk kering ditimbang seksama dalam botol timbang dangkal bertutup yang sebelumnya telah dipanaskan pada suhu 105oC selama 30 menit dan telah ditara. Zat diratakan dalam botol timbang hingga merupakan lapisan setebal 5–10 mm, dimasukkan ke dalam lemari pengering, tutupnya dibuka lalu dikeringkan pada suhu 105oC hingga bobot tetap. Sebelum setiap pengeringan, biarkan botol dalam keadaan tertutup mendingin dalam deksikator hingga suhu kamar. Susut pengeringan dihitung tehadap bahan awal (Depkes, 1980).
3.7.3 Penetapan kadar abu total
3.7.4 Penetapan kadar abu tidak larut dalam asam
Penetapan kadar abu tidak larut dalam asam dilakukan sama seperti penetapan kadar abu tidak larut dalam asam terhadap simplisia (Depkes, 1980).
Hasil pemeriksaan karakteristik natrium alginat dapat dilihat pada Tabel 4.3, halaman 33 dan hasil perhitungannya dapat dilihat pada Lampiran 7, halaman 52 sampai halaman 54.
3.7.5 Penetapan viskositas
Metode yang digunakan untuk pengukuran kekentalan adalah metode kapiler yaitu penetapan waktu yang dibutuhkan oleh sejumlah volume cairan tertentu untuk mengalir melalui kapiler. Pengukuran natrium alginat dilakukan dengan tingkat kekentalan 2 % (b/v).
Alat yang digunakan Viskometer Ostwald. Cara penetapan:
Tabung diisi dengan sejumlah tertentu cairan (atur suhu 200C), diatur miniskus cairan dalam tabung kapiler hingga garis batas atas dengan bantuan pengisapan. Buka tabung kapiler agar cairan dapat mengalir turun. Catat waktu (dalam detik) yang diperlukan cairan untuk mengalir dari batas atas hingga batas bawah dalam tabung kapiler (Ditjen POM, 1995). Hasil pemeriksaan dapat dilihat pada Tabel 4.4, halaman 34.
3.7.6 Karakteristik natrium alginat secara spektrofotometri inframerah FTIR
BAB IV
HASIL DAN PEMBAHASAN
4.1 Hasil Identifikasi Tumbuhan
Hasil identifikasi tumbuhan yang dilakukan di Lembaga Ilmu Penelitian Indonesia Pusat Penelitian Oseanografi, Jakarta adalah alga coklat jenis
Sargassum plagyophyllum (Mertens) J.G. Agardh, divisi Phaeophyta, kelas
Phaeophyceae, bangsa Fucales, suku Sargassaceae dan marga Sargassum.
4.2 Hasil Karakteristik Tumbuhan Segar dan Simplisia
Hasil pemeriksaaan makroskopik tumbuhan segar yang diperoleh dari
Sargassum plagyophyllum (Mertens) J.G. Agardh adalah memiliki bau yang khas,
warna coklat kehitaman, rasa asin, ”batang” silindris, “daun” oval atau lonjong, panjang sekitar 4 cm, lebar 1,4 cm, pinggir daun bergerigi, memiliki holdfast dan bentuk percabangan selang seling teratur.
Hasil pemeriksaan makroskopik simplisia diperoleh berupa “batang” dan “daun” yang menciut, berwarna coklat kehitaman, tidak berbau dan tidak berasa, sedangkan hasil mikroskopik serbuk simplisia Sargassum plagyophyllum
(Mertens) J.G. Agardh terlihat adanya sel parenkim yang berisi pigmen berwarna coklat keemasan dan terdapat sel-sel propagule yang mempunyai dua sel yang berfungsi untuk menghasilkan cabang pada talus alga (Dawes, 1981 ; Marpaung, 2005).
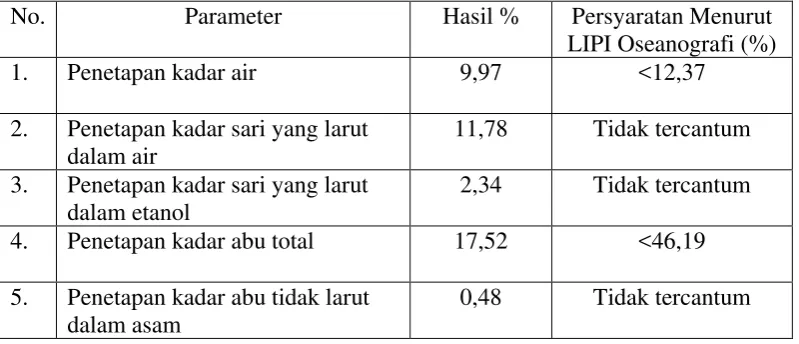
Tabel 4.1 Hasil pemeriksaan karakteristik simplisia Sargassum plagyophyllum
(Mertens) J.G. Agardh
No. Parameter Hasil % Persyaratan Menurut
LIPI Oseanografi (%)
1. Penetapan kadar air 9,97 <12,37
2. Penetapan kadar sari yang larut dalam air
11,78 Tidak tercantum 3. Penetapan kadar sari yang larut
dalam etanol
2,34 Tidak tercantum
4. Penetapan kadar abu total 17,52 <46,19
5. Penetapan kadar abu tidak larut dalam asam
0,48 Tidak tercantum
Hasil penetapan kadar air yang diperoleh lebih kecil dari 12,37%, hasil ini memenuhi persyaratan yang ditetapkan. Kadar air dalam simplisia menunjukkan jumlah air yang terkandung dalam simplisia tersebut, kadar air dalam simplisia berhubungan dengan proses pengeringan simplisia. Pengeringan merupakan usaha untuk menurunkan kadar air simplisia sampai tingkat yang diinginkan. Penetapan kadar air dilakukan untuk memberikan batasan kandungan air yang memenuhi persyaratan, karena kandungan air dalam simplisia merupakan salah satu faktor yang mempengaruhi aktivitas enzim dan aktivitas mikroba (Badan POM RI, 2005).
sari yang larut dalam air lebih tinggi daripada kadar sari yang larut dalam etanol, hal ini disebabkan alga coklat mengandung karbohidrat yang cukup tinggi (Atmadja, dkk., 1996).
Penetapan kadar abu total dilakukan untuk mengetahui kadar senyawa anorganik dan kandungan mineral dalam simplisia yang biasanya terdiri dari natrium, kalsium, fosfor, magnesium. Kadar abu yang terkandung dalam suatu produk menunjukkan tingkat kemurnian produk tersebut. Tingkat kemurnian ini sangat dipengaruhi oleh komposisi dan kandungan mineral. Hasil pemeriksaan kadar abu total yang diperoleh cukup tinggi, karena umumnya alga coklat mengandung mineral yang tinggi (Sulistijo dan Rachmaniar, 1996).
4.3 Hasil Isolasi Natrium Alginat
Metode ekstraksi yang digunakan adalah maserasi pada suhu diatas suhu kamar bertujuan untuk meningkatkan kelarutan senyawa yang akan diekstraksi dalam waktu relatif singkat (Supomo, 2002).
Sedangkan penambahan dengan larutan kalsium klorida bertujuan untuk memisahkan alginat dengan polimer asidik lain seperti laminaran sehingga diperoleh endapan kalsium alginat. Penambahan asam klorida bertujuan untuk mengubah kalsium alginat menjadi asam alginat yang mengapung di permukaan larutan dan perendaman dengan larutan hidrogen peroksida ke dalam asam alginat ini bertujuan untuk menghasilkan serbuk natrium alginat yang lebih putih. Pada penambahan larutan natrium karbonat, asam alginat tersebut diubah kembali menjadi natrium alginat (pH 9). Menurut Rowe, dkk., (2009) garam alginat paling stabil pada pH antara 4-10. Larutan natrium alginat diendapkan dengan larutan isopropanol 95% yang bertujuan untuk memurnikan natrium alginat, karena isopropanol mempunyai kemampuan dalam mengikat air dari larutan natrium alginat sehingga natrium alginat dapat tertinggal dan mengendap (Mushollaeni, 2011). Pengeringan dilakukan pada suhu 50oC selama 15 jam, kemudian digerus hingga didapatkan serbuk natrium alginat.
peroksida sangat stabil pada kondisi asam dan hidrogen peroksida sering digunakan pada tahap akhir rangkaian proses pemutihan dan menghasilkan peningkatan derajat putih.
Identifikasi natrium alginat yang dilakukan secara kualitatif dengan penambahan natrium hidroksida 0,1N dan kalsium klorida memberikan hasil yang positif yaitu terbentuk endapan keruh seperti jeli sedangkan penambahan asam sulfat 4N dan kalsium klorida memberikan hasil yang positif yaitu terbentuk endapan berat seperti jeli. Identifikasi natrium alginat secara kualitatif dapat memenuhi persyaratan yang telah ditetapkan oleh Farmakope Indonesia (1995).
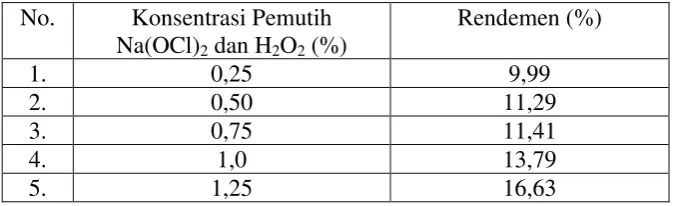
[image:48.595.118.455.422.525.2]Rendemen dari natrium alginat dengan berbagai konsentrasi pemutih dapat dilihat pada Tabel 4.2 berikut:
Tabel 4.2 Hasil rendemen natrium alginat dengan berbagai konsentrasi pemutih
Berdasarkan Tabel 4.2 dapat dilihat bahwa rendemen natrium alginat yang diperoleh dari hasil isolasi 100 g simplisia Sargassum plagyopyllum (Mertens) J.G. Agardh dengan konsentrasi pemutih 0,25% lebih kecil, sedangkan rendemen natrium alginat dengan konsentrasi pemutih 1,25% lebih besar. Menurut Ekstra Farmakope Indonesia (1974), syarat rendemen natrium alginat adalah >18%. Nilai rendemen yang diperoleh dari penelitian ini relatif rendah sehingga tidak memenuhi persyaratan yang ditetapkan. Hal ini diduga karena pada saat pencucian asam alginat banyak yang terbuang dan tentunya berpengaruh pada
No. Konsentrasi Pemutih Na(OCl)2 dan H2O2 (%)
Rendemen (%)
1. 0,25 9,99
2. 0,50 11,29
3. 0,75 11,41
4. 1,0 13,79
bobot hasil akhir ekstraksi, sehingga pada saat dihitung nilai rendemennya menjadi rendah. Hal lain juga disebabkan karena rendemen natrium alginat sangat ditentukan oleh berbagai faktor antara lain jenis alga coklat, metode isolasi yang digunakan dan jumlah daun juga menentukan kadar natrium alginat yang ada, karena di dalam daun terdapat alginat yang lebih banyak daripada batang dan akar (Taylor, 1979). Nilai rendemen dihitung berdasarkan perbandingan berat isolasi yang dihasilkan terhadap berat kering simplisia.
4.4 Hasil Karakteristik Natrium Alginat
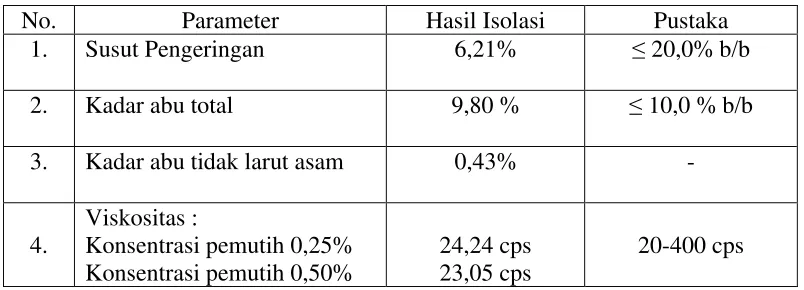
[image:49.595.112.514.455.600.2]Karakteristik natrium alginat meliputi penentuan susut pengeringan, penetapan kadar abu total, penetapan kadar abu tidak larut asam, penetapan viskositas dan warna dapat dilihat pada Tabel 4.3 dan Tabel 4.4 berikut:
Tabel 4.3 Spesifikasi natrium alginat aasil isolasi dibandingkan dengan pustaka (Handbook of Pharmaceutical Excipients)
No. Parameter Hasil Isolasi Pustaka
1. Susut Pengeringan 6,21% ≤ 20,0% b/b
2. Kadar abu total 9,80 % ≤ 10,0 % b/b
3. Kadar abu tidak larut asam 0,43% -
4.
Viskositas :
Konsentrasi pemutih 0,25% Konsentrasi pemutih 0,50%
24,24 cps 23,05 cps
20-400 cps
yang tidak larut dalam air namun, jenis dan habitat juga berpengaruh terhadap kandungan mineral, tetapi penggunaan larutan asam klorida 5% pada tahap leaching, juga dapat mengurangi jumlah garam-garam mineral yang menempel pada alga. Menurut Mushollaeni (2011), pada permukaan alga banyak terdapat garam kalsium yang dapat meningkatkan jumlah mineral dan kadar abu alginat.
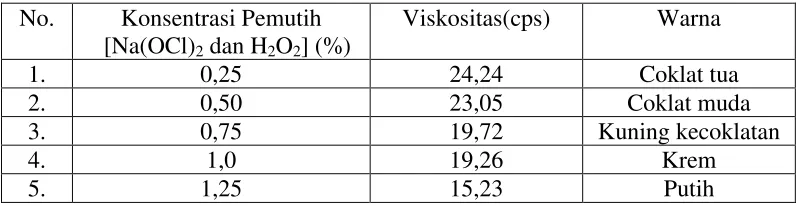
Tabel 4.4 Viskositas dan warna natrium alginat dengan berbagai konsentrasi pemutih
No. Konsentrasi Pemutih [Na(OCl)2 dan H2O2] (%)
Viskositas(cps) Warna
1. 0,25 24,24 Coklat tua
2. 0,50 23,05 Coklat muda
3. 0,75 19,72 Kuning kecoklatan
4. 1,0 19,26 Krem
5. 1,25 15,23 Putih
Menurut Sulastri (2011), faktor-faktor fisika yang mempengaruhi sifat-sifat larutan natrium alginat adalah suhu, konsentrasi dan ukuran polimer karena viskositas merupakan salah satu sifat yang penting dari natrium alginat (Rasyid, 2003).
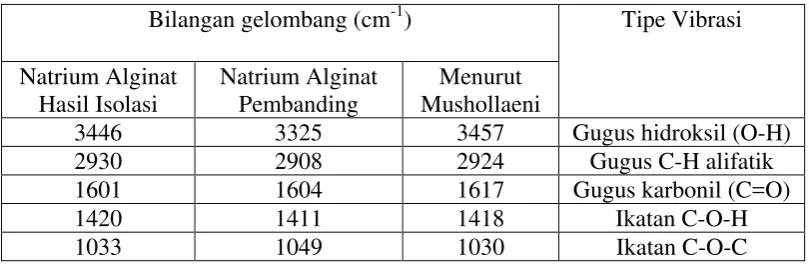
[image:51.595.113.518.290.422.2]Data spektrum gugus fungsi natrium alginat hasil isolasi dan pembanding dapat dilihat pada Tabel 4.5 berikut:
Tabel 4.5 Data spektrum inframerah natrium alginat hasil isolasi dan natrium
alginat pembanding
Bilangan gelombang (cm-1) Tipe Vibrasi
Natrium Alginat Hasil Isolasi Natrium Alginat Pembanding Menurut Mushollaeni
3446 3325 3457 Gugus hidroksil (O-H)
2930 2908 2924 Gugus C-H alifatik
1601 1604 1617 Gugus karbonil (C=O)
1420 1411 1418 Ikatan C-O-H
1033 1049 1030 Ikatan C-O-C
Penentuan gugus fungsi natrium alginat dilakukan dengan menggunakan spektrofotometer inframerah. Spektrum inframerah digunakan untuk senyawa murni yang dapat diidentifikasi dengan menggunakan spektrum inframerah, dengan salah satu sistem identifikasi. Untuk keperluan konfirmasi identitas, pada uji bahan baku murni, dapat membandingkan spektrum inframerah sampel dengan spektrum inframerah pembanding (Satiadarma, dkk., 2004).
C-O-C. Spektrum natrium alginat yang dihasilkan dari jenis Sargassum
plagyophyllum (Mertens) J.G. Agardh, menunjukkan serapan yang sama dengan
BAB V
KESIMPULAN DAN SARAN
5.1 Kesimpulan
Berdasarkan hasil penelitian yang telah dilakukan, maka diperoleh kesimpulan sebagai berikut:
a. Hasil karakteristik simplisia dari Sargassum plagyophyllum (Mertens) J.G. Agardh diperoleh kadar air 9,97%, kadar sari larut air 11,78%, kadar sari larut etanol 2,34%, kadar abu total 17,52%, kadar abu tidak larut asam 0,48%. b. Hasil rendemen natrium alginat tertingi adalah 16,63% dengan konsentrasi
pemutih 1,25% dan rendemen natrium alginat terendah adalah 9,99% dengan konsentrasi pemutih 0,25%.
c. Hasil penetapan viskositas adalah 24,24 cps yang diperoleh dari konsentrasi pemutih 0,25% dengan warna serbuk coklat tua, sedangkan konsentrasi pemutih 1,25% diperoleh 15,23 cps dengan warna serbuk putih. Berdasarkan hal tersebut, maka penambahan konsentrasi pemutih dapat mempengaruhi warna dan nilai viskositasnya.
5.2 Saran
DAFTAR PUSTAKA
Anggadiredja, J.T., Achmad, Z., Heri, P., dan Sri, I. (2011). Rumput Laut. Jakarta: Penebar Swadaya. Halaman 3, 66-67.
Aris, S., Djendakita, P., dan Azizah, N. (2012). Isolasi dan Karakterisasi Natrium Alginat dari Algae Coklat Sargassum ilicifolium (Turner) C. Agardh Serta Uji Afinitas Terhadap Logam Pb dan Cd. Prosiding Abstrak Seminar
Nasional Farmasi. Departemen Teknologi Farmasi USU.
Aryani, Y. (2004). Karakterisasi Simplisia dan Isolasi Alginat dari Talus Rumput Laut Sargassum polycystum C. Agardh. Skripsi. Medan: Jurusan Farmasi FMIPA USU.
Aslan, L.M. (1998). Budidaya Rumput Laut. Jakarta: Kanisius. Halaman 16. Atmadja, W.S., Achmad, K., Sulistijo, Rachmaniar, S. (1996). Pengenalan
Jenis-Jenis Rumput Laut Indonesia. Jakarta: Puslitbang Oseanologi-LIPI.
Halaman 56.
Badan POM RI. (2005). Penyiapan Simplisia untuk Sediaan Herbal. Jakarta: Badan POM RI. Halaman 11-12.
Belitz, H.D., dan Grosch, W. (1987). Food Chemistry. New York: Springer Verlag Berlin. Halaman 237-238.
Brunetton, J. (1995). Pharmacognosy, Phytochemistry dan Medicinal Plants. New York: Lavoiser Publishing. Halaman 46.
Chapman, V.J., dan Chapman, D.J. (1980). Seaweed and Their Uses. Edisi ketiga. London: Chapman and Hall. Halaman 194.
Dawes, C.J. (1981). Marine Botany. Florida: A Wiley-Interscience Publication. Halaman 148.
Depkes RI. (1980). Materia Medika Indonesia. Jilid IV. Jakarta: Departemen Kesehatan RI. Halaman 153-158.
Ditjen POM. (1995). Farmakope Indonesia. Edisi keempat. Jakarta: Departemen Kesehatan RI. Halaman 47, 1038.
Depkes, RI. (1974). Ekstra Farmakope Indonesia. Edisi pertama. Jakarta: Departemen Kesehatan RI. Halaman 45.
Indriani, H., dan Sumiarsih, E. (1999). Budidaya, Pengolahan, dan Pemasaran
Lachman, L., Lieberman, H.A., dan Kanig, J.L. (1989). Teori dan Praktek
Farmasi Industri. Edisi ketiga. Jakarta: UI-press. Halaman 286.
Lobban, C.S., dan Wynne, M.J. (1981). The Biology of Seaweeds. Volume 17. Oxford London: Blackwell Scientific Publications. Halaman 357.
Marpaung, P.E.N. (2005). Karakterisasi dan Isolasi Alginat dari Ampas Ekstraksi Aseton Talus Rumput Laut Turbinaria decurrens Bory. Skripsi. Medan: Jurusan Farmasi FMIPA USU.
Martin, A., Swarbick, J., dan Cammarata, A. (1993). Farmasi Fisik. Edisi ketiga. Jakarta: UI-Press. Halaman 1077-1081.
Mushollaeni, W. (2011). Karakterisasi Natrium Alginat dari Sargassum sp.
Turbinaria sp. dan Padina sp. Jurnal Teknol. dan Industri Pangan 22(1):
26-32.
Rachmat, R. (2012). Kandungan dan Karakteristik Fisiko Kimia Alginat dari Sargassum sp. yang Dikumpulkan dari Perairan Indonesia. Jurnal
Oseana.33(2) : 259-265.
Rasyid, A. (2003). Algae Coklat (Phaeophyta) Sebagai Sumber Alginat. Jurnal
Oseana. 28(1): 33-38.
Rasyid, A. (2005). Beberapa Catatan Tentang Alginat. Jurnal Oseana. 30(1): 9-14.
Rowe, R.C., Paul, J.S., dan Marian, E.Q. (2009). Handbook of Pharmaceutical
Excipient. Edisi keenam. New York: Pharmaceutical Press. Halaman 623.
Sastrohamidjojo, H. (1991). Spektroskopi. Cetakan pertama. Yogyakarta: Liberty. Halaman 45-70.
Sastrohamidjojo, H. (1992). Spektroskopi Inframerah. Edisi pertama. Yogyakarta: Liberty. Halaman 12, 123-132.
Satiadarma, K., Muhammad, M., Daryono, H.T., dan Rahmana, E.K. (2004). Asas
Pengembangan Prosedur Analis. Edisi Pertama. Surabaya: Airlangga
University Press. Halaman 111-113.
Sukardjo. (2003). Kimia Fisika. Jakarta: Rineka Cipta. Halaman 108-109. Sulastri, S. (2011). Alginat. Bogor: Fakultas Teknik Industri IPB. Halaman 4. Supomo. (2002). Karakterisasi Simplisia dan Isolasi Alginat dari Talus Rumput
Supratman, U. (2010). Elusidasi Struktur Senyawa Organik. Bandung: Widya Padjajaran. Halaman 66-105.
Susanti, E. (2003). Karakterisasi Simplisia dan Isolasi Alginat dari Talus Rumput Laut Hormophysa triquetra (L) J. Agardh. Skripsi. Medan: Jurusan Farmasi FMIPA USU.
Taylor, W.R. (1979). Marine Alga of the Easterm Tropical and Subtropical Coast
of the Americas. Michigan: The University of Michigan. 76-80
Winarno, F.G. (1990). Teknologi Pengolahan Rumput Laut. Jakarta: Pustaka Sinar Harapan. Halaman 13, 48-50.
World Health Organization. (1998). Quality Control Methods for Medicinal Plant
Materials. Geneva: World Health Organization. Halaman 33-35.
Yulianto, K. (2007). Pengaruh Konsentrasi Natrium Hidroksida Terhadap Viskositas Natrium Alginat yang Diekstrak dari Sargassum duplicatum, J. G. Agardh (Phaeophyta). Jurnal Oseanologi dan Limnologi. (33): 295-306.
Lampiran 2. Gambar makroskopik tumbuhan segar dan simplisia Sargassum
plagyophyllum (Mertens) J.G. Agardh
A. Makroskopik tumbuhan segar
B. Makroskopik simplisia
Keterangan: 1 = “daun” 2 = “batang” 3 = holdfast
1
2
3
Lampiran 4. Gambar mikroskopik serbuk simplisia Sargassum plagyophyllum
(Mertens) J.G. Agardh (perbesaran 10x40)
Keterangan: 1 = sel propagule yang memiliki dua sel
2 = sel parenkim berisi pigmen berwarna coklat
Lampiran 5. Perhitungan pemeriksaan karakteristik simplisia Sargassum
plagyophyllum (Mertens) J.G. Agardh
1. Perhitungan kadar air
% Kadar air simplisia = Volumeair (ml)
Beratsampel (g)
x
100%
No. Berat sampel (g) Volume awal (ml) Volume akhir (ml) 1.
2. 3.
5,017 5,016 5,016
1,80 2,30 2,80
2,30 2,80 3,30
% Kadar air = volumeakhir−volumeawal
Beratsampel
x
100%
1. Kadar air = 2,30−1,80
5,017
x
100% =
9,97 %2. Kadar air = 2,80−2,30
5,016
x
100% =
9,97 %3. Kadar air = 3,30−2,80
5,016
x
100% =
9,97 %% Rata-rata kadar air = 9,97%+9,97%+9,97%
Lampiran 5. (lanjutan)
2. Perhitungan kadar sari larut dalam air
% Kadar sari larut dalam air = Beratsari (g)
Beratsampel (g)
x
100
20
x
100%
No. Berat sampel (g) Berat sari (g) 1.
2. 3.
5,002 5,003 5,004
0,1172 0,1178 0,1188
1. Kadar sari larut dalam air = 0,1172
5,002
x
100
20
x
100% =
11,71%2. Kadar sari larut dalam air = 0,1178
5,003
x
100
20
x
100% =
11,77%3. Kadar sari larut dalam air = 0,1188
5,004
x
100
20
x
100% =
11,87%% Rata-rata kadar sari larut dalam air = 11,71%+11,77%+11,87%
3
x 100%
Lampiran 5. (lanjutan)
3. Perhitungan kadar sari larut dalam etanol
% Kadar sari larut dalam etanol = Beratsari (g)
Beratsampel (g)
x
100
20
x
100%
No. Berat sampel (g) Berat sari (g) 1.
2. 3.
5,003 5,004 5,003
0,0217 0,0226 0,0262
1. Kadar sari larut dalam etanol = 0,0217
5,003
x
100
20
x
100% =
2,17%2. Kadar sari larut dalam etanol = 0,0226
5,004
x
100
20
x
100% =
2,23%3. Kadar sari larut dalam etanol = 0,0262
5,003
x
100
20
x
100% =
2,62%% Rata-rata kadar sari larut dalam etanol = 2,17%+2,23%+2,62%
3
x 100%
Lampiran 5. (lanjutan)
4. Perhitungan kadar abu total
% Kadar abu total = Beratabu (g)
Beratsampel (g)
x
100%
No. Berat sampel (g) Berat abu (g) 1.
2. 3.
2,003 2,003 2,004
0,3556 0,3410 0,3564
1. Kadar abu total = 0,3556
2,003
x
100% =
17,75%2. Kadar abu total = 0,3410
2,003
x
100% =
17,02%3. Kadar abu total = 0,3564
2,004
x
100% =
17,78%Lampiran 5. (lanjutan)
5. Perhitungan kadar abu tidak larut asam
% Kadar abu tidak larut asam = Berat abu (g)
Berat sampel (g)
x
100%
No. Berat sampel (g) Berat abu (g) 1.
2. 3.
2,003 2,003 2,004
0,0117 0,0090 0,0850
1. Kadar abu tidak larut asam = 0,0117
2,003
x
100% =
0,58%2. Kadar abu tidak larut asam = 0,0090
2,003
x
100% =
0,45%3. Kadar abu tidak larut asam = 0,0850
2,004
x
100% =
0,42%% Rata-rata kadar abu tidak larut asam =0,58%+0,45%+0,42%
3
x 100
%Lampiran 6. Bagan isolasi dan karakterisasi natrium alginat
Direndam dengan Na2CO3 5% pada suhu 50o-60o C, 2 jam Disaring
Direndam dengan HCl 5%, 2 jam, disaring 100 g serbuk simplisia
Dicuci dengan air suling sampai netral (pH 7)
Diputihkan dengan NaOCl2 (0,25%, 0,50%, 0,75%, 1,0% dan 1,25%,) 2,5 jam, disaring
Dicuci dengan air suling sampai netral (pH 7)
Ditambahkan CaCl2 1%
Asam alginat (floating)
Ditambahkan dengan Na2CO3 5%
Larutan Natrium Alginat
Dikeringkan (suhu 50o C) dan dihaluskan
Susut pengeringan Spektrofotometri inframerah Filtrat Residu Filtrat Resid Filtrat Residu
Dicuci dengan air suling sampai netral (pH 7)
Diputihkan dengan H2O2 (0,25%, 0,50%, 0,75%, 1,0% dan 1,25%), 6 jam, disaring
Dicuci dengan air suling sampai netral (pH 7)
Dikarakterisasi
Viskositas Endapan kalsium alginat
Ditambahkan HCl 5% sedikit demi sedikit
Diendapkan dengan isopropanol 95%
Serbuk Natrium Alginat
Diidentifikasi
Kadar abu tidak larut asam Kadar abu
Lampiran 7. Perhitungan karakteristik natrium alginat yang diperoleh dari Sargassum plagyophyllum (Mertens) J.G. Agardh
1. Perhitungan rendemen natrium alginat
Rendemen dihitung dengan menggunakan rumus sebagai berikut :
% Rendemen Natrium alginat = Berathasilisolasi (gram)
Beratsampelmula−mula (gram)
x
100 %Contoh perhitungan :
% Rendemen natrium alginat = 16,63
100
x
100%Lampiran 7. (lanjutan)
2. Perhitungan penetapan susut pengeringan
% Susut pengeringan = a−b
a
x
100 %a = berat bahan awal
b = berat bahan setelah pengeringan
No. Berat sampel (g) Berat sampel setelah pengeringan (g) 1.
2.
1,0042 1,0028
0,9406 0,9418
1. % Susut pengeringan = 1,0042g−0,9406g
1,0042g
x
100% = 6,33%2. % Susut pengeringan = 1,0028g−0,9418g
1,0028g
x
100% = 6,08%% Rata-rata susut pengeringan = 6,33 % +6,08 %
Lampiran 7. (lanjutan)
3. Perhitungan viskositas natrium alginat Viskositas relatif dihitung dengan persamaan:
η
rel=
t �₀t = waktu alir cairan uji (detik)