ENKAPSULASI IBUPROFEN DENGAN NATRIUM
ALGINAT-PEKTIN MENGGUNAKAN METODE
GELASI IONIK
YAYAT NURHIDAYAT SYAHRON
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM INSTITUT PERTANIAN BOGOR
PERNYATAAN MENGENAI SKIRIPSI DAN
SUMBER INFORMASI SERTA PELIMPAHAN HAK CIPTA*
Dengan ini saya menyatakan bahwa skripsi berjudul Enkapsulasi Ibuprofen dengan Natrium Alginat-Pektin Menggunakan Metode Gelasi Ionik adalah benar karya saya dengan arahan dari komisi pembimbing dan belum diajukan dalam bentuk apa pun kepada perguruan tinggi mana pun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir skripsi ini.
Dengan ini saya melimpahkan hak cipta dari karya tulis saya kepada Institut Pertanian Bogor.
ABSTRAK
YAYAT NURHIDAYAT SYAHRON. Enkapsulasi Ibuprofen dengan Natrium Alginat-Pektin Menggunakan Metode Gelasi Ionik. Dibimbing oleh TETTY KEMALA dan NOVIYAN DARMAWAN.
Ibuprofen merupakan obat anti inflamasi non-steroid yang memiliki waktu paruh pendek dan dapat mengiritasi lambung. Enkaspulasi adalah salah satu cara yang dapat digunakan untuk memperkecil risiko tersebut. Dalam penelitian ini dipelajari enkapsulasi ibuprofen menggunakan natrium-alginat pektin menggunakan metode gelasi ionik. Komposisi natrium alginat-pektin dan konsentrasi CaCl2 digunakan sebagai variabel utama yang ingin dievaluasi
pengaruhnya pada efisiensi enkapsulasi dan profil disolusi. Rentang efisiensi enkapsulasi yang diperoleh antara 71% dan 90%. Efisiensi enkapsulasi tertinggi diperoleh pada komposisi natrium alginat-pektin 2:1 (% b/v) pada konsentrasi CaCl2 10%. Kapsul yang dihasilkan memiliki bentuk yang semakin mendekati
bulat dengan berkurangnya jumlah pektin. Pola pelepasan ibuprofen pada formula A1, A2, dan C1 menunjukkan pola pelepasan yang bertahap.
Kata kunci: enkapsulasi, gelasi ionik, ibuprofen, natrium alginat, pektin
ABSTRACT
YAYAT NURHIDYAT SYAHRON. Encapsulation of Ibuprofen with Sodium Alginat-Pectin Using Ionotropic Gelation Method. Supervised by TETTY KEMALA and NOVIYAN DARMAWAN.
Ibuprofen is a non-steroid anti-inflamatory drugs that has a short half-life and may irritate stomach. Encapsulation is one way that can be used to minimize the risk. In this experiment, ibuprofen encapsulated with sodium alginat-pectin using ionotropic gelation method was studied. The composition of sodium alginat-pectin and the concentration of CaCl2 were used as the main variable that would
be determined for the encapsulation efficiency and the dissolution profile. The encapsulation efficiency was between 90% and 71%. The highest encapsulation efficiency was exhibited by 2:1 (% b/v) composition of sodium alginat-pectin with 10% of CaCl2 concentration. The produced capsules have merely spherical
with a reduced pectin constituent. The release pattern of ibuprofen on the A1, A2, and C1 formula showed a gradual release pattern.
Skripsi
sebagai salah satu syarat untuk memperoleh gelar Sarjana Sains
pada
Departemen Kimia
ENKAPSULASI IBUPROFEN DENGAN NATRIUM
ALGINAT-PEKTIN MENGGUNAKAN METODE
GELASI IONIK
YAYAT NURHIDAYAT SYAHRON
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM INSTITUT PERTANIAN BOGOR
PRAKATA
Puji dan syukur penulis panjatkan kepada Allah subhanahu wa ta’ala atas segala rahmat dan karunia-Nya sehingga karya ilmiah dapat diselesaikan. Tema yang dipilih dalam penelitian yang dilaksanakan sejak bulan Januari 2015 ini ialah penyalutan ibuprofen, dengan judul Enkapsulasi Ibuprofen dengan Natrium Alginat-Pektin Menggunakan Metode Gelasi Ionik.
Terima kasih penulis ucapkan kepada Dr Tetty Kemala, MSi selaku pembimbing I dan Dr rer nat Noviyan Darmawan, MSc selaku pembimbing II. Di samping itu, ucapan terima kasih penulis sampaikan kepada seluruh staf Laboratorium Kimia Anorganik (Bapak Sawal, Bapak Sunarsa, Bapak Mulyadi, dan Kakak Rohmat) serta staf di Laboratorium Biofisika Material Departemen Fisika IPB dan Laboratorium Jasa Pengujian dan Penelitian Fakultas Farmasi Universitas Pancasila yang telah banyak memberikan saran dan bantuan kepada penulis selama penelitian. Selain itu ucapan terima kasih penulis sampaikan kepada para murobbi luar biasa, Kakak Achmad Deni, Ustadz Syaefudin, dan Ustadz Salahuddin El Ayyubi serta rekan-rekan dalam lingkaran tarbiyah mubarokah, rekan-rekan satu bimbingan, keluarga Kimia Anorganik khususnya Taufiq, Firdaus, Ahas, dan Erwa, keluarga besar Kimia angkatan 48, dan keluarga satu perjuangan di IKMT 48, FSDMA 48, Serum-G Pelangi Inspirasi 1434H, dan Serum-G Transformasi 1435H, serta para Ksatria Kujang PPSDMS NF Regional V angkatan VI yang telah memberikan semangat, masukan, dan dukungan kepada penulis. Ucapan terima kasih tak terhingga penulis ucapkan kepada Ibu, Ayah, dan segenap keluarga atas doa, dukungan dan kasih sayang yang telah diberikan.
Semoga karya tulis ini bermanfaat.
DAFTAR ISI
DAFTAR GAMBAR vi
DAFTAR LAMPIRAN vi
PENDAHULUAN 1
METODE 2
Bahan dan Alat 2
Lingkup Penelitian 2
HASIL DAN PEMBAHASAN 4
Kapsul Natrium Alginat-Pektin 4
Panjang Gelombang Maksimum dan Kurva Standar 6
Efisiensi Enkapsulasi 7
Pelepasan Ibuprofen 8
SIMPULAN DAN SARAN 10
Simpulan 10
Saran 10
DAFTAR PUSTAKA 11
LAMPIRAN 13
DAFTAR GAMBAR
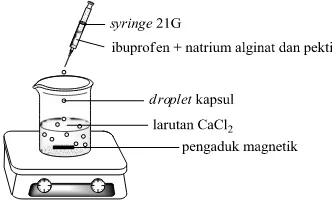
1 Ilustrasi penetesan suspensi ibuprofen dalam larutan natrium
alginat- pektin ke dalam larutan CaCl2 2
2 (a) Kapsul natrium alginat-pektin basah, dan (b) kapsul natrium
alginat-pektin kering 5
3 Hasil pengamatan bentuk kapsul dengan mikroskop stereo 5 4 (a) Interaksi natrium alginat dengan Ca2+, (b) model egg-box pada
natrium alginat, dan (c) hasil gelasi pada pektin dengan derajat
metoksil tinggi 6
5 Efisiensi enkapsulasi kapsul natrium alginat-pektin dengan
konsentrasi CaCl2 5%, 7.5%, dan 10% 8
6 Pelepasan ibuprofen dari kapsul formula A1 dengan komposisi natrium alginat-pektin 2:1 (% b/v) dan A2 dengan komposisi natrium alginat-pektin 2.25:0.75 (% b/v) pada konsentrasi CaCl2
5% 9
7 Pelepasan ibuprofen dari kapsul formula A1 dengan konsentrasi
CaCl2 5% dan C1 dengan konsentrasi CaCl2 10% 9
8 Sisa kapsul (a) A1, (A2), dan (c) C1 setelah uji disolusi 10
DAFTAR LAMPIRAN
1 Diagram alir penelitian 13
2 Pembuatan larutan bufer fosfat pH 7.2 14
3 Absorbans larutan ibuprofena pada panjang gelombang maksimum 15 4 Konsentrasi dan absorbans larutan ibuprofen pada pembuatan
kurva standar ibuprofen (maks = 221.5 nm) 16
5 Efisiesnsi penyalutan ibuprofen dalam kapsul natrium
alginat-pektin 17
6 Persentase rerata pelepasan ibuprofen dalam uji disolusi medium
basa dari kapsul natrium alginat-pektin 18
PENDAHULUAN
Rematik merupakan salah satu penyakit peradangan atau inflamasi yang berasal dari luka. Gejala yang timbul pada rematik antara lain timbulnya rasa nyeri di bagian lutut, siku, pergelangan, dan bagian sendi lainnya. Orang yang mengalami inflamasi biasanya memilih cara yang sederhana untuk mengatasinya, salah satunya dengan mengonsumsi obat. Ibuprofen merupakan salah satu jenis obat anti-inflamasi non-steroid atau AINS yang banyak digunakan sebagai obat untuk menghambat peradangan (Tang et al. 2014). Selain untuk peradangan, ibuprofen banyak juga digunakan sebagi obat pereda demam, kram menstruasi, dan rasa nyeri pada sendi.
Ibuprofen dapat menimbulkan efek samping pada penggunanya, antara lain dispepsia ringan hingga pendarahan pada lambung (Arica et al. 2005). Hal ini terjadi karena kerja ibuprofen yang tidak selektif terhadap penghambatan enzim siklooksigenase (COX) 1 dan 2. Penghambatan pada COX 2 memberikan efek anti peradangan dari ibuprofen, sedangkan penghambatan pada COX 1 meninmbulkan efek iritasi pada saluran pencernaan (Febrianti dan Wahyuningsih 2013). Waktu paruh ibuprofen dalam plasma yang cukup singkat, yaitu sekitar 1 sampai 3 jam menjadi salah satu penyebab konsumsi ibuprofen yang cukup tinggi (Saravanan et al. 2003). Dengan waktu paruh yang cukup singkat, konsumsi ibuprofen menjadi lebih tinggi karena efeknya yang cepat berkurang. Untuk mengatasi masalah tersebut, dilakukan inovasi sistem penghantaran obat yang dapat mengontrol pelepasan ibuprofen secara perlahan di dalam tubuh.
Sistem penghantaran obat memiliki beberapa keunggulan, yaitu mengurangi efek samping dari obat, memperpanjang waktu paruh, bioaktivitas obat yang terkontrol, dan meningkatkan efisisensi terapeutik obat (Yu et al. 2009). Pada penelitian ini, sistem penghantaran obat dilakukan dengan metode enkapsulasi atau pengungkungan obat. Enkapsulasi obat banyak dilakukan dengan menggunakan polimer yang memiliki sifat biodegradasi dan biokompatibel, beberapa polimer yang dijadikan bahan penyalut obat antara lain poli(asam laktat) (PLA) dan poli(asam laktat ko-glikolat) (PLGA) (Felder et al. 2003), polikaprolakton (PCL) (Kim et al. 2010), PLA-PCL (Kemala et al. 2010), kitosan (Estevinho et al. 2013), pektin (Jung et al. 2013) dan beberapa polimer alam lain seperti natrium alginat, guar gum, dan xanthan gum (Vajpayee et al. 2011).
2
Metode enkapsulasi yang digunakan untuk penyalutan dengan polisakarida seperti natrium alginat dan pektin adalah gelasi ionik. Metode ini didasarkan pada kemampuan larutan polielektrolit untuk melakukan ikatan silang dengan kehadiran ion yang memiliki muatan berlawanan untuk membentuk suatu hidrogel (Patil et al. 2010). Tujuan dari penelitian ini adalah membuat kapsul dari kombinasi natrium alginat-pektin yang memiliki waktu pelepasan yang lambat. Kapsul yang terbentuk diuji efisiensi penyalutan dan waktu perilisannya dalam simulan cairan usus.
METODE
Bahan dan Alat
Bahan-bahan yang digunakan dalam penelitian ini adalah ibuprofen pro- analis (PT Indofarma Tbk), natrium alginat (Setia Guna), pektin (HM USP Pectin E440, Yantai Andre Pectin Co, Ltd. Jepang), CaCl2, akuades, dan larutan bufer
fosfat pH 7.2 (NaH2PO4-Na2HPO4). Alat-alat yang digunakan selama proses
penelitian antara lain alat gelas, neraca analitik, pengaduk magnetik, jarum suntik 21G, mikroskop, alat disolusi tipe dayung (Guoming RC-6) dan spektrofotometer ultraviolet (Shimadzu UV-1601).
Lingkup Penelitian
Penelitian ini terdiri atas beberapa tahap (Lampiran 1), yaitu pembuatan kapsul ibuprofen dengan natrium alginat dan pektin, kemudian kapsul yang terbentuk diuji efisiensi penyalutan dan disolusinya dalam larutan bufer fosfat pH 7.2. Bentuk kapsul yang diperoleh diamati menggunakan mikroskop stereo.
Pembuatan Kapsul Ibuprofen dengan Metode Gelasi Ionik (Vajpayee et al.
2011 dengan modifikasi)
Sebanyak 10 mL larutan penyalut yang dibuat dari natrium alginat dan pektin dengan total konsentrasi 3% (b/v) dicampurkan dengan bantuan pengadukan menggunakan pengaduk magnetik selama 30 menit, ke dalam larutan tersebut ditambahkan 100 mg ibuprofen dan terus diaduk sampai terdispersi. Campuran yang telah terdipersi kemudian diteteskan ke dalam 30 mL larutan CaCl2 menggunakan jarum suntik 21G (Gambar 1).
3
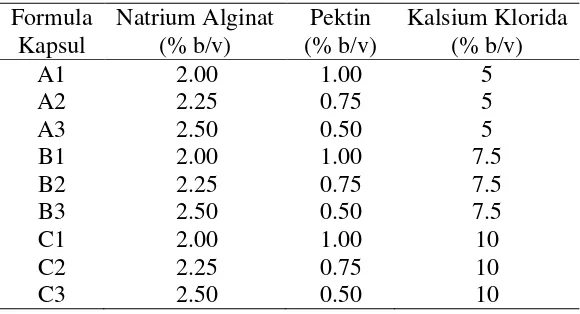
Setelah terbentuk butiran-butiran kapsul, pengadukan menggunakan pengaduk magnetik dilanjutkan selama 3 jam. Setelah pengadukan selesai, kapsul-kapsul tersebut disaring dan ditempatkan dalam wadah terbuka, kemudian dikeringudarakan selama 48 jam. Kapsul yang diperoleh kemudian ditimbang bobotnya. Komposisi natrium alginat, pektin, dan variasi konsentrasi CaCl2 dapat
dilihat pada Tabel 1.
Tabel 1 Komposisi pencampuran natrium alginat dan pektin Formula
Penentuan Panjang Gelombang Maksimum dan Pembuatan Kurva Standar (Prihatiningsih 2008 dengan modifikasi)
Larutan ibuprofen dalam bufer fosfat pH 7.2 (Lampiran 2) dengan konsentrasi 10 ppm diukur absorbansnya pada panjang gelombang (λ) 210−240 nm menggunakan spekrofotometer UV. Panjang gelombang maksimum (λmaks)
yang diperoleh digunakan untuk analisis selanjutnya. Kurva standar dibuat dengan mengukur absorbans larutan ibuprofen dengan konsentrasi 0.1, 0.5, 1, 2, 4, 6, 8, 10, 12, 14, 16, 18, dan 20 ppm pada panjang gelombang maksimum. Hasil yang diperoleh merupakan hubungan konsentrasi ibuprofen dengan absorbans.
Penentuan Efisiensi Penyalutan (Jelvehgari et al. 2014 dengan modifikasi)
Sebanyak 25 mg hasil enkapsulasi ditimbang dan dilarutkan ke dalam 50 mL bufer fosfat pH 7.2. Campuran tersebut diaduk menggunakan pengaduk magnetik selama 7 jam lalu disaring. Filtrat diencerkan sebanyak 5 kali dan dibaca absorbansnya dengan spektrofotometer UV pada panjang gelombang maksimum. Absorbans yang diperoleh digunakan untuk menentukan konsentrasi ibuprofen dengan menggunakan kurva standar.
Uji Disolusi secara In Vitro (Joshi et al. 2012 dengan modifikasi)
4
ibuprofen dalam larutan alikuot diukur menggunakan spektrofotometer UV pada
λmaks. Data yang diperoleh dibuat kurva hubungan antara persen pelepasan
ibuprofen dan waktu disolusi.
HASIL DAN PEMBAHASAN
Kapsul Natrium Alginat-Pektin
Pembuatan kapsul natrium alginat-pektin pada penelitian ini dilakukan dengan metode gelasi ionik. Prinsip dari metode ini adalah pembentukan hidrogel dari bahan penyalut yang merupakan suatu polielektrolit. Metode ini sangat bergantung pada kemampuan bahan penyalut untuk bertaut silang dengan muatan ion yang berlawanan untuk membentuk hidrogel (Patil et al. 2012). Kapsul hidrogel dapat terbentuk secara spontan dengan meneteskan bahan penyalut ke dalam larutan yang mengandung ion dengan muatan berlawanan. Natrium alginat dan pektin yang digunakan merupakan polielektrolit negatif, dengan gugus –COO -pada rantai guluronat (natrium alginat) dan rantai galakturonat (pektin). Penaut silang yang digunakan adalah Ca2+ dalam larutan CaCl2. Khazaeli et al. (2008)
sebelumnya telah melakukan enkapsulasi ibuprofen dengan metode yang sama menggunakan beberapa jenis penaut silang, yaitu Mn, Co, Sn, Pb, Ba, dan Ca. Kapsul yang diperoleh dari hasil taut silang dengan Mn, Co, dan Sn berbentuk tipis dan rapuh. Sementara itu, kapsul yang dihasilkan dari taut silang dengan Pb, Ba, dan Ca berbentuk bulat, tetapi Pb dan Ba tidak digunakan lebih lanjut karena efek toksiknya terhadap tubuh.
Pencampuran natrium alginat dan pektin dilakukan melalui pencampuran biasa menggunakan pengadukan dan dihasilkan larutan yang homogen. Ibuprofen didisperikan ke dalam larutan natrium alginat-pektin sebelum dilakukan penetesan. Dalam metode gelasi ionik, ada dua cara mencampurkan zat aktif untuk dienkapsulasi. Mandal et al. (2010) menyebut kedua cara tersebut sebagai cara berurutan dan cara simultan. Pada cara berurutan, zat aktif didispersikan pada larutan yang mengandung bahan penyalut kemudian diteteskan ke dalam larutan yang mengandung penaut silang. Sementara itu, pada cara simultan zat aktif didispersikan pada larutan yang mengandung penaut silang, kemudian larutan yang mengandung bahan penyalut diteteskan ke dalamnya. Mandal et al. (2010) dan Khazaeli et al. (2008) yang melakukan kedua cara tersebut menemukan bahwa cara simultan menghasilkan efisiensi enkapsulasi yang lebih kecil, sehingga pada tahap selanjutnya digunakan cara berurutan untuk melakukan enkapsulasi. Ketika penetesan berlangsung, dilakukan pengadukan dengan pengaduk magnetik untuk menguatkan dan menambah stabilitas kapsul (Joshi et al. 2012).
Selama proses pembentukan kapsul, ibuprofen terperangkap di dalam hidrogel natrium alginat-pektin. Ibuprofen yang tidak terenkapsulasi akan terdapat pada larutan CaCl2 dalam bentuk tidak larut (Wukirsari 2006). Kapsul yang
5
(a) (b)
Gambar 2 (a) Kapsul natrium alginat-pektin basah, dan (b) kapsul natrium alginat-pektin kering
Hasil pengamatan menggunakan mikroskop stereo untuk masing-masing formula (Gambar 3) menunjukkan bahwa semakin sedikit pektin yang digunakan, kapsul yang terbentuk semakin mendekati bentuk bulat. Penggunaan pektin yang semakin banyak menyebabkan kapsul yang dihasikan berbentuk lonjong dan ukurannya relatif lebih besar jika dibandingkan dengan kapsul yang menggunakan sedikit pektin. Struktur alami pektin yang memiliki gula netral seperti xylosa, galaktosa, dan arabinosa menjadi penyebab terjadinya elongasi pada kapsul yang terbentuk (Jaya et al. 2010). Secara fisik, kapsul yang dibuat dengan konsentrasi CaCl2 yang lebih tinggi bersifat lebih kaku dan lebih keras. Hal tersebut terjadi
karena semakin banyak ion Ca2+ yang tersedia, semakin banyak ikatan taut silang yang terjadi dengan natrium alginat-pektin sehingga strukturnya menjadi lebih kompak (Jelvehgari et al. 2004).
Gambar 3 Hasil pengamatan bentuk kapsul dengan mikroskop stereo B3
C2 C3
B2
A1 A2
B1
C1
6
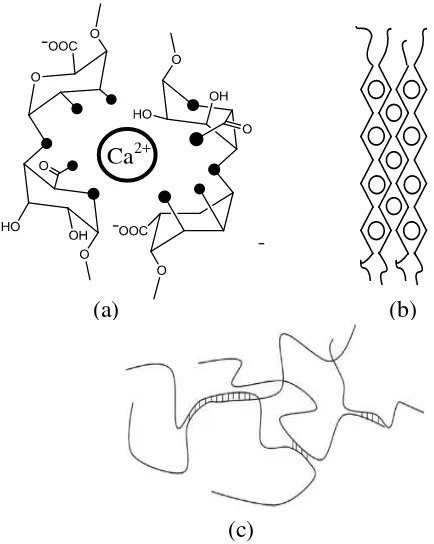
Kapsul natrium alginat-pektin dapat terbentuk karena terjadinya pertukaran ion antara Na+ dari rantai natrium alginat dan H+ dari rantai pektin dengan Ca2+ dari larutan kalsium klorida sehingga terbentuk hidrogel dengan model egg-box. Egg-box pada natrium alginat terbentuk karena tautan silang ion kalsium dengan unit asam guluronat pada rantai natrium alginat (Fang et al. 2007). Gambar 4a dan 4b masing-masing menunjukkan ikatan yang terbentuk antara ion Ca2+ dengan unit asam guluronat dan model egg-box yang terbentuk pada hidrogel natrium alginat. Sementara itu, egg-box pada pektin terbentuk pada unit galakturonat. Pada pektin dengan derajat metoksil tinggi Fang et al. (2008) menyatakan bahwa pengikatan Ca2+ didominasi oleh interaksi elektrostatik sehingga hampir tidak ada egg-box yang terbentuk. Hasil gelasi yang terbentuk pada pektin dengan derajat metoksil tinggi diilustrasikan Morris et al. (2010) pada Gambar 4c.
(a) (b)
(c)
Gambar 4 (a) Interaksi natrium alginat dengan Ca2+, (b) model egg-box pada natrium alginat (Fang et al. 2007), dan (c) hasil gelasi pada pektin dengan derajat metoksil tinggi (Morris et al. 2010)
Panjang Gelombang Maksimum dan Kurva Standar
Pelarut yang digunakan dalam pembuatan larutan ibuprofen adalah bufer fosfat pH 7.2. Nilai pH tersebut digunakan untuk menyesuaikan dengan pH usus dan biasa digunakan sebagai medium disolusi tablet ibuprofen (Depkes 1995). Penentuan panjang gelombang dilakukan pada daerah ultraviolet karena larutan ibuprofen memiliki serapan sinar ultraviolet akibat adanya struktur ikatan terkonjugasi (Fachrurazie 2012). Pengukuran sampel dilakukan pada maks karena
7
demikian akan didapatkan kepekaan dan sensitivitas pengukuran yang maksimum. Pada penelitian ini diperoleh nilai maks sebesar 221.5 nm (Lampiran 3). Nilai
tersebut mendekati nilai dari literatur sebesar 222 nm (Depkes 1995).
Persamaan kurva standar yang diperoleh adalah y = 0.047x - 0.0019 dengan nilai r sebesar 0.9997 (Lampiran 4). Persamaan kurva standar tersebut digunakan dalam perhitungan efisiensi enkapsulasi dan persentase pelepasan ibuprofen dari kapsul natrium alginat-pektin. Linearitas suatu metode analisis merupakan ukuran yang menunjukkan tingkat kesesuaian atau korelasi antara kadar analit dan sinyal detektor, dinyatakan sebagai koefisien korelasi (r) (Depkes 2001). Dengan nilai r sebesar 0.9997, kurva standar yang digunakan telah memenuhi syarat kurva standar yang telah ditetapkan menurut AOAC (2002) yaitu 0.9900. Nilai koefisien korelasi yang tinggi menunjukkan hubungan linear antara sinyal detektor terukur dengan jumlah ibuprofen dalam sampel, sehingga galat sistematik selama pengukuran dapat diabaikan.
Efisiensi Enkapsulasi
Efisiensi enkapsulasi merupakan salah satu parameter yang dapat digunakan untuk menentukan keberhasilan suatu proses enkapsulasi. Parameter ini menunjukkan persentase zat aktif (ibuprofen) yang berhasil dikungkung di dalam kapsul yang dibuat. Hasil penentuan efisiensi enkapsulasi pada penelitian ini (Lampiran 5) menunjukkan bahwa rentang efisiensi enkapsulasi yang diperoleh berkisar antara 71% sampai 90%. Kapsul yang dibuat dengan komposisi natrium alginat pektin 2:1 (% b/v) dan konsentrasi CaCl2 10% menghasilkan nilai efisiensi
sebesar 90.41%, sementara nilai efisiensi terkecil diperoleh pada kapsul dengan komposisi natrium alginat pektin 2.5:0.5 (% b/v) dan konsentrasi CaCl2 5%.
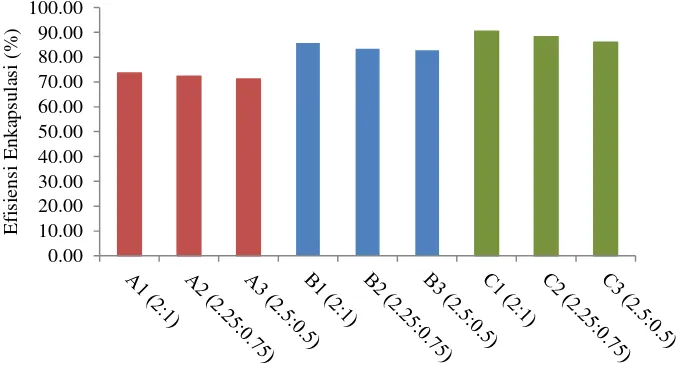
Gambar 5 menunjukkan adanya kecenderungan efisiensi enkapsulasi yang menurun seiring dengan penurunan jumlah pektin, tetapi meningkat dengan kenaikan konsentrasi CaCl2.
Pada konsentrasi CaCl2 yang sama, efisiensi enkapsulasi menurun dengan
berkurangnya jumlah pektin. Ukuran kapsul yang terbentuk akibat pengaruh jumlah pektin menjadi faktor yang mempengaruhi efisiensi enkapsulasi. Jelvehgari et al. (2014) menyatakan bahwa butiran kapsul yang lebih besar dapat mengungkung obat yang lebih banyak. Kapsul yang menggunakan lebih banyak pektin menghasilkan ukuran yang lebih besar sehingga efisiensi enkapsulasinya lebih besar. Hasil ini sesuai dengan hasil yang diperoleh Goudanavar et al. (2005) dan Jelvehgari et al. (2014). Sementara itu, dengan konsentrasi CaCl2 yang
berbeda diperoleh efisiensi enkapsulasi yang meningkat dengan semakin tingginya konsentrasi CaCl2 yang digunakan. Dengan ketersiediaan ion Ca2+ yang
8
Gambar 5 Efisiensi enkapsulasi kapsul natrium alginat-pektin dengan konsentrasi CaCl2 5% ( ), 7.5% ( ), dan 10% ( )
Pelepesan Ibuprofen
Disolusi merupakan proses masuknya zat padat ke dalam larutan. Menurut Kemala (2010), disolusi merupakan proses melarutnya zat padat yang dikendalikan oleh afinitas antara zat padat dengan pelarut. Pengujian disolusi yang dilakukan secara in vitro pada penelitian ini menggunakan medium disolusi dengan pH 7.2 tanpa enzim selama 6 jam. Kapsul yang digunakan untuk uji disolusi adalah kapsul dengan formula A1 (2:1, CaCl2 5%), A2 (2.25:0.75, CaCl2
5%), dan C1 (2:1, CaCl2 10%). Data hasil uji disolusi untuk ketiga kapsul tersebut
ditunjukkan pada Lampiran 6 dan 7.
Kapsul dengan formula A1 dan A2 digunakan untuk membandingkan pengaruh komposisi natrium alginat-pektin terhadap pola pelepasan ibuprofen. Kedua kapsul tersebut dibentuk pada konsentrasi CaCl2 yang sama, tetapi
9 Gambar 6 Pelepasan ibuprofen dari kapsul formula A1 dengan komposisi natrium
pektin 2:1 (% b/v) dan A2 dengan komposisi natrium alginat-pektin 2.25:0.75 (% b/v) pada konsentrasi CaCl2 5%
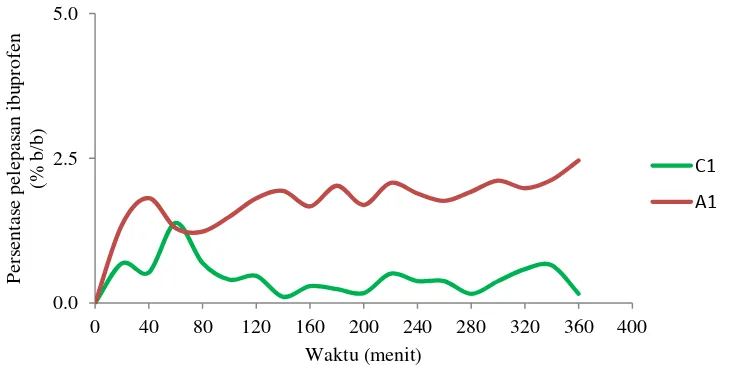
Kapsul dengan formula A1 dan C1 digunakan untuk membandingkan pengaruh konsentrasi CaCl2. Gambar 7 menunjukkan pola pelepasan ibuprofen
pada kapsul formula A1 dan C1. Kedua formula kapsul tersebut menggunakan komposisi natrium alginat-pektin yang sama (2:1) tetapi dibentuk pada konsentrasi CaCl2 yang berbeda. Dalam waktu yang sama, kapsul dengan formula
C1 yang dibentuk pada konesntrasi CaCl2 lebih tinggi daripada kapsul A1
menunjukkan persentase pelepasan ibuprofen yang lebih sedikit. Tingginya konsentrasi Ca2+ menyebabkan banyaknya ikatan taut silang dengan natrium alginat dan pektin, sehingga kapsul yang terbentuk menjadi kokoh dan kaku (Jung et al. 2013; Jelvehgari et al. 2014). Hal tersebut menyebabkan ibuprofen lebih sulit untuk keluar menuju media disolusi.
Gambar 7 Pelepasan ibuprofen dari kapsul formula A1 dengan konsentrasi CaCl2
10
Rendahnya persentase pelepasan ibuprofen pada ketiga formula kapsul tersebut dipengaruhi oleh beberapa faktor, antara lain konsentrasi CaCl2 yang
tinggi (Jung et al. 2013; Jelvehgari et al. 2014) dan lamanya waktu gelasi atau waktu pengadukan (Joshi et al. 2012). Kedua faktor tersebut membuat kapsul yang terbentuk menjadi kaku dan kokoh. Selain itu, waktu pengeringan juga dapat membuat polimer menyusut dan rapat sehingga penetrasi medium disolusi lebih sulit. Gambar 8b menunjukkan sisa kapsul A2 yang mengalami kerusakan lebih banyak dibandingkan kapsul A1 (Gambar 8a). Sementara itu, Gambar 8c menunjukkan bahwa kapsul C1 sebagian besar masih utuh dan hanya mengalami pembenkakan setelah pengujian disolusi. Profil disolusi pada kapsul formula A1 dan A2 menunjukkan pola pelepasan yang bertahap pada menit ke 20 sampai menit ke-360. Waktu eliminasi ibuprofen komersial pada umumnya sekitar 2 jam (Sinuhaji 2012), sehingga hasil penelitian ini telah memperlambat pelepasan ibuprofen.
(a) (b) (c)
Gambar 8 Sisa kapsul (a) A1, (b) A2, dan (c) C1 setelah uji disolusi
SIMPULAN DAN SARAN
Simpulan
Enkapsulasi ibuprofen dengan natrium alginat-pektin menggunakan metode gelasi ionik berhasil dilakukan. Dengan berkurangnya komposisi pektin, kapsul yang dihasilkan berbentuk bulat dan lebih. Efisiensi enkapsulasi yang diperoleh berkisar antara 71.22% sampai 90.41% yang dipengaruhi oleh komposisi pektin dan konsentrasi CaCl2. Profil disolusi menunjukkan pelepasan ibuprofen yang
berjalan lambat kapsul dan persentase pelepasannya dipengaruhi oleh komposisi pektin dan konsentrasi CaCl2.
Saran
11
DAFTAR PUSTAKA
[AOAC] Association of Official Analytical Chemists. 2002. AOAC International methods committee guidelines for validation of qualitative and quantitative food microbiological official methods of analysis. [terhubung berkala]. J AOAC Int. 85:1-5
Arica B, Calis S, Atilla P, Durlu NT, Cakar N, Kas HS, Hincal AA. 2005. In vitro and in vivo studies of ibuprofen-loaded biodegradable alginate beads. J Microencapsulation. 22(2):153-165.doi:10.1080/02652040400026319. [Depkes RI] Departemen Kesehatan Reppublik Indonesia. 1995. Farmakope
Indonesia. Ed ke-4. Jakarta: Departemen Kesehatan RI.
[Depkes RI] Departemen Kesehatan Republik Indonesia. 2001. Petunjuk Operasional Penerapan CPOB. Ed ke-2. Jakarta: Departemen Kesehatan RI. Jakarta: Departemen Kesehatan RI.
Estevinho BN, Rocha F, Santos L, Alves A. 2013. Microencapsulation with chitosan by spray drying for industry applications - a review. Trends Food Sci Technol. 31:138-155.doi:10.1016/j.tifs.2013.04.001.
Fachrurazie. 2012. Mikroenkapsulasi ibuprofen tersalut poli(asamlaktat)-lilin lebah dengan pengemulsi poli(vinil alkohol) [skripsi]. Bogor (ID): Institut Pertanian Bogor.
Fang Y, Al-Assaf S, Phillips GO, Nishinari K, Funami T, Williams PA, Li L. 2007. Multiple steps and critical behaviors of the binding of calcium to alginate. J Phys Chem. 111(10): 2456-2462.doi:10.1021/jp0689870.
Fang Y, Al-Assaf S, Phillips GO, Nishinari K, Funami T, Williams PA. 2008. Binding behavior of calcium to polyuronates: comparison of pectin with alginate. Carbohydr Polym. 72:334–341.doi:10.1016/j.carbpol.2007.08.021. Febrianti RV, Wahyuningsih I. 2013. Efek ulcerogenic dispersi padat
ibuprofen-polivinilpirolidon (PVP) pada tikus putih jantan. Pharmaciana. 3(2):29-36. Felder CHB, Blanco-Prieto MJ, Heizmann J, Merkle HP, Gander B. 2003.
Ultrasonic atomization and subsequent polymer desolvation for peptide and protein microencapsulation into biodegradable polyesters. J Microencapsulation. 20(5):553-567.doi:10.3109/02652040309178346. Goudanavar PS, Bagali RS, Chandrashekhara S, Patil SM. 2010. Design and
characterization of diclofenac sodium microbeads by ionotropic gelation technique. Int J Pharm Bio Sci. 1(2):1-10.
Jaya S, Durance TD, Wang R. 2010. Physical characterization of drug loaded microcapsules and controlled in vitro release study. The Open Biomaterial J. 2:9-17.doi:10.2174/1876502501002010009.
Jelvehgari M, Mobaraki V, Montazam SH. 2014. Preparation and evaluation of mucoadhesive beads/discs of alginate and algino-pectinate of piroxicam for colon-specific drug delivery via oral route. Jundishapur J Nat Pharm Prod. 9(4):1-10.doi:10.17795/jjnpp-16576.
12
Jung J, Arnold RD, Wicker L. 2013. Pectin and charge modified pectin hydrogel
beads as a colon-targeted drug delivery carrier. Colloids and Surf, B: Biointerfaces. 104:116-121.doi:10.1016/j.colsurfb.2012.11.042.
Kemala T. 2010. Mikrosfer polipaduan poli(asam laktat) dengan poli(ɛ -kaprolakton) sebagai pelepasan terkendali ibuprofen secara in vitro [disertasi]. Jakarta (ID): Universitas Indonesia.
Khazaeli P, Pardakhty A, Hassanzadeh F. 2008. Formulation of ibuprofen beads by ionotropic gelation. Iranian J Pharm Research. 7(3):163-170.
Kim HJ, Kim TH, Kang KC, Pyo HB, Jeong HH. 2010. Microencapsulation of rosmarinic acid using polycaprolactone and various surfactants. Int J Cosmetic Sci. 32:185–191.doi:10.1111/j.1468-2494.2010.00526.x.
Madziva H, Kailasapathy K, Phillips M. 2005. Alginate–pectin microcapsules as a potential for folic acid delivery in foods. J Microencapsulation. 22(4):343– 351.doi:10.1080/02652040500100931.
Mandal M, Kumar SS, Krishnamoorthy B, Basu SK. 2010. Development and evaluation of calcium alginate beads prepared by sequential and simultaneous methods. Brazilian J Pharm Sci. 46(4):785-793.doi:10.1590/S1984-82502010000400021.
Morris GA, Kok MS, Harding SE, Adams GG. 2010. Polysaccharide drug delivery system based on pectin and chitosan. Biotechnol Gen Eng review. 27:257-284.doi:10.1080/02648725.2010.10648153.
Patil P, Chavanke D, Wagh M. 2012. A review on ionotropic gelation method: novel approach for controlled gastroretentive gelispheres. Int J Pharmacy Pharmaceutical Sci. 4(4):27-32.
Saravanan M, Bhaskar K, Srinivasa RG, Dhanaraju D. 2003. Ibuprofen-loaded ethylcellulose/polystyrene microspheres: an approach to get prolonged drug release with reduced burst effect and low ethylcellulose content. J Microencapsulatiion. 20(3):289-302.doi:10.1080/0265204031000093087. Sinuhaji Putriana M. 2012. Pelepasan Ibuprofen dari Mikrokapsul Tersalut
Paduan Lilin Lebah dan Poli(Asam Laktat) Secara In Vitro [skripsi]. Bogor (ID): Institut Pertanian Bogor.
Tang C, Guan YX, Yao SJ, Zhu ZQ. 2014. Preparation of ibuprofen-loaded
chitosan films for oral mucosal drug delivery using supercritical solution
impregnation. Int J Pharm. 473:434–441.doi:10.1016/j.ijpharm.2014.07.039. Wukirsari T. 2006. Enkapsulasi ibuprofen dengan penyalut alginat-kitosan
[skripsi]. Bogor (ID): Institut Pertanian Bogor.
Vajpayee A, Fartyal S, Singh AP, Jha SK. 2011. Formulation and evaluation of colon targeted curcumin microspheres using natural polymers. J Pharm Research Opinion. 1(4):108-112.
13
Lampiran 1 Diagram alir penelitian
Natrium alginat Pektin
Larutan penyalut Pengadukan Komposisi natrium
alginat:pektin (% b/v): 2:1, 2.25:0.75, 2.5:0.5
Ibuprofen
CaCl2 5% CaCl2 7.5% CaCl2 10%
Kapsul Natrium Alginat-Pektin
Penentuan panjang gelombang maksimum dan pembuatan
kurva standar
Uji efisiensi penyalutan
Uji disolusi Pengamatan bentuk kapsul
14
Lampiran 2 Pembuatan larutan bufer fosfat pH 7.2
Larutan bufer fosfat yang digunakan pada penelitian ini dibuat dari campuran NaH2PO4.H2O dan Na2HPO4.7H2O dengan konsentrasi 0.2 M untuk
masing-masing larutan. Larutan NaH2PO4.H2O 0.2 M (larutan A) dibuat dengan
melarutkan 27.598 g kristal NaH2PO4.H2O dalam akuades, kemudian volumenya
ditepatkan dengan pelarut yang sama menjadi 1000 mL dalam labu takar. Larutan Na2HPO4.7H2O 0.2 M (larutan B) dibuat dengan melarutkan 53.614 g kristal
Na2HPO4.7H2O dalam akuades, kemudian volumenya ditepatkan dengan pelarut
15
Lampiran 3 Absorbans larutan ibuprofen* pada panjang gelombang maksimum
maks (nm) Absorbans
221.5 0.4560
Keterangan: * = larutan ibuprofen dengan konsentrasi 10 ppm
A
b
so
rb
an
s
16
Lampiran 4 Konsentrasi dan absorbans larutan ibuprofen pada pembuatan kurva standar ibuprofen (maks = 221.5 nm)
[Ibuprofen]
(ppm) Absorbans
0.1 0.0055
0.5 0.0271
1 0.0442
2 0.0906
4 0.1908
6 0.2770
8 0.3737
10 0.4639
12 0.5553
14 0.6477
16 0.7423
18 0.8477
20 0.9502
y = 0.047x - 0.0019 R² = 0.9997
0.00 0.20 0.40 0.60 0.80 1.00
0 2 4 6 8 10 12 14 16 18 20 22
A
b
so
rb
an
s
17
Lampiran 5 Efisiensi penyalutan ibuprofen dalam kapsul natrium alginat-pektin
Formula
A : bobot total kapsul yang diperoleh
B : bobot kapsul yang digunakan untuk penentuan efisiensi mikroenkapsulsi C : absorbans filtrat hasil disolusi kapsul setelah diencerkan 5 kali
18
Lampiran 6 Persentase rerata pelepasan ibuprofen dalam uji disolusi medium basa dari kapsul natrium alginat-pektin
Kapsul formula A1
Waktu (menit) Persentase pelepasan ibuprofen (% b/b)
Ulangan 1 Ulangan 2 Rerata
Waktu (menit) Persentase pelepasan ibuprofen (% b/b)
19
Lanjutan Lampiran 6 Kapsul formula C1
Waktu (menit) Persentase pelepasan ibuprofen (% b/b)
Ulangan 1 Ulangan 2 Rerata
0 0.0000 0.0000 0.0000
20 0.5465 0.8228 0.6846
40 0.5493 0.5035 0.5264
60 1.5836 1.1840 1.3838
80 0.2161 1.1636 0.6898
100 0.6467 0.1566 0.4016
120 0.3938 0.5441 0.4689
140 0.0847 0.1262 0.1055
160 0.3737 0.2098 0.2918
180 0.3951 0.0831 0.2391
200 0.2216 0.1188 0.1702
220 0.4775 0.5392 0.5083
240 0.4889 0.2667 0.3778
260 0.6542 0.1019 0.3780
280 0.2104 0.1031 0.1567
300 0.2591 0.4968 0.3779
320 0.7491 0.4219 0.5855
340 0.4990 0.8037 0.6514
20
23
Keterangan:
FP media : faktor pengenceran media bufer fosfat 7.2 Contoh perhitungan (Kapsul A1 ulangan 1, menit ke-20)
[ ]
24
RIWAYAT HIDUP
Penulis dilahirkan di Cianjur, 26 September1992. Penulis merupakan putra ke-7 dari 8 bersaudara dari ayah Oon Syahroni dan ibu Mimin. Tahun 2011 penulis lulus dari SMA Negeri 1 Sukaresmi. Pada tahun tersebut pula, penulis diterima sebagai mahasiswa Departemen Kimia, Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor melalui jalur Seleksi Nasional Masuk Perguruan Tinggi Negeri (SNMPTN) Undangan.