PENETAPAN KADAR ETIL DIKLOFENAK SECARA
SPEKTROFOTOMETRI ULTRAVIOLET
SKRIPSI
OLEH:
IMOM SUHENDRA SIREGAR
NIM 121524015
PROGRAM EKSTENSI SARJANA FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
PENETAPAN KADAR ETIL DIKLOFENAK SECARA
SPEKTROFOTOMETRI ULTRAVIOLET
SKRIPSI
Diajukan sebagai salah satu syarat untuk memperoleh Gelar Sarjana Farmasi pada Fakultas Farmasi
Universitas Sumatera Utara
OLEH:
IMOM SUHENDRA SIREGAR
NIM 121524015
PROGRAM EKSTENSI SARJANA FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
KATA PENGANTAR
Puji dan syukur kehadirat Allah SWT yang telah memberikan karunia
yang berlimpah sehingga penulis dapat menyelesaikan penelitian dan penyusunan
skripsi yang berjudul “Penetapan Kadar Etil Diklofenak Secara Spektrofotometri
Ultraviolet”. Skripsi ini diajukan sebagai salah satu syarat untuk memperoleh
gelar Sarjana Farmasi di Fakultas Farmasi Universitas Sumatera Utara.
Pada kesempatan ini, dengan segala kerendahan hati penulis mengucapkan
terima kasih kepada Bapak Prof. Dr. Sumadio Hadisahputra, Apt., selaku Dekan
Fakultas Farmasi Universitas Sumatera Utara dan Ibu Prof. Dr. Julia Reveny,
M.Si., Apt., selaku Wakil Dekan I Fakultas Farmasi Universitas Sumatera Utara
yang telah menyediakan fasilitas kepada penulis selama masa perkuliahan. Penulis
juga mengucapkan terima kasih kepada Bapak Drs. Ismail, M.Si., Apt., dan
Bapak Prof.Dr. rer.nat. Effendy De Lux Putra, S.U., Apt., yang telah meluangkan
waktu dan tenaga dalam membimbing penulis dengan penuh kesabaran dan
tanggung jawab, memberikan petunjuk dan saran-saran selama penelitian hingga
selesainya skripsi ini. Ucapan terima kasih juga penulis sampaikan kepada Bapak
Drs. Fathur Rahman Harun, M.Si., Apt., selaku ketua penguji, Ibu Dra. Sudarmi,
M.Si., Apt., dan Ibu Sri Yuliasmi, S.Farm., M.Si., Apt., selaku anggota penguji
yang telah memberikan saran untuk menyempurnakan skripsi ini, dan Ibu Dra.
Azizah Nasution, M.Si., Ph.D., Apt., selaku dosen pembimbing akademik serta
Bapak dan Ibu staf pengajar Fakultas Farmasi Universitas Sumatera Utara yang
Penulis juga mempersembahkan rasa terima kasih yang tak terhingga
kepada orang tua tercinta, Ayahanda Alm. Rosul Jamaluddin Siregar dan Ibunda
Normaini Harahap, S.Pd., atas limpahan kasih sayang, doa yang tulus, nasehat dan
dukungan baik moril maupun materil. Ucapan terima kasih juga penulis
sampaikan kepada adinda tercinta Rada Husna, Siska, Rizal, Kiki dan sahabat
tercinta Ichi, Dira, Nia, Yudhi, Didi, Dadang serta teman-teman Ekstensi Sarjana
Farmasi Tahun 2012 serta semua pihak yang tidak dapat disebutkan satu persatu
atas motivasi, doa dan segala bantuan dalam penyelesaian skripsi ini.
Penulis menyadari sepenuhnya bahwa penulisan skripsi ini masih belum
sempurna, oleh karena itu penulis mengharapkan saran dan kritik yang
membangun demi kesempurnaan skripsi ini. Akhir kata penulis berharap semoga
skripsi ini bermanfaat bagi ilmu pengetahuan khususnya di bidang farmasi.
Medan, Juli 2015
Penulis,
PENETAPAN KADAR ETIL DIKLOFENAK SECARA SPEKTROFOTOMETRI ULTRAVIOLET
Abstrak
Anti-Inflamasi Non Steroid (AINS) adalah salah satu terapi klinis yang berguna untuk pengobatan nyeri, demam, dan inflamasi. Kalium diklofenak adalah derivat fenilasetat yang termasuk AINS yang terkuat daya antiradangnya dengan efek samping yang kurang kuat dibandingkan dengan obat lainnya. Akan tetapi, penggunaan obat ini dalam jangka waktu yang panjang dapat menimbulkan beberapa efek samping yang tidak diinginkan seperti tukak dan iritasi lambung. Untuk mengatasi efek samping yang tidak diinginkan tersebut, telah disintesis senyawa etil diklofenak oleh saudari Rani Purwanti Tambunan yang dilakukan di Laboratorium Kimia Organik Fakultas Farmasi USU, etil diklofenak ini diduga mempunyai efek samping lebih kecil terutama dalam hal iritasi lambung. Tujuan dari penelitian ini adalah untuk menentukan kadar senyawa hasil sintesis etil diklofenak dengan membandingkan pada kadar sediaan kalium diklofenak yang ada dipasaran dalam pelarut KOH 0,2 N secara Spektrofotometri Ultraviolet dan uji validasi dengan parameter uji ketepatan (Akurasi), ketelitian (Presisi), batas deteksi (Limit Of Detection) dan batas kuantitasi (Limit Of Quantitation).
Hasil dari kadar yang diperoleh pada panjang gelombang 276,5 dari etil diklofenak sebesar 97,52 % ± 3,461 dan 103,43% ± 0,444 pada sediaan kalium diklofenak yang ada dipasaran sedangkan hasil uji validasi metode memenuhi persyaratan dengan persen perolehan kembali 94,83%, Relative Standard
Deviation (RSD) 1,1λ1%, batas deteksi (LOD) 0,317 g/ml dan batas kuantitasi
(LOQ) 1,057 g/ml.
Hasil ini menunjukkan bahwa proses sintesis Etil Diklofenak dikatakan baik dengan membandingkan pada penetapan kadar sediaan Kalium Diklofenak yang ada di pasaran yang memenuhi persyaratan kadar tablet menurut USP 36, 2013 yaitu tidak kurang dari 90% dan tidak lebih dari 110% dari jumlah yang tertera pada etiket.
DETERMINATION OF CONCENTRATION ETHYL DICLOFENAC BY ULTRAVIOLET SPECTROPHOTOMETRY
Abstract
Non-Steroidal Anti-Inflammatory Drugs (NSAIDs) is one of the most useful clinic therapeutic for pain, fever, and inflammation. Diclofenac potassium is derivate fenilasetat including NSAIDs the most mighty power with resolvent of side effects are less strong as opposed to other medicine. But the use of this medicine in along period of time could cause some unwanted side effects such as gastric ulcers and irritation. To deal with side effects of the undesirable, has been synthesized a compound of ethyl diclofenac have synthesized compound ethyl diclofenac by Rani Purwanti Tambunan conducted at the Laboratory of Organic parameter accuracy, precision, limit of detection and the limit of quantitation.
Results of the levels obtained at a wavelength of 276.5 from ethyl diclofenac by 97.52% and 103.43% ± 3.461 ± 0.444 in preparation diclofenac potassium in the market while the results of the validation test method meet the requirements of the percent recovery of 94.83% , Relative Standard Deviation
(RSD) 1.1λ1%, the limit of detection (LOD) 0.317 g/ml and the limit of
quantitation (LOQ) 1.057 ug / ml.
The results indicate that the synthesis of Ethyl Diclofenac is good by comparing the assay preparation Diclofenac Potassium on the market that meets the content requirements of tablets according to USP 36. 2013. not less than 90% and not more than 110% of the amount listed on the label.
The keywords: ethyl diclofenac, ultraviolet spektrophotometry, validation
2.1.6 Mekanisme reaksi pembentukan diklofenak ... 9
3.6.2 Pembuatan larutan Induk Baku Kalium Diklofenak dalam pelarut KOH 0,2 N ... 22
3.6.3 Penetapan Panjang Gelombang Serapan Maksimum dalam pelarut KOH 0,2 N ... 22
3.6.4 Penetapan kurva kalibrasi kalium diklofenak dalam pelarut KOH 0,2 N ... 23
3.6.6 Penentuan Kadar Kalium Diklofenak dalam
sediaan Tablet ... 23
3.7 Uji Validasi dengan Parameter Akurasi, Presisi, Batas Deteksi dan Batas Kuantitas ... 24
3.7.1 Uji Akurasi dengan Persen Perolehan Kembali ... 24
3.7.2 Uji Presisi ... 25
3.7.3 Penentuan Batas Deteksi Dan Batas Kuantitas ... 25
3.7.4 Analisis Data secara statistik ... 26
BAB IV HASIL DAN PEMBAHASAN ... 27
4.1 Hasil Penentuan Panjang Gelombang Serapan Maksimum Kalium Diklofenak ... 27
4.2 Hasil Pembuatan dan Penentuan Linieritas Kurva kalibrasi Kalium Diklofenak ………. 30
4.3 Hasil Penentuan Kadar Hasil Sintesis Etil Diklofenak ... 31
4.4 Hasil Uji Validasi Metode spektrofotometri Ultraviolet ... 31
BAB V KESIMPULAN DAN SARAN ... 34
4.1 Kesimpulan ... 34
4.2 Saran ... 34
DAFTAR PUSTAKA ... 35
DAFTAR TABEL
Halaman
Tabel 4.1 Data Absorbansi dari Kurva Serapan Maksimum Kalium
Diklofenak ... 28
Tabel 4.2 Data Absorbansi dari Kurva Serapan Maksimum Etil
Diklofenak ... 29
Tabel 4.3 Data Kurva Kalibrasi dari Kalium Diklofenak ... 30
DAFTAR GAMBAR
Halaman
Gambar 4.1 Kurva serapan Kalium Diklofenak dalam pelarut
KOH 0,2 N ... 28
Gambar 4.2 Kurva serapan Eti Diklofenak dalam pelarut KOH 0,2 N ... 29
Gambar 4.3 Kurva Kalibrasi Kalium Diklofenak dalam pelarut
DAFTAR LAMPIRAN
Halaman
Lampiran 1. Perhitungan konsentrasi pengukuran ... 37
Lampiran 2. Tabel Perhitungan Persamaan Regresi Kalium
Diklofenak dalam pelarut KOH 0,2 N ……… ... 38
Lampiran 3. Contoh Perhitungan Penimbangan Sampel Etil
Diklofenak .. ... 39
Lampiran 4. Contoh Perhitungan Penimbangan Sampel Tablet
Cataflam ... 40
Lampiran 5. Tabel Data Kadar Etil Diklofenak dan Tablet Cataflam
dalam Pelarut KOH 0,2 N ... 41
Lampiran 9. Contoh perhitungan Penimbangan Analit pada Persen
perolehan kembali ... 48
Lampiran 10. Contoh perhitungan Penimbangan Bahan Baku pada
persen perolehan kembali ... 49
Lampiran 17. Tabel Data kadar etil diklofenak dan tablet Cataflam
dalam pelarut KOH 0,2 N ... 56
Lampiran 18. Sertifikat Bahan Baku kalium diklofenak dari PT. Dexa
Medica ... 57
Lampiran 19. Sampel dari Hasil Sintesis Etil Diklofenak dan Tablet
Cataflam ... 58
Lampiran 20. Tabel Nilai Distribusi t ... 59
PENETAPAN KADAR ETIL DIKLOFENAK SECARA SPEKTROFOTOMETRI ULTRAVIOLET
Abstrak
Anti-Inflamasi Non Steroid (AINS) adalah salah satu terapi klinis yang berguna untuk pengobatan nyeri, demam, dan inflamasi. Kalium diklofenak adalah derivat fenilasetat yang termasuk AINS yang terkuat daya antiradangnya dengan efek samping yang kurang kuat dibandingkan dengan obat lainnya. Akan tetapi, penggunaan obat ini dalam jangka waktu yang panjang dapat menimbulkan beberapa efek samping yang tidak diinginkan seperti tukak dan iritasi lambung. Untuk mengatasi efek samping yang tidak diinginkan tersebut, telah disintesis senyawa etil diklofenak oleh saudari Rani Purwanti Tambunan yang dilakukan di Laboratorium Kimia Organik Fakultas Farmasi USU, etil diklofenak ini diduga mempunyai efek samping lebih kecil terutama dalam hal iritasi lambung. Tujuan dari penelitian ini adalah untuk menentukan kadar senyawa hasil sintesis etil diklofenak dengan membandingkan pada kadar sediaan kalium diklofenak yang ada dipasaran dalam pelarut KOH 0,2 N secara Spektrofotometri Ultraviolet dan uji validasi dengan parameter uji ketepatan (Akurasi), ketelitian (Presisi), batas deteksi (Limit Of Detection) dan batas kuantitasi (Limit Of Quantitation).
Hasil dari kadar yang diperoleh pada panjang gelombang 276,5 dari etil diklofenak sebesar 97,52 % ± 3,461 dan 103,43% ± 0,444 pada sediaan kalium diklofenak yang ada dipasaran sedangkan hasil uji validasi metode memenuhi persyaratan dengan persen perolehan kembali 94,83%, Relative Standard
Deviation (RSD) 1,1λ1%, batas deteksi (LOD) 0,317 g/ml dan batas kuantitasi
(LOQ) 1,057 g/ml.
Hasil ini menunjukkan bahwa proses sintesis Etil Diklofenak dikatakan baik dengan membandingkan pada penetapan kadar sediaan Kalium Diklofenak yang ada di pasaran yang memenuhi persyaratan kadar tablet menurut USP 36, 2013 yaitu tidak kurang dari 90% dan tidak lebih dari 110% dari jumlah yang tertera pada etiket.
DETERMINATION OF CONCENTRATION ETHYL DICLOFENAC BY ULTRAVIOLET SPECTROPHOTOMETRY
Abstract
Non-Steroidal Anti-Inflammatory Drugs (NSAIDs) is one of the most useful clinic therapeutic for pain, fever, and inflammation. Diclofenac potassium is derivate fenilasetat including NSAIDs the most mighty power with resolvent of side effects are less strong as opposed to other medicine. But the use of this medicine in along period of time could cause some unwanted side effects such as gastric ulcers and irritation. To deal with side effects of the undesirable, has been synthesized a compound of ethyl diclofenac have synthesized compound ethyl diclofenac by Rani Purwanti Tambunan conducted at the Laboratory of Organic parameter accuracy, precision, limit of detection and the limit of quantitation.
Results of the levels obtained at a wavelength of 276.5 from ethyl diclofenac by 97.52% and 103.43% ± 3.461 ± 0.444 in preparation diclofenac potassium in the market while the results of the validation test method meet the requirements of the percent recovery of 94.83% , Relative Standard Deviation
(RSD) 1.1λ1%, the limit of detection (LOD) 0.317 g/ml and the limit of
quantitation (LOQ) 1.057 ug / ml.
The results indicate that the synthesis of Ethyl Diclofenac is good by comparing the assay preparation Diclofenac Potassium on the market that meets the content requirements of tablets according to USP 36. 2013. not less than 90% and not more than 110% of the amount listed on the label.
The keywords: ethyl diclofenac, ultraviolet spektrophotometry, validation
BAB I PENDAHULUAN 1.1 Latar Belakang
Anti-Inflamasi Non Steroid (AINS) adalah salah satu terapi klinis yang
berguna untuk pengobatan nyeri, demam, dan inflamasi. AINS menimbulkan efek
antiradang melalui beberapa kemungkinan, antara lain adalah menghambat
biosintesis dan pengeluaran prostaglandin dengan cara memblok secara
terpulihkan enzim siklooksigenase sehingga menurunkan gejala keradangan
(Siswandono dan Soekardjo, 2000; Suryawhanshi, dkk., 2013).
Kalium diklofenak adalah derivat fenilasetat yang termasuk
Anti-Inflamasi Non Steroid (AINS) yang terkuat daya antiradangnya dengan efek
samping yang kurang kuat dibandingkan dengan obat lainnya (indometasin,
piroxicam). Obat ini sering digunakan untuk segala macam nyeri, juga pada
migren dan encok. Kalium diklofenak cepat diabsorbsi setelah pemberian oral dan
mempunyai waktu paruh yang pendek, Akan tetapi, penggunaan obat ini dalam
jangka waktu yang panjang dapat menimbulkan beberapa efek samping yang tidak
diinginkan seperti tukak dan iritasi lambung (Tan dan Rahardja, 2008).
Untuk mengatasi efek samping yang tidak diinginkan tersebut, telah
dirancang Pro-drug, dimana Pro-drug dirancang untuk mengubah sifat
fisika-kimia obat, dengan melindungi gugus asam bebas pada suatu molekul AINS, yang
dapat melindungi saluran pencernaan dari iritasi lokal, salah satu pembuatannya
adalah dengan pembentukan ester. Etil diklofenak merupakan hasil sintesis
melalui reaksi esterifikasi antara asam diklofenak dengan etanol dengan bantuan
samping yang lebih kecil dibandingkan dengan senyawa garamnya seperti natrium
diklofenak atau kalium diklofenak terutama dalam hal iritasi lambung karena
gugus asam pada diklofenak yang berperan sebagai tukak lambung telah
dilindungi oleh gugus etil (Aiache dan Devissaguet, 1993; Suryawhanshi, dkk.,
2013).
Menurut Moffat, dkk., (2004), diklofenak diidentifikasi dalam pelarut
basa pada panjang gelombang 275 nm dengan nilai A11 = 351b. Berdasarkan
srtuktur rumus molekulnya etil diklofenak mempunyai gugus kromofor dan
ausokrom, sehingga kemungkinan dapat ditentukan kadarnya secara
Spektrofotometri Ultraviolet.
Dimana salah satu kegunaan metode spektrofotometri ultraviolet secara
kuantitatif adalah untuk menentukan kadar senyawa yang mengabsorpsi radiasi
ultraviolet dengan membandingkan absorban senyawa standar yang
konsentrasinya diketahui dan diukur pada kondisi larutan yang sama (Satiadarma,
dkk., 2004).
Mengingat hal tersebut di atas maka penulis tertarik untuk melakukan
penelitian tentang penetapan kadar dari hasil sintetis etil diklofenak dengan
membandingkan pada kadar sediaan kalium diklofenak yang ada di pasaran secara
spektrofotometri ultraviolet, selain diperlukan metode alternatif yang memerlukan
alat dan biaya operasional yang lebih murah serta lebih mudah dalam
pelaksanaannya namun masih dapat memberikan hasil dengan akurasi dan presisi
yang baik. Dimana Metode ini memiliki keuntungan antara lain dapat digunakan
untuk analisis suatu zat dalam jumlah kecil, pengerjaannya cepat, sederhana,
1.2 Perumusan Masalah
Berdasarkan latar belakang di atas, maka perumusan masalah untuk
penelitian ini adalah:
1. Apakah hasil sintesis etil diklofenak dapat ditentukan kadarnya dengan
membandingkan pada kadar sediaan kalium diklofenak yang ada di
pasaran secara Spektrofotometri Ultraviolet?
2. Apakah metode Spektrofotometri Ultraviolet yang digunakan pada
penetapan kadar etil diklofenak dalam pelarut KOH 0,2 N Memenuhi
syarat uji validasi?
1.3 Hipotesis
Berdasarkan perumusan masalah diatas, maka perumusan masalah utuk
penelitian ini adalah:
1. Hasil sintesis etil diklofenak dapat ditentukan kadarnya dengan
membandingkan pada kadar sediaan kalium diklofenak yang ada dipasaran
secara Spektrofotometri Ultraviolet.
2. Metode Spektrofotometri Ultraviolet yang digunakan pada penetapan
kadar etil diklofenak dalam pelarut KOH 0,2 N Memenuhi syarat uji
validasi.
1.4 Tujuan Penelitian
Tujuan Penelitian adalah:
1. Untuk mengetahui kadar senyawa hasil sintesis etil diklofenak dengan
membandingkan pada kadar sediaan kalium diklofenak yang ada di
2. Untuk Mengetahui bahwa metode Spektrofotometri Ultraviolet pada
penetapan kadar etil diklofenak memenuhi syarat uji validasi dengan
parameter uji ketepatan (akurasi), ketelitian (presisi), batas deteksi (Limit
Of Detection) dan batas kuantitasi (Limit Of Quantitation)
1.5 Manfaat Penelitian
Adapun Manfaat Dari Penelitian ini adalah untuk mengetahui kadar etil
diklofenak dengan membandingkan pada kadar sediaan kalium diklofenak yang
ada di pasaran Secara Spektofotometri Ultraviolet dan untuk mengetahui hasil uji
BAB II
TINJAUAN PUSTAKA
2.1 Diklofenak
2.1.1Kalium diklofenak
Menurut Anonim (2009), uraian tentang kalium diklofenak adalah sebagai
berikut:
Rumus bangun :
Rumus molekul : C14H10Cl2KNO2
Berat molekul : 334,24
Nama kimia : Benzeneacetic acid, 2-[(2,6-dichlorophenyl)amino]
monopotassium salt
Nama lain : Potassium [o-(2,6-dichloroanilino)phenyl]acetate
Nama dagang : Cataflam (Novartis)
Persen komposisi : C 50,31%, H 3,02%, Cl 21,21%, K 11,70%, N 4,19%,
O 9,57%
Kelarutan : Sedikit larut dalam air, mudah larut dalam metanol,
2.1.2Etil diklofenak
Menurut Dannhardt dan Sorbera (2014), uraian tentang etil diklofenak
adalah sebagai berikut:
Rumus bangun :
Rumus molekul : C16H15Cl2NO2
Berat molekul : 324,20
Nama kimia : 2-[(2,6-dichlorophenyl)amino] Benzeneacetic acid
Ethyl Ester
Nama lain : Ethyl 2-(2,6-Dichloroanilino)phenylacetate
Nama dagang : -
Karakteristik : Kristal putih
Titik lebur : 66 - 690C
Kelarutan : Sedikit larut dalam air, mudah larut dalam metanol,
2.1.3Asam diklofenak
Menurut Moffat, dkk., (2004), uraian tentang asam diklofenak adalah
sebagai berikut:
Rumus bangun :
Rumus molekul : C14H11Cl2NO2
Berat molekul : 296,15
Nama kimia : 2-[(2,6-dichlorophenyl)amino]benzeneacetic acid
Nama lain : [o-(2,6-dichloroanilino)phenyl]acetic acid
Nama dagang : Voltarol (Novartis)
Karakteristik : Kristal dari eter-petroleum eter
Titik lebur : 156 - 1580C
Persen komposisi : C 56,78%, H 3,74%, Cl 23,94%, N 4,73%, O 10,80%
2.1.4 Efek Farmakologi
Diklofenak mempunyai aktivitas analgesik, antipiretik dan antiradang.
Senyawa ini merupakan inhibitor siklooksigenase, dan potensinya jauh lebih besar
dari pada indometasin, naproksen atau beberapa senyawa lain. Selain itu
diklofenak menurunkan konsentrasi intrasel arakidonat bebas dalam leukosit yaitu
dengan mengubah pelepasan dan pengambilan asam lemak tersebut. Diklofenak
dicapai 2 jam setelah pemberian oral, dengan waktu paruh eliminasi 3-6 jam
(Roberts dan Morrow, 2001; Siswandono dan Soekardjo, 1995).
Mekanisme kerjanya, bila membran sel mengalami kerusakan oleh suatu
rangsangan kimiawi, fisik, atau mekanis, maka enzim fosfolipase diaktifkan untuk
mengubah fosfolipida menjadi asam arachidonat. Asam lemak poli tak jenuh ini
kemudian untuk sebagian diubah oleh enzim cylo-oksigenase menjadi
endoperoksida dan seterusnya menjadi prostaglandin. cylo-oksigenase terdiri dari
dua iso-enzim, yaitu COX-1 (tromboxan dan prostacyclin) dan COX-2
(prostaglandin). Kebanyakan COX-1 terdapat di jaringan, antara lain dipelat-pelat
darah, ginjal dan saluran cerna. COX-2 dalam keadaan normal tidak terdapat di
jaringan tetapi dibentuk selama proses peradangan oleh sel-sel radang.
Penghambatan COX-2 lah yang memberikan efek anti radang dari obat AINS.
AINS yang ideal hanya menghambat COX-2 (peradangan) dan tidak menghambat
COX-1 (perlindungan mukosa lambung) (Tan dan Rahardja, 2008).
2.1.5 Efek samping
Diklofenak menimbulkan efek samping pada sekitar 20% pasien,
akibatnya sekitar 2% pasien menghentikan terapi. Efek saluran cerna merupakan
yang paling umum, perdarahan dan pembentukan ulser atau perforasi dinding
usus. Respon lain yang tidak diinginkan terhadap diklofenak antara lain efek SSP,
ruam kulit, reaksi alergi, retensi cairan, edema dan yang jarang, gangguan fungsi
ginjal. Obat ini tidak dianjurkan untuk anak-anak, ibu menyusui, atau wanita
2.1.6 Mekanisme Reaksi Pembentukan Senyawa Diklofenak
(Sumber: Ismail, 2012). Diklofenak
2.1.7 Hidrolisis Etil Diklofenak
Asam Diklofenak
2.1.8 Saponifikasi Etil Diklofenak
( Sumber: Kice dan Marvell,1965). Etil diklofenak
2.2 Spektrofotometri Ultraviolet
2.2.1 Teori Spektrofotometri Ultraviolet
Spektrofotometri sesuai dengan namanya adalah alat yang terdiri dari
spektrometer dan fotometer. Spektrometer menghasilkan sinar dari spektrum
dengan panjang gelombang tertentu, dan fotometer adalah alat pengukur intensitas
cahaya yang ditransmisikan atau yang diabsorbsi. Jadi Spektrofotometri
digunakan untuk mengukur energi secara relatif jika energi tersebut
ditransmisikan, direfleksikan, atau diemisikan sebagai fungsi dari panjang
gelombang (Khopkar, 2007).
Spektrofotometri serapan merupakan pengukuran suatu interaksi antara
radiasi elektromagnetik dan molekul atau atom dari suatu zat kimia, teknik yang
sering digunakan dalam analisis farmasi meliputi spektrofotometri ultraviolet,
sinar tampak, inframerah, dan serapan atom. Jangkauan panjang gelombang untuk
daerah ultraviolet adalah 200-400 nm, daerah cahaya tampak 400-800 nm,
inframerah dekat 800-3000 nm, dan daerah serapan atom 2,5-40 m atau 4000
-250/cm (Ditjen POM, 1995).
Radiasi ultraviolet dan sinar tampak diabsorpsi oleh molekul organik
aromatik, molekul yang mengandung elektron-π terkonjugasi dan atau atom
dengan elektron-n yang menyebabkan transisi elektron di orbital terluarnya dari
tingkat energi dasar ke tingkat energi tereksitasi. Besarnya serapan radiasi tersebut
sebanding dengan banyaknya molekul analit yang mengabsorpsi sehingga dapat
Gugus fungsi yang menyerap radiasi di daerah ultraviolet dekat dan daerah
tampak disebut gugus kromofor dan hampir semua gugus ini mempunyai ikatan
tak jenuh. Pada kromofor jenis ini transisi elektron terjadi dari π → π*, yang
menyerap radiasi pada panjang gelombang maksimum kurang dari 200 nm,
misalnya pada >C=C< dan –C ≡ C–. Kromofor ini merupakan tipe transisi dari
sistem yang mengandung elektron π pada orbital molekulnya. Untuk senyawa
yang mempunyai sistem konyugasi, perbedaan energi antara keadaan dasar dan
keadaan tereksitasi menjadi lebih kecil sehingga penyerapan terjadi pada panjang
gelombang yang lebih besar (Dachriyanus, 2004).
Gugus fungsi, seperti –OH, -NH2, -Cl, dan –OCH3 yang mempunyai
elektron-elektron valensi bukan ikatan (memberikan transisi n → π*) disebut
gugus auksokrom yang tidak dapat menyerap radiasi ultraviolet-sinar tampak,
tetapi apabila gugus ini terikat pada gugus kromofor mengakibatkan pergeseran
panjang gelombang ke arah yang lebih besar (pergeseran batokromik) dengan
intensitas yang lebih kuat. Efek hipsokromik adalah suatu pergeseran panjang
gelombang maksimum ke panjang gelombang lebih pendek, biasanya terjadi jika
senyawa dengan ausokrom basa terion dan pasangan elektron menyendirinya tidak
dapat lagi berinteraksi dengan elektron-elektron kromofor (Dachriyanus, 2004;
Cairns 2003).
2.2.2 Hukum Lambert-Beer
Pengukuran serapan cahaya oleh larutan molekul diatur dengan hukum
Lambert- Beer, yang ditulis sebagai berikut:
Dengan I0 adalah intensitas radiasi yang masuk, It adalah intensitas radiasi yang
ditransmisikan , A dikenal sebagai absorbansi dan merupakan ukuran jumlah
cahaya yang diserap oleh sampel, ε adalah tetapan yang dikenal sebagai koefisien
ekstingsi molar dan merupakan absorbans larutan 1 M analit tersebut, b adalah
panjang jalur sel dalam cm, biasanya 1 cm, dan c adalah konsentrasi analit dalam
mol per liter (Watson, 2010).
Dalam produk farmasi, konsentrasi dan jumlah biasanya dinyatakan dalam
gram atau miligram dan bukan dalam mol sehingga untuk keperluan analisis
produk ini, hukum Lambert-Beer ditulis dalam bentuk berikut ini:
A = A (1%, 1cm) bc
A adalah absorbans yang diukur, A (1%, 1cm) adalah absorbans larutan
1% b/v (g/100 ml) dalam satu sel berukuran 1 cm, b adalah panjang jalur dalam
cm, dan c adalah konsentrasi sampel dalam g/100 ml. Karena pengukuran
biasanya dibuat dalam sel berukuran 1 cm (Watson, 2010).
2.2.3 Penggunaan Spektofotometri Ultraviolet
Spektrum UV-Vis dapat digunakan untuk analisis kualitatif dan kuantitatif.
1. Aspek Kualitatif
Kegunaan spektrofotometri ultraviolet dan sinar tampak dalam analisis
kualitatif sangat terbatas, karena rentang daerah radiasi yang sangat sempit (500
nm) hanya dapat mengakomodasi sedikit sekali puncak absorpsi maksimum dan
minimum, karena senyawa tidak diketahui, tidak memungkinkan. Kegunaannya
gelombang puncak absorpsi maksimum, nilai absorptivitas, nilai absorptivitas
molar atau nilai ekstingsi, yang khas untuk suatu senyawa yang dilarutkan dalam
suatu pelarut pada pH tertentu (Satiadarma, dkk., 2004).
2. Aspek Kuantitatif
Dalam aspek kuantitatif, suatu berkas radiasi dikenakan pada cuplikan
(larutan sampel) dan intensitas sinar radiasi yang diteruskan diukur besarnya.
Radiasi yang diserap oleh cuplikan ditentukan dengan membandingkan intensitas
sinar yang diteruskan dengan intensitas sinar yang diserap jika tidak ada spesies
penyerap lainnya. Intensitas atau kekuatan radiasi cahaya sebanding dengan
jumlah foton yang melalui satu satuan luas penampang perdetik. Serapan dapat
terjadi jika foton/radiasi yang mengenai cuplikan memiliki energi yang sama
dengan energi yang dibutuhkan untuk menyebabkan terjadinya perubahan tenaga.
Penetapan kadar dilakukan dengan mengukur absorban pada panjang
gelombang maksimum, agar dapat memberikan absorban tertinggi untuk setiap
konsentrasi. Bila suatu senyawa mempunyai lebih dari satu puncak, lebih
diutamakan panjang gelombang maksimum yang absorptivitasnya terbesar dan
memberikan kurva kalibrasi linier dalam rentang konsentrasi yang relatif lebar
dan meningkat yang ditentukan dengan persamaan regresi yang merupakan
hubungan antara konsentrasi dan serapan (gandjar dan Rohman, 2007;
Satiadarma, 2004):
Y = aX + b
Dimana :
X = konsentrasi
a = koefisien regresi (juga menyatakan slope/kemiringan)
b = tetapan regresi dan juga disebut dengan intersep
Koefisien regresi (a) dapat diperoleh dengan metode kuadrat terkecil (least square
method).
∑ ̅ ̅
∑ ̅
Selanjutnya b dihitung dari hubungan ̅ ̅
Menurut Gandjar dan Rohman (2007), Sebelum dilakukan perhitungan
analisis lebih lanjut berdasarkan persamaan regresi linier yang didapat, terlebih
dahulu harus ditentukan apakah ada korelasi yang bermakna antara kedua besaran
yang diukur. Untuk itu perlu dihitung besarnya koefisien korelasi (r) berdasarkan
rumus berikut :
r = ∑ ̅ ̅
√ ∑ ̅ ∑ ̅
2.2.4 Peralatan Untuk Spektrofotometri
Unsur -unsur terpenting suatu spektrofotometer adalah sebagai berikut:
1. Sumber sinar
Untuk sinar tampak digunakan lampu tungsten. Lampu ini terbuat dari
logam tungsten. Lampu tungsten mengemisikan sinar pada panjang
gelombang 350 – 2000 nm. Untuk senyawa-senyawa yang menyerap
lampu deuterium merupakan sumber energi tinggi yang mengemisikan
sinar pada panjang gelombang 200 – 370 nm dan digunakan untuk
semua spektroskopi dalam daerah spektrum ultraviolet (Gandjar dan
Rohman, 2012).
2. Monokromator
Pada pengukuran kuantitatif, sinar harus bersifat mokromatik, yakni
sinar dengan satu panjang gelombang tertentu. Hal ini dicapai dengan
melewatkan sinar polikromatik yaitu sinar dengan beberapa panjang
gelombang melalui suatu monokromator. Monokromator adalah suatu
sistem celah dan suatu unsur dispersif. Radiasi dari sumber difokuskan
ke celah masuk, kemudian disejajarkan oleh sebuah lensa atau cermin
sehingga suatu berkas sejajar jatuh ke unsur pendispersi, yang berupa
Prisma atau suatu kisi difraksi (Gandjar dan Rohman, 2012; Day dan
Underwood, 1986).
3. Kuvet (sel)
Kuvet (sel) digunakan sebagai wadah sampel yang akan di analisis.
Pada pengukuran di daerah sinar tampak, kuvet kaca dapat digunakan,
tetapi untuk pengukuran pada daerah ultraviolet harus menggunakan
sel kuarsa karena gelas pengukuran di daerah sinar tampak, kuvet kaca
dapat digunakan, tetapi untuk pengukuran pada daerah ultraviolet
harus menggunakan sel kuarsa karena gelas tidak tembus cahaya pada
daerah ini. Kuvet umumnya mempunyai ketebalan 1 cm (Day dan
4. Detektor
Detektor berperan untuk memberikan respon terhadap cahaya pada
berbagai panjang gelombang. Detektor akan mengubah intensitas
berkas sinyal menjadi kedalam sinyal elektrik yang dapat diukur
dengan mudah dan akan ditampilkan oleh penampil data dalam bentuk
angka (Khopkar, 2007; Gandjar dan Rohman, 2012).
5. Recorder
Recorder digunakan sebagai perekam absorbansi yang dihasilkan dari
pengukuran (Day and Underwood, 1986).
2.3 Validasi Metoda Analisis
Validasi metoda analisis adalah suatu tindakan penilaian terhadap parameter
tertentu, berdasarkan percobaan laboratorium, untuk membuktikan bahwa
parameter tersebut memenuhi persyaratan untuk penggunaannya. Beberapa
Parameter analisis yang ditentukan pada validasi yaitu akurasi, presisi, batas
deteksi, batas kuantitasi, dan rentang kadar dan ketahanan (Gandjar dan Rohman,
2007; Harmita, 2004).
1. Akurasi
Akurasi (kecermatan) adalah ukuran yang menunjukkan derajat kedekatan hasil
analisis dengan kadar analit sebenarnya. Akurasi dinyatakan sebagai persen
perolehan kembali (% recovery) analit yang ditambahkan dan dapat ditentukan
melalui dua cara, yaitu metode simulasi (spiked placebo recovery) dan metode
sejumlah analit bahan murni (senyawa pembanding) ditambahkan ke dalam
campuran bahan pembawa sediaan farmasi lalu campuran tersebut dianalisis dan
hasilnya dibandingkan dengan kadar analit yang ditambahkan (kadar yang
sebenarnya). Dalam metode penambahan baku, sampel dianalisis lalu sejumlah
tertentu analit yang diperiksa ditambahkan ke dalam sampel dicampur dan
dianalisis lagi. Selisih kedua hasil dibandingkan dengan kadar yang sebenarnya.
Persen perolehan kembali ditentukan sebagai rasio antara hasil yang diperoleh
dari analisis dengan hasil sebenarnya yang dihitung secara teoritis. Hal yang
penting untuk diperhatikan adalah metode kuantitasi yang digunakan dalam
penentuan akurasi harus sama dengan metode kuantitasi yang digunakan untuk
menganalisis sampel dalam penelitian (Harmita, 2004).
Menurut Harmita (2004), persen perolehan kembali dapat dihitung dengan
menggunakan rumus sebagai berikut:
% Perolehan Kembali = 100%
Keterangan :
A = konsentrasi sampel yang diperoleh setelah penambahan baku
B = konsentrasi sampel sebelum penambahan baku
C = konsentrasi baku yang ditambahkan
2. Presisi
Presisi dari suatu metode analisis adalah derajat kesesuaian diantara
masing-masing hasil uji, jika prosedur analisis diterapkan berulang kali pada sejumlah
cuplikan yang diambil dari sampel homogen. Presisi juga diartikan sebagai ukuran
relatif (RSD). Sesuai dengan International Conference on Harmonization (ICH),
presisi harus dilakukan pada 3 tingkatan yang berbeda yaitu:
a. Keterulangan yaitu ketepatan pada kondisi percobaan yang sama
(berulang) baik orangnya, peralatannya, tempatnya, maupun waktunya.
b. Presisi antara yaitu ketepatan pada kondisi percobaan yang berbeda, baik
orangnya, peralatannyan tempatnya, maupun waktunya.
c. Ketertiruan merujuk pada hasil-hasil dari laboratorium yang lain.
Pengujian pada presisi biasanya dilakukan replikasi sebanyak 6-15 pada sampel
tunggal untuk tiap-tiap konsentrasi. Pengujian dengan KCKT Nilai RSD antara
1-2% biasanya dipersyaratkan untuk senyawa-senyawa aktif dalam jumlah yang
banyak, sedangkan untuk senyawa-senyawa dengan kadar sekelumit, RSD
berkisar antara 5-15% (Gandjar dan Rohman, 2007; Satiadarma, dkk., 2004).
3. Batas Deteksi (LOD) dan Batas Kuantitas (LOQ)
Menurut Harmita (2004), Batas deteksi (limit of detection) didefinisikan
sebagai konsentrasi analit terendah dalam sampel yang masih dapat terdeteksi.
sedangkan Batas kuantitas adalah konsentrasi analit terendah dalam sampel yang
dapat ditentukan dengan presisi dan akurasi yang dapat diterima pada kondisi
operasional metode yang digunakan. Hal ini dapat dihitung dengan rumus sebagai
berikut:
Batas deteksi (LOD) =
Batas Kuantitas (LOQ) =
BAB III
METODOLOGI PENELITIAN
3.1 Jenis Penelitian
Jenis yang digunakan pada penelitian ini adalah penelitian deskriptif
kuantitatif laboratorik dengan menggunakan metode Spektrofotometri Ultraviolet
( UV mini 1240 Shimadzu).
3.2 Tempat dan waktu penelitian
Penelitian ini dilakukan di Laboratorium Biofarmasetika dan
Farmakokinetik Fakultas Farmasi Universitas Sumatera Utara, dimulai dari
Oktober 2014 sampai dengan November 2014.
3.3 Alat
Alat–alat yang digunakan dalam penelitian adalah Spektrofotometer
Ultraviolet (UV mini-1240 Shimadzu), neraca analitik (Mettler Toledo), kuvet,
karet penghisap, spatula, alat-alat gelas dan alat-alat lainnya yang diperlukan
dalam penyiapan sampel. (Gambar Spektrofotometer UV dapat dilihat pada
Lampiran 17, halaman 38).
3.4 Bahan-bahan
Bahan yang digunakan dalam penelitian ini adalah baku pembanding
kalium diklofenak (PT. Dexa Medica), KOH 0,2 N, etanol (pro analis), hasil
sintesis etil diklofenak dan tablet sediaan kalium diklofenak dengan nama dagang
3.5 Pengambilan Sampel
Sampel dari penelitian ini adalah Tablet sediaan kalium diklofenak
(Cataflam) yang ada di pasaran dan etil diklofenak diperoleh dari saudari Rani
Purwanty Tambunan, merupakan hasil sintesis dari kalium diklofenak yang
dilakukan di Laboratorium Kimia Organik Fakultas Farmasi USU.
3.6 Prosedur Penelitian
3.6.1 Pembuatan Pereaksi KOH 0,2 N
Larutkan 11,222 gram KOH pekat dalam akuades bebas CO2 hingga
1000 ml (Ditjen POM,1979).
3.6.2 Pembuatan Larutan Induk Baku Kalium Diklofenak
Ditimbang seksama 25 mg kalium diklofenak, dimasukkan ke dalam labu
tentukur 25 ml, ditambahkan dengan etanol hingga larut, kemudian dicukupkan
volumenya dengan KOH 0,2 N, dikocok homogen, sehingga diperoleh larutan
dengan konsentrasi 1000 µg/ml, larutan ini disebut dengan larutan induk baku
(LIB I). Dari larutan ini dipipet 2,5 ml dimasukkan ke dalam labu tentukur 25 ml,
diencerkan dengan KOH 0,2 N sampai garis tanda sehingga diperoleh konsentrasi
100 µg/ml (LIB II).
3.6.3 Penetapan Panjang Gelombang Serapan Maksimum
Dipipet 3 ml dari larutan induk baku II (100 µg/ml) dimasukkan ke dalam
labu tentukur 25 ml, diencerkan dengan KOH 0,2 N sampai garis tanda. Lalu
dikocok homogen sehingga diperoleh konsentrasi 12 µg/ml. Kemudian diukur
3.6.4 Pembuatan dan Penetapan Kurva Kalibrasi Kalium Diklofenak
Dipipet larutan induk baku II (100 µg/ml) 1,5 ml; 2,25 ml; 2,75 ml; 3,5 ml;
dan 4,25 ml, masing masing dimasukkan ke dalam labu tentukur 25 ml,
ditambahkan KOH 0,2 N sampai garis tanda. Lalu dikocok sampai homogen.
Diperoleh larutan dengan konsentrasi 6 µg/ml; 9 µg/ml; 11 µg/ml; 14 µg/ml;
17 µg/ml. Kemudian diukur serapannnya pada panjang gelombang maksimum
yang diperoleh dan sebagai blanko digunakan KOH 0,2 N, kemudian dihitung
persamaan regresi dan koefisien kolerasi.
3.6.5 Penentuan Kadar Hasil Sintesis Etil Diklofenak dalam pelarut KOH 0.2 N
Ditimbang serbuk etil diklofenak tidak kurang dari 24,25 mg
(penimbangan dilakukan sebanyak 6 kali perlakuan), dimasukkan ke dalam labu
tentukur 25 ml, lalu ditambahkan 5 ml etanol, kocok hingga larut, kemudian
ditambahkan KOH 0,2 N sampai garis tanda, lalu dikocok homogen. Kemudian
dipipet 2,5 ml dimasukkan ke dalam labu 25 ml, dicukupkan dengan KOH 0,2 N
hingga garis tanda dan dikocok homogen. Kemudian dipipet 3 ml larutan,
dimasukkan ke dalam labu tentukur 25 ml. lalu dicukupkan volumenya dengan
KOH 0,2 N hingga garis tanda, dikocok homogen. Lalu diukur serapannya pada
panjang gelombang maksimum yang diperoleh.
3.6.6 Penentuan Kadar Kalium Diklofenak dalam Sediaan Tablet dalam pelarut KOH 0,2 N
Ditimbang dan diserbukkan tidak kurang dari 20 tablet. Ditimbang
seksama serbuk setara dengan 50 mg Kalium Diklofenak (penimbangan dilakukan
sebanyak 6 kali perlakuan), dimasukkan ke dalam labu tentukur 50 ml, kemudian
KOH 0,2 N sampai garis tanda, lalu dikocok homogen. Kemudian disaring, 10 ml
filtrat pertama dibuang, lalu dipipet 5 ml dimasukkan ke dalam labu 50 ml,
dicukupkan dengan KOH 0,2 N hingga garis tanda dan dikocok homogen.
Kemudian dipipet 3 ml larutan, dimasukkan ke dalam labu tentukur 25 ml. Lalu
dicukupkan dengan KOH 0,2 N hingga garis tanda, dikocok homogen. Kemudian
diukur serapannya pada panjang gelombang maksimum yang diperoleh.
Penetapan kadar bahan obat hasil sintesis ditentukan dengan menggunakan
persamaan persamaan regresi, yaitu:
Y = aX + b
3.7 Uji Validasi dengan Parameter Akurasi, Presisi, Batas Deteksi dan Batas Kuantitas
3.7.1 Uji Akurasi dengan Persen Perolehan Kembali (% Recovery)
Uji akurasi dilakukan dengan metode penambahan baku (Standard
Addition Method) yaitu dengan membuat 3 konsentrasi analit sampel dengan
rentang spesifik 80, 100 dan 120 %, dimana masing-masing dilakukan sebanyak 3
kali replikasi. Setiap rentang spesifik mengandung 70% analit sampel dan 30%
baku pembanding, kemudian dianalisis dengan perlakuan yang sama seperti pada
penetapan kadar sampel (Harmita, 2004).
Hasil dapat dilihat pada Tabel 3, halaman 17
Menurut Harmita (2004), Persen perolehan kembali (% recovery) dapat
dihitung dengan rumus sebagai berikut:
Keterangan:
A = Konsentrasi sampel yang diperoleh setelah penambahan baku
B = Konsentrasi sampel sebelum penambahan baku
C = Konsentasi baku yang ditambahkan
3.7.2 Uji Presisi
Menurut Harmita (2004), Uji presisi (keseksamaan) ditentukan dengan
parameter RSD ( Relative standard Deviasi) dengan rumus:
RSD =
̅
Keterangan:
RSD = Relative Standard Deviasi
SD = Standard deviasi
̅ = Kadar rata-rata diklofenak dalam sampel
3.7.3 Penentuan Batas Deteksi (LOD) dan Batas Kuantitas (LOQ)
Menurut Harmita, 2004, Untuk menentukan bats deteksi (LOD) dan batas
3.7.4 Analisis Data Secara Statistik
Menurut Gandjar dan Rohman (2007), Standar deviasi merupakan akar
jumlah kuadrat deviasi masing-masing hasil penetapan terhadap rata-rata dibagi
dengan derajat kebebasannya. Untuk menghitung Standar deviasi (SD) digunakan
rumus:
√∑
Untuk mengetahui apakah data diterima atau ditolak digunakan rumus seperti
dibawah ini:
Untuk mencari kadar sebenarnya dengan taraf kepercayaan 99 persen, dengan
derajat kebebasan dk = n-1, digunakan rumus:
BAB IV
HASIL DAN PEMBAHASAN
4.1 Hasil Penentuan Panjang Gelombang Serapan Maksimum Kalium Diklofenak
Penentuan kadar dilakukan dengan mengukur absorban pada panjang
gelombang maksimum (puncak kurva), agar dapat memberikan absorban tertinggi
pada setiap konsentrasi. Untuk memilih panjang gelombang maksimum dilakukan
dengan membuat kurva hubungan antara absorbansi dengan panjang gelombang
dari suatu larutan baku pada setiap konsentrasi tertentu, karena disekitar panjang
gelombang maksimum, bentuk kurva absorbansi datar dan pada kondisi tersebut
hukum Lambert-Beer terpenuhi. Bila suatu senyawa mempunyai lebih dari satu
puncak absorpsi maksimum, lebih diutamakan panjang gelombang absorpsi
maksimum yang absorptivitasnya terbesar dan memberikan kurva kalibrasi linier
dalam rentang konsentrasi yang relatif besar ( Gandjar dan Rohman, 2007;
Satiadarma, dkk., 2004).
Pada penentuan panjang gelombang serapan maksimum kalium diklofenak
dilakukan dengan mengukur absorbansi dari larutan baku dengan konsentrasi
lebih kurang 12 µg/ml pada rentang panjang gelombang 200-400 nm dengan
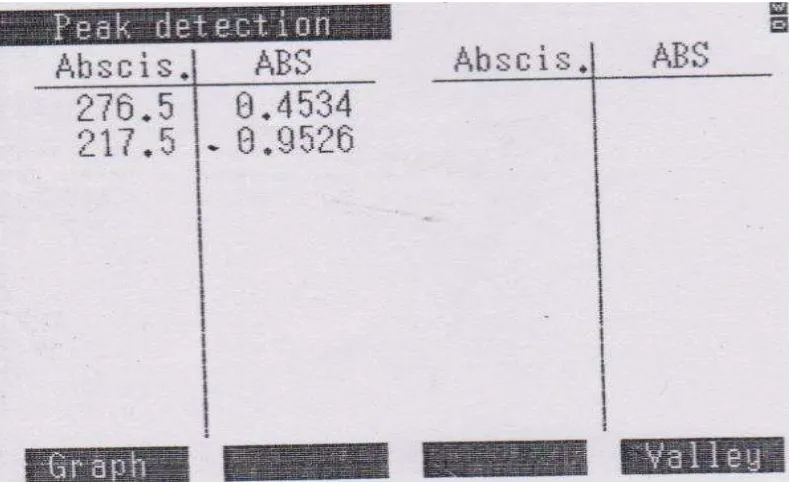
menggunakan Spektrofotometri Ultraviolet. Dari Pengukuran dilakukan dalam
pelarut KOH 0,2 N diperoleh serapan 0,4534 dengan panjang gelombang serapan
maksimum pada = 276,5 nm.
Berdasarkan The United States Pharmacopoeia (2013), kalium diklofenak
mempunyai spektrum panjang gelombang serapan maksimum 276 nm dalam
dalam batas-batas yang diterima menurut Farmakope Indonesia edisi IV. Kurva
panjang gelombang serapan maksimum dapat dilihat pada Gambar 4.1 dan Tabel
4.1 berikut ini.
Gambar 4.1 Kurva Serapan Kalium Diklofenak (konsentrasi 12 µg/ml) dalam pelarut KOH 0,2 N.
Gambar 4.2 Kurva Serapan Etil Diklofenak (konsentrasi 12 µg/ml) dalam pelarut KOH 0,2 N.
4.2 Hasil Pembuatan dan Penentuan Linieritas Kurva Kalibrasi Kalium Diklofenak
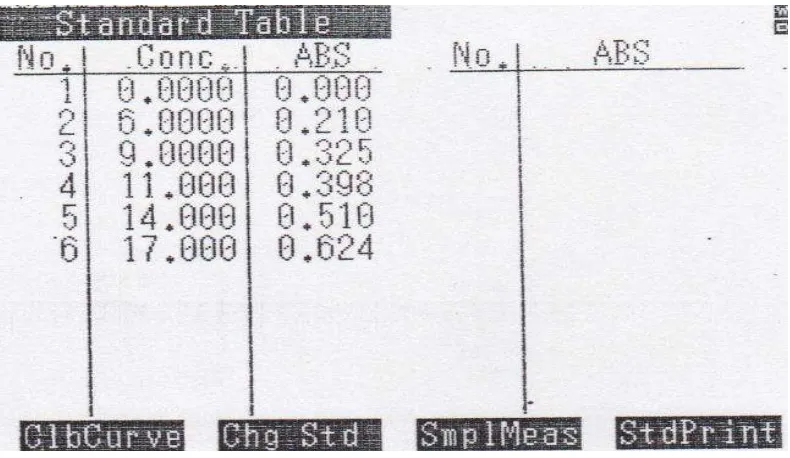
Pada Penentuan Kurva Kalibrasi Kalium Diklofenak dilakukan dalam
pelarut KOH 0,2 N dengan konsentrasi 6, 9, 11, 14 dan 17 µg/ml pada panjang
gelombang 276,5 nm dengan menggunakan KOH 0,2 N sebagai blanko. hasil
dapat dilihat pada Tabel 4.3 dan Gambar 4.3 berikut ini.
Gambar 4.3 Kurva Kalibrasi Kalium Diklofenak dalam pelarut KOH 0,2 N pada panjang gelombang 276,5 nm.
Hasil pembuatan kurva kalibrasi dalam pelarut KOH 0,2 N diperoleh
hubungan yang linier antara serapan dan konsentrasi dengan koefisien korelasi
(r) = 0,9998 dan persamaaan regresi Y= 0,0367 X- 0,0041.
Koefisien korelasi yang diperoleh ini memenuhi kriteria persamaan untuk
korelasi adalah r ≥ 0,λ5 (Shargel, 1λ85).
(Perhitungan dapat dilihat pada Lampiran 2, halaman 20)
4.3 Hasil Penentuan Kadar Etil Diklofenak Hasil Sintesis
Hasil penentuan kadar hasil sintesis etil diklofenak dalam pelarut
KOH 0,2 N yaitu 97,52 % ± 3,461, Sedangkan hasil penentuan kadar kalium
diklofenak pada sediaan tablet Cataflam yaitu 103,43 % ± 0,444.
Hasil ini menunjukkan bahwa proses sintesis etil diklofenak dapat
dikatakan cukup baik dengan membandingkan pada kadar sediaan kalium
diklofenak yang ada dipasaran yang memenuhi persyaratan yang tertera pada USP
36 (2013) yaitu tidak kurang dari 90% dan tidak lebih dari 110 % dari jumlah
yang tertera pada etiket (Perhitungan dapat dilihat pada Lampiran 6 dan 7,
halaman 24-27).
4.4 Hasil Uji Validasi Metode Spektrofotometri Ultraviolet
Uji Validasi metoda analisis merupakan suatu tindakan penilaian terhadap
parameter tertentu, berdasarkan percobaan laboratorium, untuk membuktikan
bahwa parameter tersebut memenuhi persyaratan untuk penggunaannya (Harmita,
Pada penelitian ini dilakukan Uji Validasi dengan penambahan bahan baku
(Standard Addition Method) terhadap sampel hasil sintesis etil diklofenak dalam
pelarut KOH 0,2 N yang meliputi Uji Akurasi dengan parameter persen perolehan
kembali (% recovery), Uji Presisi dengan parameter RSD (Relatif standard
Deviasi), batas deteksi (LOD) dan batas kuantitas (LOQ)
Uji akurasi dengan parameter persen perolehan kembali dilakukan dengan
membuat 3 konsentrasi analit dengan rentang spesifik 80%, 100% dan 120%,
masing-masing dengan 3 replikasi dan setiap rentang spesifik mengandung 70%
analit dan 30% baku pembanding (Perhitungan dapat dilihat pada Lampiran 8,
halaman 28).
Berikut tabel data hasil pengujian perolehan kembali Etil Diklofenak
dengan metode penambahan baku (Standard Addition Method).
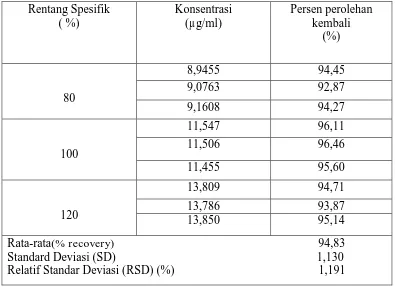
Tabel 4. Data Hasil Pengujian Perolehan Kembali Etil Diklofenak Dengan Metode Penambahan Baku (Standard Addition Method)
Hasil di atas diperoleh kadar rata-rata persen Recovery, yaitu 94,83%
dengan Standard Deviasi (SD) sebesar 1,130, Hasil Persen perolehan kembali ini
memenuhi persyaratan uji akurasi dimana rentang rata-rata hasil persen perolehan
kembali adalah 80-100%. Sedangkan dari hasil uji presisi dengan parameter
Relative Standard Deviation (RSD) adalah 1,191%. Hasil Relative Standard
Deviation (RSD) ini memenuhi persyaratan presisi, dimana nilai RSD yang
diizinkan adalah 2% (Harmita 2004).
Hasil penelitian disimpulkan bahwa penetapan kadar Etil Diklofenak
secara Spektrofotometri Ultraviolet memberikan batas deteksi (LOD) sebesar
0,317µg/ml dan batas kuantitas (LOQ) sebesar 1,057 µg/ml (Perhitungan dapat
BAB V
KESIMPULAN DAN SARAN
5.1 Kesimpulan
Berdasarkan penelitian yang dilakukan, maka dapat diambil kesimpulan:
1. Pada Penetapan Kadar Etil Diklofenak secara Spektrofotometri Ultraviolet
dalam pelarut KOH 0,2 N menunjukkan bahwa kadar hasil sintesis etil
diklofenak yang dianalisis yaitu 97,52% ± 3,461. Kadar sediaan kalium
diklofenak pada tablet Cataflam yang dianalisis yaitu 103,43% ± 0,444.
Hasil ini menunjukkan bahwa proses sintesis etil diklofenak dikatakan
cukup baik dengan membandingkan pada kadar sediaan kalium
diklofenak yang ada di pasaran memenuhi persyaratan kadar tablet
menurut USP 36 (2013) yaitu tidak kurang dari 90% dan tidak lebih dari
110% dari jumlah yang tertera pada etiket.
2. Hasil penelitian menunjukkan bahwa validasi metode Spektrofotometri
Ultraviolet yang digunakan memenuhi persyaratan uji dengan Parameter
Akurasi (% recovery) sebesar 94,83%, Presisi sebesar 1,191%, Batas
Deteksi (LOD) sebesar 0,317 µg/ml, Batas Kuantitas (LOQ) sebesar
1,057µg/ml.
5.2 Saran
Disarankan kepada peneliti selanjutnya untuk menentukan kadar hasil sintesis
etil diklofenak dengan menggunakan metode KCKT dan melakukan uji
DAFTAR PUSTAKA
Aiache, J.M., Devissaguet, J., dan Hermann, A.M.G. (1982). Galenica 2 – Biopharmacie. Edisi kedua. Penerjemah: Widji Soeratri dan Nanizar Zaman Joenoes. (1993) Farmasetika 2 Biofarmasi. Surabaya: Airlangga University Press. Halaman 165.
Anonim. (2009). British Pharmacopoeia 2009. London: The Stationery Office. Halaman 1889-1892.
Cairns, D. (2004). Essentials of Pharmaceutical Chemisty. Edisi kedua. Penerjemah: Rini Maya Puspita. (2004). Intisari Kimia Farmasi. Jakarta: Penerbit Buku Kedokteran EGC. Halaman 150-153.
Dachriyanus. (2004). Analisis Struktur Senyawa Organik Secara
Spektrofotometri. Cetakan pertama. Padang: CV. Trianda Anugrah
Pratama. Halaman: 1-6.
Dannhardt, G., dan Sorbera, L. (2014). Diclofenac Ethyl Ester. http://www.scbt.com/data sheet-207560-diclofenac-ethyl-ester.html. (5 juni 2014).
Day, R.A., dan Underwood, A.L. (1986). Quantitative Analysis. Edisi kelima. . Penerjemah: Aloysius Hadyana Pudjaatmaka. (2005). Analisis Kimia Kuantitatif. Jakarta: Penerbit Erlangga. Halaman: 393, 398-401.
Ditjen POM RI. (1979). Farmakope Indonesia. Edisi ketiga. Jakarta: Departemen Kesehatan Republik Indonesia. Jakarta. Halaman 748.
Ditjen POM RI. (1995). Farmakope Indonesia. Edisi keempat. Departemen Kesehatan RI. Jakarta. Halaman: 1061.
Gandjar, I.G., dan Rohman, A. (2007). Kimia Farmasi Analisis. Cetakan pertama. Yogyakarta: Pustaka Pelajar. Halaman 30-31, 240-241, 254, 446-468.
Gandjar, I.G., dan Rohman, A. (2012). Analisis Obat Secara Spektrofotometri Dan Kromatografi. Cetakan kesepuluh. Yogyakarta: Pustaka Pelajar. Halaman: 80-83.
Harmita. (2004). Petunjuk Pelaksanaan Validasi Metode dan Cara Perhitungannya. Majalah Ilmu Kefarmasian. I (3): 117-128, 130
Khopkar, S.M. (2007). Basic Concepts of Analytical Chemistry. Penerjemah; A. Saptoraharjo. (1990). Konsep Dasar Kimia Analitik. Cetakan Pertama. Jakarta: UI Press. Halaman 201-220.
Kice, John L dan Marvell, Elliot N (1965). Modern Principles of Organic Chemistry. Edisi kedua. New York: Collier Macmillan Internotional. Halaman 388-389.
Moffat, A.C., Osselton, M.D., dan Widdop, B. (2004). Clarke’s Analysis of
Drugs and Poisons. Edisi ke-4. London: Pharmaceutical Press. Halaman:
1238.
Roberts, L.J., dan Morrow, J.D. (2001). Senyawa Analgesik-Antipiretik dan Antiradang serta Obat-Obat yang digunakan dalam Penanganan Pirai. Dalam buku: Goodman & Gilman’s Dasar Farmakologi Terapi. Edisi kedua. Volume 2. Penerjemah: Tim alih bahasa Sekolah Farmasi ITB. (2012) Jakarta: Penerbit Buku Kedokteran EGC. Halaman 666, 689.
Satiadarma, K., Mulja, M., dan Tjahjono, D.H. (2004). Azas Pengembangan Prosedur Analisis. Edisi Pertama. Surabaya: Airlangga University Press. Halaman 47, 87-91, 94.
Shargel, L. (1985). Applied Biopharmaceutics and Pharmacokinetics. Edisi kedua. Penerjemah: Fasich dan Siti Sjamsiah. (1998). Biofarmasetika Dan Farmakokinetika Terapan. Surabaya: Penerbit Unversitas Airlangga. Halaman 16.
Siswandono., dan Soekardjo, B.H. (2000). Kimia Medisinal. Edisi Kedua. Surabaya: Airlangga University Press. Halaman 291, 301-302.
Suryawhanshi, S.B., Osman, A.O., Shaikh, Y.I., dan Nazeruddin, G.M. (2013). Synthesis of Various Esters of Diclofenac (NSAIDs) as Pro-Drugs and Their Biological Evaluation. Chemical Science Transactions. 3(2): 562-565.
Tan, H.T., dan Rahardja, K. (2008). Obat-Obat Penting. Edisi keenam. Jakarta: PT Elex Media Komputindo. Halaman 332.
The United States Pharmacopoeia. (2013). Kalium Diklofenak. II (36): 3219.
Lampiran 1. Perhitungan Konsentrasi Pengukuran
Diketahui: Nilai Absorptivitas spesifik (A11= 351b) = 276 nm
Tebal sel (b) = 1 cm
A = A11 x b x c
c =
c =
c = 0,001237 g/100ml
c = 12,37 µg/ml
Lampiran 2. Tabel Perhitungan Persamaan Regresi Kalium Diklofenak dalam
Lampiran 3. Contoh Perhitungan Penimbangan Sampel (Etil Diklofenak)
Berat Molekul Sampel (etil diklofenak) = 324,20
Berat molekul baku pembanding (kalium diklofenak) = 334,24
Jadi, berat penimbangan sampel adalah 24,25 mg.
Sampel yang ditimbang dimasukkan kedalam labu tentukur 25 ml, lalu
ditambahkan etanol hingga larut, kemudian ditambahkan KOH 0,2 N dan
dicukupkan hingga garis tanda, dikocok homogen. (Konsentrasi larutan uji
= 969,96 µg/ml). Kemudian dipipet 2,5 ml dari larutan uji, dimasukkan kedalam
labu tentukur 25 ml, dilarutkan dengan pelarut KOH 0,2 N dan dicukupkan
dengan KOH 0,2 N sampai garis tanda dan dikocok sampai homogen.
Kadar larutan uji =
x 969,96 µg/ml = 96,969 ml.
Lalu dipipet lagi 3 ml dari larutan uji, dimasukkan kedalam labu tentukur 25 ml
dan dilarutkan dengan KOH 0,2 N, dicukupkan dengan KOH 0,2 N sampai garis
tanda dan dikocok homogen.
Kadar larutan uji =
Lampiran 4. Contoh Perhitungan Penimbangan Sampel (Tablet Cataflam)
Berat 20 tablet = 6331,2 mg
Kandungan kalium diklofenak pada etiket = 50 mg
Dibuat larutan uji dengan kadar lebih kurang 12 µg /ml.
Ditimbang serbuk seksama serbuk setara dengan 50 mg kalium diklofenak, maka
berat sampel yang ditimbang adalah:
0,2 N dan dicukupkan hingga garis tanda, dikocok homogen lalu disaring, 10 ml
filtrat pertama dibuang (Konsentrasi larutan uji = 1000 µg/ml).
Setelah disaring, kemudian filtrat larutan uji dipipet 5 ml, lalu dimasukkan ke
dalam labu tentukur 50 ml dan dicukupkan dengan pelarut KOH 0,2 N sampai
garis tanda dan dikocok homogen.
Kadar larutan uji =
x 1000 µg/ml = 100 µg/ml.
Lalu dipipet lagi 3 ml dari larutan uji, dimasukkan kedalam labu tentukur 25 ml,
kemudian dicukupkan dengan KOH 0,2 N sampai garis tanda dan dikocok
homogen.
Kadar larutan uji =
Lampiran 6. Tabel Perhitungan Statistik Kadar Hasil Sintetis Etil Diklofenak
distribusi t diperoleh nilai t tabel = 4,03
karena thitung ttabel maka data diterima, maka kadar sebenarnya terletak antara:
µ = ̅% ± t(1-1/2α)dk x
√ %
= 97,52% ± (4,03 x 2,10348/ √ ) %
Lampiran 7. Tabel Perhitungan Statistik Kadar Kalium Diklofenak pada Tablet
distribusi t diperoleh nilai t tabel = 4,03
karena thitung ttabel maka data diterima, maka kadar sebenarnya terletak antara:
µ = ̅% ± t(1-1/2α)dk x
√ %
= 103,428% ± (4,03 x 0,26987/ √ ) %
Lampiran 8. Contoh Perhitungan Persentase Perolehan Kembali (% recovery)
Berat Molekul Sampel (etil diklofenak) = 324,20
Berat molekul baku pembanding (kalium diklofenak) = 334,24
Jadi, Berat kesetaraan penimbangan sampel pada penetapan kadar = 24,25 mg.
Perolehan 80%
Sampel yang ditimbang = 13,60 mg
Bahan baku 30% (PT. Dexa Medica)
x 19,4
x 99,8% = 5,98 mg
Perolehan 100%
Sampel yang ditimbang = 16,99 mg
Bahan baku 30% (PT. Dexa Medica)
x 24,25
x 99,8% = 7,485 mg
Baku yang ditimbang = 7,5 mg
Perolehan 120%
Bahan baku 30% (PT. Dexa Medica)
x 29,1
x 99,8% = 8,98 mg
Lampiran 9. Contoh Perhitungan Penimbangan Analit pada Persen Perolehan
Sampel yang ditimbang = 13,60 mg
Sampel yang ditimbang dimasukkan kedalam labu tentukur 25 ml, lalu
ditambahkan etanol hingga larut, kemudian ditambahkan KOH 0,2 N dan
dicukupkan hingga garis tanda dikocok homogen.
Kadar larutan uji =
= 544 µg/ml.
Kemudian dipipet 2,5 ml dari larutan uji, dimasukkan kedalam labu tentukur 25
ml, dilarutkan dengan pelarut KOH 0,2 N dan dicukupkan dengan KOH 0,2 N
sampai garis tanda dan dikocok sampai homogen.
Kadar larutan uji =
x 544 µg/ml = 54,4 µg/ml.
Lalu dipipet lagi 3 ml dari larutan uji, dimasukkan kedalam labu tentukur 25 ml
dan dilarutkan dengan KOH 0,2 N, dicukupkan dengan KOH 0,2 N sampai garis
tanda dan dikocok homogen.
Kadar larutan uji =
Lampiran 10. Contoh Perhitungan Penimbangan Bahan Baku pada Persen Perolehan Kembali
Perolehan 80%
Bahan baku 30% (PT. Dexa Medica)
x 19,4
x 99,8% = 5,98 mg
Baku yang ditimbang = 6,1 mg
Baku yang ditimbang dimasukkan kedalam labu tentukur 25 ml, lalu ditambahkan
etanol hingga larut, kemudian ditambahkan KOH 0,2 N dan dicukupkan hingga
garis tanda dikocok homogen.
Kadar larutan uji =
= 244 µg/ml.
Kemudian dipipet 2,5 ml dari larutan uji, dimasukkan kedalam labu tentukur 25
ml, dilarutkan dengan pelarut KOH 0,2 N dan dicukupkan dengan KOH 0,2 N
sampai garis tanda dan dikocok sampai homogen.
Kadar larutan uji =
x 24,4 µg/ml = 24,4 µg/ml.
Lalu dipipet lagi 3 ml dari larutan uji, dimasukkan kedalam labu tentukur 25 ml
dan dilarutkan dengan KOH 0,2 N, dicukupkan dengan KOH 0,2 N sampai garis
tanda dan dikocok homogen.
Kadar larutan uji =
Lampiran 11. Contoh Perhitungan Persen Perolehan Kembali dengan Metode Penambahan Bahan Baku (Standard Addition Method) dari sampel etil diklofenak.
% Recovery = X 100%
Dimana:
A = Konsentrasi sampel yang diperoleh setelah penambahan bahan baku
B = Konsentrasi sampel sebelum penambahan bahan baku
C = Konsentrasi baku yang ditambahkan
% Recovery etil diklofenak =
Lampiran 12. Tabel Data hasil persen perolehan kembali Etil Diklofenak dengan Metode penambahan baku (Standard Addition Method).
Lampiran 13. Tabel Contoh Perhitungan Batas Deteksi (LOD) dan Batas Kuantitasi (LOQ)
Persamaan garis regresi adalah Y= 0,0367 X – 0,0041
Lampiran 14. Tabel Data uji perolehan kembali (% Recovery)
1. Rentang 80%
Sebelum penambahan baku
Lampiran 15. Tabel Data uji perolehan kembali (% Recovery)
1. Rentang 100%
Sebelum penambahan baku
Lampiran 16. Tabel Data uji perolehan kembali (% Recovery)
1. Rentang 120%
Sebelum penambahan baku
Setelah penambahan baku
Lampiran 17. Data kadar Etil Diklofenak dan Tablet Cataflam dalam pelarut KOH 0,2 N
1. Data kadar etil diklofenak
Lampiran 19. Hasil Sintesis Etil Diklofenak dan Tablet Cataflam
Cataflam® (PT. Novartis Indonesia) No. Batch : ID4094
No. Reg : DKL 9930408316B1 Expire Date : Oktober 2017