PENGARUH KONSENTRASI STARTER Saccharomyces cereviceae
DAN WAKTU FERMENTASI TERHADAP HASIL DAN MUTU
MINYAK KELAPA VIRGIN COCONUT OIL
T E S I S
OLEH
ROMMEL DOLOKSARIBU
077030020
PROGRAM MAGISTER BIOLOGI
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
UNIVERSITAS SUMATERA UTARA
MEDAN
2010
PENGARUH KONSENTRASI STARTER Saccharomyces cereviceae
DAN WAKTU FERMENTASI TERHADAP HASIL DAN MUTU
MINYAK KELAPA VIRGIN COCONUT OIL
T E S I S
Diajukan sebagai salah satu syarat untuk memperoleh gelar Magister Sains dalam Program Studi Biologi
Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Sumatera Utara
OLEH
ROMMEL DOLOKSARIBU
077030020
PROGRAM MAGISTER BIOLOGI
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
UNIVERSITAS SUMATERA UTARA
Judul Penelitian : PENGARUH KONSENTRASI STARTER Saccharomyces
cereviceae DAN WAKTU FERMENTASI TERHADAP
HASIL DAN MUTU MINYAK KELAPA VIRGIN COCONUT
OIL
Nama : ROMMEL DOLOKSARIBU
NIM : 077030020
Program Studi : BIOLOGI
Menyetujui : Komisi Pembimbing
Dr. Ir. Herla Rusmarilin, M.Sc Prof. Dr. Dwi Suryanto, M.Sc
Ketua Anggota
Ketua Program Studi Dekan
Prof. Dr. Dwi Suryanto, M.Sc Dr. Sutarman, M.Sc
Ketua Program Studi Biologi Direktur SPs USU
Tanggal Lulus : 02 September 2010 Prof. Dr. Ir. T. Chairun Nisa, B. M.Sc
Telah diuji pada
Tanggal : 02 September 2010
PANITIA PENGUJI TESIS
PERNYATAAN
PENGARUH KONSENTRASI STARTER Saccharomyces cereviceae DAN WAKTU FERMENTASI TERHADAP HASIL DAN MUTU
MINYAK KELAPA VIRGIN COCONUT OIL
TESIS
Dengan ini saya menyatakan bahwa dalam tesis ini tidak terdapat karya yang pernah diajukan untuk memperoleh gelar kesarjanaan di suatu perguruan tinggi dan sepanjang pengetahuan saya juga tidak terdapat karya atau pendapat yang pernah ditulis atau diterbitkan oleh orang lain kecuali secara tertulis diacu dalam naskah ini dan disebutkan dalam daftar pustaka.
Medan, September 2010 Penulis
Rommel Doloksaribu
ABSTRAK
Penelitian ini bertujuan untuk memperoleh konsentrasi S. cereviceae dan lama fermentasi yang optimum dalam fermentasi minyak kelapa VCO. Variasi konsentrasi starter S. cereviceae adalah 0% (sebagai kontrol), 5, 10, 15, 20% (V/V) dengan lama fermentasi 12 jam, 24 jam, 36 jam, 48 jam. Metode penelitian ini menggunakan rancangan faktorial dengan Pola Rancangan Acak Lengkap (RAL). Parameter yang dianalisis adalah rendemen minyak, kadar air, asam lemak bebas, asam laurat, bilangan peroksida.
Hasil analisis sidik ragam menunjukkan bahwa konsentrasi starter S. cereviceae memberikan pengaruh yang berbeda nyata terhadap rendemen minyak,
pengaruh sangat nyata terhadap asam lemak bebas, kadar asam laurat, bilangan peroksida dan tidak berbeda nyata terhadap kadar air. Interaksi antara konsentrasi starter S. cereviceae dan lama fermentasi memberikan pengaruh sangat nyata terhadap asam lemak bebas, pengaruh yang tidak nyata terhadap rendemen minyak, kadar air, kadar asam laurat dan pengaruh nyata terhadap bilangan peroksida. Konsentrasi starter S. cereviceae 15% dan lama fermentasi 24 jam menghasilkan minyak kelapa murni yang lebih baik.
ABSTRACT
The purpose of this research was to obtain the concentration of S. cereviceae and the duration of the optimum fermentation in the fermentation of
VCO coconut oil. The research had been performed using factorial completely rendomized design with two factors i.e : starter consentration of S. cereviceae (C) : 0,5, 10, 15, 20% and fermentation time (T) : 12,24,36,48 hours. Parameter analyzed were rendemen of oil, moisture content, free fatty acid content, lauric acid, peroxide value.
The results showed that S. cereviceae starter concentration had significant effect on rendemen, highly significant on free fatty acid content, lauric acid content, peroxide value and not significant effect on moisture content. The interaction of S. cereviceae starter concentration and fermentation time had significant effect on peroxide value and had highly significant effect on free fatty acid content, not significant effect on rendemen, moisture content, lauric acid content and significant effect on peroxide value. The results obtained from each parameter show that the highest results of combination C3T2 from each 100 cc milk coconut oil. The 15% S. cereviceae starter concentration and 24 hours fermentation time gave the best and more acceptable quality of Virgin Coconut Oil.
Key word : S. cereviceae, Virgin Coconut Oil, Fermentation, Rendemen, Moisture Content, Free Fatty Acid Content, Lauric Acid, Peroxide Value.
PENGHARGAAN
Puji dan syukur Penulis panjatkan kehadirat Tuhan Yang Maha Esa atas
berkat dan kasih karuniaNya sehingga Penulis dapat menyelesaikan tesis dengan
judul “PENGARUH KONSENTRASI STARTER Saccharomyces cereviceae
DAN WAKTU FERMENTASI TERHADAP HASIL DAN MUTU MINYAK KELAPA VIRGIN COCONUT OIL”.
Tesis ini dibuat sebagai salah satu syarat untuk menyelesaikan studi Program
Studi Magister Biologi Sekolah Pascasarjana Universitas Sumatera Utara Medan.
Dengan selesainya penulisan tesis ini, penulis ingin menyampaikan terimakasih yang
sebesar-besarnya kepada:
1. Direktur Program Pacasarjana USU, Prof. Dr. Ir. T.Chairun Nisa B, M.Sc. atas
kesempatan yang diberikan kepada saya menjadi mahasiswa pada Program
Pascasarjana USU.
2. Ibu Dr. Ir. Herla Rusmarilin, M.Sc selaku pembimbing utama, yang dengan tulus
dan penuh perhatian membimbing penulis sehingga penelitian dan penulisan tesis
ini dapat terselesaikan.
3. Prof. Dr. Dwi Suryanto, M.Sc. sebagai Ketua Program Studi Magister Biologi
Sekolah Pascasarjana Universitas Sumatera Utara, sekaligus sebagai pembimbing
penulis yang telah memberikan bimbingan dan arahan sehingga penelitian dan
4. Prof. Dr. Erman Munir, M.Sc sebagai Penguji, yang telah memberikan masukan
dalam penulisan tesis ini.
5. Dr. Ir. Edy Batara, M.Sc selaku penguji yang telah banyak memberikan masukan
dan arahan selama proses penulisan tesis ini.
6. Seluruh Dosen dan Staf Pengajar di Sekolah Pascasarjana Program Studi Biologi
Universitas Sumatera Utara Medan yang telah membekali Penulis dengan
berbagai disiplin ilmu.
7. Gubernur Provinsi Sumatera Utara dan Ketua Bapeda Sumatera Utara yang telah
memberikan Beasiswa S-2 kepada penulis sehingga penulis dapat menyelesaikan
Studi S-2 pada Program Pascasarjana USU.
8. Kepala SMA Negeri 21 Medan dan seluruh rekan staf pengajar dan pegawai yang
telah memberikan dukungan sepenuhnya kepada penulis selama mengikuti studi
pada Program Pascasarjana USU.
9. Kepada semua pihak yang telah membantu penulis selama penulisan tesis ini.
Kepada Istri terkasih Dra. Tetty Siagian dan Ananda terkasih Yonadab
Doloksaribu dan Yolanda Doloksaribu yang telah memberi dukungan sepenuhnya
dan pengertian yang dalam serta kesabaran selama penulis mengikuti studi sampai
terselesaikan, penulis mengucapkan terima kasih yang sedalam-dalamnya.
Medan, Juli 2009
Penulis
RIWAYAT HIDUP
Penulis dilahirkan di Pematang Siantar, pada tanggal 06 Agustus 1962,
sebagai anak ke-lima dari delapan bersaudara, dengan nama Ayah M. Doloksaribu
dan Ibu T. Br. Panggabean.
Memasuki sekolah dasar SD Taman Harapan Medan dan lulus tahun 1976,
melanjut ke SMP Advent 1 Medan lulus tahun 1980, kemudian lulus dari SMA
Negeri 11 Medan tahun 1983. Pada tahun 1983 penulis diterima sebagai mahasiswa
pada program Pendidikan Diploma 3 Jurusan Biologi FMIPA IKIP Medan, dan lulus
pada tahun 1986.
Penulis ditempatkan sebagai tenaga pendidik pada bulan Maret tahun 1987 di
SMA Negeri Pintu Padang Tapanuli Selatan. Pada tahun 1991, penulis pindah tugas
sebagai tenaga pendidik di SMA Negeri 5 Medan. Penulis melanjutkan studi pada
Universitas Negeri Medan, dan lulus tahun 1995. Pada tahun 2004 penulis pindah
tugas sebagai pengajar di SMA Negeri 21 Medan. Kemudian pada tahun 2007
mendapat kesempatan belajar pada Strata-2 Sekolah Pasca Sarjana USU Program
Studi Biologi Konsentrasi Mikrobiologi.
Medan, Juli 2009
DAFTAR ISI
Fermentasi dan Peranan Mikroorganisme ... 10
Kandungan Kimia Minyak Kelapa Murni atau Virgin Coconut Oil (VCO)... 12
Teknik Pengolahan Minyak Pemanasan ... 15
Teknik Pengolahan Minyak Tanpa Pemanasan ... 16
Kerusakan Minyak Kelapa ... 17
BAHAN DAN METODE PENELITIAN
Bahan Penelitian ... 19
Peralatan dan Bahan Kimia yang Digunakan ... 19
Tempat Penelitian ... 19
Metode Penelitian ... 19
Analisis Data ... 21
Pembuatan Santan Kelapa ... 21
Pembuatan Kultur Murni S. cereviceae ... 22
Pembuatan Starter ... 23
Pembuatan Minyak Kelapa ... 23
Penyaringan ... 24
Analisis Rendemen Minyak ... 24
Analisis Kadar Air ... 25
Analisis Kadar Asam Lemak Bebas... 25
Analisis Kadar Asam Laurat ... 25
Analisis Bilangan Peroksida ... 26
HASIL DAN PEMBAHASAN ... 27
KESIMPULAN DAN SARAN Kesimpulan ... 43
Saran ... 44
DAFTAR PUSTAKA ... 45
DAFTAR TABEL
Tabel Halaman
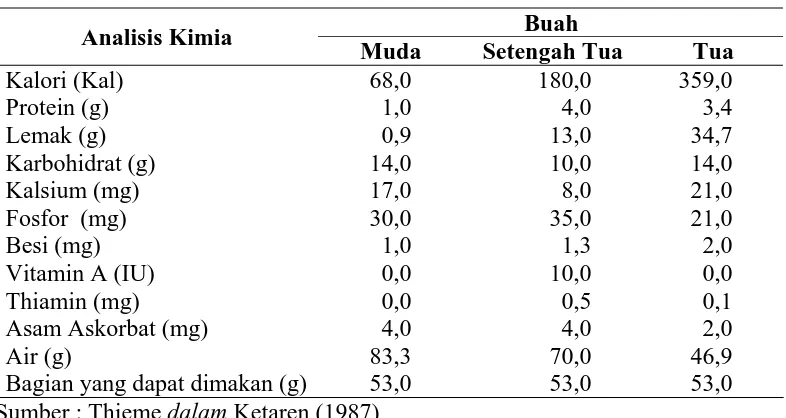
1 Komposisi Buah Kelapa... 5 2 Komposisi Kimia Daging Buah Kelapa pada Berbagai
Tingkat Kematangan ... 6 3 Komposisi Asam Lemak Minyak Kelapa ... 13 4. Pengaruh Konsentrasi Starter Saccharomyces
cereviceae Terhadap Rendemen Minyak (%) ... 29 5. Pengaruh Waktu Fermentasi (Jam) Terhadap
Rendemen Minyak (%) ... 31 6. Pengaruh Konsentrasi Starter Saccharomyces
cereviceae terhadap Kadar Air (%)... 33 7. Pengaruh Lama Fermentasi (Jam) terhadap
Kadar Air (%)... 34 8. Pengaruh Interaksi Konsentrasi Starter Saccharomyces
cereviceae dan Lama Fermentasi terhadap Asam Lemak Bebas (%) ... 35 9. Pengaruh Konsentrasi Starter S. cereviceae
terhadap Kadar Asam Laurat (%) ... 38 10. Pengaruh Lama Fermentasi terhadap Kadar Asam Laurat (%) ... 39 11. Pengaruh Interaksi Konsentrasi Starter
S. cereviceae dan Lama Fermentasi (Jam)
Terhadap Bilangan Peroksida (meq/kg) ... 40
DAFTAR GAMBAR
Gambar Halaman
1. Histogram hubungan antara konsentrasi starter
S. cereviceae terhadap rendemen minyak ... 29
2. Histogram hubungan lama fermentasi terhadap rendemen minyak ... 30
3. Histogram hubungan antara konsentrasi starter
S. cereviceae terhadap kadar air ... 32
4. Histogram hubungan antar lama fermentasi terhadap kadar air ... 33
5. Histogram pengaruh interaksi starter S. cereviceae
dan lama fermenasi terhadap asam lemak bebas ... 36
6. Histogram hubungan antara konsentrasi starter
S. cereviceae terhadap asam laurat ... 37
7. Histogram pengaruh lama fermentasi terhadap asam laurat ... 39
8. Histogram pengaruh interaksi antara konsentrasi starter
DAFTAR LAMPIRAN
Lampiran Halaman
1. Skema Penentuan Kultur S. cereviceae ... 47
2. Skema Pembuatan Starter S. cereviceae ... 48
3. Skema Pembuatan Minyak Kelapa ... 49
4. Data Pengamatan Rendemen Minyak (%) ... 50
5. Data Pengamatan Kadar Air (%) ... 51
6. Data Pengamatan Kadar Asam Lemak Bebas (%) ... 52
7. Data Pengamatan Kadar Asam Laurat (%) ... 53
8. Data Pengamatan Bilangan Peroksida ... 54
9. Proses Fermentasi Krim pada Setiap Perlakuan ... 55
10.Minyak Kelapa Murni Hasil Fermentasi pada Setiap Perlakuan ... 57
ABSTRAK
Penelitian ini bertujuan untuk memperoleh konsentrasi S. cereviceae dan lama fermentasi yang optimum dalam fermentasi minyak kelapa VCO. Variasi konsentrasi starter S. cereviceae adalah 0% (sebagai kontrol), 5, 10, 15, 20% (V/V) dengan lama fermentasi 12 jam, 24 jam, 36 jam, 48 jam. Metode penelitian ini menggunakan rancangan faktorial dengan Pola Rancangan Acak Lengkap (RAL). Parameter yang dianalisis adalah rendemen minyak, kadar air, asam lemak bebas, asam laurat, bilangan peroksida.
Hasil analisis sidik ragam menunjukkan bahwa konsentrasi starter S. cereviceae memberikan pengaruh yang berbeda nyata terhadap rendemen minyak,
pengaruh sangat nyata terhadap asam lemak bebas, kadar asam laurat, bilangan peroksida dan tidak berbeda nyata terhadap kadar air. Interaksi antara konsentrasi starter S. cereviceae dan lama fermentasi memberikan pengaruh sangat nyata terhadap asam lemak bebas, pengaruh yang tidak nyata terhadap rendemen minyak, kadar air, kadar asam laurat dan pengaruh nyata terhadap bilangan peroksida. Konsentrasi starter S. cereviceae 15% dan lama fermentasi 24 jam menghasilkan minyak kelapa murni yang lebih baik.
ABSTRACT
The purpose of this research was to obtain the concentration of S. cereviceae and the duration of the optimum fermentation in the fermentation of
VCO coconut oil. The research had been performed using factorial completely rendomized design with two factors i.e : starter consentration of S. cereviceae (C) : 0,5, 10, 15, 20% and fermentation time (T) : 12,24,36,48 hours. Parameter analyzed were rendemen of oil, moisture content, free fatty acid content, lauric acid, peroxide value.
The results showed that S. cereviceae starter concentration had significant effect on rendemen, highly significant on free fatty acid content, lauric acid content, peroxide value and not significant effect on moisture content. The interaction of S. cereviceae starter concentration and fermentation time had significant effect on peroxide value and had highly significant effect on free fatty acid content, not significant effect on rendemen, moisture content, lauric acid content and significant effect on peroxide value. The results obtained from each parameter show that the highest results of combination C3T2 from each 100 cc milk coconut oil. The 15% S. cereviceae starter concentration and 24 hours fermentation time gave the best and more acceptable quality of Virgin Coconut Oil.
Key word : S. cereviceae, Virgin Coconut Oil, Fermentation, Rendemen, Moisture Content, Free Fatty Acid Content, Lauric Acid, Peroxide Value.
PENDAHULUAN
Latar Belakang
Minyak kelapa sudah dikenal di Indonesia sejak lama. Penggunaan minyak
kelapa dalam kehidupan sehari-hari sangat luas seperti untuk minyak goreng/ bahan
makanan, obat-obatan, bahan pembuat sabun dan lain sebagainya. Ada beberapa cara
yang dikenal untuk membuat minyak kelapa yakni cara pressing, rendering, ekstraksi
dengan bahan pelarut atau gabungan dari cara tersebut (Hasbullah, 2001). Minyak
kelapa yang dihasilkan selama ini bermutu kurang baik, hal tersebut ditandai dengan
adanya kadar air dan asam lemak bebas yang cukup tinggi dalam minyak kelapa
dengan warna minyaknya agak kecoklatan dan mudah berbau tengik. Daya
simpannya tidak lama, sekitar 2 bulan saja.
Untuk melakukan perbaikan mutu minyak kelapa, Balai Penelitian Tanaman
Kelapa dan Palma Lain (BALITKA) Manado telah melakukan serangkaian pengujian
untuk memperbaiki teknik pengolahan minyak kelapa. Dari hasil pengujian diperoleh
minyak kelapa yang mutunya jauh lebih baik dari sebelumnya. Minyak kelapa yang
dihasilkan memiliki kadar air dan asam lemak bebas yang rendah, bewarna bening
dan berbau harum. Daya simpan minyak lama, dapat lebih dari satu tahun. Minyak itu
disebut sebagai virgin coconut oil atau minyak kelapa murni (Novrianto, 2005).
Banyak manfaat yang diperoleh dari minyak kelapa murni seperti obat
penyakit jantung dan kanker. Dengan mengkonsumsi minyak kelapa murni dapat
membantu mencegah infeksi virus, mendukung sistem kekebalan tubuh, menyediakan
sumber energi dengan cepat, menyediakan nutrisi penting untuk kesehatan,
memperbaiki sistem pencernaan dan penyerapan nutrisi, membantu kulit tetap lembut
dan halus, tidak menaikkan kolesterol darah dan tidak menyebabkan kegemukan.
Minyak kelapa murni juga dimanfaatkan dalam industri farmasi, kosmetika dan susu
formula. Pada saat ini, minyak kelapa murni digunakan untuk produk shampo,
detergen, minyak telon dan minyak rambut (Siswono, 2006)
Ada berbagai metode untuk memperoleh minyak kelapa murni. Salah satu
metode yang telah dikenal cara basah yang modern. Prinsip cara basah ini adalah
proses fermentasi yang didasarkan atas pengrusakan lapisan protein yang melindungi
emulsi minyak yang terdapat pada santan kelapa (Hasbullah, 2001) Salah satu bahan
yang dapat digunakan untuk proses fermentasi adalah S. cereviceae. Beberapa faktor
yang mempengaruhi produksi minyak kelapa secara fermentasi diantaranya lamanya
fermentasi, konsentrasi inokulum, suhu, bahan baku kelapa dan pH (Sukmadi dan
Nugroho, 2001).
Bertitik tolak dari uraian tersebut di atas, penulis ingin mengetahui bagaimana
cara fermentasi dengan S. cereviceae. Dalam penelitian ini dengan perbedaan
konsentrasi S. cereviceae dalam pembuatan starter dan perbedaan waktu fermentasi
diharapkan dapat diperoleh taraf perlakuan yang paling baik untuk pemecahan
sempurna emulsi minyak dalam santan kelapa sehingga dengan demikian dapat
diketahui apakah pengolahan minyak kelapa dengan cara fermentasi ini dapat
menghasilkan jumlah minyak kelapa dan kualitas yang lebih baik.
Perumusan Masalah
Minyak kelapa murni digunakan secara luas dalam kehidupan sehari-hari
sebagai minyak goreng, obat-obatan, bahan makanan, bahan pembuatan sabun dan
lain sebagainya. Minyak kelapa murni dapat juga digunakan untuk membantu
mencegah infeksi virus, melindungi sistem kekebalan tubuh, menyediakan sumber
energi dengan cepat, menyediakan nutrisi untuk kesehatan, memperbaiki sistem
pencernaan dan penyerapan nutrisi, membantu kulit tetap halus, tidak menaikkan
kolesterol darah dan tidak menyebabkan kegemukan. Di samping dapat
menyembuhkan penyakit, minyak kelapa murni juga dimanfaatkan dalam industri
farmasi, kosmetika dan susu formula.
Atas dasar tersebut pembuatan suatu produk minyak kelapa murni perlu
ditingkatkan melalui berbagai cara. Ada berbagai metode untuk memperoleh minyak
kelapa murni, salah satu adalah dengan fermentasi menggunakan starter S. cereviceae
yang dapat memproduksi enzim amilase. Selain itu waktu fermentasi harus
diperhatikan untuk mendapatkan produksi minyak kelapa murni yang optimum oleh
karena itu, perlu dilakukan penelitian mengenai apakah ada pengaruh konsentrasi
starter S. cereviceae dan waktu fermentasi dalam pengolahan kelapa untuk
menghasilkan minyak goreng secara fermentasi sehingga pemanfaatan kelapa untuk
Tujuan Penelitian
Penelitian ini bertujuan untuk mengetahui pengaruh perbedaan konsentrasi
starter S. cereviceae dan waktu fermentasi terhadap rendemen dan mutu minyak
kelapa yang diproses dengan cara fermentasi.
Hipotesis
a. Terdapat pengaruh konsentrasi starter 5 – 20% S. cereviceae terhadap jumlah
produksi dan mutu virgin coconut oil.
b. Lamanya fermentasi 12 – 48 jam memberikan produksi dan mutu virgin coconut
oil yang lebih tinggi.
c. Terdapat interaksi antara konsentrasi starter 5 – 20% S. cereviceae dengan
lamanya waktu fermentasi 12 – 48 jam terhadap parameter virgin coconut oil.
Kegunaan Penelitian
a. Sebagai bahan informasi bagi masyarakat untuk mendapatkan minyak kelapa
melalui fermentasi dalam pembuatan virgin coconut oil yang lebih efisien.
b. Untuk memperoleh data bagaimana konsentrasi starter S. cereviceae dan lamanya
waktu fermentasi yang optimal untuk memperoleh virgin coconut oil dalam
jumlah dan mutu yang maksimal.
TINJAUAN PUSTAKA
Tanaman kelapa (Cocos nucifera. L) merupakan tanaman yang sangat berguna
dalam kehidupan ekonomi pedesaan di Indonesia. Karena semua bagian dari pohon
kelapa dapat dimanfaatkan untuk memenuhi kebutuhan manusia. Salah satu bagian
kelapa yang mempunyai banyak manfaat adalah daging buah (Palungkung, 2004).
Berikut komposisi buah dapat dilihat pada Tabel 1.
Tabel 1. Komposisi Buah Kelapa
Kelapa segar mengandung 30-50% minyak, bila dikeringkan menjadi kopra
kadar lemaknya mencapai 63-65%. Kadar minyak sangat dipengaruhi oleh tingkat
ketuaan buah, semakin tua buah semakin tinggi kadar minyaknya. Buah kelapa yang
sudah tua atau matang umumnya dipanen pada umur 11–12 bulan (Rindengan et al.,
1995). Oleh karena itu buah kelapa yang sesuai untuk diolah menjadi minyak kelapa
murni harus berumur 12 bulan (Rindengan dan Riyanto, 2004). Komposisi kimia
daging buah kelapa ditentukan oleh umur buah kelapa pada berbagai tingkat
Tabel 2. Komposisi Kimia Daging Buah Kelapa pada Berbagai Tingkat Sumber : Thieme dalam Ketaren (1987)
Daging buah kelapa dapat diolah menjadi santan (juice extract) dengan air
atau tanpa penambahan air. Adapun komposisi dari santan adalah 66% air,
28% minyak dan 6% kandungan non minyak (Suhardiyono, 1988). Santan kelapa
merupakan sistem emulsi dalam air yang berwarna putih susu. Emulsi tersebut
distabilkan oleh stabilizer yang berupa campuran karbohidrat dan protein dalam
bentuk lapisan kuat.
Menurut Winarno (1984) sistem emulsi dapat mengalami pemecahan
sehingga membentuk dua lapisan yang tidak bercampur. Perusakan stabilizer
dilakukan oleh enzim yang dihasilkan S. cereviceae. Ekstraksi santan kelapa tanpa
menggunakan campuran air menghasilkan ampas yang beratnya sekitar 56% dari
berat daging kelapa semula dengan kandungan minyak sebesar 50% (Hagen Maier,
1977). Efisiensi ekstraksi akan meningkat dengan penambahan air sebelum
pemisahan dilakukan. Menurut Arih Surjadi dan Sumaatmadja (1975) pembuatan
santan dari perbandingan 1 : 3 (g/v) telah cukup untuk menghasilkan ampas dengan
kadar lemak 23,85% dan dari satu pembuatan santan satu bagian berat kelapa dengan
daging kelapa segar mengandung kadar lemak 64,02%.
Minyak Kelapa
Minyak kelapa merupakan bagian paling berharga dari buah kelapa.
Kandungan minyak pada daging buah kelapa tua sebanyak 34,7%. Minyak kelapa
digunakan sebagai bahan baku industri atau sebagai minyak goreng. Minyak kelapa
dapat diekstrak dari daging kelapa segar atau diekstrak dari daging kelapa yang telah
dikeringkan atau yang biasa disebut kopra (Tarwiyah, 2001).
Pengolahan minyak kelapa dilakukan dengan cara kering dan basah. Cara
kering dilakukan dengan pengepresan kopra. Cara kering dilakukan di pabrik
pengolahan minyak kelapa karena memerlukan investasi yang cukup besar untuk
pembelian alat dan mesin-mesin. Cara basah dilakukan dengan cara membuat santan
dari daging kelapa dan dipanaskan untuk memisahkan minyak dari bagian yang
mengemulsinya. Cara lain untuk mendapatkan minyak kelapa secara basah adalah
secara fermentasi (Hasbullah, 2001).
Fermentasi dilakukan dengan menggunakan mikroorganisme sebagai
inokulum seperti bakteri dan khamir. Pembuatan minyak kelapa secara fermentasi ini
dapat dilakukan dengan skala besar maupun rumah tangga. Cara fermentasi memiliki
tidak terlalu tinggi. Minyak kelapa yang dihasilkan lebih banyak dan warnanya lebih
jernih (Sukmadi dan Nugroho, 2003).
Untuk mendapatkan minyak kelapa secara fermentasi dapat juga dilakukan
dengan enzim papain. Enzim ini merupakan enzim proteolitik yang diperoleh dari
getah pepaya yang dapat mengkatalisis reaksi pemecahan, reaksi peptida pada protein
dengan mengkatalisis ikatan peptidanya menghasilkan senyawa yang lebih sederhana
(Purnomo, 2006).
Minyak kelapa berdasarkan kandungan asam lemak digolongkan ke dalam
minyak asam laurat karena kandungan asam lauratnya paling tinggi jika dibandingkan
dengan asam lemak lainnya. Berdasarkan tingkat ketidak jenuhannya yang
dinyatakan dengan bilangan iod (iodine value), minyak kelapa dapat dimasukkan ke
dalam golongan non drying oils karena bilangan iod minyak tersebut berkisar antara
7,5-10,5 (Djatmiko dan Widjaya, 1973).
Minyak kelapa secara fisik berwujud cairan yang berwarna bening sampai
kuning kecokelatan dan memiliki karakteristik bau yang khas. Zat warna yang
termasuk golongan ini terdapat secara alamiah dalam bahan yang banyak
mengandung minyak dan ikut terekstrak bersama minyak dalam proses ekstraksi.
Warna pada minyak kelapa disebabkan oleh zat warna dan kotoran-kotoran lainnya.
Zat warna alamiah yang terdapat pada minyak kelapa adalah betakaroten yang
merupakan hidrokarbon tidak jenuh dan tidak stabil pada suhu tinggi. Proses
pengolahan minyak kelapa dengan udara panas menyebabkan warna kuning berubah
akibat karoten mengalami degradasi (Suhardijono dan Syamsiah, 1987).
Kualitas minyak kelapa sangat tergantung pada stabilitas penyimpanan,
pemasakan, karakteristik penggorengan, serta perangkat fisik dan nutrisinya.
Hidrolisis yang terjadi dapat mengakibatkan rasa yang tidak diinginkan. Selama
penggorengan terdapat lebih sedikit asam lemak teroksidasi, sehingga makanan tidak
terasa lengket di lidah karena titik leleh minyak berada di bawah suhu tubuh.
Kerugian penggunaan minyak kelapa untuk tujuan memasak dan menggoreng
diantaranya tingginya penyerapan minyak oleh makanan (Ketaren, 1987).
Sifat Fisika Kimia Minyak Kelapa
Sifat fisika kimia minyak kelapa sangat diperlukan dalam perancangan proses,
pengembangan proses, pengembangan produk, dan penanganan sistem
penyimpanannya. Sifat fisika kimia biasanya berada dalam suatu kisaran nilai. Oleh
karena perbedaannya cukup kecil, nilai tersebut dinamakan konstanta. Konstanta fisik
minyak kelapa yang dianggap cukup penting adalah berat jenis, indeks bias, dan titik
cair. Konstanta kimia yang penting lainnya adalah bilangan iod, bilangan
penyabunan, bilangan Reichert Meissel, bilangan Polenske, bilangan asam, dan angka
tak tersabunkan (Syah, 2005).
Minyak kelapa memiliki titik cair dan bilangan penyabunan yang lebih tinggi
serta bilangan iod yang lebih rendah dibandingkan minyak nabati lainnya. Titik cair
minyak ditentukan oleh beberapa faktor sebagai berikut :
1. Kandungan lemak, semakin pendek rantai karbon asam lemak penyusun
2. Semakin banyak ikatan ganda pada asam lemak, semakin rendah titik cair
minyaknya (Ketaren, 2005).
Fermentasi dan Peranan Mikroorganisme
Fermentasi adalah reaksi disimilasi anaerobik senyawa-senyawa organik yang
disebabkan oleh aktivitas mikroorganisme atau ekstrak dari sel-sel tersebut. Oleh
karena itu mikroorganisme adalah kunci keberhasilan atau kegagalan suatu
fermentasi, dimana jenis dan jumlah hasil fermentasi tergantung dari jenis
mikroorganisme dan perlakuannya. Dari ribuan jenis spesies mikroorganisme yang
mampu melakukan proses fermentasi hanya beberapa puluh saja yang dipilih untuk
digunakan dalam industri, yakni yang memiliki keunggulan-keunggulan yang
diperlukan untuk berhasilnya suatu proses fermentasi (Sa’id, 1987).
Makanan yang mengalami fermentasi biasanya mempunyai nilai gizi yang
tinggi daripada bahan asalnya. Tidak hanya disebabkan karena mikroba bersifat
katabolik atau memecah komponen yang komplek menjadi zat-zat yang lebih
sederhana sehingga lebih mudah dicerna, tetapi mikroba juga dapat mensintesa
beberapa vitamin yang kompleks. Melalui fermentasi juga dapat terjadi pemecahan
oleh enzim-enzim tertentu terhadap bahan-bahan yang tidak dapat dicerna oleh
manusia (Winarno, 1980).
Ada tiga karakteristik penting yang harus dimiliki oleh mikroorganisme bila
akan digunakan dalam fermentasi, yaitu :
a. Mikrobiologi harus mampu tumbuh dengan cepat dalam suatu substrat dan
lingkungan yang cocok dan mudah untuk dibudidayakan dalam jumlah besar.
b. Organisme harus memiliki kemampuan untuk mengatur ketahanan fisiologis
dalam kondisi seperti di atas, dan menghasilkan enzim-enzim essensial dengan
mudah dan dalam jumlah besar agar perubahan-perubahan kimia yang
dikehendaki dapat terjadi.
c. Kondisi lingkungan yang diperlukan bagi pertumbuhan dan produksi maksimum
secara komparatif harus sederhana (Desrosier, 1988).
Ragi tape merupakan bentuk awetan dari mikroba berbentuk padatan dan
kering. Mikroba dalam ragi tape merupakan campuran terutama dari yeast dan mold
seperti Mucor, Aspergillus, Penicillium, Rhizopus, Saccharomyces, Candida, dan
Hansenula (Dwijoseputro, 1970). Secara teoritis hampir semua jenis ragi (yeast)
dapat digunakan dalam ekstraksi minyak, hanya tergantung pada keaktifan
mikrobanya. Salah satu yeast yang memberikan hasil yang baik untuk merombak
karbohidrat yang dikandung suatu bahan adalah S. cereviceae (Anonimus, 1977).
Dalam pertumbuhannya mikroorganisme memerlukan faktor-faktor pertumbuhan
antara lain unsur C, H, O, N, S dan P yang diperolehnya dengan mengubah protein,
karbohidrat, dan zat-zat lain dalam media pertumbuhannya, sehingga zat-zat dalam
jauh lebih banyak daripada yang dibutuhkan, dan produk-produk disimilasi akan tidak
berguna bahkan menghambat banyak organisme (Winarno dan Fardiaz, 1984).
Fermentasi tidak dapat berlangsung tanpa adanya enzim. Enzim yang biasa
dihasilkan oleh mikroorganisme adalah enzim amilase, enzim protease dan pektinase.
Enzim amilase menghidrolisis pati menjadi dekstrin dan senyawa-senyawa gula
sederhana, kemudian hasil-hasil ini diubah menjadi asam-asam organik. Enzim
protease memutus rantai-rantai peptida dari protein yang mempunyai berat molekul
tinggi menjadi molekul-molekul yang sederhana dan akhirnya menjadi
peptida-peptida dan asam-asam amino. Aktivitas mikroba akan menghasilkan asam sehingga
akan menurunkan pH, pada pH tertentu tercapailah titik isoelektris pada protein yang
merupakan lapisan pelindung emulsi minyak. Protein akan menggumpal akhirnya
mudah dipisahkan dari minyak (Suhardijono dan Syamsiah, 1988).
Kandungan Kimia Minyak Kelapa Murni atau Virgin Coconut Oil (VCO)
Minyak kelapa murni dikenal sebagai minyak laurat tinggi mengandung asam
lemak jenuh (Saturated Fatty Acid) yang bersama gliserol membentuk trigliserida
rantai sedang (Medium Chain Triglyceride). Minyak ini dibuat dari daging kelapa
segar yang diolah dalam suhu rendah atau tanpa melalui pemanasan sehingga
kandungan yang penting dalam minyak tetap dapat dipertahankan. Minyak kelapa
murni mempunyai warna yang lebih jernih dan dapat tahan disimpan selama 2 tahun
tanpa menjadi tengik (Rindengan dan Riyanto, 2005).
Tingginya asam lemak jenuh ini menyebabkan minyak kelapa murni tahan
terhadap proses ketengikan akibat oksidasi (Alamsyah, 2005). Menurut Van der
Vossen dan Umail (2001) minyak kelapa murni mengandung lebih dari 95%
trigliserida (trigliserol) serta beberapa jenis asam lemak jenuh dan tidak jenuh. Asam
lemak jenuh meliputi asam laurat, meristat, palmitat, dan stearat, sedang asam lemak
tidak jenuhnya meliputi asam oleat, linoleat dan linolenat. Asam lemak jenuh yang
dominan adalah asam laurat.
Woodroof (1979) menyebutkan bahwa kandungan asam-asam lemak utama di
dalam minyak kelapa murni adalah laurat (45%), miristat (18%), palmitat (9,5%),
oleat (8,2%), kaprilat (7,8%), kaprat (7,6%) dan stearat (5%). Minyak kelapa murni
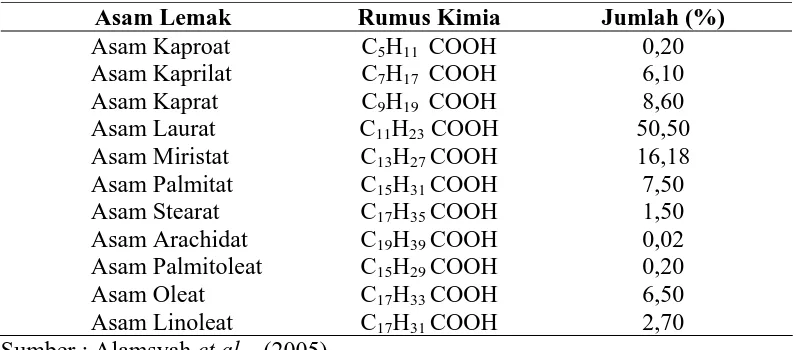
dikenal sebagai minyak laurat tinggi mengandung asam lemak jenuh. Komposisi
asam lemak minyak kelapa murni dapat dilihat pada Tabel 3.
Tabel 3. Komposisi Asam Lemak Minyak Kelapa
Asam lemak jenuh bukanlah kelompok homogen, tetapi terdiri atas tiga sub
kelompok. Pertama, kelompok minyak dengan asam lemak rantai pendek atau short
chain triglceride (STC). Kedua kelompok minyak dengan rantai sedang atau medium
chain triglceride (MCT), dan ketiga adalah long chain triglceride (LTC). Perbedaan
panjang rantai karbon ini merupakan faktor utama yang menentukan mekanisme
lemak dapat dicerna dan dimetabolisir tubuh, serta cara lemak tersebut mempengaruhi
tubuh.
Asam lemak rantai sedang atau Medium Chain Trigliceride (MCT) pada
minyak kelapa murni lebih khusus asam laurat yang merupakan asam lemak dominan
yang terkandung pada minyak kelapa murni ternyata memiliki khasiat yang sama
dengan Air Susu Ibu (ASI) yaitu sebagai anti virus, anti bakteri dan anti partosiat. Di
dalam tubuh asam laurat akan berubah bentuk menjadi monolaurin agar lebih
berfungsi dalam menjaga kesehatan manusia (Wibowo, 2006). Asam lemak rantai
sedang mempunyai kekentalan lebih rendah daripada minyak lain. Penyebabnya
adalah panjang rantai asam lemaknya lebih pendek dan terkait dengan ukuran
molekulnya yang lebih kecil. Sifat kekentalan MCT yang rendah menyebabkan
mudah tersebar dan melekat di permukaan serta menghasilkan keseragaman dengan
baik (Alamsyah, 2005).
Sifat utama MCT stabilitas oksidatifnya tinggi yang dapat memperpanjang
umur simpan produk akhir. MCT dapat digunakan untuk memperbaiki stabilitas
oksidatif minyak konvensional. Perbaikan sifat stabilitas menjadi konvensional
dibutuhkan untuk mencegah terjadinya ketengikan pada minyak (Rindengan dan
Novarianto, 2005). MCT sangat stabil pada suhu yang sangat rendah dan tinggi,
misalnya tidak mengental meskipun dalam waktu yang lama digunakan pada suhu
penggorengan. Warna MCT tidak berubah hitam akibat penambahan panas
sebaliknya sebagian besar minyak nabati apabila dipanaskan pada suhu tinggi akan
berubah warna serta menjadi kebal dan kental. Selain itu MCT masih berwujud cairan
jernih dan tidak mengental meskipun berada pada suhu 0°C (Alamsyah, 2005).
Secara luas MCT banyak digunakan dalam industri, flavour (industri aroma
atau rasa) karena kualitas organoleptik yang baik dan kelarutannya yang tinggi.
Industri farmasi memanfaatkan kelebihan sifat daya larut MCT dalam vitamin dan
formulasi obat. Kualitas MCT terjamin dan tidak berbau, tidak berasa, dan hampir
tidak berwarna, oleh karena itu MCT tidak memberikan efek buruk pada produk
(Rindengan dan Novarianto, 2004).
Kelebihan lain yang ditawarkan MCT adalah asam lemak rantai sedang dapat
bersifat jenuh secara alami, sehingga tidak mengandung lemak trans yang dapat
menyebabkan penyakit jantung. MCT dapat digunakan untuk menggantikan beberapa
atau semua bagian tertentu dan minyak terhidrogenasi dalam suatu varietas atau
formula (Alamsyah, 2005).
Teknik Pengolahan Minyak Dengan Pemanasan
Tahapan proses pembuatan minyak kelapa murni dengan cara pemanasan
tidak membutuhkan perlakuan yang sangat khusus. Hal ini disebabkan proses
dilakukan petani. Dalam pembuatan minyak kelapa murni ini ada beberapa tahapan
yang perlu dilakukaan yaitu pembuatan santan, pemisahan krim, pemanasan krim
santan, pemanasan minyak dan penyaringan minyak (Setiaji dan Prayugo, 2006).
Krim merupakan bagian dari santan kelapa yang kaya dengan kandungan
minyak. Agar kandungan minyak dapat diambil dari krim diperlukan proses
pemanasan. Lama pemanasan santan hingga diperoleh minyak yang belum matang
sekitar tiga jam. Minyak belum masak ini diperoleh dengan penyaringan blondo.
Blondo tersebut masih mengandung minyak sebanyak 10-15% sehingga perlu dipres
untuk mengeluarkan kandungan minyaknya (Rindengan dan Novarianto, 2005).
Minyak kelapa murni yang diperoleh melalui proses pemanasan bertahap atau
pengolahan terkontrol dengan perbaikan pada cara pengolahan tradisional memiliki
mutu yang lebih baik. Beberapa kriteria mutu minyak yang diperoleh melalui proses
pemanasan bertahap adalah kadar asam lemak bebas (ALB) 0,02%, kadar air
0,02-0,03%, tidak berwarna (bening) dan berbau harum. Bahkan daya simpan
minyaknya masih lebih baik yaitu 6-8 bulan (Alamsyah, 2005).
Teknik Pengolahan Minyak Tanpa Pemanasan
Pengolahan minyak kelapa murni tanpa proses pemanasan merupakan proses
pengolahan menggunakan enzim atau mikroba penghasil enzim-enzim yang berperan
pada pemisahan ikatan lemak dengan protein dan karbohidrat. Dengan cara itu
minyak akan langsung terpisah pada lapisan atas (Anonimous, 2005).
Ada tiga cara umum yang dilakukan yaitu melalui minyak pancing, kemudian
metoda fermentasi dan enzimatis. Metoda fermentasi menggunakan sel hidup seperti
mikroba yang disimpan sebagai ragi. Sementara sistem enzimatik menggunakan
enzim. Metode berikutnya adalah cara mekanis yang sering disebut sentrifugasi
(Alamsyah, 2005). Dengan metode pemancingan molekul minyak dalam santan
ditarik oleh minyak umpan sampai akhirnya bersatu. Tarikan itu membuat air dan
protein yang sebelumnya terikat dengan molekul santan menjadi putus. Teknik
pemancingan pada dasarnya adalah mengubah bentuk emusi air-minyak menjadi
minyak-minyak (Setiaji dan Prayugo, 2005).
Kerusakan Minyak Kelapa
Bahan makanan berlemak merupakan medium yang baik bagi pertumbuhan
beberapa jenis jamur dan bakteri. Kerusakan lemak dalam minyak kelapa dapat
terjadi selama proses pengolahan seperti pemanasan dan penyimpanan. Kerusakan
pada minyak berupa ketengikan yang menyebabkan bau dan rasa yang tidak enak
pada minyak. Kerusakan tersebut dapat disebabkan oleh air, cahaya, panas, oksigen,
logam, basa dan enzim (Alamsyah, 2005).
Sifat dan daya tahan minyak terhadap kerusakan sangat tergantung pada
komponen penyusunnya, terutama kandungan asam lemak. Minyak yang
mengandung asam lemak tidak jenuh cenderung mudah teroksidasi, sedangkan yang
banyak mengandung asam lemak jenuh lebih mudah terhidrolisis. Asam lemak pada
Penyebab utama terjadinya ketengikan hidrolisis adalah adanya air, baik yang
terdapat di dalam minyak maupun gliserol dan asam lemak. Reaksi dipercepat oleh
basa, asam dan enzim-enzim. Proses hidrolisis mudah terjadi pada minyak yang
berasal dari bahan dengan kadar air tinggi. Minyak kelapa yang diperoleh melalui
proses ekstraksi secara basah (wet rendering) cenderung lebih banyak mengandung
air, sehingga mudah mengalami kerusakan hidrolisis dan tidak tahan lama (Djatmiko
dan Widjaya, 1973).
Kerusakan minyak yang utama adalah timbulnya bau dan rasa tengik yang
disebut proses ketengikan. Hal ini disebabkan oleh autooksidasi radikal asam lemak
tidak jenuh dalam minyak. Proses oksidasi yang berlangsung bila terjadi kontak
antara antara oksigen dengan minyak (Winarno, 1986).
BAHAN DAN METODE PENELITIAN
Bahan Penelitian
Bahan baku yang digunakan dalam penelitian ini berupa daging buah kelapa
(Cocos nucifera L.) yang cukup tua, ragi roti yang diperoleh dari Pasar Kotamadya
Medan dan air kelapa yang digunakan untuk pembuatan starter.
Peralatan dan Bahan Kimia yang digunakan
Saringan santan, panci/waskom, timbangan, kain saring, parutan kelapa,
kompor, plastik penutup, inkubator, autoclove, erlenmeyer, gelas piala, pipet,
patridish, petroleum ether, alkohol 96%, KOH 0,1 N, indikator thymol blue, aquades,
Glukosa Yeast Pepton Agar (GYPA), Glukosa Yeast Pepton Broth (GYPB), Potato
Dextrose Agar (PDA) dan Plate Count Agar (PCA).
Tempat Penelitian
Penelitian ini dilakukan di Laboratorium Biokimia dan Laboratorium
Mikrobiologi FMIPA Universitas Sumatera Utara Medan dan Pusat Penelitian Kelapa
Sawit (PPKS) Medan.
Metode Penelitian
Penelitian ini menggunakan rancangan percobaan faktorial dengan pola
Rancangan Acak Lengkap (RAL), dengan perlakuan kombinasi yang dicobakan
Faktor I : Kadar ragi yang digunakan dalam pembuatan starter (C) dengan 4 taraf
percobaan yakni :
C0 = 0% (Kontrol)
C1 = 5% (v/v)
C2 = 10% (v/v)
C 3 = 15% (v/v)
C 4 = 20% (v/v)
Faktor II :
Waktu fermentasi (T), dengan 4 taraf percobaan yakni :
T1 = 12 jam
T2 = 24 jam
T3 = 36 jam
T4 = 48 jam
Kombinasi perlakuan (treatment combination) sebanyak 16.
Adapun perlakuan kombinasi yang dicobakan adalah sebagai berikut :
1. C1 T1 5. C2 T1 9. C3 T1 13. C4 T1
2. C1 T2 6. C2 T2 10. C3 T2 14. C4 T2
3. C1 T3 7. C2 T3 11. C3 T3 15. C4 T3
4. C1 T4 8. C2 T4 12. C3 T4 16. C4 T4
Banyaknya ulangan yang digunakan :
T (n – 1) ≥ 15
16 (n – 1) ≥ 15
16 n – 16 ≥ 15
16n ≥ 31
n ≥ 31/16
n ≥ 1,9375
untuk ketelitian dilakukan 2 ulangan.
Analisis Data
Data yang diperoleh dianalisis dengan analisis sidik ragam. Analisis sidik
ragam dimaksudkan untuk menguji hipotesis tentang pengaruh perlakuan terhadap
keragaman data hasil percobaan. Data terlebih dahulu diuji parameter atau non
parameter, kemudian uji homogenitas. Bila terdapat perbedaan nyata, diuji lebih
lanjut dengan uji DMRT (Duncan Multiple Range Test) (Hanafiah, 1991).
Pembuatan Santan Kelapa
Daging buah kelapa diparut dan dibuat santan dengan cara mengekstraknya
dengan air hangat (suhu antara 35-40°C) yang dicampur dengan air kelapa dengan
perbandingan 1 : 1 (g/l). Ekstraksi santan dilakukan dua kali kemudian santan
dicampur jadi satu dan didiamkan selama 1 jam sehingga terpisah antara krim,
skimnya dan air. Penggunaan air kelapa sebagai air perasan santan didasarkan pada
aspek manfaat, karena air kelapa sebagai limbah pada hal ketersediaannya mencapai
25% dari berat total buah kelapa (Jefri dan Kaunang, 1990). Menurut Rumokoi, 1991,
bagi perkembangan mikroba yang berperan membantu proses perusakan komponen
minyak dan santan.
Pembuatan Kultur Murni S. cereviceae
Kultur murni S. cereviceae dibuat dari ragi roti. Sebanyak 1 g ragi roti diambil
secara aseptis dan dilarutkan ke dalam 10 ml akuades steril dan divortex hingga
homogen. Kemudian dipipet 0,1 ml ke cawan petri yang berisi media GYPA dan
diinkubasi selama 24 jam pada suhu 30 °C. Koloni yang tumbuh di subkulturkan pada
media miring dalam tabung reaksi yang berisi PDA dan diinkubasi sebagai stok
kultur (Lay, 1994).
Kultur S. cereviceae diambil secara aseptis dan dilarutkan ke dalam aquades
steril, kemudian dilakukan pengenceran. Suspensi S. cereviceae yang telah
diencerkan dimasukkan ke dalam larutan GYPB sebanyak 1 ml lalu diguncang dan
diinkubasi selama 24 jam. Suspensi S. ereviceae diambil secara aseptis 1 ml suspensi
S. cereviceae dan diteteskan ke dalam cawan petri yang berisi medium PCA supaya
dapat tumbuh lalu disebarkan dengan Hockey stick steril dan dibiarkan beberapa saat
supaya suspensi meresap ke dalam agar media. Kultur di inkubasi pada suhu 30°C
selama 24 jam (Lay, 1994).
Maka sel hidup dapat dihitung berdasarkan rumus :
Penentuan kultur S. cereviceae dilakukan dengan standar Mc Farland dengan
membandingkan kekeruhan suspensi kultur S. cereviceae (Lorian, 1980). Skema
penentuan kultur S. cereviceae dapat dilihat pada Lampiran 1.
Pembuatan Starter
Krim, skim dan air kemudian dipisahkan dengan tabung dekantasi kemudian
krim disimpan di dalam lemari pendingin sedangkan skim di campur dengan air
kelapa dengan perbandingan volume 3 : 1 dan disterilkan dalam otoklaf pada suhu ±
110°C selama 30 menit tutup segera setelah disterilkan. Sebanyak 108 sel
S. cereviceae diinokulasikan ke dalam campuran air kelapa dan skim disimpan dalam
suhu kamar selama 24 jam. Menurut Rumokoi (1991) penggunaan air kelapa sebagai
starter karena mengandung bahan kimia dan nutrisi yang cukup tinggi, berfungsi
sebagai zat perangsang tumbuh yang berguna bagi perkembangan S. cereviceae.
Skema pembuatan stater dapat dilihat pada Lampiran 2.
Pembuatan Minyak Kelapa
Krim santan dengan volume 100 ml per unit percobaan dimasukkan ke dalam
gelas piala, kemudian ditambahkan dengan starter sesuai dengan perlakuan dan
dihomogenkan dengan mengaduknya secara merata. Masing-masing gelas piala
ditutup dengan lembaran plastik sesuai dengan taraf perlakuan waktu fermentasi yang
48 jam, air yang terdapat pada lapisan bawah dipisahkan. Masing-masing kombinasi
perlakuan diulangi sebanyak dua kali. Skema pembuatan minyak kelapa dapat dilihat
pada Lampiran 3.
Penyaringan
Pemisahan minyak dilakukan, menurut Sukmadi dan Nugroho (2000) yaitu
dengan memisahkan 3 lapisan berupa air, minyak dan blondo dengan labu pemisah.
Campuran minyak dan protein kemudian dipanaskan pada suhu ± 100°C selama
5 menit sehingga terlihat pemisahan antara minyak dan protein. Blondo yang
dihasilkan kemudian dipres lagi secara manual sehingga minyak dapat diperoleh
secara maksimum. Protein menggumpal dan selanjutnya disentrifugasi pada 5000
rpm selama 15 menit. Untuk memisahkan bagian minyak dan gumpalan protein
minyak yang diperoleh diukur volumenya sebagai virgin coconut oil yang berwarna
kuning, minyak diperoleh secara maksimum.
Analisis Rendemen Minyak
Rendemen kelapa hasil fermentasi dihitung sebagai persentase
perbandingan volume minyak yang diperoleh dengan volume krim santan mula-mula
(Soeka et al., 2008 )
Rendemen = x100%
Santan Krim
Volume
Minyak Volume
Analisis Kadar Air
Contoh minyak ditimbang sebanyak 10 g di dalam petridish yang telah
ditentukan berat kosongnya. Kemudian dimasukkan ke dalam oven suhu 60 ± 1°C
selama 3 jam. Petridish didinginkan dalam eksikator selama 15 menit kemudian
dimasukkan kembali ke dalam oven selama 30 menit dan didinginkan kembali dalam
eksikator selama 15 menit. Perlakuan ini diulangi hingga tercapai berat yang konstan
dari minyak (Sudarmadji et al., 1989).
Kadar air = x100%
Analisis Kadar Asam Lemak Bebas
Contoh minyak ditimbang sebanyak 5,0 gram di dalam erlenmeyer 100 ml yang sudah ditentukan beratnya, kemudian ditambahkan 20 ml petroleum eter.
Setelah minyak melarut ditambahkan lagi 20 ml alkohol 96%. Larutan lemak ini
dititrasi dengan KOH 0,1N dan thymol-blue sebagai indikatornya sampai tepat warna
merah jambu (Sudarmadji et al., 1989).
Kadar ALB (%FFA) = 100%
Analisis Kadar Asam Laurat
Contoh minyak ditimbang 0,5 g dalam tabung reaksi dan ditambahkan larutan
BF3 metanol (15% BF dalam metanol) lalu dipanaskan pada suhu 65°C selama
divorteks, selanjutnya ditambahkan 1 ml NaCl jenuh untuk memisahkan gliserol dan
di vortex lalu didiamkan selama 5 menit. Lapisan atas yang terbentuk diinjeksikan ke
dalam kromatografi gas (Yunita et al., 2007).
Analisis Bilangan Peroksida
Minyak atau lemak sebanyak 5 gr dilarutkan dalam campuran asetat dan
kloroform (3 : 2) dibiarkan selama 30 detik sambil sesekali digoyang, kemudian
diteteskan KI ± 0,25 ml lalu ditambah aquades sebanyak 30 ml, kemudian dititrasi
dengan natrium thiosulfat sampai warna kuning hampir hilang campuran. Ditetesi
dengan indikator pati ± 0,5 ml, kemudian dititrasi sampai warna biru hampir hilang
(Sudarmadji et al., 1989).
HASIL DAN PEMBAHASAN
Tiga belas butir kelapa digunakan untuk menghasilkan parutan daging buah
seberat 6,24 kg. Santan kelapa merupakan sistim emulsi dalam air yang berwarna
putih susu. Emulsi tersebut distabilkan oleh stabilizer berupa campuran protein dan
karbohidrat dalam bentuk lapisan yang sangat kuat. Menurut Winarno (1984) sistem
emulsi dapat mengalami pemecahan sehingga membentuk dua lapisan yang tidak
bercampur. Ekstraksi dilakukan menggunakan air hangat (35 – 40°C) yang dicampur
dengan air kelapa dengan perbandingan 1 : 1 (v/v) menghasilkan krim santan
sebanyak 4,25 liter. Menurut Duryatmo, (2005) pada suhu 35°C asam kaprat mulai
terurai, dan pada suhu di atas 60°C asam-asam lemak menguap. Pembuatan starter
menggunakan skim dan air kelapa dengan perbandingan 3 : 1 (v/v) dan disterilkan
pada suhu 110°C. Menurut Rumokoi, 1991, air kelapa mengandung bahan kimia dan
nutrisi yang cukup tinggi yang berfungsi bagi perkembangan mikroba yang berperan
membantu proses perusakan komponen minyak dan santan. Hasil proses fermentasi
krim santan kelapa dengan penambahan starter S. cereviceae pada variasi waktu dan
konsentrasi starter menghasilkan volume minyak yang bervariasi. Volume minyak
dari semua kombinasi perlakuan berkisar antara 27 - 37,75 ml dari 100 ml krim
santan.
Analisis sidik ragam (lampiran 4) menunjukkan bahwa kombinasi perlakuan
konsentrasi starter dan waktu menunjukkan tidak ada perbedaan yang nyata terhadap
kombinasi C3T2 merupakan kombinasi paling baik dengan hasil 37,75 ml minyak
VCO. Volume paling sedikit diperoleh dari kombinasi perlakuan C1T1 yaitu 27,75 ml.
Jumlah ini lebih banyak dibandingkan dengan rendemen minyak yang diperoleh
Soeka et al., (2008) yang menggunakan inokulum yang berasal dari khamir dan
kapang dengan memvariasikan inokulum 1 : 1, 1 : 2,5, 1 : 5 dan 1 : 10. Mereka
mendapatkan rendemen minyak berkisar antara 18 – 25% dalam 100 ml krim santan.
Rendemen ini juga lebih tinggi bila dibandingkan dengan fermentasi minyak kelapa
dengan enzim papain oleh Lydia (2006) dengan memvariasikan konsentrasi enzim
papain menghasilkan minyak berkisar 7 – 16%. Hasil ini juga lebih tinggi bila
dibandingkan yang diperoleh Yurnaliza (2007) dengan menggunakan inokulum
Citrobacter sp yaitu 26 – 31%. Hal ini mungkin disebabkan oleh perbedaan jenis
inokulum, sumber enzim, kualitas kelapa dan air yang digunakan untuk ekstraksi
parutan kelapa.
Variasi konsentrasi starter yang digunakan menunjukkan perbedaan nyata
terhadap rendemen minyak kelapa yang dihasilkan. Pada penggunaan starter 0%
tidak menghasilkan rendemen minyak kelapa, hal ini disebabkan proses fermentasi
tidak berlangsung dalam emulsi santan. Menurut Sukmadi dan Nuguroho (2002),
salah satu faktor yang mempengaruhi produksi minyak kelapa secara fermentasi
adalah konsentrasi starter semakin tinggi konsentrasi starter, rendemen minyak
semakin tinggi, sampai penggunaan starter 15% yaitu 33,94 ml, turun pada
penggunaan starter 20% yaitu 32,50%. Dari analisis rendemen minyak, dapat dipilih
kombinasi perlakukan yang efektif adalah kombinasi C3T2 yaitu sebanyak 37,75%.
Variasi konsentrasi stater terhadap rendemen minyak yang dihasilkan digambarkan
Konsentrasi Starter S. cereviceae (%)
Gambar 1. Pengaruh konsentrasi starter S. cereviceae terhadap rendemen minyak (%)
Pengaruh konsentrasi starter S. cereviceae dalam pembuatan VCO terhadap
rendemen minyak telah diuji dengan DMRT (Duncan Multiple Range Test) seperti
pada pada Tabel 4.
Tabel 4. Pengaruh Konsentrasi Starter S. cereviceae Terhadap Rendemen Minyak (%)
Konsentrasi Starter S. cereviceae Rataan
C1 (5%) 32,00 bB C2 (10%) 33,44 aA C3 (15%) 33,94 aA C4 (20%) 32,50 bB
Keterangan : Notasi huruf yang berbeda menunjukkan beda nyata pada taraf 5% dan sangat nyata pada taraf 1% berdasarkan uji DMRT
Dari Tabel 4 terlihat bahwa rendemen minyak yang diperoleh pada
penggunaan konsentrasi starter S. cereviceae 10% dan 15% dalam pembuatan VCO
10% dan 15% menghasilkan volume minyak tidak berbeda nyata. Peningkatan
rendemen minyak terjadi karena kerusakan yang terjadi semakin sempurna akibat
semakin banyaknya S. cereviceae yang berperan dalam memecahkan emulsi minyak
dalam krim santan. Menurut Pelczar dan Chan (1986) proses ekstraksi krim secara
fermentasi melibatkan enzim amilase pemecah emulsi krim santan dan aktifitas enzim
akan menurun atau berhenti. Dengan menurunnya aktifitas enzim maka rendemen
minyak yang dihasilkan akan semakin menurun.
Analisis sidik ragam (Lampiran 4) dapat dilihat bahwa pengaruh lama
fermentasi memberi pengaruh yang berbeda sangat nyata terhadap rendemen minyak
kelapa murni (VCO) yang dihasilkan. Semakin lama waktu fermentasi, semakin
tinggi rendemen minyak yang dihasilkan sampai waktu fermentasi 24 jam, turun
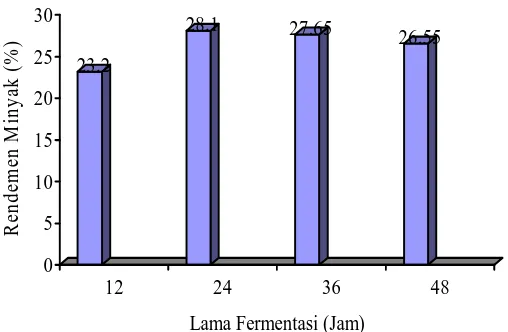
penggunaan waktu 36 – 48 jam. Rendemen minyak yang dihasilkan dapat
digambarkan pada Gambar 2.
23.2
Gambar 2. Pengaruh lama fermentasi terhadap rendemen minyak (%)
Pengaruh waktu fermentasi terhadap rendemen minyak telah diuji dengan
DMRT seperti pada Tabel 5
Tabel 5. Pengaruh Lama Fermentasi (Jam) Terhadap Rendemen Minyak (%)
Lama Fermentasi (Jam) Rataan
T1 (12 Jam) 23,20 cC T2 (24 Jam) 28,10 aA T3 (36 Jam) 27,65 bB T4 (48 Jam) 26,55 bB
Keterangan : Notasi huruf yang berbeda menunjukkan beda nyata pada taraf 5% dan sangat nyata pada taraf 1% berdasarkan uji DMRT
Dari Tabel 5 variasi waktu 12 jam menunjukkan perbedaan yang sangat nyata
dengan lama fermentasi 24 - 48 jam. Sementara penggunaan waktu 36 jam dan
48 jam terlihat perbedaan yang tidak nyata.
Dari Gambar 2 terlihat bahwa terjadi peningkatan rendemen minyak pada
perlakuan waktu fermentasi 12 jam sampai 24 jam. Setelah itu penambahan waktu
fermentasi menyebabkan rendemen minyak menurun. Peningkatan rendemen minyak
yang terjadi disebabkan pada awal fermentasi sel-sel S. cereviceae berada dalam
keadaan pertumbuhan sehingga mencapai jumlah yang maksimum. Dengan demikian
enzim pemecah karbohidrat dan protein berada dalam keadaan maksimum.
Penurunan rendemen minyak setelah 24 jam waktu fermentasi mungkin disebabkan
oleh digunakannya unsur-unsur penyusun minyak sebagai sumber dan pertumbuhan
sel S. cereviceae.
Hasil analisis sidik ragam (Lampiran 5) menunjukkan bahwa kombinasi
perbedaan yang nyata. Kadar air yang terdapat dalam minyak berkisar antara
0,20 – 0,60%. Jumlah ini menunjukkan bahwa kandungan air dalam minyak kelapa
murni sangat rendah dan rendahnya kadar air inilah yang memungkinkan minyak
kelapa murni tahan lama untuk disimpan dan tidak cepat menjadi tengik. Hasil
penelitian yang diperoleh Elisabeth et al., (2003) VCO yang dioleh secara fermentasi
dengan jenis air perasan, mereka mendapatkan kadar air 0,22%. Jumlah ini hampir
sama dengan yang diperoleh. Hasil analisis menunjukkan bahwa mutu minyak kelapa
murni yang dibuat telah sesuai dengan standar yang dipersyaratkan yaitu berkisar
antara 0,1 – 0,6% (Alamsyah, 2005).
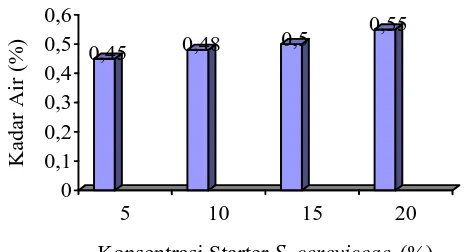
Analisis sidik ragam (Lampiran 5) variasi starter yang digunakan
menunjukkan pengaruh tidak berbeda nyata. Semakin tinggi konsentrasi starter, kadar
air semakin tinggi seperti yang disajikan pada Gambar 3.
0,45 0,48 0,5
Konsentrasi Starter S. cereviceae (%)
Gambar 3. Pengaruh konsentrasi starter S. cereviceae terhadap kadar air (%)
Pengaruh konsentrasi starter S. cereviceae dalam pembuatan VCO terhadap
kadar air telah diuji dengan DMRT seperti pada Tabel 6.
Tabel 6. Pengaruh Konsentrasi Starter S. cereviceae terhadap Kadar Air (%) Konsentrasi Starter S. cereviceae Rataan
C1 (5%) 0,45 aA C2 (10%) 0,48 aA C3 (15%) 0,50 aA C4 (20%) 0,55 aA
Keterangan : Notasi huruf yang berbeda menunjukkan beda nyata pada taraf 5% dan sangat nyata pada taraf 1% berdasarkan uji DMRT
Dari Tabel 6 terlihat bahwa kadar air VCO yang diperoleh pada perlakuan
konsentrasi starter 5–20% menghasilkan kadar air tidak ada perbedaan yang nyata.
Peningkatan kadar air VCO terjadi karena enzim amilase yang digunakan memecah
emulsi santan yang merupakan emulsi minyak dalam air menjadi emulsi air dalam
minyak. Pemecahan emulsi ini berlangsung melalui reaksi hidrolisis. Dengan adanya
enzim amilase yang berfungsi mengkatalisis reaksi pemecahan karbohidrat.
Analisis sidik ragam (Lampiran 5) dapat dilihat bahwa variasi waktu
fermentasi yang digunakan memberikan pengaruh tidak nyata terhadap kadar air
VCO yang dihasilkan. Semakin lama waktu fermentasi kadar air dalam VCO semakin
tinggi sampai penggunaan waktu 36 jam, turun penggunaan waktu 48 jam. Kadar air
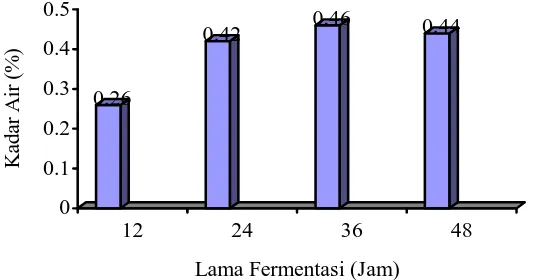
yang dihasilkan dapat dilihat pada Gambar 4.
0.26
Pengaruh lama fermentasi S. cereviceae dalam pembuatan VCO terhadap
kadar air telah diuji dengan DMRT seperti pada Tabel 7.
Tabel 7. Pengaruh Lama Fermentasi (Jam) terhadap Kadar Air (%)
Lama Fermentasi (Jam) Rataan
T1 (12 Jam) 0,26 bB T2 (24 Jam) 0,42 aA T3 (36 Jam) 0,46 aA T4 (48 Jam) 0,44 aA
Keterangan : Notasi huruf yang berbeda menunjukkan beda nyata pada taraf 5% dan sangat nyata pada taraf 1% berdasarkan uji DMRT
Dari Tabel 7 terlihat bahwa kadar air yang tertinggi diperoleh pada perlakuan
lama fermentasi 24 – 48 jam tidak berbeda nyata. Waktu fermentasi 12 jam
menunjukkan perbedaan sangat nyata dengan kandungan air terendah. Peningkatan
kadar air dalam VCO disebabkan semakin lama waktu fermentasi maka terjadi
pemecahan rantai peptida pada protein menjadi senyawa yang lebih sederhana cukup
tinggi pula. Hal ini mengakibatkan semakin banyak minyak yang terekstrak keluar
dan membawa molekul air yang ikut bercampur dengan minyak sehingga kadar air
yang dihasilkan meningkat.
Analisis sidik ragam (Lampiran 6) dapat dilihat bahwa pengaruh kombinasi
perlakuan konsentrasi starter dan waktu fermentasi memberikan pengaruh yang
berbeda sangat nyata terhadap asam lemak bebas VCO yang dihasilkan. Kadar asam
lemak bebas yang terdapat dalam minyak berkisar antara 0,07 – 0,24%. Jumlah ini
menunjukkan bahwa kadar asam lemak bebas dalam minyak kelapa murni sangat
rendah. Kadar asam lemak bebas yang diperoleh Elisabeth et al., (2003) pada VCO
yang diolah secara fermentasi dengan jenis air perasan, mereka mendapatkan 0,13%
jumlah ini hampir sama dengan kadar asam lemak bebas yang diperoleh.
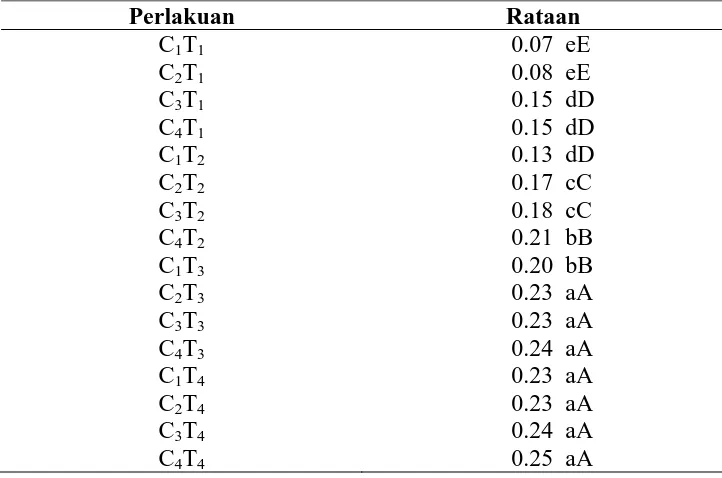
Pengaruh interaksi konsentrasi starter S. cereviceae dan lama fermentasi
terhadap asam lemak bebas telah diuji dengan DMRT seperti pada Tabel 8.
Tabel 8. Pengaruh Interaksi Konsentrasi Starter S. cereviceae dan Lama Fermentasi terhadap Asam Lemak Bebas (%)
Perlakuan Rataan
Keterangan : Notasi huruf yang berbeda menunjukkan beda nyata pada taraf 5% dan sangat nyata pada taraf 1% berdasarkan uji DMRT
Dari Tabel 8 dapat dilihat bahwa kombinasi perlakuan antara konsentrasi
starter S. cereviceae dan lama fermentasi memberikan pengaruh yang berbeda sangat
nyata terhadap asam lemak bebas. Asam lemak bebas tertinggi diperoleh dari
kombinasi perlakuan C4 T4 sebesar 0,25% dan terendah diperoleh pada C1 T1 sebesar
0,07%. Hasil analisis menunjukkan bahwa kandungan asam lemak bebas dalam VCO
disimpan dan tidak cepat menjadi tengik. Standar asam lemak bebas yang
dipersyaratkan pada mutu VCO sebesar ≤ 0,5% (Alamsyah, 2005). Hasil analisis
menunjukkan bahwa kadar asam lemak bebas dalam VCO dibuat telah sesuai dengan
standar. Semakin tinggi konsentrasi starter S. cereviceae dan semakin lama
fermentasi maka asam lemak bebas akan meningkat yang dapat dilihat pada Gambar
5. Peningkatan asam lemak bebas ini disebabkan oleh minyak yang mengandung air
sehingga menghidrolisis ikatan ester dari trigliserida yang menghasilkan asam lemak
dan gliserol, dimana peristiwa ini akibat jumlah enzim yang diproduksi oleh
mikrobial yang berlebihan dan waktu fermentasi yang lama menyebabkan ekstraksi
lemak sangat cepat.
Gambar 5. Pengaruh interaksi starter S. cereviceae dan lama fermentasi terhadap asam lemak bebas (%)
Hasil analisis sidik ragam (Lampiran 6) menunjukkan bahwa kombinasi
perlakuan konsentrasi starter dan waktu menunjukkan pengaruh berbeda
tidak nyata, tapi asam laurat yang dihasilkan berkisar 20,69–34,88%. Yang
dapat dilihat pada Gambar 6. Kandungan asam laurat menurut standar yang
dipersyaratkan berkisar 43,0 - 53,0% (Alamsyah, 2005). Menurut Novariyanto H. dan
Tulalo M. (2007) kadar asam laurat dipengaruhi oleh jenis inokulum.
Variasi konsentrasi starter yang digunakan menunjukkan pengaruh berbeda
sangat nyata terhadap kadar asam laurat VCO yang dihasilkan. Semakin tinggi
konsentrasi starter dalam pembuatan VCO, kadar asam laurat semakin tinggi sampai
penggunaan starter 15% sebesar 31,55%, turun penggunaan starter 20% yaitu 31,07%
yang disajikan pada Gambar 6.
25,18
Konsentrasi Starter S. cereviceae (%)
Gambar 6. Pengaruh konsentrasi starter S. cereviceae terhadap asam laurat (%)
Pengaruh konsentrasi starter S. cereviceae dalam pembuatan VCO terhadap
Tabel 9. Pengaruh Konsentrasi Starter S. cereviceae terhadap Kadar Asam Laurat (%)
Konsentrasi Starter S. cereviceae Rataan
C1 (5%) 25,18 bB C2 (10%) 29,58 aA C3 (15%) 31,55 aA C4 (20%) 31,07 aA
Keterangan : Notasi huruf yang berbeda menunjukkan beda nyata pada taraf 5% dan sangat nyata pada taraf 1% berdasarkan uji DMRT
Dari Tabel 9 dapat dilihat bahwa kadar asam laurat yang diperoleh pada
perlakuan konsentrasi starter 5% berbeda sangat nyata bila dibandingkan dengan
perlakuan konsentrasi starter 10% - 20%. Pada perlakuan stater 15% menghasilkan
asam laurat tertinggi yaitu sebesar 31,55% dan terendah perlakuan 5% yaitu 25,18%,
Hasil analisis kadar asam laurat minyak kelapa murni (VCO) pada penelitian ini
lebih rendah dibanding dengan kadar asam laurat hasil fermentasi yang diperoleh oleh
Soeka, et al., (2008) yang menggunakan khamir Saccharomycopsis yang
memvariasikan inokulum 1 : 1, 1 : 5, 1 : 10. Mereka mendapatkan kadar asam laurat
sebesar 46,70%. Hal ini mungkin disebabkan perbedaan varietas kelapa. Menurut
Novarianto H. dan Tulalo M. (2007) kadar asam laurat dipengaruhi oleh varietas
kelapa, tinggi tempat tumbuh, dan tempat analisis laboratorium.
Variasi waktu yang digunakan menunjukkan pengaruh berbeda sangat nyata
terhadap kadar asam laurat yang dihasilkan. Semakin lama waktu fermentasi, kadar
asam laurat semakin tinggi sampai penggunaan waktu fermentasi 48 jam dan dapat
dilihat pada Gambar 7.
19,9
Gambar 7. Pengaruh lama fermentasi terhadap asam laurat (%)
Pengaruh lama fermentasi S. cereviceae dalam pembuatan VCO terhadap
kadar asam laurat telah diuji dengan DMRT seperti Tabel 10.
Tabel 10. Pengaruh Lama Fermentasi terhadap Kadar Asam Laurat (%)
Lama Fermentasi (Jam) Rataan
T1 (12 Jam) 19,90 bB T2 (24 Jam) 23,02 aA T3 (36 Jam) 24,84 aA T4 (48 Jam) 26,15 aA
Keterangan : Notasi huruf yang berbeda menunjukkan beda nyata pada taraf 5% dan sangat nyata pada taraf 1% berdasarkan uji DMRT
Dari Tabel 10 dapat dilihat bahwa kadar asam laurat pada perlakuan waktu
24 – 48 jam tidak ada perbedaan nyata, sementara pada perlakuan waktu 12 jam
terlihat ada perbedaan sangat nyata. Peningkatan kadar asam laurat disebabkan oleh
semakin lama waktu fermentasi yang digunakan untuk memecah protein pada emulsi
santan oleh enzim protease menyebabkan semakin meningkatnya asam-asam organik
Analisis sidik ragam (Lampiran 8) dapat dilihat bahwa pengaruh interaksi
konsentrasi starter S. cereviceae dan lama fermentasi memberikan pengaruh yang
nyata terhadap bilangan peroksida VCO yang dihasilkan, tapi bilangan peroksida
yang terdapat pada minyak berkisar antara 0,90 – 3,50 meq/kg. Penelitian yang
diperoleh Elisabeth et al., (2003) pada VCO yang diolah secara fermentasi dengan
menggunakan air perasan santan dari campuran air kelapa dan air hangat 1 : 1 mereka
mendapatkan 0,46 meq/kg. Jumlah ini lebih besar bila dibandingkan dengan bilangan
peroksida yang dihasilkan. Pengaruh interaksi konsentrasi stater S. cereviceae dan
lama fermentasi terhadap bilangan peroksida telah diuji dengan DMRT seperti pada
Tabel 11.
Tabel 11. Pengaruh Interaksi Konsentrasi Starter S. cereviceae dan Lama Fermentasi (Jam) terhadap Bilangan Peroksida (meq/kg)
Perlakuan Rataan
Keterangan : Notasi huruf yang berbeda menunjukkan beda nyata pada taraf 5% dan sangat nyata pada taraf 1% berdasarkan uji DMRT
Dari Tabel 11 dapat dilihat bahwa kombinasi perlakuan antara konsentrasi
starter S. cereviceae dan lama fermentasi memberikan pengaruh yang berbeda nyata
terhadap bilangan peroksida. Bilangan peroksida tertinggi diperoleh dari kombinasi
perlakuan C4T4 sebesar 3,5 meq/kg minyak dan terendah diperoleh pada C1T1 sebesar
0,19 meq/kg minyak. Semakin tinggi konsentrasi starter S. cereviceae dan semakin
lama fermentasi maka bilangan peroksida akan semakin meningkat seperti terlihat
pada Gambar 8.
Konsentrasi Starter S. cereviceae (%)
T1 (12 Jam) T2 (24 Jam) T3 (36 Jam) T4 (48 Jam)
Gambar 8. Pengaruh interaksi antara konsentrasi starter S. cereviceae dan lama fermentasi terhadap bilangan peroksida (meq/kg)
Menurut standar yang dipersyaratkan CODEX Rev.2 – 1999 (Alamsyah,
2005) besar bilangan peroksida ≤ 3 meq/kg minyak. Kombinasi perlakuan konsentrasi
starter 10 – 20% dan lama fermentasi 24 – 48 jam menghasilkan bilangan peroksida
Peningkatan bilangan peroksida ini disebabkan oleh aktifitas enzim yang
memecahkan emulsi lemak sehingga menghasilkan asam lemak tidak jenuh. Asam
lemak tidak jenuh akan mengalami penambahan oksigen pada ikatan rangkap yang
merupakan senyawa yang tidak stabil dan kemudian dilanjutkan dengan proses
hidroperoksida (H2O2) peningkatan konsentrasi S. cereviceae akan meningkatkan
asam lemak tidak jenuh. Semakin meningkat konsentrasi stater dan waktu fermentasi
makin meningkat asam lemak tidak jenuh.