PEMANFAATAN SIRUP GLUKOSA HASIL HIDROLISA SELULOSA DARI DAMI NANGKA (Artocarpus heterophyllus lamk) SEBAGAI PEMANIS
PADA PEMBUATAN MANISAN DARI DAGING BUAH KELAPA (Cocos nucifera L)
SKRIPSI
NURMALA SARI
060802039
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
UNIVERSITAS SUMATERA UTARA
PEMANFAATAN SIRUP GLUKOSA HASIL HIDROLISA SELULOSA DARI DAMI NANGKA (Artocarpus heterophyllus lamk) SEBAGAI PEMANIS
PADA PEMBUATAN MANISAN DARI DAGING BUAH KELAPA (Cocos nucifera L)
Diajukan untuk melengkapi tugas dan memenuhi syarat mencapai gelar Sarja Sains
NURMALA SARI
060802039
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
UNIVERSITAS SUMATERA UTARA
PERSETUJUAN
Judul : PEMANFAATAN SIRUP GLUKOSA HASIL
HIDROLISA SELULOSA DARI DAMI NANGKA (Artocarpus heterophyllus lamk) SEBAGAI PEMANIS PADA PEMBUATAN MANISAN DARI BUAH KELAPA (Cocos nucifera L)
Kategori : SKRIPSI
Nama : NURMALA SARI
Nomor Induk Mahasiswa : 060802039 Program Studi : SARJANA (S1) Departemen : KIMIA
Fakultas : MATEMATIKA DAN ILMU PENGETAHUAN
ALAM (FMIPA) UNIVERSITAS SUMATERA UTARA
Disetujui di
Medan, Desember 2010
Komisi Pembimbing
Pembimbing II, Pembimbing I,
Dra.Hj.Emma Zaidar Nst.Msi Prof. Dr. RA. Harlinah S.P.W,M. Sc NIP 195509181987012001 NIP 130175778
Diketahui/Disetujui oleh
Departemen Kimia FMIPA USU Ketua,
PERNYATAAN
PEMANFAATAN SIRUP GLUKOSA HASIL HIDROLISA SELULOSA DARI DAMI NANGKA (Artocarpus heterophyllus lamk) SEBAGAI PEMANIS
PADA PEMBUATAN MANISAN DARI DAGING BUAH KELAPA (Cocos nucifera L)
SKRIPSI
Saya mengakui bahwa skripsi ini adalah hasil kerja saya sendiri, kecuali beberapa
kutipan dan ringkasan yang masing-masing disebutkan sumbernya.
Medan, Desember 2010
NURMALA SARI
PENGHARGAAN
Puji dan syukur penulis panjatkan kepada ALLAH SWT yang telah memberikan
rahmat dan hidayah-Nya sehingga penulis dapat menyelesaikan skripsi ini yang
berjudul
“PEMANFAATAN SIRUP GLUKOSA HASIL HIDROLISA
SELULOSA DARI DAMI NANGKA (Artocarpus heterophyllus lamk)
SEBAGAI PEMANIS PADA PEMBUATAN MANISAN DARI
DAGING BUAH KELAPA (Cocos nucifera L)
“.
Dalam kesempatan inipenulis ingin mebgucapkan terimah kasih kepada :
1. Ayahanda Wahono, Ibunda Suparmi, adek Kumala Dewi dan adek Sofia Wilda
yang sangat penlis cintai dan sayangi, atas doa dan bantuannya selama ini baik
secara material maupun moril kepada panelis.
2. Ibu Prof.Dr.RA.Harlinah S.P.W.M.Sc selaku komisi pembimbing I dan Ibu
Drs.Hj.Emma Zaidar Nst.Msi selaku komisi pembimbing II penulis yang
dengan sabar telah meluangkan waktunya untuk membimbing peneliti dalam
melakukan penelitian dan penyusunan skripsi ini hingga selesai.
3. Ketua Departemen kimia Ibu Dr. Rumondang Bulan, Ms serta sekretaris
Departemen kimia Bapak Drs. Firman Sebayang,Ms. Serta semua Bapak dan
Ibu dosen pengajar di jurusan kimia di FMIPA USU Medan, khususnya
kepada Bapak dan Ibu dosen bidang Biokimia, Prof.Dr.RA.Harlina SPW,Msc,
Dr.Ribu Surbakti,MS, Drs.Firman Sebayang,MS, Dr.Yuniarti Yusak,MS,
Dr.Rumondang Bulan,MSi, Dra.Emma Zaidar,Msi, atas semua ilmu dan saran
yang diberikan.
4. Semua keluarga asisten Biokimia di Laboratorium Biokima/KBM fmipa USU:
Eko, Nora, Agung, Egi, Ardi, Decy, Erpina, Oki, Arini, Tiwi, Annisa, Ferri,
Soraya dan juga teman – teman seperjuangan dalam penelitian : Nelviana,
Febri, Rani, Nuraida, Mardiana, ester,ai, Jimmy dan semua teman – teman
Analitik di Laboratorium Analitik : Sevia dkk, Asisten Organik : Mima dkk,
dan Irma dkk di Laboratorium Farmasi Kuantitatif USU.
5. Sahabat – sahabat terbaikku yang saya sayangi Afrima, Nora, Fatma, nia,
Holida, Yeni, dan Halima
6. Dan semua pihak yang tidak dapat penulis sebutkan satu persatu yang telah
banyak memberikan bantuan kepada penlis dapat menyelesaikan tulisan
ini.Semoga ALLAH SWT akan membalasnya
Penulis sadar atas kekurangan materi yang disajikan dalam skripsi ini,
disebabkan keterbatasan literature dan pengetahuan yang dimiliki penulis.
Dengan kerendehan hati, penulis mempersembahkan skripsi ini kepada para
pembaca, semoga bermanfaat.
Penulis,
ABSTRAK
THE USE OF GLUCOSE SYRUP AS PRODUCT OF SELULOSA HIDROLYZE FROM THE DAMI OF JACKFRUIT (Artocarpus heterophyllus lamk) AS SWEETENER ON CANDIES
PRODUCTION FROM THE COCONUT PALM (Cocos nucifera L)
ABSTRACT
BAB 4 HASIL DAN PEMBAHASAN 37
4.1. Hasil Penelitian 37
4.1.1. Perhitungan Kadar Serat Kasar Dami Nangka 37 4.1.2. Pengolahan Data Pengukuran Absorbansi Glukosa 38 Hasil Hidrolisis Selulosa Dami Nangka
4.1.3. Perhitungan Kadar Glukosa Hasil Hidrolisis Selulosa 39
4.2. Pembahasan 43
BAB 5 KESIMPULAN DAN SARAN 44
5.1. Kesimpulan 44
5.2. Saran 44
DAFTAR PUSTAKA 45
DAFTAR TABEL
Halaman
Tabel.1.1.Data Hasil Perhitungan Kadar Serat Dami Nangka 48
Tabel.2.2.Data Absorbansi Larutan Glukosa Standar (0,05 mg/ml) 49
pada berbagai panjang gelombang
Tabel.3.3 Data Absorbansi Larutan Glukosa Standar pada berbagai konsentrasi 50
pada maksium 761 nm
Tabel.4.4.Data Hasil Perhitungan Kadar Gula Reduksi bedasarkan 51
Absorbansi Glukosa Hasil Hidrolisis Selulosa dami Nangka
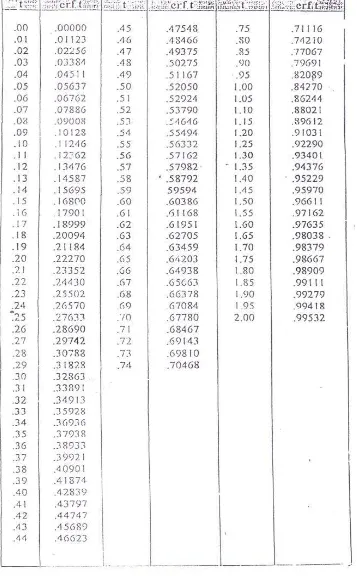
Tabel 5.5. Harga erf (t) atau ert (hx) dari harga T 52
Tabel 6.6. Data Hasil pengukuran organoleptik terhadap warna manisan Kelapa 53
Tabel 6.7. Data Hasil Pengukuran Organoleptik terhadap rasa manisan kelapa 54
DAFTAR GAMBAR
Halaman
Gambar 2.1 Dami Nangka 8
Gambar 2.3 Struktur Selulosa 12
Gambar.2.3.1.2.Mekanisme Hidrolisa Selulosa 14
Gambar 1.1. Kurva spektrum maks larutan glukosa standar 48
ABSTRAK
THE USE OF GLUCOSE SYRUP AS PRODUCT OF SELULOSA HIDROLYZE FROM THE DAMI OF JACKFRUIT (Artocarpus heterophyllus lamk) AS SWEETENER ON CANDIES
PRODUCTION FROM THE COCONUT PALM (Cocos nucifera L)
ABSTRACT
BAB 1
PENDAHULUAN
1.1Latar Belakang
Polisakarida yang terdapat di alam dapat dihidrolisis oleh asam ataupun enzim,
menghasilkan monosakarida atau turunan monosakarida. Polisakarida dapat berfungsi
sebagai polisakarida struktur maupun polisakarida turunan. Polisakarida struktur yang
paling banyak terdapat didalam tumbuhan ialah selulosa (Girindra.A.1990).
Dalam tubuh selulosa tidak dapat dicerna karena dari dalam tubuh tidak
mempunyai enzim yang dapat menguraikan selulosa. Tetapi ternyata polisakarida
dapat dimanfaatkan, dimana dengan menggunakan asam encer tidak dapat dihidrolisis,
tetapi oleh asam dengan konsentrasi tinggi yaitu secara kimiawi menggunakan HCl
30% dapat terhidrolisis menjadi D-glukosa (Poedjiadi.A.1994).
Di samping kulit buah dan biji, dami nangka merupakan bagian buah nangka
yang sering di buang atau merupakan limbah. Dami nangka menempati porsi cukup
besar yaitu 40-50% dari total limbah yang dihasilkan. Agar dami nangka bermanfaat,
bermutu tinggi dan memiliki nilai jual perlu adanya teknologi pengolahan pangan.
Namun, kebanyakan masyarakat membuang dami nangka begitu saja, karena banyak
masyarakat yang belum mengetahui bahwa dami nangka mengandung pectin sehingga
dapat di jadikan sebagai produk olahan
Jadi, semua limbah yang mengandung selulosa, seperti dami nangka, biji
alpukat, ampas kelapa dll. Ternyata dapat dihirolisis menjadi sirup glukosa, sirup
glukosa dapat dimanfaatkan dengan menggunakan gula pasir, dan limbah-limbah
lainnya ternyata juga sangat baik, jadi dengan pelestarian lingkungan untuk
kreaktif untuk memanfaatkan berbagai sumber bahan makanan untuk memenuhi
kebutuhan sehari-hari. Apabila limbah ini ditentukan adalah selulosa, dimana caranya
ditentukan dengan metode warenwet.
Hidrolisis selulosa dengan asam berlangsung bertahap melalui reaksi sebagai
berikut :
Selulosa selubiosa glukosa
Dimana glukosa termasuk :
- Monosakarida
- Rasanya manis
- Sifatnya mereduksi ion Cu++ dari kupri sulfat menjadi ion Cu+ yang kemudian
mengendap dengan endapan warna merah bata Cu2O.
Suatu fakta teramat penting tentang gula belakangan ini adalah harganya yang
melambung terus. Kebutuhan gula Indonesia mencapai 3,3 juta ton/tahun, sementara
produksi dalam negeri hanya 1,7 ton atau 51,5% dari kebutuhan nasional, sehingga
impor menjadi pilihan. Ironisnya, harga gula impor lebih murah dibandingkan dengan
gula produksi dalam negeri. Dalam situasi seperti ini, gula produksi dalam negeri
menjadi sulit dipasarkan tanpa kebijakan yang mampu melindunginya dari serbuan
gula impor.
Sirup glukosa atau sering juga disebut gula cair dibuat melalui proses hidrolisis.
Perbedaannya dengan gula pasir atau sukrosa yaitu sukrosa merupakan gula
disakarida, terdiri atas ikatan glukosa dan fruktosa, sedangkan sirup glukosa adalah
monosakarida, terdiri atas satu monomer yaitu glukosa. Sirup glukosa dapat dibuat
dengan cara hidrolisis asam atau dengan cara enzimatis dapat dikembangkan
dipedesaan karena tidak banyak menggunakan bahan kimia sehingga aman dan tidak
mencemari lingkungan.
1.2Permasalahan
Kebanyakan masyarakat membuang dami nangka begitu saja, karena banyak
masyarakat yang belum mengetahui bahwa dami nangka mengandung pectin sehingga
dapat di jadikan sebagai produk olahan. Dami nangka merupakan bagian buah nangka
yang sering di buang atau merupakan limbah. Dami nangka menempati porsi cukup
besar yaitu 40-50% dari total limbah yang dihasilkan. Oleh karena itu timbul
permasalahan bagaimana pengembangan kearah pemanfaatan dami nangka, sehingga
bermutu tinggi dan memiliki nilai jual perlu adanya teknologi pengolahan pangan.
Tingginya harga gula dipasaran menjadikan alasan seseorang untuk mencari
alternatif bahan pemanis lain sebagai pengganti gula. Oleh karena itu timbul
permasalahan bagaimana pengembangan kearah pemanfaatan dami nangka atau
selaput tipis antar buah.Dalam hal ini penulis tertarik untuk memanfaatkan selulosa
pada dami nangka untuk pembuatan manisan kelapa, sehingga muncul permasalahan
apakah selulosa pada dami nangka dapat dijadikan pemanis untuk mensubsitusikan
gula pasir.
1.3Pembatasan Masalah
Dalam penelitian ini masalah dibatasi sebagai berikut:
1. Perolehan sampel dibatasi hanya dami nangka yang diperoleh dari penjual
buah di pajak Pagi Setia Budi
2. Hidrolisis dilakukan dengan menggunakan HCl 30%.
3. Jenis polisakarida yang digunakan adalah Selulosa dari Dami nangka.
4. Penentuan kadar glukosa dengan cara spektrofotometri metode Nelson
1.4Tujuan Penelitian
Adapun tujuan dari penelitian ini adalah untuk mengetahui pengaruh penambahan
sirup glukosa hasil hidrolisa dari selulosa dami nangka terhadap kemanisan pada
pembuatan manisan dari buah kelapa dan untuk memanfaatkan selulosa dari dami
nangka untuk pembuatan sirup glukosa melalui proses hidrolisis dengan HCl 30%
serta membandingkan kadar glukosanya (1:0 , 1:1 , 1:2 , 1:3).
1.5Manfaat Penelitian
Manfaat penelitian ini antara lain :
- Untuk mengoptimalkan pemanfaatkan limbah dami nangka
- Untuk memberikan informasi kepada masyarakat tentang kandungan dari
Dami Nangka yang dapat dijadikan bahan pemanis sebagai pengganti gula
pasir.
1.6Lokasi Penelitian
Penelitian ini dilakukan di Laboratorium Biokimia/KBM (Kimia Bahan Makanan)
FMIPA USU dan Laboratorium Kimia Analitik Kuantitatif FARMASI USU.
1.7 Metodologi Penelitian
Penelitian ini bersifat penelitian laboratorium. Sampel berupa Dami Nangka diperoleh
dari satu lokasi yaitu Pajak Pajak Pagi Setia Budi Medan. Selulosa dari Dami Nangka
dihidrolisis dengan menggunakan HCl 30% sehingga menghasilkan sirup glukosa dan
kadar glukosanya ditentukan dengan metode Nelson Somogyi menggunakan alat
Spektrofotometer pada panjang gelombang 761 nm. Sirup glukosa hasil hidrolisis
BAB 2
TINJAUAN PUSTAKA
2.1 Tanaman Nangka
Tanaman Nangka diduga merupakan tanaman asli India yang kini telah menyebar luas
keseluruh dunia, terutama Asia Tenggara. Ada dua macam nangka, yakni :
1 . Artocarpus heterophyllus Lamk atau Artocarpus integer (Thumb) Merr yang biasa
disebut nangka, dan
2. Artocarpus champeden (Lour) Stokes atau Artocarpus integrifolia Lf yang biasa
disebut cempedak.
Nangka merupakan tanaman hutan yang pohonnya dapat mencapai tinggi 25 m,
kayunya besar, bila telah tua berwarna kuning hingga kemerahan. Seluruh bagian
tanaman bergetah dan getah nangka disebut pulut (Sunarjono. 2008)
Nangka yang bernama ilmiah (Artocarpus integra atau Artocarpus heterophyllus )
memiliki beberapa jenis buah yang enak rasanya. Ada beberapa jenis nangka yang
populer di masyarakat karena keunikannya. Buahnya tak terlalu komersial.
Keistimewaannya yang membuat banyak orang tertarik membudidayakannya dan
memburu bibitnya, jenis nangka unik itu ialah nangka mini dan nangka celeng.
Adapun jenis yang tergolong komersial antara lain sebagai berikut :
a.Nangka Kunir
Nangka juara pertama lomba buah unggul Jawa Timur tahun 1990 ini memang
istimewa. Tidak mengherankan bila Menteri Pertanian menetapkannya sebagai
varietas unggul. Ukurannya buahnya besar, bobot per buah dapat mencapai 50 kg,
diameter 40 cm, dan panjangnya 45-50 cm. Buahnya bulat, berduri jarang, dan
(bahasa Jawa Kunir). Aromanya wangi, daging buahnya manis dan sedikit
mengandung air. Dami atau selaput tipis antar daging buah sangat sedikit dan masih
enak dimakan .Oleh karena berbagai keistimewaannya itulah, harga jual nangka kunir
jauh diatas jenis nangka lainnya.
b.Nangka dulang
Jenis nangka ini banyak ditemukan didaerah Pasar. Kelebihan nangka ini
terletak pada daminya yang berukuran besar dan berasa manis. Selain itu, daging
buahnya memang manis, berwarna kuning menarik, besar, dan tebal. Bila digigit,
daging buah nangka dulang terasa renyah karena kandungan airnya sedikit. Nangka
jenis ini banyak ditanam oleh petani karena rajin sekali berbuah. Bobot satu buah
nangka dulang sekitar 7-20 kg.
c.Nangka merah
Nangka asal Kalimantan ini memiliki warna daging buah yang menarik.
Penampilan buah dari luar seperti nangka biasa, tanpa keistimewaan apa-apa. Namun,
begitu dibelah baru akan terlihat daging buahnya yang kemerahan. Bentuknya bulat
agak lonjong dengan duri yang banyak dan bobot per buah 8 – 14 kg. Rasanya pun
sangat manis. Daminya cukup banyak seperti nangka biasa. Daminya ada yang
berwarna merah dan berasa manis, tetapi ada juga yang kuning muda dan tidak enak
dimakan . Nangka ini memang belum begitu memasyarakat.
d.Nangka Mini
Nangka mini memang berukuran mini. Bukan karena sengaja dibuat berukuran
mungil, tetapi memang sudah tumbuh kecil dari aslinya. Tingginya hanya 6-9 m, jauh
dibawah nangka biasa yang tingginya dapat mencapai 25 m. Nangka mini termasuk
nangka genjah atau cepat berbuah .Umur 18 bulan sejak tanam sudah muncul calon
buahnya dibatang. Dalam waktu 4 bulan buah nangka sudah matang dipohon. Jenis
nangka mini ada yang berupa nangka bubur, nangka mini bulat, nangka mini lonjong,
e.Nangka celeng
Nangka celeng disukai karena berbuah dipangkal batang dan menempel
ditanah. Sebagai tanaman perkarangan atau kebun, penampilan yang unik ini amat
menarik perhatian. Buahnya lebat, berukuran normal, bahkan tergolong besar. Daging
buahnya tebal dengan rasa yang enak, berwarna kuning atau orange. Nangka unik ini
banyak ditemukan didaerah Banjar Baru, Kalimantan Selatan, serta Banyuwangi dan
Lumajang di Jawa Timur. Nama lainnya ialah nangka bilulang. Potensi nangka ini
sebagai buah komersil terbuka luas asal penanamannya dan lebih dikenalkan kepada
umum (Muchlisan.F.1994).
Tanaman nangka adalah tanaman asli dari daerah Ghats bagian barat, India.
Karena sudah dibudidayakan oleh manusia sekian lama tanaman nangka sudah
menyebar keseluruh dunia terutama dikawasan tropis. Marga lain yang sama dengan
tanaman nangka adalah keluwih,sukun dan bendo (Ashari.1995).
Variasi genetis tanaman cukup tinggi, hal ini disebabkan karena bahan
tanamnya masih berasal dari biji. Perbanyakan tanaman secara vegetatif baik okulasi
maupun grafting menghasilkan persentasi jadi rendah. Hal ini kemungkinan
disebabkan karena kandungan getah tanaman nangka yang tinggi sehingga
mengganggu proses pertautan sel-sel batang bawah dengan batas atas (Ashari
Variasi genetis yang tinggi tersebut salah satunya dapat dilihat dari kisaran
berat buahnya yaitu antara 1-20 kg per buah. Selanjutnya, kandungan gizi buah ini
setiap 100g daging buahnya mengandung 72 - 77,2 g air; 1,3 - 2 g protein; 0,1 – 0,4 g
lemak; 18,9 - 25,4 g pati; 0,8 - 1,11 g serat; 0,8 - 1,4 g abu; 22 - 37 mg kalsium ;
18-38 mg fosfor; besi 0,4 - 1,1 mg; sodium 2 mg; potassium 407 g , vitamin A 175 - 540
IU ; vitamin C 8 - 10 mg; dan nilai energi sekitar 395 - 410 kJ untuk setiap 100 g
daging buah (Ashari.1995).
Dami adalah bagian dari buah nangka, berupa serabut-serabut putih yang
daging buah. Biasanya, dami hanya dibuang begitu saja setelah nangka dibuka dan
menjadi limbah
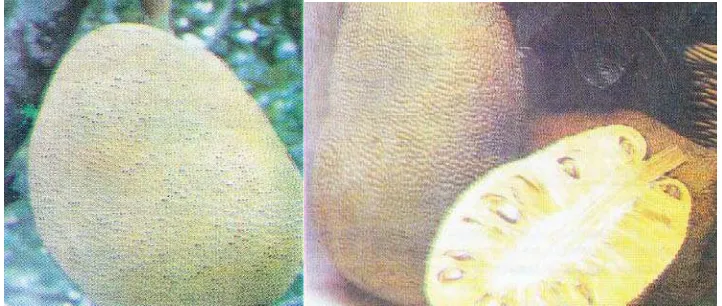
Gambar 2.1. Buah Nangka ( Rukmana.R.1997 ).
Buah nangka mengandung gizi cukup tinggi, kandungan gizi dalam buah nangka
dapat dilihat dalam table di bawah ini :
Tabel.2.1.1.Kandungan Gizi Nangka
No Kandungan Gizi Nangka Masak Nangka Muda
1 Kalori (kal) 106,00 51,00
2 Protein (g) 1,20 2,00
3 Lemak (g) 0,30 0,40
4 Karbohidrat (g) 27,60 11,30
5 Kalsium (mg) 20,00 45,00
6 Fosfor (mg) 19,00 29,00
7 Zat Besi (mg) 0,90 0,50
8 Vitamin A (SI) 330,00 25,00
9 Vitamin B1 (mg) 0,07 0,07
10 Vitamin C (mg) 7,00 9,00
11 Air (g) 70,00 85,40
12 Bagian dapat
dimakan (%)
28,00 80,00
2.1.1.Taksonomi tanaman nangka
Tanaman nangka termasuk tumbuhan tahunan (perennial). Dalam sistematika
(taksonomi) tumbuhan, kedudukan tanaman nangka diklasifikasikan sebagai berikut :
Kingdom : Plantae (tumbuh-tumbuhan)
Divisi : Spermatophyta (tumbuhan berbiji)
Sub-divisi : Angiospermae (berbiji tertutup)
Kelas : Dicotyledonae (biji berkeping dua)
Ordo : Morales
Famili : Moraceae
Genus : Artocarpus
Spesies : A. Heterophyllus Lamk .(jackfruit = nangka) (Rukmana.R.1997)
2.2 Tanaman Kelapa
Tanaman kelapa tumbuh di daerah tropis, dapat dijumpai baik di dataran rendah
maupun dataran tinggi. Pohon ini dapat tumbuh dan berubah dengan baik didaerah
dataran rendah dengan ketinggian 0 - 450 m dari permukaan laut. Pada ketinggian
450-1000 m dari permukaan laut, walaupun pohon ini dapat tumbuh, waktu
berbuahnya lebih lambat, produksinya lebih sedikit dan kadar minyaknya rendah.
Kelapa merupakan tanaman perkebunan / industri dengan batang lurus, famili
palma. Kata coco pertama kali digunakan oleh Vasco da Gama, atau dapat juga
disebut Nux Indica , al djanz al kindi,ganz-ganz , nargil ,narlie , tenga ,temuai,
coconut .Kelapa juga disebut pohon kelapa (Kelapa,cocos nucifera ,
Tanaman kelapa (Cocos nucifera L) merupakan tanaman serbaguna yang
mempunyai nilai ekonomi yang tinggi. Seluruh bagian pohon kelapa dapat
batang, daun sampai buahnya dapat diguanakan untuk kebutuhan kehidupan manusia
sehari-hari.
Buah kelapa terdiri dari sabut, tempurung, daging buah dan air kelapa. Berat
buah kelapa yang telah tua kira-kira 2 kg per butir. Buah kelapa digunakan hampir
seluruh bagiannya, diamana daging buahnya dapat langsung dikonsumsi
(Amin.S.2009).
Tanaman kelapa merupakan jenis tanaman palem yang paling dikenal, banyak
tersebar didaerah tropis. Kelapa dapat tumbuh dipinggir laut hingga dataran
tinggi.Kelapa termasuk famili palma ,dibagi tiga : (1) Kelapa dalam dengan varietas :
viridis (kelapa hijau), rubescens (kelapa merah), macrocorpu (kelapa kelabu),
sakarina (kelapa manis), (2) Kelapa genjah dengan varietas eburnea (kelapa gading),
regia (kelapa raja), pumila (kelapa puyuh), pretiosa (kelapa raja malabar), dan (3)
Kelapa hibrida
(Kelapa ,cocos nucifera
2.2.1.Taksonomi tanaman kelapa
Dalam sistematika (taksonomi) tumbuhan, tumbuhan kelapa diklasifikasikan sebagi
berikut :
Kingdom: Plantae (Tumbuhan)
Subkingdom: Tracheobionta (Tumbuhan berpembuluh)
Super Divisi: Spermatophyta (Menghasilkan biji)
Divisi: Magnoliophyta (Tumbuhan berbunga)
Kelas: Liliopsida (berkeping satu / monokotil)
Sub Kelas: Arecidae
Ordo: Arecales
Famili
Genus:
Daging buah kelapa merupakan jaringan yang berasal dari inti lembaga yang
disebut sel kelamin jantan dan membelah diri. Daging buah kelapa berwarna putih,
lunak, dengan tebal sekitar Daging buah kelapa merupakan jaringan yang berasal dari
inti lembaga yang disebut sel kelamin jantan dan membelah diri. Daging buah kelapa
berwarna putih, lunak, dengan tebal sekitar 8-10 mm.
Daging buah kelapa merupakan sumber protein yang penting dan mudah
dicerna. Kandungan zat dan gizinya tergantung umur buah, seperti yang tercantum
pada tabel1.2. Lengkapnya kandungan zat pada daging buah kelapa menyebabkan
dapat diolah menjadi berbagai produk kebutuhan rumah tangga seperti bumbu dapur,
santan, kopra, minyak kelapa dan kelapa parut kering (Amin.S.2009).
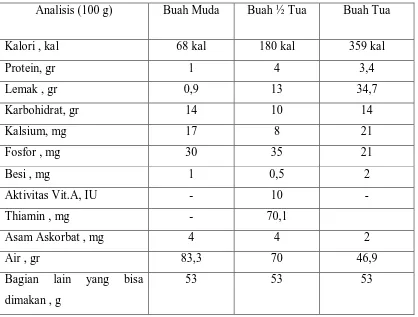
Tabel 2.2.1.2 Komposisi Daging Kelapa Berbagai Tingkat Umur
Analisis (100 g) Buah Muda Buah ½ Tua Buah Tua
Kalori , kal 68 kal 180 kal 359 kal
Protein, gr 1 4 3,4
Lemak , gr 0,9 13 34,7
Karbohidrat, gr 14 10 14
Kalsium, mg 17 8 21
Fosfor , mg 30 35 21
Besi , mg 1 0,5 2
Aktivitas Vit.A, IU - 10 -
Thiamin , mg - 70,1
Asam Askorbat , mg 4 4 2
Air , gr 83,3 70 46,9
Bagian lain yang bisa
dimakan , g
53 53 53
2.3. Selulosa
Selulosa terdapat dalam tumbuhan sebagai bahan pembentuk dinding sel. Serat kapas
boleh dikatakan seluruhnya adalah selulosa. Dalam tubuh kita selulosa tidak dapat
dicernakan karena kita tidak mempunyai enzim yang dapat menguraikan selulosa.
Dengan asam encer tidak dapat terhidrolisis, tetapi oleh asam dengan konsentrasi
tinggi dapat terhidrolisis menjadi selobiosa dan D-glukosa. Selobiosa adalah suatu
disakarida yang terdiri atas dua molekul glukosa yang berikatan glikosidik antara
atom karbon 1 dengan atom karbon 4.
Meskipun selulosa tidak dapat digunakan sebagai bahan makanan oleh tubuh,
namun selulosa yang terdapat sebagai serat – serat tumbuhan, sayuran atau buah –
buahan, berguna untuk memperlancar pencernaan makanan. Adanya serat-serat dalam
saluran pencernaan gerak peristaltik ditingkatkan dan dengan demikian memperlancar
proses pencernaan dan dapat mencegah konstipasi. Tentu saja jumlah serat yang
terdapat dalam bahan makanan tidak boleh terlalu banyak (Poedjiadi.A.1994).
Selulosa membentuk komponen serat dari dinding sel tumbuhan. Ketegaran
selulosa disebabkan oleh struktur keseluruhannya. Molekul selulosa merupakan
rantai-rantai, dari D-glukosa sampai sebanyak 14.000 satuan yang terdapat sebagai
berkas-berkas terpuntir mirip tali, yang terikat satu sama lain oleh ikatan hidrogen.
Suatu molekul tunggal selulosa merupakan polimer lurus dari 1,4’-β
-glukosa. Hidrolisis lengkap dalam HCl 40 % dalam-air, hanya menghasilkan
D-glukosa. Disakarida yang terisolasi dari selulosa yang terhidrolisis sebagian adalah
selobiosa, yang dapat dihidrolisis lebih lanjut menjadi D-glukosa dengan suatu katalis
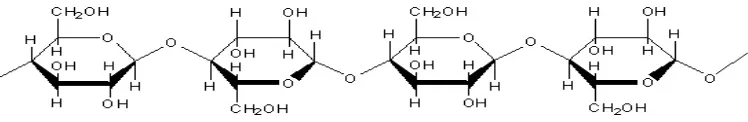
Gambar 2.3. Struktur Molekul Selulosa
http://www.google.co.id/imglanding?q=struktur selulosa.com
Selulosa merupakan homopolisakarida linier tidak bercabang, terdiri dari
10.000 atau lebih unit D-glukosa yang dihubungkan oleh ikatan β-1,4-glikosidik
(Lehninger.A.L.1988).
Selulosa lebih sukar diuraikan dan mempunyai sifat-sifat sebagai berikut :
memberi bentuk atau struktur pada tanaman, tidak larut dalam air dingin maupun air
panas, tidak dapat dicerna oleh pencernaan manusia sehingga tidak dapat
menghasilkan energi (Winarno.F.G.1995).
Selulosa merupakan komponen utama penyusun dinding sel tanaman dan
hampir tidak pernah ditemui dalam keadaan murni dialam melainkan berikatan debgan
lignin dan hemiselulosa membentuk lignoselulosa (Lynd.L.R.2002).
Lignin berikatan dengan hemiselulosa melalui ikatan kovalen namun ikatan
yang terjadi antara selulosa dan lignin belum diketahui secara lengkap. Adanya lignin
disekeliling selulosa merupakan hambatan utama dalam menghidrolisis selulosa.
Selulosa terproteksi dari degradasi dengan adanya lignin. Selulosa tidak dapat
dihidrolisis kecuali lignin dilarutkan dan dihilangkan (Lynd.L.R.2002).
2.3.1.Hidrolisis Selulosa
Hidrolisis lengkap dengan HCl hanya menghasilkan D-glukosa. Disakarida yang
terisolasi dari selulosa yang terhidrolisis sebagian adalah selobiosa, yang dapat
dihidrolisis lebih lanjut menjadi D-glukosa dengan suatu katalis asam atau enzim
2.3.1.1.Hidrolisis selulosa secara enzimatis
Reese at al (1950) menyatakan bahwa hidrolisis selulosa diawali dengan tahap
aktivasi dan diikuti reaksi hidrolisa sebagai berikut :
C1 Cx β-glukosidase
Selulosa selulosa reaktif selubiosa glukosa
Aktivasi disebabkan oleh enzim non hidrolisa yang disebut C1. Hidrolisa dari selulosa
reaktif dilakukan oleh enzim hidrolisa Cx, sedangkan mikrooganisme yang hanya
menguraikan selulosa akan kekurangan enzim C1 tapi akan menghasilkan enzim Cx.
Enzim-enzim selobiohidrolase dan β-glukosidase merupakan enzim penghidrolisa
selulosa ( Fogarty.W.M.1983 ).
2.3.1.2.Hidrolisis selulosa secara kimiawi
Hidrolisis selulosa dengan asam berlangsung bertahap melalui reaksi sebagi berikut :
selulosa selubiosa glukosa
Dalam hal ini, asam (asam sulfat, asam klorida, dan asam perklorat)
mengidrolisis selulosa menjadi glukosa secara acak artinya tudak ada pola tertentu
dalam pemutusan ikatan glikosidik yang terdapat dalam selulosa.
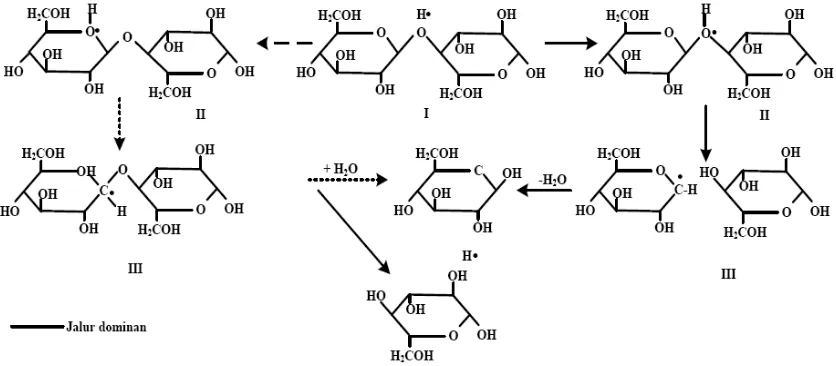
Dasar mekanisme molekuler hidrolisis dalam suasana asam dapat dilihat dalam
Gambar 2.3.1.2.2.Mekanisme hidrolisa selulosa
Hidrolisis dalam suasana asam, akhirnya menghasilkan pemecahan ikatan
glikosidik, berlangsung dalam tiga tahap. Dalam tahap pertama, proton yang bertindak
sebagai katalisator asam berinteraksi cepat dengan oksigen glikosida yang
menghubungkan dua unit gula (I), membentuk asam konjugat (II). Langkah ini diikuti
dengan pemecahan yang lambat dari ikatan C-O, yang menghasilkan zat antara kation
karbonium siklis (III). Protonasi dapat juga terjadi pada oksigen cincin ( II’),
menghasilkan pembukaan cincin dan kation karbonium non siklis ( III’ ). Tidak ada
kepastian ion karbonium mana yang paling mungkin terbesar pada kation siklis.
Akhirnya kation karbonium mulai mengadisi molekul air dengan cepat, membentuk
hasil akhir yang stabil dan melepaskan proton (Wijayanti.L.2005).
2.4.Sirup Glukosa
Sirup glukosa pertama kali digunakan sebagai pengganti gula pada masa Napoleon.
Sirup glukosa dibuat dengan mereaksikan pati dengan asam dengan menghidrolisis
karbohidrat terlebih dahulu untuk memecah gula atau oligosakarida, kemudian untuk
menggandakan gula maltosa (atau gula gandum) dan hasil akhirnya berupa
monosakarida yaitu glukosa. Sirup glukosa dikenal juga dengan nama glukosa
Sirup glukosa merupakan suatu larutan yang diperoleh dari proses hidrolisis
dengan bantuan katalis. Sirup glukosa adalah salah satu produk bahan pemanis
makanan dan minuman yang berbentuk cairan, tidak berbau dan tidak berwarna tetapi
memiliki rasa manis yang tinggi. Sirup glukosa atau gula cair mengandung D-glukosa,
maltosa, dan polimer D-glukosa melalui proses hidrolisis (Cakebread, 1975).
Bahan baku yang dapat digunakan untuk pembuatan sirup glukosa adalah
tapioka, pati umbi-umbian, sagu, jagung, dan serat. Sirup glukosa dapat dibuat dengan
cara hidrolisis asam ataupun secara enzimatis.
Industri makanan dan minuman memiliki kecenderungan untuk menggunakan
sirup glukosa. Hal ini didasari oleh beberapa kelebihan sirup glukosa dibandingkan
sukrosa, diantaranya sirup glukosa tidak mengkristal seperti halnya sukrosa jika
dilakukan pemanasan pada suhu tinggi.
Sirup glukosa telah dimanfaatkan oleh industri permen, minuman ringan,
biskuit, dan sebagainya. Pada pembuatan produk es krim, glukosa dapat meningkatkan
kehalusan tekstur dan menekan titik beku. Dan untuk kue dapat menjaga kue tetap
awet dalam waktu yang lama dan mengurangi keretakan. Untuk permen, glukosa lebih
disenangi karena dapat mencegah kerusakan oleh mikrobiologis dan memperbaik
tekstur (Dziedzic and Kearsley. 1984)
2.5. Abu
Abu adalah zat anorganik sisa hasil pembakaran suatu bahan organik. Kandungan abu
dan komposisinya tergantung pada bahan dan cara pengabuannya. Kadar abu ada
hubungannya dengan mineral suatu bahan. Mineral yang terdapat dalam suatu bahan
dapat merupakan dua macam garam yaitu garam organik dan garam anorganik, Selain
dua garam tersebut, kadang-kadang mineral berbentuk sebagai senyawaan kompleks
yang bersifat organis. Apabila akan ditentukan jumlah mineralnya dalam bentuk
sisa-sisa pembakaran garam mineral tersebut, yang dikenal dengan pengabuan
(Sudarmadji.1989).
2.6.Metode Analisa Kuantitatif Glukosa
2.6.1. Metode Nelson – Somogyi
Metode ini dapat digunakan untuk mengukur kadar gula reduksi dengan menggunakan
pereaksi tembaga arsenomolibdat. Kupri mula-mula direduksi menjadi bentuk kupro
dengan pemanasan larutan gula. Kupro yang terbentuk selanjutnya dilarutkan dengan
arsenomolibdat menjadi molibdenum berwarna biru yang menunjukkan ukuran
konsentrasi gula dengan membandingkannya dengan larutan standar, konsentrasi gula
dalam sampel dapat ditentukan. Reaksi warna yang terbentuk dapat menentukan
konsentrasi gula dalam sampel dengan mengukur absorbansinya (Sudarmadji.S.1984).
2.6.2.Metode Lane-Eynon
Penetapan gula pereduksi dengan metode ini dilakukan secara volumetrik. Biasanya
digunakan untuk penentuan laktosa (anhidrat atau monohidrat) glukosa, fruktosa,
maltosa (anhidrat atau monohidrat) dan lainnya. Penetapan gula pereduksi dengan
metode ini didasarkan atas pengukuran volume larutan gula pereduksi standar yang
dibutuhkan untuk mereduksi pereaksi tembaga basa yang diketahui volumenya. Titik
akhir titrasi ditunjukkan dengan metilen biru yang warnanya akan hilang karena
kelebihan gula pereduksi diatas jumlah yang dibutuhkan untuk mereduksi tembaga.
2.6.3.Metode Shaffer-Somogyi
Metode ini dapat diterapkan untuk segala jenis bahan pangan. Terutama berguna
untuk menetapkan sampel yang mengandung sedikit gula pereduksi. Gula pereduksi
akan mereduksi Cu2+ menjadi Cu+. Cu+ akan dioksidasi oleh I2 (yang terbentuk dari
dengan Na2S2O3. Dengan menggunakan blanko, maka kadar gula pereduksi dalam
sampel dapat ditentukan.
2.6.4.Metode Anthrone
Metode ini dapat digunakan untuk semua jenis bahan makanan. Anthrone
(9,10-dihidro-9-oxanthracena) merupakan hasil reduksi anthraquinone. Anthrone bereaksi
secara spesifik dengan karbohidrat dalam asam sulfat pekat menghasilkan warna biru
kehijauan yang khas.
2.6.5.Metode Munson Walker
Penentuan gula reduksi berdasarkan atas banyaknya endapan Cu2O yang terbentuk,
kemudian dengan melihat tabel Hadmond dapat diketahui jumlah gula pereduksinya.
Jumlah Cu2O ditentukan secara gravimetris, yaitu dengan menimbang larutan endapan
Cu2O yang terbentuk. Dapat juga ditentukan secara volumetrik yaitu dengan titrasi
menggunakan larutan Na-tiosulfat atau K-permanganat (Apriyanto.A.1989).
2.7. Spektrofotometer UV-Visibel
Spektrometri adalah pengukuran absorbansi selektif radiasi elektromagnetik yang
dipakai untuk analisis kualitatif dan kuantitatif senyawa kimia. Sedangkan
spektrofotometri merupakan suatu metode yang sangat penting dalam analisis kimia
kualitatif dan kuantitatif. Banyak kelebihan yang dimilikinya, antara lain :
a. Dapat digunakan secara luas dalam pengukuran secara kualitatif dan
kuantitatif untuk senyawa-senyawa organik maupun senyawa anorganik
b. Kepekaan tinggi, karena dapat mengukur dalam satuan ppm (part per million),
bahkan ppb (part per billion) sehingga dapat mengukur komponen trace (renik)
c. Sangat selektif bila suatu komponen x akan diperiksa dalam suatu campuran,
dengan cara mengatur panjang gelombang cahaya dimana hanya komponen x
yang akan mengabsorbsi cahaya tersebut. Lebih teliti karena hanya
mempunyai persen kesalahan 1 - 3 % bahkan dengan teknik tertentu dapat
2.7.1.Aspek Kualitatif dan Kuantitatif Spektofotometri UV-Vis
Spektra UV-Via dapat digunakan untuk informasi kualitatif dan sekaligus dapat
digunakan untuk analisis kuantitatif.
1. Aspek kualitatif
Data yang diperoleh dari spektroskopi UV dan Vis adalah panjang gelombang
maksimal, intensitas, efek pH, dan pelarut ; yang kesemuanya itu dapat
diperbandingkan dengan data yang sudah dipublikasikan.Misal : dari data
spektra yang diperoleh dapat dilihat, serapan (absorbansi) berubah atau tidak
karena perubahan pH. Jika berubah, bagaimana perubahannya apakah dari
batokromik ke hipsokromik dan sebaliknya atau dari hipokromik
kehiperkromik, dan sebagainya.
2. Aspek Kuantitatif
Dalam aspek kuantitatif, suatu berkas radiasi dikenakan pada cuplikan (larutan
sampel) dan intensitas sinar radiasi yang diteruskan diukur besarnya. Radiasi
yang diserap oleh cuplikan ditentukan dengan membandingkan intensitas sinar
yang diteruskan dengan intensitas sinar yang diserap jika tidak ada spesies
penyerap lainnya. Intensitas atau kekuatan radiasi cahaya sebanding dengan
jumlah foton yang melalui satu satuan luas penampang perdetik. Serapan dapat
terjadi jika foton/radiasi yang mengenai cuplikan memiliki energi yang sama
denagan energi yang dibutuhkan untuk menyebabkan terjadinya perubahan
tenaga. Kekuatan radiasi juga mengalami penurunan denagan adanya
penghamburan dan pemantulan cahaya, akan tetapi penurunan karena hal ini
sangat kecil dibandingkan dengan proses penyerapan (Rohman.A.2007).
2.8.Manisan Buah
Pengawetan dalam bentuk manisan adalah bentuk usaha untuk mempertahankan
tekstur dan warna, mempertahankan dan mengubah citra rasa, sekaligus bentuk usaha
tergantung musim. Harapannya, buah dapat dinikmati setiap saat,tanpa terjadi
perubahan tekstur dan warna, serta citra rasa menjadi lebih baik.
Manisan buah adalah buah yang diawetkan dengan pemberian kadar gula yang
tinggi. Penambahan gula bertujuan untuk memberikan rasa manis sekaligus mencegah
tumbuhnya mikroorganisme seperti jamur. Mikroorganisme ini yang mempercepat
terjadinya perubahan warna, tekstur, citra rasa, dan pembusukan pada buah. Peristiwa
ini juga dipicu oleh proses fisika, seperti sinar matahari dan pemotongan yang terjadi
pada buah .Dalam pembuatan manisan tidak hanya gula yang dapat diberikan, tetapi
juga kapur, garam, dan senyawa yang mengandung sulfur. Tujuan pemberian ini sama
halnya dengan pemberian gula. Dengan pemberian bahan –bahan ini, diharapkan buah
akan memiliki masa simpan lebih lama.
Dikenal ada dua bentuk olahan manisan buah, yaitu manisan basah dan
manisan kering. Hal mendasar yang membedakan keduanya adalah cara pembuatan,
daya awet, dan penampakannya. Manisan basah diperoleh setelah penirisan buah dari
larutan gula, sedangkan manisan kering diperoleh jika manisan basah dijemur sampai
kering. Daya awet manisan kering tentu lebih lama dibandingkan dengan manisan
basah. Kadar air manisan kering lebih rendah tetapi kadar gulanya lebih tinggi.
Sementara itu, penampilan manisan basah lebih menarik dibandingkan dengan
manisan kering, karena hampir sama dengan aslinya.
Pada prinsipnya, semua buah bisa diolah menjadi manisan basah atau manisan
kering, Namun, berdasarkan beberapa alasan seperti tidak enak, tidak tahan lama, dan
penampakannya tidak menarik, kadang-kadang buah hanya diolah menjadi satu
bentuk manisan, yaitu manisan basah atau manisan kering. Meskipun, tidak menutup
kemungkinan dibuat menjadi dua bentuk olahan tersebut. Biasanya buah yang cukup
keras cendrung diolah menjadi manisan basah. Buah yang lunak biasanya dioalah
2.8.1.Faktor-faktor yang mempengaruhi kualitas manisan
Beberapa faktor yang mempengaruhi kualitas manisan adalah penampilan ,citra rasa
dan aroma, daya tahan, kandungan unsur gizi dan kalori, hiegienitas, dan hasil
rendeman pangolahan yang diperoleh .
a . Penampilan
penampilan merupakan penentu utama kualitas suatu produk .Penampilan suatu
produk olahan ditentukan oleh faktor sebagai berikut:
1 . Warna
Warna asli dari buah itu sendiri biasanya lebih diminati. Sayangnya, warna asli
buah tidak sepenuhnya dapat dipertahankan karena memudar selama proses
pengolahan. Karena itu, warna dapat dipertajam dengan menambahkan bahan pewarna
dalam larutan gula ketika sedang diolah .
2 . Keseragaman Bentuk dan Ukuran
Keseragaman bentuk dan ukuran, terutama dalam satu wadah kemasan sangat
mempengaruhi. Sebaliknya, bentuk dan ukuran yang beraneka ragam menimbulkan
kesan bahwa bahan yang digunakan cacat, rusak, dan tidak lolos sortir .
b .Kemasan
Manisan yang tidak dikemas dengan baik akan mudah tercemar debu, kotoran, embun,
cairan, dan uap air dari udara. Apalagi manisan kering yang terkena cairan, gulanya
akan menempel dan meleleh. Akibatnya, penampilan manisan kering menjadi tidak
menarik lagi. Dengan menempatkannya dalam wadah atau kemasan yang sesuai, rapi,
dan bersih ,produk akan terlihat mengesankan. Kemasan yang dipakai sebaiknya
c .Citra Rasa dan Aroma
Citra rasa manisan harus berasal dari citra rasa buah aslinya. Namun, agar citra rasa
makin memikat dapat ditambahkan bahan pewangi atau bumbu yang sesuai.
Sementara itu, aroma merupakan unsur yang sangat peka terhadap pemanasan,
karenanya sulit dipertahankan. Namun, citra rasa yang kompak dapat menutup
kekurangan dari unsur aroma ini .
d .Daya Tahan
Manisan termasuk produk awetan. Karena itu, dituntut untuk dapat disimpan dalam
jangka waktu yang relatif lama. Daya tahan ini dapat diciptakan dengan memperkecil
kadar air dalam buah, meningkatkan konsentrasi gula dalam buah ,memberikan bahan
pengawet, serta mengemasnya dalam wadah yang tertutup rapat tanpa memberi
kesempatan masuknya bahan- bahan pencemar.
e .Kandungan Zat Gizi dan Kalori
Buah memiliki kandungan gizi, mineral, dan kalori. Beberapa kandungan gizi
biasanya akan hilang karena proses pengolahan. Karena itu, proses pengolahan harus
memperhatikan teknik atau tata caranya sehingga kandungan gizi dalam buah bisa
diselamatkan. Untuk menjaga kulaitas manisan tetap baik, bisa dilakukan penambahan
vitamin C kedalam manisan
f .Higienis
Pembuatan manisan yang tidak memperhatikan syarat – syarat kesehatan , hasil
akhirnya akan berkualitas rendah, tampak kotor, daya simpannya pendek, dan
penampilan tidak menarik. Karena itu , syarat – syarat kesehatan, baik kebersihan alat
dan bahan maupun lingkungan pengolahan harus benar – benar di utamakan
Pengelolahan buah menjadi manisan juga sering dikerjakan di
Indonesia,mempergunakan gula pasir.Pada manisan Buah ,buah yang telah dikuliti
dipotong-potong dan direbus dalam larutan gula pasir sampai menjadi kering dan
pekat. Buah yang dibuat manisan biasanya yang aslinya tidak mempunyai rasa
manis,tetapi lebih masam.Rasa manis pada buah berasal dari sukrosa ,gluko sa,maltose
atau sukrosa. Yang mengandung frukrosa, buah akan terasa lebih manis, sedangkan
glukosa dan maltose kurang begitu manis (Sediaoetama.D.A.2009).
2.9.Uji Organoleptik
Uji organoleptik adalah penilaian penggunaan indra,penilaian menggunakan
kemampuan sensorik, tidak dapat diturunkan pada orang lain.Salah satu cara
pengujian organoleptik adalah dengan metode uji pencicipan yang disebut juga
dengan “Acceptance Tests”. Uji pencicipan menyangkut penilaian seseorang akan
suatu sifat atau kualitas suatu bahan yang menyebabkan orang menyenangi.Pada uji
pencicipan dapat dilakukan menggunakan panelis yang belum berpengalaman. Dalam
kelompok uji pencicipan ini termasuk uji kesukaan (hedonik).
2.9.1.Faktor-faktor yang mempenagaruhi suatu bahan makanan
1.Warna
Faktor-faktor yang mempengaruhi suatu bahan makanan antara lain tekstur, warna,
citra rasa, dan nilai gizinya. Sebelum faktor-faktor yang lain dipertimbangkan secara
visual. Faktor warna lebih berpengaruh dan kadang-kadang sangat menentukan suatu
bahan pangan yang dinilai enak, bergizi, dan teksturnya sangat baik, tidak akan
dimakan apabila memiliki warna yang tidak indah dipandang atau member kesan telah
2.Aroma
Aroma dapat didefinisi sebagai suatu yang dapat diamati dengan indera pembau untuk
data yang menghasilkan aroma, zat harus dapat menguap, sedikit larut dalam air dan
sedikit larut dalam lemak. Senyawa berbau sampai ke jaringan pembau dalam hidung
bersama-sama dengan udara. Penginderaan cara ini memasyarakatkan
bahwa senyawa berbau bersifat atsiri.
3.Tekstur
Tekstur adalah faktor kualitas makanan yang paling penting,sehingga memberikan
kepuasan terhadap kebutuhan kita. Oleh karena itu kita menghendaki makanan yang
mempunyai rasa dan tekstur yang sesuai dengan selera yang kita harapkan,sehingga
bila kita membeli makanan,maka pentingnya nilai gizi biasanya ditempatkan pada
mutu setelah harga, tekstur, dan rasa.
4.Rasa
Rasa merupakanfaktor yang cukup penting dari suatu produk makanan. Komponen
yang dapat menimbulkan rasa yang diinginkan tergantung senyawa penyusunnya.
Umumnya bahan pangan tidak hanya terdiri dari satu macam rasa yang terpadu
sehingga menimbulkan cita rasa makanan yang utuh. Perbedaan penilaian panelis
terhadap rasa yang dapat diartikan penerimaannya terhadap flavor atau cita rasa yang
dihasilkan oleh kombinasi bahan yang digunakan (Deman,J.M.1997 ).
Pada uji hedonic,panelis dimintakan tanggapan pribadinya tentang kesukaan
atau sebaliknya ketidaksukaan. Disamping panelis mengemukakan tanggapan
senang,suka atau kebalikannya, mereka juga mengemukakan tingkat
kesukaannya.Tingkat–tingkat kesukaan ini disebut skala hedonik. Dalam
penganalisaan,skala hedonic ditransformasi menjadi skala numeric menurut tingkat
kesukaan. Dengan data numeric ini dapat dilakukan analisis-analisis statistik.
2.9.2.Evaluasi Organileptik
Evaluasi Organileptik ialah pemeriksaan dan penilaian dengan mempergunakan panca
indra. Ada lima jenis modalitas indra (a) penglihatan, (b) penciuman, (c) perabaan, (d)
pendengaran dan (e) pengecap (taste). Yang paling penting dipergunakan dalam
pemeriksaan bahan makanan ialah indra penglihatan dan indra penciuman, indra
perabaan dan pengecap jarang dipergunakan, sedangkan indra pendengaran praktis
BAB 3
METODE PENELITIAN
3.1. Alat dan Bahan
3.1.2. Alat-alat
- Neraca Analitis Mettler Toledo
- Indikator Universal Merck
- Spektrofotometer Genesys 20
- Labu takar Pyrex
- Gelas ukur Pyrex
- Gelas beaker Pyrex
- Labu erlenmeyer Pyrex
- Tabung reaksi Pyrex
- Rak tabung reaksi
- Corong Pyrex
- Penangas air Fisons
- Termometer Fisher
- Botol akuades
- Batang Pengaduk Pyrex
- Oven Memmert
- Pendingin bola Pyrex
- Tanur Gallenkamp
- Inkubator Fisher
- Desikator
- Blender
3.1.2. Bahan-bahan
- C6H12O6 E. Merck
- Na2CO3 E. Merck
- KNaC4H4O6.4H2O E. Merck
- NaHCO3 E.Merck
- Na2SO4 E. Merck
- CuSO4.5H2O E. Merck
- H2SO4 (p) E. Merck
- (NH4)6Mo7O24.4H2O E. Merck
- Na2HAsO4.7H2O E. Merck
- NaOH E. Merck
- HCl (p) E. Merck
- Alkohol 96% E. Merck
- Na-sitrat E.Merck
- Akuades
- Buah Kelapa
- Dami Nangka
3.2. Prosedur Penelitian
3.2.1. Pengambilan Sampel
Sampel berupa Dami nangka atau selaput tipis antar daging buah nangka dan
buah Kelapa diperoleh dari 1 lokasi yaitu Pajak Pagi Setia Budi Medan.
Tanaman Nangka dengan spesies Artocarpus heterophyllus lamk dan Tanaman
Kelapa dengan spesies Cocos nucifera L.
3.2.2. Pembuatan Larutan
3.2.2.1.Pembuatan H2SO4 1,25 N
Di masukkan 8,5 ml H2SO4(P) dalam labu takar 250 ml kemudian diencerkan
dengan akuades sampai garis tanda.
3.2.2.2.Pembuatan NaOH 1,25 N
Dilarutkan 12,5 g NaOH dengan akuades kemudian dimasukkan kedalam labu
takar 250 ml dan diencerkan garis tanda.
3.2.2.3.Pembuatan Larutan NaOH 3%
Dilarutkan 3 g NaOH dengan akuades kemudian dimasukkan kedalam labu
takar 100 ml dan diencerkan sampai garis tanda.
3.2.2.4.Pembuatan Larutan HCl 30 %
Dimasukkan 203 ml HCl 37% dalam labu takar 250 ml kemudian diencerkan
dengan akuades sampai garis tanda.
3.2.2.5.Pembuatan pereaksi Benedict
Dengan bantuan pemanasan, dilarutkan 173 g Na-sitrat dan 100 g Na2CO3
dalam 800 ml air . Disaring lalu ditambahkan aquades sampai volume larutan 850 ml
Bila larutan diatas sudah dingin maka dengan perlahan – lahan ditambahkan kedalam
larutan I . Kemudian ditambahkan dengan akuades sampai 1 liter.
3.2.2.6.Larutan Glukosa 20 mg/100 ml
Sebanyak 20 mg glukosa anhidrat dilarutkan dengan akuades dalam labu takar
100 ml sampai garis tanda dan dikocok sampai homogen.
3.2.2.7.Larutan pereaksi Nelson
Nelson A :
Dilarutkan12,50000 g Natrium karbonat anhidrat, 12,5000 g garam Rochelle
(K-Na-Tartrat), 10 g Natrium Bikarbonat dan 100 g Natrium Sulfat anhidrat dalam 300 ml
akuades dan diencerkan sampai 500 ml.
Nelson B :
Dilarutkan 7,5000 g CuSO4.5H2O dalam 50 ml akuades dan ditambahkan 1 tetes asam
sulfat pekat.
Pereaksi Nelson dibuat dengan cara mencampur 25 bagian larutan Nelson A dan I
bagian Nelson B. Pencampuran dilakukan setiap kali akan digunakan.
3.2.2.8.Larutan Arsenomolibdat
Dilarutkan 25 g ammonium molibdat dalam 450 ml aquades dan ditambahkan
25 ml H2SO4(p) .Dilarutkan pada tenpat yang lain 3 g Na2HAsO4.7H2O dalam 25 ml
akuades kemudian dituangkan larutan ini kedalam larutan yang pertama.
Disimpan dalam botol, berwarna coklat dan diinkubasi pada suhu 37oC selama 24 jam.
3.2.3.Cara Kerja
3.2.3.1.Penyediaan Sampel Selulosa Dami Nangka
3.2.3.1.Isolasi selulosa dari dami nangka
Sebanyak 500 g Dami Nangka dikeringkan pada suhu 1100C. Dami nangka
yang telah kering kemudian dihaluskan. Dami nangka yang telah halus kemudian
ditimbang. Setelah itu ditambahkan 200 ml alkohol 96%. Lalu, ditambahkan 200 ml
H2SO4 1,25 N direfluks selama 30 menit lalu disaring. Residu dicuci dengan akuades
panas sampai pH netral. Residu ditambahkan 200 ml NaOH 1.25 N dan direfluks
selama 30 menit. Residu dicuci dengan akuades panas sampai pH netral. Dikeringkan
dioven pada suhu 1100C selama 1 jam.
3.2.3.2.Analisa kandungan serat kasar dar dami nangka
5,0010 g dami nangka yang telah dihilangkan lemaknya ditambahkan 50 ml
H2SO4 1,25 N direfluks selama 30 menit dan disaring. Residu dicuci dengan akuades
panas sampai netral. Residu ditambahkan 50 ml NaOH 1,25 N dan direfluks selama
30 menit. Residu dicuci dengan akuades panas sampai pH netral. Dikeringkan dioven
pada suhu 1100C selama 1 jam kemudian ditanur pada suhu 6000C selama 3 jam lalu
ditimbang hingga beratnya konstan.
3.2.3.3.Hidrolisis Dami Nangka
● Ditimbang 0,5002 g sampel dimasukkan kedalam labu erlenmeyer kemudian ditambah 5 ml akuades lalu dipanaskan pada suhu 72 – 90oC.
● Lalu ditambahkan 8 ml HCl 30 % dan dihidrolisis di penangas air selama 2 jam lalu
didinginkan.
● Ditambah NaOH 3 % hingga pH netral lalu di saring,Sebanyak 1 ml filtrat
dimasukkan kedalam tabung reaksi kemudian ditambahkan 5 ml larutan benedict
3.2.3.4.Pengukuran Panjang Gelombang Maksimum Larutan Glukosa Standar.
● Ditimbang 20 mg glukosa anhidrat dan dilarutkan denagan aquades sampai volume 100 ml (larutan glukosa 0,2 mg/ml). Dipipet 25 ml larutan lalu diencerkan dengan
akuades sampai volume 100 ml (larutan glukosa 0,05 mg/ml).
● Dipipet 1 ml larutan glukosa 0,05 mg/ml kedalam tabung reaksi,lalu ditambahkan 1
ml pereaksi Nelson lalu ditutup dengan kapas dan dipanaskan pada waterbath
sampai mendidih selama 30 menit lalu didinginkan.
● Lalu di tambahkan 1 ml larutan arsenomolibdat lalu dikocok hingga semua endapan
larut.Ditambahkan 7 ml akuades lalu dikocok hingga homogen.
● Diukur serapan panjang gelombang pada 400 – 800 nm. (diperoleh panjang
gelombang maksimum).
3.2.3.5.PenyiapanKurva Standar Glukosa
● Disiapkan larutan glukosa standar dalam beberapa tabung reaksi dengan konsentrasi bertingkat dari 0,02 – 0,18 mg/ml.
● Ditambahkan 1 ml larutan Nelson kemudian dipanaskan hingga mendidih selama
30 menit dan didinginkan.
● Ditambahkan 1 ml larutan arsenomolibdat lalu dikocok. Ditambahkan 7 ml akuades lalu dikocok hingga homogen.
● Diukur serapannya pada panjang gelombang 761 nm
● Dibuat kurva standar yang menunjukkan hubungan antara konsentrasi gula standar
dan absorbansi.
3.2.3.6.Analisa Kandungan Glukosa Sampel
● Dipipet 1 ml filtrat hasil hidrolisa Dami Nangka lalu diencerkan dalam labu ukur 50 ml dan diambil 1 ml untuk dianalisa. Ditambahkan 1 ml larutan Nelson kemudian
● Ditambahkan 1 ml larutan arsenomolibdat lalu dikocok.Ditambahkan 7 ml akuades lalu dikocok hingga homogen.
● Diukur serapannya pada panjang gelombang 761 nm sehingga dapat dihitung kadar
gula reduksinya.
3.2.3.7.Pembuatan Manisan Kelapa
● Buah Kelapa ,setelah disortasi dicuci hingga bersih , lalu kulitnya di kupas.
● Potong buah Kelapa menjadi 4 bagian yang sama besarnya
● Rendam potongan buah dalam larutan kapur 10 % selama 1 jam ● Tiriskan
● Rendam kembali buah dalam larutan garam dapur 10 % selama 12 jam ● Selanjutnya lakukan blanching selama 3 menit
● Tiriskan dan cuci dengan air dingin yang mengalir
● Setelah ditiriskan , buah direndam dalam larutan gula yang telah disaring setelah
terlebih dahulu direbus dengan berbagai konsentrasi gula yang berbeda (1:0 , 1:1 ,
1:2 , 1:3 )
3.2.3.8.Penentuan Nilai Organoleptik
Uji ini meliputi warna, rasa, bau dan tekstur yang ditentukan dengan uji kesukaan oleh
15 orang panelis,dimana para panelis bukan perokok dan sebelum mencicipinya
diharuskan minum air putih terlebih dahulu. Uji ini ditentukan dengan skala hedonik,
sebagai berikut:
Uji Kesukaan (Skala hedonik) Skala Numerik
Amat sangat suka 5
Sangat suka 4
Suka 3
Kurang suka 2
3.3. Bagan Penelitian
3.3.1. Isolasi Selulosa dari dami nangka
500 g Dami Nangka
Dikeringkan pada suhu 110oC Dihaluskan
Dami Nangka Halus
453,2213 g Dami Nangka Halus
Ditambahkan 200 ml Alkohol 96% Disaring
Filtrat 272,9083 g Residu
Dicuci dengan akuades panas hingga pH netral Ditambah 200 ml NaOH 1,25 N
Direfluks selama 30 menit Disaring
Filtrat 163,9183g Residu
Dicuci dengan akuades panas hingga pH netral
Dikeringkan pada suhu 110oC Ditimbang
Hasil
Filtrat
3.3.2. Analisa Kadar Serat Kasar dari Dami Nangka
5,0010 g Dami Nangka yang telah dihilangkan lemaknya
Ditambah 50 ml H2SO4 1,25 N Direfluks selama 30 menit Disaring
3,6944 g residu
Dicuci dengan akuades panas sampai pH netral Disaring
filtrat
1,6250 g residu
Ditambah 50 ml NaOH 1,25 N Direfluks selama 30 menit Disaring
filtrat
1,6525 g residu
Dicuci dengan akuades panas sampai pH netral Disaring
1,6208 g residu
Dikeringkan pada suhu 110oC Ditimbang
0,7250 g residu
Ditanur pada suhu 600oC selama 3 jam Ditimbang
filtrat
filtrat
filtrat
3.3.3. Hidrolisis Selulosa serta Uji gula Reduksinya
0,5002 g Selulosa
Ditambahkan 5 ml akuades sambil diaduk Ditambahkan 5 ml akuades sambil diaduk
Dipanaskan di penangas air pada suhu 72-90oC
Campuran sampel dan air
Sampel terhidrolisis
Dinetralkan dengan NaOH 3% Disaring
Dipipet 1 ml filtrat kedalam tabung reaksi
Dipanaskan dipenangas air
Residu filtrat
Ditambahkan 5 ml larutan Benedict secara kualitatif
Endapan merah bata Ditambah 8 ml HCl 30% Ditutup dengan alumunium foil
3.3.4. Analisa Kandungan Glukosa Hasil Hidrolisis
25 filtrat hasil hasil hidrolisis selulosa
Dimasukkan kedalam labu takar 250 ml
Diencerkan dengan akuades sampai garis tanda
Dipipet sebanyak 1 ml
1 ml larutan glukosa sampel
Dimasukkan kedalam tabung reaksi
Ditambahkan 1 ml pereaksi Nelson
Ditutup dengan kapas
Dipanaskan dipenangas air pada suhu 100oC selama 30 menit
Didinginkan dibawah air yang mengalir
Larutan dengan endapan merah bata
Diaduk hingga homogen
Ditambahkan 1 ml larutan arsenomolibdat
Diaduk hingga endapan larut
Larutan berwarna biru
Ditambahkan 7 ml akuades
Diaduk hingga homogen
Diukur absorbansinya pada panjang gelombang 761 nm
3.3.5. Pembuatan Manisan
3.3.6.Penentuan Nilai Organoleptik 100 g Buah kelapa
Dilakukan sortasi
Dikupas kulitnya
Dicuci hingga bersih
Dirajang
Hasil
Direndam dalam larutan kapur 10%
Ditiriskan dan dicuci dengan air bersih Direndam dengan larutan gula
Panelis
Di undang ke Laboratorium Di sajikan sampel
Diharuskan kepada panelis
meminum air putih terlebih dahulu
Panelis dan Sampel
Dilakukan uji kesukaan (warna , rasa ,bau dan tekstur).
Ditentukan skor nilainya
BAB 4
HASIL DAN PEMBAHASAN
4
.1.Hasil Penelitian4.1.1.Perhitungan Kadar Serat Kasar Dami Nangka
Perhitungan kadar serat kasar dapat dihitung dengan rumus sebagai berikut :
Dimana :
B = Berat sampel setelah pengeringan 1100 C S = Berat sampel setelah pengeringan 6000 C
BS = Berat sampel mula – mula
Maka kadar serat kasarnya adalah :
S = Kadar serat kasar
S1 = 5,2338 %
S2 = 6,1134 %
S3 = 5,8455 %
( Hasil pengukuran kadar serat kasar selengkapnya terdapat pada tabel 3.3)
4.1.2. Pengolahan Data Pengukuran absorbansi Glukosa Hasil Hidrolisis Selulosa Dami Nangka
Pengolahan data pengukuran absorbansi glukosa hasil hidrolisis selulosa dami
nangka dilakukan secara statistik dengan metode Chauvenet Criterion Test (CCT)
yang diambil dari data absorbansi pada tabel 4.4.
Untuk melakukan metode Chauvenet Criterion Test (CCT) perlu harga ht dan hh dapat
dihitung dengan menggunakan rumus:
Maka ht = 22,6852
Sedangkan hhitung adalah
Karena 22,6852 > 18,7969 ( ht > hh ), maka data signifikan dan dapat diterima, data
pengukuran pertama dan ketiga juga signifikan.
4.1.3. Perhitungan Kadar Glukosa Hasil Hidrolisis Selulosa Dami Nangka
Untuk Menghitung kadar glukosa hasil hidrolisis selulosa dami nangka terlebih dahulu
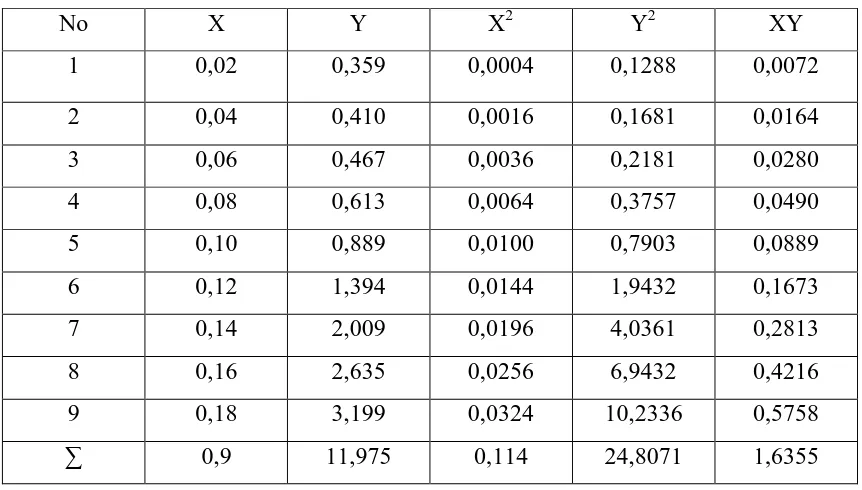
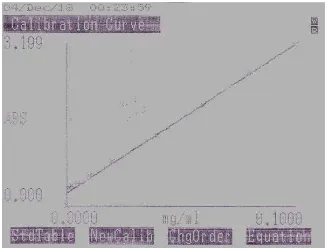
harus dicari persamaan garis regresi larutan glukosa standar dari berbagai konsentrasi.
Tabel 4.1. Larutan Glukosa Standar Pada Berbagai Konsentrasi
(
)
Maka persamaan garis regresinya adalah
Y = aX + b
Absorbansi suatu pengukuran adalah 0,3881 dengan volume labu takar 250 ml dan
berat sampel kering 0,5000 g(500 mg) , maka :
0484
Setelah diperoleh harga Xsampel kemudian disubstitusikan kedalam rumus:
%
Hasil pengukuran kadar gula reduksi hasil hidrolisis selulosa selengkapnya terdapat
S2 =
Sedangkan hhitung adalah
Karena 13,7174 > 8,2840 ( ht > hh ), maka data signifikan dan dapat diterima, data
4.2. Pembahasan
Hidrolisis selulosa dapat dilakukan dengan menggunakan asam atau enzim. Jika
selulosa dipanaskan dengan asam maka akan terurai menjadi monomer – monomernya
lebih kecil dengan tahapan yang berbeda tapi hasilnya yaitu glukosa.
Dari hasil hidrolisis selulosa dami nangka dengan menggunakan HCl 30%
maka dihasilkan sirup glukosa. Setelah diidentifikasi secara kualitatif dengan reagen
Benedict menunjukkan hasil positif bahwa amilum selulosa dami nangka
mengandung glukosa (gula reduksi) dengan terbentuknya endapan merah bata.
Selanjutnya ditentukan kandungan glukosa dengan metode Nelson Somogyi
menggunakan alat spektrofotometer pada panjang gelombang 761 nm.
Dari penelitian ini diperoleh kadar serat selulosa diperoleh sebesar 5,7303%
untuk 5,0021 g kering dami nangka. Kadar glukosa hasil hidrolisis selulosa sebesar
2,4667 %. Hal tersebut menunjukkan bahwa selulosa dari dami nangka dapat menjadi
salah satu alternatif pengganti gula pasir.
Dari penelitian ini dapat diketahui bahwa sirup glukosa dari selulosa dami
nangka dapat dimanfaatkan sebagai pemanis untuk mengganti gula pasir.
Berdasarkan uji organoleptik yang dilakukan dapat diketahui bahwa manisan
buah kelapa dengan gula pasir lebih disukai oleh panelis dibandingkan dengan
manisan dari sirup glukosa. Perbandingan antara gula pasir dan sirup glukosa adalah
1 : 0, 1 : 1, 1 : 2, dan 1 : 3. Untuk perbandingan 1 : 0, panelis memberikan skor 4 pada
manisan. Untuk perbandingan 1 : 1, panelis memberikan skor 3 pada manisan. Untuk
perbandingan 1 : 2, panelis memberikan skor 3 pada manisan. Dan untuk
perbandingan 1 : 3, panelis memberikan skor 3 pada manisan. Namun dalalm hal ini
peneliti membuat manisan dengan perbandingan pemanis menggunakan glukosa
BAB 5
KESIMPULAN DAN SARAN
5.1. Kesimpulan
Dari hasil penelitian dapat disimpulkan bahwa selulosa yang terdapat dalam dami
nangka setelah dihidrolisis menjadi sirup glukosa memberikan kemanisan pada
pembuatan manisan dari buah kelapa dan dapat dimanfaatkan sebagai pengganti gula
pasir.
5.2. Saran
Kepada peneliti selanjutnya, disarankan untuk membuat sirup glukosa dari limbah
lainnya dengan membuat manisan dengan perbandingan pemanis menggunakan
DAFTAR PUSTAKA
Apriyanto. A. 1989. Analisa Pangan . Bogor : IPB Press.
Amin. S. 2009. Cocopreneurship Aneka Peluang Bisnis Dari Kelapa. Yogyakarta: Andi Offset.
Ashari. S.2006. Meningkatkan Keunggulan Buahan Tropis Indonesia. Yogyakarta: Andi Offset.
Cakebread. S. 1975. Sugar And Chocolate Confectionery. Oxford University Press : London.
Day. R. A.,Underwood. A. L. 1999. Analisa Kimia Kuantitatif. Edisi keempat. Erlannga : Jakarta.
Deman. J.M. 1997. Kimia Makanan.Terjemahan Kosasih Padmawinata. Bandung : Penerbit ITB
Dziedzic. S. Z. and Kearsley, M. W. (1984).Glucose Syrups: Science and Technology, England : Elsevier Applied Science Publishers Ltd.
Fatah. M.A.dan Bachtiar,Y.2004. Membuat Manisan Buah.Jakarta : PT. AgroMedia Pustaka.
Fengel. D. 1992. Kayu,Kimia,Ultrastruktur,Reaksi-Reaksi. Yogyakarta : Gadjah Mada Press
Fessenden. R.J.,Fessenden.J.S.1999.Kimia Organik.Edisi Ketiga.Jilid kedua. Jakarta : Erlangga.
Fogarty. W.M.1983.Microbial Enzyme and Biotechnology. London : Applied sciences Publishing.
Girindra. A. 1990. Biokimia 1. Jakarta : PT Gramedia
Ketaren. S. 1986.Pengantar Teknologi Minyak dan Lemak Pangan. Jakarta: Penerbit Universitas Indonesia (UI Press).
Lynd. L.R. 2002.Microbial Cellulosa Utilization Fundamental & Biotechnology. London : Applied Sciene Publisher.
Muchlisan. F. 1994.Buah Komersil. Jakarta : PT. Penebar Swadaya.
Poedjiadi. A. 1994. Dasar-Dasar Biokomia. Jakarta : UI-Press.
Rohman. A. 2007. Kimia Farmasi Analisis : Spektrofotometri UV dan Tampak
(visibel). Yogyakarta : Pustaka Pelajar.
Rukmana. R.1997.Budi Daya Nangka.Yogyakarta : Kanisius
Sediaoetama. A.J.1986. Ilmu Gizi. Jakarta : Penerbit Dian Rakyat
Soekarto.S.T. 1981. Penilaian Organoleptik untuk Industri Pangan dan Hasil
Pertanian .Bogor : ITB.
Sunarjono. H.H. 2008. Berkebun 21 Jenis Tanaman Buah. Jakarta: Penebar Swadaya.
Sudarmadji. S. 1989. Analisa Bahan Makanan dan Pertanian. Yogyakarta : Liberti
Thieme. J. G.1968.Tanaman Kelapa Budidaya dan Pemanfaatannya.Penerbit Kanisius.
Winarno. F. G. 1997. Kimia Pangan dan Gizi. Yogyakarta: PT. Gramedia Pustaka Utama.
Winarno.F.G. 1893. Enzim Pangan. Jakarta : PT. Gramedia Pustaka Utama
Winarno.F.G.1995.Pengantar Teknologi Pangan.Jakarta : Gramedia Pustaka Utama.
Wijayanti. L.2005.Pengaruh Temperatur dan Durasi Inkubasi Kadar Alkohol dari
Fermentasi Glukosa Hasil Hidrólisis Rumput Gajah (PennisetumPpurperum) dengan HCl 3% menggunakan Saccharomyces cereviciae.Skripsi S-1.Jurusan
Lampiran 1.
Tabel 1.1. Data Hasil Perhitungan Kadar Serat Dami Nangka Perulangan Berat Abu
( g )
Kadar Serat Kasar ( % )
Rata-rata
I 0,4632 5,233 %
5,73%
II 0,4192 6,113 %
II 0,4326 5,845 %
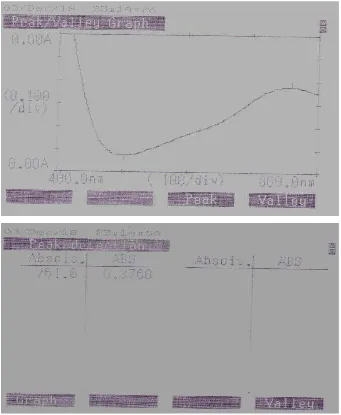
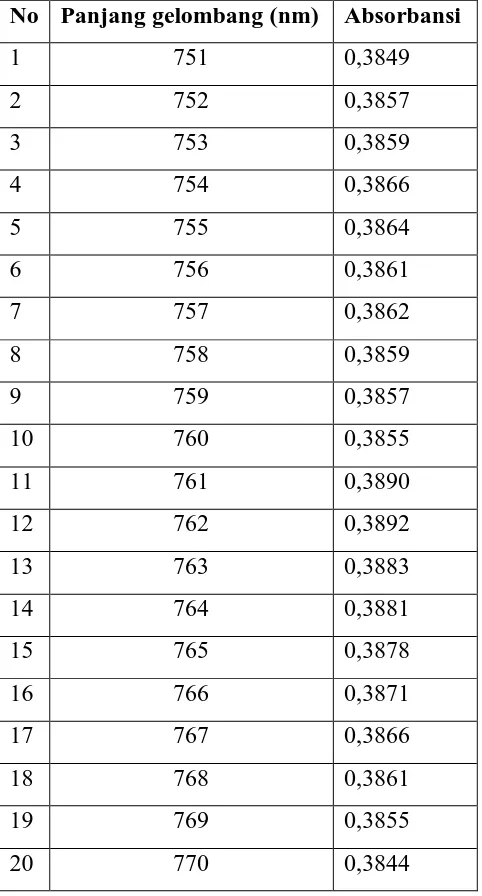
Tabel. 2.2. Data Absorbansi Larutan Glukosa Standar(0,05 mg/mL) Pada Berbagai panjang delombang
No Panjang gelombang (nm) Absorbansi
1 751 0,3849
2 752 0,3857
3 753 0,3859
4 754 0,3866
5 755 0,3864
6 756 0,3861
7 757 0,3862
8 758 0,3859
9 759 0,3857
10 760 0,3855
11 761 0,3890
12 762 0,3892
13 763 0,3883
14 764 0,3881
15 765 0,3878
16 766 0,3871
17 767 0,3866
18 768 0,3861
19 769 0,3855
Lampiran 3.
Tabel. 3.3. Data Absorbansi Larutan Glukosa Standar Pada Berbagai Konsentrasi pada λ Maksimum 761 nm
Konsentrasi ( mg/mL ) Absorbansi
0,02 0,359
0,04 0,410
0,06 0,467
0,08 0,613
0,10 0,889
0,12 1,394
0,14 2,009
0,16 2,635
0,18 3,199
Lampiran. 4. Data Analisa Kandungan Glukosa Hasil Hidrolisis Dami Nangka
Tabel. 4.4. Data Hasil Perhitungan Kadar Gula Reduksi Berdasarkan Absorbansi Glukosa Hasil Hidrolisis Selulosa Dami Nangka
No Absorbansi Kadar Gula Reduksi
( % )
Ratrata
1 0,3811 2,395 %
2,4667 %
2 0,4497 2,585 %
Lampiran. 5.
Lampiran 6.
Tabel 6.6. Data Hasil Pengukuran Organoletik Terhadap Warna Manisan kelapa
Panelis
Gula Pasir : Sirup Glukosa Hasil Hidrolisis Selulosa dami nangka
1 : 0
( mL )
1: 1
( mL )
1 : 2
( mL )
1 : 3
( mL )
1 5 3 3 4
2 5 4 3 4
3 5 4 3 3
4 4 3 3 3
5 3 3 4 4
6 3 3 4 3
7 3 3 3 4
8 4 3 3 2
9 4 2 4 3
10 4 2 4 2
11 4 3 4 4
12 3 3 2 3
13 5 3 2 4
14 3 4 3 3
15 4 4 3 4
Total 59 47 48 50
Tabel 6.7. Data Hasil Pengukuran Organolerptik TerhadapRasa Manisan kelapa
Panelis
Gula Pasir : Sirup Glukosa Hasil Hidrolisis Selulosa Dami Nangka
1 : 0
( mL )
1: 1
( mL )
1 : 2
( mL )
1: 3
( mL )
1 3 3 2 3
2 5 3 3 3
3 5 2 5 2
4 5 2 3 3
5 5 2 3 3
6 3 4 3 2
7 4 4 4 2
8 3 3 4 4
9 4 3 2 3
10 4 2 2 3
11 4 1 1 3
12 5 2 3 3
13 3 3 1 2
14 5 1 3 4
15 4 3 3 4
Total 62 38 42 44
Tabel 6.8. Data Hasil Pengukuran Organoleptik Terhadap Aroma Manisan kelapa
Panelis
Gula Pasir : Sirup Glukosa hasil hidrolisis Selulosa Dami Nangka
1 : 0
( mL )
1 : 1
( mL )
1: 2
( mL )
1 : 3
( mL )
1 4 3 4 3
2 4 3 3 4
3 4 3 3 4
4 4 1 3 4
5 4 4 3 4
6 3 4 3 3
7 5 4 2 2
8 3 3 3 2
9 5 2 2 3
10 3 4 2 3
11 5 3 4 3
12 5 1 4 3
13 5 3 3 2
14 3 3 3 2
15 4 4 3 2
Total 61 45 45 44