ANALISA PERUBAHAN KANDUNGAN NITRIT ( NO2
-)
DALAM HASIL REBUSAN SAYUR BAYAM HIJAU DENGAN
METODE SPEKTROFOTOMETRI
TESIS
Oleh:
HAPOSAN MANALU
097006002/KIM
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
UNIVERSITAS SUMATERA UTARA
ANALISA PERUBAHAN KANDUNGAN NITRIT (NO2
-)
DALAM HASIL REBUSAN SAYUR BAYAM HIJAU DENGAN
METODE SPEKTROFOTOMETRI
TESIS
Diajukan sebagai salah satu syarat untuk memperoleh gelar Magister Sains Dalam Program Studi Ilmu Kimia Pada Fakultas Matematika dan Ilmu
Pengetahuan Alam Universitas Sumatera Utara Medan
Oleh:
HAPOSAN MANALU
097006002/KIM
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
UNIVERSITAS SUMATERA UTARA
Judul Tesis
: ANALISA PERUBAHAN KANDUNGAN
NITRIT (NO
2
-) DALAM HASIL REBUSAN
SAYUR BAYAM HIJAU DENGAN METODE
SPEKTROFOTOMETRI
Nama Mahasiswa : HAPOSAN MANALU Nomor Pokok : 097006002
Program Studi : Ilmu Kimia
Fakultas : Matematika dan Ilmu Pengetahuan Alam Universitas Sumatera Utara Medan
Menyetujui: Komisi Pembimbing :
Dr. Tini Sembiring, MS.
Ketua Anggota
Drs. Ahmad Darwin, MSc.
Ketua Program Studi : Dekan :
Prof. Basuki Wirjosentono, MS, Ph. D.
NIP: 195204181980021001 NIP: 196310261991031001 Dr. Sutarman, MSc.
Telah diuji pada Tanggal 29 Juli 2011
PANITIA PENGUJI TESIS
Ketua : Dr. Tini Sembiring, MS Anggota : 1. Drs. Ahmad Darwin, MSc
PERNYATAAN ORISINALITAS
ANALISA PERUBAHAN KANDUNGAN NITRIT (NO2
-)
DALAM REBUSAN SAYUR BAYAM HIJAU DENGAN METODE
SPEKTROFOTOMETRI
TESIS
Dengan ini saya menyatakan bahwa yang tertulis dalam tesis ini benar-benar hasil karya sendiri dan sepanjang pengetahuan saya tidak terdapat pendapat atau karya yang pernah ditulis atau diterbitkan oleh orang lain kecuali secara tertulis diacu dalam naskah dan disebutkan sumbernya dalam daftar pustaka. Pendapat atau temuan dalam tesis ini dikutip berdasarkan kode ilmiah.
Medan, 29 Juli 2011
Penulis,
PERNYATAAN PERSETUJUAN PUBLIKASI
KARYA ILMIAH UNTUK KEPENTINGAN AKADEMIS
Sebagai civitas akademika Universitas Sumatera Utara , saya yang bertanda tangan di bawah ini :
Nama : HAPOSAN MANALU
NIM : 097006002
Program Studi : Ilmu Kimia Jenis Karya Ilmiah : Tesis
Demi pengembangan ilmu pengetahuan, menyetujui untuk memberikan kepada Universitas Sumatera Utara Hak Bebas Royalti Non-Eksklusif (Non Exclusive Royalty Free Right) atas tesis saya yang berjudul:
ANALISA PERUBAHAN KANDUNGAN NITRIT (NO2-) DALAM HASIL
REBUSAN SAYUR BAYAM HIJAU DENGAN METODE
SPEKTROFOTOMETRI
Beserta perangkat yang ada (jika diperlukan). Dengan hak bebas royalty non eksklusif ini, Universitas Sumatera Utara berhak menyimpan, mengalih media, memformat, mengelola dalam bentuk data base, merawat dan mempublikasikan tesis saya tanpa meminta izin dari saya selama tetap mencantumkan nama saya sebagai penulis dan pemegang dan atau sebagai pemilik hak cipta.
Medan, 29 Juli 2011
Penulis,
ANALISA PERUBAHAN KANDUNGAN NITRIT (NO
2-) DALAM
HASIL REBUSAN SAYUR BAYAM HIJAU DENGAN METODE
SPEKTROFOTOMETRI
ABSTRAK
Penelitian tentang perubahan kandungan nitrit (NO2-) dalam hasil rebusan
sayur bayam hijau telah dilakukan. Sayur bayam diperoleh dari kebun sayur petani Desa Kebun Baru, Kecamatan Hamparan Perak, Kabupaten Deli Serdang. Kandungan nitrit ditentukan pada rebusan sayur bayam dan air rebusan sayur bayam dengan metode spektrofotometri. Dari hasil penelitian diperoleh nilai kandungan pada rebusan sayur bayam dengan variasi waktu 0, 1, 2, 3, 4, dan 5 jam masing-masing adalah 4,159; 5,319; 7,239; 8,719; 10,149 dan 11,559 mg/kg. Nilai kandungan nitrit pada air rebusan sayur bayam masing-masing 1,729; 3,349; 3,889; 4,969; 6,129 dan 7,079 mg/kg. Sehingga diperoleh nilai total kandungan nitrit pada rebusan sayur bayam dan air rebusan sayur bayam adalah 5,888; 8,668; 11,128; 13,688; 16,278 dan 18,638 mg/kg. Penyimpanan hasil rebusan sayur bayam hijau selama 5 jam aman dikonsumsi untuk seseorang yang berat badannya 60 kg sebanyak ± 428,16 gr hasil rebusan sayur bayam sesuai ketentuan ADI (Acceptable Daily Intake)/Jumlah Asupan Harian menurut WHO (Word Healthy Organisation).
ANALYSIS OF NITRITE (NO
2-) CHANGE VEGETABLE
IN THE RESULT OF THE BOILED GREEN SPINACH
VEGETABLE SPECTROPHOTOMETRY METHOD
ABSTRACT
The research has been carried out on the changing of nitrite (NO2-) content in a vegetable stew of green spinach. Vegetable spinach were obtained from Kebun Baru Village farmers, Kecamatan Hamparan Perak, Kabupaten Deli Serdang. Content of nitrite were determined at vegetable spinach and the water of boiled vegetable spinach using spectrophotometric methods. From the results of the research it was obtained with variations in time 0, 1, 2, 3, 4, and 5 hours were 4,159; 5,319; 7,239; 8,719; 10, 149 dan 11,559 mg/kg. Value content of nitrites content of the the water boiled spinach were 1,729; 3,349; 3,889; 4,969; 6,129 dan 7,079 mg/kg. Respectively in order to obtain the total value of the content at boiled vegetable spinach there for of were 5,888; 8,668; 11,128; 13,688; 16,278 dan 18,638 mg/kg. Storaging of result of boiled vegetable spinach during 5 hours was seaved for consumtion for the people with its weight body 60 kgs in the result of boiled spinach vegetable according to total amount 428,16 grams of the result according with maximum limit of Acceptable Daily Intake (ADI).
KATA PENGANTAR
Puji dan syukur kepada Tuhan yang Maha Esa karena atas berkat dan
rahmat-Nya, penulis dapat menyelesaikan tesis ini dengan judul: ˮ Analisa Perubahan
Kandungan Nitrit (NO2-) dalam Rebusan Sayur Bayam Hijau dengan Metode
Spektrofotometri ˮ yang merupakan salah satu syarat bagi penulis dalam
menyelesaikan pendidikan dalam Program Magister Ilmu Kimia pada Fakultas
Matematika dan Ilmu Pengetahuan Alam Universitas Sumatera Utara Medan.
Dalam penulisan tesis ini tidak terlepas dari bimbingan, dukungan dan bantuan
dari berbagai pihak, baik secara moril maupun materil. Untuk itu penulis
menyampaikan ucapan terima kasih yang sebesar-besarnya kepada :
1. Ibu Dr. Tini Sembiring, MS., selaku Ketua Komisi Pembimbing yang telah banyak
memberikan arahan dan bimbingan.
2. Bapak Drs. Ahmad Darwin, MSc., selaku Anggota Komisi Pembimbing yang telah
membantu penulis selama penyelesaian tesis.
3. Bapak Prof. Basuki Wirjosentono, MS, PhD, selaku Ketua Program Studi yang
sudah memberikan bimbingan.
4. Kepada seluruh staf dosen di Program Magister Kimia yang memberikan mata
kuliah.
5. Kepada pegawai, kak Leli yang telah banyak membantu dalam administrasi.
6. Kepada pihak Universitas Sumatera Utara yang telah memberi wadah pendidikan
kepada penulis dalam melanjutkan pendidikan.
7. Istriku Helena Gultom, SP., dan putraku Surya Andreas Manalu yang telah
memberikan semangat dan dukungan mulai dari perkuliahan sampai penyelesaian
tesis.
8. Frans Simanjuntak, SSi., Asisten Pusat Penelitian Universitas Sumatera Utara
9. Rekan-rekan mahasiswa Program Studi Ilmu Kimia S2 kelas Regular angkatan
2009 (Sumatera Tarigan, Hendry Faisal, Lintong S. Pane, Ahmad Hafizullah,
Fendi Sinaga, Elliwati Hasibuan, Cut Wira, Ely Suryani Harahap dan Sri
Kuncoro), semoga tetap terjalin kebersamaan walaupun latar belakang, tugas dan
tempat yang berbeda.
10. Ibu Dra. Norma Sinaga, selaku pembimbing selama penelitian di Laboratorium
Kesehatan Medan.
11. Kakak Johana Gultom, SE dan abang ipar Tiopan Gultom yang telah memberi
dukungan dan bantuan kepada penulis.
12. Mertua penulis ibu Elmina Simanjuntak, yang sedang menjalani perawatan di
Rumah Sakit Penang.
13. Orangtua penulis, ibu Tiomas Nababan yang memberikan dukungan kepada
penulis.
14. Semua pihak yang tidak dapat penulis sebutkan satu persatu yang memberikan
dukungannya kepada penulis.
Penulis menyadari bahwa apa yang disajikan dalam tesis ini masih jauh dari
kesempurnaan, untuk itu penulis mengharapkan saran dan kritik yang membangun
dari pihak pembaca untuk perbaikan tulisan penulis di kemudian hari.
Akhirnya kepada semua pihak yeng telah membantu dan mendukung
penyelesaian tesis ini , penulis mengucapkan terima kasih. Semoga tesis ini
bermanfaat bagi pembaca.
Medan, 29 Juli 2011
Penulis,
DAFTAR RIWAYAT HIDUP
DATA PRIBADI
Nama : HAPOSAN MANALU
Tempat/Tanggal Lahir : Siborongborong/1 Desember 1969
Jenis Kelamin : Laki-laki
Agama : Kristen
Alamat : Jl. Belibis I No. 16 Perumnas Mandala Medan -
20226
No. Hp : 081264432116
E-mail : haposan_manalu_12@yahoo.co.id
PENDIDIKAN
- SD : SD Negeri No. 173311 Siborongborong, kabupaten Tapanuli Utara
tahun 1976-1982.
- SMP : SMP Negeri 1 Siborongborong, kabupaten Tapanuli Utara
tahun 1982-1985.
- SMA : SMA Negeri 9 Medan tahun 1985-1988.
- Strata -1 : Universitas HKBP Nommensen Medan Fakultas Pertanian Jurusan
Teknologi Hasil Pertanian tahun 1989-1995.
- Akta – IV : Universitas Negeri Medan tahun 2003.
- Strata – 2 : Universitas Sumatera Utara Medan Program Studi Ilmu Kimia tahun
DAFTAR ISI
Halaman
ABSTRAK i
ABSTRACT ii
KATA PENGANTAR iii
DAFTAR RIWAYAT HIDUP v
DAFTAR ISI vi
DAFTAR TABEL viii
DAFTAR GAMBAR ix
DAFTAR LAMPIRAN x
BAB 1. PENDAHULUAN 1.1. Latar Belakang 1
1.2. Rumusan Masalah 3
1.3. Pembatasan Masalah 3
1.4. Tujuan Penelitian 3
1.5. Manfaat Penelitian 4
1.6. Lokasi Penelitian 4
BAB 2. TINJAUAN PUSTAKA 2.1. Sayuran 5
2.1.1. Pengertian Sayuran 5
2.1.2. Kandungan Gizi Sayuran 5
2.1.3. Manfaat Sayuran Bagi Kesehatan 6
2.2. Tumbuhan Bayam 6
2.3. Nitrit 9
2.3.1. Defenisi Nitrit 9
2.3.2. Sifat Fisik dan Struktur Kimia Nitrit 11
2.3.3. Methemoglobin 12
2.3.4. Keracunan Nitrit 14
2.4. Kinetika Kimia 14
2.4.1. Efek Katalis 14
2.5. Karbon Aktif 17
2.6. Istilah dalam Penulisan 19
BAB 3. METODE PENELITIAN 3.1. Alat dan Bahan 20
3.2. Bahan-bahan 21
3.3. Prosedur Penelitian 21
3.3.1. Penyediaan Bahan Pereaksi 21
3.3.2. Lokasi Pengambilan Sampel 22
3.3.3. Metoda Pengambilan Sampel 22
3.3.4. Prosedur Pengukuran Sampel 22
3.4. Bagan Penelitian 26
3.4.1. Preparasi Sampel 26
3.4.2. Pengukuran Konsentrasi nitrit 27
BAB 4. HASIL DAN PEMBAHASAN 4.1. Hasil Analisis Sampel 32
4.1.1. Pengukuran Kadar Nitrit 32
4.1.2. Penurunan Persamaan Garis Regresi 32
4.1.3. Perhitungan Koefisien Korelasi 34
4.1.4. Penentuan Penyerapan Nitrit oleh Karbon Aktif 34
4.1.5. Penentuan Kadar Nitrit 36
4.1.6. Perhitungan Jumlah Hasil Sayur Bayam yang Dapat Dikonsumsi Setiap hari Berdasarkan Kadar Nitrit dalam Sayur Bayam 40
4.2. Pembahasan 42
BAB V KESIMPULAN DAN SARAN 5.1. Kesimpulan 45
5.2. Saran 45
DAFTAR PUSTAKA 46
DAFTAR TABEL
Nomor Judul Halaman
Tabel 1.1. Komposisi Zat Gizi Bayam dalam 100 g Bayam Segar 8
Tabel 4.1. Hasil Pengukuran Absorbansi Larutan Standar Nitrit untuk Kurva Kalibrasi tanpa Karbon Aktif 33
Tabel 4.2. Hasil Pengukuran Absorbansi Larutan Standar Nitrit untuk Kurva Kalibrasi dengan Karbon Aktif 33
Tabel 4.3. Hasil penyerapan konsentrasi nitrit oleh karbon aktif Pada larutan standar 34
Tabel 4.4. Penurunan Persamaan Garis Regresi dengan Metode Least Square 34
Tabel 4,5. Hasil Pengukuran Kadar Nitrit pada Sayur Bayam tanpa Direbus 37
Tabel 4.6. Hasil Pengukuran Kadar Nitrit pada Rebusan Sayur Bayam 38
Tabel 4.7. Hasil Pengukuran Kadar Nitrit pada Air Rebusan Sayur Bayam 39
Tabel 4.8. Total Pengukuran Kadar Nitrit Sayur Bayam yang Direbus 40
Tabel 4,9. Jumlah Rebusan Sayur Bayam + Air Rebusan Bayam yang Aman untuk Dikonsumsi Setiap Hari dengan Kandungan Nitrit yang Sesuai Batas ADI 41
DAFTAR GAMBAR
Nomor Judul Halaman
Gambar 2.1. Grafik kecepatan awal terbentuknya hasil reaksi (P) pada keadaan mantap untuk berbagai konsentrasi awal
substrat (S) 17
DAFTAR LAMPIRAN
Nomor Judul Halaman
Lampiran 1. Contoh Perhitungan 49
Lampiran 2. Surat Keterangan Melakukan Penelitian 50
Lampiran 3. Gambar Gambar 1. Lokasi Pengambailan Sampel 51
Gambar 2. Teknik Pengambilan Sampel 51
Gambar 3. Balai Laboratorium Kesehatan Medan 52
Gambar 4. Spektrofotometer Sinar Tampak Spek 300 52
Gambar 5. Larutan Seri Standar Nitrit 53
Gambar 6. Stamper dan mortir penggilingan bayam 53
Gambar 7. Sampel mengandung karbon aktif 54
Gambar 8. Sampel yang sudah ditambah Reagent 54
Gambar 9. Karbon Aktif 55
ANALISA PERUBAHAN KANDUNGAN NITRIT (NO
2-) DALAM
HASIL REBUSAN SAYUR BAYAM HIJAU DENGAN METODE
SPEKTROFOTOMETRI
ABSTRAK
Penelitian tentang perubahan kandungan nitrit (NO2-) dalam hasil rebusan
sayur bayam hijau telah dilakukan. Sayur bayam diperoleh dari kebun sayur petani Desa Kebun Baru, Kecamatan Hamparan Perak, Kabupaten Deli Serdang. Kandungan nitrit ditentukan pada rebusan sayur bayam dan air rebusan sayur bayam dengan metode spektrofotometri. Dari hasil penelitian diperoleh nilai kandungan pada rebusan sayur bayam dengan variasi waktu 0, 1, 2, 3, 4, dan 5 jam masing-masing adalah 4,159; 5,319; 7,239; 8,719; 10,149 dan 11,559 mg/kg. Nilai kandungan nitrit pada air rebusan sayur bayam masing-masing 1,729; 3,349; 3,889; 4,969; 6,129 dan 7,079 mg/kg. Sehingga diperoleh nilai total kandungan nitrit pada rebusan sayur bayam dan air rebusan sayur bayam adalah 5,888; 8,668; 11,128; 13,688; 16,278 dan 18,638 mg/kg. Penyimpanan hasil rebusan sayur bayam hijau selama 5 jam aman dikonsumsi untuk seseorang yang berat badannya 60 kg sebanyak ± 428,16 gr hasil rebusan sayur bayam sesuai ketentuan ADI (Acceptable Daily Intake)/Jumlah Asupan Harian menurut WHO (Word Healthy Organisation).
ANALYSIS OF NITRITE (NO
2-) CHANGE VEGETABLE
IN THE RESULT OF THE BOILED GREEN SPINACH
VEGETABLE SPECTROPHOTOMETRY METHOD
ABSTRACT
The research has been carried out on the changing of nitrite (NO2-) content in a vegetable stew of green spinach. Vegetable spinach were obtained from Kebun Baru Village farmers, Kecamatan Hamparan Perak, Kabupaten Deli Serdang. Content of nitrite were determined at vegetable spinach and the water of boiled vegetable spinach using spectrophotometric methods. From the results of the research it was obtained with variations in time 0, 1, 2, 3, 4, and 5 hours were 4,159; 5,319; 7,239; 8,719; 10, 149 dan 11,559 mg/kg. Value content of nitrites content of the the water boiled spinach were 1,729; 3,349; 3,889; 4,969; 6,129 dan 7,079 mg/kg. Respectively in order to obtain the total value of the content at boiled vegetable spinach there for of were 5,888; 8,668; 11,128; 13,688; 16,278 dan 18,638 mg/kg. Storaging of result of boiled vegetable spinach during 5 hours was seaved for consumtion for the people with its weight body 60 kgs in the result of boiled spinach vegetable according to total amount 428,16 grams of the result according with maximum limit of Acceptable Daily Intake (ADI).
BAB 1 PENDAHULUAN
1.1. Latar Belakang
Bayam (Amarantus tricolor L) termasuk jenis sayuran daun yang sudah lama
dikenal dan dibudidayakan secara luas di Indonesia. Bayam merupakan salah satu
jenis sayuran komersil yang mudah diperoleh di setiap pasar, baik pasar tradisional
maupun pasar modern. Bayam umumnya diperdagangkan dalam bentuk bayam cabut
dan bayam petik. Harganya relatif murah sehingga dapat terjangkau oleh semua
lapisan masyarakat (Sutarno. H, 1994).
Menurut hasil survey tanaman sayuran Indonesia (Rukmana, 1994) tanaman
bayam (Amarantus tricolor L) tersebar hampir di seluruh wilayah nusantara.
Tanaman bayam menempati urutan ke-11 dari 18 jenis sayuran komersil yang
dibudidayakan dan dihasilkan di Indonesia. Bayam juga merupakan bahan sayuran
daun yang bergizi tinggi sehingga termasuk salah satu tanaman pekarangan yang
dianjurkan dalam rangka menunjang Usaha Perbaikan Gizi Keluarga (UPGK).
Bahkan di beberapa negara berkembang bayam dipromosikan sebagai sumber protein
nabati.
Bayam mengandung sedikit kalori dengan kandungan karbohidrat dan lemak
yang relatif rendah, tetapi kaya akan kandungan β-karoten (provitamin A), vitamin C
(asam askorbat), kalsium dan mineral terutama zat besi (Direktorat Gizi Depkes RI,
1996).
Selain sebagai sayuran yang bergizi tinggi, bayam juga dapat dimanfaatkan
sebagai obat berbagai macam penyakit. Kandungan vitamin A dalam bayam berguna
untuk memberikan ketahanan tubuh dalam menanggulangi penyakit mata, sakit
pernafasan, kesehatan kulit dan selaput lendir, Vitamin B dapat mencegah penyakit
beri-beri, memperkuat syaraf, dan melenturkan otot rahim, Vitamin C dapat
penyakit anemia (kurang darah) dan sakit kuning serta memperkuat tulang dan gigi
(Bandini. Y, 2001).
Tetapi bayam juga mengandung zat yang bersifat merugikan, salah satunya
adalah asam oksalat. Pemanasan sayur bayam yang berulang dan disimpan dalam
waktu lama akan meningkatkan kandungan asam oksalat yang dapat menghambat
penyerapan zat besi dan kalsium dalam tubuh. Zat besi (Fe2+) yang tinggi pada bayam juga dapat berinteraksi dengan udara (teroksidasi) dan berubah menjadi Fe3+ yang
bersifat racun bagi tubuh
Selain mengandung zat besi, bayam juga mengandung zat nitrat (NO3-). Kalau
tereduksi dengan udara, maka akan menjadi NO2- (nitrit). Nitrit adalah senyawa yang
tidak berwarna, tidak berbau dan bersifat racun bagi tubuh manusia. Menurut John S
Wishnok, bayam segar yang baru dicabut dari persemaiannya telah mengandung
senyawa nitrit kira-kira sebanyak 5 mg/kg. Bila bayam disimpan di lemari es selama 2
minggu, kadar nitrit akan meningkat sampai 300 mg/kg.
Dengan kata lain, dalam 1 hari penyimpanan, senyawa nitrit akan meningkat
21 mg/kg (7%). Efek toksik (meracuni tubuh) yang ditimbulkan oleh nitrit bermula
dari reaksi oksidasi nitrit dengan zat besi dalam sel darah merah, tepatnya di dalam
hemoglobin (Hb). Fungsi hemoglobin adalah mengikat oksigen untuk disalurkan ke
seluruh organ tubuh. Ikatan nitrit dengan hemoglobin disebut methemoglobin,
mengakibatkan hemoglobin tidak mampu mengikat oksigen. Jika jumlah
methemoglobin mencapai lebih dari 15% dari total hemoglobin, maka akan terjadi
keadaan yang disebut sianosis, yaitu suatu keadaan dimana seluruh jaringan tubuh
manusia kekurangan oksigen. Jika hal ini terjadi pada bayi dikenal dengan nama “Blue
Baby”.
Menurut Silalahi dalam Darius (2007) bahwa jumlah asupan harian (ADI) oleh
FAO/WHO untuk 60 kg berat badan adalah 8 mg nitrit.
Secara umum masyarakat sudah mengetahui bahwa rebusan sayur bayam tidak
dapat disimpan terlalu lama ataupun dipanaskan, tetapi banyak yang tidak
keracunan. Dari uraian di atas peneliti ingin menganalisa perubahan kandungan nitrit
(NO2-) pada hasil rebusan sayur bayam hijau dan air rebusan bayam yang sering
dikonsumsi masyarakat serta berapa lama dapat disimpan setelah dimasak, aman
untuk dikonsumsi.
1.2. Rumusan Masalah
Dalam penelitian ini yang menjadi rumusan masalah adalah:
1. Sejauh mana perubahan kandungan nitrit (NO2-) pada hasil rebusan sayur bayam.
2. Berapa lama hasil rebusan sayur bayam dapat disimpan (tidak beracun) sebelum
dikonsumsi.
3. Apakah ada perbedaan kandungan nitrit (NO2-) antara rebusan sayur bayam dan
air rebusan bayam.
1.3. Pembatasan Masalah
1. Sampel yang digunakan adalah bayam yang diambil dari kebun sayur petani di
desa Kebun Baru, kecamatan Hamparan Perak, kabupaten Deli Serdang.
2. Sampel yang dianalisa adalah rebusan sayur bayam hijau dan air rebusan bayam.
3. Kandungan yang dianalisa dalam sampel adalah nitrit (NO2-).
1.4. Tujuan Penelitian
Berdasarkan permasalahan di atas, penelitian ini bertujuan:
1. Untuk mengetahui kandungan nitrit (NO2-) rebusan sayur bayam hijau selama
penyimpanan.
2. Untuk mengetahui kandungan nitrit (NO2-) air rebusan bayam hijau selama
penyimpanan.
3. Untuk mengetahui sejauh mana perubahan kandungan nitrit pada hasil rebusan
sayur bayam selama penyimpanan.
4. Untuk mengetahui lama penyimpanan hasil rebusan sayur bayam yang aman
1.5. Manfaat Penelitian
Hasil yang diperoleh dari penelitian ini diharapkan dapat bermanfaat:
1. Sebagai bahan informasi untuk masyarakat dalam mengkonsumsi sayur bayam
secara aman.
2. Sebagai informasi tambahan bagi instansi terkait dalam memberikan penyuluhan
pola makan yang sehat.
3. Sebagai acuan bagi pihak pedagang makanan (nasi dan lauk pauk) dalam
menyediakan makanan yang sehat dan bernilai gizi yang tinggi bagi konsumen.
1.6. Lokasi Penelitian
BAB 2
TINJAUAN PUSTAKA
2.1. Sayuran
2.1.1. Pengertian sayuran
Istilah sayuran biasanya digunakan untuk merujuk pada tunas, daun, dan buah
tanaman yang lunak dan dapat dimakan secara utuh atau sebagian, segar/mentah atau
dimasak, sebagai pelengkap pada makanan (Ronoprawiro, 1993). Sayuran merupakan
bagian dari menu makanan yang berperan menyediakan vitamin, mineral atau serat
dan juga mempunyai khasiat lain untuk kesehatan, kebugaran maupun kecantikan
(Novary, 1997).
Sayuran adalah bahan yang mudah rusak (perishable). Oleh karena itu,
penanganan sayuran sejak pemanenan, pengemasan, hingga akan pemasaran harus
dilakukan dengan hati-hati untuk menghindari kerusakan tekstur sayuran. Jika tekstur
sayuran rusak, maka akan mudah terjadi pencemaran baik oleh mikroorganisme
maupun bahan pencemar kimia seperti residu peptisida, logam berat, dan lain-lain.
Untuk mengurangi ataupun menghindari pencemaran pada sayuran, maka perlu
dilakukan pengolahan sayuran yang meliputi pencucian dan pemasakan secara benar
dan higienis (Karnisa. 2000).
2.1.2. Kandungan gizi sayuran
Hampir semua sayuran mengandung zat gizi yang dibutuhkan oleh tubuh,
hanya jumlahnya yang berbeda. Walaupun karbohidrat, protein dan lemak juga
terdapat didalamnya, tetapi jumlahnya relatif kecil dibandingkan kandungan vitamin
dan mineral. Berikut ini beberapa jenis vitamin dan mineral yang terdapat dalam
sayuran, yaitu: Vitamin (A, B1, B2, B3, B6, C dan E), Mineral Kalsium (Ca), Mineral
2.1.3. Manfaat Sayuran Bagi Kesehatan
Sayuran dikenal sebagai bahan pangan yang mempunyai banyak khasiat bagi
kehidupan manusia. Beberapa khasiat sayuran diantaranya adalah sebagai berikut:
1. Sebagai sumber vitamin dan mineral
Vitamin dan mineral adalah zat gizi yang dibutuhkan tubuh dalam jumlah yang
lebih sedikit dibandingkan zat gizi lainnya. Kekurangan dan kelebihan vitamin
maupun mineral mempunyai efek yang tidak baik bagi kesehatan tubuh.
2. Memelihara kesehatan tubuh
Sayuran mampu memelihara bahkan mengatasi gangguan kesehatan tubuh
karena terdapat zat-zat gizi maupun non-gizi yang berperan dalam hal kesehatan,
Sebagai contoh: vitamin A mencegah kebutaan, vitamin C mencegah sariawan,
mineral besi mencegah anemia, kalsium mencegah rematik dan lain sebagainya.
3. Mengontrol berat badan
Sayuran merupakan bahan pangan yang tinggi serat. Oleh karenanya,
mengkonsumsi sayuran sering dianjurkan kepada orang yang ingin mengontrol berat
badannya, baik sebagai bagian dari menu makan, pengganti snack, maupun sebagai
minuman (jus). Serat yang dikonsumsi mampu menimbulkan rasa kenyang lebih lama
sehingga kecenderungan makan berlebih dapat dikurangi atau dicegah.
4. Menunda proses penuaan
Sayuran segar mengandung suatu zat antioksidan yang melindungi sel-sel
tubuh dari proses penuaan. Selain itu, zat antioksidan ini juga mencegah adanya
radikal bebas merusak sel atau program genetik (Novary, 1997).
2.2. Tumbuhan Bayam
Tumbuhan bayam berasal dari Amerika tropik. Sampai sekarang, tumbuhan ini
sudah tersebar di daerah tropis dan subtropis seluruh dunia. Bayam sebagai sayur
umumnya dikenal di Asia Timur dan Asia Tenggara, sehingga dalam bahasa Inggris
disebut Chinese amaranth. Di Indonesia, bayam dapat tumbuh sepanjang tahun dan
tumbuh lebih subur di dataran rendah pada lahan terbuka yang udaranya agak
panas.Tanaman setahun, tegak atau agak condong, tinggi 0,4-1 m, dan bercabang.
Batang lemah dan berair. Daun bertangkai, berbentuk bulat telur, lemas, panjang 5-8
cm, ujung tumpul, pangkal runcing, serta warnanya hijau, merah, atau hijau keputihan.
Bunga berbentuk bulir. Bayam yang dijual di pasaran dan biasa dikonsumsi sebagai
sayuran dikenal dengan bayam cabut.
Terdapat tiga varietas bayam yang termasuk ke dalam Amaranthus tricolor,
yaitu bayam hijau biasa, bayam merah (Blitum rubrum), yang batang dan daunnya
berwarna merah, dan bayam putih (Blitum album), yang berwarna hijau
keputih-putihan. Daun dan batang bayam merah mengandung cairan berwarna merah. Selain
Amaranthus tricolor, terdapat bayam jenis lain, seperti bayam kakap (A. hybridus),
bayam duri (A. spinosus), dan bayam tanah (A. blitum). Jenis bayam yang sering
dibudidayakan adalah A. tricolor, sedangkan jenis bayam lainnya tumbuh liar. Panen
bayam cabut paling lama dilakukan selama 25 hari. Setelah itu, kualitasnya akan
menurun karena daunnya menjadi ka
adalah klasifikasi ilmiah dari bayam yang diuji:
Kerajaan : Plantae
Divisi : Magnoliophyta
Kelas : Magnoliopsida
Ordo : Caryophyllales
Famili : Amaranthaceae
Upafamili : Amaranthoideae
Genus : Amaranthus
Bayam cabut termasuk genus Amarantus yang terdiri dari sekitar 60 spesies
yang secara luas mencakup jenis tanaman biji-bijian, tanaman sayuran dan gulma.
Pembudidayaan bayam untuk pemanfaatan daunnya sebagai sayuran diperkirakan
telah berlangsung sejak 2000 tahun yang lewat. Pada akhir-akhir ini bayam ditanam
secara luas sebagai sumber serat dan bahan pangan yang bergizi dengan kandungan
Di Sumatera Utara, bayam termasuk sayuran umum hasil produksi pertanian
rakyat yang dikonsumsi dalam jumlah yang relatif cukup besar . Dari data statistik
tanaman sayuran “ Sumatera Utara dalam Angka 2000” (BPS SU, 2000), bayam
menurut jumlah luas panen tahunan sayuran termasuk jenis sayur potensil di Sumatera
Utara.
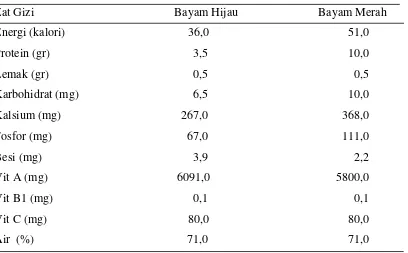
Bayam memiliki kandungan gizi yang sangat lengkap dan penting untuk
kesehatan tubuh kita. Komposisi kandungan gizi bayam dalam 100 gram dapat dilihat
pada tabel berikut :
Tabel 1. Komposisi Zat Gizi Bayam dalam 100 g Bayam Segar
Zat Gizi Bayam Hijau Bayam Merah
Energi (kalori) 36,0 51,0
Protein (gr) 3,5 10,0
Lemak (gr) 0,5 0,5
Karbohidrat (mg) 6,5 10,0
Kalsium (mg) 267,0 368,0
Fosfor (mg) 67,0 111,0
Besi (mg) 3,9 2,2
Vit A (mg) 6091,0 5800,0
Vit B1 (mg) 0,1 0,1
Vit C (mg) 80,0 80,0
Air (%) 71,0 71,0
Sumber: Daftar komposisi bahan makanan, Departemen Kesehatan RI, 1996.
Akar bayam juga dapat dimanfaatkan sebagai obat untuk menghilangkan
panas, menghilangkan racun (antitoksik), obat diare dan membersihkan darah dengan
cara meminum air sari rebusan akar bayam. Dapat juga menyembuhkan bengkak atau
bisul dengan cara menggiling lalu dioleskan pada bagian yang sakit.
Tanaman bayam juga digunakan untuk merawat rambut agar tumbuh sehat,
dan diyakini dapat mencegah tumbuhnya uban, caranya dengan menyiram kulit kepala
bahan utama tanaman bayam. Dengan demikian dapatlah disimpulkan bahwa dengan
mengkonsumsi bayam secara teratur dapat menjaga kesehatan dan membantu
pertumbuhan secara baik (Bandini. Y, 2001).
Bayam dapat diolah menjadi berbagai jenis masakan. Bayam dapat disayur
bening, dibuat gado-gado, pecal, atau direbus untuk lalap. Untuk industri kecil, daun
bayam yang muda dan lebar digunakan pula sebagai bahan rempeyek. Sewaktu
memasak bayam tidak boleh terlalu lama. Bayam cukup hanya direbus selama ± 5
menit. Memasak bayam terlalu lama akan menyebabkan daunnya menjadi hancur,
rasanya tidak enak, dan kandungan vitamin C-nya menguap (menghilang). Menurut
Sudarmadji (1989) dalam
suhu tinggi menyebabkan vitamin C teroksidasi menjadi asam dehidroaskorbat.
2.3. Nitrit
2.3.1. Defenisi Nitrit
Nitrit (NO2-) adalah ion-ion anorganik alami, yang merupakan bagian dari
siklus nitrogen. Aktifitas mikroba di tanah atau air menguraikan sampah yang
mengandung nitrogen organik pertama-tama menjadi ammonia, kemudian
dioksidasikan menjadi nitrit dan nitrat. Oleh karena nitrit dapat dengan mudah
dioksidasikan menjadi nitrat, maka nitrat adalah senyawa yang paling sering
ditemukan di dalam air tanah maupun air permukaan. Nitrogen bebas merupakan 79%
dari udara. Unsur nitrogen hanya dapat dimanfaatkan oleh tumbuhan, umumnya
dalam bentuk nitrat, dan pengambilannya khususnya lewat akar. Terbentuknya nitrat
karena bantuan mkroorganisme.
Beberapa genus bakteri yang hidup bebas di dalam tanah mampu mengikat
molekul-molekul nitrogen untuk dijadikan senyawa-senyawa pembentuk tubuh
tanaman, misalnya protein. Jika sel-sel tanaman mati, timbullah zat hasil urai seperti
karbondioksida dan gas amoniak. Sebagian besar dari amoniak terlepas di udara, dan
sebagian lain dapat dipergunakan oleh genus bakteri untuk membentuk nitrit. Nitrit
Oksidasi amoniak menjadi nitrit dan oksidasi nitrit menjadi nitrat berlangsung
di dalam lingkungan yang aerob. Peristiwa seluruhnya disebut nitrifikasi. Tahap
pertama yaitu pengoksidasian amoniak menjadi nitrit dilakukan oleh Nitrosomonas,
Nitrosococcus dan beberapa spesies lainnya, sedangkan pengoksidasian nitrit menjadi
nitrat dilakukan oleh Nitrosobacter. Penguraian protein dengan mikroorganisme
dimulai dengan hidrolisis protein secara enzimatik menjadi asam amino
masing-masing, selanjutnya asam amino yang dibebaskan dimetabolisme lebih lanjut. Selama
jalannya metabolisme ini gugusan amino paling sering dibebaskan sebagai amoniak.
Reaksi pembentukan NO2- berlangsung dengan pereduksian nitrat menjadi
nitrit dikatalis dengan enzim nitrat reduktase (NR). Cara kerja Enzim ini dengan
mengikat 2 elektron dari NADH atau NADPH2 menghasilkan nitrit, NAD- dan H2O
menurut reaksi :
NR
NO3- + NADH + H+ NO2- + NAD+ + H2O
Mekanisme kerja NR yaitu Nitrat Reduktase akan mereduksi NO3- menjadi
NO2-, selanjutnya oleh nitrit reduktase akan direduksi menjadi Ammonium (NH4+).
Nitrat Reduktase (NR) merupakan enzim yang mengkatalis nitrat menjadi
nitrit dan bersifat inducible karena aktivitasnya dapat ditingkatkan dengan
penambahan substrat (Tjitrosoepomo, 1987). Tumbuhan memperoleh nitrogen dengan
cara menyerap nitrat atau ion amonia yang ada dalam tanah, penyerapan kedua
senyawa ion tersebut digunakan untuk membentuk berbagai senyawa nitrogen
misalnya protein (Salisbury and Roos, 1995).
Menurut Loveless (1990) aktivitas enzim nitrat reduktase pada daun tanaman
dewasa berhubungan dengan hasil tanaman, sehingga tingkat aktivitas enzim nitrat
reduktase dapat digunakan sebagai kriteria seleksi untuk memilih genotip dari suatu
tanaman yang berdaya hasil tinggi. Enzim nitrat reduktase berguna untuk merubah
nitrat menjadi nitrit yang kemudian setelah melalui serangkaian kerja enzim lain nitrit
ini akan diubah menjadi asam amino. Alnopri (1995) manambahkan bahwa aktivitas
pemuliaan tanaman. Pendekatan berdasarkan aktivitas nitrat reduktase sebagai kriteria
seleksi dapat dipertimbangkan, karena enzim yang dikendalikan oleh gen yang secara
langsung terlibat dalam proses biosintesis protein. Aktivitas nitrat reduktase
merupakan enzim pertama yang berperan dalam mereduksi nitrat menjadi amonia,
Sebagian besar tumbuhan tingkat tinggi mampu mereduksi nitrat sampai ke tahap
ammonia (Anderton, 1996).
2.3.2. Sifat Fisik dan Struktur Kimia Nitrit
Nitrat dibentuk dari asam nitrit yang berasal dari ammonia melalui proses
oksidasi katalitik. Nitrit juga merupakan hasil metabolisme dari siklus nitrogen.
Bentuk pertengahan dari nitrifikasi dan denitrifikasi. Nitrat dan nitrit adalah
komponen yang mengandung nitrogen berikatan dengan atom oksigen, nitrat
mengikat tiga atom oksigen sedangkan nitrit mengikat dua atom oksigen. Di alam,
nitrat sudah diubah menjadi bentuk nitrit atau bentuk lainnya.
Struktur kimia dari nitrat
Berat molekul: 62,05
Struktur kimia dari nitrit
O = N – O-
Berat molekul: 46,006
Pada kondisi yang normal, baik nitrit maupun nitrat adalah komponen yang
stabil, tetapi dalam suhu yang tinggi menjadi tidak stabil dan dapat meledak pada suhu
yang sangat tinggi dan tekanan yang sangat besar. Biasanya, adanya ion klorida,
bahan metal tertentu dan bahan organik akan mengakibatkan nitrat dan nitrit menjadi
tidak stabil. Jika terjadi kebakaran, maka tempat penyimpanan nitrit maupun nitrat
sangat berbahaya untuk didekati karena dapat terbentuk gas beracun dan bila terbakar
dapat menimbulkan ledakan. Bentuk garam dari nitrat dan nitrit tidak berwarna dan
tidak berbau serta tidak berasa. Nitrat dan nitrit bersifat higroskopis (Wahyudi, 2007).
Di dalam air, sering ditemukan konsentrasi nitrit tinggi yang terlarut dalam
dengan amina/amida dengan bantuan mikroorganisme sebagai katalis dengan syarat
konsentrasi nitrat cukup tinggi (minimal 10 ppm N-NO3 dan nitrit 1 ppm N-NO2 )
untuk mulai dapat melangsungkan reaksi nitrosasi (pembentukan nitrosamin).
E. coli, Acetobacter , Proteus morganii, Pseudomonas aeruginosa, Paracoccus
denitrificans, dan Bacillus coagulans adalah mikroorganisme yang paling banyak
terlibat dalam reaksi nitrosasi terutama E. coli yang memiliki sifat katalis yang paling
kuat untuk melangsungkan nitrosasi. Toksisitas dan sifat karsinogenik nitrosamine
identik dengan nitrit, lebih bersifat toksik pada pH rendah dan kadar garam rendah.
Sifat karsinogenik dan mutagenetik nitrosamin diduga kuat penyebab nekrosis yakni
pematian sebagian jaringan sel mahluk hidup sebagai stadium awal serangan kanker.
2.3.3. Methemoglobin
Hemoglobin adalah suatu senyawa protein, mempunyai struktur kuartener
yang mempunyai 4 gugus aktif yaitu
α
1, α
2, β1 dan β2 sehingga senyawa tersebutmampu mengikat 4 molekul oksigen (1 mol oksigen/1 gugus aktif). Apabila 1 gugus
aktif telah berikatan dengan 1 molekul oksigen , maka gugus aktif ini akan memicu
(merangsang) atau bertindak sebagai aktivator pada gugus di sebelahnya, begitu
seterusnya sehingga keempat gugus aktif akan berikatan dengan molekul oksigen.
Secara skematis proses tersebut dapat digambarkan sebagai berikut:
Hb
Mekanisme pengikatan mol O2 oleh Hb dapat digambarkan sebagai berikut:
Dimana: Konstanta kecepatan reaksi K1 << K2 Konstanta kecepatan reaksi K5 >> K6
Konstanta kecepatan reaksi K3 == K4
α1 α2
β1 β2
O2 K1
K2
O2 O2 K3
K4
O2 O2 K5
K6
O2 O2
Setelah oksigen sampai kepada target (organ) penerima oksigen, maka satu
persatu molekul oksigen tersebut dilepaskan lalu disubstitusi oleh melekul CO2
dengan mekanisme yang sama, dan baru dilepas setelah sampai di paru-paru untuk
disekresikan (dibuang). Bila di dalam aliran darah terdapat zat-zat inhibitor seperti
senyawa-senyawa nitrit, maka terjadi persaingan yang cukup kuat antara zat tersebut
dengan molekul oksigen untuk berikatan dengan gugus aktif Hb. Bila kadar zat
tersebut relatif tinggi maka zat tersebut akan mengisi (berikatan) dengan gugus aktif
Hb. Hb dalam keadaan ini disebut dengan Methemoglobin. Mekanisme pengikatan
zat-zat inhibitor ini hampir sama pada saat Hb berikatan dengan molekul oksigen.
Methemoglobin bukan merupakan senyawa beracun, tetapi dapat
mengakibatkan berkurangnya daya angkut oksigen di dalam tubuh (Robert W, Mc
Gilery, 1996).
2.3.3. Keracunan Nitrit
Nitrit dapat digunakan sebagai pengawet pada makanan dan mempertahankan
warna, tetapi jika dosisnya di atas ambang batas maka akan mengakibatkan keracunan
sampai kematian bagi yang mengkonsumsinya.
Sebuah harian lokal di Cina (Xinhua terbitan 8 April 2011) menyatakan 3
orang anak tewas dan 35 orang jatuh sakit setelah minum susu di Provinsi Gansu
China barat laut. Pemeriksaan oleh instansi terkait menunjukkan bahwa susu yang
telah diminum anak-anak tersebut keracunan garam nitrit. Garam nitrit yang
ditemukan pada susu kemungkinan berasal dari makanan ternak. Orang-orang yang
kekebalan tubuhnya lemah, seperti bayi dan anak-anak, rawan keracunan garam nitrit,
Peristiwa keracunan makanan juga terjadi di salah satu sekolah TK Marabahan
di Banjarmasin yang diberitakan Banjarmasin post tanggal 3 Februari 2011 yang
menyebabkan 14 siswa dirawat di rumah sakit setelah mengkonsumsi makanan
pemeriksaan terhadap makanan diketahui kalau pada kuah santan makanan tersebut
mengadung mikroba yang di dalamnya berproses menghasilkan nitrit (N02-) yang
dapat menyebabkan keracunan bagi yang mengonsumsinya (dalam http: //
banjarmasin. tribunnews. com/red/artikel/ 2011/2/3/ 73312/ keracunan-akibat-nitrit).
Dosis letal dari nitrit pada orang dewasa bervariasi antara 0.7 dan 6 g NO2
-(atau sekitar10 sampai 100 mg NO2-/kg berat badan).
2.4. Kinetika Kimia
Kinetika kimia membahas tentang laju dan mekanisme reaksi. Berdasarkan
penelitian yang dilakukan oleh Wilhelmy diperoleh bahwa kecepatan reaksi
berbanding lurus dengan konsentrasi / tekanan zat – zat yang bereaksi. Laju reaksi
dinyatakan sebagai perubahan konsentrasi atau tekanan dari produk atau reaktan
terhadap waktu. Selain itu kecepatan reaksi juga dipengaruhi oleh suhu dan katalis.
Makin tinggi suhu maka laju reaksi makin cepat.
2.4.1. Efek Katalis
Katalis adalah suatu senyawa yang dapat menaikkan laju reaksi, tetapi tidak
ikut menjadi reaktan / produk dalam sistem itu sendiri. Setelah reaksi selesai, katalis
dapat diperoleh kembali tanpa mengalami perubahan kimia. Katalis berperan dengan
menurunkan energi aktivasi. Sehingga untuk membuat reaksi terjadi, tidak diperlukan
energi yang lebih tinggi. Dengan demikian, reaksi dapat berjalan lebih cepat.
2.4.2. Katalis Enzim
Enzim adalah protein yang khusus disintesa oleh sel hidup untuk mengkatalisa
reaksi yang sedang berlangsung. Setiap kenaikan suhu 100C kecepatan reaksi naik dua kali. Suhu mempunyai dua pengaruh yang saling berlawanan terhadap aktivitas
enzim. Pertambahan suhu akan meningkatkan aktivitas enzim, sebaliknya juga akan
Enzim dikatakan sebagai suatu kelompok protein yang berperan dalam
aktivitas biologis. Enzim ini berfungsi sebagai katalisator dalam sel dan sifatnya
sangat khas. Dalam jumlah yang sangat kecil, enzim dapat mengatur reaksi tertentu
sehingga dalam keadaan normal tidak terjadi penyimpangan hasil reaksinya.
Enzim akan kehilangan aktivitasnya karena panas, asam dan basa kuat, pelarut
organik atau apa saja yang bisa menyebabkan denaturasi protein. Enzim dinyatakan
mempunyai sifat yang sangat khas karena hanya bekerja pada substrat tertentu
(Girinda,1990).
Fungsi penting dari enzim adalah sebagai biokatalisator, reaksi kimia secara
kolektif membentuk metabolisme perantara sel, suatu bagian yang sangat kecil dari
suatu molekul besar protein, enzim sangat berperan untuk katalis reaksi. Bagian yang
kecil ini dinamakan bagian aktif enzim. Aktivitas katalik enzim dapat ditentukan juga
melalui struktur tiga dimensi molekul enzim tersebut. Enzim disini mempunyai
peranan katalis dalam menurunkan aktivitas dari reaksi energi. Aktivasi dapat
diartikan sebagai sejumlah energi atau kalori yang diturunkan oleh suatu mol zat pada
temperatur tertentu untuk membawa molekul ke dalam aktifnya atau keadaan aktifnya
(Wirahadikusuma, 1989).
Menurut Martoharsono, 1998, enzim dapat berfungsi sebagai berikut:
a. Menurunkan energi aktivasi.
b. Mempercepat reaksi pada suhu dan tekanan tetap tanpa mengubah besarnya tetapan
seimbangnya.
c. Mengendalikan reaksi.
Sedangkan faktor-faktor yang mempengaruhi kerja enzim (Poedjiati, 1994)
antara lain:
a. Konsentrasi enzim; pada suatu konsentrasi substrat tertentu, kecepatan reaksi
bertambah dengan bertambahnya konsentrasi enzim.
b. Suhu; kenaikan suhu dapat menyebabkan denaturasi, sehingga bagian aktifnya
terganggu, akibatnya konsentrasi spesifik enzim berkurang dan kecepatan
c. Konsentrasi substrat; perubahan substrat akan menambah kecepatan reaksi.
d. Pengaruh pH; struktur ion enzim tergantung pada pH lingkungannya, enzim dapat
terbentuk ion (+) atau (-) atau bermuatan ganda (zwitter ion). pH dapat
menyebabkan proses denaturasi yang dapat mengakibatkan menurunnya aktivitas
enzim.
e. Pengaruh inhibitor; dapat berupa hambatan inversibel yang disebabkan oleh
terjadinya destruksi atau modifikasi sebuah gugus fungsi atau lebih, yang terdapat
pada molekul enzim. Hambatan reversibel dapat berupa hambatan bersaing dan tak
bersaing
Hubungan antara substrat (S) dan produk (P) dengan adanya enzim (E) dapat
dituliskan :
S +E → SE → P + E
Enzim yang terbentuk pada akhir reaksi dapat bereaksi kembali dengan substrat
sampai semuanya substrat dirombak menjadi produk. Dalam penelitian ini yang
berperan sebagai substrat adalah nitrat, produk adalah nitrit sedangkan enzim
dihasilkan oleh bakteri yang terbawa oleh udara sewaktu sayur bayam didiamkan
sebelum dikonsumsi.
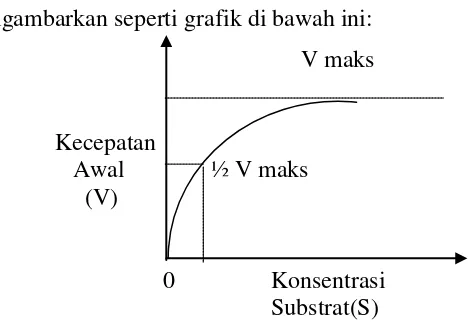
Pengaruh konsentrasi substrat terhadap produk dengan katalis enzim dapat
digambarkan seperti grafik di bawah ini:
V maks
Kecepatan
Awal ½ V maks
(V)
0 Konsentrasi
[image:34.612.122.358.484.645.2]Substrat(S)
2.5. Karbon aktif
Karbon aktif atau sering juga disebut sebagai arang aktif, adalah suatu jenis
mengaktifkan karbon atau arang tersebut. Hanya dengan satu gram karbon aktif, akan
didapatkan suatu material yang memiliki luas permukaan kira-kira sebesar 500 m2 (didapat dari pengukura
bertujuan untuk memperbesar luas permukaannya saja, namun beberapa usaha juga
berkaitan dengan meningkatkan kemampuan adsorpsi karbon aktif itu sendiri.
Pada abad XV, diketahui bahwa arang aktif dapat dihasilkan melalui komposisi
kayu dan dapat digunakan sebagai adsorben warna dari larutan. Aplikasi komersial
baru dikembangkan pada tahun 1974 yaitu pada industri gula sebagai pemucat, dan
menjadi sangat terkenal karena kemampuannya menyerap uap gas beracun.
Arang aktif dapat mengadsorpsi gas dan senyawa-senyawa kimia tertentu atau
sifat adsorpsinya selektif, tergantung pada besar atau volume pori-pori dan luas
permukaan. Daya serap arang aktif sangat besar, yaitu 25- 1000% terhadap berat
arang aktif. Karena hal tersebut maka karbon aktif banyak digunakan oleh kalangan
industri. Hampir 60% produksi arang aktif di dunia ini dimanfaatkan oleh
industri-industri gula dan pembersihan minyak dan lemak, kimia dan farmasi.
Karbon atau arang aktif adalah material yang berbentuk butiran atau bubuk
yang berasal dari material yang mengandung karbon misalnya batubara, kulit kelapa,
dan sebagainya. Dengan pengolahan tertentu yaitu proses aktivasi seperti perlakuan
dengan tekanan dan suhu tinggi, dapat diperoleh karbon aktif yang memiliki
permukaan dalam yang luas.
Arang merupakan suatu padatan berpori yang mengandung 85-95% karbon,
dihasilkan dari bahan-bahan yang mengandung karbon dengan pemanasan pada suhu
tinggi. Ketika pemanasan berlangsung, diusahakan agar tidak terjadi kebocoran udara
di dalam ruangan pemanasan sehingga bahan yang mengandung karbon tersebut
hanya terkarbonisasi dan tidak teroksidasi. Arang selain digunakan sebagai bahan
luas permukaan partikel dan kemampuan ini dapat menjadi lebih tinggi jika terhadap
arang tersebut dilakukan aktifasi dengan bahan-bahan kimia ataupun dengan
pemanasan pada temperatur tinggi. Dengan demikian, arang akan mengalami
perubahan sifat-sifat fisika dan kimia.
Secara umum proses pembuatan arang aktif dapat dibagi dua yaitu:
1. Proses Kimia
Bahan baku dicampur dengan bahan-bahan kimia tertentu, kemudian dibuat
padat. Selanjutnya padatan tersebut dibentuk menjadi batangan dan dikeringkan serta
dipotong-potong. Aktifasi dilakukan pada temperatur 100°C. Arang aktif yang
dihasilkan, dicuci dengan air selanjutnya dikeringkan pada temperatur 300°C. Dengan
proses kimia, bahan baku dapat dikarbonisasi terlebih dahulu, kemudian dicampur
dengan bahan-bahan kimia.
2. Proses Fisika
Bahan baku terlebih dahulu dibuat arang. Selanjutnya arang tersebut digiling,
diayak untuk selanjutnya diaktifasi dengan cara pemanasan pada temperatur 1000°C
yang disertai pengaliran uap. Proses fisika banyak digunakan dalam aktifasi arang
yaitu:
a. Proses Briket
Bahan baku atau arang terlebih dahulu dibuat briket, dengan cara
mencampurkan bahan baku atau arang halus dengan “ter”. Kemudian, briket yang
dihasilkan dikeringkan pada 550°C untuk selanjutnya diaktifasi dengan uap.
b. Destilasi kering
Merupakan suatu proses penguraian suatu bahan akibat adanya pemanasan
pada temperatur tinggi dalam keadaan sedikit maupun tanpa udara. Hasil yang
diperoleh berupa residu yaitu arang dan destilat yang terdiri dari campuran metanol
dan asam asetat. Residu yang dihasilkan bukan merupakan karbon murni, tetapi masih
mengandung abu dan “ter”. Hasil yang diperoleh seperti metanol, asam asetat dan
arang tergantung pada bahan baku yang digunakan dan metoda destilasi. Diharapkan
daya serap arang aktif yang diaktifkan dengan menyertakan bahan-bahan kimia. Juga
dengan cara ini, pencemaran lingkungan sebagai akibat adanya penguraian
senyawa-senyawa kimia dari bahan-bahan pada saat proses pengarangan dapat diihindari.
2.6. Istilah dalam Penulisan
Dalam penelitian ini yang dimaksud dengan hasil rebusan sayur bayam adalah
rebusan sayur bayam dan air rebusan bayam (sayur bayam + air rebusannya), rebusan
sayur bayam adalah sayur bayam yang sudah direbus dipisahkan dari airnya, air
BAB 3
METODE PENELITIAN
3.1. Alat-alat
Adapun alat-alat yang digunakan adalah sebagai berikut:
- Neraca analitik Chyo
- Gelas ukur Pyrex
- Labu ukur Pyrex
- Erlenmeyer Pyrex
- Pipet volumetri Pyrex
- Kompor masak
- Panci masak
- Spatula
- Spektrofotometer Sinar Tampak Spek 300
- Botol Aquadest
- Mortir
- Stamper
- Sendok kecil
- Pengaduk
3.2. Bahan-Bahan
Adapun bahan-bahan yang digunakan adalah sebagai berikut:
- Kertas saring Whatman no. 42
- Asam Klorida pekat p.a (E.Merck)
- Asam Sulfat pekat p.a (E.Merck)
- Sulfanilamide p.a (E.Merck)
- N- naftilendiamin dihidroklorida p.a (E.Merck)
- Natrium nitrit p.a (E.Merck)
- Natrium Oksalat p.a (E.Merck)
- Karbon aktif p.a (E.Merck)
- Sayur bayam hijau
- Aquades
3.3. Prosedur Penelitian
3.3.1. Penyedian Bahan Pereaksi (SNI 06–2484–2002)
Larutan-larutan yang disediakan sebagai berikut:
- Larutan sulfanilamide (1%)
Dilarutkan 5 g sulfanilamide dalam 300 ml aquades lalu ditambahkan 50 ml HCl
pekat dan diencerkan sampai volume 500 ml.
- Larutan NED dihidroklorida (0,1 %)
Dilarutkan 0,1 g N- naftilendiamin dihidroklorida dengan aquades dan diencerkan
sampai volume 100 ml.
- Pembuatan Larutan Baku Nitrit 1000 mg/L
Ditimbang 1,5 g natrium nitrit, dilarutkan dengan aquades lalu dimasukkan ke dalam
labu ukur 1000 ml dan diencerkan sampai garis tanda.
- Larutan Standar Nitrit 100 mg/L
Dipipet 10 ml dari larutan 1000 mg/L ke dalam labu ukur 100 ml dan diencerkan
- Larutan Standar Nitrit 10 mg/L
Dipipet 10 ml dari larutan 100 mg/L ke dalam labu ukur 100 ml dan diencerkan
dengan aquades hingga garis tanda.
- Pembuatan Larutan Seri Standar Nitrit
Ke dalam 5 buah labu ukur 100 ml yang bersih dan kering secara terpisah dipipet
dengan tepat 2,0; 4,0; 6,0; 8,0 ml larutan standar Nitrit 10 mg/L dan diencerkan
dengan aquades hingga sampai garis tanda (larutan ini mengandung berturut-turut
Nitrit 0,2; 0,4; 0,6; 0,8 mg/L).
3.3.2. Lokasi Pengambilan Sampel
Sampel berupa sayur bayam diperoleh dari kebun sayur petani di desa Kebun Baru,
kecamatan Hamparan Perak, kabupaten Deli Serdang, provinsi Sumatera Utara.
3.3.3. Metoda Pengambilan Sampel
Pengambilan sampel dilakukan secara acak (random sampling) dari kebun
sayur petani dengan cara mencabut bayam dari tanah. Lalu dipetik daun dan batang
yang segar dan muda, kemudian dicuci dengan air bersih. Setelah itu ditiriskan dan
dimasukkan ke dalam wadah plastik berpori, dibawa ke laboratorium dan disimpan di
lemari pendingin sebelum dianalisa.
3.3.4. Prosedur Pengukuran Sampel 3.3.4.1. Preparasi sampel
1. Ditimbang 100 g daun dan batang bayam yang sudah bersih.
2. Direbus ± 5 menit ke dalam wadah yang berisi 1000 ml aquades yang sudah
dididihkan.
3. Sampel disaring dengan alat penyaring untuk memisahkan rebusan sayur
bayam dan air rebusan.
4. Rebusan sayur bayam dan air rebusan didiamkan (0, 1, 2 ,3, 4 dan 5) jam.
3.3.4.2. Prosedur Pengukuran Konsentrasi Nitrit 3.3.4.2.1. Prosedur Pembuatan Kurva Kalibrasi Nitrit
1. Ke dalam 5 buah labu ukur 100 ml yang bersih dan kering secara terpisah
dipipet dengan tepat 2,0; 4,0; 6,0; 8,0 ml larutan standar Nitrit 10 mg/L.
2. Ditambahkan aquades sampai volume 100 ml.
3. Ditambahkan 1 ml larutan sulfanilamide.
4. Ditambahkan 1 ml larutan naftiletilendiamin dihidroklorida.
5. Larutan diaduk dan dibiarkan selama 5 menit.
6. Diambil 10 ml masing-masing dari larutan di atas, lalu dimasukkan ke dalam
kuvet yang bersih, dibaca absorbansinya pada spektrofotometer sinar tampak
pada panjang gelombang 543 nm.
7. Dibuat kurva absorbansi versus konsentrasi.
3.3.4.2.2. Prosedur Pembuatan Kurva Kalibrasi Nitrit dengan Karbon Aktif
1. Ke dalam 5 buah labu ukur 100 ml yang bersih dan kering secara terpisah
dipipet dengan tepat 2,0; 4,0; 6,0; 8,0 ml larutan standar Nitrit 10 mg/L.
2. Ditambahkan 0,5 g serbuk karbon aktif, lalu ditambahkan aquades sampai
volume 100 ml.
3. Dibiarkan 5 menit, lalu disaring.
4. Ditambahkan 1 ml larutan sulfanilamide.
5. Ditambahkan 1 ml larutan naftiletilendiamin dihidroklorida.
6. Diaduk dan dibiarkan selama 5 menit.
7. Diambil 10 ml masing-masing dari larutan di atas, lalu dimasukkan ke dalam
kuvet yang bersih, dibaca absorbansinya pada spektrofotometer sinar tampak
pada panjang gelombang 543 nm.
3.3.4.2.3. Prosedur Pengukuran Konsentrasi Nitrit untuk Sayur Bayam Tanpa Direbus
1. Ditimbang 10 g sayur bayam segar, lalu dihaluskan.
2. Ditambahkan 0,5 g serbuk karbon aktif, lalu ditambahkan aquades sampai
volume 100 ml.
3. Dibiarkan 5 menit, lalu disaring.
4. Ditambahkan 1 ml larutan sulfanilamide.
5. Ditambahkan 1 ml larutan naftilendiamin dihidroklorida.
6. Diaduk dan dibiarkan selama 5 menit.
7. Diambil 10 ml filtrat, lalu dimasukkan ke dalam kuvet yang bersih, dibaca
absorbansinya pada spektrofotometer sinar tampak pada panjang gelombang
543 nm.
8. Dihitung konsentrasi nitrit dari sampel dengan mensubstitusi absorbansi
sampel ke dalam persamaan least square.
9. Dilakukan pengulangan 3 kali.
3.3.4.2.4. Prosedur Pengukuran Konsentrasi Nitrit untuk Rebusan Sayur Bayam.
1. Ditimbang 10 g sayur bayam yang sudah direbus (0 jam), lalu dihaluskan.
2. Ditambahkan 0,5 g serbuk karbon aktif, lalu ditambahkan aquades sampai
volume 100 ml.
3. Dibiarkan 5 menit, lalu disaring.
4. Ditambahkan 1 ml larutan sulfanilamide.
5. Ditambahkan 1 ml larutan naftilendiamin dihidroklorida.
6. Diaduk dan dibiarkan selama 5 menit.
7. Diambil 10 ml filtrat, lalu dimasukkan ke dalam kuvet yang bersih, dibaca
absorbansinya pada spektrofotometer sinar tampak pada panjang gelombang
8. Dihitung kadar nitrit dari sampel dengan mensubstitusi absorbansi sampel ke
dalam persamaan least square.
9. Dengan cara yang sama dilakukan pengukuran konsentrasi nitrit terhadap
rebusan sayur bayam yang sudah didiamkan (1, 2, 3, 4 dan 5) jam.
10. Dilakukan pengulangan 3 kali.
3.3.4.2.5. Prosedur Pengukuran Konsentrasi Nitrit untuk Air Rebusan Bayam
1. Diambil 10 ml air rebusan sayur bayam (jam 0).
2. Ditambahkan 0,5 g serbuk karbon aktif, lalu ditambahkan aquades sampai
volume 100 ml.
3. Dibiarkan 5 menit, lalu disaring.
4. Ditambahkan 1 ml larutan sulfanilamide.
5. Ditambahkan 1 ml larutan naftilendiamin dihidroklorida.
6. Diaduk dan dibiarkan selama 5 menit.
7. Diambil 10 ml filtrat, lalu dimasukkan ke dalam kuvet yang bersih, dibaca
absorbansinya pada spektrofotometer sinar tampak pada panjang gelombang
543 nm.
8. Dihitung kadar nitrit dari sampel dengan mensubstitusi absorbansi sampel ke
dalam persamaan least square.
9. Dengan cara yang sama dilakukan pengukuran konsentrasi nitrit terhadap air
rebusan sayur bayam yang sudah didiamkan (1,2,3,4 dan 5) jam.
BAB 4
HASIL DAN PEMBAHASAN
[image:50.612.187.458.241.346.2]4.1 Hasil Analisis Sampel 4.1.1 Pengukuran Kadar Nitrit
Tabel 4.1. Hasil Pengukuran Absorbansi Larutan Standar Nitrit untuk Kurva Kalibrasi tanpa Karbon Aktif
Tabel 4.2. Hasil Pengukuran Absorbansi Larutan Standar Nitrit untuk Kurva Kalibrasi dengan Karbon Aktif
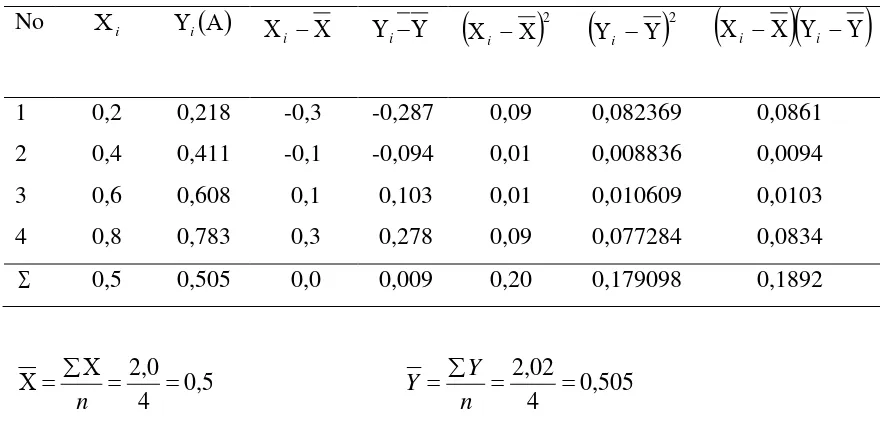
4.1.2. Penurunan Persamaan Garis Regresi
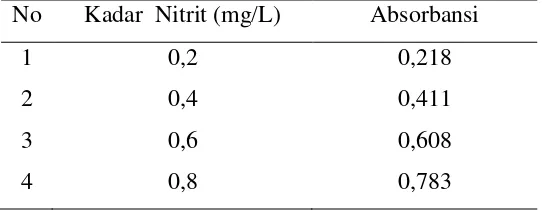
Hasil pengukuran absorbansi seri larutan standar nitrit pada tabel 4.1.
diplotkan terhadap kosentrasi larutan standar sehingga diperoleh suatu kurva kalibrasi
berupa garis linear yang diturunkan dengan metode Least Square dengan perhitungan
seperti tabel di bawah:
No Kadar Nitrit (mg/L) Absorbansi
1 0,2 0,218
2 0,4 0,411
3 0,6 0,608
4 0,8 0,783
No Kadar Nitrit (mg/L) +
Karbon Aktif 0,5 g Absorbansi
1 0,2 0,198
2 0,4 0,374
3 0,6 0,568
[image:50.612.187.455.404.514.2]Tabel 4.3. Penurunan Persamaan Garis Regresi dengan Metode Least Square
No Χi Υi
( )
Α Χ −Χi Υi−Υ
(
)
2
Χ −
Χi
(
)
2
Υ −
Υi
(
Χi −Χ)(
Υi −Υ)
1 2 3 4 0,2 0,4 0,6 0,8 0,218 0,411 0,608 0,783 -0,3 -0,1 0,1 0,3 -0,287 -0,094 0,103 0,278 0,09 0,01 0,01 0,09 0,082369 0,008836 0,010609 0,077284 0,0861 0,0094 0,0103 0,0834
Σ 0,5 0,505 0,0 0,009 0,20 0,179098 0,1892
0,5 4 2,0 = = Χ ∑ = Χ
n 4 0,505 2,02= = ∑ = n Y Y
Persamaan garis regresi untuk kurva kalibrasi dapat diturunkan dari persamaan garis:
y = ax + b
di mana, a = slope
b = intersep
Selanjutnya harga slope dapat ditentukan dengan menggunakan metode Least Square
sebagai berikut :
(
)(
)
(
)
∑
∑
− − − = 2 X Xi Y Yi X Xi a 2 , 0 1892 , 0 = aSedangkan harga intersep (b) dapat diperoleh melalui persamaan :
X a
Y = +b
X a Y b= −
4.1.3. Perhitungan Koefisien Korelasi
[image:52.612.131.512.360.580.2]Koefisien korelasi (r) dapat ditentukan sebagai berikut :
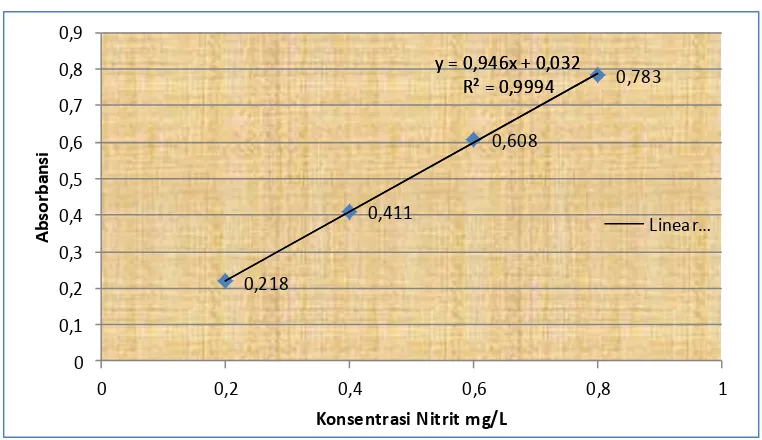
Gambar 4.1. Kurva Absorbansi Vs Konsentrasi Larutan Standar Nitrit
4.1.4. Penentuan Penyerapan Nitrit oleh Karbon Aktif
Konsentrasi nitrit pada penambahan karbon aktif dapat ditentukan dengan
menggunakan metode kurva kalibrasi dengan mensubtitusi nilai Y (absorbansi) yang
diperoleh dari hasil pengukuran terhadap garis regresi dan kurva kalibrasinya
0,218
0,411
0,608
0,783 y = 0,946x + 0,032
R² = 0,9994 y = 0,946x + 0,032
R² = 0,9994
0 0,1 0,2 0,3 0,4 0,5 0,6 0,7 0,8 0,9
0 0,2 0,4 0,6 0,8 1
A b so rb a n si
Konsentrasi Nitrit mg/L
y = 0,946 x + 0,032 sehingga diperoleh konsentrasi akhir nitrit. Untuk pengukuran
konsentrasi nitrit dengan penambahan karbon aktif pada larutan seri standar nitrit
diperoleh nilai absorbansi :
Ak1 = 0,198 ; Ak2 = 0,374 ; Ak3 = 0,568 ; Ak4 = 0,732
(Ak1 = Nilai absorbansi stándar nitrit 0,2 mg/L dengan penambahan karbon aktif)
Dengan mensubtitusikan nilai Y (absorbansi) ke persamaan regresi :
Y = 0,946 x + 0,032
Diperoleh : Xk1 = 0.175
mg/L, Xk2 =
0.362 mg/L, Xk3 = 0.567 mg/L,
Xk4 = 0.740 mg/L
(Xk1 = Nilai konsentrasi stándar nitrit 0,2 mg/L dengan penambahan karbon aktif)
Untuk menentukan penyerapan karbon aktif pada larutan seri standar nitrit dapat
dihitung dengan rumus:
Penyerapan karbon aktif = Konsentrasi awal – Konsentrasi akhir
Sehingga diperoleh konsentrasi penyerapan nitrit oleh karbon aktif pada tabel 4.3
[image:53.612.120.528.467.599.2]berikut.
Tabel 4.4. Hasil penyerapan konsentrasi nitrit oleh karbon aktif pada larutan seri standar
Rata-rata penyerapan nitrit oleh karbon aktif = 0,039 mg/L, jika diasumsikan 1liter air
murni = 1 kg (Berat Jenis air = 1), maka 0,039 mg/L= 0,039 mg/kg.
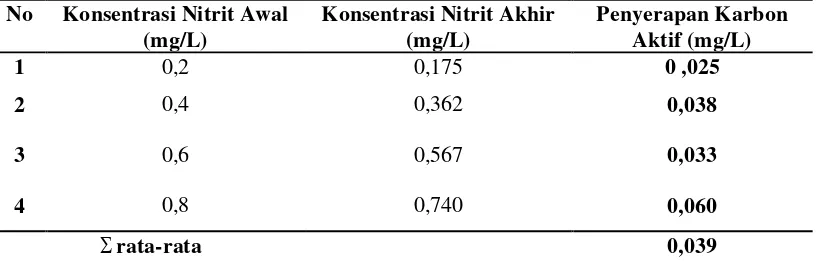
4.1.5 Penentuan Kadar Nitrit
No Konsentrasi Nitrit Awal (mg/L)
Konsentrasi Nitrit Akhir (mg/L)
Penyerapan Karbon Aktif (mg/L)
1 0,2 0,175 0 ,025
2 0,4 0,362 0,038
3 0,6 0,567 0,033
4 0,8 0,740 0,060
Kadar nitrit dapat ditentukan dengan menggunakan metode kurva kalibrasi
dengan mensubtitusi nilai Y (absorbansi) yang diperoleh dari hasil pengukuran
terhadap garis regresi dan kurva kalibrasinya y = 0,946 x + 0,032 sehingga diperoleh
konsentrasi nitrit. Untuk pengukuran kadar nitrit pada rebusan sayur bayam diperoleh
nilai absorbansi :
A1 = 0,422 ; A2 = 0,424 ; A3 = 0,421
(A1= Absorbansi kadar nitrit rebusan sayur bayam pada pengukuran 0 jam ulangan
1)
Dengan mensubtitusikan nilai Y (absorbansi) ke persamaan regresi :
Y = 0,946 x + 0,032
Diperoleh : X1 = 0,412 mg/L, X2 = 0,414 mg/L, X3 = 0,411 mg/L.
(K1= Konsentrasi kadar nitrit rebusan sayur bayam pada pengukuran 0 jam ulangan 1)
Jumlah sampel yang dianalisa sebanyak 10 g dilarutkan dalam 100 ml aquades
sehingga konsentrasi nitrit pada rebusan Sayur bayam adalah :
C(mg/kg) = X (mg/L) x Volume Larutan gram sampel
= 0,412 mg/L x 100 mL
10 g
= 0,412 mg/L x 0,1L 10 g
= 0,0412 mg 10 g
= 0,412 mg 0,01 kg
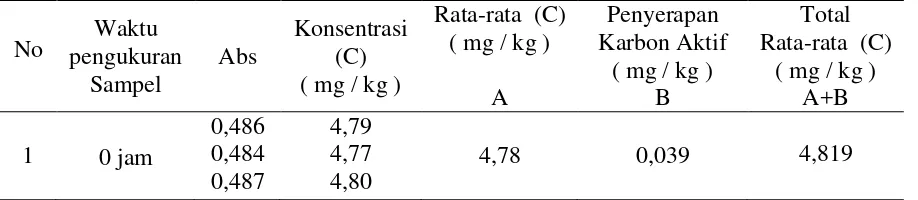
Tabel 4.5. Hasil Pengukuran Kadar Nitrit pada Sayur Bayam tanpa Direbus
Tabel 4.6. Hasil Pengukuran Kadar Nitrit pada Rebusan Sayur Bayam No pengukuran Waktu
Sampel
Abs
Konsentrasi (C) ( mg / kg )
Rata-rata (C) ( mg / kg )
A
Penyerapan Karbon Aktif
( mg / kg ) B
Total Rata-rata (C)
( mg / kg ) A+B
1 0 jam
0,486 0,484 0,487 4,79 4,77 4,80
4,78 0,039 4,819
No Waktu pengukuran Sampel Abs Konsentrasi (C) ( mg / kg )
Rata-rata (C) ( mg / kg )
A
Penyerapan Karbon Aktif
( mg / kg ) B
Total Rata-rata (C)
( mg / kg ) A+B
1 0 jam
0,422 0,424 0,421 4,12 4,14 4,11
4,12 0,039 4,159
2 1 jam
0,532 0,535 0,531 5,28 5,31 5,27
5,28 0,039 5,319
3 2 jam
0,714 0,713 0,716 7,20 7,19 7,23
7,20 0,039 7,239
4 3 jam
0,856 0,852 0,853 8,71 8,66 8,68
8,68 0,039 8,719
5 4 jam
0,988 0,992 0,989 10,10 10,14 10,11
10,11 0,039 10,149
6 5 jam
1,121 1,123 1,124 11,51 11,53 11,54
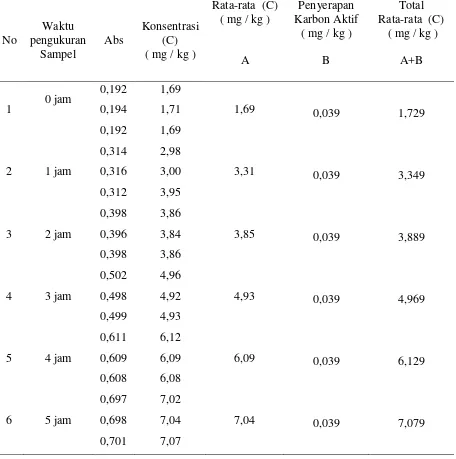
[image:55.612.117.561.272.717.2]Tabel 4.7. Hasil Pengukuran Kadar Nitrit pada Air Rebusan Sayur Bayam No Waktu pengukuran Sampel Abs Konsentrasi (C) ( mg / kg )
Rata-rata (C) ( mg / kg )
A
Penyerapan Karbon Aktif
( mg / kg )
B
Total Rata-rata (C)
( mg / kg )
A+B
1 0 jam
0,192 0,194 0,192 1,69 1,71 1,69
1,69 0,039 1,729
2 1 jam
0,314 0,316 0,312 2,98 3,00 3,95
3,31 0,039 3,349
3 2 jam
0,398 0,396 0,398 3,86 3,84 3,86
3,85 0,039 3,889
4 3 jam
0,502 0,498 0,499 4,96 4,92 4,93
4,93 0,039 4,969
5 4 jam
0,611 0,609 0,608 6,12 6,09 6,08
6,09 0,039 6,129
6 5 jam
0,697 0,698 0,701 7,02 7,04 7,07
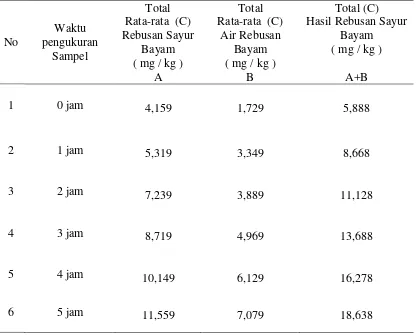
Tabel 4.8. Pengukuran Kadar Nitrit Hasil Rebusan Sayur Bayam
No
Waktu pengukuran
Sampel
Total Rata-rata (C) Rebusan Sayur
Bayam ( mg / kg )
A
Total Rata-rata (C)
Air Rebusan Bayam ( mg / kg )
B
Total (C) Hasil Rebusan Sayur
Bayam ( mg / kg )
A+B
1 0 jam 4,159 1,729 5,888
2 1 jam 5,319 3,349 8,668
3 2 jam 7,239 3,889 11,128
4 3 jam 8,719 4,969 13,688
5 4 jam 10,149 6,129 16,278
4.1.6. Perhitungan jumlah Hasil Rebusan Sayur Bayam yang Dapat Dikonsumsi Setiap Hari Berdasarkan Kadar Nitrit dalam sayur Bayam
Jumlah hasil rebusan sayur bayam yang dapat dikonsumsi setiap hari
berdasarkan kandungan Nitrit pada sayur bayam tersebut dapat diketahui dengan
berpedoman pada ADI (Acceptable Daily Intake) maksimum yang diterima dan
dicerna tanpa mengalami gangguan kesehatan sebesar 8 mg/60 kg berat badan, Di
Indonesia berat badan standard untuk orang dewasa 50-60 kg dan untuk anak-anak
20-30 kg. Hasil perhitungan jumlah maksimum hasil rebusan sayur bayam yang dapat
dikonsumsi berdasarkan kandungan Nitrit sesuai dengan batas ADI dapat dilihat pada
[image:58.612.109.567.372.681.2]tabel 4.9.
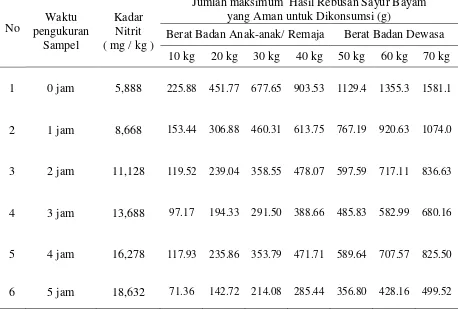
Tabel 4.9. Jumlah Hasil Rebusan Sayur Bayam yang Aman untuk Dikonsumsi Setiap Hari dengan Kandungan Nitrit yang Sesuai Batas ADI
No pengukuran Waktu Sampel
Kadar Nitrit ( mg / kg )
Jumlah maksimum Hasil Rebusan Sayur Bayam yang Aman untuk Dikonsumsi (g)
Berat Badan Anak-anak/ Remaja Berat Badan Dewasa
10 kg 20 kg 30 kg 40 kg 50 kg 60 kg 70 kg
1 0 jam 5,888 225.88 451.77 677.65 903.53 1129.4 1355.3 1581.1
2 1 jam 8,668 153.44 306.88 460.31 613.75 767.19 920.63 1074.0
3 2 jam 11,128 119.52 239.04 358.55 478.07 597.59 717.11 836.63
4 3 jam 13,688 97.17 194.33 291.50 388.66 485.83 582.99 680.16
5 4 jam 16,278 117.93 235.86 353.79 471.71 589.64 707.57 825.50
Dan hasil perhitungan jumlah maksimum rebusan sayur bayam yang dapat
dikonsumsi berdasarkan kandungan Nitrit sesuai dengan batas ADI dapat dilihat pada
[image:59.612.110.567.221.530.2]tabel 4.10.
Tabel 4.10. Jumlah Rebusan Sayur Bayam yang Aman untuk Dikonsumsi Setiap Hari dengan Kandungan Nitrit yang Sesuai Dengan Batas ADI
No
Waktu pengukuran
Sampel
Kadar Nitrit ( mg / kg )
Jumlah maksimum Rebusan Sayur Bayam yang Aman untuk Dikonsumsi (g)
Berat Badan Anak-anak/ Remaja Berat Badan Dewasa
10 kg 20 kg 30 kg 40 kg 50 kg 60 kg 70 kg
1 0 jam 4,159 319,79 639,58 959,37 1.279 1.598 1.918 2.238
2 1 jam 5,319 250,05 500,09 750,14 1.000 1.250 1.500 1.750
3 2 jam 7,239 183,73 367,45 551,18 734,91 918,64 1.102 1.286
4 3 jam 8,719 152,54 305,08 457,62 610,16 762,70 915,24 1.067
5 4 jam 10,149 131,05 262,09 393,14 524,19 655,24 786,28 917,33
4.2. Pembahasan
Pada penelitian ini digunakan karbon aktif untuk menghilangkan warna hijau
daun (klorofil) pada saat pengujian sampel dengan spektrofotometer. Untuk
mengetahui adanya penyerapan karbon aktif terhadap nitrit pada sampel yang diuji
maka dilakukan pembuatan larutan seri standar nitrit dengan menambahkan karbon
aktif dan tanpa menambahkan karbon aktif. Dari hasil pengujian diperoleh selisih nilai
absorbansi dengan penambahan dan tanpa penambahan karbon aktif. Setelah
disubtitusi ke persamaan regresi maka diperoleh rata-rata selisih konsentrasi nitrit
pada larutan seri standar nitrit sebesar 0,0369 mg/L. Pegujian ini menyatakan bahwa
karbon aktif dapat menyerap kandungan nitrit pada sampel sebesar 0,0369 mg/L .
Maka pada perhitungan hasil akhir total rata-rata konsentrasi kandungan nitrit pada
masing-masing sampel ditambahkan 0,0369 mg/L .
Dari penelitian