STUDI PENAMBAHAN SARI BUAH TERHADAP
KARAKTERISTIK MINUMAN SINBIOTIK EKSTRAK DAUN
CINCAU DAN PENGARUHNYA TERHADAP STATUS
ANTIOKSIDAN HATI MENCIT
Oleh
IKE LESY RIYANTI SYAH
TESIS
Sebagai Salah Satu Syarat untuk Mencapai Gelar MAGISTER SAINS
Pada
Program Studi Pascasarjana Teknologi Industri Pertanian Fakultas Pertanian Universitas Lampung
PROGRAM STUDI PASCASARJANA
MAGISTER TEKNOLOGI INDUSTRI PERTANIAN FAKULTAS PERTANIAN
UNIVERSITAS LAMPUNG BANDAR LAMPUNG
ABSTRAK
Cincau hijau berpotensi sebagai bahan baku pembuatan minuman sinbiotik. Selain mengandung pektin sebagai substrat pertumbuhan bakteri asam laktat, estrak daun cincau hijau mengandung aktivitas antioksidan sebesar 44,38%. Pemberian ekstrak daun cincau hijau terhadap kadar antioksidan hati tikus tidak berbeda nyata dengan perlakuan tikus yang diberi pakan standar. Sehingga dibutuhkan sayur atau buah-buahan yang dapat menambah kandungan antioksidannya. Buah-buahan yang mengandung antioksidan, mudah diperoleh di Indonesia serta murah harganya diantaranya adalah jambu biji dengan kandungan antioksidan sebesar 64,13% dan sari buah nanas mengandung aktivitas antioksidan sebesar 58,27%. Namun belum diketahui jenis sari buah dan konsentrasi sari buah yang dapat menghasilkan karakteristik terbaik yang dapat menurunkan status antioksidan hati mencit. Tujuan dari penelitian ini adalah menentukan jenis dan konsentrasi sari buah yang memiliki karakteristik minuman sinbiotik terbaik dan mengevaluasi pengaruh minuman sinbiotik terbaik terhadap status antioksidan hati mencit.
Minuman sinbiotik cincau dengan penambahan sari buah jambu biji 15% dengan total bakteri asam laktat sebesar sebesar 11,22 log koloni/ml, nilai pH sebesar 3, 65, total asam laktat sebesar 0,61%, aktivitas antioksidan sebesar 77,11%, warna dengan skor 3,83 (suka), aroma dengan skor 3,69 (suka), rasa dengan skor 3,72 (suka), dan penerimaan keseluruhan dengan skor 3,74 (suka). Sedangkan minuman sinbiotik cincau dengan penambahan sari buah nanas 15% menghasilkan total bakteri asam laktat sebesar sebesar 11,23 log koloni/ml, nilai pH sebesar 3,51, total asam laktat sebesar 0,60%, aktivitas antioksidan sebesar 68,23%, warna dengan skor 3, 65 (suka), aroma dengan skor 3,56 (suka), rasa dengan skor 3,54 (suka), dan penerimaan keseluruhan dengan skor 3,50 (suka). Perlakuan yang terbaik yaitu minuman sinbiotik cincau yang ditambah sari buah jambu biji 15%, karena memiliki nilai karakteristik yang lebih tinggi dibandingkan dengan penambahan sari buah nanas 15%.
Minuman sinbiotik yang memiliki karakteristik terbaik yaitu dengan penambahan jenis sari buah jambu biji dengan penambahan konsentrasi sari buah jambu biji 15%. Menghasilkan total bakteri asam laktat sebesar sebesar 11,22 log koloni/ml, nilai pH sebesar 3, 65, total asam laktat sebesar 0,61%, aktivitas antioksidan sebesar 77,11%, warna dengan skor 3,83 (suka), aroma dengan skor 3,69 (suka), rasa dengan skor 3,72 (suka), dan penerimaan keseluruhan dengan skor 3,74 (suka). Kadar MDA hati mencit kelompok yang diberi perlakuan minuman sinbiotik cincau hijau dengan penambahan sari buah jambu biji tidak berbeda nyata dengan kelompok perlakuan minuman sinbiotik cincau hijau dan kontrol aquades.
Dengan mengucap rasa syukur kehadirat Allah
SWT, Ku persembahkan sebentuk goresan tangan
dan curahan pikiranku sebagai tanda cinta dan
baktiku untuk ayah dan ibu tercinta, adik-adikku
tersayang, dosen-dosen sebagai orang tuaku di
kampus yang telah membimbingku, dan
iii
1. Tahap I (Optimasi Jenis dan Konsentrasi Penambahan Sari Buah) ... 13
1.4. Pembuatan Sari Buah Jambu Biji dan Nanas... 19
1.5. Pembuatan minuman sinbiotik ekstrak daun cincau hijau dengan kombinasi sari buah jambu biji dan sari buah nanas….. 21
2. Penelitian Tahap II ... 22
E. Pengamatan ... 25
iv
3. Nilai Derajat Keasaman (pH) ... 26
4. Aktivitas Antioksidan ... 27
5. Uji Organoleptik ... 27
B. Penelitian Tahap II ... 28
Analisis Malonaldehida (MDA) Hati Mencit ... 28
IV. HASIL DAN PEMBAHASAN ... 30
A. Penelitian Tahap I... 30
1. Total Bakteri Asam Laktat ... 30
2. Derajat Keasaman (pH) ... 34
3. Total Asam Laktat ... 37
4. Aktivitas Antioksidan ... 40
5. Uji Organoleptik ... 42
6. Penentuan Perlakuan Terbaik ... 49
B. Penelitian Tahap II ... 50
Kadar MDA Hati Mencit ... 50
V. SIMPULAN DAN SARAN ... 55
A. Simpulan ... 55
B. Saran ... 55
DAFTAR PUSTAKA ... 57
I. PENDAHULUAN
A. Latar Belakang dan Masalah
Akhir-akhir ini kajian tentang probiotik sering dikaitkan dengan prebiotik. Di
dalam usus, prebiotik merupakan nutrisi yang sesuai bagi bakteri yang
menguntungkan seperti bakteri asam laktat (Lactobacillus). Kombinasi antara
probiotik dan prebiotik untuk meningkatkan kesehatan tubuh disebut sinbiotik.
Salah satu sumber prebiotik yang potensial adalah ekstrak cincau hijau karena
kandungan pektinnya. Oleh karena itu cincau hijau berpotensi sebagai bahan
baku pembuatan minuman sinbiotik.
Antioksidan merupakan salah satu senyawa kimia fungsional yang penting karena
antioksidan dapat melindungi organisme hidup dari efek negatif oksidasi. Secara
alami tubuh telah membuat antioksidan endogen untuk menangkal radikal bebas
yang masuk dalam tubuh. Namun ketidak seimbangan antara oksidan dan
antioksidan di dalam tubuh dapat menyebabkan kerusakan oksidatif yang
mengakibatkan terjadinya berbagai macam penyakit (Winarsih, 2007). Oleh
karena itu diperlukan makanan atau minuman yang dapat menjadi sumber
antioksidan. Selain mengandung pektin sebagai substrat pertumbuhan bakteri
asam laktat, estrak daun cincau hijau mengandung aktivitas antioksidan sebesar
pemberian ekstrak daun cincau hijau terhadap kadar antioksidan hati tikus tidak
berbeda nyata dengan perlakuan tikus yang diberi pakan standar.
Ekstrak cincau hijau sebagai sumber antioksidan, dapat ditambahkan sayur atau
buah-buahan yang dapat menambah nilai atau kandungan antioksidannya.
Buah-buahan yang mengandung antioksidan, mudah diperoleh di Indonesia serta murah
harganya diantaranya adalah jambu biji dengan kandungan antioksidan sebesar
64,13% dan sari buah nanas mengandung aktivitas antioksidan sebesar 58,27%.
Namun belum diketahui jenis sari buah dan konsentrasi sari buah yang dapat
menghasilkan karakteristik terbaik yang dapat menurunkan status antioksidan hati
mencit.
B. Tujuan Penelitian
Tujuan dari penelitian ini adalah :
1. Menentukan jenis dan konsentrasi sari buah yang memiliki karakteristik
minuman sinbiotik terbaik
2. Mengevaluasi pengaruh minuman sinbiotik terbaik terhadap status antioksidan
hati mencit.
C. Kerangka Pemikiran
Menurut Pitojo (1998), daun cincau hijau mempunyai kandungan gizi sebagai
berikut : protein 2,39-2,70%, karbohidrat total yang teranalisis 8,41-8,96%, lemak
0,45-0,51%, serat kasar 6,23-6,70%, dan air 66,33-74,54%. Ekstrak tersebut
menunjukkan ekstrak daun cincau hijau mengandung pektin yang termasuk jenis
serat pangan larut air yang dapat difermentasi dengan baik oleh mikroflora usus
besar (Gallaher, 2000; Dongowski, et.al., 2002; Aprikian, et.al., 2003). Dari
karakteristiknya, diduga pektin yang terkandung pada ekstrak cincau hijau adalah
pektin bermetoksi rendah yang lebih mudah difermentasi (Dongowski, et.al.,
2002). Nurdin dan Nurainy (2007) menyatakan bahwa ekstrak cincau hijau dapat
dijadikan sebagai substrat pertumbuhan bakteri probiotik L. casei dan L.
plantarum.
Berdasarkan potensi tersebut, perlu dikembangkan pemanfaatan cincau hijau
sebagai sumber serat pangan dan sumber antioksidan. Salah satu cara pemanfaatan
daun cincau hijau yaitu diolah menjadi produk minuman sinbiotik. Konsumsi
sinbiotik diharapkan dapat meningkatkan jumlah bakteri yang menguntungkan
seperti Lactobacillus casei, dan menurunkan bakteri merugikan seperti Koliform,
E. coli, dan Salmonella.
Daun cincau hijau juga mengandung senyawa antioksidan yaitu flavonoid,
polifenol dan alkaloid (Chalid, 2002). Ekstrak daun cincau juga mengandung
senyawa antioksidan (Nurdin, 2005; Chalid, 2002), dapat menghambat
pertumbuhan kanker (Chalid, 2002). Berdasarkan berbagai penelitian in vitro dan
in vivo tersebut maka ekstrak cincau hijau dapat digolongkan sebagai serat pangan
antioksidan (antioxidant dietary fibre) (Saura-Calixto, 2003). Ekstrak cincau
hijau yang diekstrak dengan larutan asam sitrat memiliki aktivitas antioksidan
yang lebih baik dan menunjukkan karakteristik fungsional yang menguntungkan,
2005). Untuk menambah persentase antioksidan maka ditambahkan sumber
antioksidan dari buah jambu biji (Psidium guajava L) dan nanas (Ananas
comosus). Jambu biji mengandung antioksidan yaitu vitamin C, provitamin A,
karoteinoid 19 jenis tetapi yang dominan yaitu beta karoten, lutein, zeaxanthin,
cryptoxanthin dan likopen, sedangkan buah nanas memiliki kandungan
antioksidan vitamin C, karotenoid (Lingga, 2012). Pada penelitian ini diharapkan
terdapat jenis sari buah dan persentase sari buah yang tepat untuk mendapatkan
minuman sinbiotik dengan aktivitas antioksidan tertinggi.
Di dalam tubuh manusia secara terus menerus terbentuk radikal bebas melalui
metabolisme sel normal, peradangan, kekurangan gizi, dan akibat pengaruh dari
luar tubuh seperti polusi lingkungan, ultraviolet, asap rokok, dan lainnya. Sistem
antioksidan tubuh sebagai mekanisme perlindungan terhadap serangan radikal
bebas, secara alami telah ada dalam tubuh manusia (Winarti, 2010).
Asam lemak tak jenuh yang mengalami peroksidasi yang membentuk produk
Malonaldehide. Salah satu tolok ukur yang menentukan seberapa banyak oksidan
yang terbentuk didalam tubuh adalah dengan diketahuinya kadar MDA. Hepar
sebagai pintu gerbang semua bahan yang masuk tubuh melalui saluran cerna
merupakan organ yang sangat potensial menderita keracunan lebih dahulu
sebelum organ yang lain. Untuk mengetahui manfaat minuman sinbiotik ekstrak
daun cincau hijau sari buah yang dihasilkan maka dilakukan evaluasi minuman
sinbiotik pada jangka waktu tertentu terhadap status antioksidan mencit dengan
D. Hipotesis Penelitian
Hipotesis penelitian ini adalah :
1. Terdapat jenis dan konsentrasi sari buah yang dapat menghasilkan
karakteristik minuman sinbiotik terbaik.
2. Terdapat pengaruh minuman sinbiotik terbaik terhadap status antioksidan hati
mencit.
II. TINJAUAN PUSTAKA
A. Minuman Sinbiotik
Sinbiotik merupakan probiotik dan prebiotik yang dikombinasikan dalam produk
makanan. Probiotik merupakan mikroorganisme non patogen yang hidup sebagai
mikroflora pencernaan yang dapat memberikan pengaruh positif terhadap
kesehatan manuia, sedangkan prebiotik merupakan substrat atau bahan makanan
bagi bakteri probiotik dimana substrat ini akan membantu meningkatkan
pertumbuhan dan keaktifan satu atau lebih bakteri probiotik yang berada dalam
satu kolon sehingga diperoleh kondisi fisiologis dan metabolik yang dapat
memberikan perlindungan pada kesehatan saluran pencernaan.
Minuman sinbiotik yaitu minuman yang mengandung prebiotik dan probiotik.
Mekanisme kerja prebiotik dan probiotik dalam meningkatkan daya tahan usus
antara lain dengan cara mengubah lingkungan saluran usus baik pH ataupun kadar
oksigennya, berkompetisi dengan bakteri jahat hingga mengurangi kesempatan
untuk bakteri jahat berkembang biak. Penggunaan sinbiotik memungkinkan untuk
mengontrol jumlah mikroflora baik di dalam saluran pencernaan. Kombinasi
yang baik antara prebiotik dan probiotik dapat meningkatkan jumlah bakteri baik
(probiotik) yang mampu bertahan hidup dalam saluran pencernaan dengan
Manfaat produk sinbiotik telah banyak diungkapkan. Salah satu yang terpenting
adalah kemampuannya untuk mengatasi diare yang disebabkan bakteri patogen
dan menjaga keseimbangan mikroflora saluran pencernaan. Menurut Collins dan
Gibson (1999) mekanisme penting dari pengaruh sinbiotik adalah melalui
pengaruhnya terhadap mikroflora usus besar. Konsumsi sinbiotik diharapkan
dapat meningkatkan jumlah bakteri yang menguntungkan, seperti Bifidobacteria
dan Lactobacillus dan menurunkan bakteri merugikan penyebab diare.
B. Ekstrak Daun Cincau Hijau
Tumbuhan cincau hijau (Premna oblongifolia Merr.) merupakan tanaman berkayu
yang tumbuh tegak dan bebas. Daun cincau hijau mengandung flavonoid,
saponin, polifenol dan alkaloid. Flavonoid adalah senyawa yang memiliki aktifitas
antioksidan yang dapat mempengaruhi beberapa reaksi yang tidak diinginkan
dalam tubuh, misalnya dapat menghambat reaksi oksidasi, sebagai pereduksi radikal hidroksil dan superoksid serta radikal peroksil (Djam’an, 2008).
Cincau sangat baik dikonsumsi oleh semua kalangan. Bahan ini sangat kaya
mineral terutama kalsium dan fosfor. Cincau dipercaya mampu meredakan panas
dalam, sembelit, perut kembung, demam dan diare. Serat bermanfaat untuk
membersihkan organ pencernaan dari zat karsinogen penyebab kanker. Selain itu,
cincau juga baik dikonsumsi bagi orang yang sedang menjalani diet karena
memiliki kandungan serat yang tinggi namun rendah kalori (Sutomo, 2006).
Ekstrak daun cincau hijau yang mengandung pektin hingga 40% (Nurdin, 2005).
olongifolia Merr) menunjukkan potensinya sebagai serat pangan yang bersifat
laksatif.
C. Sari Buah
Sari buah adalah sari alami yang bersumber dari buah. Sari buah dapat diperoleh
dari hasil perasan buah. Sari buah dapat diperoleh dari berbagai buah-buahan,
adapun buah yang dapat diambil sarinya yaitu buah nanas dan jambu biji. Nanas
berasal dari kata pina, nama yang diberikan oleh orang spanyol yang mirip dengan
buah cemara (pinecone) yang berbentuk mengerucut. Berbeda dengan buah
lainnya nanas tidak mempunyai pati, namun mempunyai karbohidrat dalam
bentuk gula ketika nanas dipanen. Karbohidrat pati dalam nanas akan diubah
langsung menjadi gula ketika nanas masak (matang) (Herliani, 2010).
Zat gizi nanas terutama adalah mineral-mineral seperti kalsium, potassium,
mangan magnesium dan fosfor. Selain itu terdapat vitamin B6, thiamin, dan folat,
juga senyawa fitokimia yang baik untuk kesehatan (Herliani, 2010). Nanas
merupakan salah satu buah yang banyak mengandung mangan. Mineral mikro ini
sangat diperlukan tubuh untuk memproduksi enzim SOD yang berperan sebagai
antioksidan endogen. Kemampuan nanas sebagai antioksidan semakin lengkap
karena buah ini mengandung vitamin C dan beta karoten yang cukup tinggi
(Lingga, 2012).
Jambu merupakan buah sebagai sumber vitamin A (beta karoten) dan kaya dengan
vitamin C. buah jambu biji mempunyai kandungan vitamin C tertinggi
seperti likopen dan karoten, polifenol dan flavonoid (Herliani, 2010). Vitamin C
memiliki aktivitas biologic yang sangat baik sebagai antioksidan. Aktivitas
antioksidan vitamin C tidak sendirian, melainkan dibantu oleh karotenoid yang
banyak terdapat pada jambu biji, karotenoid yang paling dominan adalah beta
karoten. Beta karoten dan beberapa karotenoid lainnya merupkan pro vitamin A
dimana nantinya akan diubah menjadi vitamin A yang dapat dimanfaatkan oleh
tubuh untuk berbagai aktivitas biologis termasuk sebagai antioksidan (Lingga,
2012).
D. Antioksidan
Antioksidan merupakan senyawa kimia yang dapat menyumbangkan satu atau
lebih elektron kepada radikal bebas, sehingga radikal bebas tersebut dapat
diredam (Suhartono, 2002). Antioksidan dapat menetralisir radikal bebas sehingga
atom dengan elektron yang tidak berpasangan, mendapatkan pasangan
elektronnya. Peran positif dari antioksidan adalah membantu sistem pertahanan
tubuh bila ada unsur pembangkit penyakit memasuki dan menyerang tubuh
termasuk penyakit degeneratif pada usia lanjut seperti arteriosklerosis, demensu
penyakit Alzheimer serta membantu menekan proses penuaan. (Barus, 2009).
Antioksidan digunakan sebagai upaya untuk memperkecil terjadinya proses
oksidasi dari lemak dan minyak, memperkecil terjadinya proses kerusakan dalam
makanan, memperpanjang masa pemakaian dalam industri makanan,
meningkatkan stabilitas lemak yang terkandung dalam makanan serta mencegah
faktor yang cukup berperan dalam kerusakan selama dalam penyimpanan dan
pengolahan makanan.
Berdasarkan sumber perolehannya ada 2 macam antioksidan, yaitu antioksidan
alami dan antioksidan buatan (sintetik) (Dalimartha dan Soedibyo, 1999).
Antioksidan alami mampu melindungi tubuh terhadap kerusakan yang disebabkan
spesies oksigen reaktif, mampu menghambat terjadinya penyakit degeneratif serta
mampu menghambat peroksidae lipid pada makanan. Meningkatnya minat untuk
mendapatkan antioksidan alami terjadi beberapa tahun terakhir ini. Antioksidan
alami umumnya mempunyai gugus hidroksi dalam struktur molekulnya (Sunarni,
2005). Antioksidan sintetik merupakan antioksidan yang diperoleh dari hasil
sintesa reaksi kimia. Contoh antioksidan sintetik yang diizinkan penggunaan
untuk makanan yaitu Butil Hidroksi Anisol (BHA), Butil Hidroksi Toluen (BHT),
propil galat (PG), Tert-Butil Hidoksi Quinon (TBHQ) dan tokoferol. Antioksidan
tersebut merupakan antioksidan alami yang telah diproduksi secara sintetis untuk
tujuan komersial (Buck 1991)
E. Hati Mencit
Mencit (Mus musculus L) merupakan salah satu species atau jenis tikus, termasuk
oleh Rodentia, Sub ordo Myomorpha, famili Muridae. Famili Muridae merupakan
famili yang dominan dari ordo Rodentia karena mempunyai daya reproduksi yang
tinggi, pemakan segala macam makanan dan mudah beradaptasi dengan
lingkungan yang diciptakan dengan lingkungan yang diciptakan manusia. Jenis
tikus yang sering ditemukan adalah jenis Rattus dan Mus (Anonim, 1984 dalam
malam hari serta mudah ditangani. Mencit laboratorium mempunyai berat badan
kira-kira sama dengan mencit liar, tetapi setelah diternakkan secara selektif
selama delapan puluh tahun yang lalu, sekarang terdapat berbagai warna bulu dan
timbul banyak galur dengan berat badan berbeda-beda. Berat badan bervariasi,
tetapi umumnya pada umur empat minggu berat badan mencapai 18 g - 20 g.
Hati sebagai pintu gerbang semua bahan yang masuk tubuh melalui saluran cerna
merupakan organ yang sangat potensial menderita keracunan terlebih dahulu
sebelum organ yang lain. Struktur anatomik hati mencit terdiri atas lobulus yang
berisi vena porta, arteria hepatica, sinusoid, vena sentral, saluran empedu,
hepatosit, sel kupler, jaringan saraf, dan jaringan ikat. Jika terjadi keracunan
senyawa metabolit maka akan terjadi kerusakan di sekitar vena sentralis lebih
dahulu sebagai nekrosis sentralobularis. Selain itu akibat keracunan juga dapat
III. BAHAN DAN METODE
A. Tempat dan Waktu Penelitian
Penelitian ini dilakukan di Laboratorium Analisis Hasil Pertanian dan
Laboratorium Pengolahan Hasil Pertanian dan Biomassa Jurusan Teknologi Hasil
Pertanian, Fakultas Pertanian, Universitas Lampung. Penelitian ini dilaksanakan
pada bulan November 2012 sampai bulan Maret 2013.
B. Bahan dan Alat
Bahan yang digunakan dalam penelitian adalah daun cincau dari tanaman cincau
pohon (Premna oblongifolia Merr) yang dipetik mulai dari daun ke 5 ke arah
pangkal, daun cincau diperoleh dari Daerah Way Halim, Bandar Lampung. Buah
nanas (Ananas comosus) jenis queen dan jambu biji (Psidium guajava L) dengan
tingkat kematangan mature yang diperoleh dari Chandra Super Store. Mencit
(Mus musculus L.) usia 2 bulan sampai 3 bulan yang diperoleh dari Balai Penyidik
dan Pengujian Veteriner (BPPV) Regional III Bandar Lampung. Inokulum kultur
murni Lactobacillus casei FNCC 0900 yang diperoleh dalam bentuk murni dari
Pusat Antar Universitas (PAU) Pangan dan Gizi Universitas Gajah Mada,
Yogyakarta. Susu skim, sukrosa dan asam sitrat diperoleh dari Chandra Super
Store. Glukosa yang diperoleh dari CV. Animo Bandar Lampung. Ransum
Bahan analisis yang digunakan adalah De Mann Ragosa Sharp (MRS) Broth,
MRS Agar sebagai media tumbuh dan analisis Bakteri Asam Laktat, aquadest,
larutan NaCl, alkohol 70%, larutan NaOH 0,1N, indikator phenolphtlein, DPPH
0,08 mM, etanol, PBS Tablet, KCl, Buffer phosphat, potassium chloride, sodium
chloride, TBA, BHT, HCl, TCA dan bahan analisis lainnya.
Alat-alat yang digunakan antara lain timbangan analitik dua digit (Mettler PJ
3000), laminary flow (merk Esco), oven (Heraeus dan Philips Harris Ltd), blender
(Sharp), inkubator (Memmert), spektrofotometri UV (HACH), pH meter (Hanna
Instruments 8424), autoclave (Wise Calve, Daihan Scientific), colony counter
(Stuart Scientific), mikropipet (Thermo Scientific), erlenmeyer, tabung reaksi,
cawan petri, gelas ukur, dan alat-alat gelas lainnya untuk analisis kimia dan
mikrobiologi. Sedangkan alat-alat yang digunakan untuk uji in vivo adalah spuit
volume 1 ml yang telah ditumpulkan sebagai alat pemberian sampel secara oral,
seperangkat kandang percobaan, tempat air minum mencit, tempat makan mencit,
timbangan mencit, gunting untuk membedah mencit, sarung tangan, cool box,
vortex.
C. Metode Penelitian
Pada penelitian ini dilakukan dua tahap penelitian, yaitu penelitian tahap I
(Pengaruh Jenis dan Konsentrasi Penambahan Sari Buah) dan penelitian tahap II
(Uji In Vivo)
1. Tahap I (Pengaruh Jenis dan Konsentrasi Penambahan Sari Buah)
Rancangan percobaan yang digunakan pada penelitian tahap pertama adalah
Faktor Pertama adalah jenis sari buah yang terdiri dari dua taraf yaitu sari buah
jambu biji merah (G) dan sari buah nanas (N). Faktor kedua adalah konsentrasi
sari buah yang terdiri dari lima taraf yaitu konsentrasi 0% (1), 5% (2), 10% (3),
15% (4), dan 20% (5). Data yang diperoleh diuji kesamaan ragamnya dengan uji
Bartlet dan uji kemenambahan data dengan uji Tuckey, kemudian data dianalisis
sidik ragam untuk mengetahui ada tidaknya perbedaan antar perlakuan. Data
dianalisis lanjut dengan uji Beda Nyata Terkecil (BNT) pada taraf 5%.
Masing-masing produk minuman sinbiotik dianalisis untuk mendapatkan produk yang
terbaik berdasarkan parameter total bakteri asam laktat, total asam laktat, pH, uji
organoleptik dengan parameter berupa warna, rasa, aroma, dan penerimaan
keseluruhan, dan aktivitas antioksidan.
2. Tahap II (Uji In Vivo)
Penelitian tahap kedua (uji In Vivo) adalah pengujian pada hewan percobaan
dengan menggunakan mencit untuk dievaluasi status antioksidan hati. Penelitian
ini bertujuan untuk mendapatkan informasi pengaruh pemberian minuman
sinbiotik sari buah terbaik terhadap kadar peroksida lipid mencit. Perlakuan dosis
ditetapkan berdasarkan dosis anjuran untuk susu fermentasi bagi manusia dengan
berat badan 70 kg yaitu sekitar 100-200 ml/hari (Riyanto, 2011), serta berdasarkan
anjuran konsumsi minuman probiotik komersial yaitu 100 ml per orang per hari.
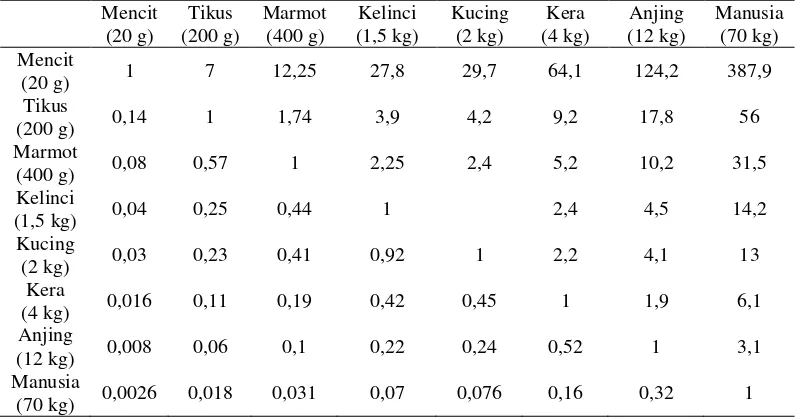
Konversi berat badan mencit 20 g dengan berat badan manusia 70 kg adalah
0,0026 (Amalina, 2009) seperti disajikan pada Tabel 1.
Uji status antioksidan hati mencit dibagi dalam 3 kelompok yaitu kelompok 1
kelompok 3 minuman sinbiotik ekstrak cincau hijau yang dikombinasikan sari
buah dengan aktivitas antioksidan tertinggi. Perlakuan dilakukan selama 30 hari.
Masing-masing kelompok terdiri dari 9 ekor mencit sehingga jumlah mencit untuk
uji tersebut ada 27 ekor. Rancangan percobaan yang digunakan pada penelitian
tahap kedua adalah Rancangan Acak Lengkap (RAL). Data yang diperoleh diuji
kesamaan ragamnya dengan uji Bartlet dan uji kemenambahan data dengan uji
Tuckey, kemudian data dianalisis sidik ragam untuk mengetahui ada tidaknya
perbedaan antar perlakuan. Data dianalisis lanjut dengan uji Beda Nyata Terkecil
(BNT) pada taraf 5%.
Sumber : Laurence dan Bacharach, 1964 (dalam Amalina, 2009)
D. Pelaksanaan Penelitian
1. Penelitian Tahap I
Penelitian tahap I bertujuan untuk mendapatkan minuman sinbiotik ekstrak cincau
untuk perlakuan dengan pemberian oral pada uji in vivo mencit. Pembuatan
minuman sinbiotik ekstrak cincau hijau terdiri dari beberapa tahapan, yaitu :
1.1.Pembuatan Bubuk Daun Cincau Hijau Kering
Pembuatan bubuk daun cincau dilakukan dengan menggunakan metode Nurdin
dkk. (2004). Daun cincau dicuci dengan air hingga bersih dan tangkainya
dibuang. Daun cincau yang telah dibersihkan dipotong 3 cm x 1,5 cm, kemudian
dikeringkan dengan oven pada suhu 50 oC selama kurang lebih 24 jam. Daun dianggap kering bila daun terasa renyah bila diremas. Daun cincau yang telah
kering kemudian dihancurkan dengan menggunakan blender hingga menjadi
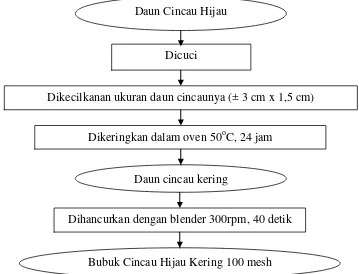
bubuk. Diagram alir pembuatan bubuk daun cincau hijau dapat dilihat pada
Gambar 1.
Gambar 1. Diagram alir pembuatan bubuk daun cincau hijau kering Sumber : Nurdin, dkk. (2004)
Daun Cincau Hijau
Dicuci
Dikecilkanan ukuran daun cincaunya (± 3 cm x 1,5 cm)
Dikeringkan dalam oven 50oC, 24 jam Daun cincau kering
Dihancurkan dengan blender 300rpm, 40 detik
1.2. Proses Ekstraksi Bubuk Daun Cincau Hijau
Sebanyak 25 g bubuk daun cincau hijau dicampurkan dengan air panas (suhu +
100oC) sebanyak 500 ml. Air yang akan digunakan sebelumnya ditambahkan asam sitrat 0,1% (b/v). Kemudian dilakukan pencampuran menggunakan stirrer
dengan kecepatan penuh selama 15 menit untuk membantu proses ekstraksi.
Campuran tersebut disaring dengan menggunakan kain saring sambil dilakukan
peremasan hingga diperoleh cairan kental ekstrak daun cincau. Cairan ekstrak
daun cincau tersebut dikeringkan dalam oven pada suhu 50oC selama 48 jam. Hasil pengeringan tersebut kemudian dihancurkan dengan menggunakan blender
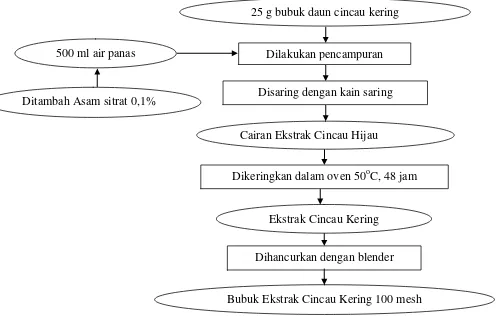
hingga tingkat kehalusan tertentu. Diagram alir proses ekstraksi bubuk daun
cincau hijau dapat dilihat pada Gambar 2.
Gambar 2. Diagram alir pembuatan bubuk ekstrak daun cincau Sumber : Nurdin, dkk. (2004)
500 ml air panas
Ditambah Asam sitrat 0,1%
Dikeringkan dalam oven 50oC, 48 jam
Dihancurkan dengan blender Ekstrak Cincau Kering
Bubuk Ekstrak Cincau Kering 100 mesh Cairan Ekstrak Cincau Hijau
Dilakukan pencampuran
1.3.Persiapan Starter
Persiapan starter dilakukan dengan memodifikasi metode Rizal dkk. (2006).
Kultur bakteri yang akan digunakan (Lactobacillus casei) dipindahkan dari kultur
stok ke dalam tabung reaksi berisi media MRS Broth steril. Dari MRS Broth
Steril, selanjutnya diinkubasi selama 24 jam pada suhu 37oC. Kemudian sebanyak sebanyak 4% (v/v) kultur ditumbuhkan ke dalam media yang
mengandung 5% (b/v) susu skim yang telah disterilisasi pada suhu 121o C selama 15 menit dan diinkubasi selama 48 jam pada suhu 37oC. Kultur yang dihasilkan disebut kultur induk.
Selanjutnya dari kultur induk diinokulasikan ke media yang sama yaitu sebanyak
4% (v/v) kultur ditumbuhkan ke dalam media yang mengandung 5% (b/v) susu
skim yang telah disterilisasi pada suhu 121o C selama 15 menit dan diinkubasi selama 48 jam pada suhu 37oC sehingga dihasilkan kultur antara. Kemudian kultur antara diinokulasikan sebanyak 4% (v/v) ke dalam media yang
mengandung 5% (b/v) susu skim steril dengan penambahan sukrosa 3% (b/v),
kemudian diinkubasi pada suhu 37oC selama 24 jam untuk mendapatkan kultur kerja. Pada proses pembuatan minuman sinbiotik ekstrak daun cincau hijau dan
minuman sinbiotik ekstrak daun cincau hijau yang diformulasi sari buah, kultur
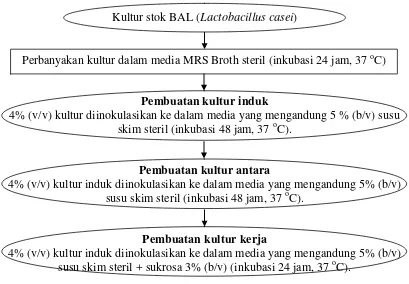
kerja sebanyak 4% (v/v) akan digunakan sebagai starter atau inokulum. Diagram
Perbanyakan kultur dalam media MRS Broth steril (inkubasi 24 jam, 37 oC) Kultur stok BAL (Lactobacillus casei)
Pembuatan kultur induk
4% (v/v) kultur diinokulasikan ke dalam media yang mengandung 5 % (b/v) susu skim steril (inkubasi 48 jam, 37 oC).
Pembuatan kultur antara
4% (v/v) kultur induk diinokulasikan ke dalam media yang mengandung 5% (b/v) susu skim steril (inkubasi 48 jam, 37 oC).
Pembuatan kultur kerja
4% (v/v) kultur induk diinokulasikan ke dalam media yang mengandung 5% (b/v) susu skim steril + sukrosa 3% (b/v) (inkubasi 24 jam, 37 oC).
Gambar 3. Diagram alir pembuatan starter
Sumber : Rizal, dkk. (2006),yang telah dimodifikasi
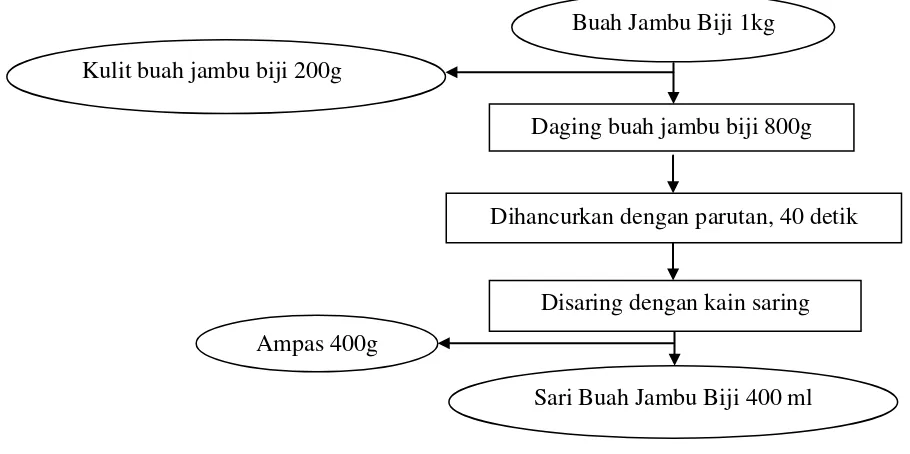
1.4. Pembuatan Sari Buah Jambu Biji dan Nanas
Buah jambu biji mula-mula dikupas kulitnya lalu dicuci. Dilakukan
penghancuran dengan diparut selama 40 detik, kemudian dilakukan penyaringan
sehingga diperoleh sari buah jambu biji. Prosedur pembuatan sari buah jambu biji
dapat dilihat pada Gambar 4. Buah nanas mula-mula dikupas kulitnya dan
dibersihkan mata nanasnya lalu dicuci. Dilakukan penghancuran dengan diparut
selama 40 detik, kemudian dilakukan penyaringan sehingga diperoleh sari buah
Gambar 4. Pembuatan sari buah jambu biji
Sumber : Rizal, dkk. (2006), yang telah dimodifikasi
Gambar 5. Pembuatan sari buah nanas
Sumber : Rizal, dkk. (2006),yang telah dimodifikasi
1.5.Pembuatan minuman sinbiotik ekstrak daun cincau hijau dengan kombinasi sari buah jambu biji dan sari buah nanas
Proses pembuatan minuman sinbiotik dari ekstrak cincau hijau dengan
menggunakan metode yang telah dilakukan pada penelitian sebelumnya (Nurdin, Buah Jambu Biji 1kg
Daging buah jambu biji 800g Kulit buah jambu biji 200g
Sari Buah Jambu Biji 400 ml Ampas 400g
Dihancurkan dengan parutan, 40 detik
Disaring dengan kain saring
Daging buah nanas 700g Buah Nanas 1kg Kulit buah dan mata nanas 300g
Sari Buah Nanas 400g Ampas 300g
Dihancurkan dengan parutan, 40 detik
dkk, 2007). Diagram alir pembuatan minuman sinbiotik ekstrak cincau hijau
dengan kombinasi sari buah jambu biji dan sari buah nanas dapat dilihat pada
Gambar 6. Sebanyak 2% (b/v) susu skim ditambah ekstrak cincau hijau sebanyak
0,5% (b/v), dilakukan penambahan sari buah jambu biji dan sari buah nanas ke
dalam masing-masing fermentor dengan konsentrasi 0, 5, 10, 15, 20% (b/v),
selanjutnya dilakukan penambahan aquades hingga volumenya menjadi 120 ml
kemudian campuran ini diaduk hingga rata menggunakan spatula kaca selama 30
detik, kemudian dipasteurisasi 76 oC selama 15 menit, selanjutnya didinginkan hingga suhu 37 oC. Kultur kerja Lactobacillus casei diinokulasi sebanyak 4% (v/v) dan diinkubasi dalam inkubator pada suhu 37 oC selama 48 jam.
2. Penelitian Tahap II
Pengujian in vivo menggunakan mencit (Mus musculus L.) jantan umur 2 sampai
3 bulan dengan berat rata-rata 20 g sampai 30 g. Mencit yang digunakan untuk uji
in vivo diperoleh dari Balai Penyidik dan Pengujian Veteriner (BPPV) Regional
III Bandar Lampung. Pakan mencit berupa pellet ayam diperoleh dari CV. Sanusi
Taufik Bandar Lampung. Sedangkan air minum yang diberikan adalah air
mineral (merk Aqua). Sebelum diberi perlakuan, mencit diadaptasi selama 7 hari
pada kandang percobaan dengan diberi pakan pellet ayam dan air minum secara
ad libitum agar dapat menyesuaikan diri dengan lingkungannya. Setelah 7 hari
adaptasi, dilakukan penimbangan berat badan mencit, selanjutnya mencit dibagi
dalam 3 kelompok yaitu kelompok 1 kontrol (Aquades), kelompok II minuman
sinbiotik ekstrak cincau hijau, dan kelompok 3 minuman sinbiotik ekstrak cincau
Dosis anjuran untuk susu fermentasi bagi manusia dengan berat badan 70 kg yaitu
sekitar 100-200 ml/hari (Riyanto, 2011), serta berdasarkan anjuran konsumsi
minuman probiotik komersial yaitu 100 ml per orang per hari. Konversi berat
badan mencit 20 g dengan berat badan manusia 70 kg adalah 0,0026 (Amalina,
2009) seperti disajikan pada Tabel 5. Berdasarkan tabel konversi, contoh
perhitungan untuk penentuan dosis minuman sinbiotik ekstrak cincau hijau pada
mencit, dosis anjuran untuk susu fermentasi bagi manusia dengan berat badan 70
kg yaitu sekitar 100-200 ml/hari, bila dikonversi ke mencit dengan berat badan 20
gram adalah sebagai berikut : 0,0026 x 100 ml aquades = 0,26 ml aquades, 0,0026
x 100 ml minuman sinbiotik ekstrak cincau hijau = 0,26 ml minuman sinbiotik
ekstrak cincau hijau. 0,0026 x 100 ml minuman sinbiotik ekstrak cincau hijau
dengan penambahan sari buah = 0,26 ml minuman sinbiotik ekstrak cincau hijau
dengan penambahan sari buah. Dosis perlakuan yang diberikan pada mencit
dikonversi sesuai berat badan mencit setiap harinya.
Uji status antioksidan hati menggunakan 27 ekor mencit, masing-masing
kelompok terdiri dari 9 ekor mencit. Aquades, minuman sinbiotik ekstrak daun
cincau hijau, dan minuman sinbiotik ekstrak cincau hijau yang dikombinasikan
sari buah dengan aktivitas tertinggi yang telah didapat berdasarkan tahap I,
diberikan secara oral dengan menggunakan spuit volume 1 ml yang ditumpulkan
sebagai alat perlakuan secara oral pada mencit sesuai dengan dosis perlakuan
selama 30 hari. Selama 30 hari perlakuan, mencit tetap diberi pakan pellet ayam
dan air minum secara ad libitum. Proses pengambilan hati mencit melalui cara
pembedahan. Sebelum proses pembedahan, diberi perlakuan anestesi
hati. Selanjutnya, hati di letakkan pada alumunium foil dan dibungkus hingga
rapat. Alumunium foil yang berisi hati dimasukkan ke dalam box ice yang telah
berisi es dengan tujuan agar hati tidak mengalami kerusakan sebelum dilakukan
pengujian MDA. Secara keseluruhan, diagram alir proses pengujian tahap kedua
secara keseluruhan disajikan pada Gambar 7.
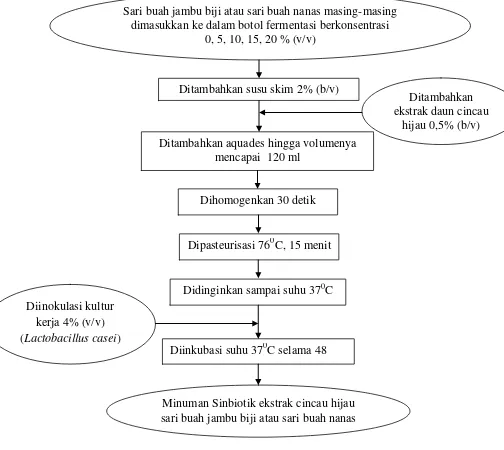
Gambar 6. Diagram alir pembuatan minuman sinbiotik ekstrak daun cincau hijau dengan kombinasi sari buah jambu biji dan sari buah nanas Sumber : Nurdin, dkk. (2007) yang telah dimodifikasi
Ditambahkan ekstrak daun cincau
hijau 0,5% (b/v) Ditambahkan aquades hingga volumenya
mencapai 120 ml
Sari buah jambu biji atau sari buah nanas masing-masing dimasukkan ke dalam botol fermentasi berkonsentrasi
0, 5, 10, 15, 20 % (v/v)
Ditambahkan susu skim 2% (b/v)
Dihomogenkan 30 detik
Diinkubasi suhu 370C selama 48 Dipasteurisasi 760C, 15 menit Didinginkan sampai suhu 370C Diinokulasi kultur
kerja 4% (v/v) (Lactobacillus casei)
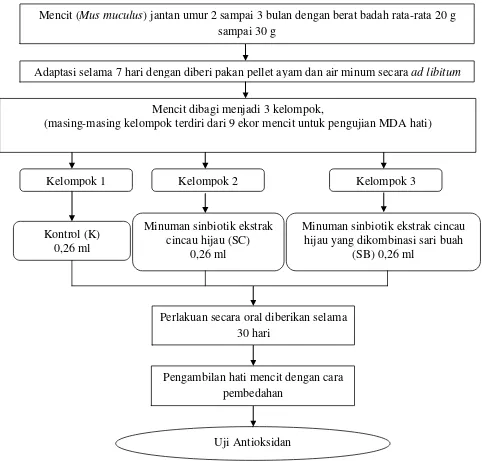
Gambar 7. Diagram alir proses pengujian tahap kedua secara keseluruhan
E. Pengamatan A. Penelitian Tahap I
1. Total Bakteri Asam Laktat (BAL)
Sebanyak 1 ml sampel ditambah dengan 9 ml larutan garam fisiologis steril. Dari
campuran tersebut didapat larutan pengenceran 10-1. Campuran kemudian dihomogenkan dan diambil 1 ml larutan dari tabung pertama dan dimasukkan ke Mencit (Mus muculus) jantan umur 2 sampai 3 bulan dengan berat badah rata-rata 20 g
sampai 30 g
Adaptasi selama 7 hari dengan diberi pakan pellet ayam dan air minum secara ad libitum
Mencit dibagi menjadi 3 kelompok,
(masing-masing kelompok terdiri dari 9 ekor mencit untuk pengujian MDA hati)
Kelompok 1 Kelompok 2 Kelompok 3
Kontrol (K) 0,26 ml
Minuman sinbiotik ekstrak cincau hijau (SC)
0,26 ml
Minuman sinbiotik ekstrak cincau hijau yang dikombinasi sari buah
(SB) 0,26 ml
Pengambilan hati mencit dengan cara pembedahan
Uji Antioksidan
dalam tabung reaksi kedua yang juga berisi 9 ml larutan garam fisiologis sehingga
diperoleh pengenceran 10-2 dan seterusnya sampai diperoleh pengenceran yang diinginkan. Dari pengenceran yang dikehendaki diambil dengan pipet 1ml sampel
lalu dimasukkan ke dalam cawan petri steril, lalu ditambahkan kira-kira 10-15
media MRS Agar steril. Cawan yang telah berisi media dan sampel ini diratakan
dengan cara menggerakkan secara vertikal membentuk angka 8 dan biarkan
sampai membeku, kemudian cawan diinkubasi dengan posisi terbalik pada suhu
37 oC selama 24 jam dan dihitung koloni yang tumbuh dengan menggunakan alat penghitung koloni (colony counter). Total koloni yang terhitung harus memenuhi
standar “International Commision Microbiology Food” (ICMF) yaitu antara 30
sampai 300 koloni per cawan petri (Fardiaz, 1989).
1
Total BAL (cfu/ml) = Jumlah koloni terhitung x Faktor Pengenceran
2. Total Asam Laktat
Pengujian total asam laktat ditentukan dengan metode AOAC (2000). Sebanyak 1
ml sampel ditambahkan 9 ml air destilat. Campurkan tersebut kemudian dititrasi
dengan larutan NaOH 0,1 N. Untuk mengamati perubahan warna menjadi merah
muda digunakan phenolphtalein sebagai indikator titik akhir titrasi.
Total asam tertitrasi ditentukan sebagai asam laktat dengan persamaan : ml NaoH x N NaOH x 90 x 0,1 Total asam laktat (% b/v) =
Volume sampel (ml)
3. Derajat Keasaman (pH)
Menurut Fardiaz, dkk. (1989), nilai pH ditentukan dengan menggunakan pH
meter. Sebelum dilakukan pengukuran, pH meter harus dikalibrasi terlebih
pengukuran terhadap larutan sampel dengan mencelupkan elektrodanya ke dalam
larutan sampel dan dibiarkan beberapa saat sampai diperoleh pembacaan yang
stabil.
4. Aktivitas Antioksidan
Absorbansi control, Larutan DPPH dengan konsentrasi 0,08 mM dalam etanol
96% v/v diambil 10 ml, kemudian diinkubasi pada suhu 370C selama 30 menit. Setelah itu diukur absorbansinya pada panjang gelombang 517 nm. Absorbansi
sampel, masing-masing sampel dicentrifuge dengan kecepatan 3500 rpm selama
15 menit. Setelah terpisah sampel cair dengan padatan diambil sampel cair
sebanyak 7,5 ml dan ditambahkan larutan DPPH 0,08 mM dalam etanol 96% v/v
sebanyak 2,5 ml. Setelah itu diinkubasi pada suhu 370C selama 30 menit, kemudian dimasukan ke dalam kuvet untuk diukur absorbansinya pada panjang
gelombang 517 nm. Nilai % Aktivitas Antioksidan diperoleh dengan rumus
(Molyneux, 2003).
(Absorbansi Kontrol – Absorbansi Sampel)
Persen Aktivitas Antioksidan = x100%
Absorbansi Kontrol
5. Uji Organoleptik
Penilaian organoleptik minuman sinbiotik cincau hijau dilakukan dengan uji
skoring terhadap warna, aroma, rasa, dan penerimaan keseluruhan (Soekarto,
1985). Sebelum dilakukan uji organoleptik, pada masing-masing minuman
sinbiotik terlebih dahulu ditambahkan larutan sukrosa 65 % dengan perbandingan
1:1. Hal ini dilakukan untuk mengurangi rasa asam yang ditimbulkan oleh
Nama panelis : ... Tanggal : ... Ulangan : ...
Dihadapan saudara disajikan sampel minuman sinbiotik cincau hijau yang diberi kode acak. Anda diminta untuk menilai kesukaan terhadap warna, rasa, dan aroma serta penerimaan keseluruhan, dengan skor dari 1 sampai 7. Jangan lupa untuk berkumur-kumur dengan air minum yang telah disajikan setelah saudara mencicipi satu sampel sebelum beralih ke sampel berikutnya.
panelis. Pada kuisioner dibuat deskripsi untuk masing-masing parameter,
kemudian deskripsi akan dihitung persentasenya. Contoh kuesioner yang
digunakan dapat dilihat pada Tabel 2.
Tabel 2. Contoh kuisioner yang digunakan dalam uji organoleptik.
Penelitian Tahap II
Analisis Malonaldehida (MDA) Hati Mencit
Analisis Malonaldehida (MDA) menggunakan metode Singh, et.al., 2002 (dalam
1 ml supernatan hati ditambah 4 ml campuran larutan dingin (HCl dingin 0,25 N
(2,23 ml HCl pekat/100ml) yang mengandung 15% TCA, 0,38% TBA 0,5 %
BHT). Campuran dipanaskan 800C selama 1 jam. Setelah dingin, campuran disentrifius 3500rpm selama 10 menit. Absorbansi supernatant diukur pada 532
V. SIMPULAN DAN SARAN
A. Simpulan
Berdasarkan hasil penelitian dapat diambil kesimpulan sebagai berikut :
1. Minuman sinbiotik yang memiliki karakteristik terbaik yaitu dengan
penambahan jenis sari buah jambu biji dengan penambahan konsentrasi sari
buah jambu biji 15%.
2. Minuman sinbiotik yang ditambahkan sari buah jambu biji dengan konsentrasi
15%, menghasilkan total bakteri asam laktat sebesar sebesar 11,22 log
koloni/ml, nilai pH sebesar 3, 65, total asam laktat sebesar 0,61%, aktivitas
antioksidan sebesar 77,11%, warna dengan skor 3,83 (suka), aroma dengan
skor 3,69 (suka), rasa dengan skor 3,72 (suka), dan penerimaan keseluruhan
dengan skor 3,74 (suka).
3. Kadar MDA hati mencit kelompok yang diberi perlakuan minuman sinbiotik
cincau hijau dengan penambahan sari buah jambu biji tidak berbeda nyata
dengan kelompok perlakuan minuman sinbiotik cincau hijau dan kontrol
aquades.
B. Saran
Perlu dilakukan penelitian lebih lanjut mengenai waktu perlakuan mencit
DAFTAR PUSTAKA
Amalina, N. 2009. Uji Toksisitas Akut Ekstrak Valerian (Valeriana officinalis) Terhadap Hepar Mencit BALB/C. Laporan Akhir Penelitian Karya Tulis Ilmiah. Universitas Diponegoro Semarang. 64 halaman.
Anggraini, D. 2006. Pengaruh Konsentrasi Asam Sitrat Terhadap Total Pektin Dan Aktivitas Antioksidan Serat Pangan Dari Cincau Pohon (Premna oblongifolia Merr). (Skripsi). Universitas Lampung. 54 hlm.
AOAC. 2000. Official methods of analysis of the association of official analytical chemist, chapter 28. Washington DC. Association of Official Chemist.
Aprikian, O., V. Duclos, S. Guyot, C. Besson, C. Manach, A. Bernalier, C. Morand, C. Remesy, and C. Demigne. 2003. Apple pectin and a polyphenol-rich apple concentrate are more effective together than separately on cecal fermentation and plasma lipids in rats.Jurnal Nutrisi. 133:1860-1865.
Asiedu, M.S, W. Wardy, F.K. Saalia, A.S. Budu and S.S Dedeh. 2009. A comparison of some physical, chemical and sensory attributes of three pineapple (Ananas cosmosus) varieties grown in ghana.African Journal of Science 3(1) : 022-025.
Axelsson, L.T. 1993. Lactic acid bacteria, classification and physiology. In Salminen, S and A.V. Wright. Lactic acid bacteria. Marcel Dekker, Inc. New York.
Badan Standarisasi Nasional. 2009. Minuman susu fermentasi berperisa. Badan Standardisasi Nasional. Jakarta.
Bartlett, J.G. and B.F. Polk. 1984. Bacterial flora of the vagina: quantitative study. 6:S67-72.
Barus, P. 2009. Pemanfaatan Bahan Pengawet dan Antioksidan Alami pada Industri Bahan Makanan. (Skripsi). Universitas Sumatra Utara. Medan.
Buck, D.F. 1991. Antioxidants. Didalam: J. Smith, editor. Food additive user’s handbook. UK: Blackie Academic & Profesional, Glasgow.
Cahyono, R. 1996. Produksi dan Aktivitas Antibakteri Minuman Sehat Kaya Vitamin B12 Hasil Fermentasi Laktat Dari Sari Wortel. (Skripsi). Fateta.
IPB. Bogor.
Chalid, S.Y. 2002. Pengaruh Ekstrak Daun Cincau Hijau (Cyclea barbata L. Miers dan Premna oblongifolia Merr) Terhadap Aktivitas Enzim Antioksidan Dan Pertumbuhan Tumor Kelenjar Susu Mencit C3H Tranplantable. (Tesis). IPB.
Collins, M.D. and G.R.Gibson.1999. Probiotics, prebiotics, and synbiotics: approaches for modulating the microbial ecology of the cut. Jurnal Nutrisi. 69(5):1052S-1057S.
Dalimartha, S. dan M. Soedibyo1999. Awet muda dengan tumbuhan obat dan diet supleme. Trubus Agriwidya, Jakarta.
Djam’an, Q. 2008. Pengaruh Air Perasan Daun Cincau Cyclea barbata Miers
(cincau hijau) Terhadap Konsentrasi HCl Lambung Dan Gambaran Histopatologik Lambung Tikus Galur Wistar Yang Diinduksi Acetylsalicylic Acid. (Tesis). Magister Ilmu Biomedik. Universitas Dipenegoro. Semarang.
Dongowski, G., Lorenz, A., and Proll. 2002. The degree of methylation influence the degradation of pectin in the intestinal tract of rats and in vitro. Jurnal Nutrisi. 132:1935-1944.
Endugrol, O., and F. Erbilir. 2006. Isolation and characterization of Lactobacillus bulgaricus and Lactobacillus casei from various foods. Jurnal Bioteknologi. 30:39-44.
Fardiaz, S. 1989. Penuntun Praktikum Mikrobiologi Pangan. Fakultas teknologi Pertanian. Institut Pertanian Bogor.
Fuller, R. 1989. Probiotic in man and animals. Journal Bacteriol. 66:365-378.
Gallaher, D. 2000. Dietary fiber and its physiological effect in essential of functional food. Schmidl, MK. And Labuza, TP (Eds). An Aspen Publisher. Maryland.
Gulo, N. 1995. Peningkatan Kandungan Vitamin B1 Dan B2 Serta Aktivitas
Antitrombopik Susu Kacang Tanah Merah dan Tolo Fermentasi Oleh Lactobacillus casei subsp. Rhamnosus. (Tesis). IPB. Bogor.
Herliani, L. 2010. 33 macam buah-buahan untuk kesehatan. Alfabeta. Bandung. 184 hlm.
Kandler, O. and N. Weiss. 1986. Bergey’s manual of systematic bacteriology. 2:1208-1234.
Kullisaar, T., M. Zilmer, M. Mikelsaar, T. Vihelmn, H. Annuk, C. Kamane and A. Klik . 2001. Two antioxidant lactobacilli strains ad promising probiotics. Food Microbiology Journal (72) ; 215-224
Kurniasih, E. 1997. Kajian Pembuatan Minuman Kesehatan Belimbing Manis Dan Pengaruhnya Terhadap Penurunan Kadar Kolestrol, Trigliserida Dan HDL Serum Darah Dan Hati Tikus Sprague dawle. (Skripsi). IPB.
Lee, Y.K. and S.F. Wong. Stability of lactic acid bacteria in fermented milk. 1993. In Salminen, S and A.V. Wright. Lactic acid bacteria. Marcel Dekker, Inc. New York.
Lingga, L. 2012. The healing power of antioksidan. PT. Gramedia. Jakarta. 400hlm.
Molyneux, P. 2003. The use of the stable free radical diphenylpicrylhydrazyl (DPPH) for estimating antioxidant Activity. Journal Science Technology. 26(2) : 211-219.
Murini, T., Fiki F., Marda AS., Siti M., dan Totok U. 2009. Pengaruh Juh Buah Jambu Biji Merah (Psidium guajava L.) Terhadap Profil Lipid Darah dan Kejadian Aterosklerosis pada Tikus Putih yang Diberi Diet Tinggi Lemak. http://www.jambubiji.htm. Diakses tanggal 14 Maret 2012.
Ngatidjan. 2009. Metode Laboratorium Dalam Toksikologi. Fakultas Kedokteran Universitas Gajah Mada. Yogyakarta. 240hlm.
Nurdin, S.U., A.S.Zuidar, dan R. Krisnawati. 2004. Pengaruh konsentrasi asam sitrat terhadap rendemen dan sifat serat pangan dari daun cincau pohon (Premna oblongifolia Merr). Prosiding Seminar Nasional dan Kongres PATPI. Jakarta, 17-18 Desember 2004.
Nurdin, S.U. 2005. Green cincau leaves (Premna oblongifolia Merr) as potential sources of pectin-rich plant extract.Artocarpus 5 (1): 24-27.
Nurdin, S.U., S. dan F. Nurainy. 2007. Produksi Minuman Sinbiotik Dari Ekstrak Cincau Hijau (Premna oblongifolia Merr.) Sebagai Minuman Fungsional. Laporan Penelitian Dosen Muda. Universitas Lampung. Bandar Lampung. 52 hlm.
Oberman, H. and Z. Libudzisz. 1998. Fermented milks. In Wood, B.JB. Microbiology of fermented foods, Secon Edition Vol. 1. Blackie Academic and Professional.
Prangdimurti, E., Muchtadi, D., M., Astawan, dan F.R. Zakaria. 2006. Aktivitas antioksidan ekstrak daun suji (Pleomele angustifolia N.E. Brown). Jurnal Teknologi dan Industri Pangan Volume XVII No. 2 Tahun 2006. 9 halaman.
Pribadi, I. 2009. Uji Aktivitas Penangkapan Radikal Buah Psidium guajava L. Dengan Metode DPPH (1,1-Difenil-2-Pikril Hidrazil) Serta penetapan Kadar Fenolik dan Flavanoid Totalnya. (Skripsi). Fakultas Farmasi. Universitas Muhammadiyah Surakarta.
Priest, F.G and I. Campbell. 1999. Brewing microbiology, second edition. Aspen Publishers, Inc. Gaithersburg. Maryland.
Pujakesuma, E. D. 2005. Pengaruh Penambahan Glukosa dan Skim Terhadap Karakteristik Sari Buah Jeruk Yang Difermentasi oleh Lactobacillus casei. (Skripsi). Unila. Bandar Lampung.
Putri, D. R. 2009. Efek Antioksidan Fraksi Larut Etil Asetat Ekstrak Etanol Daun Jambu Biji (Psidium guajava L.) Pada Kelinci yang Dibebani Glukosa. (Skripsi). Universitas Muhammadiyah Surakarta. Surakarta.
Rahman, A. S. Fardiaz, WP. Rahayu, Suliantari dan CC. Nurwitri. 1992. Teknologi fermentasi susu. Departemen Pendidikan dan Kebudayaan Direktorat Jendral Pendidikan Tinggi Pusat Antar Universitas Pangan dan Gizi Institut Pertanian Bogor.
Rachmawati, AK. 2009. Ekstrak dan Karakterisasi Pektin Cincau Hijau (Premna oblongifolia Merr.) untuk Pembuatan Edible Film. (Skripsi). Fakultas Pertanian. Universitas Sebelas Maret.
Richard, K., dan Robinson. 2000. Encyclopedia of food microbiology academic press. California. USA.
Rizal, S., Marniza dan S.U.Nurdin. 2006. Optimasi Proses Pengolahan Minuman Probiotik Dari Kulit Nenas Dan Pengaruhnya Terhadap Mikroflora Usus Besar Tikus Percobaan. Laporan Akhir Penelitian. TPSDP Unila. Bandar Lampung.
Rohman, A., dan Sugeng R. 2005. Aktivitas Antioksidan Ekstrak Buah Mengkudu (Morinda citrifolia, L). 25(3):131-13.
Satria, H.N. 2005. Pembentukan asam organik oleh isolat bakteri asam laktat pada media ekstrak daging buah durian (Durio zibethinus Murr.). Jurnal Bioscientiae 2(1).
Saura-Calixto, F.D. 2003. Antioxidant dietary fibre. EJEAFChe. 2(1):223-226.
Setioningsih, E., R. Setyaningsih, dan A. Susilowati. 2004. Pembuatan minuman probiotik dari susu kedelai dengan inokulum L.casei, L.plantarum dan L. acidopillus. Jurnal Biotechnology 1(1) :1-6.
Setyaningsih, I. 1992. Pengaruh Jenis Kultur Lactobacillus casei, Penambahan Susu Skim terhadap Mutu Yakult Kedelai. (Skripsi). Fakultas Teknologi Pertanian. IPB. Bogor. 45 hlm.
Soekarto, S.T. 1985. Penilaian Organoleptik Untuk Industri Pangan dan Hasil Pertanian. Bharata Karya Aksara. Jakarta. 121 hlm.
Stamer, J.R. 1979. Lactic Acid Bakteria. Food Mikrobiologi Publish Health Spoilage Aspect. The AVI Publishing INC. Westport. Connecticut.
Suhartono, E., Fujiati, I. Aflanie. (2002). Oxygen Toxicity By Radiation And Effect of Glutamicpiruvat Transamine (GPT) Activity Rat Plasma After Vitamine C Treatmen, Diajukan pada Internatinal seminar on Environmental Chemistry and Toxicology, Yogyakarta.
Sunarni, T. 2005. Aktivitas antioksidan penangkap radikal bebas beberapa kecambah dari biji tanaman familia papilionaceae. Jurnal Farmasi Indonesia 2 (2) : 53-61.
Sutomo, B. 2006. Manfaat cincau. Artikel.
http://budiboga.blogspot.com/2006/ 10/manfaat-cincau.html. Diakses tanggal 14 Maret 2012.
Wahyudi, A. dan S. Samsundari. 2008. Bugar Dengan Susu Fermentasi Rahasia Hidup Sehat Panjang Umur. Universitas Muhammadiyah Malang Press, Malang.
Winarsi, H. 2007. Antioksidan Alami dan Radikal Bebas Potensi dan Aplikasi Dalam Kesehatan. Kanisius. Yogyakarta. 281 hlm.
Winarti, S. 2010. Makanan Fungsional. Graha Ilmu. Yogyakarta. 27 hlm.
Yusmarini dan R. Efendi. 2004. Evaluasi mutu soyghurt yang dibuat dengan penambahan beberapa jenis gula. Jurnal Natur Indonesia 6(2):104-110.
Zakaria, F.R. 2002. Kajian lanjut aktivitas fungsional, toksisitas dan bioavaibilitas komponen bioaktif cincau hijau (Cyclea barbata L. Miers dan Premna oblongifolia Merr).Laporan Hibah Bersaing Perguruan Tinggi 2001-2002 IPB. Bogor.