ADSORBEN LOGAM BERAT DARI KOPOLIMERISASI
CANGKOK BINER ASAM AKRILAT DAN AKRILAMIDA
PADA ONGGOK
AGY WIRABUDI PRANATA
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM INSTITUT PERTANIAN BOGOR
PERNYATAAN MENGENAI SKRIPSI DAN
SUMBER INFORMASI SERTA PELIMPAHAN HAK CIPTA*
Dengan ini saya menyatakan bahwa skripsi berjudul Adsorben Logam Berat dari Kopolimerisasi Cangkok Biner Asam Akrilat dan Akrilamida pada Onggok adalah benar karya saya dengan arahan dari komisi pembimbing dan belum diajukan dalam bentuk apa pun kepada perguruan tinggi manapun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir skripsi ini.
Dengan ini saya melimpahkan hak cipta dari karya tulis saya kepada Institut Pertanian Bogor.
Bogor, Januari 2014
Agy Wirabudi Panata
ABSTRAK
AGY WIRABUDI PRANATA. Adsorben Logam Berat dari Kopolimerisasi Cangkok Biner Asam Akrilat dan Akrilamida pada Onggok. Dibimbing oleh MOHAMMAD KHOTIB dan MUHAMMAD ANWAR NUR.
Dalam rangka meningkatkan sifat polimer superabsorben (PSA) yang disintesis dari onggok (hasil samping pengolahan tapioka), telah dilakukan pencangkokan campuran monomer biner asam akrilat dan akrilamida ke onggok dalam medium berair menggunakan amonium persulfat sebagai inisiator. Faktor yang dipelajari dari pembuatan superabsorben ini, di antaranya adalah urutan pemuatan monomer, penambahan penautsilang, dan kapasitas penyerapannya. Dilakukan juga analisis dengan spektroskopi inframerah. Hasil penelitian menunjukkan bahwa PSA A1, yang dibuat melalui pencangkokan asam akrilat kemudian akrilamida tanpa penautsilang memilki daya serap air paling tinggi sebesar 370 g/g. PSA A1 efektif menyerap air pada pH 9 dan kemampuan serapnya dipengaruhi oleh kadar salinitas medium. PSA tersebut juga berpotensi sebagai adsorben ion logam Cu2+.
Kata kunci: adsorpsi, akrilamida, asam akrilat, kopolimerisasi cangkok biner, onggok, polimer superabsorben
ABSTRACT
AGY WIRABUDI PRANATA. Heavy Metal Adsorbent from Binary Graft Copolymerization Acrylic Acid and Acrylamide on Onggok. Supervised by MOHAMMAD KHOTIB and MUHAMMAD ANWAR NUR.
To improve properties of superabsorbent polymer (PSA) synthesized from onggok (cassava residual pulp), we have grafted binary monomer mixture of acrylic acid and acrylamide onto onggok in aqueous medium using APS as initiator. Some factors of the synthesis studied were loading sequence of monomer, addition of cross-linker, and absorption capacity. Testing was also performed by infrared spectroscopy. The PSA A1, which is created by grafting of acrylic acid and acrylamide without cross-linker, showed the highest water absorption of 370 g/g. The PSA A1 effectively absorbed water at pH 9 and the absorption capabilities were affected by levels of salinity of the medium. The PSA also potential as Cu2+ metal ion adsorbent.
Skripsi
sebagai salah satu syarat untuk memperoleh gelar Sarjana Kimia
pada
Departemen Kimia
ADSORBEN LOGAM BERAT DARI KOPOLIMERISASI
CANGKOK BINER ASAM AKRILAT DAN AKRILAMIDA
PADA ONGGOK
AGY WIRABUDI PRANATA
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM INSTITUT PERTANIAN BOGOR
Judul Skripsi : Adsorben Logam Berat dari Kopolimerisasi Cangkok Biner Asam Akrilat dan Akrilamida pada Onggok
Nama : Agy Wirabudi Pranata NIM : G44090106
Disetujui oleh
Mohammad Khotib, MSi Pembimbing I
Prof (em) Dr Ir M Anwar Nur, MSc Pembimbing II
Diketahui oleh
Prof Dr Dra Purwatiningsih Sugita, MS Ketua Departemen
PRAKATA
Puji dan syukur penulis panjatkan kepada Allah subhanahu wa ta’ala atas segala karunia-Nya sehingga karya ilmiah ini berhasil diselesaikan. Tema yang dipilih dalam penelitian yang dilaksanakan sejak bulan Mei 2013 ini ialah sintesis superabsorben berbasis limbah tapioka, dengan judul Adsorben Logam Berat dari Kopolimerisasi Cangkok Biner Asam Akrilat dan Akrilamida pada Onggok.
Terima kasih penulis ucapkan kepada Bapak Mohammad Khotib, MSi dan Bapak Prof (em) Dr Ir M Anwar Nur, MSc selaku pembimbing, serta Bapak Muhammad Farid, MSi yang telah banyak memberi saran. Penulis juga mengucapkan terima kasih kepada Labolatorium Terpadu IPB yang telah memfasilitasi dan membiayai kegiatan penelitian yang dilakukan penulis. Di samping itu, penghargaan penulis sampaikan kepada kak Yono, Kak Samsul, Kak Dail, Kak Baim, Kak Indah, Ilham, Pebri, Fahmi, Denar, Cris, Tari, Shinta, Tati, Mia, Rahma, Noni, Rahmi, dan Seluruh Staff di Labolatorium Terpadu IPB, yang telah membantu memberikan masukan selama penelitian dilaksanakan. Ungkapan terima kasih juga disampaikan kepada ayah, ibu, serta seluruh keluarga, atas segala doa dan kasih sayangnya. Untuk yang terakhir penulis juga menyampaikan terimakasih kepada saudara-saudara di Asrama Masjid Al Hurriyyah, Birena, SDM, dan LDK Al Hurriyyah, Asrama Indramayu, KIMIA 46 yang senantiasa mendukung penulis untuk menyelesaikan tugas akhirnya.
Semoga karya ilmiah ini bermanfaat.
Bogor, Januari 2014
DAFTAR ISI
DAFTAR TABEL vi
DAFTAR GAMBAR vi
DAFTAR LAMPIRAN vi
PENDAHULUAN 1
Latar Belakang 1
METODE 2
Bahan 2
Alat 2
Pembuatan Superabsorben Onggok 2
Uji Kinerja Superabsorben 4
HASIL DAN PEMBAHASAN 6
Kopolimerisasi Cangkok Biner 6
Analisis Gugus Fungsi 7
Kadar Nitrogen, Nisbah Pencangkokan, dan Efisiensi Pencangkokan PSA 7
Daya Serap Air PSA 8
Daya Jerap PSA pada Ion Logam Cu2+, Pb2+, dan Cr6+ 9
Daya Serap Air PSA dalam Larutan NaCl 11
Daya Serap Air PSA dalam Larutan Berbagai Nilai pH 12
Adsorpsi Isotermal PSA 12
SIMPULAN DAN SARAN 13
Simpulan 13
Saran 14
DAFTAR PUSTAKA 14
LAMPIRAN 16
RIWAYAT HIDUP 30
DAFTAR TABEL
1 Desain percobaan pembuatan kopolimersisasi cangkok biner asam
akrilat-akrilamida 3
2 Kadar Nitrogen, nisbah pencangkokan, dan efisiensi pencangkokan
PSA 8
3 Adsorpsi PSA A1 pada ion logam Cu2+, Pb2+, dan Cr6+ selama 24
DAFTAR GAMBAR
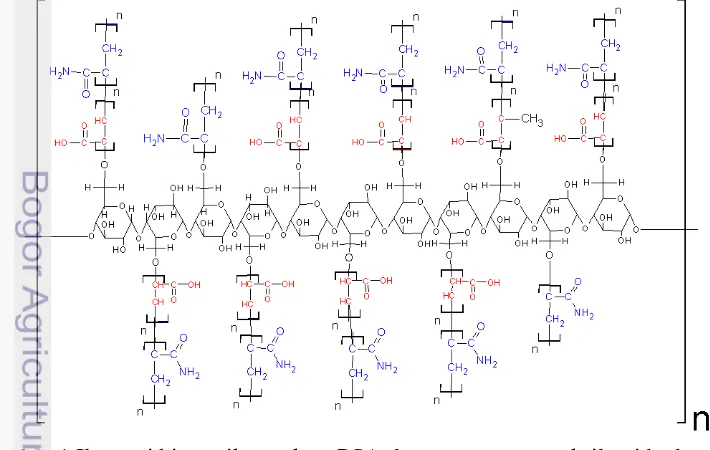
1 Ilustrasi hipotetik struktur PSA dengan monomer akrilamida dan
asam akrilat tanpa penautsilang (PSA A1) 6
2 Spektrum gabungan onggok murni, PSA M1, dan M2 7 3 Daya serap air superabsorben dari berbagai PSA. 9 4 Ilustrasi model penjerapan logam pada PSA (Wang et al. 2011) 10 5 Grafik daya adsorpsi ion logam Cu2+, Pb2+, dan Cr6+ oleh PSA
selama 30 menit 10
6 Daya serap air PSA dalam larutan NaCl 11
7 Grafik daya serap superabsorben pada larutan di berbagai nila pH 12 8 Grafik isoterm Freundlich ion logam Cu2+, Pb2+, dan Cr6+ 13
DAFTAR LAMPIRAN
1 Diagram alir penelitian 16
2 Radas kopolimerisasi engcangkokan dan penautsilangan onggok
dengan asam akrilat dana akrilamida 17
3 Mekanisme sintesis PSA A1 18
4 Spektrum FTIR onggok murni, PSA A1, dan A2 23 5 Spektrum FTIR onggok murni, PSA A3 dan A4 23 6 Spektrum FTIR onggok murni, PSA M3 dan M4 24
7 Perhitungan kadar N secara teoritis 25
8 Perhitungan kadar N dengan metode kjeldahl 25 9 Daya serap air dari berbagai macam jenis PSA 26 10 Penjerapan ion logam Cu2+, Pb2+, dan Cr6+ oleh berbagai jenis PSA
(30 menit) 27
11 Penjerapan ion logam Cu2+, Pb2+, dan Cr6+ oleh berbagai jenis PSA
24 jam) 28
12 Penjerapan logam Cu2+ dengan berbagai macam nilai konsentrasi
oleh PSA A1 28
13 Penjerapan logam Pb2+ dengan berbagai macam nilai konsentrasi
oleh PSA A1 29
14 Penjerapan logam Cr6+ dengan berbagai macam nilai konsentrasi
oleh PSA A1 29
15 Penjerapan logam Pb2+, Cu2+, dan Cr6+ oleh PSA untuk isoterm
adsorpsi 29
1
PENDAHULUAN
Latar Belakang
Ketela pohon (Manihot esculenta) merupakan tanaman pangan yang termasuk famili euphorbiaeae dan memilki nama lain ubi kayu atau singkong. Ketela pohon mengandung pati sebanyak 64-75%, sehingga banyak dimanfaatkan sebagai sumber karbohidat selain beras dan jagung (Lidiasari et al. 2006). Produksi ketela pohon di Indonesia pada tahun 2011 mencapai 23.6 juta ton (BPS 2013). Dalam pemanfaatannya, ketela pohon biasanya diolah dengan cara dimasak langsung, difermentasi, dikeringkan, dan dibuat menjadi tepung tapioka. Pada industri pembuatan tepung tapioka, dihasilkan produk samping dalam bentuk padat (onggok) dalam jumlah besar. Dalam pengolahan 1 ton ketela pohon dapat dihasilkan 250 kg tepung tapioka dan 114 kg onggok (Virlandia 2005). Onggok biasanya dimanfaatkan sebagai pakan ternak atau sebagai bahan material obat nyamuk bakar. Oleh karena itu perlu dibuat upaya untuk membuat onggok menjadi sesuatu yang lebih bermanfaat dan meningkat nilai jualnya seperti polimer superabsorben (PSA).
PSA adalah polimer tautsilang hidrofilik yang dapat mengembang, menyerap dan mempertahankan air dalam jumlah besar (Buchholz dan Graham 1997). Polimer superabsorben secara luas digunakan dalam banyak aplikasi, seperti popok sekali pakai, bahan pembalut wanita (Mehr dan Kabiri 2008), dan media untuk pertanian dan hortikultura (Liang et al. 2009). Selain itu PSA juga dimanfaatkan sebagai senyawa pembawa obat (Gils et al. 2009), dan pengolahan limbah yang mengandung logam berat (Dhodapkar et al. 2009). Pembuatan superabsorben dari karbohidrat maupun turunannya mempunyai keunggulan seperti ramah lingkungan (mudah terurai secara alami), dapat diperbaharui, dan tidak beracun (Sadeghi and Hosseinzadeh 2008).
2
METODE
Bahan
Bahan-bahan yang digunakan adalah limbah padat tapioka (onggok) yang didapatkan dari industri pengolahan tepung tapioka di Bogor, Indonesia. N,N’ -metilena-bis-akrilamida (MBA) (PT Sigma Aldrich, Indonesia). Gas N2 (PT BOC, Indonesia). Amonium persulfat (APS), asam akrilat, dan akrilamida (Merck, Jerman), metanol, dan etanol (PT. Smart Lab, Indonesia).
Alat
Alat-alat yang digunakan adalah radas reaktor sintesis, bilah pengaduk, alat-alat gelas, motor pengaduk, alat-alat penghalus/penggiling, alat-alat kocok, hotplate, FTIR Shimadzu IR prestige-21, Atomic Absorption Spectrophotometer (AAS) Shimadzu AA 6300, dan komputer beserta perangkat lunaknya (CurveExpert 1.4).
Pembuatan Superabsorben Onggok
Penelitian pembuatan PSA cangkok biner dari onggok dilakukan dalam tiga tahap, yaitu perlakuan pendahuluan, pembuatan PSA dengan kopolimerisasi cangkok biner, dan pencirian PSA cangkok biner yang telah dibuat. Diagram alir penelitian dapat dilihat pada Lampiran 1.
Perlakuan Pendahuluan
Onggok tapioka dicuci dengan air keran sampai filtrat hasil pencucian jernih kemudian dijemur di bawah sinar matahari kurang lebih selama 2 hari sampai onggok kering. Onggok tersebut lalu diayak dengan ayakan berukuran 100 mesh.
Pembuatan PSA dengan Kopolimerisasi Cangkok Biner (Modifikasi Mas’ud
et al. 2013)
3 Tabel 1 Desain percobaan pembuatan kopolimersisasi cangkok biner asam
akrilat-akrilamida
Kode Komposisi Cangkok Tahap 1 Komposisi Cangkok Tahap 2
A1 asam akrilata akrilamida
A2 asam akrilata akrilamida dan penautsilang
A3 asam akrilata dan penautsilang akrilamida
A4 asam akrilata dan penautsilang akrilamida dan penautsilang
M1 akrilamida asam akrilata
M2 akrilamida asam akrilata dan penautsilang M3 akrilamida dan penautsilang asam akrilata
M4 akrilamida dan penautsilang asam akrilata dan penautsilang
a
Asam akrilat yang digunakan, dinetralisasi dahulu dengan NaOH sampai ternetralkan 80%.
Presipitasi Gel (Modifikasi Mas’ud et al. 2013)
Produk hasil sintesis (dalam bentuk gel) ditambahkan dengan 200 mL metanol dan diaduk selama 30 menit dengan kecepatan pengadukan 200 rpm. Setelah itu, Produk ditambahkan 150 mL etanol dan diaduk dengan kecepatan 200 rpm selama 5 menit, lalu didiamkan selama 30 menit. Gel dan cairan alkohol dipisahkan. Selanjutnya, gel dipanaskan dengan 200 mL aseton pada suhu 70 °C selama 1 jam menggunakan metode refluks. Gel kemudian dikeringkan dalam oven pada suhu 60 °C hingga mencapai bobot konstan kemudian dihaluskan. Produk yang dihasilkan dinamakan polimer superabsorben (PSA).
Analisis Gugus Fungsi dengan FTIR
Sebanyak 0.5 g PSA direndam dalam 50 mL akuades kemudian didiamkan selama 24 jam. Campuran kemudian dibuat lapisan tipis dengan cara mengeringkan PSA yang telah terbentuk di atas kertas tahan air yang berbentuk persegi dengan bantuan oven bersuhu 60 °C. lapisan tipis tersebut dianalisis dengan spektrometer FTIR Shimadzu dengan resolusi 8 cm-1 dengan metode transmisi. Pada pembacaan spektrum gugus fungsi onggok murni, sebanyak 100 mg KBr dan 10 mg PSA dicampur hingga homogen. Campuran dibuat pelet lalu ditempatkan pada wadah sampel. Pemayaran dilakukan pada kisaran bilangan gelombang 400-4000 cm-1.
Nisbah Pencangkokan dan Efisensi Pencangkokan Akrilamida (Hashem et al.
2005; Mostafa et al. 2007)
Nisbah pencangkokan akrilamida (NP) dan efisiensi pencangkokan (EP) dapat diketahui dengan menentukan kadar N dari PSA yang dihasilkan. Sebanyak 0.1 g PSA ditimbang ke dalam labu bulat. Setelah itu, PSA ditambahkan 2 sudip selenium, 10 mL H2SO4 pekat, dan didestruksi dengan proses pemanasan dengan api sampai berwarna hijau bening. Hasil destruksi dimasukan ke dalam labu Kjeldahl 2 mL. Labu bulat dibilas dengan 150 mL akuades dan diikuti dengan penambahan 50 mL NaOH 40% ke dalam labu Kjeldahl tersebut. Kadar N yang diperoleh kemudian dimasukan kedalam rumus berikut:
[N
a la a n t n ]
4 24 jam. Setelah 24 jam, PSA yang telah maksimal menyerap air disaring dengan penyaring 100 mesh hingga tidak ada air yang menetes lagi. Kapasitas daya serap dihitung dengan menggunakan persamaan: ditambahkan dan didiamkan pada suhu ruang selama 24 jam. Setelah 24 jam, PSA yang telah maksimal menyerap air disaring dengan penyaring 100 mesh dan ditiriskan selama 15 menit. Kapasitas daya serap dihitung dengan menggunakan persamaan (3).
Uji Daya Serap dalam Larutan NaCl (Mas’ud et al. 2013)
Sebanyak 0.1 g PSA dimasukan ke dalam gelas piala kemudian direndam ke dalam 200 mL larutan NaCl dengan konsentrasi yang berbeda-beda (0.04, 0.08, 0.12, 0.16, 0.20, 0.50, dan 1.00 M) selama 24 jam. Kemudian PSA yang telah mengembang disaring dengan saringan 100 mesh dan ditiriskan selama 15 menit. Berat dari PSA yang mengembang (W1) dihitung dan kapasitas daya serapnya di hitung dengan persamaan (3).
Uji Daya Jerap Logam (Ekebafe et al. 2012)
5 CuSO4.5H2O; dan 1.4144 g K2Cr2O4 masing-masing dalam 1000 ml air deionisasi dengan pH 6-6.5. Perubahan konsentrasi Pb2+, Cr6+, dan Cu2+ karena penjerapan ditentukan dengan AAS. Dipisahkan zat penjerap dari ion logam yang tidak terjerap oleh PSA melalui penyaringan dengan kertas saring dalam corong. Konsentrasi ion logam dalam larutan tersebut ditentukan dengan menggunakan AAS.
- ………(4)
Keterangan:
Z = konsentrasi ion logam yang di jerap Y = konsentrasi ion logam saat awal
X = konsentrasi logam yang tidak terjerap (ppm)
Dengan metode yang sama namun dengan waktu perendaman yang lebih lama (24 jam), dilakukan pula uji daya jerap logam oleh satu PSA yang telah dipilih. Selain itu, model penjerapan logam oleh PSA ditentukan dengan menggunakan model isoterm Freundlich dan isoterm Langmuir. Data penjerapan yang dimasukan ke dalam model isoterm tersebut didapatkan dengan metode yang telah disebutkan sebelumnya (penjerapan logam dengan waktu perendaman 30 menit), namun dengan modifikasi variasi konsentrasi. Variasi konsentrasi yang digunakan adalah 15, 30, 45, 60, dan 75 ppm. Penentuan nilai parameter adsorpsi isoterm Freundlich didapatkan dari persamaan berikut:
a
b………….………
..(5)ln
lna
bln
………….…….(6)Dengan q merupakan bobot zat yang terjerap per unit bobot zat penjerap (mg/g), C merupakan konsentrasi logam yang terjerap (mg/dm3), a dan b
merupakan konstanta penjerapan dari sistem. Penantuan kesesuaian sistem adsorpsi dengan sistem adsorpsi isoterm Langmuir sesuai dengan persamaan:
……….……(7)
6
HASIL DAN PEMBAHASAN
Kopolimerisasi cangkok biner
Sintesis kopolimer cangkok biner onggok dilakukan dengan monomer akrilamida dan asam akrilat. Tahap pertama dari sintesis senyawa PSA adalah onggok dibersihkan dengan cara dicuci dengan air bersih sebelum direaksikan untuk menghilangkan pengotor, lalu dihaluskan hingga berukuran ±100 mesh agar meningkatkan luas permukaan onggok sehingga reaksi yang terjadi lebih sempurna. Inisiator dan penaut silang yang digunakan adalah APS dan MBA. Selama berlangsungnya pencangkokan, gas nitrogen dialirkan untuk mengusir oksigen yang dapat mengakibatkan terbentuknya radikal peroksida. Pembentukan senyawa peroksida perlu dihindarkan karena senyawa tersebut dapat menghambat reaksi kopolimerisasi akibat dari pembentukan homopolimer (Kurniadi 2010).
Proses pencangkokan dilakukan dengan membentuk radikal pada onggok melalui bantuan inisiator. Pada tahap awal, APS akan bereaksi dengan air membentuk radikal ·OH yang akan bereaksi membentuk radikal pada tulang punggung polimer tersebut. Tahap tersebut dikenal dengan istilah tahap inisiasi. Mekanisme lain dari proses inisiasi yang terjadi adalah reaksi langsung APS dengan gugus OH dari glukosa di posisi rantai C-6. Tahap selanjutnya adalah tahap propagasi. Pada tahap propagasi terjadi proses pencangkokan monomer pada tulang punggung polimer dari onggok. Mekanisme tersebut dimulai dengan penyerangan oleh radikal yang berasal dari onggok pada ikatan karbon rangkap pada monomer yang tersedia. Proses propagasi akan terus berlanjut hingga struktur polimer membesar. Mekanisme sintesis PSA berakhir dengan terjadinya tahap terminasi (Lampiran 3). Gambar 1 menunjukan ilustrasi hipotetik struktur PSA yang telah disintesis.
7 Analisis Gugus Fungsi
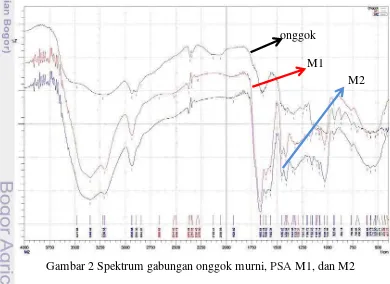
Indikasi keberhasilan proses sintesis PSA dapat diamati melalui pita serapan gugus fungsi dalam spektrum IR. Pada Gambar 2, Lampiran 4, 5, dan 6 terlihat perbedaan puncak serapan dari sampel onggok yang belum tergrafting dan onggok yang telah tergrafting. Gambar 2 memperlihatkan pada pita M1 dan M2 terdapat serapan pada bilangan gelombang 3209, 1661, dan 1616 cm-1 yang mengindikasikan adanya vibrasi ulur dari N-H, vibrasi ulur C=O, dan vibrasi tekuk dari N-H dari gugus amida. selain itu, adanya serapan pada panjang gelombang 1450 cm-1 yang berasal dari vibrasi ulur C-N memperkuat indikasi keberadaan gugus amida yang telah tergrafting pada onggok tersebut. Indikasi keberhasilan proses grafting asam akrilat, dibuktikan dengan adanya serapan tajam yang terlihat pada bilangan gelombang 1406 cm-1 yang menunjukan adanya vibrasi ulur C=O simetrik akrilat yang telah ditambahkan. Serapan lebar pada bilangan gelombang 3348 cm-1 dan 3477.66 cm-1 menunjukan adanya vibrasi ulur
-OH yang berasal dari gugus hidroksil pada pati maupun dari gugus hidroksil pada COOH yang belum terionisasi (Kitkamjornworng et al. 2000).
Selain itu, pada bilangan gelombang 1080 dan 1026 cm-1 terdapat serapan yang cukup tajam dan merupakan indikasi dari adanya vibrasi ulur C-O-C yang berasal dari ikatan glikosida pada pati. Dari keseluruhan spektrum yang terbaca, diketahui bahwa perbedaan urutan penambahan monomer tidak menghasilkan polimer yang diperkirakan berbeda gugus fungsi penyusunnya.
Gambar 2 Spektrum gabungan onggok murni, PSA M1, dan M2
Kadar Nitrogen, Nisbah Pencangkokan, dan Efisiensi Pencangkokan PSA
Kandungan nitrogen pada PSA digunakan untuk menentukan NP dan EP monomer akrilamida pada onggok. Tabel 2 menunjukkan kadar nitrogen, NP, dan EP dari seluruh PSA yang dibuat. Data lengkap hasil perhitungan kadar nitrogen
onggok M1
8
dapat dilihat pada Lampiran 7 dan 8. Dari nilai NP dan EP yang didapatkan, diketahui bahwa semua PSA yang dibuat memiliki akrilamida yang tidak terlalu berbeda. Namun terlihat bahwa PSA A1 memiliki kadar nitrogen yang kecil dibandingkan PSA A2, A3, dan A4. Hal tersebut sejalan dengan pola daya serap air dari PSA tersebut. Terlihat bahwa semakin kecil kadar nitrogen maka daya serap airnya semakin baik. Untuk PSA M1, M2, dan M4 kadar nitrogennya juga mengikuti pola daya serap airnya. Hanya PSA M3 yang pola penyerapan airnya tidak sesuai dengan kadar nitrogen yang dimilikinya. Hal tersebut diduga akibat tidak sempurnanya proses grafting yang terjadi sehingga daya serapnya tidak begitu baik.
Tabel 2 Kadar nitrogen, nisbah pencangkokan, dan efisiensi pencangkokan PSA Sampel Kadar N
Kadar N merupakan dari kadar nitrogen akrilamida dari PSA.
Daya Serap Air PSA
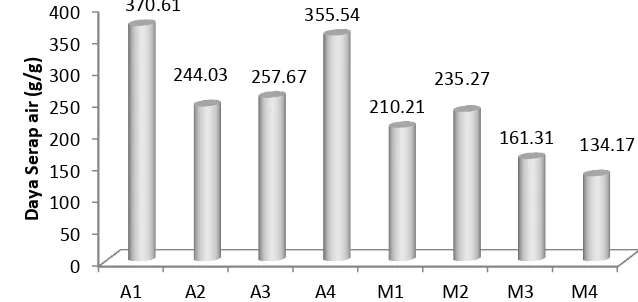
Penentuan daya serap air merupakan salah satu parameter utama dari penentuan kualitas polimer superabsorben (Azizah et al. 2012). Gambar 3 menunjukkan data hasil uji daya serap air pada berbagai Jenis PSA yang dibuat. Pencangkokan asam akrilat terlebih dahulu menghasilkan PSA yang memiliki daya serap air lebih baik dibandingkan PSA yang dihasilkan saat mencangkok akrilamida terlebih dahulu. Hal tersebut terlihat dari lebih besarnya daya serap A1 dengan M1, A2 dengan M2, A3 dengan M3, dan M4 dengan A4 pada penambahan penautsilang yang sama. Asam akrilat memiliki gugus COOH yang saat dinetralkan berubah menjadi COO-. Keberadaan Gugus fungsi COO -membuat struktur jaringan PSA sangat mudah mengembang akibat adanya gaya tolak menolak di antara gugus COO- yang ada. Selain itu, adanya muatan dari Na+ dari penetralan asam akrilat membuat PSA tersebut memiliki tekanan osmosis yang tinggi sehingga air sangat mudah masuk kedalam struktur jaringan PSA. Pencangkokan asam akrilat terlebih dahulu diduga dapat memberikan susunan asam akrilat yang lebih baik dalam struktur jaringan PSA yang terbentuk.
9 penelitian ini, PSA yang dibuat dengan tanpa penautsilang memiliki daya serap air yang lebih tinggi (PSA A1 memberikan daya serap air terbesar 370.61 g/g). Dengan pencangkokan monomer yang sama pada pati singkong namun dengan model pencangkokan yang berbeda, daya serap air yang dihasilkan PSA A1 lebih tinggi dari PSA yang dibuat Kiatkamjornwong et al. (2000) yang hanya sebesar 143,12 g/g. PSA yang dibuat dengan penambahan penautsilang di luar jumlah optimumnya (menambahkan penautsilang secara berlebih) terjadi penurunan elastisitas struktur polimer dan terlalu tingginya densitas polimer yang terbentuk sehingga daya serapnya menurun. Hal tersebut juga pernah disampaikan oleh Hua dan Wang (2009). Dugaan lain dari tingginya daya serap air PSA tanpa penambahan penautsilang adalah terbentuknya tautsilang diri dari interaksi antar monomernya (asam akrilat dan akrilamida) sehingga membentuk tautsilang tanpa bantuan senyawa penautsilang.
Gambar 3 Daya serap air superabsorben dari berbagai PSA.
Daya Jerap PSA pada Ion Logam Cu2+, Pb2+, dan Cr6+
PSA dapat dimanfaatkan untuk menjerap logam, termasuk di dalamnya adalah golongan logam berat seperti Ni, Cu, Pb (Ekebafe et al. 2012), Cr (Nada et al. 2007) Mn, Hg (Wang et al. 2011). Kemampuan adsorpsi PSA dipengaruhi gugus fungsi yang ada dan strukturnya (Bagheri et al. 2010). Selain itu, kemampuan adsorpsi PSA juga dipengaruhi ukuran atau radius atom logam dan elektronegativitas dari logam yang diadsorpsi (Nada et al. 2007). Kemampuan dari PSA tersebut diakibatkan karena adanya gugus karboksilat (COO-) yang dapat menjerap logam dengan cara membentuk senyawa kelat antara logam dengan gugus karboksilatnya. Struktur PSA yang berbentuk tiga dimensi membantu PSA untuk melakukan penjerapan logam. Gambar 4 menunjukan ilustrasi model penjerapan logam oleh PSA yang mengandung gugus karboksilat.
10
Gambar 4 Ilustrasi model penjerapan logam pada PSA (Wang et al. 2011)
Gambar 5 Daya adsorpsi ion logam Cu2+, Pb2+, dan Cr6+ oleh PSA selama 30
dicangkok pada onggok, digunakan 0.5 g
sampel untuk menjerap 50 ppm logam 47.82
Hasil penelitian
Pb2+ akrilamida dan
asam akrilat
dicangkok pada onggok , digunakan 0.5
g sampel untuk menjerap 50 ppm logam 41.3
Hasil penelitian
Cr6+ akrilamida dan
asam akrilat
dicangkok pada onggok , digunakan 0.5
g sampel untuk menjerap 50 ppm logam 11.06
Hasil penelitian
Cu2+ akrilonitril
dicangkok pada pati singkong, digunakan 0.5 g sampel untuk menjerap
50 ppm logam, selama 30 menit
64.52 Ekebafe et
al. 2013
Pb2+ akrilonitril
dicangkok pada pati singkong , digunakan 0.5 g sampel untuk menjerap
50 ppm logam selama 30 menit
54.1 Ekebafe et
al. 2014
Pb2+ akrilamida
dicangkok pada bubur kayu , digunakan 0.1 g sampel untuk menjerap 20 ppm
logam selama 30 menit
90 Nada et
al. 2007
Cr6+ akrilamida
dicangkok pada bubur kayu , digunakan 0.1 g sampel untuk menjerap 20 ppm
logam selama 30 menit
11 Hasil penjerapan ion logam Cu2+, Pb2+, dan Cr6+ selama 30 menit terlihat pada Gambar 5 dan Lampiran 10. PSA A1 memiliki kemampuan menjerap ion logam Cr6+ dan Pb2+ paling baik. Hal tersebut diakibatkan karena daya serap air
PSA A1 paling baik sehingga saat polimernya mengembang, maka kemungkinan masuknya logam pada struktur jaringan polimer menjadi lebih tinggi dibandingkan PSA lainnya. Oleh karena itu, PSA A1 dipilih untuk karakterisasi selanjutnya. Tabel 3 menunjukan kemampuan PSA A1 dalam mengadsorpsi ion logam Cu2+, Pb2+, dan Cr6+ selama 24 jam. Saat waktu kontak antara adsorben dan adsorbatnya lebih panjang (24 jam), logam yang paling banyak terjerap PSA A1 adalah ion Cu2+. Ion logam Cu2+ memiliki radius atom yang paling kecil sehingga paling mudah diadsorpsi oleh permukaan PSA. Logam Pb memiliki muatan yang sama dengan Cu2+, namun karena radius atomnya lebih besar dari Cu2+ sehingga relatif lebih sukar untuk teradsorpsi permukaan PSA. Adsorpsi unsur Cr6+ dilakukan menggunakan K2Cr2O7. K2Cr2O7 saat dilarutkan dalam air akan terionisasi menjadi K+ dan Cr2O72-. Saat dilakukan penjerapan Cr6+, ion logam tersebut berada dalam bentuk anion Cr2O72- sehingga sulit teradsorpsi oleh PSA yang cenderung bermuatan negatif.
Daya Serap Air PSA dalam Larutan NaCl
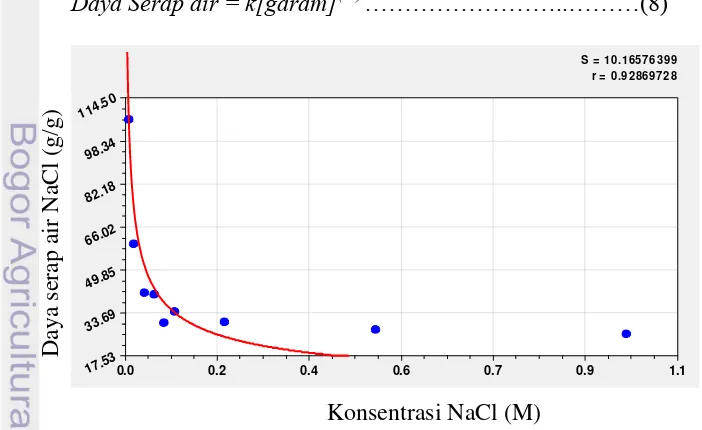
Kapasitas penyerapan air PSA juga sangat dipengaruhi oleh kehadiran garam. Uji kali ini dimaksudkan untuk mengetahui kemampuan PSA pada larutan yang mengandung garam NaCl dengan konsentrasi yang berbeda. Kehadiran garam dapat menurunkan tekanan osmotik pada PSA sehingga kemampuan penyerapannya dapat menurun. Penurunan tekanan osmotik tersebut terjadi akibat menurunnya perbedaan konsentrasi ionik antara struktur jaringan PSA dan larutan yang berada di luar struktur jaringan PSA (Mas’ud et al. 2013; Sadeghi 2011; Sadeghi dan Soleimani 2011). Persamaan yang sering digunakan untuk melihat hubungan antara daya serap suatu absorben dan konsentrasi garamnya adalah sebagai berikut:
a a a a a a -n ………..………(8)
Gambar 6 Daya serap air PSA dalam larutan NaCl
12
Nilai konstanta k dan n beda-beda untuk setiap PSA. Nilai k menunjukan kapasitas daya serap dari PSA saat konsentrasi garam tinggi, dan nilai n menunjukan nilai konsentrasi maksimum saat daya serap air PSA sudah tidak tergantung konsentrasi garamnya. Dari pengamatan yang telah dilakukan, diketahui bahwa terjadi penurunan kemampuan penyerapan air seiring dengan meningkatnya konsentrasi NaCl yang ada. Penurunan kemampuan penyerapan secara signifikan terjadi pada konsentrasi NaCl 0.01, 0.02, dan 0.04 M. Berdasarkan persamaan (8), nilai konstanta k dan n untuk PSA A1 adalah 11.93 g/g dan 0.45 M. Hal ini menunjukan bahwa saat konsentrasi garam dalam larutan melebihi 0.45 M, daya serap air PSA tidak dipengaruhi secara signifikan oleh konsentrasi NaCl. PSA A1 memiliki konsentrasi maksimum (n) lebih tinggi dibandingkan PSA yang telah dibuat Mas’ud et al. (2013) yang memiliki nilai n dan k sebesar 0.35 M, dan 29.06 g/g.
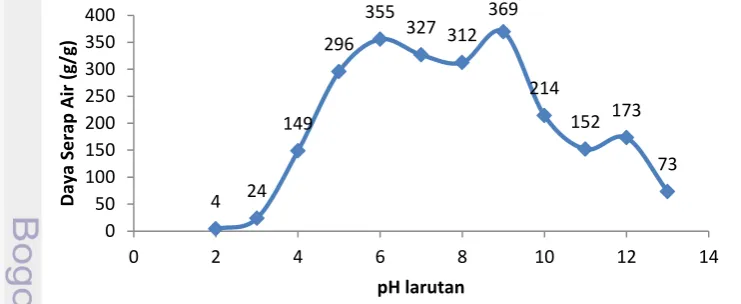
Daya Serap Air PSA dalam Larutan Berbagai Nilai pH
Dalam media asam, sebagian besar asam karboksilat terprotonasi, sehingga saat terjadinya penurunan gaya tolak antar anion kemampuan menyerap dari PSA
menurun. Pada pH 5 sd 9, gugus karboksilat mulai terionisasi menjadi anion-anionnya, sehingga mengakibatkan meningkatkan gaya tolak antar anionnya sehingga kemampuan penyerapannya meningkat. Gambar 4 menunjukan pola penyerapan air oleh PSA di berbagai nilai pH. Pada kondisi pH tinggi (dalam keadaan basa), kemampuan PSA menurun akibat dari pengaruh kation (ion Na+) yang dapat menimbulkan efek penambahan muatan pada larutan yang akan mengisi struktur jaringan PSA. Hal tersebut juga mengakibatkan menurunnya tekanan osmosis yang ada sehingga daya serap airnya menjadi rendah (Souleimani dan Sadeghi 2012).
Gambar 7 Daya serap PSA pada larutan di berbagai nilai pH
Adsorpsi Isotermal PSA
13 Langmuir dapat menunjukan terbentuknya lapisan monolayer yang memiliki energi adsorpsi yang konstan dan tidak terjadi perpindahan adsorbat pada permukaan tersebut. Dari hasil pengamatan yang dilakukan, isoterm yang paling cocok untuk penjerapan logam Pb2+ merupakan isoterm Freundlich (Gambar 8). menunjukan terjadinya pembentukan beberapa lapisan pada permukaan adsorben dan adsorpsi akan meningkat seiring dengan meningkatnya konsentrasi adsorbat. Linieritas grafik yang dihasilkan dari hasil penelitian dapat menunjukan kecocokan sistem adsorpsi yang terjadi dengan sistem adsorpsi yang diusulkan. Karena penjerapan ion logam Cu2+ dan Cr6+ oleh PSA A1 memiliki linieritas yang kecil baik pada model isoterm Langmuir dan isoterm Freundlich, maka diduga model penjerapan yang terjadi ada logam-logam tersebut adalah model isoterm penjerapan yang lain.
Gambar 8 Isoterm Freundlich ion logam Cu2+, Pb2+, dan Cr6+
SIMPULAN DAN SARAN
Simpulan
Pembuatan PSA dengan metode kopolimerisasi cangkok biner dari onggok dengan monomer asam akrilat dan akrilamida dapat dilakukan dan menghasilkan PSA terbaik dengan mencangkok asam akrilat terlebih dahulu. PSA terbaik (PSA
14
Saran
Metode pembuatan PSA dengan kopolimerisasi cangkok biner perlu dilakukan optimasi untuk menghasilkan karakter yang lebih baik. Analisis keberhasilan sintesis yang lebih baik perlu dilakukan untuk mengetahui secara tepat bentuk struktur polimer yang terbentuk. Uji kinerja PSA yang lebih variatif (seperti uji adsorpsi dengan model isoterm yang lain) perlu dilakukan untuk mengetahui karakter lain dari PSA yang dihasilkan.
DAFTAR PUSTAKA
Alka T, Neeraj S. 2012. Efficiency of superparamagnetic nano iron oxide loaded poly(Acrylamide-co-Acrylic acid) hidrogel in uptaking Pb2+ ion from water. Int Res J Env. Sci 1:6-13.
Azizah A, Irwan A, Sunardi. 2012. Sintesis dan karakterisasi polimer superabsorben berbasis selulosa dari tanaman purun tikus (Eleocharis dulcis) tercangkok akrilamida(AAM). Sains Ter Kim 6:59-70.
Bagheri B, Abdouss M, Aslzadeh MM, Shoushtari AM. 2010. Efficient removal of Cr3+ Pb2+ and Hg2+ ion from industrial effluents by hydrolyzed/thioaminated polyacrylonitrile fibers. Iran Pol J. 19:911-925. Badan pusat Statistik [BPS]. 2013. Luas panen, produktivitas dan produksi ubi
kayu menurut provinsi 2011.[Internet].[diunduh 2013 Okt 15];tersedia pada [http//www.bs.go.id/tnmn_pgn.php].
Buchholz FL, Graham A.T. 1997. Modern Superabsorbent Polymer Technology. New York: Wiley.
Dhodapkar R, Borde P, Nandy T. 2009. Superabsorbent polymers in environmental remediation. Glob NEST J. 11:223-234.
Ekebafe LO, Ogbeifun DE, Okieimen FE. 2012. Removal of heavy metals from aqueous media using native cassava starch hydrogel. Afr J Env Sci Tech.
6:275-282.
Gils PS, Ray D, Mohanta GP, Manavalan R, Sahoo PK. 2009. Designing of new acrylic based macroporous superabsorbent polymer hydrogel and its suitability for drug delivery. Int J of Pharm pharmac Sci. 1:43-54. Hashem A, Afifi MA, El-Alfy EA, Hebeish A. 2005. Synthesis, characterization
and saponification of poly (AN)-starch composites and properties of their hydrogels. Am J Appl Sci. 2:614-621.
Hua S, Wang A. 2009. Synthesis, characterization and swelling behaviors of sodium alginate-g-poly(acylic acid)/sodium humate superabsorbent. Car Pol. 75:79-84.
15 Kurniadi T. 2010. 2005. Kopolimerisasi grafting monomer asan akrilat pada onggok singkong dan karakterisasinya [Tesis]. Bogor: Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor.
Lanthong P, Nuisin R, Kiatkamjornwong S. 2006. Graft copolymerization, characterization, and degradation of cassava starch-g-acrylamide/itaconic acid superabsorbents. Car Pol. 66 : 229–245.
Liang R, Yuan H, Xi G, Zhou Q. 2009. Synthesis of wheat straw-g-poly(acrylic acid) superabsorbent composites and release of urea from it. Car Pol.
77:181-187.
Lidiasari E, Syafutri MI, Syaiful MS. 2006. Influence of drying temperature difference on physical and chemical qualities of partially fermented cassava flour. JIIPI. 8:141-146.
Mas’ud ZA, Khotib M, Farid M, Nur MA, Amroni M. 2013. Superabsorbent
derived from cassava waste pulp. Intl J Recl Org Was Agr 2:1-8.
Mehr MJZ, Kabiri K. 2008. Superabsorbent polymer material: a review. Iran Pol J. 17:451-477.
Mostafa Kh M, Samerkandy AR, El-sanabay AA. 2007. Modification of carbohydrate polymers part 2: grafting of methacrylamide onto pregelled starch using vanadium-mercaptosuccinic acid redox pair. J Appl Sci Res
3:681-689.
Nada AA, Alkady MY, Fekry HM. 2007. Synthesis and characterization of grafted cellulose for use in water and metal ions sorption. BioRecources
3:46-59.
Sadeghi M. 2011. Synthesis, and investigation of swelling behavior natural based
superabsorbent composites with high thermal resistance. Aus J Bas App
Sci. 5:887-895.
Sadeghi M, Hosseinzadeh H. 2008. Synthesis and swelling behavior of starch-poly (sodium acrylate-co-acrylamide) superabsorbent hydrogel. Turk j Chem 32:375-388.
Sadeghi M, Soleimani F. 2011. Synthesis and characterization superabsorbent hydrogels for oral drug delivery systems. Int J of Chem Eng App. 2:314-316.
Seo KW, Kim DJ, Park KN. 2004. Swelling properties of poly(AM-co-AA)/chitosan pH sensitive superporous hydrogel. J Ind Eng Chem.
10:794-800.
Soleimani F, Sadeghi M. 2012. Synthesis of pH-sensitive hydrogel based on starch-polyacrylate superabsorbent. J Biom Nangy. 3:310-314.
Virlandia F. 2005. Pemanfaatan onggok tapioka sebagai bahan baku pembuatan minyak melalui metode biokonversi [Skripsi]. Bandung: Fakultas Pertanian, Universitas Padjajaran.
Wang W. et al. 2011. Synthesis, swelling and responsive properties of a new composite hydrogel based on hydroxyethyl cellulose and medicinal stone.
Composites Part B 42: 809-818.
Wang WB, Xu JX, Wang AQ. 2011. A pH-, salt-, and solvent- responsive carboxymethylcellulose-g-poly(sodium acrylate)/medical stone superabsorbent composite with enhance swelling and responsive properties.
16
Lampiran 1 Diagram alir penelitian
Sampel onggok segar
Perlakuan pendahuluan 1. Pencucian 2. Penyaringan
Sampel onggok siap sintesis
1. Uji daya serap Air 2. Uji jerap logam Hidrogel
Superabsorben
Sintesis PSA 1. Kopolimerisasi
cangkok biner 2. Presipitasi
Hidrogel Superabsorben
terbaik
1 Uji daya serap pada berbagai nilai pH
2 Uji daya serap dalam larutan HCl
17 Lampiran 2 Radas kopolimerisasi pengcangkokan dan penautsilangan onggok
18
Lampiran 3 Mekanisme sintesis PSA A1
Inisiasi tahap 1
Propagasi tahap 1
50 ◦C
19 Lampiran lanjutan
20
Lampiran lanjutan
Inisiasi tahap 2
21 Lampiran lanjutan
Propagasi tahap 2
22
Lampiran lanjutan
23 Lampiran 4 Spektrum FTIR onggok murni, PSA A1, dan A2
Lampiran 5 Spektrum FTIR onggok murni, PSA A3 dan A4
A2 Onggok
A1
A3
24
Lampiran 6 Spektrum FTIR onggok murni, PSA M3 dan M4
M3 M4
25 Lampiran 7 Perhitungan kadar N secara teoritis
Sampel Bobot (g) kadar N
Keterangan: Aam = akrilamida; AA = asam akrilat Contoh perhitungan (sampel A1) :
Kadar N =
x bobot total sampel x 100%
Kadar N =
x 45.9006 x 100% = 8.90 g/g
Lampiran 8 Perhitungan kadar N dengan metode kjeldahl
Sampel Bobot awal
Contoh perhitungan (sampel A1) :
Kadar N =
Kadar N
=
26
Lampiran 9 Daya serap air dari berbagai macam jenis PSA
Sampel Bobot Awal
Contoh perhitungan (Sampel A1 ulangan ke-1)
27
Ket: FP = faktor pengenceran Contoh perhitungan (A1 pada Pb)
28
Lampiran 12 Penjerapan logam Cu2+ dengan berbagai macam nilai konsentrasi oleh PSA A1
Keterangan: m adalah bobot adsorben, x adalah masa terjerap Contoh perhitungan
[aktual tersisa] = [Tersisa terbaca] x FP = 0.6850 x 10
= 6.8500 ppm
29
Keterangan: m adalah bobot adsorben, x adalah masa terjerap
Lampiran 14 Penjerapan logam Cr6+ dengan berbagai macam nilai konsentrasi oleh PSA A1
Keterangan: m adalah masa adsorben, x adalah masa terjerap
30
Lampiran 16 Isoterm adsorpsi langmuir PSA A1