PERUBAHAN KONSENTRASI LARUTAN GULA PADA
DEHIDRASI OSMOTIK IRISAN MANGGA
(Mangifera indica L.) DAN PENGARUHNYA TERHADAP
KEBUTUHAN DAYA PENGADUKAN
SKRIPSI
Oleh :
FIBULA YUDISAPUTRO
F14080019
FAKULTAS TEKNOLOGI PERTANIAN
INSTITUT PERTANIAN BOGOR
BOGOR
CHANGES CONCENTRATION SUGAR SOLUTION IN THE OSMOTIC
DEHYDRATION OF MANGO SLICES
(Mangifera indica L.)
AND IT
IS EFFECT ON POWER REQUIREMENT
Fibula Yudisaputro and Leopold Oscar Nelwan
Departement of Mechanical and Biosystem Engineeirng, Faculty of Agricultural Technology, Bogor Agricultural University, IPB Darmaga Campus, PO Box 220, Bogor, West Java, Indonesia.
Phone +62 856 4166 1127, e-mail : fibula08@gmail.com
ABSTRACT
During osmotic dehydration, water leaving the product may dilute the osmotic solution, especially for conditions having low product solution ratio. The main objectives of this study were to obtain the characteristic of sugar solution concentration during osmotic dehydration of mango and its effect on stirring power requirement. Solution concentration used in this study was 61o brix. Three level of solution temperature, i.e 30 oC, 40 oC, 50 oC and three levels of stirring speed, i.e 100 rpm, 300 rpm and 500 rpm were used as the process variables. Stirring speed and high temperature solution will increase the water loss, while the final moisture content of the sample will be lower. Highest water loss by 70% and the lowest final moisture content of 35.3% wb occur at 30oC temperature treatment and stirring speed 500 rpm. Solid gain at high stirring speed increased temperatures 30oC (4.59%), 40oC (7.92%) and 50oC (11.9%), while the solid gain with medium and low stirring speed did not increase. High stirring speed (500 rpm) at a temperature of 30oC solution, 40oC and 50oC produces Reynolds number greater than the low (100 rpm) and medium (300 rpm) stirring speed for 8 hours. The decresing osmotic solution concentration due to the water leaving the mango during the osmotic process provided the reduction solution viscosity. These conditions caused in the stirring rotation speed increased, so the need for stirrer motor power decreased during the osmotic dehydration process.
FIBULA YUDISAPUTRO. F14080019. Perubahan Konsentrasi Larutan Gula pada Dehidrasi Osmotik Irisan Mangga (Mangifera indica L.) dan Pengaruhnya Terhadap
Kebutuhan Daya Pengadukan
.
Di bawah bimbingan Leopold Oscar Nelwan. 2012RINGKASAN
Dehidrasi osmotik merupakan salah satu alternatif untuk pengeringan buah-buahan yang dapat dipilih untuk mengurangi kandungan air dari dalam bahan. Dehidrasi osmotik merupakan teknik perendaman bahan dalam larutan hipertonik yang dapat mendorong pengeluaran air melalui membran sel dari bahan (Sereno et al. 2001). Untuk produk buah-buahan umumnya menggunakan larutan gula sebagai larutan hipertonik.Membran sel pada buah akan bertindak sebagai jaringan semipermeabel yang akan melewatkan air yang terkandung di dalam jaringan sel keluar menuju larutan akibat adanya perbedaan tekanan osmosis.
Pada aplikasi dehidrasi osmotik rasio larutan osmotik dengan jumlah berat mangga yang digunakan akan lebih besar dibandingkan pada saat penelitian atau kajian ilmiah mengenai dehidrasi osmotik. Rasio yang digunakan untuk penelitian akan lebih kecil, hal ini untuk memudahkan dalam mengetahui kondisi perlakuan yang diberikan seperti perubahan konsentrasi larutan gula selama dehidrasi osmotik. Perubahan konsentrasi larutan osmotik diakibatkan karena rasio larutan osmotik lebih rendah daripada berat sampel mangga, sehingga air dari sampel akan lebih mudah keluar dan akan tercampur ke dalam larutan osmotik.
Penurunan kadar air sampel dipengaruhi oleh kenaikan suhu larutan. Semakin tinggi suhu larutan mengakibatkan sampel menjadi lebih cepat kering. Suhu larutan yang tinggi dapat mempercepat perpindahan massa air dari dalam sampel ke larutan gula. Kecepatan pengadukan juga mempengaruhi penurunan kadar air sampel. Pada perlakuan suhu 30oC dengan kecepatan rendah memiliki penurunan kadar air yang lebih rendah dibandingkan dengan perlakuan dengan kecepatan sedang maupun tinggi. Hal ini juga dapat dilihat pada kecepatan pengadukan perlakuan suhu 40oC dan suhu 50oC. Perlakuan suhu 50oC dengan kecepatan pengadukan tinggi menghasilkan penurunan kadar air yang paling tinggi. Semakin cepat pengadukan dapat meningkatkan proses laju transfer massa dari larutan gula yang memiliki konsentrasi zat yang lebih tinggi ke konsentrasi zat yang lebih rendah yaitu ke dalam sampel mangga, sehingga penurunan kadar air menjadi lebih cepat dan proses dehidrasi osmotik menjadi lebih merata ke setiap permukaan sampel.
Water loss merupakan pengurangan jumlah air yang terdapat dalam sampel setelah terjadinya dehidrasi osmotik. Konsentrasi larutan merupakan salah satu yang memengaruhi nilai water loss. Semakin tinggi konsentrasi larutan gula yang digunakan maka beda konsentrasi dan tekanan osmotik akan semakin besar. Perubahan water loss dipengaruhi oleh suhu dan kecepatan pengadukan. Nilai WL yang paling tinggi pada perlakuan T3K3 (suhu 50oC dan dengan kecepatan pengadukan tinggi) yaitu sebesar 70.00% sedangkan nilai WL paling rendah terjadi pada perlakuan T1K1 (suhu 30oC dan kecepatan pengadukan rendah) yaitu 59.06%. Dari data tersebut menunjukkan bahwa penurunan kadar air berpengaruh terhadap tingkat kehilangan air pada sampel saat proses dehidrasi osmotik. Nilai kadar air akhir yang semakin rendah akan menghasilkan nilai WL semakin tinggi.
Solid gain menunjukkan banyaknya jumlah padatan terlarut yang masuk ke dalam sampel. Dalam proses dehidrasi osmotik, semakin tinggi nilai SG maka jumlah padatan terlarut yang masuk ke dalam sampel semakin banyak. Sedangkan, semakin rendah nilai SG maka jumlah padatan terlarut yang masuk ke sampel semakin sedikit. Untuk memberikan rasa sampel yang tidak terlalu manis maka nilai SG harus serendah mungkin. Nilai SG yang diperoleh sangat beragam di setiap perlakuan meskipun kadar air akhir yang diperoleh semakin rendah setiap perlakuan. Peningkatan suhu yang diberikan hanya mempengaruhi nilai SG pada kecepatan pengadukan tinggi. Kadar air akhir dan tingkat kehilangan air tidak berpengaruh terhadap padatan terlarut gula yang masuk ke dalam sampel. Nilai solid gain (SG) yang ditunjukkan pada kecepatan pengadukan tinggi mengalami peningkatan dari suhu 30oC (4.59%), 40oC (7.92%) dan 50oC (11.9%), sedangkan pada kecepatan rendah dan sedang tidak mengalami peningkatan.
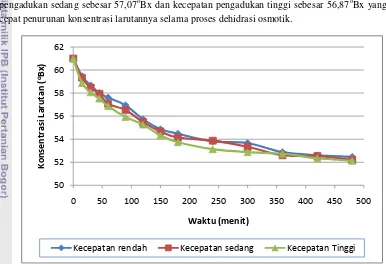
dan 50oC menghasilkan bilangan Reynolds yang lebih besar daripada kecepatan pengadukan rendah (100 rpm) dan sedang (300 rpm) selama waktu 8 jam. Kecepatan pengadukan saat proses dehidrasi osmotik berpengaruh terhadap kecepatan penurunan konsentrasi larutan dalam waktu tertentu. Pada suhu 50oC dan kecepatan pengadukan 500 rpm (T3K3) memberikan pengaruh yang besar terhadap penurunan konsentrasi larutan, meskipun untuk perlakuan lainnya hanya memberikan pengaruh yang sedikit.
Saat pengadukan larutan osmotik terbentuk suatu aliran fluida, karena adanya gerakan tertentu yang akan menimbulkan reduksi gerakan pada sampel ataupun larutan di dalam panci dehydrator. Gerakan hasil reduksi tersebut mempunyai pola sirkulasi yang dapat menimbulkan terjadinya pencampuran. Jenis aliran fluida terdiri dari aliran laminer dan aliran turbulen. Untuk mengetahui pola aliran pengadukan yang terjadi pada saat proses dehidrasi osmotik, maka dapat dihitung besarnya menggunakan bilangan Reynolds dengan parameter-parameter yang diketahui besarnya. Kecepatan pengadukan tinggi (500 rpm) pada suhu larutan 30oC, 40oC dan 50oC menghasilkan bilangan Reynolds yang lebih besar daripada kecepatan pengadukan rendah (100 rpm) dan sedang (300 rpm) selama waktu 8 jam. Nilai rata-rata bilangan Reynolds terbesar saat kecepatan pengadukan tinggi (500 rpm) adalah perlakuan dengan suhu 50oC sebesar 75031.
Kebutuhan daya yang dihasilkan saat proses pengadukan larutan osmotik dengan penggunaan sampel irisan mangga dan tanpa penggunaan irisan mangga berbeda. Pengadukan larutan osmotik dengan penggunaan irisan mangga menyebabkan beban kecepatan pengaduk akan lebih besar karena aliran larutan terhalang oleh beberapa sampel irisan mangga yang terdapat dalam wadah panci, sedangkan untuk pengadukan larutan osmotik tanpa penggunaan irisan mangga menyebabkan beban kecepatan pengaduk akan lebih kecil dan aliran larutan osmotik akan lebih mudah tercampur.
Tegangan listrik motor berpengaruh terhadap berbagai kecepatan pengadukan yang diinginkan. Semakin tinggi tegangan maka kecepatan putaran motor akan lebih tinggi. Untuk berbagai perlakuan kecepatan pengadukan (rendah, sedang, tinggi) menghasilkan kecepatan putaran motor dan daya motor saat terdapat sampel irisan mangga yang dihasilkan akan lebih tinggi dibandingkan dengan tanpa menggunakan sampel irisan mangga yang kecepatan putaran motor dan daya motor yang dihasilkan lebih rendah.
Pengukuran konsumsi energi dilakukan pada proses saat terdapatnya sampel mangga dalam larutan osmotik dan tidak terdapatnya sampel mangga dalam larutan osmotik. Dalam penentuan konsumsi energi ini, diperlukan data-data dari pengukuran sifat reologi dan sifat fisik fluida. Karakteristik power dari suatu pencampuran, biasanya disajikan dalam bentuk grafik hubungan antara bilangan Reynolds dengan bilangan daya.
PERUBAHAN KONSENTRASI LARUTAN GULA PADA
DEHIDRASI OSMOTIK IRISAN MANGGA
(Mangifera indica L.) DAN PENGARUHNYA TERHADAP
KEBUTUHAN DAYA PENGADUKAN
SKRIPSI
Sebagai Salah Satu Syarat untuk Memperoleh Gelar
SARJANA TEKNOLOGI PERTANIAN
pada Departemen Teknik Mesin dan Biosistem
Fakultas Teknologi Pertanian
Institut Pertanian Bogor
Oleh :
FIBULA YUDISAPUTRO
F14080019
FAKULTAS TEKNOLOGI PERTANIAN
INSTITUT PERTANIAN BOGOR
Judul Skripsi : PERUBAHAN KONSENTRASI LARUTAN GULA PADA DEHIDRASI
OSMOTIK IRISAN MANGGA (Mangifera indica L.) DAN
PENGARUHNYA TERHADAP KEBUTUHAN DAYA PENGADUKAN
Nama : Fibula Yudisaputro
NIM : F14080019
Menyetujui, Pembimbing Akademik,
Dr. Ir. Leopold O. Nelwan, M. Si
NIP. 19701208 199903 1 001
Mengetahui : Ketua Departemen,
Dr. Ir. Desrial, M. Eng
NIP. 19661201 199103 1 004
PERNYATAAN MENGENAI SKRIPSI DAN
SUMBER INFORMASI
Saya menyatakan dengan sebenar-benarnya bahwa skripsi dengan judul “Perubahan
Konsentrasi Larutan Gula Pada Dehidrasi Osmotik Irisan Mangga (Mangifera indica L) dan
Pengaruhnya Terhadap Kebutuhan Daya Pengadukan” adalah hasil karya saya sendiri dengan
arahan dosen pembimbing akademik, dan belum diajukan dalam bentuk apapun pada perguruan
tinggi manapun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun
tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar
Pustaka di bagian akhir skripsi ini.
Bogor,Desember 2012 Yang membuat pernyataan
© Hak cipta milik Fibula Yudisaputro, tahun 2012 Hak cipta dilindungi
Dilarang mengutip dan memperbanyak tanpa izin tertulis dari
BIODATA PENULIS
Penulis dilahirkan di Pati, Jawa Tengah pada tanggal 28 Februari 1990 sebagai anak pertama dari 2 bersaudara dari pasangan Yudi Hudiono dan Etty Rustina. Penulis memiliki seorang adik yang bernama Tibia Yudi Saputri dan Muhhamad Nabila Yudi Saputra
Penulis memulai pendidikan pada saat usia 5 tahun di TK Bayangkara 42 (1995-1996) dan kemudian melanjutkan pendidikan dasar di SDN 01 Pati Kidul (1997-2002). Pendidikan menengah pertama ditempuh di SMPN 3 Pati (2002-2005). Sedangkan pendidikan menengah atas ditempuh di SMAN 1 Pati (2005-2008). Penulis diterima di Institut Pertanian Bogor sebagai mahasiswa melalui jalur Undangan Seleksi Masuk IPB (USMI) pada tahun 2008 dan mengambil mayor Teknik Pertanian Departemen Teknik Mesin dan Biosistem, Fakultas Teknologi Pertanian.
Selama menempuh pendidikan di bangku kuliah, penulis pernah mengikuti berbagai organisasi baik organisasi kemahasiswaan maupun organisasi mahasiswa daerah. Organisasi kemahasiswaan yang pernah diikuti adalah IKMP (Ikatan Keluarga Mahasiswa Pati), IMATETANI (Ikatan Mahasiswa Teknik Pertanian Nasional) dan Himateta (Himpunan Mahasiswa Teknik Pertanian).
i
KATA PENGANTAR
Puji syukur dan kehadirat Allah SWT atas segala rahmat dan karunia-Nya yang telah diberikan kepada penulis, sehingga pada akhirnya penulis dapat menyelesaikan pelaksanaan Penelitian dan penulisan laporan skripsi. Penelitian dilaksanakan di Laboratorium Energi dan Elektrifikasi Pertanian dengan judul Perubahan Konsentrasi Larutan Gula Pada Dehidrasi Osmotik Irisan Mangga (Mangifera indica L) dan Pengaruhnya Terhadap Kebutuhan Daya Pengadukan. Pelaksanaan penelitian di laksanakan antara bulan April – Juni 2012.
Pada kesempatan ini penulis menyampaikan terima kasih kepada
1. Dr. Ir. Leopold O. Nelwan, M. Si selaku dosen pembimbing akademik yang telah memberikan bimbingan dan arahan kepada penulis.
2. Dr. Ir. Edy Hartulistiyoso, M.Sc dan Ir. Susilo Sarwono selaku dosen penguji tugas akhir. 3. Ayah Drs. Yudi Hudiono, M.Si dan Ibu Dra. Etty Rustina selaku orang tua dan adik-adikku,
Tibia Yudi Saputri dan Muhhamad Nabila Yudi Saputra yang selalu memberikan dukungan dan doannya.
4. Teman-teman satu bimbingan Yuliana, Yulfi Nizzatal Maulia, Delimy Okta Riski, dan Rizki Muhammad Thariq yang telah membantu dalam penelitian.
5. Liba Silvia Bunga Kasih yang selalu memberikan semangat dan dukungannya.
6. Teman-teman satu kontrakan “Wisma Zero”, Haratul Lisan, Faiz Ridhan Faroka, Angga Rakay Fatahilah, Angga Herviona, Dimas Kholis, Ahmad Eriska, Rudiansyah yang telah memberikan semangat serta bantuannya dalam penelitian.
7. Pak Harto, Pak Firman dan Pak Suliyaden yang telah memberikan bantuan dalam penelitian. 8. Seluruh teman-teman Teknik Pertanian 2008 (Magenta 45) atas kebersamaan, kerjasama dan
dukungan selama penulis melaksanakan studi di IPB.
9. Seluruh pihak yang telah mendukung dan membantu penulis dalam menyelesaikan tugas akhir penelitian ini.
Penulis berharap agar skripsi ini dapat bermanfaat dan memberikan kontribusi yang nyata terhadap perkembangan ilmu pengetahuan.
Bogor, Desember 2012
ii
DAFTAR ISI
halaman
KATA PENGANTAR ...i
DAFTAR ISI ...ii
DAFTAR TABEL ...iii
DAFTAR GAMBAR ...iv
DAFTAR LAMPIRAN ...vi
I. PENDAHULUAN ...1
A. Latar Belakang ...1
B. Tujuan ...2
II. TINJAUAN PUSTAKA ...3
A. Mangga (Mangifera indica L.) ...3
B. Dehidrasi Osmotik ...5
C. Pengadukan dan Pencampuran ...7
D. Daya Lisrik dan Daya Mekanik ...11
III. METODE PENELITIAN ...13
A. Waktu dan Tempat ...13
B. Alat dan Bahan ...13
C. Prosedur Penelitian ...14
D. Rancangan Penelitian ...15
E. Pengamatan...17
IV. HASIL DAN PEMBAHASAN ...20
A. Kadar Air ...20
B. Water Loss dan Solid Gain ...21
C. Perubahan Konsentrasi Larutan dan Bilangan Reynolds ...23
D. Hubungan Daya Motor dengan Kecepatan Pengadukan dan Bilangan Reynolds ...29
V. PENUTUP ...38
A. Kesimpulan ...38
B. Saran ...38
DAFTAR PUSTAKA ...39
iii
DAFTAR TABEL
halaman
Tabel 1. Produksi buah mangga di Indonesia ...4
Tabel 2. Sifat fisika dan kimia daging buah dan beberapa varietas mangga ...5
Tabel 3. Jenis dan kombinasi perlakuan ...15
iv
DAFTAR GAMBAR
halaman
Gambar 1. Buah mangga varietas Indramayu ...5
Gambar 2. Bentuk – bentuk pengaduk ...9
Gambar 3. Tipe - tipe pengaduk jenis turbine ...9
Gambar 4. Tipe - tipe pengaduk jenis propeller ...9
Gambar 5. Tipe - tipe pengaduk jenis paddle...9
Gambar 6. Motor losses ...12
Gambar 7. Grafik karakteristik motor DC ...12
Gambar 8. Osmotic Dehydrator ...15
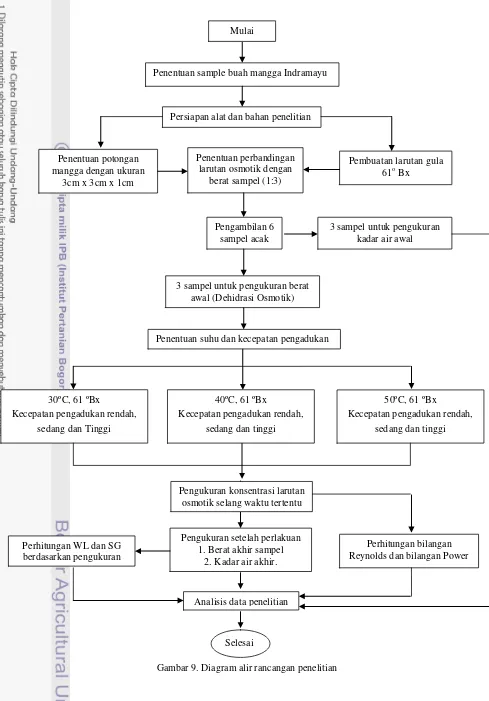
Gambar 9. Diagram alir rancangan penelitian ...16
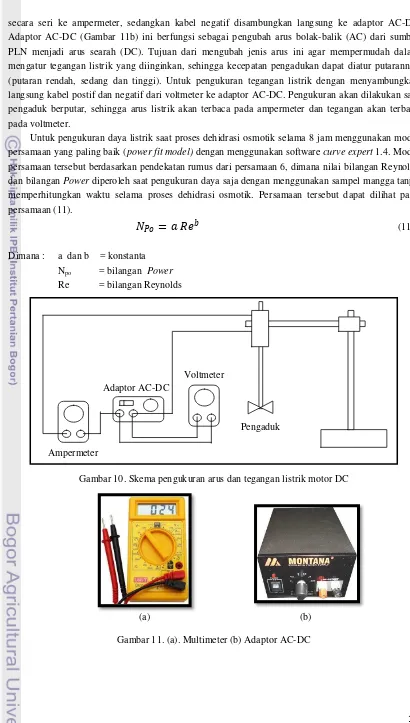
Gambar 10. Skema pengukuran arus dan tegangan listrik motor DC ...19
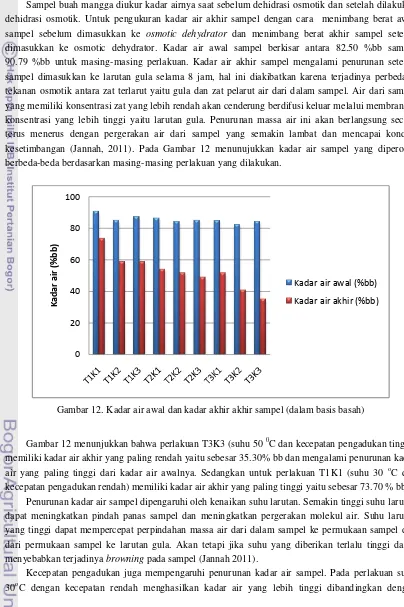
Gambar 11a. Multimeter ...19
Gambar 11b. Adaptor AC - DC ...19
Gambar 12. Kadar air awal dan kadar akhir akhir sampel (dalam basis basah) ...20
Gambar 13. Nilai water loss (WL) saat proses dehidrasi osmotik ...21
Gambar 14. Nilai solid gain (SG) saat proses dehidrasi osmotik ...22
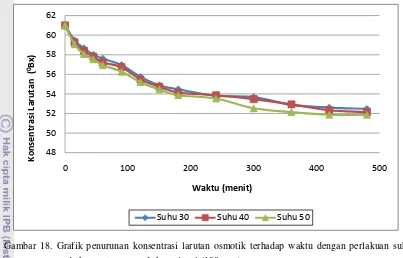
Gambar 15. Grafik penurunan konsentrasi larutan osmotik terhadap waktu pada suhu 30oC ...23
Gambar 16. Grafik penurunan konsentrasi larutan osmotik terhadap waktu pada suhu 40oC ...24
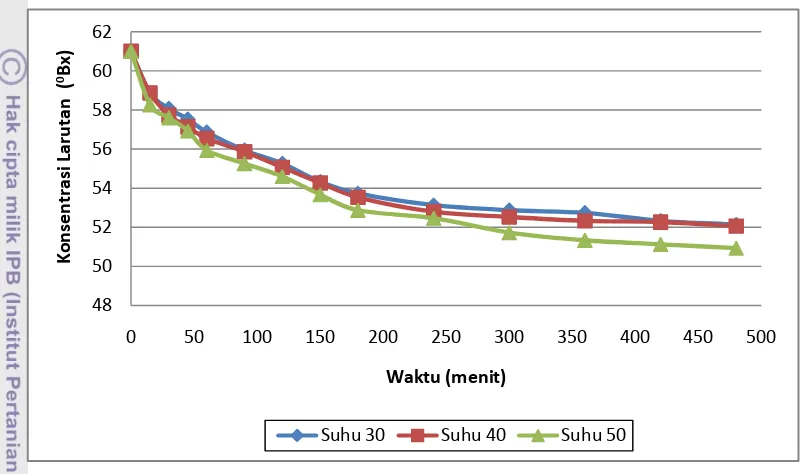
Gambar 17. Grafik penurunan konsentrasi larutan osmotik terhadap waktu pada suhu 50oC ...24
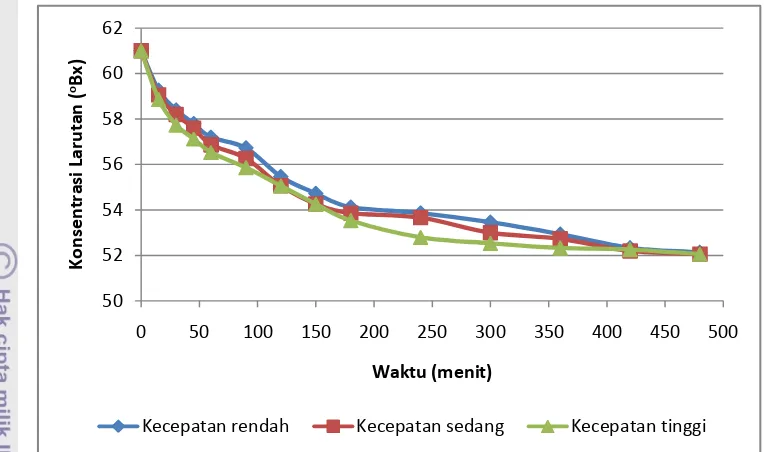
Gambar 18 Grafik penurunan konsentrasi larutan osmotik terhadap waktu dengan perlakuan suhu pada kecepatan pengadukan tinggi (100 rpm) . ...25
Gambar 19 Grafik penurunan konsentrasi larutan osmotik terhadap waktu dengan perlakuan suhu pada kecepatan pengadukan tinggi (300 rpm) . ...25
Gambar 20 Grafik penurunan konsentrasi larutan osmotik terhadap waktu dengan perlakuan suhu pada kecepatan pengadukan tinggi (500 rpm) . ...26
Gambar 21. Grafik hubungan bilangan Reynolds terhadap waktu pada suhu 30oC ...27
Gambar 22. Grafik hubungan bilangan Reynolds terhadap waktu pada suhu 40oC ...27
Gambar 23. Grafik hubungan bilangan Reynolds terhadap waktu pada suhu 50oC ...28
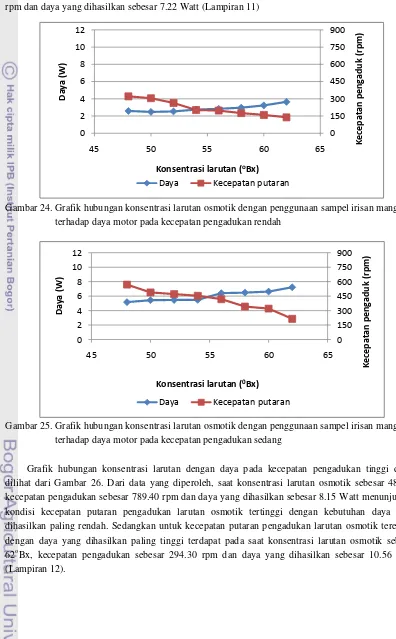
Gambar 24. Grafik hubungan konsentrasi larutan osmotik dengan penggunaan sampel irisan mangga terhadap daya motor pada kecepatan pengadukan rendah ...30
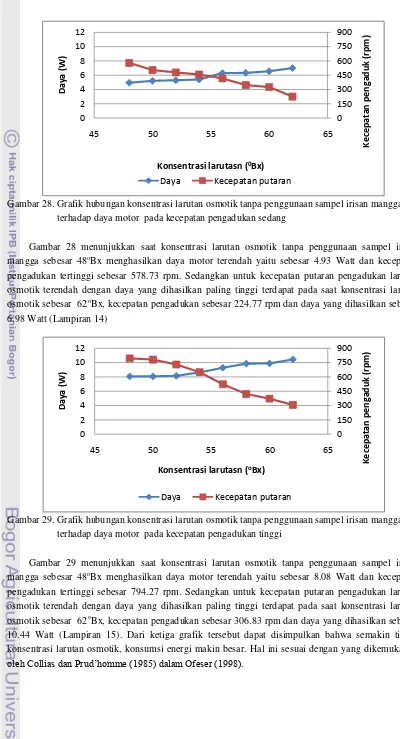
Gambar 25. Grafik hubungan konsentrasi larutan osmotik dengan penggunaan sampel irisan mangga terhadap dayamotor pada kecepatan pengadukan sedang ...30
Gambar 26. Grafik hubungan konsentrasi larutan osmotik dengan penggunaan sampel irisan mangga terhadap daya motor pada kecepatan pengadukan tinggi ...31
Gambar 27. Grafik hubungan konsentrasi larutan osmotik tanpa penggunaan sampel irisan mangga terhadap daya motor pada kecepatan pengadukan rendah ...31
Gambar 28. Grafik hubungan konsentrasi larutan osmotik tanpa penggunaan sampel irisan mangga terhadap daya motor pada kecepatan pengadukan sedang ...32
Gambar 29. Grafik hubungan konsentrasi larutan osmotik tanpa penggunaan sampel irisan mangga terhadap daya motor pada kecepatan pengadukan tinggi ...32
v
penggunaan sampel irisan mangga ...33 Gambar 32. Grafik hubungan daya listrik saat proses dehidrasi osmotik pada suhu 30oCselama selang waktu 8 jam dengan kecepatan pengadukan yang berbeda ...35 Gambar 33. Grafik hubungan daya listrik saat proses dehidrasi osmotik pada suhu 40oC
selama selang waktu 8 jam dengan kecepatan pengadukan yang berbeda ...35 Gambar 34. Grafik hubungan daya listrik saat proses dehidrasi osmotik pada suhu 50oC
selama selang waktu 8 jam dengan kecepatan pengadukan yang berbeda ...36 Gambar 35. Grafik hubungan bilangan Reynolds terhadap bilangan Reynoldssaat proses
vi
DAFTAR LAMPIRAN
halaman
Lampiran 1. Bilangan Reynolds yang dihasilkan selama proses dehidrasi osmotik denganperlakuan suhu 30oC dan kecepatan pengadukan rendah...42 Lampiran 2. Bilangan Reynolds yang dihasilkan selama proses dehidrasi osmotik dengan
perlakuan suhu 30oC dan kecepatan pengadukan sedang ...43 Lampiran 3. Bilangan Reynolds yang dihasilkan selama proses dehidrasi osmotik dengan
perlakuan suhu 30oC dan kecepatan pengadukan tinggi ...44 Lampiran 4. Bilangan Reynolds yang dihasilkan selama proses dehidrasi osmotik dengan
perlakuan suhu 40oC dan kecepatan pengadukan rendah...45 Lampiran 5. Bilangan Reynolds yang dihasilkan selama proses dehidrasi osmotik dengan
perlakuan suhu 40oC dan kecepatan pengadukan sedang ...46 Lampiran 6. Bilangan Reynolds yang dihasilkan selama proses dehidrasi osmotik dengan
perlakuan suhu 40oC dan kecepatan pengadukan tinggi ...47 Lampiran 7. Bilangan Reynolds yang dihasilkan selama proses dehidrasi osmotik dengan
perlakuan suhu 50oC dan kecepatan pengadukan rendah...48 Lampiran 8. Bilangan Reynolds yang dihasilkan selama proses dehidrasi osmotik dengan
perlakuan suhu 50oC dan kecepatan pengadukan sedang ...49 Lampiran 9. Bilangan Reynolds yang dihasilkan selama proses dehidrasi osmotik dengan
perlakuan suhu 50oC dan kecepatan pengadukan tinggi ...50 Lampiran 10. Daya yang dihasilkan saat larutan osmotik dengan penggunaan mangga pada
kecepatan pengadukan rendah ...51 Lampiran 11. Daya yang dihasilkan saat larutan osmotik dengan penggunaan mangga pada
kecepatan pengadukan sedang ...52 Lampiran 12. Daya yang dihasilkan saat larutan osmotik dengan penggunaan mangga pada
kecepatan pengadukan tinggi ...53 Lampiran 13. Daya yang dihasilkan saat larutan osmotik tanpa penggunaan mangga pada
kecepatan pengadukan rendah ...54 Lampiran 14. Daya yang dihasilkan saat larutan osmotik tanpa penggunaan mangga pada
kecepatan pengadukan sedang ...55 Lampiran 15. Daya yang dihasilkan saat larutan osmotik tanpa penggunaan mangga pada
kecepatan pengadukan tinggi ...56 Lampiran 16. Bilangan Reynolds dan Bilangan Power pada pengukuran daya pengaduk
larutan osmotik dengan penggunaan sampel mangga ...57 Lampiran 17. Bilangan Reynolds dan Bilangan Power pada pengukuran daya pengaduk
larutan osmotik tanpa penggunaan sampel mangga ...58 Lampiran 18. Grafik hubungan Bilangan Reynolds terhadap Bilangan Reynoldssaat proses
dehidrasi osmotik pada suhu 40oC selama selang waktu 8 jam ...59 Lampiran 19. Grafik hubungan Bilangan Reynolds terhadap Bilangan Reynoldssaat proses
1
I.
PENDAHULUAN
A.
LATAR BELAKANG
Mangga (Mangifera indica L.) merupakan buah tropika yang banyak mengandung sumber vitamin A, vitamin B-karoten, serta vitamin C. Indonesia merupakan salah satu negara dengan berbagai jenis dan varietas mangga yang beraneka ragam. Mangga biasa disajikan dalam keadaan segar ataupun dalam bentuk olahan industri. Penyajian mangga dalam bentuk olahan industri bertujuan untuk dapat menjaga kualitas cita rasa dan mutu dari produk itu. Produksi buah mangga di Indonesia dipengaruhi oleh kondisi cuaca yang tidak menentu, karena buah mangga merupakan buah musiman yang hanya ada pada waktu tertentu. Apabila pada saatnya mangga berbunga mengalami musim hujan maka akan mengalami penundaan mangga untuk berbuah. Berdasarkan data dari Departemen Pertanian, produksi mangga Indonesia pada tahun 2011 mencapai 1,84 juta ton.
Salah satu cara pengawetan adalah dengan cara dehidrasi. Dehidrasi dilakukan untuk dapat menurunkan kadar air pada buah atau makanan agar tercapai kadar air tertentu atau yang diinginkan dan menurunkan aktifitas mikroorganisme. Pengeringan biasa dilakukan secara konvensional, yaitu pengeringan dengan memanfaatkan sinar matahari. Pengeringan konvensional sering dimanfaatkan masyarakat karena dapat menekan biaya. Akan tetapi kekurangan dari pengeringan secara konvensional adalah kebutuhan energi yang tinggi, karena dengan pengeringan secara konvensional terjadi perubahan fase. Pengeringan secara konvensional ini tidak dianjurkan dalam pengeringan mangga ataupun buah-buahan karena dapat menurunkan kualitas produk.
Dehidrasi osmotik merupakan salah satu alternatif untuk pengeringan buah-buahan yang dapat dipilih untuk mengurangi kandungan air dari dalam bahan. Dehidrasi osmotik merupakan teknik perendaman bahan dalam larutan hipertonik yang dapat mendorong pengeluaran air melalui membran sel dari bahan (Sereno et al. 2001). Untuk produk buah-buahan umumnya menggunakan larutan gula sebagai larutan hipertonik. Membran sel pada buah akan bertindak sebagai jaringan semipermeabel yang akan melewatkan air yang terkandung di dalam jaringan sel keluar menuju larutan akibat adanya perbedaan tekanan osmosis. Pada aplikasi dehidrasi osmotik rasio larutan osmotik dengan jumlah berat mangga yang digunakan akan lebih besar dibandingkan pada saat penelitian atau kajian ilmiah mengenai dehidrasi osmotik. Rasio yang digunakan untuk penelitian akan lebih kecil, hal ini untuk memudahkan dalam mengetahui kondisi perlakuan yang diberikan seperti perubahan konsentrasi larutan gula selama dehidrasi osmotik. Perubahan konsentrasi larutan osmotik diakibatkan karena rasio larutan osmotik lebih rendah daripada berat sampel mangga, sehingga air dari sampel akan lebih mudah keluar dan akan tercampur ke dalam larutan osmotik.
2
Nilai dari water loss (WL) dan solid gain (SG) dipengaruhi oleh beberapa faktor antara lain konsentrasi larutan osmotik, waktu kontak, suhu larutan, rasio larutan osmotik/solid, ukuran dan bentuk solid, ukuran molekul solid dan kecepatan pengadukan. Dua faktor yang dikaji selama proses dehidrasi osmotik adalah faktor kecepatan pengadukan dan faktor suhu. Suhu yang semakin tinggi dapat mengakibatkan laju transfer massa. Perpindahan aliran massa yang berlawanan dari perpindahan air yang keluar dari bahan menuju larutan osmosis mengakibatkan kadar air bahan menjadi lebih rendah dan kecepatan water loss akan semakin tinggi serta perpindahan padatan dari larutan osmotik menuju ke dalam bahan pangan akan semakin tinggi. Pada saat yang sama, air yang keluar dari bahan akan mengakibatkan viskositas larutan osmotik menjadi lebih rendah dan konsentrasi larutan osmotik akan berubah. Hal ini terjadi terutama ketika rasio produk dan larutan relatif rendah.Perubahan konsenrasi larutan selama dehidrasi osmotik ini sangat penting untuk dikaji, diharapkan untuk mengetahui kebutuhan recovery larutan agar konsentrasi larutan osmotik dapat dijaga konstan selama proses dehidrasi osmotik. Pengetahuan tersebut juga sangat penting untuk menentukan besarnya energi yang dibutuhkan saat pengadukan larutan. Konsentrasi larutan osmotik yang lebih rendah mengakibatkan viskositas yang lebih rendah. Diduga perubahan kecepatan pengadukan akan terjadi pada saat perubahan viskositas larutan osmotik atau perubahan konsentrasi larutan osmotik yang dapat memengaruhi daya listrik yang dibutuhkan motor untuk proses pengadukan larutan osmotik.
B.
TUJUAN
Tujuan dari penelitian ini adalah :
1. Mengetahui pengaruh suhu dan kecepatan pengadukan larutan osmotik terhadap perubahan water loss (WL), solid gain (SG) dan penurunan konsentrasi larutan selama proses dehidrasi osmotik mangga.
2. Mengetahui perubahan bilangan Reynolds dari sistem pengaduk tipe paddle selama dehidrasi osmotik mangga akibat pengenceran larutan osmotik.
3. Mengetahui hubungan bilangan Reynolds dan bilangan daya dari sistem pengaduk tipe paddle selama dehidrasi osmotik mangga akibat pengenceran larutan osmotik.
3
II. TINJAUAN PUSTAKA
A.
MANGGA
Mangga merupakan tanaman tropika yang berasal dari lembah Indus, yaitu perbatasan antara Burma dan India. Kemudian mangga menyebar ke Asia Tenggara dibawa pedagang India sekaligus menyebarkan agama Hindu dan Budha sekitar 1450 tahun yang lalu. Istilah mangga berasal dari bahasa Tamil di India yaitu man-kayatau man-gas. Dalam bahasa botani, mangga disebut Mangifera indica L., yang berarti tanaman mangga berasal dari India. Sebutan mangga dalam Bahasa Indonesia mirip sekali dengan Bahasa Tamil yaitu man-gas (Pracaya 2011)
Klasifikasi botani tanaman mangga adalah sebagai berikut: Divisi : Spermatophyta
Sub divisi : Angiospermae Kelas : Dicotyledonae Keluarga : Anarcadiaceae Genus : Mangifera Spesies : Mangifera spp
Tanaman mangga tumbuh dalam bentuk pohon berbatang tegak, bercabang banyak, serta bertajuk rindang dan hijau sepanjang tahun. Tinggi tanaman dewasanya bisa mencapai 10-40 m dengan umur biasa mencapai lebih dari 100 tahun. Morfologi tanaman mangga terdiri atas akar, batang, daun dan bunga. Bunga menghasilkan buah dan biji (pelok) yang secara generatif dapat tumbuh menjadi tanaman baru.
Dalam keadaan normal, bunga tumbuh dari tunas ujung. Bunga mangga terangkai dalam tandan sebagai bunga majemuk. Rangkaian bunganya berbentuk kerucut yang melebar di bagian bawah dengan panjang 10-60 cm. Kuntum bunga mangga bertangkai pendek, berdaun kecil dan harum. Jumlah bunga setiap tandan berkisar 1000-6000 kuntum. Ukuran bunganya kecil-kecil dengan diameter 6-8 mm. Dari setiap rangkaian bunga, terdapat bunga jantan dan bunga hermaprodit (berkelamin ganda, jantan dan betina).
Benang sari bunga mangga ada lima, tetapi yang subur hanya satu atau dua, sedangkan lainnya steril. Benang sari yang subur biasanya hampir sama panjang dengan putik, yakni sekitar 2 mm, sedangkan benang sari yang steril berukuran lebih pendek. Warna kepala putik kemerah-merahan yang akan berubah menjadi ungu pada saat kepala sari membuka. Tujuannya adalah untuk memberi kesempatan tepung sari dewasa menyerbuki kepala putik. Bakal buah pada tanaman mangga tidak bertangkai, satu ruangan dan terletak pada satu piringan. Tangkai putik terdapat mulai dari tepi bakal buah dan di bagian ujung terdapat kepala putik yang bentuknya sederhana. Dalam satu bunga kadang-kadang terdapat tiga bakal buah.
4
Daging buah mangga ada yang berserat dan tidak berserat, berair dan tidak berair, serta manis. Warnanya ada yang kuning, krem atau jingga. Serat-serat yang berasal dari kulit biji (endokarp) kadang-kadang bisa menembus ke daging buah sehingga daging buahnya berserat. Pada mangga berserat, umumnya yang dikonsumsi adalah cairan buahnya saja (Pracaya 2011).Mangga masih dapat tumbuh sehat pada temperatur 4ºC-10ºC. Namun kondisi itu bukan merupakan temperatur optimum untuk pertumbuhan mangga. Temperatur pertumbuhan mangga yang optimum berkisar antara 24ºC-27ºC. Mangga membutuhkan curah hujan minimal 1000 mm, dan musim kering 4-6 bulan per tahun. Setiap bulan rata-rata hujan tidak lebih dari 60 mm. Di Jawa, mangga berbunga pada bulan Juli-Agustus, panen antara bulan September-November (Pracaya 2001). Produksi buah mangga di Indonesia dapat di lihat pada Tabel 1.
Tabel 1.Produksi buah mangga di Indonesia
Tahun Jumlah Produksi (ton)
2007
2008
2009
2010
2011*)
1 818 619
2 105 085
2 243 440
1 287 287
2 129 608
*) Angka Sementara
Badan Pusat Statistik Nasional
Komponen daging buah mangga yang paling banyak adalah air dan karbohidrat. Karbohidrat daging buah mangga terdiri dari gula sederhana, tepung dan selulosa. Gula sederhananya berupa sukrosa, glukosa dan fruktosa yang memberikan rasa manis yang akan bermanfaat bagi pemulihan tenaga pada tubuh manusia. Selulosa dan pektin pada buah mangga dipercaya akan melancarkan saluran pencernaan. Selain itu tanin pada buah mangga menyebabkan rasa kelat (sepet) dan menyebabkan buah mangga menjadi hitam setelah diiris. Terkadang, tanin juga membuat buah mangga menjadi pahit. Rasa asam dari asam sitrat disebabkan oleh adanya vitamin C yang juga bermanfaat bagi tubuh.
Berbagai jenis varietas tanaman mangga biasa dikembangkan secara generatif. Selain itu pengembangan mangga juga dilakukan secara vegetatif yang akan diperoleh populasi tanaman baru yang tidak akan berubah sifatnya dan memiliki mutu yang tinggi.
Masing-masing varietas mangga dapat dibedakan berdasarkan ukuran, warna daging, rasa, aroma, karakter dan bentuk buah. Selain itu juga dapat dibedakan berdasarkan sifat pohon, ukuran dan bentuk daun.
5
Di Indonesia beberapa jenis dan varietas mangga komersial yang sudah terkenal bagus mutunya antara lain golek, arumanis, manalagi, endog, madu, lalijiwo, keweni, pekel, kemang dan cengkir (Indramayu). Mangga cengkir banyak ditanam di Indramayu (Jawa Barat) dapat dikenal juga dengan sebutan mangga indramayu (Gambar 1). Bentuk buahnya bulat telur, berbobot 400-500 g per buah. Daging buahnya tebal, berwarna kuning, bertekstur lembut, memiliki rasa sedikit manis, tidak berserat kecuali pada daging buah yang dekat kulit biji, memiliki kandungan air sedikit dan beraroma sedikit harum (Pracaya 2011). Sifat fisik dan kimia daging buah mangga terdapat pada Tabel 2.
Tabel 2. Sifat fisika dan kimia daging buah beberapa varietas mangga
Sifat Fisika dan Kimia Varietas Mangga
Arumanis Cengkir Gadung Gedong
Padatan terlarut total (oBx) 14.8-16.6 13.0-15.0 20.8-21.2 16.0-17.8
Asam total (%) 0.22-0.56 0.26-0.88 0.18-0.47 0.12-17.8
Vitamin C (mg/100g) 22.0-46.9 37.8-58.2 20.0-21.5 36.2-96.2
Kadar air (%) ± 81.1 ± 84.3 ± 80.34 ± 82.9
Bobot utuh (g) ± 376.2 ± 320.1 ± 411.1 ± 232.4
Bagian yang dapat dimakan (%) ± 66.0 ± 65.8 ± 66.0 ± 59.0
Warna daging buah Kuning Kekuningan Kuning Jingga
Sumber : Broto 2003
Buah mangga dipanen dengan tingkat ketuaan 85% yaitu berumur 110-120 hari semenjak bunga mekar dengan warna hijau dengan pangkal kemerahan. Buah mangga dipanen dengan menyisakan tangkai sepanjang 10-15 mm. Hal ini dikarenakan dengan menyisakan tangkai tidak akan terjadi penyebaran getah. Getah ini diperkirakan akan mempercepat kerusakan buah dan mendorong terjadinya stem end rot dan akan mengotori permukaan. Dalam tahap pemanenan buah tidak boleh dilempar untuk mengurangi kerusakan akibat memar. Waktu petik disarankan adalah pada pagi hari yaitu pada pukul 07.00-08.00 WIB, tetapi pada beberapa daerah tertentu, waktu petik lebih disesuaikan pada budaya serta kebiasaan daerah setempat. Setelah pemetikan sebaiknya buah jangan langsung terkena sinar matahari, karena akan mempercepat kerusakan buah.
B.
DEHIDRASI OSMOTIK
6
Menurut Lenart 1996, dehidrasi osmotik merupakan salah satu metode pengawetan bahan pangan menggunakan tekanan osmotik untuk mengeluarkan sebagaian kandungan air pada bahan. Dehidrasi osmosik dapat digunakan untuk perlakuan awal sebelum proses pengeringan yang dapat menurunkan kadar air bahan sampai 50% dari kadar air awal (Khan et al. 2008). Pada dehidrasi osmotik, bahan pangan direndam ke dalam media osmosis yang memiliki tekanan osmotik lebih tinggi dari tekanan osmotik bahan, sehingga air dari dalam bahan akan keluar ke arah media untuk menyeimbangkan tekanan osmotik. Sebagai akibat pengeluaran air dari dalam bahan tanpa perubahan fase cairan, maka proses dehidrasi osmotik dianggap sebagai metode pengawetan bahan pangan dan hasil pertanian yang menghasilkan mutu tinggi.Pemilihan jenis dan konsentrasi solut dalam larutan osmotik dipengaruhi oleh beberapa faktor, misalnya pengaruhnya terhadap kualitas organoleptik, rasa, kemampuan untuk mengurangi aktifitas air, kelarutan solut, permeabilitas solut terhadap membran sel dan kemampuan mengawetkan. Dua jenis solut yang paling umum digunakan adalah gula (sukrosa) dan NaCl.
Gula sering digunakan dalam pengawetan buah-buahan. Apabila gula ditambahkan ke dalam bahan pangan dengan konsentrasi yang tinggi (>40% padatan terlarut), air yang tersedia untuk pertumbuhan mikroorganisme akan berkurang. Menurut Buckle et al. (1985) diacu dalam Lutfi (2010) apabila gula ditambahkan ke dalam bahan pangan dalam konsentrasi tinggi minimun 40% padatan terlarut, menyebabkan sebagian air yang ada menjadi tidak tersedia untuk pertumbuhan mikroorganisme dan aktivitas air (aw) bahan pangan akan berkurang. Konsentrasi gula yang tinggi (sampai 70%) sudah dapat menghambat pertumbuhan mikroba perusak makanan.
Kinetika dehidrasi osmotik ditentukan berdasarkan kecepatan water loss (WL) dan solid gain (SG). Water loss (WL) didefinisikan sebagai pengurangan berat air netto pada produk dehidrasi osmotik berdasarkan berat bahan mula-mula. Solid gain (SG) adalah penambahan berat solid netto pada produk dehidrasi osmotik berdasarkan berat bahan mula-mula. Dehidrasi buah mangga dapat dilakukan dengan metode osmotik pada tahap awal, yakni merendan daging buah mangga ke dalam larutan gula pada konsentrasi dan jangka waktu tertentu. Setelah itu, dikeringkan pada suhu 45-55°C dan kelembaban nisbi yang rendah. Metode dehidrasi tersebut terbukti mampu memberikan hasil buah kering yang awet dengan kadar air sekitar 14%, sehingga kerusakan kimiawi, biologis, dan enzimatis dapat dihindari. Perendaman irisan daging buah mangga kweni kedalam larutan gula 60°Brix selama 10 jam, kemudian dikeringkan pada suhu 55°C dan kelembaban (RH) 60% selama 9 jam menghasilkan manisan mangga kweni kering, berpenampilan menarik, warna kuning merata, manis, dan memiliki kadar air optimum 14.4% (Broto 2003).
Potongan mangga kering yang memiliki kualitas paling baik adalah potongan mangga dengan perlakuan osmotik tanpa kitosan karena penyusutan potongan mangga dengan perlakuan osmotik lebih kecil dibandingkan potongan mangga segar selama dehidrasi. Selain itu dengan adanya perlakuan osmotik sebelum dehidrasi menyebabkan potongan mangga dapat mempertahankan warna alaminya selama dehidrasi, walaupun warna dehidrasi mangga selama perlakuan menjadi lebih tua/ matang (Sophia 2011).
Semakin tinggi nilai water loss maka menunjukkan tingkat tingginya kehilangan air pada sampel. Sedangkan nilai solid gain merupakan parameter yang menunjukkan banyaknya jumlah padatan terlarut yang masuk ke dalam sampel. Kecepatan keluarnya air dari padatan dipengaruhi oleh beberapa faktor antara lain konsentasi larutan osmotik, waktu perendaman, rasio larutan osmotik/solid, suhu, intensitas pengadukan dan ukuran (Soetjipto Reynaldy et al, 2005).
7
larutan osmotik dapat meningkatkan water loss dan solid gain sampai batas tertentu. Sebagai contoh, konsentrasi larutan gula sekitar 60oBx paling sesuai digunakan untuk dehidrasi osmotik. Ertekin 2000 melaporkan bahwa penggunaan larutan osmotik 66oBx menghasilkan kenaikan water loss dan solid gain yang hampir sama dengan penggunaan larutan osmotik 60oBx.C.
PENGADUKAN DAN PENCAMPURAN
Pengadukan (agitation) merupakan suatu aktivitas operasi pencampuran dua atau lebih zat agar diperoleh hasil campuran yang homogen dan menciptakan gerakan dari bahan yang diaduk seperti molekul-molekul, zat-zat yang bergerak atau komponennya menyebar (terdispersi).
Tujuan dari pengadukan adalah:
Mencampur dua cairan yang saling melarut
Melarutkan padatan dalam cairan
Mendispersikan gas dalam cairan dalam bentuk gelembung
Untuk mempercepat perpindahan panas antara fluida dan dinding bejana
Pencampuran adalah operasi yang menyebabkan tersebarnya secara acak suatu bahan yang lain dimana bahan-bahan tersebut terpisah dalam dua fasa atau lebih. Proses pencampuran bisa dilakukan dalam sebuah tangki berpengaduk. Hal ini dikarenakan faktor-faktor penting yang berkaitan dengan proses ini, dalam aplikasi nyata bisa dipelajari dengan seksama dalam alat ini. Pada dasarnya pencampuran mencakup dua faktor kunci yaitu peralatan yang digunakan dan bahan yang akan dicampur. Kedua faktor tersebut harus memiliki hubungan yang erat untuk memperoleh hasil pencampuran yang baik. Geometri peralatan dapat mempengaruhi produksi secara umum, kondisi operasi proses khususnya aerasi dan pengadukan serta konsumsi energi (Sailah 1994)
Bentuk pengaduk berpengaruh terhadap pola aliran yang dihasilkannya. Berdasarkan pola aliran yang dihasilkan, pengaduk dapat dibagi menjadi empat jenis yaitu menghasilkan pola aliran radial, axial, laminar dan turbulen. Aliran radial yaitu aliran mendatar dari blade pengaduuk ke dinding vessel (tangki) dan membentuk dua daerah, yaitu daerah atas dan daerah bawah. Sedangkan aliran axial adalah aliran vertikal ke atas dan bawah pengaduk. Pola aliran yang dihasilkan juga dipengaruhi oleh sifat reologi dari bahan yang diaduk (Sailah 1993). Pola aliran laminar adalah pola aliran yang mengalir dalam lapisan dan alirannya tenang (Hudges dan Brighton 1967). Aliran turbulen adalah aliran yang bersifat bergejolak (Earle 1969).
Pada proses pencampuran, salah satu sifat bahan yang sangat penting untuk dipertimbangkan adalah sifat reologi bahan. Reologi menurut Mackay (1988) adalah ilmu tentang sifat aliran suatu bahan. Menurut sifat reologinya, fluida dapat dibagi menjadi dua golongan besar, yaitu Newtonian dan fluida non-Newtonian. Pada fluida Newtonian, nilai kekentalan adalah konstan dan tidak dipengaruhi oleh nilai laju geser, tetapi dipengaruhi oleh suhu dan tekanan. Sedangkan fluida non-Newtonian, nilai kekentalan merupakan fungsi dari laju geser.
Pola aliran pada suatu tangki berpengaduk sangat dipengaruhi oleh kecepatan pengaduk, jenis pengaduk dan sifat reologi bahan yang diaduk (Ranade dan Joshi 1990). Meskipun dengan fluida dan kecepatan pengadukan yang sama, penggunaan pengaduk yang berbeda akan menghasilkan pola aliran yang berbeda pula.
Menurut aliran yang dihasilkan, pengaduk dapat dibagi menjadi tiga golongan:
1. Pengaduk aliran aksial yang akan menimbulkan aliran yang sejajar dengan sumbu putaran. 2. Pengaduk aliran radial yang akan menimbulkan aliran yang berarah tangensial dan radial
8
vortex dan terjadinya pusaran, dan dapat dihilangkan dengan pemasangan baffle atau cruciform baffle.3. Pengaduk aliran campuran yang merupakan gabungan dari kedua jenis pengaduk di atas. Pengadukan mekanis adalah metoda pengadukan menggunakan peralatan mekanis yang terdiri atas motor, poros pengaduk (shaft) dan alat pengaduk (impeller). Peralatan tersebut digerakkan dengan motor bertenaga listrik. Pemilihan pengaduk yang tepat menjadi salah satu faktor penting dalam menghasilkan proses dan pencampuran yang efektif. Menurut Mc Cabe 1993, berdasarkan bentuk pengaduk dapat dibagi menjadi 3 golongan:
1. Propeller
Kelompok ini biasa digunakan untuk kecepatan pengadukan tinggi dengan arah aliran aksial. Pengaduk ini dapat digunakan untuk cairan yang memiliki viskositas rendah dan tidak bergantung pada ukuran serta bentuk tangki. Kapasitas sirkulasi yang dihasilkan besar dan sensitif terhadap beban head.
Pengaduk propeller menimbulkan arah aksial, arus aliran meninggalkan pengaduk secara kontinu melewati fluida ke satu arah tertentu sampai dibelokkan oleh dinding atau dasar tangki (Gambar 3).
2. Turbine
Istilah turbine ini diberikan bagi berbagai macam jenis pengaduk tanpa memandang rancangan, arah discharge ataupun karakteristik aliran. Turbine merupakan pengaduk dengan sudu tegak datar dan bersudut konstan (Gambar 4). Pengaduk jenis ini digunakan pada viskositas fluida rendah halnya pengaduk jenis propeller (Uhl dan Gray 1966). Pengaduk turbin menimbulkan aliran arah radial dan tangensial. Di sekitar turbin terjadi daerah turbulensi yang kuat, arus dan geseran yang kuat antar fluida.
Salah satu jenis pengaduk turbine adalah pitched blade. Pengaduk jenis ini memiliki sudut sudu konstan. Aliran terjadi pada arah aksial, meski demikian terdapat pola aliran pada arah radial. Aliran ini akan mendominasi jika sudu berada dekat dengan dasar tangki.
3. Paddles
Pengaduk jenis ini sering memegang peranan penting pada proses pencampuran dalam industri. Bentuk pengaduk ini memiliki minimum 2 sudu, horizontal atau vertical, dengan nilai D/T yang tinggi (Gambar 5). Paddle digunakan pada aliran fluida laminar, transisi atau turbulen tanpa baffle.
Pengaduk paddle menimbulkan aliran arah radial dan tangensial dan hampir tanpa gerak vertikal sama sekali. Arus yang bergerak ke arah horisontal setelah mencapai dinding akan dibelokkan ke atas atau ke bawah. Bila digunakan pada kecepatan tinggi akan terjadi pusaran saja tanpa terjadi agitasi.
(a) (b) (c) Gambar 2. Bentuk–bentuk pengaduk
9
Disamping itu masih ada bentuk–bentuk pengaduk lain yang biasanya merupakan modifikasi dari ketiga bentuk di atas.(a) (b) (c) Gambar 3. Tipe-tipe pengaduk jenis turbine
(a) (b) (c) Gambar 4. Tipe-tipe pengaduk jenis propeller
(a) (b) (c) Gambar 5. Tipe-tipe pengaduk jenis paddle
Salah satu variasi dasar dalam proses pengadukan dan pencampuran adalah kecepatan putaran pengaduk yang digunakan. Variasi kecepatan putaran pengaduk bisa memberikan gambaran mengenai pola aliran yang dihasilkan dan daya listrik yang dibutuhkan dalam proses pengadukan dan pencampuran. Secara umum klasifikasi kecepatan putaran pengaduk dibagi tiga, yaitu : kecepatan putaran rendah, sedang dan tinggi. Menurut Soetjipto Reynaldy 2005, dengan penggunaan diameter tangki larutan sebesar 20 cm dan tinggi tangki sebesar 28 cm maka kecepatan pengadukan rendah yang digunakan sebesar 100 rpm, kecepatan pengadukan sedang sebesar 500 rpm dan kecepatan pengadukan tinggi sebesar 1000 rpm, akan mempengaruhi perbedaan kecepatan pengadukan dapat mempengaruhi nilai water loss dan solid gain.
Fluida adalah suatu zat yang mempunyai kemampuan berubah secara kontinu apabila mengalami geseran, atau mempunyai reaksi terhadap tegangan geser sekecil apapun. Dalam keadaan diam atau dalam keadaan keseimbangan, fluida tidak mampu menahan gaya geser yang bekerja padanya, oleh sebab itu fluida mudah berubah bentuk tanpa pemisahan massa.
Faktor-faktor yang memengaruhi proses pengadukan dan pencampuran diantaranya adalah perbandingan antara geometri tangki dengan geometri pengaduk, bentuk dan jumlah pengaduk, posisi sumbu pengaduk, kecepatan putaran pengaduk, penggunaan sekat dalam tangki dan juga properti fisik fluida yang diaduk yaitu densitas dan viskositas.
a. Flate Blade b. Curved Blade c. Pitched Blade
a. Standard three blades b. Weedless c. Guarded
10
Menurut Setiawan 2008, density atau rapat jenis (ρ) suatu zat adalah ukuran untuk konsentrasi zat tersebut dan dinyatakan dalam massa persatuan volume. Sifat ini ditentukan dengan cara menghitung nisbah (rasio) massa zat yang terkandung dalam suatu bagian tertentu terhadap volume bagian tersebut. Hubungannya dapat dinyatakan pada persamaan (1)=
� (1)Dimana: m = massa fluida (kg) v = volume fluida (m3)
Viskositas adalah suatu pernyataan “tahanan untuk mengalir” dari suatu sistem yang mendapatkan suatu tekanan. Makin kental suatu cairan, makin besar gaya yang dibutuhkan untuk membuatnya mengalir pada kecepatan tertentu. Viskositas dispersi kolodial dipengaruhi oleh bentuk partikel dari fase dispers. Koloid-koloid berbentuk bola membentuk sistem dispersi dengan viskositas rendah, sedang sistem dispersi yang mengandung koloid-koloid linier viskositasnya lebih tinggi. Hubungan antara bentuk dan viskositas merupakan refleksi derajat solvasi dan partikel (Moechtar 1990). Bila viskositas gas meningkat dengan naiknya temperatur, maka viskositas cairan justru akan menurun jika temperatur dinaikkan. Fluiditas dari suatu cairan yang merupakan kebalikan dari viskositas akan meningkat dengan makin tinggi temperatur (Martin 1993). Menurut Setiawan 2008, Viskositas dinyatakan dalam dua bentuk, yaitu:
Viskositas dinamik
Viskositas dinamik adalah perbandingan tegangan geser dengan laju perubahannya, besarnya nilai viskositas dinamik tergantung dari faktor-faktor diatas tersebut, untuk viskositas dinamik air pada temperatur standar lingkungan (27oC) adalah 8.6 x 10-4 kg/ms. Persamaan viskositas dinamik dapat dilihat pada persamaan (2)
�
=
��=
�
∆�∆ (2)Dimana: � = tegangan geser (N/m2) F = gaya geser (N) A = luas permukaan (m2) v = kecepatan (m/s) y = jarak vertikal (m) � = viskositas dinamik (Pa.s)
Viskositas kinematik
Viskositas kinematik merupakan perbandingan viskositas dinamik terhadap kerapatan (density) massa jenis dari fluida tersebut. Viskositas kinematik ini terdapat dalam beberapa penerapan antara lain dalam bilangan Reynolds yang merupakan bilangan tak berdimensi, nilai viskositas kinematik air pada temperatur standar (27oC) adalah 8.7 x 10-7m2/s. Persamaan viskositas kinematik dapat dilihat pada persamaan (3)
�
=
� (3)Dimana: v = viskositas kinematik (m2/s) � = viskositas dinamik (Pa.s)
= massa jenis (kg/m3)
Bilangan Reynolds pada tangki berpengaduk
11
bilangan Reynolds-nya dengan menggunakan persamaan (8). Dimana, N adalah putaran/menit, d adalah diameter impeler dan v adalah viskositas kinematis larutan. Dalam sistem pengadukan terdapat 3 jenis bentuk aliran yaitu laminer, transisi dan turbulen. Bentuk aliran laminer terjadi pada bilangan Reynolds kurang dari 2100, sedangkan aliran turbulen terjadi pada bilangan Reynolds lebih dari 4000 dan aliran transisi berada diantara keduanya. Pengadukan dengan aliran turbulen menghasilkan water loss lebih tinggi daripada aliran laminar. Namun untuk solid gain, pada aliran turbulen maupun laminar tidak menunjukkan perbedaan yang signifikan (Soetjiptoet al
. 2005).
D.
DAYA LISTRIK DAN DAYA MEKANIK PADA MOTOR DC
Motor DC (Direct Current)
Meskipun energi tidak dapat diciptakan atau dihancurkan, akan tetapi energi dapat diubah dari satu bentuk ke bentuk lain tanpa ada yang hilang. Saat mesin mengalami perubahan energi dari satu bentuk ke bentuk lainnya, maka akan terjadi kehilangan energi atau daya tertentu. Motor mengubah energi listrik menjadi energi mekanik untuk melayani beban tertentu. Motor listrik pengaduk larutan dapat menggunakan listrik arus searah atau DC (Direct Current) ialah aliran arus yang keluarannya tetap atau konstan terhadap waktu. Arus searah merupakan arus negatif atau elektron yang mengalir dari kutub negatif ke kutub positif. Sumber listrik dari arus searah ini biasanya dari batu baterai, accumulator atau hasil proses dari photovoltaic atau tenaga surya. Akan tetapi, sumber listik arus searah dari motor listrik juga bisa diperoleh langsung dari PLN yang memiliki listrik arus bolak balik (AC). Untuk mengubah arus AC ke DC biasa digunakan adaptor AC-DC converter, sehingga dalam penggunaannya akan lebih mudah.
Gambar 6. Motor losses (US DOE)
Gambar 7. Grafik karakteristik motor DC (Tsukasa Electric 2012) Motor Losses
Load
12
Pada proses ini, kehilangan energi ditunjukkan dalam Gambar 6. Efisiensi motor ditentukan oleh kehilangan dasar yang dapat dikurangi hanya oleh perubahan pada rancangan motor dan kondisi operasi. Kehilangan dapat bervariasi, mulai dari kurang lebih dua persen hingga 20 persen.Kehilangan energi atau daya itu akan menyebabkan peningkatan suhu dan menurunkan efisiensi dari mesin. Kehilangan energi atau daya ini sangat penting karena akan memberikan petunjuk mengenai bagaimana mereka dapat berkurang. Efisiensi motor dapat didefinisikan sebagai perbandingan antara daya output dengan daya inputnya. Faktor-faktor yang mempengaruhi efisiensi adalah usia, kapasitas motor, kecepatan motor, jenis motor dan suhu (US DOE).Hubungan antara torsi, kecepatan putar dan arus listrikadalah linier seperti yang ditunjukkan pada Gambar 7, saat beban kerja motor meningkat maka kecepatan putaran motor akan berkurang. Grafik pada Gambar 7 ini mewakili berbagai tipe karakteristik motor DC. Selama motor bekerja, daerah dengan efisiensi tinggi (daerah yang diarsir) memiliki kinerja yang lebih baik dan motor menjadi lebih tahan lama. Namun dengan menggunakan motor di luar daerah arsiran tersebut suhu dari motor akan meningkat sehingga dapat terjadi kerusakan pada motor. Gambar 7 menunjukkan saat di bawah kecepatan putaran tertentu, efisiensi motor DC tidak berubah terhadap kecepatan putar tetapi berubah terhadap torsi, sehingga hubungan antara kecepatan putar dan efisiensi adalah linier.
Komponen motor listrik dapat dibagi menjadi dua kelompok, yaitu bagian motor yang berputar (rotor, stator, generator dan lainnya) dan bagian motor yang tidak berputar (transformator, reaktor dan lainnya). Pada mesin yang berputar kehilangan energi terjadi pada daya input (daya listrik) dan daya output (daya mekanik), sedangkan pada mesin stasioner atau diam mengalami kehilangan energi hanya pada daya input atau daya listrik (TAFE Queensland 2008).
Daya Listrik (Input Power)
Daya masukan merupakan energi input atau daya input yang terdapat pada motor listrik atau mesin listrik. Pada motor listrik, masukannya berupa energi listrik, generator masukannya berupa energi mekanik, dalam baterai masukannya berupa energi kimia dan termokopel masukannya berupa energi panas. Daya listrik didefinisikan sebagai laju hantaran energi listrik dalam sirkuit listrik. Satuan SI daya listrik adalah watt yang menyatakan banyaknya tenaga listrik yang mengalir per satuan waktu (joule/detik). Arus listrik yang mengalir dalam rangkaian dengan hambatan listrik menimbulkan kerja. Peranti mengkonversi kerja ini ke dalam berbagai bentuk yang berguna, seperti panas (pemanas listrik), cahaya (pada bola lampu), energi kinetik (motor listrik) dan suara (loudspeaker). Pengukuran daya listrik dapat dilihat pada persamaan (10). Masukan daya listrik pada motor listrik dapat ditentukan apabila aliran arus dan tegangannya dapat diketahui (TAFE Queensland 2008).
Daya Mekanik (Output Power)
Daya keluaran merupakan energi output atau daya output yang terdapat pada suatu mesin. Hasil output dari motor listrik berupa energi mekanik, output dari generator berupa energi listrik, output dari baterai dan termokopel juga berupa energi listrik. Daya keluaran motor atau daya mekanik merupakan daya yang disalurkan melalui poros output motor. Daya mekanik dari motor listrik dapat dilihat pada persamaan (4). Daya mekanik atau daya output dari motor tergantung pada kecepatan rotasi dan torsi yang dihasilkan (TAFE Queensland 2008).
�
=
2 ��60 (4)
Dimana: P = daya mekanik (Watt) T = torque (Nm)
13
III.
METODOLOGI PENELITIAN
A.
WAKTU DAN LOKASI PENELITIAN
Penelitian ini dilaksanakan mulai bulan Februari 2012 sampai dengan Juni 2012 di Laboratorium Energi dan Elektrifikasi Pertanian, Departemen Teknik Mesin dan Biosistem, Fakultas Teknologi Pertanian, Institut Pertanian Bogor.
B.
ALAT DAN BAHAN
a. Alat
1) Osmotic Dehydrator
Komponen dari osmotic dehydrator yang digunakan berupa dua panci terbuat dari stainless steel merupakan baja tahan karat. Panci utama yang berfungsi sebagai penyalur panas ke sampel telah dirangkai satu dengan elemen pemanas (heater). Sedangkan panci yang lain digunakan sebagai wadah sampel dan larutan osmotik ini dirangkai satu dengan elemen termostat dan pengaduk (stirer). Heater yang digunakan sebanyak 2 unit dengan daya masing-masing sebesar 1000 Watt. Termostat berfungsi mengontrol suhu larutan osmotik agar konstan selama pengukuran, selain itu untuk memastikan suhunya konstan digunakan satu buah termometer. Stirer digunakan untuk menggerakkan/mengaduk larutan osmotik agar panas yang diberikan merata ke dalam wadah sampel. Stirer digerakkan oleh motor DC yang disambungkan ke adaptor pengubah tegangan, sehingga kecepatan putar pengaduk dapat diubah menjadi 100 rpm, 300 rpm dan 500 rpm. Foto dan skema alat dapat dilihat pada Gambar 2 dan Lampiran 18.
2) Refraktometer merk Atago model N1 dan K Fuji 13978 3) Pisau
4) Kertas saring / tissue 5) Timbangan digital 6) Stopwatch 7) Gelas ukur
8) Jangka sorong/mistar
9) Drying oven, cawan, tray, dan penjepit cawan 10)Desikator
11)Termometer 12)Tachometer 13)Voltmeter 14)Ampermeter
b.Bahan
14
C.
PROSEDUR PENELITIAN
1. Pembuatan Larutan Osmotik
Larutan osmotik yang digunakan adalah campuran dari larutan gula dan aquades. Konsentrasi larutan osmotik yang akan digunakan pada penelitian adalah 61oBx. Pembuatan konsentrasi larutan osmotik ini berdasarkan rasio perbandingan antara massa gula dengan massa pelarut (air). Untuk pembuatan larutan gula 61oBx, membutuhkan gula putih sebanyak 3.84 kg dilarutkan dalam 2500 ml air. Kemudian diukur kadar TPT (Total Padatan Terlarut) dengan menggunakan refraktometer. Meskipun dengan penggunaan rasio, konsentrasi larutan yang diinginkan tidak sesuai karena gula di pasaran tidak murni dan kadar air masih tinggi. Apabila angka refraktometer menunjukkan < 61oBx maka ditambahkan gula ke dalam larutan, dan sebaliknya ditambah aquades apabila angka menunjukkan > 61oBx.
2. Prosedur Penelitian Dehidrasi Osmotik
Langkah kerja dalam dehidrasi osmotik adalah sebagai berikut:
a. Mangga dicuci, dibersihkan, dikupas kulitnya, dan dipotong dengan ukuran 3 cm x 3 cm x 1 cm. b. Mengambil enam sampel secara acak untuk mengetahui berat awal dan kadar air awal
c. Tiga sampel diambil untuk dimasukkan ke dalam osmotic dehydrator dan tiga lainnya dimasukkan ke dalam oven untuk pengukuran kadar air awal.
d. Larutan osmotik dimasukkan ke dalam heater. Konsentrasi larutan osmotik diukur dengan menggunakan refraktometer sebesar 61oBx. Kemudian larutan osmotik dipanaskan di dalam heater sesuai dengan suhu perlakuan yaitu 30oC, 40o C dan 50oC.
e. Mengatur kecepatan pengadukan larutan osmotik yaitu dengan kecepatan 100 rpm (kecepatan rendah), 300 rpm (kecepatan sedang) atau 500 rpm (kecepatan tinggi).
f. Wadah yang berisi sampel dimasukkan ke dalam heater yang telah terisi oleh larutan osmotik dengan perbandingan berat 1 : 3 (sampel : larutan), kisaran sampel 700 gram dan larutan osmotik sebanyak 2000 ml.
g. Mengamati perubahan konsentrasi larutan osmotik menggunakan refraktometer dan mengamati perubahan kecepatan pengadukan selama 8 jam. Selang waktu yang digunakan adalah menit ke 0, 15, 30, 45, 60, 90, 120, 150, 180, 240, 300, 360, 420, dan 480.
15
D.
RANCANGAN PENELITIAN
Rancangan penelitian ini dilakukan menggunakan rancangan faktorial dengan 2 perlakuan yang masing-masing memiliki 3 taraf perlakuan. Jadi, dari kedua jenis perlakuan yang berbeda diperoleh 9 kombinasi perlakuan yang terdapat pada Tabel 3 . Sedangkan diagram alir dapat dilihat pada Gambar 9.
Perlakuan yang digunakan dalam penelitian terdiri dari : Perlakuan 1 : T1 = suhu larutan osmotik 30o C
T2 = suhu larutan osmotik 40o C T3 = suhu larutan osmotik 50o C
Perlakuan 2 : K1 = kecepatan pengadukan rendah (100 rpm) K2 = kecepatan pengadukan sedang (300 rpm) K3 = kecepatan pengadukan tinggi (500 rpm)
Tabel 3. Jenis dan kombinasi perlakuan Perlakuan
Notasi Perlakuan Suhu Larutan Kecepatan Pengadukan
30o C Rendah (100 rpm) T1K1
Sedang (300 rpm) T1K2
Tinggi (500 rpm) T1K3
40oC Rendah (100 rpm) T2K1
Sedang (300 rpm) T2K2
Tinggi (500 rpm) T2K3
50oC Rendah (100 rpm) T3K1
Sedang (300 rpm) T3K2
Tinggi (500 rpm) T3K3
16
Gambar 9. Diagram alir rancangan penelitianMulai
Penentuan sample buah mangga Indramayu
Penentuan suhu dan kecepatan pengadukan Persiapan alat dan bahan penelitian
Penentuan potongan mangga dengan ukuran
3cm x 3cm x 1cm
Pembuatan larutan gula 61o Bx
Pengambilan 6 sampel acak Penentuan perbandingan
larutan osmotik dengan berat sampel (1:3)
3 sampel untuk pengukuran kadar air awal
3 sampel untuk pengukuran berat awal (Dehidrasi Osmotik)
Pengukuran setelah perlakuan 1. Berat akhir sampel
2. Kadar air akhir.
Analisis data penelitian Pengukuran konsentrasi larutan
osmotik selang waktu tertentu
Perhitungan WL dan SG berdasarkan pengukuran
Perhitungan bilangan Reynolds dan bilangan Power
Selesai
o
40ºC, 61 ºBx
Kecepatan pengadukan rendah, sedang dan tinggi 30ºC, 61 ºBx
Kecepatan pengadukan rendah, sedang dan Tinggi
50ºC, 61 ºBx
17
E.
PENGAMATAN
Pengamatan yang dilakukan terdiri atas:
1. Kadar Air Metode Oven
Langkah awal dalam pengukuran kadar air sampel (potongan buah mangga) yaitu dengan mengeringkan cawan kosong di dalam oven bersuhu 105oC selama ±15 menit kemudian didinginkan dalam desikator dan ditimbang. Sampel sejumlah a gram dimasukkan ke dalam cawan tersebut dan dikeringkan di dalam oven bersuhu 105oC sampai perubahan massa tidak terjadi lagi. Setelah perubahan massa tidak terjadi lagi sampel dikeluarkan dari oven dan didinginkan di dalam desikator dan ditimbang. Perbedaan berat sampel sebelum dan sesudah dehidrasi osmotik dihitung sebagai persen kadar air dapat dilihat pada persamaan (5)
� � �� % = − 100% (5)
Dimana: a = berat sampel sebelum dikeringkan (g) b = berat sampel setelah dikeringkan (g)
2. Water Loss (WL) dan Solid Gain (SG)
Water loss didefinisikan sebagai pengurangan jumlah air yang terdapat di dalam sampel setelah dilakukan proses dehidrasi osmotik. Sedangkan solid gain merupakan penambahan berat sampel setelah dehidrasi osmotik berdasarkan berat sampel awal atau banyaknya sampel yang masuk ke dalam sampel. Berdasarkan Souza et al. (2007) untuk mengetahui besarnya WL dapat dihitung dengan menggunakan persamaan (6), sedangkan untuk mengetahui SG dapat dihitung dengan menggunakan persamaan (7). Perhitungan water loss dan solid gain dilakukan sebanyak tiga kali ulangan. Untuk mendapatkan nilai water loss dan solid gain sampel yang akan diukur adalah massa sampel sebelum dan sesudah proses dehidrasi osmotik selama 8 jam serta nilai kadar air awal dan kadar air akhir sampel.
WLt= (m0- mt �0) (6)
SGt = �100− � − 0(100− 0)
0 (7)
Dimana: W0= berat awal sampel (g)
Wt= berat sampel pada waktu t (g)
m0= Kadar air awal sampel (%bb)
mt= Kadar air sampel pada waktu t (%bb)
3. Bilangan Reynolds dan Bilangan Power
18
�
=
��2� (8)Dimana : Re = bilangan Reynolds = densitas fluida (kg/m3) � = visikositas fluida (kg/ms) D = diameter impeler (m)
N = kecepatan pengadukan (putaran/detik)
Viskositas dan densitas larutan osmotik ditentukan berdasarkan suhu yang diberikan dan setiap penurunan konsentrasi larutan osmotik pada kecepatan putar pengadukan yang berbeda. Viskositas dan densitas larutan osmotik didapatkan dengan menggunakan aplikasi online Sugar Engineers.
Menurut Foucault 2012, bilangan tidak berdimensi yang biasa digunakan untuk menghitung power (daya) atau tenaga yang dibutuhkan pada percobaan yang akan dilaksanakan yaitu bilangan power. Secara matematis dapat ditulis pada persamaan (9)
�
�0=
�3�5(9)
Dimana : NPo = bilangan power P = daya masukan motor D = diameter pengaduk
n = kecepatan putaran pengaduk ρ = densitas
Pada persamaan (9), seharusnya daya yang digunakan adalah daya keluaran atau daya mekanik dari motor, akan tetapi pada penelitian ini daya yang digunakan adalah daya masukan atau daya listrik motor, karena pada penelitian ini daya keluaran dari motor DC tidak dilakukan pengukuran. Berdasarkan Gambar 7 saat rpm rendah di atas torsi tertentu, efisiensi motor DC tidak berubah terhadap kecepatan putar motor, sehingga hubungan antara daya keluaran dengan daya masukan motor DC adalah linier.
4. Daya Listrik
Pengukuran tegangan listrik dan arus listrik dilakukan pada tiga kali kecepatan putar pengaduk yang berbeda (100 rpm, 300 rpm dan 500 rpm). Setiap penurunan konsentrasi larutan osmotik dilakukan pengukuran menggunakan voltmeter dan ampermeter sebanyak tiga kali ulangan, daya listrik dapat dihitung dengan menggunakan persamaan (10).
�
=
�
(10)Dimana : P = daya listrik dalam satuan Watt (W) V = tegangan listrik dalam satuan Volt (V) I = arus listrik dalam satuan Ampere (A)
19
secara seri ke ampermeter, sedangkan kabel negatif disambungkan langsung ke adaptor AC-DC Adaptor AC-DC (Gambar 11b) ini berfungsi sebagai pengubah arus bolak-balik (AC) dari sumber PLN menjadi arus searah (DC). Tujuan dari mengubah jenis arus ini agar mempermudah dalam mengatur tegangan listrik yang diinginkan, sehingga kecepatan pengadukan dapat diatur putarannya (putaran rendah, sedang dan tinggi). Untuk pengukuran tegangan listrik dengan menyambungkan langsung kabel postif dan negatif dari voltmeter ke adaptor AC-DC. Pengukuran akan dilakukan saat pengaduk berputar, sehingga arus listrik akan terbaca pada ampermeter dan tegangan akan terbaca pada voltmeter.Untuk pengukuran daya listrik saat proses dehidrasi osmotik selama 8 jam menggunakan model persamaan yang paling baik (power fit model) dengan menggunakan software curve expert 1.4. Model persamaan tersebut berdasarkan pendekatan rumus dari persamaan 6, dimana nilai bilangan Reynolds dan bilangan Power diperoleh saat pengukuran daya saja dengan menggunakan sampel mangga tanpa memperhitungkan waktu selama proses dehidrasi osmotik. Persamaan tersebut dapat dilihat pada persamaan (11).
�
�=
�
(11)Dimana : a dan b = konstanta Npo = bilangan Power Re = bilangan Reynolds
Gambar 10. Skema pengukuran arus dan tegangan listrik motor DC
(a) (b)
Gambar 11. (a). Multimeter (b) Adaptor AC-DC Ampermeter
Voltmeter Adaptor AC-DC
[image:34.595.105.515.68.791.2]20
IV.
HASIL DAN PEMBAHASAN
A.
KADAR AIR
[image:35.595.108.512.162.769.2]Sampel buah mangga diukur kadar airnya saat sebelum dehidrasi osmotik dan setelah dilakukan dehidrasi osmotik. Untuk pengukuran kadar air akhir sampel dengan cara menimbang berat awal sampel sebelum dimasukkan ke osmotic dehydrator dan menimbang berat akhir sampel setelah dimasukkan ke osmotic dehydrator. Kadar air awal sampel berkisar antara 82.50 %bb sampai 90.79 %bb untuk masing-masing perlakuan. Kadar air akhir sampel mengalami penurunan setelah sampel dimasukkan ke larutan gula selama 8 jam, hal ini diakibatkan karena terjadinya perbedaan tekanan osmotik antara zat terlarut yaitu gula dan zat pelarut air dari dalam sampel. Air dari sampel yang memiliki konsentrasi zat yang lebih rendah akan cenderung berdifusi keluar melalui membran ke konsentrasi yang lebih tinggi yaitu larutan gula. Penurunan massa air ini akan berlangsung secara terus menerus dengan pergerakan air dari sampel yang semakin lambat dan mencapai kondisi kesetimbangan (Jannah, 2011). Pada Gambar 12 menunujukkan kadar air sampel yang diperoleh berbeda-beda berdasarkan masing-masing perlakuan yang dilakukan.
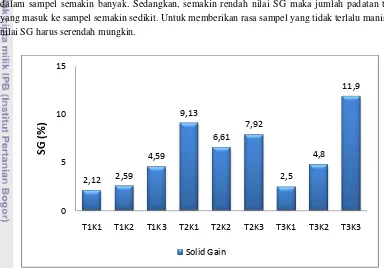
Gambar 12. Kadar air awal dan kadar akhir akhir sampel (dalam basis basah)
Gambar 12 menunjukkan bahwa perlakuan T3K3 (suhu 50 0C dan kecepatan pengadukan tinggi) memiliki kadar air akhir yang paling rendah yaitu sebesar 35.30% bb dan mengalami penurunan kadar air yang paling tinggi dari kadar air awalnya. Sedangkan untuk perlakuan T1K1 (suhu 30 oC dan kecepatan pengadukan rendah) memiliki kadar air akhir yang paling tinggi yaitu sebesar 73.70 % bb.
Penurunan kadar air sampel dipengaruhi oleh kenaikan suhu larutan. Semakin tinggi suhu larutan dapat meningkatkan pindah panas sampel dan meningkatkan pergerakan molekul air. Suhu larutan yang tinggi dapat mempercepat perpindahan massa air dari dalam sampel ke permukaan sampel dan dari permukaan sampel ke larutan gula. Akan tetapi jika suhu yang diberikan terlalu tinggi dapat menyebabkan terjadinya browning pada sampel (Jannah 2011).
Kecepatan pengadukan juga mempengaruhi penurunan kadar air sampel. Pada perlakuan suhu 30oC dengan kecepatan rendah menghasilkan kadar air yang lebih tinggi dibandingkan dengan
0 20 40 60 80 100
K
ad
ar
ai
r (
%
b
b
)
Kadar air awal (%bb)
21
perlakuan dengan kecepatan sedang maupun tinggi. Hal ini juga dapat dilihat pada kecepatan pengadukan perlakuan suhu 40oC dan suhu 50oC. Semakin cepat pengadukan dapat meningkatkan proses laju transfer massa air dari larutan gula yang memiliki konsentrasi zat yang lebih tinggi ke konsentrasi zat yang lebih rendah yaitu ke dalam sampel mangga, menyebabkan penurunan kadar air menjadi lebih cepat dan proses dehidrasi osmotik menjadi lebih merata ke setiap permukaan sampel.B.
WATER LOSS
DAN
SOLID GAIN
Water loss merupakan pengurangan jumlah air yang terdapat dalam sampel setelah terjadinya dehidrasi osmotik. Konsentrasi larutan merupakan salah satu yang mempengaruhi nilai water loss. Semakin tinggi konsentrasi larutan gula yang digunakan maka beda konsentrasi dan tekanan osmotik akan semakin besar. Berdasarkan data pada Gambar 13 nilai WL yang paling tinggi pada perlakuan T3K3 (suhu 50oC dan dengan kecepatan pengadukan tinggi) yaitu sebesar 70.00% sedangkan nilai WL paling rendah terjadi pada perlakuan T1K1 (suhu 30oC dan kecepatan pengadukan rendah) yaitu 59.06%. Dari data tersebut menunjukkan bahwa penurunan kadar air berpengaruh terhadap tingkat kehilangan air pada