ALTERNATIF PENGGUNAAN HIDROGEN
PEROKSIDA PADA TAHAP AKHIR
PROSES PEMUTIHAN PULP
TESIS
OLEH
HASNAH ULIA
047022007/TK
SEKOLAH PASCASARJANA
UNIVERSITAS SUMATERA UTARA
ALTERNATIF PENGGUNAAN HIDROGEN
PEROKSIDA PADA TAHAP AKHIR
PROSES PEMUTIHAN PULP
TESIS
Untuk memperoleh gelar Magister Teknik
dalam Program Studi Magister Teknik Kimia
pada Sekolah Pascasarjana Universitas Sumatera Utara
OLEH
HASNAH ULIA
047022007/TK
SEKOLAH PASCASARJANA
UNIVERSITAS SUMATERA UTARA
Judul Tesis : ALTERNATIF PENGGUNAAN HIDROGEN PEROKSIDA PADA TAHAP AKHIR PROSES PEMUTIHAN PULP.
Nama : Hasnah Ulia
NIM : 047022007
Program Studi : Magister Teknik Kimia
Menyetujui Komisi Pembimbing :
Prof.Dr.Ir. Setiaty Pandia Ketua
Dr.Ir. Rosdanelli Hasibuan, M.T Anggota
Direktur,
Prof.Dr. T. Chairun Nisa B, MSc NIP. 130 535 852
Ketua Prgram Studi,
Prof.Dr.Ir. Setiaty Pandia NIP. 130 372 214
Telah diuji pada
Tanggal
: 05 Desember 2007
___________________________________________________________
PANITIA PENGUJI TESIS
Ketua
: Prof. Dr. Ir. Setiaty Pandia
Anggota
: 1. Dr. Ir. Rosdanelli Hasibuan, M.T
2. Dr. Rumondang Bulan, M.S
3. Dr. Halimatuddahliana, S.T, M.Sc
4.
Drs.
Chairuddin,
M.Sc
RIWAYAT HIDUP
Nama Lengkap : Hasnah Ulia
Tempat, Tanggal Lahir : Nan 7 Tilatang, 15-01-1973
Riwayat Pendidikan, tamat : - SDN Hilir Lama, 1985
- SMPN Magek, 1988
- SMAN Tilatang Kamang, 1991
- Akademi Teknologi Industri Padang (DIII Teknik
Kimia), 1994
- Universitas Sumatera Utara (S1 Teknik Kimia), 1998
Pekerjaan : Dosen Akademi Teknologi Industri Padang
Nomor Induk Pegawai : 090021638
Nama Suami : Sulaiman
Nama Anak : Salman Hadi
Nama Orang Tua
Ayah : Nasrullah
UCAPAN TERIMA KASIH
Puji syukur kehadirat Tuhan Yang Maha Esa atas rahmat yang telah
dilimpahkan sehingga tesis ini dapat diselesaikan.
Ucapan terimakasih yang sebesar-besarnya penulis sampaikan kepada:
1. Bapak Rektor Universitas Sumatera Utara atas kesempatan dan fasilitas yang
diberikan kepada penulis selama mengikuti pendidikan magister.
2. Ibu Direktur Sekolah Pascasarjana Universitas Sumatera Utara atas
kesempatan dan fasilitas yang diberikan kepada penulis selama mengikuti
pendidikan magister.
3. Ibu Prof. Dr. Ir. Setiaty Pandia selaku Ketua Jurusan Magister Teknik Kimia
sekaligus pembimbing yang telah meluangkan waktu dan pemikiran
memberikan petunjuk kepada penulis dalam menyelesaikan tesis ini.
4. Ibu Dr. Ir. Rosdanelli Hasibuan, M.T, selaku anggota komisi pembimbing
yang telah memberikan bimbingan dalam menyelesaikan tesis ini.
5. Bapak Dompak Maruli Siregar, selaku Manager Research and Development
Department di PT. RAPP yang telah berkenan memberikan kesempatan,
fasilitas dan pemikiran dalam menyelesaikan penelitian ini.
6. Pimpinan, para staf, teknisi dan analis R and D Department dan Technical
7. Bapak dan Ibu dosen pembahas yang telah memberikan masukan berharga
dalam penulisan tesis ini.
8. Teman-teman seperjuangan, mahasiswa Magister Teknik Kimia USU yang
telah memberikan semangat dan masukan dalam penelitian dan penulisan tesis
ini.
9. Orang tua, Suami dan anak tercinta yang telah memberikan kesempatan,
dorongan semangat serta doa selama menyelesaikan pendidikan.
Medan, Desember 2007
ALTERNATIF PENGGUNAAN HIDROGEN PEROKSIDA
PADA TAHAP AKHIR PROSES PEMUTIHAN PULP
INTISARI
Efisiensi penggunaan hidrogen peroksida pada tahap akhir proses pemutihan pulp dibandingkan dengan ClO2 dengan menggunakan bahan baku akasia. Parameter uji yang digunakan adalah derajat putih, penurunan derajat putih, viskositas, kekuatan kertas (indeks sobek dan indeks tarik) dan nilai ekonomi. Dilakukan dua urutan tahapan proses pemutihan pulp yaitu: tahap klorin dioksida (D0); tahap ekstraksi (E); tahap klorin dioksida (D1); tahap klorin dioksida (D2) yang disingkat dengan tahapan D0ED1D2, sedangkan tahapan yang kedua adalah tahap klorin dioksida (D0); tahap ekstraksi (E); tahap klorin dioksida (D1); tahap hidrogen peroksida (P) yang disingkat dengan tahapan D0ED1P. Pada tahap hidrogen peroksida (P) dilakukan variasi dosis H2O2 dan temperatur reaksi dengan waktu 180 menit. Proses pemutihan berlangsung dalam plastik tertutup yang berada dalam water bath.
Pada tahap hidrogen peroksida (P) pada temperatur reaksi 75 0C diperoleh derajat putih yang sama dengan tahap klorin dioksida (D2) dengan penambahan dosis H2O2 0,1% (tahap P) dan dosis ClO2 0,2 % (tahap D2), demikian juga dengan penambahan dosis H2O2 0,2% (tahap P) dan dosis ClO2 0,4 % (tahap D2). Viskositas pulp dan penurunan derajat putih tahap hidrogen peroksida (P) lebih lebih rendah daripada tahap klorin dioksida (D2). Sedangkan indeks sobek dan indeks tarik kertas tahap hidrogen peroksida (P) lebih tinggi dari pada pulp tahap klorin dioksida (D2). Biaya bahan kimia pemutih pulp tahap hidrogen peroksida lebih besar 10 % dari pada biaya tahap klorin dioksida (D2).
ALTERNATIVE OF USAGE OF HYDROGEN PEROXIDE
AT FINAL STAGE IN KRAFT PULP BLEACHING
ABSTRACT
E
fficiency of hydrogen peroxide at final stage of pulp bleaching on acacia kraft pulp was compared with chlorine dioxide in terms of brightness, brightness reversion, viscosity, paper strenght (tear and tensile index) and economic point of view. Bleaching was conducted by two bleaching sequences, chlorine dioxide stage (D0); extraxtion stage (E); chlorine dioxide stage (D1); chlorine dioxide stage (D2and chlorine dioxide stage (D0); extraction stage (E); chlorine dioxide stage (D1);
hydrogen peroxide stage (P) ) or D0ED1D2 and D0ED1P. The first sequence was used
as reference. In hydrogen peroxide stage (P) of this sequence, various hydrogen peroxide charges and temperatures were applied with the time of reaction 180 minute. All the stages of bleaching pulp were carried out in sealed polyethylene bags in hot water bath.
Pulp treated in hydrogen peroxide (P) stage at 75 0C obtained brightness which is equal to chlorine dioxide stage(D2) with H2O2 charge 0.1% and ClO2 charge
0.2% and so it is with H2O2 charge 0.2% and ClO2 charge 0.4% (D2). Pulp viscosity
and brightness reversion of peroxide stage (P) were lower than chlorine dioxide stage (D2). Most of the pulp which is treated in hydrogen peroxide (P) stage showed
better paper strenght (tear and tensile index) than chlorine dioxide stage. Bleaching chemical costs of hydrogen peroxide stage 10 % higher than chlorine dioxide stage.
DAFTAR ISI
Halaman
HALAMAN PENGESAHAN...iii
RIWAYAT HIDUP...v
UCAPAN TERIMAKASIH...vi
INTISARI...viii
ABSTRACT... ...ix
DAFTAR ISI ...x
DAFTAR TABEL...xii
DAFTAR GAMBAR...xiii
DAFTAR LAMPIRAN...xv
BAB I. PENDAHULUAN ...1
1.1. Latar Belakang ………... 1
1.2. Rumusan Masalah ………... 3
1.3. Tujuan ………...4
1.4. Ruang Lingkup ………... 4
1.5. Manfaat ………... .5
BAB II. TINJAUAN PUSTAKA ...6
2.1. Pemutihan Pulp Unsur Klorin ………...………6
2.2. Hidrogen Peroksida Sebagai Bahan Pemutih ………...…. .8
2.4. Penurunan Derajat Putih ………. .13
2.5. Variabel Proses ………...17
BAB III. METODOLOGI PENELITIAN ...21
3.1. Lokasi dan Waktu Penelitian ………...21
3.2. Bahan dan Peralatan ………...21
3.3. Prosedur Kerja ………...…22
3.4. Analisis Hasil Percobaan ………...… 26
3.5. Rancangan Percobaan ………... 26
BAB IV. HASIL PERCOBAAN DAN PEMBAHASAN………... 30
4.1. Pemutihan Pulp Tahap D0-E-D1 ………...30
4.2. Pemutihan Pulp Tahap D2 dan P ………... 31
4.2.1. Derajat Putih Pulp ………. ... 31
4.2.2. Penurunan Derajat Putih ………...36
4.2.3. Viskositas Pulp ………... 39
4.2.4. Residu H2O2 ………...… 41
4.2.5. Kekuatan Kertas ………...43
4.2.6. Perbandingan Nilai Ekonomi ………...47
BAB V. KESIMPULAN DAN SARAN ... 50
5.1. Kesimpulan ……….. 50
5.2. Saran ………...51
DAFTAR PUSTAKA ……….... 52
DAFTAR TABEL
Halaman
Tabel 2.1. Metoda Standar Uji Stabilitas Derajat Putih ……… 17
Tabel 2.2. Dosis H2O2 Optimum untuk Berbagai Variasi Dosis H2O2
Dalam Proses Pemutihan Pulp Kraft ………18
Tabel 4.1. Hasil Pemutihan Pulp Tahap D0-E-D1 ……….. 30
Tabel 4.2. Biaya Kebutuhan Bahan Kimia Pemutihan Pulp Tahap D2 dan P …….. .48
Tabel 4.3. Biaya Kebutuhan Bahan Kimia Pemutihan Pulp Tahap D2 dan P
DAFTAR GAMBAR
Halaman
Gambar 2.1. Derajat Putih Pulp dengan Tahapan Pemutihan DEDP
dan DEP dengan Variasi Dosis H2O2 ………..………... 9
Gambar 2.2. Reaksi Anion Perhidroksil dengan Struktur O-Kuinon …………...11
Gambar 2.3. Reaksi Degradasi Selulosa oleh Hidroksil dan Superoksida Radikal..13
Gambar 2.4. Stabilitas Derajat Putih Pulp pada Proses Pemutihan
dengan Urutan Tahap yang Berbeda untuk Pulp Eucalyptus…….….16
Gambar 2.5. Pengaruh Temperatur dan Waktu Reaksi Terhadap
Derajat Putih Pulp Spruce yang diputihkan dengan H2O2………..…20
Gambar 3.1. Blok Diagram Proses Pemutihan Pulp D0-E-D1-D2 …………..…….28
Gambar 3.2. Blok Diagram Proses Pemutihan Pulp D0-E-D1-P ……….……29
Gambar 4.1. Derajat Putih Sampel Pulp Tahap D2 dan P
dengan Derajat Putih yang sama ………... 32
Gambar 4.2a. Pengaruh Dosis H2O2 Terhadap Derajat Putih Rata-Rata………...…34
Gambar 4.2b. Pengaruh Temperatur Terhadap Derajat Putih Rata-Rata…………...34
Gambar 4.2c. Pengaruh Faktor Dosis H2O2 dan Temperatur Terhadap
Derajat Putih Rata-Rata……… ……..36
Gambar 4.3. Penurunan Derajat Putih Sampel Pulp
Gambar 4.4a. Pengaruh Dosis H2O2 Terhadap Penurunan Derajat Putih ………...38
Gambar 4.4b. Pengaruh Temperatur Terhadap Penurunan Derajat Putih ……… …38
Gambar 4.5. Viskositas Pulp Tahap D2 dan P ………...…………...… …...39
Gambar 4.6a. Pengaruh Dosis H2O2 Terhadap Viskositas Pulp Rata-Rata……. …..41
Gambar 4.6b. Pengaruh Temperatur Terhadap Viskositas Pulp Rata-Rata……. …..41
Gambar 4.7a. Pengaruh Dosis H2O2 Terhadap Residu H2O2 Rata-Rata…………...42
Gambar 4.7b. Pengaruh Temperatur Terhadap Residu H2O2 Rata-Rata………….. 42
Gambar 4.8a. Indeks Sobek Kertas Tahap D2 dan P dari D1 1% ………....….….…44
Gambar 4.8b. Indeks Sobek Kertas Tahap D2 dan P dari D1 1,3% ………...… .…44
Gambar 4.9a. Pengaruh Dosis H2O2 Terhadap Indeks Sobek………...……….…....45
Gambar 4.9b. Pengaruh Temperatur Terhadap Indeks Sobek ………..……...45
Gambar 4.10a. Indeks Tarik Kertas Tahap D2 dan P dari D1 1%... ………..…46
Gambar 4.10b. Indeks Tarik Kertas Tahap D2 dan P dari D1 1,3%... ………..…...46
Gambar 4.11a. Pengaruh Dosis H2O2 Terhadap Indeks Tarik……….…....47
DAFTAR LAMPIRAN
Halaman
Lampiran 1. Gambar Peralatan Water Bath Tempat Proses Pemutihan Pulp ...54
Lampiran 2. Gambar Sampel Pulp ...55
Lampiran 3. Data derajat Putih Pulp Tahap D2 dan P ...57
Lampiran 4. Data Derajat Putih Pulp Setelah Dipanaskan 4 jam, 105 0C ...58
Lampiran 5. Data Viskositas Pulp Tahap D2 dan P ...59
Lampiran 6. Data Residu ClO2 dan H2O2 Tahap D2 dan P ...60
Lampiran 7. Data Indeks Tarik Kertas dari Pulp Tahap D2 dan P ...61
Lampiran 8. Data Indeks Sobek Kertas dari Pulp Tahap D2 dan P ...62
Lampiran 9. Data Dosis NaOH dan pH Tahap D2 dan P ... 63
Lampiran 10. Biaya Bahan kimia Pemutihan Pulp ...64
Lampiran 11. Kualifikasi Produksi Pulp di PT. RAPP ...64
Lampiran 12.Hasil Analisa Data Desain Faktorial...65
Lampiran 13. Analisis Derajat Putih ...81
Lampiran 14. Analisis Penurunan Derajat Putih ...83
Lampiran 15. Analisis Viskositas Pulp ... 84
Lampiran 16. Analisis pH Pulp ...86
Lampiran 17. Penentuan Konsentrasi H2O2 dan Residual H2O2 ... 87
Lampiran 19. Penentuan Konsistensi Pulp ……… 92
BAB I
PENDAHULUAN
1.1. Latar Belakang
Pengawasan terhadap masalah pencemaran lingkungan semakin meningkat
terutama tentang penggunaan senyawa klorin. Hal ini menyebabkan industri pulp
mengevaluasi kembali proses dan bahan kimia yang digunakan dalam proses
pemutihan pulp. Solusi yang diterapkan oleh banyak industri pulp adalah proses
pemutihan pulp dengan sistem bebas unsur klorin (Elemental Chlorine Free, ECF).
PT. Riau Andalan Pulp and Paper (RAPP) adalah perusahaan yang
memproduksi pulp dan kertas yang menggunakan sistem ECF pada proses pemutihan
pulp. Perusahaan ini telah beroperasi sejak tahun 1995 dan saat ini kapasitas produksi
pulp mencapai lebih kurang 2 juta ton/tahun (RAPP, 2005). PT. RAPP terletak 75 km
bagian tenggara kota Pekanbaru, tepatnya di Desa Pangkalan Kerinci, Kecamatan
Langgam, Kabupaten Pelalawan, Riau. PT.RAPP menggunakan empat tahap proses
pemutihan pulp yaitu D0, Eo, D1, D2, dimana pada tahap D0, D1 dan D2 menggunakan
klorin dioksida (ClO2) sebagai bahan pemutih, sedangkan tahap Eo merupakan proses
ekstraksi lignin yang menggunakan oksigen dan natrium hidroksida (NaOH).
Hidrogen Peroksida digunakan dalam tahap ekstraksi (Eop) untuk pulp mixed hard
wood (MHW) bersama-sama dengan natrium hidroksida dan oksigen.
Proses pemutihan pulp bertujuan untuk meningkatkan derajat putih dan sifat
produksi pulp. Namun konsumen mengeluhkan derajat putih pulp yang menurun
selama masa penyimpanan, transportasi dan proses produksi kertas.
Untuk mengatasi masalah penurunan derajat putih ini digunakan bahan
pemutih yang dapat menjadikan pulp dengan derajat putih yang relatif stabil. Bahan
pemutih yang digunakan adalah hidrogen peroksida (H2O2). Sejak tahun 1970-an
telah diketahui bahwa hidrogen peroksida telah mampu memisahkan lignin pada pulp
kraft. Selama beberapa tahun terakhir ini hidrogen peroksida telah digunakan pada
proses pemutihan pulp kraft. Dengan penambahan yang relatif rendah, hidrogen
peroksida dapat meningkatkan derajat putih (Anderson, 1992). Pulp yang diputihkan
dengan menggunakan hidrogen peroksida pada tahap akhir proses pemutihan
menghasilkan pulp dengan derajat putih yang lebih stabil dibandingkan dengan
menggunakan klorin dioksida. (Suss, 2003; Senior dan Ragauskas, 1996; Dence dan
Reeve, 1996).
Dengan mengganti klorin dioksida dengan hidrogen peroksida pada tahap
akhir proses pemutihan pulp dapat mengurangi pencemaran lingkungan oleh senyawa
klor organik sekaligus meningkatkan stabilitas derajat putih pulp.
Sebelum ini, penelitian tentang penggunaan hidrogen peroksida dalam proses
pemutihan ECF kraft pulp telah dilakukan (Anderson, 1992; Bouchard dkk, 1996 ;
Malinen dan Marimus, 1993; Lachapelle dkk, 1992; Ulrich, 2003; Suss dkk. 2004;
dan lain-lain). Pada umumnya penelitian-penelitian itu dilakukan terhadap kayu
berdaun jarum (softwood), sebagian kecil kayu berdaun lebar (mixed hardwood).
belum pernah dilakukan terhadap akasia yang ada di daerah tropis (Asia tenggara).
Berdasarkan hal tersebut maka riset mengenai pemutihan kraft pulp dari tropical
hardwood yaitu akasia menggunakan hidrogen peroksida perlu dilakukan.
1.2. Rumusan Masalah
Saat ini PT. RAPP menggunakan klorin dioksida sebagai bahan pemutih pada
proses pemutihan pulp dengan empat tahapan yaitu D0-Eo-D1-D2 . Dalam upaya
mengurangi pemakaian klorin dioksida dan meningkatkan kualitas pulp terutama
derajat putih yang stabil maka perlu dilakukan pengkajian tentang penggunaan
hidrogen peroksida sebagai bahan alternatif untuk pemutihan pulp. Penelitian ini
dilakukan dengan mengganti tahap akhir (D2) yang menggunakan klorin dioksida
pada proses pemutihan pulp tersebut dengan menggunakan hidrogen peroksida.
Dalam hal ini akan diteliti sejauh mana hidrogen peroksida sebagai bahan pemutih
dapat meningkatkan kualitas pulp dan nilai ekonomisnya dalam proses pemutihan
pulp.
Penulis telah melakukan penelitian pendahuluan terhadap proses pemutihan
pulp tahap D0ED1D2 dan D0ED1P. Dari kedua proses tersebut diperoleh derajat putih
yang sama pada tahap klorin dioksida (D2) dengan dosis ClO2 0,5% dan tahap
hidrogen peroksida (P) dengan dosis H2O2 0,25%. Oleh sebab itu konsentrasi H2O2
pada percobaan ini ditetapkan kurang lebih setengah dari dosis ClO2 pada tahap
1.3. Tujuan
Tujuan penelitian ini adalah untuk mengetahui efisiensi hidrogen peroksida
pada tahap akhir proses pemutihan pulp dengan bahan baku akasia terhadap kualitas
pulp dan nilai ekonomisnya.
1.4. Ruang Lingkup
Penelitian ini merupakan studi kasus proses pemutihan pulp di PT. RAPP
yang menggunakan proses kraft. Penelitian dilakukan mulai dengan tahapan proses
pemutihan yang terdiri dari:
a. D0, pada tahap ini digunakan ClO2 dengan dosis 2%.
b. E, pada tahap ini dilakukan ekstraksi lignin dengan menggunakan NaOH
dengan dosis 1%.
c. D1, pada tahap ini digunakan ClO2 dengan dosis 1% ; 1,3%.
d. P, pada tahap ini digunakan H2O2 dengan dosis 0,1% ; 0,2% ; 0,4% pada
temperatur reaksi 65 0C ; 75 0C ; 85 0C ; 95 0C.
e. D2, tahap ini dilakukan sebagai pembanding (setelah D1) dengan variasi
dosis ClO2 : 0,2% ;0,4% ; 0,7%
(Dosis bahan kimia dalam % berat kering pulp)a
Parameter uji yang digunakan untuk menganalisis pulp hasil proses pemutihan
H2O2, sifat fisik pulp yaitu uji kekuatan sobek (tear test) dan uji kekuatan tarik
(tensile test).
1.5. Manfaat
Penelitian ini diharapkan dapat memberikan informasi bagi peneliti dan
industri pulp tentang penggunaan H2O2 sebagai alternatif pengganti ClO2 pada tahap
BAB II
TINJAUAN PUSTAKA
2.1. Pemutihan Pulp Bebas Unsur Klorin (Elemental Chlorine Free-ECF)
Negara-negara di seluruh dunia saat ini memasuki era globalisasi yang
ditandai dengan adanya gejala global yang terdiri dari pasar terbuka, aspek
lingkungan dan pemasaran pulp dan kertas yang kompetitif. Oleh sebab itu teknologi
pembuatan pulp yang ramah lingkungan berkembang dengan pesat. Aspek
lingkungan yang dominan pada industri pulp terletak pada proses pemutihan.
Pemutihan pulp secara konvensional dengan menggunakan senyawa klorin
(Cl2) ternyata menimbulkan persoalan lingkungan yang serius. Dampak negatif yang
ditimbulkan adalah pada buangannya yang mengandung senyawa klorin organik yang
berbahaya bagi lingkungan hidup.
Untuk menentukan jumlah zat organik terklorinasi adalah dengan mengukur
AOX (adsorbable organic halogen). Reaksi antara klorin dengan pulp belum putih
membentuk zat organik terklorinasi yang bersifat racun yang dikenal dengan dioksin
dan furan. Pembentukan AOX adalah proporsional dengan jumlah elemental klorin
yang dikonsumsi. Kenaikan AOX juga berhubungan linier dengan jumlah Cl yang
digunakan dalam proses pemutihan pulp, misalnya dalam ClO2 (Tjahjono, 2006).
Alternatif mengurangi senyawa klor organik antara lain dengan menerapkan
teknologi pemutihan pulp yang tidak memakai klorin dalam bentuk elemen. Sistem
pemutihan ini adalah : ClO2, NaOH, O2, H2O2 dan kadang-kadang dapat
dikombinasikan dengan ozon (O3).
Untuk mendapatkan pulp dengan derajat putih yang maksimal, proses
pemutihan pulp biasanya dilakukan dengan beberapa tahap yang disingkat dengan
simbol-simbol sebagai berikut :
a. D : tahap klor dioksida : yaitu reaksi dengan ClO2 dalam media asam
b. E : tahap ekstraksi : yaitu pelarutan hasil reaksi dengan NaOH
Untuk meningkatkan derajat putih biasanya
pada tahap E ditambahkan O2 atau H2O2.
c. P : tahapPeroksida : yaitu reaksi dengan H2O2 dalam media alkali
d. O : tahap oksigen : yaitu reaksi dengan O2 pada tekanan tinggi
dalam media alkali
f. Z : tahap ozon : yaitu reaksi dengan ozon dalam media asam.
Pemutihan pulp sistem ECF dengan beberapa tahapan dapat dimodifikasi sesuai
dengan kebutuhan dimana setiap tahap diselingi dengan proses pencucian, misalnya ;
OD0ED1D2, OD0EopD1D2, OD0EopD1P, D1ED2ED3 dan lain-lain.
Saat ini sistem ECF merupakan proses pemutihan yang dominan dilakukan
pada industri pulp dan kertas. Lebih dari 90% produk pulp dunia menggunakan
2.2. Hidrogen Peroksida Sebagai Bahan Pemutih Pulp
Hidrogen peroksida adalah bahan pemutih berbentuk cair dan tidak berwarna.
Hidrogen peroksida mudah terurai bila terkena cahaya menghasilkan air dan oksigen.
Biasanya hidrogen peroksida disimpan pada konsentrasi 50 % dengan sifat-sifat fisik:
b. berat jenis pada 25 0C : 1,19
c. titik beku : -52 0C
d. tekanan parsial pada 25 0C : 13,5 mmHg
e. Titik didih : 114 0C
(Dence dan Reeve,1996)
Hidrogen peroksida telah digunakan secara luas pada industri pulp. Efek
pemutihan dengan hidrogen peroksida adalah pada kemampuannya untuk bereaksi
dengan gugus karbonil lignin. Hidrogen peroksida yang digunakan pada tahap akhir
proses pemutihan pulp dapat meningkatkan derajat putih dan stabilitasnya.(Suss dkk,
2004; Senior dan Ragauskas,1996).
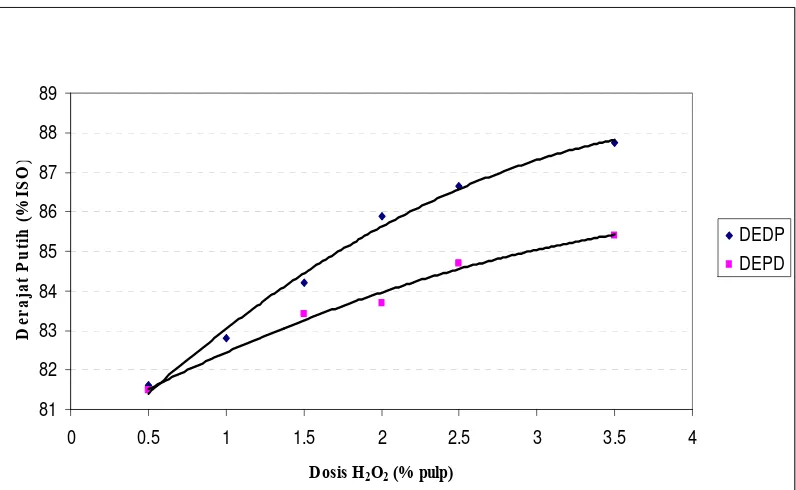
Urutan tahap peroksida pada proses pemutihan ECF berpengaruh terhadap
derajat putih yang dihasilkan. Senior dan Ragauskas (1996) telah melakukan
penelitian pada dua proses pemutihan pulp kayu berdaun jarum dengan urutan tahap
yang berbeda yaitu; D1ED2P dan D1EPD2. Kedua proses menggunakan bahan kimia
dengan dosis dan kondisi yang sama tetapi menghasilkan derajat putih yang berbeda
seperti yang dapat dilihat pada Gambar 2.1.
Derajat putih pulp pada akhir proses (final brightness) yang diperoleh pada
dioksida pada tahap D2 di proses pertama lebih efektif menghilangkan lignin aromatik
dari pada tahap peroksida (P) pada proses kedua. Hidrogen peroksida lebih efektif
bereaksi dengan spesies non aromatik seperti struktur karbonil dan kuinon. (Senior
dan Ragauskas, 1996).
81 82 83 84 85 86 87 88 89
0 0.5 1 1.5 2 2.5 3 3.5 4
Dosis H2O2 (% pulp)
D
er
a
ja
t P
u
ti
h
(%
IS
O
)
DEDP DEPD
Gambar 2.1. Derajat Putih Pulp dengan Tahapan Pemutihan DEDP dan DEPD dengan Variasi Dosis H2O2 ( Senior dan Ragauskas, 1996)
2.3. Reaksi Hidrogen Peroksida
Mekanisme dekomposisi hidrogen peroksida dalam proses pemutihan pulp
merupakan reaksi yang kompleks. Hidrogen peroksida bereaksi optimal dengan lignin
dalam kondisi alkali (basa). Mekanisme reaksi dekomposisi hidrogen peroksida
H2O2 → OOH− + H+ (2.1)
H2O2 → OH+ + OH− (2.2)
H2O2 → OOH⋅ + H⋅ (2.3)
H2O2 → OH⋅ + OH⋅ (2.4)
H2O2 + OH− → OOH− + H2O (2.5)
H2O2 + OOH− → H2O + OH− + O2 (2.6)
H2O2 + H+ → OH+ + H2O (2.7)
H2O2 → H2O + 1/2O2 (2.8)
Anion perhidroksil (OOH-) adalah bahan yang aktif bereaksi dengan struktur
karbonil pada lignin sehingga lignin terpecah-pecah, larut dan diekstraksi dalam
larutan NaOH. Konsentrasi ion perhidroksil meningkat dengan bertambahnya
konsentrasi H2O2 dan NaOH. Persamaan laju reaksi dekomposisi H2O2 adalah :
-d[H2O2]T/dt = k[H2O2] [OOH−] (2.9)
Dimana :
[H2O2]T = total dekomposisi hidrogen peroksida, [H2O2] + [OOH−]
k = konstanta laju reaksi pada temperatur T
[OOH−] = konsentrasi anion perhidroksil
[H2O2] = konsentrasi H2O2 yang terionisasi
Formasi anion perhidroksil diatur melalui pH dan temperatur dalam suasana
alkali. Jadi pH yang tinggi merupakan syarat utama delignifikasi atau pemutihan
pulp dengan menggunakan hidrogen peroksida. (Anderson, 1992).
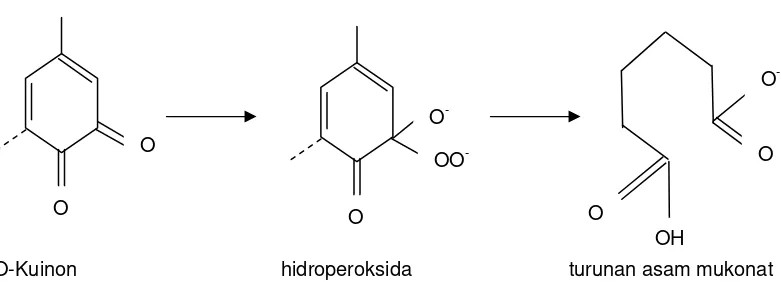
Anion perhidroksil adalah oksidan lunak yang bereaksi terutama dengan
gugus karbonil. Anion perhidroksil menyerang gugus karbonil terutama struktur
kuinon dan menguraikannya menjadi senyawa-senyawa yang tidak berwarna. Pada
Gambar 2.2 dapat dilihat reaksi anion perhidroksil menyerang struktur O-kuinon yang
menghasilkan hidroperoksida dan selanjutnya terurai menjadi turunan asam mukonat
(Sjostrom, 1998).
O-Kuinon hidroperoksida turunan asam mukonat
O
O
O
OO -O
-O
OH
O O
-Gambar 2.2. Reaksi Anion Perhidroksil Dengan Struktur O-Kuinon (Sjostrom, 1998)
Radikal OOH. dan OH. yang terbentuk dari Persamaan (2.3) dan (2.4) juga
ikut berperan dalam proses pemutihan pulp untuk mendegradasi lignin. Namun
oksidan ini tidak selektif sehingga dapat juga mendegradasi selulosa(Sjostrom, 1998 ;
Dekomposisi hidrogen peroksida dalam proses pemutihan pulp dikatalisasi
oleh unsur metal transisi seperti Fe, Mn dan Cu yang secara normal terkandung dalam
pulp. Metal transisi berperan dalam pembentukan hidroksil radikal (OH.) dan anion
superoksida radikal (O2-) seperti pada reaksi berikut ini.
Mn+ + H2O2 HO. + OH+ + M(n+1) (2.10)
HO. + OOH- O2- + H2O (2.11)
O2 + H2O2 O2- + HO. + OH- (2.12)
M : Metal transisi
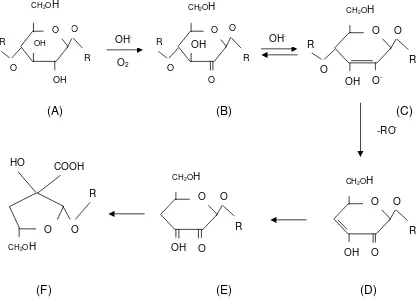
Gambar 2.3 menunjukkan reaksi pemutusan rantai polisakarida oleh radikal
O2- dan OH. Reaksi yang disebabkan oleh radikal O2- dan OH. adalah pembentukan
gugus karbonil pada kedudukan C2 dari unit monomer selulosa (B) yang
mengakibatkan pemutusan ikatan polisakarida dengan mengeliminasi -alkoksi.
Oksidasi kedudukan C3 (C) dan oksidasi hidroksil C6 (D) menghasilkan reaksi yang
dapat menyebabkan pemutusan rantai. Jika kedudukan C2 dan C3 dioksidasi secara
simultan maka terbentuk struktur 2, 3 diketo (E) yang dapat berubah menjadi gugus
karboksifuranosida (F) tanpa pemutusan rantai atau mudah didegradasi dalam media
OH OH O O R R
CH2OH
O O OH R O O
CH2OH
O
OH.
OH
R O
CH2OH
O O -R O R O OH. O2
(A) (B) (C)
-RO -O R COOH HO O
CH2OH
O OH
O
CH2OH
O O
R O
CH2OH
OH
R O
(F) (E) (D)
Gambar 2.3. Reaksi Degradasi Selulosa oleh Hidroksil dan Superoksida Radikal (Fengel dan Gerd 1989)
2.4. Penurunan Derajat Putih (Brightness Reversion)
Derajat putih adalah parameter yang penting dalam produksi pulp. Pulp yang
berkualitas dengan derajat putih yang tinggi sangat diharapkan. Namun derajat putih
pulp mengalami penurunan dengan berubah warna menjadi menguning selama masa
transportasi, penyimpanan dan pembuatan kertas.
1. Thermal yellowing, adalah perubahan warna yang disebabkan oleh
penyimpanan kertas dalam waktu yang lama pada temperatur lingkungan
(ambien) di tempat yang gelap dan berkelembaban tinggi.
2. Photo yellowing, adalah perubahan warna yang disebabkan oleh adanya
cahaya terhadap pulp atau kertas, terutama sinar ultra violet.
Penguningan pulp yang disebabkan oleh panas terjadi melalui oksidasi gugus
hidrokuinon lignin. Penguningan pulp dan kertas akan bertambah seiring dengan
meningkatnya temperatur dan kelembaban.
Lignin mempunyai kemampuan yang tinggi untuk menyerap sinar ultraviolet.
Penyerapan terjadi pada struktur kromofor di dalam jaringan lignin. Kromofor adalah
gugus-gugus yang mempunyai kontribusi terhadap warna pulp dan kertas.
Gugus-gugus dasar kromofor terdiri dari :
f. Gugus fungsional : gugus karbonil, etilen, cincin aromatik.
g. Zat antara : kuinon, kuinon metida dll.
Gugus karbonil menyerap energi radiasi ultraviolet menjadi tereksitasi
membentuk senyawa radikal seperti hidroksil fenol. Senyawa radikal ini akhirnya
berubah menjadi struktur kuinon yang menyebabkan warna pulp dan kertas
menguning. (Dence dan Reeve, 1996).
Pada pulp kimia, faktor-faktor yang mempengaruhi penguningan pulp dan
kertas antara lain adalah ; residual lignin, kandungan ekstraktif, ion metal dan residu
bahan pemutih. Namun demikian pada dasarnya historikal pembuatan pulp mulai dari
memberikan pengaruh terhadap penurunan derajat putih pulp dan kertas seperti
terlihat pada skema berikut ini.
BAHAN
BAKU
PROSES
PRODUKSI
PENYIMPANAN
PRODUK
• Jenis kayu
• Umur, pertumbuhan,
lokasi
• Komposisi
• Kondisi dan lamanya
waktu penyimpanan
• Metoda
• Parameter proses
• Bahan kimia
pemutih
• Aditif
• Pencetakan
• Cahaya
• Udara (O2)
• Sirkulasi udara
• Panas
• Kelembaban
• Polutan
• Waktu
(Sumber: Dence dan Reeve, 1996)
Bahan kimia pemutih dan urutan tahap proses pemutihan multitahap terutama
pada tahap akhir mempunyai peran penting dalam menghasilkan pulp dengan derajat
putih yang tinggi dan stabil. Menurut Nhan (2005), pulp yang diputihkan dengan
hidrogen peroksida pada tahap akhir proses pemutihan menghasilkan pulp dengan
penurunan derajat putih yang lebih kecil dibandingkan dengan menggunakan ClO2.
memanaskan pulp pada 100 0C, kelembaban relatif 100% selama 1 jam. Hasilnya
dapat dilihat pada Gambar 2.4.
82 83 84 85 86 87 88 89 90 91 92
DoEpD1 DoEpD1D2 DoEpD1P
D
e
ra
ja
t P
u
ti
h
(%
IS
O
)
Derajat putih sebelum pemanasan Derajat putih setelah pemanasan
Gambar 2.4. Stabilitas Derajat Putih Pulp pada Proses Pemutihan dengan Urutan Tahap yang Berbeda Untuk Pulp dengan Bahan Baku Eucalyptus (Nhan, 2005)
Penurunan derajat putih disebabkan oleh adanya struktur karbonil dan kuinon
dalam pulp. Hidrogen peroksida efektif memecahkan dan melarutkan struktur
karbonil dan kuinon sedangkan klorin dioksida tidak dapat menghancurkannya
dengan sempurna. (Dence dan Reeve, 1996; Senior dan Ragauskas, 1996).
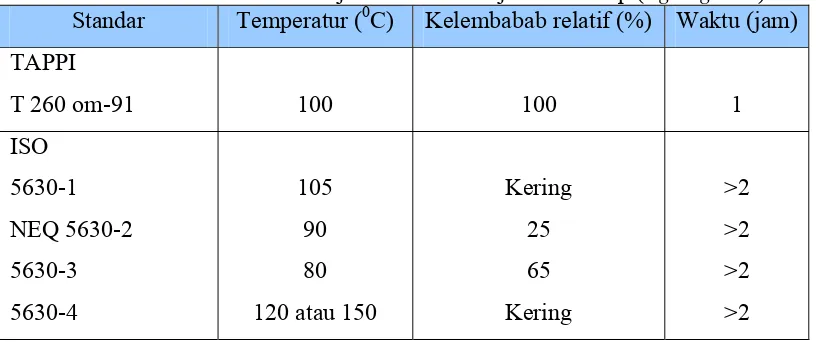
Untuk mengetahui stabilitas derajat putih pulp, dilakukan uji dengan metoda
digunakan untuk menentukan penurunan derajat putih adalah seperti pada tabel
[image:33.612.114.522.180.351.2]berikut ini.
Tabel 2.1. Metoda Standar untuk Uji Stabilitas Derajat Putih Pulp (Ageing Test) Standar Temperatur (0C) Kelembabab relatif (%) Waktu (jam) TAPPI
T 260 om-91 100 100 1 ISO
5630-1 NEQ 5630-2 5630-3 5630-4
105 90 80 120 atau 150
Kering 25 65 Kering
>2 >2 >2 >2
(Sumber: Dence dan Reeve, 1996)
2.5. Variabel Proses
Konsentrasi Hidrogen Peroksida
Dosis H2O2 yang digunakan pada proses pemutihan berpengaruh secara
langsung terhadap derajat putih pulp. Peningkatan konsentrasi H2O2 menghasilkan
kenaikan derajat putih yang signifikan seperti terlihat pada Gambar 2.1.
Konsentrasi Alkali (pH)
Konsentrasi alkali merupakan variabel yang penting dalam proses pemutihan
pulp tahap hidrogen peroksida. Jika konsentrasi NaOH terlalu rendah H2O2 tidak akan
berfungsi dengan efektif, tetapi bila terlalu tinggi akan mengakibatkan pulp berwarna
gelap atau menguning. Pada pH yang terlalu tinggi, laju dekomposisi H2O2 akan
Pada pH yang terlalu rendah, konsentrasi anion perhidroksil tidak cukup untuk
meningkatkan derajat putih. Pada tahap peroksida, reaksi pemutihan berlangsung
pada pH 10-11 (Dence dan Reeve, 1996).
Proses pemutihan pulp menggunakan H2O2 akan menghasilkan derajat putih
yang maksimum bila disertai dengan penambahan dosis alkali (NaOH) yang
optimum. Dari hasil penelitian sebelumnya diperoleh dosis NaOH optimum untuk
[image:34.612.113.522.359.522.2]berbagai variasi dosis H2O2 seperti pada tabel berikut ini.
Tabel 2.2. Dosis NaOH Optimum untuk Berbagai Variasi Dosis H2O2 dalam Proses Pemutihan Pulp Kraft.
Dosis H2O2 (% berat kering pulp) Dosis NaOH (% berat kering pulp) 1 2 – 2,5
1,5 2 – 3
2 2 – 3
3 2,5 – 3,5
4 3 - 4
Kondisi operasi : Temperatur 90 0C, 2 jam, konsistensi 10%-15%
(Sumber : Dence dan Reeve, 1996)
Temperatur dan Waktu
Temperatur dan waktu reaksi proses pemutihan sangat erat hubungannya
dengan derajat putih dan kualitas pulp. Pengurangan waktu tinggal reaksi dapat
dapat dicapai dengan temperatur yang lebih rendah dan waktu tinggal reaksi yang
lebih lama.
Temperatur yang tinggi dapat merusak kualitas pulp. Reaksi dekomposisi
H2O2 yang terlalu cepat dapat menurunkan selektivitas sehingga sellulosa juga ikut
terdegradasi. Selain dari pada itu, temperatur yang tinggi juga dapat menurunkan
derajat putih pulp. Hubungan temperatur dan waktu tinggal reaksi terhadap derajat
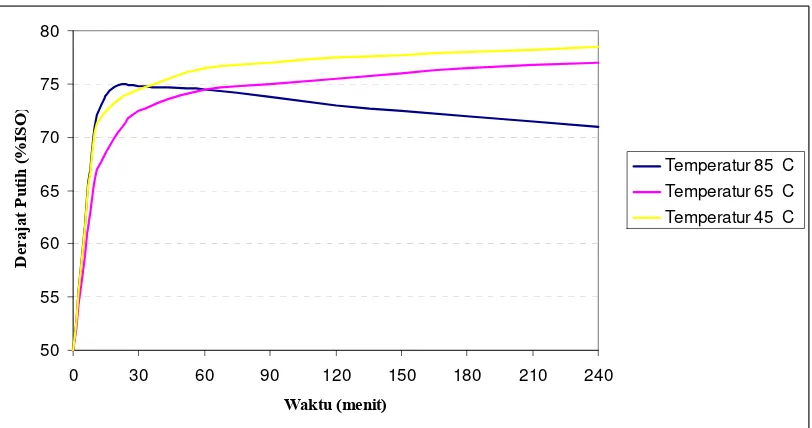
putih dapat dilihat pada Gambar 2.5.
Pada Gambar 2.5 terlihat bahwa pada temperatur 85 0C, derajat putih naik
dengan cepat dan derajat putih maksimum diperoleh pada waktu reaksi kurang dari
30 menit, tetapi selanjutnya derajat putih mengalami penurunan sampai akhir reaksi
(240 menit). Namun pada temperatur 65 0C dan 45 0C derajat putih pulp meningkat
seiring dengan bertambahnya waktu reaksi. Pada temperatur 85 0C reaksi pemutihan
berlangsung dengan cepat. Pada kondisi ini mengaktifkan metal transisi seperti Fe,
Mn dan Cu yang secara normal terkandung dalam pulp. Metal transisi berperan dalam
50 55 60 65 70 75 80
0 30 60 90 120 150 180 210 240
Waktu (menit)
D
er
a
ja
t P
u
ti
h
(%
IS
O
)
[image:36.612.119.525.113.327.2]Temperatur 85 C Temperatur 65 C Temperatur 45 C
Gambar 2.5. Pengaruh Temperatur dan Waktu Reaksi Terhadap Derajat Putih
Pulp Spruce yang Diputihkan dengan H2O2 . Konsentrasi H2O2 4%, Konsistensi 30%.(Dence dan Reeve, 1996)
Konsistensi
Konsistensi adalah persentase berat pulp kering dalam bubur pulp (pulp
basah). Konsistensi pulp berpengaruh terhadap derajat putih dan konsumsi bahan
pemutih pulp. Untuk mencapai derajat putih yang sama, proses pemutihan pulp
dengan konsistensi yang rendah membutuhkan H2O2 yang lebih banyak dari pada
BAB III
METODOLOGI PENELITIAN
3.1. Lokasi dan Waktu Penelitian
Penelitian dilaksanakan di PT. Riau Andalan Pulp and Paper (RAPP),
Pangkalan Kerinci, Riau. Penelitian dilakukan selama 10 bulan, mulai Juli 2006
sampai April 2007.
3.2. Bahan dan Peralatan
Bahan baku pulp yang digunakan dalam penelitian ini diambil dari keluaran
tahap oksigen delignifikasi di unit fiberline 2 PT. RAPP. Peralatan utama yang
digunakan dalam penelitian ini adalah kantong plastik yang dilengkapi penutup
(polyethylene bag) dan water bath dengan temperatur yang dapat dikendalikan.
Bahan kimia pemutih yang digunakan adalah ClO2 dengan konsentrasi 9,5 g/L dan
NaOH 1 N diperoleh dari unit chemical plant di PT. RAPP. H2O2 yang digunakan
pada tahap hidrogen peroksida dengan konsentrasi 600 g/L diperoleh dari perusahaan
Degussa , Jerman.
3.3. Prosedur Kerja.
• D0-E-D1-D2
• D0-E-D1-P
Sampel pulp diambil dari keluaran unit O2 delignifikasi. Sebelum sampel
diputihkan dilakukan pengukuran derajat putih pulp. Temperatur, tekanan, waktu dan
pH akhir reaksi pada tahapan D0-E-D1-D2 masing- masing disesuaikan dengan
keadaan proses pemutihan yang berlangsung di pabrik pulp PT. RAPP.
Prosedur kerja percobaan proses pemutihan pulp adalah sebagai berikut.
Tahap D0
1. Pulp dari unit O2 delignifikasi ditimbang sebanyak 100 gram (berat kering) di
dalam kantong plastik yang dilengkapi penutup, kemudian ditambahkan
H2SO4 (untuk mengontrol pH agar diperoleh pH akhir 3,5-4,5) dan air
sehingga konsistensi pulp pada proses pemutihan menjadi 10%. Pulp diaduk
di dalam kantong plastik dan selanjutnya dilakukan pengukuran pH sebagai
pH awal pulp.
2. ClO2 dengan dosis 2% ditambahkan ke dalam plastik berisi pulp dan plastik
ditutup dengan cepat, kemudian dilakukan pengadukan sehingga pulp dan
ClO2 tercampur dengan merata.
3. Pulp dimasukkan ke dalam water bath dengan temperatur 65 0C selama 60
4. Setelah waktu reaksi tercapai, pulp diangkat dan disaring dalam wadah
saringan. Filtrat hasil penyaringan diambil dan dianalisis untuk mengetahui
pH akhir dan kadar residu ClO2.
5. Pulp dicuci dengan air demineral dalam wadah saringan dan selanjutnya pulp
yang mengandung air diperas dan dihomogenkan.
6. Pulp yang siap untuk dianalisis disimpan dalam plastik tertutup dan terlindung
dari cahaya.
Tahap E
1. Pulp hasil pemutihan tahap D0 ditimbang 100 gram (berat kering) di dalam
kantong plastik yang dilengkapi penutup.
2. NaOH dengan dosis 1% dan air ditambahkan ke dalam kantong plastik yang
berisi pulp sehingga konsistensi menjadi 10%. Pulp diaduk dan dilakukan
pengukuran pH sebagai pH awal.
3. Pulp dimasukkan ke dalam water bath dengan temperatur 80 0C selama 90
menit.
4. Setelah waktu reaksi tercapai, pulp diangkat dan disaring dalam wadah
saringan. Filtrat hasil penyaringan diambil dan dianalisis untuk mengetahui
pH akhir.
5. Pulp dicuci dengan air demineral dalam wadah saringan dan selanjutnya pulp
yang mengandung air diperas dan dihomogenkan.
6. Pulp yang siap untuk dianalisis disimpan dalam plastik tertutup dan terlindung
Tahap D1
1. Pulp dari hasil tahap ekstraksi (E) ditimbang sebanyak 100 gram (berat
kering) di dalam kantong plastik yang dilengkapi penutup, kemudian
ditambahkan NaOH (untuk mengontrol pH agar diperoleh pH akhir 3,5-4,5)
dan air sehingga konsistensi pulp pada proses pemutihan menjadi 10%. Pulp
diaduk di dalam kantong plastik dan selanjutnya dilakukan pengukuran pH
sebagai pH awal pulp.
2. ClO2 dengan variasi dosis yang telah ditetapkan (1% ; 1,3%) ditambahkan ke
dalam plastik berisi pulp dan plastik ditutup dengan cepat. Kemudian pulp
diaduk sehingga pulp dan ClO2 tercampur dengan merata.
3. Pulp dimasukkan ke dalam water bath dengan temperatur 75 0C selama 180
menit.
4. Setelah waktu reaksi tercapai, pulp diangkat dan disaring dalam wadah
saringan. Filtrat hasil penyaringan diambil dan dianalisis untuk mengetahui
pH akhir dan kadar residu ClO2.
5. Pulp dicuci dengan air demineral dalam wadah saringan dan selanjutnya pulp
yang mengandung air diperas dan dihomogenkan.
6. Pulp yang siap untuk dianalisis disimpan dalam plastik tertutup dan terlindung
dari cahaya.
Tahap D2
1. Pulp dari hasil tahap D1 ditimbang sebanyak 100 gram (berat kering) di dalam
(untuk mengontrol pH agar diperoleh pH akhir 3,5-4,5) dan air sehingga
konsistensi pulp pada proses pemutihan menjadi 10%. Pulp diaduk di dalam
kantong plastik dan selanjutnya dilakukan pengukuran pH sebagai pH awal
pulp.
2. ClO2 dengan variasi dosis yang telah ditetapkan (0,2%; 0,4%; 0,7%)
ditambahkan ke dalam plastik berisi pulp dan plastik ditutup dengan cepat.
Kemudian pulp diaduk sehingga pulp dan ClO2 tercampur dengan merata.
3. Prosedur selanjutnya sama dengan nomor 4, 5 dan 6 pada tahap D1.
Tahap P
1. Pulp dari hasil tahap D1 ditimbang sebanyak 100 gram (berat kering) di dalam
kantong plastik yang dilengkapi penutup, kemudian ditambahkan NaOH
(untuk mengontrol pH agar diperoleh pH akhir 10,5-11,5) dan air sehingga
konsistensi pulp pada proses pemutihan menjadi 10%. Pulp diaduk di dalam
kantong plastik dan selanjutnya dilakukan pengukuran pH sebagai pH awal
pulp.
2. H2O2 dengan variasi dosis yang telah ditetapkan (0,1%; 0,2%; 0,4%)
ditambahkan ke dalam plastik berisi pulp dan plastik ditutup dengan cepat.
Kemudian pulp diaduk sehingga pulp dan H2O2 tercampur dengan merata.
3. Pulp dimasukkan ke dalam water bath dengan temperatur reaksi yang telah
4. Setelah waktu reaksi tercapai, pulp diangkat dan disaring dalam wadah
saringan. Filtrat hasil penyaringan diambil dan dianalisis untuk mengetahui
pH akhir dan kadar residu H2O2.
5. Pulp dicuci dengan air demineral dalam wadah saringan dan selanjutnya pulp
yang mengandung air diperas dan dihomogenkan.
6. Pulp yang siap untuk dianalisis disimpan dalam plastik tertutup dan terlindung
dari cahaya.
Skema prosedur kerja percobaan proses pemutihan pulp ini dapat dilihat pada
Gambar 3.1 dan Gambar 3.2.
3.4. Analisis Hasil Percobaan
Analisis terhadap bahan baku pulp dan hasil percobaan dilakukan menurut
prosedur TAPPI (Technical Association for the Pulp and Paper Industry-USA) dan
Departemen Technical PT.RAPP, yaitu derajat putih, penurunan derajat putih,
viskositas, pH, residual H2O2, residual Cl2, sifat-sifat fisik pulp yaitu uji kekuatan
sobek (tear test) dan uji kekuatan tarik ( tensile test).
3.5. Rancangan Percobaan dan Pengolahan Data Hasil Percobaan
Rancangan percobaan dilakukan dengan metode Design of Experiment
menggunakan analisis desain faktorial. Pembuatan rancangan dan analisa data
Variabel bebas yang ditetapkan adalah :
- dosis ClO2 tahap D1 : 1% ; 1,3%
- dosis H2O2 : 0,1%; 0,2%; 0,4%
- temperatur reaksi : 65 0C : 75 0C ; 85 0C; 95 0C
Sebagai variabel respon adalah :
- derajat putih
- penurunan derajat putih
- viskositas
- residu H2O2
- indeks sobek
- indeks tarik
Percobaan dilakukan dengan replikasi dua kali sehingga untuk analisa variabel respon
PROSES PEMUTIHAN PULP D0-E-D1-D2
PULP dari unit O2 delignifikasi
Penyaringan
Pencucian
D0
T=65 0C; t= 60 mnt
Air Air limbah
Residu ClO2
ClO2
H2SO4
Air
E
T=80 0C; t= 90 mnt
NaOH Air
Limbah Penyaringan
Air Air limbah
ClO2
NaOH Air
Residu ClO2
Air Air limbah
ClO2
NaOH Air
D1
T=75 0C; t= 180 mnt
D
2T=75 0C; t= 180 mnt
Penyaringan Residu ClO2
Air Air limbah
Pencucian
Pencucian Pencucian Penyaringan
[image:44.612.175.480.136.681.2]PULP PUTIH
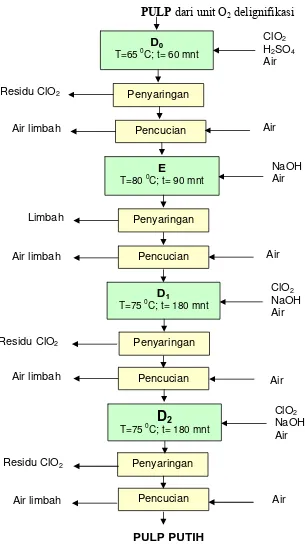
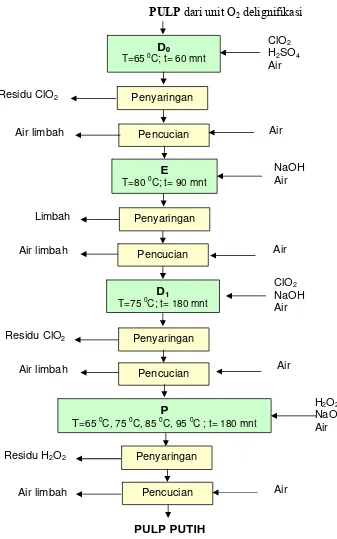
PROSES PEMUTIHAN PULP D0-E-D1-P
PULP dari unit O2 delignifikasi
Penyaringan
Pencucian
D0
T=65 0C; t= 60 mnt
Air Air limbah
NaOH Air E
T=80 0C; t= 90 mnt
Residu ClO2
ClO2
H2SO4
Air
Penyaringan
Air Air limbah
ClO2
NaOH Air
Residu ClO2
Air Air limbah
H2O2
NaOH Air
D1
T=75 0C; t= 180 mnt
P
T=65 0C, 75 0C, 85 0C, 95 0C ; t= 180 mnt
Penyaringan Residu H2O2
Pencucian Penyaringan
Pencucian
Air limbah Pencucian
PULP PUTIH
[image:45.612.168.505.136.675.2]Air Limbah
BAB IV
HASIL PERCOBAAN DAN PEMBAHASAN
4.1. Pemutihan Pulp Tahap D0-E-D1
Proses pemutihan pulp tahap D0-E-D1 dilakukan untuk mempersiapkan
sampel pulp pada tahap D2 dan P. Pada akhirnya dapat dibandingkan pulp hasil
proses pemutihan dengan tahapan D0-E-D1-D2 dengan tahapan D0-E-D1-P.
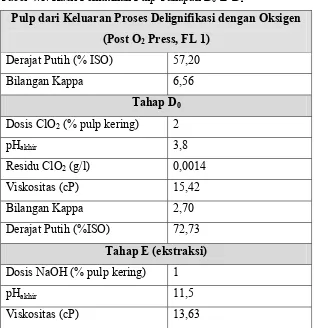
[image:46.612.122.436.372.700.2]Hasil pemutihan pulp tahap D0-E-D1 dapat dilihat pada Tabel 4.1 berikut ini.
Tabel 4.1. Hasil Pemutihan Pulp Tahapan D0-E-D1
Pulp dari Keluaran Proses Delignifikasi dengan Oksigen (Post O2 Press, FL 1)
Derajat Putih (% ISO) 57,20 Bilangan Kappa 6,56
Tahap D0 Dosis ClO2 (% pulp kering) 2
pHakhir 3,8 Residu ClO2 (g/l) 0,0014
Viskositas (cP) 15,42 Bilangan Kappa 2,70 Derajat Putih (%ISO) 72,73
Tahap E (ekstraksi)
Dosis NaOH (% pulp kering) 1
pHakhir 11,5
Bilangan Kappa 2,10 Derajat Putih (%ISO) 73,73
Tahap D1
Dosis ClO2 (% pulp kering) 1 1,3 Dosis NaOH (kontrol pH, %) 0,15 0,28 Temperatur (0C) 75 75 pHakhir 4,2 3,8 Residu ClO2 (g/l) 0.0007 0.0046 Residu H2O2 (g/l) - -Viskositas (cP) 12,86 12,76 Derajat Putih (%ISO) 89,27 90,08 Penurunan Derajat Putih,
setelah pemanasan 105 0C, 4 jam (%ISO)
4,50 4,30
4.2. Pemutihan Pulp Tahap D2 dan P
4.2.1. Derajat Putih Pulp
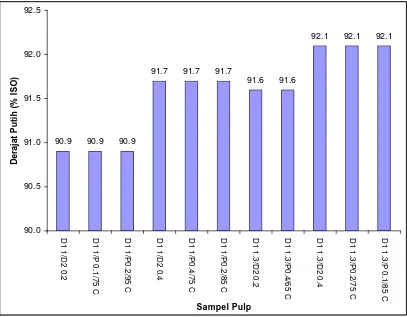
Gambar 4.1 menunjukkan bahwa pada perolehan derajat putih yang sama,
tahap P membutuhkan dosis H2O2 setengah dari dosis ClO2 pada tahap D2 dengan
temperatur reaksi 75 0C – 85 0C. Derajat putih pulp yang sama dapat juga diperoleh
pada temperatur 65 0C dan 95 0C tetapi dengan dosis H2O2 yang lebih besar . Jadi
temperatur reaksi yang efektif untuk pemutihan pulp akasia tahap P dengan waktu
90.9 90.9 90.9
91.7 91.7 91.7
91.6 91.6
92.1 92.1 92.1
[image:48.612.117.524.115.432.2]90.0 90.5 91.0 91.5 92.0 92.5 D1 1/ D2 0. 2 D1 1/ P 0. 1/ 75 C D1 1/ P 0. 2/ 95 C D1 1/ D2 0. 4 D1 1/ P 0. 4/ 75 C D1 1/ P 0. 2/ 85 C D1 1. 3 /D2 0. 2 D1 1. 3 /P 0. 4/ 65 C D1 1. 3 /D2 0. 4 D1 1. 3 /P 0. 2/ 75 C D1 1. 3 /P 0. 1/ 85 C Sampel Pulp De ra ja t P u ti h (% I S O )
Gambar 4.1 Derajat Putih Sampel Pulp Tahap D2 dan Tahap P dengan Derajat Putih yang Sama
Grafik pengaruh dosis H2O2 dan temperatur terhadap derajat putih pulp seperti
yang dapat dilihat pada Gambar 4.2a dan 4.2b merupakan hasil pengolahan data
menggunakan program minitab (Lampiran 12). Pada Gambar 4.2a menunjukkan
bahwa penambahan dosis H2O2 dapat meningkatkan derajat putih pulp. Pada dosis
H2O2 0,1% diperoleh derajat putih yang rendah karena dosis H2O2 yang tidak
mencukupi kebutuhan untuk bereaksi dengan lignin yang terkandung dalam pulp.
rata-rata pada sampel D1 1,3–P lebih tinggi 0,6% ISO dari pada sampel D1 1–P (selisih
rata-rata derajat putih rata-rata sampel D11,3-P dan D11-P). Hal ini disebabkan karena
sampel pulp D1 1,3–P memiliki dosis ClO2 yang lebih tinggi pada tahap D1 sehingga
senyawa lignin aromatik di dalam pulp lebih banyak berkurang. Namun respon
penambahan dosis H2O2 terhadap peningkatan derajat putih rata-rata pada sampel D1
1–P lebih tinggi dari pada sampel D1 1,3–P. Peningkatan derajat putih rata-rata untuk
sampel D1 1–P adalah 1,1% ISO dan 0,8% ISO untuk sampel D1 1,3–P. Hal ini
dipengaruhi oleh kondisi kandungan lignin pulp pada tahap D1. Sampel D1 1–P yang
memiliki dosis ClO2 yang lebih sedikit menyisakan lebih banyak kandungan lignin
untuk dilanjutkan pada tahap P.
Perbandingan pertambahan dosis H2O2 tidak sama dengan peningkatan
derajat putih. Penambahan dosis H2O2 0,1%; 0,2%; 0,4% pada sampel D11% dengan
derajat putih 89,3% ISO mengalami peningkatan derajat putih berturut-turut adalah
1,2 ; 1,6 ; 2,0 (% ISO) dan untuk sampel D1 1,3–P dengan derajat putih 90,1% ISO
peningkatan derajat putih adalah 1,2; 1,9; 2,3 (% ISO). Peningkatan derajat putih
diperoleh dari pengurangan derajat putih pulp tahap P dengan derajat putih tahap D1.
Jadi penambahan dosis dua kali lebih besar tidak serta merta menghasilkan
peningkatan derajat putih yang dua kali lebih tinggi.
Pada Gambar 4.2b dapat dilihat bahwa temperatur reaksi pada proses
pemutihan pulp berpengaruh sangat signifikan terhadap derajat putih pulp. Pada
temperatur 65 0C dihasilkan pulp dengan derajat putih yang rendah. Pada temperatur
lambat dan tidak optimal. Oleh sebab itu penguraian struktur karbonil lignin tidak
maksimal sehingga dihasilkan pulp dengan derajat putih yang rendah (Dence dan
Reeve, 1996)
Kenaikan temperatur dari 65 0C menjadi 75 0C meningkatkan derajat putih
rata-rata sebesar 0,7% ISO untuk sampel D1 1–P dan 1% ISO untuk sampel D1 1,3-P.
Kenaikan temperatur dari 75 0C menjadi 85 0C tidak menghasilkan peningkatan
derajat putih rata-rata yang signifikan ( kurang lebih 0,2% ISO). Daerah temperatur
75 0C sampai dengan 85 0C adalah kondisi yang optimal untuk mendapatkan derajat
[image:50.612.125.521.207.525.2]putih yang maksimal.
Gambar 4.2a. Pengaruh Dosis H2O2 Terhadap Derajat Putih Rata-Rata 90.7 91.4 91.5 90.8 91.1 92.1 92.4 91.2 90.6 90.8 91 91.2 91.4 91.6 91.8 92 92.2 92.4 92.6
60 65 70 75 80 85 90 95 100 Tem peratur (0C)
D e ra ja t P u ti h R a ta -Ra
Gambar 4.2b. Pengaruh Temperatur Terhadap Derajat Putih Rata-Rata ta (% IS O )
D1 1 - P D1 1.3 - P 90.5 91. 91. R a ta a ta (% 2 91.6 3 91.7 92.1 89.3 90.1 89.0 89.5 90.0 90.5 91.0 91.5 92.0 92.5
0 0.1 0.2 0.3 0.4 0.5
Dosis H2O2 (%)
D e ra ja t P u ti h -R I S O )
Pada temperatur reaksi 95 0C diperoleh pulp dengan derajat putih yang
rendah, setara dengan derajat putih pulp yang dihasilkan pada temperatur 65 0C. Hal
ini menguatkan pendapat sebelumnya bahwa pemutihan pulp pada temperatur yang
tinggi dan waktu reaksi yang lama menghasilkan pulp dengan derajat putih yang
rendah (Dence dan Reeve, 1996). Hal ini disebabkan karena pada temperatur tinggi
dapat mengaktifkan ion metal transisi seperti Fe, Mn dan Cu yang secara normal
terkandung dalam pulp. Ion metal transisi ini membentuk radikal OH. dan OOH. yang
dapat menurunkan derajat putih pulp (Dence dan Reeve, 1996).
Pada Gambar 4.2c dapat diketahui bahwa untuk semua dosis H2O2 pada
temperatur 75 0C menghasilkan derajat putih yang tidak jauh berbeda (rata-rata 0,3%
ISO) dengan pulp pada temperatur 85 0C. Namun pada temperatur 65 0C dan 95 0C
diperoleh derajat putih yang rendah. Hal ini berlaku untuk kedua jenis sampel pulp.
Derajat putih paling rendah yaitu 89,9% ISO diperoleh dari sampel D1 1 – P 0,1 yang
mempunyai dosis H2O2 paling kecil pada temperatur reaksi 95 0C, sedangkan derajat
putih yang paling tinggi yaitu 92,7% ISO dicapai oleh sampel D1 1,3 – P 0,4 pada
89.5 90.0 90.5 91.0 91.5 92.0 92.5 93.0
60 65 70 75 80 85 90 95 100
Temperatur (0C)
D
e
ra
ja
t Pu
ti
h
R
a
ta
-R
a
ta
(%
IS
O
)
D1 1 - P 0.1
D1 1 - P 0.2
D1 1 - P 0.4
D1 1.3 - P 0.1
D1 1.3 - P 0.2
[image:52.612.118.523.115.369.2]D1 1.3 - P 0.4
Gambar 4.2c. Pengaruh Faktor Dosis H2O2 dan Temperatur Terhadap Derajat Putih Pulp Rata-Rata
4.2.2. Penurunan Derajat Putih Pulp
Penurunan derajat putih pulp ditentukan dengan menghitung derajat putih
pulp yang hilang setelah pulp dipanaskan dalam oven selama 4 jam dan temperatur
105 0C (TAPPI T 260).
Pada Gambar 4.3 dapat dilihat bahwa pulp tahap D2 dan P yang memiliki
derajat putih yang sama mengalami penurunan derajat putih yang berbeda setelah
dipanaskan. Penurunan derajat putih pulp rata-rata tahap D2 lebih besar rata-rata 0,8
% ISO daripada tahap P sehingga pulp tahap P relatif lebih stabil. Hal ini sesuai
tidak efektif menghancurkan struktur karbonil dan kuinon penyebab penguningan
pada pulp, sedangkan H2O2 dapat memecahkan dan melarutkannya dengan baik.
90.9 90.9 90.9
91.7 91.7 91.7 91.6 91.6
92.1 92.1 92.1
89.4 89.5 88.7 89.0 88.1 88.7 89.0 88.2 88.2 88.1 87.4 85.0 86.0 87.0 88.0 89.0 90.0 91.0 92.0 93.0 D1 1/ D2 0. 2 D1 1/ P 0. 1/ 7 5 C D 1 1 /P 0 .2 /9 5 C D1 1/ D2 0. 4 D 1 1 /P 0 .4 /7 5 C D 1 1 /P 0 .2 /8 5 C D1 1. 3 /D2 0. 2 D1 1. 3 /P 0. 4 /65 C D1 1. 3/ D2 0. 4 D1 1. 3 /P 0. 2 /75 C D1 1. 3 /P 0. 1 /85 C Sampel Pulp D e ra ja t P u tih ( % IS O )
[image:53.612.116.526.166.586.2]Pulp yang diputihkan Pulp putih yang dipanaskan (T260)
Gambar 4.3. Penurunan Derajat Putih Pulp Tahap D2 dan P dengan Derajat Putih yang Sama
Gambar 4.4a dan 4.4b adalah grafik yang diperoleh dari pengolahan data
H2O2 berpengaruh terhadap penurunan derajat putih pulp. Penurunan derajat putih
semakin kecil seiring dengan pertambahan dosis H2O2. Pada dosis H2O2 0,1 %
dihasilkan pulp dengan penurunan derajat putih yang besar. Dosis H2O2 yang rendah
tidak cukup memadai untuk menghancurkan karbonil lignin dan kuinon yang menjadi
penyebab penguningan pada pulp dan kertas. Penurunan derajat putih terendah
diperoleh pada pulp dengan penambahan dosis H2O2 0,4%.
Penurunan derajat putih rata-rata pada sampel pulp D11,3-P lebih kecil dari
pada sampel D11-P. Hal ini disebabkan sampel pulp D11,3-P memiliki dosis ClO2
yang lebih besar pada tahap D1 sehingga kandungan lignin lebih banyak berkurang.
2.87 2.79 2.69 2.72 2.80 2.68 2.60 2.70 2.80 2.90
0 0.2 0.4 0.6
Dosis H2O2 (%)
P e n u ru n a n D e ra ja t P u ti h (% IS O)
D1 1 - P D1 1.3 - P
3.00 2.74 2.70 2.69 2.64 2.62 2.99 2.70 2.50 2.60 2.70 2.80 2.90 3.00 3.10
60 65 70 75 80 85 90 95 100
Temperatur (0C)
P e nur una n D e ra ja t P uti h (%I S O )
D1 1 - P D1 1.3 - P
[image:54.612.123.527.299.630.2]Gambar 4.4a. Pengaruh Faktor Dosis H2O2 Terhadap Penurunan Derajat Putih Pulp
Kandungan lignin yang lebih rendah menghasilkan pulp dengan derajat putih yang
lebih stabil.
Pada Gambar 4.4b dapat dilihat bahwa peningkatan temperatur pada proses
pemutihan pulp tahap P dapat mengurangi penurunan derajat putih. Pada temperatur
65 0C pulp mengalami penurunan derajat putih rata-rata yang besar yaitu 3,0 % ISO.
Pada temperatur yang relatif rendah anion perhidroksil yang dihasilkan tidak
maksimal menghancurkan struktur karbonil dan kuinon yang menjadi penyebab
penguningan pulp. Pada temperatur 75 0C penurunan derajat putih berkurang yaitu
menjadi 2,7% ISO. Kondisi ini tidak berubah secara signifikan sampai dengan
temperatur 95 0C. Hal ini menunjukkan bahwa mulai pada temperatur 75 0C
kandungan karbonil lignin dan kuinon sudah berkurang dan relatif tak berubah lagi
dengan penambahan temperatur.
4.2.3. Viskositas Pulp
Pada Gambar 4.5 dapat dilihat perbandingan viskositas pulp tahap D2 dan P.
Untuk semua dosis ClO2 viskositas pulp tahap D2 12,75 cP – 11,40 cP dan untuk
semua dosis H2O2 viskositas pulp tahap P 12,41 cP – 9,17 cP. Pada dosis yang sama,
pulp tahap P memiliki viskositas yang lebih rendah dibandingkan dengan tahap D2.
Hal ini disebabkan tingkat selektivitas H2O2 yang lebih rendah dari pada ClO2 yang
mengakibatkan sellulosa terdegradasi lebih banyak. Viskositas paling rendah
9.0 9.5 10.0 10.5 11.0 11.5 12.0 12.5 13.0 13.5 14.0 D 2 0. 2/ 7 5 C D 2 0. 4/ 75 C D 2 0. 7/ 75 C P 0. 1/ 65 C P 0. 1/ 75 C P 0. 1/ 85 C P 0. 1/ 95 C P 0. 2/ 65 C P 0 .2 /7 5 C P 0 .2 /8 5 C P 0 .2 /9 5 C P 0 .4 /6 5 C P 0 .4 /7 5 C P 0. 4/ 85 C P 0 .4 /9 5 C Sampel Pulp V isko si tas ( cP )
D0-E-D1 1% - D0ED1 1.3%
-Gambar 4.5. Viskositas Pulp tahap D2 dan P
Pada Gambar 4.6a dapat diketahui bahwa penambahan dosis H2O2
berpengaruh negatif terhadap viskositas pulp (hasil pengolahan data dengan program
minitab pada Lampiran 12). Semakin tinggi dosis H2O2 yang ditambahkan semakin
banyak selulosa yang terdegradasi sehingga viskositas pulp menjadi rendah.
Penurunan viskositas pulp untuk dosis H2O2 . Viskositas sampel D11-P dan D1 1,3-P
tidak berbeda secara signifikan pada tiap-tiap penambahan dosis H2O2. Viskositas
terendah diperoleh pada penambahan dosis H2O2 0.4% dan tertinggi pada dosis 0,1%.
Respon viskositas terhadap kenaikan temperatur dapat dilihat pada Gambar
4.6b (hasil pengolahan data dengan program minitab pada Lampiran 12). Viskositas
[image:56.612.118.525.115.381.2]menyebabkan viskositas pulp menurun. Pada temperatur tinggi proses dekomposisi
H2O2 berlangsung maksimal dan cepat sehingga penyerangan terhadap lignin dan
rantai selulosa semakin tinggi. Selain sifat H2O2 yang kurang selektif, dimungkinkan
perhidroksil radikal yang terbentuk berpotensi dalam mendegradasi sellulosa
sehingga viskositas pulp menjadi rendah. (Sjostrom, 1998 ; Fengel dan Gerd, 1989).
Pada tiap peningkatan temperatur viskositas, sampel D1 1-P dan D1 1,3-P tidak
berbeda secara signifikan.
4.2.4. Residu H2O2
Gambar 4.7a menunjukkan bahwa penambahan dosis H2O2 mengakibatkan
peningkatan residu H2O2 yang terkandung dalam filtrat hasil proses pemutihan pulp
[image:57.612.122.517.329.588.2]tahap P (hasil pengolahan data pada Lampiran 12). Residu rata-rata yang tertinggi Gambar 4.6a. Pengaruh Dosi
H2O2 Terhada Viskositas Pulp s p 12.16 .50 .27 11.82 .35 11.33 10.0 10.5 11.0 11.5 12.0 12.5
0 0.1 0.2 0.3 0.4 0.5
Dosis H2O2 (%)
V is ko s R at a-R at a (cP )
Ga bar 4.6b. Pengaruh Temperatur Terhadap Viskositas Pulp m 10 10 11 it as
D1 1 - P D1 1.3 - P
12.01 11.35 10.40 17 . 11.40 11.84 10.0 10.5 11.0 11.5 12.0 12.5
60 65 70 75 80 85 90 95 100
Temperatur (0C) V isko as R a ta-R at a (cP ) 11. 11.21 10 53 si t
D1 1 - P D1 1.3 - P
Gambar 4.6a. Pengaruh Dosis H2O2 Terhadap Viskositas Pulp Tahap P
diperoleh pada dosis H2O2 0,4%. Hal ini dimungkinkan karena H2O2 yang tersedia
melebihi kebutuhan untuk bereaksi dengan lignin sehingga menghasilkan residu yang
tinggi. Kondisi ini tidak menguntungkan karena banyak H2O2 yang terbuang. Residu
yang besar memberikan indikasi proses pemutihan yang kurang efektif. Sampel pulp
D1 1-P menghasilkan residu H2O2 rata-rata yang lebih rendah kurang lebih 0,01 g/L
dari pada sampel pulp D1 1,3-P. Pada Sampel pulp D1 1-P mengandung lebih banyak
lignin pada tahap D1 (terbukti dari derajat putih yang lebih rendah) sehingga
[image:58.612.133.506.340.595.2]konsumsi H2O2 lebih banyak pada tahap P.
Gambar 4.7a. Pengaruh Dosis H2O2 Terhadap Residu H2O2 Tahap P
Gambar 4.7.b Pengaruh Temperatur Terhadap Residu H2O2 Tahap P 0.13 0.05 0.02 0.02 0.14 0.07 0.04 0.01 0.00 0.02 0.04 0.06 0.08 0.10 0.12 0.14 0.16
60 65 70 75 80 85 90 95 100 Tem peratur (0C)
R e s idu H 2 O2 R a ta -R a ta (g/ l)
D1 1 - P D1 1.3 - P 0.03 0.05 0.08 0.04 0.06 0.09 0.02 0.04 0.06 0.08 0.10
0 0.1 0.2 0.3 0.4 0.5
Dos is H2O2 (%)
R e s idu H 2 O2 R a ta -R a ta (g/ l)
D1 1 - P D1 1.3 - P
Gambar 4.7b menunjukkan pengaruh temperatur yang signifikan terhadap
residu H2O2 . Peningkatan temperatur dapat mengurangi residu H2O2. Pada
konsumsi H2O2 dalam hal ini adalah anion perhidroksil juga meningkat. Akhirnya
setelah proses pemutihan selesai hanya meninggalkan sedikit residu H2O2.
Untuk mengefektifkan konsumsi H2O2 penambahan dosis harus diikuti
dengan peningkatan temperatur reaksi. Pada temperatur yang rendah (65 0C) reaksi
dekomposisi H2O2 berlangsung lambat sehingga pada saat reaksi dihentikan (setelah
180 menit) masih banyak terdapat H2O2 yang belum terdekomposisi. Hal ini
menyebabkan residu yang tinggi pada temperatur yang rendah terutama pada dosis
H2O2 yang tinggi. Sebaliknya pada temperatur tinggi hampir semua H2O2
terdekomposisi sehingga residu H2O2 pada akhir proses pemutihan menjadi rendah.
Jadi residu H2O2 yang paling rendah diperoleh pada sampel pulp dengan dosis H2O2
yang paling kecil (0,1%) dan temperatur paling besar (95 0C). Sebaliknya residu H2O2
yang tinggi diperoleh pada dosis H2O2 yang tinggi (0,4%) dan temperatur yang
rendah (65 0C).
4.2.5. Kekuatan Kertas - Indeks Sobek (Tear Index)
Gambar 4.8a dan 4.8b adalah grafik indeks sobek rata-rata kertas tahap D2 dan
P. Indeks sobek rata-rata diambil dari data indeks sobek kertas yang dihasilkan pada
temperatur pemutihan pulp 75 0C dan 85 0C.
Pada Gambar 4.8a dan 4.8b dapat dilihat perbandingan indeks sobek pulp
tahap P dan D2. Dari grafik tersebut dapat diketahui bahwa indeks sobek tahap P lebih
(besar sama) dengan indeks sobek tahap D2 pada tiap revolusi. Indeks sobek yang
paling rendah pada tiap revolusi diperoleh pada sampel tahap D2 dengan dosis ClO2
terbesar (0,7%). 2 3 4 5 6 7 8 9 10
0 1000 2000 3000 4000 5000
Revolusi (rpm) In d eks so b ek ( m N m 2/g
D1 1 - P 0.1 D1 1 - P 0.2 D1 1 - P 0.4 D1 1 - D2 0.2 D1 1 - D2 0.4 D1 1 - D2 0.7
2 3 4 5 6 7 8 9 10
0 1000 2000 3000 4000 5000
Revolusi (rpm) In d e ks so b ek ( m N m 2/g
[image:60.612.130.511.217.590.2]D1 1.3 - P 0.1 D1 1.3 - P 0.2 D1 1.3 - P 0.4 D1 1.3 - D2 0.2 D1 1.3 - D2 0.4 D1 1.3 - D2 0.7
[image:60.612.341.510.223.528.2]Gambar 4.8a. Indeks Sobek Kertas Tahap D2 dan P dari D1 1%
Gambar 4.8b. Indeks Sobek Kertas Tahap D2 dan P dari D1 1,3%
Gambar 4.9a menunjukkan bahwa penambahan dosis bahan pemutih yang
besar menghasilkan kertas dengan indeks sobek yang rendah karena bahan pemutih
selain menyerang lignin juga mendegradasi selulosa sehingga kertas yang dihasilkan
Gambar 4.9b menunjukkan bahwa indeks sobek memberikan respon positif
terhadap kenaikan temperatur. Pada temperatur 85 0C diperoleh indeks sobek yang
lebih tinggi dari pada indeks sobek pada temperatur 75 0C dengan kenaikan 0,4
mNm2/g untuk sampel D1 1-P dan 0,2 mNm2/g untuk sampel D1 1,3-P. Sampel D1
1-P mempunyai indeks sobek yang lebih tinggi daripada sampel D1 1,3-1-P.
7.30 7.10 7.05 6.55 7.06 7.10 6.4 6.6 6.8 7.0 7.2 7.4
0 0.2 0.4 0.6
Dosis H2O2 (%)
In d e ks S o b e k ( m N m 2/g )
D1 1 - P D1 1.3 - P
6.98 7.33 6.81 6.99 6.7 6.8 6.9 7.0 7.1 7.2 7.3 7.4
70 75 80 85 90
Tem peratur (0C)
In d eks S o b ek ( m N m 2/g )
[image:61.612.126.513.266.458.2]D1 1 - P D1 1.3 - P
Gambar 4.9a. Pengaruh Dosis H2O2 Terhadap Indeks Sobek
Gambar 4.9b. Pengaruh Temperatur Terhadap Indeks Sobek
- Indeks Tarik (Tensile Index)
Gambar 4.10a dan 4.10b adalah grafik indeks tarik rata-rata kertas tahap D2
dan P. Indeks tarik rata-rata diambil dari data indeks tarik kertas yang dihasilkan pada
[image:61.612.330.515.269.456.2]Gambar 4.10a dan 4.10b menunjukkan bahwa indeks tarik tahap P lebih
tinggi dari pada tahap D2 terutama pada dosis H2O2 dan ClO2 yang sama. Indeks tarik
tertinggi untuk tiap revolusi beating dicapai oleh sampel D11–P 0,1 dan D11,3–P 0,1
2 12 22 32 42 52 62 72 82 92
0 1000 2000 3000 4000 5000
Revolusi (rpm) Inde k s Ta ri k ( N m/ g)
D1 1 - P 0.1 D1 1 - P 0.2
D1 1 - P 0.4 D1 1 - D2 0.2
D1 1 - D2 0.4 D1 1 - D2 0.7
2 12 22 32 42 52 62 72 82 92
0 1000 2000 3000 4000 5000
Revolusi (rpm) Inde k s Ta ri k ( N m /g )
D1 1.3 - P 0.1 D1 1.3 - P 0.2 D1 1.3 - P 0.4 D1 1.3 - D2 0.2 D1 1.3 - D2 0.4 D1 1.3 - D2 0.7
Gambar 4.10a. Indeks Tarik Kertas Tahap D2 dan P dari D1 1%
Gambar 4.10b. Indeks Tarik Kertas Tahap D2 dan P dari D1 1,3%
Respon indeks tarik terhadap dosis H2O2 ditunjukkan oleh Gambar 4.11a.
Dari gambar tersebut diketahui bahwa penambahan dosis H2O2 dapat menurunkan
indeks tarik pulp, sehingga indeks tarik terendah diperoleh pada dosis H2O2 yang
menurunkan kekuatan kertas dalam hal ini indeks tarik. Kondisi ini disebabkan
karena sebagian selulosa ikut terdegradasi bersama lignin sehingga kertas menjadi
[image:63.612.114.520.305.532.2]rapuh.
Gambar 4.11b menunjukkan bahwa peningkatan temperatur dari 750C ke
850C dapat meningkatkan indeks tarik kertas dengan kenaikan indeks tarik sebesar
1,27 Nm/g untuk sampel D11–P dan 3,76 Nm/g untuk sampel D11,3–P.
57.91 56.94 56.4 55.61 57.98 57.08 55.0 55.5 56.0 56.5 57.0 57.5 58.0 58.5
0 0.2 0.4 0.6
Dosis H2O2 (%)
In de k s Ta ri k ( N m /g)
D1 1 - P D1 1.3 - P
56.5 57.7 55.0 58.8 54.0 55.0 56.0 57.0 58.0 59.0
70 75 80 85 90
Tem peratur (0C)
In d eks T a ri k (N m /g )
D1 1 - P D1 1.3 - P
Gambar 4.11a. Pengaruh Dosis H2O2 Terhadap Indeks Tarik
Gambar 4.11b. Pengaruh Temperatur Terhadap Indeks Tarik
4.2.6. Perbandingan Nilai Ekonomi
Perhitungan biaya pemutihan pulp tahap D2 dan P dilakukan berdasarkan
digunakan pada masing-masing percobaan pemutihan pulp tahap D2 dan P adalah
[image:64.612.105.530.221.585.2]seperti pada Tabel 4.2.
Tabel 4.2. Biaya Kebutuhan Bahan Kimia Pemutihan Pulp Tahap D2 dan P
No Sampel Pulp Derajat Putih
(% ISO)
Total ClO2
(Kg/ton pulp)
H2O2
Kg/ton pulp) NaOH Kg/ton pulp) Biaya (USD/ton pulp)
1 D11-D2 0,2 90,9 12 0 0,6 4,795
2 D11-D2 0,4 91,7 14 0 1,1 5,702
3 D11-D2 0,7 92,1 17 0 1,8 7,050
4 D11-P 0,1 / 65 90,2 10 1 3,0 5,487
5 D11-P 0,2 / 65 90,8 10 2 3,0 6,301
6 D11-P 0,4 / 65 91,2 10 4 3,5 8,065
7 D11-P 0,1 / 75 90,9 10 1 3,0 5,487
8 D11-P 0,2 / 75 91,4 10 2 3,0 6,301
9 D11-P 0,4 / 75 91.7 10 4 3,5 8,065
10 D11-P 0,1 / 85 90,8 10 1 3,0 5,487
11 D11-P 0,2 / 85 91,7 10 2 3,0 6,301
12 D11-P 0,4 / 85 92,0 10 4 3,5 8,065
13 D11-P 0,1 / 95 89,9 10 1 4,0 5,758
14 D11-P 0,2 / 95 90,9 10 2 4,5 6,708
15 D11-P 0,4 / 95 91,5 10 4 5,5 8,607
16 D11,3-D2 0,2 91,6 15 0 0,3 5,871
17 D11,3-D2 0,4 92,1 17 0 0,8 6,779
18 D11,3-D2 0,7 92,8 20 0 1,5 8,127
19 D11,3-P 0,1 / 65 90,6 13 1 3,0 6,645
20 D11,3-P 0,2 / 65 91,0 13 2 3,0 7,459
21 D11,3-P 0,4 / 65 91,6 13 4 3,5 9,223
22 D11,3-P 0,1 / 75 91,8 13 1 3,0 6,645
23 D11,3-P 0,2 / 75 92,1 13 2 3,0 7,459
24 D11,3-P 0,4 / 75 92,5