BIOTRANSFORMASI BERBERIN OLEH JAMUR ENDOFIT DARI TUMBUHAN AKAR KUNING (Arcangelisia flava (L.) Merr:
MENISPERMACEAE)
SKRIPSI
Diajukan sebagai salah satu syarat untuk
memperoleh gelar Sarjana Farmasi (S. Far)
Oleh:
SUVRELA ARTIANI
106102003374
PROGRAM STUDI FARMASI
FAKULTAS KEDOKTERAN DAN ILMU KESEHATAN
UNIVERSITAS ISLAM NEGERI SYARIF HIDAYATULLAH
i
LEMBAR PERSETUJUAN SKRIPSI
NAMA : SUVRELA ARTIANI
NIM : 106102003374
JUDUL :BIOTRANSFORMASI BERBERIN OLEH JAMUR ENDOFIT DARI TUMBUHAN AKAR KUNING ( Arcangelisia
flava (L.) Merr: MENISPERMACEAE)
Telah Disetujui Oleh :
Pembimbing I Pembimbing II
Dr. Andria Agusta Zilhadia, M.Si., Apt NIP.196908161994031003 NIP.197308222008012007
Mengetahui,
Ketua Program Studi Farmasi
Fakultas Kedokteran dan Ilmu Kesehatan
UIN Syarif Hidayatullah Jakarta
ii
LEMBAR PERNYATAAN
Dengan ini saya menyatakan bahwa skripsi yang berjudul:
BIOTRANSFORMASI BERBERIN OLEH JAMUR ENDOFIT DARI TUMBUHAN AKAR KUNING (Arcangelisia flava (L.) Merr: MENISPERMACEAE)
Adalah karya saya sendiri dan belum pernah diajukan dalam bentuk apapun kepada perguruan tinggi manapun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun yang tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam daftar pustaka
iii
LEMBAR PENGESAHAN SKRIPSI
Skripsi Dengan Judul
BIOTRANSFORMASI BERBERIN OLEH JAMUR ENDOFIT DARI TUMBUHAN AKAR KUNING (Arcangelisia flava (L.) Merr:
MENISPERMACEAE)
Telah disetujui, diperiksa, dan dipertahankan dihadapan tim penguji oleh:
Nama : Suvrela Artiani NIM : 106102003374
Menyetujui,
Pembimbing
1. Pembimbing I Dr.Andria Agusta ………
2. Pembimbing II Zilhadia,M.Si.,Apt ………
Penguji
1. Ketua Penguji M.Yanis Musdja M.Sc.,Apt ……..………...……
2. Anggota Penguji I M.Yanis Musdja M.Sc.,Apt ……….
3. Anggota Penguji II Ofa Suzanti Betha,M.Si.,Apt ……….………
4. Anggota Penguji III Azrifitria,M.Si.,Apt ……….
Mengetahui,
Dekan Fakultas Kedokteran dan Ilmu Kesehatan UIN Syarif Hidayatullah
Jakarta
Prof.DR (hc). Dr. M.K Tadjudin, Sp.And
iv
KATA PENGANTAR
Bismillahhirrahmaanirrahiim,
Alhamdulillah, puji syukur penulis panjatkan kehadirat Allah SWT atas berkah,
rahmat, dan ridha-Nya sehingga penulis dapat menyelesaikan skripsi yang
berjudul “Biotransformasi Beberin Oleh Jamur Endofit Dari Tumbuhan Akar Kuning (Arcangelisia flava (L.) Merr: MENISPERMACEAE)”. Shalawat serta salam tidak lupa penulis sampaikan kepada Nabi Muhammad SAW beserta
keluarga dan para sahabatnya, semoga kita dapat memperoleh syafaatnya dihari
akhir.
Dalam penulisan skripsi ini penulis banyak mendapatkan doa, bantuan,
bimbingan, dan dorongan dari berbagai pihak. Oleh karena itu, pada kesempatan
ini penulis mengucapkan terima kasih kepada:
1. Bapak Dr. Andria Agusta selaku pembimbing I yang telah banyak mengajarkan
ilmu, memberikan arahan, nasehat, motivasi dan dengan penuh kesabaran
memberikan bimbingan selama penulis melaksanakan penelitian dan menyusun
skripsi. Serta telah memberikan kesempatan kepada penulis untuk dapat
melakukan penelitian di Laboratorium Fitokimia, Puslit Biologi LIPI Cibinong.
2. Ibu Zilhadia M.Si., Apt. selaku pembimbing II yang telah mengajarkan ilmu,
memberikan arahan, nasehat, motivasi, dan dengan penuh kesabaran
membimbing selama penulis melaksanakan penelitian dan penyusunan skripsi.
3. Bapak Prof.DR.(hc).dr.M.K. Tadjudin, Sp.And selaku Dekan Fakultas
Kedokteran dan Ilmu Kesehatan yang telah memberikan kesempatan kepada
penulis untuk melakukan penelitian.
4. Bapak Drs. M. Yanis Musdja, M.Sc., Apt. selaku Ketua Jurusan Farmasi UIN
Syarif Hidayatullah Jakarta yang memberikan telah memberikan kesempatan
penulis untuk melaksanakan penelitian skripsi.
5. Ayahanda H.Abdul Hamid, S.H. dan Ibunda Rasmihandani, S.E. serta
adik-adik tersayang Ina dan Fita yang telah memberikan doa, dukungan moril dan
v
6. Ibu Ofa Suzanti Betha, M.Si.,Apt. selaku pembimbing akademik penulis yang
telah memberikan nasihat dan motivasi selama penulis menjalani pendidikan di
Program Studi Farmasi UIN Syarif Hidayatullah Jakarta.
7. Dosen – dosen beserta karyawan Farmasi UIN Syarif Hidayatullah Jakarta yang penulis hormati yang telah memberikan motivasi, nasehat, mengajarkan
ilmu kepada penulis sehingga penulis bisa menyelesaikan perkuliahan di
Program Studi Farmasi UIN Syarif Hidayatullah Jakarta.
8. Ibu Yuliasri, Ibu Hertina, Kak Asep, Kak Toni yang telah membantu penulis
selama melakukan penelitian di Laboratorium Fitokimia, Puslit Biologi LIPI
Cibinong.
9. Eka W, Wida, Syifa, Amalia, Dani, Shobir, Ardian serta teman –teman farmasi angkatan 2006 dan kakak-kakak kelas yang telah banyak memberikan doa,
dukungan selama penulis kuliah dan menyusun skripsi. Dan juga Eka P.P. serta
Baun A.Md.,RO. yang telah banyak memberikan doa, dukungan dan
mengajarkan kesabaran selama penelitian dan penyusunan skripsi ini.
10. Yaya, Omi, Dini Fris, Dini Mai, Reza, Emil, Rijal yang telah memberikan doa,
motivasi, serta bantuan selama penulis melakukan penelitian dan menyusun
skripsi.
11. Semua pihak yang telah membantu penulis sehingga dapat menyelesaikan
skripsi ini.
Semoga bantuan yang diberikan menjadi amal saleh bagi kita semua dan
mendapat balasan dari Allah SWT. Semoga skripsi ini bisa bermanfaat kepada
siapa saja terutama yang membacanya. Tiada kata terhenti sampai disini karena
ilmu seseorang harus bertambah seiring berjalannya waktu dan penulis
mengharapkan kritik dan saran yang membangun demi kesempurnaan skripsi ini.
Terima Kasih.
Jakarta, Juli 2010
vi
ABSTRAK
BIOTRANSFORMASI BERBERIN OLEH JAMUR ENDOFIT DARI TUMBUHAN AKAR KUNING (Arcangelisia flava (L.) Merr:
MENISPERMACEAE)
Jamur endofit merupakan kelompok jamur yang hidup di dalam jaringan
tumbuhan seperti akar, batang, dan daun. Jamur endofit memiliki kemampuan
untuk menghasilkan metabolit sekunder dan ada juga yang mampu melakukan
proses biotransformasi suatu senyawa. Jamur endofit AFKR–5 yang diisolasi dari tumbuhan akar kuning (Arcangelisia flava (L.)Merr MENISPERMACEAE) mampu melakukan biotransformasi berberin pada medium GYP. Jamur endofit
AFKR–5 ditumbuhkan dalam medium GYP 5x200 ml selama 4 hari kemudian ditambahkan berberin 5x20 ml dengan konsentrasi 1 mg dalam 1 ml metanol.
Setelah dua minggu kultur jamur kemudian diekstrak menggunakan diklorometan
: metanol = 5:1 kemudian dipartisi dengan n-heksana lalu dikeringkan dengan
rotary evaporator sehingga diperoleh ekstrak sebanyak 210,2 mg. Fraksinasi ekstrak dilakukan dengan kromatografi kolom menggunakan fase diam sephadex
LH-20 dan eluen metanol 90 % sehingga didapatkan satu fraksi yang mengandung
produk biotransformasi dan substrat berberin. Purifikasi lebih lanjut dengan KLT
preparatif (adsorben silica gel 60 F254 dan eluen diklorometan : metanol :
amoniak = 5:3:0,5) menghasilkan dua fraksi (F 1.A dan F 1.B). Produk hasil
biotransformasi terdapat difraksi F 1.A (28,5 mg) dan dianalisis menggunakan
MS.
vii
ABSTRACT
BIOTRANSFORMATION OF BERBERINE BY ENDOPHYTIC FUNGI FROM AKAR KUNING (Arcangelisia flava (L.) Merr:
MENISPERMACEAE)
Endophytic fungi is a fungi group living inside of plant tissue like roots, stems, and leaves. Endophytic fungi show their ability to produce secondary metabolites. Some of them are able to biotransform a chemical compound into their derivative. Endophytic fungus AFKR-5 isolated from the roots of akar kuning plant (Arcangelisia flava (L.) Merr) is able to perform biotransformation process of berberine in GYP medium. Endophytic fungus AFKR-5 was grown in five erlenmeyer (500 ml) containing 200 ml of GYP medium. After grew for 4 days, 20 ml of berberine (1 mg/ml methanol) was added into cultivation medium. After two weeks, all of fungal culture extracted with dichloromethane: methanol (5:1) and then partitioned with n-hexane, and then dried under reduce pressure to obtain 210.2 mg brownish extract. Furthermore, the extract was subjected into sephadex LH-20 column chromatography (275 ml) dan eluted with methanol 90%. The biotransformation product and berberine containing fraction was further purify through preparative TLC (silica gel 60 F254 adsorbent and eluent dichloromethane:
methanol: ammonia = 5:3:0,5) to yielded F 1.A (28.5 mg) and F 1. B ( 11,9 mg). Biotransformation products was then analyzed by using Mass Spectroscopy.
viii
2.1.4 Kandungan Kimia Tumbuhan..…….……….
2.1.5 Manfaat dan Kegunaan Tumbuhan...……….
2.2Jamur Endofit...……… ……….
2.3Isolasi Jamur Endofit...……….….
2.4Biotransformasi...………...………..…
4.1Tempat dan Waktu Penelitian……….
ix
4.3.1.3 Kultivasi Jamur Endofit... 4..3.1.4 Penambahan Substrat Pada Kultur... 4.3.1.5 Monitoring Hasil Biotransformasi ... 4.3.1.6 Ekstaksi Kultur Jamur Endofit... 4.3.2 Scalling Up Proses Biotransformasi.……….………..
4.3.2.1 Pembuatan Medium Kultivasi………... 4.3.2.2 Kultivasi Jamur Endofit AFKR-5 ……….. 4.3.2.3 Penambahan Substrat Pada Kultur Jamur AFKR-5.…… 4.3.2.4 Monitoring Hasil Biotransformasi……… 4.2.3.5 Ekstraksi Kultur Jamur Endofit AFKR-5……….. 4.3.2.6 Partisi Ekstrak Hasil Biotransformasi AFKR-5………… 4.3.2.7 Fraksinasi Hasil Biotransformasi AFKR-5……….……. 4.3.2.8 Purifikasi Produk Biotransformasi………. 4.3.2.9 Karakterisasi Hasil Produk Biotransformasi
Dengan Spektrofotometer Massa………...
BAB V
HASIL DAN PEMBAHASAN
x
DAFTAR GAMBAR
Halaman
Gambar 1. Tumbuhan Arcangelisia flava (L.) Merr……… 5 Gambar 2. Struktur senyawa dari (a) berberin, (b) jatorrhizin,
(c) palmatin, (d) kolumbamin………... 7 Gambar 3. Reaksi biotransformasi (-)-epikatekin menjadi
(-)-(2R,3S)-dihidrokuersetin oleh jamur endofit
(Diaporthesp)………. 12
Gambar 4. Reaksi biotransformasi kuinin menjadi kuinin-1-N-oksida
oleh jamur endofit Xylariasp………... 12
Gambar 5. Struktur Kimia Berberin ………. 15
Gambar 6. Profil kromatogram KLT ekstrak diklorometan-metanol dari kultur jamur endofit AFKR-2, 3, 5, dan 13
pada medium GYP dan PDB saat 14 hari penambahan berberin. (fase diam silica gel 60 F254, fase gerak
diklorometan : metanol = 6:1 ditambahkan 1 tetes asam asetat.S=berberin; C=blanko medium; 2,3,5,13=AFKR-2,3, 5,13 (a) sinar UV 254 nm, (b)sinar UV 366 nm
(pada medium GYP),(c) sinar UV 245 nm,
(d) sinar UV 366 nm (pada medium PDB)……… 29
Gambar 7. Profil ktomatogram KLT ekstrak diklorometan – metanol kultur jamur endofit AFKR-5 pada medium GYP. (S = berberin, 1 = AFKR–5 ditambahkan berberin, 2 = AFKR-5 tanpa penambahan berberin),
(a) UV 254 nm, (b) UV 366 nm……… 31 Gambar 8. Jamur endofit AFKR–5 pada medium PDA (a) satu
minggu, (b) dua minggu……… 32
Gambar 9. Kultur jamur endofit AFKR – 5 pada medium glucose yeast-ekstrak pepton (GYP). (a) saat kultivasi, (b) 4 hari kultivasi (sebelum penambahan berberin), (c) 1 hari, (d) 10 hari, (e) 14 hari
(telah ditambahkan berberin)………. 33 Gambar 10.Hasil kromatogram HPLC menggunakan kolom Capcell
pak C-18 (Shiseido 4,5 mm x 260 mm), fase diam air millipore : asetonitril = 90 %: 10%,
laju alir : 1 ml/menit, lama aliran 30 menit,
xi
penambahan berberin………. 34
Gambar 11.Profil kromatogram KLT kultur jamur endofit AFKR-5 pada medium GYP (a) di bawah sinar UV 254 nm,
(b) di bawah sinar UV 366 nm (10 hari penambahan berberin), (c) di bawah sinar UV 254 nm, (d) di bawah sinar UV 366 nm (14 hari penambahan berberin). S = berberin,
E = ekstrak jamur………. 35 Gambar 12. Profil kromatogram KLT hasil purifikasi fase satu.
Fase diam silica gel 60 F254 dan fase gerak diklrometan
: metanol=6:1 (7 ml) ditambah asam asetat 1 tetes(1-A = atas, 1-B = bawah). (a) UV 254 nm, (b) UV 366 nm,
(c) disemprot dragendroff……… 37
Gambar 13.Hasil spektrum produk biotransformasi
menggunakan spektrofotometer massa MS Water LCT
xii
DAFTAR TABEL
Tabel 1. Hasil fraksinasi dengan kromatografi kolom dari ekstrak diklorometan–metanol biotransformasi kultur AFKR–5
pada medium GYP ………. 36
Tabel 2. Hasil purifikasi fraksi 1 ekstrak diklorometan – metanol dengan fase gerak diklorometan : metanol = 6:1 (7 ml) ditambah asam
xiii
DAFTAR LAMPIRAN
Lampiran 1. Komposisi medium yang digunakan ……… 43
Lampiran 2. Skema Kerja
2.1 Skrining Biotransformasi ………. 44
2.2 Scalling up Proses Biotransformasi Berberin Oleh
Jamur AFKR-5 ………. 45
2.3 Ekstraksi Hasil Biotransformasi ………. 46
2.4Partisi Ekstrak Hasil Biotransformasi ………. 47 2.5 Fraksinasi,Purifikasi,dan Karakterisasi
Hasil Biotransformasi ………. 47
Lampiran 3. Gambar jamur endofit AFKR–2 ,3 ,5, dan 13
yang digunakan untuk skrining proses biotransformasi………. .. 48 Lampiran 4. Hasil perbesaran spektrum produk biotransformasi
menggunakan MS Water LCT Premier Xe Micromass
Technology ………....… 49
Lampiran 5. Hasil perbersaran spektrum produk biotransformasi menggunakan MS Water LCT Premier Xe Micromass
1
BAB I
PENDAHULUAN
1.1Latar Belakang
Akar kuning atau yang memiliki nama latin Arcangelisia flava (L.)
Merr secara empiris telah banyak digunakan dalam pengobatan alami untuk
mengatasi gangguan pencernaan dan digunakan sebagai pembersih luka
(Unesco, 1998). Tumbuhan ini banyak terdapat di Cina, Thailand, Malaysia,
dan berbagai pulau di Indonesia seperti Kalimantan, Sumatera, dan Jawa
(Unesco, 1998). Telah dilakukan penelitian terhadap tumbuhan kayu kuning
ini dan menunjukkan bahwa infus batang akar kuning memiliki efek antidiare
terhadap tikus putih serta dapat mengurangi kontraksi otot polos usus marmut
(Sa’roni et al., 1995). Salah satu senyawa utama yang terdapat pada batang tumbuhan Arcangelisia flava (L.) Merr adalah berberin (Verpoorte et al., 1982).
Berberin merupakan alkaloid berwarna kuning yang terdapat di
akar, batang, rhizoma dari berbagai tanaman seperti Hydrastic canadensis,
Coptis chinensis, Berberis aquifolium, Beberis vulgaris, dan Berberis
aristata. Banyak penelitian dilakukan untuk membuktikan kegunaan berberin. Berberin menunjukkan aktivitas antimikroba, seperti dalam melawan bakteri,
virus, jamur, serta protozoa (Dharmananda, 2005). Berberin menunjukkan
aktivitas bakterisid terhadap V. cholera pada konsentrasi 35 µg/ml dan
2
tumor (Issat, et al., 2006). Begitu banyak manfaat berberin dalam kehidupan
sehingga perlu dilakukan penelitian lebih lanjut mengenai senyawa ini, salah
satunya dengan mengetahui transformasi dari berberin.
Mikroorganisme merupakan makhluk hidup yang tidak bisa lepas dari
kehidupan manusia. Beragam mikroorganisme dapat membantu dalam
kehidupan manusia, salah satunya adalah mikroba endofit. Salah satu dari
mikroba endofit tersebut adalah jamur endofit, yang memiliki kemampuan
untuk menghasilkan senyawa metabolit sekunder. Seperti pada jamur endofit
Apiospora montagnei yang diisolasi dari Polysiphonia violacea yang mampu menghasilkan senyawa diterpenmirocin, (+)-asam heksilitakonik dalam
medium semisintetik (Klemke et al., 2004). Selain dapat menghasilkan senyawa metabolit sekunder, jamur endofit ada yang memiliki kemampuan
untuk melakukan biotransformasi metabolit sekunder. Seperti pada jamur
endofit Diaporthe sp. dari tumbuhan teh yang dapat melakukan biotransformasi (-)-epigalokatekin-3-O-galat menjadi (-)-2R,3S -dihidromirisetin (Agusta, 2007).
Pada tumbuhan Arcangelisia flava (L.) Merr terdapat jamur endofit yang memiliki kemampuan untuk melakukan proses transformasi berberin
menjadi turunannya. Telah dilakukan skrining biotransformasi berberin oleh
16 isolat jamur endofit yang diisolasi dari tumbuhan Arcangelisia flava (L.) Merr pada medium GYP. Dari skrining tersebut terdapat beberapa isolat
jamur yang dapat melakukan reaksi transformasi berberin yaitu AFKR-1, 2, 3,
7, 10, 13, 15, dan 16. Dari 8 isolat jamur endofit tersebut, dipilih dua isolat
3
dan AFKR-3 untuk kemudian ditumbuhkan dalam skala besar pada medium
glucose yeast-extract peptone (GYP) dan potato dextro broth (PDB) (Mahesa, 2009). Untuk itu perlu dilakukan penelitian lebih lanjut untuk
mencari jenis jamur endofit selain AFKR-1,3 dari tumbuhan Arcangelisia flava (L.) Merr yang memiliki kemampuan untuk mengubah struktur berberin. Dengan dilakukannya penelitian ini diharapkan dapat diketahui
jamur endofit lainnya dari Arcangelisia flava (L.) Merr yang memiliki kemampuan untuk mengubah struktur kimia berberin.
1.2 Perumusan Masalah
1. Apakah jamur endofit selain AFKR-1,3 yang diisolasi dari tumbuhan
Arcangelisia flava (L.) Merr dapat melakukan biotransformasi terhadap senyawa berberin?
2. Bagaimanakah kondisi reaksi biotransformasi oleh jamur endofit yang
diisolasi dari tumbuhan Arcangelisia flava (L.) Merr?
3. Bagaimana mengisolasi dan mengkarakterisasi produk hasil
biotransformasi berberin?
4. Bagaimana struktur kimia produk biotransformasi berberin?
1.3 Hipotesis
Berberin dapat dibiotransformasi menjadi produk turunannya dengan
4
1.4 Tujuan Penelitian
Penelitian ini bertujuan untuk:
1.Menskrining jamur endofit selain AFKR-1,3 yang diisolasi dari
Arcangelisia flava (L.) Merr yang mampu melakukan biotransformasi senyawa berberin.
2.Mengetahui kondisi reaksi biotransformasi oleh jamur endofit yang diisolasi
dari Arcangelisia flava (L.) Merr.
3.Mengetahui bagaimana mengisolasi dan mengkarakterisasi produk hasil
biotransformasi berberin.
4.Mengetahui struktur kimia produk hasil biotransformasi berberin.
1.5 Manfaat Penelitian
Hasil penelitian ini diharapkan dapat memberikan informasi mengenai
jamur endofit mana yang dapat melakukan biotransformasi berberin pada
suatu kondisi, serta dapat mengetahui bagaimana perubahan struktur kimia
hasil biotransformasi senyawa berberin oleh mikroorganisme jamur endofit
5
BAB II
TINJAUAN PUSTAKA
2.1Tumbuhan Akar Kuning ( Arcangelisia flava (L.) Merr )
Gambar 1. Tumbuhan Arcangelisia flava (L.) Merr. (www.stuartxchange.com)
2.1.1 Klasifikasi (www.plantamor.com)
Tumbuhan yang secara empiris banyak digunakan untuk mengatasi
gangguan pencernaan ini juga telah dikenal memberikan manfaat dalam
pengobatan secara alami. Secara taksonomi Arcangelisia flava (L.) Merr dapat diklasifikasikan:
Kingdom : Plantae
Subkingdom : Tracheobionta
Superdivisi : Spermatophyta
Divisi : Magnoliophyta
Kelas : Magnoliopsida
SubKelas : Magnoliidae
6
Famili : Menispermaceae
Genus : Arcangelisia
Spesies : Arcangelisia flava (L.) Merr
2.1.2 Sinonim (Unesco, 1998)
Arcangelisia lemniscata ( Miers) Becc, Arcangelisia loureiri (Pierre) Diels
2.1.3 Nama daerah Indonesia (Unesco, 1998)
Areuy ki koneng (Sunda), sirawan (Jawa), daun bulan (Maluku)
2.1.4 Kandungan Kimia Tumbuhan
Tumbuhan Archangelisia flava (L.) Merr memiliki berbagai kandungan kimia. Pada batang tumbuhan ini terkandung senyawa furanoditerpen
seperti 6-hydroxyarchangelisin, 2-dehydroarchangelisinol, tynophyloll,
6-hydroxyfibleucin, fibleucin, fibraurin, serta 6-hidroksifibraurin
(Toshinobu et al., 1985). Selain furanoditerpen, pada batang tumbuhan
ini juga terkandung alkaloid seperti berberin, jatorrhizin, palmatin dan
7
2.1.5 Manfaat dan Kegunaan Tumbuhan
Tumbuhan akar kuning banyak digunakan dalam pengobatan tradisional
untuk mengatasi gangguan saluran cerna, sebagai ekspektoran, serta
tonik. Dekok dari batang tumbuhan ini digunakan untuk mengatasi sakit
kuning, cacingan, serta diare. Selain itu, dekok dari batang tumbuhan
ini dapat digunakan untuk membersihkan luka, koreng. Getah dari
tumbuhan ini diminum untuk mengatasi demam sedangkan bunga dari
tumbuhan ini digunakan untuk mengatasi disentri (Unesco, 1998).
2.2 Jamur Endofit
Mikroorganisme merupakan makhluk hidup yang banyak terdapat
di sekitar manusia, ada yang menguntungkan tetapi juga ada yang merugikan.
Seperti Candida albicans, Mycobacterium yang merupakan mikroorganisme
patogen yang dapat merugikan kesehatan manusia. Namun terdapat juga
mikroorganisme yang menguntungkan seperti Lactobacillus sp. yang
membantu dalam pencernaan makanan di dalam usus (Agusta, 2009).
Salah satu dari jenis mikroorganisme adalah jamur. Berdasarkan
8
tunggal dan jamur yang memiliki banyak sel (Agusta, 2009).Jamur memiliki
berbagai manfaat dalam kehidupan manusia. Seperti dalam penggunaanya
sebagai bahan pangan serta membantu dalam proses pembuatan makanan
seperti jamur tempe (Rhyzopus oryzae) (Agusta, 2009). Selain itu, jamur digunakan sebagai penghasil metabolit sekunder yang dapat digunakan untuk
obat, seperti pada Penicillium yang menghasilkan penisilin yang digunakan sebagai antibiotik (Agusta, 2009).
Salah satu dari jenis jamur yaitu jamur endofit. Endofit berasal dari
Bahasa Yunani, “endo” berarti di dalam dan “fit” berarti tumbuhan (Agusta, 2009). Endofit dapat didefinisikan sebagai koloni organisme hidup tanpa
menimbulkan gejala patogenik pada jaringan internal inangnya, walaupun
pada periode waktu tertentu akan berakibat timbulnya penyakit (Agusta,
2009). Jamur endofit dapat diisolasi dari bagian tumbuhan inangnya seperti
pada batang, akar, daun dan kemudian ditumbuhkan pada media yang sesuai.
Yangmin et al., mengisolasi 80 jamur endofit dari akar, batang, dan daun tumbuhan Eucommia ulmoides(Yangmin et al., 2007). Pada tumbuhan
teh, Camellia sinensis (L.) O.K., berhasil diisolasi 6 jenis jamur endofit (Agusta, 2007). Pada tumbuhan anggrek, Lepanthes, juga berhasil diisolasi
jamur endofit Xylaria sp. dan Rhizoctonia (Bayman et al., 1996). Dari daun tumbuhan pandan wangi (Pandanus amarylifolius) telah berhasil diisolasi 2 isolat jamur endofit yang merupakan Drechslera sp. dan Colletotricum sp.,
sedangkan dari akar tumbuhan tersebut berhasil diisolasi 7 isolat jamur
9
Berbagai manfaat telah diperoleh dari jamur endofit, seperti
penggunaanya sebagai biokontrol patogen pada Theobroma cacao (Meji’a, et al.,2008). Ekstrak etil asetat dari jamur endofit PWA2 memperlihatkan
aktivitas dalam menghambat Saccharomyces cerevisiae (Jamal et al., 2009). Dua puluh enam isolat jamur endofit yang diisolasi dari tumbuhan di bagian
utara Thailand memiliki kemampuan untuk memproduksi enzim selulase
(Lumyong et al., 2002). Jamur endofit CR200 (Cytospora sp.) dan CR146 (Diaporthe sp.) yang diisolasi dari Conocarpus erecta dan Forstenia spiccata
menghasilkan senyawa sitosporon yang menunjukkan aktivitas sebagai
antibiotik (Brady et al., 2000).
Jamur endofit juga dapat menghasilkan metabolit sekunder dengan
beragam aktivitas biologi. Jamur endofit dapat menghasilkan metabolit
sekunder lebih banyak dibandingkan mikroba endofit lainnya (Zhang et al.,
2006). Berbagai golongan metabolit sekunder yang dihasilkan seperti
alkaloid, steroid, terpenoid, turunan isokumarin, kuinon, dan senyawa lainnya
( Zhang et al., 2006). Brady et al., 2000, telah berhasil mengisolasi sitoskirin
dari jamur endofit Cytospora yang diisolasi dari batang tumbuhan
Conocarpus erecta. Diaporthe sp. isolat E dapat memproduksi metabolit
bisantrakinon, yaitu (+)-2,2’ – episitoskirin dan (+) -1,1’ – bislunatin dalam medium cair potato dextro broth (PDB) (Agusta et al., 2006).
Selain itu, potensi jamur endofit telah banyak diketahui seiring
dengan dilakukannya penelitian yang membuktikan kemampuannya dalam
10
senyawa flavan-3-ol dari tanaman teh menjadi leukoantosianidin (Agusta,
2007) .
2.3 Isolasi Jamur Endofit
Satu jenis tumbuhan dapat memiliki berbagai jenis jamur endofit.
Jamur endofit dapat terdapat di akar, batang, atau daun dari suatu tumbuhan.
Untuk memperoleh jamur endofit dari suatu tumbuhan, dilakukanlah suatu
teknik isolasi. Isolasi jamur endofit dari tumbuhan dapat dilakukan dengan
cara (Jamal et al,. 2009) :
1.Bagian tumbuhan seperti daun, batang, atau akar dicuci dengan air sampai
bersih, lalu dipotong–potong dengan ukuran panjang tertentu. Misalnya pada isolasi jamur endofit dari daun pandan wangi, daun dipotong sekitar
5–7 cm.
2.Permukaan daun yang telah dipotong selanjutnya disterilisasi dengan
merendamnya dalam 75 % etanol selama 2 menit, 5,3 % natrium hipoklorit
selama 5 menit dan kembali dengan 75 % etanol selama setengah menit.
3.Bagian tumbuhan yang telah disterilkan permukaannya kemudian dipotong
memanjang sekitar 0,5 cm.
4.Potongan daun tadi kemudian diletakkan di atas medium corn-meal malt
agar (CMMA) yang mengandung kloramfenikol dengan konsentrasi 0,05 mg/ml.
5.Selanjutnya diinkubasi pada suhu 27 oC selama 1 – 2 minggu.
6.Setelah tumbuh, setiap koloni jamur selanjutnya dipindah beberapa kali ke
11
Untuk mengidentifikasi isolat jamur endofit tersebut dapat dilakukan
dengan mengamati ciri dan karakter morfologi baik secara makroskopis
maupun mikroskopis dari koloni jamur yang ditumbuhkan di atas PDA pada
suhu ruang. Secara makroskopis karakter jamur yang dapat diamati seperti
warna, permukaan koloni, serta tekstur. Sedangkan pengamatan secara
mikroskopis dapat dilakukan dengan bantuan mikroskop untuk mengamati
pigmentasi hifa, bentuk dan ornamentasi tangkai spora.
2.4 Biotransformasi
Biotransformasi merupakan suatu proses dimana suatu senyawa
dapat berubah menjadi senyawa lainnya (Borge, 2007). Pada proses ini
digunakan mikroorganisme untuk membantu mengubah senyawa tersebut
(Borge,2007).Mikroorganisme yang telah banyak diteliti karena
kemampuaannya dalam mentransformasikan senyawa kimia yaitu jamur
endofit. Seperti yang dilakukan oleh jamur endofit Diaporhe sp. E yang diisolasi dari tanaman teh yang berparasit dengan Scurrula atopurpurea,
mampu melakukan biotransformasi terhadap senyawa (-)-epikatekin menjadi
senyawa (-)-(2R,3R,4R0-3,4,5,7,3’,4’ heksahidroksiflavan (Agusta et al., 2005).
Selain itu, jamur endofit Diaporthe sp. E juga mampu melakukan biotransformasi senyawa (-)-epikatekin menjadi (-)-(2R,3S)-dihidrokuersetin
12
Gambar 3. Reaksi biotransformasi (-)-epikatekin menjadi (-)-(2R,3S)-dihidrokuersetin oleh jamur endofit (Diaporthe sp.).
Jamur Xylaria sp yang diisolasi dari Cinchona pubescens dalam medium potato dextrose broth (PDB) dapat melakukan transformasi empat bentuk alkaloid kina yaitu kuinin hidroklorida, kuinidin hidroklorida,
kinkonidin hidroklorida, dan kinkonin hidroklorida dengan melakukan
pemasukan atom oksigen pada posisi 1-N atom alkaloid kina (Shibuya et al.,
2003).
13
Pada proses biotransformasi Xylaria sp. ini diperlihatkan mekanisme
reaksi yang menarik. Penambahan substrat kina dalam jumlah besar (20 mg)
ke dalam 200 ml kultur jamur Xylaria sp. berumur 3 hari gagal menghasilkan
produk biotransformasi. Sedangkan penambahan substrat dalam jumlah kecil
(2 mg) ke dalam kultur jamur berumur 1 hari dan kemudian dilanjutkan
penambahan 20 mg substrat pada hari ketiga dan diinkubasi pada suhu 27 oC,
selama 20 hari berhasil menghasilkan produk biotransformasi. Mekanisme
reaksi tersebut mengindikasikan bahwa jamur endofit memerlukan stimulasi
sejumlah kecil substrat untuk mengaktifkan sistem enzimatik untuk
melakukan reaksi pemasukan atom oksigen pada posisi 1-N- pada molekul
kina alkaloid. Sehingga hal tersebut menunjukkan bahwa proses
biotransformasi juga dipengaruhi jumlah penambahan substrat ke dalam
kultur jamur endofit.
Contoh lainnya dari proses biotransformasi yaitu pada jamur endofit
Diaporthe sp. isolat E yang diisolasi dari tanaman teh, Camellia sinensis (L.) O.K. yang dapat mengubah senyawa flavan-3-ol dari tanaman teh menjadi
leukoantosianidin dan reaksi biotransformasi ini bersifat selektif terhadap
struktur ruang dari molekul substrat dengan konfigurasi 2R-fenil tersubstitusi
yang merupakan tipe alami dari flavan-3-ol dalam tumbuhan teh (Agusta,
2007). Salah satu senyawa flavan-3-ol yang ditransformasi oleh Diaporthe sp. isolat E yaitu (-)-epigalokatekin-3-O-galat menjadi
(-)2R,3R,4R-leukodelfinidin dengan kemampuan biotransformasi sebesar 43% (Agusta,
14
Dalam proses biotransformasi, jamur endofit memiliki enzim untuk
mengkatalisasi reaksi biotransformasi komponen kimia tumbuhan inangya
dalam medium semisintetis (Agusta, 2009). Reaksi biotransformasi juga
dipengaruhi oleh medium dimana jamur endofit dikulturkan. Reaksi
biotransformasi akan berjalan jika menggunakan medium yang sesuai untuk
pertumbuhan optimal dalam memproduksi enzimnya, karena pertumbuhan
dan kerja jamur juga dipengaruhi nutrisi yang terkandung dalam nutrisi
tempatnya dikulturkan ( Shibuya et al.,2003 ).
Proses biotransformasi juga dipengaruhi lingkungan seperti udara,
cahaya, dan suhu. Seperti pada proses biotransformasi (-)-EGCG oleh fungi
endofit Diaporthe sp. isolat E yang pada reaksi tahap ketiga (oksidasi lanjutan pada atom C-4 untuk membentuk gugus karbonil) sensitif terhadap perubahan
lingkungan dimana pada kondisi gelap berhasil dibentuk suatu produk
sedangkan pada kondisi terang tidak (Agusta, 2009) .
Selain dengan mikroorganisme, terdapat suatu proses
biotransformasi yang dilakukan oleh kultur sel. Seperti kultur sel dari
tanaman Papaver somniferum yang mampu mengubah senyawa (+)-(S)-retikulin menjadi (-)-(S)-(+)-(S)-retikulin serta (-)-(S)-cheilanthifolin (Furuya et al.,
1978).
2.5 Berberin
Berberin temasuk ke dalam golongan alkaloid yang telah banyak
digunakan dalam pengobatan Cina dan Ayurveda. Berberin digunakan
sebagai obat trakoma, antiradang, antidepresan, antioksidan, antidiabetes, anti
15
telah dilakukan untuk membuktikan manfaat dari berberin yang diisolasi dari
tanaman Arcangelisia flava (L.) Merr, seperti kemampuannya untuk menghambat pertumbuhan bakteri Babesia gibsoni pada konsentrasi 10
µg/mL dan 100 µg/ml (Subeki et al., 2005). Berberin juga dapat menghambat pertumbuhan bakteri patogen seperti Diplococcus pneumonia, Salmonella typhosa, Neisseria gonorrhoeae (Unesco, 1998). Penelitian lain menunjukkan
bahwa berberin yang diisolasi dari tanaman Berberis heterophylla
menunjukkan aktivitas secara in vitro dan in vivo dalam menghambat
Candida albicans (Freile et al., 2006).
o
o N
OCH3
OCH3
+
Gambar 5. Struktur Kimia Berberin.
Penelitian juga dilakukan untuk membuktikan kemampuan
berberin dalam mengobati penyakit kardiovaskular karena dapat menurunkan
16
BAB III
KERANGKA KONSEP
Skrining jamur endofit yang mampu melakukan reaksi biotransformasi
Jamur endofit AFKR-2, 3, 5, 13 yang diisolasi dari
Arcangelisia flava (L.) Merr
Kultur jamur endofit dengan penambahan
berberin pada medium tumbuh GYP,PDB
Scaling up proses biotransformasi
Ekstraksi Hasil Biotransformasi
Fraksinasi ekstrak
Purifikasi fraksi satu
Karakterisasi produk biotransformasi Jamur endofit AFKR-5
17
BAB IV
METODOLOGI PENELITIAN
4.1 Tempat dan Waktu Penelitian
4.1.1 Tempat :
Penelitian Biotransformasi Berberin Oleh Jamur Endofit Dari
Tumbuhan Akar Kuning (Arcangelisia flava (L.) Merr: MENISPERMACEAE) dilaksanakan di Laboratorium Fitokimia,
Puslit Biologi LIPI Cibinong.
4.1.2 Waktu :
Penelitian ini dilaksanakan pada bulan Februari 2010 sampai dengan
Juni 2010.
4.2 Alat dan Bahan
4.2.1 Alat
Alat yang digunakan dalam penelitian ini adalah rotary evaporator,
labu evaporator, Vortex Sibata, syringe drivenfilter unit (Millex GP) ukuran 0,20 µm, vial, UV cabinet, chamber, cawan petri, timbangan
analitik, lemari asam, pipa kapiler, corong, corong pisah, pipet tetes,
erlenmeyer, gelas kimia, gelas ukur, pipet takar, laminar airflow, autoklaf, shaker, kolom kromatografi, MS Water LCT Premier Xe
Micromass Technology, HPLC Shimadzu LC-20 AB, dan pipet
mikro.
4.2.2 Bahan Uji
18
4.2.3 Bahan Kimia
Bahan–bahan kimia yang digunakan pada penelitian ini adalah plat KLT (silica gel 60 F254), sephadex LH–20, kolom Capcell Pak C-18
(Shiseido 4,5 mmx260 mm), asetonitril, air millipore, metanol, aquadest, diklorometan, n-heksana, asam asetat glasial, reagen
dragendroff, reagen serium, air sumur, medium glucose yeast-extract peptone (GYP), medium potato dextro broth (PDB), medium potato dextrose agar (PDA) (komposisi medium dapat dilihat pada lampiran
1), dan gas N2.
4.3 Prosedur Kerja
4.3.1 Skrining Biotransformasi Berberin
4.3.1.1 Isolat Jamur
Jamur yang digunakan adalah 4 isolat jamur endofit yang
diisolasi dari tanaman akar kuning, yaitu AFKR–2, 3, 5, dan 13.
4.3.1.2 Pembuatan Medium Kultivasi
Medium GYP dibuat dengan melarutkan 2,5 gram pepton, 0,5
gram yeast extract, 10 gram glukosa, 0,25 gram KH2PO4,
0,25 gram MgSO4.7H2O, 5 mg FeSO4.7H2O, 0,1 gram
CaCO3 ke dalam 500 ml air sumur. Setelah semua komponen
larut, bagi medium tersebut ke dalam erlenmeyer 300 ml
masing-masing sebanyak 100 ml sesuai jumlah isolat jamur
19
disterilkan menggunakan autoklaf pada suhu 121 0C selama
20 menit.
Medium PDB dibuat dengan melarutkan 12 gram PDB ke
dalam 500 ml air sumur. Setelah semua komponen larut,
medium tersebut dibagi ke dalam lima erlenmeyer 300 ml
masing–masing sebanyak 100 ml kemudian ditutup dengan aluminium foil. Semua erlenmeyer berisi medium kemudian
disterilkan dengan autoklaf pada suhu 121 0C selama 20
menit.
4.3.1.3 Kultivasi Jamur Endofit
Seluruh isolat jamur yang ditumbuhkan pada medium PDA
dipotong kecil kurang lebih 0,5x0,5 cm kemudian diambil
sebanyak 4 potong lalu jamur tersebut dipindahkan ke dalam
medium GYP dan PDB yang telah disterilkan dan
didinginkan. Satu erlenmeyer disiapkan sebagai blanko
dengan hanya berisi medium GYP dan PDB. Pengerjaan
kultivasi jamur endofit dilakukan dalam keadaan steril di
dalam laminar airflow. Medium GYP dan PDB yang telah
berisi jamur endofit kemudian diinkubasi dengan shaker pada suhu 27 0C dengan kecepatan 120 rpm selama 4 hari.
4.3.1.4 Penambahan Substrat Pada Kultur
Penambahan substrat berberin dilakukan setelah kultur
berumur 4 hari. Substrat yang ditambahkan pada kultur
20
metanol. Kemudian larutan tersebut disaring dengan
menggunakan syringe Millex GP dengan diameter pori 0,20 µm dalam keadaan steril.
Larutan berberin yang telah disterilkan tersebut dipipet
sebanyak 10 ml dengan konsentrasi berberin 1 mg dalam 1
ml metanol, kemudian masing–masing dimasukkan ke dalam kultur jamur endofit dan blanko. Kemudian kultivasi
dilanjutkan dengan menginkubasi menggunakan shaker pada
suhu 27 0C dengan kecepatan 120 rpm.
4.3.1.5 Monitoring hasil biotransformasi
Biotransformasi dimonitoring untuk memantau apakah telah
terjadi biotransformasi berberin dengan cara pengambilan
sampel terhadap kultur jamur endofit yang telah ditambahkan
substrat berberin. Sampling pertama dilakukan setelah 1 hari
penambahan berberin pada kultur jamur endofit.
Erlenmeyer yang berisi blanko dan kultur jamur endofit
dalam medium GYP dan PDB yang telah ditambahkan
substrat berberin dipipet kira–kira 5 ml dan kemudian dipindahkan ke dalam tabung reaksi. Setelah itu tambahkan
dengan diklorometan : metanol = 5:1 sebanyak 5 ml,
kemudian dikocok dengan vortex dan didiamkan 10 menit
sehingga akan terbentuk dua lapisan. Lapisan bawah tersebut
kemudian dipipet dan dipindahkan ke labu evaporator dan
21
ekstrak kental. Ekstrak kemudian dianalisis dengan KLT
(fase diam silica gel 60 F245 dan fase gerak diklorometan :
metanol = 6:1 (7 ml) yang ditambahkan asam asetat glasial 1
tetes). Noda yang muncul diamati di bawah sinar UV pada
panjang gelombang 254 nm dan 366 nm kemudian disemprot
dengan reagen dragendroff.
Pengambilan sampel dilakukan pada 1 hari, 2 hari, 3 hari, dan
7 hari setelah penambahan berberin.
4.3.1.6 Ekstraksi Kultur Jamur Endofit
Ekstraksi kultur jamur endofit dalam medium GYP dan PDB
dilakukan 14 hari setelah penambahan berberin ke kultur
jamur dengan pelarut diklorometan : metanol = 5:1. Ekstraksi
dilakukan dengan corong pisah dan diambil lapisan bawah
kemudian dikeringkan dengan rotary evaporator. Ekstrak yang telah dikeringkan lalu ditimbang. Setelah itu, ekstrak di
analisis menggunakan KLT dengan fase diam silica gel 60
F254 dan fase gerak diklorometan : metanol = 6:1 (7 ml) dan
ditambahkan asam asetat glasial 1 tetes. Noda yang muncul
diamati dibawah sinar UV pada panjang gelombang 254 nm
dan 366 nm kemudian disemprot dengan reagen dragendroff.
4.3.2 Scalling up Proses Biotransformasi 4.3.2.1 Pembuatan Medium Kultivasi
Medium GYP dibuat dengan melarutkan 5 gram pepton, 1
22
gram MgSO4.7H2O, 10 mg FeSO4.7H2O, 0,2 gram CaCO3
ke dalam 1000 ml air sumur. Setelah semua komponen larut,
bagi medium tersebut ke dalam erlenmeyer masing–masing sebanyak 200 ml dalam erlenmeyer 500 ml sesuai jumlah
isolat jamur kemudian tutup dengan aluminium foil. Kelima
erlenmeyer berisi medium disterilkan dengan autoklaf pada
suhu 121 0C selama 20 menit.
4.3.2.2Kultivasi jamur endofit AFKR-5
Jamur endofit AFKR-5 yang ditumbuhkan pada medium
PDA dipotong kecil kurang lebih 0,5 x 0,5cm dan diambil
sebanyak 4 buah kemudian dimasukkan ke dalam medium
GYP yang telah disterilkan dan didinginkan. Pengerjaan
kultivasi jamur endofit dilakukan dalam keadaan steril di
dalam laminar airflow. Medium yang telah berisi jamur endofit diinkubasi menggunakan shaker pada suhu 27 0C dengan kecepatan 120 rpm selama 4 hari.
4.3.2.3 Penambahan substrat pada kultur jamur endofit AFKR-5
Penambahan substrat berberin dilakukan seperti saat skrining.
Substrat yang akan ditambahkan pada kultur dibuat dengan
menambahkan 100 mg berberin ke dalam 100 ml metanol.
Kemudian larutan tersebut disaring dengan menggunakan
23
Larutan berberin steril dengan konsentrasi 1 mg/ml dipipet
sebanyak 20 ml kemudian dimasukkan ke dalam setiap kultur
jamur endofit. Kultivasi dilanjutkan dengan menginkubasi
medium menggunakan shaker hingga hari ke-14.
4.3.2.4 Monitoring hasil biotransformasi
Biotransformasi dimonitoring untuk memantau apakah telah
terjadi biotransformasi berberin dengan cara melakukan
pengambilan sampel terhadap kultur jamur endofit pada hari
ke-10 setelah penambahan berberin.
Kultur jamur endofit dalam medium GYP saat 10 hari setelah
penambahan substrat berberin dipipet sebanyak ± 5 ml dan
kemudian dipindahkan ke dalam tabung reaksi. Setelah itu
tambahkan dengan diklorometan : metanol = 5:1 sebanyak ±
5 ml, kemudian dikocok menggunakan vortex dan didiamkan beberapa menit sehingga akan terbentuk dua lapisan. Lapisan
bawah tersebut kemudian dipipet dan dipindahkan ke labu
evaporator kemudian dikeringkan.
Ekstrak kemudian dianalisis dengan KLT (fase diam silica
gel 60 F254 dan fase gerak diklorometan : metanol = 6:1 (7
ml) yang ditambahkan asam asetat glasial 1 tetes). Noda yang
muncul diamati di bawah sinar UV pada panjang gelombang
254 nm dan 366 nm. Selain dengan KLT, hasil
penyamplingan ini juga dianalisis menggunakan HPLC
24
x 250 mm) , fase gerak air millipore : asetonitril = 90 % : 10
%, laju alir 1 ml/menit, lama aliran 30 menit, detektor UV
dengan panjang gelombang 266 nm.
4.3.2.5 Ekstraksi kultur jamur endofit AFKR-5
Kultur jamur endofit setelah 14 hari penambahan berberin
dikecilkan ukurannya menggunakan spatula. Kemudian
kultur tersebut diekstrak menggunakan diklorometan :
metanol = 5:1. Sebanyak ± 50 ml pelarut campur dimasukkan
ke dalam kultur jamur, kemudian dikocok menggunakan
magnetic stirer selama 10 menit. Setelah itu,jamur dipisahkan
dengan filtrat menggunakan saringan. Proses ini diulang
sebanyak 3 kali. Hasil saringan filtrat merupakan ekstrak
yang kemudian dikeringkan lalu ditimbang kemudian
dianalisis dengan KLT (fase diam silica gel 60 F254 dan eluen
diklrometan : metanol = 6:1 (7 ml) yang ditambah 1 tetes
asam asetat glasial). Noda yang muncul diamati di bawah
sinar UV pada panjang gelombang 254 nm dan 366 nm.
Selain dengan KLT, hasil pengambilan sampel ini juga
dianalisis menggunakan HPLC dengan kondisi HPLC =
Capcell Pak C-18 (Shiseido 4,6 mm x 250 mm) , fase gerak
air millipore : asetonitril = 90 % : 10 %, laju alir 1 ml/menit,
lama aliran 30 menit, detektor UV dengan panjang
25
4.3.2.6 Partisi ekstrak hasil biotransformasi
Ekstrak kental hasil ekstraksi dilarutkan dengan metanol
kemudian dipartisi menggunakan n-heksan. Partisi ini
dilakukan dengan corong pisah sehingga kemudian
didapatkan dua lapisan (lapisan atas air, lapisan bawah
diklorometan) dan diambil lapisan bawah. Lapisan bawah
tersebut kemudian dikeringkan menggunakan rotary evaporator. Ekstrak kental yang didapat kemudian dianalisis
dengan KLT (fase diam silica gel 60 F254 dan fase gerak
diklorometan : metanol = 6:1 (7 ml) yang ditambahkan asam
asetat glasial 1 tetes). Noda yang muncul diamati dibawah
sinar UV pada panjang gelombang 254 nm dan 366 nm
kemudian disemprot dengan reagen serium.
4.3.2.7 Fraksinasi hasil biotransformasi AFKR-5
Ekstrak hasil partisi difraksinasi dengan menggunakan kolom
kromatografi dengan fase diam sephadex LH–20 (volume 275 ml) dan fase gerak metanol 90%. Hasil fraksinasi
ditampung dengan tabung reaksi dan setiap tabung dicek
dengan analisis KLT (fase diam silica gel 60 F254 dan fase
gerak diklorometan : metanol = 6:1 (7 ml) ditambah asam
asetat glasial 1 tetes). Noda yang muncul diamati di bawah
sinar UV pada panjang gelombang 254 nm dan 366 nm
kemudian disemprot dengan pereaksi dragendroff. Isi
26
kromatogram KLT digabungkan menjadi satu fraksi. Tabung
3-6 digabung menjadi fraksi satu. Tabung 7-8 digabung
menjadi fraksi dua dan tabung 9-11 digabungkan menjadi
fraksi tiga.
4.3.2.8 Purifikasi produk biotransformasi AFKR - 5 fraksi 1
Ketiga fraksi yang diperoleh dari fraksinasi menggunakan
kromatografi kolom kemudian dianalisis dengan KLT (fase
diam silica gel 60 F254 dan fase gerak diklorometan : metanol
= 6 : 1 (7 ml) dan ditambah asam asetat glasial 1 tetes). Noda
yang muncul diamati di bawah sinar pada panjang gelombang
UV 254 nm dan 366 nm kemudian disemprot dragendroff.
Fraksi satu kemudian dipurifikasi menggunakan KLT
preparatif dengan fase diam silica gel 60 F254 dan fase gerak
diklorometan : metanol : amoniak 25 % = 5:3:0,5 . Noda
yang muncul diamati di bawah sinar UV pada panjang
gelombang 254 nm dan 366 nm. Setelah itu noda tersebut
dikerok kemudian dilarutkan dengan diklorometan dan
metanol, kemudian disaring dengan menggunakan kertas
saring. Hasil saringan yang didapatkan dikeringkan dan
kemudian dianalisis dengan KLT menggunakan fase gerak
diklorometan : metanol = 6:1 (7 ml) dengan ditambahkan
asam asetat glasial 1 tetes. Noda yang muncul diamati di
bawah sinar UV pada panjang gelombang 254 nm dan 366
27
4.3.2.9 Karakterisasi produk hasil biotransformasi dengan MS
Senyawa hasil biotransformasi berberin dianalisis
menggunakan MS Water LCT Premier Xe Micromass
28
BAB V
HASIL DAN PEMBAHASAN
5.1 Skrining Biotransformasi Berberin
Dengan dilakukannya skrining biotransformasi berberin ini, dapat
dilihat kemampuan dari 4 isolat jamur endofit dalam melakukan proses
biotransformasi dalam medium GYP dan PDB. Monitoring terhadap proses
biotransformasi oleh jamur endofit tersebut dilakukan dengan cara melakukan
penyamplingan setelah 1 hari, 2 hari, 3 hari dan 7 hari penambahan berberin
ke dalam kultur jamur endofit. Proses transformasi diamati dengan
melakukan analisis Kromatografi Lapis Tipis (KLT) terhadap ekstrak kultur
jamur. KLT tersebut kemudian dielusi dengan menggunakan fase gerak
diklorometan : metanol = 6:1 dan ditambahkan 1 tetes asam asetat glasial.
Namun hingga penyamplingan hari ke-7, kromatogram hasil KLT belum
menampakkan terjadinya reaksi biotransformasi. Reaksi biotransformasi baru
terlihat pada ekstrak kultur jamur pada 14 hari penambahan berberin (gambar
6).
Hasil skrining memperlihatkan bahwa reaksi biotransformasi terjadi
pada kultur jamur endofit AFKR-5 dan AFKR-13 pada medium GYP.
Sedangkan pada jamur endofit yang dikultivasi pada medium PDB tidak
memperlihatkan berjalannya reaksi biotransformasi. Berikut adalah profil
29
a b
c d
Gambar 6. Profil kromatogram KLT (fase diam silica gel 60 F254, fase gerak
diklorometan : metanol = 6:1 (7 ml) ditambah 1 tetes asam asetat glasial) ekstrak diklorometan-metanol dari kultur jamur endofit AFKR-2, 3, 5, dan 13 pada medium GYP dan PDB saat 14 hari penambahan berberin. (fase diam silica gel 60 F254, fase gerak
diklorometan : metanol = 6:1 ditambahkan 1 tetes asam asetat.S=berberin; C=blanko medium; 2,3,5,13=AFKR-2,3,5,13. (a) sinar UV 254 nm, (b)sinar UV 366 nm (pada medium GYP),(c) sinar UV 245 nm, (d) sinar UV 366 nm (pada medium PDB)
Dari hasil skrining yang dilakukan terhadap 4 isolat jamur endofit
dari akar kuning terlihat bahwa AFKR–5 dan AFKR-13 pada medium GYP dapat melakukan reaksi biotransformasi terhadap berberin. Hasil skrining ini
juga memperlihatkan berbedanya kemampuan setiap jamur endofit dalam
mentransformasikan senyawa berberin bergantung pada medium kultur. Hal
tersebut terlihat pada hasil noda dari hasil skrining dimana jamur endofit produk
30
AFKR–5 dan AFKR–13 mampu melakukan biotransformasi pada medium GYP sedangkan jamur–jamur endofit tersebut tidak memperlihatkan kemampuan biotransformasi pada medium PDB. Medium kultur yang
berbeda akan memberikan hasil biotransformasi yang berbeda dimana
medium memberikan pengaruh nutrisi yang diterima oleh jamur endofit,
sehingga medium kultur jamur yang berbeda akan memperoleh nutrisi yang
berbeda pula.
Hasil skrining yang dilakukan memperlihatkan bahwa jamur endofit
AFKR–5 dan AFKR–13 pada medium GYP dapat melakukan biotransformasi berberin. Oleh karena itu dilakukanlah scalling up reaksi biotransformasi
berberin dengan salah satu isolat jamur endofit yang dapat melakukan reaksi
biotransformasi yaitu AFKR-5 pada medium GYP. Dari hasil KLT saat
skrining biotransformasi (gambar 6) AFKR-5 memperlihatkan noda produk
hasil biotransformasi yang lebih besar dibandingkan dengan AFKR–13. Untuk membuktikan bahwa senyawa produk biotransformasi tidak
dihasilkan oleh jamur endofit AFKR–5 sebagai metabolit sekunder jamur tersebut dilakukan dengan bantuan analisis KLT. Hal tersebut dilakukan
dengan membandingkan KLT dari kultur jamur AFKR–5 yang ditambahkan berberin dengan kontrolnya yaitu yang tidak ditambahkan berberin (Gambar
7). Hasil KLT tersebut memperlihatkan bahwa jamur endofit AFKR–5 pada medium GYP tidak menghasilkan produk hasil biotransformasi. Noda yang
31
memperlihatkan bahwa senyawa hasil biotransformasinya bersifat relatif lebih
nonpolar dibandingkan berberin.
a b
Gambar 7. Profil ktomatogram KLT (fase diam silica gel 60 F254, fase gerak
diklorometan : metanol = 6:1 (7 ml) ditambah 1 tets asam asetat glasial) ekstrak diklorometan – metanol kultur jamur endofit AFKR-5 pada medium GYP. (S = berberin, 1 = AFKR–5 ditambahkan berberin, 2 = AFKR-5 tanpa penambahan berberin), (a) UV 254 nm, (b) UV 366 nm.
5.2 Profil Jamur AFKR– 5
Jamur endofit AFKR–5 diisolasi dari tumbuhan akar kuning. Jamur ini kemudian ditumbuhkan pada medium potato dextrose agar (PDA). Hasil pengamatan secara makroskopis terhadap jamur endofit AFKR-5 akan
membentuk miselium berwarna putih setelah 4 hari ditumbuhkan pada
medium PDA. Saat satu minggu terbentuk miselium yang lebih banyak dan
pada minggu kedua terlihat miselium berwarna kuning (gambar 8) yang
kemungkinan merupakan metabolit sekunder yang dihasilkan oleh jamur
endofit AFKR-5.
produk
32
a b
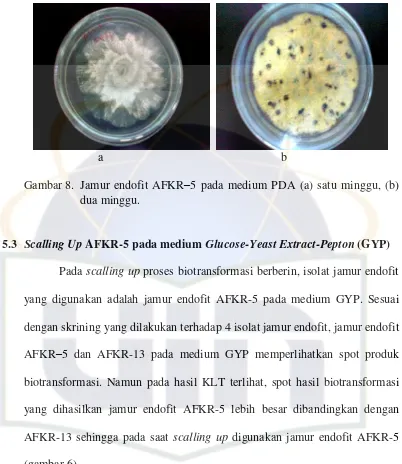
Gambar 8. Jamur endofit AFKR–5 pada medium PDA (a) satu minggu, (b) dua minggu.
5.3 Scalling Up AFKR-5 pada medium Glucose-Yeast Extract-Pepton (GYP)
Pada scalling up proses biotransformasi berberin, isolat jamur endofit
yang digunakan adalah jamur endofit AFKR-5 pada medium GYP. Sesuai
dengan skrining yang dilakukan terhadap 4 isolat jamur endofit, jamur endofit
AFKR–5 dan AFKR-13 pada medium GYP memperlihatkan spot produk biotransformasi. Namun pada hasil KLT terlihat, spot hasil biotransformasi
yang dihasilkan jamur endofit AFKR-5 lebih besar dibandingkan dengan
AFKR-13 sehingga pada saat scalling up digunakan jamur endofit AFKR-5 (gambar 6).
Untuk tujuan isolasi dan karakterisasi produk biotransformasi tersebut,
maka dilakukan kultur jamur endofit AFKR-5 pada skala lebih besar, yaitu
5x200 ml di dalam erlenmeyer 500 ml. Kultur jamur yang telah berumur 4
hari terlihat terbentuk seperti filamen berwarna putih yang banyak (Gambar
33
a b c
d e
Gambar 9. Kultur jamur endofit AFKR – 5 pada medium glucose yeast-ekstrak pepton (GYP). (a) saat kultivasi, (b) 4 hari kultivasi (sebelum penambahan berberin), (c) 1 hari (d) 10 hari (e) 14 hari (telah ditambahkan berberin).
Pada hari ke-10 penambahan berberin dilakukan penyamplingan untuk
mengamati terjadinya proses biotransformasi. Hasil penyamplingan kemudian
diekstrak dengan diklorometan-metanol (5:1) dan kemudian dianalisis dengan
HPLC dan KLT. Dari hasil kromatogram HPLC terlihat puncak berberin
masih tinggi (10C) dan dari hasil kromatogram KLT terlihat berberin dan
ekstrak kultur menunjukkan noda yang sama (gambar 11a,b). Saat 14 hari
penambahan berberin pada kultur jamur endofit AFKR-5, dilakukan ekstraksi
34
Gambar 10. Hasil kromatogram HPLC menggunakan kolom Capcell pak C-18 (Shiseido 4,5 mm x 260 mm), fase diam air millipore : asetonitril = 90 %: 10%, laju alir : 1 ml/menit, lama aliran 30 menit, detektor UV λ 266 nm. (A) jamur endofit AFKR-5 tanpa penambahan berberin, (B) standar berberin, (C) kultur jamur 10 hari setelah penambahan berberin, (D) kultur jamur 14 hari setelah penambahan berberin.
35
a b c d
Gambar 11. Profil kromatogram KLT (fase diam silica gel 60 F254, fase
gerak diklorometan : metanol = 6:1 (7 ml) ditambah 1 tets asam asetat glasial) kultur jamur endofit AFKR-5 pada medium GYP (a) di bawah sinar UV 254 nm, (b) di bawah sinar UV 366 nm (10 hari penambahan berberin), (c) di bawah sinar UV 254 nm, (d) di bawah sinar UV 366 nm (14 hari penambahan berberin). S = berberin, E = ekstrak jamur.
Dari hasil kromatogram HPLC saat penyamplingan hari ke-10
penambahan berberin (gambar 10C) dengan kromatogram setelah 14 hari
penambahan berberin (gambar 10D) terlihat hasil yang berbeda. Pada 14 hari
penambahan berberin terjadi penurunan puncak berberin, dipihak lain terjadi
kemunculan puncak baru (gambar 10D). Puncak baru yang muncul pada 14
hari penambahan berberin merupakan produk hasil biotransformasi berberin.
Hal ini diperkuat dengan hasil KLT (11c,d) saat 14 hari penambahan berberin
yang memperlihatkan telah terdapatnya produk hasil biotransformasi.
Hasil ekstrak kultur jamur endofit AFKR–5 setelah diekstraksi dan dianalisis dengan HPLC dan KLT kemudian dipartisi dengan n–heksana untuk menghilangkan lemak agar mudah difraksinasi. Setelah dipartisi
ekstrak ini kemudian dikeringan dengan rotary evaporator lalu ditimbang dan diperoleh ekstrak sebanyak 210,2 mg. Ekstrak ini kemudian difraksinasi
produk
36
menggunakan kromatografi kolom dengan fase diam sephadex–LH 20 dan fase gerak metanol 90 % sehingga diperoleh tiga fraksi.
Tabel 1. Hasil fraksinasi dengan kolom kromatografi (fase diam sephadex
LH-20, fase gerak methanol 90%) dari ekstrak diklorometan– metanol biotransformasi kultur AFKR–5 pada medium GYP.
Fraksi Tabung Warna Fraksi Berat ( mg )
1 3,4,5,6 Coklat 36,6
2 7,8 Kuning tua 21,1
3 9,10,11 Kuning muda 30,5
Untuk mengetahui di fraksi mana senyawa hasil biotransformasi berberin
maka dilakukan KLT terhadap fraksi–fraksi tersebut dengan membandingkannya terhadap berberin murni. Dari hasil KLT, fraksi satu
memiliki kandungan hasil biotransformasi berberin.
Fraksi satu tersebut kemudian dipurifikasi kembali dengan
menggunakan KLT preparatif dengan fase gerak diklorometan : metanol :
amoniak 25 % = 5 : 3 : 0,5 sehingga diperoleh 2 fraksi, yaitu 1 – A dan 1 - B. Fraksi 1 - A merupakan hasil biotransformasi berberin sedangkan fraksi 1 - B
merupakan substrat berberin yang tidak dikonversi oleh jamur endofit
AFKR-5. Hal tersebut terlihat dari noda pada plat KLT (gambar 12). Selain itu, nilai
Rf antara fraksi 1-B dengan Rf berberin sama yaitu 0,31 sedangkan Rf fraksi
1-A yaitu 0,40. Hasil yang didapatkan setelah purifikasi menghasilkan 28,5
mg produk utama yang berarti kemampuan jamur endofit AFKR-5 mengubah
37
a b c
Gambar 12. Profil kromatogram KLT hasil purifikasi fase satu (fase diam silica gel 60 F254 dan fase gerak diklrometan : metanol = 6:1
(7 ml) ditambah asam asetat glasial 1 tetes). 1-A = atas,1-B = bawah, (a) UV 254 nm, (b) UV 366 nm, (c) disemprot dragendroff.
Tabel 2. Hasil purifikasi fraksi 1 ekstrak diklorometan–metanol dengan fase gerak diklorometan : metanol = 6:1 (7 ml) ditambah asam asetat
glasial 1 tetes.
Produk hasil biotransformasi kemudian dikarakterisasi
menggunakan spektorfotometer massa. Hasil spektrofotometer massa
menunjukkan produk hasil biotransformasi memiliki bobot massa 352. Hal ini
menunjukkan terjadinya penambahan ion molekul sebanyak 16 amu yang
diduga oksigen terhadap berberin yang memiliki bobot massa 336. No Fraksi Warna Fraksi Rf Berat ( mg )
1 1 – A coklat muda 0,40 28,5
38
39
BAB VI
KESIMPULAN DAN SARAN
6.1 Kesimpulan
Dari penelitian yang telah dilakukan dapat diambil kesimpulan sebagai
berikut:
Jamur endofit AFKR – 5 yang diisolasi dari tanaman Arcangelisia flava (L.) Merr mampu melakukan biotransformasi senyawa berberin menjadi satu
produk yang memiliki berat molekul 16 amu lebih tinggi dibanding substrat
pada medium GYP dengan kondisi inkubasi menggunakan shaker pada
kecepatan 120 rpm dengan suhu 27 0C dengan kemampuan konversi sebesar
27.18% dalam waktu 2 minggu.
6.2 Saran
1.Perlu dilakukan identifikasi jamur endofit AFKR – 5.
2.Perlu dilakukan analisis lebih lanjut untuk mengetahui struktur dari produk
biotransformasi dengan menggunakan UV, IR, dan NMR.
3.Perlu dilakukan uji aktivitas farmakologi terhadap produk biotransformasi
yang dihasilkan serta membandingkannya dengan senyawa asal untuk
mengetahui apakah aktivitas produk biotransformasi lebih baik dari
40
DAFTAR PUSTAKA
Agusta A, Maehara S, Ohashi K, Simanjutak P and Shibuya H. 2005. Stereoselective Oxidation at C-4 Flavans by the Endophytic Fungus
Diaporthe sp. Isolated from a Tea Plant. Chem. Pharm. Bull. 53: 1565 – 1569.
Agusta A, Ohashi K, and Shibuya H. 2006. Bisanthraquinone Metabolites Produced by Endophytic Fungus Diaporthe sp. Chem Pharm Bull. 54 : 579-582.
Agusta, A. 2007. Biotransformasi (-)-Epigalokatekin-3-O-galat Menjadi (-)-2R,3S-Dihidromirisetin oleh Fungi Endofit Diaporthe sp. Isolat E dari Tumbuhan Teh. Hayati Journal Of Biosciences, p150-154.
Agusta, A. 2009. Biologi dan Kimia Jamur Endofit. Bandung: ITB Press.
Agusta, A. 2009. (2R,3S)-Dihidrokuersetin,Suatu Produk Biotransformasi (-)-Epikatekin Oleh Jamur Endofit Diaporthe sp.E. Berita Biologi, 9 (4).
Archangelisia flava. diakses 26 Mei 2010 dari www.plantamor.com
Bayman P, Ligia L, Raymond L.T., and D.J. Lodge. 1996. Variation in Endophytic Fungi from Roots and Leaves of Lepanthes ( Orchidaceae).
New Phytol. 135: 145 – 149.
Brady S.F., Singh M.P., Jeff E.J., and Clardy J. 2000. Cytoskyrins A and B, New BIA Active Bisanthraquinones Isolated from an Endophytic Fungus.
Organic Letters, Vol.2, No.25, 4047 – 4049.
Brady S.F., Wagenaar M.M., Singh M.P., Janso J.E., and Clardy J. 2000. The Cytosporones, New Octaketide Antibiotics Isolated from an Endophytic Fungus. Organic Letters, Vol.2, No.25, 4043 – 4046.
Borge K.B. 2007. Endophytic fungi as models for the Stereoselective Biotransformation of Thioridazine. Appl Microbiol Biotechnol 77:669– 674.
Dharmananda, Subhuti. 2005. New Uses Of Berberine. A Valuable Alkaloid from
Herbs for “Damp –Heat” Syndrome.
41
Freile M, Gianni F, Sortino M, Zamora M, Juarez A, Zacchino S, Enriz D. 2006. Antifungal Activity of Aqueous Extracts and of Berberine Isolated from Berberis heterophyll. Acta Farm. Bonaerense 25 (1): 83-8.
Furuya T, Nakano M, Yoshikawa T. 1978. Biotransformation of (RS)-Reticuline And Morphinan Alkaloids By Cell Cultures of Papaver somniferum.
Phytochemistry. Vol 17, pp 891 – 893.
Grycova’ L, Dosta J., Marek R. 2007. Quatenary Protoberberine Alkaloids. Phytochemistry 68,150-175.
Issat T, Jakobislak M, Golab J. 2006. Berberine, A Natural Cholesterol Reducing Product, Exerts Antitumor Cytostatic,Cytotoxic Effects Independently From The Mevalonate Pathway. Oncology Reports 16: 1273 – 1276. Jamal Y, Ilyas M, Kanti A, Agusta A. 2009. Keragaman Jenis Jamur Endofit pada
Pandan Wangi (Pandanus amarylifolius) dan Aktivitas Antijamur Metabolit yang Diproduksinya. Biota Vol. 14 (2): 81 – 86.
Klemke C, Kehraus S, Wright A.D., and Konig G.M. 2004. New Secondary Metabolit from the Marine Endophytic Fungus Apiospora montagnei. J.Nat. Prod.,67,1058-1063.
Kunii T, Kagei K, Kawakami Y, Nagai Y, Nezu Y, and Sato T. 1985. Indonesian Medicinal Plants: Furanoditerpens from Arcangelisa flava. Chem Pharm Bull 33 (2) 479 – 487.
Lumyong Salsamon, Pipob Lumyong, Eric H.C., McKenzie, and Kevin D. 2002. Enzymatic Activity Of Endophytic Fungi Of Six Native Seedlings Species From Doi Suthep-Pui National Park, Thailand. Canadian Journal Of Microbiology; 48,12.
Ma Y, Zhu H., Su Y, Shi Q, and Li Y. 2007. Isolation and Identification of Endophytic Fungi from Eucommia ulmoides. International Symposium on Eucommia ulmoides,Vol.1, No.1, 82 – 85.
Meji’a L.C, Rojas E.I, Maynard Z, Bael SV, Arnold A.E, Hebbar P, Samuels GJ, Robbins N, Herre EA. 2008. Endophytic Fungi as Biocontrol Agents of Theobroma cacao Pathogens. Biological Control 46 : 4 – 14.
Phillipine Medicinal Plants. Archangelisia flava. diakses 26 Mei 2010 dari www.stuartxchange.org/Abutra.html
Verpoorte R, Siwon J, Essen GFA, Tieken M, Svendsen AB. 1982. Studies On Indonesian Medicinal Plants. VII. Alkaloids of Arcangelisia flava.
42
Sa’roni, Adjirni, Winarno W. 1995. Efek Antidiare Infus Batang Kayu Kuning Archangelisia flava L. pada Tikus Putih dan Toksisitas Akut. Pusat Penelitian dan Pengembangan DepKes RI. Jakarta.
Shibuya H, Kitamura C, Maehara S, Nagahata M, Winarno H, Simanjutak P, Kim H.S, Wataya Y, Ohashi K. 2003. Transformation of Cinchona Alkaloids into 1-N-Oxide Derivatives by Endophytic Xylaria sp. Isolated from
Cinchona pubescens. Chem Pharm Bull. 51(1) 71 – 74.
Singh A, Duggal S, Kaur N, Singh J. 2010. Berberine: Alkaloid with wide spectrum of pharmacological activities. Journal of Natural Products, Vol. 3:64-75.
Subeki, Matsuura H, Takahashi K, Yamasaki M, Yamato O, Maede Y, Katakura K, Suzuki M, Trimurningsih, Chairul, Yoshihara T. 2005. Antibabesial Activity of Protoberberine Alkaloids and 20 Hydroxyedysone form
Arcangelisia flava against Babesia gibsoni in Culture. J. Vet. Med.Sci. 67 (2): 223 – 227.
Unesco.1998. Plant Resources of South East Asia. No.12(2).
Zhang HW, Song YC, and Tan RX. 2006. Biology and Chemistry Of Endophytes.
43
Lampiran 1. Komposisi medium yang digunakan
No. Nama Medium Komposisi Jumlah
1. GYP (glucose yeast-extract peptone) Pepton 5 gr
yeast extract 1 gr
Glukosa 20 gr
KH2PO4 0,5 gr
MgSO4.7H2O 0,5 gr
FeSO4.7H2O 10 mg
CaCO3 0,2 gr
air sumur 1 l
2. PDB (potato dextrose broth) potaoes infusion 200 gr
dekstrosa 20 gr
air sumur 1 l
3. PDA (potato dextrose agar) Agar 15 gr
dekstrosa 20 gr
potatoes infusion 4 gr