REKAYASA PROSES HIDROLISIS AMPAS TAPIOKA
MENGGUNAKAN PEMANASAN GELOMBANG MIKRO
UNTUK PRODUKSI ETANOL
EUIS HERMIATI
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
PERNYATAAN MENGENAI DISERTASI DAN
SUMBER INFORMASI
Dengan ini saya menyatakan bahwa disertasi Rekayasa Proses Hidrolisis Ampas Tapioka Menggunakan Pemanasan Gelombang Mikro untuk Produksi Etanol adalah karya saya dengan arahan dari komisi pembimbing dan belum diajukan dalam bentuk apa pun kepada perguruan tinggi mana pun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir disertasi ini.
ABSTRACT
EUIS HERMIATI. Process engineering of cassava pulp hydrolysis using microwave heating for ethanol production. Under direction of DJUMALI MANGUNWIDJAJA, TITI C. SUNARTI, ONO SUPARNO, and BAMBANG PRASETYA
Cassava pulp is a potential source of carbohydrates. In this work, characteristics of the cassava pulp were analyzed and validity of microwave irradiation for hydrolysis of carbohydrates, especially starch present in the cassava pulp, was estimated as a non-enzymatic saccharification technique. The hydrolysis was performed in water and acid medium. In addition, the role of activated carbon in the microwave-assisted hydrolysis was also evaluated. An optimization of the hydrolysis was conducted using Central Composite Design (CCD) and was analyzed using Response Surface Methodology (RSM). Fermentation of cassava pulp hydrolysates produced from microwave-assisted acid hydrolysis was performed to those added with activated carbon (25% w/w) and those without activated carbon by Saccharomyces cerevisiae. There were two types of activated carbon, which have different adsorption properties, used in this experiment. Results of the cassava pulp characterization shows that the starch granules in the cassava pulp were trapped in biomass matrices, so that the starch was harder to hydrolyze than the free starch, such as that in tapioca flour. Microwave-assisted hydrolysis of cassava pulp can be completed in less than 15 minutes in water medium, and less than 10 minutes in acid medium. The addition of activated carbon improved hydrolysis of cassava pulp starch in water medium with suppression of formation of the secondary decomposed materials. The highest glucose yield obtained from cassava pulp was 46% of dry matter or 52% of theoretical, which was about 60% higher than the one without the addition of activated carbon. On the contrary, the addition of activated carbon decreased the glucose yield when the hydrolysis was performed in acid medium (0.5% H2SO4). The glucose yield could reach 80.8% of dry matter or 91.5% of theoretical yield when no activated carbon was added in the acid medium. The estimated optimum condition for cassava pulp hydrolysis under microwave irradiation was using 0.88% sulfuric acid with 9 minutes of heating time, which resulted in 85% of theoretical glucose yield and 140 g/L glucose concentration. At the end of the fermentation the ethanol yield and concentration obtained in the samples treated with activated carbon (0.41-0.43 g ethanol / g glucose consumed; 34-35 g/L) were lower than that not treated with activated carbon or those treated with activated carbon which was added after hydrolysis (0.48 g ethanol / glucose consumed; 38-39 g/L). However, the fermentation was completed very much faster in the hydrolysates treated with the activated carbon which has a high adsorption capacity than in that not treated with activated carbon or those treated with activated carbon of low adsorption capacity. Therefore, ethanol productivities (0.44-0.55 g/L/h) of the former were higher than the latter (0.28-0.34 g/L/h). Keywords: Cassava pulp, microwave-assisted hydrolysis, activated carbon,
RINGKASAN
EUIS HERMIATI. Rekayasa proses hidrolisis ampas tapioka menggunakan pemanasan gelombang mikro untuk produksi etanol. Dibimbing oleh DJUMALI MANGUNWIDJAJA, TITI C. SUNARTI, ONO SUPARNO dan BAMBANG PRASETYA
Ampas tapioka adalah limbah padat industri tapioka yang banyak mengandung karbohidrat (± 95%), khususnya pati, sehingga merupakan salah satu bahan yang potensial sebagai sumber glukosa. Oleh karena itu, proses hidrolisis pati ampas tapioka menjadi glukosa merupakan tahapan utama yang perlu mendapat perhatian. Hidrolisis pati dapat dilakukan menggunakan cara hidrotermal, menggunakan larutan asam, enzim ataupun kombinasi ketiganya. Setiap metode yang digunakan mempunyai kelebihan dan kekurangan. Pemanasan gelombang mikro adalah salah satu alternatif metode yang dapat digunakan untuk hidrolisis pati. Tujuan umum penelitian ini adalah untuk mengkaji proses hidrolisis ampas tapioka menggunakan pemanasan gelombang mikro, dan pemanfaatan hasil hidrolisis untuk produksi etanol. Secara khusus penelitian bertujuan untuk mempelajari peranan faktor-faktor yang terlibat dalam proses hidrolisis ampas tapioka menggunakan pemanasan gelombang mikro, mendapatkan kondisi optimum proses hidrolisis dan mempelajari pengaruh penambahan karbon aktif terhadap kinerja fermentasi hidrolisat ampas tapioka menjadi etanol.
Penelitian diawali dengan karakterisasi ampas tapioka, dan dilanjutkan dengan hidrolisis ampas tapioka menggunakan iradiasi gelombang mikro. Hidrolisis dilakukan dalam medium air maupun asam, baik dengan maupun tanpa penambahan karbon aktif. Optimasi hidrolisis dilakukan menggunakan Central Composite Design (CCD) dan dianalisis dengan Response Surface Methodology (RSM) dengan bantuan piranti lunak Minitab® Release 16. Selanjutnya, dilakukan percobaan fermentasi terhadap hidrolisat yang diperoleh dari proses hidrolisis pada kondisi optimum.
Granula pati di dalam ampas tapioka masih terikat pada matriks serat biomassa, sehingga proses hidrolisisnya lebih sulit dibandingkan dengan proses hidrolisis pati dalam tapioka yang granulanya sudah dalam keadaan bebas. Selain pati, ampas tapioka juga mengandung senyawa karbohidrat lain, yaitu selulosa dan hemiselulosa, yang terdiri dari arabinan, rhamnan, galaktan, xilan, dan mannan. Pola spektrum difraksi sinar X pati ampas tapioka mirip dengan pola spektrum pati tapioka, yaitu mendekati pola spektrum pati tipe A.
Pada proses hirolisis pati ampas tapioka dalam medium air menggunakan iradiasi gelombang mikro maltooligomer mulai terdeteksi pada suhu 220 °C. Karbohidrat lain yang terkandung dalam ampas tapioka juga terlarut secara bertahap. Senyawa arabinan adalah yang paling mudah larut, diikuti oleh rhamnan, mannan, galaktan dan xilan. Adapun selulosa merupakan komponen yang paling tahan dan tetap berada dalam residu ampas tapioka setelah pemanasan pada suhu 240 °C. Rendemen glukosa tertinggi yang diperoleh masih rendah, yaitu 28,59% dari berat bahan kering atau 32,41% dari teoritis.
gelombang mikro. Penambahan karbon aktif (1,0 g/g) menghasilkan rendemen glukosa lebih tinggi (45-46% dari teoritis) dengan suhu hidrolisis yang lebih rendah (220 °C selama 5 menit) dibandingkan yang diperoleh dari hidrolisat tanpa penambahan karbon aktif (32,41% dari teoritis pada 230 °C selama 5 menit). Warna hidrolisat yang dihasilkan lebih terang yang menandakan lebih rendahnya kadar senyawa hasil dekomposisi sekunder karbohidrat. Rendemen glukosa tertinggi (52,27% dari teoritis) dari ampas tapioka diperoleh setelah hidrolisis dengan penambahan karbon aktif (1,0 g/g) pada suhu 210 °C selama 15 menit.
Dengan menggunakan asam sulfat 0,5% dan hidrolisis selama 10 menit pada tingkat iradiasi 550 W dapat diperoleh rendemen glukosa tertinggi (80,80% dari berat bahan kering atau 91,52% dari teoritis). Jika karbon aktif ditambahkan pada proses hidrolisis, maka rendemen yang diperoleh menjadi lebih rendah. Peningkatan konsentrasi substrat meningkatkan konsentrasi glukosa dalam hidrolisat, namun menurunkan rendemen glukosa. Konsentrasi substrat 15% menghasilkan perolehan glukosa per g pati tertinggi, namun perolehan tersebut tidak berbeda nyata dengan penggunaan konsentrasi substrat 20%. Penelitian selanjutnya dilakukan pada konsentrasi substrat 20%. Hasil analisis ragam pada proses optimasi menggunakan RSM menunjukkan bahwa model regresi kuadratik yang diperoleh bersifat nyata dan layak untuk digunakan. Kondisi optimum hidrolisis adalah pada tingkat konsentrasi asam sulfat 0,88% dan lama pemanasan 9 menit dengan hasil rendemen glukosa 85% dari teoritis dan konsentrasi glukosa 140 g/L. Validasi model pada beberapa titik pengamatan menunjukkan bahwa model dapat digunakan untuk memprediksi rendemen glukosa pada proses hidrolisis asam ampas tapioka menggunakan iradiasi gelombang mikro.
Pada proses fermentasi dipelajari pengaruh penggunaan dua jenis karbon aktif dengan sifat adsorpsi berbeda terhadap kinerja fermentasi hidrolisat ampas tapioka yang dihasilkan pada kondisi optimum. Karbon aktif (25% b/b) ditambahkan ke dalam suspensi ampas tapioka sebelum hidrolisis menggunakan pemanasan gelombang mikro atau ke dalam hidrolisat sebelum fermentasi. Fermentasi hidrolisat menggunakan Saccharomyces cerevisiae LIPI MC 0070 (10% v/v) dilakukan pada suhu kamar dengan kecepatan 150 rpm selama 120 jam. Di akhir fermentasi hasil dan konsentrasi etanol yang diperoleh dari proses dengan penambahan karbon aktif saat hidrolisis (0,41-0,43 g etanol / g glukosa; 34-35 g/L) lebih rendah dari proses tanpa penambahan karbon aktif maupun dengan penambahan karbon aktif setelah hidrolisis (0,48 g etanol / g glukosa; 38-39 g/L). Fermentasi berlangsung jauh lebih cepat pada hidrolisat dengan penambahan karbon aktif yang mempunyai daya adsorpsi yang tinggi dibandingkan dengan pada hidrolisat tanpa karbon aktif atau dengan penambahan karbon aktif yang memiliki daya adsorpsi yang rendah. Produktivitas etanol yang dihasilkan pun (0,44-0,55 g/L/jam) lebih tinggi pada perlakuan tersebut dibandingkan dengan pada perlakuan lainnya (0,28-0,34 g/L/jam).
Hidrolisis menggunakan iradiasi gelombang mikro dengan penambahan karbon aktif dapat dijadikan sebagai salah satu alternatif metode hidrolisis ampas tapioka menjadi glukosa yang selanjutnya akan digunakan untuk produksi etanol, dengan hasil yang setara atau lebih baik dari metode lain yang telah diteliti. Kata kunci: ampas tapioka, hidrolisis, gelombang mikro, karbon aktif, asam
©Hak Cipta milik IPB, tahun 2012
Hak Cipta dilindungi Undang-Undang
Dilarang mengutip sebagian atau seluruh karya tulis ini tanpa mencantumkan atau menyebutkan sumbernya. Pengutipan hanya untuk kepentingan pendidikan, penelitian, penulisan karya ilmiah, penyusunan laporan, penulisan kritik, atau tinjauan suatu masalah; dan pengutipan tersebut tidak merugikan kepentingan yang wajar IPB
REKAYASA PROSES HIDROLISIS AMPAS TAPIOKA
MENGGUNAKAN PEMANASAN GELOMBANG MIKRO
UNTUK PRODUKSI ETANOL
EUIS HERMIATI
Disertasi
Sebagai salah satu syarat untuk memperoleh gelar Doktor pada
Program Studi Teknologi Industri Pertanian
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
Penguji pada Ujian Tertutup: Dr. Ir. Liesbetini Hartoto, MS
Prof. Dr. Ir. Khaswar Syamsu, M.Sc.St. Penguji pada Ujian Terbuka: Dr. Ir. Koesnandar, M.Eng.
PRAKATA
Segala puji dan syukur penulis panjatkan kehadirat Allah SWT atas segala Rahmat dan HidayahNya, sehingga penulis dapat menyelesaikan penyusunan disertasi yang berjudul Rekayasa Proses Hidrolisis Ampas Tapioka Menggunakan Pemanasan Gelombang Mikro untuk Produksi Etanol.
Pada kesempatan ini penulis menyampaikan rasa terimakasih kepada yang terhormat Prof. Dr. Ir. Djumali Mangunwidjaja, DEA selaku Ketua Komisi Pembimbing, Dr. Ir. Titi Candra Sunarti, M.Si, Dr. Ono Suparno, S.TP, MT dan Prof. Dr. Ir. Bambang Prasetya, M.Sc. selaku Anggota Komisi Pembimbing yang senantiasa memberikan bimbingan, arahan dan dorongan kepada penulis, sehingga penulis dapat menyelesaikan penyusunan disertasi ini.
Ucapan terimakasih penulis sampaikan kepada Ketua dan Sekretaris Program Studi Teknologi Industri Pertanian (TIP), Dekan Fakultas Teknologi Pertanian IPB, Sekolah Pascasarjana IPB yang telah banyak membantu dalam kelancaran studi S3 di IPB. Ungkapan yang sama penulis sampaikan kepada Pengelola Program Karyasiswa Kementerian Riset dan Teknologi yang telah memberikan beasiswa kepada penulis untuk menempuh jenjang pendidikan S3 di Sekolah Pascasarjana IPB, kepada Kepala UPT Balai Penelitian dan Pengembangan Biomaterial – LIPI yang telah membantu dan memberikan kemudahan untuk melakukan penelitian, serta kepada keluarga besar UPT BPP Biomaterial – LIPI atas segala dorongan semangat dan bantuannya selama penulis mengikuti progarm S3. Penulis sangat menghargai bantuan, saran dan arahan dari Prof. Jun-ichi Azuma dan Dr. Shuntaro Tsubaki dari Kyoto University selama penulis melakukan penelitian di Kyoto University, Jepang. Penulis juga berterimakasih atas semua saran dan masukan dari Dr. Ir. Liesbetini Hartoto MS dan Prof. Dr. Ir. Khaswar Syamsu, M.Sc.St. sebagai penguji luar komisi serta dari Dr. Ir. Machfud, MS dan Dr. Ir. Sugiyono M.App.Sc., masing-masing selaku Ketua Program Studi TIP dan Pimpinan Sidang pada ujian tertutup. Ucapan yang sama penulis sampaikan kepada Dr. Ir. Koesnandar M.Eng. dan Dr. Ir. Meika Syahbana Rusli, M.Sc.Agr. yang telah berkenan menjadi penguji luar komisi pada ujian terbuka serta kepada teman-teman mahasiswa S3 TIP IPB angkatan 2008 atas kerjasama dan dorongan semangat yang diberikan.
Terimakasih yang tak terhingga kepada keluarga, terutama ibunda (alm), suami dan anak-anak, atas doa, pengertian, kesabaran, pengorbanan dan dukungan yang diberikan kepada penulis selama menempuh program S3.
Penulis menyadari bahwa karya ilmiah ini tidak sempurna. Oleh karena itu, kritik dan saran sangat diharapkan untuk perbaikan di masa mendatang. Penulis berharap semoga hasil penelitian ini bermanfaat bagi yang membutuhkannya.
RIWAYAT HIDUP
Penulis dilahirkan di Jakarta pada tanggal 23 September 1960 sebagai anak sulung dari enam bersaudara dari pasangan Suherman (Alm) dan Anisah (Alm). Penulis menyelesaikan pendidikan dasar dan menengah di Jakarta. Pendidikan sarjana ditempuh pada Jurusan Teknologi Hasil Pertanian, Fakultas Teknologi Pertanian IPB, lulus pada tahun 1983. Pada tahun 1986 penulis memperoleh beasiswa Overseas Fellowship Program dari Kementerian Riset dan Teknologi Republik Indonesia untuk melanjutkan studi pada program studi Food Science, Graduate School, Rutgers University, New Brunswick, New Jersey, AS dan menamatkannya pada tahun 1989. Kesempatan untuk melanjutkan ke program doktor pada program studi Teknologi Industri Pertanian, Sekolah Pasca Sarjana IPB dengan beasiswa dari Kementerian Riset dan Teknologi Republik Indonesia diperoleh pada tahun 2008.
Penulis memulai karir sebagai staf peneliti pada Lembaga Fisika Nasional (sekarang Pusat Penelitian Fisika) – LIPI di Bandung pada tahun 1984. Setelah itu, pada tahun 1989 penulis mendapat tugas pada Balai Pengembangan Teknologi Tepat Guna – LIPI di Subang dan pada tahun 1990-1992 pada Balai Penelitian dan Pengembangan Sumberdaya Laut, Pusat Penelitian Oseanologi (sekarang Balai Konservasi Biota Laut, Pusat Penelitian Oseanografi) – LIPI di Ambon. Pada tahun 1997-2002 penulis bertugas di Pusat Penelitian dan Pengembangan Fisika Terapan (sekarang Pusat Penelitian Fisika) – LIPI di Serpong. Sejak tahun 2002 sampai saat ini penulis menjadi staf peneliti pada UPT Balai Penelitian dan Pengembangan Biomaterial – LIPI di Cibinong, Bogor.
Selagi menempuh pendidikan S3 penulis memperoleh JSPS Invitation Fellowship dari JSPS (Japan Society for the Promotion of Science) dan beasiswa pemagangan dari Kementerian Riset dan Teknologi, keduanya digunakan untuk melakukan penelitian di Laboratory of Forest Biochemistry, Graduate School of Agriculture, Kyoto University, Jepang, masing-masing pada bulan April – Juni 2010 dan Oktober – November 2010.
Selama menempuh pendidikan S3 penulis mengikuti beberapa seminar dan simposium, antara lain National Conference on Biomass Utilization for Alternative Energy and Chemicals, The 1st International Symposium for Sustainable Humanosphere, Innovation in Polymer Science and Technology 2011, International Symposium on Sustainable Use of Tropical Rainforest with the Intensive Forest Management and Advanced Utilization of Forest Resources dan The 2nd Korea-Indonesia Workshop and International Symposium on Bioenergy from Biomass. Beberapa karya ilmiah yang merupakan bagian dari program S3 penulis juga telah dan akan diterbitkan pada jurnal ilmiah nasional maupun internasional, sebagai berikut.
2. Hermiati E, Mangunwidjaja D, Sunarti TC, Suparno O, Prasetya B. 2010. Application of microwave heating in biomass hydrolysis and pretreatment for ethanol production. Annales Bogorienses 14(1): 1-9.
3. Hermiati E, Mangunwidjaja D, Sunarti TC, Suparno O, Prasetya B. 2012. Potential utilization of cassava pulp for ethanol production in Indonesia. Scientific Research and Essays 7(2): 100-106.
4. Hermiati E, Azuma J, Mangunwidjaja D, Sunarti TC, Suparno O, Prasetya B. 2011. Hydrolysis of carbohydrates in cassava pulp and tapioca flour under microwave irradiation. Indo J Chem 11: 238-245.
5. Hermiati E, Azuma J, Tsubaki S, Mangunwidjaja D, Sunarti TC, Suparno O, Prasetya B. 2012. Improvement of microwave-assisted hydrolysis of cassava pulp and tapioca flour by addition of activated carbon. Carbohydr Polym 87: 939-942.
6. Hermiati E, Mangunwidjaja D, Sunarti TC, Suparno O, Prasetya B. 2012. Microwave-assisted acid hydrolysis of starch polymer in cassava pulp in the presence of activated carbon. Procedia Chem (diterima untuk publikasi). 7. Hermiati E, Mangunwidjaja D, Sunarti TC, Suparno O, Prasetya B, Risanto L.
DAFTAR ISI
Halaman
DAFTAR TABEL ... xxi
DAFTAR GAMBAR ... xxiii
DAFTAR LAMPIRAN ... xxv
BAB I PENDAHULUAN ... 1
1.1. Latar Belakang ... 1
1.2. Perumusan Masalah ... 7
1.3. Tujuan Penelitian ... 9
1.4. Ruang Lingkup ... 9
1.5. Kerangka Pemikiran ... 10
BAB II HIDROLISIS AMPAS TAPIOKA DALAM MEDIUM AIR MENGGUNAKAN PEMANASAN GELOMBANG MIKRO 13 Abstrak ... 13
2.1. Pendahuluan ... 14
2.2. Bahan dan Metode ... 17
2.3. Hasil dan Pembahasan ... 19
2.4. Simpulan dan Saran ... 33
BAB III PENINGKATAN HIDROLISIS AMPAS TAPIOKA MENGGUNAKAN PEMANASAN GELOMBANG MIKRO DENGAN PENAMBAHAN KARBON AKTIF ... 35
Abstrak ... 35
3.1. Pendahuluan ... 36
3.2. Bahan dan Metode ... 36
3.3. Hasil dan Pembahasan ... 38
3.4. Simpulan dan Saran ... 50
BAB IV PENINGKATAN HIDROLISIS AMPAS TAPIOKA PADA PEMANASAN GELOMBANG MIKRO DENGAN PENGGUNAAN MEDIUM ASAM ... 51
Abstrak ... 51
4.1. Pendahuluan ... 52
4.2. Bahan dan Metode ... 54
4.3. Hasil dan Pembahasan ... 56
Halaman BAB V FERMENTASI ETANOL TERHADAP HASIL
HIDROLISIS ASAM AMPAS TAPIOKA
MENGGUNAKAN PEMANASAN GELOMBANG MIKRO DAN KARBON AKTIF DENGAN Saccharomyces
cerevisiae ... 73
Abstrak ... 73
5.1. Pendahuluan ... 74
5.2. Bahan dan Metode ... 76
5.3. Hasil dan Pembahasan ... 79
5.4. Simpulan dan Saran ... 90
BAB VI PEMBAHASAN UMUM ... 93
6.1. Karakteristik ampas tapioka ... 93
6.2. Peranan pemanasan gelombang mikro pada hidrolisis ampas tapioka dalam medium air ... 94
6.3. Peranan pemanasan gelombang mikro pada hidrolisis ampas tapioka dalam medium asam ... 95
6.4 Peranan karbon aktif pada hidrolisis dan kinerja fermentasi ... 96
6.5. Potensi penggunaan pemanasan gelombang mikro untuk proses hidrolisis ampas tapioka ... 100
BAB VII SIMPULAN DAN SARAN ... 103
7.1. SIMPULAN ... 103
7.2. SARAN ... 104
DAFTAR PUSTAKA ... 105
DAFTAR TABEL
Halaman 1.1 Estimasi potensi etanol yang dapat dihasilkan dari ampas tapioka .. 3 2.1 Komposisi kimia ampas tapioka dan tapioka ... 21 2.2 Komposisi relatif gula netral dalam ampas tapioka ... 21 2.3 Kristalinitas ampas tapioka dan tapioka ... 23 2.4 Hasil glukosa yang diperoleh dari hidrolisis ampas tapioka dan
tapioka menggunakan pemanasan gelombang mikro ... 28 2.5 Komposisi relatif gula netral dalam ampas tapioka dan residu
ampas tapioka setelah pemanasan gelombang mikro ... 33 3.1 Karakteristik karbon aktif ………. 39 3.2 Pengaruh suhu pemanasan dan jenis karbon aktif terhadap nilai pH
dan pembentukan senyawa berwarna coklat dalam hidrolisat
ampas tapioka ... 45 3.3 Pengaruh lama pemanasan dan jumlah karbon aktif terhadap fraksi
terlarut, hasil glukosa, nilai pH, dan pembentukan senyawa berwarna coklat pada hidrolisat ampas tapioka setelah pemanasan gelombang mikro pada suhu 210 °C ... 49 4.1 Karakteristik karbon aktif ………. 57 4.2 Nilai pH hidrolisat ampas tapioka setelah hidrolisis dalam medium
asam sulfat 0,5% menggunakan pemanasan gelombang mikro ... 61 4.3 Nilai absorbansi pada 490 nm hidrolisat ampas tapioka setelah
hidrolisis dalam medium H2SO4 0,5% menggunakan iradiasi
gelombang mikro ... 62 4.4 Kadar HMF (mg/100 g) dalam hidrolisat ampas tapioka setelah
hidrolisis dalam medium H2SO4 0,5% menggunakan iradiasi
gelombang mikro ... 62 4.5 Pengaruh lama pemanasan terhadap hidrolisat ampas tapioka
setelah iradiasi gelombang mikro pada tingkat daya 550 W dengan H2SO4 0,5% ... 64 4.6 Pengaruh konsentrasi H2SO4 terhadap hidrolisat ampas tapioka
setelah iradiasi gelombang mikro pada tingkat daya 550 W selama 10 menit ... 64 4.7 Pengaruh konsentrasi substrat suspensi ampas tapioka terhadap
perolehan glukosa dari hidrolisis dalam medium asam sulfat 0,5% menggunakan pemanasan gelombang mikro ... 66 4.8 Rancangan CCD dengan nilai respon percobaan dan nilai dugaan
hasil glukosa yang diperoleh dari hidrolisis asam ampas tapioka
Halaman 4.9 Analisis ragam model regresi derajat dua hasil glukosa ……….... 69
4.10 Nilai percobaan dan nilai dugaan hasil glukosa pada berbagai
kondisi hidrolisis untuk validasi model ... 70 5.1 Perubahan kadar gula total, gula pereduksi dan derajat
polimerisasi gula dalam hidrolisat ampas tapioka selama
fermentasi dengan S. cerevisiae ... 83 5.2 Produksi etanol dari hidrolisat ampas tapioka selama fermentasi
dengan S. cerevisiae ... 86 5.3 Hasil etanol yang diperoleh dari proses fermentasi hidrolisat
ampas tapioka dengan S. cerevisiae ... 87 6.1 Konsumsi energi pada proses hidrolisis ampas tapioka
DAFTAR GAMBAR
Halaman 1.1 Kerangka pemikiran penelitian ... 11 2.1 Citra SEM ampas tapioka dan tapioka ... 22 2.2 Difraktogram sinar X ampas tapioka dan tapioka ... 23 2.3 Pengaruh suhu pemanasan gelombang mikro terhadap kelarutan dan
kadar gula total hidrolisat ampas tapioka (pemanasan pendahuluan 4 menit, pemanasan pada suhu yang diinginkan 5 menit) ... 25 2.4 Pengaruh lama pemanasan pendahuluan terhadap kelarutan dan kadar
gula total hidrolisat ampas tapioka (suhu 230 °C, 5 menit) ... 25 2.5 Kromatogram HPLC hasil degradasi pati dalam ampas tapioka dan
tapioka setelah pemanasan gelombang mikro pada berbagai suhu ... 26 2.6 Pengaruh suhu pemanasan gelombang mikro terhadap pH hidrolisat
ampas tapioka dan tapioka (pemanasan pendahuluan 4 menit,
pemanasan pada suhu yang diinginkan 5 menit) ... 29 2.7 Pengaruh lama pemanasan pendahuluan terhadap pH hidrolisat ampas
tapioka dan tapioka (suhu 230 °C, 5 menit) ... 30 2.8 Hidrolisat ampas tapioka dan tapioka setelah pemanasan gelombang
mikro pada suhu 140-240 °C selama 5 menit ... 31 2.9 Pengaruh suhu pemanasan gelombang mikro terhadap nilai
absorbansi pada 490 nm dan kadar HMF pada hidrolisat ampas tapioka dan tapioka (pemanasan pendahuluan 4 menit, pemanasan
pada suhu yang diinginkan 5 menit) ... 32 2.10 Citra SEM residu ampas tapioka setelah pemanasan gelombang mikro
pada suhu 140-230 °C ... 34 3.1 Fraksi terlarut dalam hidrolisat ampas tapioka dan hasil glukosa
setelah iradiasi gelombang mikro selama 5 menit ... 41 3.2 Kromatogram HPLC dari senyawa glukosa dan maltooligomer dalam
hidrolisat ampas tapioka dengan perlakuan karbon aktif granul
(KAG) dan karbon aktif tepung (KAT) ... 42 3.3 Kromatogram HPLC dari senyawa glukosa dan maltooligomer dalam
hidrolisat dan rendemen glukosa dari tapioka setelah hidrolisis selama 5 menit menggunakan iradiasi gelombang mikro tanpa dan dengan
penambahan karbon aktif granul (KAG) ... 43 3.4 Hidrolisat ampas tapioka dari pemanasan gelombang mikro (180-230
°C) selama 5 menit dalam medium air dengan penambahan karbon aktif granul dan karbon aktif tepung ... 45 3.5 Citra SEM residu ampas tapioka setelah pemanasan gelombang mikro
Halaman 3.6 Kromatogram HPLC dari senyawa glukosa dan maltooligomer yang
terdapat dalam hidrolisat ampas tapioka setelah pemanasan
gelombang mikro pada suhu 210 °C dengan variasi lama pemanasan dan setelah pemanasan gelombang mikro pada suhu 210 °C selama
12 menit dengan variasi rasio karbon aktif (KA) / ampas tapioka (AT) 47 3.7 Citra SEM residu ampas tapioka setelah pemanasan gelombang mikro
pada suhu 210 °C selama 5 dan 18 menit dengan penambahan karbon aktif granul (KAG) . ... 48 4.1 Kadar total padatan terlarut hidrolisat ampas tapioka setelah hidrolisis
dalam medium H2SO4 0,5% menggunakan pemanasan gelombang
mikro ... 58 4.2 Hasil glukosa yang diperoleh dari hidrolisis ampas tapioka dalam
medium H2SO4 0,5% menggunakan iradiasi gelombang mikro pada tingkat daya iradsiasi 330 W dan 550 W ... 59 4.3 Citra SEM residu ampas tapioka setelah iradiasi gelombang mikro
pada tingkat daya 550 W dengan asam sulfat 0,5% ... 65 4.4 Citra SEM residu ampas tapioka setelah iradiasi gelombang mikro
pada tingkat daya 550 W selama 10 menit dengan variasi konsentrasi
asam sulfat ……….…... 65
4.5 Plot kontur dan plot permukaan pengaruh konsentrasi asam dan lama pemanasan terhadap hasil glukosa yang diperoleh dari hidrolisis
asam ampas tapioka menggunakan iradiasi gelombang mikro ... 70 5.1 Diagram alir proses persiapan hidrolisat ampas tapioka sampai
fermentasi ... 77 5.2 Pengaruh jumlah karbon aktif terhadap hasil glukosa dan kadar HMF
hidrolisat ampas tapioka ... 80 5.3 Perubahan pH hidrolisat selama fermentasi ... 81 5.4 Perubahan kadar total padatan terlarut dalam hidrolisat selama
DAFTAR LAMPIRAN
Halaman 1 Prosedur analisis komponen kimia bahan (analisis proksimat, kadar
serat kasar, pati dan amilosa) ... 115 2 Prosedur analisis arang aktif (pH, daya serap terhadap senyawa I2,
daya serap terhadap biru metilena dan luas permukaan) ... 127 3 Prosedur analisis komponen kimia hasil hidrolisis ampas tapioka ... 129 4 Perhitungan produksi dan hasil etanol dari proses fermentasi
PENDAHULUAN
1.1. Latar Belakang
Ubikayu (Manihot esculenta Crantz) merupakan salah satu tanaman yang penting di dunia. Tanaman ini merupakan salah satu sumber bahan pangan yang banyak dikonsumsi di Asia, Afrika dan Amerika Latin. Produksi ubikayu Indonesia pada tahun 2010 mencapai 23,9 juta ton, menempati urutan ketiga setelah Nigeria dengan produksi 37,5 juta ton dan Brazilia dengan produksi 24,4 juta ton (FAO 2012). Urutan ke empat dan ke lima produsen ubikayu pada tahun 2010 ditempati oleh Thailand dengan produksi 22,0 juta ton dan Republik Demokratik Kongo dengan produksi 11,5 juta ton (FAO 2012).
Ubikayu dikonsumsi setelah diolah menjadi beberapa bahan makanan tradisional, gaplek ataupun tapioka. Ketersediaan ubikayu sebagai bahan pangan belakangan ini dikhawatirkan terancam karena gencarnya upaya substitusi bahan bakar minyak dengan bioetanol menggunakan bahan dasar ubikayu; padahal ubikayu adalah komoditas yang sangat berperanan dalam mencukupi kebutuhan pangan masyarakat di Asia, Afrika dan Amerika Latin. Dengan demikian, kebijakan mengolah bahan pangan untuk bahan bakar tampaknya perlu ditinjau kembali, karena masih banyak bahan lain yang bukan merupakan bahan pangan yang dapat dimanfaatkan sebagai penghasil bioetanol. Di antara bahan tersebut adalah ampas tapioka atau yang biasa kita kenal dengan sebutan onggok yang merupakan salah satu limbah padat industri tapioka disamping kulit ubikayu. Kandungan utama ampas tapioka adalah karbohidrat, yaitu pati dan serat atau selulosa. Dengan demikian, bahan ini sangat berpotensi untuk dijadikan sebagai salah satu bahan penghasil bioetanol.
jika ampas tapioka akan digunakan sebagai pakan ternak. Pada produksi biogas ampas tapioka juga perlu dicampur dengan bahan lain yang mempunyai kadar nitrogen lebih tinggi agar diperoleh nilai rasio C/N yang memungkinkan proses digesti anaerobik oleh bakteri untuk menghasilkan gas metana dapat berjalan dengan baik.
Pengolahan 250-300 ton umbi ubikayu menghasilkan sekitar 1,16 ton kulit dan 280 ton ampas tapioka dengan kadar air sekitar 85% (Pandey et al. 2000). Hasil analisis terhadap ampas tapioka yang diperoleh dari beberapa tempat di Brazilia dan diambil pada waktu yang berbeda-beda menunjukkan kadar air 5,02-11,20 g/100 g bahan kering, protein 0,32-1,61, lipid 0,53-1,06, serat 14,88-50,55, abu 0,66-1,50 dan karbohidrat 40,50-63,85g/100 g bahan kering (Pandey et al. 2000). Dilihat dari komposisi kimianya, ampas tapioka lebih mudah untuk dikonversi menjadi bioetanol, karena tidak lagi memerlukan proses pretreatment
(perlakuan pendahuluan) seperti yang harus dilakukan pada bahan berlignoselulosa, dan karbohidrat yang ada dapat dengan mudah dirombak oleh mikroorganisme, dengan proses kimiawi maupun hidrotermal.
Data Badan Pusat Statistik (2009) melaporkan bahwa produksi tapioka pada tahun 2009 adalah 675.266.703 kg, menurun cukup drastis dari produksi tahun 2007 sebesar 1.195.617.247 kg (BPS 2007) maupun produksi tahun 2008 sebesar 1.181.706.784 kg (BPS 2008). Penyebab terjadinya penurunan produksi bukan disebabkan oleh menurunnya produksi ubikayu di Indonesia, karena produksi ubikayu meningkat dari 20 juta ton pada tahun 2007 menjadi 21,6 juta ton pada tahun 2008 dan 21, 8 juta ton pada tahun 2009 (FAO 2012). Penurunan produksi tapioka diduga karena terjadinya pergeseran penggunaan ubikayu untuk keperluan lain, misalnya untuk produksi bioetanol.
0,44 kL dan 8,7 kL etanol per hari. Adapun potensi total etanol yang dapat dihasilkan dari ampas tapioka di seluruh Indonesia adalah 295.000 kL per tahun. Saat ini kebutuhan akan premium adalah 24 juta kL per tahun, sedangkan pertamax 800 ribu kL per tahun. Dengan target substitusi etanol sebesar 5%, maka dibutuhkan etanol sekitar 1,24 juta kL per tahun. Dengan demikian, potensi produksi bioetanol dari ampas tapioka sebesar 295.000 kL per tahun dapat membantu memenuhi kebutuhan akan bioetanol untuk substitusi bensin di Indonesia sebesar sekitar 23%. Selain itu, dengan dimanfaatkannya ampas tapioka sebagai bahan penghasil bioetanol, maka pencemaran limbah padat tapioka yang sangat mengganggu lingkungan di sekitar pabrik tapioka dapat diatasi, dan ketersediaan ubikayu sebagai bahan baku tapioka dan bahan pangan dapat tetap terjaga.
Tabel 1.1 Estimasi potensi etanol yang dapat dihasilkan dari ampas tapioka
Skala
(per hari) 20.000 86.957 17.391 8.735 Total Indonesia
(per tahun) 675.266.703 2.935.942.187 587.188.437 294.911.486
a)
Faktor konversi dari umbi ubikayu menjadi tapioka dan ampas tapioka masing-masing diasumsikan 0,23 dan 0,20
b)
Asumsi kadar pati 70%; konversi pati ke glukosa 1,11; konversi glukosa ke etanol 0,51; kerapatan etanol 0,789
Srinorakutara et al. 2004, 2006; Yamaji et al. 2006, 2007; Rattanachomsri et al.
2009, dan Kosugi et al. 2009; Thongchul et al. 2010; Djuma’ali et al. 2011; Apiwatanapiwat et al. 2011). Ampas tapioka juga dapat dimanfaatkan untuk menghasilkan beberapa produk lain, misalnya untuk pakan ternak (Pandey et al. 2000; Supriyati 2003; Ali 2006), sebagai substrat untuk pertumbuhan mikroba (Pandey et al. 2000; Ray 2004; Swain dan Ray 2007), untuk bahan komposit (Matsui et al. 2003, 2004), dan untuk adsorben (Tomanee 2008).
Mengingat kandungan utama ampas tapioka adalah pati, maka potensi pati dalam bahan ini yang perlu dioptimalkan. Agar pati dalam ampas tapioka dapat dimanfaatkan untuk menghasilkan berbagai macam produk dengan nilai tambah yang lebih tinggi, maka proses hidrolisis pati menjadi glukosa merupakan tahapan utama yang perlu mendapat perhatian. Hidrolisis pati dapat dilakukan menggunakan cara hidrotermal, menggunakan larutan asam, enzim ataupun kombinasi ketiganya. Setiap metode yang digunakan mempunyai kelebihan dan kekurangan. Proses hidrotermal atau asam biasanya berlangsung dalam waktu singkat, namun berpotensi menghasilkan senyawa inhibitor seperti hidroksi metil furfural (HMF) yang dapat menghambat pada proses fermentasi. Proses enzimatis lebih ramah lingkungan, tidak berpotensi menghasilkan senyawa inhibitor, namun prosesnya berlangsung lebih lama dan seringkali lebih mahal. Beberapa penelitian menunjukkan bahwa pemanasan dengan gelombang mikro dapat membantu proses likuifikasi dan/atau hidrolisis pati(Khan et al. 1979; Yu et al.1996; Kunlan
et al. 2001; Nikolic et al. 2008; Tsubaki et al. 2009; Tsubaki dan Azuma 2011; Matsumoto et al. 2008, 2011) serta proses hidrolisis selulosa (Cullingford et al.
1993; Robinson 2010). Pemanasan menggunakan gelombang mikro dapat dilakukan dalam medium air ataupun asam, biasanya asam kuat encer seperti HCl atau H2SO4. Hidrolisis menggunakan iradiasi gelombang mikro berlangsung lebih
Johnson 1972) ataupun dalam medium asam (HCl 0,45-0,5 M) dengan waktu sekitar 1 jam (Yu et al. 1996; Warrand dan Janssen 2007).
Gelombang mikro adalah salah satu jenis gelombang elektromagnetik yang mempunyai panjang gelombang sekitar 1 m hingga 1 mm, menghasilkan frekuensi antara 0,3 GHz untuk panjang gelombang 1 m hingga 300 GHz untuk panjang gelombang 1 mm (Lidstrom et al. 2001; Jones et al. 2002). Selang ini terletak di antara panjang gelombang sinar infra merah dan gelombang radio. Gelombang mikro digunakan pada radar, komunikasi gelombang mikro, TV UHF dan oven gelombang mikro. Untuk menghindari adanya gangguan atau interferensi, maka untuk keperluan pemanasan seperti pada oven gelombang mikro untuk keperluan domestik maupun industri diatur, yaitu menggunakan panjang gelombang 12,2 cm atau frekuensi 2,45 GHz.
Gelombang elektromagnetik membawa sejumlah energi yang dapat dipindahkan secara radiasi atau tanpa medium perantara. Sebagai gelombang elektromagnetik gelombang mikro membawa medan listrik dan medan magnet. Gaya listrik yang diakibatkan medan listrik gelombang mikro akan memutar molekul-molekul yang bersifat dipolar atau mempunyai dua kutub, positif dan negatif, seperti air. Ketika berputar, molekul-molekul tersebut dapat saling bertubrukan, sehingga dihasilkan panas. Gelombang mikro juga dapat membuat molekul yang mengandung ion positif dan negatif bergerak secara dilatasi dan pergerakan ini mengakibatkan terjadinya gesekan antar molekul sehingga menimbulkan panas. Panas yang dihasilkan karena tubrukan atau gesekan antar molekul inilah yang akan meningkatkan suhu bahan yang dikenai gelombang mikro dalam sebuah oven gelombang mikro (microwave oven). Oleh karena itu pemanasan dengan gelombang mikro dinamakan juga pemanasan dielektrik.
gelombang mikro ke bahan. Aplikator yang paling umum adalah sebuah
multimode cavity yang terdiri dari kotak yang menyediakan medan elektromagnetik yang seragam. Energi gelombang mikro langsung dipindahkan ke molekul-molekul yang ada di dalam bahan. Molekul-molekul ini menjadi terstimulasi dan berputar jutaan kali per detik sebagai responnya terhadap medan elektromagnetik. Perputaran molekul ini secara cepat menghasilkan panas di dalam bahan.
Pemanasan yang terjadi pada sistem gelombang mikro berkaitan dengan sifat dielektrik bahan. Sifat dielektrik bahan biasanya digambarkan dengan konstanta dielektrik dan loss factor dielektriknya (Motwani et al. 2007). Konstanta dielektrik (ε′) menggambarkan kemampuan bahan untuk menyimpan energi dan mempolarisasikannya ketika berada dalam medan listrik, sedangkan
loss factor dielektrik (ε′′) berhubungan dengan hilangnya energi medan dielektrik dalam bahan yang dikeluarkan dalam bentuk panas. Perbandingan antara loss factor dielektrik dan konstanta dielektrik adalah nilai loss tangent dielektrik (tan
δ), yang menggambarkan kemampuan bahan untuk menyerap energi gelombang mikro dan mengubahnya menjadi panas. Semakin tinggi nilai tan δ suatu bahan, maka semakin besar kemampuan bahan tersebut dalam mengubah energi gelombang mikro menjadi energi panas (Gabriel et al. 1998; Menendez et al.
2010).
Upaya meningkatkan hasil hidrolisis pati menggunakan pemanasan gelombang mikro telah dilakukan, antara lain dengan menambahkan garam anorganik yang mengandung ion Cl¯ atau SO42¯, dimana garam dengan ion Cl¯
Karbon aktif dengan nilai tan δ (0,57-0,80) yang lebih tinggi dari nilai tan δ air (0,12) memungkinkan terjadinya peningkatan proses pengubahan energi gelombang mikro menjadi energi panas dalam air (Menendez et al. 2010). Beberapa penelitian menunjukkan bahwa karbon dapat berfungsi sebagai absorben gelombang mikro dan katalis pada beberapa proses atau reaksi menggunakan pemanasan gelombang mikro, antara lain pada degradasi senyawa polutan NOx, SO2, metana, dan congo red, serta pada proses pirolisis (Zhang et al.
2007; Menendez et al. 2010). Keberadaan karbon aktif juga dilaporkan berpengaruh positif pada proses fermentasi glukosa menjadi etanol menggunakan
Saccharomyces cerevisiae (Ikegamai et al. 2000). Namun demikian, penggunaan karbon aktif dalam hidrolisis pati menggunakan pemanasan gelombang mikro baru dilaporkan oleh Matsumoto et al. (2008, 2011), dan itu pun baru digunakan untuk hidrolisis pati jagung murni dalam medium air.
Beberapa hasil penelitian juga menunjukkan bahwa pengaruh pemanasan oleh gelombang mikro terhadap pati ternyata berbeda dengan pengaruh pemanasan konduksi biasa (Yu et al. 1996; Palav dan Seetharaman 2006, 2007; Luo et al. 2006). Hidrolisis pati menggunakan iradiasi gelombang mikro dalam medium asam pada suhu 95 °C dapat menguraikan struktur β pada pati teretrogradasi, sehingga membuat pati menjadi terlarut dan selanjutnya dapat dihidrolisis, sedangkan pada proses termohidrolisis biasa dalam medium asam pada suhu 100 °C pati teretrogradasi tidak dapat dihidrolisis (Yu et al. 1996). Dengan demikian, keunggulan utama dari proses hidrolisis pati menggunakan iradiasi gelombang mikro adalah proses yang berlangsung cepat dan dapat terurainya struktur β pada pati teretrogradasi yang memungkinkan diperolehnya rendemen glukosa yang lebih tinggi.
1.2. Perumusan Masalah
hidrolisis pati untuk menghasilkan glukosa yang dilakukan dengan pemanasan gelombang mikro semuanya menggunakan pati murni sebagai bahan dasarnya. Penelitian terhadap pati yang masih terikat dalam matriks biomassa, seperti pati dalam ampas tapioka, belum banyak dilaporkan. Penelitian hidrolisis pati menggunakan pemanasan gelombang mikro yang dilaporkan sejauh ini juga hanya sampai dengan proses hidrolisis untuk memperoleh glukosa atau gula pereduksi, belum dilanjutkan dengan proses lanjutan, misalnya fermentasi glukosa atau gula pereduksi menjadi etanol. Proses lanjutan ini penting untuk diteliti agar dapat diketahui apakah hidrolisat yang dihasilkan dapat difermentasi dengan mudah atau tidak.
Sejauh ini belum didapat laporan penggunaan karbon aktif pada proses hidrolisis pati yang masih terikat dalam biomassa menggunakan pemanasan gelombang mikro, baik dalam medium air maupun asam. Penelitian penggunaan karbon aktif pada hidrolisis pati yang dilakukan Matsumoto et al. (2008, 2011) menggunakan bahan pati murni dan dalam medium air. Dengan demikian, belum diketahui dengan jelas bagaimana peranan karbon aktif pada hidrolisis bahan yang bukan merupakan pati murni menggunakan pemanasan gelombang mikro pada medium air maupun asam. Terlebih lagi jika dikaitkan dengan sifat karbon aktif yang merupakan bahan adsorber yang baik terhadap berbagai kotoran dan polutan dalam air. Di satu sisi, penggunaan karbon aktif dalam proses hidrolisis pati menggunakan pemanasan gelombang mikro diharapkan dapat mengadsorpsi beberapa senyawa yang terbentuk selama proses hidrolisis yang bersifat sebagai inhibitor pada proses lanjutan, misalnya fermentasi glukosa menjadi etanol. Di sisi lain, karbon aktif dapat pula mengadsorpsi maltooligomer (Moon dan Cho 1997; Yoo et al. 2005; Matsumoto et al. 2008, 2010) ataupun glukosa (Ikegamai
et al. 2000). Oleh karena itu, pada penelitian ini dipelajari proses hidrolisis karbohidrat, khususnya pati yang terdapat dalam biomassa ampas tapioka, menggunakan pemanasan gelombang mikro dalam medium air dan asam serta tanpa dan dengan penambahan karbon aktif.
pengaruh karbon aktif terhadap rendemen glukosa dan konsentrasi glukosa yang dihasilkan, dapat dilakukan optimasi proses hidrolisis untuk menghasilkan glukosa yang selanjutnya akan difermentasi menjadi etanol. Hasil penelitian ini diharapkan dapat memberi alternatif pemanfaatan hasil samping industri tapioka, mengurangi pencemaran lingkungan di sekitar pabrik serta mengurangi penggunaan bahan pangan sebagai bahan baku energi. Integrasi industri bioetanol dari ampas tapioka dengan industri tapioka diharapkan dapat mengurangi biaya produksi etanol, karena bahan baku sudah langsung dipasok oleh industri tapioka. Dengan demikian, harga etanol yang dihasilkan dapat lebih bersaing.
1.3. Tujuan Penelitian
Secara umum penelitian ini bertujuan untuk mengkaji proses hidrolisis ampas tapioka menggunakan perlakuan pemanasan gelombang mikro, dan pemanfaatan hasil hidrolisis untuk produksi etanol. Secara khusus penelitian bertujuan untuk mempelajari peranan faktor-faktor yang terlibat dalam proses hidrolisis ampas tapioka menggunakan pemanasan gelombang mikro, meliputi suhu atau derajat iradiasi, waktu pemanasan, konsentrasi asam, perbandingan padatan/cairan atau konsentrasi substrat dan ada tidaknya karbon aktif. Kondisi optimum hidrolisis ampas tapioka dengan pemanasan gelombang mikro adalah salah satu tujuan lain yang ingin diperoleh. Selain itu, dipelajari pula pengaruh adanya karbon aktif yang ditambahkan pada proses hidrolisis maupun sebelum fermentasi terhadap hasil fermentasi hidrolisat ampas tapioka menjadi etanol.
1.4. Ruang Lingkup
Ruang lingkup penelitian ini mencakup tiga aspek, yaitu:
1. Hidrolisis ampas tapioka menggunakan pemanasan gelombang mikro dalam medium air atau medium asam sulfat.
2. Fermentasi hidrolisat ampas tapioka yang diperoleh dari proses hidrolisis menggunakan pemanasan gelombang mikro pada kondisi optimum menjadi etanol.
1.5. Kerangka Pemikiran
HIDROLISIS AMPAS TAPIOKA DALAM MEDIUM AIR
MENGGUNAKAN PEMANASAN GELOMBANG MIKRO
Hydrolysis of cassava pulp in water medium under microwave
heating
Abstrak
Ampas tapioka merupakan salah satu bahan baku untuk menghasilkan glukosa yang potensial. Pada penelitian ini dilakukan karakterisasi dan hidrolisis ampas tapioka dalam medium air menggunakan iradiasi gelombang mikro sebagai salah satu teknik sakarifikasi non enzimatis. Karakterisasi dilakukan terhadap kandungan kimia ampas tapioka, sifat morfologi pati dan pola spektrum pati dalam ampas tapioka. Suspensi ampas tapioka dalam air (1g/20 mL) dipanaskan menggunakan iradiasi gelombang mikro pada suhu 140-240 °C selama 5 menit setelah sebelumnya dilakukan pemanasan pendahuluan selama 4 menit. Sebagai pembanding, hal yang sama dilakukan terhadap tapioka. Kelarutan komponen dalam ampas tapioka meningkat seiring meningkatnya suhu dan mencapai maksimum (92,54%) pada suhu 220 °C. Senyawa maltooligomer dari proses degradasi pati mulai terdeteksi pada suhu 220 °C. Karbohidrat lain, seperti senyawa gula penyusun hemiselulosa, yang terkandung dalam ampas tapioka juga terlarut secara bertahap. Senyawa arabinan adalah yang paling mudah larut, diikuti oleh rhamnan, mannan, galaktan dan xilan. Selulosa merupakan komponen yang paling tahan dan tetap berada dalam residu ampas tapioka setelah pemanasan pada suhu 240 °C. Nilai pH menurun seiring dengan meningkatnya suhu, sedangkan intensitas warna coklat dan kadar hidroksi metil furfural (HMF) sebaliknya. Hasil glukosa tertinggi yang diperoleh dari ampas tapioka mencapai 28,59% dari berat bahan kering atau 32,41% basis pati, yaitu pada pemanasan gelombang mikro dengan suhu 230 °C selama 5 menit. Variasi lama pemanasan pendahuluan pada suhu 230 °C tidak memberikan pengaruh yang nyata terhadap hasil glukosa dari ampas tapioka.
Kata kunci: ampas tapioka, gelombang mikro, hidrolisis, karbohidrat, glukosa
Abstract
gradually with arabinan was the most soluble, followed by rhamnan, mannan, galactan and xylan. Cellulose was found to be the most resistant component in the cassava pulp. It remained in the residue even after heat tretament at 240 °C. The pH value of the hydrolysates decreased as the temperature increased, whereas the intensity of the brown compounds and the hydroxymethyl furfural (HMF) content were vice versa. The highest glucose yield from the cassava pulp (28.59 of dry matter or 32,41% of starch-based theoretical yield) was obtained after microwave heating at 230 °C for 5 minutes. Variation of pre-heating time at 230 °C did not give significant effects on glucose yield from the cassava pulp.
Keywords: cassava pulp, microwave, hydrolysis, carbohydrate, glucose
2.1. Pendahuluan
Hidrolisis pati pada umumnya dilakukan secara enzimatis atau dengan menggunakan asam. Metode lain yang dapat digunakan adalah menggunakan proses termal seperti hidrotermal dan pemanasan gelombang mikro. Penelitian hidrolisis asam terhadap pati yang terkandung dalam ampas tapioka telah dilaporkan oleh Ahmed et al.(1983), Srikanta et al. (1987), Woiciechowski et al. (2002), Yoonan et al. (2004) dan Thongchul et al. (2010), sedangkan proses enzimatis dilaporkan oleh Jaleel et al. (1988), Woiciechowski et al. (2002), Chotineeranat et al. (2004), Kongkiattikajorn dan Yoonan (2004), Srinorakutara et al. (2004, 2006), Rattanachomsri et al. (2009) dan Thongchul et al. (2010). Asam yang digunakan pada umumnya adalah asam klorida dan asam sulfat, walaupun ada juga yang mencoba menggunakan asam fosfat atau asam asetat. Suhu dan waktu hidrolisis bervariasi, masing-masing 100-135 °C dan 5-90 menit. Konsentrasi asam bervariasi dari 0,01 sampai 5 Molar atau Normal. Hasil glukosa maksimum yang diperoleh pada umumnya sekitar 60-70% (berdasarkan berat bahan kering), walaupun dapat mencapai lebih dari 1 g per g bahan kering ketika digunakan konsentrasi asam yang tinggi, misalnya 1,25 N H2SO4 selama 60 menit,
1,5 N H2SO4 selama 30 menit atau 1,5-2 N H3PO4 selama 60 menit seperti yang
(Thongchul et al. 2010), selulase dan pektinase dengan hasil konsentrasi gula pereduksi 6,2% setelah hidrolisis selama 25 jam (Srinorakutara et al. 2006), atau selulase, pektinase dan xilanase dengan hasil 391 mg glukosa per g bahan kering atau 571 mg gula pereduksi per g bahan kering setelah hidrolisis selama 30 jam (Rattanachomsri et al. 2009). Peneliti lain melaporkan hasil penelitian hidrolisis ampas tapioka menggunakan proses hidrotermal (Yamaji et al. 2006, 2007) atau kombinasi proses hidrotermal dan enzimatis (Kosugi et al. 2009; Nair et al. 2011; Djuma’ali et al. 2011). Rendemen glukosa yang diperoleh dapat mencapai 70-75% dari berat bahan kering atau nilai dextrose equivalent mencapai 94%. Salah satu masalah yang dihadapi pada proses menggunakan asam adalah terbentuknya senyawa berwarna coklat, seperti furfural dan hidroksi metil furfural (HMF) yang merupakan hasil degradasi lanjut karbohidrat dalam bahan, walaupun hal ini biasanya dapat diatasi dengan menggunakan bahan pengadsorpsi seperti bentonit dan kaolin (Ahmed et al. 1983). Hidrolisis enzimatis menghasilkan produk yang bebas dari senyawa berwarna coklat, namun dianggap kurang ekonomis dibandingkan dengan proses asam karena memerlukan waktu yang lebih lama dan biaya proses yang lebih tinggi (Woiciechowski et al. 2002). Hidrolisis enzimatis yang digabungkan dengan ultra-filtrasi yang dikembangkan oleh Chotineeranat et al. (2004) dapat menghasilkan proses enzimatis yang lebih ekonomis, karena sistem ini dapat meningkatkan kecepatan produksi gula pereduksi sampai 20% lebih tinggi daripada proses tanpa ultra-filtrasi.
oleh Khan et al. (1979) (10 - 30%), Palav dan Seetharaman (2007) (33 - 50%), serta Nicolic et al. (2008) (33%). Beberapa penelitian melaporkan penggunaan parameter suhu yang digunakan dalam proses, misalnya dalam Yu et al. (1996), Matsumoto et al. (2008, 2011), dan Tsubaki et al. (2009), sedangkan sebagian besar lainnya hanya melaporkan penggunaan tingkat, derajat atau persentase power ataupun besaran daya (watt) yang digunakan (Kunlan et al. 2001; Pinkrova
et al. 2003; Palav dan Seetharaman 2007; Nicolic et al. 2008). Menurut Tsubaki
et al. (2009), gelatinisasi pati kentang dengan konsentrasi pati 25% (b/b) mulai terjadi pada suhu 120 °C. Selanjutnya, dinyatakan bahwa terjadi peningkatan proses terlarutnya pati di atas suhu tersebut, dan hampir semua jenis pati sudah dapat terlarut pada suhu 200-220 °C yang disertai dengan terbentuknya warna akibat dekomposisi sekunder dari bahan yang dipanaskan. Waktu terlama yang umum digunakan pada proses degradasi atau hidrolisis pati adalah 10 menit. Sebagian besar proses dapat diselesaikan dalam waktu kurang dari 10 menit. Proses degradasi atau hidrolisis pati menggunakan iradiasi gelombang mikro dapat dilakukan dalam medium air maupun larutan asam seperti asam sulfat atau asam klorida. Hidrolisis pati dapat dipercepat dengan penambahan garam-garam anorganik yang mengandung ion-ion Cl¯ atau SO42¯, dengan ion Cl¯ memberikan
2.2. Bahan dan Metode 2.2.1. Bahan
Ampas tapioka diperoleh dari industri rumah tangga tapioka di Kabupaten Bogor. Bahan dikeringkan pada suhu 60 °C selama 30 jam, kemudian dihaluskan dan diayak sampai semua bahan lolos ayakan berukuran 20 mesh. Tepung ampas tapioka kering dimasukkan ke dalam kantong-kantong plastik dengan kapasitas sekitar 500 g tepung. Tapioka dibeli dari salah satu toko swalayan di Jakarta. bahan ini disimpan di dalam kontainer plastik dan ditutup rapat. Bahan-bahan kimia yang digunakan adalah Bahan-bahan dengan spesisfikasi untuk analisis.
2.2.2. Analisis bahan baku
Analisis proksimat (kadar air, abu, lemak dan protein kasar) bahan baku ampas tapioka dan tapioka dilakukan sebagai berikut. Kadar air ditentukan menggunakan alat uji kadar air (moisture tester) MA 35 (Sartorius Mechatronics, Sartorius AG, Goettingen, Jerman) pada suhu 105 °C. Kadar abu ditentukan dengan cara memanaskan bahan pada 600 °C selama 3 jam. Kadar lemak ditentukan dengan cara ekstraksi Soxhlet dan kadar protein dengan metode Kjeldahl. Kadar serat kasar ditentukan dengan mengacu pada Standar Nasional Indonesia (SNI) 01-2891-1992 butir 11. Kadar pati dan amilosa bahan masing-masing ditentukan menggunakan Total Starch Kit (Megazyme Ltd., Ireland) yang mengacu pada standar AOAC Official Method 996.11 dan Amylose/Amylopectin Kit (Megazyme Ltd., Ireland). Prosedur analisis yang rinci disajikan pada Lampiran 1. Komposisi relatif karbohidrat dalam ampas tapioka ditentukan dengan melakukan analisis terhadap komposisi relatif gula netral yang terdapat dalam kedua bahan tersebut. Bahan (3% b/v) dihidrolisis menggunakan asam sulfat 72% pada suhu 120 °C selama 1 jam. Hasil hidrolisis dianalisis menggunakan High-Performance Anion Exchange Chromatography (HPAEC) pada sistem Dionex DX-500 (Sunnyvale, CA, AS) dengan detektor (ED-40) dan 1.0 mM NaOH sebagai fase bergerak.
Sifat morfologi ampas tapioka dan tapioka dianalisis menggunakan
Scanning Electron Microscope (SEM) tipe VE-8800 Low Voltage (Keyence, Co.,
menggunakan Difraktometer sinar X tipe Ultima IV (Rigaku Company, Tokyo, Jepang). Pengukuran dilakukan pada selang 2 4-32° pada 40 kV, 20 mA dan kecepatan 2° per menit.
2.2.3. Hidrolisis pati menggunakan iradiasi gelombang mikro
Oven gelombang mikro yang digunakan pada penelitian ini adalah oven gelombang mikro MycroSYNTH Lab Station (2.450 MHz) (Milestone Inc., Shelton, CT, AS). Oven gelombang mikro ini merupakan oven multi mode yang dilengkapi dengan termometer termokopel untuk memonitor suhu dan waktu pemanasan ril di dalam reaktor. Suhu dan waktu pemanasn dikontrol dengan cara melakukan input kondisi proses melalui PID algorithm pada unit PC (easyWAVE 3 software, Milestone, Inc., Shelton, CT, AS). Suspensi bahan dalam air (1g/20 mL) dimasukkan ke dalam tabung Teflon® berkapasitas 100 mL dan diaduk menggunakan pengaduk magnetik agar diperoleh suspensi yang homogen. Campuran kemudian dihidrolisis pada suhu 140-240°C dengan lama pemanasan pendahuluan (waktu yang digunakan untuk menaikkan suhu dari suhu ruang ke suhu yang diinginkan) 4 menit dan lama pemanasan pada suhu yang diinginkan 5 menit. Setelah iradiasi gelombang mikro, campuran dalam tabung segera didinginkan dengan merendamnya dalam bak berisi es. Selanjutnya, iradiasi gelombang mikro dilakukan pada suhu 230 °C untuk ampas tapioka dan 240 °C untuk tepung tapioka, masing-masing dengan lama pemanasan pendahuluan 2-6 menit dan lama pemanasan 5 menit.
2.2.4. Penentuan persentase dan analisis fraksi terlarut
Hidrolisat ampas tapioka disentrifugasi pada suhu 10 °C, 5.000 g selama 15 menit. Residu dipisahkan dari supernatan, dicuci tiga kali dengan air suling 30 mL dan disentrifugasi pada suhu 10 °C, 5.000 g selama 15 menit setelah setiap pencucian. Residu kemudian dikeringkan menggunakan pengering beku.
terhadap distribusi maltooligosakarida dari fraksi terlarut menggunakan High Performance Liquid Chromatography (HPLC) dengan kolom MCI CK04SS ukuran 7,5 x 200 mm, detektor refraktif indeks Shodex SE-51, pompa Jasco PU-980, pemanas kolom Jasco CO-965, dan degasser Jasco DG 980-50. Pelarut yang digunakan adalah air dengan kecepatan elusi 0,3 mL/menit. Perhitungan dilakukan menggunakan Jasco Chrom NAV data station. Kadar glukosa ditentukan menggunakan Glucose CII test kit (Wako Junyaku, Co., Osaka), dengan rincian prosedur seperti pada Lampiran 3. Rendemen glukosa dihitung berdasarkan berat bahan kering, yang dinyatakan sebagai % dari berat bahan kering dan berdasarkan pati dalam bahan (starch-based theoretical yield), yang dinyatakan sebagai % dari teoritis. Nilai pH hidrolisat diukur menggunakan pH meter, dan pembentukan warna coklat ditentukan dengan mengukur absorbansi pada panjang gelombang 490 nm sebagaimana dalam Warrand dan Janssen (2007) serta Whistler dan Daniel (1985) dan dengan menganalisis kadar hidroksi metil furfural (HMF) mengikuti metode SNI 01-3545-2004 yang mengacu pada AOAC (980.23-1999) (BSN 2004). Rincian prosedur analisis disajikan pada Lampiran 3.
2.2.5. Analisis residu ampas tapioka
Residu ampas tapioka dianalisis komposisi gula netralnya menggunakan HPAEC sebagaimana dijelaskan pada Bab 2.2.2. setelah dilakukan hidrolisis bahan (3% b/v) menggunakan asam sulfat 72% pada suhu 120 °C selama 1 jam. Residu ampas tapioka dianalisis pula morfologi permukaannya menggunakan Low Voltage Scanning Electron Microscope (LV SEM) (Keyence VE-8800).
2.3. Hasil dan Pembahasan 2.3.1. Komposisi ampas tapioka
tapioka (79,45%) yang digunakan pada penelitian ini jauh lebih tinggi dan kadar serat kasarnya (4,84%) jauh lebih rendah dari yang dilaporkan oleh Sriroth et al.
(2000), Srinorakutara et al. (2006), dan Kunhi et al. (1981), yaitu masing-masing 60-70%, dan 10-27%. Perbedaan ini mungkin disebabkan perbedaan sumber ampas tapioka. Ampas tapioka untuk penelitian ini berasal dari industri rumah tangga tapioka di Kabupaten Bogor, Jawa Barat, dimana ubikayu dikupas sebelum diparut untuk selanjutnya diproses menggunakan peralatan yang sangat sederhana, sedangkan yang digunakan oleh peneliti lain berasal dari industri besar. Pada industri besar ubikayu tidak dikupas terlebih dahulu melainkan langsung diparut atau dihancurkan untuk proses lebih lanjut menggunakan peralatan yang lebih baik yang memungkinkan proses ekstraksi pati yang lebih efisien. Dengan demikian, kadar pati yang tersisa dalam ampas tapioka dari industri rumah tangga di Bogor akan lebih besar, sedangkan kadar seratnya menjadi lebih kecil karena proses ekstraksi pati yang kurang efisien dan dikupasnya kulit ubikayu sebelum pengolahan. Hasil analisis kadar pati dan serat kasar terhadap contoh ampas tapioka yang berasal dari industri rumah tangga di Bogor dan industri kecil serta industri besar tapioka di Propinsi Lampung (Tabel 2.1) menguatkan alasan ini. Selain itu, hasil survei Siregar (2006) pada beberapa industri tapioka di Propinsi Lampung juga menunjukkan adanya perbedaan rendemen tapioka yang diperoleh dari industri kecil (22%) dan industri besar tapioka (25%).
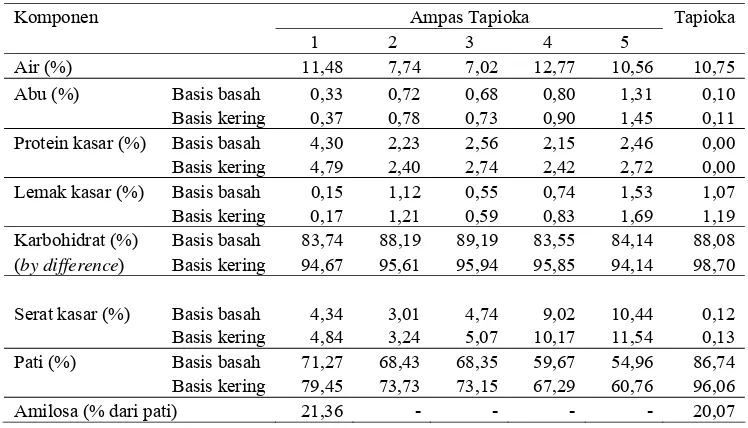
Tabel 2.1 Komposisi kimia ampas tapioka dan tapioka
Komponen Ampas Tapioka Tapioka
1 2 3 4 5 Karbohidrat (%) Basis basah 83,74 88,19 89,19 83,55 84,14 88,08
(by difference) Basis kering 94,67 95,61 95,94 95,85 94,14 98,70
1 = bahan penelitian, asal industri rumah tangga, Bogor (lolos 20 mesh) 2 dan 3 = asal industri rumah tangga, Bogor
4 = asal industri kecil, Lampung 5 = asal industri besar, Lampung
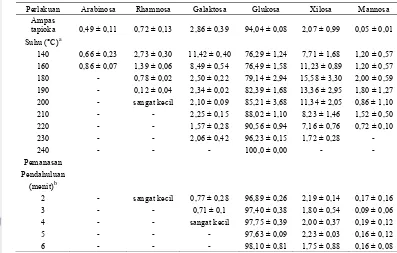
Tabel 2.2 Komposisi relatif gula netral dalam ampas tapioka Komponen Persentase relatif (%) Arabinosa 0,49 ± 0,11
2.3.2. Sifat morfologis dan fisis ampas tapioka
membungkus granula pati dalam ampas tapioka, sehingga diharapkan dapat memberi akses yang lebih besar terhadap granula pati yang akan dihidrolisis.
Gambar 2.1 Citra SEM ampas tapioka (a) dan tapioka (b).
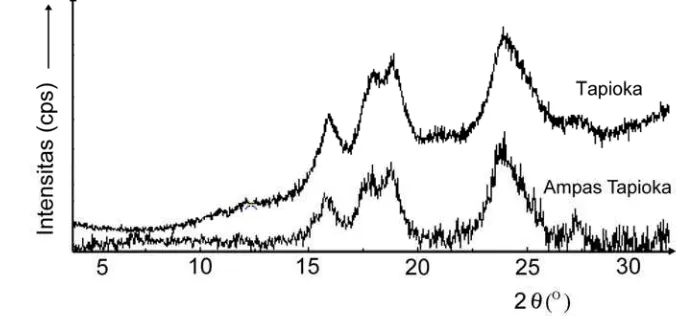
Difraktogram sinar X pada ampas tapioka dan tapioka (Gambar 2.2) menunjukkan bahwa kedua bahan mempunyai puncak yang kuat/tinggi pada nilai 2 sebesar 16°, 17°, 18°, dan 23°. Tipe spektrum ini mendekati spektrum pati tipe A seperti halnya pati jagung. Spektrum ini juga hampir sama dengan spektrum pati tapioka yang mempunyai puncak yang kuat pada 15°, 17°, 18° dan 23° seperti yang dilaporkan oleh Atichokudomchai et al. (2001). Beberapa hasil studi menunjukkan bahwa pati tapioka mempunyai dua tipe spektrum sinar X, yaitu A dan C (Sair 1967) atau spektrum tipe C (Zobel 1988), namun pola C berubah ke A setelah perlakuan panas dalam keadaan lembab (Sair 1967; Zobel 1988). Semula diduga proses pengeringan yang dilakukan dalam proses produksi tapioka menyebabkan berubahnya tipe spektrum tapioka maupun ampas tapioka dari C ke A. Namun, hasil analisis spektrum kedua bahan yang dikeringkan dengan menggunakan pengering beku masih tetap menunjukkan pola spektrum yang sama, yaitu mendekati pola spektrum pati tipe A.
Ampas tapioka mengandung pati dan serat, dimana masing-masing mempunyai sifat kristalinitas. Hasil analisis difraksi sinar X menunjukkan bahwa kristalinitas ampas tapioka yang digunakan pada penelitian ini (lolos ayakan 20 mesh) adalah 15,57%. Nilai kristalinitas ini jauh lebih rendah dari nilai kristalinitas ampas tapioka yang tidak mengalami penggilingan, yaitu 42,61% (Tabel 2.3). Hal ini menandakan bahwa penggilingan yang dilakukan terhadap
ampas tapioka menurunkan kristalinitasnya, terutama kristalinitas serat yang ada di dalam ampas tapioka. Penggilingan terhadap pati yang diekstrak dari ubikayu menjadi tapioka yang berbentuk tepung halus ternyata tidak terlalu banyak menurunkan kristalinitasnya (Tabel 2.3). Dari hasil analisis di atas diduga komponen serat lebih berperanan dalam menentukan kristalinitas ampas tapioka sebelum mengalami penggilingan, sedangkan setelah mengalami penggilingan komponen pati diduga lebih berpenanan terhadap kristalinitas ampas tapioka. Pada hidrolisis dengan menggunakan pemanasan gelombang mikro kristalinitas ampas tapioka diduga akan mengalami penurunan karena terhidrolisisnya komponen pati dalam ampas tapioka.
Gambar 2.2 Difraktogram sinar X ampas tapioka dan tapioka.
Tabel 2.3 Kristalinitas ampas tapioka dan tapioka
Bahan Kondisi Kristalinitas (%) Ampas tapioka Sebelum digiling 42,61
Sesudah digiling 15,57 Tapioka Sebelum digiling 20,93
Sesudah digiling 17,89
2.3.3. Pengaruh iradiasi gelombang mikro terhadap karbohidrat dalam ampas tapioka
2.3.3.1. Kelarutan
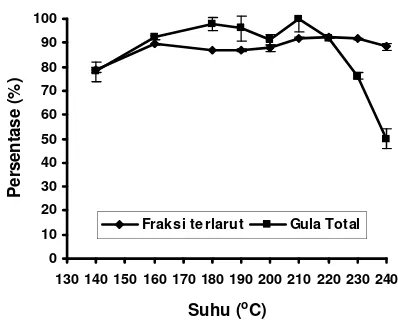
ampas tapioka tidak larut dalam air. Setelah perlakua menggunakan pemanasan gelombang mikro beberapa komponen sedikit demi sedikit mulai terlarut. Kelarutan ampas tapioka meningkat seiring dengan meningkatnya suhu pemanasan gelombang mikro dan mencapai maksimum (± 92%) pada suhu 210-220 °C, kemudian sedikit menurun pada suhu di atas 210-220 °C (Gambar 2.3). Pati dalam ampas tapioka lebih sulit larut dibandingkan dengan pati tapioka yang seluruhnya sudah larut mulai suhu 140 °C, suhu terendah yang digunakan pada penelitian ini. Meningkatnya kelarutan senyawa karbohidrat dalam ampas tapioka karena meningkatnya suhu pemanasan ditandai juga dengan meningkatnya kadar gula total dalam fraksi terlarut hidrolisat ampas tapioka. Kadar gula total mencapai sekitar 78% dan meningkat secara bertahap sampai suhu 210 °C (Gambar 2.3). Terjadi sedikit penurunan kadar gula total pada suhu 200 °C, namun dilihat dari nilai simpangan baku data pada suhu 190, 200 dan 210 °C, maka kadar gula total pada suhu 200 °C tidak berbeda dengan pada suhu 190 dan 200 °C. Di atas 210 °C kadar gula total menurun karena terjadinya degradasi sekunder pada karbohidrat yang telah mengalami depolimerisasi menjadi molekul-molekul dengan berat molekul lebih rendah, seperti furfural, hidroksi metil furfural, asam asetat, dan lain-lain. Hal ini juga terlihat dari menurunnya nilai pH dan meningkatnya nilai absorbansi pada 490 nm serta kadar HMF secara drastis pada hidrolisat setelah mendapat perlakuan pemanasan pada suhu di atas 210 °C. (Gambar 2.6 dan 2.9).
0
130 140 150 160 170 180 190 200 210 220 230 240
Suhu (oC)
Gambar 2.3 Pengaruh suhu pemanasan gelombang mikro terhadap kelarutan dan gula total hidrolisat ampas tapioka (pemanasan pendahuluan 4 menit, pemanasan pada suhu yang diinginkan 5 menit). Nilai pada titik-titik data merupakan nilai rata-rata ± SB / Simpangan Baku (n=3).
0
Gambar 2.4 Pengaruh lama pemanasan pendahuluan terhadap kelarutan dan kadar gula total hidrolisat ampas tapioka (suhu 230 °C, 5 menit). Nilai pada titik-titik data merupakan nilai rata-rata ± SB (n=3).
2.3.3.2. Produk hidrolisis
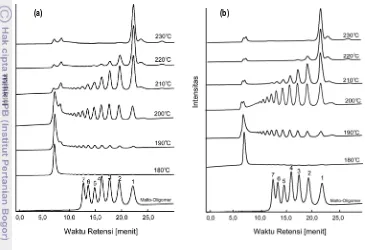
dilakukan pada suhu 210 °C. Terbentuknya maltooligomer dan glukosa dalam jumlah yang besar dalam hidrolisat ampas tapioka dan tapioka semakin terlihat dengan jelas setelah hidrolisis pada suhu 220 dan 230 °C, yang menandakan semakin banyaknya pati yang terhidrolisis menjadi maltooligosakarida dan glukosa. Pada suhu 240 °C hampir semua senyawa dengan berat molekul besar dalam hidrolisat tapioka terkonversi menjadi glukosa, sedangkan dalam hidrolisat ampas tapioka masih ada senyawa dengan berat molekul besar yang tidak terhidrolisis, yang diduga merupakan komponen selulosa.
Gambar 2.5 Kromatogram HPLC hasil degradasi pati dalam ampas tapioka (a) dan tapioka (b) setelah pemanasan gelombang mikro selama 5 menit pada berbagai suhu. Puncak nomor 1, 2, 3, 4, 5, 6, 7 menunjukkan glukosa dan maltooligomer dengan derajat polimerisasi (DP) 2-7.
ikatan α-(1,4) pada maltosa, α-(1,6) pada isomaltosa, dan β-(1,4) pada selobiosa, masing-masing 1,55 x 105, 0,40 x 105, dan 0,66 x 105. Hal ini juga mencerminkan bahwa ikatan α-(1,4) glikosidik jauh lebih mudah untuk dihidrolisis oleh asam, dibandingkan dengan ikatan α-(1,6) atau ikatan β-(1,4) glikosisdik. Oleh karena itu, diperlukan energi yang lebih besar atau suhu yang lebih tinggi untuk mendegradasi komponen selulosa dalam ampas tapioka dibandingkan dengan yang diperlukan untuk mendegradasi komponen pati.
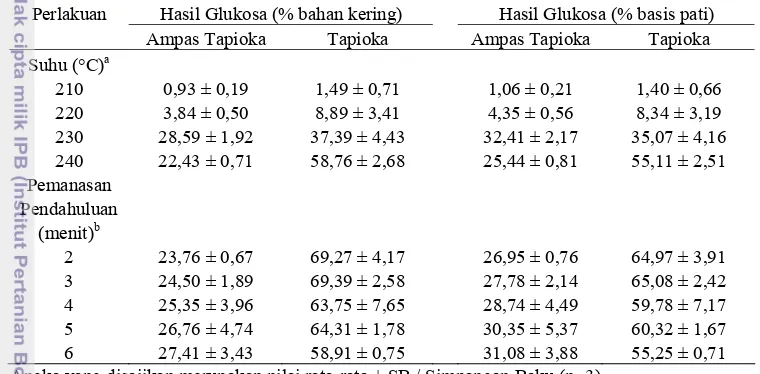
enzimatis ( 75%) (Kosugi et al. 2009). Hanya saja, proses-proses tersebut memakan waktu lebih lama, 90 menit untuk hidrolisis asam dan 48-72 jam untuk hidrolisis enzimatis, sedangkan proses menggunakan gelombang mikro memakan waktu hanya beberapa menit saja.
Tabel 2.4 Hasil glukosa yang diperoleh dari hidrolisis ampas tapioka dan tapioka menggunakan pemanasan gelombang mikro
Perlakuan Hasil Glukosa (% bahan kering) Hasil Glukosa (% basis pati) Ampas Tapioka Tapioka Ampas Tapioka Tapioka Angka yang disajikan merupakan nilai rata-rata ± SB / Simpangan Baku (n=3)
a
Pemanasan pendahuluan 4 menit dan pemanasan pada suhu yang diinginkan 5 menit
b
Suhu 230 °C untuk ampas tapioka dan 240 °C untuk tapioka dan pemanasan 5 menit
2.3.3.3. Nilai pH
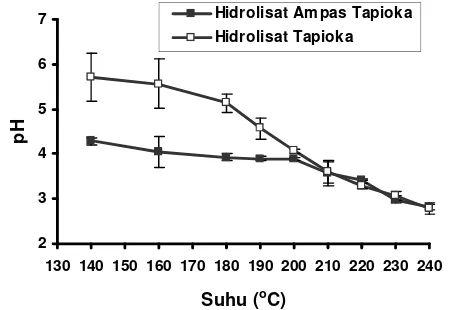
Nilai pH awal suspensi ampas tapioka dan tapioka masing-masing adalah 4,29 dan 5,10. Perbedaan nilai pH kedua suspensi diduga disebabkan perbedaan proses yang dialami oleh keduanya. Pada proses produksi tapioka pencucian terhadap pati tapioka berlangsung lebih baik, karena air dalam suspensi pati jumlahnya sangat banyak (sekitar 1:10), sedangkan ampas tapioka tidak mengalami pencucian yang baik, sehingga kemungkinan masih mengandung senyawa-senyawa yang bersifat asam atau yang mudah terdegradasi oleh mikrob dan menghasilkan asam yang mengakibatkan nilai pH yang lebih rendah.
hidrolisat kemungkinan karena terbentuknya beberapa senyawa asam organik sebagai hasil degradasi karbohidrat dalam ampas tapioka maupun dalam tapioka. Penurunan pH hidrolisat juga terjadi pada hidrolisat tepung terigu setelah perlakuan dengan iradiasi gelombang mikro (Khan et al. 1979). Pada proses hidrolisis pati dari tepung gandum dalam medium air pada wadah tertutup menggunakan suhu dan tekanan tinggi Lorenz dan Johnson (1972) mengamati terjadinya penurunan pH dan mengidentifikasi terbentuknya beberapa senyawa asam dengan jumlah rantai karbon 1 sampai dengan 6, seperti asam formiat, asetat, butirat, isobutirat, valerat, isovalerat, kaproat dan isokaproat. Mereka menduga asam-asam ini terbentuk akibat proses oksidasi senyawa aldehida, sedangkan Harmsen et al. (2010) menyatakan bahwa asam asetat berasal dari gugus asetil pada hemiselulosa.
Perbedaan waktu pemanasan pendahuluan pada suhu tinggi tidak mengakibatkan perbedaan pada nilai pH hidrolisat (Gambar 2.7), akan tetapi pH hidrolisat ampas tapioka relatif lebih tinggi daripada pH hidrolisat tepung tapioka yang mengindikasikan lebih sulitnya proses degradasi pati dalam ampas tapioka.
2 3 4 5 6 7
130 140 150 160 170 180 190 200 210 220 230 240
Suhu (oC)
pH
Hidrolisat Am pas Tapioka Hidrolisat Tapioka
Gambar 2.6 Pengaruh suhu pemanasan gelombang mikro terhadap pH hidrolisat ampas tapioka dan tapioka (pemanasan pendahuluan 4 menit,
2,5 3,0 3,5
1 2 3 4 5 6
Pemanasan pendahuluan (menit)
pH
Hidrolisat Am pas Tapioka Hidrolisat Tapioka
Gambar 2.7 Pengaruh lama pemanasan pendahuluan terhadap pH hidrolisat ampas tapioka dan tapioka (suhu 230 °C, 5 menit). Nilai pada titik-titik data merupakan nilai rata-rata ± SB / Simpangan Baku (n=3).
2.3.3.4. Senyawa berwarna coklat
Hidrolisis menggunakan pemanasan gelombang mikro yang dilakukan pada suhu yang cukup tinggi sangat memungkinkan untuk terjadinya reaksi pencoklatan non enzimatis. Hal ini terbukti dari terbentuknya hidrolisat yang berwarna gelap pada perlakuan suhu yang tinggi, yaitu mulai suhu 180 °C pada hidrolisat ampas tapioka dan mulai suhu 210 °C dan pada hidrolisat tapioka (Gambar 2.8). Pembentukan senyawa berwarna coklat dan HMF meningkat seiring dengan meningkatnya suhu pemanasan yang salah satunya ditandai dengan meningkatnya nilai absorbansi pada panjang gelombang 490 nm dan kadar HMF (Gambar 2.9). Panjang gelombang 490 nm merupakan panjang gelombang untuk warna jingga yang merupakan salah satu panjang gelombang yang biasa digunakan untuk reaksi Maillard (Whistler dan Daniel 1985). Peningkatan nilai absorbansi pada 490 nm pada hidrolisat pati akibat peningkatan suhu pemanasan gelombang mikro juga dilaporkan oleh Warrand dan Janssen (2007). Kadar HMF dalam hidrolisat ampas tapioka dan tapioka mencapai sekitar 220 mg/100 g setelah hidrolisis pada suhu 240 °C, dapat mempengaruhi pertumbuhan mikrob pada proses fermentasi.
senyawa berwarna coklat dan HMF selain berasal dari hasil degradasi glukosa menjadi HMF, juga dapat berasal dari reaksi pencoklatan (Maillard) antara gugus amino yang berasal dari protein dalam ampas tapioka (Tabel 2.1) dan glukosa yang terbentuk. Selain itu, senyawa hemiselulosa, terutama yang mempunyai gula dengan 5 atom karbon seperti arabinosa dan xilosa, di dalam ampas tapioka setelah terdepolimerisasi menjadi monosakarida juga dapat terdegradasi lebih lanjut menjadi senyawa furfural yang berwarna coklat, sehingga ikut berkontribusi terhadap dihasilkannya warna hidrolisat ampas tapioka yang lebih gelap.
Gambar 2.8 Hidrolisat ampas tapioka (atas) dan tapioka (bawah) setelah
pemanasan gelombang mikro pada suhu 140-240 °C selama 5 menit.
HMF dan furfural sendiri merupakan produk antara pada reaksi Maillard dan mempunyai nilai absorbansi yang tinggi pada panjang gelombang ultra violet (UV). Nilai absorbansi yang sangat tinggi pada panjang gelombang 490 nm menandakan bahwa reaksi Maillard sudah sampai pada tahap akhir yaitu terbentuknya senyawa melanoidin. Terbentuknya senyawa dengan berat molekul rendah seperti furfural dan HMF dapat menghambat proses lanjutan terhadap hidrolisat, misalnya proses fermentasi. Oleh karena itu, hidrolisat ini kemungkinan memerlukan perlakuan untuk menghilangkan atau mengurangi inhibitor yang ada, misalnya dengan cara menambahkan bentonit atau kaolin (Ahmed et al.1983).
140 160 180 190 200 210 220 230 240