F
A
FAKULTA
AKTIVIT
AS MATE
IN
AS ANTI
TER
BAGUS
DEPAR
EMATIKA
STITUT P
IOKSIDA
RPILAR-F
S KUSBAN
RTEMEN
A DAN ILM
PERTANI
BOGOR
2013
AN ZEOL
Fe
2O
3NDONO
KIMIA
MU PENG
IAN BOGO
LIT ALAM
GETAHUA
OR
M
PERNYATAAN MENGENAI SKRIPSI DAN
SUMBER INFORMASI SERTA PELIMPAHAN HAK CIPTA
Dengan ini saya menyatakan bahwa skripsi berjudul Aktivitas Antioksidan Zeolit Alam Terpilar-Fe2O3 adalah benar karya saya dengan arahan dari komisi pembimbing dan belum diajukan dalam bentuk apa pun kepada perguruan tinggi mana pun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir skripsi ini.
Dengan ini saya melimpahkan hak cipta dari karya tulis saya kepada Institut Pertanian Bogor.
Bogor, Mei 2013
Bagus Kusbandono
ABSTRAK
BAGUS KUSBANDONO. Aktivitas Antioksidan Zeolit Alam Terpilar-Fe2O3. Dibimbing oleh SRI SUGIARTI dan ETI ROHAETI.
Pilarisasi zeolit dengan besi oksida telah dilakukan untuk meningkatkan kemampuan adsorpsi dan karakteristiknya. Zeolit alam pada umumnya memiliki kristalinitas dan aktivitas katalitik yang rendah, ukuran porinya tidak seragam, serta mengandung banyak pengotor, sehingga aktivasi dan modifikasi sangat diperlukan. Penelitian ini bertujuan mempelajari pengaruh aktivasi zeolit alam asal Sukabumi dengan pemanasan dan pemberian asam serta pengaruh modifikasi zeolit hasil aktivasi dengan teknik pilarisasi menggunakan Fe2O3. Sifat Fe2O3 sebagai bahan semikonduktor diharapkan dapat meningkatkan aktivitas antioksidan zeolit alam melalui metode 1,1-difenil-2-pikrilhidrazil. Hasil pencirian menunjukkan bahwa zeolit alam Sukabumi ialah jenis klinoptilolit dan aktivitas antioksidan setelah pilarisasi Fe2O3 meningkat sebesar 17.73% dan 27.29% masing-masing pada zeolit setelah aktivasi dengan kalsinasi pada suhu 400 °C dan dengan HCl 2.0 M.
.
Kata kunci: antioksidan, Fe2O3, pilarisasi, zeolit
ABSTRACT
BAGUS KUSBANDONO. Antioxidant Activities of Fe2O3-Pillared Natural Zeolite. Supervised by SRI SUGIARTI and ETI ROHAETI.
AKTIVITAS ANTIOKSIDAN ZEOLIT ALAM
TERPILAR-Fe
2O
3
BAGUS KUSBANDONO
Skripsi
sebagai salah satu syarat untuk memperoleh gelar Sarjana Sains
pada
Departemen Kimia
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
Judul Skripsi : Aktivitas Antioksidan Zeolit Alam Terpilar-Fe2O3
Nama : Bagus Kusbandono
NIM : G44104030
Disetujui oleh
Sri Sugiarti, PhD Pembimbing I
Dr Eti Rohaeti, MS Pembimbing II
Diketahui oleh
Prof Dr Ir Tun Tedja Irawadi, MS Ketua Departemen
PRAKATA
Puji syukur penulis panjatkan kepada Allah subhanahu wa ta’ala karena atas segala karunia-Nya penulis dapat menyelesaikan karya ilmiah dengan judul “Aktivitas Antioksidan Zeolit Alam Terpilar-Fe2O3”. Shalawat dan salam senantiasa tercurahkan kepada manusia terbaik Nabi Muhammad Shallallahu ‘alaihi wa sallam, keluarganya, sahabatnya, dan pengikutnya hingga akhir zaman. Terima kasih penulis ucapkan kepada Ibu Sri Sugiarti, PhD dan Dr Eti Rohaeti, MS selaku pembimbing yang senantiasa memberikan arahan, semangat, dan doa selama penelitian dan penyusunan karya ilmiah ini. Ucapan terima kasih juga penulis sampaikan kepada kedua orang tua dan kakak yang selalu memberikan doa, motivasi, dan semangat selama masa studi hingga penyusunan karya ilmiah ini.
Ungkapan terima kasih juga penulis sampaikan kepada seluruh staf laboratorium Anorganik atas fasilitas yang diberikan selama penulis melakukan penelitian. Penulis juga mengucapkan terima kasih kepada sahabatku Indra Jati, Zelfi, Budi, Salman, dan teman-teman peneliti lainnya, serta pihak-pihak lain yang telah membantu penulis dalam menyelesaikan penyusunan karya ilmiah ini yang tidak dapat disebutkan satu per satu tanpa maksud mengurangi rasa terima kasih.
Semoga karya ilmiah ini bermanfaat bagi penulis maupun bagi pembaca.
Bogor, Mei 2013
DAFTAR ISI
DAFTAR TABEL vii
DAFTAR GAMBAR vii
DAFTAR LAMPIRAN vii
PENDAHULUAN 1
BAHAN DAN METODE 2
Alat dan Bahan 2
Prosedur Penelitian 2
Metode 2
HASIL DAN PEMBAHASAN 4
Ciri-ciri Zeolit Alam 4
Ciri-ciri Zeolit Alam Teraktivasi dan Terpilar-Fe2O3 6
Aktivitas Antioksidan Zeolit Alam 9
Aktivitas Antioksidan Zeolit Terpilar-Fe2O3 10
SIMPULAN DAN SARAN 11
Simpulan 11 Saran 12
DAFTAR PUSTAKA 12
LAMPIRAN 15
DAFTAR TABEL
1 Komposisi kimia zeolit alam Sukabumi 6
2 Kristalinitas zeolit alam setelah proses aktivasi 6 3 Komposisi kimia zeolit alam Sukabumi sebelum dan setelah pilarisasi
Fe2O3 dengan aktivasi kalsinasi 400 oC dan HCl 2.0 M 8 4 Aktivitas antioksidan zeolit alam sebelum dan setelah terpilar Fe2O3 11
DAFTAR GAMBAR
1 Difaktogram XRD zeolit alam Sukabumi 4
2 Morfologi permukaan zeolit alam Sukabumi (perbesaran 1000 kali) 5 3 Morfologi permukaan zeolit alam hasil aktivasi suhu 400 oC (a) dan
aktivasi HCl 2.0 M (b) setelah terpilar Fe2O3 (perbesaran 1000 kali) 7 4 Warna larutan DPPH setelah berinteraksi dengan zeolit alam hasil
aktivasi dengan kalsinasi (a) dan dengan HCl (b) sebelum terpilar
Fe2O3 9
5 Warna larutan DPPH setelah berinteraksi dengan zeolit alam hasil aktivasi dengan kalsinasi (a) dan dengan HCl (b) setelah terpilar Fe2O3 10
DAFTAR LAMPIRAN
1 Bagan alir penelitian 15
2 Pencirian XRD zeolit alam Sukabumi 16
3 Profil pola difraksi zeolit alam dibandingkan dengan literatur ICDD 16
4 Hilang pijar zeolit alam Sukabumi 17
5 Komposisi kimia zeolit alam Sukabumi dengan EDX 18 6 Pencirian XRD zeolit alam setelah aktivasi dengan kalsinasi dan
dengan asam 19
7 Komposisi kimia zeolit alam Sukabumi hasil aktivasi dengan kalsinasi 400 oC dan dengan HCl 2.0 M sebelum dan setelah pilarisasi Fe2O3 21
8 Kurva standar dan IC50 vitamin C 22
9 Aktivitas antioksidan zeolit alam Sukabumi hasil aktivasi dengan kalsinasi 400 oC dan dengan HCl 2.0 M sebelum dan setelah pilarisasi
Fe2O3 23
1
PENDAHULUAN
Penggunaan senyawa antioksidan semakin berkembang dan bahan baru yang potensial sebagai antioksidan terus dieksplorasi baik di bidang kosmetik, makanan, maupun pengobatan seiring dengan bertambahnya pengetahuan tentang aktivitas radikal bebas (Rohman et al. 2009). Senyawa antioksidan berperan penting dalam pertahanan tubuh terhadap pengaruh buruk radikal bebas. Radikal bebas dapat menginduksi kanker, aterosklerosis, dan penuaan, yang disebabkan oleh kerusakan jaringan karena oksidasi (Utami et al. 2006).
Salah satu material yang sudah diteliti berpotensi sebagai antioksidan adalah zeolit alam. Menurut Hecht (2010), produk mineral seperti zeolit alam sebagai bahan penopang diterapkan dalam bidang kesehatan dan kosmetik serta dimanfaatkan sebagai antioksidan. Zeolit alam jenis klinoptilolit telah dteliti pemanfaatannya dalam bidang kedokteran sebagai antikanker (Kresimir dan Miroslav 2001). Pengobatan menggunakan zeolit jenis klinoptilolit pada tikus dan anjing yang menderita tumor menunjukkan bahwa pemberian zeolit dapat meningkatkan kesehatannya secara keseluruhan dan menurunkan ukuran tumor, serta mampu mengurangi pembentukan dan pertumbuhan kembali tumor tanpa menimbulkan efek negatif. Zeolit alam juga banyak dimanfaatkan pada bidang peternakan sebagai bahan tambahan pakan ternak. Hasil penelitian Ipek et al. (2012) menunjukkan bahwa zeolit alam klinoptilolit sebagai suplemen pakan ternak sapi perah mampu menurunkan secara signifikan konsentrasi lipid hidroperoksida (LOOH), tetapi tidak berpengaruh pada antioksidan dan indikator oksidan lainnya. Menurut Pavelic et al. (2002), zeolit alam klinoptilolit sebagai suplemen dalam hati tikus mampu menurunkan konsentrasi LOOH.
Penelitian zeolit alam sebagai bahan penopang telah banyak dilaporkan. Modifikasi zeolit alam sebagai bahan penopang ekstrak tanaman kedawung, salam, sirih merah, jambu biji, dan bangle dapat meningkatkan aktivitas antioksidan (Hayati 2011). Menurut Pranoto (2012), zeolit alam memiliki potensi sebagai antioksidan, hanya saja aktivitasnya masih terlalu kecil. Aktivitas antioksidan zeolit alam semakin menurun dengan meningkatnya suhu dan konsentrasi asam sehingga diduga keberadaan oksida logam pengotor pada kerangka zeolitlah yang berperan sebagai antioksidan.
Salah satu metode untuk meningkatkan kemampuan zeolit alam adalah pilarisasi. Pilarisasi dilakukan dengan menginterkalasikan Fe2O3 ke dalam zeolit tanpa merusak struktur kerangka zeolit sehingga terbentuk suatu bahan berstruktur pori dengan sifat-sifat fisikokimia yang lebih baik, meliputi luas permukaan spesifik, porositas dan keasaman permukaan, serta stabilitas termalnya (Wijaya et al. 2002). Sintesis Fe2O3-monmorilonit dan aplikasinya sebagai fotokatalis untuk degradasi zat warna congo red meningkatkan luas permukaan dari 69.71 menjadi 126.49 m2/g (Wijaya et al. 2005). Modifikasi ampo terpilar-Fe2O3 melalui metode pilarisasi dapat meningkatkan kemampuan adsorpsi dan karakteristiknya dengan luas permukaan 99.56 m2/g serta kapasitas adsorpsi 117.10 m2/g terhadap lembayung metil (Yuliani et al. 2010).
2
diharapkan mampu meningkatkan aktivitas antioksidan zeolit alam. Aktivitas antioksidan diukur dengan metode 1,1-difenil-2-pikrilhidrazil (DPPH). Senyawa yang memiliki aktivitas antioksidan akan mengubah warna larutan menjadi kuning (Molyneux 2004).
Penelitian ini bertujuan menentukan pengaruh aktivasi zeolit alam Sukabumi dengan variasi suhu dan konsentrasi asam, serta modifikasi melalui pilarisasi Fe2O3 sebagai bahan semikonduktor pada aktivitas antioksidan zeolit
alam menggunakan metode DPPH. Perubahan sifat fisikokimia yang diteliti meliputi derajat kristalinitas dengan difraktometer sinar-X (XRD) serta morfologi permukaan dan kandungan logam besi dengan mikroskop elektron pemayaran-sinar-X dispersif energi (SEM-EDX).
BAHAN DAN METODE
Alat dan BahanAlat-alat yang digunakan ialah neraca analitik, peralatan kaca, shaker, cawan porselen, penangas air, corong Büchner, tanur, oven, desikator, pengaduk magnet, sentrifuga, vorteks, spektrofotometer ultraviolet-tampak (UV-Vis), XRD 6000 Shimadzu, dan SEM-EDX Zeiss 60.
Bahan-bahan yang digunakan ialah zeolit alam (Cikembar, Sukabumi), Fe2O3 p.a (Merck), HCl p.a (Merck), NaOH p.a (Merck), vitamin C p.a (Merck),
AgNO3 p.a (Merck), pH universal, DPPH (Sigma Aldrich), etanol teknis, akuades,
dan kertas saring.
Prosedur Penelitian
Prosedur penelitian dilakukan mengikuti diagram alir pada Lampiran 1 yang meliputi preparasi zeolit alam, aktivasi zeolit dengan kalsinasi, aktivasi zeolit dengan penambahan asam, modifikasi zeolit dengan pilarisasi Fe2O3, uji aktivitas
antioksidan metode DPPH, serta pencirian zeolit terpilar-Fe2O3 menggunakan
XRD dan SEM-EDX.
Metode Preparasi Zeolit Alam (Fatimah 2009)
Zeolit alam Cikembar, Sukabumi diseleksi dan dibersihkan dari pengotor, kemudian dihaluskan dan diayak hingga diperoleh ukuran butir lolos ayakan 100 mesh. Selanjutnya zeolit alam dicuci dengan akuades dan dipanaskan dalam oven pada suhu 105 °C selama 3 jam. Zeolit alam siap dicirikan menggunakan XRD dan SEM-EDX serta mengalami perlakuan lainnya.
Penentuan Hilang Pijar (Heiri et al. 2001)
3
dalam cawan tersebut dan dipanaskan pada suhu 550 °C selama 30 menit, kemudian dikeluarkan dan dipanaskan kembali pada suhu 1050 °C selama 60 menit dan ditimbang. Setelah itu, cawan berisi sampel dimasukkan dalam desikator selama 30 menit dan ditimbang. Perlakuan ini diulangi sampai diperoleh bobot yang konstan. Penentuan hilang pijar dihitung dengan persamaan
% Hilang pijar= (Cawan+zeolit) sebelum pemijaran – (Cawan + zeolit) setelah pemijaran
Bobot zeolit × 100%
Aktivasi Zeolit dengan Kalsinasi (modifikasi Syafii 2011)
Sebanyak 30 g zeolit alam 100 mesh dimasukkan ke dalam 300 mL larutan HCl 1 N, direndam selama 24 jam, kemudian disaring dan dicuci dengan akuades sampai pH netral atau ketika filtrat ditambahkan AgNO3 sudah tidak terbentuk endapan putih. Zeolit alam lalu dikalsinasi dalam tanur dengan variasi suhu 100, 200, 300, dan 400 °C selama 2 jam. Zeolit hasil aktivasi dengan kalsinasi ini dicirikan dengan menggunakan XRD dan SEM-EDX.
Aktivasi Zeolit dengan Penambahan Asam (modifikasi Syafii 2011)
Sebanyak 100 g zeolit alam 100 mesh ditambahkan ke dalam 250 mL HCl dengan variasi konsentrasi 0.5, 1.0, 1.5, dan 2.0 M. Campuran diaduk dengan pengaduk magnet selama 60 menit lalu disaring dengan saringan Büchner, dan dicuci dengan akuades sampai pH netral atau ketika filtrat ditambahkan AgNO3 sudah tidak terbentuk endapan putih. Selanjutnya zeolit alam dikalsinasi dalam tanur pada suhu 300 °C selama 3 jam. Zeolit hasil aktivasi dengan penambahan asam ini dicirikan dengan menggunakan XRD dan SEM-EDX.
Pilarisasi Zeolit-Fe2O3 (modifikasi Wijaya et al. 2005)
Sebanyak 8.5 g zeolit alam, zeolit hasil kalsinasi, dan hasil pengasaman masing-masing ditambahkan larutan NaOH 2 M sebanyak 12.5 mL dan ditambahkan Fe2O3 sebanyak 1.5 g atau 15% dari jumlah bobot keseluruhan. Campuran dimasukkan dalam botol plastik tahan panas, lalu dipanaskan dalam oven pada suhu 90 oC selama 8 jam, dilanjutkan pada oven pada suhu 120 oC selama 24 jam, kemudian sampel dicuci dengan akuades sampai pH netral. Zeolit yang telah terinterkalasi kompleks besi dikeringkan dalam oven pada suhu 110– 120 oC, kemudian digerus sampai halus dan diayak menggunakan ayakan ukuran 250 mesh. Selanjutnya zeolit terinterkalasi ini dikalsinasi pada suhu 400 oC selama 3 jam dan dicirikan komposisi kimianya dengan menggunakan SEM-EDX. Uji Aktivitas Antioksidan Metode DPPH (modifikasi Aranda et al. 2009)
Larutan DPPH 125 µM dalam etanol disiapkan. Sebanyak 0.5000 g zeolit alam, zeolit hasil aktivasi, dan zeolit hasil pilarisasi Fe2O3 masing-masing dimasukkan ke dalam tabung reaksi dan ditambahkan 5 mL larutan DPPH, lalu campuran divorteks selama 2–3 menit sebelum disentrifugasi pada kecepatan 2000 rpm selama 15 menit. Larutan hasil pencampuran diinkubasi selama 30 menit pada suhu 37 °C, kemudian diukur serapannya pada panjang gelombang 517 nm. Kapasitas penghambatan radikal bebas dihitung berdasarkan persamaan
% Aktivitas penangkapan radikal = A–B
Nilai A ialah absorbans kontrol negatif (DPPH ditambahkan etanol) dan B
ialah absorbans sampel (DPPH, sampel, dan etanol). Vitamin C digunakan sebagai kontrol positif. Standar vitamin C dibuat pada konsentrasi 2, 4, 6, 8, dan 10 ppm. Korelasi antara konsentrasi dan persentase penangkapan dialurkan sebagai kurva regresi linear.
HASIL DAN PEMBAHASAN
Ciri-ciri Zeolit Alam
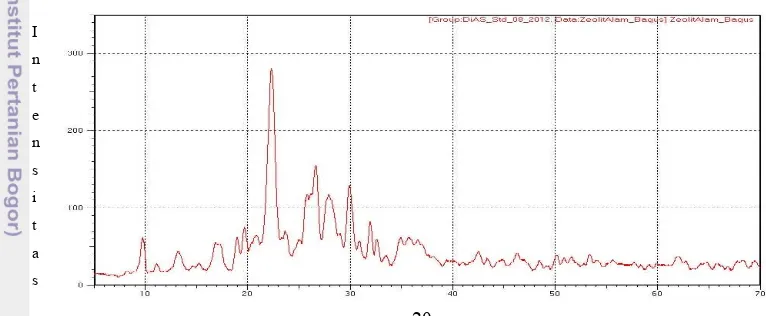
Penampakan secara visual hanya menunjukkan zeolit alam Cikembar berwarna hijau. Pencirian dengan menggunakan XRD dan SEM-EDX dilakukan untuk menentukan jenis zeolit dan komposisi kimianya. Difraktogram sinar-X zeolit alam Sukabumi (Gambar 1) memiliki intensitas yang tinggi pada daerah 2θ 9.83o, 22.33o, 26.66o, dan 29.94o serta memiliki kristalinitas 53.03% (Lampiran 2).
Gambar 1 Difaktogram XRD zeolit alam Sukabumi
Profil pola difraksi ini dibandingkan dengan data standar literatur International Center for Diffraction Data (JCPDS-ICDD). Zeolit diidentifikasi mengandung campuran jenis klinoptilolit dan mordenit, karena memiliki puncak difraksi sinar-X khas dari kedua jenis zeolit tersebut. Puncak-puncak difraksi zeolit klinoptilolit berdasarkan JCPDS No 17-0143 ialah 2θ 17.305o, 22.319o, 23.849o, 24.850o, 25.923o, 26.108o, 28.036o, 30.063o, 31.936o, dan 32.655o (Lampiran 3), sedangkan zeolit mordenit berdasarkan JCPDS No 6-239 ialah 2θ 6.44o, 9.74o, 15.32o, 22.25o, 25.63o, 26.33o, 27.65o, dan 30.93o. Korkuna et al.
(2006) melaporkan bahwa zeolit alam klinoptilolit memiliki puncak tertinggi pada 2θ 9.77o, 22.31o, 26.60o, dan 29.94o, sedangkan jenis mordenit pada 2θ 9.77o, 22.22o, 26.24o, dan 27.65o. Bentuk puncak yang tidak ramping menunjukkan bahwa kristalinitas zeolit alam kurang baik. Hal ini terjadi karena pengaruh heterogenitas kation-kation dan adanya pengotor pada zeolit alam (West 1984). Semakin ramping puncak difraksi suatu material, derajat kristalinitasnya semakin baik dengan susunan atom yang semakin rapat.
2θ
5 mikr perm zeoli perm (Gam meny (Wan fung Pemi menj mele Suka zeoli titik 16.95 (Wan Ga didom zeoli lokas mem alam (201 5. Se akan Kand 2010 Analisis rostruktur y mukaan (Fur it alam Suk mukaan kasa
mbar 2). Por yebabkan s ng dan Pen
si zeolit ala ijaran diaw jadi karbon epaskan oks abumi diper it alam, baik
leleh tingg 5%. Unsur-ng et al. 200
ambar 2 Mo Komposis minasi oleh it (Tabel 1 si penemba mberikan ha m Sukabumi 0), jenis kli ecara kimia n memengar dungan Si y 0).
mengguna yang melipu roiddun dan kabumi berb
ar, dan cen rositas relat struktur kris
ng 2010). am sebagai wali pada su n dioksida
sida logam roleh 16.95 k berupa ok gi (di atas -unsur terse 09).
orfologi per si kimia ze h oksigen, si dan Lampir akan sinar sil yang be i dapat dig inoptilolit m a, perbedaan ruhi stabilit yang lebih t
akan SEM uti topogra n Wibawa 20
bentuk sepe nderung be tif masih ke stal zeolit t
Pengotor y adsorben. O uhu 500 sam dan abu, d m (Heiri et
5% (Lampir ksida logam 1000 oC) m ebut diduga
rmukaan zeo eolit alam
ilikon, dan ran 5). Kom r-X. Penem erbeda pula golongkan s
memiliki nis n nisbah Si asnya pada tinggi akan
M-EDX d fi, morfolo 011). Foto S erti kubus t eragregasi m
cil, tertutup tidak homo yang menut Oleh sebab mpai 550 oC dilanjutkan
al. 2001). ran 4), men m Fe, Ta, Sr
maupun ba a ikut mem
olit alam Su Sukabumi aluminium mposisi ters mbakan pad a. Nisbah Si sebagai jen
sbah Si/Al i/Al dari ze a perlakuan memperkua dilakukan ogi, kompos SEM menun tidak beratu membentuk pi oleh peng ogen dan c tupi pori-po
itu, nilai hi C, ketika za
pada suhu Nilai hila nunjukkan b r, Ba, Cu, d ahan organi mbentuk ker ukabumi (pe hasil pengu sebagai pen sebut bergan da posisi i/Al dipero is klinoptil 4–4.5, seda eolit dengan panas dan at struktur b
untuk m sisi, dan kr njukkan bah uran, memil k partikel l gotor yang d
enderung b ori akan m ilang pijar d at organik
1050 oC y ang pijar z
bahwa peng dan Mg yang ik dan air,
rangka stru erbesaran 10 ukuran den nyusun stru ntung pada yang berb leh 4.17, m lolit. Menur angkan jeni
6
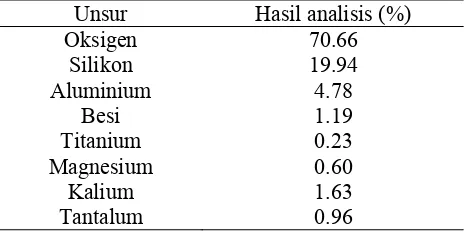
Tabel 1 Komposisi kimia zeolit alam Sukabumi Unsur Hasil analisis (%)
Oksigen 70.66 Silikon 19.94 Aluminium 4.78
Besi 1.19 Titanium 0.23 Magnesium 0.60
Kalium 1.63 Tantalum 0.96
Ciri-ciri Zeolit Alam Teraktivasi dan Terpilar-Fe2O3
Pencirian dengan XRD (Lampiran 6) zeolit alam Sukabumi setelah aktivasi dengan kalsinasi dan asam tidak menunjukkan banyak perubahan nilai 2θ dari puncak-puncak tertinggi. Variasi suhu kalsinasi dari 100 sampai 400 oC bertujuan menguapkan air yang terjerap pada pori-pori kristal zeolit sehingga luas permukaannya meningkat (Swantomo et al. 2009). Pemanasan di atas suhu 400 oC tidak dilakukan karena dikhawatirkan merusak struktur kristal zeolit.
Pemanasan pada suhu 100 oC menghasilkan kristalinitas paling besar (Tabel 2). Air telah teruapkan pada suhu tersebut sehingga luas permukaan zeolit meningkat. Namun, kristalinitas menurun seiring naiknya suhu kalsinasi. Oksida logam pengotor pada zeolit diduga turut menyumbang sifat kristal zeolit (Subariyah 2011). Suhu lebih tinggi akan menguapkan oksida ini dan menurunkan kristalinitas zeolit. Logam pengotor memiliki titik leleh yang tinggi dalam bentuk oksida dan mengalami ikatan antaratom yang kuat, tetapi dalam bentuk ion, logam pengotor akan mudah menguap pada suhu tinggi.
Tabel 2 Kristalinitas zeolit alam setelah proses aktivasi Perlakuan Variasi perlakuan Kristalinitas (%)
Zeolit alam - 53.03
Aktivasi suhu
100 oC 58.31
200 oC 55.96
300 oC 48.93
400 oC 46.88
Aktivasi asam
0.5 M 53.94
1.0 M 39.98
1.5 M 44.90
2.0 M 50.66
7 Akan elekt logam tertin Peris tidak samp dapa (Fati perm Fe2O
Gam teratu bagia diakt disisi terse antar n tetapi, tronegativita m Al dari k
Konsentra nggi (Tabel stiwa ini me k terlalu ber pai 2.0 M m at tukar pada
imah 2009) mukaan krist O3.
mbar 3 Mor akti Morfologi ur. Porosita an pori-por tivasi permu ipkan pada ebut secara rlapisan ma
ion Cl– as atom Al erangka zeo asi asam 0.5 2). Penurun enunjukkan rpengaruh p meningkatka
a kerangka ). Foto SE tal zeolit ala
rfologi perm vasi HCl 2. i permukaan as cukup b ri zeolit ya ukaan zeoli a antarlapis
umum m aupun penje
akan cen (1.61) lebi olit ini diken 5 M mengha nan signifik n bahwa kon pada kristal an kembali k
struktur ze EM (Gamb
am Sukabum
mukaan zeo 0 M (b) set n setelah ak besar, ditan ang setelah it alam men an zeolit. M masih berbe
erapan Fe2O
nderung be ih kecil dar
nal sebagai asilkan zeo kan terjadi p nsentrasi HC linitas zeoli
kristalinitas olit tertata u bar 3) mem
mi setelah d
(a)
(b) olit alam ha
elah terpilar ktivasi berb ndai oleh c h diaktivasi njadi lebih Morfologi entuk kubu O3 di permu
erikatan d ripada atom proses deal lit alam den pada aktiva Cl 0.5 M te it alam. Kon s zeolit, didu ulang dan b mperlihatka diaktivasi d
asil aktivasi r Fe2O3 (pe bentuk sepe cekungan b i tampak le
luas sehing permukaan us. Penyisip ukaan zeoli
dengan Al3 m Si (1.90).
luminasi. ngan nilai k asi dengan H erlalu rendah nsentrasi as uga karena berubah kom an perbeda dan dipilaris
i suhu 400 rbesaran 10 erti serpihan erwarna hi ebih banya gga besi ok zeolit terp pan Fe2O3 it ditunjukk
3+
karena Hilangnya kristalinitas HCl 1.0 M. h sehingga sam 1.0 M atom-atom mposisinya aan tekstur
sasi dengan
o
C (a) dan 000 kali) n dan lebih itam, yaitu ak. Setelah ksida dapat
8
bongkahan putih Fe2O3 yang terdistribusi pada permukaan luar zeolit. Penyisipan Fe2O3 juga meningkatkan jumlah mesopori pada zeolit (Udyani 2010). Porositas yang cukup besar ditunjukkan oleh cekungan berwarna hitam yang tampak lebih banyak lagi dibandingkan dengan sebelum pilarisasi.
Komposisi kimia zeolit dicirikan dengan menggunakan EDX sebelum dan setelah terpilar Fe2O3. Dipilih zeolit yang diaktivasi dengan suhu kalsinasi 400 oC dan HCl 2.0 M (Tabel 3 dan Lampiran 7) karena menurut Pranoto (2012), aktivitas antioksidan zeolit alam paling rendah pada kondisi tersebut. Besi oksida yang terkandung setelah aktivasi menurun dibandingkan dengan zeolit alam. Hal ini berpotensi menurunkan aktivitas antioksidan karena besi oksida merupakan bahan semikonduktor sehingga kombinasinya dengan zeolit alam sebagai bahan penopang diharapkan dapat meningkatkan aktivitas antioksidan. Hasil ini sesuai dengan yang dilaporkan Pranoto (2012), yaitu bahwa aktivitas antioksidan zeolit alam menurun dengan meningkatnya suhu dan konsentrasi asam.
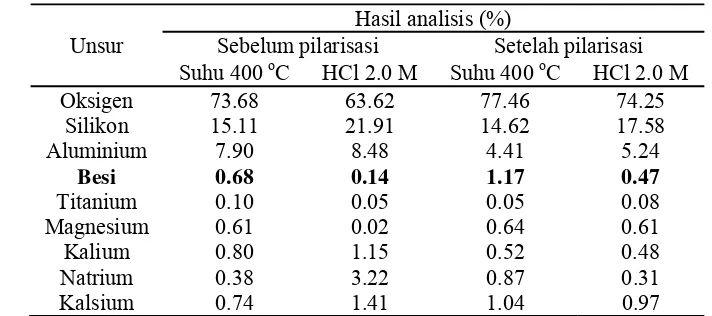
Tabel 3 Komposisi kimia zeolit alam Sukabumi sebelum dan setelah pilarisasi Fe2O3 dengan aktivasi kalsinasi 400 oC dan HCl 2.0 M
Unsur
Hasil analisis (%)
Sebelum pilarisasi Setelah pilarisasi Suhu 400 oC HCl 2.0 M Suhu 400 oC HCl 2.0 M Oksigen 73.68 63.62 77.46 74.25
Silikon 15.11 21.91 14.62 17.58 Aluminium 7.90 8.48 4.41 5.24
Besi 0.68 0.14 1.17 0.47
Titanium 0.10 0.05 0.05 0.08 Magnesium 0.61 0.02 0.64 0.61 Kalium 0.80 1.15 0.52 0.48 Natrium 0.38 3.22 0.87 0.31 Kalsium 0.74 1.41 1.04 0.97
Perlakuan asam menurunkan lebih banyak oksida logam dibandingkan dengan pemanasan. Penurunan tersebut dapat diakibatkan oleh hilangnya pengotor pada zeolit yang berbentuk oksida amorf (Lampiran 7). Nisbah Si/Al zeolit alam setelah aktivasi kalsinasi 400 oC dan HCl 2.0 M berturut-turut sebesar 1.91 dan 2.58. Hasil ini menandakan aktivasi dengan penambahan asam lebih baik dibandingkan dengan pemanasan. Kalsinasi dan penambahan asam menurunkan kandungan Al dalam zeolit (dealuminasi). Besi oksida akan menempati ruang yang ditinggalkan oleh Al tersebut sehingga kandungan Fe2O3 dalam kerangka zeolit meningkat (Lestari 2010).
9
Aktivitas Antioksidan Zeolit Alam
Penangkapan radikal DPPH merupakan salah satu metode uji untuk menentukan aktivitas antioksidan. Metode DPPH mempunyai kelebihan, yaitu mudah digunakan, memiliki sensitivitas yang tinggi, dan dapat menganalisis sejumlah besar sampel dalam jangka waktu yang singkat (Sunarni 2005). Parameter yang digunakan untuk uji penangkapan radikal DPPH ialah nilai IC50, yaitu konsentrasi suatu senyawa yang diperlukan untuk menangkap radikal DPPH sebesar 50%. Vitamin C dijadikan sebagai kontrol positif dan diperoleh nilai IC50 sebesar 1.19 µg/mL (Lampiran 8). Semakin kecil nilai IC50, senyawa uji semakin aktif sebagai penangkap radikal DPPH dan karena itu, aktif sebagai antioksidan.
Aktivitas antioksidan teraktivasi kalsinasi dan asam semakin menurun dengan semakin meningkatnya suhu kalsinasi dan konsentrasi asam. Penurunan ini menunjukkan bahwa terjadi perubahan komposisi, pengurangan bobot, dan perubahan fase. Oksida logam seperti Fe2O3 yang terkandung dalam zeolit alam hilang selama proses aktivasi. Sifat semikonduktor Fe2O3 diduga memiliki peranan penting pada aktivitas antioksidan dengan melepaskan elektron yang dimilikinya ke radikal DPPH.
Mekanisme penangkapan radikal DPPH oleh antioksidan ialah dengan sumbangan radikal hidrogen pada radikal tersebut. Radikal DPPH yang berwarna ungu akan berubah menjadi senyawa bukan radikal 1,1-difenil-2-pikrilhidrazina yang berwarna kuning. Konsentrasi radikal DPPH yang tersisa kemudian diukur dengan spektrofotometer pada panjang gelombang 517 nm (Blois 1958). Metode DPPH ini juga dapat diterapkan pada mineral alam yang memiliki pori seperti zeolit (Molyneux 2004).
Zeolit alam memiliki kemampuan menghambat senyawa radikal bebas. Nilai absorbans zeolit alam lebih kecil daripada kontrol negatif, yaitu larutan DPPH (Lampiran 9). Hal ini menunjukkan bahwa sebagian DPPH telah terjerap oleh zeolit. Dalam penelitian ini, warna ungu DPPH tidak berubah, hanya berkurang intensitasnya (Gambar 4). Hal ini disebabkan oleh aktivitas antioksidan zeolit alam yang masih kecil. Oleh karena itu, pengukuran sebaiknya dilakukan pada panjang gelombang dari warna komplementer, yaitu kuning.
(a) (b)
Gambar 4 Warna larutan DPPH setelah berinteraksi dengan zeolit alam hasil aktivasi dengan kalsinasi (a) dan dengan HCl (b) sebelum terpilar Fe2O3
10
melalui penangkapan dan penjerapan radikal bebas tersebut dalam struktur zeolit. Struktur pori dan rongga yang besar memungkinkan zeolit dapat mengadsorpsi radikal bebas dan menstabilkannya. Proses adsorpsi sangat dipengaruhi oleh beberapa faktor di antaranya sifat dan konsentrasi adsorbat atau adsorben, luas permukaan, dan ukuran partikel. Semakin besar luas permukaan, semakin banyak zat yang dapat diadsorpsi (Atkins 1999). Partikel zeolit memiliki 3 jenis pori, yaitu makropori, mesopori, dan mikropori. Makropori merupakan jalan masuk ke dalam partikel menuju mikropori. Mesopori berada di antara makropori dan mikropori. Makropori tidak berkontribusi pada besarnya luas permukaan zeolit. Mikroporilah penentu besarnya luas permukaan zeolit dan terbentuk selama proses aktivasi. Pada mikropori inilah sebagian besar peristiwa adsorpsi terjadi (Rakhmatullah et al.2007).
Aktivitas Antioksidan Zeolit Terpilar-Fe2O3
Pilarisasi zeolit dengan besi oksida diawali dengan proses interkalasi logam besi ke dalam antarlapisan zeolit yang memiliki pori dan rongga sangat besar. Logam besi yang terinterkalasi ini akan menggantikan kation-kation antarlapisan yang mudah ditukar. Selanjutnya dengan proses kalsinasi, logam besi akan berubah menjadi bentuk oksida yang dapat menyangga antarlapisan zeolit sehingga diharapkan dapat meningkatkan aktivitas antioksidan (Wijaya et al.
2004). Selama proses hidrotermal, campuran akan mengalami reaksi kondensasi. Reaksi kondensasi yang terjadi memungkinkan pemutusan dan pembentukan ikatan baru dengan dikatalisis oleh ion hidroksil dan menghasilkan ikatan penyusun material kristalin.
Penurunan intensitas warna larutan DPPH oleh zeolit alam terpilar-Fe2O3 ditunjukkan pada Gambar 5. Nilai absorbans lebih kecil dibandingkan dengan sebelum terpilar. Hal tersebut mengindikasikan peningkatan aktivitas antioksidan pada setiap perlakuan.
Gambar 5 Warna larutan DPPH setelah berinteraksi dengan zeolit alam hasil aktivasi dengan kalsinasi (a) dan dengan HCl (b) setelah terpilar Fe2O3
11
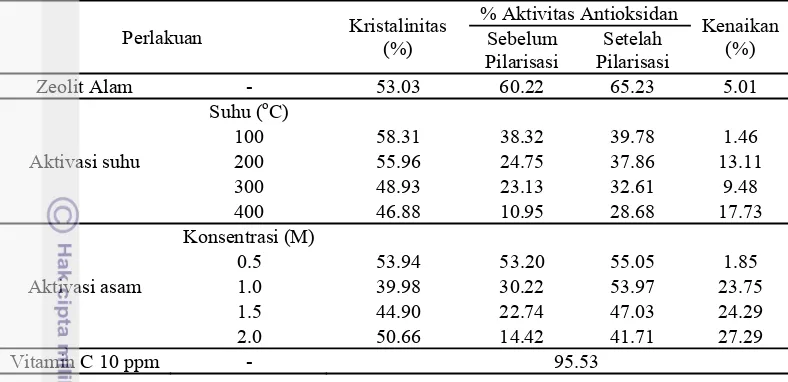
Tabel 4 Aktivitas antioksidan zeolit alam sebelum dan setelah terpilar Fe2O3
Perlakuan Kristalinitas
(%)
% Aktivitas Antioksidan
Kenaikan (%) Sebelum
Pilarisasi
Setelah Pilarisasi
Zeolit Alam - 53.03 60.22 65.23 5.01
Aktivasi suhu
Suhu (oC)
100 58.31 38.32 39.78 1.46
200 55.96 24.75 37.86 13.11
300 48.93 23.13 32.61 9.48
400 46.88 10.95 28.68 17.73
Aktivasi asam
Konsentrasi (M)
0.5 53.94 53.20 55.05 1.85
1.0 39.98 30.22 53.97 23.75
1.5 44.90 22.74 47.03 24.29
2.0 50.66 14.42 41.71 27.29
Vitamin C 10 ppm - 95.53
Aktivitas antioksidan zeolit terpilar-Fe2O3 meningkat dibandingkan dengan zeolit tanpa pilar. Hal tersebut membuktikan bahwa penambahan logam oksida Fe2O3 dapat meningkatkan aktivitas antioksidan walaupun masih sangat rendah. Aktivitas antioksidan yang diperoleh berbanding lurus dengan kristalinitas zeolit alam pada setiap perlakuan. Nilai kristalinitas yang semakin tinggi menyebabkan struktur zeolit alam semakin teratur sehingga Fe2O3 dapat diinterkalasikan dalam antarlapisan zeolit secara sempurna. Hal ini yang mengakibatkan aktivitas antioksidan semakin meningkat.
Aktivitas antioksidan zeolit alam diduga berasal dari oksida logam pada kerangka stukturnya. Kandungan Fe2O3 dalam zeolit hasil aktivasi dengan kalsinasi 400 oC (1.17%) dan dengan HCl 2.0 M (0.47%) dapat meningkatkan aktivitas antioksidan berturut-turut sebesar 17.73% dan 27.29% setelah pilarisasi dengan Fe2O3. Semakin tinggi jumlah Fe2O3 yang terpilarkan pada struktur antarlapisan zeolit, aktivitas antioksidan akan semakin tinggi.
SIMPULAN DAN SARAN
Simpulan12
Saran
Perlu dilakukan penentuan IC50 zeolit alam. Uji aktivitas antioksidan metode DPPH sebaiknya dilakukan pada panjang gelombang yang berbeda, yaitu warna komplementer kuning.
DAFTAR PUSTAKA
Aranda RS, Lopez LAP, Arroyo JL, Garza BAA, Torres NW. 2009. Antimicrobial and antioxidant activities of plants from Northeast of Mexico.
Evidence-Based Complementary and Alternative Medicine. 2011:1-6.
Atkins PW. 1999. Kimia Fisik Jilid 1. Ed ke-4. Kartohadiprojo II, penerjemah. Jakarta (ID): Erlangga. Terjemahan dari: Physical Chemistry.
Blois MS. 1958. Antioxidant determinations by the use of a stable free radical.
Nature.181:1199-1200.
Fatimah D. 2009. Peningkatan kualitas zeolit alam Cikancra, Tasikmalaya, dengan metode asam mineral: sebuah pengkajian karakter fisiko-kimia, melalui analisis tukar kation, atomic adsorption spectrometer (AAS), scanning electron microscopy (SEM) dan X-ray diffractometer (XRD). Di dalam:
Prosiding Pemaparan hasil Penelitian Pusat Geoteknologi-LIPI; 2009 Jul 14; Bandung, Indonesia. Bandung (ID): LIPI.
Furoiddun N, Wibawa G. 2011. Peningkatan kualitas zeolit alam Indonesia sebagai adsorben pada produksi bioetanol fuel grade. Di dalam: Prosiding
Seminar Nasional Teknologi Industri XV; 2011 Mei 12; Surabaya,
Indonesia. Surabaya (ID): Institut Teknologi Sepuluh Nopember Surabaya. hlm 187-193.
Hayati T. 2011. Aktivitas antioksidan beberapa tanaman obat menggunakan zeolit alam sebagai bahan penopang [tesis]. Bogor (ID): Institut Pertanian Bogor. Hecht K. 2010. Application of natural zeolites in medicine and cosmetology. Di
dalam: Proceedings International Conference Zeomedcos; 2010 Sep 29; London, Inggris. London (UK): International Academy of Science H&E. Heiri O, Lotter FA, Lemcke G. 2001. Loss on ignition as a method for estimating
organic and carbonate content in sediments: reproducibility and comparibility of results. J Paleolimnol. 25:101-110.
Ipek H, Mehmet A, Nurettin A, Mugdat Y. 2012. The effect of zeolite on oxidant/antioxidant status in healthy dairy cows. Acta Vet Brno. 81:043-047. Korkuna O, Leboda R, Skubiszewska J, Vrublevs T, Gun VM, Ryczkowski J.
2006. Structural and physicochemical properties of natural zeolites, clinoptilolite and mordenite. Microporous and Mesoporous Mat. 87:243-254.
Kresimir P, Miroslav C. 2001. Natural zeolite clinoptilolite: New adjuvant in anticancer therapy. J Mol Med. 78:708-720.
13
Mohapatra M, Anand S. 2010. Synthesis and applications of nano structured iron oxides/hydroxides. Int J Eng Sci Technol. 31(1):93-96.
Molyneux P. 2004. The use of the stable free radical diphenylpicrylhidrazyl (DPPH) for estimating antioxidant activity. J Sci Technol.26:211-219. Pavelic K, Katic M, Serko V, Marotti T, Bosnjak B, Balog T, Stojkovic R,
Radacic M, Kolic M, Poljak-Blazi M. 2002. Immunostimulatory effect of natural clinoptilolite as a possible mechanism of its antimetastatic ability. J Cancer Res Clin Oncol. 128:37-44.
Pranoto DR. 2012. Potensi zeolit alam sebagai antioksidan [skripsi]. Bogor (ID): Institut Pertanian Bogor.
Rakhmatullah DK, Wiradini G, Ariyanto NP. 2007. Pembuatan adsorben dari zeolit alam dengan karakteristik adsorption properties untuk kemurnian bioetanol [skripsi]. Bandung (ID): Institut Teknologi Bandung.
Rohman A, Riyanto S, Dahliyanti R, Pratomo DB. 2009. Penangkapan radikal 1,1-difenil-2-pikrilhidrazil (DPPH) oleh ekstrak buah Psidium guajava dan
Averrhoa carambola. J Ilmu Kefarmasian. 7(1):1-5.
Subariyah I. 2011. Adsorpsi Pb(II) menggunakan zeolit alam termodifikasi asam fosfat [tesis]. Bogor (ID): Institut Pertanian Bogor.
Sunarni T. 2005. Aktivitas antioksidan penangkap radikal bebas beberapa kecambah dari biji tanaman Familia Papilionaceae. J Pharm Indones. 2(2):53-61.
Swantomo D, Kundari NA, Pambudi SL. 2009. Adsorpsi fenol dalam limbah dengan zeolit alam terkalsinasi. Di dalam: Seminar Nasional V SDM
Teknologi Nuklir Yogyakarta; 2009 Nov 5; Yogyakarta, Indonesia.
Yogyakarta (ID): Sekolah Tinggi Teknologi Nuklir-Badan Tenaga Nuklir Nasional.
Syafii F. 2011. Modifikasi zeolit melalui interaksi dengan Fe(OH)3 untuk meningkatkan kapasitas tukar anion [skripsi]. Bogor (ID): Institut Pertanian Bogor.
Udyani K, Prasetyo I, Mulyono P, Yuliani. 2010. Pengaruh OH/Fe pada pembuatan ampo terpilar oksida besi terhadap penjerapan detergen dalam air. Di dalam: Prosiding Seminar Nasional Teknik Kimia. Pengembangan Teknologi Kimia untuk Pengolahan Sumber Daya Alam Indonesia; 2010 Jan 26; Yogyakarta, Indonesia. Yogyakarta (ID): Universitas Gadjah Mada. Utami S, Kosela S, Hanafi M. 2006. Efek peredaman radikal bebas
1,1-difenil-2-pikrilhidrazil (DPPH) dan uji toksisitas pendahuluan terhadap larva udang
Artemia salina dari ekstrak aseton daging buah Sesoot (Garcinia picrorrhiza
MIQ.). J Med. 14(3):171-176.
Wang S, Peng Y. 2010. Natural zeolite as effective adsorbent in water and waste water treatment. J Eng Chem. 156:11-24.
Wang S, Terdkiatburana T, Tade MO. 2009. Adsorption Cu(II), Pb(II), and humic acid on natural zeolite tuff in single and binary systems. Sep Purif Technol. 62:64-70.
Weitkamp J, Puppe L. 1999. Catalysis and Zeolites: Fundamental and Applications. Berlin (DE): Springer-Verlag.
14
Wijaya K, Sugiharto E, Mudasir, Tahir I, Liawati I. 2004. Sintesis komposit oksida besi montmorillonit dan uji stabilitas strukturnya terhadap asam sulfat. Indones J Chem. 4(1):33-42.
Wijaya K, Tahir I, Baikuni A. 2002. Sintesis lempung terpilar Cr2O3 dan pemanfaatannya sebagai inang senyawa p-nitroanilin. Indones J Chem.
2(1):12-21.
Wijaya K, Tahir I, Haryanti N. 2005. Sintesis Fe2O3-montmorillonit dan aplikasinya sebagai fotokatalis untuk degradasi zat pewarna congo red.
Indones J Chem. 5(1):41-47.
15
Lampiran 1 Bagan alir penelitian
Preparasi
Aktivasi
Pilarisasi Fe2O3
400 oC
2.0 M
Aktivitas antioksidan Zeolit alam
Zeolit alam 100 mesh XRD dan SEM-EDX Hilang Pijar
Zeolit kalsinasi 100, 200, 300, dan 400 oC
Zeolit aktivasi HCl 0.5, 1.0, 1.5, dan 2.0 M
Zeolit- Fe2O3
XRD XRD
16
Lampiran 2 Pencirian XRD zeolit alam Sukabumi
Puncak no
2θ
(derajat) d (Å)
Lebar setengah puncak (derajat)
Intensitas (counts)
Intensitas terintegrasi
(counts)
Kristalinitas (%)
2 9.8363 8.98492 0.46000 20 515
53.03 11 22.3342 3.97736 0.78000 96 3926
15 26.6633 3.34060 0.50000 41 1277 18 29.9490 2.98116 0.54000 33 1022
17
Lampiran 4 Hilang pijar zeolit alam Sukabumi
Ulangan
Bobot (g) Cawan Zeolit
Cawan + zeolit Hilang pijar
(%) Sebelum
pemijaran
Sesudah pemijaran
1 24.3308 1.0004 25.3312 25.1617 16.94 2 24.5276 1.0003 25.5279 25.3586 16.92 3 24.4235 1.0007 25.4242 25.2543 16.98
Contoh perhitungan:
% Hilang pijar = (Cawan + zeolit) sebelum pemijaran– (Cawan + zeolit) sesudah pemijaran
bobot zeolit × 100%
= 25.3312 ― 25.1617
1.0004 × 100%
= 16.94% Rerata = 16.94+16.92+16.98
3
18
Lampiran 5 Komposisi kimia zeolit alam Sukabumi dengan EDX
Unsur Hasil analisis
% Bobot % Atom
Oksigen 52.59 70.66
Silika 26.05 19.94
Aluminium 6.00 4.78
Besi 3.10 1.19
Titanium 0.52 0.23
Magnesium 0.68 0.60
Kalium 2.96 1.63
19
Lampiran 6 Pencirian XRD zeolit alam setelah aktivasi dengan kalsinasi dan dengan asam
Kalsinasi 100 °C Puncak
no
2θ
(derajat) d (Å)
Lebar setengah puncak (derajat)
Intensitas (counts)
Intensitas terintegrasi
(counts)
Kristalinitas (%)
16 22.4731 3.95309 0.68500 89 2913
58.31 20 26.5826 3.35056 0.39050 78 1963
19 29.7147 3.46164 0.30000 44 935
Kalsinasi 200 °C Puncak
no
2θ
(derajat) d (Å)
Lebar setengah puncak (derajat)
Intensitas (counts)
Intensitas terintegrasi
(counts)
Kristalinitas (%)
16 22.3990 3.96600 0.61670 83 2401
55.96 21 26.6133 3.34676 0.50000 53 1622
22 27.9231 3.19268 0.69670 38 1177
Kalsinasi 300 °C Puncak
no
2θ
(derajat) d (Å)
Lebar setengah puncak (derajat)
Intensitas (counts)
Intensitas terintegrasi
(counts)
Kristalinitas (%)
54 27.6359 3.22520 0.14620 93 725
48.93 52 26.5968 3.34880 0.24690 68 1068
39 22.3309 3.97794 0.39340 68 910
Kalsinasi 400 °C Puncak
no
2θ
(derajat) d (Å)
Lebar setengah puncak (derajat)
Intensitas (counts)
Intensitas terintegrasi
(counts)
Kristalinitas (%)
35 22.0942 4.02002 0.15070 120 1436
46.88 36 22.4905 3.95007 0.00000 76 0
47 26.5859 3.35015 0.26910 54 822
Aktivasi dengan HCl 0.5 M Puncak
no
2θ
(derajat) d (Å)
Lebar setengah puncak (derajat)
Intensitas (counts)
Intensitas terintegrasi
(counts)
Kristalinitas (%)
13 22.3558 3.97357 0.85000 75 1330
53.94 18 27.9016 3.19509 0.62660 50 1621
20
lanjutan Lampiran 6
Aktivasi dengan HCl 1.0 M Puncak
no
2θ
(derajat) d (Å)
Lebar setengah puncak (derajat)
Intensitas (counts)
Intensitas terintegrasi
(counts)
Kristalinitas (%)
13 22.4257 3.96134 0.71000 81 2413
39.98 17 26.5909 3.34953 0.61500 53 1672
18 27.9016 3.19509 0.72000 38 1375
Aktivasi dengan HCl 1.5 M Puncak
no
2θ
(derajat) d (Å)
Lebar setengah puncak (derajat)
Intensitas (counts)
Intensitas terintegrasi
(counts)
Kristalinitas (%)
26 22.0550 4.02708 0.13330 172 1081
44.90 44 26.6832 3.33815 0.14800 82 614
27 27.3907 3.96745 0.36360 65 821
Aktivasi dengan HCl 2.0 M Puncak
no
2θ
(derajat) d (Å)
Lebar setengah puncak (derajat)
Intensitas (counts)
Intensitas terintegrasi
(counts)
Kristalinitas (%)
32 26.6183 3.34615 0.40340 66 1346
50.66 24 22.4257 3.96134 0.75000 58 1446
21
Lampiran 7 Komposisi kimia zeolit alam Sukabumi hasil aktivasi dengan kalsinasi 400 oC dan dengan HCl 2.0 M sebelum dan setelah pilarisasi Fe2O3
Suhu 400 oC
Pilar HCl 2.0 M HCl 2.0 M
22
Lampiran 8 Kurva standar dan IC50 vitamin C
[Vitamin C] (ppm) Absorbans log [Vitamin C] % Aktivitas
2 0.502 0.3010 61.30
4 0.317 0.6021 75.56
6 0.213 0.7782 83.58
8 0.124 0.9031 90.44
10 0.058 1.0000 95.53
y = 46.3556 + 48.7228 log (x) r2 = 0.9989 50 = 46.3556 + 48.7228 log (x)
log x =
7228 . 48
3556 . 46
50−
= 0.0751 µg/mL
x = 100.0751 = 1.19 µg/mL
y = 48.7228x+ 46.3536 r² = 0.9989
0.00 10.00 20.00 30.00 40.00 50.00 60.00 70.00 80.00 90.00 100.00
0.2000 0.3000 0.4000 0.5000 0.6000 0.7000 0.8000 0.9000 1.0000
Aktivitas antioksidan (%
)
23
Lampiran 9 Aktivitas antioksidan zeolit alam Sukabumi hasil aktivasi dengan kalsinasi 400 oC dan dengan HCl 2.0 M sebelum dan setelah pilarisasi Fe2O3
a. Zeolit alam (ZA) sebelum dipilar dengan Fe2O3 Perlakuan Absorbans % Aktivitas
Blangko 1.297 -
ZA 0.516 60.22 ZA-100 0.800 38.32 ZA-200 0.976 24.75 ZA-300 0.997 23.13 ZA-400 1.155 10.95
ZA-0.5 M 0.607 53.20
ZA-1.0 M 0.905 30.22
ZA-1.5 M 1.002 22.74
ZA-2.0 M 1.110 14.42
Contoh perhitungan:
Persen aktivitas antioksidan zeolit alam aktivasi HCl 2.0 M
% Aktivitas penangkapan radikal = A–B
A × 100%
= × 100% 297
. 1
110 . 1 297 .
1 −
= 14.42%
b. Zeolit alam (ZA) setelah dipilar dengan Fe2O3 Perlakuan Absorbans % Aktivitas
Blangko 1.297 -
ZA 0.451 65.23
ZA-100 0.781 39.78 ZA-200 0.806 37.86 ZA-300 0.874 32.61 ZA-400 0.925 28.68
ZA-0.5 M 0.583 55.05
ZA-1.0 M 0.597 53.97
ZA-1.5 M 0.687 47.03
ZA-2.0 M 0.756 41.71
Contoh perhitungan:
Persen aktivitas antioksidan zeolit alam aktivasi HCl 2.0 M
% Aktivitas penangkapan radikal = A–B
A × 100%
= × 100% 297
. 1
756 . 0 297 .
1 −
RIWAYAT HIDUP
Penulis dilahirkan di Bogor pada tanggal 23 Agustus 1989 sebagai putra kedua dari bapak H. Subandi dan ibu Hj. Sri ah Indah. Tahun 2007 penulis lulus dari SMA Negeri 1 Cibinong dan pada tahun yang sama penulis diterima di Program Diploma 3 Analisis Kimia, Institut Pertanian Bogor melalui jalur PMDK dan lulus pada tahun 2010. Penulis melanjutkan pendidikan S1 Alih Jenis Kimia, Departemen Kimia, Fakultas Matematika dan Ilmu Pengetahuan Alam di Institut Pertanian Bogor pada tahun 2010.
Selama menjalani masa perkuliahan di Diploma 3 IPB, penulis pernah mengikuti Training Safety With Merck: Improving Life and Environment, Pelatihan dan Seminar HACCP & ISO 9000. Tahun 2010 penulis mengikuti Pekan Ilmiah Mahasiswa Nasional (Pimnas) XXIII di Universitas Mahasaraswati, Denpasar, Bali dan memperoleh penghargaan perak dalam penyusunan dan presentasi ilmiah PKM-M yang berjudul “Edukasi Pengembangan Sistem Motorik Kasar dan Halus Siswa SLB Dharma Wanita dan Sejahtera (Metode Puzzle, Bola, dan Keseimbangan Tubuh)”. Penulis melakukan praktik kerja lapangan di PT Indocement Tunggal Prakarsa, Tbk dengan judul laporan Penentuan C, H, N, dan S dalam Batu Bara sebagai Bahan Bakar Produksi Semen dengan Elemental Analyzers.