PENANGANAN FILLET
IKAN GURAMI
(
Osphronemus gouramy
Lacepede)
DALAM KEMASAN MODIFIKASI ATMOSFIR
SLAMET SUHARTO
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
PERNYATAAN MENGENAI TESIS DAN
SUMBER INFORMASI
Dengan ini saya menyatakan bahwa tesis
PENANGANAN FILLET IKAN
GURAMI
(
Osphronemus gouramy
Lacepede)
DALAM KEMASAN
MODIFIKASI ATMOSFIR
adalah karya saya dengan arahan dari komisi
pembimbing dan belum diajukan dalam bentuk apapun kepada perguruan tinggi
mana-pun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan
maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan
dicantumkan dalam Daftar Pustaka di bagian akhir tesis ini.
Bogor, Januari 2010
Slamet Suharto
RINGKASAN
SLAMET SUHARTO. Penanganan Fillet Ikan Gurami (
Osphronemous
gouramy
Lacepede) dalam Kemasan Modifikasi Atmosfir
.
Dibimbing oleh
I
WAYAN BUDIASTRA, dan JOKO SANTOSO.
Akhir-akhir ini terdapat kecenderungan akan kebutuhan jenis bahan makanan
yang segar, praktis dan sehat sebagai akibat perubahan perilaku masyarakat
yang semakin komplek dan sibuk. Ikan merupakan bahan pangan bernilai gizi
tinggi namun mudah mengalami kemunduran mutu
(high perisable food)
jika
tidak ditangani secara tepat. Fillet merupakan bentuk preparasi bahan
makanan yang cukup praktis (
minimaly process
) dan segar.
Penggunaan modifikasi atmosfer telah diketahui dapat meningkatkan umur
simpan bahan makanan seperti daging, sayur dan ikan. Komposisi gas dalam
kemasan bervariasi untuk masing-masing jenis makanan tersebut, termasuk
jenis ikan. Untuk mengetahui penanganan dan penggunaan komposisi
(konsentrasi) CO2 yang tepat maka perlu dilakukan penelitian.
Penelitian ini bertujuan untuk menentukan teknologi penanganan pascapanen
yang paling optimal pada pengemasan fillet ikan gurami secara MAP dengan
mengetahui bahan pencucian fillet, konsentrasi gas C
O2yang optimal dan
umur simpan fillet. Hasil penelitian ini diharapkan bermanfaat sebagai
informasi teknik penanganan fillet ikan gurami.
Penelitian dilakukan dalam 2 tahap, yaitu menentukan bahan pencuci fillet
dan komposisi gas dalam kemasan.
Dalam penelitian ini digunakan fillet dari ikan gurami ukuran + 1000g yang
diperoleh Kolam Babakan Sawah Baru Bogor. Fillet dibuat sesuai prosedur
SNI 01-4103.2-1992 yang meliputi proses pelumpuhan, pembuangan darah,
penampungan sementara, pemotongan/ penyayatan, pembuangan kulit dan
duri, dan perapihan. Sebelum dilakukan pemfilletan ikan di berok/puasakan
selama tiga hari untuk mengurangi bau lumpur.
Bahan yang digunakan berupa air bersih dengan kualitas air minum (SNI
01-4103.2-1992), larutan garam 50g garam/ 1 l air bersih, larutan air jeruk nipis
(60 ml air jeruk/ 1 l air setara dengan 1 buah, ukuran 50 g), larutan garam
yang ditambah air jeruk nipis, dan larutan klorin 10 ppm.
Hasil penelitian tahap I menunjukkan adanya pengaruh bahan pencuci fillet
terhadap nilai TPC, TVB dan umur simpan fillet. Bahan pencuci yang
memberikan efek paling paling baik adalah air jeruk yang ditambah garam
dan larutan klorin. Kedua larutan pencuci tersebut dapat mengurangi jumlah
total bakteri paling banyak (TPC paling kecil) pada fillet saat pencucian
sehingga mempengaruhi pertumbuhan bakteri selama penyimpanan.
Sampai hari ke-8 nilai log TPC fillet yang dicuci larutan klorin dan air
garam-jeruk sebesar 5.84 dan 5,06 menunjukkan bahwa fillet masih segar
(batas maksimum 7,6 menurut Ditjen POM) pada hari ke 12 semua fillet telah
melewati batas maksimum.
Penelitian tahap kedua bertujuan mengetahui pengaruh konsentrasi CO
2dalam
modifikasi atmosfir pengemasan (MAP) terhadap kualitas dan umur simpan
fillet ikan gurami yang telah mengalami perlakuan pencucian pada tahap
pertama. Ada delapan perlakuan dari kombinasi dua jenis pencucian (larutan
garam-jeruk/AGJ dan klorin/K)) dan empat konsentrasi CO
2, yaitu (1)
AGJ-CO
20%, (2) AGJ-CO
230%; (3) AGJ- CO
245% (4) AGJ-CO
260%; (5)
K-CO
20%; (6) K- CO
230%; (7) K- CO
245% dan (8) K- CO
260%. Pengamatan
dilakukan terhadap nilai TPC, TVB, pH, dan organoleptik fillet pada hari ke
0, ke-8, ke-14, ke-18, ke-21 dan ke-24 penyimpanan dalam suhu 5
oC yang
dikemas dengan plastik polyetilen. Analisi statistik terhadap hasil pengamatan
dengan one-way Anova dalam RAL pada tiap-tiap pengamatan. Penentuan
umur simpan didasarkan pada persamaan regresi nilai organoleptik fillet.
Hasil penelitian tahap II menunjukkan bahwa konsentrasi CO
2berpengaruh
terhadap nilai TPC, TVB dan organoleptik fillet dalam kemasan plastik
polyetilen yang disimpan pada suhu 5
oC selama 24 hari. Pertumbuhan bakteri
dapat dihambat dengan penambahan konsentrasi CO
2dalam kemasan yang
ditunjukkan oleh nilai TPC dan TVB yang lebih rendah dan nilai
organoleptik lebih tinggi.
berpengaruh pada nilai TVB. Konsentrasi CO2 45% dan 60% pada kedua
jenis pencuci menunjukkan nilai TVB yang rendah, berbeda nyata mulai
penyimpanan ke-14 dan sampai hari ke-18 nilai TVB fillet besarnya 30
mgN/100g.
Nilai organoleptik fillet selama penyimpanan menurun dari 9 pada awal
penyimpanan hingga 1 pada hari ke 24. Konsentarsi CO2 45% pada kedua
bahan pencuci menghasilkan nilai organoleptik paling baik dimana sampai
hari ke-14 masih menunjukkan tingkat kesegaran yang baik (nilai 7).
Berdasarkan analisis regresi untuk menentukan umur simpan fillet dengan
batas penolakan nilai 5 diperoleh umur simpan 16 hari pada CO
245% dan 12
hari filet tanpa CO
2.
Dari hasil penelitaian tahap I dan II dapat disimpulkan bahwa penggunaan
bahan pencuci yang baik adalah air jeruk yang ditambah garam. Bahan
pencuci ini dapat meningkatkan umur simpan fillet hingga 8 hari pada suhu
10
oC dan 12 hari pada suhu 5
oC. Penambahan CO
245% dapat meningkatkan
ABSTRACT
SLAMET SUHARTO.
Handling on Gouramy
(Osphronemous gouramy
Lacepede) Fillet with Modified Atmosphere Packaging
. Supervised by
I WAYAN BUDIASTRA, and JOKO SANTOSO.
The aim of this study is to determine post harvest handling technology of
gouramy fillet (
Osphronemous gouramy
Lacepede) which packed with atmosphere
modification. This study was carried out in two steps. First step is to determine 5
treatments cleaner materials
i.e.
hygienic water cleaning, salt water, lime water, lime
water added with salt and 10 ppm chlorine to produce the best quality of fillet. The
result of this first step showed that salt water added with lime and 10 ppm chlorine
was the best cleaner materials based on the value of log TPC ( 3.75). Second step is
to determine the composition and effect of the packing atmosphere modification to
the Gouramy fillet quality and self life with 4 different composition of CO
2(0, 30, 45
and 60%). Concentration 45% of CO
2was the best gas composition of atmosphere
© Hak cipta milik IPB, tahun 2010
Hak cipta dilindungi
1.
Dilarang mengutip sebagian atau seluruh karya tulis ini tanpa mencantumkan
atau menyebutkan sumber
a.
Pengutipan hanya untuk kepentingan pendidikan, penelitian, penulisan
karya ilmiah, penyusunan laporan, penulisan kritik atau tinjauan suatu
masalah
b.
Pengutipan tidak merugikan kepentingan yang wajar IPB
PENANGANAN FILLET
IKAN GURAMI
(
Osphronemus gouramy
Lacepede)
DALAM KEMASAN MODIFIKASI ATMOSFIR
SLAMET SUHARTO
Tesis
sebagai salah satu syarat untuk memperoleh gelar
Magister Sains pada
Judul Tesis
:
Penanganan Fillet Ikan Gurami (
Osphronemous Gouramy
Lacepede)
dalam Kemasan
Modifikasi
Atmosfer
Nama
: Slamet Suharto
NRP
: P 24500003
Program Studi
: Teknologi Pascapanen
Menyetujui,
1. Komisi Pembimbing
Dr. Ir. I Wayan Budiastra, MAgr
Dr. Ir. Joko Santoso, M.Si
Ketua
Anggota
Mengetahui,
Ketua Program Studi
Dekan Sekolah Pascasarjana
Teknologi Pascapanen
Dr. Ir. I Wayan Budiastra, MAgr Prof. Dr.Ir. Khairil A. Notodiputro, MS
PRAKATA
Puji syukur penulis panjatkan kehadirat Allah SWT atas rahmat dan
karunia-Nya sehingga penulis dapat menyelesaikan penelitian dengan judul Penanganan Fillet
Ikan Gurami (
Osphronemus gouramy
Lacepede) dalam Kemasan Modifikasi
Atmosfir.
Penghargaan dan ucapan terima kasih yang sebesar-besarnya disampaikan
kepada Bapak Dr. Ir. I. Wayan Budiastra, MAgr sebagai ketua komisi pembimbing
sekaligus sebagai Ketua Program Studi Teknologi Pascapanen dan Bapak
Dr.Ir. Joko Santoso, M.Si sebagai anggota komisi pembimbing yang telah
memberikan bimbingan, nasehat, arahan dan dorongan mulai dari penulisan
proposal, selama pelaksanaan penelitian berlangsung sampai selesainya penulisan
tesis ini.
Ucapan terima kasih juga saya sampaikan kepada Rektor Universitas
Diponegoro, Dekan FPIK UNDIP, Departemen Pendidikan dan Kebudayaan
Republik Indonesia melalui Dana Pendidikan BPPS sehingga studi berjalan dengan
lancar. Terima kasih saya sampaikan kepada Kepala Laboratorium Teknik
Pengolahan Pangan dan Hasil Pertanian, Laboratorium Kimia TPG FATETA dan
Laboratorium Mikrobiologi Pusat Studi Sumberdaya Hayati dan Bioteknologi
(PSSHB) IPB atas izin lokasi penelitian, serta Pak Wahid, Mbak Ari, Mbak Sri, Pak
Sulyaden, Pak Wawan, Majid, Hanum, Yosi, Pak Fajar atas bantuannya selama
penelitian. Terima kasih kepada orang tua, adik, kakak, istri dan anak tercinta atas
segala dukungan, doa dan kasih sayangnya.
RIWAYAT HIDUP
Penulis bernama Slamet Suharto dilahirkan di Pekalongan, Jawa Tengah pada
tanggal 8 Juni 1970. Penulis merupakan putera keempat dari delapan bersaudara
pasangan Bapak Khunduri dan ibu Khulsum. Pendidikan Sekolah Dasar ditempuh di
SD Negeri I Api-api Pekalongan, lulus tahun 1983. Sekolah Menengah Pertama
diselesaikan pada tahun 1986 di SMP I Wiradesa Pekalongan, Sekolah Menengah
Atas ditempuh di SMA I Pekalongan Jurusan Biologi lulus tahun 1989.
Pada tahun 1990 penulis melanjutkan di Jurusan Perikanan Fakultas
Perikanan dan Ilmu Kelautan Universitas Diponegoro Semarang dan lulus Strata 1
tahun 1996. Tahun 1999 sampai sekarang, penulis bekerja sebagai staf pengajar di
Fakultas Perikanan dan Ilmu Kelautan Universitas Diponegoro. Pada tahun 2000
penulis melanjutkan pendidikan Strata 2 di Institut Pertanian Bogor pada Program
Studi Teknologi Pascapanen (TPP). Beasiswa pendidikan pascasarjana diperoleh dari
Departemen Pendidikan dan Kebudayaan Republik Indonesia melalui Dana
Pendidikan BPPS. Penulis telah menikah dengan Tri Yusufi Mardiana, MSi dan telah
dikaruniai tiga anak, Hakimah Nur Yusla, Ghatfan Mohammad Atiwiar dan Humam
DAFTAR ISI
Halaman
DAFTAR TABEL ………
xi
DAFTAR GAMBAR ………...
xii
DAFTAR LAMPIRAN ………
xiii
PENDAHULUAN………...
Latar Belakang ……….
1
Tujuan dan Manfaat ……….
4
TINJAUAN PUSTAKA
Ikan Gurami ……….
5
Komposisi Ikan ………
6
Jeruk Nipis ………..……….
7
Garam Dapur ………
8
Klorin ………...
8
Kerusakan Daging Ikan ………
10
Modified Atmosphere Packaging
……….. 14
Pengaruh CO
2terhadap Pertumbuhan Bakteri ………...
14
Film Kemasan Plastik ………..
16
Penentuan Umur Simpan………..
17
BAHAN DAN METODE
Waktu dan Tempat ………...
18
Tahapan Penelitian ………..
18
Prosedur Analisis ……….………
22
Pengaruh Pencucian terhadap Nilai TPC………
29
Pengaruh Pencucian terhadap Nilai TVB……… ….
29
Pengaruh Pencucian terhadap Nilai pH………
31
Umur Simpan Fillet pada 10
oC……… …………..
31
Pengaruh MAP terhadap Nilai TPC……… …
32
Pengaruh MAP terhadap Nilai TVB………
33
Pengaruh MAP terhadap Nilai pH……… …..
34
Nilai Organoleptik Fillet Gurami MAP………
34
Perkiraan Umur Simpan ………
36
SIMPULAN DAN SARAN
Simpulan ………..
39
Saran ………
39
DAFTAR GAMBAR
No
Halaman
1
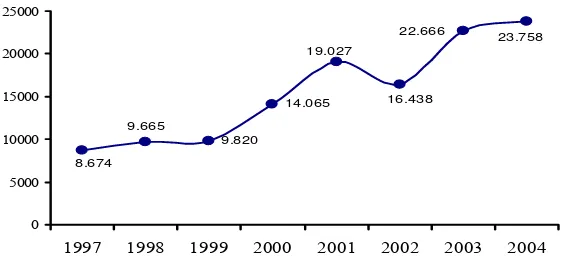
Produksi ikan gurami di Indonesia tahun 1997-2004…………..
3
2
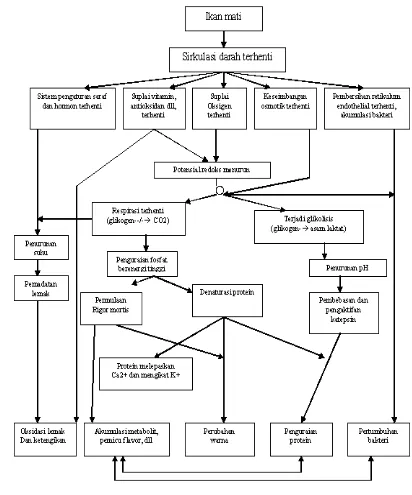
Proses perubahan yang terjadi pada ikan setelah mati…………
12
3
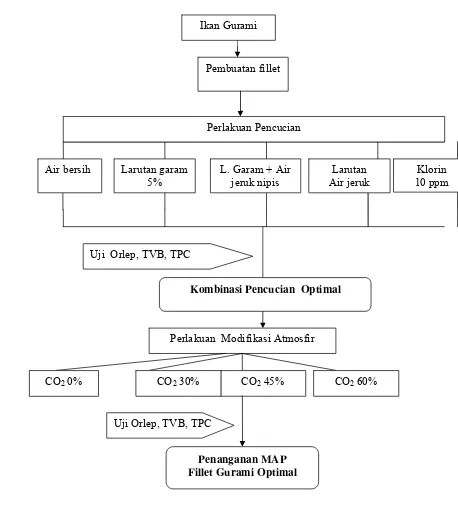
Alur penelitian pencucian dan pengemasan fillet ikan gurami
dalam MAP……….
20
4
Tren penurunan nilai organoleptik fillet gurami MAP selama
penyimpanan 24 hari………
35
5
Fillet dicuci klorin, CO
20%, 18 hari
37
6
Fillet dicuci klorin, CO
245%, 18 hari
37
7
Fillet dicuci klorin, CO
230%, 18 hari
37
8
Fillet dicuci klorin, CO
260%, 18 hari
37
9
Fillet dicuci air garam-jeruk, CO
20%, 18 hari
38
10
Fillet dicuci air garam-jeruk, CO
245%, 18 hari
38
DAFTAR TABEL
No
Halaman
1
Komposisi kimia daging ikan gurami (
Osphronemous gouramy
Lac.) ………..
6
2
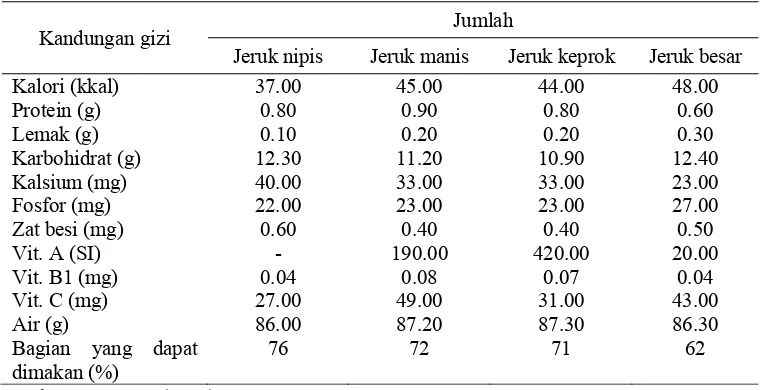
Kandungan gizi dalam tiap 100 g buah jeruk nipis dan beberapa
jenis jeruk lain………..
7
3
Komposisi kimia daging ikan gurami………..
27
4
Nilai log jumlah total bakteri per g fillet pada beberapa
perlakuan pencucian dan penyimpanan pada suhu 10
oC
(rerata±sd, kol/g)………
29
5
Nilai TVB fillet gurami pada beberapa perlakuan pencucian dan
penyimpanan pada suhu 10
oC (rerata±sd, mg/100 g)………
30
6
Nilai pH fillet gurami pada beberapa perlakuan pencucian dan
penyimpanan pada suhu 10
oC (rerata±sd)……….
31
7
Prediksi umur simpan dengan batas TVB maximal 30 mg
N/100g daging ikan ………...
32
8
Nilai log jumlah total bakteri fillet gurami dengan perlakuan
kemasan modifikasi atmosfir yang disimpan pada suhu 5
oC
(rerata±sd)………..
32
9 Nilai TVB fillet ikan gurami dengan perlakuan kemasan
modifikasi atmosfir yang disimpan pada suhu 5
oC (rerata±sd)...
33
10 Nilai pH fillet ikan gurami dengan perlakuan kemasan
modifikasi atmosfir yang disimpan pada suhu 5
oC (rerata±sd)...
34
11 Nilai organoleptik fillet gurami selama penyimpanan 24 hari
dalam kemasan modifikasi atmosfir ………..…………...
35
12 Perkiraan umur simpan fillet dengan persamaan regresi lama
penyimpanan dan skor organoleptik fillet ………
DAFTAR LAMPIRAN
No
Halaman
1
Proporsi air perasan jeruk nipis per buah jeruk ……….
45
2
Perhitungan rendemen fillet gurami ………
46
3
Form penilaian fillet segar ………. ……….
47
4
Data TVB, TPC, pH dan kadar air fillet pada percobaan 1 dan
anova masing-masing lama penyimpanan ………
50
5
Data nilai log TPC fillet gurami dalam MAP dan uji statistik …
57
6
Nilai TVB fillet gurami dalam MAP dan uji statistik…………
61
7
Nilai pH fillet gurami dalam MAP dan uji statistik……….
65
8
Nilai kadar air fillet gurami dalam MAP dan uji statistik………
69
PENDAHULUAN
Latar Belakang
Ikan merupakan bahan makanan yang memiliki nilai gizi tinggi karena
kandungan dan kualitas protein, kelengkapan asam-asam amino esensial,
kandungan kolesterol rendah dan rasanya yang enak. Namun ikan merupakan
bahan pangan yang mudah mengalami kerusakan (highly perishable food)
sehingga memiliki umur simpan yang pendek dan daerah distribusi yang terbatas.
Hasil tangkapan ikan dan invertebrata dunia mencapai 100 juta metrik ton per
tahun, hanya 20% diproses sebagai makanan dan sepertiga yang dikonsumsi,
selebihnya merupakan limbah (Shahidi 1994). Untuk dapat dimanfaatkan dalam
waktu yang lama perlu dilakukan penanganan dan atau pengolahan seperti
pembekuan, pengeringan, dan pengalengan. Akhir-akhir ini terdapat
kecenderungan adanya peningkatan permintaan akan ikan segar.
Sejalan dengan aktivitas manusia yang semakin meningkat, terdapat
kecenderungan konsumsi makanan yang lebih praktis. Konsumen menghendaki
bahan makanan yang segar, berkualitas, praktis, dan mudah penanganan dalam
memasak (ready to cook) atau dikenal dengan minimaly process. Prinsip
minimaly proces yang dikerjakan pada tingkat produksi (on farm) selain untuk
memenuhi kebutuhan trend konsumen juga memiliki keuntungan lain diantaranya
mengurangi limbah organik kota dan pemanfaatan limbah oleh petani. Menurut
Silva dan Dean (2001), diversifikasi bentuk sajian yang menarik dan diikuti oleh
upaya pemasaran intensif pada industri telah meningkatkan konsumsi perkapita
terhadap ikan cat fish dari 0.41 pound menjadi 1.07 pound selama 10 tahun
terakhir di USA.
Pada prinsipnya kesegaran ikan tidak dapat ditingkatkan tetapi masih
dapat dipertahankan untuk jangka waktu tertentu. Teknologi pascapanen
memiliki peranan yang sangat penting dalam mempertahankan kesegaran ikan
untuk waktu yang lebih lama, sehingga dapat mencapai distribusi yang lebih luas.
Salah satu teknologi dalam mempertahankan kesegaran ikan adalah Modified
komposisi gas dalam lingkungan kemasan yang dikombinasikan dengan
penyimpanan pada suhu rendah untuk mempertahankan kesegaran ikan dan
memperpanjang umur simpan. Manfaat lain dari MAP adalah praktis dalam
penanganan (handling), transportasi, menarik konsumen dan memungkinkan
ketersediaan produk secara kontinyu (Pastoriza et al. 1996).
Beberapa peneliti telah melaporkan tentang metode penyimpanan dan
pengemasan dengan sistem atmosfir termodifikasi, diantaranya Brown et al.
(1980), pada ikan rock fish dan salmon menggunakan gas CO2 sebesar 20% dan
40% dibandingkan dengan tanpa gas CO2; Banks et al. (1980), pada fin fish
menggunakan gas CO2 dan tanpa CO2 (vacum); Lannelogue et al. (1982), pada
udang brown shrimp menggunakan campuran gas CO2 dengan O2, CO2 dengan N2
dan CO2 100%; Cann (1988), pada ikan cod menggunakan campuran gas
CO2/N2/O2 dengan perbandingan 40/30/30 persen; dan Silva et al. (1994) pada
fillet ikan cat fish menggunakan campuran gas CO2/N2/O2 dengan perbandingan
90/7,5/2,5 persen. Hampir semua peneliti di atas menyimpulkan, bahwa
penyimpanan ikan segar dengan metode MAP yang menggunakan gas CO2, dapat
memperpanjang umur simpan sekitar 12-15 hari. Menurut Cann (1988), lamanya
umur simpan ikan segar dengan metode MAP dipengaruhi oleh beberapa faktor
yaitu spesies, kualitas awal ikan sebelum disimpan, suhu penyimpanan dan
campuran gas yang digunakan.
Ikan gurami (Osphronemous gouramy Lacepede) merupakan salah satu
jenis ikan yang populer dan banyak digemari bagi masyarakat Indonesia. Ikan ini
sering menjadi menu khusus dalam beberapa restoran dan memiliki harga yang
relatif mahal. Produksi nasional dalam beberapa tahun terakhir mengalami
peningkatan, yaitu 8 674 ton pada tahun 1997 menjadi 23 758 ton pada tahun
3 Gambar 1 Produksi ikan gurami di Indonesia tahun 1997-2004 (dalam ton).
Pada umumnya ikan gurami ukuran konsumsi dipasarkan dalam keadaan
masih hidup. Pemasaran ikan hidup membutuhkan penanganan yang kompleks,
mulai dari transportasi, penyajian, perawatan dan pelayanan. Transportasi ikan
hidup selain membutuhkan penanganan khusus, juga biaya yang tinggi
dikarenakan kapasitas yang terbatas. Ikan gurami juga memiliki daya tahan yang
berbeda dengan ikan lele atau ikan mas yang dapat diangkut dengan kepadatan
lebih tinggi. Penyajian ikan gurami hidup membutuhkan wadah khusus seperti
akuarium dan pelayanan penjualan yang berbeda dengan ikan lain. Hal-hal
tersebut mengakibatkan biaya pemasaran ikan hidup menjadi tinggi dan
mengakibatkan harga jual ditingkat konsumen relatif mahal.
Peningkatan produksi ikan gurami yang tidak disertai perluasan pasar
mengakibatkan harga berfluktuasi sehingga upaya untuk menambah diversifikasi
produk perlu dilakukan untuk memenuhi kebutuhan konsumen yang beragam dan
meningkatkan konsumsi. Perlu diupayakan bentuk sajian ikan gurami segar yang
praktis, mudah dan menarik serta aman diantaranya dengan teknik minimally
process seperti dalam bentuk fillet yang dikemas secara MAP.
Menurut Phillips (1996) teknik MAP yang dikombinasi dengan prosedur
dekontaminasi seperti penggunaan trisodium fosfat, larutan buffer asam
laktat/sodium laktat atau teknik irradiasi pada daging dan ikan dapat
meningkatkan umur simpan dan secara mikrobiologis aman. Penggunaan bahan
kimia seperti klorin sebagai bahan pencuci untuk mengurangi/menghilangkan
9.820
14.065 19.027
16.438
22.666 23.758
9.665
8.674
0 5000 10000 15000 20000 25000
kontaminasi sejauh ini masih digunakan sampai batas diperbolehkan. Namun
kebutuhan untuk menyediakan makanan yang sehat dan aman menuntut pencarian
bahan organik sebagai alternatif bahan pencuci fillet. Secara tradisional perasan
air jeruk nipis digunakan sebagai materi penghilang bau amis pada ikan sebelum
dimasak.
Dalam penelitian akan digunakan larutan air jeruk nipis, garam, klorin dan
air bersih sebagai bahan pencuci fillet ikan gurami yang dikemas dengan teknik
MAP.
Tujuan dan Manfaat
Penelitian ini bertujuan untuk menentukan teknologi penanganan
pascapanen yang paling optimal pada pengemasan fillet ikan gurami secara MAP
dengan mengetahui bahan pencucian fillet, konsentrasi gas CO2 yang optimal dan
umur simpan fillet. Hasil penelitian ini diharapkan bermanfaat sebagai informasi
5
TINJAUAN PUSTAKA
Ikan Gurami
Sistematika ikan gurami (Osphronemus gouramy Lacepede) menurut
Saanin (1984) adalah sebagai berikut :
Filum : Chordata
Kelas : Pisces
Bangsa : Labirinthici
Subbangsa : Anabantoidei
Suku : Anabantidae
Marga : Osphronemus
Jenis : Osphronemus gouramy Lacepede
Gurami memiliki bentuk fisik yang khas, badannya pipih, agak panjang
dan lebar. Badan tertutup sisik yang kuat dengan tepi agak kasar. Mulutnya kecil,
letaknya miring, tidak tepat di bawah ujung moncong. Bibir bawah terlihat
menonjok sedikit dibanding bibir atas. Ujung mulut dapat disumbulkan sehingga
nampak monyong. Bentuk kepala gurami akan menjadi tumpul bila sudah besar
dan jantan yang sudah tua terdapat tonjolan seperti cula. Punggungnya tinggi dan
mempunyai sirip perut dengan jari-jari yang sudah berubah menjadi alat peraba.
Badan gurami pada umumnya berwarna biru kehitaman dan bagian perut
berwarna putih. Warna tersebut akan berubah menjelang dewasa yaitu pada
bagian punggung berwarna kecoklatan dan pada bagian perut berwarna keperakan
atau kekuningan. Ujung sirip punggung dan sirip dubur dapat mencapai pangkal
ekor. Sirip berbentuk busur. (Saanin 1984).
Gurami dapat tumbuh hingga 65 cm dan berat lebih dari 10 kg. Di Jawa
ikan ini dikenal dengan nama gurami, grameh atau brami, sedangkan di Sumatera
dan Kalimantan gurami dikenal dengan nama kalui, sialui, kalua, kalau dan kalwe
Komposisi Ikan
Ikan mempunyai komposisi kimia yang bervariasi baik antar spesies, antar
individu dalam satu spesies yang sama dan bahkan antar bagian dalam satu
individu ikan. Menurut Stansby (1963), variasi tersebut disebabkan karena
pengaruh beberapa faktor antara lain umur, laju metabolisme dan aktivitas
pergerakannya. Disamping faktor-faktor di atas menurut Spinelli dan Dassow
(1982), variasi tersebut juga dipengaruhi oleh musim, lokasi penangkapan dan
tingkat kematangan seksual ikan.
Ikan sebagai sumber protein hewani, mempunyai nilai gizi yang tinggi.
Hal ini disebabkan karena kandungan proteinnya yang cukup, baik jumlah
maupun mutunya; kandungan kolesterolnya yang rendah; lemak ikan mengandung
asam lemak tak jenuh; minyak ikan merupakan sumber vitamin A dan juga
mengandung vitamin B, C, D, E dan K; ikan mengandung mineral-mineral dengan
kadar yang tinggi; dan daging ikan mempunyai sedikit tenunan pengikat sehingga
mudah dicerna (Winarno 1993).
Menurut Winarno (1993), protein hewani disebut juga sebagai protein
lengkap dan bermutu tinggi, karena mengandung semua asam-asam amino
essensial dalam jumlah cukup dan susunannya mendekati sususnan asam amino
yang terdapat dalam tubuh manusia. Komposisi daging ikan secara umum terdiri
dari air sebesar 60-80%, protein 18-30%, lemak 0.1-2.2%, karbohidrat (glikogen)
0.0-1.0% dan sisanya adalah vitamin dan mineral (Afrianto dan Liviawaty 1989).
Adapun komposisi kimia daging ikan gurami disajikan pada Tabel 1.
Tabel 1 Komposisi kimia daging ikan gurami (Osphronemous gouramy Lac.)
Unsur Gizi Persentase Basis Basah
Kadar air 76 %
Kadar abu 5.28 %
Protein 78.04 % bk
Lemak 7.90 % bk
7
Jeruk Nipis
Jeruk nipis (Citus aurantifolia Swingle) atau sering disebut jeruk mipis
(Sunda), jeruk pecel (Jawa) dan jeruk dhurga (Madura) merupakan jenis jeruk
yang banyak mengandung air, rasanya sangat masam dan aromanya sedap
(Sarwono 2001). Jeruk memiliki kandungan gizi yang baik dan mengandung zat
bioflavonoid yang berguna untuk mencegah terjadinya perdarahan pada pembuluh
nadi, kemunduran mental dan fisik serta mengurangi luka memar (brueise).
Jeruk nipis sering digunakan sebagai komponen jamu tradisional, pencampur
berbagai bahan masakan dan digunakan untuk menghilangkan bau amis ikan.
Pada Tabel 2. disajikan kandungan gizi beberapa jenis jeruk.
Tabel 2 Kandungan gizi dalam tiap 100 gram buah jeruk nipis dan beberapa jenis jeruk lain
Kandungan gizi Jumlah
Jeruk nipis Jeruk manis Jeruk keprok Jeruk besar
Kalori (kkal) 37.00 45.00 44.00 48.00
Protein (g) 0.80 0.90 0.80 0.60
Lemak (g) 0.10 0.20 0.20 0.30
Karbohidrat (g) 12.30 11.20 10.90 12.40
Kalsium (mg) 40.00 33.00 33.00 23.00
Fosfor (mg) 22.00 23.00 23.00 27.00
Zat besi (mg) 0.60 0.40 0.40 0.50
Vit. A (SI) - 190.00 420.00 20.00
Vit. B1 (mg) 0.04 0.08 0.07 0.04
Vit. C (mg) 27.00 49.00 31.00 43.00
Air (g) 86.00 87.20 87.30 86.30
Bagian yang dapat dimakan (%)
76 72 71 62
Sumber : Sarwono (2001)
Selain kandungan gizi yang baik jeruk nipis merupakan sumber minyak
atsiri “lemonen” dan asam sitrat. Kandungan asam sitrat pada jeruk nipis
mencapai 6-7% (Sarwono 2001). Asam sitrat merupakan suatu “sekuestran” (zat
pengikat logam) yang paling sering digunakan dalam bahan makanan selain fosfat
dan garam etilen diamine tetra asetat (EDTA) (Winarno 1997). Lebih lanjut
mengikat logam dalam bentuk ikatan kompleks sehingga mampu mengalahkan
sifat dan pengaruh jelek logam tersebut terhadap bahan.
Logam terdapat pada bahan alami dalam bentuk senyawa komplek
misalnya Mg pada klorofil; Fe pada ferritin, rofin, porfirin serta haemoglobin; Co
pada vitamin B12; Cu, Zn dan Mn dalam berbagai enzim. Ion-ion logam ini dapat
terlepas dari ikatan kompleksnya karena hidrolisis maupun degradasi. Ion logam
bebas mudah bereaksi mengakibatkan perubahan warna, ketengikan, maupun
perubahan rasa. Sekuestran akan mengikat ion logam sehingga menjaga
kestabilan bahan, dari perubahan warna, rasa dan tekstur.
Garam Dapur
Garam dikenal sebagai bahan pengawet paling tua, terutama dalam
pembuatan ikan asin (Hadiwiyoto 1993). Penggunaan garam disebabkan garam
memiliki sifat-sifat sebagai berikut: (1) garam dapur dapat menyebabkan
berkurangnya jumlah air dalam daging sehingga kadar air dan aktivitas air
menjadi rendah, (2) menyebabkan protein daging dan protein mikroba
terdenaturasi, (3) menyebabkan sel-sel mikroba menjadi lisis karena perubahan
tekanan osmosis, dan (4) ion klorida yang terdapat dalam garam dapur
mempunyai daya toksisitas yang tinggi pada mikroba dan dapat memblokir sistem
respirasi.
Penggunaan garam dapur dalam penanganan ikan segar telah banyak
digunakan terutama dalam pembuatan es air garam, es air laut maupun air garam
yang didinginkan. Selain karena sifat bakteriostatisnya, garam juga menyebabkan
suhu yang dihasilkan lebih rendah dibanding air murni. Penggunanan air garam
juga lazim digunakan untuk pencucian udang maupun ikan segar sebelum
9
Klorin
Klorin sering digunakan sebagai saniter di perusahaan-perusahaan
perikanan (Ilyas 1983). Pemakaian klorin bertujuan untuk mengurangi jumlah
bakteri yang ada pada bahan karena sifat antimikroba dari klor. Suparno (1992)
menyarankan perendaman 100 ppm selama 5-10 menit untuk mengurangi jumlah
bakteri pada udang windu yang akan dibekukan.
Menurut Wijayanti (1999) mekanisme klorin sebagai sanitizer yang
diharapkan dapat membunuh bakteri belum sepenuhnya diketahui. Namun diduga
asam hipoklorit (HOCl) yang merupakan senyawa paling aktif akan menghambat
oksidasi glukosa dalam sel mikroorganisme, dengan cara menghambat
enzim-enzim yang yang terlibat dalam metabolisme karbohidrat.
Klorin cair (Cl2) atau natrium hipoklorit (NaOCl) dalam air akan
terhidrolisis membentuk asam hipoklorit (HOCl). Selanjutnya asam hipoklorit
akan terdisosiasi membentuk ion hidrogen (H+) dan ion hipoklrorit (OCl-)
menurut reaksi berikut :
Cl-2 + H2OÆ HOCl + H+ + Cl-
NaOCl + H2O Æ NaOH + HOCl
HOCl Æ H+ + OCl
Asam hipoklorit akan merusak membran sel kemudian mengoksidasi
kelompok sulfidril dalam protein sehingga menyebabkan inaktivasi enzim. Klorin
juga merusak lapisan pelindung spora bakteri (Garbut 1997).
Menurut Winarno (1994) klorin dalam larutan membentuk senyawa HOCl
(asam hipoklorit) yang berfungsi sebagai senyawa aktif dan bekerja membunuh
dan menghancurkan bakteri. Pembentukan HOCl sangat tergantung pada pH.
Pada pH 4.0-5.0, HOCl terbentuk secara maksimal. Kurang atau lebih dari pH
tersebut, pembentukan HOCl menurun, demikian pula efektivitasnya. Dari segi
lain, pada pH kurang dari 5, larutan klorin bersifat sangat korosif. Agar tidak
korosif tetapi daya bunuhnya masih tetap tinggi, larutan dijaga agar berada pada
pH 6.0-7.5. Natrium dan kalsium hipoklorida akan meningkatkan pH larutan.
pH larutan tersebut yang mengakibatkan sanitizer semakin tidak efektif, karena
HOCl yang diproduksi semakin sedikit. Bila air yang digunakan bersifat basa,
harus ditambahkan asam agar menjaga agar pH larutan berada pada kisaran
6.5-7.0 (Winarno 1994).
Air yang digunakan sebagai bahan penolong dalam pengolahan ikan harus
memenuhi persyaratan kualitas air minum. Air yang digunakan dalam pencucian
ikan dapat ditambahkan klorin dengan kadar yang tidak melebihi 10 ppm. Selain
klorin juga dapat dilakukan dengan cara lain yang dapat digunakan untuk
meningkatkan kualitas air dalam pencucian (Kep. 01/Men/2002). Akan tetapi
penggunaaan klorin secara terus-menerus dapat menyebabkan iritasi pada kulit
(Snyder 2004).
Kerusakan Daging Ikan
Ikan merupakan bahan makanan yang mudah rusak (perishable food), hal
ini disebabkan kandungan glikogen yang rendah (Winarno 1993). Menurut
Frazier (1967) setelah ikan mati, perubahan mula-mula ialah ikan mengalami
rigor mortis, yaitu proses dimana ikan mengalami kejang, kaku dan mengeras,
selanjutnya terjadi proses autolisis yang menyebabkan sebagian cairan daging
keluar dari sel dan ini merupakan substrat yang baik bagi pertumbuhan bakteri.
Menurut Eskin (1990) suatu rangkaian reaksi biokimia dan fisikokimia
terjadi pada saat ikan mati hingga sampai dikonsumsi sebagai edible fish
Periode ini dibedakan menjadi 3 tahap, yaitu:
1. Kondisi prerigor, pada saat jaringan masih lembut dan plieble dengan sifat
kimia seperti turunnya ATP dan kreatin fosfat sebagai aktivitas glikolisis.
Glikolisis pascamati menghasilkan perubahan glikogen menjadi asam
laktat, sehingga pH turun. Banyaknya perubahan pH bervariasi dari satu
spesies dengan spesies lain, demikian juga jenis ototnya. Pada hewan
yang well-rested memiliki cadangan glikogen yang besar sehingga
11 2. Perkembangan selanjutnya ialah kondisi kejang dan kaku pada otot, yang
secara umum dikenal sebagai rigor mortis. Kejadian ini diikuti dengan
turunnya pH dan dikaitkan dengan formasi aktomiosin. Hilangnya
ekstensibilitas berkaitan dengan formasi aktomiosin menghasilkan slowly
of first dan kemudian extremly rapidly. Secara normal awal dari rigor
mortis terjadi 1-12 jam pascamati dan bisa berakhir antara 15-20 jam pada
mamalia, bergantung beberapa faktor yang mempengaruhinya. Pada ikan
rigor mortis terjadi lebih singkat sekitar 1-7 jam pascamati dengan
beberapa faktor yang mempengaruhi durasinya.
3. Postrigor, setelah rigor mortis berakhir, maka terjadi tingkat post rigor
yaitu kembali melunaknya tekstur daging ikan. Tingkat postrigor
nerupakan permulaan dari proses pembusukan yang meliputi autolisis,
pembusukan oleh bakteri, dan ketengikan. Tingkat postrigor ditandai
dengan adanya amoniak pada proses autolisis. Proses ini menyebabkan
terjadinya penguraian protein menjadi senyawa yang lebih sederhana,
yaitu polipeptida, asam amino dan amoniak yang dapat meningkatkan pH
jaringan ikan. Keadaan basa, adanya hasil pemecahan protein, lemak dan
karbohidrat merupakan media yang baik untuk pertumbuhan bakteri.
selanjutnya ikan akan mengalami kerusakan hingga mengalami
kebusukan. Proses perubahan biokimiawi dari awal hingga busuk
diuraikan secara skematis oleh Eskin (1990) seperti disajikan pada
Gambar 2.
Menurut Hadiwiyoto (1993) kerusakan ikan terjadi secara biokimiawi dan
mikrobiologis. Kerusakan biokimiawi dilakukan oleh enzim-enzim dalam tubuh
ikan yang masih aktif walaupun ikan telah mati namun berubah fungsi menjadi
perusak. Enzim akan menguraikan senyawa makromolekul menjadi
senyawa-senyawa lebih sederhana sampai akhirnya akan terbentuk senyawa-senyawa yang mudah
Gambar 2 Proses perubahan yang terjadi pada ikan setelah mati (Eskin 1990).
Kerusakan mikrobiologis disebabkan oleh aktivitas bakteri. Daging ikan
13 langsung dapat digunakan oleh bakteri. Proses autolisis daging akan membantu
menyediakan senyawa sederhana yang segera dapat dipakai mikroba. Mikroba
juga memproduksi enzim-enzim pengurai untuk mempercepat mendapatkan
senyawa sederhana. Dengan demikian proses autolisis dan aktivitas mikroflora
bersifat sinergis dalam proses kerusakan daging ikan Hadiwiyoto (1993).
Pada tubuh ikan terdapat berjuta-juta bakteri dan mikroorganisme lain.
Konsentrasi bakteri terutama terdapat pada selaput lendir permukaan tubuh ikan,
insang, dan isi perut atau usus (Burgess et al. 1967; Shewan 1961). Pada
dasarnya daging ikan tidak mengandung bakteri. Kepadatan bakteri pada
permukaan tubuh ikan sekitar 102-107 sel/cm2 dan cairan isi perut 103-108 sel/cm3
serta 103- 107 sel/gram jaringan insang. Diantara bakteri-bakteri yang ditemukan
antara lain Pseudomonas, Vibrio, dan Mycobacterium spp, diantaranya bersifat
patogen Hadiwiyoto (1993).
Menurut Graikoski (1973) dari hasil isolasi bakteri pada insang, saluran
pencernaan dan lendir kulit ikan ternyata Pseudomonas sp meliputi 60% dari
jumlah total mikroba, dan sekitar 20% terdiri dari Corynebacterium sp,
Flavobacterium sp, dan Micrococus sp. Sisanya terdiri dari campuran spesies
Alcaligenes, Proteus, Serratia dan Escherichia. Lebih jauh dijelaskan bahwa
komposisi dan konsentrasi bakteri tergantung dari kebiasaan makan ikan dan jenis
makanan yang dicerna. Disamping itu dipengaruhi oleh tempat/ lingkungan
dimana ikan tersebut ditangkap.
Frazier (1967) menyatakan bahwa jenis-jenis mikroba yang menyebabkan
pembusukan pada ikan bervariasi menurut suhu penanganan ikan tersebut. Pada
umumnya jenis psikrofilik dari spesies Pseudomonas lebih dominan, diikuti
spesies Achromobacter dan Flavobacterium, sedangkan pada suhu tinggi adalah
genus Micrococcus dan Bacillus.
Modified Atmosphere Packaging
Menurut Garthwaite (1995) pada awal 1930-an ditemukan bahwa
Pseudomonas spp dan organisme pembusuk lain pada penyimpanan dingin di
bawah 4 oC. Efek fisiologis dari CO2 ini digunakan dalam teknologi ikan untuk
mengontrol pertumbuhan Pseudomonas spp dalam pendinginan ikan dan hasilnya
dapat memperpanjang umur simpan produk ikan dingin.
Pengemasan ikan dengan komposisi atmosfir khusus dapat
memperpanjang umur simpan hingga 30% jika suhu penyimpanan dipertahankan
di bawah 2 oC Komposisi utama dari atmosfir kemasan adalah CO2, O2 dan N2.
Kemasan dengan merubah komposisi atmosfir ada dua jenis yaitu Controlled
Atmosphere Packaging (CAP) dan Modified Atmosphere Packaging (MAP).
Sistem Modified Atmosfer Packaging dilakukan dengan cara memasukkan ikan
kedalam kantong plastik (kemasan) kemudian dimasuki campuran gas sebelum
di-sealing. Plastik yang digunakan memiliki permiabilitas rendah terhadap gas
yang digunakan (Garthwaite 1995).
Pengaruh CO2 terhadap Pertumbuhan Bakteri
Mekanisme bagaimana CO2 dapat mempengaruhi pertumbuhan bakteri,
belum ada penjelasan secara sempurna. Namun pengaruh MAP secara
keseluruhan dapat menekan pertumbuhan bakteri pada lag fase yang akan
meningkatkan umur simpan produk hasil perikanan sekitar 50 –100% (Statham
1984).
Menurut Banks et al. (1980), ada dua teori yang dapat menjelaskan
mengapa CO2 dapat menghambat pertumbuhan bakteri. Teori pertama
menyatakan bahwa dalam tubuh ikan terjadi reaksi antara CO2 dengan air (H2O)
dari produk. Reaksi ini menghasilkan asam karbonat dan ion hidrogen, menurut
reaksi sebagai berikut :
CO2 + H2O Æ H2CO3 Æ H+ + HCO3
Dengan adanya reaksi tersebut akan menyebabkan pH tubuh ikan rendah.
Keadaan ini akan mempengaruhi kehidupan mikroorganisme yang sensitif
15 Bakteri-bakteri pembusuk umumnya adalah sensitif terhadap keadaan asam (pH
rendah), sehinga perlakuan CO2 akan menghambat pertumbuhannya.
Teori yang kedua, adalah bahwa CO2 mempengaruhi enzim spesifik yang
terdapat pada bakteri, dimana konsentrasi CO2 yang tinggi akan menghambat
aktivitas metabolisme bakteri yang menyebabkan pertumbuhannya menjadi
terganggu. Bakteri Gram negatif yang merupakan bakteri pembusuk pada ikan
segar (seperti Pseudomonas spp) lebih sensitif terhadap CO2 dibandingkan
dengan bakteri Gram positif (seperti Lactobacillus sp).
Sistem penyimpanan modifikasi atmosfir dengan CO2 tinggi dapat
merubah distribusi bakteri Gram positif dan Gram negatif. Flora ikan yang
dikemas dengan tanpa CO2 didominasi oleh bakteri Gram negatif yang bersifat
pembusuk dan sebaliknya ikan yang dikemas dengan CO2 didominasi oleh bakteri
Gram positif.
Menurut Lannelongue et al. (1982) tingkat konsentrasi CO2 tinggi bersifat
bakterisidal pada flora awal, sehingga dapat memperpanjang masa lag fase sekitar
6-10 hari pada brown shrimp dan fresh water crayfish (Wang dan Brown 1983).
Kemungkinan lain terganggunya pertumbuhan bakteri pada perlakuan CO2
adalah karena berkurangnya jumlah O2 dari kondisi normal. Keadaan ini tidak
sesuai dengan syarat pertumbuhan bakteri aerob sempurna (obligat aerobic), yang
mengakibatkan bakteri tersebut akan mati atau terganggu pertumbuhannya (Roger
et al. 1984).
Film Kemasan Plastik
Sistem MAP membutuhkan jenis kemasan yang spesifik untuk menjaga
agar komposisi atmosfir dalam kemasan yang ditentukan pada awalnya tidak
mengalami perubahan selama penyimpanan. Beberapa syarat yang perlu
diperhatikan dalam memilih bahan kemasan yaitu: bahan kemasan tidak
mengandung bahan kimia yang dapat bereaksi dengan produk atau zat yang
bersifat beracun bagi konsumen, sifat permiabilitas plastik diketahui, bentuk dan
ukuran kemasan disesuaikan dengan cara penanganan dan biaya kemasan
Menurut Sacharow dan Griffin (1980) film plastik yang banyak digunakan
dalam kemasan produk-produk segar adalah Polyethylene (PE), Oriented
Polypropylene (OPP) dan Polyvinylchlorida (PVC). Steck (1991) menyatakan
bahwa pengemasan produk ikan segar dengan MAP sebaiknya menggunakan
plastik yang agak kaku (semirigid) dan film yang transparan sehingga produk
mudah dilihat tanpa membuka kemasannya. Ia menyarankan penggunaan plastik
PVC atau HDPE.
Weathon dan Lawson (1985) menyarankan penggunaan bahan kemasan
dengan permiabilitas terhadap O2 sekitar 5 cc/m2/24 jam/atm pada suhu 25 oC.
Scott et al. (1984) menggunakan film dengan permiabilitas 20 cc/m2/24 jam/atm
pada suhu 25 oC untuk MAP fillet ikan snapper, sedangkan Lannelongue et al.
(1982) menggunakan plastik PVC dan LDPE dengan permiabilitas terhadap O2
berturut-turut 7.75 dan 8.06 serta terhadap CO2 37.20 dan 13.18 cc/m2/24/atm
pada 25 oC.
Pada pengemasan produk perikanan dengan modifikasi atmosfir umumnya
menggunakan tiga bentuk kemasan, yaitu kemasan dalam bentuk besar (bulk),
kemasan induk (master pack) dan kemasan eceran (retail pack). Diantara ketiga
cara tersebut cara eceran adalah yang banyak digunakan (Cann 1988).
Penyusunan produk dalam kemasan perlu dihindari pelapisan produk untuk
mendapatkan kontak dengan CO2 yang lebih baik.
Penentuan Umur Simpan
Umur simpan produk pangan merupakan selang waktu antara saat
produksi hingga komsumsi dimana produk berada dalam kondisi yang
memuaskan pada sifat-sifat penampakan, rasa, aroma, tekstur dan nilai gizi atau
secara umum produk masih dapat diterima sesuai tujuan konsumen (IFT 1974).
Umur simpan juga berarti waktu yang diperlukan dalam kondisi peyimpanan,
untuk mencapai tingkat degradasi mutu tertentu (Floros dan Gnanasekharan
17
(ESS) dan Accelerated Storage Study (ASS). ESS atau disebut juga metode
konvensional dilakukan dengan cara menyimpan produk pada kondisi normal
sehari-hari sambil dilakukan pengamatan terhadap penurunan mutunya (usable
quality) hingga mencapai tingkat mutu kadaluarsa. ASS digunakan untuk produk
yang umur simpannya lebih panjang dengan cara menggunakan suatu kondisi
lingkungan yang dapat mempercepat reaksi deteriorasi produk pangan metode
konvensional banyak digunkan untuk produk pangan yang umur simpanya kurang
dari 3 bulan, sedangkan produk pangan yang umur simpannya lebih dari 3 bulan
METODE PENELITIAN
Waktu dan Tempat
Penelitian dilakukan mulai bulan Maret-Nopember 2005, di Kolam
Babakan Sawah Baru FPIK IPB; Laboratorium Teknik Pengolahan Pangan dan
Hasil Pertanian; Laboratorium Kimia TPG FATETA dan Laboratorium
Mikrobiologi Pusat Studi Sumberdaya Hayati dan Bioteknologi (PSSHB) IPB.
Tahapan Penelitian
Penelitian dilakukan dua tahap, tahap pertama bertujuan untuk
menentukan bahan pencuci yang baik berdasarkan nilai parameter signifikan.
Tahap II bertujuan untuk menentukan komposisi atmosfer yang menghasilkan
kualitas fillet terbaik atau umur simpan tertinggi. Secara skematis disajikan pada
Gambar 3.
Pembuatan fillet
Ikan yang dibuat fillet ialah ikan gurami yang diperoleh dari Kolam
Babakan Sawah Baru dengan berat 800-1200 g. Sebelum dibuat fillet dilakukan
pemberokan (ikan dipuasakan), yang bertujuan untuk mengurangi bau lumpur dan
meningkatkan konsistensi dari daging ikan gurami yang dihasilkan.
Pemberokan dilakukan dengan cara ikan ditampung dalam bak ukuran
2,5x2x0,6 m3 dengan air jernih yang dibuat mengalir dan diberi aerasi. Lama
pemberokan 3 sampai 5 hari. Selama pemberokan tersebut ikan tidak diberi
pakan, baik pelet maupun daun talas (Khaeruman dan Amri 2003; Tanudi 2003).
Pembuatan fillet dilakukan dengan prosedur (SNI 01-4103.2-1992)
sebagai berikut :
1. Pelumpuhan
Ikan gurami hidup yang diambil dari bak pemberokan dilakukan
19 banyak bergerak/ menggelepar, selain memudahkan dalam penanganan
juga menghindari timbunan asam laktat pada daging ikan.
2. Pembuangan darah
Pembuangan darah dilakukan dengan cara memotong pembuluh darah
pada insang, belakang sirip dada insang dan pangkal ekornya (Junianto
2003).
3. Penampungan sementara
Sebelum proses lebih lanjut maka ikan ditampung dalam keranjang
dengan mencampurkan es 1:1. Diusahakan ikan tidak terendam dalam
air.
4. Pemotongan/ penyayatan
Sebelum ikan difillet, maka terlebih dahulu dilakukan pemotongan
kepala dan pembuangan isi perut. Selanjutnya dilakukan pemfilletan
dengan cara penyayatan yang dimulai dari punggung mengarah ke perut
dan ekor, sehingga didapat kepingan daging dari dua sisi tanpa terikut
tulang.
5. Pembuangan kulit dan duri
Untuk fillet gurami tanpa kulit maka, kulit dipisahkan dari daging
dengan pisau tajam dan diusahakan tidak melukai/merusak daging.
Selanjutnya dilakukan pembuangan duri dengan menggunakan pisau
kecil atau pinset.
6. Perapihan
Perapihan fillet dilakukan dengan cara membuang/menyayat daging
perut yang masih tersisa pada fillet dan membuang lapisan daging
bagian tepi fillet agar rapi dan bersih.
Fillet ikan gurami tanpa kulit yang terbentuk siap digunakan dalam
percobaan tahap I. Pada tahap ini dilakukan pengamatan secara visual untuk
Gambar 3 Alur penelitian pencucian dan pengemasan fillet ikan gurami dalam
MAP.
Pembuatan fillet
Perlakuan Modifikasi Atmosfir
CO2 45% CO2 60%
CO2 30%
Penanganan MAP Fillet Gurami Optimal
Uji Orlep, TVB, TPC
Kombinasi Pencucian Optimal
Uji Orlep, TVB, TPC
Ikan Gurami
Air bersih Larutan garam
5%
Larutan Air jeruk
Klorin 10 ppm L. Garam + Air
jeruk nipis Perlakuan Pencucian
21
Percobaan I. Penentuan Bahan Pencuci Fillet
Percobaan tahap I bertujuan untuk mengetahui teknik dan bahan
pencucian fillet ikan gurami yang optimal. Dalam percobaan ini dibuat lima
perlakuan, yaitu :
1. Pencucian dengan air bersih,
2. Pencucian air garam 5 %,
3. Pencucian larutan air jeruk,
4. Larutan air jeruk dan garam,
5. Larutan klorin 10 ppm.
Bahan-bahan pencuci adalah sebagai berikut, air bersih adalah air dengan
kualitas air minum (SNI 01-4103.2-1992). Larutan garam yang digunakan dibuat
dengan cara melarutkan 50 g garam dapur/meja merk Berlian kedalam 1 l air
bersih. Larutan jeruk nipis dibuat dengan cara melarutkan air perasan jeruk nipis
sebanyak 60 ml ke dalam 1 l air setara dengan 1 buah, ukuran 50 g (Lampiran 1).
Larutan jeruk ini memiliki pH 2-4. Jeruk nipis (Citrus aurantifolia) yang
digunakan diperoleh dari kebun Agroteko Bogor. Jeruk dipilih yang sudah tua,
tetapi belum matang, disimpan 3 hari setelah dipetik dari pohon. Larutan klorin
10 ppm dibuat dengan cara melarutkan 10 g kaporit merk Ciwi Kimia ke dalam 1
l air. Air yang digunakan untuk bahan pencucian terlebih dahulu dibuat dingin
dengan cara mencampur air dengan es batu, hingga kira-kira suhunya 10 oC .
Pencucian Fillet
Pencucian fillet dilakukan sebanyak 4 kali, yaitu: dua kali pencucian
sesuai perlakuan dan pembilasan dengan air bersih. Adapun cara pencucian
tersebut adalah:
1. Pencucian 1
Fillet dikelompokkan menjadi lima, masing-masing dicuci menurut perlakuan
1, 2, 3, 4 dan 5. Pencucian dilakukan dengan membersihkan secara hati-hati
dari permukaan fillet. Fillet yang telah dicuci (1) diletakkan dalam wadah
yang bersih.
2. Pembilasan
Fillet yang telah dicuci kemudian dibilas dengan air bersih, hingga aroma
bahan pencuci dan bau amis berkurang/hilang. Fillet kemudian diletakkan
kembali dalam wadah yang bersih.
3. Pencucian ke-2
Fillet yang telah dibilas diulangi dicuci dengan cara yang sama, seperti
pencucian ke-1 dan diletakkan dalam wadah yang bersih.
4. Pembilasan
Setelah pencucian ke-2, fillet kemudian dibilas dengan air bersih.
Fillet yang sudah dilakukan perlakuan pencucian diletakkan dalam wadah
(box) plastik berukuran 0.5 l secara individu, kemudian disimpan dalam lemari
dingin suhu 10 oC. Selanjutnya dilakukan pengamatan terhadap pH, TPC (Total
Plate Count), TVB (Total Volatile Base) dan pengamatan indrawi (penampakan,
tekstur, dan bau) pada hari ke-0, 4, 8 dan 12.
Percobaan II. Penyimpanan dalam MAP
Hasil dari percobaan I berupa bahan pencucian fillet terpilih (dalam hal ini
digunakan 2 bahan) kemudian dipakai untuk penanganan fillet pada percobaan II.
Penentuan bahan terbaik didasarkan pada nilai parameter TVB, TPC dan
pengamatan visual serta umur simpan terbaik.
Percobaan II bertujuan untuk menentukan komposisi gas MAP yang
terbaik dan mengetahui umur simpan fillet. Perlakuan percobaan terdiri atas
pencucian dengan dua jenis bahan pencuci yang terpilih sebagaimana hasil
percobaan I, dikombinasikan dengan perlakuan kemasan MAP. Perlakuan MAP
terdiri atas penambahan gas CO2 pada konsentrasi : 0, 30, 45 dan 60%,
sedangkan lama penyimpanan ialah hari ke-0, 7, 14, 21 dan 24. Fillet kemasan
23
Prosedur Analisis
Adapun penentuan nilai parameter yang diamati adalah sebagai berikut :
1. Penentuan Total Volatil Bases (TVB) (Lembaga Penelitian Perikanan 1974)
Prinsip dari pengamatan ini adalah menguapkan senyawa-senyawa volatil
basa (amoniak, mono-,di- dan tri metilamin dan lain-lain) yang terdapat dalam
ekstrak daging ikan yang bersifat basa, pada suhu 35 oC selama dua jam atau pada
suhu kamar selama satu malam. Senyawa-senyawa tersebut akan diikat oleh asam
borat dan kemudian dititrasi dengan larutan N/70.
Peralatan yang digunakan adalah timbangan analitik, erlenmeyer 250 ml,
corong, cawan conway, kertas saring, gelas ukur, pipet ukur, buret 2 ml, magnetik
stirer dan inkubator. Bahan kimia yang digunakan adalah larutan borat, larutan
campuran dari satu bagian volume 0.1% metil merah alkohol, larutan 7%
Trichloroacetic Acid (TCA), larutan 40% formalin dan vaselin.
Prosedur kerjanya, mula-mula ditimbang sebanyak 25 g sampel contoh
ikan yang telah dirajang halus dan dimasukkan ke dalam gelas plastik, lalu
diblender bersama dengan 75 ml larutan TCA 7% dan disaring sampai diperoleh
filtrat contoh. Selanjutnya dipipet 1 ml filtrat yang telah diperoleh di atas ke
dalam bagian outer chamber dan cawan conway ditutup pada posisi hampir
menutup. Kemudian ditambahkan 1 ml larutan kalium karbonat jenuh ke dalam
outer chamber yang berlawanan, dan 1 ml asam borat ke dalam inner chamber,
Selanjutnya cawan conway ditutup rapat (air tighr) dengan cara mengolesi
pinggirnya dengan vaselin.
Disamping itu dikerjakan blanko dimana larutan contoh diganti dengan
5% TCA, dengan prosedur kerja yang sama seperti di atas. Untuk setiap contoh
dan blanko dikerjakan secara duplo.
Cawan conway yang telah ditutup rapat tadi, kemudian digoyang
perlahan-lahan selama 1 menit dan disusun pada rak-rak inkubator. Selanjutnya diinkubasi
pada suhu 35 oC selama 2 jam atau suhu kamar selama 1 malam. Setelah inkubasi,
larutan asam borat dalam inner chamber cawan conway blanko dititrasi dengan
larutan N/70 HCL hingga warnanya menjadi merah muda (pink). Kemudian
sama sampai diperoleh warna merah muda seperti pada blanko. Nilai TVB
dihitung berdasarkan rumus sebagai berikut :
Kadar TVB = (ml titrasi contoh - ml titrasi blanko) x 80 ml N/100 g
daging
2. pH
Pengukuran pH didasarkan pada jumlah konsentrasi ion H+ dalam daging
ikan yang bersifat buffer.
Peralatan yang digunakan adalah pH meter, blender, pisau, stop watch,
gelas ukur, gelas piala 100 ml dan gelas piala untuk pH 4 dan pH 7 serta peralatan
laboratorium lainnya.
Contoh yang telah dirajang kecil-kecil ditimbang sebanyak 20 g,
dimasukkan ke dalam blender (diputar) selama satu menit. Hasil lumatan
dituangkan ke dalam gelas piala 100 ml, kemudian diukur pH-nya dengan alat pH
meter yang telah ditera kepekaannya dengan larutan buffer pH 4 dan pH 7.
Besarnya nilai pH adalah pembacaan jarum penunjuk pH meter setelah bergerak
selama satu menit.
3. Penentuan Total Plate Count (TPC) (Lembaga Penelitian Perikanan 1974)
Prinsip dari pengamatan ini adalah menentukan besarnya populasi bakteri
yang terdapat pada ikan, yang memberikan gambaran tentang bagaimana tingkat
kesegaran ikan tersebut, karena bakteri merupakan faktor utama penyebab
pembusukan yang sedang berlangsung.
Peralatan yang digunakan adalah gunting, pisau, timbangan analitik, pipet
1 ml, blender jars, erlenmeyer (ukuran 250 ml, 500 ml, dan 100 ml), batang
pengaduk, tabung reaksi, inkubator, stop watch, pinset, cawan petri, pemanas
bunsen dan alat hitung bakteri quebec.
Prosedur kerjanya terdiri dari empat tahap yang saling berhubungan yaitu
tahap persiapan, inokulasi, inkubasi dan penghitungan. Mula-mula ditimbang 20
25 kecepatan tinggi selama dua menit. Larutan yang didapat adalah pengenceran 1 :
10. Selanjutnya dipipet larutan 1 : 10 diatas sebanyak 1 ml lagi kedalam cawan
petri steril dan 1 ml lagi ke dalam cawan petri yang lain sebagai duplo. Kemudian
disiapkan larutan 1 : 100, dengan memipet 1 ml larutan 1 : 10 dan dimasukkan ke
dalam larutan 0.9% NaCl 9 ml lalu dikocok sampai homogen, maka diperoleh
contoh 1 : 100. Dipipet larutan contoh 1 : 100 ini dimasukkan ke dalam cawan
petri steril kedua dan secara duplo. Selanjutnya dengan cara yang sama
dikerjakan inokulasi contoh sampai pengenceran 1 : 1 000 000 yang dilakukan
secara aseptis.
Ke dalam semua cawan petri yang telah berisi larutan contoh di atas,
dituangkan secara aseptis media tumbuh Plate Count Agar (PCA) steril bersuhu
45 oC sebanyak 15 ml, dan dibiarkan selama 15-20 menit sampai agarnya
memadat. Setelah itu semua cawan petri tersebut diinkubasikan pada suhu 37 oC
dengan posisi terbalik selama 48 jam. Disamping itu dibuat blanko, yaitu ke
dalam cawan petri steril hanya dituangkan media tumbuh PCA 15 ml dan 1 ml
larutan pepton 1% steril.
Selanjutnya dilakukan perhitungan jumlah bakteri dengan menggunakan
alat hitung bakteri quebec. Perhitungan dilakukan sesuai dengan Standar Plate
Count (SPC)
4. Penilaian Organoleptik (SNI 01-2346-1991)
Pada percobaan I pengamatan organoleptik dilakukan secara deskriptif
pada awal penyimpanan hingga hari ke-12. Sedangkan pada percobaan II
pengamatan secara organoleptik dilakukan dengan uji skor oleh 10 orang
panelis tetap dengan form penilaian fillet sesuai SNI No 01-2346-1991 dan
RSNI 2005. Penilaian organoleptik meliputi parameter penampakan, tekstur
dan bau. Masing-masing parameter dinilai dengan skor tertinggi 9 untuk fillet
gurami sangat segar dan terendah 1 fillet yang sudah busuk, batas netral atau
garis penolakan 5 (Ilyas 1993). Uji organoleptik dilaksanakan di Lab. Orlep
27
Rancangan Percobaan dan Analisis Data
Rancangan percobaan yang digunakan dalam percobaan tahap I dan II
adalah rancangan acak lengkap dengan persamaan linier sebagai berikut :
Y
ij=
μ
+
τ
+
ε
ijDimana
: Y
ij=
Nilai pengamatan pada perlakuan ke-i dan ulangan ke-jµ
= rataan umumτ
= pengaruh perlakuan pencucian ke-iε
ij = galat percobaan pada perlakuan ke-i ulangan ke-jPada percobaan I terdiri atas 5 perlakuan, yaitu : pencucian dengan air
bersih, air jeruk, air garam, air jeruk dan garam dan larutan klorin. Pengamatan
dilakukan sebanyak 4 kali, yaitu pada hari ke-0, 4, 8 dan 12. Analisa keragaman
(Anova) data menggunakan one-way ANOVA pada program MINITAB 14
terhadap nilai TPC dan TVB untuk masing-masing pengamatan. Penentuan
perlakuan terbaik didasarkan perlakuan yang menghasilkan nilai TVB dan TPC
terkecil hingga pada pengamatan hari tertentu, dan pertimbangan umur simpan
yang tertinggi Selanjutnya hasil percobaan I digunakan sebagai perlakuan pada
percobaan II.
Pada percobaan II terdapat 8 perlakuan dengan rancangan acak lengkap
dengan pengamatan berulang pada hari ke-0, 7, 14, 18 dan 21 dan 24.
perlakuan tersebut adalah bahan pencuci A & B, dikombinasi dengan
komposisi gas CO2 : 0%, 30%, 45% dan 60% sehingga menjadi A.CO2 0%;
A.CO230%; A. CO2 45%; A. CO2 60%; B.CO20%; B.CO230%; B.CO245%;
dan B.CO260%. Anova dengan one-way ANOVA terhadap parameter TPC
dan TVB pada masing-masing pengamatan. Penentuan perlakuan terbaik
didasarkan pada nilai parameter yang menunjukkan kondisi filet pada umur
simpan tertinggi.
Analisis data hasil pengamatan organoleptik dilakukan dengancara
sederhana sesuai SNI No 01-2346-1991 dan RSNI 2005. Penentuan umur
bakunya) pada masing-masing amatan. Kemudian dibuat persamaan regresi
HASIL DAN PEMBAHASAN
Komposisi Proksimat Fillet Gurami
Komponen penting dari komposisi kimia ikan adalah protein dan
lemak. Ikan gurami mengandung 75-80% protein dan 6-9% lemak (basis
kering) (Tabel 3). Berdasarkan kandungan lemaknya Winarno (1993)
membagi tiga kelompok ikan, yaitu ikan berlemak rendah kurang dari 2%,
ikan berlemak sedang 2-5% dan ikan berlemak tinggi 6-20%. Ikan gurami
[image:45.612.179.473.335.433.2]termasuk ikan yang berlemak tinggi.
Tabel 3 Komposisi kimia daging ikan gurami (Osphronemous gouramy
Lac.)
Unsur Gizi Persentase
Kadar air 74.53 ± SD
Protein (bk) 77.82 ± SD
Lemak (bk) 7.85 ± SD
Kadar abu (bk) 5.32 ± SD
bk : basis kering
Rendemen Pembuatan Fillet Gurami
Ikan gurami dengan bobot 650-850 g yang dipuasakan selama 3-5 hari
mengalami penurunan bobot sebesar sebesar 3.4 ± 6%. Fillet yang dapat
dihasilkan dari ikan gurami mencapai 45 ± 3% dari bobot ikannya. Menurut
Suzuki (1981) rendemen ikan bervariasi menurut bentuk, umur dan kondisi
sebelum atau sesudah bertelur. Ikan yang berbentuk ellips mempunyai
rendemen 60% ke atas, sedangkan ikan yang berkepala besar atau ikan yang
pipih mempunyai rendemen daging 30-40%. Ikan gurami termasuk ikan yang
berbentuk pipih, namun dagingnya agak tebal. Informasi mengenai rendemen
dapat digunakan untuk memperkirakan nilai ekonomi setelah pengolahan.
Rendemen fillet sebesar 45% atau 0.45 dari bobot ikan. Jika dikonversi
28
Deskriptif Fillet Gurami
Karakteristik fillet ikan gurami diperoleh dengan pengamatan
organoleptik deskripsi secara sederhana. Secara visual daging ikan gurami
segar berwarna jernih putih kekuningan hingga merah muda sesuai jenis,
ukuran dan kematangan seksual. Menurut Winarno (1993) ikan yang
mengandung lemak 5% atau lebih dagingnya banyak mengandung pigmen
kuning, merah muda atau abu-abu, sedangkan ikan yang berlemak rendah
dagingnya cenderung putih. Fillet gurami segar nampak jernih, bersih,
cemerlang dan menarik. Garis pada daging dekat tulang maupun linea
lateralis berwarna merah cerah dan tidak terbelah.
Tekstur fillet gurami segar (sangat segar) padat dan kompak. Jika
ditekan atau dijapit dengan jari terasa kenyal. Bau fillet segar sangat spesifik.
Fillet yang dihasilkan dari ikan yang kenyang memiliki bau lebih amis
(menyengat dan kurang menarik), bau khas ikan-ikan air tawar. Bau tersebut
menurut Sarwono (2001) karena adanya geosmin yang menimbulkan bau
‘lumpur-lumut’. Tekstur daging dari hasil pemfilletan sesaat segera setelah
mati (pre rigor) berbeda dengan pemfilletan fase rigor, kurang kenyal.
Fillet yang disimpan pada suhu 10 oC selama 4 hari memiliki bau yang
masih segar, agak netral. Tidak terdapat bau seperti ikan sangat segar.
Teksturnya masih kompak, cukup elastis tapi agak lunak. Kenampakannya
mulai berbeda dengan ikan yang sangat segar, dagingnya tidak jernih namun
masih bersih, rapi. Garis tulang belakang maupun linea lateralis tidak pecah.
Pada penyimpanan hari ke-8, mulai nampak perbedaan sifat fillet
karena perlakuan. Fillet yang dicuci dengan air jeruk-garam dan fillet yang
dicuci dengan klorin 10 ppm nampak lebih bersih, bau kurang menyengat, dan
teksturnya lebih kompak dibanding fillet dengan pencucian air garam, larutan
air jeruk dan air bersih saja. Namun secara umum penampakan fillet sudah
29
kecoklatan. Pada penyimpanan hari ke-12 daging kehijauan keseluruhan,
sangat tidak menarik, garis pada tulang belakang dan linea lateralis coklat dan
terbelah. Tekstur tidak elastis, sangat lunak dan tidak kompak, bau amoniak
agak jelas, agak busuk.
Pengaruh Pencucian terhadap Nilai TPC
Pencucian berpengaruh terhadap penurunan nilai TPC dimana
perlakuan pencucian dengan air garam ditambah jeruk dan klorin 10 ppm
merupakan yang terbaik (Tabel 4). Penurunan kualitas fillet selama
penyimpanan disebabkan proses autolisis dan aktivitas bakteri (Huss 1995).
Upaya pengurangan jumlah bakteri pada awal penyimpanan fillet akan
mempengaruhi laju pertumbuhan bakteri pada daging ikan. Jumlah total
bakteri (TPC) pada fillet yang dicuci dengan bahan yang berbeda disajikan
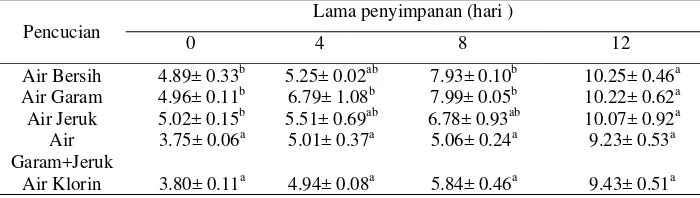
pada Tabel 4. Nilai TPC fillet paling kecil ditunjukkan pada bahan pencuci
[image:47.612.142.492.448.547.2]klorin 10 ppm dan air jeruk yang ditambah garam sejak awal penyimpanan.
Tabel 4 Nilai log jumlah total bakteri per g fillet pada beberapa perlakuan
pencucian dan penyimpanan pada suhu 10 oC (rerata ± SD, koloni/g)
Pencucian
Lama penyimpanan (hari )
0 4 8 12
Air Bersih 4.89± 0.33b 5.25± 0.02ab 7.93± 0.10b 10.25± 0.46a Air Garam 4.96± 0.11b 6.79± 1.08b 7.99± 0.05b 10.22± 0.62a
Air Jeruk 5.02± 0.15b 5.51± 0.69ab 6.78± 0.93ab 10.07± 0.92a Air
Garam+Jeruk
3.75± 0.06a 5.01± 0.37a 5.06± 0.24a 9.23± 0.53a
Air Klorin 3.80± 0.11a
4.94± 0.08a 5.84± 0.46a 9.43± 0.51a
Angka-angka pada kolom yang sama dan diikuti huruf superscript berbeda (a,b) menunjukkan berbeda nyata
Analisis statistik menunjukkan bahwa hingga penyimpanan hari
ke-8 nilai log TPC pada pencucian klorin dan air garam-jeruk berbeda nyata
dengan nilai log TPC sebesar 5.06 pada fillet yang dicuci dengan air
garam-jeruk. Nilai log TPC ikan segar 5.69 per g (SNI 01-2729-1992), sedangkan
menurut Ditjen POM (SK No. 03765/B/SK/VII/89) menyatakan batas
30
Pengaruh Pencucian terhadap Nilai TVB
Nilai TVB menunjukkan konsentrasi nitrogen volatil dalam daging
ikan sebagai indikator adanya penguraian protein akibat autolisis dan aktivitas
bakteri. TVB secara luas digunakan sebagai indikator awal kebusukan ikan
(Huss 1995) namun kurang bagus untuk mendeteksi tingkat kesegaran ikan
pada awal kemunduran mutu. Awal kemunduran mutu lebih disebabkan
proses autolisis oleh enzim dalam daging ikan dan tidak menyebabkan
meningkatnya TVB, tetapi hypoxantin (Botta, 1994). TVB lebih banyak
disebabkan oleh aktivitas bakteri.
Nilai TVB fillet ikan gurami disajikan dalam Tabel 5. Pada awal
penyimpanan jumlah TVB semua perlakuan pencucian tidak berbeda nyata
yaitu sekitar 18-19 mg N/100 g daging ikan selanjutnya mengalami kenaikan
selama penyimpanan selama 12 hari pada suhu 10 oC, dan mulai ada
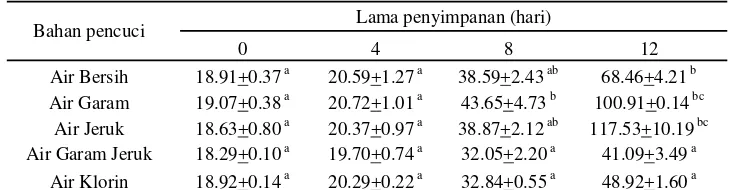
[image:48.612.137.502.436.531.2]perbedaan jumlah pada hari ke-8.
Tabel 5 Nilai TVB fillet gurami pada beberapa perlakuan pencucian dan
penyimpanan pada suhu 10 oC (rerata ± SD, mg/100 g)
Bahan pencuci Lama penyimpanan (hari)
0 4 8 12 Air Bersih 18.91+0.37 a 20.59+1.27 a 38.59+2.43 ab 68.46+4.21 b
Air Garam 19.07+0.38 a 20.72+1.01 a 43.65+4.73 b 100.91+0.14 bc Air Jeruk 18.63+0.80 a 20.37+0.97 a 38.87+2.12 ab 117.53+10.19 bc Air Garam Jeruk 18.29+0.10 a 19.70+0.74 a 32.05+2.20 a 41.09+3.49 a
Air Klorin 18.92+0.14 a 20.29+0.22 a 32.84+0.55 a 48.92+1.60 a
Angka-angka pada kolom yang sama dan diikuti huruf superscript berbeda (a,b) menunjukkan berbeda nyata
Perlakuan pencucian tidak berpengaruh langsung terhadap perubahan
nilai TVB pada fillet ikan gurami. Hal ini dapat dilihat pada hari ke-0 tidak
ada perbedaan nilai TVB pada semua perlakuan pencucian. Perbedaan nilai
TVB terjadi pada hari ke-8 dan 12, disebabkan oleh aktivitas bakteri.
31
substrat yang sesuai bagi pertumbuhannya. Dengan demikian naiknya nilai
TVB lebih banyak disebabkan oleh bakteri.
Menurut Connell (1980), pada ikan cod sangat segar jumlah TVB
sebesar 20 mg N/100 g daging ikan, sedangkan penyimpanan ikan cod dalam
es jumlah TVB meningkat hingga 60 mg N/100 g pada hari ke-20 dan
dinyatakan busuk pada hari ke-25 dengan nilai TVB 70 mg N/100 g. Pada
kasus lain digunakan standar yang berbeda. Misalnya pada ikan tuna dan
swordfish TVB tidak lebih dari 30 mg N/100 g digunakan untuk standar ikan
tuna yang akan dibekukan. Ikan asin dan ikan kering antara 100-200 mg
N/100 g.
Pengaruh Pencucian terhadap Nilai pH
Nilai pH fillet berkisar antara 6.52 hingga 7.27. Secara umum nilai pH
mengalami kenaikan selama penyimpanan. Perubahan nilai pH pada
penurunan kualitas fillet disebabkan oleh terbentuknya senyawa-senyawa basa
yang bersifat volatil (Suwedo 1993). Tidak terdapat perbedaan nyata nilai pH
antar perlakuan, sehingga perlakuan pencucian tidak berpengaruh terhadap
[image:49.612.141.508.506.588.2]nilai pH selama penyimpanan fillet.
Tabel 6 Nilai pH fillet gurami pada beberapa perlakuan pencucian dan
penyimpanan pada suhu 10 oC (rerata ± SD)
Pencucian Lama penyimpanan (hari)
0 4 8 12 Air Bersih 6.77± 0.05a 6.99± 0.04a 6.96± 0.02a 7.20± 0.16a Air Garam 6.99± 0.06a 6.85± 0.28a 7.02± 0.09a 7.27± 0.11a Air Jeruk 6.70± 0.25a 6.65± 0.34a 6.92± 0.08a 7.10± 0.06a Air Garam+Jeruk 6.65± 0.10a 6.52± 0.06a 7.05± 0.02a 7.09± 0.07a
Air Klorin 6.57± 0.09a 6.54± 0.08a 6.88± 0.06a 7.04± 0.05a
32
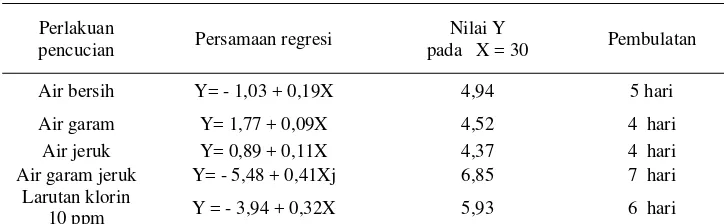
Umur Simpan Fillet pada 10 oC
Umur simpan fillet pada percobaan 1 dihitung berdasarkan
persamaan regresi nilai TVB dengan lama penyimpanan dan