LAMPIRAN
Lampiran 1. Kondisi alat Spektrofotometer Serapan Atom merek
Perkinelmer pada pengukuran konsentrasi logam Fe
No Parameter Logam Besi
1 Panjang gelombang (nm) 248,33
2 Tipe nyala Udara-C2H2
3 Kecepatan aliran gas pembakar (L/min) 2,50
4 Kecepatan aliran udara (L/min) 10
5 Lebar celah (nm) 0,2
6 Ketinggian tungku 7,5
Lampiran 2. Data Hasil Pengukuran absorbansi Larutan Standar Besi dengan
Spektrofotometer Serapan atom
Lampiran 3. Data kadar Besi pada param yang dikonsumsi dan digunakan
sebagai obat luar
A : Param yang dikonsumsi
B : Param yang dikonsumsi
Lampiran 4. Kondisi alat Spektrofotometer Serapan Atom merek
Perkinelmer padapengukuran Konsentrasi logam Tembaga
No. Parameter Logam Tembaga
1 Panjang gelombang (nm) 324,75
2 Tipe nyala Udara-C2H2
3 Kecepatan aliran gas pembawa (L/min) 2,50
4 Kecepatan aliran Udara (L/min) 10
5 Lebar celah (nm) 0,7
6 Ketinggian tungku (mm) 7,5
Lampiran 5. Data Absorbansi Larutan Standar Tembaga (Cu)
No. Sampel A1 A2 A3 �̅
Lampiran 6. Data kadar tembaga pada param yang dikonsumsi dan yang
digunakan sebagai obat luar
A : Sampel param yang dikonsumsi
B : Sampel param yang dikonsumsi
Lampiran 7. Kondisi Alat Spektrofotometer Serapan Atom merek
perkinelmer pada pengukuran Konsentrasi Zinkum
No. Parameter Logam Seng
1 Panjang Gelombang (nm) 213,86
2 Tipe nyala Udara-C2H2
3 Kecepatan aliran gas pembawa (L/min) 2,50
4 Kecepatan aliran udara (L/min) 10
5 Lebar celah (nm) 0,7
6 Ketinggian tungku (mm) 7,5
Lampiran 8. Data Absorbansi Larutan Standar Zinkum (Zn)
No. Sampel A1 A2 A3 �̅
Lampiran 9. Data kadar Zinkum pada param yang dikonsumsi dan yang
digunakan sebagai obat luar
A : Sampel param yang dikonsumsi
B : Sampel param yang dikonsumsi
DAFTAR PUSTAKA
Almatsier, R. 1987. Sample Pretreatment and Separation. New York : John wiley and sons.
Anwar, F. 2009.Makan Tepat Badan Sehat. Jakarta : PT. Mizan Publika.
Aprianto, A. 1989. Analisis Pangan. Bogor : Departemen Pendidikan dan Kebudayaan.
direktorat Jendral Pendidikan Tinggi Pusat antar Universitas Pangan dan Gizi.
Atkins, D. 2007.Seri Diet Korektif. Jakarta : PT. Alex Media Komputindo.
Bangun, R. S. 2010. Kuning pada Masyarakat Karo. Skripsi. Medan : Departemen Antropologi Sosial FISIP Universitas Sumatera Utara.
Basset,J.1994. Kimia Analisis Kuantitatif Anorganik. Edisi Keempat. Jakarta : Penerbit Buku
Kedokteran
Devi, N. 2010. Nutrition and Foot. Jakarta : PT. Kompas Media Nusantara.
Darmono.1995. Logam Dalam Sistem Biologi Mahluk Hidup. Jakarta : UI-Press
Effendi,H.2003. Telaah Kualitas Air. Yogyakarta : Penerbit Kanisisun
Ginting, E. P. 1999. Religi Karo. Kabanjahe : Abdi Karya.
Holloway, P. H dan Vaidyanathan,P.N.2010.Characterization of Metal and Alloys. New
Marks, D. B. 1996. Biokimia Kedokteran Dasar. Jakarta : Penerbit Buku Kedokteran EGC.
Noorkasiani dan Heryati. 2007. Sosiologi Keperawatan. Jakarta : Penerbit Buku Kedokteran.
Postawa, A. 2012. Best Practice Quide on Sampling and Monitoring of Metal in Dringking
Water. London : IWA Publishing.
Raimon. 1992. Perbandingan Metode Destruksi Basah dan Kering Terhadap Penentuan Fe,
Cu, dan Zn. Edisi Khusus. Palembang : BIPA.
Sari, W dan Indrawati, L. 2008. Care You Self Hepatitis. Jakarta : Penerbit Penebar Plus.
Sembiring, N. 2010.Terapi Sari Air Laut. Jakarta : Penerbit Penebar Plus.
Sudarmadji,S, Haryono, B dan Suhardi. 1989. Analisis Bahan Makanan dan Pertanian.
Jakarta : Erlangga.
Suhardjo dan Kusharto, C.M.1992. Prinsip-Prinsip Ilmu Gizi. Yogyakarta : Kanisius.
Taylor,H.E.2001. Inductively Coupled Plasma Mass Spektrometry. New York : Academic
Press.
Underwood, J. C. E. 1996. Patologi Umum dan Sistematik. Edisi Kedua. Volume I. Jakarta:
Penerbit Buku Kedokteran.
Watson,G.D.2007. Analisis Farmasi. Jakarta : Penerbit Buku Kedokteran
BAB 3
METODE PENELITIAN
3.1. Alat-alat
- Neraca Analitik Mettler PM 400
- Bola karet
- Pipet tetes
- Hot plate Fisher
- Peralatan gelas Pyrex
- Cawan krusible
- Oven Fisher
- Tanur Fisher
- Spatula
- Botol Akuades
- Matt pipet
- Kertas saring Whatman No.42
- Alu dan Lumpang
- Desikator
- Cawan penguap
-Spektrofotometer Serapan Atom Perkinelmer
3.2. Bahan
- HNO3 p.a (E.Merck)
- H2SO4 p.a (E.Merck)
- KMnO4 p.a (E.Merck)
- H2O2 p.a (E.Merck)
- Akuades
- Fe(NH4)2(SO4)2.6H2O p.a (E.Merck)
-CuSO4.5H2O p.a (E.Merck)
-ZnSO4.5H2O P.a (E.Merck
3.3. Prosedur Penelitian
3.3.1. Penyediaan Reagen
3.3.1.1. Pembuatan larutan standar Fe3+
a. Larutan standar Fe3+ 1000 mg/L
Sebanyak 50 mL akuades dimasukkan ke dalam labu erlenmeyer, ditambahkan 20
mL H2SO4(p) secara perlahan, kemudian sebanyak 7,022 g Fe(NH4)2(SO4)2.6H2O
dimasukkan ke dalam labu erlenmeyer yang telah berisi campuran akuades dan
H2SO4 (p), diaduk hingga seluruh kristal larut sempurna, dimasukkan ke dalam
labu ukur 1000 mL, ditambahkan KMnO4 0,1 N setetes demi setetes sampai
diperoleh warna merah muda kemudian diencerkan dalam labu ukur 1000 mL
sampai garis tanda dan dihomogenkan.
b. Larutan Standar Fe3+ 100 mg/L
Dipipet sebanyak 10 mL larutan induk Fe 1000 mg/L dan dimasukkan ke dalam
labu ukur 100 mL, ditambahkan akuades hingga garis tanda dan dihomogenkan.
c. Larutan Standar Fe3+ 10 mg/L
Dipipet sebanyak 10 mL larutan standar Fe 100 mg/L dan dimasukkan ke dalam
d. Larutan Standar Fe3+ 0,5; 1,0; 1,5; 2,0; dan 2,5 mg/L
Dipipet sebanyak 2,5; 5,0; 7,5; 10 dan 12,5 mL larutan standar Fe 10 mg/L
dimasukkan ke dalam labu ukur 50 mL, ditambahkan akuades sampai garis
tanda dan dihomogenkan.
e. KMnO4 0,1 N
Sebanyak 0,32 g KMnO4 dimasukkan ke dalam labu ukur 100 mL, ditambahkan
akuades hingga garis tanda dan dihomogenkan.
3.3.1.2. Pembuatan Larutan Standar Cu2+
a. Larutan Standar Cu2+ 1000 mg/L
Sebanyak 3,929 g CuSO4.5H2O dilarutkan ke dalam akuades kemudian
diencerkan dalam labu ukur 1000 mL sampai garis tanda dan dihomogenkan.
b. Larutan standar Cu2+ 100 mg/L
Dipipet sebanyak 10 mL larutan induk Cu 1000 mg/L dan dimasukkan ke dalam
labu ukur 100 mL, diencerkan dengan akuades hingga garis tanda dan
dihomogenkan.
c. Larutan standar Cu2+ 10 mg/L
Dipipet sebanyak 10 mL larutan induk Cu 100 mg/L dan dimasukkan ke dalam
labu ukur 100 mL, diencerkan dengan akuades hingga garis tanda dan
d. Larutan seri standar Cu2+ 0,5; 1,0; 1,5; 2,0; dan 2,5 mg/L
Dipipet masing-masing sebanyak 2,5; 5; 7,5; 10 dan 12,5 mL larutan standar Cu
10 mg/L dan dimasukkan ke dalam labu ukur 50 mL, diencerkan dengan akuades
sampai garis tanda dan dihomogenkan.
3.3.1.3. Pembuatan larutan standar Zn2+
a. Pembuatan larutan standar Zn2+ 1000 mg/L
Sebanyak 4,3973 g ZnSO4.5H2O dilarutkan kedalam akuades kemudian
diencerkan dalam labu ukur 1000 mL sampai garis tanda dan dihomogenkan.
b. Pembuatan larutan standar Zn2+ 100 mg/L
Dipipet sebanyak 10 mL larutan induk Zn 1000 mg/L dan dimasukkan ke dalam
labu ukur 100 mL, diencerkan dengan akuades hingga garis tanda dan
dihomogenkan.
c. Larutan standar Zn2+ 10 mg/L
Dipipet sebanyak 10 mL larutan induk Zn 100 mg/L dan dimasukkan ke dalam
labu ukur 100 mL, diencerkan dengan akuades hingga garis tanda dan
dihomogenkan
d. Larutan seri standar Zn2+ 0,5; 1,0; 1,5 ;2,0 ;2,5 mg/L
Dipipet masing-masing sebanyak 2,5; 5; 7,5; 10 dan 12,5 mL larutan standar Zn
10 mg/L dan dimasukkan ke dalam labu ukur 50 mL, diencerkan dengan akuades
3.3.2. Pengediaan sampel
Param dihaluskan dengan alu dan lumpang kemudian dipindahkan kedalam
cawan penguap lalu dimasukkan kedalam oven dengan suhu ± 105oC selama 5
jam dan dimasukkan kedalam desikator, kemudian sebanyak 5 g serbuk param
dimasukkan kedalam cawan crusibel, diabukan pada suhu ± 550oC, dipindahkan
abu kedalam gelas beaker 250 mL kemudian ditambahkan 10 mL HNO3 pekat dan
2 mL H2SO4 pekat dicampur ratakan sehingga diperoleh larutan sampel.
Larutan sampel tersebut ditambahkan 5 mL HNO3 pekat dan 3 mL H2O2
30% kemudian dipanaskan diatas hot plate selama 30 menit lalu dinginkan. Hasil
destruksi disaring dengan kertas saring Whatman No.42 kemudian filtrat
diencerkan dengan akuades sampai garis tanda dalam labu takar 100 mL dan
diatur pH=3. Kemudian dianalisa kualitatif dengan menggunakan ICP dan analisa
kuantitatif dengan menggunakan alat spektrofotometer serapan atom.
3.3.3. Pembuatan Kurva Larutan Standar Cu2+
Larutan Cu 0,5 mg/L ditentukan absorbansinya dengan menggunakan
Spektrofotometer Serapan Atom pada λ = 324,75 nm dan dilakukan hal yang sama untuk larutan seri standar Cu 1,0; 1,5; 2,0; 2,5 mg/L.
3.3.4. Pembuatan Kurva Larutan Standar Fe 3+
Larutan Fe 0,5 mg/L ditentukan absorbansinya dengan menggunakan
3.3.5. Pembuatan Kurva Larutan Standar Zn2+
Larutan Zn 0,5 mg/L ditentukan absorbansinya dengan menggunakan
Spektrofotometri Serapan Atom pada λ = 213,86 nm dan dilakukan hal yang sama
untuk larutan seri standar Zn 1,0; 1,5; 2,0; 2,5 mg/L.
3.3.6. Penentuan kadar Cu pada sampel dengan menggunakan
Spektrofotometer Serapan Atom.
Larutan sampel yang telah didestruksi ditentukan absorbansinya pada λ= 324,75 nm dengan menggunakan Spektrofotometer Serapan Atom.
3.3.7. Penentuan kadar Fe pada sampel dengan menggunakan
Spektrofotometer Serapan Atom.
Larutan sampel yang telah didestruksi ditentukan absorbansinya pada λ= 248,33 nm dengan menggunakan Spektrofotometer Serapan Atom.
3.3.8. Penentuan kadar Zn pada sampel dengan menggunakan
Spektrofotometer Serapan Atom.
3.4. Bagan Penelitian
3.4.1. Pembuatan kurva kalibrasi Tembaga (Cu)
Larutan Seri Standar Cu 0,5 mg/l
Ditentukan absorbansinya pada panjang gelombang 324,75 dengan menggunakan alat Spektrofotometer Serapan Atom
Hasil
NB : dilakukan prosedur yang sama untuk larutan seri standar Tembaga (Cu) 1,0
;1,5 ;2,0 ;2,5 mg/L
3.4.2. Pembuatan kurva kalibrasi Besi Fe
Larutan Seri Standar Fe 0,5 mg/l
Ditentukan absorbansinya pada panjang gelombang 248,33 dengan menggunakan alat Spektrofotometer Serapan Atom
Hasil
NB : dilakukan prosedur yang sama untuk larutan seri standar Besi
(Fe)1,0;1,5;2,0;2,5mg/L.
3.4.3. Pembuatan kurva kalibrasi Zinkum (Zn)
Larutan Seri Standar Zn 0,5 mg/l
Ditentukan absorbansinya pada panjang gelombang 213,86 dengan menggunakan alat Spektrofotometer Serapan Atom
Hasil
3.4.4. Preparasi sampel
Sampel Param
Dihaluskan
Dimasukkan kedalam cawan penguap
Dikeringkan didalam oven pada suhu105oC selama 5 jam Dimasukkan kedalam desikator
Sampel Kering Homogen
Abu Param
Ditimbang sebanyak 5 g
Dimasukkan kedalam cawan crusibel Diabukan pada suhu 550oC
3.4.5. Penyediaan larutan sampel
5 g sampel param kering
Dimasukkan kedalam beaker glass 250 mL
Ditambahkan 10 mL HNO3 pekat
Ditambahkan 2 mL H2SO4 pekat
Dipanaskan diatas hot plate selama 30 menit Didinginkan
Larutan Sampel
Ditambahkan 5 mL HNO3 pekat
Ditambahkan 3 mL H2O2 30%
Larutan Kuning Jernih
Dipanaskan diatas hot plate selama 30 menit Didinginkan
Disaring dengan kertas saring Whatman No.42
Filtrat Residu
Dibilas dengan akuades
Dikumpulkan dalam labu takar 100 mL Diatur pH hingga mencapai pH=3
Diencerkan dengan akuades sampai garis tanda
Hasil
Dianalisa kualitatif dengan ICP dan analisa kuantitatif dengan SSA
3.4.6. Penentuan kadar Cu dengan menggunakan alat Spektrofotometer Serapan Atom.
Larutan Cu
Hasil
Ditentukan absorbansinya pada panjang gelombang =324,75 nm dengan menggunakan alat Spektrofotometer Serapan Atom.
NB:dilakukan prosedur yang sama untuk sampel B dan C
3.4.7. Penentuan kadar Fe dengan menggunakan alat Spektrofotometer
Serapan Atom
Larutan Fe
Hasil
Ditentukan absorbansinya pada panjang gelombang = 248,33 nm dengan menggunakan alat Spektrofotometer Serapan Atom.
NB:dilakukan prosedur yang sama untuk sampel B dan C
3.4.8. Penentuan kadar Zn dengan menggunakan alat Spektrofotometer
Serapan Atom
Larutan Zn
Hasil
Ditentukan absorbansinya pada panjang gelombang = 213,86 nm dengan menggunakan alat Spektrofotometer Serapan Atom.
BAB 4
HASIL DAN PEMBAHASAN
4.1. Hasil Penelitian
4.1.1. Uji Kualitatif
Untuk uji kualitatif logam dalam param dilakukan dengan menggunakan
alat ICP-OES dengan hasil yang ditunjukkan pada tabel 4.1
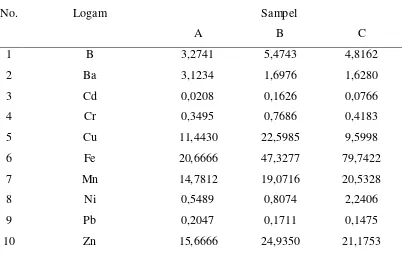
Tabel 4.1. Data hasil analisa kualitatif dengan ICP-OES
No. Logam Sampel
A B C
1 B 3,2741 5,4743 4,8162
2 Ba 3,1234 1,6976 1,6280
3 Cd 0,0208 0,1626 0,0766
4 Cr 0,3495 0,7686 0,4183
5 Cu 11,4430 22,5985 9,5998
6 Fe 20,6666 47,3277 79,7422
7 Mn 14,7812 19,0716 20,5328
8 Ni 0,5489 0,8074 2,2406
9 Pb 0,2047 0,1711 0,1475
4.1.2. Logam Besi
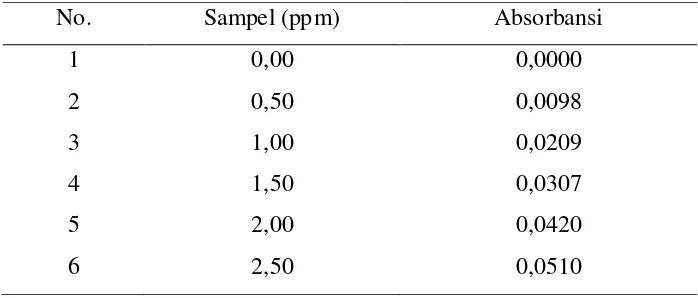
Tabel 4.2. Data pengukuran absorbansi larutan seri standar Besi
No. Sampel (ppm) Absorbansi
1 0,00 0,0000
4.1.2.1. Penurunan persamaan garis regresi
Data absorbansi yang diperoleh untuk suatu seri larutan standar Fe diplotkan
terhadap konsentrasi larutan standar sehingga diperoleh kurva kalibrasi berupa
garis linear seperti pada gambar 4.1. Persamaan garis regresi ini diturunkan
dengan metode least square, dimana konsentrasi dari larutan standar dinyatakan
sebagai Xi dan Absorbansi dinyatakan sebagai Yi seperti pada tabel berikut:
Persamaan garis regresi untuk kurva kalibrasi dapat diturunkan dari persamaan
Selanjutnya harga slope dapat ditentukan dengan menggunakan metode least
square sebagai berikut :
�= ∑(�� − ��)(�� − ��)
∑(�� − ��)2
b = Y – aX
Dengan mensubstitusikan harga-harga yang tercantum pada tabel pada persamaan
maka diperoleh :
Maka persamaan garis yang diperoleh adalah :
Y = 0,0202X + 0,0007
4.1.2.2. Penentuan koefisien korelasi untuk logam besi (Fe)
Koefisien korelasi dapat ditentukan dengan menggunakan persamaan sebagai
berikut :
�= ∑(�� − ��)(�� − ��)
�(�� − ��)2(�� − ��)2
Koefisien korelasi untuk logam Besi (Fe) adalah :
�= 0,0883
Selanjutnya absorbansi diplotkan terhadap konsentrasi larutan seri standar
sehingga diperoleh suatu kurva kalibrasi berupa garis linear seperti pada gambar
berikut :
Gambar 4.1 Kurva Kalibrasi Larutan Seri Standart Fe
4.1.2.3. Penentuan Kadar Besi dalam sampel
Kadar Besi dapat ditentukan dengan menggunakan metode kurva kalibrasi dengan
mensubstitusikan nilai Y (absorbansi) yang diperoleh dari hasil pengukuran
terhadap persamaan garis regresi dari kurva kalibrasi.
4.1.2.3.1. Penentuan kadar Besi (Fe) yang terkandung dalam Param dengan
metode Spektrofotometri Serapan Atom dalam mg/L.
Dari data pengukuran absorbansi Besi untuk sampel yang dikonsumsi diperoleh
serapan (A) sebagai berikut :
A1 = 0,0126
Konsentrasi Larutan Seri Standar Fe (mg/L)
Y-Values
Dengan mensubstitusikan nilai Y (Absorbansi) ke persamaan garis regresi
Y = 0,0202X + 0,0007, maka diperoleh:
X1 = 0,5891
X2 = 0,5940
X3 = 0,5891
Dengan demikian kadar Besi pada Param yang dikonsumsi adalah :
��= ∑��
Dari data hasil distribusi student untuk n = 3, derajat kebebasan (dk) = n- 1 = 2
untuk derajat kepercayaan 95% (p=0,05), t= 4,30
Maka, d = t(0,05 x n-1)Sx
d = 4,30 x 0,1 x 0,0016 = 0,0006
Dari data hasil pengukuran kadar Besi pada param yang dikonsumsi adalah
sebesar :
0,5907 ± 0,0006 mg/L
Hasil perhitungan untuk kadar Besi pada param yang digunakan sebagai obat luar
4.1.2.3.2 Penentuan Kadar Besi (Fe) yang Terkandung dalam Param dengan
Metode Spektrofotometri Serapan Atom dalam mg/Kg.
��������������= ����������������
����������ℎ �106 ��/��
Dengan mengkalikan hasil penentuan Besi dari sampel di atas, maka diperoleh
hasil pengukuran kadar Besi dari 5 gram sampel sebesar :
Kadar Besi pada 5 gram sampel dapat dihitung sebagai berikut :
�����= 0,5907 ��/��0,1�
5 �� � 10
6��/��
= 11,814 mg/kg
4.1.3. Logam Tembaga
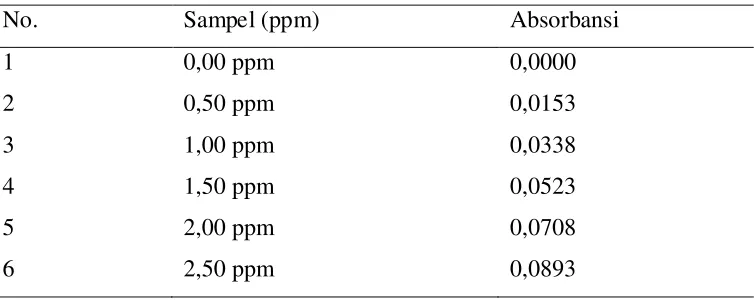
Tabel 4.3. Data Absorbansi Larutan Standar Tembaga (Cu)
No. Sampel (ppm) Absorbansi
1 0,00 ppm 0,0000
2 0,50 ppm 0,0153
3 1,00 ppm 0,0338
4 1,50 ppm 0,0523
5 2,00 ppm 0,0708
6 2,50 ppm 0,0893
4.1.3.1. Penurunan persamaan garis regresi
Data absorbansi yang diperoleh untuk suatu seri larutan standar Cu diplotkan
terhadap konsentrasi larutan standar sehingga diperoleh kurva kalibrasi berupa
garis linear seperti pada gambar 4.2. Persamaan garis regresi ini diturunkan
dengan metode least square, dimana konsentrasi dari larutan standar dinyatakan
No Xi Yi (Xi - ��) (Yi - ��) (Xi - ��)2 (Yi - ��)2 (Xi –��)(Yi- ��)
Persamaan garis regresi untuk kurva kalibrasi dapat diturunkan dari persamaan
garis :
Maka persamaan garis yang diperoleh adalah :
Y = 0,0381X+ 0,0003
4.1.3.2. Penentuan Koefisien Korelasi
Koefisien korelasi dapat ditentukan dengan menggunakan persamaan sebagai
�= ∑(�� − ��)(�� − ��)
�(�� − ��)2(�� − ��)2
Koefisien korelasi untuk logam Tembaga adalah :
�= 0,0166
�(4,3750)(0,0053)= 0,9998
Selanjutnya absorbansi diplotkan terhadap konsentrasi larutan seri standar
sehingga diperoleh suatu kurva kalibrasi berupa garis linear seperti pada gambar
berikut :
Gambar 4.2. Kurva Kalibrasi Larutan Seri standar Cu (mg/L)
4.1.3.3. Penentuan Kadar Tembaga dalam sampel
Kadar Tembaga dapat ditentukan dengan menggunakan metode kurva kalibrasi
dengan mensubstitusikan nilai Y (absorbansi) yang diperoleh dari hasil
pengukuran terhadap persamaan garis regresi dari kurva kalibrasi.
y = 0,0381x + 0,0003
Konsentrasi Larutan Seri Standar Cu (mg/L)
Y-Values
4.1.3.3.1. Penentuan kadar Tembaga (Cu) yang terkandung dalam Param
dengan metode Spektrofotometri Serapan Atom dalam mg/L.
Dari data pengukuran absorbansi Tembaga untuk sampel yang dikonsumsi
diperoleh serapan (A) sebagai berikut :
A1 = 0,0019
A2 = 0,0015
A3 = 0,0019
Dengan mensubstitusikan nilai Y (Absorbansi) ke persamaan garis regresi
Y = 0,0381X + 0,0003, maka diperoleh:
X1 = 0,0419
X2 = 0,0314
X3 = 0,0419
Dengan demikian kadar Tembaga pada Param yang dikonsumsi adalah :
��= ∑��
Dari data hasil distribusi student untuk n = 3, derajat kebebasan (dk) = n- 1 = 2
untuk derajat kepercayaan 95% (p=0,05), t= 4,30
Maka, d = t(0,05 x n-1)Sx
d = 4,30 x 0,1 x 0,0243 = 0,0104
Dari data hasil pengukuran kadar Tembaga pada param yang dikonsumsi adalah
0,0384 ± 0,0104 mg/L
Hasil perhitungan untuk kadar Tembaga pada param yang digunakan sebagai obat
luar seperti pada tabel dalam lampiran 6.
4.1.3.3.2 Penentuan Kadar Tembaga (Cu) yang Terkandung dalam Param
dengan Metode Spektrofotometri Serapan Atom dalam mg/kg.
�����������������= �� ��������������
����������ℎ � 106��/��
Kadar Tembaga pada 5 gram sampel dapat dihitung sebagai berikut :
�����= 0,0384��/��0,1�
5�� �10
6��/��
= 0,768 mg/kg
4.1.4. Logam Zinkum
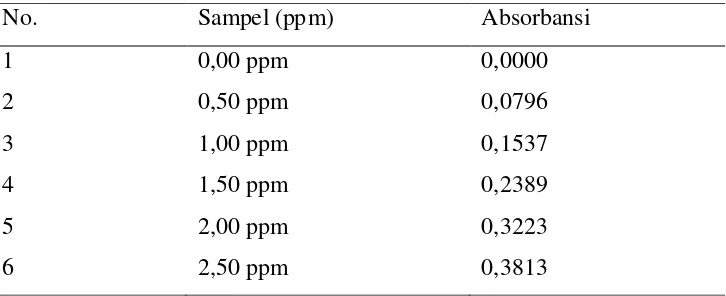
Tabel. 4.4. Data Absorbansi Larutan Standar Zinkum (Zn)
No. Sampel (ppm) Absorbansi
1 0,00 ppm 0,0000
4.1.4.1. Penurunan persamaan garis regresi
Data absorbansi yang diperoleh untuk suatu seri larutan standar Zn diplotkan
terhadap konsentrasi larutan standar sehingga diperoleh kurva kalibrasi berupa
dengan metode least square, dimana konsentrasi dari larutan standar dinyatakan
sebagai Xi dan Absorbansi dinyatakan sebagai Yi seperti pada tabel berikut:
No. Xi Yi Xi-�� Yi-�� (Xi-��)2 (Yi-��)2 (Xi-��)(Yi-��)
Persamaan garis regresi untuk kurva kalibrasi dapat diturunkan dari persamaan
garis :
Y = aX + b
Dimana :
a = slope
b = intersept
Selanjutnya harga slope dapat ditentukan dengan menggunakan metode least
square sebagai berikut :
�= ∑(�� − ��)(�� − ��)
∑(�� − ��)2
b = y – ax
Dengan mensubstitusikan harga-harga yang tercantum pada tabel pada persamaan
maka diperoleh :
�= 0,0681
4,3750= 0,1558
= 0,1955 – 0,1941
= 0,0008
Maka persamaan garis yang diperoleh adalah :
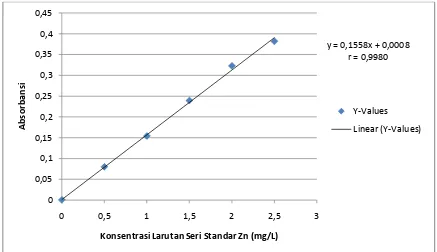
Y = 0,1558X + 0,0008
4.1.4.2. Penentuan koefisien korelasi untuk logam Zinkum (Zn)
Koefisien korelasi dapat ditentukan dengan menggunakan persamaan sebagai
berikut :
�= ∑(�� − ��)(�� − ��)
�(�� − ��)2(�� − ��)2
Koefisien korelasi untuk logam Zinkum (Zn) adalah :
�= 0,0681
�(4,3750)(0,0001)= 0,9980
Selanjutnya absorbansi diplotkan terhadap konsentrasi larutan seri standar
sehingga diperoleh suatu kurva kalibrasi berupa garis linear seperti pada gambar
berikut :
Konsentrasi Larutan Seri Standar Zn (mg/L)
Y-Values
4.1.4.3. Penentuan Kadar Zinkum dalam sampel
Kadar Zinkum dapat ditentukan dengan menggunakan metode kurva kalibrasi
dengan mensubstitusikan nilai Y (absorbansi) yang diperoleh dari hasil
pengukuran terhadap persamaan garis regresi dari kurva kalibrasi.
4.1.4.3.1. Penentuan kadar Zinkum (Zn) yang terkandung dalam Param
dengan metode Spektrofotometri Serapan Atom dalam mg/L.
Dari data pengukuran absorbansi Zinkum untuk sampel yang dikonsumsi
diperoleh serapan (A) sebagai berikut :
A1 = 0,1012
A2 = 0,0997
A3 = 0,0990
Dengan mensubstitusikan nilai Y (Absorbansi) ke persamaan garis regresi
Y = 0,1558x + 0,0008, maka diperoleh:
X1 = 0,6444
X2 = 0,6347
X3 = 0,6302
Dengan demikian kadar zinkum pada Param yang dikonsumsi adalah :
Didapatkan harga,
Dari data hasil distribusi student untuk n = 3, derajat kebebasan (dk) = n- 1 = 2
untuk derajat kepercayaan 95% (p=0,05), t= 4,30
Maka, d = t(0,05 x n-1)Sx
d = 4,30 x 0,1 x 0,0041 = 0,0017
Dari data hasil pengukuran kadar Zinkum dalam param yang dikonsumsi adalah
sebesar :
0,6364 ± 0,0017 mg/L
Hasil perhitungan untuk kadar Zinkum pada param yang digunakan sebagai obat
luar seperti pada tabel dalam lampiran 9.
4.1.3.3.2 Penentuan Kadar Zinkum yang Terkandung dalam Param dengan
Metode Spektrofotometri Serapan Atom dalam mg/Kg.
����������������= ����������������
����������ℎ �106��/��
Kadar Zinku pada 5 gram sampel dapat dihitung sebagai berikut :
�����= 0,6364��/��0,1�
5�� �10
6��/��
= 12,728 mg/kg
4.2.Pembahasan
Telah dilakukan analisis logam berat Besi, Tembaga, dan Zinkum didalam param.
Dimana sampel diambil dari daerah yang berbeda berdasarkan ketinggiannya dari
permukaan laut dimana diharapkan sampel yang berasal dari daerah yang paling
tinggi dari permukaan laut memiliki kandungan logam yang paling sedikit dan
sampel yang berasal dari daerah yang lebih rendah dari permukaan laut memiliki
kandungan logam yang lebih tinggi hal ini disebabkan karena hujan mengikis dan
membawa tanah yang mengandung logam kedaerah yang lebih rendah. Kadar
destruksi kering kemudian diikuti dengan pelarutan abunya dengan penambahan
HNO3(p) dan H2SO4(p). Sebelumnya dianalisa kualitatif dengan menggunakan
Inductively Coupled Plasma, kemudian ditentukan nilai absorbansinya dan
konsentrasi dari sampel menggunakan alat Spektrofotometer Serapan Atom pada
panjang gelombang untuk Besi (Fe)=248,33 nm, Tembaga (Cu)=324,75 nm, dan
Zinkum (Zn)=213,86 nm.
Kurva standar larutan seri standar logam Besi (Fe), Tembaga (Cu), dan
Zinkum (Zn) dibuat dengan memvariasikan konsentrasi larutan seri standar
dengan menggunakan metode least square sehingga diperoleh persamaan garis
linear untuk logam Besi (Fe) Y=0,0202X+0,0007; Tembaga (Cu)
Y=0,0381X+0,0003; dan Zinkum (Zn)Y=0,1558X+0,0008
Dalam penelitian ini diperoleh koefisien korelasi untuk logam Besi
(Fe)=0,9987; Tembaga (Cu)=0,9998; dan Zinkum(Zn)=0,9980. Hal ini
menunjukkan adanya hubungan atau korelasi positif antara konsentrasi dengan
absorbansi. Pada penelitian analitik,grafik kurva standar yang baik ditunjukkan
dengan harga ≥ 0,99.
Adanya logam Besi, Tembaga, dan Zinkum di dalam param tersebut
berasal tanah tempat tumbuh tumbuhan yang digunakan untuk membuat param
tersebut. Dimana tanaman menyerap logam dari tanah tempatnya tumbuh
sehingga logam tersebut terakumulasi dalam tanaman, akumulasi logam dalam
tumbuhan tidak hanya tergantung pada kandungan logam dalam tanah, tetapi juga
tergantung pada letak geografis tanah, unsur kimia tanah, jenis logam, pH tanah
dan spesies tanaman yangn sensitif terhadap logam berat tertentu. Tanah tempat
tumbuhan berkasiat yang digunakan untuk membuat param tersebut tidak
diketahui mengandung pupuk atau pestisida karena sampel tersebut diperoleh
dalam bentuk jadi.
Dari penelitian yang dilakukan diperoleh kadar logam Besi (Fe) dalam
logam Tembaga (Cu) dalam param yang dikonsumsi masing-masing adalah 5,738
mg/kg; 0,786 mg/kg. Kadar Zinkum (Zn) dalam param yang dikonsumsi
masing-masing adalah 12,728 mg/kg; 15,184 mg/kg. Sedangkan kadar Besi (Fe),
Tembaga (Cu), dan Zinkum dalam Param yang digunakan sebagai obat luar
masing-masing adalah 29,36 mg/kg, 32,52 mg/kg, 27,688 mg/kg dan berdasarkan
standar yang ditetapkan Badan Pengawas Obat dan Makanan (BPOM) maka kadar
Fe, Cu, dan Zn dalam param yang digunakan sebagai obat luar dan yang
BAB 5
KESIMPULAN DAN SARAN
5.1. Kesimpulan
1. Dari hasil analisis diperoleh kadar Besi didalam param yang dikonsumsi
adalah 11,814 mg/kg; 25,4 mg/kg, kadar Tembaga didalam param yang
dikonsumsi adalah 0,768 mg/kg; 5,738 mg/kg, kadar Zinkum didalam
param yang dikonsumsi adalah 12,728 mg/kg; 15,184 mg/kg. Dan kadar
Besi, Tembaga, Zinkum didalam param yang digunakan sebagai obat luar
ad alah 29,36 mg/kg; 32,52 mg/kg; 27,688 mg/kg.
2. Dari hasil penelitian diperoleh bahwa kadar Besi, Tembaga, dan Zinkum
dalam param yang digunakan sebagai obat luar dan yang dikonsumsi
masih memenuhi standar yang ditetapkan oleh BPOM.
5.2. Saran
1. Untuk penelitian selanjutnya disarankan untuk melakukan analisa
residu pestisida, aflatoksin, dan cemaran mikroorganisme yang
terkandung didalam param tersebut.
2. Untuk penelitian selanjutnya disarankan untuk menentukan kadar
BAB 2
TINJAUAN PUSTAKA
2.1. Definisi Obat Tradisional
Obat tradisional adalah ramuan bahan yang bisa berasal dari tumbuhan, hewan,
mineral, sediaan sarian atau campuran dari bahan-bahan tersebut yang secara
turun-temurun telah digunakan untuk pengobatan berdasarkan pengalaman (UU
kesehatan No.23/1992). Istilah obat herbal sendiri mengacu pada kata herb yang
berarti tanaman, yaitu obat yang berasal dari tanaman atau tumbuhan. Obat herbal
dapat berasal dari akar, batang, daun, buah, atau biji suatu tanaman. Terdapat tiga
kategori obat herbal yaitu jamu, herbal terstandar, dan fitofarmaka. (Sari et al.
2008). Param termasuk dalam kategori obat herbal jamu.
2.2. Jenis obat tradisional
Berdasarkan keputuan Kepala Badan POM RI No.HK.00.05.4.2411. tentang
ketentuan pokok pengelompokan dan penandaan obat bahan alam Indonesia, obat
tradisional dikelompokkan menjadi tiga yaitu jamu, herbal terstandar, dan
fitofarmaka.
a.jamu (Emphirical Based Herbal Medicine)
Jamu adalah obat tradisional yang berisi seluruh bahan tanaman yang
menjadi penyusun jamu tersebut. Jamu disajikan secara tradisional dalam bentuk
serbuk seduhan, pil, atau cairan. Umumnya obat tradisional ini dibuat dengan
mengacu pada resep peninggalan leluhur. Satu jenis jamu disusun dari berbagai
memerlukan pembuktian ilmiah sampai uji klinis, tetapi cukup dengan bukti
empiris, jamu juga harus memenuhi persyaratan keamanan dan standar mutu.
Jamu yang telah digunakan secara turun-temurun selama berpuluh-puluh tahun
bahkan ratusan tahun telah membuktikan keamanan dan maanfaat secara langsung
untuk tujuan kesehatan tertentu.
b. Obat Herbat Terstandar (Standarized Based Herbal Medicine)
Merupakan obat tradisional yang disajikan dari hasil ekstraksi atau
penyarian bahan alam, baik tanaman obat, binatang, maupun mineral. Dalam
proses pembuatannya, dibutuhkan peralatan yang tidak sederhana dan lebih mahal
dari pada jamu. Tenaga kerjanya pun harus didukung oleh pengetahuan dan
keterampilan membuat ekstrak. Obat herbal ini umumnya ditunjang oleh
pembuktian ilmiah berupa penelitian praklinis. Penelitian ini meliput i
standardisasi kandungan senyawa berkhasiat didalam bahan penyusun,
standardisasi pembuatan ekstrak yang higienis, serta uji toksisitas yang akut
maupun kronis.
c. Fitofarmaka (Clinical Based Herbal Medicine)
Merupakan obat tradisional yang dapat disejajarkan dengan obat modern.
Proses pembuatannya telah terstandar dan ditunjang oleh bukti ilmiah sampai uji
klinis pada manusia. Karena itu, dalam pembuatannya diperlukan peralatan
bertehnologi modern, tenaga ahli, dan biaya yang tidak sedikit.(Suharmiati at
al.2000). Pengobatan tradisional adalah salah satu upaya pengobatan dan
perawatan, diluar kedokteran dan ilmu keperawatan. Pengobatan secara
tradisional ini mencakup cara dan obat yang digunakan mengacu pada
pengetahuan, pengalaman, dan keterampilan yang diperoleh secara turun-temurun.
Karakteristik pengobatan tradisional merupakan upaya kesehatan (pengobatan
dan atau perawatan) dengan cara lain diluar ilmu kedokteran. Berdasarkan
Diterapkan sesuai dengan norma yang berlaku di masyarakat dengan cara yang
tidak bertentangan dengan kepercayaan kepada Tuhan Yang Maha Esa. Dilakukan
untuk mencapai kesembuhan, pencegahan penyakit, pemulihan, dan peningkatan
kesehatan jasmani, rohani, dan sosial masyarakat.(Noorkasiani.2007)
2.3. Obat Tradisional Karo
Obat atau tambar (dalam bahasa karo) adalah obat-obatan karo sebagai suatu
sejarah yang terus berkembang dan berasal dari banyak sumber. Ada obat-obatan
yang diturunkan dari nenek moyang, ada dari mimpi, dan hasil dari pengamatan
sendiri dalam kehidupan sehari-hari. Ada juga obat yang dituliskan nenek
moyang dalam kulit kayu yang disebut dengan pustaka najati.(Ginting. 1999)
Bagian dari tanaman obat yang bisa dimanfaatkan sebagai bahan dalam
pembuatan obat-obatan tradisional adalah akar, batang, daun, bunga, dan buah.
Obat-obatan tradisional yang terdapat pada masyarakat karo yaitu: kuning
(param), tawar, minak alun atau minyak urut, sembur, dan oukup atau mandi uap.
Diantara sekian banyak obat tradisional karo ini param adalah menjadi fokus
dalam penelitian ini.
Param adalah obat tradisional karo yang terbuat dari campuran tepung dan
ramuan yang berkhasiat sebagai obat. Tepung yang biasa digunakan adalah
tepung beras dan ramuan yang berkhasiat sebagai obat adalah bahan atau
campuran dari tanaman seperti akar, batang, daun, bunga, buah, dan lemak hewan
dan juga air. Cara pembuatan param tersebut adalah semua bahan umbi umbian
yang digunakan misalnya jahe, bawang merah, bawang putih, lada, kencur dan
bahan daun-daunan serta bunga tumbuhan dicuci terlebih dahulu kemudian
digiling hingga lumat kemudian bahan yang telah lumat tersebut dicampur dengan
campuran merata kemudian dicetak bulat-bulat dan dikeringkan cara penggunaan
param ini adalah dioleskan ke seluruh tubuh dan dimakan (Bangun. 2010)
2.4. Mineral
Kandungan logam dalam tanah sangat berpengaruh terhadap kandungan logam
dalam tanaman yang tumbuh diatasnya, sehingga kandungan logam yang
berkurang atau berlebihan dalam jaringan tanaman akan mencerminkan
kandungan logam dalam tanah (Darmono. 1995). Dari dalam tanah tumbuhan
hijau menghisap zat-zat tertentu melalui akarnya. Zat-zat ini masuk kedalam
tumbuhan dalam bentuk terlarut didalam air. Zat-zat ini biasanya berupa
garam-garaman dan dinamakan mineral. Mineral ini berlainan halnya dengan bahan
organik seperti karbohidrat, protein, dan lemak tidak dapat dibuat oleh
tumbuh-tumbuhan. Karena itu mineral tergolong bahan tak-organik, yaitu tidak berasal
dari mahluk hidup.
Kalau bahan tumbuhan seperti kayu bakar atau arang kita bakar, akan tersisa
abu. Abu ini terdiri atas bahan mineral yang telah diserap oleh tumbuhan kedalam
bagian tubuhnya. Sewaktu pembakaran, semua bahan organik habis terbakar
menjadi karbon dioksida dan air. Tetapi bahan tak-organik tersisa sebagai
garam-garaman yang bentuknya berupa abu. Didalam abu ini dapat ditemukan antara lain
logam Natrium (Na), Kalsium (Ca), Magnesium (Mg), Seng (Zn), Besi (Fe),
Mangan (Mn), dan Molibden (Mo). Logam-logam ini ada dalam bentuk senyawa
garam Fosfat yang mengandung Fosfor (P), Klorida yang mengandung Klor (Cl),
Yodida yang mengandung Yod (J), Fluorida yang mengandung Fluor (F), atau
Sulfat yang mengandung Sulfur (S).
Kalau kita makan tumbuh-tumbuhan, sudah tentu garam-garam inipun akan
memasuki tubuh kita. Didalam tubuh kita mineral seperti kalsium fosfat terdapat
didalam bagian tubuh seperti tulang dan gigi. Demikian pula mineral seperti besi
adalah suatu protein yang kerjanya mengangkut oksigen di dalam darah ke
seluruh bagian tubuh kita.
Di dalam daun-daunan hijau juga ada protein yang bentuknya hampir sama
dengan hemoglobin, yaitu klorofil. Klorofil atau hijau daun tidak mengandung
logam besi, tetapi logam Magnesium. Selain itu mineral seperti natrium dalam
bentuk garam natrium klorida, kalsium dalam bentuk kalsium hidrofosfat, serta
magnesium, dapat terlarut didalam cairan sel tubuh kita. Perananya mengatur
berbagai proses kehidupan. Kalsium misalnya diperlukan sedikit agar darah dapat
mengggumpal. Demikian pula kalsium berperan dalam peristiwa menegang dan
melemasnya otot seperti otot jantung. Sedangkan magnesium diperlukan sebagai
bahan pembentuk enzim. Natrium dan kalium diperlukan untuk mengatur tekanan
cairan tubuh di dalam sel-sel tubuh.
Jadi, mineral-mineral didalam tubuh kita mempunyai dua macam tugas. Yang
pertama ialah sebagai bahan pembentuk bagian-bagian tubuh, seperti tulang dan
gigi. Yang kedua ialah sebagai zat pengatur kelangsungan hidup. Mineral yang
diperlukan oleh manusia ialah kalsium, fosfor, magnesium, kalium, natrium,
mangan, besi, tembaga, kobalt, yodium, belerang, dan seng. Ada mineral yang
diperlukan dalam jumlah yang cukup banyak, yaitu pada kadar 100 g atau lebih
sehari bagi setiap orang dewasa. Mineral seperti ini disebut unsur hara makro.
Termasuk kedalam golongan ini ialah kalium, natrium, kalsium, fosfor,
magnesium, dan klor. Ada pula mineral yang kita perlukan dalam kadar yang
lebih rendah, yaitu tidak lebih dari beberapa mg setiap hari untuk orang dewasa.
Mineral seperti ini disebut unsur hara mikro. Termasuk kedalam golongan ini
ialah besi, yodium, seng, krom dan flour.(Nasoetion. 1995)
Mineral sangat penting bagi metabolisme tubuh. Mineral dapat diibaratkan
sebagai “busi” dari kehidupan karena mineral diperlukan untuk mengaktifkan
ribuan reaksi enzimatis dalam tubuh. Masing-masing mineral tidak bekerja
sendiri, tetapi bekerja secara seimbang satu sama lainnya. Oleh karena itu, bila
lainnya. Misalnya, kelebihan kalsium akan berakibat hilangnya magnesium dan
seng. Kelebihan natrium dan kalium akan berakibat defisiensi kalsium dan
magnesium. Kelebihan kalsium dan magnesium akan menyebabkan defisiensi
natrium dan kalium. Kelebihan natrium akan menyebabkan kehilangan kalium.
Kelebihan kalium akan berakibat hilangnya natrium. Kelebihan tembaga akan
mengakibatkan kehilangan seng. Kelebihan seng akan berakibat hilangnya
tembaga dan besi. Kelebihan fosfat akan mengakibatkan hilangnya kalsium.
Semuanya itu disebut reaksi berantai defisiensi.(Sembiring. 2000). Disamping
logam-logam yang dijelaskan diatas terdapat juga logam berat.
2.5. Logam Berat
Logam berat adalah unsur alami yang terdapat di kerak bumi dengan densitas
lebih besar dari 5 g/cm3 stabil dan tidak bisa hancur sehingga logam berat
cenderung menumpuk dalam tanah. Beberapa diantaranya berperan penting dalam
kehidupan mahluk hidup dan disebut sebagai hara mikro esensial. Secara biologis
beberapa logam dibutuhkan oleh mahluk hidup pada konsentrasi tertentu dan
dapat berakibat fatal apabila tidak dipenuhi. Oleh karena itu logam-logam tersebut
dinamakan logam atau mineral-mineral esensial tubuh tetapi jika
logam-logam esensial tersebut masuk kedalam tubuh dalam jumlah berlebihan akan
berubah fungsi menjadi racun bagi tubuh. Bahwa semua logam berat dapat
menjadi racun yang akan meracuni tubuh mahluk hidup. Logam berat masuk
kedalam jaringan tubuh mahluk hidup melalui beberapa jalan, yaitu saluran
pernapasan, pencernaan, dan penetrasi melalui kulit.
Beberap logam berat diantaranya adalah zinkum (Zn), besi (Fe), tembaga (Cu),
nikel (Ni), mangan (Mn), titanium (Ti), tungsten (W), vanadium (V), timah (Sn),
Arsenik (As), kobalt (Co). Uraian berikut ini adalah mengenai Fe, Cu, dan Zn
2.6. Logam Besi
Analisa logam besi secara kualitatif menggunakan reaksi warna yang terkenal
adalah reaksi dengan CNS- reaksi ini sensitif dan digunakan sebagai reaksi
pengenal Fe, secara kuantitatif Fe dapat ditentukan dengan spektrometri, zat besi
adalah gizi penting bagi tubuh manusia. Seorang pria dewasa yang sehat memiliki
zat besi sebanyak 40 -50 mg per kilogram berat badan. Wanita dewasa yang sehat
memiliki zat besi sebanyak 35-50 mg per kilogram berat badan. Dalam hal
tertentu, wanita lebih rentan saat mengalami kekurangan zat besi. Zat besi
berfungsi membawa oksigen dari paru-paru ke seluruh jaringan tubuh. Zat besi
menyatu dengan oksigen didalam paru-paru dan melepaskan oksigen pada
jaringan-jaringan yang memerlukan. Zat besi juga berperan dalam fungsi normal
kekebalan tubuh.
Besi dalam daging berada dalam bentuk hem yang mudah diserap. Besi
non hem dalam tumbuhan tidak mudah diserap, sebagian karena tumbuhan sering
kali mengandung oksalat, fitat, tanin, dan senyawa fenolik lain yang membentuk
kelat atau presifitat dengan besi yang tidak mudah larut. Besi diserap dalam
bentuk fero ( Fe2+). Karena bersifat toksik, di dalam tubuh besi bebas biasanya
terikat ke protein. Besi diangkut didalam darah (sebagai Fe3+) oleh
protein,apotransferin. Besi membentuk kompleks dengan apotransferin menjadi
transferin. Besi dioksidasi dari Fe2+ menjadi Fe3+ oleh feroksidase yang dikenal
sebagai seruloplasmin (enzim yang mengandung tembaga). Tingkat saturasi
transferin oleh besi biasanya hanya sepertiga. Kapasitas total darah mengikat besi,
yang terutama disebabkan oleh kandungan transferinnya adalah sekitar 300
µg/dL.(Marks. 1996)
Zat besi heme berasal dari hemoglobin dan mioglobin yang terdapat dalam
darah bahan makanan hewani. Sementara itu, umumnya, zat besi non heme
terdapat dalam bahan makanan tumbuh-tumbuhan. Zat besi non-heme, terdapat
dalam bentuk kompleks anorganik (Fe3+). Absorpsi besi non-heme sangat
terdapat didalam bahan makanan yang dikonsumsi. Sementara itu zat besi heme
tidak dipengaruhi oleh faktor penghambat. Karena itu jumlah zat besi heme yang
dapat diabsorpsi lebih banyak dari pada zat besi dalam betuk non-heme. Dari
berbagai penelitian, dibuktikan bahwa besi heme yang dapat diserap hampir 30%,
sedangkan besi non heme hanya dapat diserap sekitar 5%. (Anwar. 2009)
Kekurangan zat besi akan membuat badan kita mudah terkena penyakit.
Selain,itu karena zat gizi besi (Fe) merupakan inti molekul hemoglobin yang
merupakan unsur utama dalam sel darah merah, maka kekurangan pasokan zat
gizi besi menyebabkan menurunnya produksi hemoglobin. Akibatnya
menyebabkan pengecilan ukuran (microcytic), rendahnya kandungan hemoglobin
(hypocromic), serta berkurangnya sel darah merah. Penderita mengalami gejala
umum berupa “5L” disertai pucat, kesemutan, mata berkunang-kunang, jantung
berdegup kencang, kurang bergairah. Gejala-gejala orang yang mengalami anemia
defisiensi zat besi adalah kelelahan, lemas, pucat, kurang bergairah, nyeri dada
dan mudah berdebar, pada anemia yang kronis menentukan bentuk kuku seperti
sendok dan rapuh, pecah-pecah pada sudut mulut, lidah lunak dan sulit menelan,
sakit kepala dan mudah marah,sulit bernapas, tidak mampu berkonsentrasi dan
rentan terhadap infeksi.(Atkins.2007)
Tubuh cenderung sebisa mungkin menyimpan kelebihan zat besi. Sangat
sedikit zat besi yang dibuang atau diekskresikan oleh tubuh. Kelebihan zat besi
akan terus disimpan di dalam jaringan dan bagian tubuh dan berakumulasi
meningkatkan kadar racun. Pada jangka panjang akan meningkatkan resiko
terjadinya diabetes, sakit jantung, kerusakan hati, artritis, alzhaimer, kanker limpa,
dan kematian mendadak pada bayi, serta juga beberapa gejala kelainan seperti
konstipasi, rambut rontok, hipotiroid, hiperaktif, meningkatkan resiko terjadinya
2.7. Logam Tembaga
Tembaga merupakan logam berat yang dijumpai pada perairan alami dan
merupakan esesensial bagi tumbuhan dan hewan. Pada tumbuhan tembaga
berperan sebagai penyusun plastocyanin yang berfungsi dalam transfor elektron
dalam proses fotosintesis,kadar tembaga dalam kerak bumi kira-kira 50
mg/kg.(Effendi.2003). Tubuh manusia mengandung 1,5-2,5 mg tembaga (Cu) per
kilogram berat badan bebas lemak mineral ini tersebar diseluruh jaringan tubuh,
namun hati, otak, jantung, dan ginjal mengandung Cu dalam jumlah yang lebih
banyak. Dalam darah, tembaga terdapat dalam jumlah yang kira-kira sama pada
plasma dan eritrosit. Plasma mengandung sekitar 110 mcg/100ml dan eritrosit 115
mcg/100ml.(Suhardjo et al. 1992)
Tembaga berperan khususnya dalam beberapa kegiatan enzim pernapasan
sebagai kofaktor bagi enzim tirosinase dan sitokhrom oksidase. Tirosinase
mengkatalisis reaksi oksidasi tirosin menjadi pigmen melanin (pigmen gelap pada
kulit dan rambut). Tembaga juga diperlukan dalam proses pertumbuhan sel-sel
darah merah yang masih muda. Bila kekurangan tembaga, sel darah merah yang
dihasilkan akan berkurang. Tembaga diserap dari usus kecil kedalam saluran
darah, tempat sebagian besar jaringan bergabung pada seruplasmin, yaitu protein
yang berfungsi dalam penggunaan besi.(Winarno. 1995)
Kebutuhan tembaga sehari minimal adalah rendah (ditaksir 1-2 mg),
sedangkan makanan manusia umumnya memberikan 2-4 mg Cu sehari. Tembaga
ditemukan bersama dengan unsur-unsur lainnya dikebanyakan bahan makanan.
Kadar tembaga dalam serum yang rendah dapat berkaitan dengan adanya
defisiensi protein seperti kwashiorkor, nefrotik sindron, dan disproteinemia.
Jarang sekali defisiensi tembaga karena konsumsi makanannya, meskipun
dilaporkan sementara peneliti adanya anemia pada anak-anak karena kekurangan
Kelebihan tembaga mengakibatkan penyakit wilson yang merupakan kelainan
metabolisme tembaga yang paling penting. Ini diturunkan sebagai autosomal
resesif; tembaga terakumulasi dalam hati, ginjal, mata, dan ganglia basalis otak.
Akumulasi tembaga didalam hati dihubungkan dengan hepatitis kronis yang
sering berakhir sebagai sirosis.(Underwood.1996)
2.8.. Logam Seng
Seng diperlukan oleh tubuh untuk proses metabolisme tetapi dalam kadar tinggi
dapat bersifat sebagai racun. Dalam tubuh manusia terkandung 2 gram seng,
terutama terdapat pada rambut, tulang, mata, dan kelenjar alat kelamin pria. Seng
merupakan komponen penting dari berbagai enzim. Paling sedikit 15-20
metalo-enzim yang mengandung seng telah diisolasi dan dimurnikan. Salah satu
contohnya adalah enzim karbonat anhidrase yang terdapat dalam sel darah merah.
Disamping itu seng juga terdapat dalam karboksi peptidase dan dehidrogenase
dalam hati. Sebagai kofaktor, seng dapat meningkatkan keaktifan enzim
lainnya.(Winarno. 1995)
Jumlah mineral Zn dalam tubuh kira-kira 20 mg per kilogram berat badan
bebas lemak. Hampir semua seng darah berada dalam eritrosit yaitu 1200-1300
mcg/100ml sedangkan dalam serum hanya 120 mcg/100ml. Anhidrase karbonik
yang berpusat dalam darah merah mengandung sekitar 0,33 persen seng,
sementara itu insulin kristal mengandung seng dengan persentase kurang lebih
sama. Kekurangan atau defisiensi seng menyebabkan gangguan pertumbuhan,
terhambatnya pematangan seksual, mudah terkena infeksi, diare, gangguan kulit,
anemia, kehilangan nafsu makan, serta menurunnya kemampuan indra perasa dan
2.9.Metode Destruksi
Destruksi merupakan suatu cara perlakuan (perombakan) senyawa menjadi
unsur-unsur sehingga dapat dianalisis. Metode destruksi materi organik dapat dilakukan
dengan dua cara yang selama ini dikenal yaitu metode destruksi basah dan metode
destruksi kering. Pada dasarnya pemilihan metode destruksi tersebut adalah
berdasarkan sifat organik dalam bahan, mineral yang akan dianalisa serta
sensitivitas yang digunakan. Berdasarkan kedua metode destruksi ini, sudah tentu
memiliki tehnik pengerjaan yang berbeda pula. Penguraian sampel dengan
asam-asam kuat baik tunggal maupun campuran dikenal dengan metode destruksi basah
sedangkan penguraian sampel dengan cara pengabuan sampel dalam tanur dikenal
sebagai metode destruksi kering. (Aprianto. 1989)
2.9.1. Destruksi Basah
Metode destruksi basah dilakukan dengan memanaskan sampel (sampel organik
dan biologis) dengan adanya asam pekat atau bahkan campuran dari
asam-asam tersebut. Jika asam-asam yang digunakan cukup untuk mengoksidasi, maka
sampel dipanaskan dalam suhu yang cukup tinggi, dan jika pemanasan dilanjutkan
dalam waktu yang lama, maka sebagian besar sampel telah teroksidasi dengan
sempurna. (Almatsier.1987)
Destruksi basah digunakan untuk sampel dalam usaha penentuan trace
elemen dan logam-logam beracun. Prinsip dari destruksi basah ini adalah
menambahkan reagen kimia tertentu ke dalam sampel sebelum dilakukan
pengabuan. Berbagai reagen kimia yang sering digunakan untuk destruksi basah
ini adalah sebagai berikut :
1. Asam sulfat sering ditambahkan ke dalam sampel untuk membantu
mempercepat terjadinya reaksi oksidasi. Asam sulfat adalah bahan
pengoksidasi yang kuat, meskipun demikian waktu yang diperlukan untuk
2. Campuran H2SO4 dan K2SO4 dapat digunakan untuk mempercepat
dekomposisi sampel. K2SO4 akan menaikkan titik didih H2SO4 sehingga
suhu pengabuan dapat dipertinggi dan proses pengabuan dapat lebih cepat.
3. Campuran H2SO4 dan HNO3 banyak digunakan untuk mempercepat proses
pengabuan. Kedua asam ini merupakan oksidator yang kuat. Dengan
penambahan oksidator ini akan menurunkan suhu destruksi sampel yaitu
pada suhu 350oC, sehingga komponen yang dapat menguap pada suhu
yang tinggi dapat tetap dipertahankan dalam abu yang berarti penentuan
kadar abu lebih baik.
4. Penggunaan HClO dan HNO3 dapat digunakan untuk sampel yang sangat
sulit mengalami oksidasi. Dengan HClO yang merupakan oksidator yang
sangat baik memungkinkan pengabuan dapat dipercepat. Kelemahan
HClO ini adalah mudah meledak sehingga cukup berbahaya, untuk itu
harus sangat hati-hati dalam pengguaannya. Pengabuan dengan
menggunakan HClO dan HNO3 dapat berlangsung sangat cepat yaitu
dalam 10 menitsudah dapat selesai.(Sudarmadji et al. 1989)
2.9.2. Destruksi Kering
Penentuan kadar abu adalah dengan mengoksidasikan semua zat organik pada
suhu yang tinggi, yaitu sekitar 500-600oC dan kemudian ditimbang zat yang
tertinggal setelah proses pembakaran tersebut. Bahan yang mempunyai kadar air
tinggi sebelum pengabuan harus dikeringkan terlebih dahulu. Bahan yang
mempunyai kandungan zat yang mudah menguap dan berlemak banyak
pengabuan dilakukan dengan suhu mula-mula rendah sampai asap hilang, baru
kemudian dinaikkan suhunya sesuai dengan yang dikehendaki. Untuk bahan yang
membentuk buih waktu dipanaskan harus dikeringkan dulu dalam oven dan
ditambahkan zat anti buih misalnya olive atau parafin. Bahan yang akan diabukan
ditempatkan dalam wadah khusus yang disebut krusibel yang dapat terbuat dari
porselin, silika, quartz, nikel, platina dengan berbagai kapasitas (25-100 ml) dan
pengabuan harus diperhatikan sungguh-sungguh karena banyak element abu yang
dapat menguap pada suhu yang tinggi.
Lama pengabuan tiap bahan berbeda-beda dan berkisar antara 2-8 jam.
Pengabuan dianggap selesai apabila diperoleh sisa pengabuan yang umumnya
berwarna putih abu-abu dan beratnya konstan dengan selang waktu pengabuan 30
menit. Penimbangan terhadap bahan dilakukan dalam keadaan dingin, untuk itu
maka cawan krusibel yang berisi abu yang diambil dari dalam alat pengabuan
(muffle) harus lebih dahulu dimasukkan ke dalam oven bersuhu 105oC agar
suhunya turun, baru kemudian dimasukkan ke dalam desikator sampai dingin.
Desikator yang digunakan harus dilengkapi dengan zat penyerap uap air misalnya
silika gel atau kalsium klorida, natrium hidroksida. Penentuan abu yang tidak larut
dalam asam dilakukan dengan mencampurkan abu dalam asam klorida 10%.
Setelah diaduk kemudian dipanaskan selanjutnya disaring dengan kertas whatman
no.42. Residu merupakan abu yang tidak larut dalam asam yang terdiri atas pasir
dan silika. Apabila abu banyak mengandung bahan jenis ini maka dapat
diperkirakan proses pencucian bahan tidak sempurna ataupun terjadinya
kontaminasi dari tanah selama proses pengolahan bahan tersebut.
Penentuan abu yang larut dalam air dilakukan dengan melarutkan abu ke
dalam akuades kemudian disaring. Filtrat kemudian dikeringkan dan ditimbang
residunya. Abu yang larut dalam air ini kadang-kadang digunakan sebagai indeks
kandungan buah didalam jelly dan buah-buahan yang diawetkan. Cara yang
umum dalam penentuan abu yang larut adalah dengan mengabukan residu yang
terdapat dalam kertas saring bebas abu pada perlakuan diatas. Penentuan tahap
kedua adalah penentuan individu mineral yang ada di dalam abu. Banyak cara
yang dapat dipakai dalam penentuan mineral ini yaitu antara lain secara kimia dan
secara spektrofotometri. Untuk cara kimia memerlukan waktu yang cukup lama
sedangkan cara spektrofotometri cukup cepat dan memiliki ketelitian yang
2.10. Spektrofotometri Serapan Atom
Spektrofotometri Serapan Atom merupakan suatu metode analisa kuantitatif
dimana metode ini sangat tepat untuk analisis zat pada konsentrasi rendah dimana
metode Spektrofotometri Serapan Atom ini berprinsip pada absorpsi cahaya oleh
atom yaitu jika suatu larutan yang mengandung suatu garam logam (suatu
senyawa logam) dihembuskan kedalam suatu nyala (misalnya asetilena yang
terbakar di udara), dapatlah terbentuk uap yang mengandung atom-atom logam
ini. Beberapa atom logam dalam gas ini dapat dieksitasi ke tingkatan energi yang
cukup tinggi untuk memungkinkan pemancaran radiasi yang karakteristik dari
logam tersebut, atom logam bentuk gas itu normalnya tetap berada dalam keadaan
tak tereksitasi, atau dengan perkataan lain,dalam keadaan dasar. Atom-atom
keadaan dasar ini mampu menyerap energi cahaya yang panjang gelombang
resonansinya khas dengannya, yang pada umumnya adalah panjang gelombang
radiasi yang akan dipancarkan atom-atom itu bila tereksitasi dari keadaan dasar.
Jadi jika cahaya dengan panjang gelombang resonansi itu dilewatkan nyala yang
mengandung atom-atom yang bersangkutan, maka sebagian cahaya itu akan
diserap, dan jauhnya penyerapan akan berbanding lurus dengan banyaknya atom
keadaan dasar yang berada dalam nyala.(Basset.1994)
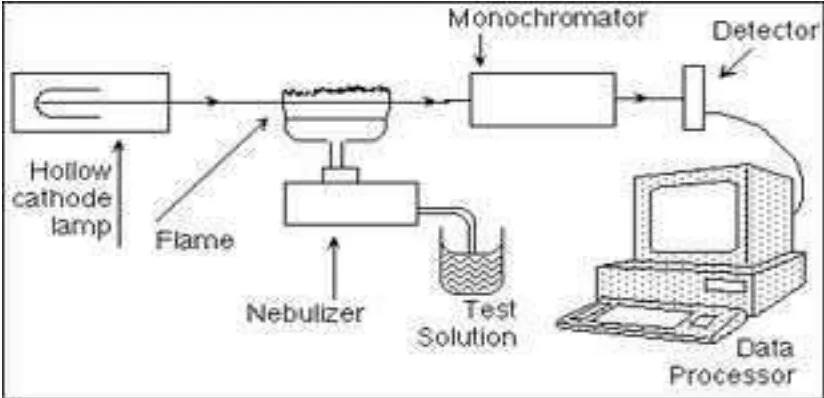
Suatu spektrofotometer serapan atom terdiri atas komponen-komponen berikut ini
:
1. Sumber cahaya.
Lampu katoda berongga yang dilapisi dengan unsur yang sedang
dianalisa.
2. Nyala.
Nyala biasanya berupa udara/asetilen, menghasilkan suhu ± 2500oC.
Dinitrogen oksida/asetilena dapat digunakan untuk menghasilkan suhu
sampai 3000oC, yang diperlukan untuk menguapkan garam-garam dari
unsur-unsur.
3. Monokromator.
Monokromator digunakan untuk mnyempitkan lebat pita radiasi yang
sedang dipancarkan oleh lampu katoda berongga . Ini menghilangkan
interferensi oleh radiasi yang dipancarkan dari nyala tersebut, dari gas
pengisi didalam lampu katoda berongga, dan dari unsur-unsur lain di
dalam sampel tersebut.
4. Detektor.
Berupa sel fotosensitif (Watson,D.G.2007)
Keuntungan yang diperoleh dalam menggunakan spektrofotometri serapan atom
adalah bahwa metode ini dapat menentukan hampir semua unsur logam dan dapat
melakukan analisa logam walaupun sampel dalam bentuk campuran. Sedangkan
kerugian dari metode tersebut adalah bahwa lampu katoda harus selalu diganti
2.11. Inductively Couple Plasma
Inductively Couple Plasma-Optical Emission (ICP-OES) adalah sebuah metode
analisa renik, dengan sensitivitas mulai dari sub-ppb sampai 100 ppb, dengan
ketepatan yang mencapai 10%. Lebih baik dari ketepatan 1% yang dapat
diperoleh dengan menggunakan metode kalibrasi.(Holloway.2010). Prinsip umum
pada pengukuran ini adalah mengukur intensitas energi atau radiasi yang
dipancarkan oleh unsur-unsur yang mengalami perubahan tingkat energi atom
(eksitasi atau ionisasi), metode ICP-OES telah digunakan secara luas dan sangat
terkenal karena alat tersebut dapat menganalisa multi-element. Dasar dari
pengukuran ICP-OES adalah dari cahaya yang ditransmisikan oleh unsur yang ada
didalam sampel yang dimasukkan ke plasma yang akan dihasilkan sebagai aerosol
didalam sebuah nebulizer atau spray chamber. Suhu yang tinggi didalam plasma
merupakan persediaan energi untuk menguapkan pelarut, menghilangkan bagian
matrik sampel, dan menaikkan atom kedalam bentuk eksitasinya. Intensitas
cahaya yang ditransmisikan berhubungan dengan nomor atom dalam plasma dan
konsentrasi analit dalam sampel. (Postawa.2012)
Keuntungan lain dari ICP karena menggunakan gas argon dengan tekanan
atmospher untuk proses atomisasi sampel dan efisiensi dari eksitasi atom. Plasma
ini memiliki energi tinggi yang terdiri dari ionisasi gas inert. Temperaturnya
kira-kira (7000-10.000 K) yang dapat menghasilkan proses atomisasi yang luar biasa
(misalnya untuk penguraian senyawa kompleks dalam sampel menjadi individu
atom) diikuti dengan eksitasi atom yang efisien. Karakteristik dari plasma ini
menghasilkan kemampuan untuk mengnalisa senyawa yang sulit terurai (sulit
mengalami atomisasi) dan dengan potensial eksitasi yang sulit tereksitasi dengan
BAB I
PENDAHULUAN
1.1. Latar Belakang
Indonesia merupakan negara tropis yang kaya akan berbagai spesies tanaman.
Dari 40.000 jenis tanaman yang tumbuh didunia, 30.000 jenis diantaranya tumbuh
di Indonesia dan 26% telah dibudidayakan, sementara sisanya masih tumbuh liar.
Kurang lebih terdapat sekitar 940 jenis tumbuhan yang mempunyai khasiat obat
dari tanaman yang telah dibudidayakan dan baru sekitar 250 jenis yang sudah
dimanfaatkan sebagai obat. Kandungan dan komposisi zat aktif setiap tanaman
dapat berbeda-beda sehingga antara tanaman obat yang satu dengan yang lainnya
mempunyai efek yang berbeda pula. (Sari. 2008)
Kekayaan spesies tanaman ini termasuk kekayaan keanekaragaman obat
tradisional atau lebih sering dikenal tanaman herbal. Obat tradisional telah dikenal
dan banyak digunakan secara turun-temurun oleh masyarakat. Umumnya,
pemanfaatan obat tradisional lebih diutamakan sebagai upaya untuk menjaga
kesehatan.
Popularitas dan perkembangan obat tradisional kian meningkat seiring
dengan slogan “kembali ke alam” yang kian menggema. Dalam penggunaan obat
tradisional ada beberapa aspek mutu yang perlu diperhatikan dalam membuat
ataupun mengkonsumsi obat tradisional menurut keputusan Kepala Badan
Pengawas Obat dan Makanan Republik Indonesia Nomor : HK.00.05.4.2411
Tahun 2004 antara lain cemaran logam berat, residu pestisida, aflatoksin, dan
cemaran mikroorganisme. Di masyarakat karo obat tradisional juga digunakan
masyarakat diantaranya adalah param, param digunakan untuk menjaga kesehatan
luar dan dapat dikonsumsi juga. Param tersebut dibuat dari daun, bunga, buah dan
biji tumbuh-tumbuhan. Dimana didalam tumbuh-tumbuhan selain terkandung zat
aktif organik juga terkandung logam dimana logam tersebut ada yang termasuk
logam-logam berbahaya yaitu logam berat yang berasal dari tanah yang diserap
oleh tumbuhan apabila param tersebut digunakan dalam waktu yang cukup lama
maka logam tersebut dapat terakumulasi didalam tubuh manusia dan dapat
menimbulkan efek samping walaupun efek yang ditimbulkannya tersebut tidak
langsung dirasakan karena logam yang terakumulasi tersebut pelan-pelan dapat
menimbulkan penyakit dan merusak organ tubuh. Param yang digunakan sebagai
obat oleh masyarakat Karo ini ada dua macam yaitu pertama hanya digunakan
sebagai obat luar dan yang kedua dapat dikonsumsi. Analisis dan penentuan
logam dapat dilakukan dengan metode Spektroskopi Nyala antara lain
Spektroskopi Serapan Atom dan Inductively Coupled Plasma Spektrometry (ICP).
ICP dapat melakukan analisis kualitatif dan kuantitatif logam dalam jumlah
sampai 45 unsur sekali analisis atau penentuan tetapi alat ini mahal,
operasionalnya agak sulit dibandingkan SSA. SSA adalah metode penentuan
logam yang paling banyak digunakan karena operasi alat tersebut lebih mudah,
cepat dan sensitif dan dapat menentukan logam berat dalam kisaran ppm.
Berdasarkan latar belakang tersebut peneliti tertarik untuk menganalisis
kandungan logam dalam param. Analisa kandungan logam didalam param secara
kualitatif dilakukan dengan ICP dan penentuan logam dalam param dengan
menggunakan metode Spektrofotometri Serapan Atom karena metode ini lebih
sensitif dan spesifik dalam menentukan kadar logam dalam sampel yang berisi
berbagai macam senyawa.
1.2.Permasalahan
1. Apakah param yang dikonsumsi dan yang digunakan sebagai obat luar
mengandung logam Fe, Cu dan Zn ?
3. Apakah kadar logam yang terkandung di dalam param tersebut masih
memenuhi standar ambang batas menurut BPOM ?
1.3.Pembatasan Masalah
1. Param yang dijadikan sampel didalam penelitian ini adalah param yang
digunakan sebagai obat luar dan yang dikonsumsi, diambil dari tiga daerah
yang berbeda di Tanah Karo Yaitu Desa Serdang, Seribujandi, dan
Tigapanah.
2. Penentuan kandungan logam Fe, Cu, dan Zn dilakukan dengan metode
Spektrofotometri Serapan Atom.
1.4.Tujuan Penelitian
1. Penelitian ini bertujuan untuk mengetahui kadar logam berat Fe, Cu, dan
Zn dari param yang digunakan sebagai obat luar dan yang dikonsumsi.
2. Penelitian ini bertujuan untuk mengetahui kadar Fe, Cu, dan Zn dari param
tersebut masih sesuai dengan standart yang ditetapakan oleh Badan
Pengawas Obat dan Makanan (BPOM).
1.5. Manfaat Penelitian
Penelitian ini diharapkan memberikan informasi ilmiah yang bermanfaat bagi
masyarakat khususnya masyarakat Karo mengenai kadar kandungan logam Fe,
Cu, dan Zn yang ada didalam param juga penelitian ini dapat menjadi data dasar
1.6. Lokasi Penelitian
Penelitian ini dilakuka n di Laboratorium Kimia Analitik Fakultas Matematika
dan Ilmu Pengetahuan Alam Universitas Sumatera Utara dan di Laboratorium
Terpadu Universitas Sumatera Utara.
1.7. Metodologi Penelitian
1. Penelitian ini merupakan eksperimen laboratorium.
2. Sampel param yang digunakan diambil secara purposif dari Desa Tigapanah,
Desa Serdang, dan Desa Seribujandi.
3. Untuk penentuan Fe, Cu, dan Zn sampel terlebih dahulu didestruksi kering.
4. Kandungan Fe, Cu, dan Zn di dalam sampel ditentukan dengan menggunakan
SSA dengan panjang gelombang untuk Fe=248,3 nm, Cu=324.75 nm, dan
ANALISIS KANDUNGAN LOGAM BESI (Fe), TEMBAGA (Cu), DAN ZINKUM (Zn) DIDALAM OBAT TRADISIONAL PARAM
ABSTRAK
THE ANALYSIS OF CONTENT IRON (Fe), CUPRUM (Cu), AND ZINK (Zn) IN TRADITIONAL MEDICINE
ABSTRACT
ANALISIS KANDUNGAN LOGAM BESI (Fe), TEMBAGA (Cu),
DAN ZINKUM (Zn) DIDALAM OBAT TRADISIONAL PARAM
SKRIPSI
DESTARIA BRAHMANA
090802044
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGEAHUAN
ALAM
ANALISIS KANDUNGAN LOGAM BESI (Fe), TEMBAGA (Cu), DAN ZINKUM (Zn) DIDALAM OBAT TRADISIONAL PARAM
SKRIPSI
Diajukan untuk melengkapi tugas dan memenuhi syarat mencapai gelar sarjana sains
DESTARIA BRAHMANA 090802044
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGEAHUAN ALAM UNIVERSITAS SUMATERA UTARA
PERNYATAAN
ANALISIS KANDUNGAN LOGAM BESI (Fe), TEMBAGA (Cu), DAN ZINKUM (Zn) DIDALAM OBAT TRADISIONAL PARAM
SKRIPSI
Saya mengakui bahwa skripsi ini adalah hasil kerja saya sendiri, kecuali beberapa kutipan dan ringkasan yang masing-masing disebutkan sumbernya.
Medan, Januari 2014
PERSETUJUAN
Judul : ANALISIS KANDUNGAN BESI (Fe), TEMBAGA (Cu), DAN ZINKUM (Zn) DIDALAM OBAT TRADISIONAL PARAM
Kategori : SKRIPSI
Nama : DESTARIA BRAHMANA NIM : 090802044
Program Studi : SARJANA ( S1 ) KIMIA Departemen : KIMIA
Fakultas : MATEMATIKA DAN ILMU PENGETAHUAN ALAM (FMIPA) UNIVERSITAS SUMATERA UTARA
Disetujui di, Medan, Januari 2014
Komisi Pembimbing
Dosen Pembimbing II Dosen Pembimbing I
Prof.Dr.Zul Alfian Prof.Dr.Harlem Marpaung NIP 195504051983031002 NIP194804141974031001
Diketahui / disetujui oleh
Departemen Kimia FMIPA USU
Ketua
PENGHARGAAN
ANALISIS KANDUNGAN LOGAM BESI (Fe), TEMBAGA (Cu), DAN ZINKUM (Zn) DIDALAM OBAT TRADISIONAL PARAM
ABSTRAK
THE ANALYSIS OF CONTENT IRON (Fe), CUPRUM (Cu), AND ZINK (Zn) IN TRADITIONAL MEDICINE
ABSTRACT
e. Larutan KMnO4 0,1 N
4.1.3..3.1. Penentuan Kadar Cu Metode SSA 39 dalam mg/L
4.1.3.3.2. Penentuan Kadar Cu Metode SSA 40 dalam mg/kg
4.1.4. Logam Zinkum 40
4.1.4.1. Penurunan Persamaan Garis Regresi 40 4.1.4.2. Penentuan Koefisien Korelasi Zn 42 4.1.4.3. Penentuan Kadar Zn Dalam Sampel 43 4.1.4.3.1. Penentuan Kadar Zn Metode SSA 43
dalam mg/L
4.1.4.3.2. Penentuan Kadar Zn Metode SSA 44 dalam mg/kg
4.2. Pembahasan 44
Bab 5. Kesimpulan dan Saran
5.1. Kesimpulan 47
5.2. Saran 47
DAFTAR TABEL
Nomor Judul Halaman Tabel
4.1. Data hasil analisa kualitatif sampel dengan ICP-OES 31
4.2. Data pengukuran absorbansi larutan seri standar Besi 32
4.3. Data pengukuran absorbansi larutan seri standar tembaga 36
DAFTAR GAMBAR
Nomor Judul Halaman Gambar
2.1. Bagan Alat Spektrofotometer Serapan Atom 18
4.1. Kurva Kalibrasi Larutan Seri Standar Fe 34
4.2. Kurva Kalibrasi Larutan Seri Standar Cu 38
DAFTAR LAMPIRAN
Nomor Judul Halaman Lamp
1. Kondisi Alat SSA Pada Pengukuran Konsentrasi Fe 51 2. Data Hasil Pengukuran Absorbansi Larutan Seri Standar Fe 51
dengan Spektrofotometer Serapan Atom
3. Data kadar Fe dalam param yang digunakan sebagai obat 51 luar dan yang dikonsumsi
4. Kondisi Alat SSA Pada Pengukuran Konsentrasi Cu 52 5. Data Hasil Pengukuran Absorbansi Larutan Seri Standar Cu 52
dengan Spektrofotometer Serapan Atom
6. Data Kadar Cu dalam yang digunakan sebagai obat 52 luar dan yang dikonsumsi
7. Kondisi Alat SSA Pada Pengukuran Konsentrasi Zn 53 8. Data Hasil Pengukuran Absorbansi Larutan Seri Standar Zn 53
Dengan Spektrofotometer Serapan Atom