39
LAMPIRAN 1
DATA HASIL PENELITIAN
L1. 1 DATA HASIL PENELITIAN
Berikut merupakan data hasil penelitian ekstraki biji sirsak (Annona muricata
L) yang telah dilakukan :
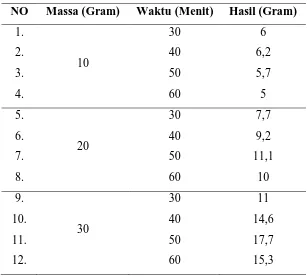
Tabel L1. 1 Data Hasil Penelitian
NO Massa (Gram) Waktu (Menit) Hasil (Gram) 1. 2. 3. 4. 10 30 40 50 60 6 6,2 5,7 5 5. 6. 7. 8. 20 30 40 50 60 7,7 9,2 11,1 10 9. 10. 11. 12. 30 30 40 50 60 11 14,6 17,7 15,3
40
LAMPIRAN 2
CONTOH HASIL PERHITUNGAN
L2. 1 PERHITUNGAN %YIELD EKSTRAK BIJI SIRSAK
Untuk menghitung %Yield yang diperoleh maka digunakan persamaan L2.1 di bawah ini:
% yield= Whasil
Wsampel x 100% L2.1
Diketahui data :
Massa sampel : 10 gram Massa hasil : 6, 2 gram
Maka :
% yield= 6, x 100% = 6 %
Perhitungan yang sama dilakukan untuk data lainnya sehingga diperoleh %Yield seperti pada tabel L2.1 di bawah ini :
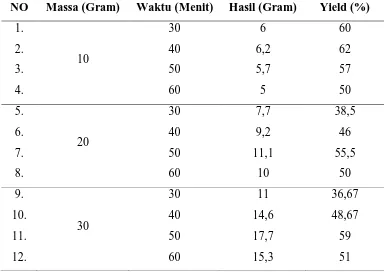
Tabel L2.1 Data %Yield Hasil Ekstraksi Biji Sirsak
NO Massa (Gram) Waktu (Menit) Hasil (Gram) Yield (%) 1. 2. 3. 4. 10 30 40 50 60 6 6,2 5,7 5 60 62 57 50 5. 6. 7. 8. 20 30 40 50 60 7,7 9,2 11,1 10 38,5 46 55,5 50 9. 10. 11. 12. 30 30 40 50 60 11 14,6 17,7 15,3 36,67 48,67 59 51
41
LAMPIRAN 3
FOTO HASIL PENELITIAN
L3.1 TAHAP PENDAHULUAN
Gambar L3.1 Biji Sirsak Sebelum Pengeringan
Gambar L3. 2 Biji Sirsak Setelah Proses Pengeringan
42
Gambar L3.3 Inti Biji Sirsak
Gambar L3.4 Inti Biji Sirsak Setelah Proses Penggilingan
43 L3.2 TAHAP EKSTRAKSI
Gambar L3.5 Rangkaian Peralatan Ekstraksi Sokletasi
L3. 3 TAHAP PEMURNIAN
Gambar L3.6 Rangkaian Peralatan Distilasi
44 L3. 4 HASIL PENELITIAN
Gambar L3.7 Hasil Ekstraksi
35
DAFTAR PUSTAKA
[1] M.A. Tijjani., F.I Abdurrahman., Muhammad Idris, “Evaluation of Proximate and Phytochemical Composition of Leaves Annona Senegalensis Pers’’, Journal of Pharmaceutical and Scientific Innovation II (Januari, 2013),
hal.7 – 9.
[2] Rifki Brahmono Idrus, Nurhayati Bialangi, La. Alio. “Isolasi dan Karakterisasi Alkaloid dari Biji Tumbuhan Sirsak (Annona muricata L).’’ Skripsi, Program Sarjana Fakultas MIPA UNG, Gorontalo, 2012, hal. 21
[3] Galih Prihasetya Hermawan, Hendrawan Laksono, “ Ekstraksi Daun Sirsak (Annona muricata L) menggunakan Pelarut Etanol”, Jurnal Teknologi Kimia dan
Industri II (April, 2013), hal.111-115.
[4] Mulyawati, A.P, Hayati E.K, Nashihuddin A, Tukimin, “ Uji Efektivitas dan Identifikasi Senyawa Ekstrak Biji Sirsak (Annona muricata Linn) yang Bersifat Bioaktif Insektisida Nabati terhadap Hama Thrips”, Alchemy II (Oktober, 2010),
hal. 104-157.
[5] Jessica Le Ven e.t all, “Identification of the Environmental Neurotoxins Annonaceous Acetogenins in and Annona Cherimolia Mill. Alcoholic Beverage Using HPLC-ESI-LTQ-Orbitrap”. Journal of Agricultural and Food Chemistry IV
(Augustus 2014), hal. 27 – 29.
[6] Ragasa Consolacion Y, e.t all. “Acetogenins from Annona Muricata”.
Phcog J IV ( November – Desember 2012), hal. 32-38.
[7] Ika Fidianingsih, Ety Sari Handayani, “Annona muricata Aqueous Extract Suppresses T47D Breast Cancer Cell Proliferation”. Universa Medicina, XXXIII
(January – April 2014), hal. 19-26.
[8] Nik Nurul Najihah, et al., “ Optimization of Soxhlet Extraction Parameter of Annona muricata Leaves Using Box-Behnken Design (BBD) Expert and Antioxidant Analysis” Jurnal Teknologi (Sciences & Engineering), 77(3) 2015 :
hal. 27-32.
[9] Shufi Ramadiani Swari. ” Penentuan Kandungan Annonaceous Acetogenin
pada Daun Sirsak dengan Metode Spektrofotometri Gugus Lakton.” Skripsi, Program Studi Ekstensi Teknik Kimia UI, Depok, 2012, hal.25 – 30.
[10] Ni Putu Rahayu Artini, Sri Wahjuni, dan Wahy Dwijani Sulihingtyas, “Ekstrak Daun Sirsak (Annona Muricata L) Sebagai Antioksidan pada Penurunan Kadar Asam Urat Tikus Wistar”, Jurnal Kimia 6(2) 2012 : hal. 127-137.
36
[11] Carlos J. Marquez – Cardozo, Jose R. Cartagena – Valenzuela, Hector J. Ciro – Velasquez, “Physicochemical Characteristics and Finite Element Simulation of Firmness in Soursop Fruits (Annona muricata L. cv. Elita)”,
Postharvest. Medellin (172) 2012 : hal. 141-147.
[12] Firmansyah Dede. “Studi Inhibisi Korosi Baja Karbon dalam Larutan Asam 1 M HCl Oleh Ekstrak Daun Sirsak (Annona murica L).” Tesis, Program Studi Metalurgi dan Material UI, Depok, 2011, hal. 43
[13] Onyechi, e.t all., “Nutrient, Phytochemical Composition and Sensory Evaluation of Soursop (Annona muricata) Pulp and Drink in South Eastern Nigeria”, International Journal of Basic & Applied Sciences IJBAS-IJENS, 12(6) 2013 : hal. 53-57.
[14] Ahmad H. Lubis. “Budidaya Tanaman Sirsak”. Fakultas Pertanian, Universitas Sumatera Utara : Medan. 2011
[15] Soheil Zorofchian Moghadamtousi, Mehran Fadaeinasab, Habsah Abdul Kadir, “Annona muricata (Annonaceae) : A Review of Its Traditional Uses, Isolated Acetogenins and Biological Activities”, International Journal of
Molecular Sciences 16 2015 : hal. 15625-15658
[16] Trupti P. Sawant and Rajendra S. Dongre “Biochemical Compositional Analysis of Annona Muricata : A Miracle Fruit’s Review”. International Journal of Universal Pharmacy and Bio Sciences 3(2) 2014 : hal. 82-105.
[17] Khaidatul Hasni. “Physical Properties of Soursop (Annona muricata) Powder Produced By Spray Drying”. Faculty of Chemical and Natural Resources Engineering Universitas Malaysia : Pahang. 2009
[18] Adib “Perbandingan Metode Ekstrasi Maserasi dan Infundasi Terhadap Kadar Asetogenin Hasil Isolasi Daun Sirsak (Annona muricata L)”. Skripsi, Program Sarjana Fakultas farmasi, Universitas Gadjah Mada, Yogyakarta, 2014, hal. 21.
[19] Komansilan Alfrits, “Survival Analysis of Natural Insectiside Soursop Seed Extract in Aedes Aegypti Larvae Vector of Dengue Haem”, Journal of Agricultural and Food Chemistry IV (Augustus 2014), hal. 27 – 29.
[20] Endah Pratiwi. “Perbandingan Metode Maserasi, Remaserasi, Perkolasi, Reperkolasi dalam Ekstraksi Senyawa Aktif Andrographolide dari Tanaman Sambiloto (Andrographis paniculata (Burn .f.) Ness). Skripsi, Program Sarjana Fakultas Teknologi Pertanian Institut Pertanian Bogor, Bogor, 2010, hal. 14. [21] Sukhdev Swami Handa, Suman Preet Singh Khanuja, Gennaro Longo, Dev Dutt Rakesh, “Extraction Technologies for Medicinal and Aromatic Plants”,
United Nations Industrial Development Organization and International Centre for Science and High Technology, 2008.
37
[22] Monica Wijaya “Ekstraksi Annonaceous Acetogenin dari Daun Sirsak, Annona muricata, sebagai Senyawa Bioaktif Antikanker” , Skripsi, Program
Sarjana Fakultas Teknik UI, Depok, 2012, hal. 15.
[23] Cheah Li Chin, Emily. “Study of Extraction Processes and Their Impact on Bioactivity of Botanicals”. Thesis. Department of Pharmacy, National University of Singapore, Singapore, 2009, page. 21.
[24] Haijun Yang, Ning Zhang, Qingqi Zeng, Qiping Yu, Shihua Ke, Xiang Li “HPLC Method for the Simultaneous Determination of Ten Annonaceous Acetogenins after Supercritical Fluid CO2 Extraction”, International Journal of
Biomedical Science, 6(3) 2010 : hal. 85.
[25] Christie J Geankoplis, Transport Processes and Unit Operations (New York: Prentice-Hall International, 1993) hal. 733
[26] G.N Sapkale, S.M Patil, U.S Surwase, P.K Bhatbhage, “Supercritical Fluid Exctraction”, Int.J chem. Sci : 8 (2), 2010, hal. 729-743.
[27] Hendra Fauzi. “Ekstraksi Bitumen dari Batuan Aspal Buton Menggunakan Gelombang Mikro dengan Pelarut n- Heptana, Toluena, dan Etanol.” Skripsi, Program Sajana Fakultas Teknik UI, Depok, 2012.
[28] Suman Preet Singh Khanuja, Gennaro Longo, Dev Dutt Rakesh, “Extraction Technologies for Medicinal and Aromatic Plants”, United Nations Industrial Development Organization and International Centre for Science and High Technology, 2008.
[29] James Hamuel Doughari. “Phytochemicals : Extraction Methods, Basic Structures and Mode of Action as Potential Chemotherapeutic Agents.” Department of Microbiology, Federal University of Technology, Yola, Nigeria. 2012.
[30] Daniel Genin, NIST, “ Percolation : Theory and Applications”, 2007 [31] Sigma-Aldrich, “Materil Safety Data Sheet Acetone”, 2012.
[32] Chen Yong, XU Shasha, Chen Jianwei, Wang Yu, Xu Xuiqing, “ Squomosa seeds extract containing annonaceous acetogenin compounds”, Jingsu Key Laboratory for Pharmacology and Safety Evaluation of Chinese Material Medica,
No. P09018, 2011, hal. 4.
[33] Amita Pandey, Shalimi Tripathi, “ Concept of Standardization, Extraction and Pre Phytochemical Screening Strategies for Herbal Drug”, Journal of Pharmacognosy and Phytochemistry 2 (5) 2014, hal. 115-119.
38
[34] Ankit Gupta, Madhu Naraniwal and Vijay Kothari, “Modern Extraction Methods for Preparation of Bioactive Plant Extracs”, International Academy of Sciences, Engineering and Technology I (Agustus, 2012), hal : 8-26.
[35] Thermo Nicolet “ Introduction to Fourier Transform Infared Spectrometry”, Thermo Nicolet Corporation, 2001.
[36] Joseph B. Lambert, et al., Introduction to Organic Spectroscopy (New York : Macmillan), 1987.
[37] Sperisa Distantina, Endah Fadilah, Artati K. Enny, “Pengaruh Rasio Berat Rumput Laut –Pelarut Terhadap Ekstraksi Agar – Agar,” Ekuilibrium 6(2) 2007:
hal : 53-58.
18
BAB III
METODOLOGI PENELITIAN
3.1 LOKASI DAN WAKTU PENELITIAN
Penelitian dilakukan di Laboratorium Operasi Teknik Kimia, Fakultas Teknik, Departemen Teknik Kimia, Universitas Sumatera Utara, Medan.
3.2 BAHAN DAN PERALATAN 3.2.1 Bahan Penelitian
Pada penelitian ini bahan yang digunakan antara lain:
1. Biji sirsak yang merupakan bahan baku dalam percobaan ini. 2. Aseton (C3H6O)
3.2.2 Peralatan Penelitian
Pada penelitian ini peralatan yang digunakan antara lain:
1. Blender 2. Sokhlet
3. Statif dan klem 4. Hot plate
5. Labu distilasi 6. Pendingin Leibig 7. Refluks Kondensor 8. Pipa bengkok 9. Erlenmeyer 10.Beaker glass
11.Gelas ukur 12.Neraca analitik 13. Termometer 14.Aluminium foil
15.Corong gelas 16.Batang pengaduk 17.Kertas Saring 18.Pipet tetes
19 3.2.3 Rangkaian Peralatan
Gambar 3.1 Rangkaian Peralatan Soxhlet
Gambar 3.2 Rangkaian Peralatan Distilasi
20 3.3 RANCANGAN PENELITIAN
Penelitian ini dilakukan dengan tahapan sebagai berikut : 1. Persiapan biji sirsak
2. Ektraksi biji sirsak dengan pelarut aseton
3. Analisa Kandungan Acetogenin dalam Ekstrak Biji Sirsak dengan FT-IR
Pada penelitian ini dilakukan variasi terhadap kondisi proses ekstraksi biji sirsak yaitu, waktu (t) dalam menit dan massa sampel (gram) yang ditunjukkan pada tabel di bawah ini :
Tabel 3.1 Rancangan Penelitian Run Massa
(Gram)
Waktu (Menit) 1
10
30
2 40
3 50
4 60
5
20
30
6 40
7 50
8 60
9
30
30
10 40
11 50
12 60
21 3.4 PROSEDUR PENELITIAN 3.4.1 Prosedur Utama
3.4.1.1Prosedur Persiapan Biji Sirsak
1. Biji sirsak yang telah disiapkan dicuci dengan air. 2. Biji dikupas sehingga diperoleh inti biji
3. Inti biji yang diperoleh di cuci dengan air
4. Dikeringkan inti biji di bawah sinar matahari selama satu hari.
5. Inti biji yang sudah kering dihaluskan dengan menggunakan blender dan diayak hingga berukuran 50 mesh.
3.4.1.2Prosedur EkstraksiBiji Sirsak
1. Ditimbang sampel 10 gram,
2. Di masukkan sampel ke dalam thimble dengan susunan : kapas, sampel dan kapas.
3. Dimasukkan pelarut aseton sebanyak 200 mL kedalam labu. 4. Dirangkai peralatan soxhlet.
5. Dipanaskan diatas hot plate selama 30 menit dengan suhu 580C.
6. Diambil hasil ekstraksi yang masih bercampur dengan pelarut.
7. Diulangi prosedur untuk variasi berat (20 dan 30 gram) dan waktu ekstraksi (40,50 dan 60 menit).
3.4.1.3Prosedur Pemurnian
1. Hasil ekstraksi dimasukkan ke dalam labu distilasi 2. Dirangkai peralatan distilasi
3. Dipanaskan di atas hot plate dengan suhu 58 oC
4. Setelah semua pelarut menguap. Diambil hasil ektraksi berupa cairan kental (pekat) kemuian ditimbang.
22 3.4.2 Prosedur Analisa
3.4.2.1 Analisa Kandungan Kimiawi dalam Ekstrak Biji Sirsak dengan FT-IR
Analisa FTIR dilakukan di Laboratorium Pusat Penelitian Kelapa Sawit Medan. Hasil ekstraksi yang diperoleh di analisa FTIR untuk melihat kandungan kimiawinya. Seperti senyawa senyawa yang menandakan keberadaan acetogenin pada hasil ekstraksi.
3.5 FLOWCHART PENELITIAN 3.5.1 Prosedur Persiapan Biji Sirsak
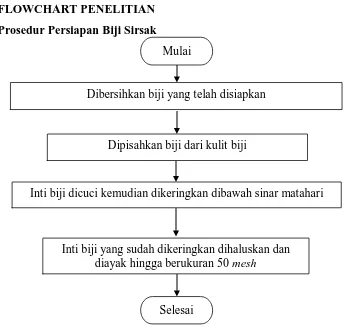
Gambar 3.3 Flowchart Prosedur Persiapan Biji Sirsak Mulai
Selesai
Dipisahkan biji dari kulit biji Dibersihkan biji yang telah disiapkan
Inti biji dicuci kemudian dikeringkan dibawah sinar matahari
Inti biji yang sudah dikeringkan dihaluskan dan diayak hingga berukuran 50 mesh
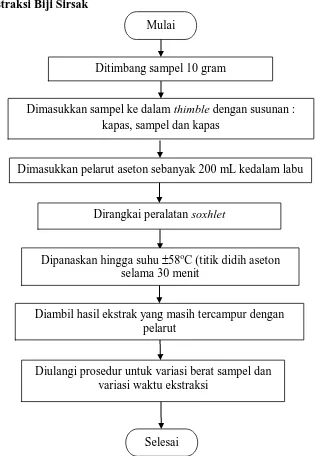
23 3.5.2 Ekstraksi Biji Sirsak
Gambar 3.3 Flowchart Prosedur Ekstraksi Biji Sirsak Mulai
Dipanaskan hingga suhu 58oC (titik didih aseton
selama 30 menit
Selesai
Dimasukkan sampel ke dalam thimble dengan susunan : kapas, sampel dan kapas
Ditimbang sampel 10 gram
Dimasukkan pelarut aseton sebanyak 200 mL kedalam labu
Diulangi prosedur untuk variasi berat sampel dan variasi waktu ekstraksi
Diambil hasil ekstrak yang masih tercampur dengan pelarut
Dirangkai peralatan soxhlet
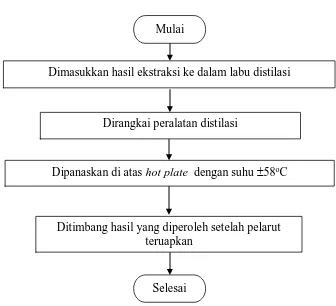
24 3.5.3 Pemurnian Hasil Ekstraksi
Gambar 3.4 Flowchart Prosedur Pemurnian Hasil Ekstraksi Mulai
Selesai
Dirangkai peralatan distilasi
Dimasukkan hasil ekstraksi ke dalam labu distilasi
Dipanaskan di atas hot plate dengan suhu 58oC
Ditimbang hasil yang diperoleh setelah pelarut teruapkan
25
BAB IV
HASIL DAN PEMBAHASAN
Pada penelitian ini dilakukan ekstraksi biji sirsak menggunakan soklet dengan pelarut aseton. Dengan variabel berubah berupa massa sampel (10, 20, dan 30 gram) serta waktu ekstraksi (30, 40, 50, dan 60 menit). Dari hasil percobaan diperoleh cairan pekat (kental) berwarna kuning jernih seperti minyak yang beragam untuk setiap variasi. Kemudian pada hasil ekstrak tersebut dilakukan analisissecara kualitatif maupun kuantitatif.
4.1 ANALISIS KUALITATIF
Analisis kualitatif yang dilakukan adalah analisa FTIR dengan tipe shimadzu. Analisis FTIR (Fourier Transform Infra Red) bertujuan untuk mengidentifikasi gugus fungsi dari struktur kimia dalam suatu senyawa pada panjang gelombang tertentu.
Analisis ini digunakan untuk melihat gugus-gugus yang terdapat pada ekstrak biji sirsak sehingga dapat menunjukkan keberadaan senyawa acetogenin.Acetogenin merupakan senyawa polikatida dengan struktur kimia sebagai berikut :
Gambar 4.1 Struktur Kimia Acetogenin [19]
Analisis ini dilakukan pada sampel dan ampas biji sirsak setelah proses ekstraksi berlangsung untuk menunjukkan bahwa proses ekstraksi acetogenin dengan pelarut aseton terhadap biji sirsak ini telah berhasil dilakukan. Kemudian dilakukan juga analisis terhadap hasil ekstrak yang diperoleh untuk memastikan keberadaan senyawa acetogenin di dalamnya.
26
4.1.1 Analisis Bahan Baku dan Ampas Biji Sirsak
Untuk memperkuat teori maka perlu dilakukan analisis terhadap bahan baku biji sirsak yang akan diekstraksi. Hal ini dilakukan agar kita dapat mengetahui kandungan apa saja yang terdapat pada bahan baku yaitu biji sirsak dan kandungan apa saja yang berhasil terekstrak selama proses berlangsung, maka dilakukan analisis FTIR pada bahan baku biji sirsak sebelum diesktraksi dan residu berupa ampas setelah sampel diekstraksi untuk mengidentifikasi zat tersebut. Berikut adalah grafik hasil analisis FTIR terhadap bahan baku sebelum dilakukan proses ekstraksi dan ampas biji sisak setelah proses ekstraksi:
Gambar 4.2 Kurva Hasil Analisis FTIR Biji Sirsak Sebelum Ekstraksi
Gambar 4.3 Kurva Hasil Analisis FTIR Ampas Biji Sirsak
27
Seperti yang disebutkan di atas bahwa gugus – gugus yang dapat menandakan adanya acetogenin dalam sampel adalah tetrahydrofuran (THF), lakton, ikatan karbon alifatik, alkohol dan sebagainya [17]
Dari kurva di atas dapat dilihat bahwa pada bahan baku sebelum diekstraksi terdapat peak-peak yang curam yang menunjukkan keberadaan senyawa acetogenin. Pada peak 1743 yang menunjukkan jenis vibrasi gugus lakton yang merupakan kunci dari keberadaan senyawa acetogenin dan pada kurva hasil analisis ampas biji sirsak peak dengan panjang gelombang 1743 tersebut tidak terbaca lagi yang menunjukkan bahwa senyawa tersebut telah berhasil terekstrak selama proses ekstraksi berlangsung. Perbandingan hasil analisis FTIR bahan baku dan ampas biji sirsak secara rinci dapat dilihat pada tabel 4.1 dibawah ini :
Tabel 4.1 Hasil Interpretasi FTIR Bahan Baku dan Ampas Biji Sirsak Jenis Vibrasi
Bilangan Gelombang
[33]
Sebelum Ekstraksi
Setelah Ekstraksi
OH (phenol) 3420 – 3250 3298 3265
CH3– CH2aliphatic 2990 – 2850 2924 2943
C=O ( lacton) 1750 – 1740 1743 -
THF (CH2def) 1375 – 1275 1373 -
C – O – C (lacton) 1280 – 1150 1161 -
CH2 dalam hidrokarbon 740-720 721 -
Dari Perbandingan kedua hasil FTIR di atas dapat dilihat bahwa gugus – gugus yang menunjukkan keberadaan acetogenin secara keseluruhan telah berhasil terekstrak selama proses ekstraksi. Hal tersebut dapat dilihat dari tabel 4.1 di atas, dimana gugus yang menunjukkan keberadaan senyawa acetogenin seperti lakton,
tetrahydrofuran, dan sebagainya sudah tidak terdapat lagi pada hasil analisis FTIR
ampas biji sirsak. Hal tersebut menunjukkan bahwa pelarut aseton berhasil mengekstrak senyawa acetogenin dari biji sirsak.
28 4.1.2 Analisis Ekstrak Biji Sirsak
Dari hasil analisis FTIR bahan baku dan ampas biji sirsak setelah proses ekstraksi dapat dilihat bahwa acetogenin telah berhasil terekstrak. Untuk membuktikan atau memperkuat argumen tersebut dilakukan analisis FTIR untuk hasil ekstrak yang diperoleh yang berupa cairan kental berwarna kuning tersebut.
Hasil analisis yang diperoleh selanjutnya dibandingkan dengan hasil peneliti terdahulu yaitu penelitian yang dilakukan oleh Chen Yong dalam ekstraksi acetogenin dari biji srikaya yang masih merupakan famili dari annonaceae. Perbandingan keduanya dapat dilihat pada gambar 4.4 dan 4.5 di bawah ini :
Gambar 4.4Kurva Hasil Analisa FTIR Ekstrak Biji Sirsak
Gambar 4.5Kurva Analisis Hasil Penelitian Chen Yong
29
Dari kedua gambar diatas dapat kita lihat bahwa keduanya memiliki beberapa peak yang memiliki panjang gelombang yang sama. Seperti terlihat pada gambar 4.4 terdapat peak dengan panjang gelombang 1743 yang menunjukkan keberadaan gugus lakton dan pada gambar 4.5 terdapat panjang gelombang yang hampir sama yaitu 1742 yang masih merupakan rentang panjang gelombang untuk gugus lakton. Selain itu masih terdapat beberapa peak yang memiliki panjang gelombang yang hampir sama untuk kedua gambar tersebut. Data lebih rinci untuk perbandingan kedua gambar tersebut dapat dilihat pada tabel 4.2 di bawah ini :
Tabel 4.2 Perbandingan Data Vibrasi Hasil Analisis FT-IR
Gugus Fungsi
Vibrasi FTIR (cm-1) Hasil
Penelitian Standar [36]
Hasil Penelitian Chen Yong [32] OH dalam carboxylic acid 3007,79 3100-2400 3422,47
CH3– CH2aliphatic 2921,96 2990 - 2850 2920
C=O ( lacton) 1743,32 1750 - 1740 1742,11
THF (CH2def) 1360,53 1375 - 1275 1385
C – O – C (lacton) 1159 1280 – 1150 -
Epoksida 913 950 – 860 -
CH2 dalam hidrokarbon 722 740-720 -
Dari tabel diatas dapat dilihat bahwa terdapat beberapa gugus yang sama untuk kedua gambar yang mana gugus tersebut merupakan gugus yang menunjukkan keberadaanacetogenin seperti lakton, THF dan sebagainya. Hal ini menunjukkan bahwa terdapat acetogenin dalam hasil ekstrak biji sirsak. Dalam jurnalnya Chen yong mengatakan bahwa untuk panjang peak yang terbaca pada gambar 4.5 diatas menunjukkan acetogenin dengan jenis cis-annonacin yang biasa terdapat pada biji tanaman famili annonaceae [32]. Maka dengan menggunakan hasil penelitian yang telah dilakukan Chen Young ini sebagai pembanding dapat dilihat bahwa hasil yang diperoleh dari ekstraksi biji sirsak dengan pelarut aseton ini tidak jauh berbeda dengan standar yang ada untuk jenis acetogenin cis annonacin.
30 4.2 ANALISIS KUANTITATIF
Analisis kuantitatif yang dilakukan adalah analisis % yield ekstrak biji sirsak yang diperoleh pada setiap variasi percobaan. Kemudian dilihat pengaruh dari variabel berubah yang dilakukan yaitu variasi massa sampel dan waktu ekstraksi terhadap % yield ekstrak biji sirsak yang diperoleh.
4.2.1 Pengaruh Massa Sampel Terhadap Massa Ekstrak
Massa sampel merupakan variabel yang berhubungan langsung dengan hasil ekstrak yang diperoleh selama proses ekstraksi. Untuk melihat pengaruh massa sampel terhadap massa ekstrak yang diperoleh pada proses ekstraksi biji sirsak ini, maka dilakukan penelitian dengan variasi massa sampel yaitu 10, 20, dan 30 gram. Pengaruh massa sampel terhadap hasil ekstrak yang diperoleh dapat dilihat pada grafik 4.6 dibawah ini :
Gambar 4.6 Grafik Pengaruh Massa Sampel Terhadap Massa Ekstrak
Dari grafik 4.6 di atas dapat dilihat bahwa penambahan massa sampel berbanding lurus dengan massa ekstrak yang dihasilkan dalam selang waktu yang sama. Secara teknis semakin besar massa sampel yang diekstraksi maka akan besar juga massa ekstrak yang dihasilkan. Secara teori semakin banyak bahan yang akan diekstraksi berarti semakin banyak solut yang terdapat di dalam bahan dan tentu saja hasil ekstrak yang diperoleh juga semakin tinggi.
Secara logika seharusnya massa ekstrak yang dihasilkan akan menunjukkan kelipatan dari massa sampel yang ada seperti pada penelitian ini untuk variasi waktu
4 6 8 10 12 14 16 18
10 20 30
M a ss a E k st ra k ( gr a m )
Massa Sampel (gram)
30 menit
40 menit
50 menit
60 menit
31
30 menit massa sampel yang digunakan adalah 10, 20 dan 30 gram dan hasil ekstrak yang diperoleh berturut-turut adalah 6; 7,7; dan 11 gram. Seharusnya hasil yang diperoleh juga menunjukkan kelipatan karena massa sampel merupakan variabel yang memang berhubungan langsung dengan hasil yang diperoleh. Dari data tersebut dapat dilihat bahwa penambahan massa sampel tidak memberikan kenaikan secara signifikan terhadap massa ekstrak yang dipeoleh. Pada saat massa sampel 10 gram massa ekstrak yang diperoleh sebesar 6 gram yang menunjukkan bahwa lebih dari setengah massa sampel dapat terekstrak, namun saat massa sampel 20 gram massa ekstrak yang diperoleh tidak mencapai setengah dari massa sampel yaitu sebesar 7,7 gram. Demikian halnya saat massa sampel 30 gram massa ekstrak yang diperoleh hanya sepertiga dari massa sampel yaitu 11 gram. Setelah meninjau hal tersebut diperoleh suatu analogi bahwa penambahan massa sampel lebih lanjut akan menghasilkan massa ekstrak yang semakin rendah. Hasil yang tidak maksimal ini dapat disebabkan oleh beberapa faktor diantaranya jumlah pelarut yang digunakan. Dalam penelitian ini digunakan jumlah pelarut yang sama untuk semua variasi massa sampel sehingga ada kemungkinan dengan penambahan massa sampel pelarut tidak dapat dengan maksimal melarutkan semua sampel dan mengurangi hasil ekstrak yang diperoleh. Namun memang besarnya massa ekstrak yang dihasilkan belum tentu memiliki % yield terbesar.
Dari grafik dapat dilihat bahwa massa ekstrak terbesar diperoleh untuk variasi massa sampel 30 gram dengan selang waktu ekstraksi 50 menit yaitu sebesar 17,7 gram. Massa ekstrak terkecil diperoleh pada massa sampel 10 gram dengan lama ekstraksi 60 menit yaitu sebesar 5 gram.
4.2.2 Pengaruh Waktu Ekstraksi Terhadap %Yield
Waktu ekstraksi merupakan salah satu variabel yang sangat berpengaruh terhadap %Yield ekstrak biji sirsak yang dihasilkan. Untuk mengamati pengaruh waktu ekstraksi terhadap % yield yang diperoleh dilakukan variasi terhadap waktu ekstraksi dan dari hasil penelitian diperoleh kenaikan dan penurunan yang cukup signifikan untuk setiap variasi. Hal ini dapat dilihat dari grafik 4.7dibawah ini :
32
Gambar 4.7 Grafik Pengaruh Waktu Ekstraksi Terhadap %Yield
Dari grafik 4.7 di atas dapat dilihat bahwa secara keseluruhan penambahan waktu ekstraksi akan meningkatkan % yield yang diperoleh. Hal ini terjadi karena penambahan waktu ekstraksi akan memberikan peluang yang lebih besar bagi pelarut untuk dapat kontak dengan padatan secara maksimum dan dapat menghasilkan % yield yang tinggi.
Pada ekstraksi sistem padat-cair, perpindahan massa terjadi secara difusi di dalam padatan [37]. Semakin lama waktu ekstraksi maka %yield yang diperoleh akan semakin tinggi. Namun jika waktu ekstraksi maksimum telah tercapai maka penambahan waktu ekstraksi tidak akan menaikkan %yield lagi [7]. Dari grafik di atas dapat dilihat bahwa pada menit ke 60 terjadi penurunan yang signifikan untuk setiap variasi. Penurunan hasil %yield yang terjadi dapat disebabkan oleh beberapa faktor antara lain, selama proses ekstraksi berlangsung pelarut akan terus mengalami siklus penguapan dan pengembunan, pada titik tertentu akan tercapai suatu kesetimbangan dimana laju difusi solut dari permukaan padatan ke pelarut akan sama besar dengan laju difusi solut dari pelarut kepadatan atau terjadi kejenuhan sehingga pelarut yang teruapkan tidak murni lagi dan menyebabkan zat yang ingin diekstrak akan ikut teruapkan dan kembali ke bagian thimble dan akan menempel pada kapas sehingga hal ini menyebabkan %yield akan berkurang. Selain itu pada proses pemurnian menggunakan distilasi, ekstrak dipanaskan dalam waktu yang cukup lama dengan suhu 580C, sedangkan zat acetogenin sendiri dapat terurai pada suhu 600C
30 35 40 45 50 55 60 65
20 30 40 50 60
% Y ie ld Waktu (menit) 10 gram 20 gram 30 gram
33
[32]. Jadi ada kemungkinan selama proses distilasi ada sebagian kecil zat acetogenin yang terdegradasi menjadi molekul yang lebih ringan dan ikut teruapkan bersama pelarut aseton yang secara otomatis akan berdampak pada penurunan hasil %yield yang dihasilkan.
Untuk variasi waktu yang samadengan variasi massa sampel ternyata menunjukkan hasil yang cukup jauh berbeda. Seperti yang dapat kita lihat untuk variasi waktu 30 menit untuk setiap variasi massa sampel : 10, 20 dan 30 gram, % yield yang diperoleh berturut-turut adalah : 60%, 38,5% dan 36,67%. Dapat dilihat bahwa % yield tertinggi terdapat pada variasi massa sampel terkecil. Hal ini berhubungan dengan metode ekstraksi yang digunakan, dalam metode penelitian ini digunakan metode sokletasi dengan jumlah pelarut yang diset tetap untuk setiap variasi yaitu 200 mL. Pada prosesnya jumlah pelarut yang teruapkan akan sama banyak untuk setiap siklus pada setiap variasi massa sampel sehingga semakin banyak sampel akan menyebabkan lama kontak antara pelarut dan padatan tidak maksimal atau belum mencapai waktu yang optimum dan menyebabkanproses difusi solut dari padatan ke pelarut tidak berlangsung secara efisien yang berdampak pada % yield yang diperoleh.
Pada penelitian ini diperoleh % yield ekstrak biji sirsak tertinggi pada variasi massa sampel 10 gram dan lama waktu ekstraksi 40 menit yaitu 62%.
34
BAB V
KESIMPULAN DAN SARAN
5.1 KESIMPULAN
Adapun kesimpulan yang dapat di ambil dari penelitian yang telah di lakukan adalah:
1. Pelarut Aseton dapat digunakan untuk mengekstraksi senyawa acetogenin yang terdapat pada biji sirsak.
2. Dari hasil analisa FTIR terhadap hasil ektraksi terdapat kandungan gugus lakton, hidroksil, THF, dan rantai alifatik yang menunjukkan keberadaan senyawa acetogenin.
3. %Yield hasil ekstraksi biji sirsak tertinggi diperoleh pada variasi massa sampel 10 gram dan waktu ekstraksi 40 menit sebesar 62 %.
5.2 SARAN
1. Disarankan menggunakan penangas air atau heating mantle agar luas pemukaan kontak dengan media pemanas lebih besar.
2. Untuk penelitian lebih lanjut perlu dikaji pengaruh siklus selama proses ekstraksi dengan menggunakan soxhlet terhadap hasil yang diperoleh.
3. Disarankan untuk melakukan pengujian dengan pembanding dengan menggunakan acetogenin komersil.
4. Disarankan melakukan tahap pemurnian yang lebih variatif seperti dengan menggunakan rotary vacuum evaporator agar diperoleh hasil yang lebih murni.
5
BAB II
TINJAUAN PUSTAKA
2.1 BUAH SIRSAK (Annona muricata Linn)
Sirsak atau yang lebih dikenal dengan durian belanda ini merupakan salah satu jenis tanaman buah tropis. Sirsak merupakan famili dari Annonaceae, yang memiliki 119 spesis [4]. Sirsak merupakan salah satu buah – buahan yang menjanjikan untuk pasar international karena karakteristik gizi dan organoleptik yang sangat baik. Namun buah ini memiliki struktur yang mudah rusak dan dapat berubah bentuk karena beberapa kondisi lingkungan yang tidak sesuai. Struktur dan reologi dari buah sirsak ini sangat mempengaruhi kualitas beberapa komponen yang terdapat dalam buah [11].
Nama sirsak berasal dari bahasa Belanda yaitu Zuurzak, yang memiliki arti kantung yang asam. Tumbuhan ini bisa tumbuh dimana saja. Buah yang besar dan banyak dapat diperoleh dengan cara ditanam di daerah yang tanahnya cukup mengandung air. Sirsak di Indonesia tumbuh dengan baik pada daerah yang mempunyai ketinggian kurang dari lima meter di atas permukaan laut.
Adapun taksonomi dari sirsak (Annona muricata L) adalah : Kingdom : Plantae
Division : Spermatophyta Sub Divisio : Angiospermae Kelas : Dicotyledonae Ordo : Polycarpiceae Famili : Annonaceae Genus : Annona
Spesies : Annona muricata Linn [12]
Buah sirsak terdiri dari 67,5 % daging buah, 20 % kulit, 8,5 % biji, dan 4 % inti biji. Bagian daging buah yang berwarna putih terdiri dari 80 – 81 % air; 1 % protein, 18 % karbohidrat; 3,43 % asam; 24,5 5 gula dan vitamin B1, B2, dan C [13].
6
Gambar 2.1 Tanaman Sirsak [4]
Salah satu tanaman family annonaceae ini setelah dipelajari ternyata mengandung senyawa aktif yang disebut acetogenin yang bersifat larvasidal dan juga sebagai insektisida, akarisida, antiparasit dan bakterisida [10].
2.2 BIJI SIRSAK
Gambar 2.2 Biji Sirsak (Annona muricata L) [10]
Biji sirsak berwarna coklat kehitaman dan keras, berujung tumpul, permukaan halus mengkilat, dengan ukuran panjang kira–kira 16,8 mm dan lebar 9,6 mm. Jumlah biji dalam satu buah bervariasi berkisar antara 20-70 butir biji normal, sedangkan yang tidak normal berwarna putih kecoklatan dan tidak berisi [14].
Biji buah sirsak merupakan biji tunggal yang saling berhimpitan dan dipisahkan oleh daging buah. Biji sirsak mengandung senyawa bioaktif yang dapat berfungsi sebagai pestisida yaitu untuk membunuh ngengat dan kecoa. Selain sebagai pestisida manfaat lain biji sirsak yang sering digunakan masyarakat adalah untuk
7
obat cacing. Masyarakat terdahulu bahkan sering menggunakan hasil ekstrak minyak dari biji sirsak ini untuk menghilangkan kutu kepala. Dan dapat digunakan sebagai racun penangkap ikan secara tradisional [12].
[image:30.595.165.475.193.277.2]Senyawa toksik yang terdapat pada biji sirsak tersebut adalah : Tabel 2.1 Senyawa Toksik Pada Biji dan Kulit biji Sirsak [11]
Parameter Biji Kulit biji
Tannin (mg/100g) 2,6 4,9
Phytate (mg/100g) 620,5 188,0
Cyanide (mg/100g) 3,7 10,8
Biji buah sirsak kaya akan minyak, protein, dan sedikit toksik. Biji sirsak terdiri dari 22,1 % minyak kulit yang berwarna kuning, dan 21,43% protein. Minyak biji ini terdiri dari 28,07% jenuh dan 71,93% tidak jenuh [9].
Pada biji sirsak ini juga terdapat senyawa acetogenin dan turunannya yang ditemukan oleh beberapa peneliti terdahulu diantaranya : annonacin, corossolone,
corossolin, solamin, cis-annonacin, annomuricatin, muricattetrocin (A,B),
epomuricanin (A,B), muricin, cis-annonamontacin, annonacinone, xylomaticin,
reticuline [15]. Yang hampir kesemuanya bersifat anti terhadap kanker paru-paru,
kanker payudara, kanker otak, hepotema dan tumor. Adapun komponen kimia dari biji sirsak ini dapat dilihat dari tabel di bawah ini :
Tabel 2.2 Komponen Kimia Biji Sirsak [16]
No Komponen Keterangan
1. 2. 3. 4. 5. 6. 7. 8. 9. 10. 11. 12. Annomonicina Annomontacina Annonacina Annomuricatina Annonacinona Javoricina Bullatacinone Muricoreacin Muihexocin C Annomuricin A, B Muricatocin A,C Muricapentocin
Lakton
13. Annomuricatina Protein
14. Linoleic acid Lipid
[image:30.595.164.479.509.737.2]8 2.3 ACETOGENIN
Acetogenin merupakan metabolit sekunder dari tanaman suku Annonaceae yang disintesis melalui reaksi antara asam asetat - turunan poliketida yang memiliki rantai panjang pada asam lemak yaitu 35-39 atom karbon. Sifat dari senyawa ini berupa rantai panjang alipatik dengan gugus fungsi hidroksil, dan asetil karbonil serta cincin 1-3 tetrahidrofuran [17].
Secara ilmiah acetogenin memiliki nama International Union of Pure and Applied Chemistry (IUPAC)
(5S)-5-Methyl-3-[(2R,8R,13R)-2,8,13-trihydroxy-13-[(2,5R)-5-[(iR)-1-hydroxytridecyl]-2-tetrahydrofuranyl] tridecyl]-5H-furan 2-one.
Molekular formula acetogenin C35H64O7 dan massa molekul relatif (Mr) 596,88
g/mol [18].
Acetogenin memiliki efek biologis yang beragam termasuk sitotoksik, antitumor, antimalaria, pestisida dan kegiatan antifeedant. Secara khusus, efek penghambatan acetogenin pada mitokondria NADH-ubiquinone oksido reduktase (kompleks I) yang menjadi catatan penting karena aktivitas biologis yang beragam. Beberapa jenis senyawa seperti bullatacin (rolliniastatin-2) dan rolliniastatin-1, adalah inhibitor yang paling ampuh dari enzim teridentifikasi sampai saat ini. Acetogenin ditandai dengan dua unit fungsional, α tetrahidrofuran hydroxylated
(THF), cincin -lakton -unsaturated, dipisahkan oleh rantai alkil panjang, meskipun dua unit masing-masing bisa memainkan peran penting dalam mengikat interaksi dengan enzim [19].
Acetogenin tersebar di hampir seluruh bagian tumbuhan sirsak seperti daging buah, daun, biji, dan akar. Dari hasil penelitian terdahulu ada lebih dari 100 jenis asetogenin yang dapat diisolasi dari tanaman sirsak ini. Berikut akan ditunjukkan beberapa struktur asetogenin yang terdapat pada beberapa bagian tumbuhan sirsak.
9
Gambar 2.3 Struktur Berbagai Jenis Asetogenin [15]
10 2.3 EKSTRAKSI
Ekstraksi adalah suatu proses pemisahan suatu senyawa dengan bantuan pelarut. Pelarut yang digunakan harus dapat mengekstrak substansi yang diinginkan tanpa melarutkan material lainnya [20].
2.3.1 Metode Ekstraksi
Adapun metode ekstraksi yang digunakan dalam ektraksi tanaman yaitu: a. Maserasi
Dalam proses ini, seluruh atau kasar bubuk simplisia (bahan yang mengandung solute yang akan diekstrak) ditempatkan dalam wadah tertutup yang diisi pelarut yang sesuai dan dibiarkan pada suhu kamar untuk jangka waktu minimal 3 hari dengan proses pengadukan sampai materi larut. Campuran kemudian disaring, marc (bahan padat basah) ditekan, sehingga diperoleh campuran solut dan pelarut yang kemudian dimurnikan untuk memperoleh ekstrak yang diinginkan [20].
b. Soxhlet Extraction (SXE)
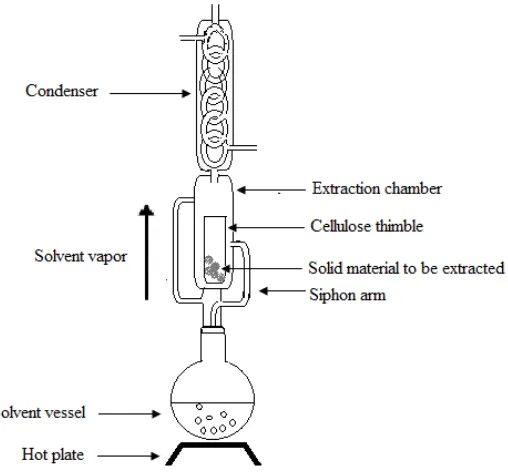
Metode Soklet merupakan standar untuk ekstraksi zat padat – cair lainnya. Fungsi soklet seperti ekstraksi kontinu dimana padatan secara kontinu dikontakkan dengan pelarut yang fresh . Padatan (serbuk) yang akan diekstrak diletakkan di dalam kertas saring (thimble) yang dimasukkan ke dalam
extraction chamber. Pelarut yang dipilih diletakkan di dalam solvent vessel
yang terletak dibagian bawah dan dipanaskan sampai titik didihnya. Pelarut akan berubah jadi uap kemudian akan mengalami kondensasi di sepanjang kondensor, kemudian pelarut yang sudah cair akan jatuh kebahan yang akan diekstrak. Kemudian akan terjadi proses maserasi antar bahan dengan hasil kondensasi pelarut. Bahan yang akan diekstrak akan terikut oleh pelarut yang mengalir kebawah dan masuk kedalam solvent vessel. Kemudian pelarut akan diuapkan kembali dan zat yang diekstrak akan tertinggal di bawah. Oleh karena itu pelarut akan selalu fresh. Dan proses akan terus berulang seperti itu [21].
11
Ekstraksi dengan menggunakan soxhlet dengan cara pemanasan dimana pelarut yang digunakan akan menguap dan terkondensasi kembali sehingga akan menjadi lebih hemat, namun acetogenin merupakan suatu senyawa yang mana ekstraknya rentan terhadap suhu tinggi, dan tidak bisa dilakukan jika suhu ekstraksi melewati 60 oC [22].
c. Ekstraksi berlawanan Arah
Aliran umpan mengandung zat terlarut A yang akan diekstraksi masuk pada ujung yang satu sedangkan aliran pelarut masuk pada ujung satunya lagi. Aliran ekstrak dan rafinat mengalir secara countercurrent dari satu tahap ke tahap lain dan produk akhir adalah aliran ekstrak V1 yang meninggalkan kolom 1 dan aliran
[image:34.595.157.510.322.402.2]rafinat LN yang meninggalkan kolom N [23].
Gambar 2.4 Ekstraksi Multi Tahap Countercurrent [23]
d. Ekstraksi Ultrasionik dan Superkritik
Cairan superkritis telah diteliti sejak abad terakhir, Pada awalnya penelitian ini berfokus pada penggunaan toluene superkritis dalam minyak bumi dan hasil samping penyulingan minyak selama tahun 1970-an. Gas superkritis juga sedang diselidiki sebagai salah satu cara menangani limbah beracun, dan sebagai media sintesis yang terbaru. Penemuan terbesar pada decade terakhir adalah dengan ditemukannya CO2 superkritis, karena memiliki nearambient sebuah suhu kritis
(31oC), sehingga bahan-bahan biologis dapat diproses di suhu sekitar 35oC.
Kepadatan superkritis CO2 sekitar 200 tekanan bar dekat hampir mendekati
kondisi untuk pelarut n- heksana, dan karakteristik solvasi juga mirip dengan heksana, dengan demikian, CO2 dianggap bersifat non polar seperti pelarut
n-heksan [24].
Metode ekstraksi konvensional, seperti ayakan dan ekstraksi menggunakan pelarut, telah menunjukkan efisiensi yang rendah dan potensi pencemaran lingkungan karena volume besar pelarut organik yang digunakan, serta waktu
12
ekstraksi yang lama dan suhu tinggi yang diperlukan dalam metode-metode. Fluida superkritis, microwave, dan metode ekstraksi ultrasonik muncul sebagai alternatif yang sangat baik bila dibandingkan dengan metode ekstraksi konvensional, terutama karena kurangnya kebutuhan untuk pelarut organik dan waktu ekstraksi yang relatif singkat. Namun, metode ekstraksi fluida superkritis memiliki beberapa kekurangan seperti waktu ekstraksi yang lebih lama dan tekanan ekstraksi yang tinggi, sehingga biaya operasi yang tinggi dan membatasi aplikasi industri skala besar [25].
Setelah mempertimbangkan kelebihan dan kekurangan dari setiap metode, maka metode yang dipilih dalam penelitian ini adalah metode sokletasi. Dengan keuntungan sebagai berikut :
1. Merupakan salah satu metode yang sudah mapan
2. Proses ekstraksi berjalan efisien karena sampel akan terus menerus kontak dengan pelarut segar.
3. Dapat menghasilkan yield yang tinggi 4. Pengoperasian sederhana
5. Ekonomis. [22]
2.3.2 Faktor –Faktor Yang Mempengaruhi Proses Ekstraksi
Ada beberapa faktor yang dapat mempengaruhi ekstraksi, diantaranya: 1. Suhu
Kelarutan bahan yang diekstraksi dan difusivitas biasanya akan meningkat dengan meningkatnya suhu, sehingga diperoleh laju ekstraksi yang tinggi. Pada beberapa kasus, batas atas untuk suhu operasi ditentukan oleh beberapa faktor, salah satunya adalah perlunya menghindari reaksi samping yang tidak diinginkan [26].
2. Penyiapan bahan sebelum ekstraksi
Agar proses ekstraksi berlangsung dengan cepat dan efisien perlu dilakukan tahap persiapan bahan baku seperti pengeringan dan penggilingan untuk memperkecil ukuran partikel dan memperbesar luas permukaan yang bersentuhan dengan pelarut. Pengurangan kadar air ini juga akan membuat bahan dapat bertahan lama sebelum proses ekstraksi berlangsung. Bahan baku
13
juga perlu disimpan pada tempat yang kering untuk menjaga kelembabannya sehingga tidak merusak kualitas hasil ekstraksi. Dengan pengeringan yang sempurna akan dihasilkan ekstrak yang memiliki kemurnian tinggi [27].
3. Ukuran partikel
Semakin kecil ukuran partikel, semakin besar luas bidang kontak antara padatan dan solven, serta semakin pendek jalur difusinya, yang menjadikan laju transfer massa semakin tinggi [28].
4. Waktu
Semakin lama waktu ekstraksi maka akan semakin tinggi yield yang diperoleh, namun bila ekstraksi telah mencapai batas maksimum maka penambahan waktu tidak akan mempengaruhi laju ekstraksi [29].
5. Faktor solven
Dalam pemilihan pelarut ada beberapa faktor yang harus dipertimbangkan : a. Selektivitas
Pelarut yang dipilih harus dapat melarutkan ekstrak yang diinginkan, bukan komponen – komponen lain dari sampel yang akan diekstraksi.
b. Kelarutan
Nilai kelarutan bahan yang diekstak terhadap pelarut harus cukup tinggi agar pelarut mampu melarutkan ekstrak.
c. Viskositas
Viskositas pelarut berpengaruh pada koefisien difusi dan laju ekstraksi. Viskositas pelarut yang rendah akan meningkatkan koefisien difusi sehingga laju ekstraksi meningkat.
d. Kecocokan dengan solut
Pada umumnya pelarut tidak boleh bereaksi atau menyebabkan perubahan secara kimia pada komponen – komponen bahan ekstraksi.
e. Titik didih
Untuk memudahkan proses pemurnian ada baiknya perbedaan titik didih antara pelarut dan bahan yang diekstrak cukup besar.
[30]
14 2.4 ASETON (C3H6O)
Aseton adalah keton yang paling penting. Cairan volatil (titik didih 56oC) dan mudah terbakar. Aseton adalah pelarut yang baik untuk senyawa organik banyak digunakan sebagai pelarut pernis, lak dan plastik. Aseton bercampur dengan air dalam segala perbandingan. Sifat ini digabungkan dengan volatilitasnya membuat aseton sering digunakan sebagai pengering alat – alat gelas laboratorium [31].
Asetogenin termasuk salah satu senyawa yang rentan terhadap suhu. Struktur asetogenin akan berubah pada suhu di atas 600C. Oleh karena itu dengan metode sokletasi yang menggunakan media pemanas diperlukan pelarut yang memiliki titik didih dibawah suhu 600C [32].
Salah satu syarat pelarut yang baik adalah selektivitas pelarut tersebut terhadap zat yang akan diekstrak. Seperti untuk mengekstrak senyawa polar digunakan pelarut yang bersifat polar begitu juga sebaliknya. Sifat fisika kimia zat aktif asetogenin yaitu memiliki nilai log P sebesar 7,71 yang menunjukkan bahwa asetogenin bersifat non polar [33].
[image:37.595.178.462.515.724.2]Kepolaran suatu senyawa dapat dilihat dari angka tetapan dielektrik [4]. Konstanta dielektrikum semakin besar maka sifat kepolaran dari suatu zat tinggi begitu juga sebaliknya semakin kecil nilai konstanta dielektrikum suatu zat maka sifat kepolarannya semakin rendah [34]. Berikut akan ditampilkan deret eluotropik menurut Stahl untuk setiap zat pada suhu 250C.
Tabel 2.3 Deret Eluotropik Pelarut [34]
Pelarut Tetapan Dielektrik Viskositas n-heksan Heptana Siklon-heksana Karbon tetrakloria Benzen Klorofom Eter (Dietil eter) Etil Asetat Piridin Aseton Etanol Metanol Air 1,890 1,924 2,023 2,238 2,284 4,806 4,34 6,02+ 12,3+ 20,7+ 24,30+ 33,62+ 80,37+ 0,326 0,409 1,02 0,969 0,652 0,580 0,233 0,55 0,974 0,316+ 1,2 0,597 1,005
15
Peneliti terdahulu banyak menggunakan etanol dan metanol sebagai pelarut dalam ekstraksi senyawa asetogenin dari tanaman sirsak ini. Dapat dilihat dari tabel di atas bahwa nilai konstanta dielektrik aseton lebih kecil dibandingkan etanol maupun metanol sehingga dapat disimpulkan bahwa aseton merupakan pelarut yang kurang polar sehingga dapat dengan baik mengekstrak asetogenin dari sampel.
2.5 FTIR (Fourier Transform Infrared Spectroscopy)
FT-IR singkatan dari Fourier Transform Infrared, metode yang merupakan spektroskopi inframerah. Dimana spektroskopi inframerah, dengan radiasi IR dilewatkan melalui sampel. Beberapa radiasi infra merah diserap oleh sampel dan beberapa di antaranya terelakkan (ditransmisikan), kemudian dihasilkan spektrum yang merupakan molekul penyerapan dan transmisi, menunjukkan karakteristik sampel. Yang mana spektrum yang terbentuk tidak akan sama untuk sampel lain dan sangat spesifik untuk suatu sampel. Hal ini membuat spektroskopi inframerah berguna untuk beberapa jenis analisis [35].
Informasi yang dapat diberikan oleh FT-IR [35] :
• Dapat mengidentifikasi bahan yang tidak diketahui
• Dapat menentukan kualitas atau konsistensi sampel
• Dapat menentukan jumlah komponen dalam campuran
Spektroskopi yang biasa digunakan adalah frekuensi spektroskopi domain di mana Radiant Data listrik dicatat sebagai fungsi frekuensi. Durasi spektroskopi domain, yang dicapai dengan Fourier Transform (FT), data daya radiasi sebagai fungsi waktu. kemudian daya radiasi (ν) diplot terhadap frekuensi (ν1) (Hz) [36].
16
Gambar 2.5 Daerah Waktu dan Frekuensi Spektrum [35]
.Beberapa keuntungan utama dari FT-IR selama teknik dispersif meliputi [34]: a) Kecepatan: Karena semua frekuensi diukur secara bersamaan, sebagian besar
pengukuran oleh FT-IR. dibuat dalam hitungan detik bukan beberapa menit. Ini kadang-kadang disebut sebagai Felgett Advantage.
b) Sensitivitas: Sensitivitas secara dramatis ditingkatkan dengan FT-IR untuk banyak alasan. Detektor dipekerjakan jauh lebih sensitif, peletakan optik jauh lebih tinggi (disebut sebagai keuntungan Jacquinot) yang menghasilkan tingkat kebisingan yang jauh lebih rendah, dan scan cepat memungkinkan coaddition beberapa scan untuk mengurangi kebisingan pengukuran acak untuk setiap tingkat yang diinginkan (disebut sebagai sinyal rata-rata).
c) Kesederhanaan Teknik: Cermin bergerak di interferometer adalah satu-satunya bagian dalam instrumen yang bergerak secara kontinu. Dengan demikian, ada sedikit kemungkinan kerusakan mekanis.
d) Internal dikalibrasi: Instrumen ini menggunakan laser HeNe sebagai panjang gelombang internal yang kalibrasi standar (disebut sebagai keuntungan
Connes). Instrumen ini adalah mengkalibrasi-diri dan tidak perlu dikalibrasi
oleh pengguna.
Dengan demikian, Fourier Transform Infrared (FT-IR) teknik telah membawa signifikan praktis keuntungan untuk spektroskopi inframerah. Ini telah memungkinkan pengembangan banyak sampel baru teknik yang dirancang untuk
17
mengatasi masalah yang menantang yang mungkin oleh lebih tua teknologi. Hal ini telah membuat penggunaan analisis inframerah hampir tak terbatas [34].
[image:40.595.137.501.189.355.2]Keberadaan suatu senyawa atau gugus dalam spektrum ditandai dengan bilangan gelombang tertentu sesuai dengan standar.
Tabel 2.4 Daftar Panjang Gelombang Suatu Senyawa /Gugus Fungsi [36] Range (cm-1) dan
intensitas Grup dan Kelas
3420 – 3250 3100 – 2400 2990 – 2850 1870 – 1830 1780 – 1760 1750 – 1730 1375 – 1275 1280 – 1150 740 – 720
- OH dalam alkohol dan fenol - OH dalam asam karboksilik
CH3– CH2 alipatik
C=O dalam lakton C=O dalam lakton C=O dalam lakton
THF (CH2def)
C – O – C lakton CH2 dalam hidrokarbon
1
BAB I
PENDAHULUAN
1.1 LATAR BELAKANG
Selama ribuan tahun manusia menggunakan sumber tanaman untuk meringankan atau menyembuhkan penyakit. Tanaman merupakan sumber senyawa kimia baru yang potensial digunakan dalam bidang kedokteran dan aplikasi lainnya. Tanaman mengandung banyak senyawa aktif seperti alkaloid, steroid, tanin, glikosida, minyak atsiri, minyak tetap, resin, fenol dan flavonoid yang disimpan di bagian-bagian tertentu seperti daun, bunga, kulit kayu, biji-bijian, buah-buahan, akar, dan lain-lain menjadi obat yang lebih bermanfaat dari bahan tanaman, biasanya hasil dari kombinasi dari produk-produk sekunder [1].
Indonesia sebagai salah satu mega biodiversity country dikenal sebagai gudang tumbuhan obat. Sekitar 30.000 jenis flora yang ada di hutan tropika Indonesia, kurang lebih 9.600 spesies telah diketahui berkhasiat sebagai obat [2]. Tanaman – tanaman ini sebelumnya dijadikan sebagai obat tradisional oleh nenek moyang kita.
Sirsak (Annona muricata L) merupakan salah satu tanaman buah yang berasal dari Karibia, Amerika Tengah dan Amerika Selatan dan dapat tumbuh dengan baik di Indonesia. [3].
Tanaman famili Annonaceae seperti sirsak yang cukup banyak terdapat di Indonesia ternyata cukup efektif digunakan sebagai obat bagi penderita kanker dan insektisida nabati. Tanaman ini biasa digunakan untuk pengidap kanker selama
phytotherapy, juga sebagai spektrum internal dan eksternal antimikroba untuk
menghadapi bakteri dan fungisidal. Hal ini disebabkan karena senyawa acetogenin yang terdapat dalam kandungan tanaman sirsak ini [4].
Asetogenin adalah senyawa polyketides dengan struktur umum dari , jenuh atau tidak jenuh - metil --lakton, gugus hidroksil, dengan rantai karbon tidak bercabang (32-34) yang terikat pada gugus 5-methyl-2-furanone pada C23 memiliki aktivitas sitotoksik [5].
Beberapa penelitian tentang ekstraksi asetogenin dari buah sirsak yang telah dilakukan dapat dilihat pada tabel 1.1 di bawah ini :
2
Tabel 1.1 Beberapa Penelitian Terdahulu Tentang Ekstraksi Acetogenin
NO Uraian Penelitian Keterangan
1. Dalam penelitian ini bahan baku yang digunakan adalah biji sirsak yang dikeringkan dengan proses
freeze-drying. Sampel kemudian diekstraksi dengan
metode maserasi menggunakan pelarut diklorometana selama 3 hari. Hasil yang diperoleh dengan menggunakan analisa kromatografi silika gel disimpulkan bahwa biji sirsak menggandung senyawa
annoreticuin-9-one, cis-annoreticuin, dan sabaelin.
[6], 2012
2. Pada penelitian ini bahan baku berupa daun, bijji dan daging buah sirsak. Bahan baku yang digunakan dikeringkan pada drying cabinet selama 96 jam hingga berbentuk serbuk. Sampel sebanyak 5 gr ditambahkan 50 ml air distilat, kemududian dipanaskan selama 15 menit untuk menghasilkan infusa. Hasil yang diperoleh dipekatkan hingga diperoleh hasil kurang dari 1 ml. Dilakukan uji sitotoksik pada hasil infusa yang diperoleh terhadap sel T47D dengan pembanding tamoksifen. Penghambat proliferasi ekstrak air terhadap sel kanker payudara T47D paling tinggi berturut – turut berasal dari daun, kemudian buah dan biji sirsak.
[7], 2014
3. Penelitian ini dilakukan untuk mencapai kondisi optimum dalam ekstraksi daun sirsak dimana digunakan metode RSM (Response Surface Methodology) menggunakan Box-Bahnken Design
dengan tiga faktor dan dua tindak balas. Pelarut yang digunakan adalah etanol dengan metode sokletasi. Dimana variabel yang dipilih adalah : konsentrasi etanol (0, 5, 10%), perbandingan rasio bahan baku dan pelarut (1:1, 1:4, 1: 6), dan waktu ekstraksi (1,4,8 jam). Diperoleh kondisi optimum pada waktu 6,8 jam, rasio bahan baku dan pelarut 1: 5,92, kepekatan etanol sebesar 1,67%. dengan pelarut etanol dan diperoleh kandungan daun sirsak yang bersifat anti kanker.
[8], 2015
Berdasarkan penelitian – penelitian yang telah dilakukan sebelumnya dapat dilihat hampir semua penelitian menggunakan metode maserasi. Hal ini dikarenakan zat acetogenin ini dapat terurai atau berubah strukturnya bila dipanaskan sampai suhu diatas 600C [9]. Namun metode maserasi memiliki beberapa kelemahan diantaranya
3
adalah membutuhkan pelarut dalam jumlah yang besar dan membutuhkan waktu ekstraksi yang lama. Untuk itu dalam penelitian ini kami memilih untuk menggunakan metode Sokletasi. Pada metode ini proses ekstraksi berjalan efisien karena zat terus menerus kontak dengan pelarut segar dan lebih hemat pelarut serta ekonomis. Namun metode sokletasi membutuhkan pemanasan untuk menguapkan pelarut sedangkan acetogenin merupakan zat yang rentan terhadap suhu. Untuk menyiasati hal ini maka dipilih pelarut yang memiliki titik didih rendah.
Acetogenin merupakan senyawa yang bersifat non polar, maka pelarut yang cocok digunakan adalah pelarut non polar seperti heksana dan aseton maupun campuran keduanya [10]. Karena senyawa ini rentan suhu tinggi maka pelarut yang dipilih yang memiliki titik didih lebih rendah dari suhu 600C. Oleh karena itu dalam
penelitian ini kami menggunakan pelarut aseton (C3H6O) dengan titik didih 560C.
Untuk bahan baku sendiri sebenarnya hampir diseluruh bagian tubuh tumbuhan sirsak tersebar senyawa acetogenin dengan kadar yang berbeda. Biji sirsak adalah bagian dari buah sirsak yang tidak diinginkan dan dibuang. Padahal sebenarnya biji sirsak juga mengandung senyawa acetogenin.
1.2 PERUMUSAN MASALAH
Dalam penelitian ini yang menjadi masalah adalah bahwa penggunaan acetogenin yang semakin meningkat terutama dalam bidang kesehatan (sebagai anti kanker) dan insektisida nabati, yang berasal dari biji sirsak belum mendapatkan hasil yang maksimal. Sehingga diperlukan cara yang efektif dalam proses ekstraksi.
1.3 TUJUAN PENELITIAN
Tujuan dari penelitian ini adalah :
1. Menentukan variabel-variabel yang berpengaruh dalam proses ekstraksi biji sirsak dalam usaha untuk mengambil acetogenin di dalamnya
2. Menentukan kondisi operasi proses ektraksi pada biji sirsak (Annona muricata
L) sehingga diperoleh % yield tinggi.
3. Senyawa acetogenin yang didapat dianalisa secara kualitatif dan kuantitatif.
4 1.4 MANFAAT PENELITIAN
Penelitian ini diharapkan dapat :
1. Memberikan informasi tambahan bagi industri tentang pemanfaatan biji sirsak (Annona muricata L) sebagai zat antioksidan dan antikanker.
2. Diperoleh kondisi operasi proses ekstraksi biji sirsak sehingga didapatkan hasil dengan % yield yang tinggi.
3. Dapat membuktikan adanya kandungan acetogenin secara kualitatif dalam ekstrak biji sirsak yang di peroleh.
1.5 RUANG LINGKUP PENELITIAN
Penelitian ini dilaksanakan pada Laboratorium Operasi Teknik Kimia, Departemen Teknik Kimia, Fakultas Teknik, Universitas Sumatera Utara. Adapun bahan yang digunakan pada penelitian ini adalah serbuk biji sirsak (Annona muricata
L) dan pelarut aseton (C3H6O), Sedangkan peralatan yang digunakan adalah neraca
analitik, oven, blender, termometer, gelas ukur, beaker glass, erlenmeyer, alat
soxhlet, dan sebagainya. Metode yang digunakan adalah ekstraksi menggunakan
soxhlet, dimana :
a. Variabel tetap
- Ukuran Partikel (mesh) : 50 - Suhu Ekstraksi (0C) : 58 - Volume Pelarut : 200 mL
- Pelarut : aseton (C3H6O)
b. Variabel berubah
- Waktu Ekstraksi (menit) : 30, 40, 50, 60 - Massa Sampel (gram) : 10, 20, 30
Analisa yang dilakukan pada ektraksi biji sirsak adalah :
1. Analisa kandungan acetogenin dalam ekstrak biji sirsak dengan menggunakan FTIR.
2. Analisa Kuantitatif (%Yield)
vii
ABSTRAK
Biji sirsak (Annona muricata L) mengandung senyawa bioaktif yang dapat berfungsi sebagai pestisida serta dapat digunakan sebagai obat cacing. Hal ini disebabkan karena biji sirsak mengandung senyawa acetogenin. Acetogenin merupakan metabolit sekunder dari tanaman suku Annonaceae yang disintetis melalui reaksi antara asam asetat yang memiliki rantai panjang asam lemak 35-39 atom karbon dan memiliki aktivitas sitotoksik. Penelitian ini bertujuan menentukan variabel–variabel yang berpengaruh dalam proses ekstraksi biji sirsak sehingga diperoleh %Yield yang tinggi, serta dapat menunjukkan keberadaan senyawa acetogenin secara kualitatif. Bahan-bahan yang digunakan adalah biji sirsak dan aseton. Variabel berubah dalam penelitian ini adalah massa sampel yaitu 10, 20, dan 30 gram serta waktu ekstraksi yaitu 30,40,50 dan 60 menit. Pelaksanaan penelitian ini dibagi dalam tiga tahap. Tahap pertama merupakan tahapan pendahuluan atau tahapan persiapan bahan baku. Tahap kedua merupakan tahapan ekstraksi biji sirsak menggunakan metode sokletasi dengan pelarut aseton sebesar 200 ml dan suhu ekstraksi 58oC. Tahap ketiga adalah
tahapan pemurnian hasil ekstraksi dengan distilasi. Hasil Penelitian diperoleh %Yield tertinggi sebesar 62 % yaitu pada variasi massa sampel 10 gram dan lama ekstraksi 40 menit. Analisa menggunakan FTIR menunjukkan keberadaan gugus seperti lakton, THF, hidroksil dan rantai alipatik yang menandakan keberadaan senyawa acetogenin.
Kata kunci : biji sirsak, acetogenin, soxhlet, FTIR.
viii
ABSTRACT
The soursop seeds (Annonamuricata L) contain bioactive compounds that can serve as a pesticide and used as an anthelmintic. It is because the seeds contain acetogenyn. Acetogenyn which was synthesized through reaction between polyketide-derived-acetic acid with 35-39 carbon atom in fatty acid, is the secondary metabolite of
Annonaceae plant. This research aims to determine the variables that influence in
soursop seeds extraction processso that high % yield value can be obtained, and to prove the presence of acetogenyn compound qualitatively. The materials used this research are soursop and acetone. The changing variables in this research is the mass of a sample that 10, 20, and 30 grams, and the extraction time is 30, 40, 50, and 60 minutes. This research is divided into three steps. The first step is the preliminary step or preparation of raw material. The second step is the extraction of soursop seeds using soxhletation method with 200 mL acetone andthe extraction temperature is 58oC. The last step is purification of the extract using distillation process. In this
research, the highest % yield value obtained is 62 % with the variation of the mass of a sample of 10 grams and extraction time is 40 minutes. FTIR analysys showedthe presence of function groups such as lactone, THF, hydroxyl and aliphatic chains
which indicates acetogenyn compound’s presence.
Keywords : Acetogenyn, FTIR, Soursop seeds, Soxhlet
EKSTRAKSI ACETOGENIN DARI BIJI SIRSAK
(Annona muricata L) DENGAN PELARUT ASETON
SKRIPSI
Oleh
SUCI DAMAYANTI SINAGA
110405037
DEPARTEMEN TEKNIK KIMIA
FAKULTAS TEKNIK
UNIVERSITAS SUMATERA UTARA
MEDAN
JANUARI 2016
EKSTRAKSI ACETOGENIN DARI BIJI SIRSAK
(Annona muricata L) DENGAN PELARUT ASETON
SKRIPSI
Oleh
SUCI DAMAYANTI SINAGA
110405037
SKRIPSI INI DIAJUKAN UNTUK MELENGKAPI SEBAGIAN
PERSYARATAN UNTUK MENJADI SARJANA TEKNIK
DEPARTEMEN TEKNIK KIMIA
FAKULTAS TEKNIK
UNIVERSITAS SUMATERA UTARA
JANUARI 2016
iii
PRAKATA
Puji dan syukur Penulis panjatkan kepada Tuhan Yang Maha Esa atas berkat dan karunia-Nya sehingga skripsi ini dapat diselesaikan. Tulisan ini merupakan Skripsi
dengan judul “Ekstraksi Acetogenin Dari Biji Sirsak (Annona muricata L) Dengan Pelarut Aseton”, berdasarkan hasil penelitian yang Penulis lakukan di Departemen Teknik Kimia Fakultas Teknik Universitas Sumatera Utara. Skripsi ini merupakan salah satu syarat untuk mendapatkan gelar Sarjana Teknik.
Hasil penelitian ini membuktikan bahwa pelarut aseton dapat mengekstrak senyawa acetogenin dari biji sirsak. Dengan adanya penelitian ini dapat memberi informasi bahwa terdapat senyawa acetogenin dalam biji sirsak yang saat ini sedang ramai diperbincangan mampu mengatasi penyakit kanker dan dapat digunakan sebagai biopestisida yang aman bagi kesehatan manusia.
Selama melakukan penelitian sampai penulisan skripsi ini penulis banyak mendapatkan bantuan dari berbagai pihak, Untuk itu Penulis mengucapkan terima kasih dan penghargaan sebesar-besarnya kepada:
1. Dra. Siswarni MZ, M.Si selaku Dosen Pembimbing yang telah banyak memberikan ilmu dan arahan dalam pelaksanaan penelitian.
2. Ir. Renita Manurung, M.T selaku Koordinator Penelitian Departemen Teknik Kimia, Fakultas Teknik, Universitas Sumatera Utara.
3. Dr. Ir. Iriany, MSi dan Farida Hanum ST,MT selaku Dosen Penguji yang telah memberikan saran dan masukan untuk kesempurnaan skripsi ini.
4. Dr. Eng. Ir. Irvan, M.Si selaku Ketua Departemen Teknik Kimia, Fakultas Teknik, Universitas Sumatera Utara.
5. Keluarga tercinta yang telah memberikan doa, perhatian, dan dorongan baik secara material maupun secara spiritual kepada penulis.
6. Nurhayani, selaku partner terbaik yang telah sabar dan membantu Penulis bekerja sama dalam menyelesaikan penelitian.
7. Sahabat – sahabat yang selalu ada Nurul, Rizka, Olip, Bunga, Gusti, Poppy, Rangga, Fauzi, dan Rio.
iv
8. Semua orang yang telah membantu penulis hingga penyusunan skripsi ini, yang tidak dapat ditulis namanya satu per satu.
Penulis menyadari bahwa skripsi ini masih jauh dari sempurna oleh karena itu Penulis mengharapkan saran dan masukan demi kesempurnaan skripsi ini. Semoga skripsi ini memberikan manfaat bagi pengembangan ilmu pengetahuan.
Medan, Januari 2016
Penulis
Suci Damayanti Sinaga
v
DEDIKASI
Skripsi ini saya persembahkan untuk :
Ayah & Ibu tercinta
Mandan Sinaga dan Rapejah Sihotang
Mereka yang menjadi asupan energi dan semangat bagiku,
perwujudan cinta murni yang takkan tergantikan, yang tak
pernah bosan memberikan kritikan dan nasehat yang
membangun. Selalu melakukan yang terbaik untuk menjagaku
hingga saat ini.
Terima kasih atas pengorbanan, cinta kasih sayang
dan do’a yang tak pernah putus selalu kalian
berikan kepadaku.
vi
RIWAYAT HIDUP PENULIS
Nama : Suci Damayanti Sinaga
NIM : 110405037
Tempat, tanggal lahir : Dolok Estate, 21 Juli 1993 Nama orang tua : M. Sinaga dan R. Sihotang Alamat orang tua : Huta III Pondok Ulu Nagori
Nanggar Bayu, Kec. Bosar Maligas, Kab. Simalungun
Asal Sekolah:
SD Negeri NO. 010204 Dolok Estate tahun 1999-2005
MTs Negeri Limapuluh tahun 2005 – 2008
SMA Negeri 1 Limapuluh tahun 2008 – 2011 Pengalaman Kerja dan Organisasi:
1. English Club Teknik USU periode 2013-2014 sebagai Sekertaris Bidang Public Speaking
2. Covalen Study Group (CSG) periode 2013-2014 sebagai Anggota Bidang Dakwah
3. Himpunan Mahasiswa Teknik Kimia (HIMATEK) FT USU periode 2014/2015 sebagai Wakil Bendahara Umum (WABENDUM) 4. Kerja Praktek di PT Ecogreen Oleochemicals Batam (2014). Artikel yang akan dipublikasikan pada :
1. Jurnal Teknik Kimia Fakultas Teknik Universitas Sumatera Utara yang berjudul “Ekstraksi Acetogenin dari Biji Sirsak (Annona muricata L) Dengan Pelarut Aseton”
vii
ABSTRAK
Biji sirsak (Annona muricata L) mengandung senyawa bioaktif yang dapat berfungsi sebagai pestisida serta dapat digunakan sebagai obat cacing. Hal ini disebabkan karena biji sirsak mengandung senyawa acetogenin. Acetogenin merupakan metabolit sekunder dari tanaman suku Annonaceae yang disintetis melalui reaksi antara asam asetat yang memiliki rantai panjang asam lemak 35-39 atom karbon dan memiliki aktivitas sitotoksik. Penelitian ini bertujuan menentukan variabel–variabel yang berpengaruh dalam proses ekstraksi biji sirsak sehingga diperoleh %Yield yang tinggi, serta dapat menunjukkan keberadaan senyawa acetogenin secara kualitatif. Bahan-bahan yang digunakan adalah biji sirsak dan aseton. Variabel berubah dalam penelitian ini adalah massa sampel yaitu 10, 20, dan 30 gram serta waktu ekstraksi yaitu 30,40,50 dan 60 menit. Pelaksanaan penelitian ini dibagi dalam tiga tahap. Tahap pertama merupakan tahapan pendahuluan atau tahapan persiapan bahan baku. Tahap kedua merupakan tahapan ekstraksi biji sirsak menggunakan metode sokletasi dengan pelarut aseton sebesar 200 ml dan suhu ekstraksi 58oC. Tahap ketiga adalah
tahapan pemurnian hasil ekstraksi dengan distilasi. Hasil Penelitian diperoleh %Yield tertinggi sebesar 62 % yaitu pada variasi massa sampel 10 gram dan lama ekstraksi 40 menit. Analisa menggunakan FTIR menunjukkan keberadaan gugus seperti lakton, THF, hidroksil dan rantai alipatik yang menandakan keberadaan senyawa acetogenin.
Kata kunci : biji sirsak, acetogenin, soxhlet, FTIR.
viii
ABSTRACT
The soursop seeds (Annonamuricata L) contain bioactive compounds that can serve as a pesticide and used as an anthelmintic. It is because the seeds contain acetogenyn. Acetogenyn which was synthesized through reaction between polyketide-derived-acetic acid with 35-39 carbon atom in fatty acid, is the secondary metabolite of
Annonaceae plant. This research aims to determine the variables that influence in
soursop seeds extraction processso that high % yield value can be obtained, and to prove the presence of acetogenyn compound qualitatively. The materials used this research are soursop and acetone. The changing variables in this research is the mass of a sample that 10, 20, and 30 grams, and the extraction time is 30, 40, 50, and 60 minutes. This research is divided into three steps. The first step is the preliminary step or preparation of raw material. The second step is the extraction of soursop seeds using soxhletation method with 200 mL acetone andthe extraction temperature is 58oC. The last step is purification of the extract using distillation process. In this
research, the highest % yield value obtained is 62 % with the variation of the mass