5
BAB II
TINJAUAN PUSTAKA
2.1 BUAH SIRSAK (Annona muricata Linn)
Sirsak atau yang lebih dikenal dengan durian belanda ini merupakan salah satu
jenis tanaman buah tropis. Sirsak merupakan famili dari Annonaceae, yang memiliki
119 spesis [4]. Sirsak merupakan salah satu buah – buahan yang menjanjikan untuk pasar international karena karakteristik gizi dan organoleptik yang sangat baik.
Namun buah ini memiliki struktur yang mudah rusak dan dapat berubah bentuk
karena beberapa kondisi lingkungan yang tidak sesuai. Struktur dan reologi dari buah
sirsak ini sangat mempengaruhi kualitas beberapa komponen yang terdapat dalam
buah [11].
Nama sirsak berasal dari bahasa Belanda yaitu Zuurzak, yang memiliki arti
kantung yang asam. Tumbuhan ini bisa tumbuh dimana saja. Buah yang besar dan
banyak dapat diperoleh dengan cara ditanam di daerah yang tanahnya cukup
mengandung air. Sirsak di Indonesia tumbuh dengan baik pada daerah yang
mempunyai ketinggian kurang dari lima meter di atas permukaan laut.
Adapun taksonomi dari sirsak (Annona muricata L) adalah :
Kingdom : Plantae
Division : Spermatophyta
Sub Divisio : Angiospermae
Kelas : Dicotyledonae
Ordo : Polycarpiceae
Famili : Annonaceae
Genus : Annona
Spesies : Annona muricata Linn
[12]
Buah sirsak terdiri dari 67,5 % daging buah, 20 % kulit, 8,5 % biji, dan 4 % inti
biji. Bagian daging buah yang berwarna putih terdiri dari 80 – 81 % air; 1 % protein, 18 % karbohidrat; 3,43 % asam; 24,5 5 gula dan vitamin B1, B2, dan C [13].
6
Gambar 2.1 Tanaman Sirsak [4]
Salah satu tanaman family annonaceae ini setelah dipelajari ternyata
mengandung senyawa aktif yang disebut acetogenin yang bersifat larvasidal dan juga
sebagai insektisida, akarisida, antiparasit dan bakterisida [10].
2.2 BIJI SIRSAK
Gambar 2.2 Biji Sirsak (Annona muricata L) [10]
Biji sirsak berwarna coklat kehitaman dan keras, berujung tumpul, permukaan
halus mengkilat, dengan ukuran panjang kira–kira 16,8 mm dan lebar 9,6 mm. Jumlah biji dalam satu buah bervariasi berkisar antara 20-70 butir biji normal,
sedangkan yang tidak normal berwarna putih kecoklatan dan tidak berisi [14].
Biji buah sirsak merupakan biji tunggal yang saling berhimpitan dan
dipisahkan oleh daging buah. Biji sirsak mengandung senyawa bioaktif yang dapat
berfungsi sebagai pestisida yaitu untuk membunuh ngengat dan kecoa. Selain sebagai
pestisida manfaat lain biji sirsak yang sering digunakan masyarakat adalah untuk
7
obat cacing. Masyarakat terdahulu bahkan sering menggunakan hasil ekstrak minyak
dari biji sirsak ini untuk menghilangkan kutu kepala. Dan dapat digunakan sebagai
racun penangkap ikan secara tradisional [12].
Senyawa toksik yang terdapat pada biji sirsak tersebut adalah :
Tabel 2.1 Senyawa Toksik Pada Biji dan Kulit biji Sirsak [11]
Parameter Biji Kulit biji
Tannin (mg/100g) 2,6 4,9
Phytate (mg/100g) 620,5 188,0
Cyanide (mg/100g) 3,7 10,8
Biji buah sirsak kaya akan minyak, protein, dan sedikit toksik. Biji sirsak
terdiri dari 22,1 % minyak kulit yang berwarna kuning, dan 21,43% protein. Minyak
biji ini terdiri dari 28,07% jenuh dan 71,93% tidak jenuh [9].
Pada biji sirsak ini juga terdapat senyawa acetogenin dan turunannya yang
ditemukan oleh beberapa peneliti terdahulu diantaranya : annonacin, corossolone,
corossolin, solamin, cis-annonacin, annomuricatin, muricattetrocin (A,B),
epomuricanin (A,B), muricin, cis-annonamontacin, annonacinone, xylomaticin,
reticuline [15]. Yang hampir kesemuanya bersifat anti terhadap kanker paru-paru,
kanker payudara, kanker otak, hepotema dan tumor. Adapun komponen kimia dari
biji sirsak ini dapat dilihat dari tabel di bawah ini :
Tabel 2.2 Komponen Kimia Biji Sirsak [16]
No Komponen Keterangan
1.
13. Annomuricatina Protein
14. Linoleic acid Lipid
8 2.3 ACETOGENIN
Acetogenin merupakan metabolit sekunder dari tanaman suku Annonaceae
yang disintesis melalui reaksi antara asam asetat - turunan poliketida yang memiliki
rantai panjang pada asam lemak yaitu 35-39 atom karbon. Sifat dari senyawa ini
berupa rantai panjang alipatik dengan gugus fungsi hidroksil, dan asetil karbonil
serta cincin 1-3 tetrahidrofuran [17].
Secara ilmiah acetogenin memiliki nama International Union of Pure and
Applied Chemistry (IUPAC) (
5S)-5-Methyl-3-[(2R,8R,13R)-2,8,13-trihydroxy-13-[(2,5R)-5-[(iR)-1-hydroxytridecyl]-2-tetrahydrofuranyl] tridecyl]-5H-furan 2-one.
Molekular formula acetogenin C35H64O7 dan massa molekul relatif (Mr) 596,88
g/mol [18].
Acetogenin memiliki efek biologis yang beragam termasuk sitotoksik,
antitumor, antimalaria, pestisida dan kegiatan antifeedant. Secara khusus, efek
penghambatan acetogenin pada mitokondria NADH-ubiquinone oksido reduktase
(kompleks I) yang menjadi catatan penting karena aktivitas biologis yang beragam.
Beberapa jenis senyawa seperti bullatacin (rolliniastatin-2) dan rolliniastatin-1,
adalah inhibitor yang paling ampuh dari enzim teridentifikasi sampai saat ini.
Acetogenin ditandai dengan dua unit fungsional, α tetrahidrofuran hydroxylated
(THF), cincin -lakton -unsaturated, dipisahkan oleh rantai alkil panjang, meskipun
dua unit masing-masing bisa memainkan peran penting dalam mengikat interaksi
dengan enzim [19].
Acetogenin tersebar di hampir seluruh bagian tumbuhan sirsak seperti daging
buah, daun, biji, dan akar. Dari hasil penelitian terdahulu ada lebih dari 100 jenis
asetogenin yang dapat diisolasi dari tanaman sirsak ini. Berikut akan ditunjukkan
beberapa struktur asetogenin yang terdapat pada beberapa bagian tumbuhan sirsak.
9
Gambar 2.3 Struktur Berbagai Jenis Asetogenin [15]
10 2.3 EKSTRAKSI
Ekstraksi adalah suatu proses pemisahan suatu senyawa dengan bantuan
pelarut. Pelarut yang digunakan harus dapat mengekstrak substansi yang diinginkan
tanpa melarutkan material lainnya [20].
2.3.1 Metode Ekstraksi
Adapun metode ekstraksi yang digunakan dalam ektraksi tanaman yaitu:
a. Maserasi
Dalam proses ini, seluruh atau kasar bubuk simplisia (bahan yang mengandung
solute yang akan diekstrak) ditempatkan dalam wadah tertutup yang diisi
pelarut yang sesuai dan dibiarkan pada suhu kamar untuk jangka waktu
minimal 3 hari dengan proses pengadukan sampai materi larut. Campuran
kemudian disaring, marc (bahan padat basah) ditekan, sehingga diperoleh
campuran solut dan pelarut yang kemudian dimurnikan untuk memperoleh
ekstrak yang diinginkan [20].
b. Soxhlet Extraction (SXE)
Metode Soklet merupakan standar untuk ekstraksi zat padat – cair lainnya. Fungsi soklet seperti ekstraksi kontinu dimana padatan secara kontinu
dikontakkan dengan pelarut yang fresh . Padatan (serbuk) yang akan diekstrak
diletakkan di dalam kertas saring (thimble) yang dimasukkan ke dalam
extraction chamber. Pelarut yang dipilih diletakkan di dalam solvent vessel
yang terletak dibagian bawah dan dipanaskan sampai titik didihnya. Pelarut
akan berubah jadi uap kemudian akan mengalami kondensasi di sepanjang
kondensor, kemudian pelarut yang sudah cair akan jatuh kebahan yang akan
diekstrak. Kemudian akan terjadi proses maserasi antar bahan dengan hasil
kondensasi pelarut. Bahan yang akan diekstrak akan terikut oleh pelarut yang
mengalir kebawah dan masuk kedalam solvent vessel. Kemudian pelarut akan
diuapkan kembali dan zat yang diekstrak akan tertinggal di bawah. Oleh karena
itu pelarut akan selalu fresh. Dan proses akan terus berulang seperti itu [21].
11
Ekstraksi dengan menggunakan soxhlet dengan cara pemanasan dimana pelarut
yang digunakan akan menguap dan terkondensasi kembali sehingga akan menjadi
lebih hemat, namun acetogenin merupakan suatu senyawa yang mana ekstraknya
rentan terhadap suhu tinggi, dan tidak bisa dilakukan jika suhu ekstraksi melewati
60 oC [22].
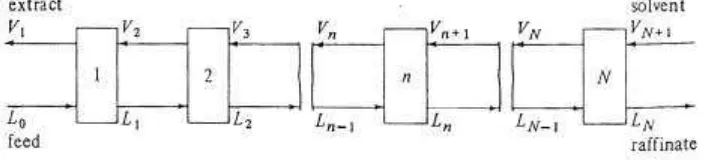
c. Ekstraksi berlawanan Arah
Aliran umpan mengandung zat terlarut A yang akan diekstraksi masuk pada ujung
yang satu sedangkan aliran pelarut masuk pada ujung satunya lagi. Aliran ekstrak
dan rafinat mengalir secara countercurrent dari satu tahap ke tahap lain dan
produk akhir adalah aliran ekstrak V1 yang meninggalkan kolom 1 dan aliran
rafinat LN yang meninggalkan kolom N [23].
Gambar 2.4 Ekstraksi Multi Tahap Countercurrent
[23]
d. Ekstraksi Ultrasionik dan Superkritik
Cairan superkritis telah diteliti sejak abad terakhir, Pada awalnya penelitian ini
berfokus pada penggunaan toluene superkritis dalam minyak bumi dan hasil
samping penyulingan minyak selama tahun 1970-an. Gas superkritis juga sedang
diselidiki sebagai salah satu cara menangani limbah beracun, dan sebagai media
sintesis yang terbaru. Penemuan terbesar pada decade terakhir adalah dengan
ditemukannya CO2 superkritis, karena memiliki nearambient sebuah suhu kritis
(31oC), sehingga bahan-bahan biologis dapat diproses di suhu sekitar 35oC.
Kepadatan superkritis CO2 sekitar 200 tekanan bar dekat hampir mendekati
kondisi untuk pelarut n- heksana, dan karakteristik solvasi juga mirip dengan
heksana, dengan demikian, CO2 dianggap bersifat non polar seperti pelarut
n-heksan [24].
Metode ekstraksi konvensional, seperti ayakan dan ekstraksi menggunakan
pelarut, telah menunjukkan efisiensi yang rendah dan potensi pencemaran
lingkungan karena volume besar pelarut organik yang digunakan, serta waktu
12
ekstraksi yang lama dan suhu tinggi yang diperlukan dalam metode-metode. Fluida
superkritis, microwave, dan metode ekstraksi ultrasonik muncul sebagai alternatif
yang sangat baik bila dibandingkan dengan metode ekstraksi konvensional, terutama
karena kurangnya kebutuhan untuk pelarut organik dan waktu ekstraksi yang relatif
singkat. Namun, metode ekstraksi fluida superkritis memiliki beberapa kekurangan
seperti waktu ekstraksi yang lebih lama dan tekanan ekstraksi yang tinggi, sehingga
biaya operasi yang tinggi dan membatasi aplikasi industri skala besar [25].
Setelah mempertimbangkan kelebihan dan kekurangan dari setiap metode,
maka metode yang dipilih dalam penelitian ini adalah metode sokletasi. Dengan
keuntungan sebagai berikut :
1. Merupakan salah satu metode yang sudah mapan
2. Proses ekstraksi berjalan efisien karena sampel akan terus menerus kontak
dengan pelarut segar.
3. Dapat menghasilkan yield yang tinggi
4. Pengoperasian sederhana
5. Ekonomis.
[22]
2.3.2 Faktor –Faktor Yang Mempengaruhi Proses Ekstraksi
Ada beberapa faktor yang dapat mempengaruhi ekstraksi, diantaranya:
1. Suhu
Kelarutan bahan yang diekstraksi dan difusivitas biasanya akan meningkat
dengan meningkatnya suhu, sehingga diperoleh laju ekstraksi yang tinggi.
Pada beberapa kasus, batas atas untuk suhu operasi ditentukan oleh beberapa
faktor, salah satunya adalah perlunya menghindari reaksi samping yang tidak
diinginkan [26].
2. Penyiapan bahan sebelum ekstraksi
Agar proses ekstraksi berlangsung dengan cepat dan efisien perlu dilakukan
tahap persiapan bahan baku seperti pengeringan dan penggilingan untuk
memperkecil ukuran partikel dan memperbesar luas permukaan yang
bersentuhan dengan pelarut. Pengurangan kadar air ini juga akan membuat
bahan dapat bertahan lama sebelum proses ekstraksi berlangsung. Bahan baku
13
juga perlu disimpan pada tempat yang kering untuk menjaga kelembabannya
sehingga tidak merusak kualitas hasil ekstraksi. Dengan pengeringan yang
sempurna akan dihasilkan ekstrak yang memiliki kemurnian tinggi [27].
3. Ukuran partikel
Semakin kecil ukuran partikel, semakin besar luas bidang kontak antara
padatan dan solven, serta semakin pendek jalur difusinya, yang menjadikan
laju transfer massa semakin tinggi [28].
4. Waktu
Semakin lama waktu ekstraksi maka akan semakin tinggi yield yang
diperoleh, namun bila ekstraksi telah mencapai batas maksimum maka
penambahan waktu tidak akan mempengaruhi laju ekstraksi [29].
5. Faktor solven
Dalam pemilihan pelarut ada beberapa faktor yang harus dipertimbangkan :
a. Selektivitas
Pelarut yang dipilih harus dapat melarutkan ekstrak yang diinginkan, bukan
komponen – komponen lain dari sampel yang akan diekstraksi. b. Kelarutan
Nilai kelarutan bahan yang diekstak terhadap pelarut harus cukup tinggi
agar pelarut mampu melarutkan ekstrak.
c. Viskositas
Viskositas pelarut berpengaruh pada koefisien difusi dan laju ekstraksi.
Viskositas pelarut yang rendah akan meningkatkan koefisien difusi sehingga
laju ekstraksi meningkat.
d. Kecocokan dengan solut
Pada umumnya pelarut tidak boleh bereaksi atau menyebabkan perubahan
secara kimia pada komponen – komponen bahan ekstraksi. e. Titik didih
Untuk memudahkan proses pemurnian ada baiknya perbedaan titik didih
antara pelarut dan bahan yang diekstrak cukup besar.
[30]
14 2.4 ASETON (C3H6O)
Aseton adalah keton yang paling penting. Cairan volatil (titik didih 56oC) dan mudah terbakar. Aseton adalah pelarut yang baik untuk senyawa organik banyak
digunakan sebagai pelarut pernis, lak dan plastik. Aseton bercampur dengan air
dalam segala perbandingan. Sifat ini digabungkan dengan volatilitasnya membuat
aseton sering digunakan sebagai pengering alat – alat gelas laboratorium [31].
Asetogenin termasuk salah satu senyawa yang rentan terhadap suhu. Struktur
asetogenin akan berubah pada suhu di atas 600C. Oleh karena itu dengan metode sokletasi yang menggunakan media pemanas diperlukan pelarut yang memiliki titik
didih dibawah suhu 600C [32].
Salah satu syarat pelarut yang baik adalah selektivitas pelarut tersebut terhadap
zat yang akan diekstrak. Seperti untuk mengekstrak senyawa polar digunakan pelarut
yang bersifat polar begitu juga sebaliknya. Sifat fisika kimia zat aktif asetogenin
yaitu memiliki nilai log P sebesar 7,71 yang menunjukkan bahwa asetogenin bersifat
non polar [33].
Kepolaran suatu senyawa dapat dilihat dari angka tetapan dielektrik [4].
Konstanta dielektrikum semakin besar maka sifat kepolaran dari suatu zat tinggi
begitu juga sebaliknya semakin kecil nilai konstanta dielektrikum suatu zat maka
sifat kepolarannya semakin rendah [34]. Berikut akan ditampilkan deret eluotropik
menurut Stahl untuk setiap zat pada suhu 250C.
Tabel 2.3 Deret Eluotropik Pelarut [34]
15
Peneliti terdahulu banyak menggunakan etanol dan metanol sebagai pelarut
dalam ekstraksi senyawa asetogenin dari tanaman sirsak ini. Dapat dilihat dari tabel
di atas bahwa nilai konstanta dielektrik aseton lebih kecil dibandingkan etanol
maupun metanol sehingga dapat disimpulkan bahwa aseton merupakan pelarut yang
kurang polar sehingga dapat dengan baik mengekstrak asetogenin dari sampel.
2.5 FTIR (Fourier Transform Infrared Spectroscopy)
FT-IR singkatan dari Fourier Transform Infrared, metode yang merupakan
spektroskopi inframerah. Dimana spektroskopi inframerah, dengan radiasi IR
dilewatkan melalui sampel. Beberapa radiasi infra merah diserap oleh sampel dan
beberapa di antaranya terelakkan (ditransmisikan), kemudian dihasilkan spektrum
yang merupakan molekul penyerapan dan transmisi, menunjukkan karakteristik
sampel. Yang mana spektrum yang terbentuk tidak akan sama untuk sampel lain dan
sangat spesifik untuk suatu sampel. Hal ini membuat spektroskopi inframerah
berguna untuk beberapa jenis analisis [35].
Informasi yang dapat diberikan oleh FT-IR [35] : • Dapat mengidentifikasi bahan yang tidak diketahui • Dapat menentukan kualitas atau konsistensi sampel • Dapat menentukan jumlah komponen dalam campuran
Spektroskopi yang biasa digunakan adalah frekuensi spektroskopi domain di
mana Radiant Data listrik dicatat sebagai fungsi frekuensi. Durasi spektroskopi
domain, yang dicapai dengan Fourier Transform (FT), data daya radiasi sebagai
fungsi waktu. kemudian daya radiasi (ν) diplot terhadap frekuensi (ν1) (Hz) [36].
16
Gambar 2.5 Daerah Waktu dan Frekuensi Spektrum [35]
.Beberapa keuntungan utama dari FT-IR selama teknik dispersif meliputi [34]:
a) Kecepatan: Karena semua frekuensi diukur secara bersamaan, sebagian besar
pengukuran oleh FT-IR. dibuat dalam hitungan detik bukan beberapa menit. Ini
kadang-kadang disebut sebagai Felgett Advantage.
b) Sensitivitas: Sensitivitas secara dramatis ditingkatkan dengan FT-IR untuk
banyak alasan. Detektor dipekerjakan jauh lebih sensitif, peletakan optik jauh
lebih tinggi (disebut sebagai keuntungan Jacquinot) yang menghasilkan tingkat
kebisingan yang jauh lebih rendah, dan scan cepat memungkinkan coaddition
beberapa scan untuk mengurangi kebisingan pengukuran acak untuk setiap
tingkat yang diinginkan (disebut sebagai sinyal rata-rata).
c) Kesederhanaan Teknik: Cermin bergerak di interferometer adalah satu-satunya
bagian dalam instrumen yang bergerak secara kontinu. Dengan demikian, ada
sedikit kemungkinan kerusakan mekanis.
d) Internal dikalibrasi: Instrumen ini menggunakan laser HeNe sebagai panjang
gelombang internal yang kalibrasi standar (disebut sebagai keuntungan
Connes). Instrumen ini adalah mengkalibrasi-diri dan tidak perlu dikalibrasi
oleh pengguna.
Dengan demikian, Fourier Transform Infrared (FT-IR) teknik telah membawa
signifikan praktis keuntungan untuk spektroskopi inframerah. Ini telah
memungkinkan pengembangan banyak sampel baru teknik yang dirancang untuk
17
mengatasi masalah yang menantang yang mungkin oleh lebih tua teknologi. Hal ini
telah membuat penggunaan analisis inframerah hampir tak terbatas [34].
Keberadaan suatu senyawa atau gugus dalam spektrum ditandai dengan
bilangan gelombang tertentu sesuai dengan standar.
Tabel 2.4 Daftar Panjang Gelombang Suatu Senyawa /Gugus Fungsi [36]
Range (cm-1) dan
intensitas Grup dan Kelas
3420 – 3250 3100 – 2400 2990 – 2850 1870 – 1830 1780 – 1760 1750 – 1730 1375 – 1275 1280 – 1150 740 – 720
- OH dalam alkohol dan fenol - OH dalam asam karboksilik
CH3– CH2 alipatik
C=O dalam lakton C=O dalam lakton C=O dalam lakton
THF (CH2def)
C – O – C lakton CH2 dalam hidrokarbon
![Gambar 2.1 Tanaman Sirsak [4]](https://thumb-ap.123doks.com/thumbv2/123dok/1774076.1128167/2.595.266.389.430.557/gambar-tanaman-sirsak.webp)
![Tabel 2.1 Senyawa Toksik Pada Biji dan Kulit biji Sirsak [11]](https://thumb-ap.123doks.com/thumbv2/123dok/1774076.1128167/3.595.164.479.509.737/tabel-senyawa-toksik-pada-biji-kulit-biji-sirsak.webp)
![Gambar 2.3 Struktur Berbagai Jenis Asetogenin [15]](https://thumb-ap.123doks.com/thumbv2/123dok/1774076.1128167/5.595.122.527.78.674/gambar-struktur-berbagai-jenis-asetogenin.webp)
![Tabel 2.3 Deret Eluotropik Pelarut [34] Tetapan Dielektrik 1,890](https://thumb-ap.123doks.com/thumbv2/123dok/1774076.1128167/10.595.178.462.515.724/tabel-deret-eluotropik-pelarut-tetapan-dielektrik.webp)
![Gambar 2.5 Daerah Waktu dan Frekuensi Spektrum [35]](https://thumb-ap.123doks.com/thumbv2/123dok/1774076.1128167/12.595.219.444.93.277/gambar-daerah-waktu-dan-frekuensi-spektrum.webp)
![Tabel 2.4 Daftar Panjang Gelombang Suatu Senyawa /Gugus Fungsi [36] Range (cm-1) dan](https://thumb-ap.123doks.com/thumbv2/123dok/1774076.1128167/13.595.137.501.189.355/tabel-daftar-panjang-gelombang-senyawa-gugus-fungsi-range.webp)