ABSTRAK
NANA RUSMANA. Optimalisasi Pembuatan Poli(asamlaktat) tanpa Katalis. Dibimbing oleh TETTY KEMALA dan AHMAD SJAHRIZA.
Poli(asamlaktat) (PLA) merupakan poliester alifatik yang dapat digunakan untuk bahan baku pembuatan plastik biodegradabel dan bahan penyalut obat. PLA dibuat dengan polikondensasi langsung asam laktat tanpa katalis pada waktu 24 dan 32 jam dengan suhu 150 dan 160 °C . PLA yang dihasilkan dicirikan dengan spektrometer inframerah transformasi fourier (FTIR) dan bobot molekul diukur dengan viskometer. Hasil penelitian menunjukkan bahwa penambahan waktu dan suhu mempengaruhi bobot molekul PLA yang dihasilkan. Bobot molekul tertinggi didapatkan dengan memanaskan asam laktat pada suhu 160 °C selama 24 jam, yaitu 12375.99 g/mol. Sementara bobot molekul terendah diperoleh pada suhu 160 °C selama 32 jam, yaitu 519.82 g/mol. Pola spektrum FTIR menunjukkan adanya vibrasi ulur C-H pada 2998.81 cm-1 dan 2946.60 cm1, gugus karbonil (C=O) pada 1763.73 cm-1, vibrasi tekuk C-C pada 1458.28 cm-1, dan vibrasi tekuk C-O pada 1184.80 cm-1.
ABSTRACT
NANA RUSMANA. Optimalitation of Poly(lacticacid) Synthesis without Catalyst. Supervised by TETTY KEMALA and AHMAD SJAHRIZA.
PENDAHULUAN
Penggunaan polimer biodegradabel
sintetik dalam dua dekade ini berkembang dengan pesat terutama di bidang farmasi dan
kemasan (Leksono 2008). Berdasarkan
laporan BPS (1999), produksi polimer
biodegradabel di dunia diproyeksikan
mencapai hampir 1,200,000 ton/tahun. Di
beberapa negara maju, bahan polimer
biodegradabel sudah ada yang diproduksi
secara komersial, seperti poli(hidroksi
alkanoat) (PHA), poli(ε-kaprolakton) (PCL), dan poli(butilena suksinat) (PBS), namun sebagian besar bahan baku untuk pembuatan
polimer biodegradabel tersebut masih
menggunakan sumberdaya alam yang tidak terbarukan (non-renewable resources) dan tidak hemat energi. Oleh karena itu, poliasamlaktat (PLA) menjadi kandidat yang menjanjikan karena dapat diproduksi dari bahan alam seperti pati-patian (Pranamuda 2001).
Aplikasi PLA dalam industri farmasi digunakan sebagai bahan penyalut obat,
benang jahit pembedahan, dan media
transplantasi jaringan atau peralatan ortopedik (Lu & Chen 2004). PLA pada umumnya dibuat dengan menggunakan katalis. Katalis yang biasa digunakan dalam pembuatan PLA adalah timah(II) oktoat (SnOct2). SnOct2
merupakan katalis homogen dan bersifat toksik. Katalis ini sulit dipisahkan bila sudah berikatan dengan polimer (Badami 2004). Hal ini, tentunya sangat berbahaya jika PLA dimanfaatkan sebagai bahan penyalut obat.
Selain dari itu, harga PLA yang ada di pasaran saat ini relatif mahal karena dalam
pembuatannya menggunakan alat-alat
canggih, teknologi tinggi, dan bobot
molekulnya tinggi. Pembuatan PLA dengan katalis menghasilkan bobot molekul yang tidak jauh berbeda dengan PLA tanpa menggunakan katalis pada kondisi suhu dan waktu yang sama (Fukuzaki et al. 1989, diacu dalam Gonzales et al. 2003). Oleh karena itu, perlu dilakukan optimalisasi pembuatan PLA tanpa menggunakan katalis.
Menurut Gonzales et al. (1999),
pembuatan PLA dengan cara kondensasi merupakan metode yang lebih sederhana, tetapi menghasilkan PLA berbobot molekul rendah. Penyederhanaan dan pengoptimalan dalam pembuatan PLA tanpa katalis perlu diteliti lebih lanjut guna mengurangi biaya produksi dan aman jika diaplikasikan dalam industri farmasi. Pengoptimalan kondisi yang
dilakukan pada penelitian ini adalah waktu polimerisasi dan suhu.
Polikondensasi asam laktat dapat
dilakukan dalam larutan pada tekanan atmosfer dan tekanan tereduksi (Dutkiewicz et al. 2003) atau polikondensasi secara langsung tanpa katalis (Fukuzaki et al. 1989, diacu dalam Gonzales et al. 1999). Penelitian ini bertujuan melihat pengaruh suhu dan waktu polimerisasi terhadap pembuatan PLA tanpa katalis kemudian membandingkan hasil PLA tanpa katalis tersebut dengan PLA yang menggunakan katalis SnOct2 dan diharapkan
pembuatan PLA tanpa katalis memiliki bobot molekul yang tidak jauh berbeda dengan bobot molekul PLA yang menggunakan katalis.
TINJAUAN PUSTAKA
Asam Laktat
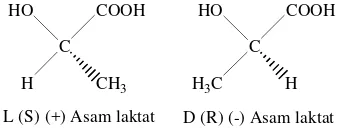
Asam laktat (asam 2-hidroksipropanoat) merupakan asam organik tiga karbon (BM 90.08 g/mol) yang memiliki gugus karboksil dan hidroksil. Asam yang dikenal dengan nama asam susu ini tersedia dalam bentuk L-(S)-(+) dan D-(R)-(-)-asam laktat (Gambar 1) (Vink et al. 2003). Dua bentuk enantiomer ini disebabkan oleh asam laktat memiliki satu atom karbon asimetris. Asam laktat yang biasa digunakan untuk pembuatan PLA adalah L-asam laktat dan campuran rasemiknya (asam dan D-(asam laktat dengan komposisi L-asam lebih besar daripada D-L-asam laktat) (Dutkiewics et al. 2003).
C COOH H HO CH3 C COOH
H3C
HO
H L (S) (+) Asam laktat D (R) (-) Asam laktat
Gambar 1 Rumus molekul D (-) dan L (+) asam laktat.
Asam laktat merupakan zat yang tidak berbau dan tidak berwarna. Asam laktat memiliki titik didih 122 °C dan titik leleh 18 °C. Asam yang dapat menyebabkan rasa lelah pada tubuh ini memiliki densitas sebesar 1.21 g/cm3 (Vink et al. 2003).
Asam laktat bersifat asam dengan
kekuatan pH 2.8 (10 g/L H2O pada suhu
PENDAHULUAN
Penggunaan polimer biodegradabel
sintetik dalam dua dekade ini berkembang dengan pesat terutama di bidang farmasi dan
kemasan (Leksono 2008). Berdasarkan
laporan BPS (1999), produksi polimer
biodegradabel di dunia diproyeksikan
mencapai hampir 1,200,000 ton/tahun. Di
beberapa negara maju, bahan polimer
biodegradabel sudah ada yang diproduksi
secara komersial, seperti poli(hidroksi
alkanoat) (PHA), poli(ε-kaprolakton) (PCL), dan poli(butilena suksinat) (PBS), namun sebagian besar bahan baku untuk pembuatan
polimer biodegradabel tersebut masih
menggunakan sumberdaya alam yang tidak terbarukan (non-renewable resources) dan tidak hemat energi. Oleh karena itu, poliasamlaktat (PLA) menjadi kandidat yang menjanjikan karena dapat diproduksi dari bahan alam seperti pati-patian (Pranamuda 2001).
Aplikasi PLA dalam industri farmasi digunakan sebagai bahan penyalut obat,
benang jahit pembedahan, dan media
transplantasi jaringan atau peralatan ortopedik (Lu & Chen 2004). PLA pada umumnya dibuat dengan menggunakan katalis. Katalis yang biasa digunakan dalam pembuatan PLA adalah timah(II) oktoat (SnOct2). SnOct2
merupakan katalis homogen dan bersifat toksik. Katalis ini sulit dipisahkan bila sudah berikatan dengan polimer (Badami 2004). Hal ini, tentunya sangat berbahaya jika PLA dimanfaatkan sebagai bahan penyalut obat.
Selain dari itu, harga PLA yang ada di pasaran saat ini relatif mahal karena dalam
pembuatannya menggunakan alat-alat
canggih, teknologi tinggi, dan bobot
molekulnya tinggi. Pembuatan PLA dengan katalis menghasilkan bobot molekul yang tidak jauh berbeda dengan PLA tanpa menggunakan katalis pada kondisi suhu dan waktu yang sama (Fukuzaki et al. 1989, diacu dalam Gonzales et al. 2003). Oleh karena itu, perlu dilakukan optimalisasi pembuatan PLA tanpa menggunakan katalis.
Menurut Gonzales et al. (1999),
pembuatan PLA dengan cara kondensasi merupakan metode yang lebih sederhana, tetapi menghasilkan PLA berbobot molekul rendah. Penyederhanaan dan pengoptimalan dalam pembuatan PLA tanpa katalis perlu diteliti lebih lanjut guna mengurangi biaya produksi dan aman jika diaplikasikan dalam industri farmasi. Pengoptimalan kondisi yang
dilakukan pada penelitian ini adalah waktu polimerisasi dan suhu.
Polikondensasi asam laktat dapat
dilakukan dalam larutan pada tekanan atmosfer dan tekanan tereduksi (Dutkiewicz et al. 2003) atau polikondensasi secara langsung tanpa katalis (Fukuzaki et al. 1989, diacu dalam Gonzales et al. 1999). Penelitian ini bertujuan melihat pengaruh suhu dan waktu polimerisasi terhadap pembuatan PLA tanpa katalis kemudian membandingkan hasil PLA tanpa katalis tersebut dengan PLA yang menggunakan katalis SnOct2 dan diharapkan
pembuatan PLA tanpa katalis memiliki bobot molekul yang tidak jauh berbeda dengan bobot molekul PLA yang menggunakan katalis.
TINJAUAN PUSTAKA
Asam Laktat
Asam laktat (asam 2-hidroksipropanoat) merupakan asam organik tiga karbon (BM 90.08 g/mol) yang memiliki gugus karboksil dan hidroksil. Asam yang dikenal dengan nama asam susu ini tersedia dalam bentuk L-(S)-(+) dan D-(R)-(-)-asam laktat (Gambar 1) (Vink et al. 2003). Dua bentuk enantiomer ini disebabkan oleh asam laktat memiliki satu atom karbon asimetris. Asam laktat yang biasa digunakan untuk pembuatan PLA adalah L-asam laktat dan campuran rasemiknya (asam dan D-(asam laktat dengan komposisi L-asam lebih besar daripada D-L-asam laktat) (Dutkiewics et al. 2003).
C COOH H HO CH3 C COOH
H3C
HO
H L (S) (+) Asam laktat D (R) (-) Asam laktat
Gambar 1 Rumus molekul D (-) dan L (+) asam laktat.
Asam laktat merupakan zat yang tidak berbau dan tidak berwarna. Asam laktat memiliki titik didih 122 °C dan titik leleh 18 °C. Asam yang dapat menyebabkan rasa lelah pada tubuh ini memiliki densitas sebesar 1.21 g/cm3 (Vink et al. 2003).
Asam laktat bersifat asam dengan
kekuatan pH 2.8 (10 g/L H2O pada suhu
2
disebabkan adanya gugus hidroksi pada posisi α.
Polikondensasi
Polimerisasi kondensasi melibatkan
pelepasan molekul kecil seperti air.
Pembentukan polimer secara kondensasi dapat dilakukan pada monomer yang memiliki gugus fungsi hidroksil dan karboksilat seperti asam laktat dan asam glikolat. Pembentukan polimer dengan cara ini diawali dengan bereaksinya dua monomer membentuk dimer dan air. Setelah itu, dimer yang terbentuk bereaksi dengan monomer membentuk trimer. Trimer yang telah terbentuk dapat bereaksi dengan dimer membentuk pentamer atau dapat pula bereaksi dengan monomer dan dimer. Reaksi ini terus berlangsung sampai terbentuk polimer. Reaksi yang terjadi pada polimerisasi yang melibatkan pelepasan air adalah:
monomer + monomer → dimer + H2O
monomer + dimer → trimer + H2O
monomer + trimer → tetramer + H2O
dimer + dimer → tetramer + H2O
dimer + trimer → pentamer + H2O
oligomer + oligomer → polimer + H2O
Reaksi polikondensasi bersifat dapat balik
sehingga air yang dilepaskan harus
dipindahkan untuk menghasilkan polimer berbobot molekul tinggi (Allcock & Lampe
1981). Polikondensasi dapat dilakukan
dengan baik pada cairan maupun padatan, yang dikenal dengan melt polycondentation. Polimer yang dapat dibuat dengan metode
melt polycondentation adalah PLA yang dibuat dari Na-kloropropionat dan PGA yang dibuat dari Na-kloroasetat. Molekul kecil yang dilepaskan pada pembentukan PLA dan PGA berupa garam NaCl (Lee et al. 2005). Sementara polimer yang dibuat dengan polikondensasi biasa di antaranya adalah PLA yang dibuat dari asam laktat dan PGA yang dibuat dari asam glikolat, poliester, dan polikaprolakton.
Poliasamlaktat (PLA)
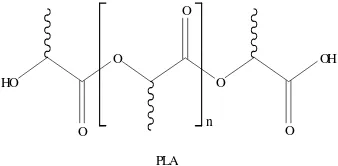
Poliasamlaktat (Gambar 2) merupakan poliester alifatik serbaguna yang tersusun atas monomer asam laktat (Gruber & O’Brien 2002). PLA telah dikenal sejak tahun 1932. PLA pertama kali disintesis oleh Wallace Carothers, peneliti Dupont, dengan cara memanaskan asam laktat pada kondisi vakum. PLA memiliki beberapa gugus hidroksil pada
ujung rantainya. Adanya gugus ini
menyebabkan PLA dapat terdegradasi. PLA merupakan polimer yang dapat terdegradasi secara alami oleh panas, cahaya, bakteri, maupun oleh proses hidrolisis. Selain itu, polimer ini juga bersifat biokompatibel, yaitu cocok dalam tubuh tanpa menimbulkan efek yang berbahaya dan bersifat termoplastik.
Gambar 2 Struktur kimia PLA.
Pembuatan PLA dapat dilakukan dengan beberapa cara, yaitu polikondensasi asam laktat dan reaksi pembukaan cincin laktida. Pembuatan PLA tidak hanya dengan cara polimerisasi asam laktat, namun PLA dapat pula dihasilkan dari pemanasan alkali-kloropropionat (natrium atau kalium
kloropropionat) (Siedler et al. 2001).
Kovalchuk et al. (2005) membuat PLA
dengan cara memanaskan
natrium-2-kloropropionat pada suhu 170 °C. PLA yang
terbentuk dari pemanasan
Na-2-kloropropionat ini berupa PLA yang memiliki bobot molekul 4170 g/mol, titik transisi gelas 45 °C, dan derajat polimerisasi sebesar 58, namun metode ini sulit mengontrol gugus ujung, bobot molekul, dan distribusi bobot
molekulnya (Badami 2004). Kelebihan
metode ini adalah mudah dikerjakan dan biaya relatif rendah.
3
BAHAN DAN METODE
Alat dan Bahan
Alat-alat yang digunakan adalah FTIR Shimadzu 8400 dan viskometer Ostwald. Bahan-bahan yang digunakan adalah asam laktat 95%, dan katalis SnOct2.
Tahapan Penelitian
Penelitian ini terdiri atas dua tahap, yaitu pembuatan PLA dengan polikondensasi asam laktat dan pencirian PLA. Pencirian yang dilakukan meliputi penentuan bobot molekul dengan metode viskometri dan pencirian gugus fungsi dengan FTIR. Diagram alir pembuatan PLA dapat dilihat pada Lampiran 1 dan 2.
Pembuatan PLA (Gonzales et al. 1999)
Pembuatan PLA dilakukan dengan
beberapa ragam, yaitu suhu (150 dan 160 ºC), waktu (24 dan 32 jam), serta adanya pembuatan PLA menggunakan katalis SnOct2
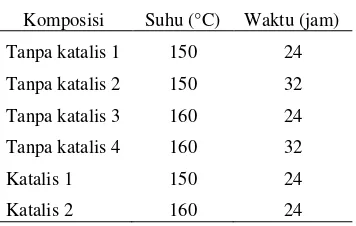
dengan tujuan untuk membandingkan bobot molekul PLA hasil sintesis tanpa katalis dengan bobot molekul PLA menggunakan katalis. Susunan modifikasi pembuatan PLA disajikan pada Tabel 1.
Gelas piala 100 mL dibersihkan,
dikeringkan, dan ditimbang bobotnya. Setelah itu, asam laktat sebanyak 25 mL dimasukkan ke dalam gelas piala dan ditimbang. Selanjutnya, asam laktat tersebut dipanaskan secara perlahan-lahan sampai suhu 120 ºC selama 1 jam. Setelah itu, pemanasan dilanjutkan sampai suhu dan waktu yang diinginkan. Kemudian PLA yang dihasilkan didinginkan pada suhu ruang dan ditimbang.
Tabel 1 Susunan modifikasi pembuatan PLA
Komposisi Suhu (°C) Waktu (jam)
Tanpa katalis 1 150 24
Tanpa katalis 2 150 32
Tanpa katalis 3 160 24
Tanpa katalis 4 160 32
Katalis 1 150 24
Katalis 2 160 24
Pencirian PLA
Pengukuran bobot molekul (Kaitian et al. 1996). Pengukuran viskositas digunakan untuk menghitung bobot molekul rata-rata. PLA dengan konsentrasi 0.1, 0.2, 0.3, 0.4, dan 0.5% dilarutkan dalam etil asetat dan diukur viskositasnya dengan viskometer Ostwald pada suhu 25 °C (suhu konstan). Setelah itu, viskositas relatif (ηr) ditentukan dengan cara
membandingkan waktu alir pelarut dengan waktu alir larutan polimer (t0/t). Viskositas
intrinsik [η] dicari dengan cara memplotkan
ηspesifik/[PLA] sebagai sumbu y dan konsentrasi
sebagai sumbu x.
Bobot molekul (Mv) dan bobot molekul
rata-rata ditentukan berdasarkan persamaan
Mark-Houwink:
[η] = k(Mv)a
k dan a merupakan tetapan yang bergantung pada pelarut, polimer, dan suhu. Pelarut dan suhu yang akan digunakan pada penelitian ini adalah etil asetat dan 25 °C. Nilai k dan a
secara berturut-turut adalah 1.58×10-4 dan 0.78.
Analisis Gugus Fungsi dengan FTIR.
Sampel ditempatkan dalam cell holder,
kemudian dicari spektrum yang sesuai.
Hasilnya didapat berupa difraktogram
hubungan antara bilangan gelombang dan transmitans (%).
HASIL DAN PEMBAHASAN
PLA Hasil Sintesis
Poliasamlaktat yang dihasilkan pada
penelitian ini menggunakan metode
polikondesasi asam laktat secara langsung dengan suhu tinggi. Metode ini merupakan metode yang lebih sederhana dibandingkan dengan metode pembuatan PLA lainnya (Gonzales et al. 1999). Pada pembuatan PLA terjadi reaksi bertahap dimulai dengan pelepasan molekul air dari molekul asam
laktat kemudian terjadi polikondensasi
menjadi laktida dan selanjutnya dengan
pemanasan terjadi dimerisasi untuk
membentuk PLA.
Keberadaan molekul air dapat
mengganggu proses polimerisasi dan
3
BAHAN DAN METODE
Alat dan Bahan
Alat-alat yang digunakan adalah FTIR Shimadzu 8400 dan viskometer Ostwald. Bahan-bahan yang digunakan adalah asam laktat 95%, dan katalis SnOct2.
Tahapan Penelitian
Penelitian ini terdiri atas dua tahap, yaitu pembuatan PLA dengan polikondensasi asam laktat dan pencirian PLA. Pencirian yang dilakukan meliputi penentuan bobot molekul dengan metode viskometri dan pencirian gugus fungsi dengan FTIR. Diagram alir pembuatan PLA dapat dilihat pada Lampiran 1 dan 2.
Pembuatan PLA (Gonzales et al. 1999)
Pembuatan PLA dilakukan dengan
beberapa ragam, yaitu suhu (150 dan 160 ºC), waktu (24 dan 32 jam), serta adanya pembuatan PLA menggunakan katalis SnOct2
dengan tujuan untuk membandingkan bobot molekul PLA hasil sintesis tanpa katalis dengan bobot molekul PLA menggunakan katalis. Susunan modifikasi pembuatan PLA disajikan pada Tabel 1.
Gelas piala 100 mL dibersihkan,
dikeringkan, dan ditimbang bobotnya. Setelah itu, asam laktat sebanyak 25 mL dimasukkan ke dalam gelas piala dan ditimbang. Selanjutnya, asam laktat tersebut dipanaskan secara perlahan-lahan sampai suhu 120 ºC selama 1 jam. Setelah itu, pemanasan dilanjutkan sampai suhu dan waktu yang diinginkan. Kemudian PLA yang dihasilkan didinginkan pada suhu ruang dan ditimbang.
Tabel 1 Susunan modifikasi pembuatan PLA
Komposisi Suhu (°C) Waktu (jam)
Tanpa katalis 1 150 24
Tanpa katalis 2 150 32
Tanpa katalis 3 160 24
Tanpa katalis 4 160 32
Katalis 1 150 24
Katalis 2 160 24
Pencirian PLA
Pengukuran bobot molekul (Kaitian et al. 1996). Pengukuran viskositas digunakan untuk menghitung bobot molekul rata-rata. PLA dengan konsentrasi 0.1, 0.2, 0.3, 0.4, dan 0.5% dilarutkan dalam etil asetat dan diukur viskositasnya dengan viskometer Ostwald pada suhu 25 °C (suhu konstan). Setelah itu, viskositas relatif (ηr) ditentukan dengan cara
membandingkan waktu alir pelarut dengan waktu alir larutan polimer (t0/t). Viskositas
intrinsik [η] dicari dengan cara memplotkan
ηspesifik/[PLA] sebagai sumbu y dan konsentrasi
sebagai sumbu x.
Bobot molekul (Mv) dan bobot molekul
rata-rata ditentukan berdasarkan persamaan
Mark-Houwink:
[η] = k(Mv)a
k dan a merupakan tetapan yang bergantung pada pelarut, polimer, dan suhu. Pelarut dan suhu yang akan digunakan pada penelitian ini adalah etil asetat dan 25 °C. Nilai k dan a
secara berturut-turut adalah 1.58×10-4 dan 0.78.
Analisis Gugus Fungsi dengan FTIR.
Sampel ditempatkan dalam cell holder,
kemudian dicari spektrum yang sesuai.
Hasilnya didapat berupa difraktogram
hubungan antara bilangan gelombang dan transmitans (%).
HASIL DAN PEMBAHASAN
PLA Hasil Sintesis
Poliasamlaktat yang dihasilkan pada
penelitian ini menggunakan metode
polikondesasi asam laktat secara langsung dengan suhu tinggi. Metode ini merupakan metode yang lebih sederhana dibandingkan dengan metode pembuatan PLA lainnya (Gonzales et al. 1999). Pada pembuatan PLA terjadi reaksi bertahap dimulai dengan pelepasan molekul air dari molekul asam
laktat kemudian terjadi polikondensasi
menjadi laktida dan selanjutnya dengan
pemanasan terjadi dimerisasi untuk
membentuk PLA.
Keberadaan molekul air dapat
mengganggu proses polimerisasi dan
4
CH3 -H2O
Reaksi yang terjadi dalam pembentukan PLA adalah:
PLA yang dihasilkan dari pemanasan asam laktat pada suhu 160 °C memiliki warna cokelat yang lebih pekat dibandingkan dengan hasil pemanasan pada suhu 150 °C karena
semakin tinggi suhu pemanasan akan
menghasilkan residu karbon yang banyak dan terjadi oksidasi yang berlebih sehingga menghasilkan warna PLA yang lebih pekat (Gambar 3).
PLA yang dihasilkan dari sintesis ini berupa campuran rasemiknya (D,L-PLA) karena menurut Dutkiewicz et al. (2003) PLA yang disintesis pada suhu lebih dari 140 оC akan dihasilkan bentuk rasemiknya. PLA dalam bentuk D,L-PLA memiliki waktu degradasi yang lebih cepat dibandingkan L-PLA (Lu & Chen 2004).
Tanpa katalis 1 Tanpa katalis 2 Katalis 1
Tanpa katalis 3 Tanpa katalis 4 Katalis 2
Gambar 3 PLA hasil sintesis.
PLA yang dihasilkan dari pemanasan selama 32 jam pada suhu 160 ºC berwarna cokelat tua yang mendekati warna hitam. Hal ini menunjukkan bahwa pemanasan lebih dari 32 jam akan menyebabkan warna PLA semakin hitam dan hangus terdegradasi oleh panas dan terjadi oksidasi yang berlebihan.
PLA mudah terdegradasi oleh panas karena memiliki beberapa gugus hidroksil pada rantai ujungnya (Arches 2006).
PLA yang dihasilkan larut dalam pelarut
aseton, diklorometana, etil asetat, dan
kloroform tetapi tidak larut dalam air, sedangkan asam laktat yang digunakan larut air dan etil asetat. Asam laktat larut dalam air karena memiliki rantai karbon yang pendek, namun apabila asam laktat telah menjadi polimer menjadi tidak larut dalam air karena sifatnya akan menjadi nonpolar (Alger 1989). Bobot dan rendemen PLA yang dihasilkan dipengaruhi oleh waktu dan suhu pemanasan (Tabel 2). Semakin tinggi suhu yang digunakan akan menurunkan bobot dan rendemen PLA yang dihasilkan begitu juga
dengan semakin bertambahnya waktu
pemanasan. Hal ini dikarenakan monomer asam laktat yang digunakan terus menguap pada saat pemanasan sehingga jika monomer tersebut telah menjadi polimer maka bobot dan rendemen yang dihasilkan akan semakin kecil. Adanya penambahan katalis pada pembuatan PLA dengan kondisi waktu dan suhu yang sama seperti pembuatan PLA tanpa katalis dihasilkan bobot dan rendemen yang lebih kecil. Hal ini disebabkan karena sebelum waktu dan suhu yang diinginkan, PLA dengan penambahan katalis akan terlebih dahulu terbentuk polimer dan saat mencapai suhu dan
waktu yang diinginkan maka laju
polimerisasinya akan menurun sehingga bobot dan rendemen yang dihasilkan lebih kecil
karena katalis berfungsi mempercepat
terjadinya proses polimerisasi. Hasil
perhitungan bobot dan rendemen PLA tiap ulangannya dapat dilihat pada Lampiran 3.
Tabel 2 Bobot dan rendemen rerata PLA yang dihasilkan pada berbagai perlakuan
Bobot (g) Rendemen
Sampel Asam PLA (%)
Laktat
Tanpa katalis 1 28.6289 6.6904 23.37
Tanpa katalis 2 28.6639 4.3118 15.04
Tanpa katalis 3 28.1222 5.5122 19.60
Tanpa katalis 4 27.9625 3.7195 13.30
Katalis 1 28.5339 6.2100 21.76
5
Bobot Molekul PLA Hasil Sintesis
Pengukuran bobot molekul dari PLA hasil sintesis menggunakan metode viskometri yang dapat dilihat pada Lampiran 5. Pelarut yang digunakan adalah etil asetat
.
Pelarut ini digunakan pada pengukuran bobot molekul PLA karena pelarut ini bersifat nonpolar, tidak beracun, dan tidak higroskopis. Fungsi penangas air pada pengukuran bobot molekul ialah untuk menjaga suhu agar tetap konstan pada suhu kamar (25 °C).Penambahan waktu polimerisasi dan suhu sangat berpengaruh besar terhadap bobot molekul yang dihasilkan. Semakin lama waktu polimerisasi akan menurunkan bobot molekul, sedangkan semakin tinggi suhu akan meningkatkan bobot molekul, namun jika suhunya juga terlalu tinggi maka PLA yang dihasilkan akan hangus dan terdegradasi sehingga bobot molekul yang dihasilkan rendah (Tabel 3).
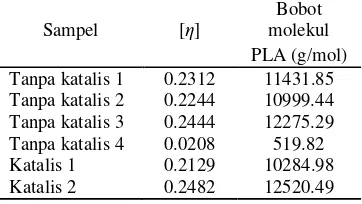
Tabel 3 Hasil rerata pengukuran viskositas intrinsik dan bobot molekul pada PLA
PLA dengan suhu reaksi 160 °C dan waktu pemanasan 32 jam (Tanpa katalis 4) memiliki bobot molekul yang lebih kecil dibandingkan dengan PLA pada suhu 150 °C dan 160 °C waktu pemanasan 24 jam (Tanpa katalis 1 dan Tanpa katalis 3) karena pada sampel PLA (Tanpa katalis 4) telah terdegradasi oleh panas dan terdeposisi sehingga rantai polimernya akan lebih pendek dan cenderung kembali sebagai esternya, sedangkan PLA dengan suhu 160 °C dengan waktu pemanasan 24 jam
(Tanpa katalis 3) menghasilkan bobot
molekul yang lebih besar daripada PLA dengan suhu 150 °C waktu pemanasan 24 jam karena rantai polimer yang dihasilkan lebih
panjang dan derajat polimerisasi yang
dihasilkan lebih besar sehingga menghasilkan bobot molekul yang tinggi.
Secara keseluruhan bobot molekul yang dihasilkan pada PLA dengan suhu 160 °C waktu pemanasan 32 jam sangat rendah
dibandingkan dengan PLA dengan suhu 150 °C dan 160 °C dengan waktu pemanasan 24 jam. Hal ini dikarenakan lamanya waktu pemanasan dan suhu yang terlalu tinggi membuat PLA yang dihasilkan hangus terjadi degradasi oleh panas dan kemungkinan terjadinya reaksi balik molekul air sehingga bobot molekul rendah. Bobot molekul PLA yang dihasilkan tidak berbeda nyata jika dibandingkan dengan bobot molekul PLA
menggunakan katalis SnOct2. Hal ini
dikarenakan pembuatan PLA menggunakan katalis pada kondisi waktu dan suhu polimerisasi yang sama dengan pembuatan PLA tanpa katalis memiliki laju polimerisasi lebih cepat dibandingkan dengan PLA tanpa katalis sehingga sebelum waktu dan suhu yang diinginkan polimerisasi akan lebih dahulu tercapai dan pada saat waktu dan suhu yang diinginkan maka laju polimerisasinya akan menurun dan menyebabkan PLA terdegradasi lebih dahulu sebelum waktunya serta bobot molekul yang dihasilkan akan lebih kecil. Hal ini sangat diharapkan bila PLA digunakan sebagai bahan penyalut obat karena PLA tanpa katalis tidak berbahaya bagi tubuh. Hasil pengukuran viskositas intrinsik dan bobot molekul PLA tiap ulangannya dapat dilihat pada Lampiran 4.
Spektrum FTIR PLA Hasil Sintesis
Uji FTIR ini dilakukan pada sampel Katalis 2 ulangan 1 (A) dan sampel Tanpa katalis 3 ulangan 2 (B). Adanya serapan yang lebar pada bilangan gelombang 3200-4000
cm-1 dengan intensitas yang rendah
menunjukkan bahwa PLA yang dihasilkan memiliki bobot molekul yang besar. Hal tersebut dikarenakan gugus OH dari monomer asam laktat telah hilang atau tereduksi karena digunakan dalam pembentukan ikatan tulang punggung polimer sehingga jumlah gugus OH pada PLA hasil sintesis tanpa atau dengan katalis berkurang dan menghasilkan bobot molekul yang besar (Kaitian et al. 1996) (Lampiran 6). Perbedaan dari kedua spektrum FTIR PLA sampel A dan sampel B (Gambar 4) dapat terlihat dari intensitas serapan yang dihasilkan dan pada bilangan gelombang 3200-4000 cm-1. Intensitas serapan pada bilangan gelombang 3200-4000 cm-1 sampel B lebih rendah dibandingkan dengan sampel A karena sampel B memiliki bobot molekul yang lebih kecil. Hal ini dikarenakan jumlah rantai karbon yang dimiliki sampel A lebih banyak dibandingkan sampel B.
Sampel [η]
Bobot molekul
PLA (g/mol)
Tanpa katalis 1 0.2312 11431.85
Tanpa katalis 2 0.2244 10999.44
Tanpa katalis 3 0.2444 12275.29
Tanpa katalis 4 0.0208 519.82
Katalis 1 0.2129 10284.98
6
A B
SIMPULAN DAN SARAN
Simpulan
Poliasamlaktat yang memiliki bobot
molekul tertinggi diperoleh pada suhu 160 ºC dengan waktu pemanasan selama 24 jam.
Peningkatan suhu pemanasan dan
penambahan waktu polimerisasi akan
mempengaruhi bobot molekul yang
dihasilkan. Penambahan katalis pada kondisi suhu dan waktu polimerisasi yang sama dengan PLA tanpa menggunakan katalis memliki bobot molekul yang tidak berbeda nyata.
Saran
Perlu dilakukan penelitian lanjutan
mengenai pembuatan PLA dengan kondisi tekanan tinggi dan pengadukan yang terus menerus guna menghasilkan bobot molekul PLA yang lebih tinggi dan perlu dilakukan
pencirian PLA dengan analisis
termogravimetri (TGA) untuk melihat
ketahanan PLA terhadap panas. Selain itu perlu dilakukan penelitian lanjutan mengenai pembuatan PLA dari sampah makanan.
DAFTAR PUSTAKA
Allcock H, Lampe FW. 1981. Contemporary Polymer Chemistry. New Jersey: Prentice Hall. Hlm 245-247.
Alger MSM. 1989. Polymer Science
Dictionary. London: Elsevier Applied Science.
Arches. 2006. What is PLA? http://www .arches.uga.edu/%7Edbagal/reerences.html [20 Agu 2009].
Badami AS. 2004. Bioresorbable electrospun tissue scaffolds of poly(ethylene glycol -lactide) copolymers for bone tissue engineering. [thesis]. Virginia. Virginia Polytechnic Institute and State University.
Clark J. 2000. Interprating an infrared
spectrum. //www.chemguide.co.uk.html
[26 Mar 2006].
Dutkiewicz S, Daniela GL, TomaszewskiW.
2003. Synthesis of poly (L(+)) lacticacid by polycondensation method in solution. Fibres & Textiles in Eastern Europe 11:66-70.
Gambar 4 Spektrum FTIR sampel katalis 2 ulangan 1 (A) dan sampel tanpa katalis 3 ulangan 2 (B). 1086.8
1763.7 2998.8
3308.3
2946.6
-CH
C-C
6
A B
SIMPULAN DAN SARAN
Simpulan
Poliasamlaktat yang memiliki bobot
molekul tertinggi diperoleh pada suhu 160 ºC dengan waktu pemanasan selama 24 jam.
Peningkatan suhu pemanasan dan
penambahan waktu polimerisasi akan
mempengaruhi bobot molekul yang
dihasilkan. Penambahan katalis pada kondisi suhu dan waktu polimerisasi yang sama dengan PLA tanpa menggunakan katalis memliki bobot molekul yang tidak berbeda nyata.
Saran
Perlu dilakukan penelitian lanjutan
mengenai pembuatan PLA dengan kondisi tekanan tinggi dan pengadukan yang terus menerus guna menghasilkan bobot molekul PLA yang lebih tinggi dan perlu dilakukan
pencirian PLA dengan analisis
termogravimetri (TGA) untuk melihat
ketahanan PLA terhadap panas. Selain itu perlu dilakukan penelitian lanjutan mengenai pembuatan PLA dari sampah makanan.
DAFTAR PUSTAKA
Allcock H, Lampe FW. 1981. Contemporary Polymer Chemistry. New Jersey: Prentice Hall. Hlm 245-247.
Alger MSM. 1989. Polymer Science
Dictionary. London: Elsevier Applied Science.
Arches. 2006. What is PLA? http://www .arches.uga.edu/%7Edbagal/reerences.html [20 Agu 2009].
Badami AS. 2004. Bioresorbable electrospun tissue scaffolds of poly(ethylene glycol -lactide) copolymers for bone tissue engineering. [thesis]. Virginia. Virginia Polytechnic Institute and State University.
Clark J. 2000. Interprating an infrared
spectrum. //www.chemguide.co.uk.html
[26 Mar 2006].
Dutkiewicz S, Daniela GL, TomaszewskiW.
2003. Synthesis of poly (L(+)) lacticacid by polycondensation method in solution. Fibres & Textiles in Eastern Europe 11:66-70.
Gambar 4 Spektrum FTIR sampel katalis 2 ulangan 1 (A) dan sampel tanpa katalis 3 ulangan 2 (B). 1086.8
1763.7 2998.8
3308.3
2946.6
-CH
C-C
OPTIMALISASI PEMBUATAN POLI(ASAMLAKTAT)
TANPA KATALIS
NANA RUSMANA
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
6
A B
SIMPULAN DAN SARAN
Simpulan
Poliasamlaktat yang memiliki bobot
molekul tertinggi diperoleh pada suhu 160 ºC dengan waktu pemanasan selama 24 jam.
Peningkatan suhu pemanasan dan
penambahan waktu polimerisasi akan
mempengaruhi bobot molekul yang
dihasilkan. Penambahan katalis pada kondisi suhu dan waktu polimerisasi yang sama dengan PLA tanpa menggunakan katalis memliki bobot molekul yang tidak berbeda nyata.
Saran
Perlu dilakukan penelitian lanjutan
mengenai pembuatan PLA dengan kondisi tekanan tinggi dan pengadukan yang terus menerus guna menghasilkan bobot molekul PLA yang lebih tinggi dan perlu dilakukan
pencirian PLA dengan analisis
termogravimetri (TGA) untuk melihat
ketahanan PLA terhadap panas. Selain itu perlu dilakukan penelitian lanjutan mengenai pembuatan PLA dari sampah makanan.
DAFTAR PUSTAKA
Allcock H, Lampe FW. 1981. Contemporary Polymer Chemistry. New Jersey: Prentice Hall. Hlm 245-247.
Alger MSM. 1989. Polymer Science
Dictionary. London: Elsevier Applied Science.
Arches. 2006. What is PLA? http://www .arches.uga.edu/%7Edbagal/reerences.html [20 Agu 2009].
Badami AS. 2004. Bioresorbable electrospun tissue scaffolds of poly(ethylene glycol -lactide) copolymers for bone tissue engineering. [thesis]. Virginia. Virginia Polytechnic Institute and State University.
Clark J. 2000. Interprating an infrared
spectrum. //www.chemguide.co.uk.html
[26 Mar 2006].
Dutkiewicz S, Daniela GL, TomaszewskiW.
2003. Synthesis of poly (L(+)) lacticacid by polycondensation method in solution. Fibres & Textiles in Eastern Europe 11:66-70.
Gambar 4 Spektrum FTIR sampel katalis 2 ulangan 1 (A) dan sampel tanpa katalis 3 ulangan 2 (B). 1086.8
1763.7 2998.8
3308.3
2946.6
-CH
C-C
7
Gonzales MF, Ruseckaite RA, Cuadrado TR. 1999. Structural changes of polylactic-acid (PLA) microspheres under hydrolytic degradation. Journal of Applied Polymer Science 71:1223-1230.
Gruber P, O’Brien M. 2006. Polylactides.
http: //www.cargildow.com/Polylactide.
html. [20 Agu 2009].
Kaitian X, Kozluca A, Denkbas EB, Piskin E. 1996. Poly(D,L-lacticacid) homopolimers:
Synthesis and characterisation. Turkey
Journal of Chemistry 20:43-53.
Kovalchuk A et al. 2005. Controlled release
of goserelin from microporous
polyglicolide and polylactide.
Macromomolecul Bioscience 5:289-298. Lee MW, Tan HT, Chandrasekaran M, Oii
CP. 2005. Synthesis and characterisation of PLLA by melt polycondensation using binary catalyst system. SIMTech Technical Reports 6:40-44.
Leksono Bowo. 2008. Ecoplas tas ramah lingkungan.http://digilib.ampl.or.id/file/pd f/percik23.pdf. [30 Des 2008].
Lu Y, Chen SC. 2004. Micro and nano-fabrication of biodegradable polymers for drug delivery. Advanced Drug Delivery Review 56:1621–1633.
Pranamuda H. 2001. Pengembangan bahan plastik biodegradabel berbahan baku pati tropis. http://std. ryu. titech. Ac. Jp /% 7 Eindonesia/ zoa.html. [20 Jan 2009].
Robani MN. 2004. Biodegradasi struktur dan morfologi mikrosfer polilaktat [skripsi]. Bogor: FMIPA, Institut Pertanian Bogor.
Siedler et al. 2001. Porous poly(D,L-lactide) and poly(D,L-lactide-co-glycolide) produ ced by thermal salt elimination from
halogenocarboxylates. Journal of
Chemistry Society 10:3140-3148.
Steven MP. 2001. Kimia Polimer. Sopyan I, penerjemah:Jakarta: Erlangga. Terjemahan dari Polymer Chemistry: An Introduction.
Vink ETH et al. 2003. Applications of life cycle assessment to Nature WorksTM polylactide (PLA) production. Jornal of Polymer Degradation and Stability
OPTIMALISASI PEMBUATAN POLI(ASAMLAKTAT)
TANPA KATALIS
NANA RUSMANA
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
ABSTRAK
NANA RUSMANA. Optimalisasi Pembuatan Poli(asamlaktat) tanpa Katalis. Dibimbing oleh TETTY KEMALA dan AHMAD SJAHRIZA.
Poli(asamlaktat) (PLA) merupakan poliester alifatik yang dapat digunakan untuk bahan baku pembuatan plastik biodegradabel dan bahan penyalut obat. PLA dibuat dengan polikondensasi langsung asam laktat tanpa katalis pada waktu 24 dan 32 jam dengan suhu 150 dan 160 °C . PLA yang dihasilkan dicirikan dengan spektrometer inframerah transformasi fourier (FTIR) dan bobot molekul diukur dengan viskometer. Hasil penelitian menunjukkan bahwa penambahan waktu dan suhu mempengaruhi bobot molekul PLA yang dihasilkan. Bobot molekul tertinggi didapatkan dengan memanaskan asam laktat pada suhu 160 °C selama 24 jam, yaitu 12375.99 g/mol. Sementara bobot molekul terendah diperoleh pada suhu 160 °C selama 32 jam, yaitu 519.82 g/mol. Pola spektrum FTIR menunjukkan adanya vibrasi ulur C-H pada 2998.81 cm-1 dan 2946.60 cm1, gugus karbonil (C=O) pada 1763.73 cm-1, vibrasi tekuk C-C pada 1458.28 cm-1, dan vibrasi tekuk C-O pada 1184.80 cm-1.
ABSTRACT
NANA RUSMANA. Optimalitation of Poly(lacticacid) Synthesis without Catalyst. Supervised by TETTY KEMALA and AHMAD SJAHRIZA.
OPTIMALISASI PEMBUATAN POLI(ASAMLAKTAT)
TANPA KATALIS
NANA RUSMANA
Skripsi
sebagai salah satu syarat untuk memperoleh gelar
Sarjana Sains pada
Departemen Kimia
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
Judul : Optimalisasi Pembuatan Poli(asamlaktat) tanpa Katalis
Nama : Nana Rusmana
NIM : G44051255
Menyetujui
Pembimbing I,
Pembimbing II,
Tetty Kemala, S.Si., M.Si.
Drs. Ahmad Sjahriza
NIP 19710407 199903 2 001
NIP 19620406 198903 1 002
Mengetahui:
Ketua Departemen Kimia
Fakultas Matematika dan Ilmu Pengetahuan Alam
Institut Pertanian Bogor,
Prof. Dr. Ir. Tun Tedja Irawadi, MS
NIP 19501227 197603 2 002
PRAKATA
Segala puji bagi Allah SWT berkat limpahan rahmat dan karunia-Nya penulis dapat menyelesaikan karya ilmiah ini. Penelitian ini dilaksanakan dari bulan April sampai Agustus 2009 yang bertempat di Laboratorium Kimia Anorganik, Departemen Kimia Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor.
Terima kasih penulis ucapkan kepada Ibu Tetty Kemala, S.Si., M.Si. dan Bapak Drs. Ahmad Sjahriza selaku pembimbing atas segala saran, kritik, dorongan, dan bimbingannya selama penelitian. Di samping itu, penghargaan penulis sampaikan kepada Bapak Yani dari departemen Fisika, Bapak Kawi dari bengkel bubut Bekasi, dan Bapak Caca dari Laboratorium Kimia Anorganik departemen Kimia yang telah membantu dalam pembuatan reaktor.
Ungkapan terima kasih tak terhingga kepada Ayah, Ibu, adik-adikku, dan
seluruh keluarga atas nasihat, semangat, bantuan materi, dan doa-doanya. Ucapan
terima kasih kepada Janti, Ivan, Zehan, Sulvi, Hafidz, Mega SL, dan Dedeh yang
telah memberikan semangat, motivasi, dan dorongan dalam menyusun karya
ilmiah ini.
Semoga tulisan ini bermanfaat dan dapat menambah wawasan ilmu
pengetahuan bagi penulis khususnya dan pembaca umumnya.
Bogor, Desember 2009
6
RIWAYAT HIDUP
Penulis dilahirkan di Jakarta pada tanggal 3 Juni 1987 dari pasangan Usman dan Ida Rusmila Dewi. Penulis merupakan anak pertama dari tiga bersaudara.
Tahun 2005 penulis lulus dari SMU Negeri 6 Bekasi dan pada tahun yang sama lulus seleksi masuk IPB melalui jalur Undangan Seleksi Masuk IPB (USMI). Penulis memilih Program Studi Kimia, Departemen Kimia, Fakultas Matematika dan Ilmu Pengetahuan Alam.
DAFTAR ISI
Halaman
DAFTAR GAMBAR ... vi
DAFTAR TABEL ... vi
DAFTAR LAMPIRAN ... vi
PENDAHULUAN ... 1
TINJAUAN PUSTAKA Asam Laktat ... 1
Polikondensasi ... 2
Poliasamlaktat (PLA)... 2
BAHAN DAN METODE Alat dan Bahan ... 3
Tahapan Penelitian ... 3
HASIL DAN PEMBAHASAN PLA Hasil Sintesis ... 3
Bobot Molekul PLA Hasil Sintesis ... 5
Spektrum FTIR PLA Hasil Sintesis ... 5
SIMPULAN DAN SARAN Simpulan ... 6
Saran ... 6
DAFTAR PUSTAKA ... 6
viii
DAFTAR TABEL
Halaman
1 Susunan modifikasi pembuatan PLA ... 3 2 Bobot dan rendemen rerata PLA yang dihasilkan pada berbagai perlakuan ... 4 3 Hasil rerata pengukuran viskositas intrinsik dan bobot molekul PLA ... 5
DAFTAR GAMBAR
Halaman
1 Rumus molekul D (-) dan L (+) asam laktat ... 1 2 Struktur kimia PLA ... 2 3 PLA hasil sintesis ... 4 4 Spektrum FTIR sampel katalis 2 ulangan 1 dan sampel tanpa katalis 3
ulangan 2 ... 5
DAFTAR LAMPIRAN
Halaman
1 Diagram alir pembuatan PLA dengan metode polikondensasi tanpa katalis……. 9 2 Diagram alir pembuatan PLA dengan metode polikondensasi dengan
PENDAHULUAN
Penggunaan polimer biodegradabel
sintetik dalam dua dekade ini berkembang dengan pesat terutama di bidang farmasi dan
kemasan (Leksono 2008). Berdasarkan
laporan BPS (1999), produksi polimer
biodegradabel di dunia diproyeksikan
mencapai hampir 1,200,000 ton/tahun. Di
beberapa negara maju, bahan polimer
biodegradabel sudah ada yang diproduksi
secara komersial, seperti poli(hidroksi
alkanoat) (PHA), poli(ε-kaprolakton) (PCL), dan poli(butilena suksinat) (PBS), namun sebagian besar bahan baku untuk pembuatan
polimer biodegradabel tersebut masih
menggunakan sumberdaya alam yang tidak terbarukan (non-renewable resources) dan tidak hemat energi. Oleh karena itu, poliasamlaktat (PLA) menjadi kandidat yang menjanjikan karena dapat diproduksi dari bahan alam seperti pati-patian (Pranamuda 2001).
Aplikasi PLA dalam industri farmasi digunakan sebagai bahan penyalut obat,
benang jahit pembedahan, dan media
transplantasi jaringan atau peralatan ortopedik (Lu & Chen 2004). PLA pada umumnya dibuat dengan menggunakan katalis. Katalis yang biasa digunakan dalam pembuatan PLA adalah timah(II) oktoat (SnOct2). SnOct2
merupakan katalis homogen dan bersifat toksik. Katalis ini sulit dipisahkan bila sudah berikatan dengan polimer (Badami 2004). Hal ini, tentunya sangat berbahaya jika PLA dimanfaatkan sebagai bahan penyalut obat.
Selain dari itu, harga PLA yang ada di pasaran saat ini relatif mahal karena dalam
pembuatannya menggunakan alat-alat
canggih, teknologi tinggi, dan bobot
molekulnya tinggi. Pembuatan PLA dengan katalis menghasilkan bobot molekul yang tidak jauh berbeda dengan PLA tanpa menggunakan katalis pada kondisi suhu dan waktu yang sama (Fukuzaki et al. 1989, diacu dalam Gonzales et al. 2003). Oleh karena itu, perlu dilakukan optimalisasi pembuatan PLA tanpa menggunakan katalis.
Menurut Gonzales et al. (1999),
pembuatan PLA dengan cara kondensasi merupakan metode yang lebih sederhana, tetapi menghasilkan PLA berbobot molekul rendah. Penyederhanaan dan pengoptimalan dalam pembuatan PLA tanpa katalis perlu diteliti lebih lanjut guna mengurangi biaya produksi dan aman jika diaplikasikan dalam industri farmasi. Pengoptimalan kondisi yang
dilakukan pada penelitian ini adalah waktu polimerisasi dan suhu.
Polikondensasi asam laktat dapat
dilakukan dalam larutan pada tekanan atmosfer dan tekanan tereduksi (Dutkiewicz et al. 2003) atau polikondensasi secara langsung tanpa katalis (Fukuzaki et al. 1989, diacu dalam Gonzales et al. 1999). Penelitian ini bertujuan melihat pengaruh suhu dan waktu polimerisasi terhadap pembuatan PLA tanpa katalis kemudian membandingkan hasil PLA tanpa katalis tersebut dengan PLA yang menggunakan katalis SnOct2 dan diharapkan
pembuatan PLA tanpa katalis memiliki bobot molekul yang tidak jauh berbeda dengan bobot molekul PLA yang menggunakan katalis.
TINJAUAN PUSTAKA
Asam Laktat
Asam laktat (asam 2-hidroksipropanoat) merupakan asam organik tiga karbon (BM 90.08 g/mol) yang memiliki gugus karboksil dan hidroksil. Asam yang dikenal dengan nama asam susu ini tersedia dalam bentuk L-(S)-(+) dan D-(R)-(-)-asam laktat (Gambar 1) (Vink et al. 2003). Dua bentuk enantiomer ini disebabkan oleh asam laktat memiliki satu atom karbon asimetris. Asam laktat yang biasa digunakan untuk pembuatan PLA adalah L-asam laktat dan campuran rasemiknya (asam dan D-(asam laktat dengan komposisi L-asam lebih besar daripada D-L-asam laktat) (Dutkiewics et al. 2003).
C COOH H HO CH3 C COOH
H3C
HO
H L (S) (+) Asam laktat D (R) (-) Asam laktat
Gambar 1 Rumus molekul D (-) dan L (+) asam laktat.
Asam laktat merupakan zat yang tidak berbau dan tidak berwarna. Asam laktat memiliki titik didih 122 °C dan titik leleh 18 °C. Asam yang dapat menyebabkan rasa lelah pada tubuh ini memiliki densitas sebesar 1.21 g/cm3 (Vink et al. 2003).
Asam laktat bersifat asam dengan
kekuatan pH 2.8 (10 g/L H2O pada suhu
2
disebabkan adanya gugus hidroksi pada posisi α.
Polikondensasi
Polimerisasi kondensasi melibatkan
pelepasan molekul kecil seperti air.
Pembentukan polimer secara kondensasi dapat dilakukan pada monomer yang memiliki gugus fungsi hidroksil dan karboksilat seperti asam laktat dan asam glikolat. Pembentukan polimer dengan cara ini diawali dengan bereaksinya dua monomer membentuk dimer dan air. Setelah itu, dimer yang terbentuk bereaksi dengan monomer membentuk trimer. Trimer yang telah terbentuk dapat bereaksi dengan dimer membentuk pentamer atau dapat pula bereaksi dengan monomer dan dimer. Reaksi ini terus berlangsung sampai terbentuk polimer. Reaksi yang terjadi pada polimerisasi yang melibatkan pelepasan air adalah:
monomer + monomer → dimer + H2O
monomer + dimer → trimer + H2O
monomer + trimer → tetramer + H2O
dimer + dimer → tetramer + H2O
dimer + trimer → pentamer + H2O
oligomer + oligomer → polimer + H2O
Reaksi polikondensasi bersifat dapat balik
sehingga air yang dilepaskan harus
dipindahkan untuk menghasilkan polimer berbobot molekul tinggi (Allcock & Lampe
1981). Polikondensasi dapat dilakukan
dengan baik pada cairan maupun padatan, yang dikenal dengan melt polycondentation. Polimer yang dapat dibuat dengan metode
melt polycondentation adalah PLA yang dibuat dari Na-kloropropionat dan PGA yang dibuat dari Na-kloroasetat. Molekul kecil yang dilepaskan pada pembentukan PLA dan PGA berupa garam NaCl (Lee et al. 2005). Sementara polimer yang dibuat dengan polikondensasi biasa di antaranya adalah PLA yang dibuat dari asam laktat dan PGA yang dibuat dari asam glikolat, poliester, dan polikaprolakton.
Poliasamlaktat (PLA)
Poliasamlaktat (Gambar 2) merupakan poliester alifatik serbaguna yang tersusun atas monomer asam laktat (Gruber & O’Brien 2002). PLA telah dikenal sejak tahun 1932. PLA pertama kali disintesis oleh Wallace Carothers, peneliti Dupont, dengan cara memanaskan asam laktat pada kondisi vakum. PLA memiliki beberapa gugus hidroksil pada
ujung rantainya. Adanya gugus ini
menyebabkan PLA dapat terdegradasi. PLA merupakan polimer yang dapat terdegradasi secara alami oleh panas, cahaya, bakteri, maupun oleh proses hidrolisis. Selain itu, polimer ini juga bersifat biokompatibel, yaitu cocok dalam tubuh tanpa menimbulkan efek yang berbahaya dan bersifat termoplastik.
Gambar 2 Struktur kimia PLA.
Pembuatan PLA dapat dilakukan dengan beberapa cara, yaitu polikondensasi asam laktat dan reaksi pembukaan cincin laktida. Pembuatan PLA tidak hanya dengan cara polimerisasi asam laktat, namun PLA dapat pula dihasilkan dari pemanasan alkali-kloropropionat (natrium atau kalium
kloropropionat) (Siedler et al. 2001).
Kovalchuk et al. (2005) membuat PLA
dengan cara memanaskan
natrium-2-kloropropionat pada suhu 170 °C. PLA yang
terbentuk dari pemanasan
Na-2-kloropropionat ini berupa PLA yang memiliki bobot molekul 4170 g/mol, titik transisi gelas 45 °C, dan derajat polimerisasi sebesar 58, namun metode ini sulit mengontrol gugus ujung, bobot molekul, dan distribusi bobot
molekulnya (Badami 2004). Kelebihan
metode ini adalah mudah dikerjakan dan biaya relatif rendah.
3
BAHAN DAN METODE
Alat dan Bahan
Alat-alat yang digunakan adalah FTIR Shimadzu 8400 dan viskometer Ostwald. Bahan-bahan yang digunakan adalah asam laktat 95%, dan katalis SnOct2.
Tahapan Penelitian
Penelitian ini terdiri atas dua tahap, yaitu pembuatan PLA dengan polikondensasi asam laktat dan pencirian PLA. Pencirian yang dilakukan meliputi penentuan bobot molekul dengan metode viskometri dan pencirian gugus fungsi dengan FTIR. Diagram alir pembuatan PLA dapat dilihat pada Lampiran 1 dan 2.
Pembuatan PLA (Gonzales et al. 1999)
Pembuatan PLA dilakukan dengan
beberapa ragam, yaitu suhu (150 dan 160 ºC), waktu (24 dan 32 jam), serta adanya pembuatan PLA menggunakan katalis SnOct2
dengan tujuan untuk membandingkan bobot molekul PLA hasil sintesis tanpa katalis dengan bobot molekul PLA menggunakan katalis. Susunan modifikasi pembuatan PLA disajikan pada Tabel 1.
Gelas piala 100 mL dibersihkan,
dikeringkan, dan ditimbang bobotnya. Setelah itu, asam laktat sebanyak 25 mL dimasukkan ke dalam gelas piala dan ditimbang. Selanjutnya, asam laktat tersebut dipanaskan secara perlahan-lahan sampai suhu 120 ºC selama 1 jam. Setelah itu, pemanasan dilanjutkan sampai suhu dan waktu yang diinginkan. Kemudian PLA yang dihasilkan didinginkan pada suhu ruang dan ditimbang.
Tabel 1 Susunan modifikasi pembuatan PLA
Komposisi Suhu (°C) Waktu (jam)
Tanpa katalis 1 150 24
Tanpa katalis 2 150 32
Tanpa katalis 3 160 24
Tanpa katalis 4 160 32
Katalis 1 150 24
Katalis 2 160 24
Pencirian PLA
Pengukuran bobot molekul (Kaitian et al. 1996). Pengukuran viskositas digunakan untuk menghitung bobot molekul rata-rata. PLA dengan konsentrasi 0.1, 0.2, 0.3, 0.4, dan 0.5% dilarutkan dalam etil asetat dan diukur viskositasnya dengan viskometer Ostwald pada suhu 25 °C (suhu konstan). Setelah itu, viskositas relatif (ηr) ditentukan dengan cara
membandingkan waktu alir pelarut dengan waktu alir larutan polimer (t0/t). Viskositas
intrinsik [η] dicari dengan cara memplotkan
ηspesifik/[PLA] sebagai sumbu y dan konsentrasi
sebagai sumbu x.
Bobot molekul (Mv) dan bobot molekul
rata-rata ditentukan berdasarkan persamaan
Mark-Houwink:
[η] = k(Mv)a
k dan a merupakan tetapan yang bergantung pada pelarut, polimer, dan suhu. Pelarut dan suhu yang akan digunakan pada penelitian ini adalah etil asetat dan 25 °C. Nilai k dan a
secara berturut-turut adalah 1.58×10-4 dan 0.78.
Analisis Gugus Fungsi dengan FTIR.
Sampel ditempatkan dalam cell holder,
kemudian dicari spektrum yang sesuai.
Hasilnya didapat berupa difraktogram
hubungan antara bilangan gelombang dan transmitans (%).
HASIL DAN PEMBAHASAN
PLA Hasil Sintesis
Poliasamlaktat yang dihasilkan pada
penelitian ini menggunakan metode
polikondesasi asam laktat secara langsung dengan suhu tinggi. Metode ini merupakan metode yang lebih sederhana dibandingkan dengan metode pembuatan PLA lainnya (Gonzales et al. 1999). Pada pembuatan PLA terjadi reaksi bertahap dimulai dengan pelepasan molekul air dari molekul asam
laktat kemudian terjadi polikondensasi
menjadi laktida dan selanjutnya dengan
pemanasan terjadi dimerisasi untuk
membentuk PLA.
Keberadaan molekul air dapat
mengganggu proses polimerisasi dan
4
CH3 -H2O
Reaksi yang terjadi dalam pembentukan PLA adalah:
PLA yang dihasilkan dari pemanasan asam laktat pada suhu 160 °C memiliki warna cokelat yang lebih pekat dibandingkan dengan hasil pemanasan pada suhu 150 °C karena
semakin tinggi suhu pemanasan akan
menghasilkan residu karbon yang banyak dan terjadi oksidasi yang berlebih sehingga menghasilkan warna PLA yang lebih pekat (Gambar 3).
PLA yang dihasilkan dari sintesis ini berupa campuran rasemiknya (D,L-PLA) karena menurut Dutkiewicz et al. (2003) PLA yang disintesis pada suhu lebih dari 140 оC akan dihasilkan bentuk rasemiknya. PLA dalam bentuk D,L-PLA memiliki waktu degradasi yang lebih cepat dibandingkan L-PLA (Lu & Chen 2004).
Tanpa katalis 1 Tanpa katalis 2 Katalis 1
Tanpa katalis 3 Tanpa katalis 4 Katalis 2
Gambar 3 PLA hasil sintesis.
PLA yang dihasilkan dari pemanasan selama 32 jam pada suhu 160 ºC berwarna cokelat tua yang mendekati warna hitam. Hal ini menunjukkan bahwa pemanasan lebih dari 32 jam akan menyebabkan warna PLA semakin hitam dan hangus terdegradasi oleh panas dan terjadi oksidasi yang berlebihan.
PLA mudah terdegradasi oleh panas karena memiliki beberapa gugus hidroksil pada rantai ujungnya (Arches 2006).
PLA yang dihasilkan larut dalam pelarut
aseton, diklorometana, etil asetat, dan
kloroform tetapi tidak larut dalam air, sedangkan asam laktat yang digunakan larut air dan etil asetat. Asam laktat larut dalam air karena memiliki rantai karbon yang pendek, namun apabila asam laktat telah menjadi polimer menjadi tidak larut dalam air karena sifatnya akan menjadi nonpolar (Alger 1989). Bobot dan rendemen PLA yang dihasilkan dipengaruhi oleh waktu dan suhu pemanasan (Tabel 2). Semakin tinggi suhu yang digunakan akan menurunkan bobot dan rendemen PLA yang dihasilkan begitu juga
dengan semakin bertambahnya waktu
pemanasan. Hal ini dikarenakan monomer asam laktat yang digunakan terus menguap pada saat pemanasan sehingga jika monomer tersebut telah menjadi polimer maka bobot dan rendemen yang dihasilkan akan semakin kecil. Adanya penambahan katalis pada pembuatan PLA dengan kondisi waktu dan suhu yang sama seperti pembuatan PLA tanpa katalis dihasilkan bobot dan rendemen yang lebih kecil. Hal ini disebabkan karena sebelum waktu dan suhu yang diinginkan, PLA dengan penambahan katalis akan terlebih dahulu terbentuk polimer dan saat mencapai suhu dan
waktu yang diinginkan maka laju
polimerisasinya akan menurun sehingga bobot dan rendemen yang dihasilkan lebih kecil
karena katalis berfungsi mempercepat
terjadinya proses polimerisasi. Hasil
perhitungan bobot dan rendemen PLA tiap ulangannya dapat dilihat pada Lampiran 3.
Tabel 2 Bobot dan rendemen rerata PLA yang dihasilkan pada berbagai perlakuan
Bobot (g) Rendemen
Sampel Asam PLA (%)
Laktat
Tanpa katalis 1 28.6289 6.6904 23.37
Tanpa katalis 2 28.6639 4.3118 15.04
Tanpa katalis 3 28.1222 5.5122 19.60
Tanpa katalis 4 27.9625 3.7195 13.30
Katalis 1 28.5339 6.2100 21.76
5
Bobot Molekul PLA Hasil Sintesis
Pengukuran bobot molekul dari PLA hasil sintesis menggunakan metode viskometri yang dapat dilihat pada Lampiran 5. Pelarut yang digunakan adalah etil asetat
.
Pelarut ini digunakan pada pengukuran bobot molekul PLA karena pelarut ini bersifat nonpolar, tidak beracun, dan tidak higroskopis. Fungsi penangas air pada pengukuran bobot molekul ialah untuk menjaga suhu agar tetap konstan pada suhu kamar (25 °C).Penambahan waktu polimerisasi dan suhu sangat berpengaruh besar terhadap bobot molekul yang dihasilkan. Semakin lama waktu polimerisasi akan menurunkan bobot molekul, sedangkan semakin tinggi suhu akan meningkatkan bobot molekul, namun jika suhunya juga terlalu tinggi maka PLA yang dihasilkan akan hangus dan terdegradasi sehingga bobot molekul yang dihasilkan rendah (Tabel 3).
Tabel 3 Hasil rerata pengukuran viskositas intrinsik dan bobot molekul pada PLA
PLA dengan suhu reaksi 160 °C dan waktu pemanasan 32 jam (Tanpa katalis 4) memiliki bobot molekul yang lebih kecil dibandingkan dengan PLA pada suhu 150 °C dan 160 °C waktu pemanasan 24 jam (Tanpa katalis 1 dan Tanpa katalis 3) karena pada sampel PLA (Tanpa katalis 4) telah terdegradasi oleh panas dan terdeposisi sehingga rantai polimernya akan lebih pendek dan cenderung kembali sebagai esternya, sedangkan PLA dengan suhu 160 °C dengan waktu pemanasan 24 jam
(Tanpa katalis 3) menghasilkan bobot
molekul yang lebih besar daripada PLA dengan suhu 150 °C waktu pemanasan 24 jam karena rantai polimer yang dihasilkan lebih
panjang dan derajat polimerisasi yang
dihasilkan lebih besar sehingga menghasilkan bobot molekul yang tinggi.
Secara keseluruhan bobot molekul yang dihasilkan pada PLA dengan suhu 160 °C waktu pemanasan 32 jam sangat rendah
dibandingkan dengan PLA dengan suhu 150 °C dan 160 °C dengan waktu pemanasan 24 jam. Hal ini dikarenakan lamanya waktu pemanasan dan suhu yang terlalu tinggi membuat PLA yang dihasilkan hangus terjadi degradasi oleh panas dan kemungkinan terjadinya reaksi balik molekul air sehingga bobot molekul rendah. Bobot molekul PLA yang dihasilkan tidak berbeda nyata jika dibandingkan dengan bobot molekul PLA
menggunakan katalis SnOct2. Hal ini
dikarenakan pembuatan PLA menggunakan katalis pada kondisi waktu dan suhu polimerisasi yang sama dengan pembuatan PLA tanpa katalis memiliki laju polimerisasi lebih cepat dibandingkan dengan PLA tanpa katalis sehingga sebelum waktu dan suhu yang diinginkan polimerisasi akan lebih dahulu tercapai dan pada saat waktu dan suhu yang diinginkan maka laju polimerisasinya akan menurun dan menyebabkan PLA terdegradasi lebih dahulu sebelum waktunya serta bobot molekul yang dihasilkan akan lebih kecil. Hal ini sangat diharapkan bila PLA digunakan sebagai bahan penyalut obat karena PLA tanpa katalis tidak berbahaya bagi tubuh. Hasil pengukuran viskositas intrinsik dan bobot molekul PLA tiap ulangannya dapat dilihat pada Lampiran 4.
Spektrum FTIR PLA Hasil Sintesis
Uji FTIR ini dilakukan pada sampel Katalis 2 ulangan 1 (A) dan sampel Tanpa katalis 3 ulangan 2 (B). Adanya serapan yang lebar pada bilangan gelombang 3200-4000
cm-1 dengan intensitas yang rendah
menunjukkan bahwa PLA yang dihasilkan memiliki bobot molekul yang besar. Hal tersebut dikarenakan gugus OH dari monomer asam laktat telah hilang atau tereduksi karena digunakan dalam pembentukan ikatan tulang punggung polimer sehingga jumlah gugus OH pada PLA hasil sintesis tanpa atau dengan katalis berkurang dan menghasilkan bobot molekul yang besar (Kaitian et al. 1996) (Lampiran 6). Perbedaan dari kedua spektrum FTIR PLA sampel A dan sampel B (Gambar 4) dapat terlihat dari intensitas serapan yang dihasilkan dan pada bilangan gelombang 3200-4000 cm-1. Intensitas serapan pada bilangan gelombang 3200-4000 cm-1 sampel B lebih rendah dibandingkan dengan sampel A karena sampel B memiliki bobot molekul yang lebih kecil. Hal ini dikarenakan jumlah rantai karbon yang dimiliki sampel A lebih banyak dibandingkan sampel B.
Sampel [η]
Bobot molekul
PLA (g/mol)
Tanpa katalis 1 0.2312 11431.85
Tanpa katalis 2 0.2244 10999.44
Tanpa katalis 3 0.2444 12275.29
Tanpa katalis 4 0.0208 519.82
Katalis 1 0.2129 10284.98
6
A B
SIMPULAN DAN SARAN
Simpulan
Poliasamlaktat yang memiliki bobot
molekul tertinggi diperoleh pada suhu 160 ºC dengan waktu pemanasan selama 24 jam.
Peningkatan suhu pemanasan dan
penambahan waktu polimerisasi akan
mempengaruhi bobot molekul yang
dihasilkan. Penambahan katalis pada kondisi suhu dan waktu polimerisasi yang sama dengan PLA tanpa menggunakan katalis memliki bobot molekul yang tidak berbeda nyata.
Saran
Perlu dilakukan penelitian lanjutan
mengenai pembuatan PLA dengan kondisi tekanan tinggi dan pengadukan yang terus menerus guna menghasilkan bobot molekul PLA yang lebih tinggi dan perlu dilakukan
pencirian PLA dengan analisis
termogravimetri (TGA) untuk melihat
ketahanan PLA terhadap panas. Selain itu perlu dilakukan penelitian lanjutan mengenai pembuatan PLA dari sampah makanan.
DAFTAR PUSTAKA
Allcock H, Lampe FW. 1981. Contemporary Polymer Chemistry. New Jersey: Prentice Hall. Hlm 245-247.
Alger MSM. 1989. Polymer Science
Dictionary. London: Elsevier Applied Science.
Arches. 2006. What is PLA? http://www .arches.uga.edu/%7Edbagal/reerences.html [20 Agu 2009].
Badami AS. 2004. Bioresorbable electrospun tissue scaffolds of poly(ethylene glycol -lactide) copolymers for bone tissue engineering. [thesis]. Virginia. Virginia Polytechnic Institute and State University.
Clark J. 2000. Interprating an infrared
spectrum. //www.chemguide.co.uk.html
[26 Mar 2006].
Dutkiewicz S, Daniela GL, TomaszewskiW.
2003. Synthesis of poly (L(+)) lacticacid by polycondensation method in solution. Fibres & Textiles in Eastern Europe 11:66-70.
Gambar 4 Spektrum FTIR sampel katalis 2 ulangan 1 (A) dan sampel tanpa katalis 3 ulangan 2 (B). 1086.8
1763.7 2998.8
3308.3
2946.6
-CH
C-C
7
Gonzales MF, Ruseckaite RA, Cuadrado TR. 1999. Structural changes of polylactic-acid (PLA) microspheres under hydrolytic degradation. Journal of Applied Polymer Science 71:1223-1230.
Gruber P, O’Brien M. 2006. Polylactides.
http: //www.cargildow.com/Polylactide.
html. [20 Agu 2009].
Kaitian X, Kozluca A, Denkbas EB, Piskin E. 1996. Poly(D,L-lacticacid) homopolimers:
Synthesis and characterisation. Turkey
Journal of Chemistry 20:43-53.
Kovalchuk A et al. 2005. Controlled release
of goserelin from microporous
polyglicolide and polylactide.
Macromomolecul Bioscience 5:289-298. Lee MW, Tan HT, Chandrasekaran M, Oii
CP. 2005. Synthesis and characterisation of PLLA by melt polycondensation using binary catalyst system. SIMTech Technical Reports 6:40-44.
Leksono Bowo. 2008. Ecoplas tas ramah lingkungan.http://digilib.ampl.or.id/file/pd f/percik23.pdf. [30 Des 2008].
Lu Y, Chen SC. 2004. Micro and nano-fabrication of biodegradable polymers for drug delivery. Advanced Drug Delivery Review 56:1621–1633.
Pranamuda H. 2001. Pengembangan bahan plastik biodegradabel berbahan baku pati tropis. http://std. ryu. titech. Ac. Jp /% 7 Eindonesia/ zoa.html. [20 Jan 2009].
Robani MN. 2004. Biodegradasi struktur dan morfologi mikrosfer polilaktat [skripsi]. Bogor: FMIPA, Institut Pertanian Bogor.
Siedler et al. 2001. Porous poly(D,L-lactide) and poly(D,L-lactide-co-glycolide) produ ced by thermal salt elimination from
halogenocarboxylates. Journal of
Chemistry Society 10:3140-3148.
Steven MP. 2001. Kimia Polimer. Sopyan I, penerjemah:Jakarta: Erlangga. Terjemahan dari Polymer Chemistry: An Introduction.
Vink ETH et al. 2003. Applications of life cycle assessment to Nature WorksTM polylactide (PLA) production. Jornal of Polymer Degradation and Stability
8
9
Lampiran 1 Diagram alir pembuatan PLA dengan metode polikondensasi tanpa katalis
Lampiran 2 Diagram alir pembuatan PLA dengan metode polikondensasi dengan katalis Dipanaskan T = 120 °C
t = 1 jam
Dipanaskan T = 150 °C dan 160 °C
t = 24 jam dan 32 jam
Asam Laktat (25 mL)
PLA
Pencirian PLA
Penentuan bobot molekul dengan
viskometer Ostwald FTIR
Asam Laktat (25 mL)
Dipanaskan T = 120 °C
t = 1 jam
t = 1 jam
Ditambahkan katalis SnOct2 (2-3 tetes)
PLA
Pencirian PLA
Penentuan bobot molekul
dengan viskometer Ostwald FTIR
Dipanaskan T = 150 °C dan 160 °C
10
Lampiran 3 Bobot dan rendemen PLA yang dihasilkan pada berbagai perlakuan
Keterangan: U 1 = Ulangan 1 U 2 = Ulangan 2
Lampiran 4 Hasil pengukuran viskositas intrinsik dan bobot molekul pada PLA
Keterangan: U 1 = Ulangan 1 U 2 = Ulangan 2
Sampel Bobot Asam laktat (g) Bobot PLA (g) Rendemen (%)
Tanpa katalis 1 U1 28.6526 6.6958 23.37
Tanpa katalis 1 U2 28.6051 6.6850 23.37
Tanpa katalis 2 U1 28.6677 4.3246 15.08
Tanpa katalis 2 U2 28.6600 4.2990 15.00
Tanpa katalis 3 U1 28.1224 5.5125 19.60
Tanpa katalis 3 U2 28.1220 5.5119 19.60
Tanpa katalis 4 U1 27.9624 3.7478 13.40
Tanpa katalis 4 U2 27.9625 3.6911 13.20
Katalis 1 U1 28.5808 6.2200 21.76
Katalis 1 U2 28.4870 6.2000 21.76
Katalis 2 U1 28.7402 4.2870 14.92
Katalis 2 U2 28.7205 4.2506 14.80
Sampel [η] Bobot molekul PLA (g/mol)
Tanpa katalis 1 U1 0.2308 11406.49
Tanpa katalis 1 U2 0.2316 11457.21
Tanpa katalis 2 U1 0.2243 10996.29
Tanpa katalis 2 U2 0.2244 11002.58
Tanpa katalis 3 U1 0.2436 12223.78
Tanpa katalis 3 U2 0.2452 12326.80
Tanpa katalis 4 U1 0.0206 515.00
Tanpa katalis 4 U2 0.0209 524.64
Katalis 1 U1 0.2131 10297.36
Katalis 1 U2 0.2127 10272.59
Katalis 2 U1 0.2482 12520.49
11
Lampiran 5 Data hasil pengukuran viskositas intrinsik pada berbagai sampel
Hasil pengukuran viskositas pada PLA yang dihasilkan pada pemanasan 150 °C selama 24 jam tanpa penambahan katalis (Tanpa katalis 1 ulangan 1)
[PLA] (g/dL) t (detik)
η
relatifη
spesifikη
reduktif (dL/g)0.0000 36.52 − − −
0.1008 37.50 1.0268 0.0268 0.2659
0.2017 38.74 1.0608 0.0608 0.3014
0.3022 40.25 1.1021 0.1021 0.3379
0.4004 41.97 1.1492 0.1492 0.3726
0.5018 43.97 1.2039 0.2039 0.4063
Contoh perhitungan:
η
relatif = t sampel t pelarut=
1.0268η
spesifik=
η
relatif–
1=
1.0268 –1=
0.0268η
reduktif
=
0.2659 dL/gPenentuan bobot molekul
Persamaan garis: y = 0.2308 + 0.3517x
Viskositas intrinsik ([η]) = 0.2308 [η] = 1.58 x 10-4 (Mv)0.78 0.2308 = 1.58 x 10-4 (Mv)0.78 (Mv) 0.78 = 1460.76
Mv = 11406.49 g/mol
[image:32.612.124.480.134.238.2]y = 0.2308 + 0.3517x R2 = 0.9997
12
Lanjutan Lampiran 5
Hasil pengukuran viskositas pada PLA yang dihasil



![Grafik hubungan [PLA] terhadap viskositas reduktif](https://thumb-ap.123doks.com/thumbv2/123dok/657767.353595/32.612.124.480.134.238/grafik-hubungan-pla-terhadap-viskositas-reduktif.webp)
![Grafik hubungan [PLA] terhadap viskositas reduktif](https://thumb-ap.123doks.com/thumbv2/123dok/657767.353595/33.612.128.480.134.239/grafik-hubungan-pla-terhadap-viskositas-reduktif.webp)
![Grafik hubungan [PLA] terhadap viskositas reduktif](https://thumb-ap.123doks.com/thumbv2/123dok/657767.353595/34.612.128.482.135.239/grafik-hubungan-pla-terhadap-viskositas-reduktif.webp)