SINTESIS DAN PENCIRIAN KOLOID NANOFERROGEL
Fe3O4-KITOSAN SEBAGAI BAHAN PENGONTRAS MRI
AGRIN FEBRIAN PRADANA
SEKOLAH PASCASARJANA INSTITUT PERTANIAN BOGOR
PERNYATAAN MENGENAI TESIS DAN
SUMBER INFORMASI SERTA PELIMPAHAN HAK CIPTA
Dengan ini saya menyatakan bahwa tesis berjudul Sintesis dan Pencirian Koloid Nanoferrogel Fe3O4-kitosan sebagai Bahan Pengontras MRI adalah benar karya saya dengan arahan dari komisi pembimbing dan belum diajukan dalam bentuk apa pun kepada perguruan tinggi mana pun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir tesis ini.
Dengan ini saya melimpahkan hak cipta dari karya tulis saya kepada Institut Pertanian Bogor.
Bogor, September 2016
Agrin Febrian Pradana
RINGKASAN
AGRIN FEBRIAN PRADANA. Sintesis dan Pencirian Koloid Nanoferrogel Fe3O4-kitosan sebagai Bahan Pengontras MRI. Dibimbing oleh PURWANTININGSIH SUGITA dan EDY GIRI RACHMAN PUTRA.
Ferrogel Fe3O4-kitosan telah berhasil disintesis melalui proses assembly ion-ion Fe3+ dan Fe2+ ke dalam hidrogel kitosan yang tertautsilang dengan glutaraldehida (GLA), serta dipresipitasi menggunakan NaOH. Ferrogel tersebut dikeringkan dengan memragamkan waktu pengeringan 2 (S2), 3 (S3), 4 (S4), dan 5 jam (S5) pada suhu 60 0C. Tujuan penelitian ini adalah menyintesis koloid nanoferrogel Fe3O4-kitosan yang stabil serta injectable sebagai agen pengontras pada MRI. Pencirian ferrogel dengan difraktometer sinar-X menunjukkan telah terbentuk fase Fe3O4. Analisis spektrum FTIR-nya diperoleh bahwa ragam pengeringan tidak menunjukkan adanya perubahan struktur kimia ferrogel yang signifikan dan hilangnya serapan gugus N−H primer kitosan di 1548 cm-1 pada sampel S2, S3, S4, dan S5 menandakan adanya interaksi berupa kelat antara Fe3O4 dengan gugus −NH2 kitosan.
Pengeringan ferrogel hanya menghilangkan kandungan air tipe imbisi pada ferrogel dan berpengaruh pada sifat magnet yang dihasilkan. Magnet saturasi maksimum sebesar 6.21 emu/gram diperoleh pada sampel S5. Meredispersikan ferrogel menggunakan ultrasonik ke dalam medium asam asetat dan air deionisasi secara bertahap diperoleh koloid nanoferrogel Fe3O4-kitosan yang stabil. Pengamatan dengan TEM menunjukkan morfologi Fe3O4 berbentuk bola dengan ukuran ~ 5 nm telah terlapisi oleh kitosan dengan ukuran ~ 20 nm. Ukuran ini juga telah dikonfirmasi menggunakan PSA. Hasil pengukuran dengan VSM menunjukkan koloid nanoferrogel tersebut bersifat superparamagnetik yang baik. Semua hasil pencirian produk koloid nanoferrogel Fe3O4-kitosan menunjukkan koloid tersebut berpotensi digunakan sebagai agen pengontras pada MRI.
SUMMARY
AGRIN FEBRIAN PRADANA. Synthesis and Characterization of Colloidal Nanoferrogel Fe3O4-chitosan as Contrast Agent MRI. Supervised by PURWANTINIGSIH SUGITA and EDY GIRI RACHMAN PUTRA.
Fe3O4-chitosan ferrogels had been successfully synthesized through the assembly process of iron ions into the chitosan hydrogel. Chitosan hydrogel, synthesized using glutaraldehyde crosslinker, was soaked in saline solution of Fe2+ and Fe3+ to induce iron ions and precipitated by using NaOH to form ferrogel. Ferrogels were then dried by heating at temperature of 60 oC with varying drying time of 2 (S2), 3 (S3), 4 (S4) and 5 (S5) hours. The aim of this study to synthesis a st
able colloida
l of nanoferrogel Fe3O4-chitosan injectable as contrast agent on MRI. Characterization of the product by X-ray diffractometer has shown the formation of Fe3O4 phase. Analysis of functional groups from FTIR spectra showed that variation of drying time hasn’t changes any chemical structure of ferrogel and peak at 1548 cm-1disappeared shown that there was interaction between Fe3O4 and −NH2 groups of chitosan by chelation mechanism.The heating process will only result in decreasing the imbition water type content within ferrogel. This water decreasing give more significant effect to ferrogel magnetic properties by increasing ferrogel magnetic saturation value. Maximum magnetic saturation of 6.21 emu/g was obtained for the sample dried for 5 hours. Redispersing ferrogel by step-wise ultrasonic process within acetic acids and DI water give final result of stable colloidal nanoferrogel. Observation using transmission electron microscope (TEM) revealed the formation of single spherical magnetic nanoparticle of ~ 5 nm homogeneously coated by chitosan and establishing ~ 20 nm nanoferrogel particles disperse within aquabase medium. This nanoferrogel size was also confirm by Particle Size Analyzer (PSA) measurement. VSM measurement on this colloid system showed a good superparamagnetic system. All the result support the prospect of nanoferrogel colloid to be applied as an MRI contrast agent.
© Hak Cipta Milik IPB, Tahun 2016
Hak Cipta Dilindungi Undang-Undang
Dilarang mengutip sebagian atau seluruh karya tulis ini tanpa mencantumkan atau menyebutkan sumbernya. Pengutipan hanya untuk kepentingan pendidikan, penelitian, penulisan karya ilmiah, penyusunan laporan, penulisan kritik, atau tinjauan suatu masalah; dan pengutipan tersebut tidak merugikan kepentingan IPB
Tesis
sebagai salah satu syarat untuk memperoleh gelar Magister Sains
pada
Program Studi Kimia
SINTESIS DAN PENCIRIAN KOLOID NANOFERROGEL
Fe3O4-KITOSAN SEBAGAI BAHAN PENGONTRAS MRI
SEKOLAH PASCASARJANA INSTITUT PERTANIAN BOGOR
BOGOR 2016
PRAKATA
Puji dan syukur penulis panjatkan kepada Allah subhanahu wa ta’ala atas segala karunia-Nya sehingga karya ilmiah ini berhasil diselesaikan. Tema yang dipilih dalam penelitian yang dilaksanakan sejak bulan Desember 2015 ini ialah bahan magnet sebagai aplikasi biomedis, dengan judul Sintesis dan Pencirian Nanoferrogel Fe3O4-kitosan sebagai Bahan Pengontras MRI.
Terima kasih penulis ucapkan kepada Prof Dr Dra Purwantiningsih Sugita, MS sebagai ketua komisi pembimbing dan Edy Giri Rachman Putra, PhD sebagai anggota komisi pembimbing atas bimbingan, arahan, dan sarannya kepada penulis. Penulis mengucapkan terima kasih kepada Ibu Prof Dr Dra Purwantiningsih Sugita yang telah membiayai studi penulis serta kepada PSTBM Batan Serpong yang telah membiayai seluruh biaya penelitian penulis. Penulis juga ucapkan terima kasih kepada Ibu Mujamilah, MSc, Ibu Grace Tj. Sulungbudi, Msc, Ibu Wildan Z Lubis, Amd, Ibu Ari Handayani, BSc, Kak Ade Mulyawan, SSi, Lutfi, Teguh, Novita, Isty, serta semua staff PSTBM gedung 42 yang telah membantu dan memberi dukungan baik secara langsung dan tidak langsung kepada penulis selama mengerjakan penelitian. Penghargaan juga penulis sampaikan kepada Alm. Abah J. Jun Zaenal Arifin Abdullah yang telah memberi motivasi, semangat, do’a, dan kasih sayangnya sehingga penulis menyelesaikan karya ilmiah ini. Ungkapan terima kasih juga penulis sampaikan kepada Ayah, Ibu, dan Adik-adik atas segala doa dan kasih sayangnya. Semoga karya ilmiah ini bermanfaat.
Bogor, September 2016
DAFTAR ISI
DAFTAR GAMBAR vi
DAFTAR LAMPIRAN vi
1 PENDAHULUAN 1
Latar Belakang 1
Perumusan Masalah 2
Tujuan Penelitian 2
Ruang Lingkup Penelitian 2
2 METODE 2
Bahan 3
Alat 3
Prosedur 3
3 HASIL DAN PEMBAHASAN 4
Ferrogel Fe3O4-kitosan 4
Analisis Fase Fe3O4 pada Ferrogel Fe3O4-kitosan 6
Analisis FTIR Ferrogel Fe3O4-kitosan 6
Koloid Nanoferrogel Fe3O4-kitosan 9
Sifat Magnet Koloid Nanoferrogel Fe3O4-kitosan 9 Distribusi Ukuran Koloid Nanoferrogel Fe3O4-kitosan 10 Morfologi Koloid Nanoferrogel Fe3O4-kitosan 11
4 SIMPULAN 12
Simpulan 12
Saran 12
DAFTAR PUSTAKA 13
LAMPIRAN 15
DAFTAR GAMBAR
1 Proses sintesis oksida besi Fe3O4 dilapisi hidrogel kitosan dengan
metode iron ions assembly 4
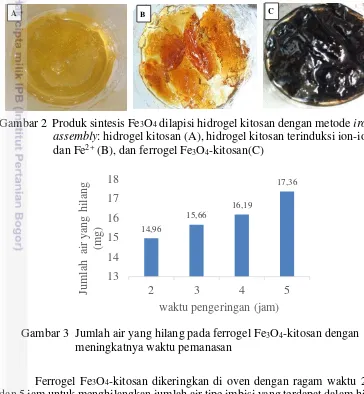
2 Produk sintesis Fe3O4 dilapisi hidrogel kitosan dengan metode iron
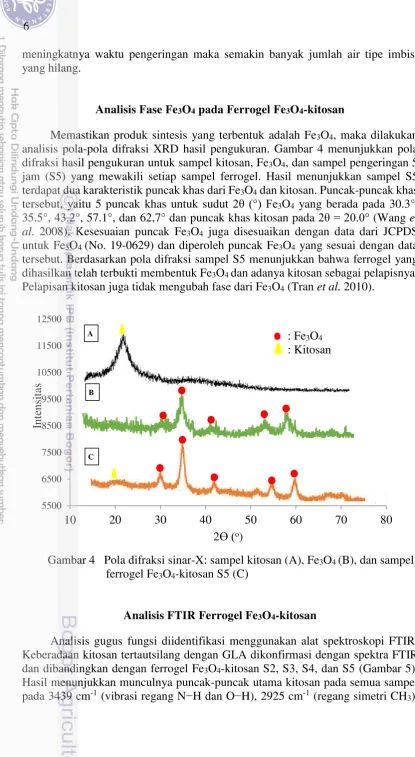
ions assembly: hidrogel kitosan (A), hidrogel kitosan terinduksi ion-ion Fe3+ dan Fe2+ (B), dan ferrogel Fe3O4-kitosan(C) 5 3 Jumlah air yang hilang pada Ferrogel Fe3O4-kitosan dengan
meningkatnya waktu pemanasan 5
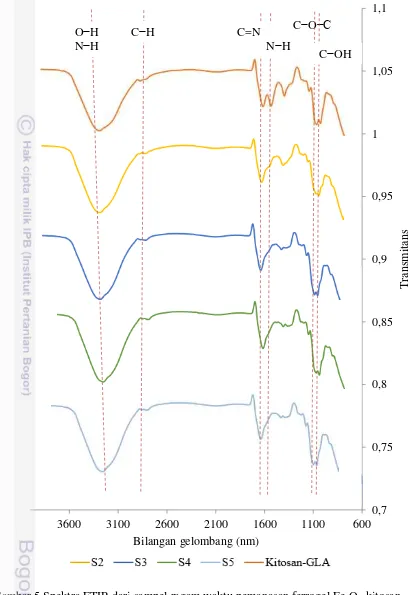
4 Pola difraksi sinar-X: sampel kitosan (A), Fe3O4 (B), dan sampel
ferrogel Fe3O4-kitosan S5 (C) 6
5 Spektra FTIR dari sampel ragam waktu pemanasan ferrogel Fe3O4 -kitosan dibandingkan dengan hidrogel -kitosan GLA
6 Pembentukan basa Schiff (imina) dari hasil reaksi kitosan dan
pentautsilang GLA 8
7 Skema proses kelat antara Fe3O4dan gugus −NH2 pada kitosan 8 8 Koloid nanoferrogel Fe3O4-kitosan stabil berdasarkan: tidak terjadinya
aglomerasi (A), dan pengujian pH (B) selama 3 bulan pengamatan 9 9 Kurva histeresis nilai Ms nanoferrogel Fe3O4-kitosan 10 10 Distribusi ukuran sampel koloid hidrogel kitosan (A), dan sampel
koloid nanoferrogel Fe3O4-kitosan S5 (B) 11
11 Foto TEM sampel koloid nanoferrogel Fe3O4-kitosan S5 tanpa pewarnaan (A= skala 50 nm, B= skala 20 nm), dan dengan pewarnaan
(C= skala 50 nm, D= skala 20 nm) 11
DAFTAR LAMPIRAN
1
Diagram alir penelitian 161 PENDAHULUAN
Latar Belakang
Teknik diagnosa penyakit organ dalam tubuh manusia yang powerful dan sensitif pada bidang biomedis saat ini adalah magnetic resonance imaging (MRI) (Laurent et al. 2008). Prinsip kerja teknik MRI ini berdasarkan waktu relaksasi magnet dari proton air dalam organ manusia (Figuerola et al. 2010). Teknik ini digunakan karena tidak menggunakan radiasi yang besar dan menghindari efek samping yang berbahaya (Stephen et al. 2011). Meskipun banyak keuntungan yang diperoleh dari MRI, masih diperlukan tingkat sensitifitas yang lebih tinggi serta diagnosa yang lebih akurat (Yoo et al. 2011). Salah satu cara untuk meningkatkan hal tersebut adalah penggunaan agen pengontras. Agen pengontras memiliki peran membedakan image antara jaringan sehat dan jaringan sakit dengan meningkatkan kualitas kontras yang dihasilkannya (Cho et al. 2010). Secara umum terdapat dua tipe agen pengontras MRI yaitu, tipe T1 dan tipe T2. Tipe T1 seperti kompleks gadolinium atau ion mangan yang kerjanya mengurangi waktu relaksasi proton secara longitudinal dan menimbulkan kontras positif (sinyal terang). Material superparamagnetik (berbasis oksida besi Fe3O4) adalah contoh agen pengontras tipe T2 (Yanga et al. 2011). Kerja agen pengontras tersebut mempersingkat waktu relaksasi proton secara transversal dan menimbulkan kontrast negatif (sinyal gelap) (Santra et al. 2012). Disebabkan oleh toksisitasnya penggunaan gadolinium sebagai pengontras (Estelrich et al. 2015), penggunaan agen pengontras superparamagentik Fe3O4 menjadi menarik perhatian peneliti karena menunjukkan berbagai keuntungan, yaitu ukuran dan bentuk dapat diatur, memungkinkan untuk dimodifikasi permukaannya, dan efektif pada konsentrasi rendah serta tidak toksik (Sadighian et al. 2015).
Sebagai agen pengontras, Fe3O4 harus dipreparasi dalam bentuk koloid yang stabil. Namun, terdapat masalah yang dihadapi dari material Fe3O4 karena sifat tarikan magnetik antar partikel Fe3O4 yang sangat kuat sehingga cenderung untuk teraglomerasi dan menghasilkan koloid yang tidak stabil (Shukla et al. 2015). Diperlukan suatu cara untuk menghindari aglomerasi tersebut, salah satunya adalah dengan memodifikasi permukaan Fe3O4 agar interaksi tarik-menarik magnet antar partikel Fe3O4 menjadi berkurang. Banyak penelitian yang telah melakukan modifikasi permukaan Fe3O4 agar meningkatkan kestabilannya, yaitu dengan menyalut permukaan Fe3O4 dengan senyawa karboksilat, anorganik, dan polimer (Laurent et al. 2008). Dekstran merupakan senyawa polimer berbasis senyawa karboksilat yang digunakan sebagai pelapis Fe3O4sebagai agen pengontras yang secara komersial dikenal dengan FeridexTM. Namun, Feridex ini telah ditarik dari pasaran disebabkan penemuan beberapa reaksi yang kurang baik dalam penggunaannya secara klinis (Weissleder et al. 2014). Alternatif penggunaan polimer berbasis senyawa karboksilat lainnya adalah kitosan yang telah banyak diteliti sebagai pelapis material (He et al. 2010).
2
biodegradabel sehingga sangat cocok untuk diaplikasikan pada bidang biologis (Unsoy et al. 2012). Penelitian ini menggunakan polimer berupa hidrogel kitosan sebagai penyalut permukaan Fe3O4 agar menghasilkan koloid yang stabil. Penelitian ini mencoba untuk menggabungkan konsep metode kopresipitasi dan
iron ions assembly (Wang et al. 2008) dalam menyintesis material Fe3O4 termodifikasi kitosan dalam bentuk gel kitosan yang berisi Fe3O4 (ferrogel). Dengan memanfaatkan kedua metode tersebut, pembentukan ferrogel Fe3O4-kitosan dihipotesa akan menghasilkan produk yang homogen, yaitu semua Fe3O4 akan termodifikasi permukaannya dengan kitosan secara menyeluruh. Selanjutnya ferrogel akan dibuat menjadi bentuk koloid agar dapat diaplikasi pada bidang biomedis dengan sistem injectable (Tsai et al. 2010).
Perumusan Masalah
Ferrogel Fe3O4-kitosan telah disintesis menggunakan prinsip iron ions
assembly oleh Pradana (2015) dengan dua variasi waktu pengeringan dan diperoleh ferrogel yang berisi nanopartikel Fe3O4 dengan ukuran <20 nm, dan tersebar merata dalam matriks hidrogel kitosan. Namun, ferrogel terlalu keras pada waktu pengeringan 16 jam dan terlalu basah pada waktu pengeringan 1 jam. Hal ini mempengaruhi sifat magnet yang dihasilkan dari ferrogel serta sulit diredispersi ke dalam medium tertentu membentuk koloid nanoferrogel yang stabil.
Tujuan Penelitian
Tujuan penelitian ini adalah menyintesis koloid nanoferrogel Fe3O4-kitosan yang stabil serta injectable sebagaiagen pengontras pada MRI.
Ruang Lingkup Penelitian
Penelitian ini terdiri atas 4 tahap (Lampiran 1). Pertama-tama, disiapkan hidrogel kitosan sebagai pelapis nanopartikel Fe3O4, lalu Fe3O4 disintesis dengan metode iron ions assembly dan dilapisi dengan hidrogel kitosan tersebut membentuk padatan ferrogel. Selanjutnya padatan ferrogel diredispersikan menjadi koloid nanoferrogel yang homogen dan stabil. Produk tersebut dicirikan dengan berbagai pencirian.
2 METODE
3 Bahan
Bahan yang digunakan dalam penelitian ini adalah kitosan yang diproduksi oleh Departemen Teknologi Hasil Perairan, Fakultas Perikanan dan Ilmu Kelautan IPB, asam asetat glasial (Merck), garam FeCl2·4H2O dan FeCl3·6H2O (Merck), glutaraldehida (GLA) 25% (Merck), dan NaOH (Merck).
Alat
Peralatan yang digunakan pada penelitian ini adalah peralatan kaca yang umum digunakan di laboratorium, neraca analitik, mixer, kuar ultrasonik (ultrasonic probe) “Sonics”, sentrifuga, indikator universal, batang magnet permanen, oven. Pencirian sampel menggunakan difraktometer sinar-X (XRD) merek PANalytical, vibrating sample magnetometer (VSM) merek Oxford 1.2H,
particle size analyzer (PSA) tipe Zetasizer Nano ZS merek Malvern, mikroskop elektron transmisi (TEM) merek JEOL JEM 1400, dan spektrofotometer inframerah transformasi Fourier (FTIR) merek Bruker Tensor 27.
Prosedur
Preparasi Hidrogel Kitosan (modifikasi Wang 2008)
Sebanyak 3 g serbuk kitosan dilarutkan ke dalam 100 mL larutan asam asetat 2% (v/v). Kemudian dipipet 20 mL larutan kitosan tersebut ke dalam template
(gelas piala 50 mL) untuk pembuatan hidrogel kitosan. Sebanyak 1.32 mL larutan GLA 12.5% (v/v) ditambahkan ke dalam 20 mL larutan kitosan tersebut sambil diaduk kuat menggunakan pengaduk magnet pada mixer dengan kecepatan 1000 rpm sampai terbentuk hidrogel kitosan. Simpan hidrogel kitosan yang telah terbentuk di dalam kulkas selama 15-20 menit.
Pelapisan Oksida Fe3O4 dengan Hidrogel Kitosan (Pradana 2015)
4
Gambar 1 Proses sintesis oksida besi Fe3O4 dilapisi hidrogel kitosan dengan metode iron ions assembly
Sintesis Koloid Nanoferrogel Fe3O4-kitosan
Sebanyak 1 gram setiap sampel ferrogel S2, S3, S4,dan S5 diredispersikan ke dalam 10 mL buffer asetat (pH = 4.6) dan diultrasonikasi sebanyak 2x1 menit. Endapan nanoferrogel dipisahkan dari supernatan dengan batang magnet permanen. Selanjutnya endapan nanoferrogel yang tersisa tersebut ditambahkan 10 mL air deionisasi. Kemudian endapan tersebut diredispersikan kembali dengan ultrasonik sampai terbentuk koloid nanoferrogel yang homogen dan stabil.
Pencirian Sampel Ferrogel dan Koloid Nanoferrogel Fe3O4-kitosan
Ferrogel S2, S3, S4,dan S5 dicirikan dengan analisis FTIR agar mengetahui gugus-gugus fungsi pada ferrogel. Sampel dengan nilai magnet yang maksimum dijadikan perwakilan sampel dalam pencirian selanjutnya. Memastikan Fe3O4 telah terbentuk sampel ferrogel dicirikan dengan XRD. Koloid nanoferrogel dianalisis nilai magnetnya dengan VSM, analisis ukurannya dengan PSA dan dianalisis morfologinya dengan TEM.
3 HASIL DAN PEMBAHASAN
Ferrogel Fe3O4-kitosan
Pelapisan Fe3O4 ke dalam matriks hidrogel kitosan akan membentuk suatu ferrogel, yaitu gel yang memiliki sifat magnet (Mora et al. 2015). Pada penelitian ini, ferrogel Fe3O4-kitosan disintesis dengan menggunakan metode kopresipitasi yang dimodifikasi dengan prinsip iron ions assembly (metode in situ). Modifikasi metode tersebut diperlukan karena metode kopresipitasi memiliki kelemahan, yaitu polidispersitas ukuran partikel yang sangat besar sehingga Fe3O4 sangat mudah teraglomerasi (Xu et al. 2014). Iron ions assembly dapat mengatasi masalah tersebut dengan menyeragamkan ukuran melalui mekanisme difusi ion-ion prekursor Fe3O4 ke dalam suatu hidrogel (Wang et al. 2008). Selain itu, cara tersebut adalah cara terbaik dalam menyiapkan pelapisan material magnetik berbasis polimer karena mengurangi jumlah tahapan proses dan mengefisiensikan waktu (Sivudu dan Rhee 2009).
Proses pelapisan diawali dengan membuat hidrogel kitosan dengan pentaut-silang glutaraldehida (GLA) (Gambar 2A). Penggunaan pentautpentaut-silang GLA akan
5 membentuk ikatan kovalen yang lebih kuat antara gugus −NH2 pada kitosan dan gugus −CHO pada GLA membentuk basa Schiff. Ikatan tersebut membuat hidrogel kitosan menjadi lebih kaku dan kokoh sebagai cetakan pelapisan material Fe3O4. Perendaman hidrogel kitosan ke dalam larutan prekursor ion Fe3+ dan Fe2+ bertujuan mendifusi masuk ion-ion tersebut ke dalam hidrogel kitosan menghasilkan hidrogel kitosan yang telah terinduksi ion-ion Fe3+ dan Fe2+(Wang
et al. 2008). Keberhasilan proses difusi tersebut ditandai dengan perubahan secara fisiologi warna hidrogel kitosan (kuning) menjadi warna ion-ion besi (jingga kemerah-merahan) (Gambar 2B). Hidrogel kitosan yang telah terinduksi ion-ion Fe3+ dan Fe2+ tersebut dipresipitasi dengan NaOH 5M menghasilkan ferrogel yang berwarna hitam (Gambar 2C). Warna hitam menunjukkan terbentuknya Fe3O4 yang berada didalam matriks hidrogel kitosan.
Gambar 2 Produk sintesis Fe3O4 dilapisi hidrogel kitosan dengan metode iron ions
assembly: hidrogel kitosan (A), hidrogel kitosan terinduksi ion-ion Fe3+ dan Fe2+ (B), dan ferrogel Fe3O4-kitosan(C)
Ferrogel Fe3O4-kitosan dikeringkan di oven dengan ragam waktu 2, 3, 4, dan 5 jam untuk menghilangkan jumlah air tipe imbisi yang terdapat dalam hidrogel kitosan. Air tipe imbisi ini adalah air yang masuk ke dalam suatu bahan dan menyebabkan pengembangan volume, tetapi bukan merupakan komponen penyusun bahan tersebut (Sugita et al. 2009). Air ini perlu dihilangkan karena dapat menurukan sifat magnet dari ferrogel. Gambar 3 menunjukan diagram hasil jumlah air yang hilang dari ferrogel dengan meningkatnya waktu pengeringan. Semakin
6
meningkatnya waktu pengeringan maka semakin banyak jumlah air tipe imbisi yang hilang.
Analisis Fase Fe3O4 pada Ferrogel Fe3O4-kitosan
Memastikan produk sintesis yang terbentuk adalah Fe3O4, maka dilakukan analisis pola-pola difraksi XRD hasil pengukuran. Gambar 4 menunjukkan pola difraksi hasil pengukuran untuk sampel kitosan, Fe3O4, dan sampel pengeringan 5 jam (S5) yang mewakili setiap sampel ferrogel. Hasil menunjukkan sampel S5 terdapat dua karakteristik puncak khas dari Fe3O4 dan kitosan. Puncak-puncak khas tersebut, yaitu 5 puncak khas untuk sudut 2θ (°) Fe3O4 yang berada pada 30.3°, 35.5°, 43.2°, 57.1°, dan 62,7° dan puncak khas kitosan pada 2θ = 20.0° (Wang et al. 2008). Kesesuaian puncak Fe3O4 juga disesuaikan dengan data dari JCPDS untuk Fe3O4 (No. 19-0629) dan diperoleh puncak Fe3O4 yang sesuai dengan data tersebut. Berdasarkan pola difraksi sampel S5 menunjukkan bahwa ferrogel yang dihasilkan telah terbukti membentuk Fe3O4 dan adanya kitosan sebagai pelapisnya. Pelapisan kitosan juga tidak mengubah fase dari Fe3O4 (Tran et al. 2010).
Gambar 4 Pola difraksi sinar-X: sampel kitosan (A), Fe3O4 (B), dan sampel ferrogel Fe3O4-kitosan S5 (C)
Analisis FTIR Ferrogel Fe3O4-kitosan
7 dengan yang dilaporkan Raut dan Khairkar (2014).
8
Pembentukan basa Schiff atau imina hasil reaksi antara gugus gugus −NH2 pada kitosan dan gugus −CHO pada GLA (Gambar 6) terkonfirmasi pada serapan ν (C=N) di 1643 cm-1. Puncak serapan yang menjadi pembeda antara sampel kitosan-GLA dengan sampel ferrogel Fe3O4-kitosan S2, S3, S4, dan S5 adalah pada bilangan gelombang 1548 cm-1, yaitu serapan gugus N−H primer pada kitosan. Hilangnya serapan gugus N−H primer kitosan di 1548 cm-1 pada sampel S2, S3, S4, dan S5 menandakan adanya interaksi yang terjadi antara gugus −NH2 sisa yang tidak tertausilang dengan Fe3O4. Adapun interaksi yang terjadi menurut Wang et al. (2009) adalah interaksi kelat antara logam Fe3O4dengan ligan −NH2 pada kitosan (Gambar 7). Hal ini menunjukkan bahwa didalam ferrogel Fe3O4-kitosan terdapat Fe3O4 berdasarkan analisis XRD dan terlapisi oleh kitosan berdasarkan analisis FTIR melalui mekanisme kelat. Pengaruh pengeringan sampel S2, S3, S4, dan S5 tidak menunjukkan perubahan yang signifikan terhadap pergeseran puncak-puncak khas yang dihasilkan. Artinya, lamanya waktu pengeringan tidak mempengaruhi atau merubah struktur kimia pada ferrogel Fe3O4-kitosan.
Gambar 6 Pembentukan basa Schiff (imina) dari hasil reaksi kitosan dan pentautsilang GLA
GLA GLA
9 Koloid Nanoferrogel Fe3O4-kitosan
Koloid nanoferrogel disintesis dengan cara meredispersikan ke dalam asam asetat yang bertujuan untuk melarutkan kembali kitosan yang berlebih dan menipiskan lapisan kitosan yang melapisan Fe3O4. Redispersi selanjutnya menggunakan medium air deionisasi menghasilkan koloid yang stabil dengan tidak adanya agglomerat dari Fe3O4 hingga 3 bulan pengamatan pada S2, S3, S4, dan S5 setelah proses sintesis (Gambar 8A). Fe3O4 yang telah terlapisi oleh kitosan ini dan membentuk koloid disebut ferrofluid (Tsai et al. 2010) atau koloid nanoferrogel dalam penelitian ini. Tidak adanya agglomerasi yang terjadi pada koloid nanoferrogel Fe3O4-kitosan menunjukkan berkurangnya interaksi tarik-menarik antar partikel Fe3O4 karena adanya kitosan yang melapisinya (Shukla et al. 2015). Pengujian kestabilan terhadap pH juga dilakukan dengan pengamatan perubahan ragam kondisi pH (1-8) terhadap waktu pengamatan selama 3 bulan. Gambar 8B menunjukkan hasil pengukuran pH selama 3 bulan pengamatan yang menunjukkan koloid nanoferrogel Fe3O4-kitosan stabil pada pH 4.5.
Sifat Magnet Koloid Nanoferrogel Fe3O4-kitosan
Koloid nanoferrogel diuji sifat magnetnya dengan menggunakan instrumen
vibrating sample magnetomter (VSM). Gambar 9 adalah kurva histeresis dari sampel S2, S3, S4, dan S5 berupa cairan koloid. Pada kurva tersebut dapat dilihat, semakin lama waktu pengeringan ferrogel kurva histeresis menunjukkan semakin superparamagnetik dengan nilai magnet saturasi (Ms) yang tinggi pula. Seperti yang telah dibahas sebelumnya, koloid nanoferrogel terdiri dari Fe3O4, kitosan dan air tipe imbisi. Semakin lama waktu pengeringan maka akan semakin banyak berkurangnya kandungan air tipe imbisi pada sampel. Air memiliki sifat diamagnetik yang akan memberi nilai Ms yang negatif sedangkan Fe3O4 bersifat Gambar 8 Koloid nanoferrogel Fe3O4-kitosan stabil berdasarkan: tidak terjadinya
aglomerasi (A), dan pengujian pH (B) selama 3 bulan pengamatan
10
superparamagnetik yang akan memberi nilai positif pada nilai Ms (Medvedeva et al. 2013). Berkurangnya kandungan air tipe imbisi ini akan menurunkan bagian diamagnetik pada sampel sehingga akan meningkatkan nilai Ms pada sampel. Selain itu kitosan juga bersifat diamagnetik yang ikut menambah berkurangnya nilai magnet yang dihasilkan (Xu et al. 2014). Sampel S5 menunjukkan nilai Ms
yang paling tinggi, yaitu 6.21 emu/gram. Kecilnya nilai Ms yang dihasilkan menunjukkan adanya kitosan yang melapisi Fe3O4. Nilai tersebut lebih tinggi dibandingkan dengan yang dilaporkan oleh Sivudu et al. (2009) menggunakan hidrogel poliakrilamida yang lebih bersifat diamagnetik, yaitu sebesar 4 emu/gram. Selain itu juga, nilai yang lebih rendah juga pernah dilaporkan oleh Cai et al. (2007) menggunakan pelapis SiO2 sebesar 1.66 emu/gram.
Distribusi Ukuran Koloid Nanoferrogel Fe3O4-kitosan
Koloid nanoferrogel diukur ukurannya dengan menggunakan instrumen
particle size analyzer (PSA). Gambar 10 menunjukkan hasil 3 kali pengukuran PSA dari sampel koloid hidrogel kitosan (10A) dan sampel koloid nanoferrogel Fe3O4 -kitosan S5 (10B). Pada sampel koloid hidrogel -kitosan murni diperoleh distribusi ukuran sebesar 22 nm, sedangkan koloid nanoferrogel S5 menjadi lebih besar, yaitu 31.3 nm. Hasil ini menunjukkan kedua partikel koloid berada pada rentang ukuran nanometer. Ukuran yang diizinkan untuk aplikasi bidang biomedis adalah kurang dari 50 nm (Khrisnan et al. 2010). Selain itu juga, ukuran tersebut berada direntang kategori intermediet (~10-100 nm) untuk aplikasi in vivo pada organ hati, limpa, sumsum tulang belakang, dan pembuluh darah (Weissleder et al. 2014). Perubahan ukuran nanopartikel antara hidrogel kitosan murni dan koloid nanoferrogel menunjukkan kitosan telah melapisi Fe3O4 dengan mekanisme kelat seperti yang telah dijelaskan sebelumnya.
Gambar 9 Kurva histeresis nilai Ms nanoferrogel Fe3O4-kitosan
11
Morfologi Koloid Nanoferrogel Fe3O4-kitosan
Morfologi koloid nanoferrogel diamati dengan menggunakan transmission electron microscope (TEM) dan didukung dengan data PSA. Gambar 11A dan 11B merupakan foto TEM sampel koloid nanoferrogel S5 tanpa pewarnaan yang menunjukkan morfologi berbentuk bola dari Fe3O4 tunggal dengan ukuran <10 nm. Sedangkan sampel dengan pewarnaan phototungstic acid (PTA) (Gambar 11C dan 11D), morfologi berbentuk bola yang lebih besar sekitar 20 nm teramati. PTA akan mewarnai kitosan dengan mekanisme absorbsi PTA ke dalam kitosan. Melaui pewarnaan ini, dapat menunjukkan bahwa partikel tunggal Fe3O4 dengan ukuran <10 nm telah terlapisi oleh hidrogel kitosan dan membentuk nanosphere sekitar 20 nm. Warna keabu-abuan disekitar warna gelap pada sampel yang diwarnai PTA menunjukkan hidrogel kitosan yang tidak melapisi Fe3O4. Hidrogel kitosan inilah yang menjadi medium dalam sistem koloid dan membuat interaksi dipol-dipol antara Fe3O4 menjadi berkurang (Pan et al. 2009). Kehadiran kitosan ini juga membuat sistem koloid menjadi lebih stabil.
Gambar 10 Distribusi ukuran sampel koloid hidrogel kitosan (A), dan sampel koloid nanoferrogel Fe3O4-kitosan S5 (B)
A B
Gambar 11 Foto TEM sampel koloid nanoferrogel Fe3O4-kitosan S5 tanpa pewarnaan (A= skala 50 nm, B= skala 20 nm), dan dengan pewarnaan (C= skala 50 nm, D= skala 20 nm)
A B
C D
Medium kitosan Fe3O4
12
4 SIMPULAN
Simpulan
Telah berhasil membuat koloid nanoferrogel Fe3O4-kitosan yang stabil dengan tidak adanya agglomerat yang terjadi dan stabil pada pH 4.5 selama 3 bulan pengamatan. Adapun karakteristik dari koloid nanoferrogel yaitu, memiliki sifat magnet (maksimum pada S5= 6.21 emu/gram), berada pada ukuran yang diizinkan pada bidang medis (<10 nm), dan terstabilkan oleh pelapisan oleh kitosan. Berdasarkan pencirian tersebut koloid nanoferrogel ini berpotensi sebagai agen pengontras MRI.
Saran
Perlunya dilakukan pengulangan secara statistik pada sampel maksimum agar diperoleh keterulangan yang baik. Selain itu ragam pembuatan template
13
DAFTAR PUSTAKA
Cho JS, Lee JH, Shin TH, Song HT, Kim EY, Cheon J. 2010. Self-confirming AND logic nanoparticles for fault-free MRI. J Am Chem Soc. 132:11015–11017. Estelrich J, Sánchez-Martín MJ, Busquets MA. 2015. Nanoparticles in magnetic
resonance imaging: from simple to dual contrast agents. Int J Nanomedicine. 10(17)27–41.
Figuerola A, Di CR, Manna L, Pellegrino T. 2010. From iron oxide nanoparticles towards advanced iron-based inorganic materials designed for biomedical applications. Pharmacol Res. 62:126–143.
He L, Yao L, Liu F, Qin B, Song R, Huang W. 2010. Magnetic Fe3O4@chitosan nanoparticle:synthesis, characterization, and application as catalyst carrier.
Nanosci Nanotechnol. 10(63): 48-55.
Kariminia S, Shamsipur A, Shamsipur M. 2016. Analytical characteristics and application of novel chitosan coated magnetic nanoparticles as an efficient drug delivery system for ciprofloxacin. Enhanced drug release kinetics by low-frequency ultrasounds. J Pharm Biomed Anal. 129:450-457.
Kean T, Thanou M. 2009. Biodegradation, biodistribution and toxicity of chitosan.
Adv Drug Delivery Rev. 62(2010): 3-11.
Krishnan KM. 2010. Biomedical nanomagnetics: A spin through possibilities in imaging, diagnostics, and therapy. IEEE T Magn. 46(7):2523-2558.
Laurent S, Forge D Port, M, Roch A, Robic C, Vander Elst L, Muller RN. 2008. Magnetic iron oxide nanoparticles: synthesis, stabilization, vectorization, physicochemical characterizations, and biological applications. Chem Rev.
108:2064-2110.
Li G, Jiang Y, Huang K, Ding P, Chen J. 2008. Preparation and properties of magnetic Fe3O4-chitosan nanoparticles. J Alloys Compd. 466:451-456. Medvedeva I, Bakhteeva J, Zhakov S, Revvo A, Bysov I, Uimin M, Yermakov A,
and Mysik A. 2013. Sedimentation and Aggregation of Magnetite Nanoparticles in Water by a Gradient Magnetic Field. J Nanopart Res. 15:2054.
Mora VS, Soares PIP, Hernandez R, Mijangos C. 2015. Composite chitosan/agarose ferrogels for potential applications in magnetic hyperthermia.
Gels. 1:69-80.
Pan C, Hu B, Li W, Sun Y, Ye H, Zeng X. 2009. Novel and efficient method for immobilization and stabilization of beta-D-galactosidase by covalent attachment onto magnetic Fe3O4-chitosan nanoparticles. J Mol Catal B: Enzymatic. 61:208-215.
Pradana AF. 2015. Sintesis dan pencirian nanopartikel Fe3O4 terlapisi hidrogel kitosan dengan metode iron ions assembly [skripsi]. Bogor (ID): Institut Pertanian Bogor.
Raut AR, Khairkar SR. 2014. Study of chitosan crosslinked with glutaraldehide as biocomposite material. World J Pharm Res. 3(9):523-532.
14
Santra S, Jativa SD, Kaittanis C, Normand G, Grimm J, Perez JM. 2012. Gadolinium-encapsulating iron oxide nanoprobe as activatable NMR/MRI contrast agent. ACS Nano. 8:7281–7294.
Stephen ZR, Kievit FM, Zhang M. 2011. Magnetite nanoparticles for medical MR imaging. Mater Today.7(8):330–338.
Sugita P, Wukirsari T, Sjahriza A, Wahyono D. 2009. Kitosan Sumber Biomaterial Masa Depan. Bogor (ID): IPB Press.
Shukla S, Jadaun A, Arora V, Sinha RK, Biyani N, Jain VK. 2015. In vitro toxicity assessment of chitosan oligosaccharide coated iron oxide nanoparticles. Toxicol Rep. 2:27–39.
Sivudu KS, Rhee KY. 2009. Preparation and characterization of pH-responsive hydrogel magnetite nanocomposite. Colloids Surf A Physicochem Eng Asp.
349:29-34.
Tran HV, Tran LD, Nguyen TN. 2010. Preparation of chitosan/magnetite composite beads and their application for removal of Pb (II) and Ni (II) from aqueous solution. Mater Sci Eng C. 30:304-310.
Tsai ZT, Wang JF, Kuo HY, Shen CR, Wang JJ, Yen TC. 2010. In situ preparation of high realxtivity iron oxide nanoparticles by coating with chitosan: A potential MRI contrast agent useful for cell tracking. J Magn Magn Mater. 322(2):208-213.
Unsoy, G., Yalcin, S. & Khodadust, R., 2012. Synthesis optimization and characterization of chitosan- coated iron oxide nanoparticles produced for biomedical applications. J Nanopart Res 14:964.
Wang Y, Li B, Zhou Y, Jia D. 2008. Chitosan-induced synthesis of magnetite nanoparticles via iron ions assembly. Polym Adv Technol. 19:1256-1261. Wang Y, Li B, Zhou Y, Jia D. 2009. In situ mineralization of magnetite
nanoparticles in chitosan hydrogel. Nanoscale Res Lett. 4:1041-1046.
Weissleder R, Nahrendorf M, Pittet MJ. 2014. Imaging macrophages with nanoparticles. Nat Mater. 13:125-138.
Xu JK, Zhang FF, Sun JJ, Sheng J, Wang F, Sun M. 2014. Bio and nanomaterials based on Fe3O4. Molecules. 19:21506-21528. doi:10.3390/molecules191221506 Yanga H, Zhuanga Y, Sund Y, Dai A, Shi X, Wue D, Li F, Hua He, Yanga S. 2011. Targeted dual-contrast T1- and T2- weighted magnetic resonance imaging of tumors using multifunctional gadolinium-labeled superparamagnetic iron oxide nanoparticles. Biomaterials 32:4584–4593
15
16
Lampiran 1 Diagram alir penelitian
Nanoferrogel Fe3O4-Kitosan
Nanoferrogel Fe3O4-Kitosan ragam waktu Sintesis Fe3O4-Kitosan
Iron ions assembly
Ragam waktu pengeringan 2-5 jam (selang 1 jam)
Pencirian Produk Ferrogel - FTIR
- XRD
Koloid Nanoferrogel Fe3O4-Kitosan Redispersi
Pencirian Produk Koloid - VSM
- PSA -TEM
18
RIWAYAT HIDUP
Penulis dilahirkan di Jambi pada tanggal 8 Februari 1994 sebagai anak pertama dari pasangan Dwi Agus Supriyono dan Sriyatun. Tahun 2011, penulis lulus dari SMA Negeri 1 Jambi dan pada tahun yang sama lulus Seleksi Nasional Masuk Perguruan Tinggi (SNMPTN) undangan di Departemen Kimia, Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor. Penulis menyelesaikan pendidikan program sarjana pada tahun 2015 dan mengikuti program sinergi S-1−S-2 (fasttrack) di Departemen Kimia, Sekolah Pascasarjana Institut Pertanian Bogor. Selama kuliah S-2, penulis bergabung sebagai anggota Kominfo Himpunan Mahasiswa Muslim (HIMMPAS) IPB. Penulis juga pernah menjadi oral presentator pada acara The International Conference on Advance Material Science and Technology 2016 di Universitas Negeri Malang. Jurnal tentang Synthesis and Characterization Colloidal of Nanoferrogel Fe3O4-chitosan