ABSTRAK
ISOLASI, IDENTIFIKASI, DAN UJI BIOAKTIVITAS SENYAWA STIGMAST-5-EN-3β-OL (β-SITOSTEROL) DARI KULIT AKAR
BAKAU MINYAK (Rhizophora apiculata)
Oleh
Rahmat Kurniawan
Pada penelitian ini telah dilakukan isolasi, identifikasi, dan uji bioaktivitas senyawa steroid dari kulit akar Bakau Minyak (Rhizophora apiculata). Proses isolasi melalui tahapan maserasi dengan metanol, pemisahan kromatografi cair vakum (KCV) dan pemurnian dengan kromatografi kolom (KK) menggunakan eluen etilasetat/n-heksana. Senyawa murni hasil isolasi berbentuk kristal jarum, bening dengan berat 0,214 gram (0,01%) yang diidentifikasi menggunakan pereaksi Liebermann-Burchard, menghasilkan spot berwarna biru
mengindikasikan steroid. Hasil KLT dengan tiga sistem eluen berbeda yaitu etilasetat/n-hekasana 1:9, kloroform/benzena 1:9, dan diklorometan/n-heksana 1:9 menghasilkan nilai Rf berturut-turut 0,25, 0,20 dan 0,15, serta titik leleh didapat 160,2o-161oC. Penentuan struktur senyawa hasil isolasi secara spektrofotometri UV-Vis, FT-IR, 13C-NMR, 1H-NMR, DEPT, dan GC-MS menunjukkan senyawa steroid, stigmast-5-en-3β-ol (β-sitosterol). Uji bioaktivitas senyawa hasil isolasi memberikan aktivitas zona hambat dengan diameter 8 mm terhadap E. coli.
ABSTRACT
ISOLATION, IDENTIFICATION, AND BIOACTIVITY TEST OF STIGMAST-5-EN-3β-OL (β-SITOSTEROL) COMPOUND FROM ROOT
BARK OF BAKAU MINYAK (Rhizophora apiculata)
By
Rahmat Kurniawan
This study had done the isolation, identification, and bioactivity test of steroids compound from root bark of Bakau Minyak (R. apiculata). The isolation proses include extraction with maceration method by methanol, separation with vacuum liquid chromatography (VLC), and purification with column chromatography (CC) using ethylacetat/n-hexane. The pure compound of isolated shown crystal needle-shaped with 0.214 grams (0.01%) was identified by Liebermann-Burchard reagent had a blue-collored spot, indicated that a steroid compound. The result of thin-layer chromatography (TLC) with three different systems of eluens that is 1:9 ethylacetat/n-hexane, 1:9 cloroform/benzene, and 1:9 DCM/n-hexane given Rf value 0.25, 0.20, and 0.15 respectively with melting point test looking for 160.2o -161oC. The pure compound of isolated was determined by UV-Vis, FT-IR, 13 C-NMR, 1H-NMR, DEPT, and GC-MS spectrophotometry. Base on analysis of data indicate that had formed a steroid compound called Stigmast-5-en-3β-ol
(β-sitosterol). Bioactivity test of isolated compound gave 8 mm zone inhibits againts E. coli.
RIWAYAT HIDUP
Penulis dilahirkan di Martapura pada tanggal 10 Oktober
1992, sebagai anak pertama dari dua bersaudara putra dari
Bapak Yono dan Ibu Nur lela.
Jenjang Pendidikan diawali dari Sekolah Dasar (SD) di
SDN 3 Labuhan Dalam, Tanjung Seneng diselesaikan pada
tahun 2004. Sekolah Menengah Tingkat Pertama di SMPN 19 Bandar Lampung
diselesaikan pada tahun 2007 dan Sekolah Menengah Atas di SMAN 9 Bandar
Lampung diselesaikan pada tahun 2010. Tahun 2010, Penulis terdaftar sebagai
Mahasiswa Jurusan Kimia FMIPA Unila.
Pada tahun 2014 Penulis telah melaksanakan Kuliah Kerja Nyata (KKN) selama
40 hari di Desa Kagungan ratu, Kec. Tulang Bawang Udik, Kab. Tulang Bawang
Barat dan Praktik Kerja Lapangan (PKL) di Laboratorium Kimia Organik Jurusan
Kimia FMIPA Unila. Selama menjadi mahasiswa penulis pernah menjadi asisten
praktikum Sains Dasar periode 2012-2013 untuk mahasiswa S1 Jurusan Fisika.
Praktikum Kimia Organik periode 2013-2014 untuk mahasiswa S1 Jurusan Kimia
FMIPA Unila, mahasiswa S1 Jurusan Biologi FMIPA Unila, mahasiswa S1
Jurusan Pendidikan Kimia FKIP Unila, dan untuk mahasiswa Keperawatan
Dalam bidang organisasi, Penulis pernah terdaftar sebagai Kader Muda Himpunan
Mahasiswa Kimia (HIMAKI) FMIPA Unila periode 2010-2011, sebagai anggota
bidang kaderisasi Himpunan Mahasiswa Kimia (HIMAKI) FMIPA Unila periode
2011-2012 dan sebagai Ketua Bidang Kaderisasi Himpunan Mahasiswa Kimia
MOTO
Hidup tidak semudah mati
(Penulis)
Tidak ada kebahagiaan tanpa berbagi
(Alexander Supertrump)
Kita begitu berbeda dalam semua kecuali dalam cinta
(Gie)
Orang yang mendustakan nikmat Tuhan diberikan pelajaran dengan tidak adanya
nikmat Tuhan. Maka janganlah kau dustakan kesehatan, nama baik, cinta,
“Dengan menyebut nama Allah Yang Maha Pengasih lagi Maha Penyayang
(Q.S. Al-Fatihah : 1)
Kupersembahkan karya ini kepada :
ALLAH S.W.T
Rosulullah SAW beserta keluarganya
Junjunganku, suri tauladanku, yang kunanti-nantikan syafa’atnya di hari
kebangkitan kelak.
Kedua Orang tua ku,
Papa dan mama yang telah merawat, menyayangi, mendidik dengan sepenuh
hati dengan begitu banyak kasih sayang dan pendidikan yang baik hingga
penulis bisa sampai pada tahap ini. Terimakasih kepada papa yang dengan baik
dan penuh kasih dan sayang yang tak terhingga membesarkan penulis, dan
dengan memberikan ilmu agama yang dapat penulis gunakan didalam menjalani
kehidupan ini. Terimakasih juga kepada mama yang dengan kasih sayangnya
melahirkan dan membesarkan penulis dengan penuh kesabaran dan kasih sayang
yang tidak terhingga sampai penulis dapat menyelesaikan karya ini dengan baik.
Oleh karena itu, karya ini penulis persembahkan untuk kalian berdua Papa dan
Mama.
Saudaraku :
Adek adi (Riadi Kurniawan) yang sangat penulis sayangi. Terimakasih.
Pembimbing Prof. Tati Suhartati, M.S. yang sudah penulis anggap sebagai ibu.
Guru-guru yang slalu membagi ilmunya untukku
Seluruh sahabat dan teman yang selalu menyemangatiku
SANWACANA
Assalamualaikum Wr. Wb
Puji dan syukur penulis panjatkan kehadirat Allah SWT, karena berkat rahmat,
ridho, dan karunia-Nya penulis dapat menyelesaikan skripsi ini. Shalawat dan
salam tidak lupa penulis haturkan kepada Nabi Muhammad SAW sebagai suri
tauladan.
Skripsi dengan judul “Isolasi, Identifikasi, dan Uji Bioaktivitas Senyawa Stigmast-5en-3β-ol (β-Sitosterol) dari Kulit Akar Bakau Minyak (Rhizophora apiculata)” merupakan syarat untuk mencapai gelar Sarjana Sains pada Jurusan Kimia, Fakultas Matematika dan Ilmu Pengetahuan Alam, Universitas Lampung.
Pada kesempatan ini penulis mengucapkan terima kasih dan penghargaan yang
tulus kepada :
1. Ibu Prof. Tati Suhartati, M.S. selaku Pembimbing Utama yang telah
membimbing penulis dengan sabar, memberikan banyak ilmu
pengetahuan, saran, kritik, arahan, bantuan dan motivasi sehingga penulis
dapat menyelesaikan skripsi ini.
2. Bapak Andi Setiawan, Ph.D. selaku Pembahas I yang telah banyak
memberikan petunjuk, arahan, saran, kritik serta nasehat dalam
3. Bapak Dr. Eng. Surpto Dwi Yuwono, M.T. selaku Pembahas II yang telah
banyak memberikan petunjuk, arahan, saran , kritik serta nasehat dalam
menyelesaikan skripsi ini.
4. Ibu Dian Septiani P., M.Si. selaku Pembimbing Akademik yang telah
memberi motivasi dan dukungannya.
5. Bapak Dr. Eng. Surpto Dwi Yuwono, M.T. selaku Ketua Jurusan Kimia
Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Lampung.
6. Bapak Prof. Dr. Suharso, Ph.D selaku Dekan Fakultas Matematika dan
Ilmu Pengetahuan Alam Universitas Lampung.
7. Mba Nora, Pak Gani, Mas Nomo, Paman, Mba Wiwit, Mbak Iin, Mas
Udin serta seluruh staf pengajar dan karyawan Jurusan Kimia, Fakultas
Matematika dan Ilmu Pengetahuan Alam Universitas Lampung.
8. Pak Yandri, Bu Dian, Bu Aspita, Bu Kamisah, Pak Sutopo, Pak Andi, Pak
Rudi, Pak Hardoko, Pak Diki dan segenap dosen yang telah mendidik dan
memberikan ilmu pengetahuan kepada penulis.
9. Papaku Drs. Yono dan Mamaku Nur Lela Kesumawati S.Ag. atas
limpahan kasih sayang yang tak pernah habis untukku, keikhlasan
merawat dan menjagaku, doa tulus yang tiada henti, dan perhatian yang
takkan pernah habis demi keberhasilan penulis.
10.Adiku Riadi Kurniawan, adik tersayang yang telah memberikan doa dan
bantuannya untuk keberhasilan penulis.
11.Keluarga besarku, Kak Windo, Kak Ando, Kak Akbar, Kak Tomi, Yuk
Uni, Mba Weni, Bunda, Wak ipul, Bu Sri, Tante Jun, Lulu, Bowo, Bagas,
12.Nci (Desi Meriyanti), yang telah memberikan dukungan, doa, bantuan, dan
cinta untuk penulis sehingga penulis dapat menyelesaikan karya ini
dengan baik.
13. Teman seperjuanganku Purniawati yang telah memberikan semangat dan
dukungan.
14.Teman-teman penelitianku, M. Nurul Fajri, Chintya Gustianda (teman
sedari SMA) untuk membantu dan menemani dalam penelitian.
15.Mbak-mbak ku yang telah memberikan bantuan dan keceriaan didalam
laboratorium, mbak eka, mbak Resca (jaguar), mbak neneng, mbak mae,
mbak teta (pinguin) juga mbak Putri Amalia, mbak Hade Sastrawiyana,
mbak Fatma Timur, mbak Fitriyanti, dan mbak Yul anak-anak mbak
Tyas Rosawinda Kh yang telah mengiringi penulis selama melakukan
penelitian.
16.Adik-adik penerus perjuangan laboratorium Kimia Organik Juned, Mirfat,
Rio, Ridho, Lili, Yuli, dan Andri.
17.Teman-teman se-angkatan 2010, Desi Meriyanti, S.Si., Funda Elisyia,
S.Si., Adetia Fatmawati, Ariyanti, Leni Astuti, S.Si., Rani Anggraini, Tata,
Rina Rachmawati S., S.Si., Purniawati S., S.Si., Fauziyyah Mu’min
S.,S.Si., Wynda Dwi A., S.Si., Fafai, Lolita, Surtini, Rini, Chyn Gus, Putri
Heriyani U., S.Si., Chintya Yolanda, S.Si., Widya Afriliani W., S.Si.,
Sevina Silvi, S.Si., Sifa, Kristi, Dilla, Silvana, Indah, Juni, Uti, Ely, Ana,
Noe, Agung, Fajri, Adit, Hanif Amrullah, S.Si., Rully, Tio dan Maria atas
18.Kakak-kakak alumni, kak Alan “culun”, kak Hery “jaula”, kak Septian,
Kak Aprianya papau, kak gunadi senang, kak Yahya, kak slem dan
kakak-kakak tingkat serta alumni lainnya.
19.Teman-teman HIMAKI dan Anggota bidang Kaderisasi terimakasih atas
perjuangan dan dedikasi untuk membangun bangsa.
20.Markas besar Hajimena, mbaknya kak septian (mbak leli) dan mama kak
Septian terimakasih telah memberikan wadah untuk berekspresi.
21.Teman-teman KKN Restu, Pakde, Rendi, Ratih, bu Dokter, Mia, Suspa,
Repi, dan Resti.
22.Saudara-saudaraku Pecinta alam (PASMALA) angkatan 18 Andre,
Dhining, Aristo, Bintang, Deblok, solenk, Ipul, Jose, dan Bupenk untuk
ikatan kekeluargaan kita.
23.Sahabat-sahabat SMA Hendro, habibi, Tantobong, Edo, Hadi dan yang
tidak dapat disebutkan satu persatu.
24.Semua pihak yang tidak dapat penulis sebutkan satu persatu yang secara
tulus memberikan bantuan moril dan materil kepada penulis.
Bandar Lampung, 18 September 2014
Penulis
i
II. TINJAUAN PUSTAKA A. Mangrove ... 4
E. Pemisahan Senyawa Secara Kromatografi ... 10
1. Kromatografi lapis tipis (KLT) ... 10
2. Kromatografi kolom (KK) ... 12
3. Kromatografi cair vakum (KCV) ... 12
4. Analisis kemurnian ... 12
F. Identifikasi Senyawa Organik Secara Spektroskopi ... 14
1. Fourier transform infrared spectroscopy (FT-IR) ... 14
2. Spektroskopi ultraungu-tampak (UV-VIS) ... 15
3. Spektroskopi resonansi magnetik nuklir (NMR) ... 16
4. Spektroskopi GC-massa (MS)... 17
G. Uji Bioaktivitas ... 17
III. METODOLOGI PENELITIAN A. Waktu dan Tempat Penelitian ... 19
ii
DAFTAR TABEL
Tabel Halaman
1. Penggolongan kromatografi berdasarkan fasa diam dan fasa gerak ... 10
2. Karakteristik frekuensi uluran beberapa gugus fungsi ... 15
3. Letak pergeseran kimia untuk proton dalam molekul organik ... 16
4. Interpretasi spektrum FT-IR (bilangan gelombang, bentuk pita, intensitas,
dan penempatan gugus terkait) dari senyawa Y ... 38
5. Data geseran kimia dari senyawa Y ... 40
6. Data hubungan perkiraan urutan nomor karbon, 13C-NMR, 1H-NMR
dan 135˚ DEPT ... 42
7. Perbandingan data 13C-NMR, 1H-NMR dan DEPT hasil penelitian
dengan literatur... 44
8. Perbandingan besarnya zona hambat dengan konsentrasi senyawa uji
iv
DAFTAR GAMBAR
Gambar Halaman
1. Tanaman bakau minyak (Rhizophora apiculata) ... 6
2. Kerangka dasar steroid dan penomorannya ... 7
3. Struktur sterol ... 8
4. Kromatogram KLT ekstrak kasar metanol dengan eluen etilasetat/
n-heksana 1:4 ... 27
5. Kromatogram KLT fraksi-fraksi KCV tahap I, II, III menggunakan
eluen etilasetat/n-heksana 1:4 ... 28
6. Kromatogram KLT fraksi X, Y dan Z eluen etilasetat/n-heksana 1:4 ... 29
7. Kromatogram KLT hasil KK fraksi X3-X9, eluen etilasetat/n-heksana 1:4 ... 30
8. Kromatogram KLT hasil KK kristal XA4-XA9, eluen etilasetat/
n-heksana 1:4 ... 31
9. Kromatogram KLT hasil KK kristal XB3-XB9, eluen etilasetat/
n-heksana 1:4 ... 31
10. Kromatogram KLT hasil KK kristal XC3-XC8, eluen etilasetat/
n-heksana 1:4 ... 32
11. Kromatogram hasil KK kristal Y3-Y9, eluen etilasetat/n-heksana 1:4... 32
12. Kromatogram KLT hasil KK kristal YA3-YA9, eluen etilasetat/
n-heksana 1:4 ... 33
13. Kromatogram KLT hasil KK kristal YB4-YB9, eluen etilasetat/
v
14. Kromatogram KLT dengan 3 sistem eluen yang berbeda ... 34
15. Kromatogram KLT senyawa X dan Y dengan pereaksi Lieberman- Burchard, eluen etilasetat/n-heksana 1:9... 35
16. Spektrum UV-Vis senyawa Y ... 37
17. Spektrum FTIR senyawa Y ... 37
18. Spektrum 13C-NMR (125 MHz, Aseton D6) dari senyawa Y ... 39
19. Spektrum 1H-NMR dari senyawa Y ... 41
20. Spektrum 135˚ DEPT dari senyawa Y ... 42
21. Penomoran struktur senyawa Stigmast-5en-3β-ol ... 43
22. Spektrum GC-massa (MS) dari senyawaY ... 45
23. Pola fragmentasi senyawa Stigmast-5en-3β-ol ... 46
24. Spektrum massa dari senyawa Y ... 46
25. Spektrum massa dari senyawa Stigmast-5en-3β-ol ... 46
1
I. PENDAHULUAN
A. Latar Belakang
Indonesia dikenal sebagai negara maritim dikarenakan banyaknya gugusan pulau
yang membentang dari Sabang sampai Marauke. Hal ini menyebabkan negara
Indonesia memiliki garis pantai terpanjang di dunia sehingga memiliki kawasan
hutan bakau yang sangat luas. Keadaan geografis Indonesia yang beriklim tropis
dengan curah hujan yang tinggi sepanjang tahun memberikan keanekaragaman
jenis bakau yang tumbuh di Indonesia. Hutan bakau memiliki fungsi yang sangat
penting, yaitu untuk mencegah terjadinya abrasi oleh air laut dan menahan
terjangan tsunami yang menghantam pantai. Hutan bakau adalah habitat berbagai
jenis burung, serangga, ular laut, dan wilayah sekitar akar bakau merupakan
habitat bagi berbagai jenis ikan dan kepiting bakau.
Salah satu jenis bakau yang terdapat di Indonesia adalah bakau minyak
(Rhizophora apiculata). Bakau minyak (R. apiculata) merupakan salah satu
pohon yang hidup di hutan Mangrove. Tanaman ini termasuk dalam famili
Rhizophoraceae, GenusRhizophoradan spesiesR. apiculata(Duke, 2006).
Tanaman ini menyebar di seluruh daerah tropis di lingkungan pantai, namun
belum dibudidayakan secara khusus. Bakau jenisR. apiculatabanyak
2
Ekstrak metanol batangR. apiculatamemiliki aktivitas inhibitor tirosinase yang
tinggi (Abdullah, 2011). Asam piroligneus yang memiliki sifat antioksidan yang
tinggi diisolasi dari batangR. apiculata(Loo dan Jain, 2008), dan kulit kayu
menghasilkan tanin yang digunakan sebagai sumber antioksidan alami (Rahimet
al., 2008). Bagian kulit batang biasa digunakan masyarakat pesisir Lampung
sebagai bahan pewarna alami, kayu bakau dalam bidang industri sebagai bahan
baku kertas. Kulit akar dan batang tumbuhanR. apiculatayang diekstrak dengan
metanol mengandung senyawa flavonoid, alkaloid, dan tanin (Abdullah, 2011).
Pada penelitian ini sampel yang digunakan adalah kulit akarR. apiculatayang
didapat dari Balai Besar Budidaya Pengembangan Laut (BBBPL) Lempasing,
Lampung. Sangat menarik untuk diteliti bahwaR. apiculata merupakan
tumbuhan yang mampu beradaptasi dengan air laut yang mengandung garam
cukup tinggi. Interaksi langsung kulit akarR. apiculatadengan air laut
mendorong tumbuhan untuk memproduksi senyawa metabolit sekunder agar dapat
mempertahankan diri terhadap kondisi lingkungan. Berdasarkan uji pendahuluan
pada bagian kulit akar mengandung senyawa alkaloid, flavonoid, dan sebagian
besar merupakan senyawa steroid.
Metode isolasi senyawa steroid dilakukan dengan cara maserasi menggunakan
metanol. Pemisahan dengan cara kromatografi cair vakum (KCV) dan pada tahap
pemurnian dengan kromatografi kolom (KK). Identifikasi kemurnian dengan
metode kromatografi lapis tipis (KLT) tiga sistem eluen yang berbeda dan uji titik
leleh. Penentuan struktur molekul dengan analisis spektroskopi ultraungu-tampak
3
resonansi magnetik nuklir (NMR), dan spektroskopi GC-massa (MS). Uji
bioaktivitas dengan metode difusi agar menggunakanpaper diskbertujuan untuk
mengetahui kemampuan senyawa hasil isolasi terhadap pertumbuhan
mikroorganisme tertentu.
B. Tujuan Penelitian
Tujuan penelitian ini adalah :
1. Mengisolasi senyawa Stigmast-5en-3β-ol (β-Sitosterol) dari kulit akar bakau
minyak (R. apiculata) dari Balai Besar Budidaya Pengembangan Laut
(BBBPL) Lempasing, Lampung.
2. Menentukan struktur molekul senyawaβ-Sitosterol hasil isolasi.
3. Mengetahui bioaktivitas senyawaβ-Sitosterol hasil isolasi.
C. Manfaat Penelitian
Penelitian ini diharapkan dapat memberikan informasi mengenai penemuan
senyawa steroid dari kulit akar bakau minyak (R. apiculata), dalam rangka
penggalian dan pengembangan potensi sumber daya alam Provinsi Lampung
4
II. TINJAUAN PUSTAKA
A. Mangrove
Hutan mengrove merupakan ekosistem unik dan berfungsi ganda dalam
lingkungan hidup, yaitu fungsi ekologis, ekonomi, seperti pariwisata, penelitian
dan pendidikan. Hutan mangrove terdapat hampir di perairan Indonesia yang
berpantai landai dan merupakan ekosistem yang mudah rusak jika terjadi
perubahan pada salah satu unsur pembentukannya, sehingga dikenal sebagai
fragile ecosystem(Arief, 2003). Flora mangrove memiliki karakteristik morfologi
khas akibat kondisi lingkungan yang ekstrim. Hal tersebut menyebabkan
tumbuhnya mangrove memiliki perakaran yang khas untuk menahan ombak
sekaligus mencengkram substrat yang labil (Bengen, 1994).
B. FamiliRhizophoraceae
FamiliRhizophoraceaememiliki spesies yang paling banyak ditemukan.
Rhizophoraceaememiliki akar tunjang berbentuk jangkar (stilt root), akar lutut
(knee root) dan akar papan (Darwes, 1981).Rhizophoraceaebanyak ditemukan di
pantai yang berlumpur ataupun berbatu dan berpasir yang terpengaruh pasang
surut. Kelebihan garam disimpan dalam vakuola sel daun. Buah bersifatvivipari
(berkecambah ketika buah masih menempel di pohon), berbentuk silinder
5
sehingga memudahkan penancapan hipokotil di atas substrat yang berlumpur dan
labil. Pada daerah pantai berlumpur dan berarus tenang,Rhizophora mucronata
banyak ditemukan (Sugianto, 1983). Di daerah pantai yang berpasir dan memiliki
pecahan karang, hanya ditemukan jenisRhizophora stylosa(Whittenet al., 2000).
Rhizophoira apiculatamemerlukan substrat berlumpur yang tidak terlalu dalam
(Monket al., 2000).
C. Bakau Minyak (R. apiculata)
Bakau (R. apiculata) merupakan salah satu pohon yang hidup di hutan mangrove.
Tanaman ini termasuk dalam familiRhizophoraceae,GenusRhizophoradan
spesiesR. apiculata( Duke, 2006).R. apiculatadikenal dengan nama bakau
minyak, memiliki beberapa nama daerah, yaitu bako-bako, bangkita baruang,
dan parai. BakauRhizophora apiculata(Gambar 1), atau dikenal dengan nama
bakau minyak, ialah nama sekelompok tumbuhan di hutan mangrove dari genus
Rhizophoradan familiRhizophoraceae. Tinggi tumbuhan bakau ini bisa
mencapai 30 m dengan diameter batang mencapai 50 cm, dan memiliki perakaran
yang khas hingga mencapai 5 m, kulit kayu berwarna abu-abu dan ranting daunnya
berwarna hijau tua dengan hijau muda pada bagian tengah dan kemerahan di
bagian bawah. Bentuk buahnya membulat telur atau berbentuk seperti buah pir
terbalik, berwarna coklat, panjang 2,0–3,5 cm (Purnobasuki, 2005). BakauR.
apiculata banyak dimanfaatkan dalam bidang kesehatan seperti di India dan Cina
sebagai anti diare, obat mual, dan muntah (Gaoet al.,2008), serta memiliki
aktivitas hipoglikemik (Suret al.,2004). Batang bakau menghasilkan asam
6
menghasilkan tanin yang digunakan sebagai sumber antioksidan alami (Rahim
et al.,2008).
Gambar 1. Tanaman bakau minyak (Rhizophora apiculata)
Ekstrak kasar etanol dari tanaman bakau memiliki aktivitas anti bakteri patogen,
Escherichia coli, P. aeruginosa, K. pneumonia, Enterobacter sp dan
Streptococcus aureusdengan menggunakan metodedisk diffusion(Ravikumaret
al.,2010).
D. Senyawa Steroid
Steroid adalah senyawa metabolit sekunder. Secara biogenesis senyawa steroid
berasal dari asam asetat setalah diaktifkan oleh koenzim A melakukan kondensasi
jenis Claisen menghasilkan asam asetoasetat. Senyawa ini dengan asam asetat
koenzim A melakukan kondensasi secara aldol menghasilkan rantai cabang seperti
yang ditemukan pada asam mevalonat. Reaksi-reaksi berikutnya ialah fosforilasi,
7
(IPP) yang selanjutnya berisomerisasi menjadi dimetilalil pirofosfat (DMAPP)
oleh enzim isomerase. IPP sebagai unit isopren aktif bergabung secara kepala ke
ekor dengan DMAPP, penggabungan ini terjadi karena serangan elektron dari
ikatan rangkap IPP terhadap atom karbon DMAPP yang kekurangan elektron
diikuti oleh penyingkiran ion pirofosfat. Serangan ini menghasilkan Geranil
pirofosfat (GPP). Penggabungan selanjutnya satu unit GPP dan IPP dengan
mekanisme yang sama seperti antara IPP dan DMAPP menghasilkan Farnesil
pirofosfat (FPP). Terbentuknya skualen dari dua molekul FPP yang bergabung
secara ekor-ekor yang segera diubah menjadi 2, 3-epoksiskualen, senyawa ini
kemudian akan menjadi kolesterol pada hewan dan sikloartenol pada tumbuhan
keduanya merupakan golongan senyawa steroid (Achmad, 1986). Ciri umum
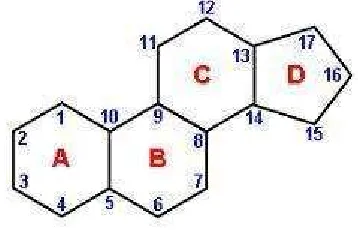
steroid ialah sistem empat cincin yang tergabung. Cincin A, B dan C
beranggotakan enam atom karbon, dan cincin D beranggotakan lima.
Gambar 2. Kerangka dasar steroid dan penomorannya (Achmad, 1968).
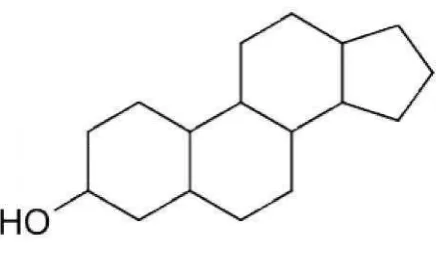
Lemak sterol (bahasa Yunani: stereos, padat) adalah steroid tak jenuh dengan
kerangka kolestana yang mengandung gugus hidroksil-3β dan rantai sisialifatik
dengan minimal 8 atom karbon yang terikat. Lemak sterol merupakan kelompok
8
Jenis zoosterol yang penting antara lain adalah kol
dangkan pada fitosterol dikenal kampesterol, si
Gambar 3. Struktur sterol
pat lebih dari 40 senyawa sterol (Gambar 3) ya
ma fitosterol, yaitu:β-sitosterol, kampesterol, da
).β-sitosterol merupakan senyawa yang efektif di
n penyakit asma, sehingga memungkinkan seny
gai obat terapi penyakit alergi (Yuket al., 2007
ntimikrobial dengan rentang 10 mm sampai 14 m
ruginosa, Escherichia coli, Staphylococcus aureus
t al.,2012).
oid
ibusi secara luas dalam tanaman dan memiliki be
penuaan daun (senescence), mengakibatkan leng
putan,menghambat proses gugurnya daun,mening n sel tumbuhan,menghambat pertumbuhan akar tum
9
meningkatkan resistensi pucuk tumbuhan kepada stress lingkungan,
menstimulasi perpanjangan sel di pucuk tumbuhan,merangsang pertumbuhan pucuk tumbuhan dan merangsang diferensiasixylemtumbuhan. Senyawa
steroid juga menunjukkan aktivitasantifertility, anti-implamasi,antipyretic,
anti diabetes, anti oksidan, agen anti stres dan menunjukkan aktivitas anti
mikroba (Senet al., 2012)
2. Ekstraksi dan Isolasi Steroid
Ekstraksi dilakukan menggunakan metode maserasi. Maserasi merupakan
proses perendaman sampel dengan pelarut organik yang digunakan pada
temperatur ruangan. Proses ini sangat menguntungkan dalam isolasi senyawa
bahan alam karena dengan perendaman sampel tumbuhan akan terjadi
pemecahan dinding dan membran sel akibat perbedaan tekanan antara di
dalam dan di luar sel sehingga senyawa metabolit sekunder yang ada dalam
sitoplasma akan terlarut dalam pelarut organik dan ekstrasi senyawa akan
sempurna karena dapat diatur lama perendaman yang dilakukan (Lenny,
2006). Proses ini dilakukan beberapa kali dan ekstrak kemudian disatukan
lalu diuapkan dengan menggunakan penguap-putar vakum (Markham, 1988).
Setelah dilakukan proses ekstraksi, tahap isolasi selanjutnya adalah analisis
senyawa dengan menggunakan beberapa jenis kromatografi.
10
Kromatografi merupakan pemisahan suatu senyawa yang didasarkan atas
perbedaan laju perpindahan dari komponen-komponen dalam campuran.
Pemisahan dengan metode kromatografi dilakukan dengan cara memanfaatkan
sifat-sifat fisik dari sampel, seperti kelarutan, adsorbsi, keatsirian dan kepolaran.
Kelarutan merupakan kecenderungan molekul untuk melarut dalam cairan.
Adsorpsi penjerapan adalah kecenderungan molekul untuk melekat pada
permukaan serbuk halus (Johnson dan Stevenson, 1991).
Berdasarkan jenis fasa diam dan fasa gerak yang dipartisi, kromatografi dapat
digolongkan menjadi beberapa golongan yang ditabelkan pada Tabel 1.
Tabel 1. Penggolongan kromatografi berdasarkan fasa diam dan fasa gerak.
Fasa Diam Fasa Gerak Sistem kromatogafi
Padat
1. Kromatografi Lapis Tipis (KLT)
Kromatografi Lapis Tipis ialah metode pemisahan fisikokimia yang terdiri
atas bahan berbutir-butir (fase diam), ditempatkan pada penyangga berupa
pelat gelas, logam, atau lapisan yang cocok. Campuran yang akan dipisah,
berupa larutan, ditotolkan berupa bercak atau pita. Setelah pelat atau lapisan
diletakkan di dalam bejana tertutup rapat yang berisi larutan pengembang
11
(pengembangan). Selanjutnya, senyawa yang tidak berwarna harus
ditampakkan (dideteksi) (Stahl, 1985).
Kromatogarafi Lapis Tipis merupakan cara analisis cepat yang memerlukan
bahan yang sedikit. Untuk peneliti pendahuluan kandungan flavonoid suatu
ekstrak, sudah menjadi kebiasaan umum untuk menggunakan pengembang
beralkohol pada pengembangan pertama dengan kromatografi lapis tipis,
misalnya butanol-asam asetat-air (Markham, 1988).
Kromatografi Lapis Tipis digunakan untuk memisahkan senyawa-senyawa
yang sifatnya hidrofob seperti lipida-lipida dan hidrokarbon. Sebagai fase
diam digunakan senyawa yang tak bereaksi seperti silika gel atau alumina.
Silika gel biasa diberi pengikat yang dimaksudkan untuk memberikan
kekuatan pada lapisan dan menambah adesi pada gelas penyokong. Pengikat
yang biasa digunakan adalah kalsium sulfat (Sastrohamidjojo, 2002).
Metode dalam KLT dapat dihitung nilaiRetention factor(Rf) dengan
persamaan :
Tetapi pada gugus-gugus yang besar dari senyawa-senyawa yang susunannya
mirip, sering kali harga Rf berdekatan satu sama lainnya (Sastrohamidjojo,
2002).
12
Pada prinsipnya Kromatografi Kolom (KK) digunakan untuk pemisahan
campuran beberapa senyawa yang diperoleh dari isolasi tumbuhan. Dengan
menggunakan fase padat dan fasa cair maka fraksi-fraksi senyawa akan
menghasilkan kemurnian yang cukup tinggi.
Teknik KK pada dasarnya sama dengan KCV, yaitu merupakan kromatografi
cair-adsorpsi, hanya saja KK dilakukan pada sistem yang bekerja pada
kondisi normal tanpa vakum. Waktu yang dibutuhkan dalam pelaksanaannya
lebih lama, namun diharapkan akan mendapat hasil dengan pemisahan yang
lebih baik dan lebih murni.
3. Kromatografi Cair Vakum (KCV)
Teknik KCV dilakukan dengan suatu sistem yang bekerja pada kondisi
vakum secara terus-menerus sehingga diperoleh kerapatan kemasan yang
maksimum atau menggunakan tekanan rendah untuk meningkatkan laju alir
fasa gerak. Urutan eluen yang digunakan dalam kromatografi cair diawali dari
eluen yang mempunyai tingkat kepolaran rendah kemudian kepolarannya
ditingkatkan secara perlahan-lahan (Hosstetmannet al., 1995).
4. Analisis Kemurnian
Analisis kemurnian senyawa hasil isolasi dilakukan dengan kromatografi
lapis tipis (KLT) dan uji titik leleh. KLT dilakukan dengan mengelusi larutan
sampel yang ditotolkan pada lempeng silika gel 60 F254 dengan fase gerak
13
dengan sinar tampak, UV 254 nm dan UV 366 nm kemurnian senyawa
ditetapkan secara semi kuantitatif dengan densitometer pada λ maks = 347 nm
(Margono dan Zendrato, 2006). Senyawa hasil analisis dikatakan murni
apabila memberikan noda tunggal pada KLT dengan berbagai fase gerak
(Setyowatiet al., 2007).
Sedangkan titik leleh merupakan ciri penting senyawa organik padat. Titik
leleh memiliki arti penting dalam identifikasi dan pengukuran kemurnian.
Penggunaan untuk identifikasi didasarkan pada fakta bahwa semua senyawa
murni mempunyai titik leleh yang tajam ketika berubah sempurna dari padat
ke cair. Selain itu, penggunaan titik leleh untuk identifikasi juga didasarkan
pada fakta bahwa senyawa yang tidak murni menunjukkan 2 fenomena,
pertama yaitu suhu leleh yang lebih rendah, dan kedua memiliki jarak leleh
yang lebih lebar. Alat yang digunakan untuk menguji titik leleh suatu
senyawa adalah termopan. Untuk identifikasi kualitatif, titik leleh merupakan
tetapan fisika yang penting terutama untuk suatu senyawa hasil sintesis,
isolasi, maupun kristalisasi. Titik leleh suatu kristal padat adalah suhu ketika
padatan mulai berubah menjadi cairan pada tekanan udara 1 atm. Jika suhu
dinaikkan, molekul senyawa akan menyerap energi. Semakin tinggi suhu
maka akan semakin banyak energi yang diserap sehingga akan menaikkan
gerakkan vibrasi dan rotasi molekul (Hadiprabowo, 2009).
14
Spektroskopi merupakan ilmu yang mempelajari tentang cara menganalisis
spektrum suatu senyawa dan interaksi antara radiasi elektromagnetik. Teknik
spektroskopi dapat digunakan untuk menentukan struktur dari senyawa organik
tersebut (Fessenden dan Fessenden, 1999). Metode spektroskopi yang dipakai
pada penelitian ini antara lain,Fourier Transform Infrared Spectroscopy(FTIR),
spektroskopi ultraungu-tampak (UV-VIS), spektroskopi resonansi magnetik nuklir
(NMR), dan spektroskopi GC-massa (MS).
1. Fourier Transform Infrared Spectroscopy(FT-IR)
Pada spektroskopi inframerah (IR), senyawa organik akan menyerap berbagai
frekuensi radiasi elektromagnetik inframerah. Molekul-molekul senyawa
akan menyerap sebagian atau seluruh radiasinya. Penyerapan ini berhubungan
dengan adanya sejumlah vibrasi yang terkuantisasi dari atom-atom yang
berikatan secara kovalen pada molekul-molekul itu. Penyerapan ini juga
berhubungan dengan adanya perubahan momen dipol dari ikatan kovalen
pada waktu terjadinya vibrasi (Supriyanto, 1999). Pada dasarnya
spektrofotometer FT-IR (Fourier Trasform Infra Red) sama dengan
spektrofotometer IR dispersi, perbedaan terletak pada sistem optik sebelum
berkas sinar infra merah melewati sampel. Pada sistem optik FT-IR
digunakan radiasi LASER (Light Amplification by Stimulated Emmission of
Radiation) yang berfungsi sebagai radiasi yang diinterferensikan dengan
15
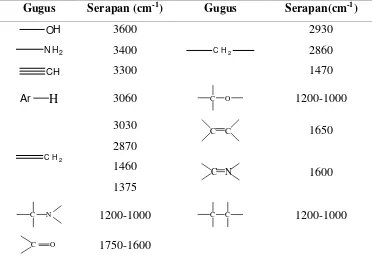
secara utuh dan lebih baik. Karakteristik frekuensi uluran beberapa gugus
molekul ditunjukkan pada Tabel 2.
Tabel 2. Karakteristik frekuensi uluran beberapa gugus fungsi.
Gugus Serapan (cm-1) Gugus Serapan(cm-1)
OH 3600
Ar 3060 C O 1200-1000
C H2
C N 1200-1000 C C 1200-1000
C O 1750-1600
(Banwell dan Mc Cash, 1994).
2. Spektroskopi Ultraungu-Tampak (UV-VIS)
Dalam spektoskopi UV-VIS penyerapan sinar tampak dan ultraviolet oleh
suatu molekul akan menghasilkan transisi di antara tingkat energi elektronik
molekul tersebut. Transisi tersebut pada umumnya antara orbital ikatan,
orbitalnon-ikatan atau orbital anti-ikatan. Panjang gelombang serapan yang
muncul merupakan ukuran perbedaan tingkat-tingkat energi dari orbital suatu
16
3. Spektroskopi Resonansi Magnetik Nuklir (NMR)
Analisis spektroskopi NMR akan memberikan informasi tentang posisi
atom-atom karbon yang memiliki proton atau yang tidak memiliki proton. Selain
itu juga untuk mengenali atom-atom lainnya yang berkaitan dengan proton.
Spektroskopi NMR juga dapat memberikan informasi tentang jumlah dan
jenis atom karbon yang ada pada struktur senyawa organik. Teknik
spektroskopi ini didasarkan pada penyerapan gelombang radio
elektromagnetik oleh inti atom hidrogen atau karbon (Silversteinet al.,1986).
Letak pergeseran kimia untuk proton pada beberapa molekul organik dapat
dilihat pada Tabel 3.
Tabel 3. Letak pergeseran kimia untuk proton dalam molekul organik.
17
4. Spektroskopi GC-Massa (MS)
GC-MS merupakan metode pemisahan senyawa organik yang menggunakan
dua metode analisis senyawa, yaitu kromatografi gas (GC) untuk
menganalisis jumlah senyawa secara kuantitatif dan spektrometri massa (MS)
untuk menganalisis struktur molekul senyawa analit (Fowlis, 1998).
Gas kromatografi merupakan salah satu teknik spektroskopi yang
menggunakan prinsip pemisahan campuran berdasarkan perbedaan kecepatan
migrasi komponen-komponen penyusunnya. Gas kromatografi biasa
digunakan untuk mengidentifikasi suatu senyawa yang terdapat pada
campuran gas dan juga menentukan konsentrasi suatu senyawa dalam fase
gas (Fowlis, 1998).
G. Uji Bioaktivitas
Meningkatnya penggunaan antibiotik dalam mengatasi berbagai penyakit yang
disebabkan oleh bakteri melai menimbulkan masalah baru, terutama karena
sebagian besar bahan antibakteri yang digunakan merupakan zat kimia berbahaya
dan sifatnya tidak aman bagi kesehatan ( Nimahet al.,2012). Sampai saat ini
penanggulangan penyakit yang disebabkan oleh bakteri masih mengandalkan
antibiotik sintesis. Hal ini menimbulkan kekuatiran akan munculnya strain Bakteri
baru yang resisten terhadap antibiotik (Tirtodiharjo, 2011). BakteriEscherichia
colidanBacillus subtilismerupakan kelompok bakteri enterobacteriaceae yang
hidup di dalam saluran pencernaan manusia sebagai penghuni usus (enteron) dan
bersifat patogen. BakteriE. colidapat menyebabkan gastroenteritis pada manusia,
18
juga dapat mengakibatkan gastroenteritis pada manusia yang mengkonsumsinya.
Alternatif yang memungkinkan untuk dikembangkan adalah pemanfaatan
senyawa bioaktif yang dihasilkan oleh tumbuhan secara alami ekstrak tanaman
dapat dimanfaatkan untuk memproduksi agen terapeutik. Karena tanaman juga
menghasilkan beberapa senyawa antimikroba yang efektif terhadap beberapa
mikroba untuk perlindungan diri (Nidhi, 2013). Uji bioaktivitas dilakukan untuk
mengetahui kemampuan suatu senyawa menghambat pertumbuhan suatu
19
III. METODE PENELITIAN
A. Waktu dan Tempat Penelitian
Penelitian telah dilakukan pada bulan Maret 2014 - Juli 2014, bertempat di
Laboratorium Kimia Organik Jurusan Kimia Fakultas MIPA Universitas
Lampung. Analisis spektroskopi yang digunakan adalah spektroskopi
ultraungu-tampak (UV-Vis),Fourier Trasform Infra Red(FT-IR) dilakukan di Laboratorium
Biomassa, spektroskopi resonansi magnetik nuklir (NMR) di Laboratorium
NMR-LIPI Serpong, spektroskopi GC-massa (MS) di Laboratorium Kimia Organik
Jurusan Kimia Fakultas MIPA Universitas Gajah Mada, Yogyakarta.
B. Alat dan Bahan
1. Alat-alat yang digunakan
Alat-alat yang digunakan dalam penelitian ini meliputi alat-alat gelas,
penguap putar vakum, satu set alat kromatografi cair vakum (KCV), satu set
alat kromatografi kolom (KK), pengukur titik leleh, lampu UV, pipet kapiler,
penguap putar vakum, spektrofotometer FT-IR merk Scimitar 2000,
spektrofotometer ultraungu-tampak (UV-VIS) merk Cary 50,
spektrofotometer NMR, spektrofotometer GC-massa (MS) merk Shimadzu
20
2. Bahan-bahan yang digunakan
Bahan yang digunakan adalah kulit akar bakau minyak yang telah
dikeringkan dan dihaluskan, diperoleh dari Balai Besar Budidaya
Pengembangan Laut (BBBPL) Lempasing, Lampung. Pelarut yang
digunakan untuk ekstraksi dan kromatografi berkualitas teknis yang telah
didestilasi sedangkan untuk analisis spektrofotometer berkualitas pro-analisis
(p.a). Bahan kimia yang dipakai meliputi etil asetat (EtOAc), metanol
(MeOH),n-heksana (n-C6H14), aseton (C3H6O2), akuades (H2O), serium
sulfat 1,5% dalam asam sulfat (H2SO4) 2N, benzena (C6H6), kloroform,
diklorometana (CH2Cl2), silika gel Merck G 60 untuk impregnasi, silika gel
Merck 60 (35-70 Mesh) untuk KCV dan KK, untuk KLT digunakan plat KLT
silika gel Merck kiesegal 60 F2540,25 mm.
C. Prosedur Penelitian
1. Persiapan sampel
Kulit akar tumbuhan Bakau Minyak (R. apiculata) diperoleh dari Balai Besar
Budidaya Pengembangan Laut (BBBPL) dari daerah Lempasing, Lampung.
Setelah itu, dilakukan determinasi untuk menentukan Spesies di Herbarium
Bogoriensis bidang Botani Pusat Penelitian Biologi Lembaga Ilmu
Pengetahuan Indonesia (LIPI) Cibinong, Jawa Barat.
Kulit akar Bakau Minyak dicuci bersih dengan air dan diiris kecil-kecil
kemudian dikeringkan dengan cara dijemur di bawah panas sinar Matahari
21
serbuk halus ini yang kemudian digunakan sebagai sampel dalam penelitian
ini.
2. Ekstraksi dengan Metanol
Serbuk halus kulit akar Bakau Minyak ditimbang sebanyak 2000 gram
kemudian direndam dengan menggunkan metanol selama 24 jam. Ekstrak
hasil perendaman kemudian disaring dengan kertas saring. Filtrat yang
didapat lalu dipekatkan denganrotary evaporator. Ekstrak pekat yang didapat
lalu ditimbang.
3. Kromatografi Cair Vakum (KCV)
Ekstrak kasar difraksinasi dengan KCV. Terlebih dahulu fasa diam silika gel
halus sebanyak 3 kali berat sampel dimasukkan ke dalam kolom. Kemudian
kolom dikemas kering dalam keadaan vakum menggunakan alat vakum.
Eluen yang kepolarannya rendah, dimasukkan ke permukaan silikagel halus
terlebih dahulu kemudian divakum kembali. Kolom dihisap sampai kering
dengan alat vakum dan siap digunakan.
Ekstrak kasar yang telah dilarutkan dalam aseton dan diimpregnasikan kepada
silika gel kasar, kemudian dimasukkan pada bagian atas kolom yang telah
berisi fasa diam dan kemudian dihisap secara perlahan-lahan ke dalam
kemasan dengan cara memvakumkannya. Setelah itu kolom dielusi dengan
etil asetat/n-heksan 0% sampai dengan etil asetat 100%. Kolom dihisap
dengan vakum sampai kering pada setiap penambahan eluen (tiap kali elusi
22
pola fraksinasinya. Fraksinasi sampel dengan teknik KCV dilakukan
berulang kali dengan perlakuan yang sama seperti tahapan KCV awal di atas.
4. Kromatografi Lapis Tipis (KLT)
Uji KLT dilakukan terhadap fraksi-fraksi yang akan difraksinasi dan juga
fraksi-fraksi yang didapat setelah perlakuan fraksinasi. Uji KLT dilakukan
menggunakan sistem campuran eluen menggunakan pelarutn-heksana,
etilasetat, kloroform, benzena, metanol, dan diklorometana. Hasil
kromatogram tersebut kemudian disemprot menggunakan larutan serium
sulfat untuk menampakkan bercak/noda dari komponen senyawa tersebut.
Ketika diperoleh fraksi yang lebih sedikit bercak/noda dilihat dibawah lampu
UV setelah dilakukan elusi terhadap plat KLT. Setiap fraksi yang
menghasilkan pola pemisahan dengan Rf (Retention factor) yang sama pada
kromatogram, digabung dan dipekatkan sehingga diperoleh beberapa fraksi
gabungan yang akan difraksinasi lebih lanjut.
5. Kromatografi Kolom (KK)
Setelah dihasilkan fraksi-fraksi dengan jumlah yang lebih sedikit, tahapan
fraksinasi selanjutnya dilakukan menggunakan teknik kromatografi kolom.
Adsorben silika gel Merck (35-70 Mesh) dilarutkan dalam pelarut yang akan
digunakan dalam proses pengelusian. Slurrydari silika gel dimasukkan
terlebih dahulu ke dalam kolom, atur fasa diam hingga rapat (tidak berongga)
dan rata. Selanjutnya masukkan sampel yang telah diimpregnasi pada silika
23
dimasukkan, usahakan agar kolom tidak kering/kehabisan pelarut karena akan
mengganggu fasa diam yang telah dikemas rapat, sehingga proses elusi tidak
akan terganggu.
6. Analisis Kemurnian
Uji kemurnian dilakukan dengan metode KLT dan uji titik leleh. Uji
kemurnian secara KLT menggunakan beberapa campuran eluen. Kemurnian
suatu senyawa ditunjukkan dengan timbulnya satu noda dengan berbagai
campuran eluen yang digunakan, kemudian disemprot menggunakan larutan
serium sulfat untuk menampakkan bercak/noda dari komponen senyawa
tersebut dan pereaksi Liebermann-Burchard yaitu asam asetat glasial dalam
asam sulfat pekat untuk identifikasi senyawa steroid.
Untuk kristal yang berukuran besar, kristal terlebih dahulu digerus hingga
berbentuk serbuk kemudian kristal yang akan ditentukan titik lelehnya
diletakkan pada lempeng kaca, diambil sedikit dengan menggunakan pipet
kapiler, alat dihidupkan dan titik leleh diamati dengan bantuan kaca
pembesar. Suhu pada saat kristal pertama kali mulai meleleh sampai semua
zat meleleh, itulah titik leleh dari senyawa tersebut.
7. Spektroskopi Ultraungu–tampak (UV-VIS)
Sampel berupa kristal murni sebanyak 0,0001 g dilarutkan dalam 10 mL
metanol. Larutan ini digunakan sebagai persediaan untuk beberapa kali
pengukuran. Pertama, sampel diukur serapan maksimumnya dalam metanol.
24
8. Fourier Transform Infrared Spectroscopy(FT-IR)
Sampel kristal hasil isolasi yang telah murni dianalisis menggunakan
spektrofotometer inframerah. Kristal yang telah murni dibebaskan dari air
kemudian digerus bersama-sama dengan halida anorganik, KBr. Gerusan
kristal murni dengan KBr dibentuk menjadi lempeng tipis atau pelet dengan
bantuan alat penekan berkekuatan 8-10 ton per satuan luas kemudian pelet
tersebut diukur puncak serapannya (Sudjadi, 1983).
9. Spektroskopi Resonansi Magnetik Nuklir (NMR)
Sampel berupa kristal murni yang akan diidentifikasi dilarutkan ke dalam
pelarut inert yang tidak mengandung proton seperti CCl4dan CDCl3,
kemudian ditambahkan sedikit senyawa acuan. Larutan ini ditempatkan
dalam tabung gelas tipis dengan tebal 5 mm di tengah-tengah kumparan
frekuensi radio (rf) di antara dua kutub magnet yang sangat kuat kemudian
energi dari kumparan rf ditambah secara terus-menerus. Energi pada
frekuensi terpasang dari kumparan rf yang diserap cuplikan direkam dan
memberikan spektrum NMR (Silverstein dan Morcill,1986).
10. Spektroskopi GC-Massa (MS)
Spektroskopi GC-MS merupakan jenis kromatografi yang digunakan dalam
kimia organik untuk pemisahan dan analisis. GC dapat digunakan untuk
menguji kemurnian dari bahan tertentu atau memisahkan berbagai komponen
dari campuran. Dalam beberapa situasi, GC dapat membantu dalam
25
yang bergerak ataumobile phaseadalah sebuah operator gas yang biasanya
gas murni seperti helium atau yang tidak reaktif seperti gas nitrogen.
Stationaryatau fasa diam merupakan tahap mikroskopis lapisan cair atau
polimer yang mendukung gas murni di dalam bagian dari sistem pipa-pipa
kaca atau logam yang disebut kolom. Instrumen yang digunakan untuk
melakukan kromatografi gas disebut gaschromatographatauaerograph(gas
pemisah) (Paviaet al.,2006).
11. Uji Bioaktivitas
Uji aktivitas antibakteri pada penelitian ini menggunakan metode difusi agar
(Lay, 1994). Isolat bakteri uji yang telah dikultur dalamnutien broth
dioleskan pada permukaannutrien agarmenggunakan kapas lidi steril.
Sebanyak 20 µL ekstrak diteteskan padapaper diskmenggunakan pipet
mikro, selanjutnyapaper diskyang telah mengandung ekstrak diletakan pada
permukaan media inokulasi menggunakan pinset. Bakteri diinkubasi selama
24 jam pada suhu 30oC. Diameter zona hambat yang terbentuk diukur
dengan penggaris. Semua proses di atas dilakukan secara aseptis (Rasyid,
49
V. SIMPULAN DAN SARAN
A. Simpulan
Berdasarkan pembahasan hasil penelitian yang telah dilakukan, maka diperoleh
simpulan sebagai berikut:
1. Pada penelitian ini telah berhasil diisolasi dan diidentifikasi senyawa steroid
dari kulit akar bakau minyak (Rhizophora apiculata)yang dikenal dengan
Stigmast-5en-3β-ol (β-Sitosterol).
2. Senyawa steroid yang didapatkan sebanyak 0,214 gram (0,01%) memiliki sifat
fisik berupa kristal jarum, bening dengan titik leleh 160,2-161oC.
3. β-Sitosterol hasil isolasi memiliki bioaktivitas terhadap bakteriE. coli.
B. Saran
1. Penelitian lebih lanjut terhadap bagian lainR. apiculataperlu dilakukan
sehingga memperoleh informasi baru tentang jenis-jenis senyawa metabolit
sekunder yang terkandung.
2. Pelarut yang berbeda pada saat maserasi atau partisi sehingga diharapkan
51
DAFTAR PUSTAKA
Achmad, S. A. 1986.Kimia Organik Bahan Alam.Karunika Jakarta. Jakarta.
Achmad, S.A., E.H. Hakim, L.J. Dewi, L. Makmur, dan Y.A. Maolana. 2006. Hakekat Perkembangan kimia Organik Bahan Alam Dari Tradisional ke Moderen dan Contoh terkait Dengan Tumbuhan Lauraceae, Moraceae, dan Dipterocarpaceae Indonesia. Akta Kimindo.1. 55-66.
Abdullah. 2011.Potensi Bakau Rhizopora apiculata sebagai Inhibitor Tirosinase dan Antioksidan. (Tesis). Institut Pertanian Bogor. Bogor. Hlm 23.
Arief, A. 2003.Hutan Mangrove Fungsi dan Manfaatnya. Kanisius. Yogyakarta.
Banwell, C.N. and E.M. McCash. 1994. Fundamental of Molecular Spectroscopy. Mc Graw-Hill Book Company. London.
Bengen, D. G. 1994.Pedoman Teknis Pengenalan dan Pengelolaan Ekosistem Mangrove. Institut Pertanian Bogor. Bogor.
Darwes, J. C. 1981.Marine Botany.A Wiley Interscience Publication. University of South Florida. Florida.
Duke, C. N. 2006. Rhizophora apiculata, R. mucrona, R. stylosa, R. annamalal, (indo-west pasific still mangrove), species profile for Pasific Island forestry.International Journal of Mangrove Plants.II. 1-20.
Fessenden, R.J. dan J. S. Fessenden. 1999.Kimia OrganikJilid I. Erlangga. Jakarta. Hlm 525.
52
Gao, M., H. Xiao, and S. Yang. 2008. Screening of Antitumor Compound from Rhizophora apiculata blume.Journal of Biotechnology.IV. 577-588. Gritter, R.J., J.M. Bobbitt, dan A.E. Schwarting. 1991.Pengantar Kromatografi.
Institut Teknologi Bandung. Bandung. Hlm 266.
Hadiprabowo, T. 2009.Optimasi Sintesis Analog Curcumarin 1,3-Bis- (4-Hidroksi-3-Metoksi Benzilidin) Urea pada Rentang pH 3-4. (Skripsi). Universitas Muhammadiyah Surakarta. Surakarta. Hlm 10-11.
Hostettman, K., M. Hostettman, dan A. Manson. 1995.Cara kromatografi Preparatif Penggunaan pada Senyawa Bahan Alam. Alih bahasa Kosasih Padmawinata. Institut Teknologi Bandung. Bandung. Hlm 27-34.
Johnson, L.E. dan R. Stevenson. 1991.Dasar Kromatografi Cair. Alih bahasa Kosasih Padmawinata. Institut Teknologi Bandung. Bandung. Hlm 365.
Lalitha, M. K. 2004.Manual on Antimicrobial Susceptibility Testing.Christian Medical College. Tamil Nadu.
Lay, B. W. 1994.Analisis Mikroba di Laboratorium.Grafindo Persada. Jakarta.
Lenny, S. 2006.Senyawa Flavonoida, Fenilpropanoida, dan alkaloid.Karya ilmiah. Departemen Kimia. FMIPA.Universitas Sumatera Utara. Medan. Hlm 7.
Loo, A. and Y. Jain. 2008. Stilbenes with tyrosinase inhibitor activity.Current Science.II.44-52.
Nidhi., K, Utam., and K, Sumit. 2013. Identification and screening of bioactive compoundsBarleria prionitis Linnrhizome exhibiting antibacteria activity.International Journal of Biochemistry.3. 1-6.
Nimah, S., W. F. Maruf and A. Trianto. 2012. Uji aktivitas ekstrakHolothuria scabaterhadap bakteriPseudomonas aeruginosa danBacilluscereus. Jurnal Perikanan.1. 1-9.
53
Markham, K.R. 1988.Cara Mengidentifikasi Flavonoid. Alih Bahasa Kosasih Padmawinata. Institut Teknologi Bandung. Bandung. Hlm 117.
Monk, K. A., Y. D. Fretes., G. Reksodihardjo-Lilley. 2000.Ekologi Nusa Tenggara dan Maluku.Prehalindo. Jakarta.
Pavia, D., L., G. M. Lampman,, G. S. Kritz, and R. G. Engel.
2006. Introduction to Organic Laboratory Techniques (4th Ed.).Thomson Brooks/Cole. 797–817.
Purnobasuki, H. 2005.Potensi Mangrove Sebagai Tanaman Obat.Jurnal.Biota IX 2.125-126.
Rahim, A., E. Rocca, J. Steinmetz, M. Kassim, M. Ibrahim, And H. Osman. 2008. Antioxidant Activities of Mangrove Rhizophora apiculata Bark Ekstracts. Journal of Food Chemistry.8(2). 200-207.
Rasyid, A. 2012.Identifikasi Senyawa Metabolit Sekunder-Serta Uji Aktivitas Antibakteri dan Antioksidan Ekstrak Metanol Teripang Stichopus hermanii.Institut Pertanian Bogor. Bogor.
Ravikumar, S., M. Gnanadesigan., P. Suganthi, and A. Ramalaksmi. 2010. Antibacterial potential of chosen mangrove plants againts isolated urinary tract infectious bacterial pathogens.International Journal of Medicine and Medical Sciences.2(3). 94-99.
Saeidnia, S., M, Azadeh., R. G. Ahmad, and A. Mohammad. 2014. The Story of Beta-sitosterol- A Review.European Journal of Medicine Plants.4(5) Salempa, P., A. Noor., N. H. Soekamto, dan T. Harlim. 2009. Bioaktivitas Fraksi
n-heksan dan Senyawa β-sitosterol dari Kayu Akar Pterospermum subpeltatum C.B.Rob. Farmakologi .4(2), Hlm 45-50.
Sastrohamidjojo, H. 2002.Kromatografi. Liberty. Yogyakarta. Hlm 35-36.
Sen, A., P, Dhavan., K, K, Shukla., S, Singh, and G, Tejovathi. 2012. Analysis of IR, NMR and Antimicrobial Activity ofβ-Sitosterol Isolated from
54
Setyowati, E. P., U. A. Jenie, Sudarsono, B. Kardono, R. Rahmat, dan E.
Meiyanto. 2007. Isolasi Senyawa Sitotoksik Spons Kaliasis.M. Far. Indo.
18(4). Hlm 183-189.
Silverstein, B., dan Morcill. 1986.Penyelidikan Spektrometrik Senyawa Organik. Alih bahasa Drs. A. J. Hartomo. ITS. Semarang. Hlm 191-195.
Stahl, E. 1985.Analisis Obat Secara kromatografi dan Mikroskopi. diterjemahkan oleh Kosasih Padmawinata dan Iwang Soediro. Institut Teknologi
Bandung. Bandung. Hlm 3-17.
Sudjadi. 1983.Penentuan Struktur Senyawa Organik. Ghalia Indonesia. Jakarta. Hlm 283.
Sugianto. 1983.Kenalilah Flora Pantai Kita.Widjaya. Jakarta.
Supriyanto, R. 1999. Buku Ajar Kimia Analitik III. FMIPA Universitas Lampung. Bandar Lampung. Hlm 2-3.
Sur, T. K., T. Seal, S. Pandit, dan D. Bhattacharyya. 2004. Hypoglicemic Activities of a Mangrove Plant Rhizophora apiculata blume. Natural Product Science.Hlm 11-15.
Tirtodiharjo, M. K. 2011.Strategi mengatasi bakteri yang resisten terhadap antibiotik.Universitas Gajah Mada. Yogyakarta.
Tukiran., B. E. Hamdani., R. Mahyudi., S. H. Hi Syarief, dan N. Hidayati. 2009. Beberapa Senyawa Hasil Isolasi dari Kulit Batang Tumbuhan Kedoya. Universitas Negeri Surabaya. Surabaya.
Patra, A., S. Jha., P. N. Murthy., Manik, and A. Sharone. 2010. Isolation and Characterization of Stigmast-5en-3β-ol from the leaves ofHygrophila spinosa. International Journal of Pharma Science and Research.I. 95-100. Volk, W.A. and Wheeler. 1988.Mikrobiologi Dasar.Jilid I Edisi kelima. Alih
Bahasa Markham. Erlangga. Jakarta. Hal 221-230.
Whitten, T., R. E. Soeriaatmadja, and S. Afiff. 2000.Ecology of Java and Bali. Periplus. Singapore.
Yuk, J.K., J. S. Woo., C. Y. Yun., J. S. Lee., J. H. Kim., Y. G. Song., E. J. Yang., I. K. Hur, and I. S. Kim. 2007. Effects of Lactose-β-sitosterol and