SKRIPSI
PENGARUH PENCELUPAN TAHU DALAM PENGAWET ASAM ORGANIK TERHADAP MUTU SENSORI DAN UMUR SIMPAN
Oleh
DODY SETYADI F24104068
2008
FAKULTAS TEKNOLOGI PERTANIAN INSTITUT PERTANIAN BOGOR
DODY SETYADI. F24104068. Pengaruh Pencelupan Tahu dalam Pengawet
Asam Organik Terhadap Mutu Sensori dan Umur Simpan. Di bawah bimbingan : Joko Hermanianto. 2008
RINGKASAN
Tahu termasuk bahan pangan yang cepat rusak sehingga dapat digolongkan ke dalam golongan high perishable food (Shurtleff dan Aoyagi, 1975). Tahu banyak mengandung air, protein, lemak, karbohidrat, vitamin, dan mineral sehingga menjadikannya sebagai media yang cocok sebagai tempat tumbuh mikroba. Tahu yang dibiarkan pada udara terbuka tanpa perlakuan pengawetan apapun hanya dapat bertahan sekitar 10 jam pada suhu kamar. Dalam upaya memperpanjang umur simpan, pihak industri kerap kali menggunakan formalin untuk memperpanjang umur simpan. Penggunaan formalin yang berlebihan (>0.05 ppm) dapat menyebabkan kanker pada manusia.
Aktivitas antimikrobial asam organik ditentukan oleh besarnya persentase molekul asam yang tidak terurai (undissociated), yang ditetapkan dengan nilai pKa. Bahan makanan yang memiliki pH rendah, banyaknya persentase molekul asam organik yang tidak terurai meningkat, sehingga kemampuan sebagai antimikrobial juga akan meningkat.
Penelitian ini bertujuan untuk (1) mempelajari pengaruh penggunaan asam organik terhadap mutu sensori dan umur simpan tahu, (2) mengaplikasikan secara nyata penggunaan asam organik pada tahu dengan biaya yang relatif rendah. Sedangkan indikator keberhasilan dari penelitian ini adalah (1) Penggunaan asam organik mampu mempertahankan mutu tahu pada penyimpanan suhu ruang minimal selama 2 hari, (2) Penggunaan asam organik pada tahu mampu menghasilkan nilai penerimaan konsumen pada analisis sensori (uji hedonik) sebesar 5 dari 7 skala nilai.
Proses pengawetan dilakukan dengan pencelupan bahan tahu dalam formulasi larutan pengawet asam organik selama 1 menit. Tahu yang sudah dicelup kemudian dikemas dalam plastik HDPE yang dirapatkan dengan menggunakan sealer. Penyimpanan dilakukan pada suhu ruang. Pengamatan dilakukan setiap hari terhadap uji total mikroba, total asam tertitrasi, pH, warna, dan tekstur.
Larutan asam organik yang digunakan, baik cuka pasar ataupun asam asetat glasial untuk setiap konsentrasi, dapat digunakan berulang kali untuk mencelup tahu sampai dengan 10 kali pencelupan. Hal tersebut dapat dilihat dari keefektifan asam organik untuk mengawetkan pada pencelupan ke-10 tidak berbeda seperti pada pencelupan pertama. Oleh karena itu, penghematan dapat dicapai dengan menggunakan teknik pengawetan tersebut.
Data yang dihasilkan pada penelitian menunjukkan bahwa formula larutan pengawet asam asetat dan cuka pasar dengan konsentrasi masing-masing 2% dan 2.5% dapat memperpanjang umur simpan sampai 2 hari. Hal ini dapat dilihat dari jumlah mikroba yang sudah melebihi batas SNI dan sudah mulai timbul lendir pada tahu pada hari ke-2. Perlakuan formulasi terbaik untuk mempertahankan umur simpan tahu adalah tahu dengan asetat 3% dan cuka pasar 3%. Tahu dengan perlakuan formulasi tersebut dapat mempertahankan umur simpan sampai 3 hari.
Hasil yang didapat pada uji hedonik memperlihatkan bahwa panelis lebih menyukai tahu dengan pengawet cuka pasar 3% daripada tahu dengan asam asetat glasial 3% dalam hal rasa dan aroma. Nilai skor rasa dan aroma tahu dengan cuka pasar 3% tidak berbeda secara signifikan dengan tahu kontrol sehingga bisa dikatakan rasa dan aroma tahu dengan cuka pasar 3% tidak jauh berbeda dengan rasa dan aroma tahu segar (tanpa perlakuan pengawetan).
Biaya pengawetan dengan perlakuan cuka pasar 3% lebih rendah dibandingkan dengan asam asetat glasial 3% dan formalin 3%. Biaya pengawetan cuka pasar 3% hanya sekitar Rp. 2,11/kg tahu, sedangkan asetat glasial 3% sebesar Rp. 2,68/kg tahu, dan formalin 3% sebesar Rp. 4.22/Kg tahu.
Berdasarkan kemampuan mempertahankan umur simpan dan
pertimbangan ekonomi, dapat disimpulkan bahwa pengawet cuka pasar 3% memberikan hasil terbaik dalam mengawetkan tahu, sehingga cuka pasar 3% dapat direkomendasikan untuk mengawetkan tahu.
PENGARUH PENCELUPAN TAHU DALAM PENGAWET ASAM ORGANIK TERHADAP MUTU SENSORI DAN UMUR SIMPAN
SKRIPSI
Sebagai salah satu syarat untuk memperoleh gelar
SARJANA TEKNOLOGI PERTANIAN
Pada Jurusan Ilmu dan Teknologi Pangan, Fakultas Teknologi Pertanian,
Institut Pertanian Bogor
Oleh
DODY SETYADI F24104068
2008
FAKULTAS TEKNOLOGI PERTANIAN INSTITUT PERTANIAN BOGOR
PENGARUH PENCELUPAN TAHU DALAM PENGAWET ASAM ORGANIK TERHADAP MUTU SENSORI DAN UMUR SIMPAN
SKRIPSI
Sebagai salah satu syarat untuk memperoleh gelar
SARJANA TEKNOLOGI PERTANIAN
Pada Jurusan Ilmu dan Teknologi Pangan, Fakultas Teknologi Pertanian,
Institut Pertanian Bogor
Oleh
DODY SETYADI F24104068
Dilahirkan pada tanggal 22 Maret 1986 di Bogor
Tanggal Lulus : Agustus 2008
Menyetujui, Bogor, Agustus 2008
Dr. Ir Joko Hermanianto Dosen Pembimbing
Dr. Ir. Dahrul Syah, MSc.
RIWAYAT HIDUP PENULIS
Penulis dilahirkan di Kota Bogor pada tanggal 22 Maret 1986. Penulis adalah anak kedua dari tiga bersaudara dari keluarga Bapak Tamsil dan Ibu Ratna Wilis. Penulis mengawali jenjang pendidikannya di TK Akbar Bogor pada tahun 1991-1992, menempuh pendidikan dasar di SD Negeri Polisi IV Bogor pada tahun 1992-1998, menempuh sekolah lanjutan di SLTPN 1 Bogor pada tahun 1998-2001, serta SMUN 1 Bogor pada tahun 2001-2004.
Penulis lulus seleksi penerimaan mahasiswa IPB pada tahun 2004 melalui jalur Undangan Seleksi Masuk IPB (USMI) dan terdaftar di Departemen Teknologi Pangan dan Gizi (yang sekarang dirubah menjadi Departemen Ilmu dan Teknologi Pangan), Fakultas Teknologi Pertanian, Institut Pertanian Bogor (Fateta, IPB).
Selama di bangku sekolah dan perkuliahan penulis aktif dalam kegiatan akademik, non akademik, dan organisasi. Dalam kegiatan akademik, penulis pernah menjadi juara dalam lomba "Cerdas Cermat tingkat SD se-Kota Bogor" pada tahun 1997 dan juara lomba "Debat Bahasa Inggris se-IPB" yang diadakan oleh BEM KM IPB pada tahun 2005. Dalam bidang non akademik, penulis pernah mengikuti "Lomba Lintas Alam" yang diselenggarakan oleh Fakultas Kehutanan IPB pada tahun 2005. Dalam bidang organisasi, penulis pernah menjadi pengurus OSIS SMUN I Bogor sebagai anggota sekbid 7 periode 2002-2003 dan pengurus HIMITEPA (Himpunan Mahasiswa Ilmi dan Teknologi Pangan) sebagai anggota divisi Sosial dan Kemasyarakatan periode 2005-2006.
Penulis menyelesaikan tugas akhir berupa penelitian yang berjudul “Pengaruh Pencelupan Tahu dalam Pengawet Asam Organik Terhadap Mutu dan Umur Simpan“ di Laboratorium Departemen Ilmu dan Teknologi Pangan di bawah bimbingan Dr. Ir. Joko Hermanianto.
KATA PENGANTAR
Puji dan syukur dipanjatkan ke hadapan Allah, karena hanya dengan rahmat-Nyalah maka skripsi ini dapat penulis selesaikan.
Penulis mengucapkan terima kasih kepada :
1. Kedua orangtua (Bapak Tamsil dan Ibu Ratna Wilis) atas semua doa, kasih sayang, semangat, pengorbanan, tetes darah dan keringat, perlindungan, bantuan moril dan materil tiada henti kepada penulis sehingga penulis dapat terus maju, dan juga kepada Kakak (Rita Ariyani) dan Adik (Amelia Agustina) atas semua support dan semangat yang diberikan.
2. Dr. Ir. Joko Hermanianto selaku dosen pembimbing akademik atas pengarahan, bimbingan, dan bantuan sehingga penulis dapat menyelesaikan tugas akhir ini, serta nasehat yang sangat berharga bagi kehidupan penulis kelak.
3. Dr. Ir. Slamet Budijanto, MAgr dan Dr. Ir. Sukarno, MSc yang telah meluangkan waktunya menjadi dosen penguji, terima kasih atas kritik dan saran yang sangat membangun untuk pengevaluasian diri.
4. Nina Nurmayanti yang telah memberikan dukungan moril dan kebersamaan selama penulis melakukan studi di Fakultas Teknologi Pertanian.
5. Rais, Lutfi, Bima, Ancha, dan Anto, sebagai partner sejati dalam permainan WE.
6. Teman satu bimbingan Nene, Cici, Nina, Tiyu, Nanda, Muji, Tedy, Kak Denang, Mbak Ajeng, terima kasih atas bantuannya.
7. Zambros, Manto, Memed, Sisi, Nene, Soun, Rina, terima kasih atas kebersamaan dalam kelompok praktikum dari awal masuk kuliah sampai semester terakhir.
8. Tim futsal ITP 41: Aris, Ancha, Anto, Iqbal, Boink, Dikun, Nanang. Terima kasih atas dua tahun berturut-turut sebagai juara futsal ITP.
9. Teman-teman satu lab. penelitian: Nene, Cici, Aris, Nanang, Ety, Umul, terima kasih atas pinjaman alat dan bantuannya.
10. Jamal Zamrudi dan Arif Murtaqi atas pinjaman laptop dan LCD sewaktu sidang.
11. Dyah, Fina, Dikun, Ameh, dan Nina, atas kebersamaan dalam PKM es krim bekatul.
12. Rais, Wulan, Tedy, terima kasih atas Gede-Pangrango 3 Desember 2006. 13. Seluruh mahasiswa ITP 41 Wardi, Arif otot, Ary, Sukma, Arum, Rani, Kani,
Yuli, Vera, Hans CW, Hans PK, Riska, Tika A, Tika I, Dini, Wachu, Tuko, Au, Citra, Cece, Ratih, Eci, Ofa, Erma, Eka F, Farid, Yuke, Chabib, Ros, Nduters, Gema, Kurnia,Tomi, April, Yunita, Sinta, Sofian, Jamal L,dll, terima kasih atas 4 tahun yang tak terlupakan.
14. Yohan, Dito, Rejos, Regi, Aswan, Islam yang masih eksis bersama dalam tim futsal Smansa
15. Dito, Regi, Ikhsan, atas kebersamaannya dalam band yang belum pernah manggung.
16. Fakri, Aji, Bacek "Handsome Devil", terima kasih atas Taman Topi, LC, Spektrum, that's when We Rock n Roll.
17. Anak-anak "Under Tree", Arab, Pipit, Gondrong, moron, beruk, dll, Thank's for the Rock Time
18. Hesti, Wiwi, Aji, Haris, Jaqaw, Nanda, Fera, Umam, Midun, Venty (terima kasih atas pinjaman pedoman skripsi), dan anak-anak ITP 42 dan 43 lainnya, terima kasih atas dukungannya.
19. Pa Gatot, Mas Edi, Pa Sidik, Pa Sobirin, Pa Mul, Pa Yahya, Pa Rojak, Pa Koko, Pa Wahid, Bu Rubiyah, Bu Antin, Mba Ida, Mba Darsih, atas segala bantuan kepada penulis selama menyelesaikan pendidikan.
20. Semua pihak yang tidak dapat disebutkan satu persatu yang selama ini telah membantu penulis secara langsung maupun tidak langsung dalam menyelesaikan pendidikan di IPB.
Akhirnya kritik dan saran sangat penulis harapkan demi perbaikan tulisan selanjutnya.
DAFTAR ISI
Halaman
KATA PENGANTAR ... iii
DAFTAR TABEL ... viii
DAFTAR GAMBAR ... ix
DAFTAR LAMPIRAN ... xi
I. PENDAHULUAN ... 1
A. LATAR BELAKANG ... 1
B. TUJUAN ... 3
C. INDIKATOR KEBERHASILAN PENELITIAN ... 3
D. MANFAAT ... 3
II. TINJAUAN PUSTAKA ... 4
A. TAHU ... 4
B. KERUSAKAN TAHU ... 6
C. ASAM ORGANIK ... 8
D. MEKANISME PENGAWETAN ASAM ORGANIK ... 10
E. METODE PENGAWETAN DENGAN PENCELUPAN ... 11
F. PENGEMASAN ... 12
III. METODE PENELITIAN ... 13
A. BAHAN DAN ALAT ... 13
B. METODE PENELITIAN ... 13
1. Penelitian Pendahuluan ... 13
2. Penelitian Utama ... 14
C. PERLAKUAN ... 15
1. Jenis Pengawet Asam Organik ... 15
2. Konsentrasi Pengawet Asam Organik ... 15
3. Kondisi Pengemasan ... 16
D. PENGAMATAN ... 16
1. Total Asam Tertitrasi ... 16
2. Total Mikroba ... 16
4. Uji Organoleptik ... 18 5. pH ... 18 6. Intensitas Warna ……… 19 7. Tekstur ……… 20 8. Uji Statistik ... 20 9. Analisis Biaya ... 20 E. RANCANGAN PERCOBAAN ... 20
IV. HASIL DAN PEMBAHASAN ... 21
A. PENELITIAN PENDAHULUAN ……… 22
1. pH ……… 22
2. Total Asam Tertitrasi (TAT) ……….. 25
3. Total Mikroba ……… 27
4. Pengamatan Visual ………. 30
B. PENELITIAN UTAMA ………. 33
1. pH ……… 34
2. Total Asam Tertitrasi (TAT) ……….. 38
3. Total Mikroba (TPC) ……….. 42 4. Tekstur ……… 47 5. Warna ………. 50 6. Analisis Organoleptik ………. 58 a. Aroma ……….. 59 b. Rasa ……….. 60 7. Analisis Biaya ……… 62
V. KESIMPULAN DAN SARAN ………. 64
A. KESIMPULAN ……… 64
B. SARAN ………. 65
DAFTAR PUSTAKA... 66
DAFTAR TABEL
Halaman Tabel 1. Jumlah batasan maksimal asam organik yang dapat dimakan
per hari oleh manusia ... 2
Tabel 2. Komposisi kimia dan kandungan gizi tahu ... 5
Tabel 3. Kriteria mutu tahu ... 5
Tabel 4. Solubilitas asam organik sebagai bahan pengawet makanan ... 9
Tabel 5. Konsentrasi hambatan asam organik terhadap mikroorganisme ... 10
Tabel 6. Pengawetan tahu dengan metode pencelupan ... 12
Tabel 7. Formulasi konsentrasi larutan pengawet asam organik pada tahap penelitian pendahuluan ... 14
Tabel 8. Penilaian mutu sensori tahu ... 17
DAFTAR GAMBAR
Halaman
Gambar 1. Nilai pH tahu pada penelitian pendahuluan ……… 23
Gambar 2. Nilai TAT tahu pada penelitian pendahuluan ... 25
Gambar 3. Total mikroba tahu pada penelitian pendahuluan ... 27
Gambar 4. Grafik hasil uji keawetan secara sensori pada sampel tahu dengan beberapa jenis pengawet asam organik ... 30
Gambar 5. Nilai pH tahu dengan pengawet asam asetat glasial selama penyimpanan ... 34
Gambar 6. Nilai pH tahu dengan pengawet cuka pasar selama penyimpanan ... 35
Gambar 7. Nilai TAT pada tahu dengan pengawet asam asetat glasial .... 39
Gambar 8. Nilai TAT pada tahu dengan pengawet cuka pasar ... 40
Gambar 9. Total mikroba pada tahu dengan pengawetan asam asetat glasial selama penyimpanan ... 42
Gambar 10. Total mikroba tahu dengan pengawet cuka pasar ... 44
Gambar 11. Kekenyalan tahu dengan pengawet asam asetat glasial ... 48
Gambar 12. Kekenyalan tahu dengan pengawet cuka pasar ... 49
Gambar 13. Kecerahan tahu dalam pengawet asam asetat glasial ... 52
Gambar 14. Kecerahan tahu dalam pengawet cuka pasar ... 52
Gambar 15. Nilai intensitas warna merah (a) pada tahu dengan pengawetan dalam asam asetat glasial ... 54
Gambar 16. Nilai intensitas warna merah (a) pada tahu yang direndam dalam cuka pasar ... 55
Gambar 17. Intensitas warna kuning (b) pada tahu yang direndam dalam asam asetat glasial ... 57
Gambar 18. Intensitas warna kuning pada tahu yang direndam dalam cuka pasar ... 58
Gambar 19. Respon panelis terhadap aroma tahu ... 59
Gambar 20. Respon panelis terhadap rasa tahu ... 61
DAFTAR LAMPIRAN
Halaman
Lampiran 1. Skema pembuatan tahu secara umum ……… 69
Lampiran 2. Hasil pengamatan pH tahu pada penelitian pendahuluan …. 70 Lampiran 3. Hasil pengamatan total mikroba tahu pada penelitian
pendahuluan ……….. 70
Lampiran 4. Hasil pengamatan total asam tertitrasi tahu pada penelitian pendahuluan ... 70 Lampiran 5. Nilai sensori tahu pada penelitian pendahuluan ... 71 Lampiran 6. Hasil pengamatan pH tahu dengan pengawet asam asetat
glasial ... 71 Lampiran 7. Hasil pengamatan pH tahu dengan pengawet cuka pasar ... 71 Lampiran 8. Hasil pengamatan total mikroba tahu dengan pengawet
asam asetat glasial ... 72 Lampiran 9. Hasil pengamatan total mikroba tahu dengan pengawet
cuka pasar ... 72 Lampiran 10. Hasil pengamatan total asam tertitrasi tahu dengan
pengawet asam asetat glasial ... 72 Lampiran 11. Hasil pengamatan total asam tertitrasi tahu dengan cuka
pasar ... 73 Lampiran 12. Hasil pengamatan kekenyalan tahu dengan pengawet asam
asetat glasial ... 73 Lampiran 13. Hasil pengamatan kekenyalan tahu dengan pengawet cuka
pasar ... 73 Lampiran 14. Hasil pengamatan kecerahan tahu dengan pengawet asam
asetat glasial ... 74 Lampiran 15. Hasil pengamatan kecerahan tahu dengan pengawet cuka
pasar ... 74 Lampiran 16. Hasil pengamatan intensitas merah tahu dengan pengawet
Lampiran 17. Hasil pengamatan intensitas merah tahu dengan pengawet cuka pasar ... 75 Lampiran 18. Hasil pengamatan intensitas kuning tahu dengan pengawet
asam asetat glasial ... 75 Lampiran 19. Hasil pengamatan intensitas kuning tahu dengan pengawet
cuka pasar ... 75 Lampiran 20. Analisis sidik ragam pH pada penelitian pendahuluan hari
ke-1 ... 76 Lampiran 21. Analisis sidik ragam pH pada penelitian pendahuluan hari
ke-2 ... 76 Lampiran 22. Analisis sidik ragam pH pada penelitian pendahuluan hari
ke-3 ... 77 Lampiran 23. Analisis sidik ragam total mikroba pada penelitian
pendahuluan hari ke-1 ... 77 Lampiran 24. Analisis sidik ragam total mikroba pada penelitian
pendahuluan hari ke-2 ... 78 Lampiran 25. Analisis sidik ragam total mikroba pada penelitian
pendahuluan hari ke-3 ... 79 Lampiran 26. Analisis sidik ragam total asam tertitrasi pada penelitian
pendahuluan hari ke-1 ... 79 Lampiran 27. Analisis sidik ragam total asam tertitrasi pada penelitian
pendahuluan hari ke-2 ... 80 Lampiran 28. Analisis sidik ragam total asam tertitrasi pada penelitian
pendahuluan hari ke-3 ... 80 Lampiran 29. Analisis sidik ragam pH tahu yang diawetkan dengan asam
asetat glasial hari ke-1 ... 81 Lampiran 30. Analisis sidik ragam pH tahu yang diawetkan dengan asam
asetat glasial hari ke-2 ... 81 Lampiran 31. Analisis sidik ragam pH tahu yang diawetkan dengan asam
asetat glasial hari ke-3 ... 82 Lampiran 32. Analisis sidik ragam pH tahu yang diawetkan dengan cuka
Lampiran 33. Analisis sidik ragam pH tahu yang diawetkan dengan cuka pasar hari ke-2 ... 83 Lampiran 34. Analisis sidik ragam pH tahu yang diawetkan dengan cuka
pasar hari ke-3 ... 83 Lampiran 35. Analisis sidik ragam total asam tertitrasi tahu yang
diawetkan dengan asam asetat glasial hari ke-1 ... 84 Lampiran 36. Analisis sidik ragam total asam tertitrasi tahu yang
diawetkan dengan asam asetat glasial hari ke-2 ... 84 Lampiran 37. Analisis sidik ragam total asam tertitrasi tahu yang
diawetkan dengan asam asetat glasial hari ke-3 ... 85 Lampiran 38. Analisis sidik ragam total asam tertitrasi tahu yang
diawetkan dengan cuka pasar hari ke-1 ... 85 Lampiran 39. Analisis sidik ragam total asam tertitrasi tahu yang
diawetkan dengan cuka pasar hari ke-2 ... 86 Lampiran 40. Analisis sidik ragam total asam tertitrasi tahu yang
diawetkan dengan cuka pasar hari ke-3 ... 86 Lampiran 41. Analisis sidik ragam total mikroba tahu yang diawetkan
dengan asam asetat glasial hari ke-1 ... 87 Lampiran 42. Analisis sidik ragam total mikroba tahu yang diawetkan
dengan asam asetat glasial hari ke-2 ... 87 Lampiran 43. Analisis sidik ragam total mikroba tahu yang diawetkan
dengan asam asetat glasial hari ke-3 ... 88 Lampiran 44. Analisis sidik ragam total mikroba tahu yang diawetkan
dengan cuka pasar hari ke-1 ... 89 Lampiran 45. Analisis sidik ragam total mikroba tahu yang diawetkan
dengan cuka pasar hari ke-2 ... 89 Lampiran 46. Analisis sidik ragam total mikroba tahu yang diawetkan
dengan cuka pasar hari ke-3 ... 90 Lampiran 47. Analisis sidik ragam kekenyalan tahu yang diawetkan
dengan asam asetat glasial hari ke-1 ... 91 Lampiran 48. Analisis sidik ragam kekenyalan tahu yang diawetkan
Lampiran 49. Analisis sidik ragam kekenyalan tahu yang diawetkan dengan asam asetat glasial hari ke-3 ... 92 Lampiran 50. Analisis sidik ragam kekenyalan tahu yang diawetkan
dengan cuka pasar hari ke-1 ... 92 Lampiran 51. Analisis sidik ragam kekenyalan tahu yang diawetkan
dengan cuka pasar hari ke-2 ... 93 Lampiran 52. Analisis sidik ragam kekenyalan tahu yang diawetkan
dengan cuka pasar hari ke-3 ... 93 Lampiran 53. Analisis sidik ragam kecerahan (L) tahu yang diawetkan
dengan asam asetat glasial hari ke-1 ... 94 Lampiran 54. Analisis sidik ragam kecerahan (L) tahu yang diawetkan
dengan asam asetat glasial hari ke-2 ... 95 Lampiran 55. Analisis sidik ragam kecerahan (L) tahu yang diawetkan
dengan asam asetat glasial hari ke-3 ... 95 Lampiran 56. Analisis sidik ragam kecerahan (L) tahu yang diawetkan
dengan cuka pasar hari ke-1 ... 96 Lampiran 57. Analisis sidik ragam kecerahan (L) tahu yang diawetkan
dengan cuka pasar hari ke-2 ... 97 Lampiran 58. Analisis sidik ragam kecerahan (L) tahu yang diawetkan
dengan cuka pasar hari ke-3 ... 97 Lampiran 59. Analisis sidik ragam warna merah (a) tahu yang diawetkan
dengan asam asetat glasial hari ke-1 ... 98 Lampiran 60. Analisis sidik ragam warna merah (a) tahu yang diawetkan
dengan asam asetat glasial hari ke-2 ... 99 Lampiran 61. Analisis sidik ragam warna merah (a) tahu yang diawetkan
dengan asam asetat glasial hari ke-3 ... 99 Lampiran 62. Analisis sidik ragam warna merah (a) tahu yang diawetkan
dengan cuka pasar hari ke-1 ... 100 Lampiran 63. Analisis sidik ragam warna merah (a) tahu yang diawetkan
dengan cuka pasar hari ke-2 ... 101 Lampiran 64. Analisis sidik ragam warna merah (a) tahu yang diawetkan
Lampiran 65. Analisis sidik ragam warna kuning (b) tahu yang diawetkan
dengan asam asetat glasial hari ke-1 ... 102
Lampiran 66. Analisis sidik ragam warna kuning (b) tahu yang diawetkan dengan asam asetat glasial hari ke-2 ... 102
Lampiran 67. Analisis sidik ragam warna kuning (b) tahu yang diawetkan dengan asam asetat glasial hari ke-3 ... 103
Lampiran 68. Analisis sidik ragam warna kuning (b) tahu yang diawetkan dengan cuka pasar hari ke-1 ... 103
Lampiran 69. Analisis sidik ragam warna kuning (b) tahu yang diawetkan dengan cuka pasar hari ke-2 ... 104
Lampiran 70. Analisis sidik ragam warna kuning (b) tahu yang diawetkan dengan cuka pasar hari ke-3 ... 104
Lampiran 71. Form Kuisioner Uji Hedonik ... 105
Lampiran 72. Respon panelis terhadap aroma tahu yang telah diawetkan .. 106
Lampiran 73. Respon panelis terhadap rasa tahu yang telah diawetkan ... 107
Lampiran 74. Analisis sidik ragam uji hedonik terhadap atribut aroma ... 108
Lampiran 75. Analisis sidik ragam uji hedonik terhadap atribut rasa ... 109
Lampiran 76. Daftar harga pengawet ... 110
Lampiran 77. Biaya pengawetan tahu pada penelitian pendahuluan ... 110
Lampiran 78. Biaya pengawetan tahu pada penelitian utama ... 111
Lampiran 79. Biaya pengawetan tahu dengan menggunakan formalin ... 111
Lampiran 80. Penentuan waktu optimum untuk pencelupan tahu (pada formula asetat 5%) ……… 112
Laampiran 81. Penentuan jumlah celupan dalam setiap larutan asam organik yang dipakai ... 112
I. PENDAHULUAN
A. LATAR BELAKANG
Penggunaan berbagai macam pengawet sintetis yang berbahaya,seperti formalin telah berkembang luas di setiap daerah di Indonesia. Konsumsi produk pangan yang mengandung formalin dapat menimbulkan gangguan kesehatan yang berbahaya. Efek terburuk dari mengkonsumsi formalin dalam produk pangan adalah timbulnya kanker, salah satu faktor utama penyebab kematian tertinggi di dunia.
Salah satu produk makanan yang sering diawetkan dengan menggunakan formalin adalah tahu. Tahu merupakan produk pangan yang cepat mengalami kerusakan karena memiliki kandungan air yang cukup tinggi. Tahu yang dibiarkan pada udara terbuka tanpa mendapat perlakuan pengawetan apapun hanya dapat bertahan selama 10 jam.
Menurut Undang Undang RI No. 7 Tahun 1996 tentang Pangan, pada Bab II mengenai Keamanan Pangan, Pasal 10 tentang Bahan Tambahan Makanan menyatakan bahwa (1) setiap orang yang memproduksi pangan untuk diedarkan dilarang menggunakan bahan apapun sebagai bahan tambahan pangan yang dinyatakan terlarang atau melampaui ambang batas maksimal yang telah ditetapkan, (2) pemerintah menetapkan lebih lanjut bahan yang dilarang dan atau dapat digunakan sebagai bahan tambahan pangan dalam kegiatan atau proses produksi pangan serta ambang batas maksimal sebagaimana pada ayat (1).
Tahu memiliki komposisi asam amino terlengkap dibandingkan dengan produk olahan kedelai lainnya sehingga memiliki nilai gizi yang baik. Di samping itu, banyak masayarakat mengkonsumsi tahu karena tahu tergolong ke dalam produk yang murah (Rp. 4.600,00/kg).
Permasalahan inilah yang menuntut untuk dicarikannya solusi mengenai pengawet alami seperti asam organik untuk diterapkan sebagai pengawet namun aman dikonsumsi oleh manusia dan tidak mempunyai efek samping
terhadap kesehatan. Asam organik yang digunakan sebagai pengawet bahan makanan dapat mempunyai daya kerja menurunkan pH dan mencegah pertumbuhan mikroorganisme yang ada.
Metode yang digunakan untuk mengawetkan tahu dengan menggunakan asam organik cukup sederhana. Tahu yang akan diawetkan cukup dicelupkan ke dalam larutan asam organik kemudian disimpan pada suhu ruang dengan menggunakan plastik HDPE yang dirapatkan dengan sealer.
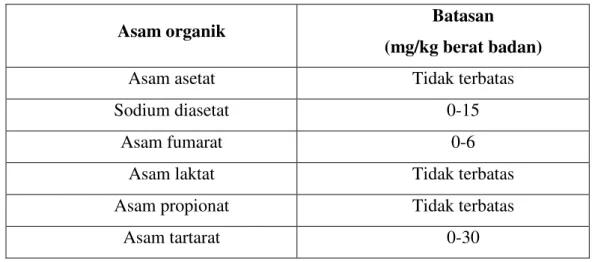
Asam organik tidak memiliki efek negatif terhadap kesehatan. Senyawa ini tidak memiliki batasan maksimal dalam penggunaannya seperti terlihat pada Tabel 1.
Tabel 1. Jumlah batasan maksimal asam organik yang dapat dimakan per hari
oleh manusia
Asam organik Batasan
(mg/kg berat badan)
Asam asetat Tidak terbatas
Sodium diasetat 0-15
Asam fumarat 0-6
Asam laktat Tidak terbatas
Asam propionat Tidak terbatas
Asam tartarat 0-30
Sumber : (Doores, 1993)
Produsen tahu sendiri menginginkan peningkatan umur simpan tahu minimal selama 2 hari sehingga dapat meningkatkan nilai ekonomisnya. Tahu yang memiliki umur simpan yang relatif lebih lama dapat didistribusikan ke tempat yang lebih jauh, sehingga pangsa pasar yang dapat dijangkau semakin luas.
B. TUJUAN
1. Mempelajari pengaruh penggunaan asam organik terhadap mutu sensori dan umur simpan tahu.
2. Penggunaan asam organik pada tahu mampu diaplikasikan secara nyata dengan biaya yang relatif rendah.
C. INDIKATOR KEBERHASILAN PENELITIAN
1. Penggunaan asam organik mampu mempertahankan mutu tahu pada penyimpanan suhu ruang minimal selama 2 hari.
2. Penggunaan asam organik pada tahu mampu menghasilkan nilai penerimaan konsumen pada analisis sensori (uji hedonik) sebesar 5 dari 7 skala nilai.
D. MANFAAT
Penelitian ini memiliki manfaat yang dapat diaplikasikan secara langsung oleh para produsen pangan khususnya produsen tahu sehingga dapat meningkatkan kualitas keawetan dari produknya tanpa membahayakan kesehatan konsumen.
II. TINJAUAN PUSTAKA
A. TAHU
Tahu merupakan makanan tradisional yang sudah lama dikenal di Indonesia dan memegang peranan penting dalam pola makanan sehari-hari masyarakat Indonesia pada umumnya, baik sebagai lauk maupun sebagai makanan tambahan. Shurleff dan Aoyagi (1975) menyatakan bahwa tahu adalah gumpalan protein dari susu kedelai sesudah dipisahkan dari air tahu (whey) dengan cara pengepresan. Sedangkan Hardjo (1964) menyatakan bahwa tahu merupakan hasil pengendapan suatu larutan kental yang mengandung protein terdispersi yang berasal dari kedelai.
Tahu merupakan makanan yang menyehatkan dan mengandung zat-zat yang dibutuhkan untuk memperbaiki gizi. Kedelai mengandung protein, karbohidrat, lemak, dan zat-zat mineral. Menurut pengamatan Kastyanto (1990), satu kilogram kedelai mengandung kurang lebih 300-400 gram protein (40%), karbohidrat 200-350 gram (35%) dan minyak atau lemak 150-200 gram (20%). Tahu mempunyai kadar protein antara 8-12% (Lembaga Kimia Nasional, 1984) dengan mutu protein, yang dinyatakan sebagai NPU, sebesar 65.
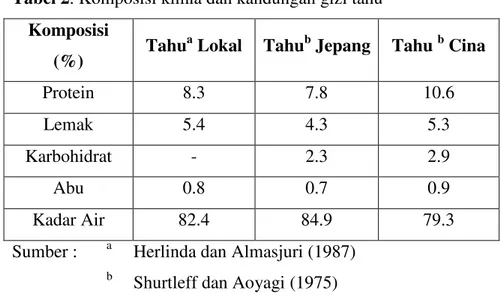
Ditinjau dari komposisi kimia dan kandungan gizinya, tahu mengandung kalori, air, lemak, dan lain sebagainya, yang dapat dilihat pada Tabel 2 berikut.
Tabel 2. Komposisi kimia dan kandungan gizi tahu Komposisi
(%) Tahu
a
Lokal Tahub Jepang Tahu b Cina
Protein 8.3 7.8 10.6
Lemak 5.4 4.3 5.3
Karbohidrat - 2.3 2.9
Abu 0.8 0.7 0.9
Kadar Air 82.4 84.9 79.3
Sumber : a Herlinda dan Almasjuri (1987)
b
Shurtleff dan Aoyagi (1975)
Tahu yang masih segar harus memenuhi kriteria sesuai dengan standar yang ditetapkan oleh SNI seperti terlihat pada Tabel 3.
Tabel 3. Kriteria mutu tahu
Parameter Satuan Persyaratan
Bau - Normal tahu
Rasa - Normal tahu
Warna
- Putih normal atau kuning
normal Penampakan
- Normal tidak berlendir
dan tidak berjamur Cemaran Mikroba :
Angka lempeng total Koloni/g 1.0 x 106
Escherichia coli Angka paling mungkin/g <3
Salmonella koloni/g Negatif/25g Sumber : (SNI 01-3142-1992)
B. KERUSAKAN TAHU
Tahu termasuk bahan pangan yang cepat rusak sehingga dapat digolongkan ke dalam golongan high perishable food (Shurtleff dan Aoyagi, 1975). Tahu banyak mengandung air, protein, lemak, karbohidrat, vitamin, dan mineral sehingga menjadikannya sebagai media yang cocok sebagai tempat tumbuh mikroba.
Secara organoleptik, tanda-tanda yang dapat diamati untuk mengetahui telah terjadinya kerusakan tahu antara lain timbul bau masam sampai busuk, permukaan tahu berlendir, warna dan penampakan menjadi tidak cerah, serta kadang-kadang berjamur pada permukaannya.
Kerusakan tahu memiliki kaitan yang erat dengan aktivitas mikroorganisme. Menurut Frazier dan Westhoff (1978), mikroorganisme penyebab kerusakan pada bahan pangan berkadar air tinggi dengan pH sekitar netral terutama adalah golongan bakteri. Shurleff dan Aoyagi (1975) menyatakan bahwa penyebab utama kerusakan tahu adalah bakteri. Kerusakan mikrobiologis tahu tergantung dari beberapa faktor, antara lain adanya bakteri tahan panas seperti golongan pembentuk spora dan termodurik, adanya bakteri kontaminan yang mengkontaminasi tahu selama proses pembuatan sampai tahu siap dikonsumsi, suhu penyimpanan, adanya enzim tahan panas yang dihasilkan oleh golongan bakteri tertentu (Shurleff dan Aoyagi, 1975).
Komposisi suatu bahan pangan sangat menentukan jenis
mikroorganisme yang dapat tumbuh dengan baik pada bahan pangan tersebut. Menurut Frazier dan Westhoff (1978), beberapa golongan bakteri yang dapat tumbuh baik pada bahan pangan yang banyak mengandung protein, kadar air tinggi dengan pH netral antara lain : golongan bakteri proteoloitik, bakteri asam laktat, dan golongan termodurik, seperti Micrococcus, Bacillus, dan Brevibakteria.
Penyimpanan tahu pada suhu rendah (15oC) hanya dapat mempertahankan kesegaran tahu selama 1-2 hari (Datson et al., 1977). Tahu yang direndam di dalam air yang diganti setiap hari pada suhu kamar telah menjadi busuk selama 1.5 hari (Pontecarvo dan Bourne, 1978). Sedangkan
tahu yang dibiarkan pada udara terbuka tanpa perendaman di dalam air pada suhu kamar hanya tahan sekitar 10 jam.
Koagulan merupakan bahan yang digunakan untuk mendenaturasi protein didalam susu kedelai sehingga dihasilkan curd (gumpalan tahu). Jenis koagulan yangdigunakan antara lain kalsium/magnesium-klorida; kalsium sulfat; glukano-D-laktone; dan koagulan asam (asam laktat, asam asetat). Kalsium/magnesium-klorida akan menghasilkan tahu dengan flavor sangat baik; pembentukan curd cepat tetapi daya ikat airnya rendah sehingga rendemen yang diperoleh kecil dan tekstur tahu cenderung kasar. Kalsium sulfat merupakan koagulan yang paling umum digunakan. Koagulan ini kelarutannya didalam air lambat sehingga pembentukan curd juga berlangsung lambat. Daya ikat airnya tinggi, sehingga rendemen tahu yang dihasilkan akan lebih banyak daripada Ca/Mg-klorida dan tekstur tahunya halus. Glukano-D-laktone merupakan koagulan asam, memiliki daya ikat air yang tinggi, dan membentuk tahu dengan tekstur seperti gel dan flavor sedikit asam. Koagulan ini biasa digunakan untuk membuat tahu sutra. Sementara itu, koagulan asam (asam laktat, asam asetat) memberikan rendemen yang rendah, dengan tekstur tahu yang rapuh (mudah hancur) dan flavor agak asam (Syamsir, 2008)
Batu tahu (CaSO4) paling umum digunakan untuk menggumpalkan dan sering digunakan berdasarkan perkiraan saja, dimana batu tahu diencerkan dalam air secukupnya lalu ditambahkan ke dalam susu kedelai sampai menggumpal dan penggunaan batu tahu dihentikan. Penambahan batu tahu akan menyebabkan terjadinya koagulasi. Hal ini disebabkan oleh ion Ca++ yang bereaksi dan berikatan dengan protein susu kedelai dan bersama lipid membentuk gumpalan (Santoso,1993).
Disamping sebagai zat penggumpal, asam cuka juga berperan sebagai pengawet dimana asam akan menurunkan pH bahan pangan sehingga dapat menghambat pertumbuhan bakteri pembusuk dan jumlah asam yang cukup akan menyebabkan denaturasi protein bakteri. Asam cuka juga dapat berfungsi untuk menambah cita rasa, mengurangi rasa manis dan dapat pula memperbaiki tekstur (Winarno dan Rahman, 1974).
Jenis zat penggumpal batu tahu menghasilkan kadar protein, kadar air, pH, rasa-aroma dan tekstur yang lebih tinggi daripada jenis zat penggumpal asam cuka. Nilai pH yang lebih rendah dijumpai pada perlakuan jenis zat penggumpal asam cuka. Nilai tekstur tahu yang lebih tinggi dijumpai pada penggunaan jenis zat penggumpal batu tahu. Menurut Lee dan Rha (1979), tahu yang digumpalkan dengan batu tahu lebih lunak, rendemen lebih tinggi, daya pegang air lebih tinggi bila dibandingkan dengan tahu yang digumpalkan dengan asam cuka, hal ini disebabkan penggumpalan dengan batu tahu membuat pH dari larutan tidak terlalu asam sehingga proses penggumpalan lebih baik.
C. ASAM ORGANIK
Asam organik dapat dihasilkan secara alami oleh tumbuhan maupun hewan. Beragam jenis asam organik antara lain asam sitrat, asam sorbat, dan asam benzoat ditemukan pada buah-buahan, sedangkan pada daging ditemukan asam laktat. Asam organik yang digunakan sebagai pengawet bahan makanan seperti asam sitrat dapat mempunyai daya kerja menurunkan pH dan mencegah pertumbuhan mikroorganisme yang ada. Pemberian asam organik diharapkan dapat memperpanjang masa simpan dan mencegah kerusakan bahan pangan tersebut (Ray dan sandine, 1992).
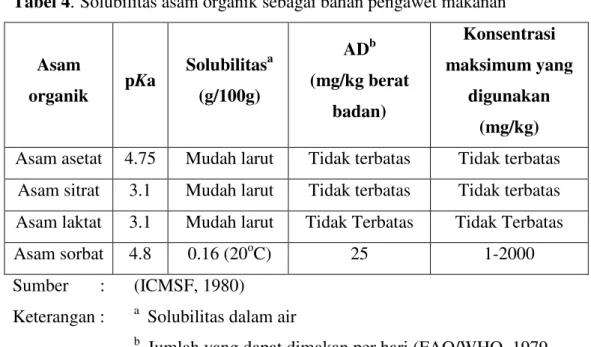
Pemilihan jenis asam organik yang digunakan sebagai pengawet bahan makanan didasarkan atas daya kelarutannya, rasa asam yang ditimbulkan pada bahan pangan, dan keamanan penggunaannya. Asam organik kebanyakan mudah larut dalam air, sebagaimana ditunjukkan pada Tabel 4. Menurut FAO/WHO (ICMSF, 1980), sampai saat ini asam organik merupakan bahan pengawet makanan yang dianggap aman. Ada bermacam-macam asam organik yang dapat digunakan sebagai antimikrobial bahan pangan seperti asam asetat, asam laktat, asam propionat, dan asam sitrat (Rahman, 1999). Menurut Rahman (1999) dan Doores (1993), asam organik lipofilik, seperti asam asetat, asam propionat, dan asam benzoat sering digunakan sebagai antimikrobial bahan makanan
Tabel 4. Solubilitas asam organik sebagai bahan pengawet makanan Asam organik pKa Solubilitasa (g/100g) ADb (mg/kg berat badan) Konsentrasi maksimum yang digunakan (mg/kg)
Asam asetat 4.75 Mudah larut Tidak terbatas Tidak terbatas Asam sitrat 3.1 Mudah larut Tidak terbatas Tidak terbatas Asam laktat 3.1 Mudah larut Tidak Terbatas Tidak Terbatas
Asam sorbat 4.8 0.16 (20oC) 25 1-2000
Sumber : (ICMSF, 1980)
Keterangan : a Solubilitas dalam air
b
Jumlah yang dapat dimakan per hari (FAO/WHO, 1979
Asam asetat (CH3COOH) merupakan asam organik monokarbonik,
memiliki bau dan rasa tajam, bersifat sangat mudah larut dalam air. Asam asetat aman digunakan sebagai bahan pengawet produk makanan dan tidak ada batasan maksimal yang boleh dikonsumsi oleh manusia. Doores (1993) melaporkan bahwa efektifitas asam asetat antara pH 4 sampai 6. Asam laktat (CH3CHOHCOOH) berbentuk cair, bersifat higroskopis dan merupakan hasil
fermentasi sucrosa oleh Lactobacillus sp., dan tersedia dalam bentuk cairan kental dengan rasa asam yang kuat (Budavari et al., 1996).
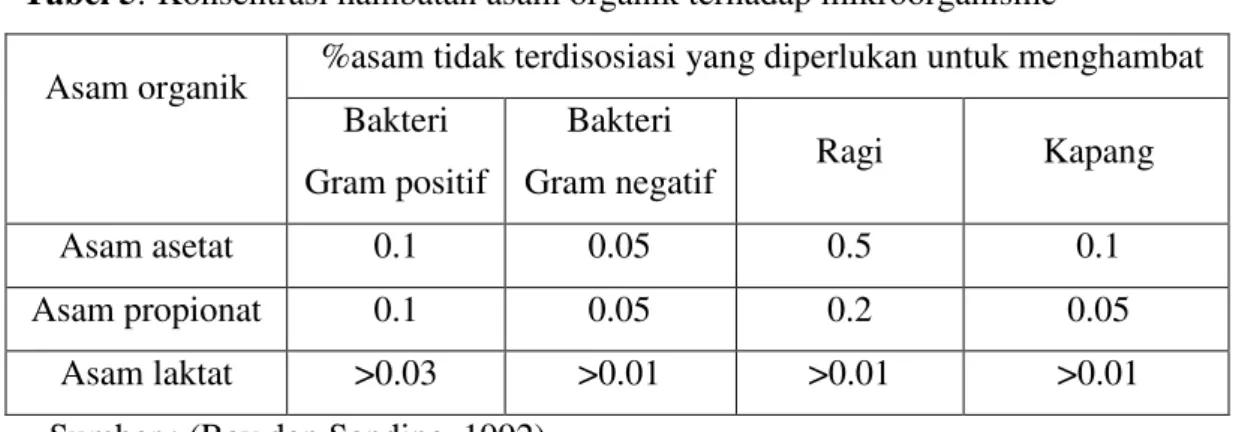
Persentase asam asetat yang tidak terdisosiasi sebanyak 1% sampai 2% pada daging, ikan, dan sayuran mampu menghambat dan membunuh mikroorganisme. Pertumbuhan bakteri berspora dan penghasil toksin dalam makanan dihambat 0.1%, sedangkan pertumbuhan jamur penghasil mikotoksin dihambat 0.3% dari asam, seperti terlihat pada Tabel 5.
Tabel 5. Konsentrasi hambatan asam organik terhadap mikroorganisme
%asam tidak terdisosiasi yang diperlukan untuk menghambat Asam organik
Bakteri Gram positif
Bakteri
Gram negatif Ragi Kapang
Asam asetat 0.1 0.05 0.5 0.1
Asam propionat 0.1 0.05 0.2 0.05
Asam laktat >0.03 >0.01 >0.01 >0.01
Sumber : (Ray dan Sandine, 1992)
Penambahan asam laktat tergantung pada konsentrasi dan pH, untuk memberikan efek bakteriostatik dan bakteriosid pada media pertumbuhan mikroorganisme. Asam laktat mampu menghambat bakteri berspora pada pH 5, tetapi tidak efektif untuk menghambat cendawan. Pada pH lebih dari 5, asam laktat memiliki efek antibakterial yang sangat terbatas. Telah dilaporkan bahwa asam laktat mampu menambah citarasa dan bau pada daging dengan menggunakan 1% sampai 2% apabila ditambahkan garam (Ray dan Sandine, 1992; Doores, 1993).
D. MEKANISME PENGAWETAN ASAM ORGANIK
Kemampuan antimikrobial suatu asam organik tergantung pada tiga faktor, antara lain: efek dari kemampuan asam tersebut dalam menurunkan pH, kemampuan asam untuk berdisosiasi, dan efek spesifik yang berhubungan dengan molekul asam itu sendiri (Smulders, 1995). Pemilihan jenis asam organik yang digunakan sebagai pengawet bahan makanan didasarkan atas daya kelarutannya, rasa asam yang ditimbulkan pada bahan pangan, dan tingkat toksisitasnya.
Aktivitas antimikrobial asam organik ditentukan oleh besarnya persentase molekul asam yang tidak terurai (undissociated), yang ditetapkan dengan nilai pKa. Bahan makanan yang memiliki pH rendah, banyaknya persentase molekul asam organik yang tidak terurai meningkat, sehingga
kemampuan sebagai antimikrobial juga akan meningkat. Nilai pKa adalah nilai dimana 50% total asam merupakan bentuk yang tidak terurai.
Asam organik yang memiliki pKa lebih tinggi maka banyaknya molekul yang tidak terdisosiasi dalam larutan lebih banyak, sehingga pH larutan menjadi asam. Oleh karena itu, proton yang jumlahnya lebih banyak akan masuk ke dalam sitoplasma sel mikroorganisme. Untuk mencegah terjadinya penurunan pH dan denaturasi di dalam sel, proton-proton yang berada di dalam sel berusaha dikeluarkan oleh sel mikroorganisme. Pertumbuhan sel mikroorganisme menjadi lebih lambat bahkan berhenti sama sekali karena dibutuhkan energi untuk mengeluarkan proton dari dalam sel. (Eklund, 1989; Fardiaz, 1989).
Asam asetat merupakan kelompok asam lemah. Meskipun demikian, asam ini memiliki kemampuan untuk meracuni mikroba. Mekanisme asam asetat dalam menginaktivasi bakteri adalah sebagai berikut :
Asam lemah dapat terurai seperti ini : R-COOH → RCOO- + H+. Asam yang terurai membuat ion H+ yang terbentuk semakin banyak. Pada larutan asam lemah, adanya ion H+ dalam jumlah banyak, akan membuat kesetimbangan reaksi bergeser ke kiri menuju bentuk yang tidak terurai (R-COOH). Bentuk yang tidak terurai ini dapat larut dalam lemak sehingga memungkinkannya masuk menembus membran sel yang sebagian besar terdiri dari posfolipid dan lemak. Banyaknya larutan asam asetat membuat semakin banyak bentuk tidak terurai yang masuk ke dalam sel. Di dalam sel yang memiliki kondisi pH netral, R-COOH dapat terurai menjadi RCOO- dan H+. Banyaknya ion H+ yang terbentuk membuat pH di dalam sel menjadi turun. Penurunan pH ini dapat menyebabkan sel mati karena aktifitas enzim dan asam nukleatnya terganggu (Garbutt, 1997).
E. METODE PENGAWETAN PANGAN DENGAN PENCELUPAN
Pengawetan produk pangan ditujukan untuk memperpanjang umur simpan suatu makanan dan dalam hal ini dengan jalan menghambat pertumbuhan mikroba.Salah satu metode untuk mengawetkan produk pangan
yaitu pencelupan ke dalam larutan pengawet. Metode pencelupan sangat umum dilakukan pada produk pangan khususnya produk yang memiliki permukaan yang lebih luas. Hal ini ditujukan agar bahan pengawet dapat membunuh sejumlah besar mikroba yang tumbuh pada permukaan produk pangan selain itu juga memudahkan bahan pengawet untuk berdifusi ke dalam produk pangan. Hal yang harus diperhatikan dalam mengawetkan produk pangan dengan metode pencelupan adalah waktu pencelupan yang optimal. Penentuan waktu pencelupan didasarkan pada karakteristik masing-masing produk pangan.
Pengawetan produk tahu dengan proses pencelupan sudah dilakukan oleh peneliti sebelumnya dengan menggunakan bahan pengawet yang berbeda, seperti terlihat pada Tabel 6.
Tabel 6. Pengawetan tahu dengan metode pencelupan
Perlakuan Pengawetan Umur Simpan (suhu kamar) Sumber
Asam benzoat 1000 ppm, 72 jam Saputra (2006)
Metil parabens 1000 ppm 72 jam Saputra (2006)
Kalium sorbat 1000 ppm 48 jam Saputra (2006)
Perendaman dalam
formalin 0.1-0.15% selama semalam
3 minggu Winarno dan Rahayu
(1994)
F. PENGEMASAN
Pengemasan merupakan suatu cara dalam memberikan kondisi lingkungan atau sekeliling yang tepat bagi bahan pangan dengan demikian memerlukan pemikiran dan perhatian yang lebih besar daripada biasanya diketahui (Buckle, 1985). Fungsi dari pengemasan adalah untuk mempertahankan agar bahan pangan tetap bersih dan memberikan perlindungan terhadap kotoran dan pencemaran lainnya (mikroba) dan memberikan perlindungan terhadap kerusakan fisik, oksigen, sinar, sehingga bahan yang dikemas memiliki umur simpan yang lebih lama.
Pada penelitian ini, tahu yang sudah dicelup kemudian dimasukan ke dalam plastik HDPE dan ditutup rapat (sealing). Maksud dari kegiatan sealing ini adalah agar tidak ada mikroba kontaminan yang dapat masuk dan mencemari bahan pangan, serta untuk mencegah oksigen maksud sehingga tidak terjadi reaksi oksidasi.
Beberapa keuntungan dalam penggunaan kemasan plastik adalah dapat melindungi isi dengan baik, ringan sehingga menurunkan biaya transportasi, tidak mudah pecah sehingga mengurangi faktor resiko dan kerugian selama penyimpanan dan transportasi, dapat dibuat dalam berbagai macam bentuk sesuai dengan selera, tidak korosif serta tahan terhadap beberapa bahan kimia.
Polyethilen (PE) merupakan jenis plastik yang banyak digunakan dalam industri karena sifat-sifatnya yang mudah dibentuk, serta cukup tahan terhadap berbagai bahan kimia. PE merupakan polimer etilen dan berdasarkan densitasnya (gram/cm3) dikenal 3 jenis PE yaitu LDPE, MDPE, dan HDPE.
III. METODE PENELITIAN
A. BAHAN DAN ALAT
Bahan-bahan yang digunakan dalam penelitian ini adalah tahu putih dengan dimensi 4 x 4 x 2 cm dan berat 70 g, asam asetat glasial, cuka pasar, dan asam laktat. Bahan-bahan yang digunakan untuk uji mikrobiologi yaitu PCA (Plate Count Agar), larutan pengencer, dan alkohol 70%. Bahan–bahan yang digunakan untuk analisis total asam tertitrasi adalah NaOH 0,1 ml, kalium pthalat, indikator phenoftalein. Alat yang digunakan dalam penelitian ini adalah baskom, pisau, pengaduk, dan plastik HDPE. Alat-alat yag digunakan dalam analisis adalah pH meter, stomacher, bunsen, inkubator, buret, erlenmeyer, gelas piala, Chromameter, Texture Analyzer, cawan petri, mikro pipet, tabung pengencer, dan labu takar.
B. METODE PENELITIAN
1. Penelitian Pendahuluan
Penelitian pendahuluan dilakukan untuk mencari dan mendapatkan jenis dan konsentrasi larutan pengawet asam organik (asam laktat, asam asetat, dan kombinasi asam asetat-laktat) yang efektif untuk tahu sehingga memiliki umur simpan minimal 2 hari dalam suhu ruang. Perlakuan yang diberikan yaitu sebagai berikut.
a. Waktu pencelupan optimal
b. Jumlah celupan tahu ke dalam larutan asam organik c. Jenis Pengawet
Jenis pengawet yang digunakan adalah asam laktat, asam asetat, dan kombinasi asam asetat-laktat
d. Konsentrasi Larutan Pengawet yang digunakan e. Perbandingan antara Asam Laktat dan Asam Asetat
Formulasi larutan pengawet asam organik yang dipakai pada penelitian pendahuluan ini dapat dilihat pada Tabel 7.
Tabel 7. Formulasi konsentrasi larutan pengawet asam organik pada tahap
penelitian pendahuluan
Formula Konsentrasi
Formula 1 (X) Asam Asetat 5 %
Formula 2 (Y) Asam Laktat 10 %
Formula 3 (Z) 2/3 Asam Asetat 5 % + 1/3 Asam Laktat 10 %
Pemilihan asam asetat dan laktat sebagai pengawet didasarkan pada kemampuan asam organik tersebut dalam menghambat pertumbuhan mikroba lebih baik dibandingkan jenis asam organik yang lain. Hal tersebut dapat dilihat dari nilai pKa dari kedua jenis asam organik tersebut paling tinggi di antara yag lain (Tabel 5). Pemilihan konsentrasi 5% pada asam asetat karena pada konsentrasi 4% saja asam asetat mampu menghambat pertumbuhan mikroba Salmonella dan sthaphylococcus (Furia, 1972). Apabila konsentrasi ditingkatkan menjadi lebih dari 5%, maka dikhawatirkan akan terjadi hidrolisis protein oleh asam sehingga menyebabkan tekstur tahu menjadi lunak, begitu pula dengan pemilihan konsentrasi 10% pada asam laktat.
Pengamatan yang dilakukan pada penelitian pendahuluan antara lain pengamatan total mikroba, pH, dan total asam tertitrasi. Formulasi asam organik yang memiliki nilai total mikroba, pH, dan total asam tertitrasi terbaik kemudian digunakan pada penelitian utama.
2. Penelitian Utama
Pada tahap penelitian utama ini, dilakukan pencelupan bahan pangan tahu dalam formulasi larutan pengawet asam organik terbaik yang telah dihasilkan pada penelitian pendahuluan (selama 1 menit). Asam organik yang dipakai pada penelitian utama ini adalah jenis asam asetat
glasial dan cuka pasar. Tahu yang sudah dicelup kemudian dikemas dalam plastik HDPE yang dirapatkan dengan menggunakan sealer. Penyimpanan dilakukan pada suhu ruang. Pengamatan dilakukan setiap hari untuk uji total mikroba, total asam tertitrasi, pH, warna, dan tekstur.
C. PERLAKUAN
1. Jenis Pengawet Asam Organik
K : Sampel tahu sebagai kontrol, tidak mendapat perlakuan pencelupan
ke dalam pengawet asam organik.
A : Pencelupan (coating) sampel tahu pada larutan asam asetat glasial. B : Pencelupan (coating) sampel tahu pada larutan asam cuka pasar.
2. Konsentrasi Pengawet Asam Organik
A0 : Tahu dengan asam asetat glasial 0 % (kontrol)
A1 : Pencelupan (coating) sampel tahu pada larutan asam asetat glasial 2%
A2 : Pencelupan (coating) sampel tahu pada larutan asam asetat glasial 2.5%
A3 : Pencelupan (coating) sampel tahu pada larutan asam asetat glasial 3%
B0 : Tahu dengan cuka pasar 0 % (kontrol)
B1 : Pencelupan (coating) sampel tahu pada larutan asam cuka pasar 2%
B2 : Pencelupan (coating) sampel tahu pada larutan asam cuka pasar 2.5%
3. Kondisi Pengemasan
Penyimpanan tahu dilakukan pada kondisi suhu ruang selama maksimal 15 hari dengan menggunakan kemasan plastik HDPE untuk melihat tingkat efektifitas dari masing-masing formula larutan pengawet dalam mengawetkan bahan pangan tersebut.
D. PENGAMATAN
1. Total Asam Tertitrasi (Apriyantono et al., 1989)
Sebanyak 10 gram sampel ditambahkan sedikit air, kemudian dihancurkan sampai menjadi bubur. Setelah itu, campuran dipanaskan sampai mendidih dan dipindahkan ke dalam labu takar 100 ml. Selanjutnya, ditambahkan akuades sampai tanda tera. Kemudian diambil 25 ml larutan dan ditambahkan indikator fenolftalein 3 tetes. Larutan kemudian dititrasi dengan NaOH 0.01 N sampai terbentuk warna merah muda yang merupakan titik akhir titrasi.
2. Total Mikroba (Fardiaz, 1992)
Sebanyak 10 gram sampel yang ditimbang secara aseptik dimasukkan ke dalam plastik stomacher steril. Kemudian ditambahkan 90 ml larutan pengencer fisiologis (NaCl) lalu dihancurkan selama 1 menit. Sampel yang telah dihancurkan dengan stomacher kemudian dilakukan pengenceran hingga 10-4 dan dilakukan pemupukan duplo 10-4 dan 10-5.
Media PCA cair kemudian ditambahkan untuk menguji total mikroba dan dibiarkan hingga media membeku. Setelah membeku, diinkubasikan pada suhu 30oC selama 2 hari dengan posisi terbalik. Setelah waktu inkubasi selesai, dihitung koloni total dengan metode Harrigan seperti di bawah ini:
Batas koloni yang dihitung : 25 – 250 cfu
Keterangan :
N : Total koloni per ml atau gram sampel
C : Jumlah koloni dari semua cawan yang masuk batas perhitungan n1 : Jumlah cawan pada pengenceran pertama
n2 : Jumlah cawan pada pengenceran kedua
d : Tingkat pengenceran pertama saat mulai perhitungan
3. Pendugaan Umur Simpan secara Visual
Sampel tahu diamati secara visual dan dilakukan penilaian setiap hari pengamatan. Parameter-parameter yang menunjukkan mutu tahu yang buruk adalah (1) adanya lendir, (2) teksturnya lunak, (3) adanya kapang, dan (4) berbau asam. Penilaian kriteria mutu sensoris tahu mengacu pada Tabel 8 yang merupakan hasil dari pengamatan 5 orang panelis.
Tabel 8. Penilaian mutu sensori tahu
Parameter Nilai
Penampakan Warna Bau Rasa Tekstur
2 Permukaan halus
tanpa lendir Putih cerah
Khas tahu segar (++++) Normal tahu Kompak dan kenyal 1 Mulai berlendir (+) Putih kusam Sedikit asam (+++) Agak hambar Mulai lunak dan lengket (+) 0 Berlendir (++) Abu-abu kusam Bau asam dan basi Tidak enak dan sangat masam Rapuh, basah, dan lengket (++) N = C [(1 * n1) + (0.1 * n2)] * d
Keterangan : +++++ Sangat banyak ++++ Lebih banyak
+++ Cukup
++ Lebih sedikit
+ Sangat sedikit
4. Uji Organoleptik (Soekarto, 1985)
Pengujian organoleptik tahu mencakupi 2 macam atribut sensori, yaitu pengujian terhadap rasa dan aroma. Uji yang dilakukan adalah uji kesukaan (hedonik). Sampel tahu yang dipergunakan adalah sampel terbaik berdasarkan uji mikrobiolgis, pH, dan TAT sebelumnya. Sampel tahu yang diuji merupakan tahu yang sudah mengalami proses pengolahan (penggorengan). Pengujian ini dilakukan oleh 30 orang panelis. Skala hedonik yang digunakan terdiri dari 7 titik dengan urutan menaik menurut tingkat kesukaan seperti terlihat pada Tabel 9 sebagai berikut :
Tabel 9. Skala pengukuran uji hedonik
Skor Penilaian
1 Sangat Tidak suka
2 Tidak suka
3 Agak tidak suka
4 Biasa
5 Agak Suka
6 Suka
7 Sangat Tidak suka
5. pH (Apriyantono et al., 1989)
Nilai pH tahu diukur setiap hari dengan menggunakan pH meter. pH meter dikalibrasi terlebih dahulu menggunakan buffer pH 4 dan 7. Sampel tahu yang akan dianalisis, ditimbang sebanyak 1 gram dan dicampur
dengan akuades sebanyak 10 ml. Campuran ini dihancurkan selama 1 menit, setelah campuran merata baru dilakukan pengukuran pH.
6. Intensitas Warna (Pomeranz, et al., 1978)
Intensitas warna diukur dengan menggunakan kromameter CR-200 merek “Minolta”. Pada kromameter ini digunakan sistem warna L, a, b. L menunjukkan kecerahan, a dan b adalah koordinat-koordinat kromatis dimana a untuk warna hijau (a negative) ke merah (a positif) dan b untuk biru (b negative) sampai kuning (b positif).
Sebelum dilakukan pengukuran terhadap tahu, kromameter CR-200 dikalibrasi terlebih dahulu dengan menggunakan Calibration Plate dengan L = 47.49 ; a = 41.49 ; b = 18.36. Setelah alat dikalibrasi, tahu dianalisis dengan diukur tingkat kecerahannya serta intensitas warna merah dan kuning dari masing-masing produk. Pengukuran tiap produk dilakukan sebanyak 2 kali.
7. Tekstur
Prinsip pengukuran bahan pangan dengan textur analyzer adalah dengan memberikan gaya kepada bahan dengan besaran tertentu sehingga profil tekstur bahan pangan tersebut dapat diukur. Jenis bahan yang dianalisis berpengaruh pada jenis probe yang digunakan. Bila dihubungkan dengan program analisisnya, dapat diketahui profil sampel tersebut saat menerima gaya yang diberikan. Parameter tekstur yang diukur untuk sampel tahu ini adalah kekenyalan.
Langkah pertama adalah menyalakan alat textur analyzer, kemudian memasang probe yang sesuai, lalu melakukan kalibrasi ketinggian probe. Setelah itu, computer dinyalakan untuk menjalankan program textur analyzer. Kemudian kondisi pengukuran diatur. Terakhir, Texture Profile Analysis diukur dengan melakukan dua kali pemberian gaya tekan pada sampel.
8. Uji Statistik
Data hasil penelitian akan diolah secara statistik menggunakan program komputer statistik SPSS 11.0, untuk uji keragaman (ANOVA/ Analysis of Variance) dan Uji Duncan. Uji-uji ini digunakan untuk menarik kesimpulan, apakah sampel atau perlakuan yang diuji berbeda nyata atau tidak dengan kontrol.
9. Analisis Biaya
Analisis biaya dilakukan untuk mengetahui berapa banyak biaya yang diperlukan untuk mengawetkan satu kilogram tahu dengan larutan asam organik. Pengujian terhadap analisis biaya ini dilakukan dengan menghitung selisih volume larutan sebelum pencelupan dengan volume setelah pencelupan. Analisis ini nantinya digunakan untuk mengetahui nilai jual tahu setelah pengawetan.
E. RANCANGAN PERCOBAAN
Rancangan percobaan yang digunakan adalah rancangan faktorial acak lengkap dengan dua faktor yaitu jenis pengawet asam organik dan konsentrasi pengawet asam organik.
Rumus dasarnya :
Y
ijkr= µ + A
i+ B
j+ AB
ij+ ε
ijkrketerangan :
µ
= rata-rata umumAi
= pengaruh perlakuan jenis pengawet asam organik ke-iB
j = pengaruh perlakuan konsentrasi pengawet asam organik ke-jAB
ij = pengaruh interaksi perlakuan jenis pengawet asam organik ke-idan konsentrasi pengawet asam organik ke-j
ε
ijkr = galat percobaan dalam kombinasi perlakuan ijkk
= ulanganIV. HASIL DAN PEMBAHASAN
Tahu termasuk bahan pangan yang cepat rusak sehingga dapat digolongkan ke dalam golongan high perishable food (Shurtleff dan Aoyagi, 1975). Tahu banyak mengandung air, protein, lemak, karbohidrat, vitamin, dan mineral sehingga menjadikannya sebagai media yang cocok sebagai tempat tumbuh mikroba.
Kerusakan tahu memiliki kaitan yang erat dengan aktivitas mikroorganisme. Menurut Frazier dan Westhoff (1978), mikroorganisme penyebab kerusakan pada bahan pangan berkadar air tinggi dengan pH sekitar netral terutama adalah golongan bakteri.
Penyimpanan tahu pada suhu rendah (15oC) hanya dapat mempertahankan umur simpan tahu selama 1-2 hari (Datson et al., 1977). Tahu yang direndam di dalam air yang diganti setiap hari pada suhu kamar telah menjadi busuk selama 1.5 hari (Pontecarvo dan Bourne, 1978). Sedangkan tahu yang dibiarkan pada udara terbuka tanpa perendaman di dalam air pada suhu kamar hanya tahan sekitar 10 jam.
Para pedagang tahu biasanya menggunakan formalin untuk
memperpanjang umur simpan tahu. Takaran yang biasa mereka pakai adalah tiga sendok makan ke dalam 50 liter air untuk 50 kg tahu atau sekitar 250 ppm. Batas konsentrasi formaldehide yang tidak berpengaruh terhadap kesehatan manusia hanyalah sebesar ≤ 0.05 ppm.
Sampel tahu yang diperoleh berasal dari industri tahu yang berlokasi di daerah Cibanteng, Bogor. Tahu yang diperoleh dari industri tidak mengalami penambahan pengawet lainnya karena telah dipesan khusus. Oleh karena itu kondisi tahu masih segar tanpa pengawet. Distribusi tahu dari industri ini ternyata telah mencakupi semua pasar-pasar di daerah Bogor, oleh karena itu sampel diambil dari pabrik ini karena banyak diperjualbelikan di pasar-pasar.
Sampel yang diambil dari produsen tahu tersebut kemudian dibawa menuju tempat penelitian dengan menggunakan box plastik yang tertutup rapat,
dengan terlebih dahulu dibungkus dengan kantung plastik. Hal ini dilakukan agar tidak ada mikroba yang mengkontaminasi tahu selama distribusi, sehingga kondisi mikrobiologis tahu diharapkan tidak berubah pada saat pertama kali diproduksi.
Prosedur kerja yang dilakukan pada penelitian ini adalah pencelupan sampel tahu dalam larutan pengawet asam organik selama ± 1 menit; pengemasan sampel tahu yang telah dicelup dengan plastik HDPE; penyimpanan sampel pada suhu ruang selama maksimal 15 hari; dilakukan analisis sensori, analisis warna, analisis tekstur, pH, total asam tertitrasi, dan analisis mikrobiologi selama masa penyimpanan
A. PENELITIAN PENDAHULUAN
Waktu pencelupan optimum untuk mengawetkan tahu dalam larutan organik adalah 1 menit. Data yang dihasilkan menunjukkan bahwa pencelupan tahu ke dalam larutan asam organik selama lebih dari 1 menit akan menyebabkan perubahan tekstur tahu, dimana tahu akan menjadi semakin lunak karena konsistensi tekstur tahu semakin berkurang, selain itu rasa dan aroma asam timbul sangat menyengat (Lampiran 80).
Jumlah celupan tahu dalam setiap larutan asam organik menunjukkan keefektifan pengawetan sampai celupan maksimum yang memungkinkan. Pada penelitian pendahuluan ini dilakukan uji keefektifan pada larutan asetat 5% untuk mengetahui jumlah celupan maksimum yang masih dapat dilakukan pada larutan tersebut. Hasil yang diperoleh menunjukkan bahwa larutan dapat mempertahankan keefektifannya untuk mengawetkan sampai pada celupan ke-10 (Lampiran 81).
1. pH
Nilai pH tahu selama penyimpanan ternyata bervariasi pada ketiga jenis perlakuan pencelupan asam. Akan tetapi, semua pH dari ketiga perlakuan masih dikatakan asam karena memiliki pH rata-rata masih di
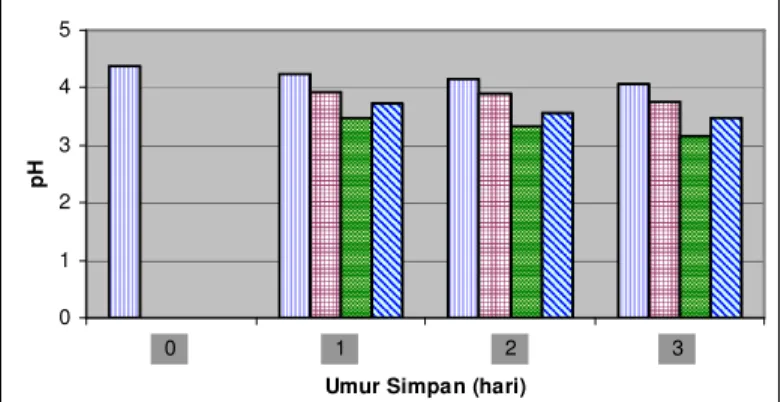
bawah 5. Adapun nilai pH yang terukur pada tahu selama penyimpanan dapat dilihat pada Gambar 1.
0 1 2 3 4 5 1 2 3 4
Umur Simpan (hari)
p
H
kontrol asetat 5%(X) laktat 10%(Y) campuran asetat-laktat(Z)
3 2
1 0
Gambar 1. Nilai pH tahu pada penelitian pendahuluan
Analisis penentuan nilai pH tahu menunjukkan bahwa tahu tanpa perlakuan (kontrol) pada hari 0 memiliki nilai pH 4.37, sedangkan pH kontrol pada penyimpanan hari 1, 2, dan 3 mengalami penurunan menjadi 4.23 ; 4.15 ; dan 4.08. Tahu X mengalami penurunan nilai pH yang relatif kecil pada hari 1, 2, dan 3, yaitu : 3.94 ; 3.89 ; dan 3.77. Tahu Y juga mengalami penurunan nilai pH yang relatif kecil pada hari 1, 2, dan 3 yaitu : 3.47 ; 3.32 ; dan 3.15. Demikian pula pada tahu Z mengalami penurunan nilai pH yang relatif kecil pada hari 1, 2, dan 3 yaitu: 3.73 ; 3.57 ; dan 3.46. Berdasarkan data tersebut, maka dapat disimpulkan bahwa tahu Y memiliki pH yang paling kecil pada setiap hari penyimpanan.
Analisis sidik ragam hari pertama menunjukkan bahwa nilai pH untuk semua perlakuan asam organik (X, Y, dan Z) sama tetapi berbeda dengan kontrol (Lampiran 20). Analisis sidik ragam hari kedua (Lampiran 21) menunjukkan hal yang sama dengan hari pertama. Sedangkan untuk analisis sidik ragam hari ketiga (Lampiran 22) nilai pH bervariasi, dimana terdapat perbedaan antara nilai pH X, Y, dan Z. Nilai pH kontrol pada hari ketiga sama dengan pH X. Dari hasil tersebut dapat disimpulkan bahwa hampir tidak perbedaan nilai pH antar perlakuan pengawet (X, Y, dan Z)
tetapi ketiga nilai pH pengawet tersebut masih berbeda secara nyata dengan kontrol.
Bahan makanan yang memiliki pH rendah, banyaknya persentase molekul asam organik yang tidak terurai meningkat, sehingga kemampuan sebagai antimikrobial juga akan meningkat (ICMSF, 1980). Nilai pKa adalah nilai dimana 50% total asam merupakan bentuk yang tidak terurai. Asam organik yang memiliki pKa lebih tinggi maka banyaknya molekul yang tidak terdisosiasi dalam larutan lebih banyak, sehingga pH larutan menjadi asam. Proton yang jumlahnya lebih banyak akan masuk ke dalam sitoplasma sel mikroorganisme, sehingga untuk mencegah terjadinya penurunan pH dan denaturasi di dalam sel, maka proton-proton yang berada di dalam sel berusaha dikeluarkan oleh sel mikroorganisme. Pertumbuhan sel mikroorganisme menjadi lebih lambat bahkan berhenti sama sekali karena dibutuhkan energi untuk mengeluarkan proton dari dalam sel. (Eklund, 1989; Fardiaz, 1989).
Penurunan pH yang terjadi untuk setiap sampel selama tiga hari pengamatan disebabkan oleh adanya aktivitas mikroba terutama dari golongan pembentuk asam dan golongan proteolitik. Peningkatan keasaman atau penurunan pH terutama disebabkan oleh aktivitas bakteri asam laktat (Lactobacillus bulgaricus, Lactobacillus Lactis,dan Streptococcus thermophilus) (Datson et al., 1977).
Nilai pH untuk ketiga perlakuan pengawet masih lebih besar dari 3. Hal ini menandakan perlakuan pengawet masih belum efektif dalam menghambat pertumbuhan kapang, karena kapang efektif tumbuh pada pH di bawah 3.
Nilai pH pada tahu kontrol relatif sama untuk tiga hari pengamatan dan lebih tinggi dibandingkan dengan tahu X, Y, dan Z. Nilai pH yang tinggi dari tahu kontrol ini disebabkan oleh terbentuknya senyawa-senyawa hasil penguraian protein oleh mikroba yang bersifat basa seperti amoniak atau NH3. Peningkatan pH ini menunjukkan bahwa telah terjadi
penurunan kualitas tahu, dimana semakin tinggi pH maka kesempatan mikroba untuk merusak tahu akan semakin besar (Fennema, 1985).
Dari data yang dihasilkan pada kedua ulangan, dapat disimpulkan bahwa asam laktat (Y) memiliki pengaruh yang paling tinggi terhadap penurunan pH, sehingga memiliki nilai pH terkecil. Hal ini disebabkan oleh asam laktat memiliki pKa yang tinggi dan konsentrasi larutannya tinggi, sehingga persentase molekul asam organik yang tidak terurai meningkat dan menyebabkan penurunan pH. Nilai pH yang cukup rendah dari laktat ini memberikan efek penurunan jumlah mikroba yang tumbuh pada tahu sehingga tahu dapat lebih awet
2. Total Asam Tertitrasi (TAT)
Analisis total asam tertitrasi (TAT) merupakan analisis untuk mengukur kandungan seluruh asam yang terlarut dalam bahan pangan. Nilai TAT pada tahu yang dicelupkan dalam pengawet asam menunjukkan seberapa banyak asam yang mampu berdifusi ke dalam tahu sehingga dapat diketahui seberapa banyak aktivitas asam untuk menghambat pertumbuhan mikroba. Nilai TAT dalam penelitian pendahuluan ini dapat dilihat pada Gambar 2.
0 2 4 6 8 10 1 2 3 4
Umur Simpan (Hari)
T o ta l A s a m T e rt it ra s i (% )
kontrol asetat 5%(X) laktat 10%(Y) campuran asetat-laktat(Z)
3 2
1 0
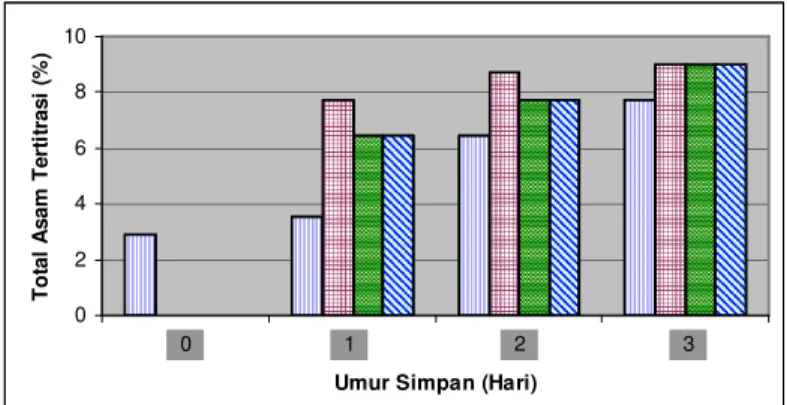
Gambar 2. Nilai TAT tahu pada penelitian pendahuluan
Analisis penentuan nilai TAT tahu menunjukkan bahwa tahu tanpa perlakuan (kontrol) pada hari 0 memiliki nilai TAT 2.90 %. Sedangkan pada penyimpanan hari 1, 2, dan 3 TAT kontrol mengalami kenaikan
secara terus-menerus yaitu : 3.54%; 6.44%; dan 7.73%. Tahu X mengalami kenaikan nilai TAT pada hari 1, 2, dan 3 yaitu : 7.73%; 8.70%; dan 9.02%. Tahu Y juga mengalami kenaikan nilai TAT pada hari 1, 2, dan 3 yaitu : 6.44% ; 7.73% ; dan 9.02%. Demikian pula dengan tahu Z, mengalami kenaikan nilai TAT pada hari 1, 2, dan 3 yaitu : 6.44% ; 7.73%; dan 9.02%. Tahu X, Y, dan Z memiliki nilai TAT yang lebih besar daripada nilai TAT pada kontrol. Hal ini disebabkan oleh asam dari larutan pengawet yang berdifusi ke dalam tahu tersebut.
Analisis sidik ragam pada hari ke-1, 2, dan 3 (Lampiran 26, 27, dan 28) menunjukkan tidak adanya perbedaan nilai TAT antar sampel. Nilai TAT tahu dengan pengawet X, Y, dan Z adalah sama dan tidak berbeda pula secara signifikan dengan kontrol.
Berdasarkan hasil yang ditunjukkan pada Gambar 2, dapat dilihat bahwa tahu dengan asetat 5% (X) memiliki nilai TAT yang lebih besar dibandingkan dengan tahu laktat 10% (Y) maupun campuran asetat-laktat (Z) pada hari pertama dan kedua, sehingga aktivitas antimikrobanya juga lebih tinggi. Hal disebabkan oleh asam asetat memiliki pKa tertinggi dibandingkan asam laktat maupun campuran asetat-laktat Nilai pKa yang tinggi ini menunjukkan jumlah asam dari pengawet yang mampu berdifusi ke dalam tahu juga semakin besar. Hal ini menyebabkan pertumbuhan mikroba pada tahu dapat ditekan karena mikroba berusaha mengeluarkan asam yang sudah masuk ke dalam sitoplasma mikroba. Proses pengeluaran asam ini membutuhkan energi yang besar sehingga mikroba pun menjadi semakin lemah.
Trend yang terjadi untuk setiap sampel adalah kenaikan nilai TAT selama penyimpanan. Kenaikan total asam lebih disebabkan oleh terbentuknya asam laktat oleh aktivitas bakteri asam laktat. Kandungan whey yang tinggi pada tahu akan menguntungkan bagi pertumbuhan bakteri asam laktat.
Pada hari ketiga, nilai TAT tahu X, Y, dan Z memiliki nilai yang sama. Hal ini bukan menandakan jumlah asam yang berdifusi ke dalam tahu dari pengawet sama, tetapi lebih dikarenakan oleh asam yang
ditimbulkan oleh kerusakan mikrobiologis tahu Y dan Z sudah mulai tinggi. Sedangkan tahu X pada hari ketiga ini belum menunjukkan adanya kerusakan mikrobiologis yang ditimbulkan.
3. Total Mikroba
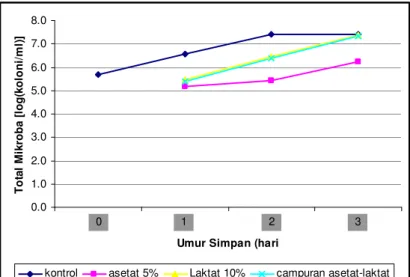
Analisis mikrobiologis dapat menunjukkan jumlah koloni mikroba yang tumbuh dalam bahan makanan sehingga mempengaruhi daya terima produk pada konsumen. Adapun pemaparan jumlah koloni total mikroba yang terbentuk pada tahu selama 3 hari penyimpanan dapat dilihat pada Gambar 3. 0.0 1.0 2.0 3.0 4.0 5.0 6.0 7.0 8.0 1 2 3 4
Umur Simpan (hari
T o ta l M ik ro b a [ lo g (k o lo n i/ m l) ]
kontrol asetat 5% Laktat 10% campuran asetat-laktat 3 2
1 0
Gambar 3. Total mikroba tahu pada penelitian pendahuluan
Analisis mikrobiologi yang dilakukan pada penelitian pendahuluan ini adalah analisis TPC (Total Plate Count). Analisis mikrobiologi tahu menunjukkan bahwa tahu tanpa perlakuan (kontrol) pada hari 0 memiliki nilai TPC 4.8 x 105 koloni/ml. Sedangkan pada penyimpanan hari 1, 2, dan 3 nilai TPC tahu kontrol mengalami kenaikan secara drastis yaitu : 3.7 x 106 koloni/ml ; >2.5 x 107 koloni/ml ; dan >2.5 x 107 koloni/ml. Menurut SNI 01-3142-1992, jumlah maksimum total mikroba pada tahu adalah 1.0 x 106 koloni/ml. Berdasarkan persyaratan tersebut, maka setelah hari ke-1, tahu kontrol sudah tidak layak dikonsumsi.