BAB 2 TINJAUAN PUSTAKA
2.1 Nanopartikel
Istilah nanoteknologi digunakan untuk mendeskripsikan kreasi suatu material yang memiliki ukuran struktur diantara atom dan material ukuran besar yang didimensikan dengan ukuran nanometer yaitu sekitar 1-100 nm. Sifat dari material dengan dimensi nano sangat berbeda secara signifikan dari atomnya juga dari partikel besarnya. Kontrol yang baik terhadap sifat tersebut bisa menuntun ke pengetahun baru yang sesuai dengan peralatan dan teknologi baru. Pentingnya nanoteknologi pertama kali dikemukakan oleh Feynman pada tahun 1959.
Nanoteknologi adalah ilmu rekayasa dalam menciptakan material, struktur fungsional, maupun piranti alam skala nanometer. Material berukuran nanometer memiliki sejumlah sifat kimia dan fisika yang lebih unggul dari material berukuran besar (bulk). Di samping itu material dengan ukuran nanometer memiliki sifat yang kaya karena menghasilkan sifat yang tidak dimiliki oleh material ukuran besar. Sejumlah sifat tersebut dapat diubah-ubah dengan melalui pengontrolan ukuran material, pengaturan komposisi kimiawi, modifikasi permukaan, dan pengontrolan interaksi antar partikel. Material nanopatikel adalah material-material buata manusia yyang berskala nano, yaitu lebih kecil dari 100 nm.
Selain nanopartikel juga dikembangkan material nanostruktur, yaitu material yang tersusun oleh beberapa material nanopartikel. Untuk menghasilkan material nanostruktur maka partikel-partikel penyusunnya harus diproteksi sehingga apabila partikel-partikel tersebut digabung menjadi material yang berukuran besar maka sifat individualnya dipertahankan. Sifat material nanostruktur sangat bergantung pada
a. Ukuran maupun distribusi ukuran
b. Komponen kimiawi unsur-unsur penyusun material tersebut c. Keberadaan interface(grain boundary)
d. Interaksi antar grain penyusun material nanostruktur.
elektron. Nanowire adalah material berukuran nanometer yang dapat mengurung elektron secara 2-dimensi dan bebas bergerak di dimensi yang ketiga, yaitu ke depan atau ke belakang.
Sintesis nanopartikel dapat dilakukan dalam fasa padat, cair, maupun gas. Proses sintesis pun dapat berlangsung secara fisika atau kimia. Proses sintesis secara fisika tidak melibatkan reaksi kimia. Yang terjadi hanya pemecahan material besar menjadi material berukuran nanometer, atau pengabungan material berukuran sangat kecil, seperti kluster, menjadi partikel berukuran nanometer tanpa mengubah sifat bahan. Proses sintesis srecara kimia mengakibatkan reaksi kimia dari sejumlah material awal (precursor) sehingga dihasilkan material lain yang berukuran nanometer. Contohnya adalah pembentukan nanopartikel garam dengan mereaksikan asam dan basa yang bersesuaian.
2.2 Nanopartikel Magnetik Fe3O4
Nanopartikel magnetik memiliki sifat fisis dan kimia yang bervariasi dan dapat diaplikasikan dalam berbagai bidang. Salah satu partikel magnetik tersebut yang dapat dijadikan berukuran nanometer adalah besi oksida seperti Fe3O4
(magnetit). Fe3O4 merupakan salah satu fase dari oksida besi yang bersifat amfoter
(kemampuan suatu zat yang dapat berpindah sifat keasaman dari asam ke sifat basa) dan memiliki daya serap yang tinggi. Magnetit (Fe3O4) merupakan salah satu mineral
golongan besi oksida yang memiliki sifat magnetik paling kuat di alam dengan struktur kristal berbentuk kubus. Kelainan dapat diperoleh dari alam yaitu dari pasir besi, bahan ini juga dapat disintesis dari bahan-bahan lain menggunakan reaksi kimia dan larutan-larutan kimia tertentu.
Perubahan ukuran partikel magentit Fe3O4 akan memperngaruhi sifat-sifat
yang dimilikinya. Daftar sifat fisika dan kimia dari bahan magnetit(Fe3O4) disajikan
Tabel 1. Sifat Fisika dan Kimia Magnetit (Fe3O4)
Sifat Fisika Sifat Kimia
1. Warna : Hitam 2. Kilau : kusam
3. Kristal magnetit tidak tembus pandang (buram)
4. Struktur kristal spinel 5. Tingkat kekerasan 681-792
kg/mm2
6. Kepadatan : 5,2 g/cm3 7. Temperatur Curie (Tc) =
575ºC - 585ºC
1. Rumus kimia : Fe3O4
2. Unsur yang terkandung : Fe, O 3. Unsur pengotor (impuritas) : Mn,
Mg, Zn, Ni, Cr, Ti, V dan Al
Sumber: Clara Saragih, 2016
Fe3O4 berukuran nano memiliki sifat ferimagnetik dan memiliki peluang
aplikasi luas. Dalam pengaplikasiannya Fe3O4 yang berukuran parikel nano
merupakan alternatif yang diperlukan untuk memenuhi kebutuhan bahan baku industri di bidang elektronik. Seperti aplikasi pada bidang industri berukuran naopartikel adalah pada keramik, sebagai katalis, energy storage, magnetic data storage, ferofluida, maupun dalam diagnosis medis. Agar dapat diaplikasikan dalam berbagai bidang tersebut, sangatlah penting untuk mempertimbangkan ukuran partikel, sifat magnetik, dan sifat permukaan dari partikel nano itu sendiri.
Rumus kimia magnetit (Fe3O4) sering ditulis dalam bentuk FeO.Fe2O3 di
mana satu bagian adalah wustite (FeO) dan bagian lainnya adalah hematit (Fe2O3).
Selain itu magnetit mempunyai struktur kristal spinel dengan sel unit kubik yang terdiri dari 32 ion oksigen, di mana celah-celahnya ditempati oleh ion Fe2+ dan Fe3+.
oktan (kubus spinel), masing-masing berukuran a/2, empat oktan yang berarsir memiliki ukuran isi yang sama, begitu pula dengan cara yang sama, tetrahedral di oktan terarsir dan oktahedral di oktan tidak terarsir.
2.3 Metode Kopresipitasi
Kopresipitasi merupakan proses kimia yang diawali dengan adanya zat terlarut yang mengendap sehingga menghasilkan endapan yang diinginkan. Pengendapan terjadi sebagai akibat pembentukan kristal campuran. Selain itu endapan ini dapat pula terbentuk karena adanya absorbsi (penyerapan) ion-ion selama proses pengendapan. Setelah endapan terbentuk, langkah selanjutnya adalah meningkatkan kemurnian dari endapan dengan cara menyaring endapan , melarutkannya lagi dan mengendapkan lagi secara berulang-ulang. Hal ini dilakukan agar terjadi dekomposisi ion-ion yang terikat oleh larutan pengikat (larutan basa) sedangkan ion-ion yang tidak terikat oleh larutan pengikat akan bereaksi membentuk produk/hasil reaksi. Kopresipitasi memiliki reaksi fisik dan kimia yang dapat dilihat pada Tabel 2.
Tabel 2. Sifat Fisik dan Kimia dari Metode Kopresipitasi
Sifat Fisik Sifat Kimia
1. Suhu reaksi yang diperlukan <100ºC
2. Pada kopresipitasi dilakukan pengadukan secara terus-menerus agar larutan homogen 3. Memiliki ukuran partikel hasil
sintesis lebih kecil daripada metode sol state dan lebih besar daripada metode sol gel
1. Proses kopresipitasi akan meningkatkan pH
2. Kopresipitasi dilakukan pada larutan encer agar memudahkan proses penyaringan
3. Tingkat homogenitas dapat ditingkatkan dengan
penambahan larutan
Waktu kopresipitasi merupakan salah satu metode sintesis senyawa anorganik yang didasarkan pada pengendapan lebih dari satu substansi secara bersama-sama ketika melewati titik jenuhnya. Kopresipitasi merupakan metode yang menjanjikan karena prosesnya menggunakan suhu rendah dan mudah untuk mengontrol ukuran partikel sehingga waktu yang dibutuhkan relatif lebih singkat. Beberapa zat yang paling umum digunakan sebagai zat pengendap dalam kopresipitasi adalah hidroksida, karbonat, sulfat dan oksalat.
Produk dari metode ini diharapkan memiliki ukuran partikel yang lebih kecil dan lebih homogen daripada metode solid state dan ukuran partikel yang lebih besar daripada metode sol gel.
Bila suatu endapan memisah dari dalam suatu larutan, endapan itu tidak selalu sempurna murninya, kemungkinan mengandung berbagai jumlah zat pengotor, bergantung pada sifat endapan dan kondisi pengendapan. Kontaminasi endapan oleh zat-zat yang secara normal larut dalam cairan induk dinamakan kopresipitasi. Kita harus membedakan dua jenis kopresipitasi yang penting. Yang pertama adalah yang berkaitan dengan adsorbsi pada permukaan partikel yang terkena larutan, dan yang kedua adalah yang sehubungan dengan oklusi zat asing sewaktu proses pertumbuhan kristal dari partikel-partikel primer.
Jenis kopresipitasi yang kedua terjadi sewaktu endapan dibangun dari partikel-partikel primernya. Partikel primer ini akan mengalami adsorbsi permukaan sampai tingkat tertentu dan sewaktu partikel-partikel ini saling bergabung, zat pengotor itu akan hilang sebagian jika terbentuk kristal-kristal tunggal yang besar dan prosesnya berlangsung lambat, atau jika saling bergabung itu cepat mungkin dihasilkan kristal-kristal besar yangg tersusun dari kristal-kristal kecil yang terikat lemah, dan sebagian zat pengotor mungkin terbawa masuk ke balik dinding kristal besar. Jika zat pengotor ini isomorf atau membentuk larutan-padat dengan endapan, jumlah kopresipitasi kemungkinan akan sangat banyak, karena tidak akan ada kecenderungan untuk menyisihkan zat pengotor sewaktu proses pematangan.
Pascapresipitasi adalah pengendapan yang terjadi di atas permukaan endapan pertama sesudah terbentuk. Ini terjadi pada zat-zat yang sedikit terlarut, yang membentuk larutan lewat-jenuh, zat-zat ini umumnya mempunyai satu ion yang sama dengan salah satu ion endapan primer. Maka pada pengendapan kalsium sebagai oksalat dengan adanya magnesium, magnesium oksalat berangsur-angsur memisah dari larutan dan mengendap di atas kalsium oksalat, makin lama endapan dibiarkan bersentuhan dengan larutan itu, maka makin besar sesatan yang ditimbulkan oleh penyebab ini.
Pascapresipitasi berbeda dari kopresipitasi dalam segi:
a) Kontiminasi bertambah dengan bertambah lamanya endapan dibiarkan bersentuhan dengan cairan induk pada pascapresipitasi, tetapi biasanya berkurang pada kopresipitasi
b) Pada pascapresipitasi, kontaminasi akan bertambah dengan semakin cepatnya larutan diaduk, baik dengan cara-cara mekanis ataupun termal. Pada kopresipitasi keadaannya umumnya adalah kebaikannya
c) Banyaknya kontaminasi pada pascapresipitasi dapat jauh lebih besar dari pada kopresipitasi.
Sintesis nano partikel magnetit (Fe3O4) menggunakan metode kopresipitasi
dipengaruhi oleh perbandingan/rasio antara ion ferrous (Fe2+) dan ion ferric
(Fe3+) dalam medium basa (pH > 7). Pada sintesis nano partikel magnetit (Fe3O4), diperlukan garam-garam yang digunakan sebagai bahan dasar yang
Larutan yang telah diaduk sampai homogen perlu ditambahkan larutan pengendap sedemikian rupa sehingga endapan yang didapatkan mempunyai homogenitas yang tinggi (Negara, dkk. 2008).
2.4 PEG (Polyethylene Glycol)
PEG merupakan polimer yang banyak digunakan dalam industri pangan, kosmetik dan farmasi. Secara kimiawi PEG disebut juga makrogol, merupakan polimer sintetik dari oksietilen. PEG umumnya memiliki bobot molekul antara 200-300000. Penamaan PEG umumnya ditentukan dengan bilangan yang menunjukkan bobot molekul rata-rata.(Leuner and Dressman, 2000)
PEG adalah suatu polimer yang terdiri dari beberapa ikatan monomer. Monomer ini adalah suatu senyawa yang dapat dipolimerisasi. PEG mempunyai sifat stabil, mudah larut dalam air hangat, tidak beracun, nonkorosi, tidak berbau, tidak berwarna dan memiliki titik lebur yang sangat tinggi (580ºF), tersebar merata, higoskopik (mudah menguap) dan juga dapat mengikat pigmen.
Fungsi PEG dalam penelitian ini, dapat dipakai untuk membentuk dan mengontrol ukuran dan struktur pori partikel yang dilapisi. Dalam hal ini PEG tidak terbentuk agregat, hal ini dikarenakan PEG terjebak pada permukaan partikel dan menutupi ion negatif pada besi, dan pada akhirnya akan diperoleh hasil partikel dengan bentuk bulatan yang seragam. Akat tetapi jumlah PEG yang ditambahkan jumlah cukup besar agar bekerja sesuai dengan fungsi.
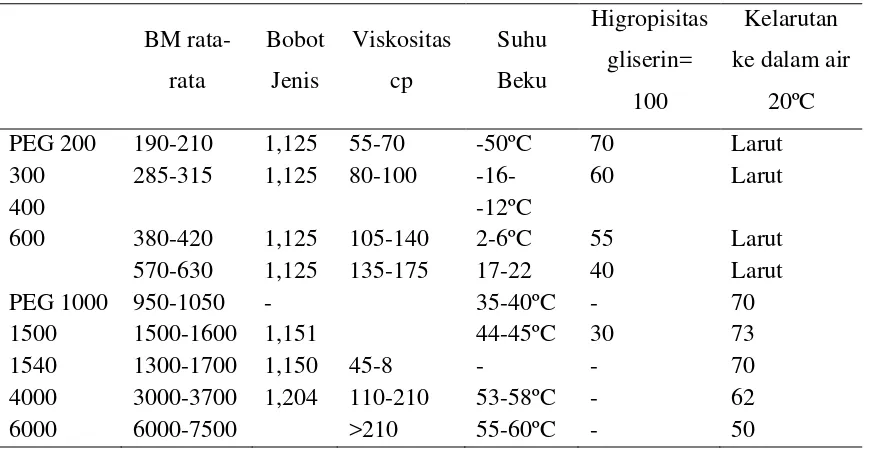
Tabel 3. Sifat Kelarutan Masing-Masing PEG
PEG umumnya memiliki bobot molekul antara 200-300000, penamaan PEG umumnya di tentukan dengan bilangan yang menunjukkan bobot molekul rata-rata. Konsistensinya sangat dipengaruhi oleh bobot molekul. PEG dengan bobot molekul 200-600 berbentuk cairan, PEG 1500 semi padat dan PEG 3000-20000 atau lebih berupa padatan semi kristalin, dan PEG yang lebih dari 100000 berbentuk seperti resin pada suhu kamar. Umumnya PEG dengan bobot molekul 1500-20000 yang digunakan untuk dispersi padat. Polimer ini mudah larut dalam berbagai pelarut, titik leleh dan toksisitasnya rendah, berada dalam bentuk semikristalin. Kebanyakan PEG yang digunakan memiliki bobot molekul antara 4000 dan 20000, khusunya PEG 4000 dan PEG 6000.
2.5. Sifat Kemagnetan Bahan
Bahan magnetik adalah suatu bahan yang memiliki sifat kemagnetan dalam komponen pembentuknya. Menurut sifatnya terhadap adanya pengaruh kemagnetan, bahan dapat digolongkan menjadi 5 yaitu:
2.5.1. Bahan Diamagnetik
sehingga menghasilkan resultan medan magnet atomis yang arahnya berlawanan dengan medan magnet luar tersebut. Contoh bahan diamagnetik yaitu bismut, perak, emas, tembaga dan seng.
2.5.2. Bahan Paramagnetik
Bahan Paramagnetik adalah bahan yang resultan medan magnet atomis masing-masing molekulnya tidak nol, tetapi resultan medan magnet atomis total seluruh atom/molekul dalam bahan nol. Bahan ini jika diberi medan magnet luar, maka elektron-elektronnya akan berusaha sedemikian rupa sehingga resultan medan magnet atomisnya searah dengan medan magnet luar. Sifat ini ditimbulkan oleh momen magnetik spin yang menjadi terarah oleh medan magnet luar. Pada bahan ini, efek diamagnetik (efek timbulnya medan magnet yang melawan medan magnet penyebabnya) dapat timbul, tetapi pengaruhnya sangat kecil.
2.5.3. Bahan Ferromagnetik
Bahan Ferromagnetik adalah bahan yang mempunyai resultan medan atomis besar. Hal ini terutama disebabkan oleh momem magnetik spin elektron. Pada bahan ferromagnetik banyak spin elektron yang tidak berpasangan, misalnya pada atom besi terdapat empat buah spin elektron yang tidak berpasangan. Masing-masing spin elektron yang tidak berpasangan ini akan memberikan medan magnetik, sehingga total medan magnetik yang dihasilkan oleh suatu atom lebih besar.
2.5.4. Bahan Superparamagnetik
Superparamagnetik adalah jenis magnetik yang terjadi pada nanopartikel ferromagnetik atau ferrimagnetik yang kecil. Ukurannya sekitar beberapa nanometer yaitu sekitar puluhan nanometer yang tergantung pada materialnya. Selain itu, nanopartikel ini adalah partikel
single domain. Pendekatan yang sederhana, total momen magnetik pada nanopartikel dapat dianggap sebagai salah satu momen magnetik raksasa, yang terdiri dari semua momen magnetik pada atom-atom yang membentuk partikel nano (Benz, 2012).
mudah dipengaruhi oleh medan magnet eksternal maupun fluktuasi termal. Dalam orde tertentu, nanopartikel magnetik juga menunjukkan keadaan yang khas dimana koersivitas partikel tersebut sama dengan nol (Hc = 0) atau Hc<100 Oe. Keadaan ini yang disebut dengan keadaan superparamagnetik (Guimaraes, 2009).
Superparamagnetik didasarkan pada hukum aktivasi untuk waktu relaksasi pada magnetisasi partikel:
� = � exp ∆ (2.1) ΔΕadalah energi barrier saat pembalikan, kBT adalah energi termal. Faktor pra-ekponensial τo bekisar dari 10-10 – 10-12 s dan bergantung pada suhu.
Energi barrier memiliki efek intrinsik dan ekstrinsik seperti magneto kristal
dan bentuk anisotropi. Namun untuk uniaksial anisotropi, ΔΕ sama dengan
hasil konstanta anisotropi dan volume.
ΔE = KV(2.2)
Ini perbandingan langsung antara ΔE dan V yang merupakan alasan
bahwa superparamagnetik secara termal berbalik arah pada arah jumlahan
momen magnetik dan untuk partikel kecil, karena untuk partikel kecil ΔE
sebanding dengan kT pada suhu kamar
Dibawah suhu tertentu material bulk memiliki energi magnetik anisotropi yang jauh lebih besar daripada energi termal kT (Gambar 1 garis biru). Energi termal pada partikel nano tidak cukup mudah untuk membalikkan arah spin magnetik, sehingga materialnya disebut ferromagnetik.
Namun, untuk partikel nano yang berukuran kecil menghasilkan energi anisotropi yang jauh lebih kecil dibandingkan dengan energi termalnya. Energi termalnya cukup mudah untuk membalikkan arah spin magnetiknya (Gambar 1 garis merah). Material ini disebut superparamagnetik yang memiliki jumlah magnetisasi sama dengan nol (Xu, 2004).
Ukuran tertentu pada partikel nano, perubahan suhu dapat juga menyebabkan transisi antara ferromagnetik ke superparamagnetik. Suhu transisi dari ferromagnetik ke superparamagnetik disebut sebagai suhu
blocking (TB)
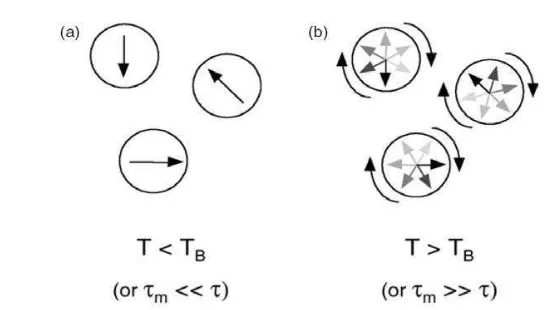
Gambar 2. Ilustrasi konsep superparamagnetik, lingkaran menggambarkan tiga nanopartikel magnetik dan panah mewakili arah jumlahan magnetisasi dalam partikel tersebut (Xu, 2004).
Pengamatan superparamagnetik tergantung pada suhu dan waktu
pengukuran τm pada eksperimen yang digunakan. Jika τ<<τm yaitu waktu
relaksi τ lebih pendek dari pada waktu pengukuran τm, maka partikel
magnetik tersebut dikatakan dalam keadaan superparamagnetik. Momen magnetik dalam keadaan ini melakukan putaran dengan cepat (tak stabil). Sementara jika τ>>τm, maka partikel dikatakan dalam keadaan terblok (quasi-static), seperti yang ditunjukkan dalam ilustrasi gambar 2.11. Kondisi momen magnetik quasi-static, keadaan magnetisasi tidak nol dapat diamati dalam pengukuran. Kondisi yang demikian disebut dengan keadaan ferro/ferri magnetik (Xu, 2004)
2.6. Magnesium Ferit ( MgFe2O4)
Magnesium Ferit (MgFe2O4) termasuk kedalam jenis soft ferrite yang
memiliki struktur spinel. Ferrite memiliki persamaan umum AB2O4 dengan A
merupakan metal kation divalent dan B menunjukkan metalkation trivalent. Dalam struktur spinel normal, kation divalent (A) dan sisa kation trivalen (B) menempati ruang tetrahedral dengan 64 ion dalam unit cell sedangkan kation trivalen (B) menempati ruang oktahedral dengan 32 ion dalam unit cell. Kebalikan dari spinel normal, pada spinel invers ruang tetrahedral ditempati oleh kation trivalen (B) dan ruang oktahedral ditempati oleh kation divalen (A) dan sisa kation trivalen (B) (Kim
et al., 2008). Magnesium ferrite (MgFe2O4) memiliki struktur inverse spinel dengan
sisi (A) merupakan tetrahedral yang terisi oleh ion-ion Fe3+ dan sisi (B) merupakan oktahedral yang terisi ion-ion Fe3+ dan Mg2+ (Hyeon et al., 2002).
Saat ini riset dibidang nanopartikel magnesium ferrite (MgFe2O4) sedang
banyak dilakukan. Beberapa alasan yang menyebabkan MgFe2O4 banyak menarik
perhatian para peneliti dibandingkan ferit yang lainnya adalah potensinya yang besar untuk diaplikasikan karena MgFe2O4 memiliki nilai magnetisasi saturasi yang tinggi,
temperatur curie dan resitivitas listrik yang tinggi. MgFe2O4 adalah soft magnetic
material dan salah satu kelompok spinel invers yang sangat penting. MgFe2O4 juga
merupakan material semikonduktor tipe n yang dapat diaplikasikan sebagai
menarik dari MgFe2O4 ini adalah sifat kimia dan stabilitas termalnya yang unik, serta
ketergantungan sifat magnetik pada ukuran partikel.
Nanopartikel MgFe2O4 juga sapat berprilaku sebagai nanopartikel
superparamagnetik. Ketika medan eksternalnya dihilangkan, maka jumlah momen magnetik dari nanopartikel magnetik masing-masing berada dalam arah yang berbeda, dengan demikian keseluruhan momen bulk adalah nol. Ketika medan magnet eksternal diterapkan, magnetiknya dapat diinduksi untuk nanopartikel magnetik ini. Hal ini terjadi karena adanya interaksi magnetik antarananopartikel magnetik dengan medan magnet eksternal yang mempengaruhinya. Interaksi magnetik tersebut membuat magnetisasi nanopartikel magnetiknya sejajar. Sifat superparamagnetik umumnya muncul dari material ferromagnetik dan ferrimagnetik yang memiliki ukuran partikel yang sangat kecil (orde nanometer). Dengan demikian kajian penelitian tentang pengontrolan distribusi ukuran nanopartikel dan sifat kemagnetannya sangat dibutuhkan (Hermawan, 2015).
2.7. Teknik Pengukuran ( Karakterisasi Material )
Untukmengetahui sifat-sifatdankemampuansuatumaterialmakaperlu dilakukan pengujian dan analisis.Beberapa jenis pengujian dan analisis yang dibahasuntukkeperluanpenelitianiniantaralain:Karakterisasisifatfisis (densitas) dengan pengujian true density, analisa ukuran partikeldengan menggunakan Optical Microscopy(OM) dan Field Emission Scanning Electron Microscopy (FE-SEM), analisa ukuran partikel menggunakan alat Particle Size Analyzer (PSA), karakterisasi sifat kemagnetan dengan pengujian VSM serta analisa struktur kristal dengan menggunakan alat uji XRD. Adapun pengujian Atomic Absorbsion Spectroscopy(AAS) dilakukan untuk mengetahui sifat penyerapan material.
2.7.1 Optical Microscopy (OM)
(Sianipar, 2015). Analisis mikrostruktur dengan menggunakan OM bertujuan untuk mengetahui distribusi partikel dalam ukuran mikro yang nantinya akan dianalisa menggunakan software imageJ.
2.7.2 Densitas
Densitas (ρ) adalah suatu ukuran massa (m) persatuam volume (V) suatu material dalam satuan gram/cm3. Beberapa faktor yangmempengaruhi densitasadalah ukuran dan berat atom suatu elemen, kuatnya pengepakan atom dalam struktur kristal dan besarnya porositas dalam mikrostruktur.
Densitas merupakan ukuran kepadatan dari suatu material. Pengukuran densitas yang dilakukan pada penelitian ini adalah pengukuran true density. Pengukuran densitas ini tak lain adalah cara pengukuran densitas suatu bahan berupa serbuk menggunakan alat yang disebut picnometer. Untuk mengetahui densitas serbuk dilakukan secara piknometris menggunakan persamaan 2.3.
�
=
3− 12− 1 −( 4− 3)
×
�
(2.3)Keterangan:
ρs = Truedensitysampel(kg/m3)
m1 = Massapicnometer kosong(kg)
m2 = Massapicnometer diisilarutan uji(kg)
m3 = Massapicnometer diisiserbuk sampel(kg)
m4 = Massapicnometer diisiserbuk sampeldan larutan uji (kg) ρlarutan = Densitas mediacair / larutan uji(kg/m3
)
2.7.3 X-Ray Diffraction Spectroscopy(XRD)
Gambar3.DifraksiBidang Atom (Randy, J.S. 2015).
Gambar3.menunjukkansuatuberkassinarXdenganpanjanggelombangλ, jatuhpada
sudutθpada sekumpulanbidangatomberjarakd. Sinaryang
dipantulkandengansudutθhanyadapatterlihatjikaberkasdarisetiapbidang yang berdekatansalingmenguatkan.Olehsebabitu,jaraktambahansatuberkas
dihamburkandari setiapbidangyang berdekatan,dan menempuhjarak sesuai denganperbedankisiyaitusamadenganpanjang gelombang nλ.Sebagai contoh,berkaskeduayang ditunjukkangambar3.harusmenempuhjaraklebih jauhdariberkaspertama sebanyak PO+OQ.Syarat pemantulandansaling menguatkan dinyatakanoleh :
nλ=PO +OQ =2ON sinθ =2d sinθ (2.4) Persamaan (4) disebut dengan hukum Bragg dan harga sudut kritis θuntukmemenuhi hukum tersebut dikenal dengan sudut Bragg.
Di dalam kisi kristal, tempat kedudukan sederetan ion atauatom disebut bidang kristal.Bidang kristaliniberfungsisebagaicerminuntukmerefleksikan sinar– Xyang datang.PosisidanarahdaribidangkristalinidisebutIndeksMiller. Setiapkristalmemiliki bidang kristaldenganposisidanarahyang khas,sehingga jika disinaridengansinar-XpadaanalisisXRDakanmemberikandifraktogram yangkhas pula. Dari data XRD yang diperoleh, dilakukan identifikasi puncak-puncak grafikXRDdengancaramencocokkanpuncak
yangadapadagrafiktersebut.Setelahitu,dilakukanrefinementpada data XRD. Melaluirefinementtersebut,fasebesertasruktur,spacegroup,danparameterkisiyangadap adasampelyangdiketahui (Randy, J.S. 2015).MelaluigrafikXRD,grainsizedarisampel jugadapatdiperkirakan. Perhitungan distribusi ukuran sampel (grain size) dilakukan dengan menggunakan persamaan 2.2 Yang dikenal dengan persamaan Scherrer.
=
��cos� (2.5) Dengan t adalah ukuran butir kristal, k adalah konstanta Scherrer (0.89), λ adalah panjang gelombang sinar-X, β adalah nilai dari full width half maximum (FWHM)
dan θ adalah besar sudut dari puncak dengan intensitas tertinggi (Hermawan, 2015).
2.7.4 Vibrating Sample Magnetometer (VSM)
Semuabahan mempunyai momen magnetikjikaditempatkan dalam medan magnetik. Momen magnetik per satuan volume dikenal sebagai magnetisasi. Secara prinsip ada dua metoda untuk mengukur besar magnetisasi ini, yaitu metoda induksi(induction method) dan metodagaya(forcemethod). Padametoda induksi,magnetisasidiukurdarisinyalyang ditimbulkan/diinduksikanoleh cuplikan yang bergetar dalam lingkungan medan magnet pada sepasang kumparan.Sedangkanpadametodagayapengukurandilakukanpadabesamya gayayang ditimbulkanpadacuplikanyang beradadalamgradienmedanmagnet. VSM(VibratingSampleMagnetometer)merupakansalah satualatukur magnetisasiyangbekerjaberdasarkanmetoda induksi.
sinyalteganganACpadakumparanpengambil(pick-up coilatausensecoil)yang ditempatkansecaratepatdalamsistemmedanmagnetini.SelanjutnyasinyalAC ini akan dibacaolehrangkaianpre-amp danLock-in amplifier.Frekuensidari Lock-in amplifierdisetsarnadengan frekuensigetaransinyalreferensidari pengontrolgetaran cuplikan.Lock inamplifierini akan membacasinyaltegangan dari kumparan yang sefasa dengan sinyal referensi. Kumparan pengambil biasanyadirangkaiberpasangandengankondisiarahlilitan yang berlawanan.Hal ini untuk menghindari terbacanya sinyal yang berasal dari selain cuplikan, misalnyadari akibat adanyaperubahan medan magnet luar itu sendiri.
Selanjutnya dalamprosespengukuran,medanmagnetluaryangdiberikan,suhu cuplikan, sudut dan interval waktu pengukuran dapat divariasikan melalui kendali komputer. Komputer akan merekam data tegangan kumparan sebagai fungsi medanmagnetluar, suhu, sudutataupunwaktu (Mujamilah dkk, 2000).
2.7.5 Atomic Absorption Spectroscopy (AAS)
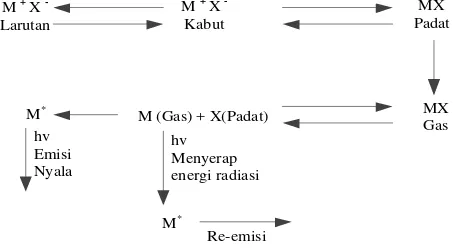
Suatu larutan yang mengandung garam-garam logam (atau senyawa-senyawa logam lain) jika dibakar dengan nyala asetelen udara atau yang sejenis akan terbentuk uap yang mengandung atom-atom logam. Uap atom-atom logam ini dapat memancarkan atau menyerap energi dengan mengalami transisi elektronik (melepas atau menangkap elektron). Besarnya energi yang diserap atau dipancarkan sangat tergantung dari karakteristik pada masing atom suatu unsur. Dimana masing-masing atom suatu unsur memiliki sifat dan karakteristik yang berbeda-beda. Proses penyerapan dan pemancaran energi oleh spektroskopi dapat dilihat sesuai skema pada Gambar 2.4.
Dari skema tersebut tampak bahwa pada spektroskopi emisi radiasi dipancarkan oleh atom-atom yang terdapat dalam keadaan tereksitasi, sedangkan pada spektroskopi serapan atom, arom-atom dalam keadaan dasar (groundstate) dapt menyerap tenaga radiasi. Sesuai konsep diatas maka ada dua hal yang dikembangkan yaitu fotometri nyala dan spektroskopi serapan atom (Atomic Absorpsion Spectroscopy) atau lebih dikenal dengan AAS. Alat spektrofotometer serapan atom pada intinya terdiri atas lima bagian utama yaitu : sumber radiasi (biasanya lampu katoda cekung), system pengatoman, monokromator, detektor dan sistem pembacaan (Kristianingrum, 2004)
Spektrofotometer serapan atom (AAS) merupakan teknik analisis kuantitatif dari unsur-unsur yang pemakaiannya sangat luas diberbagai bidang karena prosedurnya selektif, spesifik, biaya analisa relatif lebih murah, sensitif tinggi (ppm-ppb), dapat dengan mudah mudah membuat matriks yang sesuai dengan standar, waktu analisa sangat cepat dan mudah dilakukan.
Analisis AAS pada umumnya digunakan untuk analisa unsur. Teknik AAS menjadi alat yang canggih dalam analisis. Hal ini disebabkan karena sebelum pengukuran tidak selalu memerlukan pemisahan unsur yang ditentukan, karena kemungkinan penentuan satu logam unsur dengan kehadiran unsur lain dapat dilakukan, asalkan katoda berongga yang diperlukan tersedia.
AAS dapat digunakan untuk mengukur logam sebanyak 61 logam. Sumber cahaya pada AAS adalah sumber cahaya dari lampu katoda yang berasal dari elemen yang sedang diukur kemudian dilewatkan dalam nyala api yang berisi sampel yang telah terakomisasi, kemudian radiasi tersebut diteruskan ke detektor melalui monokromator.
2.7.6 Field Emission Scanning Electron Microscopy (FE-SEM)
Field Emission Scaning Electron Microscopy (FE-SEM) dapat diartikan pencitraan material yang menggunakan prinsip mikroskop. Cara kerja FE-SEM adalah menggunakan sinar elektron yang dipercepat dengan anoda dan difokuskan menuju sampel. Sinar elektron yang terfokus memindai keseluruhan sampel dengan diarahkan oleh koil pemindai. Ketika elektron mengenai sampel maka sampel akan mengeluarkan elektron baru yang akan diterima oleh detektor dan dikirim ke monitor. Intensitas elektron baru ini tergantung pada nomor atom unsur yang ada pada permukaan spesimen. Mikroskop elektron mampu mencapai resolusi yaitu sekitar 10-1 – 10-2 nm. Dengan menggunakan elektron kita juga bisa mendapatkan beberapa jenis pantulan yang berguna untuk kepentingan karakterisasi. Jika elektron mengenai suatu benda maka akan timbul dua jenis pantulan yaitu pantulan elastis dan pantulan non elastis. Elektron dihasilkan dari katoda (electroda gun) melalui efek foto listrik dan dipercepat menuju anoda. Filamen yang digunakan pada umumnya adalah tungsten atau Lanthanum Heksaborida (LaB6). Kumparan pemindai akan