Jurnal Farmasi Galenika (Galenika Journal of Pharmacy) 2018; 4 (1): 1 – 11
ISSN : 2442-8744 (electronic) http://jurnal.untad.ac.id/jurnal/index.php/Galenika/index DOI : 10.22487/j24428744. 2018.v4.i1.9209
Kurkumin Meningkatkan Sensitivitas Sel Kanker Payudara terhadap
Tamoksifen Melalui Penghambatan Ekspresi P-glikoprotein dan
Breast
Cancer Resistance Protein
(Curcumin Increased Breast Cancer Cells Sensitivity to Tamoxifen Through Inhibition of P-glycoprotein and Breast Cancer Resistance Protein Expressions)
Erlia Anggrainy Sianipar1, Melva Louisa2 dan Septelia Inawati Wanandi3
1
Program Studi Farmasi, Fakultas Kedokteran, Universitas Katolik Indonesia Atma Jaya, Jakarta, Indonesia
2Departemen Farmakologi dan Terapi, Fakultas Kedokteran, Universitas Indonesia, Jakarta, Indonesia
3
Departemen Biokimia, Fakultas Kedokteran, Universita s Indonesia , Jakarta, Indonesia
Article Info:
Received : 12 Februari 2018 in revised form: 21 Maret 2018 Accepted: 30 Maret 2018 Available Online: 30 Maret 2018
ABSTRACT
The decreasing of sensitivity or resistance to tamoxifen occured after long-term treatment in breast cancer. One of the major factor in tamoxifen resistance is over expression of efflux transporter P-glycoprotein (P-gp) and Breast Cancer Resistance Protein (BCRP). Curcumin has known as inhibitor of P-gp and BCRP. The addition of curcumin to the tamoxifen resistant cells is expected to increase the sensitivity of breast cancer cells to tamoxifen. This study aim to know the effect of curcumin in increasing the cell sensitivity to tamoxifen through inhibition of P-gp and BCRP transporter efflux. MCF-7 breast cancer cell line was induced with tamoxifen 1 µM for 10 passage (MCF-7(T)), then cell viability and mRNA expression of P-gp and BCRP were analyzed. To the MCF-7(T) cells, curcumin was given at of 5/10/20 µM with or without tamoxifen for 5 days and cell viability and mRNA expression of P-gp and BCRP were analyzed on day 5th. As positive control, verapamil 50 µM was used as P-gp inhibitor, ritonavir 15 µM and nelfinavir 15 µM were used as BCRP inhibitor. The results showed that MCF-7(T) cells sensitivity to tamoxifen decreased with 11.8 times, the cell viability increased 10.82 fold and mRNA expression of P-gp and BCRP increased 4.04 fold. Then after administration of curcumin with or without tamoxifen for 5 days, the cell viability and the mRNA expression of P-gp and BCRP decreased. As conclusion, curcumin increased the sensitivity of MCF-7(T) to tamoxifen characterized by the decreasing of cell viability and mRNA expression of P-gp and BCRP. However, the administration of combination of curcumin with tamoxifen was more potent than just curcumin. The increased sensitivity was estimated at least partly through the inhibition of P-gp and BCRP mRNA expression by curcumin.
Keywords: Tamoxifen Curcumin P-gp BCRP
Corresponding Author: Erlia Anggrainy Sinaipar Program Studi Farmasi, FK, Universitas Katolik Indonesia Atma Jaya Jakarta, 14440, Indonesia Mobile : 081210445684 Email:
erlia.anggarainy@atmajaya.ac.id
Copyright © 2017 JFG-UNTAD This open access article is distributed under a Creative Commons Attribution (CC-BY-NC-SA) 4.0 International license.
How to cite (APA 6th Style):
ABSTRAK
Penurunan sensitivitas hingga resistensi terhadap tamoksifen sering terjadi dalam pengobatan kanker payudara jangka panjang. Salah satu penyebab utamanya adalah peningkatan ekspresi transporter efluks
P-glikoprotein (P-gp) dan Brea st Cancer Resistance Protein (BCRP). Kurkumin diketahui sebagai penghambat
P-gp dan BCRP. Pemberian kurkumin pada sel yang telah menurun sensitivitasnya terhadap tamoksifen mampu meningkatkan sensitivitas sel kanker payudara terhadap tamoksifen melalui penghambatan kedua transporter tersebut. Tujuan penelitian ini adalah untuk mengetahui efek kurkumin dalam meningkatkan sensitivitas sel terhadap tamoksifen dengan cara menghambat kerja transporter effluks P-gp dan BCRP. Sel MCF-7 dipaparkan dengan tamoksifen 1 µM selama 10 pasasi (sel MCF-7(T)), kemudian dianalisis perubahan sensitivitas sel terhadap tamoksifen melalui viabilitas sel dan ekspresi mRNA P-gp dan BCRP. Pada sel MCF-7(T), kurkumin diberikan dalam dosis 5;10;20 µM dengan atau tanpa tamoksifen selama 5 hari dan dianalisis viabilitas sel dan ekspresi mRNA P-gp dan BCRP pada hari ke-5. Sebagai kontrol positif, verapamil 50 µM digunakan sebagai penghambat P-gp, ritonavir 15 µM dan nelfinavir 15 µ M sebagai penghambat BCRP. Hasil penelitian menunjukkan bahwa sel MCF-7(T) telah menurun sensitivitasnya terhadap tamoksifen yang dibuktikan dengan
terjadinya pergeseran CC50 sebesar 11.8 kali, peningkatan viabilitas sel sebesar 10.82 kali, dan peningkatan
ekspresi mRNA P-gp dan BCRP sebesar 4.04 kali. Kemudian setelah pemberian kurkumin dengan atau tanpa tamoksifen selama 5 hari, viabilitas sel dan ekspresi mRNA P-gp dan BCRP menjadi menurun. Kesimpulan penelitian ini adalah kurkumin meningkatkan sensitivitas sel MCF-7(T) terhadap tamoksifen yang ditandai dengan penurunan viabilitas sel dan ekspresi mRNA P-gp dan BCRP. Namun demikian, pemberian kombinasi kurkumin dengan tamoksifen lebih kuat dibandingkan kurkumin saja. Peningkatan sensitivitas tersebut diduga terjadi melalui penghambatan ekspresi mRNA P-gp dan BCRP oleh kurkumin.
Kata Kunci : Tamoksifen, Kurkumin, P-glikoprotein, BCRP
PENDAHULUAN
Diperkirakan lebih dari satu juta orang di seluruh dunia menderita kanker payudara dan lebih dari 400.000 kematian terjadi setiap tahunnya (Zhou
et al, 2012). Pengobatan dengan antiestrogen tamoksifen merupakan terapi lini pertama untuk
sebagian besar pasien kanker payudara
(Lykkesfeldt et al, 1994). Namun dalam tiga dasawarsa terakhir, ribuan wanita yang mendapat pengobatan tamoksifen mengalami penurunan respon atau bahkan tidak memberikan respon
terhadap pengobatan kemoterapi kanker
payudara. Hal ini mungkin terjadi karena timbulnya resistensi (University of California, 2011). Sekitar 40% pasien akhirnya kambuh dan meninggal karena resistensi setelah terapi selama 7-10 bulan (Ring et al, 2004 & Wind et al, 2011).
Beberapa studi telah menunjukkan bahwa resistensi tamoksifen berkaitan dengan multi-drug resistance (MDR). MDR adalah suatu fenomena resistensi terhadap sejumlah bahan kemoterapeutik yang strukturnya berbeda setelah pemaparan suatu obat anti kanker (Choi et al, 2007). Peningkatan ekspresi transporter efluks P-gp dan BCRP diduga menjadi penyebab utama
terjadinya MDR pada kanker payudara (Zhou et al, 2012).
Telah dilaporkan bahwa sekitar 30% dari MDR disebabkan oleh over ekspresi P-gp dan kejadian pada kanker payudara lebih dari 50% (Zhou et al, 2012 & Bansal et al, 2009). Selain itu, pemaparan obat kemoterapi atau terapi hormonal
setelah kurang lebih 7-10 bulan telah
menunjukkan peningkatan ekspresi P-gp pada kanker payudara sebesar 1.8 kali lipat. 1.5 BCRP bekerja sebagai pompa efluks di sel tumor, timbulnya BCRP yang terekspresi berlebihan mengakibatkan peningkatan konsentrasi obat di dalam sel dan menurunkan efek sitotoksik. Secara klinis telah dilaporkan korelasi positif antara ekspresi BCRP berlebihan dan penurunan efek antikanker terhadap pasien di hematologi dan tumor padat (Mao et al, 2005. Ee et al, 2004).
Penghambat P-gp atau BCRP biasanya diberikan untuk meningkatkan akumulasi dan efikasi obat antikanker dalam kemoterapi (Anuchapreeda et al, 2002). Salah satu senyawa sintetik yang telah diidentifikasi sebagai penghambat P-gp adalah
verapamil sedangkan yang merupakan
Namun, pada studi hewan coba dan uji klinik efikasi dari senyawa-senyawa tersebut berkurang karena bersifat toksik (Mao et al, 2005 & Anuchapreeda et al, 2002)
Kurkumin merupakan salah satu penghambat P-gp dan BCRP yang poten (Shukla et al, 2009). Kurkumin memiliki aktivitas biologis dan farmakologi yang sangat luas seperti antioksidan, antiinflamasi dan antikanker. Hal ini penting
untuk mengatasi peningkatan ekspresi
transporter efluks dan meningkatkan sensitivitas sel kanker payudara terhadap antikanker dalam kemoterapi (Anuchapreeda et al, 2002).
Kurkumin adalah suatu senyawa polifenol, berupa pigmen berwarna kuning yang terdapat
dalam rhizome Curcuma longa. Kandungan
polifenol ini mengindikasikan bahwa kurkumin
dapat mencegah dan mengobati kanker.
Kurkumin bekerja dengan menurunkan ekspresi P-gp dan menurunkan efluks yang dimediasi oleh P-gp pada sel kanker yang resisten terhadap suatu obat. Kurkumin juga secara langsung berinteraksi dengan P-gp (Anuchapreeda et al, 2002, Aggarwal et al, 2003)
Wind (2011) dalam studinya menjelaskan bahwa kurkumin mampu menghambat overekspresi BCRP yang diinduksi oleh mitoxantrone dan pheophorbide A pada sel kanker payudara (MCF-7). Selain itu, Shukla (2009) juga telah meneliti tentang penghambatan transporter efluks BCRP oleh kurkumin pada mencit yang diinduksi sulfasalazin dan menyimpulkan bahwa kurkumin dapat meningkatkan absorbsi dan distribusi obat yang dipengaruhi oleh BCRP. Sugiarti (2012) telah melakukan penelitian mengenai pencegahan penurunan sensitivitas sel kanker payudara (MCF-7) terhadap tamoksifen oleh kurkumin. Penelitian tersebut menunjukkan bahwa telah terjadi penurunan sensitivitas sel dengan pemberian tamoksifen 1 µM selama 12 hari yang ditandai dengan peningkatan ekspresi mRNA P-gp dan viabilitas sel. Namun dengan pemberian kurkumin sejak awal, ekspresi P-gp dan viabilitas sel tersebut menurun.
Oleh karena itu, dalam penelitian ini kurkumin diharapkan dapat meningkatkan sensitivitas sel kanker payudara (MCF-7) terhadap pemberian
antikanker tamoksifen jangka panjang selama kurang lebih 10 pasasi. Di samping itu, ingin diketahui apakah peningkatan sensitivitas sel
tersebut diperantarai oleh penghambatan
transporter efluks P-gp dan BCRP oleh kurkumin.
METODE PENELITIAN Alat dan Bahan
Biosafety Cabinet Class II (Biohazard),
inkubator CO2 (Esco Memmert), mikroskop
inverted (Zeiss), Haemocytometer Improved
Neubauer Chamber, Thermo Scientific
Centrifuge Eppendorf Sorval® Legend Micro 17, Centrifuge Sorval® Legend RT, Biorad Chromo 4 Real Time PCR Detection System,
Ultrospec 4300 pro UV/Visible
Spectrophotometer, Microplate reader
Benchmark Biorad.
Galur sel kanker payudara MCF-7 (Makmal Terpadu Imunoendokrinologi FKUI). Tamoksifen (Santa Cruz (USA)). Kurkumin, verapamil, ritonavir dan dimethylsulfoxide (DMSO) (Sigma- Aldrich Ltd (Singapura)). Nelfinavir (PT Kimia Farma). Dulbecco Minimal Essential Medium (DMEM) dan Fetal Bovine
Serum (FBS), Penisilin/Streptomisin,
Gentamisin, Fungizone, Dubelco Phosphate Buffer Solution (D-PBS), dan Tryple Express (Gibco Ltd (Singapura)).
Reagen isolasi total RNA Mini Kit Tripure Isolation Reagent diperoleh dari Roche Diagnostics (Singapura). Primer P-gp, BCRP, dan β-mikroglobulin diperoleh dari 1st BASE
Pemaparan tamoksifen 1 µM pada sel MCF-7
Sel MCF-7 diberi perlakuan dengan
memaparkan tamoksifen 1 µM secara terus menerus selama 10 pasasi, sel ini selanjutnya dinamakan sel MCF-7(T).
Perlakuan sel MCF-7(T) dengan kurkumin
Sel MCF-7(T) dibagi menjadi beberapa
kelompok perlakuan antara lain pemberian tamoksifen 1 µM saja, pemberian kombinasi tamoksifen 1 µM dengan kurkumin 5;10;20 µM, kombinasi tamoksifen 1µM dengan verapamil 50
µM/ritonavir 15 µM/nelfinavir 15 µM,
pemberian kurkumin 5;10;20 µM saja, dan pemberian verapamil 50 µM, ritonavir 15 µM, nelfinavir 15 µM saja selama 5 hari. Analisis viabilitas sel dan ekspresi mRNA P-gp dan BCRP masing-masing kelompok perlakuan dilakukan pada hari ke-5. Masing-masing perlakuan dilakukan dalam dua kali percobaan rangkap dua.
Hitung sel menggunakan Tryphan Blue Exclusion Method
Sel yang telah konfluen 80-90%, dipanen dengan cara ditripsinisasi dengan menggunakan Tryple Express selama 5 menit, kemudian ditambahkan medium DMEM. Suspensi sel diambil sebanyak 20 µ L dan ditambahkan 10 µl trypan blue. Sel dihitung dengan menggunakan kamar hitung Neubaeuer. Sel yang dihitung adalah sel yang hidup yaitu sel yang tidak diwarnai oleh trypan blue.
Isolasi RNA
Sel yang telah konfluen dipanen dan RNA total diekstraksi menggunakan Tripure Isolation Reagent sesuai prosedur yang telah diberikan oleh produsen. Kadar RNA total dikuantifikasi menggunakan Spektrofotometer
Ultrospec 4300 pro UV/Visible dengan
mengukur serapan pada panjang gelombang 260 nm dikalikan dengan konstanta 40 ng/µl.
Analisis ekspresi mRNA P-gp dan BCRP menggunakan qRT PCR
Sekuens primer yang digunakan pada qRT PCR yaitu β2-microglobulin (F:5’
-CCAGCAGAGAATGGAAAGTC-3’; R:3’
-CATGTCTCGATCCCACTTAAC-5’), P-gp
(F:5’-CCCATCATTGCAATAGCAGG-3’;
R:3’-TGTTCAAACTTCTGCTCCTGA-5’),
BCRP F:5’A
GATGGGTTTCCAAGCGTTCAT-3’; R:3’ -CCAGTCCCAGTACGACTGTGACA-5’) (Albermann et al, 2005).
Sampel dipersiapkan dengan mencampurkan 200 nM masing-masing primer, 5 µ L KAPA SYBR® Fast qPCR Master Mix, 0,2 µ L KAPA RT Mix (50x), 0,2 µ L dUTP, 500 ng RNA template, dan RNAse free water hingga 10 µ L. Sampel kemudian diinkubasi pada mesin qRT-PCR dengan kondisi sebagai berikut: untuk sintesis
cDNA dilakukan pada suhu 42oC selama 5
menit, kemudian 5 menit pada suhu 95oC untuk inaktivasi enzim reverse transcriptase, dan 40 siklus yang terdiri dari 3 detik pada suhu 95oC untuk tahap denaturasi, 20 detik pada suhu 60oC untuk tahap annealing dan 20 detik pada suhu
72oC untuk tahap ekstensi. Setelah itu,
dilanjutkan untuk tahap melting curve yaitu dimulai pada suhu 60oC sampai dengan 95oC.
HASIL DAN PEMBAHASAN
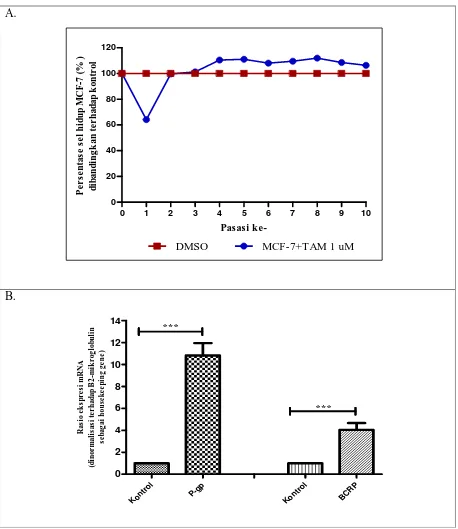
Pada pengamatan viabilitas sel MCF-7(T) menunjukkan bahwa tamoksifen masih dapat menekan pertumbuhan sel pada pasasi ke-1, namun mulai dari pasasi ke-2 efek tamoksifen menurun sehingga tidak dapat membunuh sel kanker (Gambar 1A). Terjadi peningkatan ekspresi mRNA transporter efluks P-gp dan BCRP pada sel MCF-7(T) yaitu berturut-turut sebesar 10.82 kali dan 4.04 kali dibandingkan terhadap kontrol (Gambar 1B).
Analisis viabilitas sel MCF-7(T)
A.
Gambar 1. (A). Persentase sel hidup MCF-7 yang dipaparkan dengan tamoksifen 1 µM pada pasasi ke-1 hingga pasasi ke-10. Kontrol adalah sel 7 yang dipaparkan DMSO. (B). Perubahan tingkat ekspresi mRNA P-gp dan BCRP pada sel
MCF-7(T). Kontrol adalah sel MCF-7 yang tidak diinduksi tamoksifen 1 µM. Tanda (***) menyatakan bermakna pada p<0,001 setelah uji ANOVA dilanjutkan dengan multiple comparison metode Tukey. Hasil disajikan dalam rerata ± SD yang
A.
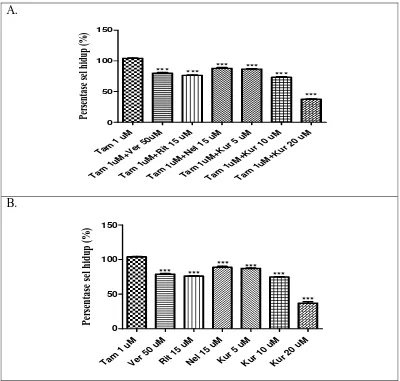
Gambar 2. Persentase sel hidup MCF-7(T) setelah pemaparan kurkumin selama 5 hari dengan atau tanpa pemberian tamoksifen. (A). Viabilitas sel MCF-7(T) setelah pemaparantamoksifen 1 µM + kurkumin 5/10/20 uM. (B). Viabilitas sel MCF-7(T) padapemaparan kurkumin 5;10;20 µM. Tiap percobaan merupakan hasil dari dua percobaan rangkap dua. Hasil
disajikan dalam rerata ± SD. Tanda (***) menyatakan bermakna pada p<0,001 setelah uji ANOVA dilanjutkan dengan multiple comparison metode Tukey dibandingkan terhadap tamoksifen 1 µM.
A2.
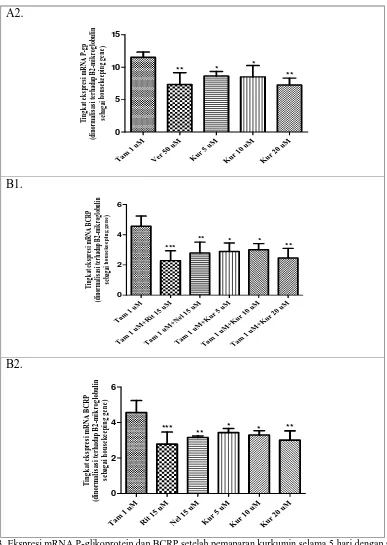
Gambar 3. Ekspresi mRNA P-glikoprotein dan BCRP setelah pemaparan kurkumin selama 5 hari dengan atau tanpa pemberian tamoksifen pada sel MCF-7(T). (A1). Ekspresi mRNA P-gp pada sel MCF-7(T) yang dipaparkan dengan tamoksifen 1 µM + kurkumin 5;10;20 uM. (A2). Ekspresi mRNA P-gp pada sel MCF-7(T) yang dipaparkan dengan kurkumin 5;10;20 uM. (B1). Ekspresi mRNA BCRP pada sel MCF-7(T) yang dipaparkan dengan tamoksifen 1 µM + kurkumin 5;10;20
uM. (B2). Ekspresi mRNA BCRP pada sel MCF-7(T) yang dipaparkan dengan kurkumin 5;10;20 uM. Tiap percobaan merupakan hasil dari dua percobaan rangkap dua. Hasil disajikan dalam rerata ± SD. Tanda (*) menyatakan bermakna pada
p<0,05; (**)/(***) bermakna pada p<0,001 setelah uji ANOVA dilanjutkan dengan multiple comparison metode Tukey
proporsional sesuai kadar, bermakna secara statistik. Penurunan viabilitas sel tertinggi dicapai pada kurkumin dengan dosis 20 µM yaitu sekitar 67%, lebih besar dibandingkan kontrol positif verapamil, nelfinavir, dan ritonavir yang hanya mampu menurunkan viabilitas sel berturut-turut sebesar 25%, 16%, dan 28% (Gambar 2).
Analisis ekspresi mRNA P-gp dan BCRP pada sel MCF-7(T)
Ekspresi mRNA P-gp dan BCRP pada sel MCF-7(T) yang diberi perlakuan dengan kurkumin pemberian kurkumin berbagai kadar termasuk
kontrol positif verapamil 50 µM baik
dikombinasi dengan atau tanpa tamoksifen, dapat menurunkan ekspresi P-gp. Pada hari ke-5, paparan kombinasi kurkumin dengan tamoksifen pada kadar yang lebih besar yaitu 10 µM dan 20 µM menurunkan ekspresi mRNA P-gp secara bermakna yaitu menjadi 5,5 kali dan 6
kali. Sedangkan pada kelompok yang
dipaparkan kurkumin saja, hanya kurkumin 20 µM yang dapat menurunkan ekspresi mRNA P-gp secara bermakna yaitu menjadi 7,25 kali. Kontrol positif verapamil 50 µM juga menurunkan ekspresi mRNA P-gp secara bermakna pada hari ke-5 (Gambar 3A1 dan 3A2).
Pada analisis ekpresi mRNA BCRP, pemberian kurkumin 5, 10, dan 20 µM dan kontrol positif ritonavir 15 µM dan nelfinavir 15 µM, baik dikombinasi dengan atau tanpa tamoksifen, sama-sama mempengaruhi ekspresi mRNA BCRP pada hari ke-5. Kombinasi kurkumin dengan tamoksifen dapat menurunkan ekspresi mRNA BCRP menjadi 2,46 kali pada dosis 20 µM sedangkan dengan paparan dengan kurkumin saja ekspresi mRNA BCRP menurun menjadi 3,01 kali. Kontrol positif ritonavir 15 µM dan nelfinavir 15 µM juga menurunkan
ekspresi mRNA BCRP secara bermakna pada hari ke-5 (Gambar 3B1 dan 3B2).
Meningkatnya viabilitas mulai dari pasasi ke-2 pada pemaparan tamoksifen 1 µM selama 10 pasasi (± 44 hari) pada galur sel kanker payudara MCF-7 menunjukkan bahwa sel MCF-7 telah menurun sensitivitasnya terhadap pemberian tamoksifen. Penurunan sensitivitas ini terlihat mulai pasasi ke-2 (hari ke-6) dan menetap hingga pasasi ke-10. Namun, model penelitian ini belum dapat memastikan apakah peningkatan viabilitas sel tersebut sudah stabil dan dapat dikatakan resisten karena waktu pemaparan tamoksifen yang relatif singkat. Hal ini sejalan dengan penelitian yang dilakukan Kurniawan et al (2012) dan Sugiarti et al (2012) dimana pemberian tamoksifen 1 µM sudah tidak dapat menekan pertumbuhan sel MCF-7 mulai pada hari ke-6. Penggunaan tamoksifen kadar 1 µM juga sejalan dengan penelitian Motahariet
al, 2005 pada sel kanker T47D dan
Lykkesfeldtet al, 1994 pada sel MCF-7 yang telah resisten terhadap tamoksifen. Keduanya menyatakan bahwa kadar tamoksifen 1 µM merupakan kadar dimana viabilitas sel masih cukup baik yaitu ± 65% pada T47D dan ± 50% pada sel MCF-7. Penelitian oleh Motahari et al
(2005), mengungkapkan untuk dapat
menghasilkan sel MCF-7 resisten yang stabil maka sel MCF-7 harus dipaparkan dengan tamoksifen minimal selama 3 bulan. Louieet al, 2010dalam penelitiannya juga mengembangkan sel MCF-7 yang resisten terhadap tamoksifen
(MCF-7 TamR) dengan memaparkan
tamoksifen pada konsentrasi 10 µM selama kurang lebih 6 bulan. Resistensi sel MCF-7TamR ini ditandai dengan cepatnya laju pertumbuhan sel dibandingkan dengan sel
MCF-7 apabila dipaparkan tamoksifen,
sedangkan pada kondisi normal tanpa paparan tamoksifen laju pertumbuhan sel MCF-7TamR dan MCF-7 sama.
Peningkatan ekspresi mRNA P-gp
sebesar 10,82 kali pada sel MCF-7(T) juga sejalan dengan penelitian Kurniawanet al, 2012
dan Sugiarti et al, 2012 dimana ekspresi mRNA
meningkat pada hari ke-6 sebesar 1,10 kali. Selain itu penelitian oleh Sane et al juga
menyatakan bahwa besarnya peningkatan
ekspresi mRNA P-gp pada sel hepatosit manusia HepG2 dan sel kanker kolon LS174T yang masing-masing dipaparkan tamoksifen pada kadar 1 µM, 2.5 µM, dan 5 µM selama 72 jam adalah berturut-turut sebesar 1.17 kali, 1.37 kali, dan 1.60 kali pada sel HepG2 dan 1.46 kali, 1.9 kali, dan 2.98 kali pada sel LS174T.
Penelitian ini menemukan bahwa
ekspresi mRNA BCRP pada sel MCF-7(T) meningkat sebesar 4.04 kali. Farabegoli et al, 2010 dalam penelitiannya, membuktikan bahwa pada sel MCF-7 yang resisten terhadap
tamoksifen terdapat peningkatan ekspresi
mRNA P-gp dan BCRP, kemudian setelah
diberi perlakuan dengan
Epigallocatechin-3-gallate (EGCG) pada dosis 100 ug/ml selama 48 jam maka ekspresi mRNA P-gp dan BCRP tersebut menurun sebesar 53% dan 20%. Jika dibandingkan dengan hasil yang didapat dalam penelitian ini, ditemukan bahwa lamanya paparan/induksi dengan tamoksifen sangat mempengaruhi peningkatan ekspresi mRNA P-gp dan BCRP. Semakin lama waktu induksi dengan tamoksifen, maka akan memberikan peningkatan ekspresi mRNA P-gp dan BCRP yang lebih tinggi.
Berdasarkan hasil yang diperoleh dari analisis viabilitas sel, efek pemberian kurkumin dengan maupun tanpa tamoksifen pada sel MCF-7(T) selama 5 hari membuktikan bahwa kurkumin mampu menekan viabilitas sel. Menurut Shehzad et al, 2010 kurkumin dapat menekan pertumbuhan sel kanker melalui berbagai cara seperti menghambat faktor transkripsi (NF-kB dan AP-1), menghambat enzim (COX-2 dan MMPs), menghambat sitokin dan STAT, menghambat cyclin D1, menginduksi apoptosis, dan lain sebagainya.
Pada analisis tingkat ekspresi mRNA P-gp dan BCRP, pemberian kombinasi kurkumin dengan tamoksifen lebih kuat menurunkan ekspresi mRNA P-gp dan BCRP dibandingkan terhadap pemberian kurkumin saja. Hasil ini menunjukkan bahwa kemungkinan pemberian
kombinasi kurkumin dengan tamoksifen
menghasilkan efek sinergis sehingga lebih kuat menekan ekspresi mRNA P-gp dan BCRP dibandingkan terhadap pemberian kurkumin saja. Jiang et al, 2013 dalam penelitiannya mengenai kurkumin meningkatkan sensitivitas tamoksifen pada sel kanker payudara MCF-7/LCC2 dan MCF-7/LCC9 mengemukakan bahwa pemberian kombinasi kurkumin dengan tamoksifen dapat meningkatkan sensitivitas sel MCF-7 terhadap tamoksifen sebesar 2.4 kali dibandingkan dengan pemberian tamoksifen saja.
Penurunan ekspresi mRNA P-gp dan BCRP oleh kurkumin dalam penelitian ini, tidak sebanding dengan penurunan viabilitas sel MCF-7 (T), baik pada pemberian kombinasi maupun dengan kurkumin saja. Berdasarkan hasil tersebut, maka dapat disimpulkan bahwa
pemberian kurkumin dapat meningkatkan
sensitivitas sel MCF-7 (T) terhadap tamoksifen, namun bukan hanya melalui penghambatan transporter efluks P-gp dan BCRP. Hal ini
kemungkinan disebabkan karena dosis
kurkumin yang digunakan kurang tinggi atau waktu paparan yang kurang lama sehingga efek kurkumin dalam menurunkan ekspresi mRNA P-gp dan BCRP belum terlihat maksimal. Selain
itu, diduga bahwa terdapat mekanisme
transporter lain yang mempengaruhi kerja kurkumin dalam menghambat P-gp dan BCRP tersebut. Chearwae et al, 2005 dalam studinya
menemukan bahwa kurkumin dapat
menurunkan ekspresi transporter efluks MRP-1 pada galur sel embrionik ginjal manusia HEK293 sehingga meningkatkan sensitivitasnya terhadap etoposide. Krisnamurti et al, 2013 dalam penelitiannya juga menunjukkan bahwa kurkumin mampu menurunkan ekspresi mRNA MRP-2 secara bermakna setelah pemaparan selama 5 hari.
pengikatan terhadap P-gp melalui fotoafinitas analog dari substrat, mengindikasikan bahwa kurkumin menghambat P-gp pada tahap imunoreaktif protein dan menurunkan ekspresi pada tahap mRNA. Selain itu, studi oleh
Aggarwal et al, 2006 melaporkan bahwa
kurkumin merupakan inhibitor yang sangat kuat
terhadap faktor transkripsi AP-1, yang
berkorelasi positif dalam mengatur ekspresi
P-gp. Pada penelitian Waiwut et al, 2002
dikatakan bahwa mekanisme kurkumin
menghambat P-gp kemungkinan karena
kurkumin dapat menghambat translokasi NF-kB dan aktivitas dan ekspresi dari c-jun/AP1.
Penelitian ini merupakan penelitian pertama yang meneliti tentang efek kurkumin dalam menghambat transporter efluks BCRP pada sel MCF-7 yang resisten terhadap
tamoksifen. Penelitian sebelumnya oleh
Chearwae et al, 2006 menyatakan bahwa
kurkumin merupakan penghambat fungsi BCRP yang poten, namun bukan bekerja pada tingkat protein tetapi kurkumin menstimulasi hidrolisis ATP dari transporter BCRP.
KESIMPULAN
Pemberian kurkumin dengan atau tanpa tamoksifen dapat mensensitisasi kembali sel kanker payudara MCF-7 terhadap tamoksifen sehingga menurunkan viabilitas sel dan ekspresi mRNA P-gp dan BCRP. Namun temuan ini
perlu diklarifikasi lebih lanjut dengan
melakukan pengukuran kadar tamoksifen
ekstraseluler untuk memastikan kerja
penghambatan P-gp dan BCRP oleh kurkumin. Hasil penelitian ini mendukung penggunaan kombinasi tamoksifen dan kurkumin pada sel kanker yang telah resisten.
DAFTAR PUSTAKA
Aggarwal, BB., Kumar, A., Bharti, AC. (2003). Anticancer Potential of Curcumin: Preclinical and Clinical Studies. Anticancer
Research, 23, 363-398.
Aggarwal, BB., Shishodia, S. (2006). Molecular targets of dietary agents for prevention and
therapy of cancer. Biochemical
Pharmacology, 7,1397-1413. relationship with the expression in intestine and liver. Biochemical Pharmacology, 70, 949-958.
Anuchapreeda, S., Leechanachai, P., Smith, MM., Ambudkar, SV., Limtrakul, P. (2002). Modulation of P-glycoprotein Expression and Function by Curcumin in Multidrug-Resistant Human KB Cells. Biochemical
Pharmacology, 64, 573-582.
Bansal, T., Jaggi, M., Khar, RK., Talegaonkar,S.. (2009). Emerging Significance of Flavonoids as P-glycoprotein Inhibitors in Cancer Chemoterapy. Journal of Pharmacy
&Pharmaceutical Sciences, 12, 46-78.
Chearwae, W., Wu, CP., Chu, HY., et al. (2005). Curcuminoids purified from turmeric powdermodulate the function of human multidrug resistance protein 1(ABCC1),
Cancer Chemotherapy and Pharmacology,
57, 376–388.
Chearwae, W., Shukla, S., Limtrakul, P., Ambudkar, SV. (2006). Modulation of the function of the multidrug resistance-linked ATP-binding cassete transporter ABCG2 by the cancer chemopreventive agent curcumin. Molecular
Cancer Therapeutics, 5(8),1995-2004.
Choi, HK., Yang, JW., Roh, SH., et al. (2007). Induction of Multidrug Resistance Associated Protein 2 in Tamoxifen-Resistant Breast Cancer Cells. Endocrine- Related
Cancer, 14, 293-303.
Ee, PLR., He, X., Ross, DD., Beck, WT. (2004). Modulation of Breast Cancer Resistance Protein (BCRP/ABCG2) Gene Expression Using RNA Interference. Molecular Cancer
Therapeutics, 3, 1577-1583.
Farabegoli, F., Papi, A., Bartolini, Ostan, R., Orlandi, M. (2010). (-)-Epigallocatechin-3-gallate downregulates P-gp and BCRP in a Tamoxifen Resistant MCF-7 Cell Line.
Phytomedicine, 17, 356-362.
death and restores tamoxifen sensitivity in the antiastrogen-resistant breast cancer cell lines MCF-7/LCC2 and MCF-7/LCC9.
Molecules, 18, 701-720.
Krisnamurti, DGB. (2013). Peningkatan Sensitivitas Sel Kanker Payudara Terhadap Antikanker
Tamoksifen oleh Kurkumin Melalui
Penghambatan Transporter Efluks: Studi in
vitro pada Sel MCF-7, Universitas
Indonesia, Jakarta.
Kurniawan, SV. (2012).Peran piperin sebagai
penghambat P-glikoprotein dalam
pencegahan resistensi sel kanker payudara
terhadap tamoksifen, Universitas Indonesia,
Jakarta.
Louie, MC., McClellan, A., Siewit, C. (2010). Estrogen receptor regulates E2F1 expression to mediate tamoxifen resistance. Molecular
Cancer Research, 8,343-352.
Lykkesfeldt, AE., Madsen, MW., Briand, P. (1994). Altered Expression of Estrogen Regulated Genes in a Tamoxifen Resistant and ICI 164,384 and ICI 182,780 Sensitive Human Breast Cancer Cell Line, MCF-7/TAMR-1.
Cancer Research, 54, 1587-1595.
Mao, Q., Unadkat, JD. (2005). Role of the Breast Cancer Resistance Protein (ABCG2) in Drug Transport. American Association
ofPharmaceuticalScientistsJournal, 7,
E118-129.
Motahari, Z., Etebary, M., Azizi, E. (2005). Studying the role of P-glycoprotein in resistance to tamoxifen in human breast
cancer T47D cells by
immunocytochemistry,International Journal
of Pharmacology, 1, 112-117.
Ring, A., Dowset, M. (2004). Mechanism of Tamoxifen Resistance. Endocrine- Related
Cancer, 11, 643-648.
Shukla, S., Zaher, H., Hartz A, Bauer, B., Ware, JA., Ambudkar, SV. (2009). Curcumin Inhibits the Activity of ABCG2/BCRP1,A Multidrug Resistance-Linked ABC Drug Transporter in Mice. Pharmaceutical Research, 26 (2), 480-486.
Sugiarti, L. (2012). Penghambatan MDR1 dengan Kurkumin Sebagai Usaha Pencegahan
Resistensi Terhadap Antikanker Tamoksifen,
Universitas Indonesia, Jakarta..
Sane, RS., Buckley, DJ., Buckley, AR., Nallani, SC., Desai, PB. (2008). Role of human pregnane X receptor in tamoxifen and
4-hydroxytamoxifen-mediated CYP3A4 induction in primary human hepatocytes and LS174T cells. The Journal of Pharmacology
and Experimental Therapeutics, 36,
946-954.
Shehzad, A., Wahid, F., Lee, YS. (2010). Curcumin in cancer chemoprevenion: Molecular targets, pharmacokinetics, bioavailability, and clinical trials.Arch Pharm Chemistry In
Life Sciences, 9, 489-499.
University of California - San Francisco. (2011, November 14).Tamoxifen Resistance and How to Defeat it. ScienceDaily, Retrieved from
http://www.sciencedaily.com/releases/2011/ 11/111113141409.htm
Waiwut, P., Anuchapreeda, S., Limtrakul, P. (2002). Curcumin inhibit the P-glycoprotein level in carcinoma of cervix cells (KB-carcinoma cell lines) induced by vinblastine. Chiang
Mai MedicalJournal, 41, 139-145.
Wind, NS., &Holen, I. Multidrug Resistance in Breast Cancer: From In Vitro Models to Clinical Studies. (2011). International
Journal of Breast Cancer, 2011, 1-10.
Zhou, G., & Zhang, X. (2012). Multidrug Resistance
and Breast Cancer, Targeting New
Pathways and Cell Death in Breast Cancer.
Available from