STUDI KONDUKTIVITAS FILM ELEKTROLIT POLIMER KITOSAN/PEG+KCl
MUHAMAR KADAPI
DEPARTEMEN FISIKA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM INSTITUT PERTANIAN BOGOR
BOGOR 2013
PERNYATAAN MENGENAI SKRIPSI DAN
SUMBER INFORMASI SERTA PELIMPAHAN HAK CIPTA
Dengan ini saya menyatakan bahwa skripsi Studi Konduktivitas Film Elektrolit Polimer Kitosan/PEG+KCl adalah benar karya saya dengan arahan dari komisi pembimbing dan belum diajukan dalam bentuk apa pun kepada perguruan tinggi mana pun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir skripsi ini.Dengan ini saya melimpahkan hak cipta dari karya tulis saya kepada Institut Pertanian Bogor.
Bogor,Mei 2013 Muhamar Kadapi NIM G74080018
ABSTRAK
MUHAMAR KADAPI. Studi Konduktivitas Film Elektrolit Polimer Kitosan/PEG+KCl. Dibimbing oleh AKHIRUDDIN dan IRMANSYAH.
Elektrolit polimer padat dapat dikelompokkan sebagai bahan padat yang memiliki kemampuan untuk menghantarkan arus listrik dengan cara pergerakan ion dan memiliki fungsi yang sama seperti larutan elektrolit. Telah dihasilkan film elektrolit polimer kitosan/PEG+KCl. Proses pembuatan dilakukan dengan pencampuran larutan asam asetat dengan kitosan, PEG dan garam Kalium Chloride (KCl), untuk selanjutnya dicetak menjadi film ektrolit polimer. Film elektrolit polimer dengan konduktivitas konduktivitas yang paling baik dikarakterisasi lebih lanjut yaitu analisis FTIR untuk diidentifikasi gugus fungsinya. Hasil analisis FTIR menunjukkan bahwa telah terbentuk kompleks elektrolit polimer kitosan/PEG+KCl. Konduktivitas terbaik kitosan/PEG+KCl didapat pada sampel F dengan penambahan 45% wt KCl, sebesar 5.786 x 10-6 Scm-1. Energi aktivasi diperoleh dengan menggunakan plot Arhennius, energi aktivasi sampel dengan konduktivitas yang paling baik adalah sebesar 0.270 eV.
Kata kunci: Energi aktivasi, film elektrolit polimer,PEG, plot Arrhenius
ABSTRACT
Muhamar Kadapi Studies. Conductivity Studies of Film Electrolyte Chitosan/PEG+KCl. Guided by AKHIRUDDIN and IRMANSYAH.
Solid polymer electrolyte can be classified as a solid material that has the ability to conduct electric current by the movement of ions and has the same functions as an electrolyte solution. Polymer electrolyte film based on chitosan/PEG+KCl have been produced. The process of making is done by mixing a solution of acetid acid with chitosan, PEG and Potassium Chloride (KCl), polymer electrolyte were obtained by the casting technique. Polymer electrolyte with good ionic conductivity properties were characterized by FTIR analysis for the identification of the functional group. The results of FTIR analysis indicates that complexes of polymer electrolyte have formed. The best ionic conductivity values of 5.786 x 10-6 Scm-1 were obtained for the sample containing 45%wt of KCl. Activation energy obtained by using Arrhenius plot, activation energy from polymer electrolyte film with good conductivity is 0.270 eV.
STUDI KONDUKTIVITAS ELEKTROLIT POLIMER KITOSAN/PEG+KCl
MUHAMAR KADAPI
Skripsi
sebagai salah satu syarat untuk memperoleh gelar Sarjana Sains
pada Departemen Fisika
DEPARTEMEN FISIKA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM INSTITUT PERTANIAN BOGOR
Judul Skripsi : Studi Konduktivitas Elektrolit Polimer Kitosan/PEG+KCl
Nama : Muhamar Kadapi
NIM : G74080018
Disetujui oleh
Dr.Akhiruddin Maddu. S.Si.M.Si Dr.Ir. Irmansyah. M.Si
Pembimbing 1 Pembimbing 2
Diketahui oleh
Dr.Akhiruddin Maddu, S.Si.M.Si Ketua Departemen Fisika
PRAKATA
Puji dan syukur kehadirat Allah SWT, karena berkat rahmat dan hidayah-Nya penulis dapat menyelesaikan peneltian dengan judul “Studi Konduktivitas Film Elektrolit Polimer Kitosan/PEG+KCl”.
Sebagai salah satu syarat kelulusan program sarjana di Departemen Fisika Institut Pertanian Bogor. Penulis mengucapkan terima kasih kepada pihak-pihak yang telah membantu dan membimbing dalam penulisan skripsi ini. diantaranya kepada :
1. Allah SWT yang memberikan banyak rahmat dan kasih sayang kepada penulis selaku hamba-Nya.
2. Kedua orang tua saya Bapak Buhari Lubis dan Ibu Murniati Matjik yang selalu memberikan dukungan dan semangat.
3. Bapak Dr.Akhiruddin Maddu. S.Si M.Si dan Bapak Dr.Irmansyah. M.Si selaku dosen pembimbing yang sudah memberikan banyak dukungan dan arahan sehingga penelitian ini dapat diselesaikan.
4. Kakak-kakak penulis, Dian, Yuli, Apri, dan Ratna terimakasih untuk motivasi dan perhatiannya serta keluarga besar penulis.
5. Teman-teman kelompok PKM Superkapasitor (Doni, Khakim, Zainal, dan Firda) yang banyak membantu dalam menjalankan penelitian ini. 6. Teman-teman fisika (Yasin, Rizki, Pandu, Luthfi, Afif, Haqqie, Yuas,
Jalimas, dan Mulyana)
7. Semua pihak yang telah membantu yang tidak bisa penulis ucapkan satu persatu, terimakasih banyak atas dukungannya.
Penulis menyadari dalam tulisan ini masih terdapat kekurangan, oleh karena itu penulis mengharapkan saran dan kritik yang membangun untuk hasil yang lebih baik. Semoga penelitian ini dapat memberikan manfaat.
Bogor, Mei 2013
DAFTAR ISI
DAFTAR TABEL vi DAFTAR GAMBAR vi DAFTAR LAMPIRAN vi PENDAHULUAN 1 Latar Belakang 1 Rumusan Masalah 2 Tujuan Penelitian 2 Hipotesis 2 TINJAUAN PUSTAKA 3Elektrolit Polimer Padat 3
Konduktivitas Ionik 3
Persamaan Arrhenius 4
Kitosan 4
PEG 4
BAHAN DAN METODE 6
Waktu dan TempatPenelitian 6
Alat dan Bahan 6
Metode Penelitian 6
Pembuatan film kitosan/PEG+KCl 6 Pengukuran konduktivitas film kitosan/PEG+KCl 6 Analisis spektrofotometri FTIR film kitosan/PEG+KCl 7
HASIL DAN PEMBAHASAN 9
Konduktivitas ionik film kitosan/PEG+KCl 9
Pengaruh suhu terhadap konduktivitas film kitosan/PEG+KCl 10 Energi aktivasi film kitosan/PEG+KCl 12 Analisa spektrofotometri FTIR film kitosan/PEG+KCl 14
KESIMPULAN 20
SARAN 20
DAFTAR PUSTAKA 21
DAFTAR TABEL
1 Kombinasi bahan yang digunakan dalam pembuatan
Film elektrolit polimer 7
2 Karakterisasi sampel film elektrolit polimer 8 3 Energi aktivasi elektrolit polimer kitosan/PEG+KCl 13 4 Data identifikasi gugus fungsi kitosan 16 5 Data identifikasi gugus fungsi kitosan/PEG 19 6 Data identifikasi gugus fungsi kitosan/PEG+KCl 19
DAFTAR GAMBAR
1 Struktur kimia kitosan 4
2 Struktur kimia PEG 5
3 Diagram alir penelitian 8
4 Variasi konduktivitas ionik elektrolit polimer kitosan/PEG
(60:40) terhadap persentase penambahan KCl (% wt) 9 5 Kurva Hubungan konduktivitas ionik kitosan/PEG terhadap suhu 11 6 Plot arrhenius sampel A, D dan F 13 7 Kurva energi aktivasi sampel A, D dan F 14
8 Spektrum FTIR Kitosan 16
9 Spektrum FTIR Kitosan/PEG 18
10 Spektrum FTIR Kitosan/PEG+KCl 19
DAFTAR LAMPIRAN
1 Gambar alat dan bahan yang digunakan dalam penelitian 24 2 Tahap pembuatan film elektrolit polimer kitosan/PEG+KCl 25 3 Nilai konduktivitas ionik film polimer elektrolit kitosan/PEG
+KCl 27
4 Variasi konduktivitas ionik sampel A terhadap suhu 28 5 Perhitungan plot Arrhenius elektrolit polimer sampel A 28
6 Cara menghitung energi aktivasi elektrolit polimer sampel A
dari plot Arrhenius 29
7 Variasi konduktivitas ionik sampel D terhadap suhu 30
8 Perhitungan plot Arrhenius elektrolit polimer sampel D 30
9 Cara menghitung energi aktivasi elektrolit polimer sampel D dari plot Arrhenius 31
10 Variasi konduktivitas ionik sampel F terhadap suhu 32
11 Perhitungan plot Arrhenius elektrolit polimer sampel F 32
12 Cara menghitung energi aktivasi elektrolit polimer sampel F dari plot Arrhenius 33
13 Spektrum hasil analisa FTIR kitosan 34
14 Spektrum hasil analisa FTIR sampel A 34
PENDAHULUAN
Latar Belakang
Elektrolit polimer merupakan suatu disiplin ilmu yang mempelajari tentang material, mencakup aspek elektrokimia, sains polimer, kimia organik, dan kimia non-organik. Sejak dua dekade yang lalu, berbagai modifikasi elektrolit polimer gencar dilakukan agar dihasilkan suatu bahan polimer yang konduktif.1 Saat ini penelitian elektrolit padat dengan bahan polimer telah banyak dilakukan.
Banyak keunggulan dari penggunaan elektrolit polimer pada perangkat elektronik seperti tidak mudah bocor, bebas dari pelarut, bentuknya stabil, penanganannya mudah dan kestabilan elektrokimianya melebihi elektrolit cair.2
Bahan polimer alam saat ini banyak diteliti untuk dijadikan sebagai elektrolit polimer karena sifatnya yang ramah lingkungan. Bahan polimer alam yang saat ini banyak diteliti salah satunya adalah kitosan karena sifatnya yang polielektrolit kationik karena adanya gugus amino, biodegradable, dan bisa membentuk film.3
Kitosan juga berperan sebagai polimer media untuk elektrolit karena kitosan dapat melarutkan garam-garam ionik untuk meningkatkan konduktivitas ioniknya.2 Kitosan dapat dimodifikasi dengan cara dicampur dengan polimer lain seperti polivinil alkohol (PVA) dan polietilen glikol (PEG). Campuran kitosan/PEG dapat dimanfaatkan sebagai elektrolit polimer untuk berbagai macam aplikasi. Hal ini dapat dilihat dari kedua sifat bahan tersebut. Kitosan bersifat polielektrolit kationik karena adanya gugus amino, biodegradable, bisa membentuk film dan bisa berfungsi sebagai agen pengkelat ion logam.3 Sedangkan PEG memiliki sifat mekanik yang bagus dan mampu terdegradasi alami pada kondisi tertentu. Beberapa penelitian menyatakan bahwa penambahan PEG dapat memperbaiki elastisitas dari kitosan.4
Pada penelitian ini akan dilakukan proses pembuatan film polimer elektrolit berbasis polimer kitosan/PEG dengan perbandingan 60:40 yang akan divariasikan dengan berbagai konsentrasi garam Kalium Chloride (KCl) sehingga akan didapatkan film polimer elektrolit dengan konduktivitas optimum.
Tujuan Penelitian
1. Membuat film elektrolit polimer campuran kitosan/PEG dengan penambahan garam KCl.
2. Mengkarakterisasi film elektrolit campuran kitosan/PEG terhadap penambahan garam KCl, meliputi konduktivitas, struktur kimia, dan energi aktivasi.
Perumusan Masalah
1. Bagaimana pengaruh penambahan KCl terhadap nilai energi aktivasi dari elektrolit polimer?
2. Bagaimana pengaruh penambahan KCl terhadap nilai konduktivitas elektrolit polimer?
Hipotesis
Nilai konduktivitas optimum elektrolit polimer kitosan/PEG+KCl terdapat pada penambahan konsentrasi KCl pada rentang 35 - 55% wt.
TINJAUAN PUSTAKA
Elektrolit Polimer Padat
Elektrolit polimer padat dapat dikelompokkan sebagai bahan padat yang dapat menghantarkan arus listrik dengan cara pergerakan ion dan memiliki fungsi yang sama seperti larutan elektrolit.3 Polimer elektrolit padat memiliki banyak keunggulan seperti tidak mudah bocor, bentuknya stabil, bebas dari pelarut, penanganannya mudah dan kestabilan elektrokimianya melebihi elektrolit cair.2 Untuk mendapatkan nilai konduktivitas ionik yang tinggi pada sistem polimer dapat disiasati dengan menambahkan berbagai bahan tambahan seperti bahan anorganik ke dalam matriks polimer tersebut.3
Konduktivitas Ionik
Konduktivitas listrik muncul karena adanya migrasi ion atau migrasi elektron. Konduktivitas elektronik adalah konduktivitas listrik yang disebabkan oleh migrasi elektron-elektron. Sedangkan konduktivitas ionik adalah konduktivitas yang terjadi karena adanya migrasi ion-ion. Konduktivitas ionik elektrolit polimer bergantung pada kemampuan host polimer melarutkan garam-garam ionik.5
Nilai konduktivitas listrik dapat diperoleh menggunakan persamaan.
𝜎 = 𝐺(𝐿𝐴) (1)
Keterangan :
𝜎 = Konduktivitas (siemens/cm) G = Konduktansi (siemens) L = Tebal bahan (cm)
Persamaan Arrhenius
Mekanisme konduktivitas ionik pada elektrolit polimer dapat ditentukan berdasarkan pada grafik konduktivitas ionik (σ) terhadap suhu (T)3 yang diberikan oleh persamaan Arrhenius :
𝜎 = 𝜎0𝑒𝑥𝑝 [−𝐸𝑎
𝑘𝑇] (2)
Keterangan
σ0 = konduktivitas pada suhu kamar
Ea = Energi aktivasi
k= konstanta Boltzmann T = suhu
Kitosan
Kitosan adalah suatu biopolimer dari D-glukosamin yang diperoleh melalui deasetilasi kitin dengan menggunakan alkali kuat.7 Struktur kimia dari kitosan dapat dilihat pada Gambar 1 berikut:
Gambar 1 Struktur kimia kitosan.7
Secara umum kitosan berbentuk padatan amorf yang berwarna putih dengan struktur kristal yang tidak berubah dari bentuk kitin mula-mula. Kelarutan kitosan yang paling baik adalah dalam larutan asam asetat 1%.8
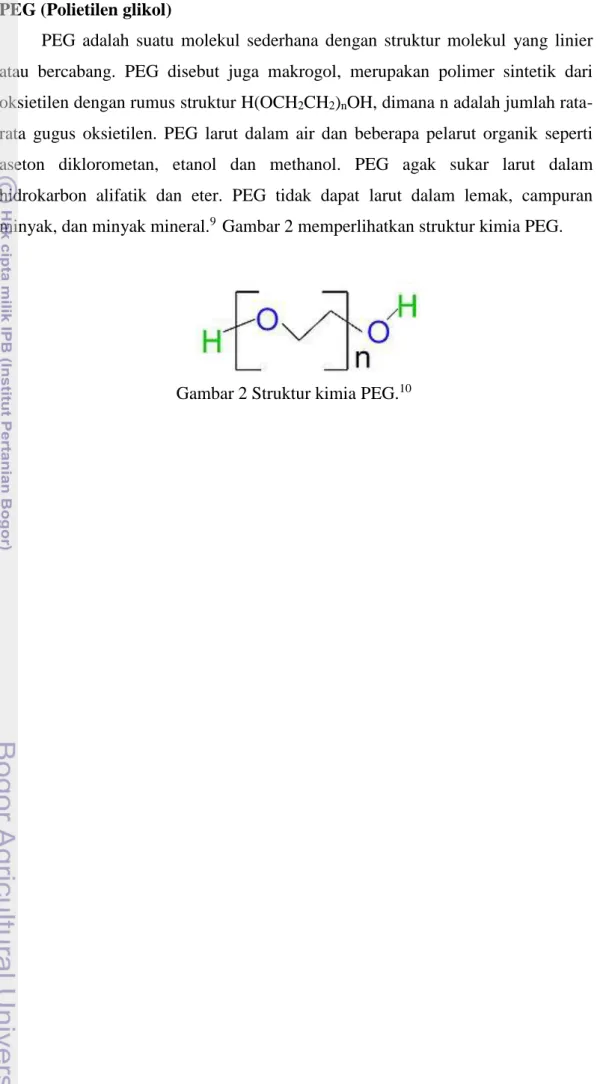
PEG (Polietilen glikol)
PEG adalah suatu molekul sederhana dengan struktur molekul yang linier atau bercabang. PEG disebut juga makrogol, merupakan polimer sintetik dari oksietilen dengan rumus struktur H(OCH2CH2)nOH, dimana n adalah jumlah
rata-rata gugus oksietilen. PEG larut dalam air dan beberapa pelarut organik seperti aseton diklorometan, etanol dan methanol. PEG agak sukar larut dalam hidrokarbon alifatik dan eter. PEG tidak dapat larut dalam lemak, campuran minyak, dan minyak mineral.9 Gambar 2 memperlihatkan struktur kimia PEG.
BAHAN DAN METODE
Waktu dan Tempat Penelitian
Penelitian ini dilakukan di Laboratorium Biofisika Material dan Laboratorium Analisis Bahan Departemen Fisika IPB, dari bulan Juli 2012 sampai Maret 2013.
Bahan dan Alat
Bahan-bahan yang digunakan dalam penelitian ini adalah kitosan, polietilen glikol, aquades, asam asetat 1%, dan garam KCl. Alat yang digunakan dalam penelitian ini adalah neraca analitik, gelas piala, pipet tetes, gelas ukur Iwaki 10 ml, hot plate stirrer, mikrometer sekrup, potensiometer, dan LCR meter Hitester 3522-50. Alat karakterisasi FTIR yang digunakan adalah FTIR ABB series 3200.
Metode Penelitian
Pembuatan Film Kitosan/PEG+KCl
Kitosan sebanyak 0.3 gram dicampur dengan 0.2 gram PEG. Campuran kitosan/PEG dilarutkan dalam 10 ml asam asetat 1%, proses pencampuran dilakukan dengan menggunakan hot plate stirrer pada putaran 350 rpm dengan suhu 600 C selama 90 menit sampai campuran homogen. Setelah campuran homogen, suhu diturunkan menjadi suhu ruang, campuran kitosan/PEG yang telah homogen ditambahkan KCl dengan variasi konsentrasi 0% wt, 5% wt, 15% wt, 25% wt, 35% wt, 45% wt, dan 55% wt, proses pencampuran dilakukan selama ± 6 jam. Campuran kitosan/PEG+KCl yang telah homogen didinginkan pada suhu ruang sehingga mengering dan membentuk film elektrolit polimer. Film elektrolit polimer kemudian diukur konduktivitasnya. Kombinasi bahan yang digunakan dalam penelitian dapat dilihat pada Tabel 1.
Tabel 1 Kombinasi bahan yang digunakan dalam pembuatan film elektrolit polimer
Kode sampel Kitosan (g) PEG (g)
Asam asetat 1% (mL) Garam KCl (g) A 0.3 0.2 10 - B 0.3 0.2 10 0.005 C 0.3 0.2 10 0.015 D 0.3 0.2 10 0.025 E 0.3 0.2 10 0.035 F 0.3 0.2 10 0.045 G 0.3 0.2 10 0.055
Pengukuran Konduktivitas Film Kitosan/PEG+KCl
Nilai Konduktivitas listrik diukur dengan menggunakan LCR Meter Hitester 3522-50. Besarnya nilai konduktivitas listrik diperoleh dengan mencari nilai konduktansinya. Tahap pengukuran meliputi elektrolit polimer dipotong dengan ukuran 2x2 cm2, kemudian dijepit pada plat pengukur konduktivitas sebagai elektrodanya, frekuensi yang digunakan adalah 1 KHz.11
Film elektrolit kitosan/PEG+KCl dengan nilai konduktivitas optimum akan dikarakterisasi lebih lanjut, karakterisasi yang dilakukan yaitu analisis FTIR.
Analisis Spektrometri FTIR Film Kitosan/PEG+KCl
Analisis struktur film elektrolit polimer dilakukan dengan spektroskopi FTIR. Pengukuran dilakukan dengan menggunakan panjang gelombang 4000 sampai 500 cm-1 resolution dengan FTIR ABB series 3200. Spektrum FTIR dinormalisasi dan band getaran utama telah diidentifikasi terkait dengan kelompok kimia utama yang terbentuk. Hasil analisis diharapkan menunjukkan sinyal yang khas untuk spektrum elektrolit polimer.3
Tabel 2 Karakterisasi sampel film elektrolit polimer Kode sampel Penambahan KCl Karakterisasi (% wt) Konduktivitas Konduktivitas terhadap suhu Analisis FTIR A 0 v v v B 5 v C 15 v D 25 v v E 35 v F 45 v v v G 55 v
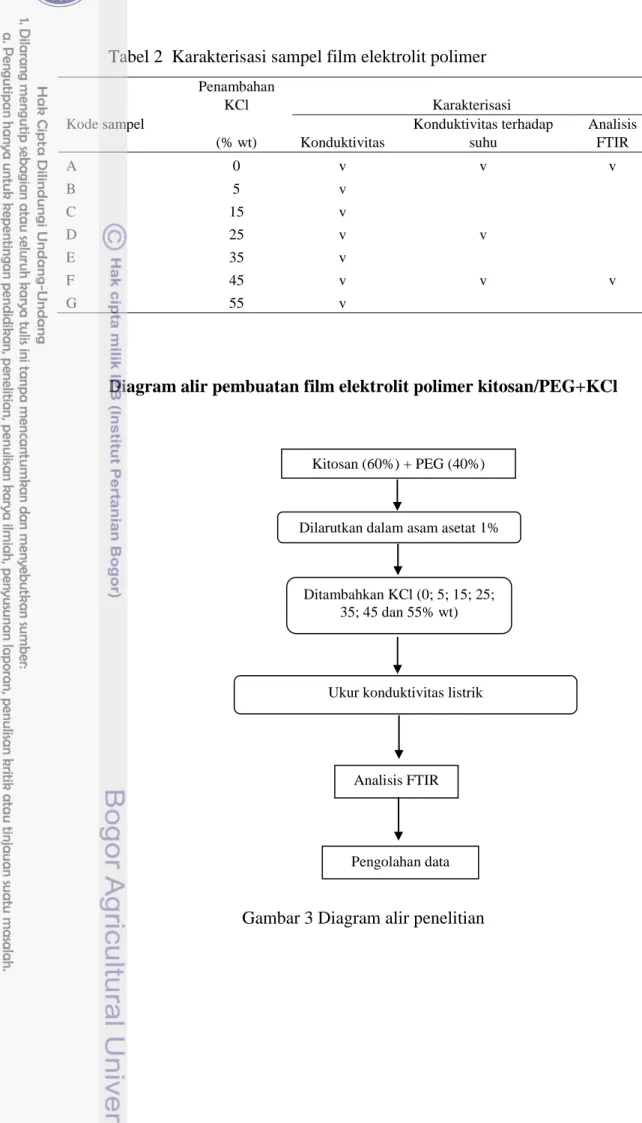
Diagram alir pembuatan film elektrolit polimer kitosan/PEG+KCl
Gambar 3 Diagram alir penelitian
Analisis FTIR
Pengolahan data Kitosan (60%) + PEG (40%)
Dilarutkan dalam asam asetat 1%
Ditambahkan KCl (0; 5; 15; 25; 35; 45 dan 55% wt)
HASIL DAN PEMBAHASAN
Konduktivitas ionik film elektrolit kitosan/PEG+KCl
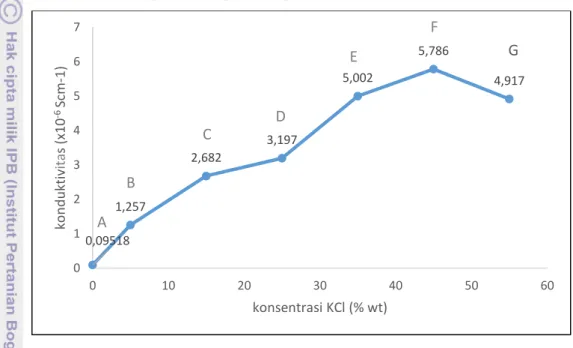
Konduktivitas ionik merupakan salah satu parameter penting dari suatu elektrolit polimer. Pengaruh penambahan garam KCl terhadap konduktivitas ion yang dihasilkan sampel A sampai G dapat dilihat pada Gambar 4.
Gambar 4 Konduktivitas ionik elektrolit polimer kitosan/PEG terhadap persentase penambahan KCl (% wt)
Gambar 4 memperlihatkan nilai konduktivitas ionik meningkat dengan semakin meningkatnya konsentrasi KCl pada rentang 0-45% wt yang ditambahkan pada host polimer kitosan/PEG. Adanya peningkatan konduktivitas ion tersebut akibatnya meningkatnya mobilitas ion-ion seiring meningkatnya konsentrasi KCl. Konduktivitas ionik pada elektrolit polimer umumnya dipengaruhi oleh jumlah ion yang bergerak dan pergerakan dari ion tersebut.12
Konduktivitas ionik yang didapat pada kitosan/PEG tanpa penambahan KCl sebesar 9.380 x 10-8 Scm-1, nilai ini lebih besar dibandingkan dengan
konduktivitas ionik elektrolit polimer PEG murni yang telah dilakukan Polu and Kumar, yaitu sebesar 4.033 x 10-8 Scm-1. Penambahan kitosan pada PEG terbukti dapat meningkatkan konduktivitas ionik elektrolit polimer karena kitosan sendiri merupakan polimer yang bersifat polielektrolit.3
0,09518 1,257 2,682 3,197 5,002 5,786 4,917 0 1 2 3 4 5 6 7 0 10 20 30 40 50 60 ko n d u kt iv ita s (x10 -6 Scm -1) konsentrasi KCl (% wt) A B C D E F G
Nilai konduktivitas optimum elektrolit campuran kitosan/PEG+KCl didapat pada sampel F yaitu pada sampel dengan penambahan KCl 45% wt sebesar 5.786 x 10-6 Scm-1. Penambahan KCl dengan persentase optimum akan menghasilkan elektrolit polimer dengan konduktivitas ionik paling tinggi. Persentase KCl yang paling baik tergantung pada polimer yang digunakan. Polimer yang berbeda akan memiliki persentase penambahan KCl yang berbeda pula.3 Hal ini karena host polimer memiliki kemampuan yang berbeda dalam melarutkan garam-garam.5
Penambahan KCl pada batas tertentu mengakibatkan penurunan nilai konduktivitas ionik elektrolit polimer kitosan/PEG. Pada Gambar 4 dapat dilihat pada sampel G atau sampel pada penambahan KCl lebih dari 45% wt menghasilkan elektrolit polimer dengan konduktivitas ionik yang menurun, hal ini disebabkan elektrolit polimer dalam komposisi yang mencapai batas komposisi jenuh. Konsentrasi ion yang tinggi dalam polimer dapat menghambat pergerakan ion-ion tersebut dan menyebabkan kekakuan pada rantai polimer yang mengakibatkan menurunnya nilai konduktivitas ionik elektrolit polimer.14 Selain
itu jarak antara ion-ion pada suatu polimer yang terlalu rapat akan menurunkan nilai konduktivitas ionik elektrolit polimer tersebut, karena dapat terjadi penggabungan ion dan membentuk pasangan ion netral yang tidak memberikan kontribusi terhadap konduktivitas.11
Pengaruh suhu terhadap konduktivitas ionik
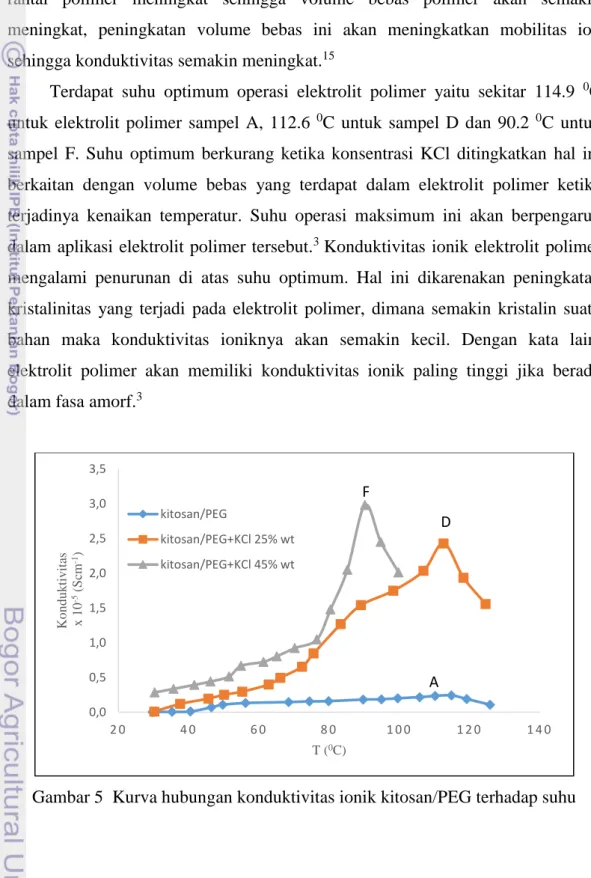
Hubungan konduktivitas ionik elektrolit polimer kitosan/PEG+KCl terhadap suhu dapat dilihat pada Gambar 5, yang memperlihatkan bahwa konduktivitas ionik semakin tinggi ketika suhu dinaikkan sampai batas tertentu. Pada Gambar 5, kurva A merupakan kurva elektrolit polimer sampel A (tanpa penambahan KCl), sampel A menghasilkan nilai konduktivitas yang lebih rendah selain itu perubahan nilai konduktivitas sampel A cenderung lebih lambat. Kurva D merupakan kurva elektrolit polimer sampel D (penambahan KCl 25% wt), yang memperlihatkan bahwa terjadi perubahan nilai konduktivitas yang cukup ekstrim pada suhu diatas 66.1 0C, perubahan nilai konduktivitas pada suhu dibawah 66.1
0C relatif lambat. Kurva F merupakan kurva elektrolit polimer sampel F
(penambahan KCl 45% wt), sampel F merupakan sampel dengan konduktivitas optimum.
Pada kurva F terjadi perubahan nilai yang ekstrim pada suhu diatas 70.2 0C, pada suhu dibawah 70.2 0C perubahan nilai konduktivitasnya relatif lambat. Peningkatan konduktivitas terhadap suhu dapat dihubungkan dengan meningkatnya flexibilitas rantai polimer tersebut.15 Pada suhu tinggi, flexibilitas rantai polimer meningkat sehingga volume bebas polimer akan semakin meningkat, peningkatan volume bebas ini akan meningkatkan mobilitas ion sehingga konduktivitas semakin meningkat.15
Terdapat suhu optimum operasi elektrolit polimer yaitu sekitar 114.9 0C untuk elektrolit polimer sampel A, 112.6 0C untuk sampel D dan 90.2 0C untuk sampel F. Suhu optimum berkurang ketika konsentrasi KCl ditingkatkan hal ini berkaitan dengan volume bebas yang terdapat dalam elektrolit polimer ketika terjadinya kenaikan temperatur. Suhu operasi maksimum ini akan berpengaruh dalam aplikasi elektrolit polimer tersebut.3 Konduktivitas ionik elektrolit polimer
mengalami penurunan di atas suhu optimum. Hal ini dikarenakan peningkatan kristalinitas yang terjadi pada elektrolit polimer, dimana semakin kristalin suatu bahan maka konduktivitas ioniknya akan semakin kecil. Dengan kata lain, elektrolit polimer akan memiliki konduktivitas ionik paling tinggi jika berada dalam fasa amorf.3
Gambar 5 Kurva hubungan konduktivitas ionik kitosan/PEG terhadap suhu
0,0 0,5 1,0 1,5 2,0 2,5 3,0 3,5 2 0 4 0 6 0 8 0 1 0 0 1 2 0 1 4 0 Ko n d u k ti v it as x 10 -5 (S cm -1) T (0C) kitosan/PEG kitosan/PEG+KCl 25% wt kitosan/PEG+KCl 45% wt A D F
Energi aktivasi kitosan/PEG+KCl
Energi aktivasi (Ea) adalah energi minimum yang dibutuhkan agar suatu
reaksi kimia dapat berlangsung. Kata aktivasi memiliki makna bahwa suatu reaksi kimia membutuhkan tambahan energi untuk dapat berlangsung.16 Hubungan
energi aktivasi dengan laju reaksi adalah berbanding terbalik. Semakin besar energi aktivasi maka laju reaksinya semakin lambat karena energi minimum untuk terjadi reaksi semakin besar.16
Perubahan suhu dapat mempengaruhi nilai konduktivitas. Jika suhu dinaikkan sampai batas tertentu maka nilai konduktivitas akan meningkat. Hal ini terjadi karena semakin tinggi suhu maka energi kinetik suatu partikel akan meningkat, sehingga pergerakan partikel akan semakin meningkat. Ini membuktikan bahwa semakin tinggi suhu maka energi aktivasinya akan semakin kecil sehingga akan memperbesar harga laju reaksi. Hal ini sesuai dengan teori dimana energi aktivasi berbanding terbalik dengan laju reaksi.16
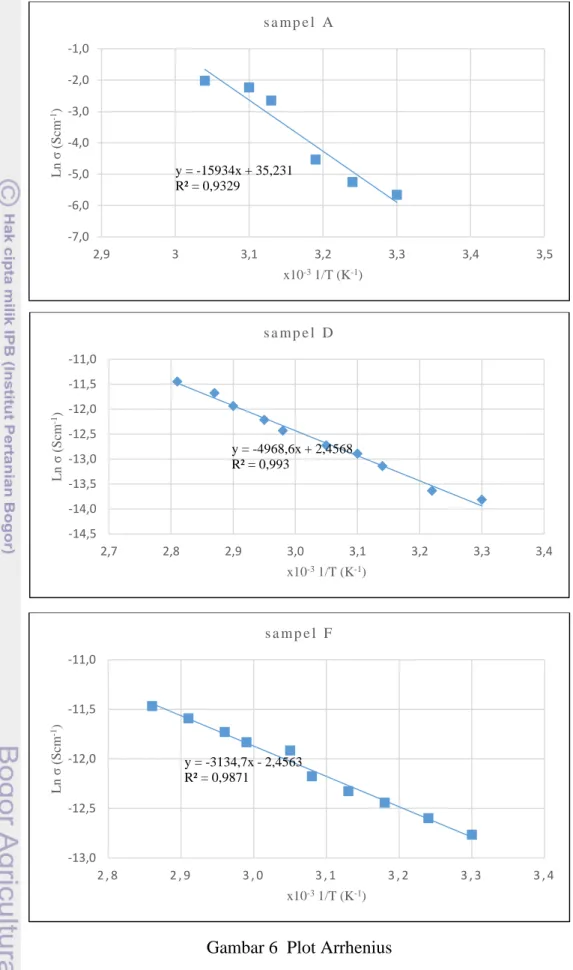
Dari hubungan konduktivitas terhadap suhu maka akan dapat dihitung energi aktivasi. Melalui proses perhitungan (analisis data pada lampiran 6, 9, dan 12) didapat data dalam Plot Arrhenius yaitu kurva hubungan konduktivitas terhadap 1/T, seperti ditampilkan pada Gambar 6. Dari Plot Arrhenius tersebut dapat ditentukan energi aktivasi.
Hubungan energi aktivasi dengan laju reaksi adalah berbanding terbalik. Semakin besar energi aktivasi maka laju reaksinya semakin lambat karena energi minimum untuk terjadi reaksi semakin besar.16 Plot Arrhenius elektrolit polimer
sampel A, D, dan F dapat dilihat pada Gambar 6. Semakin curam gradien yang dihasilkan pada kurva, maka Ea yang dihasilkan akan semakin besar. Pada Tabel 3
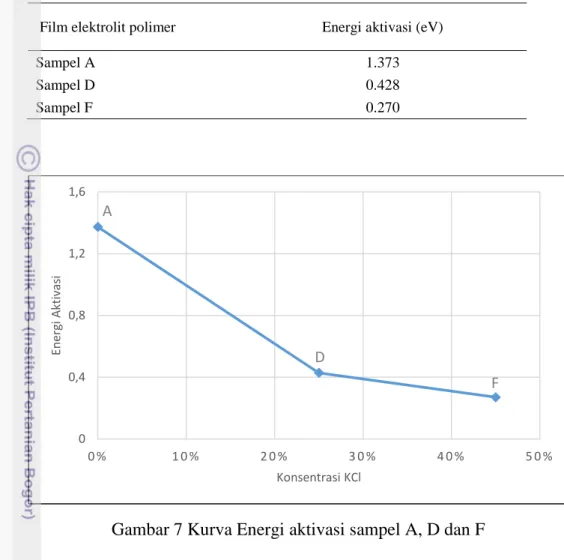
dan Gambar 7 dapat dilihat energi aktivasi dari elektrolit polimer sampel A. Energi aktivasi elektrolit polimer sampel A lebih besar dibanding elektrolit polimer sampel D dan F. Energi aktivasi elektrolit polimer sampel F lebih kecil dibanding energi aktivasi elektrolit polimer sampel D. Hal ini membuktikan bahwa penambahan konsentrasi KCl dapat menurunkan energi aktivasi yang diperlukan kation untuk bergerak dari satu kisi ke kisi yang lain dan meningkatkan mobilitas kation sehingga konduktivitas meningkat.17
Gambar 6 Plot Arrhenius
-7,0 -6,0 -5,0 -4,0 -3,0 -2,0 -1,0 2,9 3 3,1 3,2 3,3 3,4 3,5 L n σ ( S cm -1) x10-31/T (K-1) s a m p e l A y = -15934x + 35,231 R² = 0,9329 -14,5 -14,0 -13,5 -13,0 -12,5 -12,0 -11,5 -11,0 2,7 2,8 2,9 3,0 3,1 3,2 3,3 3,4 L n σ ( S cm -1) x10-31/T (K-1) s a m p e l D y = -4968,6x + 2,4568 R² = 0,993 -13,0 -12,5 -12,0 -11,5 -11,0 2 , 8 2 , 9 3 , 0 3 , 1 3 , 2 3 , 3 3 , 4 L n σ ( S cm -1) x10-31/T (K-1) s a m p e l F y = -3134,7x - 2,4563 R² = 0,9871
Tabel 3 Energi aktivasi elektrolit polimer kitosan/PEG+KCl
Film elektrolit polimer Energi aktivasi (eV)
Sampel A 1.373
Sampel D 0.428
Sampel F 0.270
Gambar 7 Kurva Energi aktivasi sampel A, D dan F
Analisis FTIR
FTIR digunakan untuk meneliti struktur suatu elektrolit polimer. Seperti untuk melihat adanya kompleks garam-polimer dalam elektrolit polimer dan mengetahui interaksi antara berbagai unsur dalam elektrolit polimer, interaksi ini dapat menyebabkan perubahan dalam moda vibrasi dari molekul pada elektrolit polimer.18 Menurut Kolhe dan Kannan spektrum kitosan murni terdapat pita serapan pada bilangan gelombang 1251, 1580 dan 1650 cm-1.19 Spektrum PEG murni terdapat pita serapan pada bilangan gelombang 843, 947, dan 1280 cm-1.20 Sedangkan menurut Song et al, pada spektrum PEG murni terdapat pita serapan pada bilangan gelombang 842, 962, 1113, 1360, 1371, dan 1466 cm-1. Dari hasil penelitian yang telah dilakukan spektrum gugus fungsi kitosan murni terdapat pita serapan pada bilangan gelombang 1643 dan 1257 cm-1.
0 0,4 0,8 1,2 1,6 0 % 1 0 % 2 0 % 3 0 % 4 0 % 5 0 % En erg i A kt ivasi Konsentrasi KCl A D F
Pada penelitian ini spektrum gugus fungsi kitosan pada elektrolit polimer kitosan/PEG terdapat pita serapan pada bilangan gelombang 1643 cm-1, spektrum gugus fungsi PEG didapat pada bilangan gelombang 949, 1281, dan 1466 cm-1. Sedangkan spektrum gugus fungsi kitosan pada elektrolit polimer kitosan/PEG+KCl terdapat pita serapan pada bilangan gelombang 1651 cm-1, spektrum gugus fungsi PEG didapat pada bilangan gelombang 949 dan 1366cm-1. Hal ini tidak jauh berbeda dari hasil FTIR yang dilakukan oleh Kolhe dan Kannan dan Song et al.
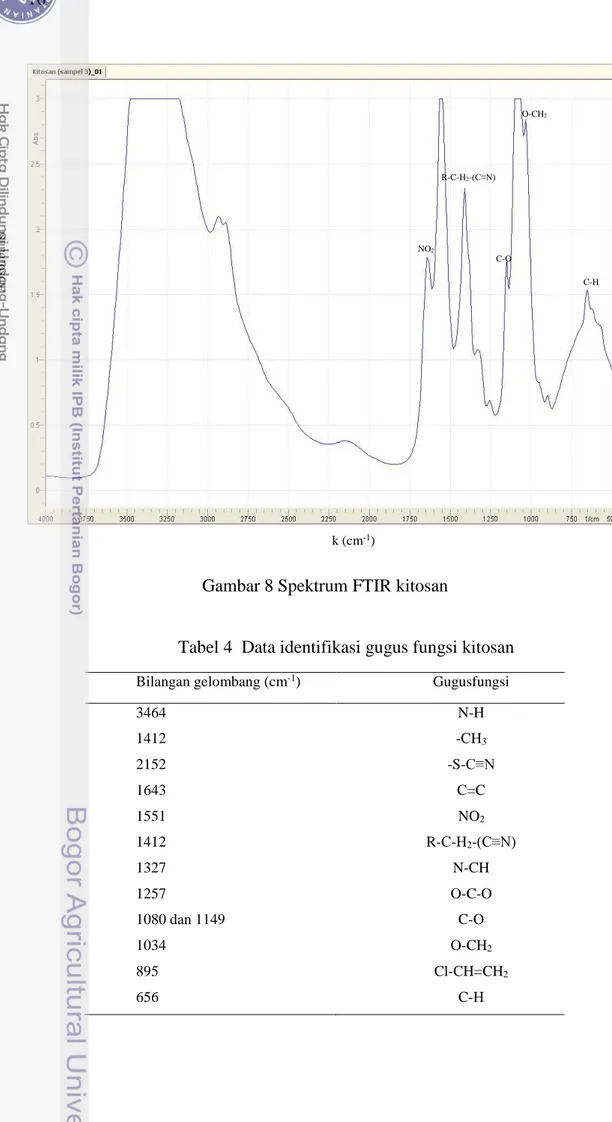
Spektrum gugus fungsi FTIR untuk kitosan murni dapat dilihat pada Gambar 8 dan Tabel 4. Dimana spektrum FTIR menunjukkan adanya gugus fungsi N-H pada bilangan gelombang 3464 cm-1, terdapat vibrasi –CH3 pada
bilangan gelombang 1412 cm-1. Ikatan -S-C≡N pada bilangan gelombang 2152 cm-1 dengan kekuatan sedang. Terdapat gugus fungsi C=C pada bilangan
gelombang 1643 cm-1 dan gugus fungsi NO
2 pada bilangan gelombang 1551cm-1.
Gugus fungsi R-C-H2-(C≡N) muncul pada bilangan gelombang 1412 cm-1. Amina
tersubtitusi (N-CH) muncul pada bilangan gelombang 1327 cm-1 sedangkan gugus
fungsi O-C-O ansimetrik muncul pada 1257 cm-1. Gugus fungsi C-O terdeteksi pada bilangan gelombang 1080 dan 1149 cm-1 dan eter aromatik O-CH2 terdeteksi
pada 1034 cm-1. Gugus fungsi CH2 dan C-H muncul pada bilangan gelombang
berturut-turut 895 dan 656 cm-1. Hasil FTIR kitosan murni yang dihasilkan pada penelitian ini tidak jauh berbeda dengan penelitian sebelumnya yang dilakukan oleh Rika Putri.
Gambar 8 Spektrum FTIR kitosan
Tabel 4 Data identifikasi gugus fungsi kitosan
Bilangan gelombang (cm-1) Gugusfungsi
3464 N-H 1412 -CH3 2152 -S-C≡N 1643 C=C 1551 NO2 1412 R-C-H2-(C≡N) 1327 N-CH 1257 O-C-O 1080 dan 1149 C-O 1034 O-CH2 895 Cl-CH=CH2 656 C-H k (cm-1) Ab so rb an si NO2 C-H O-CH2 C-O R-C-H2-(C≡N)
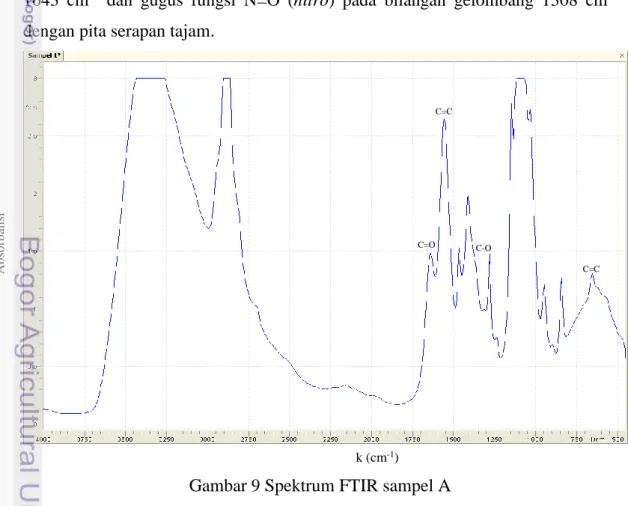
Spektrum gugus fungsi FTIR untuk film elektrolit polimer kitosan/PEG tanpa penambahan KCl dapat dilihat pada Gambar 9 dan Tabel 5. Spektrum gugus fungsi FTIR memperlihatkan puncak serapan inframerah yang lebih sederhana dibandingkan dengan puncak serapan kitosan murni. Tidak semua puncak serapan kitosan muncul dalam film elektrolit polimer kitosan/PEG kecuali gugus fungsi C-O dan C-H. Hal ini mengindikasikan bahwa telah terbentuk kompleks elektrolit polimer kitosan/PEG. Spektrum FTIR kitosan/PEG menunjukkan adanya pita serapan sedang pada bilangan gelombang 1466 cm-1 merupakan vibrasi dari CH2.
Pita serapan sedang pada bilangan 3232 dan 3438 cm-1 merupakan akibat vibrasi O-H, Adanya gugus fungsi O-H yang muncul mengindikasikan bahwa telah terjadi interaksi antar kitosan dan PEG.21 Gugus fungsi C-H dengan pita serapan sedang terdapat pada bilangan gelombang 2854 dan 2908 cm-1 dan gugus fungsi C-C terdapat pada bilangan gelombang 949 cm-1. Gugus fungsi C-N didapat pada
bilangan gelombang 1057 dan 1142 cm-1, gugus fungsi C=C didapat pada
bilangan gelombang 1558 cm-1. Pita serapan tajam pada bilangan gelombang 1281
cm-1 merupakan akibat vibrasi C-O. Gugus fungsi C=O pada bilangan gelombang
1643 cm-1 dan gugus fungsi N=O (nitro) pada bilangan gelombang 1308 cm-1 dengan pita serapan tajam.
Gambar 9 Spektrum FTIR sampel A
Ab so rb an si k (cm-1) C=O C=C C-O C=C
Tabel 5 Data identifikasi gugus fungsi kitosan/PEG
Bilangan gelombang (cm-1) Gugus fungsi
3448
O-H (alkohol, fenol dan gugus fungsi hidrogen)
3232
O-H (asam kabosilat dan gugus fungsi hidrogen) 2854 dan 2908 C-H (alkil) 1057 dan 1142 C-N 1281 C-O 949 C-C 1558 C=C 1643 C=O 1304 N=O (nitro) 1466 CH2
Spektrum gugus fungsi FTIR untuk film elektrolit polimer kitosan/PEG+KCl dapat dilihat pada Gambar 10 dan Tabel 6. Secara umum terlihat bahwa pola spektrum gugus fungsi FTIR tidak terdapat banyak perbedaan antara spektrum gugus fungsi FTIR film elektrolit polimer kitosan/PEG tanpa KCl dan film elektrolit polimer kitosan/PEG+KCl. Perbedaan hanya terjadi pada posisi puncak yang merupakan puncak-puncak gugus fungsi pada senyawa kitosan/PEG. Pergeseran puncak yang terjadi mengindikasikan bahwa ion K+ dan pasangan anionnya (Cl-) terikat pada gugus fungsi tersebut yaitu gugus fungsi O-H yang mengandung pasangan elektron bebas dan amina (N-H) yang telah terprotonisasi akibat proses pelarutan kitosan dalam asam asetat.2 Spektrum FTIR
kitosan/PEG+KCl menunjukkan adanya pita serapan sedang pada bilangan gelombang 3564 cm-1 merupakan vibrasi dari O-H. Tidak terdapat vibrasi CH
2
pada spektrum gugus fungsi kitosan/PEG+KCl seperti yang terdapat pada spektrum gugus fungsi kitosan/PEG, tetapi muncul gugus fungsi N-H dengan pita serapan sedang terdapat pada bilangan gelombang 3132cm-1 yang tidak muncul pada spektrum FTIR film elektrolit polimer kitosan/PEG tanpa KCl. Gugus fungsi C-H dengan pita serapan sedang terdapat pada bilangan gelombang 2870 dan 2939 cm-1 dan gugus fungsi C-C terdapat pada bilangan gelombang 949 cm-1 bilangan gelombang ini sama seperti pada film elektrolit polimer kitosan/PEG. Gugus fungsi C-N didapat pada bilangan gelombang 1057 dan 1026 cm-1, dan
gugus fungsi C=C didapat pada bilangan gelombang 1558 cm-1. Pita serapan tajam pada bilangan gelombang 1250 cm-1 merupakan akibat vibrasi C-O. Gugus fungsi C≡C pada bilangan gelombang 2137 cm-1 dan gugus fungsi N=O (nitro) pada bilangan gelombang 1304, 1342, dan 1366 cm-1dengan pita serapan tajam.
Gambar 10 Spektrum FTIR sampel F
Tabel 6 Data identifikasi gugus fungsi kitosan/PEG+KCl
Bilangan gelombang (cm-1) Gugus fungsi
3132 NH
3564
O-H (alkohol, fenol, dan gugus fungsi hidrogen ) 2870 dan 2939 C-H (alkil) 1026 C-N 1250 C-O 949 C-C 1651 C=O 1558 C=C
1304, 1342, dan 1366 N=O (nitro)
2137 C≡C k (cm-1) Ab so rb an si C=O C-C C=C C-O N=O
SIMPULAN DAN SARAN
Simpulan
Pembuatan film elektrolit polimer campuran kitosan/PEG telah dibuat dengan penambahan variasi konsentrasi garam KCl. Penambahan garam KCl dengan berbagai variasi konsentrasi pada elektrolit polimer berpengaruh tehadap konduktivitas elektrolit polimer tersebut.
Hasil analisis FTIR menunjukkan bahwa telah terbentuk kompleks polimer kitosan/PEG+KCl. Karena munculnya gugus fungsi baru, yang tidak muncul dalam spektrum kitosan/PEG.
Nilai konduktivitas yang paling baik dihasilkan pada sampel F dengan penambahan 45% wt KCl yaitu sebesar 5.786 x 10-6 Scm-1. Konduktivitas elektrolit polimer semakin meningkat dengan bertambahnya suhu. Namun pada suhu diatas suhu optimum konduktivitas elektrolit polimer semakin menurun. Hal ini dikarenakan peningkatan kristalisasi yang terjadi pada elektrolit polimer, dimana semakin kristalin suatu bahan maka konduktivitas ioniknya akan semakin kecil.
Energi aktivasi menurun seiring meningkatnya jumlah garam KCl yang ditambahkan pada kompleks polimer kitosan/PEG. Energi aktivasi terendah diperoleh pada sampel dengan penambahan garam KCl 45% wt. Dapat disimpulkan bahwa penambahan konsentrasi garam KCl akan menurunkan energi aktivasi elektrolit polimer tersebut.
Saran
Elektrolit polimer kitosan/PEG+KCl45% berpotensi untuk dimanfaatkan dalam aplikasi perangkat penyimpanan seperti sel surya dan baterai. Perlu dilakukan penelitian lebih lanjut untuk penerapan aplikasi tersebut.
DAFTAR PUSTAKA
1. Chew CL. Kajian kekonduksian ionik terhadap adunan elektrolit polimer PVC-getah asli terepoksi dan PVDF-getah asli terepoksi [Skripsi]. Skudai (MY): Fakulti Sains, Universiti Teknologi Malaysia; 2005.
2. [PTBIN]. Badan Teknologi Atom Negara, Pusat Teknologi Bahan Industri Nuklir. Aloma KK. Pengembangan elektrolit padat konduktivitas tinggi berbasis polimer alambiodegradable dan aplikasinya untuk sel baterai. 2010. Jakarta (ID): BATAN.
3. Putri Rika. Studi konduktivitas elektrolit polimer kitosan/PVA+KOH [tesis]. Bogor (ID): Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor; 2009.
4. Nugraha ES, Tighzert L, Copinet A. Effects of hydrophilic plasticizers on mechanical, thermal and surface properties of chitosan films. Journal of Agricultural and Food Chemistry. 2005; 53: 3950−3957. 5. Buridah MH, Teo LP, Majid SR, Yahya R, Taha R, Arof AK.
Charaterizations of chitosan-based polymer electrolyte photovoltaic cells. International Journal of Photoenergy. 2010; 1-7. doi:10.115/2010/805836.
6. Rahayu LH, Purnavita S. Optimasi pembuatan kitosan dari kitin limbah cangkang rajungan (Portunus pelagicus) untuk adsorben ion logam merkuri. Reaktor. 2007; 11(1): 45-49.
7. Nur Dewi RR. Isolasi dan identifikasi kitin, kitosan dari cangkang hewan mimi (Horseshoe Crab) menggunakan spektrofotometri infra merah [skripsi]. Malang (ID): Fakultas Sains dan Teknologi Departemen Kimia, Universitas Islam Negeri Malang; 2007.
8. Prasetyaningrum A, Rokhati N, Purwintasari S. Optimasi derajat deasetilasi pada proses pembuatan chitosan dan pengaruhnya sebagai bahan pengawet pangan. Riptek. 2007; 1(1): 39-46.
9. Margaret. Peningkatan kelarutan ibuprofen dengan Penambahan PEG 6000 [skripsi]. Depok (ID): Fakultas Matematika dan Ilmu Pengetahuan Alam Departemen Kimia, Universitas Indonesia; 2008. 10. Dified. 2009. Web. 2012 05 20. “Struktur kimia PEG”.
<https://commons.wikimedia.org/wiki/File:Polyethylene_glycol.png> 11. Sari Ratna D. Baterai cerdas dari elektrolit polimer chitosan dengan
penambahan amonium nitrat [skripsi]. Bogor (ID): Fakultas Perikanan dan Ilmu Kelautan Departemen Teknologi Hasil Perairan, Institut Pertanian Bogor; 2011.
12. Osman Z, Ibrahim V, Arof V. Conductivity enhancement due to ion dissociation in plasticized chitosan based polymer electrolytes. Carbohydrate Polymers. 2001; 44(2): 167-173. doi/10.1016/S0144-8617(00)00236-8.
13. Pollu AR, Kumar R. Conductivity, XRD, and FTIR studies of new Mg2+-ion-conducting solid polymer electrolytes: [PEG: Mg(CH3COO)2]. Journal of the Korean Physical Society. 2011; 59(1):
14. Singh THJ, Bhat SV. Orphology and conductivity studies of new solid polymer electrolyte: (PEG)xLiClO4. Bull mater sci. 2003; 26(7):
704-714.
15. Reddy Subba CHV, Zhu QY, Mai LQ, Wen C. Optical, eletrical and dicsharges profiles for (PVC+NaIO4) polymer electrolytes. Journal of
Applied Electrochemistry. 2006; 36: 1051-1056. doi: 10.1007/S10800-006-9158-3.
16. Vogel. Kimia Analisis Kuantitatif Anorganik. Jakarta : Penerbit Buku Kedokteran (EGC). 2009.
17. Ihsan M, Evvy K, Yulizar Y. Sintesis elektrolit padat berbasis gelas lithium(Ag2S)x(LiPO3)1-x. Jurnal sains materi indonesia. 2008;
176-180.
18. Pollu AR, Kumar Ranveer. Impedance spectroscopy and FTIR studies of PEG-based polymer electrolyte. E-journal of Chemistry. 2011; 8(1): 347-353.
19. Kolhe P, Kannan RM. Improvement of ductility of chitosan through blending and copolymerization with PEG: FTIR investigation of molecular interactions. Biomacromolecules. 2003; 4: 173-180.
20. Rui S, Rui X, He LH, Liu Y, Xiao QL. The structures and properties of chitosan/polyethylene glycol silica ternary hybrid organic-inorganic films. Chinese Journal of Polymer Science. 2008; 25(5): 621-630 21. He LH, Rui X, Yang DB, Rui S. Effect of blending chitosan with PEG
on surface morphology, crystallization and thermal properties. Chinese Journal of Polymer Science. 2009; 27: 501−510
Lampiran 1 Alat dan bahan yang digunakan dalam penelitian.
Neraca analitik
Hotplate
Plat pengukur konduktivitas
Lampiran 2 Tahap pembuatan film elektrolit polimer kitosan/PEG+KCl.
(a) (b) (c)
(d) (e) (f)
(i) Keterangan :
(a) Kitosan (b) PEG
(c) Asam asetat 1%
(d) Kitosan dan PEG dilarutkan dalam 10 ml asam asetat 1% dengan menggunakan hotplate, stirrer pada suhu 60o C selama 1 jam agar campuran homogen.
(e) Setelah campuran homogen turunkan suhu hotplate stirrer menjadi suhu ruang, kemudian tambahkan garam KCl dengan variasi yang sudah ditentukan.
(f) Campuran kitosan/PEG+KCl dihomogenisasi selama 5 jam dengan hotplate sampai campuran homogen.
(g) Setelah campuran kitosan/PEG+KCl homogen, kemudian campuran didiamkan pada suhu ruang sampai campuran mengering dan membentuk film tipis.
(h) Campuran kitosan/PEG+KCl yang telah mengering.
(i) Film elektrolit polimer kitosan/PEG+KCl yang telah dipotong menjadi ukuran 2x2 cm2.
Lampiran 3 Nilai konduktivitas ionik film polimer elektrolit kitosan/PEG+KCl. Ulangan Konsentrasi 0% wt 5% wt 15% wt 25% wt 35% wt 45% wt 55% wt x10- 6 S cm-1 x10-6 S cm-1 x10-6 S cm -1 x10-6 S cm-1 x10-6 S cm-1 x10-6 S cm-1 x10-6 S cm-1 1 0.0969 1.164 2.665 3.224 4.773 5.829 5.029 2 0.0995 1.175 2.704 3.237 5.068 5.551 5.110 3 0.0989 1.055 2.745 3.237 5.230 5.877 4.839 4 0.0978 1.321 2.756 3.168 4.939 5.867 4.793 5 0.0878 1.275 2.796 3.213 5.096 5.751 4.802 6 0.0866 1.296 2.714 3.235 4.859 5.660 4.896 7 0.0867 1.275 2.635 3.235 5.101 5.872 4.992 8 0.0956 1.145 2.597 3.056 5.057 5.843 4.891 9 0.1003 1.244 2.585 3.330 4.977 5.661 4.902 10 0.1007 1.324 2.597 2.944 5.089 5.664 4.739 11 0.0978 1.333 2.756 3.158 5.102 5.873 4.889 12 0.0897 1.340 2.770 3.289 5.338 5.803 5.022 13 0.0998 1.274 2.646 3.109 4.991 5.700 4.903 14 0.0914 1.245 2.697 3.158 5.052 5.754 4.892 15 0.0907 1.295 2.691 3.298 5.229 5.701 4.999 16 0.1002 1.214 2.591 3.295 4.759 5.792 5.029 17 0.0904 1.250 2.583 3.063 4.827 5.798 5.011 18 0.0890 1.302 2.699 3.213 4.818 5.840 4.898 19 0.0886 1.311 2.701 3.287 4.952 5.951 4.927 20 0.0868 1.298 2.721 3.187 4.785 5.927 4.774 rataan 0.0938 1.257 2.682 3.197 5.002 5.786 4.917
Lampiran 4 Variasi konduktivitas ionik sampel A terhadap suhu. T (oC) x10-5 σ (Scm-1) 29.7 0.003 35.3 0.005 40.5 0.011 46.5 0.071 49.7 0.107 56.2 0.133 68.5 0.146 74.4 0.155 79.9 0.159 89.7 0.183 94.9 0.186 99.6 0.201 105.8 0.217 110.2 0.235 114.9 0.243 119.2 0.191 125.9 0.107
Lampiran 5 Perhitungan plot Arrhenius elektrolit polimer sampel A.
T (oC) T (K) 1/T x10-5 σ (Scm-1) Ln σ (Scm-1) 29.7 302.7 0.00330 0.003 -5.660 35.3 308.3 0.00324 0.005 -5.251 40.5 313.5 0.00319 0.011 -4.534 46.5 319.5 0.00313 0.071 -2.651 49.7 322.7 0.00310 0.107 -2.235 56.2 329.2 0.00304 0.133 -2.020 68.5 341.5 0.00293 0.146 -1.925 74.4 347.4 0.00288 0.155 -1.862 79.9 352.9 0.00283 0.159 -1.838 89.7 362.7 0.00276 0.183 -1.700 94.9 367.9 0.00272 0.186 -1.683 99.6 372.6 0.00268 0.201 -1.606 105.8 378.8 0.00264 0.217 -1.529 110.2 383.2 0.00261 0.235 -1.450 114.9 387.9 0.00258 0.243 -1.416 119.2 392.2 0.00255 0.191 -1.657 125.9 398.9 0.00251 0.107 -13.745
Lampiran 6 Cara menghitung energi aktivasi elektrolit polimer sampel A dari plot Arrhenius.
Plot Arrhenius sampel A σ = σ0exp [ −Ea kT ] Lnσ = Ln (σ0e−EakT) Lnσ = Lnσ0+ Lne− Ea kT Lnσ = Lnσ0−Ea kT Lnσ = −Ea kT+ Lnσ0
Dengan menyesuaikan dengan persamaan grafik diatas maka diperoleh: Lnσ = −Ea kT+ Lnσ0 Lnσ = −Ea k ( 1 T) + Lnσ0 y = −15934(x) + 35.231 Eka = 15934 Ea 1.380x10−23JK−1= 15934 Ea = 2.199x10−19JK−1= 2.199x10 −19JK−1 1.602x10−19JK−1= 1.373eV -7,0 -6,0 -5,0 -4,0 -3,0 -2,0 -1,0 2,9 3 3,1 3,2 3,3 3,4 3,5 L n σ ( S cm -1) x10-31/T (K-1) y = -15934x + 35,231 R² = 0,9329
Lampiran 7 Variasi konduktivitas ionik sampel D terhadap suhu. T (oC) x10-5 σ (Scm-1) 30.2 0.010 37.6 0.120 45.6 0.196 50.1 0.252 55.3 0.297 62.8 0.399 66.1 0.496 72.3 0.655 75.6 0.847 83.3 1.068 89.1 1.242 98.3 1.550 106.9 2.035 112.6 2.429 118.3 1.934 124.6 1.557
Lampiran 8 Perhitungan Plot Arrhenius elektrolit polimer sampel D.
T (oC) T (K) 1/T (K-1) x10-5 σ (Scm-1) Ln σ (Scm-1) 30.2 303.2 0.00330 0.010 -13.817 37.6 310.6 0.00322 0.120 -13.638 45.6 318.6 0.00314 0.196 -13.143 50.1 323.1 0.00310 0.252 -12.892 55.3 328.3 0.00305 0.297 -12.728 62.8 335.8 0.00298 0.399 -12.431 66.1 339.1 0.00295 0.496 -12.215 72.3 345.3 0.00290 0.655 -11.936 75.6 348.6 0.00287 0.847 -11.679 83.3 356.3 0.00281 1.068 -11.448 89.1 362.1 0.00276 1.242 -11.296 98.3 371.3 0.00269 1.550 -11.075 106.9 379.9 0.00263 2.035 -10.803 112.6 385.6 0.00259 2.429 -10.625 118.3 391.3 0.00256 1.934 -10.853 124.6 397.6 0.00252 1.557 -11.070
Lampiran 9 Cara menghitung energi aktivasi elektrolit polimer sampel D dari plot Arrhenius.
Plot Arrhenius sampel D σ = σ0exp [−Ea kT ] Lnσ = Ln (σ0e− Ea kT) Lnσ = Lnσ0+ Lne−EakT Lnσ = Lnσ0−Ea kT Lnσ = −Ea kT+ Lnσ0
Dengan menyesuaikan dengan persamaan grafik diatas maka diperoleh: Lnσ = −Ea kT+ Lnσ0 Lnσ = −Ea k ( 1 T) + Lnσ0 y = −4968.6(x) + 2.4568 Ea k = 4968.6 Ea 1.380x10−23JK−1= 4968.6 Ea = 6.857x10−20JK−1= 6.857x10−20JK−1 1.602x10−19JK−1= 0.428eV -14,5 -14,0 -13,5 -13,0 -12,5 -12,0 -11,5 -11,0 2,7 2,8 2,9 3,0 3,1 3,2 3,3 3,4 L n σ ( S cm -1) x10-31/T (K-1) y = -4968,6x + 2,4568 R² = 0,993
Lampiran 10 Variasi konduktivitas ionik sampel F terhadap suhu. T (0C) x10-5 σ (Scm-1) 30.3 0.286 35.7 0.338 41.6 0.394 46.2 0.443 51.5 0.515 54.9 0.667 61.3 0.726 65.1 0.805 70.2 0.924 76.5 1.047 80.4 1.479 85.2 2.051 90.2 2.982 94.7 2.453 99.8 2.013
Lampiran 11 Perhitungan plot Arrhenius elektrolit polimer sampel F
T (0C) T (K) 1/T (K-1) x10-5 σ (Scm-1) Ln σ (Scm-1) 30.3 303.3 0.003297 0.286 -12.766 35.7 308.7 0.003239 0.338 -12.598 41.6 314.6 0.003179 0.394 -12.444 46.2 319.2 0.003133 0.443 -12.327 51.5 324.5 0.003082 0.515 -12.176 54.9 327.9 0.003050 0.667 -11.917 61.3 334.3 0.002991 0.726 -11.833 65.1 338.1 0.002958 0.805 -11.730 70.2 343.2 0.002914 0.924 -11.592 76.5 349.5 0.002861 1.047 -11.467 80.4 353.4 0.002830 1.479 -11.121 85.2 358.2 0.002792 2.051 -10.795 90.2 363.2 0.002753 2.982 -10.420 94.7 367.7 0.002720 2.453 -10.616 99.8 372.8 0.002682 2.013 -10.813
Lampiran 12 Cara menghitung energi aktivasi elektrolit polimer sampel F dari plot Arrhenius.
Plot Arrhenius sampel F σ = σ0exp [−Ea kT ] Lnσ = Ln (σ0e− Ea kT) Lnσ = Lnσ0+ Lne−EakT Lnσ = Lnσ0−Ea kT Lnσ = −Ea kT+ Lnσ0
Dengan menyesuaikan dengan persamaan grafik diatas maka diperoleh: Lnσ = −Ea kT+ Lnσ0 Lnσ = −Ea k ( 1 T) + Lnσ0 y = −3134.7(x) + (−3.854) Ea k = −3134.7 Ea 1.380x10−23JK−1= 3134.7 Ea= 4.326x10−20JK−1 =4.326x10−20JK−1 1.602x10−19JK−1= 0.270eV -13,0 -12,5 -12,0 -11,5 -11,0 2 , 8 2 , 9 3 , 0 3 , 1 3 , 2 3 , 3 3 , 4 L n σ ( S cm -1) x10-31/T (K-1) y = -3134,7x - 2,4563 R² = 0,9871
Lampiran 13 Spektrum hasil analisa FTIR kitosan
RIWAYAT HIDUP
Penulis dilahirkan di Jakarta pada tanggal 26 Mei 1990. Penulis adalah anak ke-lima dari lima bersaudara dari pasangan bapak Buhari Lubis dan Ibu Murniati Mattjik. Penulis menyelesaikan pendidikan di Sekolah Dasar Negeri Bintaro 02 Pagi dan lulus pada tahun 2002. Setelah itu penulis melanjutkan pendidikan di SMP Perwira Jakarta dan lulus pada tahun 2005 kemudian melanjutkan ke SMA Negeri 87 Jakarta dan lulus pada tahun 2008. Tahun 2008 penulis diterima sebagai mahasiswa di Institut Pertanian Bogor (IPB) melalui jalur Ujian Seleksi Masuk IPB (USMI) di Departemen Fisika Fakultas Matematika dan Ilmu Pengetahuan Alam. Selama menempuh pendidikan penulis juga pernah aktif di beberapa organisasi, menjadi anggota KIR (Karya Ilmiah Remaja) SMAN 87 Jakarta, anggota rohis kelas fisika angkatan 2008, dan anggota UKM (Unit Kegiatan Mahasiswa) koran kampus IPB.