PEMISAHAN RENIUM-188 DARI SASARAN WOLFRAM-188
DENGAN METODE EKSTRAKSI MENGGUNAKAN PELARUT
METIL ETIL KETON
Maria Christina P.
1, Riftanio N. Hidayat
1, Duyeh Setiawan
21) Sekolah Tinggi Teknologi Nuklir – BATAN, Jl. Babarsari, PO BOX 6101/YKBB,
Yogyakarta 55281
Telp.: (0274)48085; Fax.: (0274)489715
2) Pusat Sains dan Teknologi Nuklir Terapan – BATAN, Jl. Tamansari No.71, Bandung
40132
ABSTRAK
PEMISAHAN RENIUM-188 DARI SASARAN WOLFRAM-188 DENGAN METODE EKSTRAKSI MENGGUNAKAN PELARUT METIL ETIL KETON. Pemisahan renium-188 dari sasaran wolfram-188 secara ekstraksi dilakukan untuk mengembangkan produksi radioisotop renium-188 yang memenuhi kemurnian secara radionuklida dan radiokimia. Pemisahan kedua unsur ini disimulasikan terhadap unsur yang tidak aktif untuk mengurangi risiko paparan radioaktif. Pemisahan renium dari wolfram ini menggunakan metode ekstraksi dengan pelarut metil etil keton (MEK). Parameter yang berpengaruh terhadap pemisahan ini ditentukan melalui kondisi optimum proses ekstraksi berdasarkan pengaruh waktu pengocokan, volume MEK, pH larutan, serta nilai koefisien distribusi. Penentuan konsentrasi renium dan wolfram hasil ekstraksi dilakukan dengan metode spektrofotometer UV-Vis dengan pengompleks KSCN dalam suasana asam dan pereduktor SnCl2. Hasil percobaan menunjukkan bahwa kondisi optimum proses ekstraksi dengan umpan masing-masing 10 ppm yaitu pada waktu pengocokan selama 10 menit, volume MEK sebanyak 20 ml, dan kondisi larutan pada pH 5. Diperoleh konsentrasi maksimum renium yang terambil pada fase organik sebanyak 9,54 ppm dan nilai Kd sebesar 2,75, sementara Kd maksimum wolfram sebesar 0,08. Kondisi optimum proses ekstraksi ini selanjutnya dapat digunakan sebagai cara pemisahan renium dari wolfram yang radioaktif.
Kata kunci: koefisien distribusi, ekstraksi, renium, wolfram
ABSTRACT
SEPARATION OF RHENIUM-188 FROM TUNGSTEN-188 AS A TARGET BY EXTRACTION METHOD USING SOLVENT METHYL ETHYL KETONE. Separation rhenium-188 from tungsten-188 as a target by extraction method has been done to develop production of rhenium-188 radioisotope that fulfills radionuclide and radiochemical purity. This separation determination was by solvent extraction using methyl ethyl ketone (MEK). Prior to the separation process, it was determined beforehand the optimum conditions of extraction process based on the effect of agitation time, the volume of MEK, the pH of the solution, and distribution coefficient. Confirmation of the results of the extraction was conducted using UV-Vis spectrophotometer with a complexing KSCN under acidic conditions and SnCl2 as reductor. The results
showed that the optimum condition for extraction process to feed each of 10 ppm was as follows: agitation time 10 minutes, volume of MEK 20 ml, and the pH below 5. Maximum concentration of rhenium obtained at the organic phase was 9.5350 ppm. However, the condition of the extraction process did not affect the migration of tungsten to the organic phase. The maximum Dc value obtained was 2.7566 for rhenium and 0.0873 for tungsten. Optimum conditions of extraction process can be further tested on radioactive rhenium and tungsten as an alternative to the separation of radioisotopes.
PENDAHULUAN
Teknologi produksi radioisotop dan radiofarmaka serta pemanfaatan operasi siklotron dan reaktor nuklir harus senantiasa ditingkatkan pengembangan dan pendaya-gunaannya agar dapat memenuhi kebutuhan pemakai. Pengembangan teknologi produksi radioisotop dan radiofarmaka diarahkan pada inovasi produk berdaya guna tinggi dan strategis sehingga dapat dimanfaatkan langsung dalam bidang kesehatan, industri, dan bidang-bidang lain.
Radioisotop dapat diperoleh melalui iradiasi neutron atau iradiasi partikel bermuatan. Iradiasi neutron dilakukan di dalam reaktor nuklir sebagai penghasil neutron. Iradiasi partikel bermuatan dilakukan di fasilitas siklotron. Pada proses iradiasi, bahan sasaran/target harus sesuai dan tahan terhadap kondisi iradiasi, misalnya tahan terhadap panas. Oleh karena itu, harus dilakukan pemilihan bentuk kimia sasaran. Pemilihan bentuk kimia sasaran ini juga perlu mempertimbangkan kemudahan proses pasca-iradiasi, misalnya kemudahan dalam pelarutan dan pemisahan. [2]
Dalam pembuatan radioisotop renium-188, dilakukan iradiasi terhadap sasaran wolfram alam sehingga menghasilkan wolfram-188 yang kemudian meluruh menjadi renium-188 dengan waktu luruh 69 hari. Renium-188 yang dihasilkan kemudian dipisahkan dari induknya, yaitu wolfram-188. Dalam berbagai penelitian untuk memperoleh produk radioisotop renium-188 yang murni secara radiokimia dan radionuklida, telah dilakukan cara seperti pemisahan melalui kolom generator alumina [3] dan pemisahan secara elektrokimia [4]. Pada pemisahan melalui kolom generator alumina terdapat kelemahan, yaitu umpan yang dipisahkan harus memiliki aktivitas yang cukup besar karena kolom alumina memiliki daya serap sedikit sehingga umpan dengan aktivitas rendah sulit dipisahkan. Sementara itu, metode pemisahan secara elektrokimia masih belum memiliki prosedur yang pasti dalam proses pemisahannya. Oleh karena itu, diharapkan metode pemisahan secara ekstraksi dapat menjadi alternatif metode pemisahan yang mudah dan praktis.
Pada ekstraksi pemisahan W/Re ini, pelarut yang digunakan adalah metil etil keton (MEK). Penggunaan pelarut MEK ini merujuk
pada penelitian pemisahan Tc terhadap sasaran induk Mo [7,8], kemudian diujicobakan terhadap renium, didasarkan pada kemiripan sifat kimia Tc dengan Re. Selain itu, pelarut MEK murah dan mudah didapatkan serta merupakan pelarut yang baik untuk proses ekstraksi renium. Pelarut MEK juga memiliki polaritas tinggi jika dibandingkan dengan pelarut lainnya karena memiliki ikatan rantai karbon lebih banyak dibandingkan senyawa lainnya seperti aseton, kloroform, dan lain-lain. Beberapa faktor yang berpengaruh pada ekstraksi pemisahan renium dari wolfram adalah waktu pengocokan, volume pelarut organik, dan pH larutan. Peningkatan volume pelarut organik yang digunakan sangat penting karena akan mempengaruhi kenaikan koefisien distribusi renium di dalam pelarut organik. Namun, pelarut MEK tidak mempengaruhi kenaikan koefisien distribusi wolfram.
Dalam penelitian ini dipelajari pengaruh penambahan volume pelarut MEK, waktu pengocokan, serta pH larutan untuk proses ekstraksi terhadap koefisien distribusi (Kd) dengan tujuan untuk mengetahui tingkat keberhasilan dalam sistem pemisahan. Penelitian ini juga dilakukan terhadap renium dan wolfram yang tidak aktif, untuk mengurangi risiko paparan radiasi. Selanjutnya, kondisi optimum pemisahan digunakan untuk proses pemisahan renium dari wolfram yang radioaktif.
DASAR TEORI
Produksi RadioisotopRadioisotop dapat diperoleh melalui iradiasi neutron atau iradiasi partikel bermuatan. Iradiasi neutron dilakukan di dalam reaktor nuklir sebagai penghasil neutron. Iradiasi partikel bermuatan dilakukan di fasilitas siklotron. Pada proses iradiasi, bahan sasaran/target harus sesuai dan tahan terhadap kondisi iradiasi, misalnya tahan terhadap panas. Oleh karena itu, harus dilakukan pemilihan bentuk kimia sasaran. Pemilihan bentuk kimia sasaran ini juga perlu mempertimbangkan kemudahan proses pasca-iradiasi, misalnya kemudahan dalam pelarutan dan pemisahan. [2]
Radioisotop Renium-188
Radioisotop renium-188 diproduksi melalui penembakan proton terhadap tungsten (186W)
sebagai target, 186W(p,n)186Re atau 186W(d,2n)186Re. Karena perbedaan yang cukup besar menurut literatur, fungsi eksitasi reaksi di atas diukur kembali. Isotop 188Re bersifat radioaktif dan digunakan untuk pengobatan kanker hati. Radioisotop tersebut memiliki kedalaman penetrasi jaringan sebesar 11 mm dan waktu paruh 17 jam. 188Re juga digunakan dalam eksperimen pengobatan baru kanker pankreas, yang disampaikan melalui bakteri Listeria monocytogenes. [10&11]
Berdasarkan tabel periodik, renium memiliki kesamaan dengan teknesium. Pekerjaan yang dilakukan untuk renium ke senyawa sasaran sering kali dapat dilakukan juga untuk teknesium. Hal ini berguna dalam radiofarmasi, karena sulit untuk bekerja dengan 99mTc dalam pengobatan karena umur paruhnya yang pendek. [9]
Kesetimbangan Sekuler
Jika ada suatu radionuklida yang meluruh menjadi anak luruhnya, dan anak luruh tersebut bersifat radioaktif sehingga akan meluruh menjadi radionuklida berikutnya, peluruhan tersebut disebut peluruhan radioaktif berturutan.
Peluruhan wolfram-188 menjadi renium-188 termasuk peluruhan sekuler. Hal ini karena waktu paruh induk wolfram sekitar 100 kali waktu paruh anak renium. Kesetimbangan sekuler terjadi jika umur paruh induk jauh lebih besar daripada umur paruh anak. Perbedaan antara umur paruh induk dan anak sekitar 104 kali atau lebih besar. Karena umur paruh induk jauh lebih besar daripada umur paruh anak, maka konstanta peluruhan induk jauh lebih besar daripada konstanta peluruhan anak. Akibatnya:
2 1 2
dan e2t (1) Aktivitas tT t N e A . .
1 0,693 (2) sehingga, t e N N 0 1 1 2 1 2
t e N N 0 1 1 1 2 2.
1 1 2 2.
N ..
N (3)Pada hari pertama,
t induk anak N e N 1 0 1 0 1 2 1
(4)Untuk hari selanjutnya,
t anak anak N e N 1 1 2 0 1 2 1
(5) sehingga,
N e N n n anak anak 0 1 2 1 1 1 (6) Menentukan Tmax, 1 2 1 2 max ln 1
T (7)Pada kesetimbangan sekuler, aktivitas anak akan sama dengan aktivitas induk. Radionuklida anak akan meluruh dengan umur paruh radionuklida induk. [5]
Gambar 1. Skema Kesetimbangan Sekuler [5]
Persyaratan Radioisotop Berdasarkan IAEA
Radioisotop yang telah diproduksi di dalam reaktor nuklir selanjutnya perlu diperiksa kualitasnya untuk memastikan bahwa radioisotop yang dihasilkan tersebut memiliki spesifikasi yang memenuhi ketentuan yang ditetapkan oleh IAEA. Spesifikasi larutan radioisotop renium yang ditetapkan IAEA adalah sebagai berikut. [1]
1. Senyawa berupa larutan dalam bentuk natrium perenat (NaReO4).
2. Larutan radioisotop harus bersih, tanpa pengotor yang dapat terlihat, dan berfasa air.
3. Larutan radioisotop berwarna sedikit kekuningan.
4. pH larutan radioisotop dijaga supaya berkisar di antara 2,5–5,0.
5. Kemurnian radiokimia radioisotop lebih besar atau sama dengan 98%.
6. Kemurnian radionuklida radioisotop sebesar 99,9%.
Ekstraksi Cair-Cair
Ekstraksi cair-cair merupakan suatu teknik di mana suatu larutan (biasanya dalam air) dibuat bersentuhan dengan suatu pelarut kedua (biasanya organik), yang pada hakikatnya tak bercampur dengan larutan pertama, sehingga satu atau lebih zat terlarut (solute) dari larutan pertama berpindah ke dalam pelarut kedua.
Pemisahan dengan cara ini bersifat sederhana, bersih, cepat, dan mudah. Dalam banyak kasus, pemisahan dapat dilakukan dengan mengocok kedua larutan dalam sebuah corong pisah selama beberapa menit. Teknik ini dapat diterapkan untuk bahan-bahan dari tingkat runutan maupun yang dalam jumlah banyak.
Untuk memahami prinsip-prinsip dasar ekstraksi, terlebih dulu harus dibahas berbagai istilah yang digunakan untuk menyatakan keefektifan pemisahan. Untuk suatu zat terlarut A yang didistribusikan antara dua fase tak tercampurkan a dan b, hukum distribusi (atau partisi) Nernst menyatakan bahwa asal keadaan molekulnya sama dalam kedua cairan dan temperaturnya konstan, maka:
𝐾𝑜𝑛𝑠.𝑧𝑎𝑡 𝑡𝑒𝑟𝑙𝑎𝑟𝑢𝑡 𝑝𝑒𝑙𝑎𝑟𝑢𝑡 𝐴
𝐾𝑜𝑛𝑠.𝑧𝑎𝑡 𝑡𝑒𝑟𝑙𝑎𝑟𝑢𝑡 𝑝𝑒𝑙𝑎𝑟𝑢𝑡 𝐵= 𝐾𝐷 (8)
KD merupakan sebuah tetapan, yang dikenal sebagai koefisien distribusi (atau koefisien partisi). Hukum ini, seperti dinyatakan di atas, secara termodinamis tidak benar-benar tepat (misalnya, tak diperhitungkan aktivitas dari berbagai spesi itu dan karenanya diharapkan hanya akan berlaku dalam larutan encer di mana angka banding aktivitas mendekati 1), tetapi merupakan suatu pendekatan yang berguna. Hukum ini, dalam bentuknya yang sederhana, tak berlaku bila spesi yang didistribusikan mengalami disosiasi atau asosiasi dalam salah satu fase tersebut. [5]
METODE
Penyiapan Larutan Induk Standar
Larutan induk wolfram 1000 mg/l dibuat dengan cara menimbang WO3 sebanyak 0,1262 g, lalu dilarutkan dalam NaOH 2 N, kemudian diencerkan hingga volume akhir 100 ml. Selanjutnya dibuat larutan induk renium berkadar 200 ppm dengan menimbang logam renium sebanyak 0,01 g dan dilarutkan dalam peroksida, kemudian diuapkan hingga kisat. Selanjutnya, residu dilarutkan dalam NaCl 0,9% dan diencerkan hingga volume akhir 100 ml.
Variasi Waktu Pengocokan Ekstraksi Diambil larutan wolfram berkadar 10 ppm sebanyak 25 ml. Larutan tersebut diekstraksi menggunakan MEK dalam corong pisah selama 5 menit, dengan perbandingan fase air dengan fase organik 5:1. Setelah diekstraksi, fase air dan fase organik dipisahkan. Kadar masing-masing fase dianalisis dengan spektrofotometri UV-Vis. Ekstraksi diulang untuk lama waktu yang berbeda, yaitu 10, 15, 20, 25, dan 30 menit. Hal yang sama dilakukan pada larutan induk renium.
Variasi Penambahan Volume Pelarut MEK Diambil larutan wolfram berkadar 10 ppm sebanyak 25 ml. Larutan tersebut diekstraksi dalam corong pisah dengan menggunakan MEK, selama 10 menit, dengan volume 5 ml. Setelah diekstraksi, fase air dan fase organik dipisahkan. Kadar masing-masing fase dianalisis dengan spektrofotometri UV-Vis. Ekstraksi diulang pada volume pelarut yang berbeda, yaitu 7,5; 10; 12,5; 15; 17,5; dan 20 ml. Hal yang sama dilakukan pada larutan induk renium.
Variasi Pengaturan pH
Diambil larutan wolfram berkadar10 ppm sebanyak 25 ml. pH larutan diatur pada pH 3. Larutan tersebut diekstraksi dalam corong
pisah dengan menggunakan MEK selama 10 menit dengan volume 17,5 ml. Setelah diekstraksi, fase air dan fase organik dipisahkan. Kadar masing-masing fase dianalisis dengan spektrofotometri UV-Vis. Ekstraksi diulang dengan mengatur pH larutan yang berbeda, yaitu 3, 4, 5, 6, 7, dan 8. Hal yang sama dilakukan pada larutan induk renium.
Analisis
Analisis wolfram dan renium dilakukan dengan menggunakan spektrofotometer UV-Vis. Sebelum dilakukan pengukuran absorban, panjang gelombang diatur terlebih dulu, untuk wolfram pada 403 nm dan renium pada 420 nm. Sebagai larutan pengompleks digunakan KSCN 30% dalam suasana asam, dengan reduktor SnCl2 30%. Selanjutnya, masing-masing cuplikan diukur absorbansinya dengan spektrofotometer UV-Vis. Kemudian dapat ditentukan kadar W dan Re pada setiap variasi.
Besarnya koefisien distribusi (Kd) dapat dinyatakan sebagai berikut.
𝐾𝐷=
𝐶𝑜𝑟𝑔
𝐶𝑎𝑖𝑟 (9)
Corg = konsentrasi unsur dalam organik Cair = konsentrasi unsur dalam fase air
HASIL DAN PEMBAHASAN
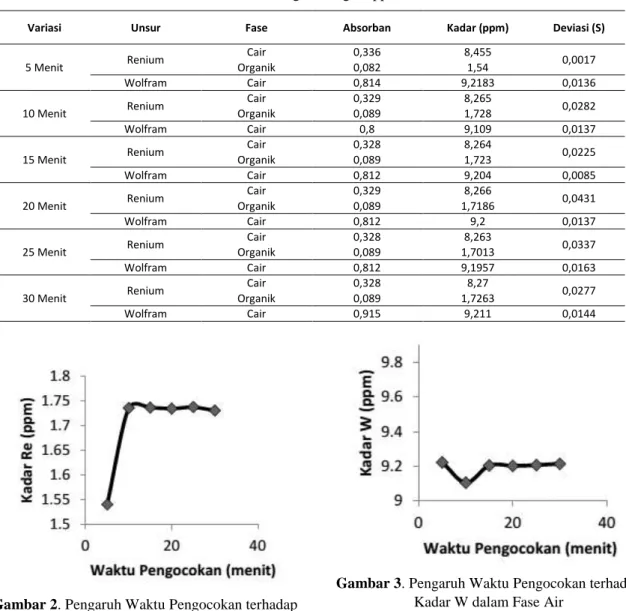
Variasi Waktu Pengocokan Ekstraksi Berdasarkan Tabel 1 serta Gambar 2 dan 3, tampak bahwa semakin lama waktu ekstraksi, Re yang terekstraksi ke dalam fase organik semakin besar. Kenaikan ini akan mencapai maksimum saat tercapai waktu kesetimbangan, yaitu jika konsentrasi Re yang terdistribusi dari fase air ke fase organik sama dengan konsentrasi Re yang terdistribusi dari fase organik ke fase air. Pada wolfram, tidak terjadi distribusi yang signifikan terhadap waktu pengocokan dan masih banyak yang tertinggal pada fase air.Tabel 1. Waktu Pengocokan Ekstraksi Wolfram dan Renium pada Kondisi Umpan Campuran
Konsentrasi Masing-Masing 10 ppm, Volume MEK 5 ml
Variasi Unsur Fase Absorban Kadar (ppm) Deviasi (S)
5 Menit Renium Cair 0,336 8,455 0,0017 Organik 0,082 1,54 Wolfram Cair 0,814 9,2183 0,0136 10 Menit Renium Cair 0,329 8,265 0,0282 Organik 0,089 1,728 Wolfram Cair 0,8 9,109 0,0137 15 Menit Renium Cair 0,328 8,264 0,0225 Organik 0,089 1,723 Wolfram Cair 0,812 9,204 0,0085 20 Menit Renium Cair 0,329 8,266 0,0431 Organik 0,089 1,7186 Wolfram Cair 0,812 9,2 0,0137 25 Menit Renium Cair 0,328 8,263 0,0337 Organik 0,089 1,7013 Wolfram Cair 0,812 9,1957 0,0163 30 Menit Renium Cair 0,328 8,27 0,0277 Organik 0,089 1,7263 Wolfram Cair 0,915 9,211 0,0144
Gambar 2. Pengaruh Waktu Pengocokan terhadap
Kadar Re dalam Fase Organik
Gambar 3. Pengaruh Waktu Pengocokan terhadap
Kadar W dalam Fase Air
Gambar 2 menunjukkan bahwa setelah ekstraksi berlangsung selama 10 menit, dengan bertambahnya waktu ekstraksi, maka Re yang masuk ke dalam fase organik relatif tetap. Berdasarkan hal ini, dapat dikatakan bahwa waktu kesetimbangan sudah tercapai. Jadi untuk selanjutnya, ekstraksi dilakukan selama 10 menit.
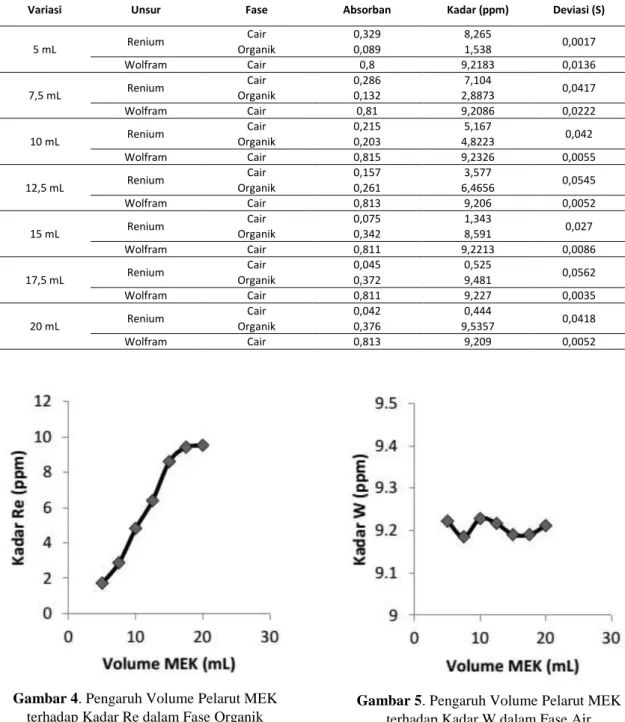
Variasi Penambahan Volume Pelarut MEK Pengaruh penambahan volume pelarut MEK disajikan dalam Tabel 2 serta Gambar 4 dan 5. Dengan bertambahnya volume pelarut, renium yang terekstraksi dalam fase organik semakin besar. Penambahan volume ini dilakukan hingga renium terbawa seluruhnya atau sampai pada kondisi kesetimbangan pelarut membawa renium pada fase organik.
Tabel 2. Volume Pelarut MEK pada Proses Ekstraksi pada Kondisi Umpan Campuran
Konsentrasi Masing-Masing 10 ppm
Variasi Unsur Fase Absorban Kadar (ppm) Deviasi (S)
5 mL Renium Cair 0,329 8,265 0,0017 Organik 0,089 1,538 Wolfram Cair 0,8 9,2183 0,0136 7,5 mL Renium Cair 0,286 7,104 0,0417 Organik 0,132 2,8873 Wolfram Cair 0,81 9,2086 0,0222 10 mL Renium Cair 0,215 5,167 0,042 Organik 0,203 4,8223 Wolfram Cair 0,815 9,2326 0,0055 12,5 mL Renium Cair 0,157 3,577 0,0545 Organik 0,261 6,4656 Wolfram Cair 0,813 9,206 0,0052 15 mL Renium Cair 0,075 1,343 0,027 Organik 0,342 8,591 Wolfram Cair 0,811 9,2213 0,0086 17,5 mL Renium Cair 0,045 0,525 0,0562 Organik 0,372 9,481 Wolfram Cair 0,811 9,227 0,0035 20 mL Renium Cair 0,042 0,444 0,0418 Organik 0,376 9,5357 Wolfram Cair 0,813 9,209 0,0052
Gambar 4. Pengaruh Volume Pelarut MEK
terhadap Kadar Re dalam Fase Organik
Gambar 5. Pengaruh Volume Pelarut MEK
terhadap Kadar W dalam Fase Air
Dalam Gambar 4, setelah penambahan volume pelarut MEK pada volume 17,5 ml, tampak bahwa dengan bertambahnya volume pelarut MEK, Re yang masuk ke dalam fase organik relatif tetap. Hal tersebut menandakan jumlah Re yang terbawa dapat dikatakan sudah mencapai tingkat maksimum. Dalam hal ini Re yang terbawa pada fase organik saat penambahan 20 ml pelarut MEK mencapai maksimum pada 9,545 ppm. Namun, hal ini tidak terjadi pada wolfram, yang tidak terpengaruh oleh penambahan volume pelarut
MEK. Konsentrasi wolfram yang terdapat pada fase air berkisar pada 9,2 ppm. Hal ini disebabkan oleh nilai Kd wolfram yang sebesar 0,08. Apabila dikaitkan dengan Persamaan (9), berapa pun jumlah solvent yang ditambahkan pada proses ekstraksi, karena nilai Kd wolfram sangat kecil maka jumlah wolfram yang bermigrasi ke fase organik tetap tidak akan banyak.
Variasi Pengaturan pH
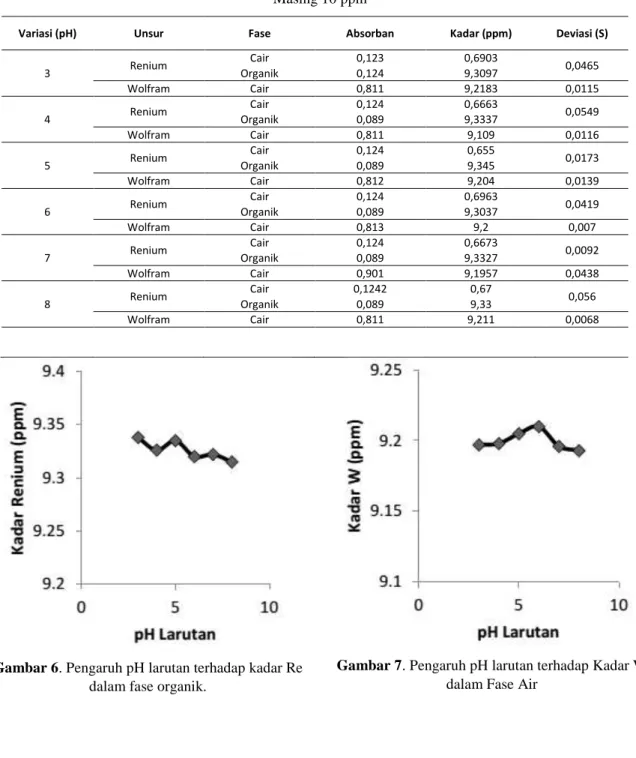
Pengaturan pH larutan dilakukan untuk mengetahui distribusi perpindahan renium atau wolfram ke dalam fase organik serta mengamati perpindahan yang paling besar pada pH tertentu. Tabel 3 serta Gambar 6 dan 7 menyajikan pengaruh pengaturan pH larutan pada proses distribusi renium dan wolfram ke dalam fase organik.
Tabel 3. pH Larutan MEK pada Proses Ekstraksi dengan Kondisi Umpan Campuran Konsentrasi
Masing-Masing 10 ppm
Variasi (pH) Unsur Fase Absorban Kadar (ppm) Deviasi (S)
3 Renium Cair 0,123 0,6903 0,0465 Organik 0,124 9,3097 Wolfram Cair 0,811 9,2183 0,0115 4 Renium Cair 0,124 0,6663 0,0549 Organik 0,089 9,3337 Wolfram Cair 0,811 9,109 0,0116 5 Renium Cair 0,124 0,655 0,0173 Organik 0,089 9,345 Wolfram Cair 0,812 9,204 0,0139 6 Renium Cair 0,124 0,6963 0,0419 Organik 0,089 9,3037 Wolfram Cair 0,813 9,2 0,007 7 Renium Cair 0,124 0,6673 0,0092 Organik 0,089 9,3327 Wolfram Cair 0,901 9,1957 0,0438 8 Renium Cair 0,1242 0,67 0,056 Organik 0,089 9,33 Wolfram Cair 0,811 9,211 0,0068
Gambar 6. Pengaruh pH larutan terhadap kadar Re
dalam fase organik.
Gambar 7. Pengaruh pH larutan terhadap Kadar W
Berdasarkan Gambar 6 dan Gambar 7 yang ditunjukkan di atas, terlihat bahwa semakin pH ditingkatkan, jumlah kadar Re yang terambil ke dalam fase organik semakin menurun, namun tidak terlalu signifikan. Oleh karena itu, kondisi ekstraksi dilakukan pada pH di bawah 5. Sementara pada wolfram, peningkatan pH tidak berpengaruh terhadap distribusi W ke dalam fase organik dan relatif dominan pada fase air pada kisaran mendekati 9,2 ppm. pH 6 merupakan titik tertinggi jumlah wolfram yang tertinggal dalam fase air.
Penentuan Koefisien Distribusi pada Kondisi Optimum
Koefisien distribusi (Kd) dilakukan untuk mengetahui perbandingan Kd renium dengan Kd wolfram. Pada penelitian ini, radioisotop yang diinginkan adalah renium. Oleh karena itu, diharapkan Kd renium lebih besar daripada Kd wolfram.
Berdasarkan data yang diperoleh, koefisien distribusi renium dan wolfram dihitung dari proses ekstraksi yang dilakukan dengan kondisi optimum pada waktu pengocokan 10 menit, volume pelarut 20 ml, serta pH larutan diatur agar berada di bawah 5. Tabel 4 dan 5 menyajikan data koefisien distribusi renium dan wolfram.
Tabel 4. Koefisien Distribusi Renium dengan
Variasi Waktu Pengocokan 10 Menit, Volume MEK 20 ml, dan pH Larutan di Bawah 5
Renium
pH
Fase Air Fase Organik Kd Kons. (ppm) Kons. (ppm)
3 0,69±0,05 9,31±0,04 13,48
4 0,69±0,05 9,34±0,05 14,08
5 0,69±0,02 9,34±0,02 14,05
Tabel 5. Koefisien Distribusi Wolfram dengan
Variasi Waktu Pengocokan 10 Menit, Volume MEK 20 ml, dan pH Larutan di Bawah 5
Wolfram
pH
Fase Air Fase Organik Kd Kons. (ppm) Kons. (ppm)
3 9,19±0,01 0,80±0,01 0,087
4 9,21±0,01 0,80±0,01 0,087
5 9,21±0,01 0,79±0,01 0,086
Dari data yang ditunjukkan oleh Tabel 4 dan 5, dapat dilihat bahwa Kd renium lebih besar daripada Kd wolfram. Hal ini dipengaruhi oleh afinitas elektron kedua unsur tersebut. Afinitas renium lebih besar daripada afinitas wolfram karena dalam sistem periodik unsur, posisi renium terletak lebih di sebelah kanan daripada wolfram. Pada proses ekstraksi, pelarut MEK lebih kuat menarik renium yang memiliki afinitas lebih besar.
Simulasi Pemisahan Renium-188 Terhadap Target Wolfram-188
Dengan menggunakan Persamaan (2) aktivitas wolfram saat selesai diiradiasi didapat sebesar 760,77 mCi dan Tmax aktivitas induk wolfram dengan anak renium 4,73 hari. Selanjutnya, jumlah renium yang dihasilkan dari peluruhan renium ditentukan dengan menggunakan Persamaan (4), (5), dan (6).
Penentuan jumlah renium yang dihasilkan dibatasi hanya sampai 100 hari. Hasil yang diperoleh ditunjukkan pada Gambar 8.
Gambar 8. Peluruhan antara Induk Wolfram
dengan Anak Renium
Berdasarkan Gambar 8, dapat dilihat bahwa laju peluruhan anak (renium) tidak terlihat signifikan dibandingkan dengan induknya. Hal ini dikarenakan perbedaan yang cukup jauh antara waktu paruh induk (wolfram) dengan waktu paruh anak (renium). Oleh karena itu, laju peluruhan anak (renium) dapat diperjelas kembali, seperti yang ditunjukkan pada Gambar 9.
Gambar 9. Peluruhan Anak Renium
Tabel data peluruhan induk (wolfram) dan anak (renium) memperlihatkan bahwa renium yang dihasilkan setiap hari hanya dalam jumlah yang cukup kecil. Dengan demikian, dapat dikatakan bahwa satu gram wolfram yang diiradiasi, tidak sepenuhnya meluruh menjadi renium. Renium dapat terus diambil setiap hari hingga aktivitas wolfram menjadi sangat kecil.
Berdasarkan perolehan pada kondisi optimum, jumlah maksimum renium yang terambil sebanyak 95,57%. Dari data ini dapat dikatakan kondisi pemisahan secara ekstraksi masih belum memenuhi ketentuan yang ditetapkan oleh IAEA, yakni ≥98%. Oleh karena itu, perlu dilakukan beberapa modifikasi terhadap proses ekstraksi yang dilakukan, seperti melakukan variasi kecepatan pengocokan agar jumlah renium yang terambil dapat ditingkatkan kembali.
Selain itu, jika proses ekstraksi dilakukan dengan bahan radioaktif, ditinjau dari segi keselamatan cukup berisiko tinggi terhadap paparan radioaktif yang akan didapat karena proses ekstraksi dilakukan hanya menggunakan peralatan corong pisah sederhana. Risiko terjadinya kontaminasi oleh radioaktif juga cukup tinggi sekalipun proses pemisahan dilakukan dalam fasilitas glove box. Oleh karena itu, selanjutnya perlu dilakukan penelitian mengenai konstruksi alat ekstraksi yang aman dan memenuhi standar keselamatan. Dengan kata lain, konstruksi proses ekstraksi yang dilakukan belum memenuhi standar keselamatan yang ditetapkan apabila dibandingkan dengan pemisahan dengan metode lain, seperti menggunakan kolom generator.
KESIMPULAN
Berdasarkan penelitian pemisahan renium-188 dari sasaran wolfram-188 menggunakan metode ekstraksi dengan pelarut metil etil keton, dapat disimpulkan sebagai berikut. 1. Proses pemisahan renium dari wolfram
dapat dilakukan dengan menggunakan ekstraktan MEK dengan waktu pengocokan 10 menit.
2. Pelarut metil etil keton yang ditambahkan mencapai maksimum pada penambahan 20 ml, dengan umpan 10 ppm.
3. Makin tinggi pH larutan, renium yang terambil semakin berkurang. pH larutan diatur pada kisaran di bawah 5.
4. Koefisien distribusi renium lebih besar, yaitu 14,08, daripada koefisien distribusi wolfram yang berkisar pada 0,08.
SARAN
1. Penetapan jadwal waktu iradiasi seharusnya tidak mundur.
2. Penelitian perlu diujicobakan pada wolfram dan renium radioaktif.
DAFTAR PUSTAKA
1. Mirzadeh, S., F.F. Knapp Jr., and A.P. Callahan, 2003. Manual for Reactor
Produced Radioisotopes. International Atomic Energy Agency.
2. PDIN-BATAN, 1998. Atomos: Radioisotop dan Radiofarmaka untuk Bidang Kesehatan, Pertanian, Hidrologi, dan Industri. Jakarta: Pusat Diseminasi IPTEK Nuklir.
3. Sriyono, H. Lubis, E. Sarmini, Herlina, dan I. Saptiama, 2013. Pemisahan
Radioisotop 188Re dari Radioisotop 188W Melalui Generator 188W/188Re Berbasis Alumina. Serpong: Pusat Radioisotop dan
Radiofarmaka.
4. Chakravarty, R., A. Dash, K. Kothari, M.R. Ambikalmajan Pillai, and M. Venkatesh. 2008. A Novel 188W/188Re Electrochemical Generator with Potential for Medical Applications. Mumbai: Atomic Research Centre.
5. Vertes, A., S. Nagy, Z. Klencsar, R.G. Lovas, and F. Rosch, 2011. “Kinetics of Radioactive Decay.” In: S. Nagy,
Handbook of Nuclear Chemistry (p. 347).
6. Baset, .J, R.C. Denney, G.H. Jeffrey, and J. Mendhan, 1994. Buku Ajar Vogel:
Kimia Analisis Kuantitatif Bab VI Ekstraksi Pelarut. Alih bahasa oleh
Pudjaatmaka, A. Hadyana, L. Setiono. Jakarta: Penerbit Buku Kedokteran EGC. 7. Yono, S., Abidin, Herlina, Sulaiman,
Sriyono, Hambali, dan H.G. Adang, 2011.
Pemekatan Larutan Teknesium- 99m Hasil Ekstraksi dengan Adsorpsi Resin dan Evaporasi Tekanan Rendah. Serpong:
Pusat Radioisotop dan Radiofarmaka. 8. Awaludin, R., H. Lubis, Sriyono, Abidin,
Herlina, dan A. Hardi, 2012. Ekstraksi Teknesium-99m dari Larutan Molibdenum Skala Besar. dalam: Seminar Nasional
VIII SDM Teknologi Nuklir.
9. Deutsch, E., K. Libson, and J.L. Vanderheyden, 1990. “The Inorganic
Chemistry of Technetium and Rhenium as Relevant to Nuclear Medicine.” in: M. Nicolini, G. Bandoli, & U. Mazzi,
Technetium and Rhenium in Chemistry and Nuclear Medicine (pp. 13-20). New
York: Raven Press.
10. Setiawan, D., 2010. Sintesis dan karakteristik 188Re Hidroksi Apatit untuk Tujuan Radioterapi Kanker. Bandung: Pusat Teknologi Nuklir Bahan dan Radiometri.
11. Hartati, E., D. Setiawan, dan Y.B. Yulitati, 2014. “Sintesis dan Karakterisasi Hidroksi Apatit (HAp) untuk Bahan Pengikat Tungstat dalam Sistem Generator 188W/188Re.” dalam: Sains dan Teknologi
EKSTRAKSI DAN STRIPPING URANIUM
HASIL PELARUTAN TOTAL MONASIT BANGKA
Noor Anis Kundari
1, Riesna Prassanti
2, Giezzella
31) STTN-BATAN, Yogyakarta, Indonesia, [email protected]
2) PTBGN-BATAN, Jakarta Selatan, Indonesia, [email protected]
3) STTN-BATAN, Yogyakarta, Indonesia, [email protected]
ABSTRAK
EKSTRAKSI DAN STRIPPING URANIUM HASIL PELARUTAN TOTAL MONASIT BANGKA. Penelitian pengolahan monasit di PTBGN-BATAN telah berhasil memisahkan logam tanah jarang dari unsur radioaktif dengan kemurnian yang tinggi, namun menghasilkan limbah berupa campuran logam tanah jarang, uranium, torium, dan unsur lain yang tidak terambil. Proses pengolahan limbah dapat dilakukan dengan memisahkan uranium terlebih dulu dengan metode ekstraksi menggunakan trioktil amin. Dalam penelitian ini dilakukan ekstraksi uranium dengan trioktil amina dan stripping uranium dengan H2SO4 untuk menentukan nilai koefisien distribusi (Kd) U, Th, LTJ2O3, dan PO4. Nilai Kd yang diperoleh digunakan untuk menentukan jumlah tingkat ekstraksi-stripping yang dibutuhkan untuk mengambil 95% uranium dari limbah umpan, dengan ekstraksi dan stripping dari kondisi yang telah diperoleh. Nilai Kd dihitung berdasarkan persamaan Nernst, sedangkan jumlah stage ekstraksi-stripping dihitung berdasarkan nilai Kd uranium dengan metode McCabe Thiele. Penelitian ini menghasilkan nilai Kd pada ekstraksi dengan komposisi ekstraktan TOA:Kerosen:isodekanol = 5:92:3 adalah U = 3,42; Th = 0,02; LTJ2O3 = 0,07; dan PO4 = 0,10. Kd pada
stripping uranium menggunakan H2SO4 3 M adalah U = 0,13 dan Th = 2,21. Berdasarkan nilai Kd ini, jumlah tingkat teoretis ekstraksi dan stripping untuk memperoleh uranium sebanyak 95% adalah 7 tingkat ekstraksi pada A/O = 2 dan 6 tingkat stripping pada A/O = 1/5.
Kata kunci: ekstraksi-stripping, uranium, penentuan jumlah stage, pelarutan total monasit Bangka
ABSTRACT
URANIUM EXTRACTION AND STRIPPING FROM TOTAL DISOLUTION OF BANGKA MONAZITE. Monazite processing research in PTBGN-BATAN has succeeded in separating the rare earth metals of radioactive elements with high purity, but produced waste in the form of a mixture of rare earth metals, uranium, thorium, and other elements that were not recovered. Waste treatment process has been carried out by first separating uranium from others by using extraction method with trioctyl amine. In this research, the extraction of uranium with trioctyl amines and stripping uranium with H2SO4 was done to determine the
value of the distribution coefficient (Kd) of U, Th, LTJ2O3, and PO4, and to determine the number of
extraction-stripping stages required to take 95% of uranium from the waste feed, to the extraction and stripping of the conditions that had been obtained. Kd was calculated based on the Nernst equation, then the number of theoretical stage of extraction stripping was calculated based on the value of Kd U with McCabe Thiele method. This research resulted in Kd values on extraction with extractant ratio TOA:kerosene:isodekanol = 5:92:3 is U = 3.42; Th = 0.02; LTJ2O3 = 0.07; and PO4 = 0.10. Kd on uranium
stripping using H2SO4 3 M is U = 0.013 and Th = 2.21. Based on this Kd value specified number of
theoretical stages of extraction and stripping to obtain uranium as much as 95%,based on calculation, the number of stages of extraction is 7 stage for comparison A/O = 2 and 6 stage stripping at A/O = 1/5.
PENDAHULUAN
Penelitian pengolahan monasit di PTBGN-BATAN telah berhasil memisahkan logam tanah jarang dari unsur radioaktif dengan kemurnian tinggi, namun menghasilkan limbah berupa campuran logam tanah jarang (LTJ), uranium (U), torium (Th), dan unsur lain yang tidak terambil. Proses pengolahan limbah dapat dilakukan dengan memisahkan uranium terlebih dulu dengan metode ekstraksi menggunakan trioktil amin.
Hasil penelitian sebelumnya menunjukkan bahwa kondisi optimum ekstraksi, yaitu pada pH umpan 1,5, dengan perbandingan O/A = 5 dan waktu ekstraksi 5 menit, 100% U dapat terekstrak, tetapi Th juga ikut terekstrak sebesar 32,44%. [1]
Untuk keperluan perancangan unit ekstraksi diperlukan nilai koefisien distribusi (Kd). Nilai ini dipengaruhi oleh jenis ekstraktan, komposisi, dan suhu. Dalam penelitian ini dilakukan variasi konsentrasi ekstraktan dan konsentrasi stripper dalam proses ekstraksi-stripping untuk menentukan koefisien distribusi pada setiap variasi komposisi ekstraktan dan koefisien distribusi
stripping pada setiap variasi konsentrasi stripper. Berdasarkan nilai koefisien distribusi
dapat ditentukan jumlah stage yang dibutuhkan untuk memperoleh uranium dengan recovery 95%. Penelitian ini perlu dilakukan karena minimnya data koefisien distribusi untuk ekstraksi uranium, dan beberapa data koefisien distribusi yang ditemui sulit untuk dijadikan data perancangan karena informasi yang ditampilkan kurang lengkap.
TEORI
Pengolahan Monasit Bangka
Pengolahan monasit di PTBGN-BATAN dimaksudkan untuk mendapatkan uranium. Proses ini terdiri atas beberapa tahapan, yaitu dekomposisi pasir monasit, pelarutan parsial, pengendapan U dan Th, pelarutan total, ekstraksi-stripping, dan pengendapan U. Dekomposisi pasir monasit dengan NaOH bertujuan untuk memecah struktur ikatan monasit dan memisahkan fosfat melalui proses pemisahan padat cair [2]. Pelarutan parsial dengan HCl pada pH 3,7 bertujuan untuk melarutkan logam tanah jarang sebanyak mungkin, namun U dan Th terlarut seminimal mungkin [3]. Pengendapan dengan NH4OH
pada pH 6,3 bertujuan untuk mengendapkan uranium dan torium sebanyak-banyaknya. Endapan dari proses pengendapan NH4OH dilarutkan dengan H2SO4 pekat, kemudian digunakan sebagai umpan ekstraksi. Pelarutan menggunakan H2SO4 ini merupakan pelarutan total yang berfungsi melarutkan semua endapan.
Ekstraksi Stripping Uranium
Ekstraksi uranium adalah proses pemisahan uranium dari campuran larutan oleh suatu pelarut organik yang tidak saling melarutkan. Selama proses ekstraksi, uranium akan terdistribusi di antara dua pelarut (fase organik dan fase cair) sesuai hukum distribusi Nernst. [4]
Uranium dalam larutan dapat berbentuk senyawa kompleks netral, anion, maupun kation. Berdasarkan hal tersebut, pelarut organik dibagi menjadi 3 (tiga) kategori. Kategori pertama adalah eter, trialkil fosfat, dan trialkil fosfin oksida yang mengekstrak kompleks netral; kategori kedua adalah alkil amin yang mengekstrak kompleks anion, dan kategori ketiga adalah alkyl orthophosporic
acid dan alkyl pyro-phosporic acid yang
mengekstrak kation. [5]
Uranium maupun torium terlarut dalam asam sulfat membentuk kompleks anion, yaitu UO2(SO4)34- atau UO2(SO4)32-, dan Th(SO4)32-. Uranil sulfat terekstrak sangat baik dengan jenis amina, sedangkan torium sulfat tidak banyak terekstrak. Torium sulfat lebih baik diekstrak dengan jenis amina primer [6]. Koefisien distribusi (Kd) unsur dalam amina tersier adalah uranium 140, torium <0,03, dan cerium <0,01 [7]. Berdasarkan nilai Kd ini, diketahui bahwa nilai Kd U memiliki perbedaan cukup jauh daripada Kd Th dan Kd Ce sehingga amina tersier cukup selektif terhadap uranium.
Ekstraksi uranium juga dapat dilakukan menggunakan TBP dalam suasana asam nitrat. Pada 30% TBP dalam kerosen, nilai Kd U = 2,030 dan Kd Th = 4,936 [8]. Berdasarkan nilai tersebut, dapat diketahui bahwa Kd U dan Th memiliki nilai yang cukup dekat sehingga apabila dilakukan ekstraksi dengan TBP pada suasana asam nitrat maka U dan Th akan lebih sulit dipisahkan.
Proses ekstraksi selalu diikuti dengan
stripping. Stripping bertujuan untuk mengambil kembali uranium dari fase organik ke fase air. Beberapa hal yang berpengaruh
dalam proses stripping adalah jenis stripper, konsentrasi stripper, suhu, perbandingan O/A, dan waktu stripping.
Morais, dkk. (2005) meneliti efek konsentrasi H2SO4 pada stripping uranium pada kisaran 2,0-5,0 mol/l. Dalam kisaran ini efisiensi stripping uranium meningkat dari 24% menjadi 75%, menunjukkan bahwa
stripping uranium dari alamina 336 menggunakan H2SO4 harus dilakukan dalam konsentrasi asam yang tinggi. Hasil yang diperoleh menunjukkan bahwa koefisien distribusi uranium berkurang secara signifikan ketika konsentrasi H2SO4 lebih dari 3,5 mol/l. Penelitian ini menggunakan variasi waktu kontak antarfase antara 3 dan 10 menit. Berdasarkan pengamatan, diketahui bahwa 5 menit sudah cukup untuk mencapai keseimbangan logam antara fase [9].
Koefisien distribusi pada proses ekstraksi dan stripping dapat ditentukan berdasarkan rumus berikut.
Koefisien Distribusi = 𝐾𝑜𝑛𝑠.𝑢𝑛𝑠𝑢𝑟 𝑑𝑙𝑚 𝑎𝑞𝑢𝑒𝑜𝑢𝑠𝐾𝑜𝑛𝑠.𝑢𝑛𝑠𝑢𝑟 𝑑𝑙𝑚 𝑜𝑟𝑔𝑎𝑛𝑖𝑘 (1) Penentuan Jumlah Stage
Penentuan jumlah stage dapat dilakukan dengan metode grafik McCabe Thiele. Penentuan dengan metode ini dapat dilakukan menggunakan grafik keseimbangan dan garis operasi yang diplotkan pada grafik konsentrasi
solute dalam rafinat (X) dan konsentrasi solute
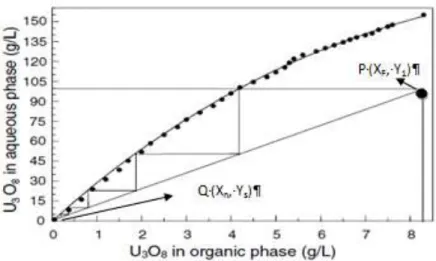
dalam ekstrak (Y). Grafik keseimbangan dapat dibuat apabila memiliki nilai koefisien distribusi ataupun nilai koefisien partisi yang didapatkan dari percobaan, sedangkan garis operasi dapat dibuat dengan menghubungkan dua koordinat, yaitu titik P(XF,Y1) dan Q(Xn,Yn+1(=Ys)). Contoh grafik kesetimbangan dan garis operasi dapat dapat dilihat pada Gambar 1.
Gambar 1. Kurva Kesetimbangan dan Garis Operasi
Jumlah stage ditentukan dengan menarik garis dari titik Q ke arah vertikal sampai bersinggungan dengan kurva kesetimbangan, kemudian ditarik secara horizontal sampai mengenai garis operasi. Begitu seterusnya sampai pada puncak titik P. Banyaknya siku yang menyinggung kurva kesetimbangan merupakan jumlah stage secara teoretis [10].
BAHAN DAN ALAT
Bahan1. Bahan yang digunakan dalam penelitian ini adalah umpan ekstraksi yang dibuat dari monasit Bangka, NaOH, HCl, H2SO4, NH4OH, kertas saring, dan akuades.
Ekstraktan yang digunakan adalah trioktil amin, isodekanol, dan kerosen, dengan beberapa perbandingan.
2. Umpan ekstraksi dibuat dari monasit Bangka, NaOH, HCl, H2SO4, NH4OH, kertas saring, dan akuades.
3. Trioktil amin, isodekanol, dan kerosen digunakan sebagai ekstraktan pada proses ekstraksi.
4. H2SO4 digunakan sebagai stripper pada proses stripping.
Alat
1. Alat yang digunakan pada saat proses adalah: gelas ukur, gelas beker, pengaduk magnetik, corong, corong pemisah, pipet
tetes, mikropipet, timbangan analitik, labu ukur, bulb pipet, stopwatch, hot plate, pH meter, termometer, buret, dan pompa vakum.
2. Alat yang digunakan untuk analisis adalah: spektrofotometer UV-Vis, timbangan analitik, pH meter, dan furnace.
LANGKAH KERJA
Ekstraksi UraniumMenentukan waktu setimbang. Larutan (U, Th,
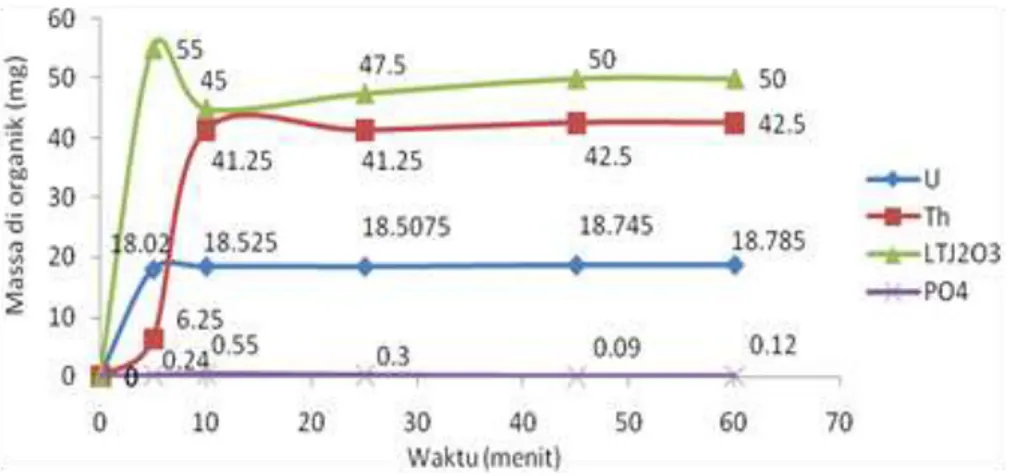
LTJ) sulfat dan ekstraktan dimasukkan ke dalam gelas beker dengan perbandingan O/A = 1, pH umpan 1,5, dan perbandingan ekstraktan TOA:Kerosen:isodekanol = 5:92:3. Larutan diekstraksi dengan variasi waktu 5, 10, 25, 45, dan 60 menit, kemudian dibiarkan terpisah selama 17 jam. Fase organik dan fase cair dipisahkan, kemudian fase cair dianalisis. Waktu setimbang digunakan sebagai waktu ekstraksi pada proses berikutnya.
Menentukan Kd berdasarkan variasi perbandingan konsentrasi ekstraktan. Larutan
(U, Th, LTJ) sulfat dan ekstraktan dimasukkan ke dalam gelas beker dengan perbandingan O/A=1, pH umpan 1,5, dan variasi perbandingan ekstraktan TOA:kerosen:isodekanol = 3:94:3; 4:93:3; 5:92:3; 6:91:3; 7:90:3; 5:95:0; 5:93:2; 5:91:4; dan 5:90:5. Ekstraksi dilakukan sesuai dengan waktu setimbang, kemudian dilakukan pemisahan dengan corong pemisah. Fase organik dan fase cair yang telah dipisahkan kemudian dianalisis.
Stripping Uranium
Menentukan waktu setimbang. Fase organik
hasil ekstraksi pada pH 1,5 dan A/O = 1/5 dengan perbandingan TOA:kerosen:isodekanol = 5:92:3 di-stripping dengan H2SO4 pada perbandingan A/O = 1 dan konsentrasi H2SO4 2,5 M. Stripping dilakukan dengan variasi waktu 5, 10, 25, 45, dan 60 menit, kemudian dibiarkan selama 16 jam. Fase organik dan fase cair dipisahkan, kemudian fase cair dianalisis. Waktu setimbang digunakan sebagai waktu
stripping pada proses berikutnya.
Menentukan Kd berdasarkan variasi konsentrasi stripper. Fase organik hasil
ekstraksi di-stripping dengan H2SO4 pada perbandingan A/O = 1 dan variasi konsentrasi H2SO4 1,5 M, 2 M, 2,5 M, 3 M, dan 3,5 M.
Stripping dilakukan sesuai dengan waktu
setimbang yang telah ditentukan. Fase organik dan fase cair dipisahkan, kemudian fase cair dianalisis.
HASIL DAN PEMBAHASAN
Nilai Kd Ekstraksi dan StrippingKd unsur pada proses ekstraksi maupun
stripping dapat dihitung apabila ekstraksi
maupun stripping yang dilakukan telah mencapai kesetimbangan. Oleh karena itu, dilakukan penentuan waktu setimbang terlebih dulu dengan variasi waktu pengadukan, kemudian dibiarkan terpisah selama waktu tertentu. Waktu pemisahan untuk ekstraksi adalah selama 17 jam dan untuk stripping adalah 16 jam.
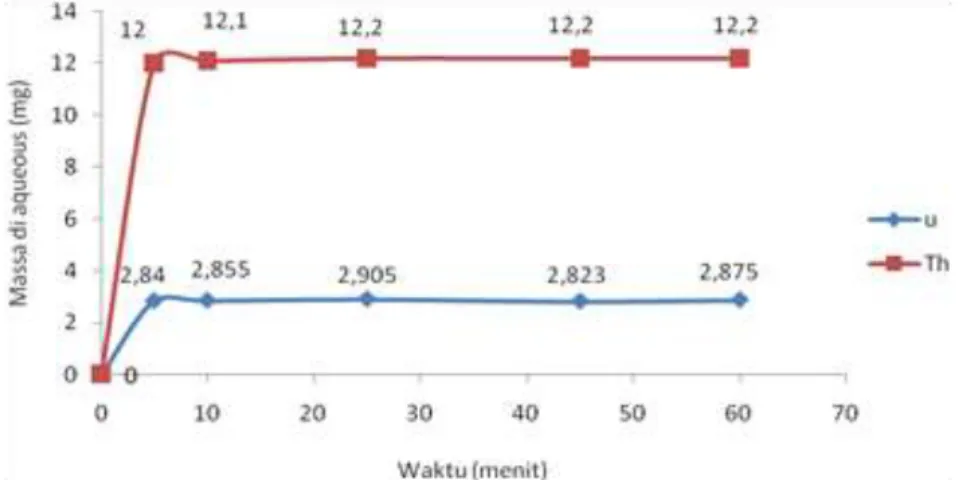
Gambar 3. Pengaruh Waktu Pengadukan Terhadap Massa Terekstrak pada Proses Stripping
Berdasarkan Gambar 2 dan Gambar 3, dapat ditentukan waktu setimbang untuk ekstraksi adalah pengadukan selama 10 menit kemudian dibiarkan terpisah selama 17 jam dan waktu setimbang stripping adalah pengadukan selama 5 menit dan dibiarkan terpisah selama 16 jam. Setiap variasi pada ekstraksi maupun stripping dilakukan pada waktu setimbang. Berdasarkan percobaan diperoleh nilai Kd pada ekstraksi dan stripping seperti ditampilkan pada Tabel 1, Tabel 2, dan Tabel 3.
Tabel 1 dan Tabel 2 digunakan sebagai data untuk mengetahui pengaruh komposisi ekstraktan terhadap Kd uranium. Adapun Tabel 3 digunakan sebagai data untuk mengetahui pengaruh konsentrasi stripper terhadap Kd uranium.
Tabel 1. Kd pada Ekstraksi Variasi TOA*
Tabel 2. Kd pada Ekstraksi Variasi Isodekanol*
Tabel 3. Kd pada Stripping Variasi Konsentrasi
Stripper
Pengaruh Perbandingan Konsentrasi Ekstraktan Terhadap Kd Uranium
Ekstraktan yang digunakan dalam proses ekstraksi adalah trioktil amin (TOA) dalam kerosen yang dimodifikasi dengan isodekanol. Pengaruh perbandingan antara TOA, kerosen, dan isodekanol dalam ekstraktan terhadap koefisien distribusi uranium diteliti dengan memvariasikan volume TOA dan volume isodekanol. Pada variasi volume TOA, isodekanol disamakan. Sementara pada variasi volume isodekanol, volume TOA disamakan. Volume kerosen mengikuti volume TOA dan isodekanol dengan jumlah perbandingan volume TOA:kerosen:isodekanol harus 100%. Data koefisien distribusi dibuat menjadi grafik yang ditunjukkan pada Gambar 4.
Gambar 4. Hubungan Perbandingan Ekstraktan (Variasi Konsentrasi TOA) dengan Kd U, Th, LTJ2O3, dan PO4 (A/O = 1, pH Umpan 1,5)
Berdasarkan Gambar 4 dapat diketahui bahwa Kd uranium semakin meningkat dengan bertambahnya konsentrasi TOA dalam campuran. Ini menunjukkan bahwa konsentrasi TOA dalam campuran ekstraktan sangat berpengaruh terhadap kemampuan ekstraktan untuk mengekstrak uranium. Ritcey (2006) menyebutkan bahwa TOA yang digunakan pada sebagian besar ekstraksi uranium adalah antara 3-5% volume atau sekitar 0,05 M sampai 0,1 M sudah cukup untuk mengekstrak uranium [11].
Gambar 4 juga memperlihatkan bahwa Kd Th dan PO4 meningkat seiring dengan bertambahnya konsentrasi TOA. Hal ini menunjukkan bahwa penambahan konsentrasi TOA pada ekstraksi dari larutan asam sulfat menggunakan TOA juga dapat meningkatkan jumlah Th dan PO4 yang terekstrak di fase organik. Meskipun demikian, peningkatan nilai Kd keduanya cukup rendah. Peningkatan persentase volume TOA dari 3% menjadi 5%
volume menyebabkan nilai Kd LTJ2O3 mengalami sedikit kenaikan, kemudian turun pada penambahan 6% volume TOA. Perubahan nilai Kd Th, LTJ2O3, dan PO4 cukup kecil sehingga penambahan persentase volume TOA tidak terlalu mempengaruhi nilai Kd ketiga unsur tersebut.
Berdasarkan Gambar 4 juga diketahui bahwa terdapat perbedaan yang jauh antara nilai Kd U dengan Th, LTJ2O3, dan PO4. Hal ini menunjukkan bahwa TOA selektif terhadap uranium. Namun apabila konsentrasi Th, LTJ2O3, dan PO4 dalam umpan jauh lebih besar daripada konsentrasi U maka pemisahan cukup sulit dilakukan. Berdasarkan nilai Kd ketiga unsur tersebut dapat dihitung kandungan Th, LTJ2O3, dan PO4 (pengotor) yang keluar dari proses.
Pengaruh persentase volume isodekanol pada perbandingan ekstraktan ditampilkan dalam Gambar 5.
Gambar 5. Hubungan Perbandingan Ekstraktan (Variasi % Volume Isodekanol) Terhadap Kd U, Th,
Penambahan alkil alkohol cukup efektif untuk membantu mengurangi terbentuknya emulsi. Isodekanol dengan 2-5% volume biasa digunakan sebagai modifier untuk ekstraksi uranium dengan amin tersier. Berdasarkan Gambar 5 diketahui bahwa Kd uranium meningkat pada penambahan 2% volume isodekanol, yaitu dari 3,13 menjadi 5,06, namun mengalami penurunan pada penambahan 3%, 4%, dan 5% volume isodekanol, seperti yang telah dikatakan oleh Coleman, dkk. (1958) bahwa kehadiran isodekanol bisa meningkatkan uranium yang terekstak sampai batas tertentu [12]. Hal ini disebutkan juga oleh Crouse & Brown (1959), yang mengatakan bahwa efisiensi ekstraksi akan berkurang apabila ke dalam ekstraktan ditambahkan sejumlah besar alkohol rantai panjang seperti isodekanol, namun penambahan 2-5% volume biasanya hanya menyebabkan penurunan yang kecil [9].
Gambar 5 menunjukkan bahwa nilai Kd LTJ2O3 dan PO4 mengalami penurunan dengan bertambahnya persentase volume isodekanol dalam ekstraktan. Berbeda dengan Kd Th yang mengalami peningkatan dengan bertambahnya persentase volume isodekanol. Berdasarkan nilai Kd ketiga unsur tersebut, dapat dihitung kandungan Th, LTJ2O3, dan PO4 (pengotor) yang keluar dari proses.
Berdasarkan Gambar 4 dan Gambar 5, dapat diketahui bahwa pada 5% volume TOA, nilai Kd U dengan penambahan 2% volume isodekanol (Kd = 5,06) lebih besar daripada nilai Kd U pada penambahan 3% volume isodekanol (Kd = 3,42). Sementara nilai Kd U pada penambahan 6% volume TOA dengan 3% volume isodekanol (Kd = 6,41) memiliki perbedaan yang cukup rendah dengan nilai Kd U pada 5% volume TOA dengan penambahan 2% volume isodekanol (Kd = 5,06). Dengan demikian, dapat dikatakan bahwa ekstraksi uranium dengan menggunakan ekstraktan TOA:kerosen:isodekanol baik digunakan pada penambahan 5% volume TOA dan 2% volume isodekanol atau pada perbandingan TOA:kerosen:isodekanol = 5:93:2. Meskipun demikian, penggunaan ekstraktan juga harus memperhatikan kekentalan TOA dalam ekstraktan. Apabila penambahan persentase isodekanol terlalu kecil maka kekentalan TOA dalam ekstraktan akan lebih besar dan dapat memperbesar kemungkinan terjadinya emulsi yang tidak diharapkan.
Pengaruh Konsentrasi Stripper Terhadap Kd Uranium
Pada penelitian ini, stripping dilakukan dari ekstraktan TOA:kerosen:isodekanol = 5:92:3 dengan H2SO4 sebagai stripper. Koefisien distribusi stripping yang sebelumnya telah ditampilkan pada Tabel 3 dibuat menjadi Grafik yang ditunjukkan pada Gambar 6.
Dari Gambar 6 dapat diketahui bahwa pada stripping uranium menggunakan H2SO4 nilai Kd U menurun dari konsentrasi 0 sampai dengan 3 M, kemudian mengalami peningkatan pada konsentrasi H2SO4 3,5 M. Nilai Kd Th juga mengalami penurunan pada konsentrasi H2SO4 0 sampai dengan 1,5 M, kemudian mengalami peningkatan. Hal ini menunjukkan bahwa uranium akan lebih banyak terambil pada konsentrasi stripper yang tinggi (keasaman tinggi), namun ada batasan tingkat keasaman atau konsentrasi stripper yang baik dalam stripping uranium, dalam hal ini pada konsentrasi 3 M. Berdasarkan penjelasan Gambar 6, torium akan banyak terambil pada konsentrasi asam yang rendah. Pada konsentrasi stripper yang tinggi (keasaman tinggi) torium akan lebih stabil dalam fase organik sehingga kelarutannya dalam stripper cukup rendah. Hal ini dikarenakan ekstraksi torium baik dilakukan pada keasaman tinggi sehingga untuk mengembalikan torium ke fase cair harus pada konsentrasi asam rendah.
Nilai Kd Th pada konsentrasi H2SO4 0 sampai dengan 1,5 M lebih kecil daripada nilai Kd U, sedangkan pada konsentrasi H2SO4 2 M sampai dengan 3 M diketahui bahwa nilai Kd U lebih kecil daripada nilai Kd Th. Hal ini menunjukkan, apabila konsentrasi U dan Th dalam umpan sama maka pada rentang konsentrasi H2SO4 0 sampai 1,5 M Th akan lebih banyak terambil daripada U, sedangkan pada konsentrasi H2SO4 2 M sampai 3 M, uranium akan terambil lebih banyak. Perbedaan nilai Kd yang cukup signifikan antara Th dan U terdapat pada konsentrasi H2SO4 3 M (nilai Kd U = 0,13 dan nilai Kd Th = 2,21). Pada konsentrasi ini, nilai Kd U lebih kecil daripada Kd Th sehingga jika kandungan U dan Th dalam umpan sama, uranium akan lebih banyak terambil. Perbedaan nilai yang sangat signifikan juga terdapat pada konsentrasi H2SO4 nol (dalam hal ini stripper yang digunakan adalah aquabidest). Pada konsentasi nol, nilai Kd Th = 4,87 dan U = 79,45. Pada keadaan ini, nilai Kd U jauh lebih
besar daripada nilai Kd Th sehingga Th yang terambil akan lebih banyak daripada U. Berdasarkan penjelasan di atas dapat diketahui bahwa stripping uranium dari ekstraktan TOA:kerosen:isodekanol (5:92:3) baik dilakukan pada konsentrasi H2SO4 3M, sedangkan stripping untuk mendapatkan torium baik dilakukan menggunakan
aquabidest (konsentrasi H2SO4 nol). Pada proses ekstraksi dan stripping, dapat dipertimbangkan untuk melakukan penambahan tahap scrubbing menggunakan
aquabidest terlebih dulu untuk mengurangi
kandungan Th dalam fase organik, kemudian fase organik di-stripping menggunakan H2SO4 3 M untuk mengambil uranium.
Gambar 6. Hubungan Konsentrasi Stripper dengan Kd U dan Kd Th
Jumlah Stage Ekstraksi dan Stripping Kandungan unsur yang masuk ke dalam ekstraksi adalah U = 1700 mg/l; Th = 46 g/l; LTJ2O3 = 90,38 g/l; PO4 = 42,64 mg/l. Untuk mendapatkan recovery 95% uranium, dilakukan perhitungan recovery pada ekstraksi dan stripping. Berdasarkan perhitungan,
recovery yang ingin dicapai pada ekstraksi
adalah 99% dan pada stripping adalah 96% sehingga diperoleh recovery uranium 95%. Jumlah stage yang dibutuhkan untuk memperoleh recovery tersebut dihitung berdasarkan nilai Kd ekstraksi pada
perbandingan TOA:kerosen:isodekanol 5:92:3 (Kd U = 3,42) dan nilai Kd stripping pada konsentrasi H2SO4 3 M (Kd U = 0,13) menggunakan metode McCabe Thiele berdasarkan konsentrasi.
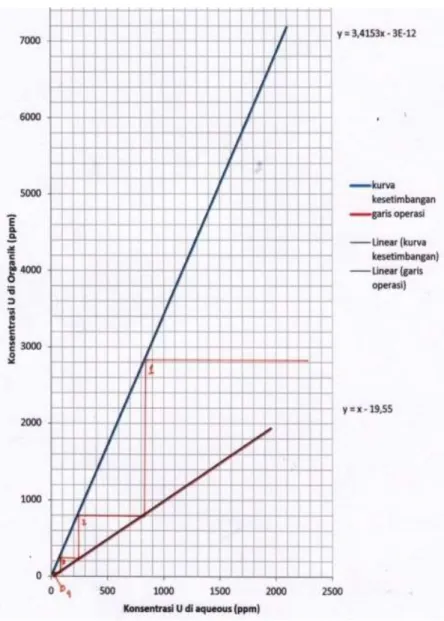
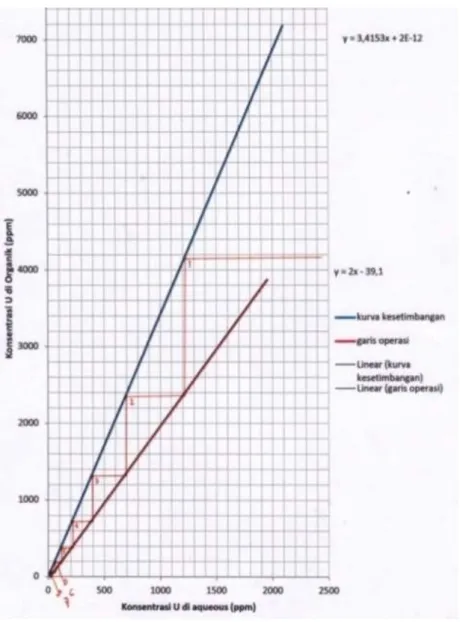
Jumlah stage teoretis untuk proses ekstraksi dihitung untuk variasi perbandingan volume cairan umpan yang masuk dan volume ekstraktan (A/O) = 1 dan 2. Jumlah stage untuk A/O = 1 ditunjukkan pada Gambar 7, sedangkan jumlah stage untuk A/O = 2 ditunjukkan pada Gambar 8.
Gambar 7. Kurva Kesetimbangan dan Garis Operasi pada Ekstraksi dengan A/O = 1
Berdasarkan Gambar 7 dan Gambar 8 dapat diketahui bahwa stage yang dibutuhkan pada ekstraksi dengan perbandingan A/O = 1 adalah sebanyak 4 stage, sedangkan jumlah
stage yang dibutuhkan pada perbandingan A/O
= 2 adalah sebanyak 7 stage. Perbandingan A/O mempengaruhi konsentrasi yang keluar dari proses ekstraksi. Semakin tinggi perbandingan A/O pada saat ekstraksi maka konsentrasi uranium dalam fase organik
menjadi semakin tinggi. Konsentrasi fase organik yang terlalu tinggi dapat menyebabkan efisiensi proses stripping berkurang. Berdasarkan nilai Kd dan jumlah stage yang terdapat pada pembahasan sebelumnya, kandungan pengotor yang keluar dari proses ekstraksi dapat dihitung. Berdasarkan perhitungan diperoleh kandungan pengotor dalam ekstraktan yang keluar dari proses, seperti ditampilkan pada Tabel 4.
Gambar 8. Kurva Kesetimbangan dan Garis Operasi pada Ekstraksi Dengan A/O = 2
Tabel 4. Kandungan Uranium dan Pengotor pada
Hasil Ekstraksi A/O Stage Kandungan Unsur U (mg/l) Th (g/l) LTJ2O3 (g/l) PO4 (mg/l) umpan - 1700 46 90,38 42,64 1 4 1683 1,06 5,85 4,139 2 7 3366 1,08 5,82 4,142
Berdasarkan Tabel 4 dapat diketahui bahwa konsentrasi pengotor yang ikut terekstrak berkurang dari konsentrasi awal di umpan ekstraksi. Hal ini menunjukkan bahwa ekstraksi cukup baik untuk mengurangi pengotor yang terekstrak. Meskipun begitu, konsentrasi Th dan LTJ2O3 dalam fase terekstrak masih lebih tinggi daripada
konsentrasi uranium. Hal ini disebabkan oleh konsentrasi Th dan LTJ2O3 di umpan yang jauh lebih besar daripada konsentrasi uranium di umpan.
Berdasarkan Tabel 4 juga dapat diketahui bahwa konsentrasi uranium dalam organik pada perbandingan A/O = 2 adalah dua kali lipat konsentrasi uranium pada perbandingan A/O = 1, sedangkan pengotor yang terdapat dalam organik pada perbandingan A/O = 1 dan A/O = 2 hampir mendekati sama sehingga ekstraksi dengan A/O = 2 lebih menguntung-kan. Selain itu, ekstraksi dengan perbandingan A/O = 2 dapat mengurangi pemakaian organik menjadi setengah dari pemakaian organik pada perbandingan A/O = 1.
Setelah menghitung jumlah stage
ekstraksi, dilakukan penentuan jumlah stage
stripping. Umpan yang masuk ke proses stripping merupakan organik hasil ekstraksi
Th, LTJ2O3, dan PO4 yang masuk ke proses
stripping telah ditampilkan dalam Tabel 4.
Perhitungan jumlah stage teoretis pada proses
stripping dilakukan untuk perbandingan A/O =
1, 1/2, dan 1/5. Grafik perhitungan jumlah
stage stripping pada masing-masing perbandingan A/O secara berurutan ditampilkan pada Gambar 9, Gambar 10, dan Gambar 11.
Gambar 10. Kurva Kesetimbangan dan Garis Operasi pada Stripping A/O = ½
Berdasarkan Gambar 9, Gambar 10, dan Gambar 11 dapat diketahui bahwa jumlah
stage teoretis yang dibutuhkan pada stripping
dengan perbandingan A/O = 1 adalah 2 stage, perbandingan A/O = 1/2 adalah 3 stage, dan perbandingan A/O = 1/5 adalah 6 stage. Pada proses stripping, semakin kecil perbandingan A/O maka konsentrasi uranium dalam larutan
stripper akan semakin tinggi sehingga akan
memudahkan proses selanjutnya, yaitu proses
pengendapan. Pada penentuan jumlah stage ini dipilih stage ekstraksi dengan perbandingan A/O = 2, yaitu 7 stage dan stage stripping dengan perbandingan A/O = 1/5, yaitu 6 stage. Pemilihan ini dilakukan berdasarkan konsentrasi uranium yang keluar dari proses
stripping pada perbandingan A/O = 1/5
menjadi lebih tinggi sehingga akan memudahkan proses pengendapan.
Gambar 11. Kurva Kesetimbangan dan Garis Operasi pada Stripping A/O = 1/5
KESIMPULAN
Peningkatan jumlah TOA pada perbandingan ekstraktan (TOA:kerosen:isodekanol) menye-babkan peningkatan nilai Kd uranium dan peningkatan hingga 2% volume isodekanol juga menyebabkan peningkatan Kd uranium, kemudian turun perlahan. Ekstraksi uranium baik dilakukan pada perbandingan ekstraktan 5:93:2.
1. Peningkatan konsentrasi stripper sampai dengan konsentrasi H2SO4 3 M menyebabkan kenaikan nilai Kd uranium, namun setelah konsentrasi H2SO4 3M nilai Kd uranium kembali turun. Stripping torium baik dilakukan pada konsentrasi H2SO4 3 M.
2. Nilai koefisien distribusi pada ekstraksi dengan perbandingan ekstraktan (TOA:kerosen:isodekanol = 5:92:3) adalah: U = 3,42; Th = 0,02; LTJ2O3 = 0,07; dan PO4 = 0,10. Nilai Kd pada
stripping uranium dari ekstraktan tersebut, dengan menggunakan H2SO4 3 M adalah U = 0,13 dan Th = 2,21. 3. Jumlah stage ekstraksi-stripping yang
di-butuhkan untuk memperoleh recovery 95% dengan ekstraksi menggunakan eks-traktan TOA:kerosen:isodekanol= 5:92:3 dan stripper H2SO4 3 M adalah 7 stage ekstraksi pada perbandingan A/O= 2 dan 6 stage stripping pada perbandingan A/O = 1/5.
DAFTAR PUSTAKA
1. Trinopiawan, K., R. Prassanti, Sumarni, & R. Pudjianto, 2012. “Pemisahan U dari Th pada Monasit dengan Metode Ekstraksi Pelarut Alamine.” dalam:
Seminar Geologi Nuklir dan Sumber Daya Tambang PPGN-BATAN. Jakarta.
2. Nuri, H.L., Prayitno, A. Jami, & M. Pancoko, 2014. “Kebutuhan Desain Awal pada Pilot Plant Pengolahan Monasit Menjadi Thorium Oksida (ThO2).” dalam: Eksplorium, Vol. 35, No.2, November, hal. 131–141.
3. Cuthbert, F., 1958. Thorium Production
Technology. USA: Addison Wesley
Publishing Company, Inc.
4. Basset, J., R. Denny, G. Jeffrey & J. Mendham, 1994. Buku Ajar Vogel Kimia
Analisis Kuantitatif Anorganik. Jakarta:
Penerbit Buku Kedokteran EGC.
5. Clegg, J. W. & D.D. Foley, 1958.
Uranium Ore Processing. USA: Addisson Wesley Publishing Company, Inc.
6. Benedict, M. & T.H. Pigford, 1957.
Nuclear Chemical Engineering. New
York Toronto London: McGraw-Hill Book Company, Inc.
7. Crouse, D. & K. Brown, 1959. Recovery of Thorium, Uranium, and Rare Earths from Monazite Sulfat Leach Liquors by the Amine Extraction (Amex) Process. Oak Ridge National Laboratory-Union Carbide Nuclear Company.
8. Setyadji, M. & E. Susiantini, 2002. “Pengaruh Prosen TBP dan Perbandingan Umpan dan Pelarut pada Ekstraksi Uranium-Thorium Proses Thorex.” dalam: Prosiding Pertemuan
dan Presentasi Ilmiah Penelitian Dasar Ilmu Pengetahuan dan Teknologi Nuklir P3TM-BATAN. Yogyakarta.
9. Morais, C., L. Gomiero, W. Filho & J. Rangel, 2005. “Uranium Stripping from Tertiary Amine by Sulfuric Acid Solution and Its Precipitation as Uranium Peroxide. in: Minerals Engineering, Vol. 18 Issues 13-14, hal.
1331–1333.
10. Warade, A., R. Gaikwad, R. Sapkal & V. Sapkal, 2011. “Simulation of Multistage Countercurrent Liquid-Liquid Extrac-tion.” in: Leonardo Journal of Science, hal. 79–94.
11. Ritcey, G., 2006. Solvent Extraction-Principles and Applications to Process Metallurgy. Canada: G.M. Ritcey & Associates Incorporated.
12. Coleman, C., K. Brown, J. Moore & D. Crouse, 1958. Solvent Extraction with
Alkyl Amine. International Mining:
EKSTRAKSI DAN STRIPPING TORIUM DARI RAFINAT HASIL
EKSTRAKSI URANIUM MONASIT BANGKA
Rida Ferliana
1, Bangun Wasito
1, Riesna Prassanti
21) Teknokimia Nuklir STTN-BATAN, Jl. Babarsari, Kotak Pos 6101 YKBB Yogyakarta
55281
2) PTBGN-BATAN, Jl. Lebak Bulus Raya No.9. Ps. Jumat, Jakarta 12440
ABSTRAK
EKSTRAKSI DAN STRIPPING TORIUM DARI RAFINAT HASIL EKSTRAKSI URANIUM MONASIT BANGKA. Pusat Teknologi Bahan Galian Nuklir–Badan Tenaga Nuklir Nasional (PTBGN-BATAN) yang bekerja sama dengan PT Timah mengimplementasikan penelitian pengolahan monasit menjadi logam tanah jarang ke dalam skala pilot plant 50 kg/hari. Kegiatan tersebut menghasilkan limbah berupa unsur radioaktif, seperti uranium dan torium. Torium merupakan alternatif pengganti bahan bakar uranium. Agar dapat dijadikan bahan bakar nuklir, torium perlu dipisahkan terlebih dahulu. Salah satu metode pemisahan adalah ekstraksi-stripping. Ekstraksi-stripping torium dilakukan dengan menggunakan rafinat hasil ekstraksi uranium pada limbah pengolahan monasit. Solvent yang digunakan dalam ekstraksi adalah TBP dan dalam stripping adalah HNO3 encer. Berdasarkan penelitian diperoleh bahwa semakin tinggi keasaman umpan, maka recovery dan koefisien distribusi torium semakin meningkat; serta semakin tinggi konsentrasi HNO3, maka recovery semakin menurun dan koefisien distribusi torium semakin meningkat. Ekstraksi selama 15 menit, pH umpan 0,09, TBP/kerosen 50/50, dan perbandingan A/O = 1/1 memberikan koefisien distribusi sebesar 13,80 dengan recovery ekstraksi sebesar 93%. Stripping selama 15 menit, konsentrasi HNO3 0,1 N, dan perbandingan A/O = 1/1 memberikan koefisien distribusi 1,57 dengan recovery sebesar 38,92%. Jika recovery torium ingin ditingkatkan menjadi 95%, maka dibutuhkan 2 stage ekstraksi pada perbandingan A/O = 1/1, 8 stage stripping pada perbandingan A/O = 2/1, dan 5 stage stripping pada perbandingan A/O = 3/1. Kata kunci: monasit, ekstraksi, stripping, torium, uranium, logam tanah jarang, koefisien distribusi, stage
ABSTRACT
THORIUM EXTRACTION AND STRIPPING FROM URANIUM EXTRACTION RAFFINATE OF BANGKA MONAZITE. Centre for Nuclear Mineral Geology–National Nuclear Energy Agency in cooperation with PT Timah (TINS) has conducted a project of turning monazite into rare earth elements pilot plant of 50 kg/day. This project would produce radioactive wastes such as uranium and thorium. Thorium is an alternative fuel source to uranium. In order to be able to be used as nuclear fuel, the impurities must be separated from the thorium. One of the separation methods is extraction-stripping. Extraction and stripping of thorium was made by using raffinate of uranium extraction of rare earth elements wastes. Solvent used in extraction is TBP and in stripping is diluted acid. This research showed that the higher the acidity of feed, the more possibility of recovery and distribution coefficients of thorium will increase in the extraction; and the higher the concentration of HNO3, the more possibility of recovery will decrease and distribution coefficients of
thorium in the stripping will increase. Extraction in 15 minutes, with feed pH 0,09, TBP/kerosene 50/50, and A/O = 1/1 resulted in a distribution coefficient of 13,8 with the recovery of thorium to be 93,24%. Stripping in 15 minutes, with HNO3 0,1 N, and A/O = 1/1 resulted in a distribution coefficient of 1,57 with the recovery
of thorium to be 38,92%. To increase recovery of thorium up to 95%, it would need two stages of extraction of A/O = 1/1, 8 stages of stripping of A/O = 2/1, and 5 stages of stripping of A/O = 3/1.
Keywords: monazite, extraction, stripping, thorium, uranium, rare earth element, distribution coefficient, stage
PENDAHULUAN
Monasit merupakan senyawa fosfat logam tanah jarang yang mengandung oksida logam tanah jarang, uranium, dan torium. Monasit Bangka merupakan hasil samping pencucian bijih timah oleh PT Timah. Monasit tersebut mengandung unsur-unsur logam tanah jarang sebesar 50,97%, uranium 0,298%, torium 4,147%, dan fosfat 23,712% [1]. Logam tanah jarang dapat digunakan pada energi nuklir, kimia, katalisator, elektronik, dan optik. Uranium dan torium digunakan sebagai bahan bakar nuklir, sedangkan fosfat digunakan dalam industri pupuk.
PTBGN-BATAN bekerja sama dengan PT Timah melakukan penelitian pengolahan monasit secara basa, dengan tahapan: preparasi monasit, dekomposisi, pelarutan parsial, pengendapan U dan Th, serta pengendapan RE(OH)3 seperti yang ditunjukkan pada Gambar 1. Berdasarkan hasil analisis di Laboratorium Chemex Canada, diperoleh RE2O3 > 55,23%, U < 2 ppm, dan Th 16 ppm, sedangkan hasil analisis di laboratorium Alfred H.K., London diperoleh RE2O3 76,12%, dengan U dan Th < 50 ppm [2].
Gambar 1. Pengolahan Monasit Secara Basa oleh
PTBGN-BATAN [3]
Penelitian tersebut diimplementasikan dalam pilot plant 50 kg/hari sehingga hasil samping yang berupa uranium dan torium perlu dipikirkan. Meskipun paparan yang diterima masyarakat sangat rendah,
pencemaran uranium dan torium sangat tidak diharapkan. Uranium-238 dan torium-232 merupakan penghasil radiasi alfa sehingga dapat menimbulkan bahaya internal yang sangat tinggi. Dengan mengambil atau mengolahnya, uranium dan torium dapat menjadi bahan bakar nuklir.
Agar dapat dijadikan bahan bakar nuklir, torium harus memiliki kemurnian tinggi, yakni lebih dari 87,42% [4]. Penelitian Trinopiawan dkk. mengenai pemisahan uranium dari torium dengan ekstraksi menggunakan alamin memberikan recovery uranium 100%, torium 32,44%, logam tanah jarang 2,24%, dan fosfat tidak terdeteksi [5]. Berdasarkan hasil tersebut, uranium sudah mampu diambil, namun torium dan logam tanah jarang dalam rafinat masih sangat tinggi. Logam tanah jarang seperti gadolinium, samarium, dan disprosium merupakan penyerap neutron yang sebaik elemen boron dan kadmium [6] sehingga torium harus dipisahkan dari logam tanah jarang.
Dalam penelitian ini akan dilakukan pemisahan torium dari rafinat hasil ekstraksi uranium dengan metode ekstraksi-stripping. Penelitian mengenai pemurnian torium menggunakan TBP sudah pernah dilakukan, namun umpan yang digunakan berbeda serta ada beberapa kondisi yang perlu dicari. Pada penelitian ini akan ditentukan pengaruh pH umpan dalam ekstraksi torium. pH umpan yang diperoleh kemudian dapat dijadikan pengontrol dalam pelarutan umpan. Setelah proses ekstraksi, dilakukan pengembalian fase organik ke dalam fase aqueous melalui proses
stripping. Data mengenai koefisien distribusi stripping belum ditemukan sehingga perlu
ditentukan besarnya koefisien distribusi pada setiap variasi konsentrasi stripper.
Penelitian ini difokuskan untuk mencari jumlah stage yang dibutuhkan untuk perancangan. Koefisien distribusi ekstraksi dan data-data yang sudah ada dapat dijadikan sebagai acuan penelitian.
TEORI
Ekstraksi Torium Menggunakan TBP Ekstraksi merupakan proses pemisahan satu atau lebih zat terlarut dari larutannya dengan menggunakan pelarut lain. Solvent yang sering digunakan dalam pemurnian torium adalah TBP, yaitu senyawa organofosfat yang bersifat netral yang mempunyai rumus struktur