PEMBUATAN PERMUKAAN SELEKTIF RADIASI
SURYA PADA PELAT ALUMINIUM
DENGAN PENCELUPAN LARUTAN NaOH 20%
TUGAS AKHIR
Diajukan untuk memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Teknik
Jurusan Teknik Mesin
Disusun oleh:
ANTONIUS ANDRI WAROTO
025214104
PROGRAM STUDI TEKNIK MESIN
JURUSAN TEKNIK MESIN
FAKULTAS TEKNIK
UNIVERSITAS SANATA DHARMA
YOGYAKARTA
THE MAKING OF SOLAR RADIATION SELECTIVE
SURFACE ON ALLUMINIUM BY DIPPING IN 20%
NaOH SOLUTION
FINAL PROJECT
Presented as Partial Fulfillment of the Requirements to Obtain the Sarjana Teknik Degree
in Mechanical Engineering
by
ANTONIUS ANDRI WAROTO
Student Number : 025214104
MECHANICAL ENGINEERING STUDY PROGRAM
MECHANICAL ENGINEERING DEPARTMENT
ENGINEERING FACULTY
SANATA DHARMA UNIVERSITY
TUGAS AKIIIR
PEMBUATAN PERMUKAAN SELEKTIF RADIASI
SURYA PADA PELAT ALUMINIUM
DENGAI\I PENCELUPAN LARUTAITI NaOH 20Vo
Disusun oleh:
Antonius Andri Waroto
NIM: 425214104
Telah disetujui oleh:
Pembimbing
PEMBUATAN PBRMUKAAN SELEKTIF RADIASI
SURYA PADA PBLAT ALUMINIUM
DENGAN PBNCELUPAN LARUTAN NaOH 2OOA
Dipersiapkan
dan ditulis oleh:
Antonius Andri Waroto
NIM:025214104
Telah dipertahankan
di depan panitia penguji
pada tanggal 24 Jnli 20A7
dan dinyatakan
memenuhi syarat
Ketua
Sekretaris
Anggota
Yogyakarta, 24 JuJi2A07
Fakultas Teknik
Universitas Sanata
Dharma
PERNYATAAN
Dengan ini saya
bahwa dalam tugas akhir ini tidak terdapat kuya
yang pernatr diajukarr untuk memperoleh gelar kesarjanaan
di suatu Perguruan
Tinggr, dan sepanjang
pengetahuan
saya juga tidak terdapatkarya atau pendapat
yang pernah ditulis atau diterbitkan oleh orang lairu kecuali yang sectra tertulis
diacu dalam naskah dan disebutkan
dalam daftar pustaka.
Yogyakarta,24
Jtufi2AA7
Penulis
INTISARI
Tujuan penelitian ini adalah untuk mengetahui pengaruh pencelupan pelat Aluminium dalam larutan NaOH 20% dengan variasi waktu, terhadap absorptivitas dan emisivitas suatu bahan. Bahan yang dipakai adalah pelat aluminium dengan tebal 2 mm.
Dalam pembuatan spesimen ada 2 variasi pencelupan yaitu : variasi A pencelupan pelat aluminium dalam larutan NaOH 20% dengan pengeringan secara alami sedangkan variasi B pencelupan pelat aluminium dalam larutan NaOH 20% dengan pengeringan dilap. Untuk setiap variasi pencelupan dibagi lagi pengerjaannya berdasarkan waktu pencelupan, yaitu : 5 detik, 10 detik dan 15 detik. Setelah dilakukan pencelupan, kemudian dilakukan pengujian radiasi untuk mengetahui besar absorptivitas surya dan emisivitas termal serta suhu yang diserap oleh aluminium yang telah mengalami pencelupan dalam larutan NaOH 20%.
Absorptivitas dan emisivitas pelat aluminium dengan metode dipping in
chemical baths (permukaan dikasarkan dengan direndam dalam larutan kimia
NaOH) dapat meningkatkan absorptivitas 5 - 10 kali lipat, emisivitas juga meningkat 2 - 3 kali lipat serta kenaikan suhu yang diserap benda uji 2 ºC - 10 ºC.
Dalam pengujian ini waktu pencelupan tidak berpengaruh secara signifikan tehadap besar kecilnya nilai absorptivitas dan emisivitas serta suhu yang diserap benda uji.
ABSTRACT
The aim of this research is to know the influence of the time variation immersion of aluminium plate into NaOH 20% towards absorptivity and emmisivity of a material. The used material is an aluminium plate of 2 mm thick.
There are two variations of immersion, namely: variation A, that is the immersion of aluminium plate into NaOH 20% with natural drying up, and variation B, that is the immersion of aluminium plate into NaOH 20% with manual drying up (using napkin). For each variation, further it can be divided based on the time of immersion, namely 5- second immersion, 10-second immersion and 15-second immersion. After the immersion, then radiation testing is done to know the amount of solar absorptivity, thermal emmisivity and temperature absorbed by aluminium which has undergone immersion into NaOH 20%.
The absorptivity and emmisivity plate aluminium using dipping in chemical baths method it can seen that it can increase absoptivity five to ten folds. Emmisivity also increases two to three folds, and temperature incresases between 2 C to 10 C. In this testing, the time of immersion it does not influence significantly towards the value of absorptivity, emmisivity, and temperature which absorber by the material.
KATA PENGANTAR
Puji syukur penulis panjatkan bagi Tuhan Yang Maha Esa yang telah memberikan kasih karunianya yang besar, yang senantiasa selalu menuntun langkah demi langkah hingga akhirnya penulis dapat menyelesaikan Tugas Akhir ini, yang merupakan salah satu syarat yang harus ditempuh untuk memperoleh gelar sarjana Teknik di jurusan Teknik Mesin Fakultas Teknik Universitas Sanata Dharma Yogyakarta.
Pada kesempatan ini penulis ingin mengucapkan banyak terima kasih atas segala bantuan yang berupa moril maupun materiil dari semua pihak terutama kepada:
1. Romo Ir. Greg. Heliarko SJ.,S.S.,B.S.T.,M.A.,M.Sc., Dekan Fakultas Teknik Universitas Sanata Dharma Yogyakarta.
2. Bapak Budi Setyahandana, S.T., M.T., Dosen Pembimbing yang telah membimbing dalam penyelesaian Tugas Akhir ini.
3. Laboran Laboratorium Teknologi Mekanik dan Laboratorium Perpindahan Panas Universitas Sanata Dharma yang telah membantu penelitian penulis. 4. Segenap dosen dan karyawan Jurusan Teknik Mesin FT-USD yang telah
membantu dan selalu membimbing dalam masa-masa kuliah.
6. Untuk teman-teman Dyah, Budi, Welly, Yohan, Pajar, Panut, Dwi, Wiwin, Beni Bantul, Sigit, Danang, Agung, Beni, dan teman-teman TM angkatan 2002 yang telah mendukung kelancaran penyusunan Tugas Akhir ini.
Tiada kata yang bisa penulis ucapkan selain terima kasih dan semoga Tuhan selalu memberkati dan membalas segala kebaikan anda semua.
Demikian usaha yang telah penulis lakukan sudah semaksimal mungkin, namun penulis menyadari bahwa penulisan Tugas Akhir ini masih jauh dari sempurna, oleh karena itu dengan terbuka dan senang hati menerima saran dan kritik yang sifatnya membangun demi kemajuan yang akan datang.
Semoga penulisan Tugas Akhir ini dapat berguna dan memberikan wawasan lebih tentang ilmu pengetahuan dan teknologi bagi semua pembaca.
Yogyakarta, 24 Juli 2007
DAFTAR ISI
HALAMAN JUDUL……….………...………... i
HALAMAN JUDUL BAHASA INGGRIS... ii
HALAMAN PENGESAHAN PEMBIMBING... iii
HALAMAN PENGESAHAN PENGUJI DAN DEKAN... iv
HALAMAN PERNYATAAN... v
INTISARI... vi
ABSTRACT... vii
KATA PENGANTAR... viii
DAFTAR ISI... x
DAFTAR GAMBAR... xiii
DAFTAR TABEL... xv
BAB I PENDAHULUAN... 1
1.1. Latar Belakang... 1
1.2. Batasan Masalah... 4
1.3. Tujuan Penelitian... 4
1.4. Sistematika Penulisan... 4
BAB II DASAR TEORI... 6
2.1. Pengantar... 6
2.2. Perpindahan Kalor... 7
2.2.2. Perpindahan Kalor Konveksi... 8
2.2.3. Perpindahan Kalor Radiasi... 8
2.3. Pelat Absorber... 14
2.3.1. Sifat-sifat Pelat Absorber... 14
2.3.2. Pembuatan Permukaan Selektif... 15
2.3.3. Bahan Pelat Absorber... 17
2.4. Alumunium... 18
2.4.1. Sifat-sifat Alumunium... 20
2.4.2. Pengaruh Unsur-unsur Logam Paduan Aluminium... 22
2.5. Larutan Kimia………... 24
2.5.1. Konsentrasi Larutan………... 24
2.5.2. Sifat-sifat Larutan………... 27
BAB III METODE PENELITIAN... 30
3.1. Skema Penelitian... 30
3.2. Cara Penelitian... 31
3.3. Proses Pembuatan Benda Uji... 32
3.4. Proses Pencelupan Dalam Larutan NaOH... 32
3.5. Larutan………... 33
3.6. Pengujian Bahan... 34
3.6.1. Pengujian Absorptivitas Surya... 34
3.6.2. Pengujian Emisivitas Thermal... 36
BAB IV DATA PENELITIAN DAN PEMBAHASAN... 41
4.1. Analisis Pengujian Absorptivitas... 41
4.2. Analisis Pengujian Emisivitas... 45
4.3. Analisis Pengujian dengan Sinar Matahari... 51
BAB V KESIMPULAN DAN PENUTUP... 55
5.1. Kesimpulan... 55
5.2. Penutup... 56
5.3. Saran... 56
DAFTAR GAMBAR
Gambar 2.1. Pengaruh Radiasi Datang... 9
Gambar 2.2. Refleksi Spekular dan Refleksi Baur... 10
Gambar 2.3. Sudut Azimut dan Sudut Polar... 11
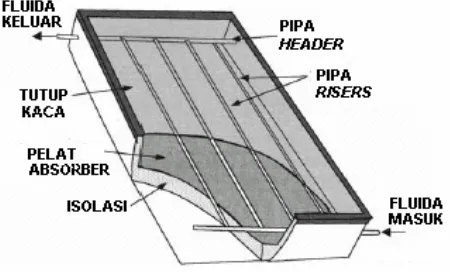
Gambar 2.4. Contoh Penggunaan Pelat Absorber... 12
Gambar 3.1. Diagram Alur Penelitian…... 30
Gambar 3.2. Bentuk Benda Uji…... 32
Gambar 3.3. Alat Penguji Absorptivitas... 35
Gambar 3.4. Pemasangan Spesimen... 37
Gambar 3.5. Panel Indikator... 38
Gambar 3.6. Pemasangan Spesimen... 40
Gambar 4.1. Diagram Absorptivitas Tanpa Pencelupan... 43
Gambar 4.2. Diagram Pengaruh Waktu Pencelupan Pada Absoptivitas... 44
Gambar 4.3. Diagram Pengaruh Waktu Pencelupan Pada Absoptivitas... 44
Gambar 4.4. Diagram Pengaruh Pencelupan NaOH Pada Absoptivitas... 45
Gambar 4.5. Diagram Emisivitas Tanpa Pencelupan………... 49
Gambar 4.6. Diagram Pengaruh Waktu Pencelupan Pada Emisivitas... 49
Gambar 4.7. Diagram Pengaruh Waktu Pencelupan Pada Emisivitas... 50
Gambar 4.8. Diagram Pengaruh Pencelupan NaOH Pada Emisivitas…... 50
Gambar 4.9. Diagram pemanasan dengan sinar matahari terhadap waktu... 52
DAFTAR TABEL
Tabel 2.1. Sifat-sifat Fisik Aluminium... 19
Tabel 2.2. Sifat-sifat Mekanik Aluminium... 19
Tabel 2.3. Contoh Beberapa Asam... 28
Tabel 2.4. Contoh Beberapa Basa……... 29
Tabel 4.1. Data Hasil Pengujian Absorptivitas Surya Material Awal... 41
Tabel 4.2. Data Hasil Pengujian Absorptivitas Surya Pengeringan Alami... 41
Tabel 4.3. Data Hasil Pengujian Absorptivitas Surya Pengeringan Dilap... 42
Tabel 4.4. Data Hasil Pengujian Emisivitas Thermal Material Awal... 46
Tabel 4.5. Data Hasil Pengujian Emisivitas Thermal Pengeringan Alami... 46
Tabel 4.6. Data Hasil Pengujian Emisivitas Thermal Pengeringan Dilap... 47
BAB I
PENDAHULUAN
1.1. Latar Belakang
Dari jaman dahulu manusia telah mengenal energi, hampir semua kegiatan manusia membutuhkan energi, tidak hanya manusia tumbuhan dan mahluk hidup lainnya pasti sangat membutuhkannya. Energi tidak bisa lepas dari kehidupan ini karena tanpa adanya energi mungkin semuanya akan punah dan untuk itu alam pun telah menyediakan banyak sekali sumber-sumber energi yang dapat dimanfaatkan untuk memenuhi itu semua. Adapun energi yang paling banyak digunakan sekarang ini berasal dari perut bumi yang sewaktu-waktu dapat habis, misalnya seperti energi minyak bumi, gas, batu bara dll. Minyak bumi itu sendiri berasal dari kumpulan fosil-fosil yang telah lama terkubur dan mengendap di dalam tanah. Seiring perkembangan jaman dan pertumbuhan jumlah penduduk yang sangat pesat maka kebutuhan akan energi semakin banyak pula dan itu memaksa untuk menggali dan mengambil energi dari perut bumi secara besar-besaran. Sementara jumlah energi yang ada di dasar perut bumi ini kian hari berkurang dan tidak menutup kemungkinan akan habis.
2
yang dapat dimanfaatkan sebagai energi pengganti minyak bumi yang jumlahnya kian menipis energi alternatif ini jumlahnya masih berlimpah dan yang tak akan pernah habis oleh waktu, contohnya : energi surya, energi gelombang, energi angin, energi air, dan akhir-akhir ini juga telah dikembangkan energi gas dari kotoran hewan dan juga energi pengganti bensin yang berasal dari tumbuh-tumbuhan. Sebagai negara yang memiliki panas matahari yang berlimpah karena musim panas lebih panjang dibandingkan dengam musim dingin maka kita dapat memanfaatkan kelebihan ini untuk memilih salah suatu energi alternatif yang cocok untuk digunakan di negara Indonesia tercinta ini yaitu menggunakan energi surya. Enegi surya selain banyak terdapat disekitar kita juga hemat dan yang tidak kalah pentingnya adalah ramah lingkungan. Dengan memanfaatkan potensi energi tersebut maka dapat digunakan teknologi radiasi termal (thermal
radiation) yaitu radiasi elektromagnetik yang dipancarkan oleh suatu benda
karena suhunya. Bila energi radiasi menimpa permukaan suatu benda maka sebagian dari radiasi itu akan dipantulkan (refleksi), sebagian diserap (absorpsi), dan sebagian lagi diteruskan (transmisi). Ada dua fenomena refleksi yang dapat diamati bila radiasi menimpa permukaan. Jika sudut jatuhnya sama dengan sudut refleksi maka dikatakan refleksi itu spekular, dilain pihak apabila berkas yang jatuh itu tersebar secara merata kesegala arah sesudah refleksi maka refleksi itu disebut baur (diffuse).
mengumpulkan radiasi surya sebanyak mungkin dan mengalirkan energi yang didapat ke fluida kerja. Hal yang harus diperhatikan dalam kolektor ini adalah efisiensi konversi, yang semuanya dipengaruhi oleh sifat-sifat pada pelat absorber pada kolektor itu sendiri. Namun demikian juga harus diperhatikan faktor-faktor yang mempengaruhi pelat absorber, dalam penggunaannya untuk menyerap radiasi surya (radiasi gelombang pendek), dalam hal ini disebut faktor absorptivitas surya, semakin besar nilai absorptivitasnya maka semakin besar efisisensi konversi pelat absorber tersebut. Dengan keadaan pelat absorber yang menyerap radiasi surya maka temperatur pelat akan naik, sehingga dengan sifat alami suatu benda yang bertemperatur lebih tinggi dari benda sekitar akan memancarkan energi secara radiasi.
Biasanya permukaan benda yang kasar lebih menunjukan sifat baur
4
1.2. Batasan Masalah
1. Material yang digunakan dalam penelitian ini adalah pelat alumunium dengan tebal 2 mm.
2. Metode peningkatan absorptivitas termal pelat yang digunakan adalah secara dipping inchemical baths.
3. Dengan metode dipping in chemical baths benda uji permukaannya dikasarkan dengan cara direndam pada larutan NaOH dengan waktu dan cara yang beragam.
4. Hanya dilakukan pengujian untuk mencari besar absorptivitas dan emisivitas.
1.3. Tujuan Penelitian
Penelitian ini dilakukan dengan tujuan untuk :
1. Mengetahui absorptivitas surya termal dan emisivitas termal pada pelat aluminium yang telah direndam pada larutan NaOH.
2. Mencari metode pencelupan yang menghasilkan absorptivitas termal yang paling tinggi.
3. Mencari data untuk mendukung pengadaan energi alternatif yang lebih hemat dan bermanfaat.
1.4. Sistematika Penulisan
BAB II
DASAR TEORI
2.1. Pengantar
Di dalam perancangan peralatan konversi energi surya sebuah kolektor berperan sangat penting untuk menentukan besar kecilnya energi yang diserap, dipantulkan dan yang diteruskan. Selain itu yang sangat menentukan pula besar atau kecilnya energi yang dikonversi adalah aliran fluidanya. Pada umumnya peralatan seperti ini menggunakan fluida cairan, karena koefisisen aliran laminer dan koefisien perpindahan panas dalam pipa sama. Untuk memperbesar perpindahan panas biasanya aliran laminer dibuat supaya menjadi turbulen dengan memberikan gangguan pada aliran itu.
2.2. Perpindahan Kalor
Perpindahan kalor atau alih bahan (heat transfer) adalah ilmu untuk meramalkan perpindahan energi yang terjadi karena adanya perbedaan suhu diantara benda atau material. Istilah-istilah yang digunakan untuk menyatakan tiga modus perpindahan kalor, yaitu konduksi atau hantaran, konveksi atau ilian dan radiasi atau sinaran.
2.2.1. Perpindahan Kalor Konduksi
Perpindahan energi terjadi dari bagian yang bersuhu tinggi kebagian yang bersuhu rendah. Kita katakan bahwa energi berpindah secara konduksi atau hantaran dan bahwa laju perpindahan kalor itu berbanding dengan gradien suhu normal :
x T A q
Jika dimasukan konstanta proporsionalitas (proportionality constant)
x T kA q
Di mana :
q = Laju perpindahan kalor, watt K = konduktivitas termal, W/(m.K)
A = luas penampang tegak lurus pada aliran panas, m2
x T
8
2.2.2. Perpindahan Kalor Konveksi
Perpindahan panas secara tak langsung/tanpa media penghantar, seperti halnya jika udara yang mengalir di atas suatu permukaan panas kemudian permukaan lain menjadi panas. Apabila aliran udara/fluida disebabkan oleh sebuah blower maka disebut konveksi paksa. Dalam perancangan sebuah kolektor surya biasanya perpindahan panas konveksi dinyatakan dengan hukum pendinginan Newton, sebagai berikut :
qhA(Tw T) Yang diketahui di mana :
h = koefisisen konveksi, W/(m2.K) A = luas permukaan, m2
Tw = temperatur dinding
T = temperatur fluida, K
Di sini laju perpindahan kalor dihubungkan dengan beda suhu menyeluruh antara dinding dan fluida, dan luas permukaan A. Besaran h disebut koefesien perpindahan kalor konveksi (convection heat transfer coefficient). Dari pembahasan di atas diharapkan bahwa perpindahan kalor konveksi bergantung pada viskositas fluida disamping ketergantungannya kepada sifat-sifat termal fluida tersebut.
2.2.3. Perpindahan Kalor Radiasi
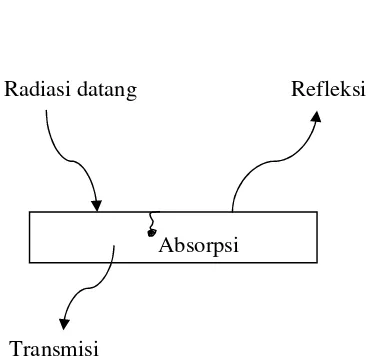
berpindah melalui daerah-daerah hampa. Mekanisme disini adalah sinaran atau radiasi elektromagnetik yang dipancarkan oleh suatu benda karena suhunya. Bila energi radiasi menimpa permukaan suatu benda, maka sebagian dari radiasi itu dipantulkan (refleksi), sebagian diserap (absorpsi), dan sebagian lagi diteruskan (transmisi), seperti digambarkan pada gambar 2.1. Fraksi yang dipantulkan kita namakan reflektivitas (ñ), fraksi yang diserap absorptivitas (á) fraksi yang diteruskan teransmisivitas( ô), maka :
á + ñ+ ô = 1
Kebanyakan benda padat tidak meneruskan radiasi termal, sehingga transmisivitas dapat dianggap nol,
á + ñ = 1
Radiasi datang Refleksi
Absorpsi
Transmisi
Gambar 2.1. Pengaruh radiasi datang
10
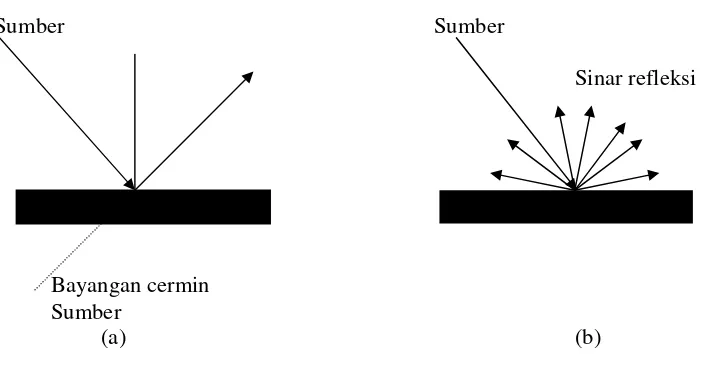
yang jatuh itu tersebar secara merata kesegala arah sesudah refleksi, maka refleksi itu disebut baur ( diffuse). Biasanya permukaan yang kasar lebih menunjukan sifat baur dari pada permukaan yang diupam mengkilap. Demikian pula permukaan yang diupam lebih spekular dari pada permukan kasar. Pengaruh kekasaran permukaan terhadap sifat-sifat radiasi termal bahan sangat besar peranannya, sehingga ini yang perlu kita pelajari lebih dalam.
Sumber Sumber
Sinar refleksi
Bayangan cermin Sumber
(a) (b)
Gambar 2.2. (a) Refleksi spekular dan (b) refleksi baur
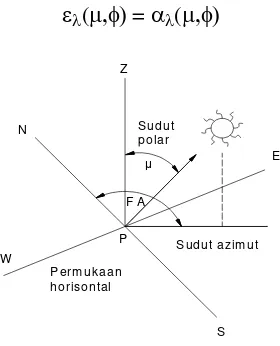
Hukum Kirchoff mengatakan bahwa suatu benda yang berada dalam kesetimbangan termodinamik akan mempunyai absorptivitas () yang sama dengan emisivitas () pada suatu panjang gelombang tertentu atau dapat dinyatakan dengan persamaan :
Persamaan di atas hanya berlaku untuk permukaan yang tidak bergantung pada sudut azimut , dan sudut polar . Jika permukaan tersebut tergantung pada sudut azimut dan sudut polar maka persamaan di atas akan menjadi :
(= (
W
E N
S P erm ukaan
horisontal
S udut azim ut F A
µ
S udut polar Z
P
Gambar 2.3. Sudut azimut dan sudut polar
Untuk permukaan yang tidak transparan (opaque) maka radiasi hanya akan diserap dan dipantulkan karena permukaan yang tidak transparan tidak meneruskan radiasi ( = 0) sehingga persamaan menjadi :
+ = + = 1
atau secara umum :
(= ((ii
Dari persamaan di atas dapat disimpulkan emisivitas dan absorptivitas dapat diketahui jika reflektivitas diketahui.
12
1. Faktor absorptivitas surya pelat absorber pada radiasi surya yang datang. 2. Emisivitas termal pelat absorber pada panjang gelombang yang panjang. 3. Kerugian panas karena konduksi, konveksi dan radiasi. Selain itu bahan
pelat absorber harus memiliki konduktivitas termal yang baik dan panas jenis yang kecil.
Efisiensi sebuah kolektor dapat dinyatakan dengan persamaan :
T a i L R R
G T T U F F
dengan :
FR : faktor pelepasan panas
: faktor transmitan-absorpan kolektor
UL : koefisien kerugian (W/(m2.K))
Ti : temperatur fluida masuk kolektor (K)
Ta : temperatur sekitar (K)
GT : radiasi yang datang (W/m2)
Dari persamaan efisiensi terlihat bahwa jika faktor absorptivitas surya () membesar maka efisiensi () akan membesar. Koefisien kerugian (UL)
merupakan fungsi beberapa faktor diantaranya emisivitas termal (). Jika emisivitas termal membesar maka koefisien kerugian membesar, sehingga efisiensi akan berkurang. Idealnya pelat absorber memiliki faktor absorptivitas surya yang besar dan emisivitas termal yang rendah. Dari beberapa metode peningkatan efisiensi kolektor, penggunaan permukaan selektif merupakan cara yang paling efektif dan ekonomis. Dari beberapa penelitian yang dilakukan ternyata peningkatan harga faktor absorptivitas surya memberikan pengaruh yang lebih besar dibandingkan penurunan faktor emisivitas termal terhadap peningkatan efisiensi kolektor. Faktor lain yang mempengaruhi koefisien kerugian adalah kualitas isolasi, makin baik isolasi maka makin kecil harga koefisien kerugian.
Perolehan panas berguna dari kolektor dapat dinyatakan dengan persamaan : )
(W/m G
.
qu T 2
Dari persamaan di atas ini terlihat bahwa jumlah panas berguna tergantung dari efisiensi kolektor.
14
4
A 4
S T
T ó å
q
dengan :
q : energi yang dipancarkan (W/m2) : emisivitas termal
: konstanta Stefan Boltzmann = 5,67 x 10-8
W/(m2.K4) TS : temperatur permukaan (K)
TA : temperatur sekitar (K)
Untuk benda hitam faktor emisivitas termal () = 1, sehingga persamaan menjadi :
4
A 4 S
b ó T T
q
dan :
b q
q
Pada penelitian ini energi yang dipancarkan (q) diukur dengan radiometer sehingga emisivitas termal () dapat diketahui.
2.3. Pelat Absorber
2.3.1. Sifat-sifat Pelat Absorber
1. Faktor absorptivitas yang besar (mendekati satu). 2. Faktor Emisivitas termal yang kecil (mendekati nol).
3. Transisi spectral yang tajam antara absorptivitas yang tinggi dengan emisivitas termal yang rendah.
4. Sifat optik dan fisik yang stabil.
5. Kualitas kontak pelat dengan lapisan selektif yang baik. 6. Mudah diaplikasikan.
7. Proses pelapisan permukaan selektif yang murah dan tidak merusak lingkungan (Pandey dan Banerjee, 1998).
2.3.2. Pembuatan Permukaan Selektif
16
a. Permukaan selektif dengan lapisan oksida tembaga.
Lapisan oksida tembaga dibentuk dengan konversi kimia, yaitu dengan mencelupkan pelat tembaga yang telah dibersihkan dan dipolis ke dalam larutan sodium hydroxide dan sodium chloride
panas selama waktu tertentu. Faktor absorptivitas surya (á) yang didapatkan sebesar 0,89 dan faktor emisivitas termal (å) yang didpatkan sebesar 0,17 (Choudhury, 2002).
b. Permukaan selektif oksida cobalt.
Dapat dibuat dengan metode electroplating pada pelat baja-nikel, dengan metode ini didapatkan faktor absorptivitas surya (á) antara 0,87 – 0,92 dan faktor emisitvitas termal (å) antara 0,07 – 0,08 (Choudhury, 2002).
c. Permukaan selektif dengan metode sputtering.
Dengan mengganti lapisan anti korosi dari nickel-chromium
menjadi copper-nickel. Dengan metode ini dapat menaikkan absorptivitas surya (á) dari 0,89 – 0,91 menjadi 0,97, dan menurunkan faktor emisivitas termal dari 0,12 menjadi 0,06 (Gelin, 2004).
d. Permukaan selektif dengan metode elektrokimia.
e. Permukaan selektif dengan metode grinding.
Untuk memperoleh permukann selektif dengan metode grinding
ini, menggunakan kekasaran permukaaan 1ìm - 2ìm. Absorptivitas surya (á) yang dihasilkan sebesar 0,90 dan emisivitas termal (å) yang dihasilkan sebesar 0,25 (Konttinen et al, 2003). Namun dengan metode grinding ini, setelah diuji dengan mikrostruktur terdapat variasi pada penggunaan komposisi dan struktur dari alat grinding. Penggunaan komposisi dan struktur yang tepat dapat mempengaruhi hasil absorptivitas surya (á) sampai diatas 0,94.
2.3.3. Bahan Pelat Absorber
18
2.4. Alumunium
Aluminium adalah unsur logam yang dapat dijumpai dalam kerak bumi dan terdapat dalam batuan seperti felspar dan mika. Aluminium juga merupakan logam yang keras, kuat, ringan dan berwarna putih meskipun sangat elektropositif bagaimanapun juga tahan terhadap korosi karena lapisan oksida yang kuat dan liat terbentuk pada permukaannya serta masih banyak lagi sifat-sifat baik lainnya sebagai sifat logam. Akan tetapi aluminium murni juga memiliki sifat mampu cor dan mekanis yang kurang baik. Oleh karena itu untuk mendapatkan sifat-sifat mekanis yang lebih baik dan yang sesuai dengan kebutuhan produksi biasanya aluminium dapat dipadukan dengan logam-logam lainnya seperti dengan penambahan Cu, Mg, Zn, Ni, dsb, secara satu persatu atau bersama-sama. Penggunaan Aluminium sebagai logam setiap tahunnya berada pada urutan kedua setelah besi dan baja, dan tertinggi diantara logam non-ferous lainnya. Hal ini disebabkan oleh sifat-sifat Alumunium yang antara lain:
- Kuat - Ringan - Tahan korosi - Mudah dibentuk
Tabel 2.1. Sifat – sifat fisik Aluminium
Kemurnian Al (%) Sifat - sifat
99,996 >99,0
Massa jenis (20o C) 2,6989 2,71
Titik cair 660,2 653-657
Panas jenis (cal/g.oC) (100oC) 0,2226 0,2297
Hantaran listrik (%) 64,94 59 (dianil)
Tahanan listrik koefisien temperatur (oC)
0,00429 0,0115
Koefisien pemuaian (20-100oC)
23,86
x
10-6 23,5x
10-6
Jenis kristal, konstanta kisi fcc fcc
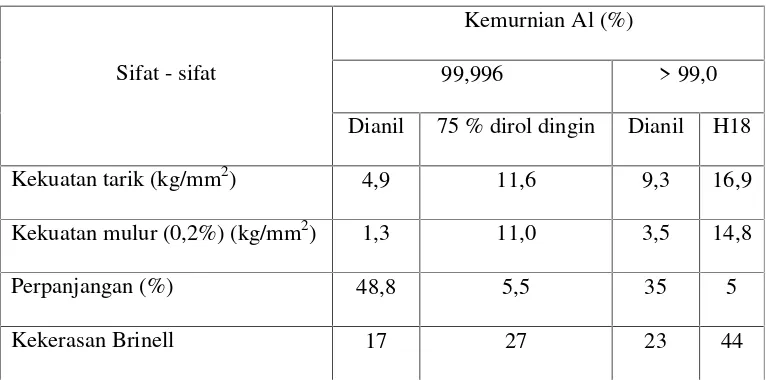
Tabel 2.2. Sifat – sifat mekanik Aluminium.
Kemurnian Al (%)
99,996 > 99,0
Sifat - sifat
Dianil 75 % dirol dingin Dianil H18
Kekuatan tarik (kg/mm2) 4,9 11,6 9,3 16,9
Kekuatan mulur (0,2%) (kg/mm2) 1,3 11,0 3,5 14,8
Perpanjangan (%) 48,8 5,5 35 5
20
2.4.1. Sifat-sifat Aluminium
Aluminium merupakan logam non-ferous yang banyak digunakan karena memiliki sifat-sifat :
1. Kerapatan (density)
Aluminium mempunyai berat jenis rendah yaitu sebesar 2700 kg/m3 (bandingan terhadap baja yang mempunyai kerapatan 7770 kg/m3)
2. Tahan terhadap korosi
Untuk logam non-ferous dapat dikatakan bahwa makin besar kerapatannya maka makin baik daya tahan korosinya, tetapi Aluminium merupakan pengecualian. Walaupun Aluminium mempunyai daya senyawa tinggi terhadap oksigen (O2) atau
logam aktif dan oleh sebab itu dikatakan bahwa Aluminium sangat mudah sekali teroksidasi (korosi), tetapi dalam kenyataan Aluminium mempunyai daya tahan yang baik terhadap korosi. Hal ini disebabkan oleh lapisan/selaput tipis oksida transparan diseluruh permukaannya. Selaput ini mengendalikan laju korosi dan melindungi lapisan di bawahnya dari serangan atmosfir berikutnya.
3. Sifat mekanis
4. Penghantar arus listrik yang baik
Disamping mempunyai daya tahan yang baik terhadap korosi, Aluminium memiliki daya hantar panas dan listrik yang tinggi. Daya hantar listrik Aluminium murni sekitar 60% dari daya hantar listrik Tembaga.
5. Tidak beracun
Aluminium dapat digunakan sebagai bahan pembungkus atau kaleng makanan dan minuman. Hal ini disebabkan karena reaksi kimia antara makanan dan minuman tersebut dengan Aluminium tidak menghasilkan zat beracun yang dapat membahayakan manusia
6. Sifat mampu bentuk (formability)
Aluminium dapat dibentuk dengan mudah. Aluminium mempunyai sifat mudah ditempa (malleability) yang memungkinkannya dibuat dalam bentuk plat/ lembaran tipis. 7. Titik lebur rendah (melting point)
Titik lebur Aluminium relative rendah (660 oC) sehingga sangat baik untuk proses penuangan dengan waktu peleburan relatif singkat dan biaya operasi akan lebih murah.
22
2.4.2. Pengaruh unsur-unsur logam pada paduan Aluminium
antara lain :
1. Si
Keuntungannya :
- Mempermudah didalam pengecoran. - Meningkatkan daya tahan terhadap korosi. - Memperbaiki sifat-sifat atau karakteristik coran. - Menurunkan penyusutan hasil coran.
Kerugiannya :
- Penurunan kekuatan terhadap beban kejut.
- Hasil coran akan rapuh jika kandungan Si terlalu tinggi. 2. Cu
Keuntungan :
- Meningkatkan kekerasan. - Memperbaiki kekuatan tarik.
- Mempermudah pengerjaan dengan mesin. Kerugian :
- Menurunkan ketahanan bahan terhadap korosi. - Mengurangi keuletan bahan.
- Menurunkan mampu bentuk dan mampu rol. 3. Mn
Keuntungan :
- Meningkatkan daya tahan terhadap korosi. - Mengurangi pengaruh buruk unsur Fe. Kerugian :
- Menurunkan kemampuan penuangan. - Kekerasan butiran partikel meningkat. 4. Mg
Keuntungan :
- Mempermudah di dalam penuangan.
- Meningkatkan kemampuan pengerjaan mesin. - Meningkatkan daya tahan terhadap korosi. - Meningkatkan kekuatan mekanis.
- Menghaluskan butiran kristal secara efektif.
- Meningkatkan ketahanan terhadap beban kejut/impack. Kerugian :
- meningkatkan kemungkinan timbulnya cacat pada hasil coran. 5. Ni
Keuntungan :
- Meningkatkan kekuatan dan ketahanan bahan pada temperatur tinggi.
- Meningkatkan daya tahan terhadap korosi. - Menurunkan pengaruh buruk Fe dalam coran. 6. Zn
24
- Meningkatkan sifat mampu cor. - Meningkatkan sifat mampu mesin. - Mempermudah pembentukan. - Meningkatkan keuletan bahan.
- Meningkatkan kekuatan terhadap beban kejut/impack. Kerugian :
- Menurunkan ketahanan korosi.
- Menurunkan pengaruh baik pada unsur besi.
- Bila kadar Zn terlalu tinggi dapat menyebabkan cacat rongga udara.
2.5. Larutan Kimia
Dalam hal ini larutan kimia yang digunakan dalam penelitian ini adalah larutan NaOH.
2.5.1. Konsentrasi Larutan
Konsenterasi dinyatakan dalam satuan fisika
Bila kita menggunakan satuan fisika, konsetrasi larutan dapat dinyatakan dengan salah satu dari cara-cara berikut : 1) Dengan massa zat terlarut per satuan volume larutan
(umpamanya, 20 gram KCl per liter larutan)
2) Dengan persen komposisi, atau jumlah satuan massa telarut per 100 satuan massa larutan.
Contoh : larutan 10% dalam air mengandung 10 g NaCl dalam 100 g larutan. 10 g NaCl dilarutakan dalam 90 g air untuk mendapatkan 100 g larutan.
3) Dengan volume zat telarut per satuan volume larutan. Konsentrasi dinyatakan dalam satuan kimia
1) Konsentrasi molar (molar concentration), M ialah jumlah mol zat terlarut yang terkandung di dalam satu liter larutan. M merupakan lambang kuantitas, yaitu konsentrasi molar, dan M lambang satuan, mol/L.
larutan volume molar
i konsentras
M molzatterlarut
26
larutan volume larutan
normalitas
N gramekuivalenzatterlarut
3) Molalitas suatu larutan ialah banyaknya mol zat terlarut per kilogram pelarut yang terkandung dalam suatu larutan. Molalitas (m) tidak dapat dihitung dari konsentrasi molar (M), kecuali jika rapatan (densitas) larutan ini diketahui.
larutan volume ) ( molar i konsentras
m n zatterlarut
4) Fraksi mol (mole fraction), x, suatu komponen dalam larutan didefinisikan sebagai banyaknya mol (n) komponen itu, dibagi dengan jumlah mol keseluruhan komponen dalam larutan itu. Jumlah fraksi mol seluruh komponen dalam setiap larutan adalah satu. Dalam larutan dua komponen,
) ( ) ( ) n(terlarut (terlarut) x pelarut n terlarut n ) ( ) ( n(pelarut) (pelarut) x pelarut n terlarut n komponen saluran mol an bersangkut yang komponen mol komponen mol fraksi
x
2.5.2. Sifat-sifat Larutan
Svante A. Arrhenius mengemukakan teori yang disebut teori asam-basa. Menurutnya :
1. Asam
Asam adalah zat yang menaikkan kosentrasi ion H+ di dalam larutan.
Contoh :
HCl yang terionisasi menjadi H+ + Cl - H2SO4 yang terionisasi menjadi 2H+ + SO42-
Asam dapat terjadi bila oksida nonlogam direaksikan dengan air :
Oksida nonlogam + Air Asam Contoh :
CO2(g) + H2 O(l) H2CO3 (aq)
Karbon dioksida asam karbonat
N2O5(g) + H2O(l) 2HNO3(aq)
Nitrogen oksida asam nitrat
Ciri-ciri larutan asam : - Rasa masam
- Bersifat korosif dan melarutkan beberapa logam
- Semua larutan asam dapat menghasilkan ion hidrogen (H+) - Larutannya bersifat elektrolit
28
Tabel 2.3. contoh beberapa asam
Nama Rumus Bentuk ionisasinya Sifat elektrolitnya
Asam Bromida Asam Nitrat Asam Sulfat Asam Fosfat Asam Sulfida
Asam Asetat
HBr HNO3
H2SO4
H3PO4
H2S
CH3COOH
H+ + Br - H+ + NO3 -
H+ + SO4 2-
H+ + PO43-
H+ + S 2- H+ + CH3 COO -
Kuat Kuat Kuat Lemah Lemah Lemah
2. Basa
Basa adalah zat yang menaikkan konsentrasi ion OH- di dalam larutan.
Contoh :
NaOH yang terionisasi menjadi Na+ + OH - Ca(OH)2 yang terionisasi menjadi Ca2+ + 2OH-
Basa dapat terjadi bila oksida logam direaksikan dengan air : Oksida logam + Air Basa
Contoh :
Na2O + H2 O NaOH
Natrium oksida natrium hidroksida CaO + H2 O Ca(OH)2
Ciri-ciri larutan basa :
- Rasanya pahit dan dapat merusak kulit
- Terasa licin di tangan (seperti merasakan larutan sabun) - Di dalam larutan membentuk ion logam atau gugus
(kumpulan atom) lain yang bermuatan positif dan ion hidroksil (OH) yang bermuatan negatif.
- Larutannya bersifat elektrolit - Membirukan kertas lakmus merah
Tabel 2.4. contoh beberapa basa
Nama Rumus Bentuk ionisasinya Sifat elektrolitnya
Natrium Hidroksida Kalsium Hidroksida Amonium Hidroksida
NaOH Ca(OH)2
NH4OH
Na+ + OH - Ca 2+ + 2OH - NH4+ + OH -
BAB III
METODE PENELITIAN
Pada bab ini dimbahas tentang metode yang digunakan dalam penelitian, bahan yang digunakan adalah pelat alumunium dan pelarut kimia yaitu NaOH teknis dengan variasi kadar 20% (pH = 13-14).
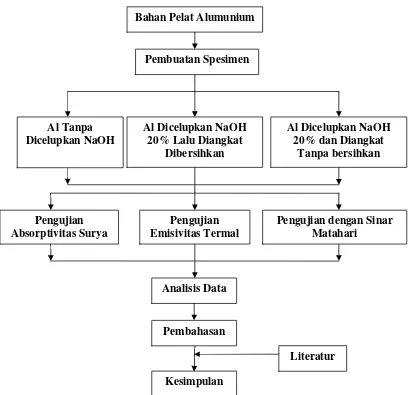
3.1. Skema Penelitian
Gambar 3.1. Diagram Alur Penelitian
Bahan Pelat Alumunium
Pembuatan Spesimen
Al Tanpa Dicelupkan NaOH
Al Dicelupkan NaOH 20% Lalu Diangkat
Dibersihkan
Al Dicelupkan NaOH 20% dan Diangkat
Tanpa bersihkan
Kesimpulan
Literatur Pengujian
Absorptivitas Surya
Pengujian Emisivitas Termal
Analisis Data
Pembahasan
3.2. Cara Penelitian
Berikut di bawah ini langkah yang dibutuhkan dalam penelitian : 1. Literatur
Mencari dan mempelajari literatur yang berhubungan dengan penelitian ini.
2. Konsultasi
Melakukan wawancara dengan pihak-pihak yang terkait dengan pengetahuan tentang penulisan ini, misalnya dosen, mahasiswa yang memiliki pengetahuan dibidang ini.
3. Pembuatan spesimen
Dalam penelitian ini spesimen dibuat di laboratorium Ilmu Teknologi Mekanik, jurusan Teknik Mesin, Universitas Sanata Dharma Yogyakarta.
4. Pengujian spesimen
Pengujian spesimen yang dilakukan adalah pengujian absorptivitas termal dan emisivitas termal, yang dilakukan di laboratorium Perpindahan Panas, jurusan Teknik Mesin, Universitas Sanata Dharma Yogyakarta.
5. Analisis data
32
3.3. Proses Pembuatan Benda Uji
Benda uji yang akan diuji, harus dipersiapkan terlebih dahulu. Persiapannya sebagai berikut : sebelum permukaan pelat dicelupkan larutan NaOH pelat diukur dan dipotong sesuai dimensi yang diinginkan, untuk pengujian langsung dengan sinar matahari pelat dipotong dengan ukuran : panjang 165mm, lebar 125 mm, tebal 2 mm, untuk pengujian absorptivitas dan emisivitas surya pelat dipotong dengan ukuran : panjang 50 mm, lebar 30 mm, dengan tebal yang sama 2 mm, seperti pada Gambar 3.2
Gambar 3.2. Bentuk Benda Uji
3.4. Proses Pencelupan dalam Larutan NaOH
1. Spesimen yang telah dibentuk sesuai dengan ukuran dibersihkan dari berbagai macam kotoran sisa yang menempel pada spesimen saat proses pembuatan.
2. Gelas kaca disiapkan untuk menempatkan larutan NaOH teknis. 3. NaOH ditimbang sesuai dengan variasi-variasi yang diinginkan. 4. Lalu NaOH yang telah ditimbang tersebut dilarutkan pada air dengan
volume tertentu untuk mendapatkan konsenterasi atau kepekatan yang diinginkan yang dinyatakan dalam satuan fisika.
5. Selanjutnya spesimen dimasukan ke dalam gelas kaca yang berisi larutan NaOH dalam jangka waktu tertentu.
6. Setelah spesimen direndam dalam larutan NaOH dalam waktu yang diinginkan lalu diangkat dan dibiarkan kering, ada dua cara pengeringan yaitu :
Dengan cara dibiarkan kering alami berlahan-lahan
Dengan cara dilap
3.5. Larutan
Pencelupan pada larutan NaOH teknis untuk tiap variasi permukaan :
1. Variasi A, Pencelupan dengan kadar NaOH 20% (pH =13-14) dengan pengeringan alami :
Diket : air : 80 g NaOH : 20 g
34
A2 waktu pencelupan = 10 detik
A3 waktu pencelupan = 15 detik
2. Variasi B, Pencelupan dengan kadar NaOH 20% (pH =13-14) pengeringan dengan lap :
Diket : air : 80 g NaOH : 20 g
B1 waktu pencelupan = 5 detik
B2 waktu pencelupan = 10 detik
B3 waktu pencelupan = 15 detik
3.6. Pengujian Bahan
Pengujian ini meliputi pengujian absorptivitas surya dan pengujian emisivitas termal serta pengujian dengan sinar matahari.
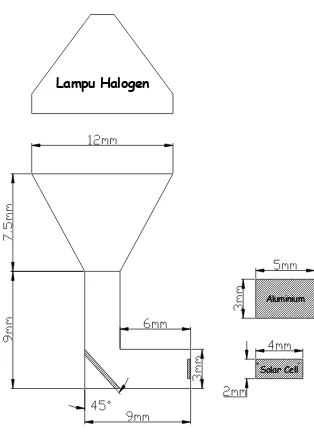
3.6.1. Pengujian Absorptivitas Surya
meter yang dinyatakan dalam tegangan (Volt) pada skala 20 Volt DC.
Lampu Halogen
Solar Cell Aluminium
Gambar 3.3. Alat Penguji Absorptivitas
36
+ = 1 Di mana :
= absorptivitas surya pada suatu panjang gelombang tertentu.
= reflektivitas surya pada suatu panjang gelombang tertentu. Tujuan pengujian absorptivitas surya:
1. Untuk mengetahui kemampuan suatu bahan dalam menyerap panas. 2. Untuk menentukan proses pembuatan permukaan.
3.6.2. Pengujian Emisivitas Termal
Pada pengujian emisiviatas termal ini digunakan alat penguji radiasi termal.
Langkah penelitian
a. Mempersiapkan benda uji
Gambar 3.4. Pemasangan Spesimen b. Pelaksanaan penelitian
Pelaksanaan penelitian dilakukan di Laboratorium Perpindahan Panas Universitas Sanata Dharma. Dengan menggunakan alat penguji radiasi termal kita dapat meneliti kemampuan radiasi suatu bahan bila diberi panas. Selanjutnya setelah benda uji terpasang dengan benar, begitu juga dengan
thermocouple dan radiometer, maka kita hidupkan source
(sumber panas) dengan memasang daya pada skala 4,5 strip. Pemasangan benda uji berjarak 50 mm dari source dan 60 mm dari radiometer dengan posisi seperti pada Gambar 3.4. Semua pengambilan data berdasarkan sebuah data dengan kondisi awal sebagai berikut:
38
TS2 = suhu akhir permukaan alumunium ( ° C )
TA = suhu sekitar ( ° C )
= 27 °C R0 = radiasi awal
= 2
R1 = radiasi akhir
t = waktu pemberian panas (menit) = 5 menit
Alat untuk membaca data suhu dan radiasi bisa dilihat Gambar 3.5 di bawah ini.
Setelah diketahui nilai radiasi akhir ( R1 ) dan suhu akhir ( TS ),
maka dapat diketahui nilai emisivitas termalnya dengan persamaan berikut:
4
A 4
S T
T
ó å
q
di mana :
q : energi yang dipancarkan (W/m2) : 5,59 × R1
: emisivitas termal
: konstanta Stefan boltzmann = 5,67 x 10-8 W/(m2.K4) TS : temperatur akhir permukaan ( K )
TA : temperatur sekitar ( K )
c. Tujuan pengujian emisivitas termal:
1. Untuk mengetahui besar panas yang dilepas oleh suatu bahan. 2. Untuk mengetahui cara mengurangi pelepasan panas suatu
bahan.
3.6.3. Pengujian dengan Sinar Matahari
Pengujian ini dilakukan dengan menggunakan sinar matahari langsung untuk mencari besarnya suhu yang dapat dicapai oleh plat dari panas sinar matahari tersebut.
Langkah penelitian
40
Bahan uji dimasukan dalam kotak yang terbuat dari kaca transparan yang berfungsi untuk menjaga suhu di dalamnya tetap stabil dapat dilihat pada Gambar 3.6.
Gambar 3.6. Pemasangan Spesimen
b. Pelaksanaan penelitian
Pelaksanaan penelitian dilakukan di tempat terbuka dan dijemur di bawah sinar matahari langsung antara pukul 12.00-13.00 WIB untuk memperoleh panas matahari yang maksimal. Dengan menggunakan alat penguji thermocouple dapat diperoleh besarnya suhu pada waktu yang sama untuk masing-masing benda uji. c. Tujuan pengujian langsung dengan sinar matahari
1. Untuk mengetahui besarnya suhu yang dicapai.
BAB IV
DATA PENELITIAN DAN PEMBAHASAN
4.1. Analisis Pengujian Absorptivitas
Pengujian absorptivitas ini bertujuan untuk mengetahui kemampuan setiap spesimen menyerap energi panas setelah dicelupkan dalam larutan NaOH dengan kadar 20 %.
Tabel 4.1. Data Hasil Pengujian Absorptivitas Surya Material Awal
Tabel 4.2. Data Hasil Pengujian Absorptivitas Surya Pengeringan Alami
S p es im en Varisasi waktu celup (detik) Tegangan Solar Cell Pantulan
dari Al (volt)
Tegangan Solar Cell Tanpa Pantulan (volt) Reflektivitas Al (ñAl)
Absorptivitas Al (áAl)
Rata-rata Absorptivitas
A1a 1.68 2.66 0.631579 0.368421
A1b 1.76 2.66 0.661654 0.338346
A1c
5
1.83 2.66 0.68797 0.312030
0.339599
A2a 1.83 2.66 0.68797 0.31203
A2b 1.83 2.66 0.68797 0.31203
A2c
10
1.88 2.66 0.706767 0.293233
0.305764
A3a 1.8 2.66 0.676692 0.323308
A3b 1.77 2.66 0.665414 0.334586
A3c
15
1.74 2.66 0.654135 0.345865
0.334586 No Material
Awal
Spesimen Tegangan Solar Cell Pantulan dari
Al (volt)
Tegangan Solar Cell Tanpa Pantulan (volt) Reflektivitas Al( ñAl )
Absorptivitas Al (áAl)
Rata-rata Absorptivitas
1 2.58 2.66 0.969925 0.030075 2
2.56 2.66 0.962406 0.037594
1 Al
3 2.56 2.66 0.962406 0.037594
42
Tabel 4.3. Data Hasil Pengujian Absorptivitas Surya Pengeringan Dengan Dilab
Dengan menambah waktu pencelupan tidak berpengaruh secara signifikan pada hasil pengujian absorptivitas. Di sini tidak dapat disimpulkan bahwa semakin lama waktu pencelupan semakin besar nilai absoptivitasnya atau sebaliknya. Hal itu kemungkinan disebabkan oleh beberapa faktor yang kurang sempurna antara lain :
- Proses pencelupan - Proses pengeringan - Pembacaan multi meter
Walaupun demikian hasil pengujian secara keseluruhan dapat mencapai angka absorptivitas yang diharapkan lebih besar dari permukaan aluminium awal/tidak diproses. Dengan pengujian radiasi dapat diketahui besar angka reflektivitas, yang besarnya berbanding terbalik dengan besar absorptivitas. Untuk mencari besar absortivitas melalui perbandingan besar tegangan solar cell pantulan dari aluminium dengan besar tegangan
S p es im en Varisasi waktu celup
(detik)
Tegangan Solar Cell Pantulan dari
Al (volt)
Tegangan Solar Cell Tanpa Pantulan (volt) Reflektivitas Al (ñAl)
Absorptivitas Al (áAl)
Rata-rata Absorptivitas
B1a 2.25 2.66 0.845865 0.154135
B1b 2.26 2.66 0.849624 0.150376
B1c
5
2.2 2.66 0.827068 0.172932
0.159148
B2a 2.3 2.66 0.864662 0.135338
B2b 2.24 2.66 0.842105 0.157895
B2c
10
2.2 2.66 0.827068 0.172932
0.155388
B3a 2.11 2.66 0.793233 0.206767 B3b 2.26 2.66 0.849624 0.150376 B3c
15
2.17 2.66 0.815789 0.184211
langsung dari solar cell, dapat dicari menggunakan persamaan sebagai berikut:
áë + ñë= 1 ... ( 1 )
di mana,
áë : absorptivitas surya
ñë : reflektivtas surya
maka,
áë= 1 - ñë ... ( 2 )
= 1 -
Solarcell Tegangan Al Pantulan cell Solar Tegangan
Diagram Uji Absorptivitas
0.0376 0.0376 0.0301 0 0.005 0.01 0.015 0.02 0.025 0.03 0.035 0.04
1 2 3
Spesimen Awal A b s o rp ti v it a s
44 0.3396 0.3346 0.3058 0 0.05 0.1 0.15 0.2 0.25 0.3 0.35 0.4
5 10 15
Waktu Pencelupan (detik)
A b s o rp ti v it a s
Gambar 4.2. Diagram pengaruh waktu pencelupan pada absorptivitas (pengeringan alami) 0.1591 0.1554 0.1805 0 0.02 0.04 0.06 0.08 0.1 0.12 0.14 0.16 0.18 0.2
5 10 15
Waktu Pencelupan (detik)
A b s o rp s iv it a s
0.3396
0.3058
0.3346
0.1591 0.1554
0.1805
0.0351
0 0.05 0.1 0.15 0.2 0.25 0.3 0.35 0.4
A A1 A2 A3 B1 B2 B3
Spesimen
A
b
s
o
rp
ti
v
it
a
s
A = tanpa perlakuan, A1 = pencelupan 5 detik (pengeringan alami), A2 = pencelupan 10 detik (pengeringan alami), A2 = pencelupan 15 detik (pengeringan alami) B1 = pencelupan 5 detik (pengeringan dengan lap), B2 = pencelupan 10 detik (pengeringan dengan lap),
B3 = pencelupan 15 detik (pengeringan dengan lap)
Gambar 4.4. Diagram pengaruh pencelupan NaOH pada absorptivitas untuk seluruh spesimen
4.2. Analisis Pengujian Emisivitas
46
Tabel 4.4. Data Hasil Pengujian Emisivitas Thermal Material Awal.
Thermocouple 1
Thermocouple 2
Tabel 4.5. Data Hasil Pengujian Emisivitas Thermal Pengeringan Alami
Thermocouple 1
S
p
es
im
e Varisasi waktu
celup (detik)
Suhu Al (TS) (°C)
Suhu Sekitar
(TA) (°C)
Radiasi Thermal (R)
Energi yg Dipancarkan (q)
(W/m2)
Emisivitas Thermal
(
å
)Rata-rata Emisivitas
A1a 47 27 18 100.62 0.7438 A1b 49 27 21 117.39 0.7812 A1c
5
48 27 22 122.98 0.8616
0.795521
A2a 44 27 19 106.21 0.9375 A2b 50 27 22 122.98 0.7789 A2c
10
50 27 22 122.98 0.7789
0.831791
A3a 46 27 22 122.98 0.9617 A3b 55 27 22 122.98 0.6243 A3c
15
51 27 24 134.16 0.8103
0.798777 No Material
Awal
Spesimen Suhu Al (TS) (°C)
Suhu Sekitar (TA) (°C) Radiasi Thermal (R) Energi yg Dipancarkan
(q) (W/m2)
Emisivitas Thermal
(
å
)Rata-rata Emisivitas
1 39 27 4 22.36 0.2866 2 40 27 3 16.77 0.1975 1 Al
3 40 27 3 16.77 0.1975
0.227176
No Material Awal
Spesimen Suhu Al (TS) (°C)
Suhu Sekitar (TA) (°C) Radiasi Thermal (R) Energi yg Dipancarkan
(q) (W/m2)
Emisivitas Thermal
(
å
)Rata-rata Emisivitas
1 39.1 27 4 22.36 0.2841 2 42.1 27 3 16.77 0.1682 1 Al
3 42.2 27 3 16.77 0.1670
Thermocouple 2
S
p
es
im
e Varisasi waktu
celup (detik)
Suhu Al (TS) (°C)
Suhu Sekitar
(TA) (°C)
Radiasi Thermal
(R)
Energi yg Dipancarkan (q)
(W/m2)
Emisivitas Thermal
(
å
)Rata-rata Emisivitas
A1a 50.2 27 18 100.62 0.6312 A1b 48.7 27 21 117.39 0.7931 A1c
5
50.7 27 22 122.98 0.7533
0.725881
A2a 48.2 27 19 106.21 0.7363 A2b 49.6 27 22 122.98 0.7943 A2c
10
50.6 27 22 122.98 0.7569
0.762501
A3a 52.2 27 22 122.98 0.7033 A3b 57.7 27 22 122.98 0.5619 A3c
15
52.5 27 24 134.16 0.7571
0.674068
Tabel 4.6. Data Hasil Pengujian Emisivitas Thermal Pengeringan Dengan Dilap Thermocouple 1 S p es im
e Varisasi waktu celup (detik)
Suhu Al (TS) (°C)
Suhu Sekitar
(TA) (°C)
Radiasi Thermal
(R)
Energi yg Dipancarkan (q)
(W/m2)
Emisivitas Thermal
(
å
)Rata-rata Emisivitas
B1a 38 27 9 50.31 0.7070
B1b 43 27 8 44.72 0.4215
B1c
5
45 27 13 72.67 0.6028 0.577123 B2a 45 27 9 50.31 0.4173
B2b 47 27 13 72.67 0.5372
B2c
10
46 27 8 44.72 0.3497 0.434757 B3a 48 27 15 83.85 0.5874
B3b 46 27 8 44.72 0.3497
B3c
15
48 Thermocouple 2 S p es im
e Varisasi waktu celup (detik)
Suhu Al (TS) (°C)
Suhu Sekitar
(TA) (°C)
Radiasi Thermal
(R)
Energi yg Dipancarkan (q)
(W/m2)
Emisivitas Thermal
(
å
)Rata-rata Emisivitas
B1a 40.2 27 9 50.31 0.5828
B1b 47.0 27 8 44.72 0.3306
B1c
5
45.7 27 13 72.67 0.5783 0.497217 B2a 45.0 27 9 50.31 0.4173
B2b 47.9 27 13 72.67 0.5118
B2c
10
44.0 27 8 44.72 0.3947 0.441296 B3a 51.9 27 15 83.85 0.4860
B3b 47.6 27 8 44.72 0.3200
B3c
15
49.4 27 12 67.08 0.4375 0.414517
Dalam pengujian ini lamanya waktu pencelupan juga tidak dapat menentukan besar kecilnya nilai emisivitas benda uji, ini disebabkan beberapa factor yang hampir sama pada pengujian absorptivitas. Hal ini bisa juga terjadi jika kurangnya pendinginan alat pemanas, yang mengakibatkan kondisi awal yang berbeda pada saat pengukuran suhu dan radiasinya.
Dengan mengetahui suhu aluminium, suhu sekitar dan radiasi dapat diketahui emisivitas thermal menggunakan persamaan sebagai berikut:
4
A 4 S T T ó å
q ... ( 3 ) dimana :
q : energi yang dipancarkan (W/m2) : 5,59 × R
å : emisivitas thermal
: konstanta Stefan boltzmann = 5,67 x 10-8 W/(m2.K4) TS : temperatur akhir permukaan ( K )
Diagram Uji Emisivitas 0.2866 0.1975 0.1975 0.1670 0.1682 0.2841 0 0.05 0.1 0.15 0.2 0.25 0.3 0.35
1 2 3
Specimen E m is iv it a s Thermocouple1 Thermocouple 2
Gambar 4.5. Diagram emisivitas tanpa pencelupan
0.8318 0.7988 0.7955 0.7259 0.7625 0.6741 0 0.1 0.2 0.3 0.4 0.5 0.6 0.7 0.8 0.9
5 10 15
Waktu Pencelupan (detik)
E m is iv it a s Thermocouple 1 Thermocouple 2
50 0.4612 0.5771 0.4348 0.4145 0.4972 0.4413 0 0.1 0.2 0.3 0.4 0.5 0.6 0.7
5 10 15
Waktu Pencelupan (detik)
E m is iv it a s Thermocouple 1 Thermocouple 2
Gambar 4.7. Diagram pengaruh waktu pencelupan pada emisivitas (pengeringan dengan dilap)
0.2272
0.7955 0.8318 0.7988
0.5771 0.4612 0.4348 0.2065 0.7259 0.7625 0.6741 0.4145 0.4413 0.4972 0 0.1 0.2 0.3 0.4 0.5 0.6 0.7 0.8 0.9
A A1 A2 A3 B1 B2 B3
Spesimen E m is iv it a s Thermocouple1 Thermocouple2
A = tanpa perlakuan, A1 = pencelupan 5 detik (pengeringan alami), A2 = pencelupan 10 detik (pengeringan alami), A2 = pencelupan 15 detik (pengeringan alami) B1 = pencelupan 5 detik (pengeringan dengan lap), B2 = pencelupan 10 detik (pengeringan dengan lap),
B3 = pencelupan 15 detik (pengeringan dengan lap)
4.3. Analisis Pengujian dengan Sinar Matahari
Pengambilan data pada pengujian langsung dengan sinar matahari ini bertujuan untuk mengetahui seberapa besarnya suatu bahan menerima panas matahari setelah merusak permukaan suatu bahan Aluminium dengan mencelupkan ke dalan larutan NaOH. Data-data yang diambil dalam penelitian ini adalah besarnya suhu pada setiap benda uji.
Tabel 4.7. Data Hasil Pengujian dengan Sinar Matahari Suhu Al
Pengeringan Alami (ºC)
Suhu Al
Pengeringan Dengan Lap (ºC)
Waktu Penjemuran
(menit)
Suhu Al Tanpa Perlakuan
(ºC) 5 detik 10 detik 15 detik 5 detik 10 detik 15 detik
0 28.9 28.5 28.5 28.7 28.5 28.9 28.6
5 41.8 44.3 48.1 49.7 51.2 46.7 47.2
10 49.1 53.6 55.7 55.3 58.8 57.6 58.2
15 54.8 59.2 60.1 60.3 63.7 61.5 62.8
20 59.2 62.9 64.1 64.2 68.1 64.4 67.6
25 61.8 65 67.4 66.6 70.2 67.9 69.9
Rata-rata 49.27 52.25 53.98 54.13 56.75 54.50 55.72
ÄT 32.9 36.5 38.9 37.9 41.7 39 41.3
52 0 10 20 30 40 50 60 70 80
0 5 10 15 20 25
Waktu Pemanasan (menit)
S u h u ( ºC )
tanpa perlakuan pencelupan 5 detik (pengeringan alami) pencelupan 10 detik (pengeringan alami) pencelupan 15 detik (pengeringan alami) pencelupan 5 detik (pengeringan dengan lap) pencelupan 10 detik (pengeringan dengan lap) pencelupan 15 detik (pengeringan dengan lap)
Gambar 4.9. Diagram pemanasan dengan sinar matahari terhadap waktu
0 10 20 30 40 50 60 70 80
0 5 10 15 20 25
Waktu Pemanasan (menit)
S u h u ( ºC )
Tanpa Perlakuan Pengeringan Alami (pencelupan 5 detik) Pengeringan Alami (pencelupan 10 detik) Pengeringan Alami (pencelupan 15 detik) Pengeringan Dengan Lap (pencelupan 5 detik) Pengeringan Dengan Lap (pencelupan 10 detik) Pengeringan Dengan Lap (pencelupan 15 detik)
Gambar 4.11. Foto Permukaan Aluminium Pengeringan Alami
Al mula-mula Variasi waktu 5 detik
Variasi waktu 10 detik Variasi waktu 15 detik
Gambar 4.12. Foto Permukaan Aluminium Pengeringan Dengan Dilap
54
BAB V
KESIMPULAN DAN PENUTUP
5.1. Kesimpulan
Dari hasil penelitian, pengujian dan analisis di laboratorium Perpindahan Panas dan laboratorium Teknologi Mekanik jurusan Teknik Mesin Fakultas Teknik Universitas Sanata Dharma, maka dapat disimpulkan:
1. Dari pengujian absorptivitas dan emisivitas, disimpulkan dengan metode
dipping in chemical baths (permukaan dikasarkan dengan direndam
dalam larutan kimia NaOH) dapat meningkatkan absorptivitas 5 – 10 kali lipat, emisivitas juga meningkat 2 – 3 kali lipat serta kenaikan suhu yang dicapai benda uji meningkat antara 2 ºC - 10 ºC.
2. Dalam pengujian ini metode pencelupan yang menghasilkan absorptivitas termal yang tinggi adalah pencelupan dalam larutan NaOH 20% dengan pengeringan alami.
3. Pada pengujian ini absorptivitas tertinggi sebesar 0,3684 terjadi pada variasi A1a dengan waktu pencelupan 5 detik dan pengeringan secara
alami sedangkan pada pengujian emisivitas mengalami peningkatan tertinggi sebesar 0.9375 pada variasi A2a dengan pencelupan 10 detik dan
pengeringan secara alami. Untuk pengujian dengan sinar matahari suhu tertinggi 70.2 ºC yang dicapai pada benda uji dengan waktu pencelupan
56
maka koefisien kerugian membesar, sehingga efisiensi akan berkurang. Idealnya pelat absorber memiliki faktor absorptivitas surya yang besar dan emisivitas termal yang rendah. Penggunaan variasi waktu pencelupan tidak memberikan hasil permukaan yang pasti atau tidak dapat menentukan absorptivitas dan emisivitas akan naik atau turun. Hal yang sama juga terjadi pada penyerapan kalor saat pengujian dengan sinar matahari, suhu yang diserap tidak dapat dipastikan akan lebih besar atau kecil jika dibandingkan antara satu spesimen dengan spesimen lain.
5.2. Penutup
Akhir kata penulis mengucapkan terima kasih kepada semua pihak yang telah banyak membantu selama proses penyusunan Tugas Akhir ini. Bila terjadi ketidak akuratan data, disebabkan keterbatasan dana, peralatan dan ketilitian dalam pengamatan. Kritik dan saran untuk kemajuan sangat penulis harapkan, sehingga ini dapat berguna bagi semua pihak.
5.3. Saran
Sebagai acuan penelitian berikutnya perlu diperhatikan hal-hal berikut : - Gunakan variasi waktu yamg lebih lama dengan kadar larutan yang kecil
untuk mengurangi pencemaran lingkungan.
- Gunakan aquadest sebagai pelarut untuk mendapatkan larutan yang lebih akurat.
Daftar Pustaka
Choudhuryn, G. M. 2002. Selective Surface for Efficient Solar Thermal
Conversion. Bangladesh Reneweble Energy News Letter. Vol. 1 No 2, Vols
1 & 2, July 2000-December 2002. Commottee for Promotion and Dissemination of Renewable Energy in Bangladesh. Banglades.
Gelin, K. 2004. Preparation and Characterization of Sputter Deposited Spectrally
Selective Solar Absorber. Comprehensive Summaries of Uppsala
Dissertations from the Faculty of Science and Technology. Uppsala University.
Holman, J. P. 1993. Perpindahan Kalor. Erlangga. Jakarta.
Jansen, T. J. Teknologi Rekayasa Surya. Pradnya Paramita. Jakarta. Rosenberg, J. L. 1996. Kimia Dasar. Erlangga. Jakarta.