LAPORAN PRAKTIKUM ANALISIS PANGAN ANALISIS PENENTUAN KADAR KAROTENOID
KELOMPOK 1 :
Intan Azizah Hs 1411105001
Anisa Intan Azizah 15110
Graciella Tio Dominika 1610511001
Ni Made Susi Kartika 1610511002
Karlina Ayu Putri Dhahana 1610511003
Bobby Frans Siahaan 1610511004
Laorent Maria Oktavia 1610511005
PROGRAM STUDI ILMU DAN TEKNOLOGI PANGAN FAKULTAS TEKNOLOGI PERTANIAN
BAB I PENDAHULUAN 1.1 Latar Belakang
Seiring dengan berkembangnya ilmu dan teknolgi pengetahuan menyebabkan berbagai jenis pangan mengandung manfaat baik bagi tubuh. Berbagai jenis pangan tersebut disebut sebagai pangan fungsional yang mengandung komponen atau senyawa ternetu yang dapat memberikan manfaat bagi kesehatan tubuh. Salah satu komponen tersebut adalah antioksidan.
Antioksidan merupakan komponen bioaktif yang dapat menunda,mencegah,memperlambat kerusakan oksidatif senyawa lain dalam tubuh, sehingga memiliki efek pelindung bagi senyawa lain tersebut (Kim dkk.,2005)
Salah satu produk pangan yang terkenal banyak mengandung antioksidan adalah teh. Daun teh segar sebagai bahan baku dari semua jenis teh memiliki beberapa kandungan komponen kimia. Menurut Nasution dan Tjiptadi (1975) membaginya menjadi 7golongan, antara lain: bahan-bahan anorganik, yaitu Al, Mn, P, Ca, Mg, Fe, Se, Cu,dan K, senyawa bernitrogen, yaitu, protein, asam amino, alkaloid, dan kafein, 3)karbohidrat, yaitu gula, pati, dan pektin, polifenol, dan turunannya, yaitu asam galat,katekin, tanin, tehaflavin, teharubigin, pigmen, yaitu klorofil, anthosianin, dan flavon, enzim, yaitu polifenol oksidase, peroksidase, pektinase, dan vitamin C dan vitamin E. Perbedaan proses pengolahan yang diaplikasikan untuk mengubah daun teh segar menjadi teh hijau, teh hitam.
BAB II
TUJUAN DAN MANFAAT
2.1 Tujuan
Tujuan dari dilaksanakannya paktikum ini adalah :
1. Untuk mengetahui kandungan antikosidan dan kadar total fenol pada sampel teh hijau dan teh hitam
2. Untuk mengetahui metode analisis kandungan antioksidan dan kadar total fenol pada sampel teh hijau dan teh hitam
2.2Manfaat
Manfaat dari dilaksanakanya praktikum ini adalah :
1. Mahasiswa dapat mengetahui kandungan antioksidan dankadar total fenol pada sampel teh hijau dan teh hitam
2. Mahasiswa dapat mengtehaui metode analisis kandungan antioksidan dan kadar total fenol pada sampel teh hijau dan teh hitam
BAB III
TINJAUAN PUSTAKA 3.1 Antioksidan
atau lebih komponen pangan. Antioksidan alami, seperti yang terdapat pada teh,dapat menghambat terjadinya reaksi oksidasi dalam minyak jagung, minyak kacang, dan minyak ikan yang sangat rentan terhadap reaksi oksidasi karena mengandung asam lemak tidak jenuh yang tinggi.Senyawa fenol tersubstitusi telah banyak digunakan sebagai antioksidan).Kerja antioksidan dalam reaksi oksidasi adalah menghambat terbentuknya radikalbebas pada tahap inisiasi atau menghambat kelanjutan reaksi berantai pada tahap propagasidari reaksi autooksidasi. Antioksidan yang baik adalah senyawa yang mampu membuatradikal fenol dari antioksidan menjadi lebih stabil. Senyawa turunan fenol tersubtitusi inibanyak terdapat pada berbagai tumbuhan tropis berupa senyawa turunan polifenol (Nelsonet dkk., 2003).
3.2 Kandungan Teh Hijau
Kandungan teh hijau yang paling utama adalah polifenol katekin yang merupakan senyawa flavonoid yang terdiri dari epicarechin (EC),epicatehin galat (ECG) , epigallocatechin galat EGCG. Merupakan yang terbanyak yaitu 50-80 % dari jumlah total katekin. Selain itu teh hijau juga mengandung kafein, vitamin K, flavonl,alkalid,spaonin,protein,asam nukleat,mineral dan fluroide ( Dewi,2008)
3.3 Kandungan Teh Hitam
Teh hitam merupakan jenis teh yang paling banyak dikonsumsi didunia. Pada teh hitam selain mengandung katekin juga mengandung theaflavin dan thearubigin sebagai hasil dari porses oksidasi enzimatik. Katekin merupakan pemburu ROS (recative oxygen species) yang efektif dan berfungsi sebagai antioksidan. Theaflavin yang terkandung dalam teh hitam berpotensi memproduksi NO dan vasorelaksasi yang lebih tinggi dari EGCG yang terdapat pada katekin. Thearubigin merupakan stimulaotr vasodilatasi dan produksi NO yang sangat efisien (Maria 2009)
3.2 Asam galat
(penangkal radikal bebas). Asam galat adalah subunit dari galotanin, yaitu polimer heterogen yang mengandung berbagai molekul asam galat yang saling terkait dengan asam galat lain serta dengan sukrosa dan gula lainnya.[1] Banyak galotanin yang menghambat pertumbuhan
tanaman karena dapat merombak enzim sitoplasma dengan cara mendenaturasi protein (enzim adalah protein), dan ketahanan tumbuhan yang mengandungnya kemungkinan disebabkan karena galatonin diangkut ke vakuola sehingga terpisah dari enzim di sitoplasma. (Salisbury dan Ross. 1995).
BAB IV METODELOGI 4.1 Alat dan Bahan
Peralatan yang digunakan pada praktikum kali ini sebagai berikut : 1. Tabung reaksi
2. Pipet mikro 3. Labu takar
6. Pipet volume 7. Gelas beaker 8. Vortex 9. Bola hisap
Bahan yang digunakana pada pratikum kali ini sebagai berikut : 1. Reagen Folin
2. Asam galat
3. Sodium karbonat 7,5% 4. Aquades
4.2 Prosedur Kerja
Berikut adalah prosedur kerja dalam pembuatan larutan standar fenol : 1. Ditimbang 0,5 g asam galat
2. Diencerkan dengan aquades sampai tanda tera
3. Dipipet 2,5 ml reagen folin ke masing-masing perlakuan 20 ppm, 40 ppm, 60 ppm,80 ppm,dan 100 ppm kedalam labu takar
4. Diinkubasi pada suhu ruang selama 2 menit
5. Ditambahakan sodium karbonat 7,5% sebanayak ± 2ml
6. Dipanaskan pada waterbath selama 15 menit dengan suhu 50oC 7. Didinginkan
8. Standar dibaca pada spektrometri λ 760 nm
Gambar 1. Diagaram alir pembuatan Larutan standar folin BAB V
HASIL DAN PEMBAHASAN 5.1 Hasil
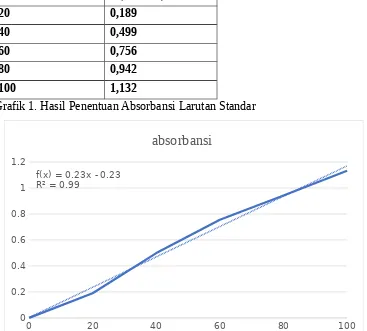
5.1.1 Hasil Penentuan Larutan Standar Tabel 1. Hasil Penentuan Larutan Standar
Konsentrasi absorbansi
Grafik 1. Hasil Penentuan Absorbansi Larutan Standar
0 20 40 60 80 100
5.1.2 Hasil Analisi Kadar Total Fenol
Tabel 2. Hasil Analisi Total Fenol pada sampel Teh hijau dan Teh Hitam Kelompok Sampel Total fenol
2. Teh hijau 3,33 %
3. Teh hijau 3,56 %
4. Teh hitam 1,79 %
5. Teh hitam 2,57%
5.2 Pembahasan
Penentuan konsentrasi fenol dari suatu bahan pangan dilakukan dengan menggunakan metode follincioucalteu. Yang mana pada metode ini digunakan reagen folinciocalteu untuk dapat menghitung kadar total fenolnya. Pada penentuan kadar phenol perlu dibuat suatu kurva standar yang meggunakan standar asam galat. Dari kurva standar yang memberikan hubungan antara konsentrasi asam galat dengan absorbansinya, maka kita dapat menentukan konsentrasi dari sampel dengan menggunakan analisis regresi linier. Asam galat digunakan sebagai larutan standar karena asam galat merupakan salah satu jenis golongan senyawa phenolik yangd imana mana asam galat ini memiliki nama lain pyrogalol. Contoh dari senyawa phenolik yang termasuk golongan pyrogalol adalah gallocatechins (EGCG ), tanin , myricetin , alkohol sinapyl berasal lignins. Pengukuran total fenol dengan metode Folin-Ciocalteau didasarkan pada reaksi oksidasi eduksi. Reagen Folin yang terdiri dari asam fosfomolibdat dan asam fosfotungstad akan tereduksi oleh senyawa polifenol menjadi malibdenum-tungsen. Reaksi ini membentuk kompleks warna biru. Semakin tinggi kadar fenol pada sampel,maka semakin banyak molekul kromagen (biru) yang terbentuk sehingga nilai
abosrbansi akan mengalami nilai peningkatan.
Hasil absorbansi yang diperoleh dari hasil analisis dapat memberikan informasi panjang gelombang dengan absorban maksimum dari senyawa atau unsur. Panjang gelombang dan absorbansi yang dihasilkan selama proses analisis digunakan untuk membuat kurva standar. Konsentrasi suatu senyawa atau unsur dapat dihitung dari kurva standar yang diukur pada panjang gelombang dengan absorban maksimum. Dari kurva standar kalibrasi, diperoleh persamaan garis:
BAB VI
KESIMPULAN DAN SARAN 6.1 Kesimpulan
Pada prakitkum kali ini sampel teh hijau dari kelompok 2 dan 3 memilki hasil total fenol yang tidak berbeda nyata yaitu 3,33 % dan 3,56 % sedangkan pada sampel teh hitam dari kelompok 4 dan 5 mendapatkan hasil total fenol sebesar 1,79% dan 2,57 %. Kandungan total fenol terbesar dari sampel didapatkan pada sampel teh hijau dengan total fenol 3,56%. K lebih teliti lah
5.2 Saran
DAFTAR PUSTAKA
Burda S. & Oleszek W. 2001.Antioxidant and anti-radical activities of flavonoids. J.Food Chemistry .49 : 2774–2779.
Crozier A, Clifford MN, Ashihara H. 2006. Plant Secondary Metabolites: Occurrence, Structure and Role in the Human Diet. Oxford: Blackwell Publishing Ltd. Hal: 11-16, 244-249. 978-1-4051-2509-3
Dewi, P.2008. Pemisahan Minyak Atsiri Daun Kemangi (olimum basilirum) Secara KLT dan Aktifitasnya Terhadap Malasezia Fusfur in Vitro, Skripsi, Fakultas Kedokteran, Universitas Diponegoro.
Golumbic C, Mattill HA. 2007. The antioxidant properties of gallic acid and allied compounds. J of the American Oil Chemists' Society 19(8):144-145.
Kim DH. Lee IA, Lee JA, Baek NI, 2005. Antihiperlipidemic effect of crocin isolated from the fructus ofGardenia jasminoides and its metabolite crocetin. Biol Pharm Bull 28(11):2106-2110.
Maria, G.M. 2009. Respon Produksi Tanaman Kangkung Darat (Iphomea reptans Poir.) Terhadap Variasi Waktu Pemberian Pupuk Kotoran Ayam. Jurnal Ilmu Tanah 7(1): 18-22. Nasution, Z. dan W. Tjiptadi. 1975. Pengolahan Teh. Bogor: Teknologi Industri
Pertanian FATETA IPB.
Nelson, J.L., P.S. Bernstein, M.C. Schmidt, M.S. Von Tress, dan E.W. Askew. 2003. Dietarymodification and moderate antioxidant supplementation defferently affect serumcarotenoids, antioxidants level and marker of oxidative stress in older humans. J.Nutr. 133: 3117-3123.