2.1Kerang
Kerang adalah salah satu hewan lunak (Mollusca) kelas Bivalvia atau Pelecypoda.
Secara umum bagian tubuh kerang dibagi menjadi lima, yaitu (1) kaki (foot byssus),
(2) kepala (head), (3) bagian alat pencernaan dan reproduksi (visceral mass), (4) selaput (mantle) dan cangkang (shell). Pada bagian kepala terdapat organ-organ syaraf sensorik dan mulut. Warna dan bentuk cangkang sangat bervariasi tergantung
pada jenis, habitat dan makanannya.
Kerang biasanya simetri bilateral, mempunyai sebuah mantel yang berupa
daun telinga atau cuping dan cangkang setangkup. Mantel dilekatkan ke cangkang
oleh sederetan otot yang meninggalkan bekas melengkung yang disebut garis mantel.
Fungsi dari permukaan luar mantel adalah mensekresi zat organik cangkang dan
menimbun kristal-kristal kalsit atau kapur. Cangkang terdiri dari tiga lapisan, yakni
(Rina Hudaya, 2010):
a. Lapisan luar tipis, hampir berupa kulit dan disebut periostracum, yang
melindungi.
b. Lapisan kedua yang tebal, terbuat dari kalsium karbonat; dan
c. Lapisan dalam terdiri dari mother of pearl, dibentuk oleh selaput mantel
dalam bentuk lapisan tipis. Lapisan tipis ini yang membuat cangkang menebal
saat hewannya bertambah tua.
2.1.1 Kandungan Cangkang Kerang
Menurut (Setyaningrum, 2009) Kulit kerang merupakan bahan sumber mineral yang
pada umumnya berasal dari hewan laut berupa kerang yang telah mengalami
penggilingan dan mempunyai karbonat tinggi. Kandungan kalsium dalam cangkang
Tabel 2.1 Kandungan Kimia Serbuk Cangkang Kerang
Komponen Kadar (% berat)
CaO 66,70
SiO2 7,88
Fe2O3 0,03
MgO 22,28
Al2O3 1,25
Sumber : Shinta Marito Siregar 2009
2.1.2 Jenis-Jenis Kerang
Rina Hudaya (2010) mengemukakan bahwa kerang merupakan sumber bahan
makanan yang banyak dikonsumsi oleh masyarakat, karena mengandung protein dan
lemak. Jenis kerang yang sering menjadi konsumsi masyarakat, yaitu kerang hijau
(Mytilus viridis), kerang darah (Anadara granosa), dan kerang bulu (Anadara antiquata).
2.1.2.1Kerang Bulu (Anadara antiquata)
Kerang darah (Anadara granosa) dan kerang Bulu (Anadara antiquata) adalah family arcidae dan genus Anadara. Secara umum kedua kerang ini memiliki ciri morfologi
yang hampir sama. Cangkang memiliki belahan yang sama melekat satu sama lain
pada batas cangkang. Perbedaan dari kedua kerang ini adalah morfologi
cangkangnya. Kerang bulu (Anadara antiquata) memiliki cangkang yang ditutupi oleh rambut-rambut serta cangkang tersebut lebih tipis daripada kerang darah
(Anadara granosa).
Kerang darah memiliki cangkang yang lebih tebal, lebih kasar, lebih bulat,
dan bergerigi dibagian puncaknya serta tidak ditumbuhi oleh rambut-rambut. Kerang
bulu pada umumnya hidup di perairan berlumpur dengan tingkat kekeruhan tinggi.
Klasifikasi kerang bulu adalah sebagai berikut:
Kingdom : Animalia
Phylum : Mollusca
Class : Bivalvia
Ordo : Arcioda
Family : Arcidae
Genus : Anadara
Spesies : Anadara antiquate
2.1.2.2Kerang Hijau (Mytilus viridis)
Kerang hijau hidup di laut tropis seperti Indonesia, terutama di perairan pantai dan
melekatkan diri secara tetap pada benda-benda keras yang ada disekelilingnya.
Kerang ini tidak mati walaupun tidak terendam selama air laut surut. Kerang hijau
termasuk binatang lunak, mempunyai dua cangkang yang simetris, kakinya berbentuk
kapak, insangnya berlapis-lapis satu dengan lainnya dihubungkan dengan cilia.
Klasifikasi kerang hijau adalah sebagai berikut:
Habitat kerang hijau belum diketahui secara merata di perairan Indonesia,
namun dapat dicatat karakteristik perairan yang sesuai bagi budidaya kerang hijau
antara lain suhu perairan berkisar antara 27oC – 37oC, pH air antara 3 – 4 , arus air
dan angin tidak terlalu kuat dan umumnya pada kedalaman air antara 10 m-20 m.
Laju pertumbuhan kerang hijau berkisar 0,7-1,0 cm/ bulan. Ukuran konsumsi yang
panjangnya sekitar 6 cm dicapai dalam waktu 6-7 bulan.
2.1.2.3Kerang Darah (Anadara granosa)
Cangkang kerang darah memiliki belahan yang sama melekat satu sama lain pada
batas cangkang. Rusuk pada kedua belahan cangkangnya sangat menonjol. Cangkang
berukuran sedikit lebih panjang dibanding tingginya tonjolan (umbone). Setiap
belahan Cangkang memiliki 19-23 rusuk.
Dibanding kerang hijau, laju pertumbuhan kerang darah relatif lebih lambat.
Laju pertumbuhan 0,098 mm/hari. Untuk tumbuh sepanjang 4-5 mm, kerang darah
memerlukan waktu sekitar 6 bulan. Presentase daging terbesar dimiliki oleh A.
granola, yaitu sebesar 24,3%. Kerang darah memijah sepanjang tahun dengan
puncaknya terjadi pada bulan Agustus/September. Hewan ini termasuk hewan
berumah dua (diocis). Kematangan gonad terjadi pada saat kerang darah mencapai
ukuran panjang 18-20 mm dan berumur kurang dari satu tahun. Adapun pemijahan
Gambar 2.3 Kerang Darah
Kerang ini hidup dalam cekungan-cekungan di dasar perairan di wilayah
pantai pasir berlumpur. Jenis kekerangan ini menghendaki kadar garam antara 13-28
g/kg, kecerahan 0,5-2,5 m, dan pH 7,5-8,4. Klasifikasi kerang darah adalah sebagai
berikut
Kingdom : Animalia
Phylum : Mollusca
Class : Bivalvia
Ordo : Arcioda
Family : Arcidae
Genus : Anadara
Spesies : Anadara granosa
2.2 Hidroksiapatit
2.2.1 Deskripsi Hidroksiapatit
Hidroksiapatit merupakan jenis biomaterial keramik yang mampu menggantikan
mineral jaringan tulang. Hal ini karena hdroksiapatit mempunyai komposisi yang
hampir mirip dengan tulang manusia yaitu tersusun dari mineral kalsium dan fosfat.
Sebagai bahan rehabilitasi jaringan tulang hidroksiapatit dapat meningkatkan
pertumbuhan sel-sel yang akan memperbaiki fungsi daur kehidupan jaringan yang
Pada umumnya berat hidroksiapatit dapat mencapai 69% dari berat tulang
alami. Hidroksiapatit memiliki struktur heksagonal dan merupakan senyawa yang
paling stabil diantara berbagai kalsium. Hidroksiapatit juga sangat stabil dalam cairan
tubuh serta diudara kering atau lembab hingga 1200o C. Kesamaan hidroksiapatit
dengan komposisi mineral pada tulang dan gigi manusia membuat hidroksiapatit ini
cocok untuk pengganti segmen yang rusak pada sistem kerangka manusia (Mahreni,
2012).
Menurut Sopyan et al. (2002) Biokeramik hidroksiapatit adalah keramik berbasis kalsiumfosfat dengan rumus kimia Ca10(PO4)6(OH)2 yang merupakan
paduan dua senyawa garam trikalsiumfosfat dan kalsiumhidroksida dengan persen
berat ideal 39,9% Ca, 18,5%P dan 3,38% OH dan rasio ideal antara Ca/P sebesar 1,67
2.2.2 Sifat-Sifat Hidroksiapatit
Pane (2004) mengemukakan bahwa sifat-sifat hidroksiapatit adalah sebagai berikut:
2.2.2.1Sifat Fisis
Hidroksiapatit merupakan contoh biokeramik bioaktif. Biokeramik ialah keramik
yang secara inovatif dimanfaatkan secara khusus yang dipergunakan untuk
memperbaiki dan merekonstruksi bagian tubuh yang terkena penyakit atau cacat.
Bioaktif berarti kemampuan suatu bahan untuk merangsang pertumbuhan tulang baru
disekitar implan.
Permukaan bahan biokeramik bioaktif melekat pada jaringan sehingga
mampu menahan beban gaya mekanis diatasnya. Sering terjadi adhesi dipermukaan
lebih besar daripada kohesi tulang atau implan, bila terjadi keretakan mekanis. Hal ini
terjadinya tidak pada permukaan melainkan pada tulang atau implan.
2.2.2.2Sifat Kimia
Pada suhu tubuh, ada dua jenis kalsium phospat yaitu dikalsium phospat atau brushit
dan hidroksiapatit yang dapat berkonta dengan stabil pada media berair misalnya
cairan tubuh. Dikalsium phospat (CaHPO4.H2O) atau brushit (C2P) stabil pada pH
Pemadatan keramik kalsium phospat terjadi pada suhu antara 1000-1500oC.
perubahan bentuk yang terjadi pada keramik phospat yang terjadi pada suhu tinggi
tidak hanya tergantung pada suhu tetapi juga pada tekanan persisi air dalam atmosfer.
Bila ada air, maka kalsium phospat dapat terbentuk menjadi hidroksiapatit stabil
sampai suhu 1350oC. Stabilitas suhu hidroksiapatit meningkat sesuai dengan tekanan
parsial.
2.2.2.3Sifat Mekanis
Perbandingan dari pengamatan sifat mekanis hidroksiapatit dapat dilihat pada tabel
2.2 berikut:
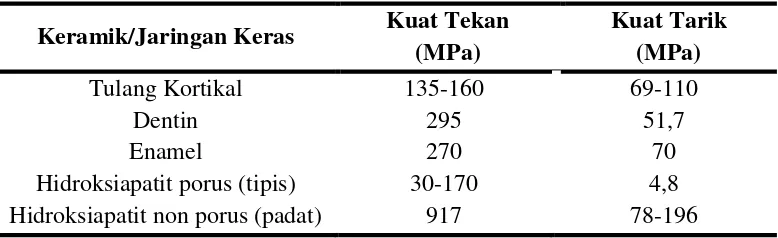
Tabel 2.2 Kuat Tekan dan Kuat Tarik dari Jaringan Keras dan Hidroksiapatit
Keramik/Jaringan Keras Kuat Tekan (MPa)
Kuat Tarik (MPa)
Tulang Kortikal 135-160 69-110
Dentin 295 51,7
Enamel 270 70
Hidroksiapatit porus (tipis) 30-170 4,8 Hidroksiapatit non porus (padat) 917 78-196
Sumber: Mai Sarah Pane 2004
Ukuran porousitas dari partikel hidroksiapatit tampaknya memegang
peranan penting pda proses pertumbuhan jaringan tulang, melalui lubang porousitas
ini cairan dari jaringan ikat masuk kepermukaan.
2.2.2.4Sifat Biologis
Hidroksiapatit memiliki kemampuan bertahan terhadap korosi, terhadap efek toksis
yang dihasilkan korosi dan kemampuan bertahan terhadap perubahan selama
pemakaian bahan dilingkungan tubuh, dan tidak menimbulkan reaksi penolakan dari
jaringan tubuh, sehingga dikatakan bahwa hidroksiapatit memiliki sifat
Hidroksiapatit yang digunakan sebagai pelapis pada logam berpori dapat
mempercepat laju pembentukan tulang dalam pori-porinya. Tetapi besarnya pori-pori
dapat mengurangi kekuatan bahan.
2.2.3 Sintesis Hidroksiapatit
Sintesis hidroksiapatit dapat dilakukan dengan beberapa metode diantaranya:
1. Metode basah, menggunakan reaksi cairan (dari larutan menjadi padatan),
merupakan metode yang umum digunakan karena sederhana dan
menghasilkan serbuk hidroksiapatit dengan sedikit Kristal atau amorf.
2. Metode kering, menggunakan reaksi padat (dari padatan menjadi padatan) dan
menghasilkan serbuk hidroksiapatit dengan butir halus dan derajat
kristalinitasnya tinggi.
3. Metode hidrotermal, menggunakan reaksi hidrotermal (dari larutan menjadi
padatan) dan menghasilkan hidroksiapatit dengan Kristal tunggal.
4. Metode alkoksida, menggunakan reaksi hidrolisa (dari larutan menjadi
padatan) dan biasanya digunakan untuk membuat lapisan tipis dan
hidroksiapatit yang dihasilkan mempunyai derajat kristalinitas tinggi.
5. Metode fluks, menggunakan reaksi peleburan garam (dari pelelehan menjadi
padatan), menghasilkan hidroksiapatit Kristal tunggal yang mengandung
unsure lain seperti boron apatit, fluorapatit dan kloroa
Sintesis hidroksiapatit dengan metode basah yaitu dengan menggunakan
larutan dan akan dihasilkan padatan. Pada metode basah ini melalui proses
presipitasi. Kristal apatit banyak mengandung gugus karbon dalam bentuk karbonat.
Pada struktur hidroksiapatit, dapat menggantikan ion OH- membentuk Kristal apatit
karbonat tipe A, dan bila menggantikan ion PO43- membentuk Kristal apatit karbonat
tipe B. Pada umumnya, presipitasi pada temperature rendah akan membentuk apatit
karbonat tipe B, sedangkan apatit hasil presipitasi dari reaksi pada suhu tinggi akan
menghasilkan apatit karbonat tipe A.Proses sintesis dengan metode basah ada 2
1. Proses yang melibatkan reaksi antara kalsium hidroksida Ca(OH)2 dan garam
posfat (NH4)2HPO4
2. Proses yang melibatkan reaksi antara asam (H3PO4) dan basa (Ca(OH)2)
Keuntungan utama sintesis dengan metode basah, adalah bahwa hasil
samping sintesisnya air, kemungkinan kontaminasi selama pengolahan sangat rendah
dan biaya pengolahan rendah. Reaksi ini sederhana, murah, cocok untuk produksi
industry skala besar dan tidak menimbulkan polusi terhadap lingkungan. Sintesis
dengan metode basah menghasilkan hidroksiapatit dengan tingkat kemurnian tinggi
(Muntamah, 2011).
2.2.4 Aplikasi Hidroksiapatit
Hidroksiapatit banyak diaplikasikan pada dunia medis karena sifatnya yang sangat
mirip dengan komponen pada organ-organ tertentu dari manusia. Salah satu aplikasi
hidroksiapatit adalah sebagai bahan dasar implant tulang.
Prasetyanti (2008) mengemukakan bahwa tulang terdiri atas matriks organik
keras yang sangat diperkuat oleh endapan garam kalsium. Tulang padat rata-rata
mengandung matriks 30% berat dan 70% garam. Garam kristal yang diendapkan di
dalam matriks tulang terdiri atas kalsium dan fosfat. Garam kristal utama dikenal
sebagai hidroksiapatit (HAp) dengan formula Ca
10(PO4)6(OH)2.
Garam kalsium yang pertama diendapkan dalam tulang adalah bukan kristal
hidroksiapatit tetapi senyawa amorf seperti dikalsium fosfat dihidrat yang merupakan
tahap awal proses pertumbuhan kristal hidroksiapatit. Dikalsium fosfat dihidrat
ukurannya kecil sehingga dalam profil XRD masih tampak seperti amorf. Kalsium
fosfat amorf memiliki rumus kimia bervariasi, rasio molar unsur Ca dan P rendah,
dan kaya akan HPO
4
2-. Strukturnya dapat terganggu dengan kedatangan ion asing2-.
Garam kalsium yang kedua, trikalsium fosfat. Peluang trikalsium fosfat kecil
akan terbentuk kristal dalam salah satu komponen mineral jaringan keras. Garam
yang ketiga, oktakalsium fosfat, strukturnya mirip dengan hidroksiapatit. Garam
atom-atom, atau melalui proses reabsorpsi dan pengendapan kembali, garam-garam ini
diubah menjadi kristal hidroksiapatit dalam waktu beberapa minggu atau beberapa
bulan. Jadi, garam kalsium dapat berada dalam berbagai fasa, yaitu fasa amorf dan
fasa kristal. Hidroksiapatit ini merupakan fasa kristal yang paling stabil dengan grup
ruang P63/m, dan struktur kristal berbentuk heksagonal.
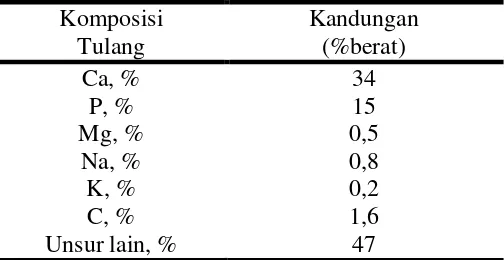
Ion magnesium, natrium, kalium dan karbon ditemukan di antara garam
tulang ditunjukkan dalam Tabel 2.3. Karbonat juga terdapat pada tulang. Kombinasi
yang demikian memberikan fungsi mekanik yang dibutuhkan oleh tulang untuk
penyangga tubuh dan pendukung gerakan, karena hidroksiapatit yang tumbuh berada
di dekat setiap segmen serat kolagen yang terikat kuat untuk menjaga kekuatan
tulang.
Tabel 2.3 Kandungan elemen inorganik pada tulang
Sumber: Fitriani Prasetyanti 2008
2.2.5 Karakterisasi Hidroksiapatit
2.2.5.1Fourier Transform Infra Red (FT-IR)
FT-IR merupakan variasi instrumental dari spektroskopi IR yang menggunakan
prinsip interferometri. Kelebihan-kelebihan dari FT-IR mencakup persyaratan ukuran
sampel yang kecil, perkembangan spectrum yang cepat, dan arena instrument ini
memiliki computer yang terdedikasi memiliki kemampuan untuk menyimpan dan
memanipulasi spectrum (Sopyan, 2001).
Spektroskopi fourier Transform infrared merupakan salah satu teknik spektroskopi inframerah yang dapat mengidentifikasi kandungan gugus kompleks
unsur penyusunnya. Bahan yang dianalisis dapat berupa padatan, cairan, dan gas.
Dalam hal ini metode spektroskopi yang digunakan adalam metode spektroskopi
absorpsi, yang didasarkan pada perbedaan penyerapan radiasi inframerah oleh
molekul suatu materi. Pada spektroskopi inframerah, spectrum inframerah terletak pada daerah panjang gelombang yang dimulai dari 0.75 μm sampai 1000 μm atau bilangan gelombang dari 12800 cm-1 sampai 1 cm-1. Dilihat dari segi aplikasi dan
instrumentasi, spectrum infrared dibagi menjadi tiga jenis radiasi yaitu infrared dekat (bilangan gelombang 12800-4000 cm-1), infrared pertengahan (bilangan gelombang 4000-200 cm-1), dan infrared jauh (bilangan gelombang 200-10 cm-1). FTIR termasuk dalam kategori radiasi infrared pertengahan.
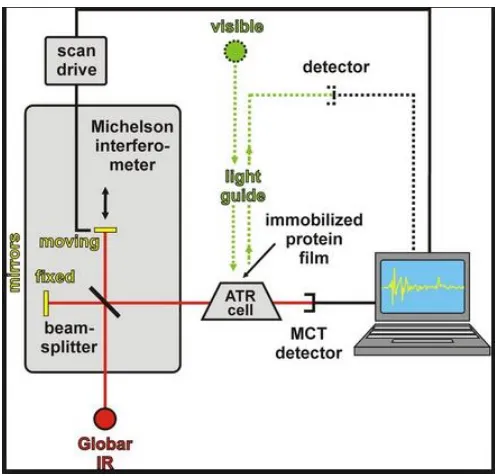
Gambar 2.4 Prinsip Kerja FT-IR
Absorpsi infrared oleh suatu materi dapat terjadi jika adanya kesesuaian
antara frekuensi radiasi inframerah dengan frekuensi vibrasional molekul sampel dan
perubahan momen dipole selama bervibrasi. Pada FTIR terdapat komponen
interferometer Michelson yang berfungsi untuk mengurai radiasi inframerah menjadi
komponen-komponen frekuensi. Cara kerja FTIR yaitu dengan mengumpulkan data
2.2.5.2XRD (X-ray Difractometer)
Teknik difraksi yang paling umum digunakan adalah metode serbuk. Dalam hal ini
sampel ditumbuk hingga membentuk partikel dengan ukuran tertentu.
Partikel-partikel tersebut akan berada pada orientasi tertentu yang memenuhi kondisi hokum
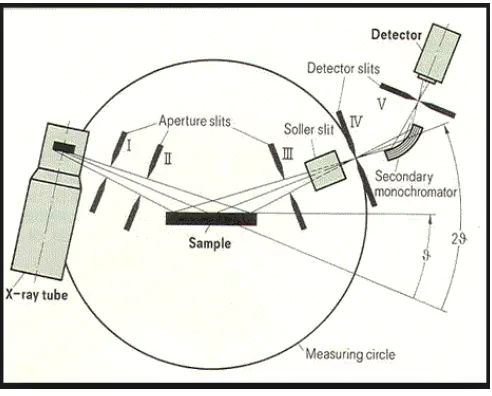
Bragg. Analisis Kristal modern menggunakan difraktometer sinar X yang dilengkapi
dengan sebuah pencacah radiasi (radiation counter). Untuk mencatat sudut dan intensitas difraksi, sebuah recorder mencatat berkas difraksi seiring dengan gerakan goniometer sinkron dengan gerakan sampel pada rentang 2θ.
Gambar 2.5 Prinsip Kerja XRD
Panjang gelombang sinar-X untuk difraksi berada pada rentang 0.05 hingga
0.25 nm (panjang gelombang sinar tampak sekitar 600 nm). Sinar-X untuk tujuan
difraksi diproduksi dengan tegangan antara katoda dan anoda sebesar 35 kV dalam
kondisi vakum. Bila filament tungsten dipanaskan, electron terlepas dari katoda melalui proses emisi termionik dan dipercepat menuju target, dan sinar-X terlepas.
Sebagian besar energi kinetik elektron dikonversi menjadi panas sehingga perlu
didinginkan dari luar (Subaer, 2008).
Berdasarkan pada hukum Bragg, suatu X-Ray dengan panjang gelombang
yang berjarak d. interferensi konstruktif dari X-Ray dihamburkan hanya akan terjadi,
jika beda lintasannya memenuhi persamaan (2.1) berikut:
𝑛𝜆 = 2𝑑 sin 𝜃 (2.1)
Berdasarkan harga hkl yang yang diperoleh dapat dilakukan perhitungan
parameter kisi untuk struktur heksagonal dengan menggunakan persamaan (2.2)
berikut:
Untuk menentukan apakah sampel yang dihasilkan memiliki ukuran dalam
daerah butir (grain) ataukah partikel, berdasarkan data hasil uji XRD dilakukan
perhitungan diameter grain dengan menggunakan menggunakan persamaan Scherrer
(Djamas, 2010) sebagai berikut:
2.2.5.3Scanning Electron Microscopy (SEM)
Prinsip kerja SEM adalah berkas electron yang dipergunakan untuk memindai
specimen dihasilkan oleh electron gun yang tersusun atas tiga komponen yaitu : 1. Filament katoda yang terbuat dari kawat tungsten, Kristal lanthanum
hexaboride (LaB6) atau cerium hexaboride (CeB6),
2. Tudung bercelah (Wehnelt Cylinder) yang mengontrol aliran dari electron (bias),
3. Plat anoda bermuatan positif yang menarik dan mempercepat electron menuju
specimen.
Ketika electron dengan energi tinggi menumbuk specimen, electron tersebut
akan dihamburkan oleh atom dari specimen. Hamburan electron menyebabkan
terjadi pada volum tertentu dibawah permukaan specimen. Dari interaksi tersebut
dihasilkan apa yang disebut dengan Secondary Electron (SE) dan Backscattered Electron (BSE) yang nantinya dipergunakan sebagai sumber sinyal untuk membentuk gambar. Zona ini biasa disebut dengan pears-head karena bentuknya yang mirip buah pir dan ukurannya bertambah dengan meningkatnya energi dari electron yang datang
(Suryadi, 2011).
Gambar 2.6 Prinsip Kerja SEM
Analisis mikrostruktur dengan SEM dapat dilakukan pada sampel yang telah
dipoles atau sampel yang tidak dipoles atau sampel fraktur (fractured specimen).
Sampel yang digunakan didalam penyelidikan SEM dipersiapkan dengan cara
sebagai berikut: Sampel dipotong hingga berukuran tebal 2.00 mm dengan diameter
10 mm. Selanjutnya material tersebut dipoles hingga ukuran 1 μm dengan pasta intan.
Sampel yang telah dibersihkan dan dikeringkan kemudian dilapisi dengan emas untuk
3.1Tempat dan Waktu Penelitian
Penelitian ini dilakukan di :
1. Laboratorium SMK-SMAK Padang.
2. Laboratorium Farmasi Universitas Andalas, Padang.
3. Laboratorium Fisika Universitas Negeri Medan, Medan.
Penelitian dilakukan pada tanggal 25 Mei – 19 Juni 2014.
3.2Peralatan dan Bahan 3.2.1 Peralatan
1. X-Ray Diffractometer (XRD)
Untuk mengetahui struktur Kristal dan susunan senyawa dari Hidroksiapatit.
2. Scanning Electron Microscopy EDX (SEM-EDX)
Untuk melihat struktur permukaan Hidroksiapatit dan unsur-unsur yang
terkandung didalamnya.
3. Fourier Transform Infra Red (FT-IR)
Untuk mengetahui gugus fungsi yang terdapat pada hidroksiapatit.
4. pH Universal
Untuk mengukur pH dari suatu larutan
5. Tabung Erlenmenyer
Sebagai wadah menampung filtrat
6. Mortar dan Pestle
Untuk menghaluskan cangkang kerang
7. Pipet Tetes
Untuk meneteskan larutan dengan kecepatan tertentu
8. Magnetic Stirrer
9. Timbangan Digital
Untuk menimbang bahan-bahan yang akan digunakan.
10. Beaker Glass
Sebagai wadah sintesis HA
11. Kertas Saring
Untuk menyaring endapan HA dari larutan
12. Cawan keramik
Sebagai wadah untuk mensintering sampel
13. Corong
Untuk menyaring endapan
14. Furnace
Untuk mensintering sampel dengan suhu yang telah di tentukan.
15. Buret
Untuk mentitrasi larutan
16. Standar dan Klem
Sebagai penyanggah buret
17. Cawan Penguap
Sebagai wadah untuk memanaskan sampel
3.3Prosedur
3.3.1 Preparasi sampel.
Cangkang kerang yang digunakan adalah cangkang kerang bulu yang
dikumpulkan dari limbah masyarakat, dimana cangkang kerang bulu yang
akan digunakan dicuci terlebih dahulu dengan air bersih lalu dikeringkan.
Setelah dikeringkan, cangkang kerang bulu dihaluskan dengan mortar dan
pestle lalu diayak dengan ukuran 200 mesh.
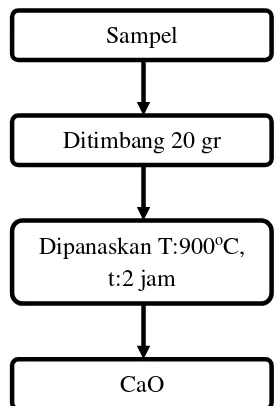
3.3.2 Pembuatan CaO
1. Ditimbang cangkang kerang yang telah dihaluskan sebanyak 20 gr.
2. Dipanaskan pada suhu 900o C selama 2 jam.
3. Didinginkan didalam desikator.
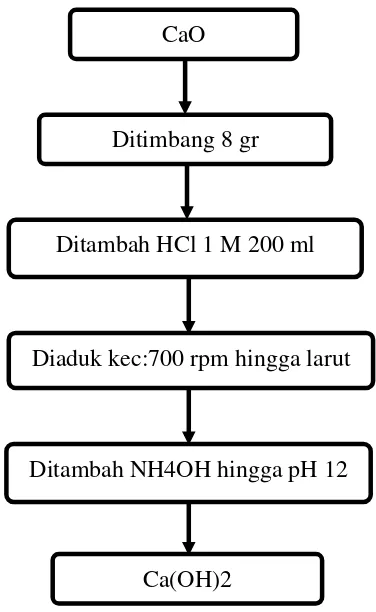
3.3.3 Pembuatan Ca(OH)2
1. Ditimbang CaO sebanyak 8 gr.
2. Dimasukkan kedalam beaker glass lalu ditambahkan HCl 1 M sebanyak 200
ml.
3. Diaduk dengan kecepatan 700 rpm hingga larut.
4. Ditambahkan NH4OH hingga larutan basa pH 12.
3.3.4 Sintesis Hidroksiapatit
1. Disediakan Ca(OH)2 yang telah dihasilkan.
2. Dititrasi larutan H3PO4 0,3 M dengan kecepatan 1 ml/detik.
3. Diaduk dengan kecepatan 700 rpm selama 6 jam.
4. Diatur pH dengan menambahkan NH4OH agar larutan basa pH 10.
5. Didiamkan selama 15 jam sampai terbentuk endapan HA.
6. Disaring endapan yang dihasilkan.
7. Dicuci endapan dengan aquades panas untuk menghilangkan ion Cl.
9. Disinterring pada suhu 700o C , 800o C , 900o C, 1000o C dan 1100o C selama
2 jam.
3.3.5 Karakterisasi Hidroksiapatit
Sampel HA yang telah disinterring pada suhu 700oC , 800oC , 900oC, 1000oC dan
1100oC diuji dengan FT-IR untuk mengetahui gugus fungsi yang terdapat pada
sampel HA tersebut. Setelah diuji dengan FT-IR, akan diambil tiga sampel yang
karakteristiknya paling mendekati dengan HA murni. Selanjutnya ketiga sampel HA
tersebut akan diuji dengan XRD untuk mengetahui tingkat kristalinitasnya.
Setelah diuji dengan XRD, akan diambil satu sampel lagi yang
karakteristiknya paling mendekati dengan HA murni dan selanjutnya akan diuji
dengan SEM-EDX untuk mengetahui struktur permukaan dari sampel HA tersebut
3.4Diagram Alir penelitian 3.4.1 Preparasi Sampel
Gambar 3.1 Diagram Alir Preparasi Sampel
3.4.2 Pembuatan CaO
Gambar 3.2 Diagram Alir Pembuatan CaO Ditimbang 20 gr
CaO
Dipanaskan T:900oC, t:2 jam
Sampel
Cangkang Kerang Bulu
Dicuci dengan air bersih
Dikeringkan
Sampel
3.4.3 Pembuatan Ca(OH)2
Gambar 3.3 Diagram Alir Pembuatan Ca(OH)2 Ditimbang 8 gr
Ca(OH)2
Ditambah HCl 1 M 200 ml CaO
3.4.4 Sintesis Hidroksiapatit
Gambar 3.4 Diagram Alir Sintesis Hidroksiapatit Disaring endapan
FT-IR
Ca(OH)2
Dititrasi dengan H3PO4 0,3 M dan diaduk kec:
700 rpm t:6 jam
Didiamkan 15 jam hingga terbentuk endapan HA Ditambah NH4OH
hingga pH 10
Dicuci dengan aquadest panas hingga ion Cl hilang
Dikeringkan
Disinterring dengan suhu yang ditentukan
Dikarakterisasi