Fisika Statistik untuk
Mahasiswa MIPA
Mikrajuddin Abdullah, DR.Eng.
Copyright➞2009 by Mikrajuddin Abdullah
All rights reserved.
Kata Pengantar
Buku ini disusun untuk membantu mahasiswa memahami Fisika Statistik lebih mudah. Uraian diberikan serinci mungkin, tahap demi tahap, sehingga mahasiswa dapat mengikutinya dengan mudah. Mata kuliah Fisika Statistik sampai sekarang menjadi momok bagi sebagian besar mahasiswa. ketidak-tersediaan buku yang menjelaskan materi secara rinci tampaknya menjadi salah satu penyebab terjadinya bottle neck keterlambatan kelulusan maha-siswa akibat gagal dalam menyelesaikan mata kuliah tersebut.
Buku ini hanya membahas dasar-dasar Fisika Statistik untuk memberi-kan bekal yang memadai bagi mahasiswa untuk memahami Fisika Statistik lanjut. Masih banyak kekurangan yang muncul disana-sini. oleh karena itu kritik dan saran yang membangun dari pembaca sangat diharapkan untuk menyempurnakan isi buku ini.
Penyelesaian buku ini tidak lepas dari tunjangan dana Hibah Penulisan Buku Teks 2009 dari Institut Teknologi Bandung yang penulis terima. Oleh karena itu penulis sampaikan terima kasih sebesar-besarnya kepada Wakil Rektor Senior Bidang Akademik ITB dan Direktur Pendidikan ITB. Terima kasih juga penulis sampaikan kepada Prof. Ismunandar dan Dr. Dhian Damajani atas support yang sangat berharga dalam proses penyelesaian buku ini.
Kepada penyunting, Dr. Siti Nurul Khatimah dari Prodi Fisika ITB, penulis sampaikan terima kasih sebesar-besaranya atas masukan dan saran yang sangat berharga. Penulis juga ingin menyampaikan terima kasih kepada para rekan-rekan dosen di Program Studi Fisika-FMIPA ITB yang secara langsung maupun tidak langsung membantu penulis menyelesaikan buku ini.
dan Ardi Khalifah) yang tiada henti-hentinya memberikan support dalam setiap langkah pengabdian penulis dan ikut terlibat dalam pengecekan ke-salahan ketik dalam naskah buku ini.
Bandung, Desember 2009
Daftar Isi
1 Pendahuluan 1
2 Statistik Maxwell-Boltzmann 5
2.1 Konfigurasi Penyusunan Sistem Klasik . . . 5
2.2 Konfigurasi dengan Probabilitas Maksimum . . . 14
2.3 Harga Rata-Rata . . . 16
2.4 Nilai Peluang Konfigurasi Maksimum . . . 19
3 Ruang Fasa 23 3.1 Definisi Ruang Fasa . . . 23
3.2 Elemen volume Ruang Fasa . . . 25
3.3 Energi Kinetik . . . 26
3.4 N Sistem dalam Ruang Fasa . . . 26
3.5 Menghitung Jumlah Keadaan . . . 28
3.6 Menentukanns . . . 31
3.7 Elemen Ruang Fasa dalam Momentum/Laju . . . 32
4 Parameter-Parameter Statistik 35 4.1 Menentukan Parameterβ . . . 35
4.2 Bagaimana Kebergantunganβ pada Suhu? . . . 39
4.3 Menentukanβ dari Energi Rata-Rata . . . 42
4.4 Menentukan Parameterα . . . 44
5 Statistik Bose-Einstein 51
5.1 Sifat Dasar Boson . . . 51
5.2 Konfigurasi Boson . . . 53
5.3 Konfigurasi Maksimum . . . 56
5.4 Parameter α untuk Photon dan Phonon . . . 59
6 Statistik Fermi-Dirac 63 6.1 Konfigurasi Fermion . . . 64
6.2 Konfigurasi Peluang Maksimum . . . 67
7 Rapat Keadaan Sistem Kuantum 71 7.1 Ketidakpastian Heisenberg . . . 71
7.2 Koordinat Spasial Satu Dimensi . . . 72
7.3 Koordinat Spasial Dua Dimensi . . . 73
7.4 Koordinat Spasial Tiga Dimensi . . . 76
8 Beberapa Besaran Gas 81 8.1 Laju dengan Peluang Maksimum . . . 81
8.2 Laju Rata-Rata . . . 84
8.3 Laju Root Mean Square . . . 85
8.4 Distribusi Partikel dalam Besaran Lain . . . 87
9 Aplikasi Statistik Maxwell-Boltzmann 93 9.1 Efek Doppler . . . 93
9.2 Atom Magnetik dalam Medan Magnet . . . 97
9.3 Dipol Listrik . . . 102
9.4 Momen Magnetik Tiga Arah Orientasi . . . 104
9.5 Momen Magnetik Orientasi Sembarang . . . 106
9.6 Vibrasi Kisi dalam Kristal . . . 110
9.7 Hopping . . . 113
9.8 Persamaan Difusi Einstein . . . 117
DAFTAR ISI ix
9.10 Pemuaian Termal Zat . . . 123
9.11 Efek Suhu Pada Difraksi Sinar-X . . . 127
9.12 Kapasitas Panas Padatan Amorf . . . 130
9.13 Konduktivitas Vogel-Tamman-Fulcher . . . 134
10 Aplikasi Statistik Bose-Einstein 139 10.1 Radiasi Benda Hitam . . . 139
10.2 Kapasitas Panas Kristal . . . 148
10.3 Kondensasi Bose-Einstein . . . 160
11 Aplikasi Distribusi Fermi-Dirac 169 11.1 Fungsi Distribusi Fermi Dirac pada Suhu 0 K . . . 169
11.2 Energi Fermi . . . 171
11.3 Distribusi Fermi Dirac pada SuhuT >0 K . . . 173
11.4 Integral Fungsi Fermi-Dirac . . . 174
11.5 Energi Rata-Rata Elektron . . . 179
11.6 Kapasitas Panas Logam . . . 181
11.7 Emisi Termionik . . . 185
11.8 Teori Bintang Katai Putih . . . 189
11.9 Paramagnetisme Pauli . . . 195
12 Termodinamika Gas 203 12.1 Entropi . . . 203
12.2 Fungsi Partisi Boltzmann . . . 205
12.3 Ungkapan Energi dalam Fungsi Partisi . . . 206
12.4 Energi Bebas Helmholtz . . . 207
12.5 Kapasitas Panas . . . 208
12.6 Perhitungan Fungsi Partisi Klasik . . . 208
12.7 Entropi Gas Semiklasik . . . 210
12.8 Fungsi Partisi Total . . . 211
12.9 Fungsi Partisi Gas Semiklasik . . . 213
12.11Suseptibilitas Paramagnetik Kuantum . . . 216
12.12Molekul Diatomik . . . 222
12.13Persamaan Saha . . . 232
13 Statistik Semikonduktor 241 13.1 Pendahuluan . . . 241
13.2 Doping Semikonduktor . . . 242
14 Pengenalan Ensembel 251 14.1 Pendahuluan . . . 251
14.2 Dinding Assembli yang Transparan Terhadap Energi . . . 252
14.3 Konsep Ensembel . . . 254
14.4 Assembli Terbuka . . . 255
Bab 1
Pendahuluan
Persoalan yang sering muncul pada kuliah fisika statistik di perguruan ting-gi adalah ketidaktersediaan buku referensi bahasa Indonesia yang memadai. Buku terbitan luar negeri yang biasa digunakan sebagai referensi umumnya tidak membahas topik secara detail. Hal ini sering menyulitkan mahasiswa memahami mata kuliah tersebut. Bertahun-tahun kuliah ini diajarkan oleh dosen pada mahasiswa-mahasiswa fisika, persoalan yang sama selalu muncul. Bahkan mata kuliah tersebut menjadi salah satu ”bottle neck” yang mem-perlambat kelulusan mahasiswa.
Cara pemahaman fisika statistik berbeda dengan mata kuliah fisika lain seperti gelombang, termodinamika, dan mekanika. Dalam fisika statistik kita akan berangkat dari persoalan abstrak yang sebenarnya merupakan bahan kajian orang matematika seperti permutasi dan kombinasi. Fisika statis-tik dapat dipandang sebagai persoalan statisstatis-tik matemastatis-tik yang diberikan syarat batas fisis, sehingga persoalan matematika murni menjadi memiliki interpretasi fisis. Diperlukan abstraksi yang cukup tinggi untuk memahami persoalan tersebut, dan tidak semua mahasiswa bisa melakukannya.
saat ini. Pendekatan yang diberikan oleh fisika statistik adalah melihat sifat rata-rata dari partikel-paerikel tersebut tanpa kita harus melihat partikel secara individual.
Karena berangkat dari persoalan statistik matematis, mahasiswa sering mengalami kesulitan memulai memahami fisika statistik. Buku-buku yang tersedia sekarang kurang memberikan penjelasan yang mendetail sehingga tidak memberikan bantuan yang cukup berarti kepada para mahasiswa un-tuk memahami konsep-konsep tersebut. Dari tahun ke tahun mahasiswa tetap mengalami kesulitan memahami mata kuliah ini, karena cara analisis yang berbeda dengan mata kuliah fisika lainnya. Tujuan penulisan buku ini adalah memberikan penjelasan yang lebih rinci kepada mahasiswa ten-tang penurunan persamaan-persamaan fisika statistik beserta beberapa ap-likasinya. Rumus-rumus diturunkan secara lengkap dengan penjelasan yang rinci pula dengan harapan mahasiswa dapat memahami lebih jelas. Sampai saat ini kita kesulitan menemukan referensi yang memberikan penjelasan yang lebih rinci tentang penurunan persamaan-persamaan tersebut. Maha-siswa terpaksa harus melakukan usaha yang luar biasa untuk memahami konsep-konsep tersebut dan tidak jarang banyak yang apatis.
Karena materi buku ini hanya diperuntukkan bagi kuliah satu semester, maka hanya dasar-dasar statistik yang dapat menjadi modal awal bagi ma-hasiswa untuk mempelajari fisika statistik lanjut yang diberikan. Topik uta-ma yang dibahas meliputi penurunan fungsi distribusi Maxwell-Boltzuta-mann, Bose-Einstein, dan Fermi-Dirac. Contoh aplikasi sederhana ketiga macam statsitik tersebut juga diberikan. Konsep ruang fasa dan kerapatan keadaan dalam ruang fasa klasik serta ruang fasa kuantum juga diberikan, karena ked-uanya digunakan untuk menghitung besaran-besaran termodinamika. Agar mahasiswa memiliki pemahaman awal tentang ensembel, maka salah satu jenis ensembel dibahas di sini, yaitu ensembel kanonik.
Pada langkah penurunan distribusi Maxwell-Boltzmann, Bose-Einstein, dan Fermi-Dirac, modal statistik yang dibutuhkan hanya permutasi. Oleh karena itu topik yang membahas panjang lebar tentang permutasi dan kom-binasi seperti yang dijumpai di kulaih-kuliah statistik yang bersifat matem-atis tidak diberikan di sini. Hal ini dimaksudkan untuk mengurangi be-ban mahasiswa sehingga mereka bisa lebih terfokus kepada aplikasi fisis dari statistik tersebut.
mende-3
finsikan sistem. Terminologi sistem yang digunakan pada buku ini mengacu kepada partikel-partikel. Contohnya, jika kita membahas tentang gas maka sistem adalah atom atau molekul gas. Untuk gas monoatomik, sistem adalah atom gas dan untuk gas diatomik maka atau yang mengandung atom lebih banyak maka sistem adalah molekul gas. Jika kita membahas tentang elek-tron dalam logam maka sistem adalah elekelek-tron-elekelek-tron tersebut. Jika kita bahas tentang radiasi benda hitam maka sistem adalah foton. Jika kita bahas getaran kisi maka sistem adalah fonon.
Bab 2
Statistik Maxwell-Boltzmann
Isi Bab ini. Bab ini berisi perumusan statistik Maxwell-Boltzmann untuk assembli yang mengandung sistem (partikel) klasik. Contoh partikel klasik adalah atom atau molekul-molekul gas. Umumnya partikel dengan massa jauh lebih besar dari massa elektron dapat dianggap sebagai partikel klasik.
Tujuan Bab ini. Tujuan bab ini adalah mahasiswa memahami bagaimana proses membangun statistik Maxwell-Boltzmann dengan menggunakan prin-sip statistik murni yang digabungkan dengan beberapa hukum kekekalan dalam fisika, seperti kekekalan energi dan jumlah partikel.
Apa yang Perlu Dikuasai Lebih Dahulu. Untuk memahami penu-runan fungsi distribusi Maxwell-Boltzmann mahasiswa perlu memahami metode permutasi untuk benda-benda yang dapat dibedakan, sifat yang ditunjukkan oleh sebuah besaran yang nilainya kekal (konstan), serta bagaimana mencari nilai maksimum dari sebuah fungsi (metode penurunan).
2.1
Konfigurasi Penyusunan Sistem Klasik
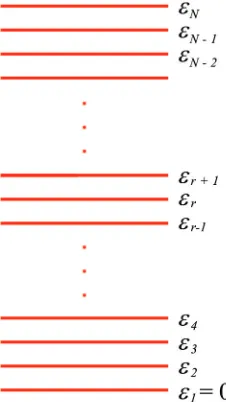
Kita akan berangkat dari asumsi bahwa energi yang dimiliki sistem-sistem dalam dianggap terdiri atas tingkat-tingkat energi. Tingkat-tingkat energi tersebut berada dalam rentangan dari nol sampai tak berhingga. Gambar 2.1 adalah ilustrasi tingkat-tingkat energi yang dimiliki assembli. Untuk sistem klasik, seperti atom gas, perbedaan energi dua tingkat berdekatan mendekati nol, atau εi+1−εi → 0. Perbedaan energi yang mendekati nol
Gambar 2.1: Tingkat-tingkat energi yang dimiliki assembli.
menempati salah satu dari tingkat energi di atas. Dalam sistem klasik tidak ada batasan jumlah sistem yang dapat menempati satu keadaan energi. Satu keadaan energi dapat saja kosong, atau ditempati oleh satu sistem, oleh dua sistem, dan seterusnya. Bahkan semua sistem berada pada satu keadaan energi pun tidak dilarang.
Agar sifat fisis dari assembli dapat ditentukan maka kita harus menge-tahui bagaimana penyusunan sistem pada tingkat-tingkat energi yang ada serta probabilitas kemunculan masing-masing cara penyusunan tersebut. Pemahaman ini perlu karena nilai terukur dari besaran yang dimiliki as-sembli sama dengan perata-rataan besaran tersebut terhadap semua ke-mungkinan penyusunan sistem pada tingkat-tingkat energi yang ada.
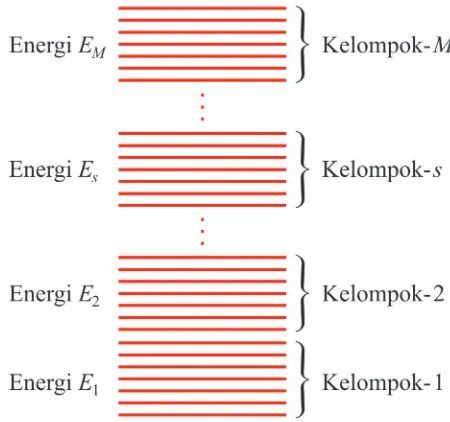
Cara menghitung berbagai kemungkinan penyusunan sistem serta proba-bilitas kemunculannya menjadi mudah bila tingkat-tingkat energi yang dimi-liki assembli dibagi atas beberapa kelompok, seperti diilustrasikan pada Gbr 2.2. Di sini kita membagi atas M kelompok. Tiap kelompok memiliki jangkauan energi yang cukup kecil sebagai berikut.
❼ Kelompok pertama memiliki jangkauan energi : 0 sampaidε
2.1 Konfigurasi Penyusunan Sistem Klasik 7
❼ Kelompok ketiga memiliki jangkauan energi : 2dε sampai 3dε
.. .
❼ Kelompok ke-s memiliki jangkauan energi : (s−1)dε sampaisdε
.. .
❼ Kelompok ke-M memiliki jangkauan energi : (M−1)dε sampaiM dε
Gambar 2.2: Kelompok-kelompok energi dalam assembli.
Satu kelompok energi mengandung sejumlah keadaan energi. Jumlah keadaan energi pada kelompok yang berbeda bisa sama dan bisa berbeda. Misalkan jumlah keadaan energi pada tiap-tiap kelompok tersebut sebagai berikut:
❼ Jumlah keadaan pada kelompok pertama : g1
❼ Jumlah keadaan pada kelompok ketiga : g3
.. .
❼ Jumlah keadaan pada kelompok ke-s: gs
.. .
❼ Jumlah keadaan pada kelompok ke-M : gM
Energi keadaan yang berbeda dalam satu kelompok umumnya berbeda. Tetapi karena perbedaan energi keadaan yang berbeda dalam satu kelompok sangat kecil (mendekati nol) maka kita dapat mengasumsi bahwa energi dalam satu kelompok diwakili oleh satu nilai energi saja. Energi tersebut dianggap sebagai energi rata-rata keadaan dalam kelompok yang bersang-kutan. Jadi,
❼ Energi rata-rata kelompok pertama : E1
❼ Energi rata-rata kelompok kedua : E2
❼ Energi rata-rata kelompok ketiga : E3
.. .
❼ Energi rata-rata kelompok ke-s: Es
.. .
❼ Energi rata-rata kelompok ke-M : EM
Misalkan pada konfigurasi tertentu tiap-tiap kelompok energi telah ditem-pati oleh sistem-sistem dengan distribusi jumlah sebagai berikut:
❼ Jumlah sistem pada kelompok energi pertama : n1
2.1 Konfigurasi Penyusunan Sistem Klasik 9
❼ Jumlah sistem pada kelompok energi ketiga : n3
.. .
❼ Jumlah sistem pada kelompok energi ke-s: ns
.. .
❼ Jumlah sistem pada kelompok energi ke-M : nM
Deskripsi tentang jumlah sistem, jumlah keadaan dan energi pada kelompok-kelompok yang telah diuraikan di atas dapat diringkas dalam Table 2.1.
Tabel 2.1: Deskripsi jumlah sistem, jumlah keadaan, dan energi yang dimiliki tiap kelompok energi.
Kelompok ke- Jumlah keadaan Energi Jumlah sistem
1 g1 E1 n1
2 g2 E2 n2
..
. ... ... ...
s gs Es ns
..
. ... ... ...
M gM EM nM
Jumlah total sistem dalam assembli adalahN. KarenaN sistem tersebut terdistribusi pada semua kelompok energi maka terpenuhi
N =
M
X
s=1
ns (2.1)
Energi total assembli memenuhi
U =
M
X
s=1
nsEs (2.2)
mempunyai peluang kemunculan yang persis sama. Dengan demikian, prob-abilitas kemunculan sebuah konfigurasi sebanding dengan jumlah penyusunan sistem yang dapat dilakukan untuk membangun konfigurasi tersebut.
Oleh karena itu, mencari probabilitas kemunculan konfigurasi dengan kondisi
❼ Adan1 sistem pada kelompok energi 1
❼ Adan2 sistem pada kelompok energi 2
❼ Adan3 sistem pada kelompok energi 3
.. .
❼ Adans sistem pada kelompok energis
.. .
❼ AdanM sistem pada kelompok energiM
ekivalen dengan mencari berapa cara penyusunan
❼ n1 sistem padag1 keadaan energi di kelompok energi 1
❼ n2 sistem padag2 keadaan energi di kelompok energi 2
❼ n3 sistem padag3 keadaan energi di kelompok energi 3
.. .
❼ ns sistem pada gs keadaan energi di kelompok energi s
.. .
2.1 Konfigurasi Penyusunan Sistem Klasik 11
Selanjutnya kita akan menentukan jumlah cara penyusunan sistem-sis-tem yang tersebar pada tingkat-tingkat energi di atas. Untuk maksud terse-but, mari kita mulai dengan menganggap semua keadaan energi kosong (tidak di tempati sistem) dan di luar ada sejumlah sistem yang akan diisi pada keadaan-keadaan tersebut. Di sini ada dua tahap proses yang terjadi. Proses I adalah membawa N buah sistem dari luar ke dalam assembli dan proses II adalah menyusun sistem pada kempompok-kelompok energi yang ada di dalam assembli.
Gambar 2.3: Cara membawa sistem dari luar masuk ke dalam assembli.
Proses I: Membawa N Buah Sistem ke Dalam Assembli. Mari kita hitung jumlah cara yang dapat ditempuh pada tiap proses pertama yaitu membawa N buah sistem dari luar ke dalam assembli. Proses ini tidak bergantung pada konfigurasi assembli. Yang terpenting adalah bagaimana membawa masuk N buah sistem ke dalam assembli. Untuk menentukan jumlah cara tersebut, perhatikan tahap-tahap berikut ini.
i) Ambil satu sistem dari daftar N buah sistem yang berada di luar assembli (Gbr. 2.3). Kita bebas memilih satu sistem ini dari N buah sistem yang ada tersebut. Jadi jumlah cara pemilihan sistem yang pertama kali dibawa masuk ke dalam assembli adalah N cara.
ii) Setelah sistem pertama dimasukkan ke dalam assembli maka tersisa
N −1 sistem dalam daftar di luar. Ketika membawa masuk sistem kedua ke dalam assembli kita dapat memilih salah satu dari N −1 buah sistem dalam daftar. Jumlah cara pemilihan sistem ini adalah
iv) Akhirnya, ketika sistem ke-N akan dimasukkan ke dalam assembli hanya ada satu sistem yang tersisa di luar. Tidak ada pilihan-pilihan yang mungkin sehingga jumlah cara memasukkan sistem ke-Nke dalam asembli adalah hanya 1 cara.
v) Dengan demikian, jumlah total cara membawa masuk N buah sistem ke dalam assembli adalah
N ×(N −1)×(N −2)×...×2×1 =N!
Proses II: Penyusunan Sistem di Dalam Kelompok-Kelompok En-ergi Selanjutnya kita tinjau proses kedua. Tahapan yang ditempuh seba-gai berikut. Tinjau kelompok 1 yang mengandungg1keadaan dan ditempati
olehn1 sistem. Sebagai ilustrasi lihat Gbr. (2.4).
Gambar 2.4: Menentukan cara menyusunn1 sistem padag1 keadaan.
Ambil partikel pertama. Kita dapat menempatkan partikel ini entah di keadaan ke-1, keadaan ke-2, keadaan ke-3, dan seterusnya hingga keadaan ke-g1. Jadi jumlah cara menempatkan partikel pertama pada kelompok-1 yang memiliki g1 keadaan adalah g1 cara. Setelah partikel-1 ditempatkan,
kita ambil partikel 2. Partikel ini pun dapat ditempatkan di keadaan ke-1, keadaan ke-2, keadaan ke-3, dan seterusnya hingga keadaan ke-g1. Dengan demikian, jumlah cara menempatkan partikel kedua jugag1 cara. Hal yang
sama juga berlaku bagi partikel ke-3, partikel ke-4, dan seterusnya, hingga partikel ke-n1 . Akhirnya, jumlah cara menempatkan n1 partikel pada g1
2.1 Konfigurasi Penyusunan Sistem Klasik 13
g1×g1×g1×...×g1 (n1buah perkalian) =g1n1
Sejumlahgn1
1 cara di atas secara implisit mengandung makna bahwa
uru-tan pemilihan partikel yang berbeda menghasilkan penyusunan yang berbe-da pula. Paberbe-dahal tiberbe-dak demikian. Urutan pemilihan yang berbeberbe-da berbe-dari sejumlah n1 partikel yang ada tidak berpengaruh pada penyusunan asal-kan jumlah partikel pada tiap bangku tetap jumlahnya. Urutan pemilihan sejumlah n1 partikel menghasilkan n1! macam cara penyusunan. Dengan
demikian, jumlah riil cara penyusunan n1 partikel pada g1 buah keadaan
seharusnya adalah
gn1
1 n1!
Penjelasan yang sama juga berlaku bagi buah partikel yang disusun pada keadaan. Jumlah cara penyusunan partikel tersebut adalah
gn2
2 n2!
Secara umum jumlah cara menempatkanns partikel di dalam kelompok
energi yang mengandung keadaan adalah
gns
s
ns!
Akhirnya jumlah cara mendistribusikan secara bersama-sama n1 sistem
pada kelompok dengan g1 keadaan, n2 sistem pada kelompok dengan g2
keadaan, .. , ns sistem padags keadaan adalah
gn1
1 n1!×
gn2
2 n2! ×
gn3
3
n3! × · · · × gnM
M
nM!
=
M
Y
s=1 gns
s
ns!
Dengan demikian, jumlah total cara menempatkan N buah sistem ke dalam konfigurasi yang mengandung n1 sistem pada kelompok dengan g1
keadaan, n2 sistem pada kelompok dengan g2 keadaan, .., ns sistem pada
kelompok dengangs keadaan adalah
W({ns}) =N! M
Y
s=1 gns
s
ns!
Sekarang kita tinjau assembli yang terisolasi dari lingkungan. Tidak ada pertukaran partikel maupun energi antara assembli dan lingkungan. Dengan demikian, jumlah sistemN dan energi totalU yang dimiliki assembli konstan. Akibatnya nilai diferensial keduanya nol, atau
δN =
M
X
s=1
δns= 0 (2.4)
δU =
M
X
s=1
Esδns= 0 (2.5)
2.2
Konfigurasi dengan Probabilitas Maksimum
Sekarang kita mencari yang memiliki probabilitas kemunculan paling besar. Kita menganggap bahwa konfigurasi yang dibentuk oleh sistem-sistem dalam assembli yang menghasilkan besaran makroskopik adalah konfigurasi den-gan probabilitas maksimum tersebut. Cara yang dilakukan adalah mencari kumpulan ns sedemikian sehingga W maksimum. Tetapi karena W
meru-pakan perkalian sejumlah faktor maka akan lebih mudah jika kita memaksi-malkan lnW. Sebab jika lnW maksimum makaW pun maksimum. Dengan cara demikian kita peroleh
lnW({ns}) = lnN! + ln M
Y
s=1 gns
s
ns!
= lnN! + ln
gn1
1 n1!×
gn2
2 n2! ×
...×g
nM
M
nM!
= lnN! + ln
gn1
1 n1!
+ ln
gn2
2 n2!
+...+ ln
gnM
M
nM!
= lnN! +
M
X
s=1
ln
gns
s
ns!
= lnN! +
M
X
s=1
{lngns
s −lnns!}
= lnN! +
M
X
s=1
{nslngs−lnns!}
2.2 Konfigurasi dengan Probabilitas Maksimum 15
Karena baikN maupunnsmerupakan bilangan-bilangan yang sangat
be-sar maka untuk mempermudah perhitungan kita dapat menggunakan pen-dekatan Stirling. Pendekatan tersebut berbentuk lnN! ∼= NlnN −N, lnns∼=nslnns−ns sehingga kita dapatkan bentuk aproksimasi
lnW ({ns})∼=NlnN −N + M
X
s=1
{nslngs−nslnns+ns} (2.7)
Dengan demikian, diferensial dari lnW ({ns}) menjadi
δlnW ∼=δNlnN −δN +δ
M
X
s=1
{nslngs−nslnns+ns}
= 0−0 +
M
X
s=1
{δnslngs+nsδlngs−δnslnns−nsδlnns+δns}
=
M
X
s=1
δnslngs+ns×0−δnslnns−ns
1
ns
δns
+δns
=
M
X
s=1
{δnslngs−δnslnns}
=
M
X
s=1
{lngs−lnns}δns
= M X s=1 ln gs ns δns (2.8)
Karena kita harus menerapkan syarat batas kekekalan energi dan jumlah partikel, maka solusi untuk ns dicari dengan menggabungkan persamaan
(2.4), (2.5), dan (2.8). Penggabungan tersebut dilakukan dengan menerap-kan pengali Langrangesebagai berikut
δlnW({ns}) +αδN+βδU = 0 (2.9)
Substitusi persamaan (2.4), (2.5), dan (2.8) ke dalam persamaan (2.9) diper-oleh M X s=1 ln gs ns
δns+α M
X
s=1
δns+β M
X
s=1
yang dapat disederhanakan menjadi
M
X
s=1
ln
gs
ns
+α+βEs
δns= 0 (2.10)
Karena kondisi ini berlaku untuk nilainsberapapun maka persamaan (2.10)
dijamin nol asal tiap suku dalam tanda sumasi berharga nol, atau
ln
gs
ns
+α+βEs= 0
ln
gs
ns
=−α−βEs
gs
ns
= exp (−α−βEs)
yang menghasilkan ungkapan untukns sebagai berikut
ns=gsexp (α+βEs) (2.11)
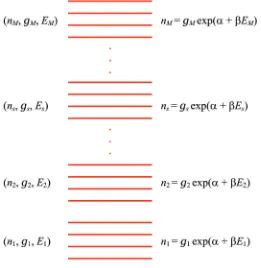
Jadi konfigurasi yang memiliki peluang kemunculan paling besar adalah yang memiliki jumlah sistem pada tiap kelompok energi yang memenuhi persamaan (2.11). Gambar 2.5 adalah ilustrasi yang menggambarkan jum-lah partikel yang menempati berbagai kelompok energi.
2.3
Harga Rata-Rata
Banyak sekali yang diperbolehkan ketika menempatkanN sistem ke dalam
M kelompok energi. Contoh konfigurasi tersebut adalah semua sistem men-empati kelompok energi pertama sedangkan semua kelompok energi lainnya kosong, atau semua kelompok ditempati oleh sistem dalam jumlah yang sama banyak, dan sebagainya. Tiap konfigurasi memiliki peluang kemuncu-lan yang berbeda-beda. Peluang kemuncukemuncu-lan terbesar terjadi pada konfig-urasi yang mengandung sistem pada tiap kelompok energi yang memenuhi persamaan (2.11).
2.3 Harga Rata-Rata 17
Gambar 2.5: Jumlah partikel yang menempati tiap kelompok energi.
Perlu diperhatikan di sini bahwa jumlah konfigurasi yang mungkin tidak sama dengan jumlah sistem atau jumlah kelompok energi dalam assembli. Nilai rata-rata X memenuhi hubungan
hXi=
X(konfig−1)P(konfig−1) +X(konfig−2)P(konfig−2) +· · · +X(konfig−R)P(konfig−R) /
P(konfig−1) +P(konfig−2) +...
+P(konfig−R)
=
R
P
t=1
X(konfig−t)P(konfig−t)
R
P
t=1
P(konfig−t)
(2.12)
Tabel 2.2: Nilai X beserta probabilitas kemunculannya Konfigurasi ke-i Nilai X Probabilitas kemunculan
1 X(konfig−1) P(konfig−1) 2 X(konfig−2) P(konfig−2)
..
. ... ...
t X(konfig−t) P(konfig−t) ..
. ... ...
R X(konfig−R) P(konfig−R)
dengan probabilitas maksimum, memiliki nilai yang jauh lebih besar daripa-da probabilitas konfigurasi-konfigurasi lainnya, maka perhitungan menjadi sangat sederhana. Misalkan P(konfig−t) = Pmaks dan terpenuhi
syarat-syarat berikut ini:
P(konfig−1)<< Pmaks P(konfig−2)<< Pmaks
.. .
P(konfig−R)<< Pmaks
maka
X(konfig−1)P(konfig−1) +X(konfig−2)P(konfig−2) +...
+X(konfig−R)P(konfig−R)∼=X(konfig−maks)Pmaks
dan
P(konfig−1) +P(konfig−2) +...+P(konfig−R)∼=Pmaks
Dengan demikian
hXi ∼= X(konfig−maks)Pmaks
Pmaks
=X(konfig−maks) (2.13)
2.4 Nilai Peluang Konfigurasi Maksimum 19
2.4
Nilai Peluang Konfigurasi Maksimum
Yang menjadi pertanyaan kita adalah benarkah probabilitas dengan mak-simum memiliki nilai yang sangat besar daripada konfigurasi lainnya. Jika ya, berarti kita dapat menggunakan persamaan (2.13) bahwa nilai rata-rata sifat assembli sama dengan nilai pada konfigurasi maksimum. Namun ji-ka tidak maji-ka penyederhanaan yang kita impiji-kan tidak terwujud. Pada bagian ini kita akan perlihatkan bahwa probabilitas konfigurasi maksimum benar-benar memilkiki nilai yang jauh lebih besar daripada konfigurasi lain-nya. Mari kita uraikan lnW di sekitar lnWmaks menggunakan deret Taylor
sebagai berikut
lnW = lnWmaks+
M
X
s=1 dlnW
dns
ns,maks
δns +1 2 M X s,q
∂2lnW ∂ns∂nq
ns,maksnq,maks
δnsδnq+...
(2.14)
Karena W hanya fungsi variablens saja maka
∂2lnW ∂ns∂nq =δs,q
d2lnW dn2
s
(2.15)
denganδs,q adalah deltaKroneckeryang memenuhiδs,q = 1 jikas=q dan
δs,q = 0 jika s 6= q. Dengan demikian kita dapatkan bentuk aproksimasi
untuk lnW sebagai berikut
lnW = lnWmaks+
M
X
s=1 dlnW
dns
ns,maks
δns + 1 2 M X s,q δs,q
d2lnW dn2
s
ns,maksnq,maks
δnsδnq+...
= lnWmaks+
M
X
s=1 dlnW
dns
ns,maks
δns + 1 2 M X s
d2lnW dn2
s
ns,maks
δn2s+...
Pada titik maksimum terpenuhi
M
X
s=1 dlnW
dns
ns,maks
δns= 0 (2.17)
sehingga persamaan (2.16) menjadi
lnW = lnWmaks+
1 2
M
X
s
d2lnW dn2
s
ns,maks
δn2s+... (2.18)
Dengan menggunakan persamaan (2.7) kita akan dapatkan
dlnW dns
=
M
X
s=1
(lngs−lnns)
d2lnW dnsdnq
=
M
X
s=1
dlngs
dnq −
dlnns
dnq = M X s=1
0− 1
ns dns dnq = M X s=1
0− 1
ns
δs,q
=−1
nq
atau
d2lnW dnsdns
= d
2lnW dn2
s
=− 1
ns
(2.19)
Dengan demikian persamaaan (2.18) dapat ditulis menjadi
lnW −lnWmaks=
1 2
M
X
s
−n1
s
δn2s+...
ln
W Wmaks
=−1 2 M X s δns ns 2
ns+...
2.4 Nilai Peluang Konfigurasi Maksimum 21
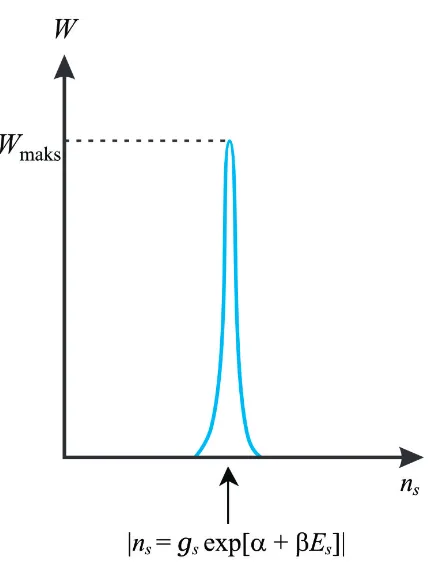
Gambar 2.6: Variasi jumlah cara menempatkan sistem terhadap konfigurasi penyusunan sistem dalam tingkat-tingkat energi assembli.
Jika kita asumsikan bahwa untuk semua nilai s, penyimpangan jumlah sistem pada tiap kelompok energi terhadap jumlah sistem dalam konfigurasi maksimum bernilai sama maka
δns
ns
∼
=ξ
sehingga diperoleh
ln
W Wmaks
=−1 2
M
X
s
ξ2ns+...
ln
W Wmaks
=−1 2ξ
2
M
X
s
ns=−1
2ξ
atau
W Wmaks
∼
= exp −ξ2N/2
(2.21)
Persamaan (2.21) dapat diilustrasikan pada Gbr. 2.6.
Sebagai ilustrasi, misalkan rasio deviasi jumlah sistem pada tiap-tiap kelompok energi terhadap jumlah pada konfigurasi maksimum adalah ξ = 10−10. Dengan rasio ini maka|n
s−gsexp[α+βEs]| ≈10−10untuk semuas
dari 1 sampaiM. Ini adalah rasio penyimpangan yang sangat kecil. Jumlah sistem dalam suatu assembli seorde dengan bilangan Avogadro, atau N ≈
1023. Dengan nilai ini maka
W Wmaks
∼
= exp −10−20×1023/2
= exp(−500)≈0
Jadi dengan rasio deviasiξ = 10−10kali konfigurasi maksimum, probabilitas
peluang konfigurasi tersebut hampir nol. Hal ini membuktikan bahwa nilai sifat assembli pada konfigurasi maksimum sama dengan nilai rata-rata sifat assembli.
Soal Latihan
1. Dari persamaan distribusi Maxwell-Boltzmann,ns=gsexp[α+βEs]
a) Jelaskan apa yang direpresentasikan olehns,gs, dan Es.
b) Buktikan bahwa parameterβ harus berharga negatif. 2. Buktikan bahwa parameterαdapat ditulisα= ln{N/P
gsexp[βEs]}.
Bab 3
Ruang Fasa
Isi Bab ini. Bab ini berisi diskusi tentang ruang fasa, yaitu ruang yang mengandung koordinat posisi dan momentum. Keadaan gerak sebuah ben-da sebenarnya lebih lengkap dinyatakan ben-dalam koordinar ruang fasa karena koordinat tersebut sekaligus memberikan informasi tentang posisi dan mo-mentum partikel sekaligus.
Tujuan Bab ini. Tujuan bab ini adalah mahasiswa memahami apa itu ruang fasa, bagaimana mencari volume ruang fasa, dan menentukan kerap-atan keadaan dalam ruang fasa. Mahasiswa juga mahir dalam melakukan transformasi kerapatan keadaan dari variable momentum ke variable energi.
Apa yang Perlu Dikuasai Lebih Dahulu. Tidak ada pengetahuan pendahuluan yang lebih khusus untuk memahami isi bab ini.
3.1
Definisi Ruang Fasa
Sebelum masuk lebih jauh untuk mencari besaran-besaran fisis suatu assem-bli, mari kita diskusikan satu jenis ruang yang dinamakan ruang fasa. Ruang fasa adalah ruang yang dibentuk oleh ruang spasial dan ruang momentum atau ruang spasial dan ruang kecepatan. Kita perlu memahami ruang fasa karena sebenarnya keadaan sistem statistik yang telah dan akan kita bahas adalah keadaan sistem tersebut dalam ruang fasa.
memerlu-kan informasi tentang kecepatan partikel tersebut. Kecepatan partikel dapat didefinisikan dengan lengkap oleh tiga koordinat kecepatan, yaituvx,vy,dan
vz. Dengan demikian, dinamika sebuah partikel dapat dijelaskan secara
lengkap oleh enam buah koordinat, yaitu tiga koordinat ruang: x,y, dan z, serta tiga koordinat kecepatan: vx,vy, danvz. Kita dapat menggabungkan
enam koordinat tersebut dalam satu ungkapan, yaitu (x, y, z, vx, vy, vz).
Karena momentum merupakan perkalian massa dan kecepatan, yaitu
~
p = m⇀v maka alternatif lain untuk mendeskripsikan dinamika partikel se-cara lengkap adalah memberikan tiga koordinat spasial dan tiga koordinat momentum. Sumbu koordinat ruang fasa tersebut dapat digambarkan se-cara skematik seperti pada Gbr. 3.1. Dalam deskripsi ini, dinamika partikel dapat dijelaskan dengan lengkap jika tiga koordinat spasial dan tiga koor-dinat momentum dapat ditentukan. Keenam koorkoor-dinat tersebut digabung dalam satu ungkapan (x, y, z, px, py, pz).
Gambar 3.1: Ilustrasi koordinat ruang fasa.
3.2 Elemen volume Ruang Fasa 25
3.2
Elemen volume Ruang Fasa
Jika ruang fasa dibangun oleh ruang spasial tiga dimensi dan ruang momen-tum tiga dimensi maka:
❼ Elemen volume ruang spasial adalah: dVs=dxdydy
❼ Elemen volume ruang momentum adalah: dVp=dpxdpydpz
❼ Elemen volume ruang fasa menjadi: dΓ =dVsdVp =dxdydzdpxdpydpz
Jika ruang fasa dibangun oleh ruang spasial dua dimensi dan ruang mo-mentum dua dimensi maka:
❼ Elemen volume ruang spasial adalah: dSs=dxdy
❼ Elemen volume ruang momentum adalah: dSp =dpxdpy
❼ Elemen volume ruang fasa menjadi: dΓ =dSsdSp=dxdydpxdpy
Ruang ini digunakan untuk mendeskripsikan keadaan partikel yang bergerak pada bidang.
Jika ruang fasa dibangun oleh ruang spasial satu dimensi dan ruang momentum satu dimensi maka:
❼ Elemen volume ruang spasial adalah: dXs=dx
❼ Elemen volume ruang momentum adalah: dPp=dpx
❼ Elemen volume ruang fasa adalah: dΓ =dXsdPp =dxdpx
Ruang ini digunakan untuk mendeskripsikan keadaan partikel yang bergerak pada kawat tipis atau tabung tipis.
3.3
Energi Kinetik
Tinjau elemen kecil volume dalam ruang fasa yang dibatasi oleh koordinat-koordinat berikut ini:
❼ Antarax sampaix+dx
❼ Antaray sampai y+dy
❼ Antaraz sampaiz+dz
❼ Antarapx sampaipx+dpx ❼ Antarapy sampai py+dpy ❼ Antarapz sampaipz+dpz
Volume ruang fasa elemen tersebut adalah
dΓ =dxdydzdpxdpydpz (3.1)
Di dalam elemen volume tersebut, komponen momentum partikel adalah
px,py, danpz. Dengan demikian, energi kinetik partikel yang berada dalam
elemen volume tersebut adalah
E= 1 2mv
2
= 1 2m v
2
x+v2y+vz2
= 1 2m
[mvx]2+ [mvy]2+ [mvz]2
= 1 2m p
2
x+p2y+p2z
(3.2)
3.4
N
Sistem dalam Ruang Fasa
N Sistem dalam Ruang Fasa
Di atas kita bahas hanya satu sistem dalam ruang fasa. Bagaimana jika terdapatN sistem? Tiap sistem akan memiliki 6 koordinat fasa yang bebas yang terdiri dari 3 koordinat ruang dan 3 koordinat momentum.
3.4 N Sistem dalam Ruang Fasa 27
❼ Koordinat sistem kedua (x2, y2, z2, p2x, p2y, p2z)
.. .
❼ dan seterusnya
Jika sistem pertama berada pada elemen volume yang dibatasi oleh koor-dinat-koordinat berikut ini
❼ Antara x1 sampaix1+dx1
❼ Antara y1 sampai y1+dy1
❼ Antara z1 sampai z1+dz1
❼ Antara p1x sampaip1x+dp1x ❼ Antara p1y sampai p1y +dp1y ❼ Antara p1z sampai p1z+dp1z
maka volume elemen ruang fasa yang menjadi lokasi sistem tersebut adalah
dΓ1 =dx1dy1dz1dp1xdp1ydp1z
Dengan cara yang sama maka akan kita peroleh elemen volume ruang fasa yang ditempati sistem kedua adalah
dΓ2 =dx2dy2dz2dp2xdp2ydp2z
dan seterusnya. Dari hasil ini maka kita dapatkan elemen total ruang fasa yang ditempati oleh buah sistem adalah
dΓ =dx1dy1dz1dp1xdp1ydp1zdx2dy2dz2dp2xdp2ydp2z
· · ·dxNdyNdzNdpN xdpN ydpN z
=
N
Y
i=1
dxidyidzidpixdpiydpiz
=
N
Y
i=1 dΓi
Di dalam elemen ruang fase tersebut, energi masing-masing sistem adalah
E1 = 1 2m p
2
1x+p21y +p21z
E2 =
1 2m p
2
2x+p22y +p22z
EN =
1 2m p
2
N x+p2N y+p2N z
Dengan demikian energi totalN sistem yang menempati ruang fasa dalam persaman (3.3) adalah
E =E1+E2+...+EN
=
N
X
i=1 Ei
=
N
X
i=1
1 2m p
2
ix+p2iy+p2iz
(3.4)
3.5
Menghitung Jumlah Keadaan
Pada penurunan fungsi distribusi kita sudah membagi energi atas kelompok-kelompok energi dari kelompok-kelompok ke-1 hingga kelompok-kelompok ke-M. Tinjau sebuah sistem dengan energiE= (p2
x+p2y+p2z)/2m. Penulisan energi di atas dapat
dibalik sebagai berikut
p2x+p2y+p2z =√2mE2 (3.5)
Bandingkan persamaan (3.5) dengan persamaan untuk bola berikut ini
X2+Y2+Z2=R2 (3.6)
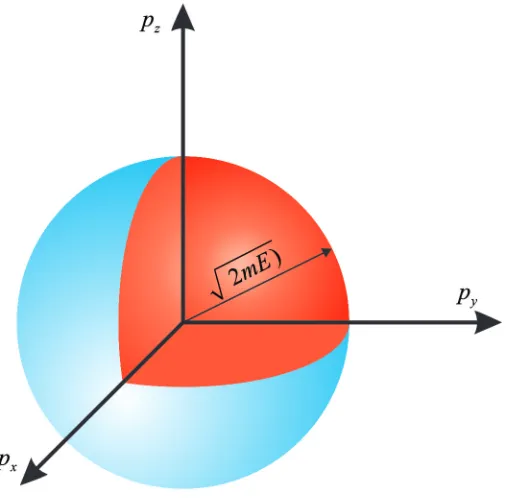
Persamaan (3.5) dan (3.6) persis sama. Pada persamaan (3.5), yang berperan sebagai jari-jari adalah √2mE (Gbr. 3.2). Ini berarti, dalam ko-ordinat momentum, nilai-nilaipx,py, danpz yang memberikanE yang
3.5 Menghitung Jumlah Keadaan 29
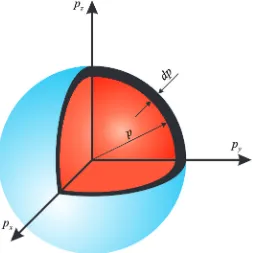
Gambar 3.2: Bola pada ruang momentum. Jari-jari bola adalah√2mE.
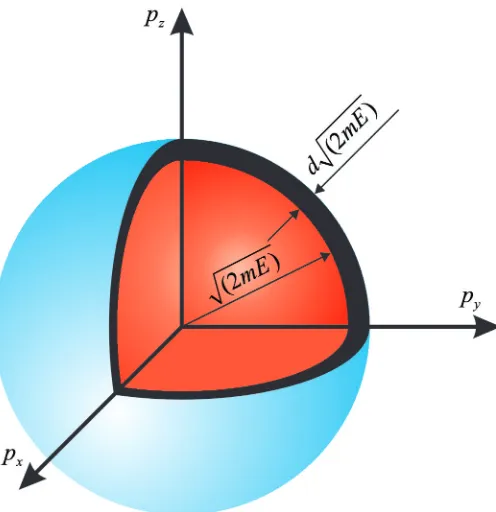
Jika kita bagi energi assembli atas kelompok-kelompok energi maka tiap kelompok akan diwakili oleh kulit bola dengan ketebalan tertentu. Mari kita ambil elemen volume pada kulit bola dengan jari-jari √2mE dan ketebalan
d(√2mE) (Gbr. 3.3). Luas kulit bola tersebut adalah
Sp = 4π
√
2mE2 = 8πmE (3.7)
Tebal kulit bola adalah
d√2mE=√2m d√E
=√2m×1
2E
−1/2dE
=
√
2m
2 E
−1/2dE
Gambar 3.3: Elemen volume dalam ruang momentum berupa kulit bola.
Dengan demikian, volume kulit bola adalah
dVp =Spd
√
2mE
= 8πmE
√
2m
2 E
−1/2dE
= 2π(2m)3/2E1/2dE
(3.9)
Volume ruang fasa yang ditempati oleh sistem yang berada pada kulit bola momentum serta dalam elemen volume spasialdVs=dxdydz adalah
dΓ =dxdydz2π(2m)3/2E1/2dE (3.10)
mengin-3.6 Menentukan ns 31
tegralkan persamaan (3.10) pada elemen ruang spasial. Hasilnya adalah
∆Γp =
Z
dxdydz2π(2m)3/2E1/2dE
= 2πV(2m)3/2E1/2dE
(3.11)
dengan V = R
dxdydz adalah volume total ruang spasial yang tidak lain merupakan volume assembli itu sendiri.
Kita belum mengetahui berapa kerapatan keadaan dalam ruang fasa. Untuk sementara kita menganggap kerapatan keadaan tersebut adalah B. Jumlah keadaan dalam elemen ruang fasa ∆Γp sama dengan volume ruang
fasa dikali kerapatannya, yaitu
B∆Γp = 2πV B(2m)3/2E1/2dE (3.12)
Persamaan (3.12) mirip dengan persamaan untuk mencari massa dengan mengalikan rapat massa dan volume. Jika kelompok-kelompok energi yang kita bangun di dalam assembli diwakili oleh kulit bola maka kita dapat menyamakan dalam persamaan (2.11) denganB∆Γp pada persamaan (3.12).
Akhirnya, kita dapatkan ungkapan untukgs sebagai
gs= 2πV B(2m)3/2E1/2dE (3.13)
3.6
Menentukan
n
sSetelah mengetahui bentuk gs dalam fungsi kontinu yaitu yang tertuang
dalam persamaan (3.13), selanjutnya kita akan menentukan ns dalam
ben-tuk kontinu juga. Dalam benben-tuk diskrit, hubungan antarans dan gs adalah
ns = gsexp [α+Es]. Pada hubungan ini, n s menyatakan jumlah sistem.
Sekarang kita mendefisikan karapat sistem, yaitu jumlah sistem per satu-an energi. Untuk kerapatsatu-an sistem kita gunaksatu-an symbol n(E). Dengan demikian, jumlah sistem dalam kulit bola yang dibatasi oleh energi E dan
E+dE adalahn(E)dE. Dengan mengganti ns dengann(E)dEdan gs
den-gan persamaan (3.13) kita dapatkan hubunden-gan antara jumlah sistem dan kerapatan keadaan dalam bentuk kontinu sebagai berikut
n(E)dE= 2πV B(2m)3/2E1/2dE ×eα+βE
3.7
Elemen Ruang Fasa dalam Momentum/Laju
Persamaan (3.11) menyatakan elemen volume ruang fasa dinyatakan dalam variabel energi. Kita juga dapat menyatakan elemen volume tersebut dalam variabel momentum atau laju. Kita mulai dari hubungan E = p2/2m
se-hingga
E1/2 =
1 2m
1/2
p (3.15)
dE = 1
mpdp (3.16)
Substitusi persamaan (3.15) dan (3.16) ke dalam persamaan (3.11) diperoleh ungkapan elemen ruang fasa dinyatakan dalam momentum sebagai berikut.
∆Γp = 2πV(2m)3/2×
1 2m
1/2 p× 1
mpdp
= 4πV p2dp
(3.17)
Mengingat hubungan antara momentum dan laju p = mv maka dp =
mdv. Konsekuensinya, kita dapat menulis elemen ruang fasa dalam koordi-nat laju sebagai berikut,
∆Γv= 4πV(mv)2(mdv)
= 4πV m3v2dv (3.18)
Dengan menggunakan persamaan (3.18) maka kita dapatkangs=B∆Γp =
4πBV m3v2dv dan kerapatan keadaan menjadi n(v)dv= gseα+βE
= 4πBV m3v2dv×eα+β(mv2/2)
= (4πBV m3eα)v2eβmv2/2dv
(3.19)
Hasil yang kita peroleh di atas akan sering kita jumpai pada bab-bab berikut-nya, khususnya saat melakukan transformasi dari penjumlahan diskrit ke integral kontinu.
Soal Latihan
3.7 Elemen Ruang Fasa dalam Momentum/Laju 33
2. Sebuah assembli mengandung N sistem. Ada berapa koordinat ruang fasa yang diperlukan untuk menggambar assembli tersebut?
3. Berapa energi kinetik suatu sistem yang memiliki koordinat ruang fasa antara (x, y, z, px, py, pz) sampai (x+dx, y+dy, z+dz, px+dpx, py+
dpy, pz+dpz).
4. Misalkan kerapatan keadaan dalam ruang fasa adalahB, berapa jum-lah keadaan dalam elemen ruang fasa antara (px, py, pz) sampai (px+
dpx, py +dpy, pz+dpz) pada seluruh ruang spasial.
Bab 4
Parameter-Parameter
Statistik
Isi Bab ini. Bab ini berisi penentuan parameter α dan β yang terdapat dalam fungsi distribusi Maxwell-Boltzmann. Parameter-parameter terse-but telah diperkenalkan untuk mengakomodasi hukum kekekalan energi dan jumlah partikel yang dimiliki assembli.
Tujuan Bab ini. Tujuan bab ini adalah mahasiswa memahami bagaimana menentukan parameterαdan β dalam fungsi distribusi Maxwell-Boltzmann dan alasan-alasan yang digunakan dalam proses penentuan parameter-para-meter tersebut.
Apa yang Perlu Dikuasai Lebih Dahulu. Pemahaman tentang isi Bab 2 dan Bab 3 sangat penting untuk mengikuti penjelasan dalam bab ini. Juga pemahaman tentang konsep entropi yang dipelajari di termodinami-ka serta dasar prinsip ekipartisi energi yang dipelajari pada gas ideal juga sangat membantu dalam memahami isi bab ini.
4.1
Menentukan Parameter
β
Sudah kita tunjukkan bahwa jumlah sistem yang menempati kelompok energi dengan energi rata-rata Es dan mengandung keadaan sebanyak gs
memenuhi persamaan (2.11) yaituns=gseα+βEs. Secara fisis kita meyakini
bahwa tidak mungkin ada sistem yang memiliki energi tak berhingga. Oleh karena itu jikaEs→ ∞maka haruslahns →0. Ini hanya mungkin terpenuhi
jikaparameterβ bernilai negatif. Lalu,bergantung pada besaran apakah parameter β?
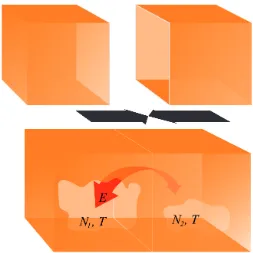
Gambar 4.1: Dua buah assembli terisolasi digabung setelah membuka masing-masing satu sisinya. Pada batas dua assembli diijinkan pertukaran energi tetapi tidak diijinkan pertukaran partikel.
Setelah mengetahui bahwa nilai parameter β harus negatif mari kita mencari bentuk ekspresi dari parameter tersebut. Untuk mempermudah mari kita tinjau dua assembli terisolasi dan berada pada suhu yang sama
T. Kesamaan suhu bermakna bahwa kedua assembli berada dalam kesetim-bangan termal. Assembli pertama memiliki N1 sistem dan assembli kedua
4.1 Menentukan Parameter β 37
Setelah dikontakkan dua assembli menjadi sebuah assembli baru yang tetap terisolasi dari lingkungan. Misalkan pada permukaan kontak dua assem-bli dipasang dinding sedemikian rupa sehingga tidak ada pertukaran sistem antara dua assembli namun pertukaran energi diperbolehkan. Akibatnya, sebelum dan sesudah dua assembli disatukan, jumlah partikel di assembli kiri maupun assembli kanan tidak berubah. Tetapi energi yang dimiliki masing-masing assembli awal bisa berubah (lihat Gbr. 4.1).
Karena assembli gabungan terisolasi dari lingkungan maka pertukaran energi antar dua assembli awal tidak mengubah energi total assembli gabun-gan. Dengan persyaratan di atas kita dapatkan beberapa konstrain berikut ini
N1= X
s
n1s= konstan (4.1)
N2= X
s
n2s= konstan (4.2)
U =U1+U2= X
s
n1sE1s+
X
s
n2sE2s = konstan (4.3)
Apabila kita nyatakan dalam bentuk diferensial, persamaan (4.1) sampai (4.3) berbentuk
δN1 =X
s
δn1s= 0 (4.4)
δN2 = X
s
δn2s= 0 (4.5)
δU =X
s
E1sδn1s+
X
s
E2sδn2s= 0 (4.6)
Sebelum ke dua assembli digabung maka jumlah penyusunan sistem pada keadaan-keadaan energi di masing-masing assembli memenuhi persamaan (2.3), yaitu
W1 =N1! Y
s
gn1s
1s
n1s!
(4.7)
W1 =N2!Y
s
gn2s
2s
n2s!
(4.8)
Ketika dua assembli digabung maka probabilitas penyusunan sistem-sistem pada assembli gabungan tersebut merupakan perkalian probabilitas penyusunan pada masing-masing assembli awal, yaitu
atau bila diungkapkan dalam notasi logaritma menjadi
lnW = lnW1+ lnW2 (4.9)
Kita akan mencari konfigurasi dengan probabilitas maksium dengan mem-perhatikan tiga konstrain pada persamaan (4.4) sampai (4.6). Ini men-syaratkan pengenalan tiga pengali Langrange α1,α2, danβ. Syarat
maksi-mum memenuhi persamaan
δlnW +α1δN1+α2δN2+βδU = 0 (4.10)
Dengan menggunakan persamaan (4.9) maka
δlnW =δlnW1+δlnW2
=X
s
∂lnW1 ∂n1s
δn1s+
X
s
∂lnW2 ∂n2s
δn2s (4.11)
Substitusi persamaan (4.4), (4.5), (4.6), dan (4.11) ke dalam persamaan (4.10) diperoleh
X
s
∂lnW1 ∂n1s
δn1s+
X
s
∂lnW2 ∂n2s
δn2s+α1 X
s
δn1s
+α2 X
s
δn2s+β
" X
s
E1sδn1s+
X
s
E2sδn2s
#
= 0
yang dapat disederhanakan menjadi
X
s
∂lnW1 ∂n1s
+α1+βE1s
δn1s+
X
s
∂lnW2 ∂n2s
+α2+βE2s
δn2s= 0
(4.12) Agar persamaan (4.12) selalu terpenuhi untuk variasiδn1s dan δn2s berapa
pun maka suku dalam kurung pada harus nol, atau
∂lnW1 ∂n1s
+α1+βE1s= 0 (4.13)
∂lnW2 ∂n2s
+α2+βE2s= 0 (4.14)
4.2 Bagaimana Kebergantungan β pada Suhu? 39
maka parameter yang menentukan β haruslah yang tidak berubah sebelum dan sesudah dua assembli digabung. Parameter tersebut hanya suhu!! Sebelum dan sesudah dua assembli digabung suhunya sama. Jadi kita simpulkan bahwa β hanya merupakan fungsi suhu, atau
β =β(T) (4.15)
4.2
Bagaimana Kebergantungan
β
pada Suhu?
Setelah kita mengetahui bahwa β merupakan fungsi suhu maka langkah se-lanjutnya adalah menentukan kebergantungan β terhadap suhu secara ek-splisit. Untuk maksud mari kita lihat assembli pada Gbr. 4.2 berikut ini. Di dalam assembli kita letakkan sebuah pemanas yang dapat mensuplai kalor ke dalam assembli.
Gambar 4.2: Kalor disuplai ke dalam assembli.
dU =dQ−pdV (4.16) Karena ada kemungkinan volume assembli berubah ketika menyerap kalor maka tingkat energi dalam assembli juga mungkin berubah. Akibatnya, en-ergi rata-rata sistem dalam satu kelompok enen-ergi, yaitu Es, juga mungkin
berubah sehingga secara umum terpenuhi δEs 6= 0. Dengan demikian.
Mengingat U = P
s
nsEs maka secara umum dalam bentuk diferensial dari
U adalah
δU =X
s
Esδns+
X
s
nsδEs (4.17)
Bagaimana hubungan persamaan (4.16) dan (4.17)? Masih ingat pela-jaran fisika modern saat membahas partikel kuantum yang terperangkap dalam kotak (sumur potensial)? Di situ dibahas bahwa tingkat energi par-tikel dalam kotak bergantung pada ukuran kotak. Makin besar ukuran kotak maka tingkat-tingkat energi makin rapat dan menjadi kontinu ketika ukuran kotak menuju tak berhingga (Gbr. 4.3). Khusus untuk kotak satu dimen-si, energi tiap tingkat energi memenuhi Ei ∝ i2/L di mana iadalah indek
keadaan (bilangan kuantum) dan L adalah lebar kotak. Kelakuan serupa juga dapat diterapkan di sini.
Ketika dalam assembli disuplai kalor, perubahan tingkat energi dalam assembli semata-mata disebabkan perubahan ukuran spasial assembli. Jadi, perubahan tingkat energi dalam assembli, yaituδEs merupakan kontribusi
dari perubahan ukuran assembli. Dengan demikian, korelasi antara per-samaan (4.16) dan (4.17) menjadi sebagai berikut:
❼ Suku pertama pada persamaan (4.17) merupakan kontribusi dari pem-berian kalor
❼ Suku kedua dalam persamaan (4.17) merupakan kontribusi dari pe-rubahan volume assembli.
Dengan demikian kita dapat mengambil kesimpulan berikut ini
X
s
Esδns =δQ (4.18)
X
s
4.2 Bagaimana Kebergantungan β pada Suhu? 41
Gambar 4.3: Pada kotak kecil, jarak antar tingkat energi lebar sedangkan pada kotak besar jarak antar tingkat energi sempit.
Jika kita menganggap bahwa dinding assembli sangat tegar sehingga tidak terjadi perubahan volume pada saat penyerapan kalor δQ maka
δU =δQ (4.20)
Dengan demikian, syarat konfigurasi dengan probabilitas maksimum menja-di
δlnW +αδN+βδQ= 0 (4.21)
Untuk assembli yang terisolasi, jumlah sistem tidak berubah sehingga
δN = 0. Akibat dari pembatasan tersebut maka persamaan (4.21) menjadi
δlnW +βδQ= 0 atau
sudah dibahas bahwa δQ bisa diubah menjadi diferensial sejati jika dibagi dengan suhu. Jadi, walaupunδQbukan diferensial sejati tetapiδQ/T meru-pakan diferensial sejati. Di termodinamika dibahas bahwaδQ/T merupakan sebuah besaran termodinamika yang bernama entropi. Dengan demikian, agar ruas kanan persamaan (4.22) menjadi diferensial sejati maka haruslah
β ∝ 1/T. Dan karena kita menunjukkan bahwa β berharga negatif, maka bentuk umumβ sebagai fungsi suhu manjadi
β =− 1
kT (4.23)
dengan k sebuah konstanta. Nanti akan kita buktikan bahwa k tidak lain daripada konstanta Boltzmann.
4.3
Menentukan
β
dari Energi Rata-Rata
Cara lain menentukan parameterβ adalah menggunakan konsep energi rata-rata yang diturunkan menggunakan teori kinetik gas ideal. Satu atom atau molekul gas yang hanya melakukan gerak translasi dalam tiga arah koordinat ruang memiliki energi kinetik rata-rata
¯
E= 3
2kT (4.24)
denganT suhu mutlak dankkonstanta Boltzmann. Kita bisa mendapatkan energi rata-rata tersebut dengan menggunakan kosep kerapatan keadaan yang telah kita pelajari pada bab terdahulu. Mari kita lakukan di sini. Dalam Bab 3 kita sudah menurunkan jumlah partikel yang berada dalam jangkauan energi antaraE sampaiE+dE adalah
4.3 Menentukan β dari Energi Rata-Rata 43
Energi rata-rata partikel dapat dinyatakan dalam bentuk
E =
∞
R
0
En(E)dE
∞
R 0
n(E)dE
=
∞
R
0
E×2πV B(2m)3/2eα+βEE1/2dE
∞
R
0
2πV B(2m)3/2eα+βEE1/2dE
=
2πV B(2m)3/2eαR∞ 0
eβEE3/2dE
2πV B(2m)3/2eαR∞ 0
βEE1/2dE
=
∞
R 0
eβEE3/2dE
∞
R
0
βEE1/2dE
(4.25)
Mari kita selesaikan integral pada pada persamaan (4.25) dengan meli-hat pembilang terlebih dahulu. Untuk menyelesaikan integral tersebut kita misalkan
eβEdE=dx (4.26a)
E3/2 =y (4.26b)
Dengan melakukan integral pada dua sisi persamaan (4.26) diperoleh
x= 1
βe
βE
dan dengan melakukan diferensial pada persamaan (4.26b) diperoleh
dy= 3 2E
1/2dE
Selanjutnya kita gunakan aturan rantai untuk integral R
(4.25) sebagai
∞
Z
0
eβEE3/2dE=
1
βe
βEE3/2 ∞ 0 − ∞ Z 0 1 βe βE 3 2E
1/2dE
=
1
βe
β×∞∞3/2
−β1eβ×003/2
−23β
∞
Z
0
E1/2eβEdE
(4.27)
Karena β negatif maka eβ×∞ →0 dan menuju nol lebih cepat daripada membesarnya ∞3/2 sehingga perkalian eβ×∞∞3/2 → 0. Dengan sifat ini maka suku pertama di sisi kanan persamaan (4.27) yaitu yang berada di dalam kurung siku nilainya nol dan integral pembilang di persamaan (4.25) menjadi
∞
Z
0
eβEE3/2dE=− 3 2β
∞
Z
0
E1/2eβEdE (4.28)
Substitusi persamaan (4.28) ke dalam persamaan (4.25) didapatkan energi rata-rata sistem menjadi
¯
E=
∞
R 0
eβEE3/2dE
∞
R
0
βEE1/2dE
=− 3 2β
∞
R 0
eβEE1/2dE
∞
R
0
βEE1/2dE
=− 3 2β
Karena energi rata-rata ini harus sama dengan 3kT /2 maka−3/2β= 3kT /2 sehingga diperoleh ungkapan untukβ
β =− 1
kT
yang persis sama dengan persamaan (4.23). Hasil ini pun membuktikan bahwa konstanta k benar-benar merupakan konstanta Boltzmann karena berasal dari ungkapan energi rata-rata sistem.
4.4
Menentukan Parameter
α
Setelah mengetahui ungkapan untuk gs, kita siap menentukan parameter
4.4 Menentukan Parameter α 45
kita lakukan penjumlahan untuk semua syang mungkin
X
s
ns=
X
s
gseα+βEs =eα
X
s
gseβEs
Penjumlahan di ruas kiri adalah jumlah total sistem. Jadi
N =eαX
s
gseβEs (4.29)
Mari kita fokuskan pada suku penjumlahan di ruas kanan persamaan (4.29). Kita gantigs dengan bentuk kontinu yang diberikan oleh persamaan
(3.13). Penjumlahan selanjutnya diganti dengan integral pada semua jangkauan energi yang mungkin, yaitu dariE= 0 sampaiE =∞. Bentuk integral yang dimaksud adalah
N =eα
∞
Z
0
2πV B(2m)3/2eβEE1/2dE
= 2πV B(2m)3/2eα
∞
Z
0
eβEE1/2dE
(4.30)
Untuk menyelesaikan integral (4.30) mari kita mendefinisikanβE =−y
sehingga
E =−y
β (4.31a)
dE=−1
βdy (4.31b)
dan
E1/2 =
−y
β 1/2
=
−1
β 1/2
y1/2 (4.31c)
di ruas kanan persamaan (4.30) menjadi
∞
Z
0
eβEE1/2dE=
∞
Z
0 e−y
−β1
1/2 y1/2
−β1
dy = −1 β
3/2Z∞
0
e−yy1/2dy
=
−β1
3/2
Γ
3 2
di mana Γ(x) adalah fungsi gamma. Dapat dibuktikan secara analitik (walaupun agak panjang) dan juga sudah ditabelkan bahwa Γ (3/2) =√π/2 sehingga
∞
Z
0
eβEE1/2dE=
−β1
3/2√π
2 (4.32)
Akhirnya, substitusi persamaan (4.32) ke dalam (4.30) diperoleh
N = 2πV B(2m)3/2eα
−β1
3/2√ π
2 (4.33)
Karena kita sudah membuktikanβ=−1/kT maka
N = 2πV B(2m)3/2eα(kT)3/2
√
π
2 =V B(2πmkT)3/2eα
Dengan demikian parameterα memenuhi
eα = N
V B(2πmkT)3/2 atau
α= ln
"
N V B(2πmkT)3/2
#
(4.34)
4.5 Makna Parameter α 47
Gambar 4.4: Fungsi distribusi Maxwell-Boltzmann (kurva) dan hasil pengukuran untuk assembli gas cesium (simbol).
Substitusi persamaan (4.23) dan (4.34) ke dalam persamaan (3.17) kita dapatkan bentuk lengkap dari fungsi distribusi Maxwell-Boltzmann menjadi
n(v)dv = 4πBV m3 N
BV(2πmkT)3/2v
2e−mv2
2kT
= 4πN m
3/2
(2πkT)3/2v
2e−mv2
/2kT
(4.35)
Gambar 4.4 adalah pembuktian secara eksperimen fungsi distrubisi Max-well-Boltzmann untuk gas cesium. Gas dalam ruang dengan suhu tertentu dikeluarkan dari lubang kecil. Distribusi laju atom/molekul gas yang kelu-ar diukur dan dibandingkan dengan fungsi Maxwell-Boltzmann yang diplot pada suhu yang sama. Terdapat kesesuaian yang sangat baik antara hasil pengamatan dan prediksi teoretik.
4.5
Makna Parameter
α
ditem-pati satu sistem adalah N/V. Jika dianggap satu sistem menempati ruang berbentuk kubus dengan panjang sisi l maka volume kubus adalah l3 dan
memenuhil3 =V /N. Jika sistem menempati pusat kubus, maka jarak rata-rata antar sistem sama dengan panjang sisi kubus, yaitul.
Energi rata-rata sistem dalam ruang tiga dimensi adalah 3kT /2. Energi ini berasal dari energi kinetik sistem tersebut. Jadi
Energi kinetik rata-rata = ¯p2/2m= 3kT /2 atau
¯
p=√3mkT (4.36) Panjang gelombang de Broglie rata-rata yang dimiliki sistem adalah
¯
λ= h ¯
p
= √ h
3mkT
(4.37)
Dengan demikian, parameterα memenuhi
eα= N/V
Bh3(2π/3)3/2 (3mkT)3/2
h3
= 1/ℓ
3
Bh3(2π/3)3/2 1 ¯
λ3
= 1
Bh3(2π/3)3/2 ¯
λ ℓ
3
(4.38)
Tampak dari persamaan (4.38) bahwa nilai α bergantung pada rasio panjang gelombang de Broglie termal sistem dengan jarak rata-rata antar sistem. Pada suhu yang sangat rendah, momentum sistem sangat kecil se-hingga panjang gelombang de Broglie sangat besar. Akibatnyaeαjauh lebih besar dari satu. Sebaliknya, pada suhu sangat tinggi, momentum sistem san-gat besar sehingga panjang gelombang de Broglie sansan-gat kecil. Akibatnya, nilaieα jauh lebih kecil daripada satu.
Soal Latihan
1. Buktikan bahwa panjang gelombang termal de Broglie memenuhiλ=
4.5 Makna Parameter α 49
Bab 5
Statistik Bose-Einstein
Isi Bab ini. Bab ini berisi perumusan statistik Bose-Einstein untuk assem-bli boson, yaitu partikel kuantum dengan spin merupakan kelipatan bulat dari~=h/2π. Contoh partikel boson adalah foton, fonon, dan atom helium.
Tujuan Bab ini. Tujuan bab ini adalah mahasiswa memahami bagaimana proses membangun statistik Bose-Einstein dengan menggunakan prinsip statis-tik murni yang digabungkan dengan prinsip kekekalan dalam fisika seperti kekekalan energi dan jumlah partikel.
Apa yang Perlu Dikuasai Lebih Dahulu. Untuk memahami penu-runan fungsi distribusi Bose-Einsten mahasiswa perlu memahami prinsip permutasi untuk benda-benda yang tidak dapat dibedakan, sifat yang ditun-jukkan oleh sebuah besaran yang nilainya kekal (konstan), serta bagaimana mencari nilai maksimum dari sebuah fungsi. Pemahaman tentang penu-runan distribusi Maxwell-Boltzmann juga merupakan modal berharga untuk memahami penurunan distribusi Bose-Einstein secara lebih mudah.
5.1
Sifat Dasar Boson
ki-ta tidak dapat membedakan satu partikel dengan partikel lainnya. Dapat dibedakan di sini hanya dari sudut pandang teori (konsep). Jika ada dua partikel yang memiliki energi berbeda dipertukarkan maka kita menganggap akan mendapatkan penyusunan yang baru.
Kalau kita melangkah ke partikel sub atomik seperti proton dan elektron maka sifat dapat dibedakan menjadi hilang. Pertukaran dua partikel yang menempati tingkat energi berbeda tidak menghasilkan jenis penyusunan baru. Dikatakan partikel-partikel ini tidak terbedakan.
Sifat partikel sub atomik yang tidak dapat dibedakan dapat dipahami dari konsep gelombang partikel. Panjang gelombang de Broglie partikel-partikel tersebut memenuhi λ=h/mv denganm massa partikel dan v laju partikel. Karena m untuk partikel sub atomik sangat kecil maka panjang gelombang λ cukup besar. Panjang gelombang yang besar menyebabkan fungsi gelombang dua partikel yang berdekatan tumpang tindih (berimpi-tan). Kalau dua fungsi gelombang tumpang tindih maka kita tidak dapat lagi membedakan dua partikel yang memiliki fungsi-fungsi gelombang terse-but.
Kondisi sebaliknya dijumpai pada partikel klasik seperti molekul-molekul gas. Massa partikel sangat besar sehingga λsangat kecil. Akibatnya tidak terjadi tumpang tindih fungsi gelombang partikel-partikel tersebut, sehingga secara prinsip partikel-partikel tersebut dapat dibedakan.
Akan kita lihat nanti bahwa pada suhu yang sangat tinggi partikel sub atomik berperilaku seperti partikel klasik. Pada suhu yang sangat tinggi ke-cepatan partikel sangat besar sehingga panjang gelombangnya sangat kecil. Akibatnya, tumpang tindih gelombang partikel-partikel menjadi hilang dan partikel menjadi terbedakan.
5.2 Konfigurasi Boson 53
5.2
Konfigurasi Boson
Mari kita mulai dengan munurunkan statistik untuk boson. Statistik ini di-namakan statistik Bose-Einstein. Agar dapat menentukan fungsi distribusi Bose-Einstein, kita terlebih dahulu harus menentukan konfigurasi dengan probabilitas paling besar. Konfigurasi ini memiliki probabilitas yang jauh lebih besar daripada konfigurasi-konfigurasi lainnya sehingga hampir seluruh waktu sistem boson membentuk konfigurasi tersebut. Sifat rata-rata assem-bli dapat dianggap sama dengan sifat pada konfigurasi maksimum tersebut. Kita tetap membagi tingkat energi sistem-sistem dalam assembli atasM
kelompok sebagai berikut:
❼ Kelompok-1 memiliki jumlah keadaan g1 dan energi rata-rataE1
❼ Kelompok-2 memiliki jumlah keadaan g2 dan energi rata-rataE2
.. .
❼ Kelompok-s memiliki jumlah keadaangs dan energi rata-rataEs
.. .
❼ Kelompok-M memiliki jumlah keadaangM dan energi rata-rataEM
Kita akan menentukan berapa cara penyusunan yang dapat dilakukan jika:
❼ Adan1 sistem di kelompok-1
❼ Adan1 sistem di kelompok-2
.. .
❼ Adans sistem di kelompok-s
.. .
5.2 Konfigurasi Boson 55
Mari kita tinjau kelompok-1 di mana terdapatg1keadaan dann1sistem.
Mari kita analogikan satu keadaan sebagai sebuah kursi dan satu sistem di-analogikan sebagai sebuah benda yang akan diletakkan di kursi tersebut. Satu kursi dapat saja kosong atau menampung benda dalam jumlah berapa saja. Untuk menghitung jumlah penyusunan benda, kita dapat melakukan-nya sebagai berikut.
Dari Gbr 5.1, apa pun cara penyusunan yang kita lakukan, yang berada di ujung bawah selalu kursi karena benda harus disangga oleh kursi (sistem harus menempati tingkat energi). Oleh karena itu, jika jumlah total kursi adalah g1 maka jumlah total kursi yang dapat dipertukarkan hanyag1−1
karena salah satu kursi harus tetap di ujung bawah. Bersama dengan orang sebanyak n1, maka jumlah total benda yang dapat dipertukarkan dengan
tetap memenuhi sifat boson adalah (g1−1) +n1=g1+n1−1. Akibatnya,
jumlah cara penyusunan benda yang dilakukan adalah (g1+n1−1)!. Karena sistem boson tidak dapat dibedakan satu dengan lainnya, maka pertukaran sesama orang dan sesama kursi tidak menghasilkan penyusunan yang berbeda. Jumlah penyusunan sebanyak (g1+n1−1)! secara implisit
memperhitungkan jumlah pertukaran antar orang dan antar kursi. Jumlah pertukaran antar orang adalahn1! dan jumlah pertukaran antar kursi adalah
g1!. Oleh karena itu, jumlah penyusunan yang berbeda untuk n1 boson di
dalamg1 keadaan hanyalah
(g1+n1−1)!
n1!g1!
(5.1)
Hal yang sama berlaku untuk kelompok-2 yang mengandungg2 keadaan
dengan populasi n2 sistem. Jumlah cara penyusunan yang berbeda
sistem-sistem ke dalam keadaan-keadaan tersebut adalah
(g2+n2−1)! n2!g2!
(5.2)
Terakhir hingga kelompok energi ke-M, jumlah cara penyusunan yang berbe-da untuknM sistem dalamgM keadaan adalah
(gM +nM −1)!
nM!gM!
(5.3)
Akhirnya, jumlah total cara penyusunan yang berbeda secara bersamaann1
gM keadaan adalah
(g1+n1−1)!
n1!g1! ×
(g2+n2−1)!
n2!g2! ×
. . .×(gM +nM −1)! nM!gM!
=
M
Y
s=1
(gs+ns−1)!
ns!gs!
(5.4) Kita harus juga memperhitungkan jumlah cara membawaN sistem dari luar untuk didistribusikan ke dalam tingkat-tingkat energi di atas. Jumlah cara pengambilan N sistem adalah N! cara. Karena sistem tidak dapat dibedakan maka jumlah tersebut harus dibagi denganN!, sehingga jumlah total cara membawa N sistem ke dalam tingkat-tingkat energi di dalam assembli adalah N!/N! = 1. Akhirnya, kita dapatkan jumlah penyusunan sistem-sistem dalam assembli boson adalah
W =
M
Y
s=1
(gs+ns−1)!
ns!gs!
(5.5)
5.3
Konfigurasi Maksimum
Selanjutnya kita akan menentukan konfigurasi dengan peluang kemunculan paling besar. Ambil logaritma ruas kiri dan kanan persamaan (5.5)
lnW = ln
M
Y
s=1
(gs+ns−1)!
ns!gs!
= M X s=1 ln
(gs+ns−1)!
ns!gs!
= ln
M
X
s=1
ln (gs+ns−1)!−lnns!−lngs!
(5.6)
Kemudian kita gunakan pendekatan Stirling untuk melakukan penyeder-hanaan sebagai berikut
ln(gs+ns−1)!∼= (gs+ns−1) ln(gs+ns−1)−(gs+ns−1)
lngs!∼=gslngs−gs
lnns!∼=nslnns−ns
Dengan pendekatan tersebut maka persamaan (5.6) menjadi
lnW ∼=
M
X
s=1
[(gs+ns−1) ln(gs+ns−1)−(gs+ns−1)
−gslngs+gs−nslnns+ns]
5.3 Konfigurasi Maksimum 57
Jumlah total sistem serta energi total assembli memenuhi N = PM
s=1 ns
dan U = PM
s=1
nsEs. Untuk assembli yang terisolasi sehingga tidak ada
per-tukaran sistem maupun energi antara assembli dan lingkungan. Jumlah sis-tem maupun energi assembli konstanta. Pembatasan ini dapat dinyatakan dalam bentuk diferensial berikut ini
δN =
M
X
s=1
δns = 0 (5.8)
δU =
M
X
s=1
Esδns= 0 (5.9)
Konfigurasi dengan probabilitas maksimum diperoleh dengan memaksi-mumkan lnW. Dengan memperhatikan konstrain pada persamaan (5.8) dan (5.9) maka konfigurasi dengan probabilitas maksimum memenuhi
δlnW +αδN+βδU = 0 (5.10)
Selanjutnya dengan mengambil diferensial persamaan (5.7) kita peroleh
δlnW ∼=
M
X
s=1
[δ(gs+ns−1) ln(gs+ns−1)−δ(gs+ns−1)
−δgslngs+δgs−δnslnns+δns]
(5.11)
Mari kita hitung suku per suku yang terkandung dalam persamaan (5.11).
i)
δ(gs+ns−1) ln(gs+ns−1)
= ∂
∂ns
(gs+ns−1) ln(gs+ns−1)δns
=
ln(gs+ns−1) + (gs+ns−1)×
1 (gs+ns−1)
δns
ii)
δ(gs+ns−1) = ∂
∂ns
(gs+ns−1)δns =δns
iii)
δgslngs=
∂ ∂ns
gslngsδns= 0
iv)
δnslnns=
∂ ∂ns
nslnnsδns
=
lnns +ns×
1
ns
δns
= [lnns + 1]δns
Persamaan (5.11) selanjutnya menjadi
δlnW ∼=
M
X
s=1
[ln(gs+ns−1) + 1]δns−δns−0 + 0−[lnns+ 1]δns+δns
=
M
X
s=1
[ln(gs+ns−1)−lnns]δns
= M X s=1 ln
gs+ns−1
ns
δns
(5.12)
Karena gs >> 1 dan ns >> 1 maka gs+ns−1 ∼= gs+ns sehingga
persamaan (5.12) dapat disederhanakan lebih lanjut menjadi
δlnW =
M
X
s=1
ln
gs+ns
ns
δns (5.13)
Substitusi persamaan (5.8), (5.9), dan (5.13) ke dalam persamaan (5.10) diperoleh M X s=1 ln
gs+ns
ns
δns+α M
X
s=1
δns+β M
X
s=1
5.4 Parameter α untuk Photon dan P