STUDI PARAMETER KIMIA PERAIRAN BAGI PERUNTUKAN BUDIDAYA KERAMBA JARING APUNG (STUDI KASUS WADUK
BILIBILI ZONA II)
SKRIPSI
GUSRIANDI 105940048110
PROGRAM STUDI BUDIDAYA PERAIRAN FAKULTAS PERTANIAN
UNIVERSITAS MUHAMMADIYAH MAKASSAR
STUDI PARAMETER KIMIA PERAIRAN BAGI PERUNTUKAN BUDIDAYA KERAMBA JARING APUNG (STUDI KASUS WADUK
BILIBILI ZONA II)
GUSRIANDI
Skripsi sebagai salah satu syarat untuk memperoleh gelar sarjana pertanian pada jurusan
budidaya perairan.
PROGRAM STUDI BUDIDAYA PERAIRAN FAKULTAS PERTANIAN
UNIVERSITAS MUHAMMADIYAH MAKASSAR
LEMBAR PENGESAHAN
Judul : Studi Parameter Kimia Perairan Bagi Peruntukan Budidaya Keramba Jaring Apung (Studi Kasus Waduk Bilibili Zona II)
Nama : Gusriandi
Stambuk : 10594 00481 10
Program Studi : Budidaya Perairan (BDP) Fakultas : Pertanian
Makassar, Desember 2014
Telah Diperiksa dan Disetujui : Komisi Pembimbing
Ir. Darmawati, M.Si Ir. Andi Khaeriyah, M.Pd
Ketua Anggota
Diketahui :
Ir. H. Saleh Molla, M.M Murni, S.Pi, M.Si
Dekan Fakultas Pertanian Ketua Program Studi
LEMBAR PENGESAHAN
Judul : Studi Parameter Kimia Perairan Bagi Peruntukan Budidaya Keramba Jaring Apung (Studi Kasus Waduk Bilibili Zona II)
Nama : Gusriandi
Stambuk : 10594 00481 10
Program Studi : Budidaya Perairan (BDP) Fakultas : Pertanian
Makassar, Desember 2014
Telah Diperiksa dan Disetujui : Komisi Pembimbing
Ir. Darmawati, M.Si Ir. Andi Khaeriyah, M.Pd
Ketua Anggota
Diketahui :
Ir. H. Saleh Molla, M.M Murni, S.Pi, M.Si
Dekan Fakultas Pertanian Ketua Program Studi
LEMBAR PENGESAHAN
Judul : Studi Parameter Kimia Perairan Bagi Peruntukan Budidaya Keramba Jaring Apung (Studi Kasus Waduk Bilibili Zona II)
Nama : Gusriandi
Stambuk : 10594 00481 10
Program Studi : Budidaya Perairan (BDP) Fakultas : Pertanian
Makassar, Desember 2014
Telah Diperiksa dan Disetujui : Komisi Pembimbing
Ir. Darmawati, M.Si Ir. Andi Khaeriyah, M.Pd
Ketua Anggota
Diketahui :
Ir. H. Saleh Molla, M.M Murni, S.Pi, M.Si
Dekan Fakultas Pertanian Ketua Program Studi
HALAMAN PENGESAHAN KOMISI PENGUJI
Judul : Studi Parameter Kimia Perairan Bagi Peruntukan Budidaya Keramba Jaring Apung (Studi Kasus Waduk Bilibili Zona II)
Nama : Gusriandi
NIM : 10594 00481 10
Program Studi : Budidaya Perairan (BDP) Fakultas : Pertanian
SUSUNAN KOMISI PENGUJI
Nama Tanda Tangan
1. Ir. Darmawati, M.Si (...) Ketua Sidang
2. Ir. Andi Khaeriyah, M.Pd (...) Sekretaris
3. Dr. Abdul Haris, S.Pi, M.Si (...) Anggota
4. Murni, S.Pi, M.Si (...) Anggota
PERNYATAAN MENGENAI SKRIPSI DAN SUMBER INFORMASI
Dengan ini saya menyatakan bahwa skripsi yang berjudul “Studi Parameter Kimia Perairan Bagi Peruntukan Budidaya Keramba Jaring Apung (Studi Kasus Waduk Bilibili Zona II) Desa Bilibili, Kecamatan Bontorannu, Kabupaten Gowa” adalah karya saya dengan arahan dari komisi pembimbing dan belum diajukan dalam bentuk apapun kepada perguruan tinggi manapun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam daftar pustaka di bagian akhir skripsi ini.
Makassar, Agustus 2014
Gusriandi
NIM 10594 00481 10
ABSTRAK
Gusriandi, Studi Parameter Kimia Perairan Bagi Peruntukan Budidaya Keramba Jaring Apung (Studi Kasus Waduk Bilibili Zona II). Dibimbing oleh Darmawati dan Andi Khaeriyah.
Penelitian ini bertujuan untuk menganalisis parameter kimia yang meliputi pH, oksigen terlarut, amoniak, dan fosfat pada waduk Bilibili Kabupaten Gowa serta menentukan lokasi yang cocok untuk peruntukan budidaya keramba jaring apung (KJA). Pengukuran parameter kimia dilakukan pada tiga titik pengamatan secara in situ untuk pH dan oksigen terlarut, dan analisis laboratorium untuk amoniak dan fosfat. Hasil penelitian menunjukkan pH pada ketiga titik pengamatan berkisar 8.27 – 9,92 mg/l, oksigen terlarut 6.2 – 8,85 mg/l, amoniak 0.004 – 0,001 mg/l, dan fosfat 0 - 0.59 mg/l. Dengan mengacu pada literatur kelayakan budidaya air tawar maka dapat disimpulkan bahwa parameter kimia pada waduk Bilibili di Kabupaten Gowa, untuk parameter oksigen terlarut dan amoniak masih berada dalam kondisi baik, sedangkan parameter pH pada minggu kedua distasiun dua, dan minggu ketiga dan minggu keempat stasiun satu, dua dan tiga dan fosfat minggu pertama dan minggu keempat pada stasiun satu, dua, dan tiga pada kedalaman 30 cm dari permukaan perairan terindikasi melewati batas baku mutu kualitas air.
Kata Kunci : Parameter kimia air, keramba jaring apung, waduk Bilibili.
HAK CIPTA
@ Hak Cipta Milik Unismuh Makassar, tahun 2014
Hak Cipta dilindungi Undang-Undang
1. Dilarang mengutip sebagaian atau seluruh karya tulis ini tanpa
mencantumkan atau menyebutkan sumber.
a. Pengutipan hanya untuk kepentingan pendidikan, penelitian, penulisan
karya ilmiah, penyusunan laporan, penulisan kritik atau tinjauan suatu
masalah.
b. Pengutipan tidak merugikan kepentingan yang wajar Unismuh
Makassar.
2. Dilarang mengumumkan dan memperbanyak sebagaian atau seluruh karya
tulis dalam bentuk laporan apapun tanpa izin Unismuh Makassar.
KATA PENGANTAR
Syukur Alhamdulillah penulis panjatkan kehadirat Allah SWT, karena berkat rahmat-Nya penulis pada penyelesaian skripsi ini. Skripsi ini diberi judul
“Studi parameter kimia perairan bagi peruntukan budidaya keramba jaring apung (studi kasus waduk bili-bili zona II)”.
Skripsi ini bertujuan untuk mengukur paramater kimia perairan waduk Bili-bili untuk mengetahui layak atau tidaknya perairan ini dilakukan budidaya keramba jaring apung.
Pada kesempatang ini, penulis mengucapkan terima kasih kepada semua pihak yang telah membantu dalam penulisan skripsi ini baik secara langsung maupun tidak langsung. Oleh karena itu penulis mengucapkan terimakasih yang sedalam dalamnya Teristimewa penulis hanturkan kepada ibunda, ayahanda keluarga tercinta atas kasih sayang, doa dan bantuanya kepada penulis.
Ucapan terima kasih dan penghargaan yang sebesar-besarnya kepada ibu Ir. Darmawati, M.Si selaku pembimbing pertama dan Ir. Andi Khaeriyah, M.Pd selaku Pembimbing kedua, yang banyak memberikan pengarahan serta bimbingan kepada penulis. Penulis juga tak lupa mengucapkan banyak terima kasih kepada :
1. Murni, S.Pi, M.Si, selaku ketua jurusan budidaya perairan di Universitas Muhammadiyah Makassar.
2. Rekan-rekan penelitian dari Universitas Muhammadiyah Makassar, semoga persahabatan dan kebersamaan tak terlupakan seumur hidup.
Penulis menyadari bahwa penyusunan skripsi ini masih jauh dari kesempurnaan dan masih banyak terdapat kekurangan, untuk itu saran dan kritik yang sifatnya membangun penulis harapkan. Mudah-mudahan skripsi ini dapat bermanfaat bagi seluruh pembaca.
Wassalam.
Makassar, maret 2014
Gusriandi
DAFTAR ISI
Halaman
DAFTAR TABEL iii
DAFTAR GAMBAR iv
DAFTAR LAMPIRAN v
I. PENDAHULUAN 1
1.1 Latar Belakang 2
1.2 Tujuan dan Kegunaan Penelitian 2
II. TINJAUAN PUSTAKA 3
2.1 Ekosistem Waduk 3
2.2 Budidaya Ikan dan Sistem Keramba Jaring Apung (KJA) 3
2.3 Faktor Kimia Perairan 5
2.3.1 Derajat Keasaman (pH) 5
2.3.2 Oksigen Terlarut (DO) 6
2.3.3 Ammonia (NH3) 7
2.3.4 Fosfat (P) 9
III.METODE PENELITIAN 13
3.2 Waktu dan Tempat 13
3.2 Alat dan Bahan 13
3.3 Prosedur Penelitian 14
3.3.1 Persiapan 14
3.3.2 Penentuan Stasiun Pengamatan 14
3.3.3 Pengambilan Sampel 15
3.3.4 Pengawetan Sampel 16
3.4 Peubah Yang Diamati 18
3.4.1 pH 18
3.4.2 Oksigen Terlarut 18
3.4.3 Fosfat 19
3.4.4 Ammonia 20
3.5 Analisis Data 20
IV. HASIL DAN PEMBAHASAN 22
4.1 Keadaan Umum 22
4.2 pH (Derajat Keasaman) 22
4.3. DO (Oksigen Terlarut) 24
4.4. Ammonia 27
4.5. Fosfat 29
V. PENUTUP 33
5.1 Kesimpulan 33
5.2 Saran 33
DAFTAR PUSTAKA 34
LAMPIRAN
DAFTAR TABEL
Halaman 1. Kelayakan parameter pH kualitas air untuk budidaya KJA air tawar 6 2. Kelayakan parameter DO untuk budidaya KJA air tawar 7 3. Kisaran optimal ammonia untuk budidaya KJA air tawar 9 4. Klasifikasi perairan berdasarkan konsentrasi PO4 11 5. Kisaran optimal fosfat untuk budidaya KJA air tawar 12 6. Alat dan bahan yang digunakan dalam penelitian antara lain 13
7. Cara pengawetan sampel air 17
8. Kelayakan kualitas air untuk budidaya KJA air tawar 21 9. Hasil rata-rata pengukuran pH waduk Bilibili zona II 23 10. Hasil rata-rata pengukuran DO waduk Bilibili zona II 25 11. Hasil analisis ammonia waduk Bilibili zona II 27 12. Hasil analisis fosfat waduk Bilibili zona II 30
DAFTAR GAMBAR
Halaman 1. Tempat penelitian di waduk Bilibili, Kabupaten Gowa 13
2. Stasiun pengambilan sampel 15
3. Nilai rata-rata pH perstasiun 24
4. Nilai rata-rata DO perstasiun 26
5. Nilai rata-rata analisis ammonia perstasiun 29
6. Nilai rata-rata analisis fosfat perstasiun 31
7. Pengukuran pH waduk Bilibili zona II 40
8. Pengukuran DO waduk Bilibili zona II 41
9. Pengambilan sampel air waduk Bilibili zona II 41
10. Botol sampel air waduk Bilibili zona II 42
11. Pengukuran fosfat di laboratorium UNHAS 42
12. Pengukuran amoniak di laboratorium UNHAS 43
13. Foto mahasiswa penelitian Bilibili 43
DAFTAR LAMPIRAN
Halaman 1. Hasil pengukuran pH waduk Bilibili zona II minggu pertama
sampai minggu keempat 38
2. Hasil rata-rata pengukuran pH waduk Bilibili zona II minggu
pertama sampai minggu keempat 38
3. Hasil pengukuran DO (oksigen terlarut) waduk Bilibili zona II
minggu pertama sampai minggu keempat 39
4. Hasil rata-rata pengukuran DO (oksigen terlarut) waduk Bilibili
Zona II minggu pertama sampai minggu keempat 39
5. Hasil rata-rata analisis ammonia waduk Bilibili zona II minggu
pertama sampai minggu keempat 40
6. Hasil rata-rata analisis fosfat waduk Bilibili zona II minggu pertama
sampai minggu keempat 40
I. PENDAHULUAN
1.1. Latar Belakang
Upaya peningkatan produksi perikanan terus dilakukan, salah satunya adalah dengan melakukan kegiatan budidaya keramba jaring apung (KJA).
Keramba jaring apung adalah sebuah sarana pembiakan perikanan yang menggunakan jaring sebagai sarana pembiakan. Pembiakan ikan biasa dilakukan di laut ataupun di media air tawar seperti danau atau waduk, dengan alasan kedalaman yang dibutuhkan untuk keramba biasanya cukup dalam, dimana kedalaman tersebut tidak tersedia di media air tawar lain seperti sungai atau tambak.
Waduk Bilibili dimanfaatkan untuk kegiatan budidaya keramba jaring apung. Dengan memanfaatkan waduk Bilibili sebagai tempat budidaya keramba jaring apung akan memberikan dampak positif terhadap peningkatan produksi ikan, peluang usaha, kesempatan bekerja, serta peningkatan pendapatan petani ikan.
Dalam suatu usaha budidaya perikanan, sangat penting untuk dipelajari kondisi kualitas suatu perairan untuk dijadikan indikasi kelayakan suatu perairan untuk budidaya perikanan. Untuk mengelola sumberdaya perikanan yang baik maka salah satu persyaratan yang harus diperhatikan adalah kualitas perairan.
Boyd (1982), menyatakan bahwa untuk tumbuhan dan organisme perairan dapat tumbuh dan berkembang dengan baik, organisme tersebut memerlukan persyaratan tertentu dalam habitat hidupnya yaitu kondisi perairan.
Berbagai masalah telah timbul di waduk Bilibili yang dapat mengganggu dan mengancam fungsi-fungsi tersebut karena telah terjadi degradasi lingkungan waduk. Berdasarkan fungsi perairan tersebut, maka informasi tentang parameter Kimia perlu dikemukakan untuk digunakan sebagai indikator kualitas perairan serta bahan pembanding dalam kegiatan peruntukan budidaya keramba jaring apung (KJA).
1.2. Tujuan dan Kegunaan Penelitian.
Penelitian ini dilakukan untuk menentukan kualitas parameter kimia perairan waduk Bilibili bagi peruntukan budidaya keramba jaring apung (KJA).
Sedangkan kegunaannya adalah untuk memperoleh gambaran tentang kualitas air di perairan waduk Bili-bili sebagai tempat peruntukan budidaya keramba jaring apung (KJA). Dari data yang didapatkan di lapangan diharapkan dapat memberikan informasi yang berguna bagi masyarakat yang ingin melakukan budidaya ikan waduk Bili-bili.
II. TINJAUAN PUSTAKA
2.1. Ekosistem Waduk
Ekosistem merupakan suatu sistem ekologi yang terdiri atas komponen- komponen biotik dan abiotik yang saling berinteraksi sehingga membentuk satu kesatuan. Di dalam ekosistem perairan terdapat faktor-faktor abiotik dan biotik (konsumen, produsen dan pengurai) yang membentuk suatu hubungan timbal balik dan saling mempengaruhi.
Ekosistem air yang terdapat di daratan (inland water) secara umum dapat dibagi 2 yaitu perairan lentik (lentic water), atau juga disebut sebagai perairan tenang, mosalnya danau, rawa, waduk, situ, telaga, dan sebagainya dan perairan lotik (lotic water), disebut juga sebagai perairan yang berarus deras, misalnya sungai, kali, kanal, parit dan sebagainya. Perbedaan utama antara perairan lotik dan lentik adalah dalam kecepatan arus air. Perairan lentik mempunyai kecepatan arus yang lambat serta terjadi akumulasi massa air yang berlangsung dengan cepat (barus, 2004).
2.2. Budidaya Ikan Sistim Keramba Jaring Apung (KJA)
Kegiatan keramba jaring apung (KJA) merupakan salah satu bentuk kegiatan perikanan akuakultur yang dilakukan pada wadah jaring yang terapung.
Dirjen Perikanan (2001) mendefinisikan keramba jaring apung sebagai tempat pemeliharaan ikan yang terbuat dari bahan jaring yang memungkinkan keluar masuknya air dengan leluasa, sehingga terjadi pertukaran ke perairan sekitarnya.
pelampung, jangkar, pemberat jaring, penutup kantung jaring, bangunan fisik dan peralatan pendukung lainnya.
Budidaya ikan sistim KJA merupakan kegiatan budidaya ikan yang dapat dikembangkan secara intensif denga kepadatan (densitas) ikan budidaya yang cukup tinggi. Karena kepadatan tebar ikan yang dibudidayakan pada KJA cukup tinggi, sehingga tidak dapat lagi hanya dengan mengandalkan sumber makanan dari yang tersedia secara alami di perairan, melainkan harus didatangkan dari luar sebagai pakan tambahan. Pada umumnya pakan tambahan yang di berikan adalah pakan buatan yang disebut dengan pelet.
Secara ekonomi usaha budidaya ikan dengan sistim keramba jaring apung mempunyai beberapa keunggulan, yang antara lain adalah: 1) menambah efisiensi penggunaan sumberdaya; 2) dapat meningkatkan produksi ikan; 3) memberikan pendapatan yang lebih teratur dibandingkan dengan hanya bergantung pada usaha penangkapan. Namun demikian, bila pengelolaan budidaya ikan keramba jaring apung (KJA) yang dilakukan dalam jumlah yang berlebihan dan teknologi yang tidak memperhatikan daya dukung lingkungan perairan akan dapat memberikan dampak yang serius terhadap lingkungan perairan tersebut, baik lingkungan biotik maupun lingkungan abiotiknya.
Menurut Beveridge (1984) kegiatan keramba jaring apung berdampak terhadap 4 (empat) hal utama yaitu (1) membutuhkan banyak tempat (space) atau permukaan perairan danau, (2) menghambat aliran air dan arus untuk transportasi oksigen, sedimen, plankton serta larva ikan, (3) menurunkan kualitas estetika perairan danau dan (4) menurunkan kualitas lingkungan hidup danau. Selanjutnya
Beveridge (1984) menyatakan bahwa kegiatan budidaya ikan keramba jaring apung berpengaruh sencara nyata terhadap lingkungan perairan, yaitu mulai dari adanya perubahan hara air, perubahan konsentrasi oksigen terlarut (DO), perubahan konsentrasi metabolik toksik serta berkembangnya organismeorganisme penyebab penyakit, sehingga perairan tersebut menjadi tidak layak lagi untuk dimanfaatkan sebagai sumber air minum, sarana rekreasi dan peruntukan perikanan itu sendiri.
2.3. Faktor Kimia Perairan
Parameter kimia perairan meliputi ; 1) pH, 2) Oksigen terlarut, 3) Ammonia, 4) Fosfat.
2.3.1. Derajat Keasaman (pH)
Derajat keasaman merupakan gambaran dari jumlah atau aktivitas ion hidrogen didalam air. Secara umum nilai pH air menggambarkan keadaan seberapa besar tingkat keasaman atau kebasaan suatu perairan. Perairan dengan nilai pH = 7 berati kondisi air bersifat netral, pH < 7 berarti kondisi air bersifat asam, sedangkan pH > 7 berarti kondisi air bersifat basa (Effendi, 2003).
Keberadaan senyawa karbonat, bikarbonat dan hidroksida dalam air akan menaikkan kebasaan air, sementara keberadaan asam mineral bebas dan asam karbonat menaikkan keasaman suatu perairan. Selanjutnya, Pescod (1973) menjelaskan bahwa nilai pH air dapat dipengaruhi oleh beberapa faktor yaitu fotosintesis, respirasi organisme akuatik, suhu dan keberadaan ion-ion di perairan
Nilai pH dapat mempengaruhi spesiasi senyawa kimia dan toksisitas dari unsur-unsur renik yang terdapat di perairan, sebagai contoh H2S yang bersifat toksik banyak ditemui di perairan yang tercemar dan perairan dengan nilai pH rendah. Perairan dengan kondisi asam kuat akan menyebabkan unsur logam berat seperti aluminium memiliki mobilitas yang meningkat dan karena logam ini bersifat toksik maka dapat mengancam kehidupan biota. Demikian juga bila pH air terlalu basa maka keseimbangan amonium dan amoniak akan terganggu, dalam hal ini kenaikan pH di atas netral akan meningkatkan konsentrasi amoniak yang juga bersifat toksik terhadap biota akuatik. Selain itu, pH air juga mempengaruhi parameter BOD5 dan kandungan nutrien dalam air seperti fosfat, nitrogen dan nutrien lainnya (Dojildo and Best, 1992).
Kisaran pH yang optimal bagi peruntukan budidaya ikan air tawar sebagai berikut:
Tabel 1. Kelayakan parameter pH kualitas air untuk budidaya KJA air tawar
Parameter Kisaran Optimal Literatur
pH 6.5 - 8 Gusrina (2008)
7 Effendi (2003)
6.5 - 8.5 EPA (1973) dan Kep MenLH (2004)
2.3.2. Oksigen Terlarut (DO)
Gas oksigen sangat dibutuhkan bagi kehidupan organisme air. Gas oksigen umumnya banyak dijumpai dilapisan permukaan, oleh karena gas oksigen umumnya banyak dijumpai dilapisan permukaan, oleh karena gas oksigen yang berasal dari udara didekatnya melalui pelarutan (difusi) ke dalam air laut. Sumber
oksigen terlarut dalam air berasal dari difusi oksigen yang terdapat di atmosfer, arus atau aliran air melalui air hujan serta aktivitas fotosintesis oleh tumbuhan air dan fitoplankton (Novonty, 1994).
Oksigen diperlukan oleh organisme air untuk menghasilkan energi yang sangat penting bagi pencernaan dan asimilasi makanan pemeliharaan keseimbangan osmotik, dan aktivitas lainnya. Jika persediaan oksigen terlarut di perairan sangat sedikit maka perairan tersebut tidak baik bagi ikan dan makhluk hidup lainnya yang hidup di perairan, karena akan mempengaruhi kecepatan pertumbuhan organisme air tersebut. Kandungan oksigen terlarut minimum 2 mg/l sudah cukup mendukung kehidupan organisme perairan secara normal (Wardana, 1995).
Kisaran parameter oksigen terlarut yang optimal bagi peruntukan budidaya ikan air tawar seperti disajikan pada tabel berikut:
Tabel 2. Kelayakan parameter DO untuk budidaya KJA air tawar.
Parameter Kisaran Optimal Literatur
DO
> 4 mg/l Asmawi (1984)
7 - 9 mg/l Effendi (2003)
5 - 6 ppm Gusrina (2008)
5 - 7 ppm Kordi G dan Tancung AB
(2005)
2.3.3. Ammonia
Dari semua parameter kualitas air yang mempengaruhi ikan, ammonia adalah yang paling penting setelah oksigen. Ammonia merupakan salah satu gas yang umum dijumpai dalam air . Ammonia mudah tertimbun di dalam sistem
penguraian sisa-sisa makanan dan bahan organik lainnya. Ada dua bentuk ammonia dalam air, yaitu ammonia tak terionisasi (disebut juga amonia bebas) dan ammonia terionisasi. Bentuk amonia tak terionisasi (NH3) sangat beracun sedang bentuk terionisasi (ion NH4+) tidak beracun. Kedua bentuk ini secara bersama-sama disebut “ammonia total”.
Di perairan alami seperti danau amonia mungkin tidak pernah mencapai tingkat yang berbahaya karena rendahnya kepadatan ikan. Konsentrasi amonia yang tinggi dan berbahaya biasanya hanya terjadi dalam sistem budidaya yang bersifat resirkulasi (air didaur ulang terus-menerus) dan di kolam budidaya setelah terjadinya kematian masal fitoplankton. Keracunan amonia juga timbul pada sistem budidaya intensif. Masalah yang dijumpai dalam sistem akuakultur biasanya berasal dari produksi ammonia yang berlebihan.
Amonia masuk ke dalam air melalui pupuk, hasil eksresi ikan dan hasil penguraian senyawa bernitrogen oleh mikroba. Dalam air, ammonia terionisasi menjadi ion amonium tetapi reaksi ini bisa kembali dengan terbentuknya amonia bebas. Efek racun yang ditimbulkan amonia tak terionisasi bisa menyebabkan kerusakan insang, ginjal, limfa, jaringan tiroid dan darah ikan (Boyd, 1982).
Beberapa faktor mengubah daya racun amonia dalam air. Sebagian faktor ini mengubah konsentrasi ammonia tak terionisasi dengan menggeser reaksi keseimbangan ammonia – amonium, sedang faktor-faktor lainnya mempengaruhi daya racun ammonia itu sendiri. Faktor-faktor tersebut, selain suhu dan aklimasi, adalah konsentrasi oksigen terlarut, pH, konsentrasi karbon dioksida, salinitas dan keberadaan racun lainnya (EPA,1973). Kalsium, kalium dan natrium juga
dilaporkan mempengaruhi daya racun ammonia (Borgmann , 1997; Soderberg dan Meade, 1992; Weirich et al., 1993).
Menurut Boyd (1982) ammonia lebih beracun bila konsentrasi oksigen telarut rendah. Satyanarayana et al. (2008) menambahkan bahwa kondisi kekurangan oksigen timbul bersamaan dengan meningkatnya konsentrasi ammonia tak terionisasi yang beracun. Allan et al. (1990) meneliti pengaruh konsentrasi oksigen terhadap daya racun ammonia. Mereka memperkirakan daya racun akut ammonia sebagai nilai LC50 96-jam.
Kisaran parameter optimal ammonia bagi peruntukan kegiatan budidaya ikan air tawar disajikan sebagai berikut:
Tabel 3. Kisaran Optimal Ammonia untuk budidaya KJA air tawar.
Parameter Kisaran Optimal Literatur
Ammonia < 1.5 ppm Gusrina (2008)
1 mg/l Frits Tatangindatu, (2013)
0.1 mg/l Puspowardoyo (1992)
2.3.4. Fosfor (P)
Fosfor merupakan salah satu bahan kimia yang keberadaanya sangat penting bagi semua mahluk hidup, terutama dalam pembentukan protein dan transfer energi didalam sel seperti ATP dan ADP. Pada ekosistem perairan, fosfor terdapat dalam bentuk senyawa fosfor, yaitu : 1) fosfor anorganik; 2) fosfor organik dalam protoplasma tumbuhan dan hewan dan 3) fosfor organik terlarut dalam air, yang terbentuk dari proses penguraian sisa-sisa organisme (Barus, 2004).
Secara alami, senyawa fosfat yang terdapat pada perairan bersumber dari hasil pelapukan batuan mineral seperti Fluorapatite (Ca5 -(PO4)3F), Hydroxylapatite (Ca5(PO4)3 OH) dan Whytlockite (Ca3(PO4)2) dan dari hasil dekomposisi sisa-sisa organisme di dalam air. Selain sumber alami, senyawa fosfot juga dapat bersumber dari faktor antropogenik yang antara lain berasal dari limbah rumah tangga seperti deterjen, limbah pertanian (pupuk), limbah perikanan dan limbah industri. Sawyer dan Mc.Carty (1978) menyatakan bahwa senyawa fosfor anorganik yang terdapat pada perairan berada dalam 2 (dua) bentuk, yaitu : 1) dalam bentuk ortofosfat, yang terdiri dari trinatrium fosfat (Na3PO4), dinatrium fosfat (Na2HPO4), mononatrium fosfat (NaH2HPO4) dan diamonium fosfat ((NH3)2HPO4); 2) dalam bentuk polyfosfat, yang terdiri dari natrium hexametafosfat (Na3(PO3)6) dan natrium tripolifosfat (Na5P3O10).
Ortofosfat merupakan bentuk senyawa fosfat yang dapat dimanfaatkan oleh tumbuhan akuatik secara langsung sebagai sumber fosfor, sedangkan polyfosfat merupakan senyawa yang tidak dapat dimanfaatkan tumbuhan secara langsung, oleh sebab itu agar senyawa polyfosfat dapat dimanfaatkan oleh tumbuhan akuatik sebagai sumber fosfor, maka senyawa polyfosfat harus terlebih dahulu mengalami hidrolisis menjadi senyawa ortofosfat.
Oleh karena senyawa orthofosfat merupakan senyawa yang sangat
dibutuhkan untuk pertumbuhan tanaman termasuk fitoplankton dan alga pada perairan, maka kesuburan suatu perairan dapat ditentukan berdasarkan kandungan orthofosfatnya. Vollenweider dalam Wetzel (1975) mengklasifikasikan tingkat
kesuburan suatu perairan berdasarkan tinggi rendahnya kandungan orthofosfat pada perairan tersebut.
Tabel 4. Klasifikasi perairan berdasarkan konsentrasi PO4
No. Klasifikasi Orthofosfat (PO₄)
1 Oligotrofik 0.003 - 0.01
2 Mesotrofik 0.011 - 0.03
3 Eutofik 0.031 - 0.1
(sumber: vollenweider dalam wetzel, 1975).
Selain berdasarkan kandungan fosfat, tingkat kesuburan suatu perairan dapat juga diklasifikasikan berdasarkan kandungan fosfor totalnya. Yoshimura dalam Liaw (1969) mengklasifikasikan tingkat kesuburan perairan berdasarkan kandungan fosfor totalnya menjadi 3 golongan,yaitu : 1) Perairan dengan tingkat kesuburan yang rendah yaitu perairan yang kandungan fosfor totalnya berkisar 0 – 0,02 mg/l; 2) Perairan dengan tingkat kesuburan yang sedang yaitu perairan yang kandungan fosfor totalnya berkisar 0,021 – 0,05 mg/l; 3) Perairan dengan tingkat kesuburan yang tinggi yaitu perairan yang kandungan fosfor totalnya berkisar 0,051 – 0,1 mg/l.
Menurut Bruno et al (1979) dalam Sumardianto, (1995) bahwa kandungan ortofosfat yang optimal bagi pertumbuhan fitoplankton adalah 0,27 - 5,51 mg/L, dimana apabila konsentrasinya kurang dari 0,02 mg/L, maka fosfat akan menjadi faktor pembatas. Selanjutnya, Moyle (1946) dalam Ardiwijaya (2002) menyatakan bahwa perairan dengan konsentrasi fosfat yang rendah (0,00-0,02 mg/l) akan didominasi oleh fitoplankton dari kelas Bacillariophyceae (Diatom), pada konsentrasi fosfat yang sedang (0,02-0,05 mg/l) akan didominasi oleh kelas
didominasi oleh kelas Chlorophyceae. Kisaran fosfat yang optimal bagi peruntukan budidaya ikan air tawar sebagai berikut:
Tabel 5. Kisaran optimal fosfat untuk budidaya KJA air tawar.
Parameter Kisaran Optimal Referensi
Fosfat
< 0.02 ppm Gusrina (2008)
0.02 - 0.1 mg/l Yoshimura dalam Liaw (1969)
> 0.02 mg/l Bruno et al (1979) dalam Sumardianto, (1995)
< 1 mg/l Cahyono (2000)
III. METODE PENELITIAN
3.1. Waktu dan Tempat
Penelitian ini dilaksanakan pada bulan Agustus sampai bulan September, bertempat di wilayah perairan terbenam (waduk Bilibili), Desa Bilibili, Kecamatan Bontorannu, Kabupaten Gowa untuk penelitian lapangan, sedangkan penelitian laboratorium dilaksanakan di laboratorium UNHAS.
Gambar 1. Tempat penelitian di waduk Bilibili, Kabupaten Gowa.
3.2. Alat dan Bahan
Adapun alat dan bahan yang digunakan dalam penelitian ini dapat dilihat pada tabel 6:
Tabel 6. Alat dan bahan yang digunakan dalam penelitian antara lain:
No. Nama Alat dan Bahan Kegunaan
1 Spektrofotometer Mengukur kadar fosfat dan amoniak
2 DO-meter Mengukur DO
3 pH-meter Mengukur pH
4 Botol sampel Wadah air sampel
6 Sampel air Media yang akan diukur/dianalisis
7 Cool box Untuk penyimpanan sampel air
8 Kertas milipore Penyaringan air sampel
9 Pipet tetes Pengambil sampel
10 Ammoniummolybdate Zat pewarna
3.3. Prosesur Penelitian
Prosedur penelitian parameter kualitas kimia air terdiri dari; (1) Persiapan, (2) Penentuan stasiun pengamatan, (3) pengambilan sampel, (4) pengawetan, dan (5) Analisis laboratorium.
3.3.1. Persiapan
Tahap persiapan meliputi pengumpulan informasi mengenai kondisi umum lokasi penelitian, studi literatur dan penentuan metode penelitian yang akan dilaksanakan.
3.3.2. Penentuan Stasiun Pengamatan
Penentuan stasiun pengamatan yang terletak pada zona II yang terdiri dari tiga stasiun pengamatan yaitu : (1) sekitar rumah makan bili-bili, (2) ditengah perairan, (3) disekitar pemukiman penduduk/aktifitas pertanian. Pengukuran parameter kualitas kimia perairan dilakukan sekali dalam seminggu dan lama penelitian yaitu empat minggu. Stasiun pengamatan sampel air pada waduk Bilibili disajikan pada gambar berikut:
Gambar 2. Stasiun pengambilan sampel air.
Keterangan :
A = Stasiun satu didaerah dekat rumah makan bili-bili.
B = Stasiun dua ditengah perairan.
C = Stasiun tiga didaerah dekat pemukiman penduduk/aktifitas pertanian.
3.3.3. Pengambilan Sampel
Pengambilan sampel dilakukan paling lambat pukul 07:00 WITA. Hal ini bertujuan agar mendpatkan kualitas air yang optimal. Metode penelitian yang digunakan pada penelitian ini adalah metode survei dan kerja langsung di lapangan, pengumpulan data dan analisis di Laboratorium. Variabel peneltian ini adalah kualitas air (pH, oksigen terlarut, amoniak, dan posfor). Pengambilan sampel air dilakukan sesuai dengan SNI 6989.57:2008 dilakukan dengan tahap
1. Siapkan alat pengambilan contoh yang sesuai dengan keadaan sumber air;
2. Bilas alat pengambil contoh dengan air yang akan diambil, sebanyak tiga kali;
3. Ambil contoh sesuai dengan peruntukan analisis dan campurkan dalam penampung sementara, kemudian homogenkan;
4. Masukkan kedalam wadah yang sesuai peruntukan analisis;
5. Lakukan segera pengujian untuk parameter suhu, kekeruhan, dan daya hantar listrik, pH dan oksigen terlarut yang dapat berubah dengan cepat dan tidak dapat diawetkan;
6. Hasil pengujian parameter lapangan dicatat dalam buku catatan khusus;
7. Pengambilan contoh untuk parameter pengujian di laboratorium dilakukan pengawetan.
Catatan : pada reinsipnya air yang akan diperiksa diusahakan mempunyai susunan dengan air aslinya. Semua tindakan yang merubah susunan kimianya harus dihindari, baik tempat pengiriman maupun peralatan serta cara pengambilan sampel air.
3.3.4. Pengawetan Sampel
Fungsi pengawetan sampel adalah memperlambat proses perubahan kimia dan biologi yang tidak terelakan. Pengawetan sangat sukar karena hampir semua pengawet mengganggu beberapa penguji. Menyimpan sampel pada suhu rendah (4oC) mungkin merupakan cara terbaik. Untuk mengawetkan contoh sampai hari berikutnya penggunaan reagent pengawet dapat dilakukan selama tidak
pengisian contoh sehingga contoh dapat diawetkan secepatnya. Tidak ada satu metode pengawetan yang memuaskan karena itu dipilih pengawetan yang sesuai dengan tujuan pemeriksa.
Makin pendek selang waktu antara pengambilan contoh dan analisis, hasilnya akan baik. Sebenarnya sukar untuk menentukan selang waktu tersebut karena tergantung dari sifat contoh air, parameter yang akan diperiksa serta cara penyimpanan. Perubahan yang dilakukan oleh kegiatan organisme dapat dicegah dengan menyimpan dalam tempat gelap dan temperatur yang rendah (lemari es) sapai pemeriksaan dilakukan. Berikut ini batasan waktu maksimal untuk pemeriksaan fisika dan kimia:
1. Air bersih 72 jam.
2. Air sedikit tercemar 48 jam.
3. Air kotor / limbah 12 jam.
Pengawetan sampel air sesuai dengan SNI 6989.57.2008 sebagai berikut:
Tabel 7. Cara pengawetan sampel air.
No. Parameter Wadah
penyimpanan
Minimum jumlah contoh diperlukanyang
(mL)
Pengawetan
penyimpananLama maksimum dianjurkan.yang
1 Oksigen G Botol BOD terlarut
Dengan 300 Langsung -
elektroda dianalisis
Metode Titrasi dapat 8 jam
2 pH P,G - Segera dianalisis 2 jam
3 Fosfat G (A) 100 Untuk fosfat 48 jam
terlarut segera disaring, didingingkan 4 Ammonia-
Nitrogen P,G 500 Analisis 7 jam
secepatnya atau tambahkan
H2SO4sampai pH < 2, didingingkan.
Keterangan :
Didingingkan pada suhu 4oC ± 2oC P : plastik (polietilen atau sejenisnya) G(A) : gelas dicuci dengan 1 + 1 HNO3
P(A) : plastik dicuci dengan 1 + 1 HNO3
3.4. Peubah Yang Diamati
3.4.1. pH
Kandungan pH pada perairan diukur langsung pada tempat atau stasiun pengambilan sampel dengan menggunakan alat pH meter. Waktu pengukuran dilakukan sebaiknya pada pukul 07:00 WITA.
3.4.2. Oksigen Terlarut.
Kandungan oksigen terlarut pada perairan diukur langsung pada stasiun pengambilan sampel air dengan menggunakan alat DO Meter. Waktu pengukuran dilakukan sebaiknya pada pukul 07:00 WITA.
3.4.3. Fosfat
Kandungan fosfat pada perairan akan dianalisia dan diukur dilaboratorium dengan menggunakan alat spektrofotometer. Pertama ambil air sampel sebanyak 25 – 50 ml, kemudian saring air tadi dengan menggunakan kertas milipore, ambil air sampel yang telah disaring sebanyak 25 ml dan masukkan kedalam testube, pengambilan air ini menggunakan pipet tetes. Kemudian tabahkan 1 ml Ammoniummolybdate, dan aduk. (air sapel akan berubah warna), kemudian sampel dianalisa menggunakan Spectrofotometer
Proses penggunaan alat spectrofotometer untuk mengukur kandungan fosfat:
a. Alat terlebih dahulu dikalibrasi untuk mendapatkan hasil analisis yang akurat, caranya dengan memasukkan larutan air aquades kewadah alat spectrofotometer.
b. Tunggu hingga proses kalibrasi selesai.
c. Setelah proses kalibrasi alat selesai, kemudian ambil sampel yang telah diberi 1 ml ammoniummolybdate tadi dan masukkan kedalam alat spectrofotometer, tunggu hingga hasil analisis dari alat spectrofotometer selesai.
d. Setelah selesai, maka akan ada angka hasil analisis, maka itulah nilai kandungan fosfat yang terdapat diperairan tempat sampel air tadi diambil.
Catatan : setelah sampel diberi larutan ammoniummolybdate, paling lama 10 -12 menit harus suda dianalisis, perubahan warna mengidentifikasi sebagai
3.4.4. Ammonia
Kandungan ammonia yang terdapat pada perairan akan dianalisa dan diukur di laboratorium dengan menggunakan alat spektrofotometer. Prosedur pengukuran kadar ammonia (NH3) pada perairan (Suprapto, 2011), sebagai berikut:
a. Menyiapkan bahan dan alat yang digunakan.
b. Mengambil air sampel sebanyak 12,5 ml yang sudah disaring dengan dengan kertas saring.
c. Menuangkan kedalam beaker glass atau Erlenmeyer.
d. Menambahkan pereaksi nessler sebanyak 2 ml. dan dihomogenkan.
e. Menunggu sampai terjadi perubahan warna.
f. Melihat kadar ammonia dengan menggunakan spektrofotometer dengan panjang gelombang 425 µm.
g. Mencatat hasil dalam ppm.
3.5. Analisis Data
Pengukuran parameter kualitas kimia air dilakukan secara langsung (in situ) untuk pengukuran pH dan DO serta analisis laboratorium untuk parameter ammonia dan fosfat. Kemudian data yang diperoleh dilapangan akan ditampilkan dalam bentuk tabel dan grafik. Kemudian data yang diperoleh akan dianalisis secara deskriptif dengan membandingkan antara data yang diperoleh dilapangan dengan kelayakan kualitas air untuk budidaya KJA. Berikut parameter kimia air untuk budidaya perairan tawar.
Tabel 8. Kelayakan kualitas air untuk budidaya KJA air tawar.
No. Parameter Kisaran optimal Literatur
1 pH 6.5 - 8.5 EPA (1973)
2 Oksigen terlarut > 4 mg/l Asmawi (1984)
3 Amoniak ≤ 1 mg/l Frits tatangindatu (2013)
4 Fosfat < 1 mg/l Cahyono (2000)
IV. HASIL DAN PEMBAHASAN
4.1. Keadaan Umum
Bendungan Bilibili merupakan bendungan terbesar di Sulawesi Selatan yang terletak di Kabupaten Gowa, sekitar 30 kilometer ke arah timur kota Makassar. Bendungan ini diresmikan pada tahun 1989. Secara geografis, daerah tangkapan waduk Bilibili yang berada di wilaya sub DAS Jeneberang terletak antara 5o11’8”-5o20’54” LS dan 119o34’30”-119o56’54” BT. Bendungan Bilibili terletak pada ketinggian 75-5000 meter diatas permukaan laut.
Waduk Bilibili memiliki luas tangkapan air besar 284,4 km2 (38.440 Ha) dengan luas genangan 18,5 km2 dan kedalaman efektif 36,6 m (JRBDP, 2004).
Adapun volume tampung total waduk Bilibili yang dapat dibendung adalah sebesar 375.000.000 m3 dengan volume tampung efektif sebesar 346.000.000 m3 dan volume tampungan mati sebesar 29.000.000 m3.
4.2. pH (derajat keasaman)
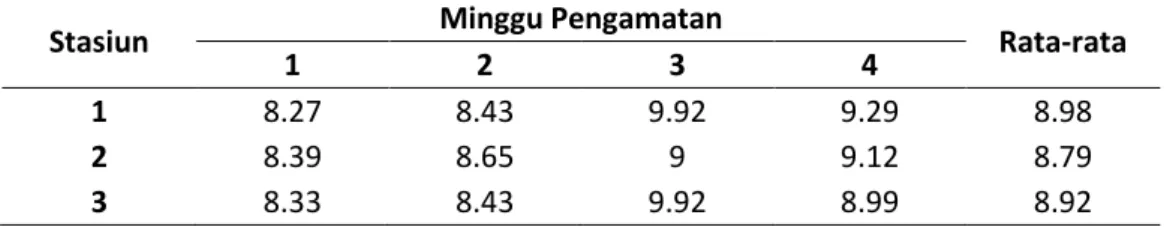
Berdasarkan hasil pengukuran pada masing-masing stasiun diketahui bahwa nilai pH pada air waduk Bilibili zona II yaitu 8.27 – 9.92 . Hasil pengukuran pH waduk Bilibili zona II pada tiga stasiun pengamatan dengan waktu pengamatan empat minggu dapat dilihat pada lampiran I sedangkan nilai rata-rata pH selama empat minggu dapat dilihat pada tebel berikut.
Tabel 9. Hasil rata-rata pengukuran pH waduk Bilibili zona II.
Stasiun Minggu Pengamatan
Rata-rata
1 2 3 4
1 8.27 8.43 9.92 9.29 8.98
2 8.39 8.65 9 9.12 8.79
3 8.33 8.43 9.92 8.99 8.92
Hasil rata-rata pengukuran pada tiga stasiun pengamatan dimana pH terendah berada di stasiun dua dengan nilai 8.79 sedangkan pH tertinggi terdapat di stasiun pertama dengan nilai 8.98, untuk lebih jelasnya dapat dilihat pada gambar 3.
Stasiun I dan II memiliki kandungan pH yang relatif lebih tinggi dibandingkan stasiun II, hal ini diduga akibat adanya pengaruh buangan limbah dari rumah makan dan rumah penduduk yang masuk keperairan waduk. Limbah atau sampah tersebut mengandung berbagai macam senyawa kimia yang bersifat basa seperti sabun (deterjen, sampo dan bahan pembersih lainnya), Sabun berasal dari asam lemak (stearat, palmitat atau oleat) yang direaksikan dengan basa Natrium hidroksida Na(OH) atau Kalium hidroksida K(OH), yang dapat meningkatkan nilai pH di perairan. Sejalan dengan pernyataan tersebut Mahida (1993) menyatakan bahwa limbah buangan industri dan rumah tangga dapat mempengaruhi nilai pH perairan.
Nilai rata-rata pH perstasiun disajikan dalam bentuk histogram seperti gambar berikut.
Gambar 3. Nilai rata-rata pH perstasiun.
Berdasarkan hasil pengukuran dilapangan diperoleh nilai rata-rata pH pada masing-masing stasiun yaitu stasiun I dengan nilai pH 8.98, stasiun II dengan nilai pH 8.79, dan stasiun III dengan nilai pH 8.92 yang menunjukkan bahwa perairan pada semua stasiun penelitian berada dalam keadaan tidak layak dilakukan usaha budidaya karena melewati batas kelayakan usaha budidaya. Menurut pernyataan EPA (1973) bahwa pH yang baik untuk kegiatan budidaya ikan air tawar berkisar 6.5 – 8.5.
4.3. DO (oksigen terlarut)
Berdasarkan hasil pengukuran dilapangan diketahui bahwa nilai oksigen terlarut pada air waduk Bilibili zona II yaitu 6.2 – 8.85 mg/l. Hasil rata-rata pengukuran DO (oksigen terlarut) di stasiun pertama, stasiun kedua, dan stasiun
8.98
8.79
8.92
8.65 8.7 8.75 8.8 8.85 8.9 8.95 9
Stasiun Satu Stasiun Dua Stasiun Tiga
Nilai rata-rata pH perstasiun
ketiga pengamatan pada kedalaman 30 cm dari permukaan perairan ditampilkan pada tabel 10.
Tabel 10. Hasil rata-rata pengukuran DO waduk Bilibili zona II.
Stasiun Minggu Pengamatan
Rata-rata
1 2 3 4
1 7.96 7.77 8.4 6.2 7.59
2 8.64 7.82 8.21 6.54 7.81
3 8.17 8.85 7.76 6.24 7.76
Hasil rata-rata pengukuran oksigen terlarut pada tiga stasiun pengamatan dimana DO terendah berada di stasiun satu dengan nilai 7.59 mg/l, sedangkan DO tertinggi terdapat di stasiun dua dengan nilai 7.81 mg/l, untuk lebih jelasnya dapat dilihat pada gambar 4. Perbedaan kandungan oksigen terlarut dalam air pada masing-masing stasiun setiap minggunya dipengaruhi oleh perbedaan waktu pengukuran sampel sehingga berpengaruh terhadap suhu yang berdampak pada kandungan oksigen terlarut diperairan. Serta faktor lain seperti aktifitas biologi, aktifitas fotosintesis, serta limbah atau pengaruh aktifitas darat. Hal ini sesuai pendapat Hadic dan Jatna (1998) bahwa penyebab utama berkurangnya oksigen terlarut didalam perairan adalah adanya bahan-bahan buangan organik yang banyak mengkomsumsi oksigen sewaktu penguraiyan berlangsung. Lanjut Effendi (2003) yang menyatakan bahwa walaupun pada kondisi terbuka, kandungan oksigen perairan tidak sama dan bervariasi berdasarkan siklus, tempat, dan musim. Kadar oksigen terlarut juga berfluktuasi secara harian, musiman, pencampuran massa air, pergerakan massa air, aktifitas fotosimtesa, resfirasi, dan
Sumber oksigen terlarut terutama berasal dari difusi oksigen yang terdapat di atmosfer. Difusi oksigen ke dalam air terjadi secara langsung pada kondisi stagnant (diam) atau karena agitasi (pergolakan massa air) akibat adanya gelombang atau angin.
Nilai rata-rata oksigen terlarut perstasiun disajikan dalam bentuk histogram seperti gambar berikut.
Gambar 4. Nilai rata-rata oksigen terlarut perstasiun.
Hal ini menunjukkan bahwa kandungan oksigen terlarut pada semua stasiun pengamatan masih layak untuk kegiatan budidaya keramba jaring apaung (KJA) karena kandungan oksigen terlarut masih dalam kisaran yang optimal seperti yang dijelaskan oleh Asmawi (1984) dan Akbar S (2001) bahwa kandungan oksigen terlarut untuk menunjang usaha budidaya adalah 5-8 mg/l.
7.59
7.81
7.76
7.45 7.5 7.55 7.6 7.65 7.7 7.75 7.8 7.85
Stasiun Satu Stasiun Dua Stasiun Tiga
Nilai rata-rata DO perstasiun
4.4. Ammonia
Berdasarkan hasil analisis untuk masing-masing stasiun diketahui bahwa nilai amonia pada air waduk Bilibili zona II yaitu sekitar 0.001 – 0.004 mg/l. . Hasil analisis ammonia ditiga stasiun pengamatan dengan lama waktu pengamatan empat minggu yang berlokasi di waduk Bilibili Kabupaten Gowa disajikan pada tabel 11.
Tabel 11. Hasil analisis ammonia waduk Bilibili zona II.
Stasiun Minggu Pengamatan
Rata-rata
1 2 3 4
1 0.003 0.002 0.001 0.004 0.003
2 0.002 0.002 0.001 0.003 0.002
3 0.002 0.002 0.001 0.003 0.002
Hasil rata-rata analisis ammonia pada tiga stasiun pengamatan dimana ammonia terendah berada di stasiun dua dan tiga dengan nilai 0.002 mg/l, sedangkan ammonia tertinggi terdapat di stasiun pertama dengan nilai 0.003 mg/l , untuk lebih jelasnya dapat dilihat pada gambar 5.
Stasiun I memiliki nilai ammonia yang relatif lebih tinggi dibandingkan yang lainnya karena stasiun I merupakan kawasan perairan yang dekat dengan kawasan rumah makan dimana limbah domestik dari rumah makan seperti diterjen, minyak goreng bekas, sisa sayur dan sisa makanan dibuang keperairan waduk sehingga mempengaruhi nilai ammonia pada perairan. Hal ini sependapat dengan Marganof, (2007) bahwa ammonia dapat berasal dari limbah domestik dan limbah industri. Ammonia juga berasal dari produk sisa metabolisme yang utama dari ikan, dikeluarkan melalui insang dan urine. Sumber utama ammonia
kebutuhan energi dan nutrien, deaminasi asam amino menjadi energi menghasilkan ammonia yang dikeluarkan sebagai sisa metabolisme.
Di perairan waduk yang luas ammonia mungkin tidak pernah mencapai tingkat yang berbahaya karena rendahnya kepadatan ikan. Konsentrasi ammonia yang tinggi dan berbahaya biasanya hanya terjadi dalam sistem budidaya yang bersifat resirkulasi (air didaur ulang terus-menerus) dan di kolam budidaya setelah terjadinya kematian masal fitoplankton. Keracunan ammonia juga timbul pada sistem budidaya intensif. Masalah yang dijumpai dalam sistem akuakultur biasanya berasal dari produksi ammonia yang berlebihan.
Ammonia di perairan waduk atau danau dapat berasal dari nitrogen organik dan nitrogen anorganik yang terdapat dalam tanah dan air berasal dari dekomposisi bahan organik oleh mikroba dan jamur. Selain itu, ammonia juga berasal dari denitrifikasi pada dekomposisi limbah oleh mikroba pada kondisi anaerob. Hal ini sesuai dengan pendapat Sastrawijaya A T, (2000) yang mengatakan bahwa ammonia juga berasal dari denitrifikasi pada limbah oleh mikroba pada kondisi anaerob.
Perbedaan nilai rata-rata kadar ammonia perstasiun disajikan dalam gambar 5.
Gambar 5. Nilai rata-rata analisis ammonia perstasiun.
Berdasarkan hasil analisis diperoleh nilai dengan rata-rata ammonia pada masing-masing stasiun, yaitu pada stasiun satu dengan kandungan ammonia 0.003 mg/l, stasiun dua dengan kandugan ammonia 0.002 mg/l, dan stasiun tiga dengan kandungan ammonia 0.002 mg/l. Hasil tersebut menunjukan bahwa nilai ammonia pada semua stasiun pengamatan cukup optimal bagi peruntukan kegiatan budidaya keramba jaring apung. Hal ini sesuai dengan pendapat Gusrina (2008) yang menyatakan bahwa kandungan ammonia yang baik untuk budidaya ikan air tawar yaitu < 1.5 mg/l.
4.4. Fosfat (P)
Berdasarkan hasil analisis untuk masing-masing stasiun diketahui bahwa
0.003
0.002 0.002
0 0.0005 0.001 0.0015 0.002 0.0025 0.003 0.0035
Stasiun Satu Stasiun Dua Stasiun Tiga
Nilai rata-rata Ammonia perstasiun
analisis fosfat pada tiga stasiun pengamatan dengan lama waktu pengamatan empat minggu yang berlokasi di waduk Bilibili Kabupaten Gowa disajikan pada tabel 12.
Tabel 12. Hasil analisis fosfat waduk Bilibili zona II.
Stasiun Minggu Pengamatan
Rata-rata
1 2 3 4
1 0.59 <0.001 <0.001 0.531 0.28
2 0.56 0.01 <0.001 0.449 0.26
3 0.56 <0.001 <0.001 0.476 0.26
Hasil rata-rata analisis fosfat pada tiga stasiun pengamatan dimana fosfat terendah berada di stasiun dua dan tiga dengan nilai 0.26 mg/l, sedangkan fosfat tertinggi terdapat di stasiun pertama dengan nilai 0.28 mg/l. Berdasarkan tabel diatas, stasiun I yang memiliki nilai fosfat yang relatif lebih tinggi dibandingkan yang lainnya karena stasiun I merupakan kawasan perairan yang dekat dengan kawasan rumah makan dimana limbah dari rumah makan seperti diterjen, tinja, tulang-tulang ikan dan sisa makanan akan mengalir keperairan waduk sehingga mempengaruhi nilai fosfat pada perairan. Hal ini sesuai pendapat Marganof, (2007) Umumnya kandungan fosfat dalam perairan alami sangat kecil dan tidak pernah melampaui 0.1 mg/l, kecuali bila ada penambahan dari luar perairan oleh faktor antropogenik seperti limbah pertanian. Selanjutnya (Nixon, 1995) menyatakan bahwa sumber zat hara fosfat berasal dari buangan antropogenik berbagai aktivitas manusia seperti pertanian, limbah rumah tangga serta peternakan yang terbawah oleh arus air hujan yang berasal dari daratan menuju ke perairan. Kemudian ditambahkan oleh Sudja (1985) bahwa sebagian senyawa
fosfat yang terlarut dalam air tanah terbawah aliran air sungai menuju laut danau/waduk. Penambahan senyawa fosfat tulang-tulang ikan yang mati, dan dari proses pemupukan yang mengandung fosfat.
Setiap senyawa fosfat tersebut terdapat dalam bentuk terlarut, tersuspensi atau terikat di dalam sel organisme air. Di daerah pertanian ortofosfat berasal dari bahan pupuk yang masuk ke dalam sungai atau danau melalui drainase dan aliran air hujan. Polifosfat dapat memasuki sungai melalui air buangan penduduk dan industri yang menggunakan bahan detergen yang mengandung fosfat, seperti industri logam dan sebagainya. Fosfat organis terdapat dalam air buangan penduduk (tinja) dan sisa makanan.
Perbedaan nilai rata-rata kadar fosfat perstasiun disajikan dalam histogram seperti pada gambar 6.
Gambar 6. Nilai rata-rata analisis fosfat perstasiun.
Berdasarkan hasil analisis diperoleh nilai rata-rata fosfat pada masing-
0.28
0.26 0.26
0.25 0.255 0.26 0.265 0.27 0.275 0.28 0.285
Stasiun Satu Stasiun Dua Stasiun Tiga
Nilai rata-rata fosfat perstasiun
dengan nilai fosfat 0.26 mg/l, dan stasiun III dengan nilai fosfat 0.26 mg/l, yang menunjukkan bahwa perairan pada semua stasiun penelitian waduk Bilibilli zona II merupakan perairan yang melewati batas optimal seperti yang tercantum dalam baku mutu air kelas dua PP 82 tahun 2001 menyaratkan kandungan total pospor sebagai fosfat maksimal 0.2 mg/l. Hal ini menunjukkan bahwa perairan tersebut tidak layak dilakukan usaha budidaya karena kandungan fosfat telah mengalami eutrofikasi. Eutrofikasi yaitu pencemaran air yang disebabkan oleh munculnya nutrient yang berlebihan kedalam ekostem air. Air dikatakan eutrofikasi jika konsentrasi fosfat dalam air berada pada rentang 0.035 – 0.1 mg/l (Saefumillah, 2002).
V. PENUTUP
5.1. Kesimpulan
Oksigen terlarut dan amoniak pada waduk Bilibili Kabupaten Gowa masih berada dalam kondisi baik dengan mengacu pada literatur kelayakan budidaya air tawar sedangkan pH dan fosfat terindikasi melewati batas baku mutu kualitas air (tidak dapat dilakukan budidaya) karena kandungan pH berkisar 8.69 – 9.92 dan kandungan fosfat <0.001 – 0.59 mg/l.
5.2. Saran
1. Persepsi masyarakat sekitar perairan waduk masih rendah, maka perlu melakukan upaya peningkatan kesadaran masyarakat untuk tidak membuang limbah langsung ke perairan waduk. Hal ini dapat dilakukan dengan penyuluhan dan pelatihan serta sosialisasi pada masyarakat sekitar perairan waduk. Selain itu, penekanan beban limbah ke perairan waduk dapat dilakukan dengan mengupayakan peningkatan fasilitas sanitasi lingkungan de sekitar perairan danau.
2. Air limbah rumah tangga (domestic) dan air dari pertanian hendaknya diolah terlebih dahulu sebelum dibuang kesaluran pembuangan yang menuju kearah waduk dengan maksud untuk menjaga kualitas air.
3. Kegiatan pemantauan dan pengelolaan haruslah terus dilakukan guna mengetahui status kualitas air waduk Bilibili apakah mengalami penurunan atau kenaikan.
DAFTAR PUSTAKA
Akbar S dan Sudaryanto, (2001). Pembenihan dan Pembesaran Kerapu Bebek.
Penerbit Penebar Swadaya, Jakarta.
Ardiwijaya, R.R. 2002. Distribusi horizontal klorofil-a dan hubungannya dengan kandungan unsur hara serta kelimpahan fitoplankton di Teluk Semangka, Lampung. Skripsi (tidak dipublikasikan). Program Studi MSP. FP IK. IPB.
Bogor.
Asmawi, S. 1984. Pemeliharaan Ikan dan Ekosikologi Pencemaran. UI Press.
Jakarta.
Barus, T.A. 2004. Pengantar Limnologi, Studi Tentang Ekosistem Sungai dan Danau. Jurusan Biologi Fakultas MIPA USU. Medan.
Barus, T.A. 2007. Keanekaragaman Hayati Ekosistem Danau Toba dan Upaya Pelestariannya. Pidato Pengukuhan Jabatan Guru Besar Tetap Bidang Ilmu Limnologi pada Fakultas MIPA USU. Medan. 3 Februari 2007.
Beveridge, M.C.M. 1984. The environmental impact of freshwater cage and pen fish farming and the use of simple models to predict carrying capacity.
FAO Technical Paper No. 255. Rome.
Boyd, C.E. 1982. Water Quality in Warm Water Fish Pond. Auburn University Agricultural Experimenta Satation. Auburn Alabama.
Brotowijoyo M D,. Dj. Tribawono., E. Mulbyantoro. 1995. Pengantar Lingkungan Perairan Budidaya Air. Penerbit Liberty, Yogyakarta.
Cahyono, Bambang. (2000). Budi Daya Ikan Air Tawar. Penerbit: Kanisius.
Yogyakarta.
Dojildo, J.R., and G.A. Best. 1992. Chemistry of Water and Water Pollution. Ellis Horwood Limited. New York.
Effendi, H. (2003).Telaah Kualitas Air: Bagi Pengelolaan Sumber Daya dan Lingkungan Perairan. Yogyakarta: Kanisius.
EPA. 1973. Water Quality Criteria. Ecological Research Series. Washington:
595p.
Frits Tatangindatu, Ockstan Kalesaran, Robert Rompas., 2013. Laporan Penelitian Studi Parameter Fisika Kimia Air pada Areal Budidaya Ikan di Danau Tondano, Desa Paleloan, Kabupaten Minahasa. 8-19 halaman.
Hardjojo B dan Djokosetiyanto. 2005. Pengukuran dan Analisis Kualitas Air.
Edisi kesatu, Modul 1 – 6. Universitas Terbuka. Jakarta.
Jeffries, M., and D. Mills. 1996. Freshwater Ecology, Principles and Applications. John Wiley and Sons. Chicester UK.
Kep MENLH No. 51 Tahun 2004. Podoman Baku Mutu Air Laut Untuk Budidaya Biota Laut.
Kordi G, Tancung AB. 2005. Pengelolaan Kualitas Air Dalam Budidaya Perairan. Rineka Cipta. Jakarta.
Kusuma, E. M. (2005). Kajian Perubahan Kualitas Air Sungai Code Setelah Melewati Kawasan Perkotaan. Skripsi. Yogyakarta: Fakultas Geografi UGM.
Liaw, M.K., 1969. Chemical and biological Studies of Fish Pond and Reseoir in Taiwan. Chine-American join Comission on rural reconstruction fish series.
Lohoo s.v., Moningkey R, 1998. Evaluasi Kandungan Sulfida (H2S) dan Amoniak (NH3) Terlarut pada Wadah Pemeliharaan Ikan Dengan Sistem Terapung di Danau Tondano. Jurnal Reseach And Development, 19 (18); Hal 49-54.
Mahida, U. N. 1993. Pencemaran air dan pemanfaatan limbah industri. PT. Raja Grafindo Persada. Jakarta.
Marganof. 2007. Modal pengendalian pencemaran perairan di danau maninjau sumatera barat, Laporan Hasil Penelitian Sekolah Pasca Sarjana IPB Bogor.
Nixon, S.W. 1995. Coastal marine eutrophication: a defijition, sosial causes, and future concens. Ophelia, 41:199-219
Novonty, V., and H. Olem. 1994. Water Quality, Prevention, Identification and Management of Diffuse Pollution. Van Nostrans Reinhold. New York.
Olivia. 2012. Studi Kualitas Air Disungai Kahayan. Universitas Kristen Palangka Raya. Skripsi 25 Hal.
Pescod, M.B. 1973. Invfestigation of Nasional Efluent and Steram Standar for Tropical Countries. AIT. Bangkok.
PP No. 82 Tahun 2001. Standar Baku Mutu Air (Kelas II) Untuk Kegiatan Budidaya.
Puspowardoyo, Harsono. (1992). Membudidayakan Gurami Secara Intensif.
Saefumillah, Asep. 2002. Eutrofikasi Problem Lingkungan Berskala Global.
http://www.limnologi.lipi.co.id/dip/ringkasan.html
Sawyer,C.N. and P.L.Mc.Carty. 1978. Chemistri For Environmental Engineering.
3nd Ed. Mc. Graw Hill Kogakusha Ltd.
Sastrawijaya A T. 2000. Pencemaran Lingkungan. Penerbit Rineka Cipta, Jakarta.
SNI 6989.57:2008. Air dan air limbah – bagian 57; Metode pengambilan contoh air permukaan. ICS 13.060.50 Badan Standardisasi Nasional.
Sudja, W.A. 1985. Ilmu Kimia Lingkungan. jakarta: universitas terbuka
Sumardianto. 1995. Struktur Komunitas Fitoplankton di perairan Teluk Pelabuhan Ratu, Jawa Barat. Program Studi Manajemen Sumberdaya Perairan Fakultas Perikanan Institut Pertanian Bogor, Bogor. 57 p.
Van Wyk P dan John Scarpa. 1999. Water Quality requiremente and management. Chapter 8 in. Farming Marine Shrip in Recirculating Freshwatwer System. Prepared by Peter Van Wyk. Megan Davishodgkins, rolland Laramore, Kevan L. Main, Joe Mountain, John Scarpa. Florida Departement of Agriculture and Consumers Servis. Horbor Branch Oceanographic Institution.
Wardhana, W. A. 1995. Dampak Pencemaran Lingkungan. Yogyakarta: Andi Offset
Wardoyo, S.T.H. 1989. Kriteria Kualitas Air untuk Pertanian dan Perikanan.
Makalah pada Seminar Pengendalia Pencemaran Air, Dirjen Pengairan Departemen Pekerjaan Umum, Bandung.
Wetzel, R.O. 1975. Limnologi. Sounders Collage Publishing. USA.
Lampiran 1. Hasil Pengukuran pH Waduk Bilibili Zona II Minggu Pertama Sampai Minggu Keempat.
Minggu Ulangan Stasiun Waktu
Pengamatan 1 2 3
I
1 8.2 8.37 8.36 9:34
2 8.27 8.38 8.29 9:50
3 8.34 8.4 8.33 10:09
Total 24.81 25.15 24.98
Rata-rata 8.27 8.39 8.33
II
1 8.45 8.52 8.75 9:31
2 8.47 8.53 7.85 9:47
3 8.36 8.88 8.67 10:04
Total 25.28 25.93 25.27
Rata-rata 8.43 8.65 8.43
III
1 8.71 9.33 10.28 7:06
2 9.33 8.84 10.62 7:21
3 11.7 8.83 8.86 7:35
Total 29.74 27 29.76
Rata-rata 9.92 9 9.92
IV
1 9.27 8.64 8.51 8:40
2 9.29 9.41 8.62 8:54
3 9.31 9.31 9.83 9:05
Total 27.87 27.36 26.96
Rata-rata 9.29 9.12 8.99
Lampiran 2. Hasil Rata-Rata Pengukuran pH Waduk Bilibili Zona II Minggu Pertama Sampai Minggu Keempat.
Minggu Pengamatan Stasiun
Rata-rata
Satu Dua Tiga
I 8.27 8.39 8.33 8.33
II 8.43 8.65 8.43 8.51
III 9.92 9 9.92 9.61
IV 9.29 9.12 8.99 9.14
Rata-rata 8.98 8.79 8.92
Lampiran 3. Hasil Pengukuran DO (Oksigen Terlarut) Waduk Bilibili Zona II Minggu Pertama Sampai Minggu Keempat.
Minggu Ulangan Stasiun Waktu
Pengamatan 1 2 3
I
1 8.22 8.74 7.91 9:34
2 7.76 8.63 8.2 9:50
3 7.9 8.53 8.4 10:09
Total 23.88 25.9 24.51
Rata-rata 7.96 8.64 8.17
II
1 7.86 7.99 8.85 9:31
2 7.75 7.79 8.89 9:47
3 7.69 7.67 8.81 10:04
Total 23.3 23.45 26.55
Rata-rata 7.77 7.82 8.85
III
1 8.23 8.23 7.54 7:06
2 8.7 8.19 7.7 7:21
3 8.26 8.2 8.04 7:35
Total 25.19 24.62 23.28
Rata-rata 8.4 8.21 7.76
IV
1 6.09 6.53 6.27 8:40
2 6.19 6.58 6.13 8:54
3 6.3 6.49 6.32 9:05
Total 18.58 19.6 18.72
Rata-rata 6.2 6.54 6.24
Lampiran 4. Hasil Rata-Rata Pengukuran DO (Oksigen Terlarut) Waduk Bilibili Zona II Minggu Pertama Sampai Minggu Keempat.
Minggu Pengamatan Stasiun
Rata-rata
1 2 3
I 7.96 8.64 8.17 8.26
II 7.77 7.82 8.85 8.15
III 8.4 8.21 7.76 8.13
IV 6.2 6.54 6.24 6.33
Rata-rata 7.59 7.81 7.76