Isolasi
β
-sitosterol dari Enhalus acoroides (Linn. f.) Royle serta
Uji Aktivitasnya terhadap Streptococcus mutans
Reski Ramdani1,a, Maulidyah2,b, Prima Endang Susilowati3,c, 1,2,3
Departemen Kimia, Fakultas Matematika dan Ilmu Pengetahuan Alam, Universitas Halu Oleo, Kendari.
a
E-mail: [email protected], bE-mail: [email protected],
c
E-mail: [email protected],
Abstrak
Telah dilakukan penelitian isolasi dan identifikasi senyawa metabolit sekunder dari lamun Enhalus acoroides (Linn. f.) Royle serta uji aktivitasnya terhadap bakteri Streptococcus mutans. Penelitian ini bertujuan untuk mengisolasi senyawa metabolit sekunder dari ekstrak metanol Enhalus acoroides (Linn. f.) Royle dari Tanjung Tiram, Sulawesi Tenggara serta aktivitasnya terhadap Streptococcus mutans. Teknik isolasi senyawa metabolit sekunder dilakukan dengan metode ekstraksi secara maserasi menggunakan pelarut metanol. Pemisahan dan pemurnian senyawa dilakukan dengan Kromatografi Lapis Tipis (KLT) dan Kromatografi Kolom Gravitasi (KKG) menggunakan campuran eluen n-heksana : etil asetat secara gradien. Proses identifikasi senyawa isolat dilakukan dengan spektroskopi Nuclear Magnetic Resonance (NMR) 1-D yang meliputi 1H-NMR dan 13C-NMR teknik DEPT. Telah berhasil diisolasi senyawa berbentuk kristal jarum berwarna putih. Berdasarkan analisis data spektroskopi NMR, menunjukkan senyawa tersebut adalah β -sitosterol. Aktivitas ekstrak metanol dari Enhalus acoroides dengan konsentrasi 1000 g/mL, 500 g/mL, 250
g/mL, dan 100 g/mL menunjukkan adanya aktivitas terhadap Streptococcus mutans dengan besar diameter daerah hambat pada masing-masing konsentrasi berturut-turut adalah 12,66 mm, 9,93 mm, 7,2 mm, dan 4,4 mm. Hasil uji aktivitas senyawa isolat dengan konsentrasi 500 g/mL, 250 g/mL, 100 g/mL, dan 50 g/mL tidak menunjukkan adanya aktivitas terhadap Streptococcus mutans.
Kata kunci: Lamun, Enhalus acoroides (Linn. f.) Royle, β-sitosterol, Streptococcus mutans
Abstract
Isolation and identification of secondary metabolite compound from seagrass Enhalus acoroides (Linn. f.) Royle and its activity assay against Streptococcus mutans has been carried out. This research aimed to isolates a secondary metabolite compound from methanol extract of Enhalus acoroides and its activity against Streptococcus mutans. The isolation of chemical compounds was performed by extraction with maceration technique using methanol. Separation and purification performed by Thin Layer Chromatography (TLC), and Gravity Column Chromatography (GCC) using a gradient eluen mixture of n-hexane : ethyl acetate. Identification of isolated compound was done by using Nuclear Magnetic Resonance (NMR) 1-D spectroscopy (1H-NMR and 13C-NMR with DEPT technique). The form of isolated compound was white needle crystals. Based on NMR spectroscopy analysis with DEPT technique, showed that the compound was β-sitosterol. The activity of methanol extract from Enhalus acoroides against Streptococcus mutans with concentrations 1000 g/mL, 500g/mL, 250g/mL, and 100g/mL showed an activity with diameter of inhibition were 12,66 mm, 9,93 mm, 7,2 mm, and 4,4 mm respectively. The activity of isolated compound with concentrations 500g/mL, 250g/mL, 100g/mL and 50 g/mL showed that the isolated compound did not have any activity against Streptococcus mutans.
1. PENDAHULUAN
Indonesia merupakan salah satu
negara dengan iklim tropis yang memiliki
keanekaragaman hayati terbesar kedua di
dunia. Survei dari PT. Eisai menyatakan,
terdapat sekitar 7000 spesies tanaman obat
di Indonesia, atau sekitar 90% dari seluruh
jenis tanaman obat yang ditemukan di
Asia. Jumlah tersebut masih sedikit sekali
yang dimanfaatkan dalam pengobatan.
Oleh karena itu, diperlukan eksplorasi
senyawa
metabolit
sekunder
dari
tumbuhan sehingga kedepannya dapat
dimanfaatkan
dengan
maksimal.
Tumbuhan memiliki banyak manfaat
khususnya dalam bidang farmasi dan
kesehatan
karena
senyawa
metabolit
sekunder yang dikandungnya.
Wilayah perairan yang sangat luas
sekitar 5.176.800 km
2dengan garis pantai
terpanjang kedua di dunia 81.290 km
(Dinas Kelautan dan Perikanan, 2009)
menyimpan banyak potensi sumberdaya
alam hayati laut yang dapat dikembangkan
sebagai bahan pangan, kosmetika dan
obat-obatan.
Salah satu tumbuhan yang
kaya akan kandungan senyawa bioaktif
adalah lamun. Telah banyak laporan
mengenai potensi lamun diantaranya
antifungi (Arumugam,
et al.
, 2010),
antiviral
(Rowley
et
al.,
2002),
antiinflamasi
(Hua
et
al.,
2006),
antidiabetes (Gokce & Haznedaroglu,
2008)
dan
aktivitas
antioksidan
(Athiperumalsamy, 2010).
Lamun (
seagrass
) termasuk dalam
sub
kelas
monocotyledonae
dan
merupakan tumbuhan berbunga (kelas
angiospermae
).
Secara
struktur
dan
fungsional, lamun memiliki kesamaan
dengan tumbuhan pada umumnya (Sidik,
2012). Telah diketahui bahwa lamun
memproduksi metabolit sekunder yang
berpotensi mengurangi atau mengontrol
pertumbuhan mikroba (Arlyza, 2008).
Ekstrak lamun jenis
Halophila
ovalis
dan
Halodule pinifolia
telah
terbukti memiliki aktivitas antibakteri
terhadap
Acinetobacter
sp,
Salmonella
typhi, Proteus
mirabilis
dan
Pseudomonas
aeruginosa (
Ummaheshwari
et al.,
2009
).
Cymodocea nodosa
mempunyai aktivitas
terhadap
Bacillus subtilis
NIOF
, S. aureus
NTOF, dan
P. aeruginosa
ATCC 10145
dan lamun
Ruppia cirrhosa
mempunyai
aktivitas terhadap
Bacillus subtilis
NIOF,
S. aurous
NTOF,
E. coli
NIOF dan
P.
aeruginosa
ATCC 10145 (El-hady
et al.
,
2007). Ekstrak methanol
Potamogeton
pectinatus
L.
(sago
pondweed),
Potamogeton perfoliatus L. (redhead
grass)
dan
Ruppia maritima L. (wigeon
grass
)
menghambat
pertumbuhan
Micrococcus,
Staphylococcus,
Streptococcus,
Bacillus,
Aerococcus,
Mycobacterium, Corynebacterium, Vibrio,
Listonella
dan
Pasteurella
(Paul &
Stephen, 2006).
Penyakit
infeksi
merupakan
penyakit yang disebabkan oleh bakteri,
Beberapa
jenis
bakteri
yang
pada
umumnya
menyebabkan
terjadinya
penyakit infeksi adalah
Escherichia coli,
Staphylococcus aureus,
dan
Salmonella
typhii.
Di Indonesia penyakit infeksi masih
menduduki peringkat atas dalam hal
penyebarannya.
Pengobatan
utama
penyakit infeksi yang disebabkan oleh
bakteri adalah antibakteri. Antibakteri
merupakan suatu senyawa yang dapat
mencegah proses pertumbuhan bakteri.
Karies gigi yang disebabkan oleh
bakteri
Streptococcus mutans
menempati
urutan pertama penyakit infeksi gigi dan
mulut yang paling banyak diderita mulai
dari anak kecil hingga orang dewasa.
Karies gigi berawal dari interaksi antara
bakteri plak, diet, dan gigi. Salah satu cara
pencegahan karies adalah mengusahakan
agar pembentukan plak pada permukaan
gigi dapat dibatasi baik. Pengendalian plak
dapat dilakukan dengan cara pembersihan
plak secara mekanis dan penggunaan
bahan antibakteri terutama untuk menekan
pertumbuhan
S. mutans
.
penyakit seperti demam, sakit gigi,
penyakit
kulit,
nyeri
otot,
masalah
pencernaan dan juga meredakan sengatan
serangga dan kalajengking (Torre-Castro
et al
., 2004). Lamun juga telah digunakan
sebagai obat pembesaran vena jurcularis
dan sebagai obat kelenjar
tuberculosa
(TBC) (Subagiyo, 2010) serta telah
digunakan
sebagai
obat
untuk
penyembuhan
luka
dan
kudis
(Parthasarathy
et al.,
1991). Pemanfaatan
lamun
E. acoroides
dalam bidang farmasi
dan
kesehatan
sangat
memerlukan
penelitian
tentang
bioaktivitasnya,
khususnya terhadap bakteri patogen yang
sering menginfeksi manusia, salah satunya
adalah bakteri
Streptococcus mutans
.
2. METODE PENELITIANa. Alat dan Bahan Penelitian
Alat-alat yang digunakan pada
penelitian
ini
yaitu
rotary
vacuum
evaporator
(Buchii), oven (
Gallenkamp
Civilab-Australia
), autoklaf (
All American,
model
No.
25X),
spektrofotometer
Nuclear Magnetic Resonance
(NMR)
(
JEOL JNM ECA
500, 500 MHz),
spektrofotometer UV-Vis,
laminar air
flow
, timbangan analitik (
Explorer Ohaus
),
lampu
UV
(
Damstadt
Germany
),
Spektrofotometer UV-Vis, seperangkat
alat kromatografi kolom gravitasi, pipet
tetes. Alat-alat gelas yaitu, erlenmeyer
berbagai
ukuran
(
Pyrex
),
chamber
(
Duran
), gelas ukur (
Pyrex
), gelas kimia
(
Pyrex
), pipet ukur (
Pyrex
), pipet volume
(
Pyrex
), cawan petri. Peralatan pendukung,
yaitu bunsen, batang pengaduk, kawat ose,
statif dan klem, botol ampul, kaca,
cutter
,
penotol/pipa kapiler, mistar, dan pisau.
Bahan yang digunakan dalam
penelitian ini yaitu tumbuhan Enhalus acoroides (Linn. f.) Royle, metanol teknis, aseton teknis, etil asetat teknis, n-heksana teknis, CeSO4, aquades, kertas saring
Whatman 42, silika GF254 (E. Merck), silika
gel G.60 (E. Merck), media Luria Bertani, dan Streptococcus mutans.
b. Preparasi Sampel Penelitian
Lamun yang digunakan dalam
penelitian ini berasal dari daerah pesisir
Tanjung
Tiram,
Kendari,
Provinsi
Sulawesi Tenggara. Sampel selanjutnya
dibersihkan dari lumpur, dicuci dengan air
tawar, dan dikeringkan. Kemudian sampel
dihaluskan hingga menjadi serbuk dan
diproses lebih lanjut di laboratorium.
c. EkstraksiSerbuk
E. acoroides
sebanyak 450
gram diekstraksi menggunakan metanol
dengan perbandingan 2:1 (pelarut dan
sampel) selama 3x24 jam dan dilakukan
penyaringan dilakukan setiap 1x24 jam.
Residu
sisa
penyaringan
dimaserasi
kembali menggunakan pelarut yang sama.
Filtrat
selanjutnya
dikumpulkan
dan
dipekatkan menggunakan
rotary vacuum
evaporator
hingga
diperoleh
ekstrak
metanol.
d. Pemisahan dan Pemurnian
1.) Kromatografi Lapis Tipis (KLT)
Ekstrak pekat yang diperoleh di uji dengan KLT menggunakan sistem pelarut n -heksana dan etil asetat. Pelarut yang digunakan dimulai dengan pelarut n-heksana yang paling polar kemudian ditingkatkan kepolarannya dengan mencampurkan etil asetat secara gradien. Setiap noda yang muncul diamati pemisahannya dan dihitung nilai Rf-nya.
2.) Kromatografi Kolom Gravitasi (KKG)
Ekstrak pekat diimpregnasi
menggunakan silica gel G.60 dengan
perbandingan 2:1 (berat silika gel G.60 : berat ekstrak). Ekstrak pekat yang telah diimpregnasi dimasukkan ke dalam kolom
kromatografi yang telah disiapkan
sebelumnya. Perbandingan eluen dibuat berdasarkan referensi dari KLT sebelumnya. Fraksi hasil KKG ditampung dalam vial dan diberi kode sesuai urutan fraksinya. Masing-masing fraksi diuji pola pembentukan nodanya dengan menggunakan metode KLT. Fraksi dengan noda yang sama dapat digabung kembali untuk memperkaya jumlah komponen yang akan diisolasi.
3.) Uji Kemurnian
Fraksi hasil KKG yang telah
e. Identifikasi
Isolat murni yang telah diperoleh diidentifikasi strukturnya menggunakan spektrofotometer 1H-NMR dan 13C-NMR dengan teknik DEPT menggunakan pelarut CDCl3. Data yang dihasilkan, diinterpretasi
dengan cara membandingkannya dengan literatur.
f. Uji Antibakteri
Tahap uji antibakteri meliputi beberapa tahapan, yaitu tahap sterilisasi alat, pembuatan dan sterilisasi media, kultur mikroorganisme uji, pembuatan larutan fisiologis, pembuatan suspensi bakteri dan pengujian antibakteri.
1.) Pembuatan dan Sterilisasi Media
Untuk uji antibakteri digunakan
media pertumbuhan Luria Bertani
(LB).
Pembuatan
media
dibuat
dengan
melarutkan 0,25 g pepton, 0,25 g
yeast
extract
, 0,75 g NaCl, 0,45 g MgSO
4.2H
2O
dan 4 g agar dengan 150 mL akuades.
Media pertumbuhan disterilkan dalam
autoklaf pada tekanan 1 atm dan suhu
121
oC selama 15 menit.
2.)
Kultur Bakteri Streptococcus mutansStreptococcus mutans
ditumbuhkan
dengan cara memindahkan biakan yang
ada pada media agar miring sebanyak 1
atau 2 ose ke dalam botol ampul berisi
media Luria Bertani (LB) cair dan
diinkubasi selama 24 jam pada suhu
37±2
oC.
3.) Pembuatan Larutan Fisiologis NaCl 0,9%
Larutan fisiologis NaCl 0,9% dibuat dengan melarutkan 0,9 g NaCl padat dalam 10 mL aquades dan mengencerkan larutan tersebut dalam labu takar 100 mL. Larutan NaCl 0,9% yang telah dibuat disterilisasi dalam autoclave pada suhu 121oC dan tekanan 1 atm selama 15 menit.
4.) Pembuatan Suspensi Bakteri
Bakteri yang telah diremajakan, disuspensikan ke dalam larutan fisiologis NaCl 0,9%. Kekeruhan media disesuaikan dengan standar Mc. Farland 0,5 menggunakan spektrofotometer UV-Vis pada panjang gelombang (λ) 625 nm.
g. Pengujian Aktivitas Antibakteri
Metode ini dilakukan dengan cara menginokulasikan suspensi bakteri uji ke
dalam 15 mL media agar yang telah dicairkan dalam cawan petri steril dan kemudian dibiarkan menjadi padat. Kertas cakram steril berdiameter 6 mm dicelupkan dalam zat uji (Adyana et al., 2004). Ekstrak metanol dibuat dalam beberapa konsentrasi yakni, 1000, 500, 250, dan 100 g/mL. Senyawa isolat dibuat dengan variasi kosentrasi 50, 100, 250 dan 500
g/mL. Hasil uji daya hambat antibakteri didasarkan pada pengukuran diameter daerah hambat (DDH) pertumbuhan bakteri yang terbentuk di sekeliling kertas cakram (Noor et al., 2006).
3. HASIL DAN PEMBAHASAN a. Isolasi Senyawa Metabolit Sekunder
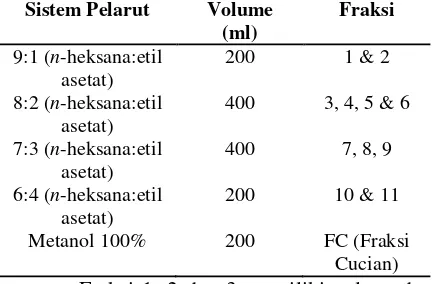
Ekstrak E. acoroides sebanyak 1,8 g dipisahkan dengan teknik kromatografi kolom gravitasi dengan fasa diam berupa silika gel G.60 dan fasa gerak berupa campuran eluen yang dibuat berdasarkan hasil uji pemisahan noda menggunakan teknik KLT. Campuran eluen yang digunakan dapat diamati pada Tabel 1.
Tabel 1. Campuran pelarut yang digunakan pada proses KKG
Sistem Pelarut Volume (ml)
Fraksi
9:1 (n-heksana:etil asetat)
200 1 & 2
8:2 (n-heksana:etil asetat)
400 3, 4, 5 & 6
7:3 (n-heksana:etil asetat)
400 7, 8, 9
6:4 (n-heksana:etil asetat)
200 10 & 11
Metanol 100% 200 FC (Fraksi Cucian)
Fraksi 1, 2 dan 3 memiliki pola noda yang relatif sama, sehingga dilakukan penggabungan dan diberi nama fraksi A1. Fraksi A1 berwujud kristal jarum berwarna putih. Hasil KLT fraksi gabungan A1 menunjukkan pola noda yang sudah dapat dipisahkan sehingga dilakukan rekristalisasi pada kristal dari fraksi gabungan A1.
dilakukan uji kemurnian dengan tiga sistem pelarut menggunakan teknik KLT. Hasil KLT senyawa isolat dapat dilihat pada Gambar 1.
Gambar 1. Kromatogram senyawa isolat dengan 3 sistem eluen dibawah sinar UV 254 nm. (a) eluen kloroform : aseton (8:2); (b) eluen n -heksan : etil asetat (8:2); (c) n-heksan : kloroform : metanol (8:1,5:0,5)
Hasil KLT dengan tiga sistem eluen menunjukkan pola noda tunggal sehingga isolat yang diperoleh dapat dikatakan sudah murni.
b. Identifikasi Struktur Isolat
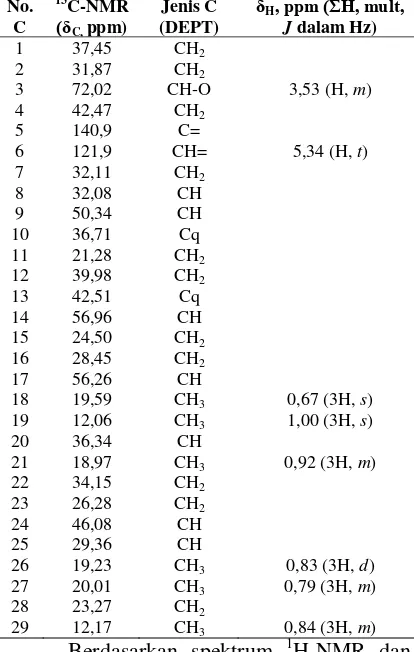
Senyawa isolat yang telah diperoleh diidentifikasi strukturnya menggunakan spektrofotometer 1H-NMR dan 13C-NMR. Hasil identifikasi dapat diamati pada Tabel 2.
Tabel 2. Data NMR senyawa isolat
No. C
13C-NMR (δC, ppm)
Jenis C (DEPT)
δH, ppm (ΣH, mult,
J dalam Hz)
1 37,45 CH2 2 31,87 CH2
3 72,02 CH-O 3,53 (H, m) 4 42,47 CH2
5 140,9 C=
6 121,9 CH= 5,34 (H, t) 7 32,11 CH2
8 32,08 CH 9 50,34 CH 10 36,71 Cq 11 21,28 CH2 12 39,98 CH2 13 42,51 Cq 14 56,96 CH 15 24,50 CH2 16 28,45 CH2 17 56,26 CH
18 19,59 CH3 0,67 (3H, s) 19 12,06 CH3 1,00 (3H, s) 20 36,34 CH
21 18,97 CH3 0,92 (3H, m) 22 34,15 CH2
23 26,28 CH2 24 46,08 CH 25 29,36 CH
26 19,23 CH3 0,83 (3H, d) 27 20,01 CH3 0,79 (3H, m) 28 23,27 CH2
29 12,17 CH3 0,84 (3H, m) Berdasarkan spektrum 1H-NMR dan
13
C-NMR dengan resolusi 500 MHz pada
Tabel 2 menunjukkan bahwa terdapat 50 jenis atom H dalam lingkungan yang berbeda serta 29 jenis atom C yang menyatakan keberadaan 29 atom C dalam struktur senyawa isolat.
Satu signal proton multiplet dengan 1H pada δH = 3,53 ppm diduga berasal dari
gugus metin yang berikatan dengan gugus hidroksi (-OH). Hal yang sama juga terjadi pada pergeseran kimia δH = 5,34 ppm yang
menunjukkan adanya 1 proton multiplet dengan intensitas 1H yang berikatan dengan atom Csp2 (-C=CH) mengakibatkan awan-awan elektron pada atom karbon membentuk ikatan phi sehingga elektron disekitar atom H yang terikat kurang terlindungi dan mengalami pergeseran kimia yang tinggi (Supratman, 2010).
Data 13C-NMR menunjukkan adanya pergesaran kimia sebesar 140,9 ppm yang menunjukan adanya karbon kuartener dan karbon metin juga muncul pada pergeseran kimia 121,9 ppm. Kedua atom karbon tersebut memungkinkan untuk membentuk suatu ikatan rangkap. Signal karbon metin pada pergeseran kimia 71,9 ppm mengindikasikan adanya atom oksigen yang terikat sehingga elektron di sekitar atom C tertarik menuju atom O yang lebih elektronegatif dan menurunkan kerapatan elektron pada atom C tersebut sehingga mengalami pergeseran yang cukup tinggi.
Rumus struktur senyawa isolat dapat digunakan untuk menentukan jenis ikatan yang terdapat dalam struktur senyawa isolat yaitu dengan cara menghitung nilai Double Bond Equivalent (DBE). Persamaan DBE adalah sebagai berikut:
DBE = (1+C) – 0,5(H+X) + 0,5 (N+P) (1)
Keterangan; C = Jumlah Atom Karbon H = Jumlah Atom Hidrogen X = Jumlah Atom Halogen N = Jumlah Atom Nitrogen P = Jumlah Atom Fosfor
HO
Gambar 2. Struktur senyawa isolat
c. Aktivitas Antibakteri
1.) Aktivitas Antibakteri Ekstrak E. calophrys
Uji aktivitas antibakteri ekstrak E. calophrys menggunakan senyawa uji berupa ekstrak E. calophrys yang dilarutkan dalam metanol (792 kg/m3) dengan menggunakan metode difusi kertas cakram (diameter kertas cakram = 6 mm). Kontrol positif yang digunakan adalah larutan ampisilin 250 µg/mL dan kontrol negatif adalah metanol. Hasil uji aktivitas dapat diamati pada Tabel 3.
Tabel 3. Data aktivitas antibakteri ekstrak E. acoroides
Pengulangan
Diameter Zona Bening (mm) Ekstrak Metanol (g/mL) Kontrol Positif Ket: Kontrol negatif = metanol
Kontrol positif = larutan ampisilin 250 µg/mL
Berdasarkan hasil uji yang dilakukan, ekstrak metanol E. acoroides memiliki aktivitas yang cukup baik terhadap bakteri S. mutans jika dilihat dari diameter zona hambat
yang terbentuk pada masing-masing
konsentrasi. Efek penghambatan oleh ekstrak metanol lamun jenis E. acoroides terhadap bakteri S. mutans dapat disebabkan oleh dua faktor. Faktor pertama dapat disebabkan oleh adanya suatu senyawa aktif yang terkandung di dalam ekstrak yang berpotensi menghambat
pertumbuhan bakteri uji dan juga
mematikannya (Wattimena, 1991). Faktor
kedua adalah senyawa-senyawa yang
terkandung dalam ekstrak metanol dari E. acoroides tersebut bersimbion satu sama lain sehingga memiliki potensi dalam menghambat bahkan membunuh bakteri uji (Siagian, 2002)
Ekstrak dengan konsentrasi 250
g/mL dapat dikatakan konsentrasi yang paling baik karena diameter zona hambat yang terbentuk pada ekstrak metanol dengan konsentrasi tersebut tidak jauh berbeda dengan senyawa antibiotik pembanding yakni
ampisilin 250 µg/mL. Hasil uji ekstrak metanol terhadap S. mutans pada kosentrasi 250 g/ml memiliki zona bening dengan nilai rata-rata sebesar 7,6 mm.
2.) Aktivitas Antibakteri Senyawa Isolat
Uji aktivitas antibakteri senyawa isolat menggunakan senyawa uji berupa senyawa isolat yang dilarutkan dalam etil asetat (897 kg/m3), kontrol positif yang digunakan adalah larutan ampisilin 250 µg/mL serta kontrol negatif yang digunakan adalah etil asetat. Hasil uji aktivitas antibakteri senyawa isolat dapat dilihat pada Tabel 4.
Tabel 4. Data aktivitas antibakteri senyawa isolat
Pengulangan
Diameter Zona Bening (mm) Senyawa Isolat
Ket: Kontrol negatif = etil asetat
Kontrol positif = larutan ampisilin 250 µg/mL
Hasil uji aktivitas menunjukkan bahwa senyawa isolat yang berhasil diisolasi dari lamun jenis E. acoroides tidak mampu menghambat pertumbuhan bakteri uji karena tidak adanya zona bening yang terbentuk di sekitar kertas cakram. Jika dilihat dari strukturnya, senyawa isolat memiliki gugus hidroksil yang bersifat hidrofilik sehingga sukar menembus dinding sel bakteri yang bersifat hidrofobik yang menyebabkan keaktifannya lemah.
Senyawa isolat yang diperoleh adalah
-sitosterol (Gambar 2). Struktur senyawa tersebut memiliki empat siklik akan tetapi tidak memiliki jembatan oksigen dalam hal ini adalah eter siklik. Menurut Sutrisno, (2001) senyawa yang berbentuk siklik yang memiliki jembatan oksigen (R-O-R) dan memiliki gugus karbonil bersifat aktif, karena dapat bertindak sebagai interkalator DNA yang dapat disisipkan diantara dua unit pasangan basa pada DNA dan dapat berinteraksi dengan DNA melalui ikatan Van der Walls sehingga dapat merusak struktur double heliks dan mencegah proses replikasi DNA.
4. KESIMPULAN
Berdasarkan hasil penelitian dan pembahasan dalam penelitian ini, maka dapat ditarik kesimpulan sebagai berikut:
(Linn. f.) Royle menggunakan teknik ekstraksi maserasi dilanjutkan dengan kromatografi lapis tipis dan kromatografi kolom gravitasi. Setelah dilakukan identifikasi menggunakan spektroskopi
1
H-NMR dan 13C-NMR dengan teknik DEPT homonuklir (1-D) serta melalui penelusuran literatur, senyawa yang diperoleh adalah β-sitosterol.
2. Ekstrak metanol dengan konsentrasi 1000
g/mL, 500 g/mL, 250 g/mL, dan 100g/mL menunjukkan aktivitas yang baik terhadap Streptococcus mutans. Senyawa isolat tidak menunjukkan adanya aktivitas terhadap Streptococcus mutans.
UCAPAN TERIMA KASIH
Ucapan terima kasih kami ucapkan kepada Universitas Halu Oleo (UHO) yang telah memberikan fasilitas dalam mengerjakan penelitian ini, kepada Lembaga Ilmu Pengetahuan Indonesia (LIPI) yang telah membantu mengidentifikasi struktur senyawa isolat.
DAFTAR PUSTAKA
Adyana, I. K., Yulinah, E., Sigit, J. I., Fisheri, N., dan Insanu, M., 2004, Efek Ekstrak Daun Jambu Biji Daging Buah Putih dan Jambu Biji Daging Buah Merah sebagai Antidiare, Acta Pharmaceutica Indonesia, XXIX (1)
Arlyza, I. S., 2008, Ekstrak Lamun Sebagai
Sumber Alternatif Antibakteri
Penghambat Bakteri Pembentuk
Biofilm, Oseanologi dan Limnologi Indonesia, 34 (2): 223 - 241
Arumugam, R., Kannan R. R., Arivuselvan R. N. dan Anantharaman P., 2010, Antimicrobial potential of some seagrasses against phytopathogens, Seaweed Research and Utilization, 32:
177–183
Athiperumalsamy, T., Devi R. V., Hastha P. S., Kumar V. dan Louis J. L., 2010, Antioxidant activity of seagrasses and seaweeds, Botanica Marina, 53: 251– 257
Dinas Kelautan dan Perikanan (DKP), 2009, Penerapan Strategi Logistik dan Rantai Suplai untuk Mendukung Daya Saing Produk Kelautan dan Perikanan,
Makalah Dinas Kelautan dan
Perikanan.
El-Hady, H. H. A, Daboor S. M., dan Ghoniemy A. E., 2007, Nutritive and Antimicrobial Profiles of Some
Seagrass From Bardawil Lake, Egypt, Egyptian J. Aq. Research, 33: 103-110 Gokce, G., dan Haznedaroglu M. Z., 2008, Evaluation of antidiabetic, antioxidant and vasoprotective effects of Posidonia oceanica extract, Journal of Ethnopharmacology, 115:122–130 Hua, K. F., Hsu H. Y., Su Y. C., Lin I. F.,
Yang S. S. dan Chen, Y. M., 2006, Study on the anti-inflammatory activity of methanol extract from seagrass Zostera japonica, Journal of Agriculture and Food Chemistry, 54 (2): 306–311
Noor, M. S., Poeloengan M., dan Yulianti T.,
2006, Analisis Senyawa Kimia
Sekunder dan Uji Daya Antibakteri
Ekstrak Daun Tanjung
(Mimuusopselengi L) Terhadap
Salmonella typhi dan Shigella boydii,
Seminar Nasional Teknologi
Peternakan dan Veteriner
Paul, J. B., dan Stephen A. M., 2006, Antibacterial compounds in estuarine submersed aquatic plants, J. exp. Mar. Biol Ecol, 331: 41-50
Rowley, D. C., Hansen M. S. T., Rhodes D., Sotriffer C. A., Ni H. dan McCammon J. A., 2002, Thalassiolins A–C: New marine – Derived inhibitors of HIV
cDNA integrase. Bioorganic
Medicinal Chemistry,10: 3619–3625 Siagian, A., 2002, Mikroba Patogen pada
Makanan dan Sumber
Pencemarannya, Fakultas Kesehatan
Masyarakat Universitas Sumatera Utara
Sidik, J. B., 2012, The Marine Angiosperms, Seagrass, Universiti Putra Malaysia Press, Serdang
Sutrisno, Soedigdo, S., Ahmad, S., dan Buchari, 2001, Isolasi Pakirizin Dari Biji Bengkuang (Pchyrryhhizus erosus, urban) dan Uji Aktivitas
Sitotoksitnya, Jurnal Farmasi
Indonesia, 2: 34-35.
Ummaheshwari, R., Thirumaran G., dan Anantharaman P., 2009, Potential Anti bacterial Activities of Seagrasses from Vellar Estuary, Southeast Coast of India, Adv. Biol. Res. 3: 140-143
Wattimena, J. R., 1991, Farmakodinamik dan Terapan Antibiotik, Gadjah Mada