HIDROTERMAL MENGGUNAKAN MODE KOLOM
SKRIPSI
NATALIA BR. SIMATUPANG 150802031
PROGRAM STUDI KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUANALAM UNIVERSITAS SUMATERA UTARA
MEDAN
2019
SINTESIS ZEOLIT DARI LIMBAH ABU TERBANG (Fly Ash) BATUBARA SEBAGAI ADSORBEN UNTUK PENGURANGAN
ION LOGAM BERAT DARI AIR GAMBUT DENGAN METODE HIDROTERMAL MENGGUNAKAN MODE KOLOM
SKRIPSI
Diajukan untuk melengkapi tugas dan memenuhi syarat mencapai gelar Sarjana Sains
NATALIA BR. SIMATUPANG 150802031
PROGRAM STUDI KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUANALAM UNIVERSITAS SUMATERA UTARA
MEDAN
2019
Judul : Sintesis Zeolit Dari Abu Terbang (Fly Ash) Batubara Sebagai Adsorben Untuk Mengurangi Ion Logam Berat Dari Air Gambut Dengan Metode Hidrotermal Menggunakan Mode Kolom
Kategori : Skripsi
Nama : Natalia br Simatupang
NomorIndukMahasiswa : 150802031
Program Studi : Sarjana (S1) Kimia
Departemen : Kimia
Fakultas : Matematika dan Ilmu Pengetahuan Alam
(MIPA) Universitas Sumatera Utara
Disetujui di, Medan, Juli 2019
Disetujui Oleh
Departemen Kimia FMIPA USU
Ketua Program Studi, Pembimbing
Dr. Cut Fatimah Zuhra, M.Si Rikson Siburian Ph.D
NIP. 197404051999032001 NIP.194804141974031001
\
PERNYATAAN
SINTESIS ZEOLIT DARI LIMBAH ABU TERBANG (Fly Ash) BATUBARA SEBAGAI ADSORBEN UNTUK PENGURANGAN ION
LOGAM BERAT DARI AIR GAMBUT DENGAN METODE HIDROTERMAL MENGGUNAKAN MODE KOLOM
SKRIPSI
Medan, Juli 2019
Natalia Br. Simatupang
150802031
PENGHARGAAN
Puji dan syukur penulis panjatkan kepada Allah Tri Tunggal, Alla Bapa, Putranya Yesus Kristus dan Roh Kudus, karena atas berkat dan kasih karunia-Nya yang senantiasa dilimpahkan kepada penulis, penulis berhasil menyelesaikan penelitian dan skripsi ini tepat pada waktunya.
Ucapan terima kasih yang tak terhingga penulis sampaikan kepada orangtua saya yang saya sangat cintai, Bapak (Miduk Simatupang) dan Ibu(Dorlan Br Sagala)telah memberikan dukungan, kasih sayang, doa yang tiada berkesudahan serta dukungan moral dan materi. Ucapan kasih sayang dari penulis kepada kakak tercinta (Dewi Simatupang, Amd), (Siska Simatupang), Abang tercinta (Ranto Simatupang) dan kepada semua keluarga yang tidak dapat penulis sebutkan satu persatu yang turut memberikan dukungan hingga akhirnya penelitian ini dapat diselesaikan. Ucapan terima kasih yang sebesar-besarnya penulis sampaikan kepada kepala laboratorium Kimia Analitik Prof. Zul Alfian,M.Sc dan Bapak Rikson Siburian Ph.D selaku pembimbing saya, yang telah memberikan waktu, motivasi, membimbing dan mengarahkan serta memberikan saran kepada penulis yang sangat membantu penulis dalam menyelesaikan penelitian dan skripsi ini.Ucapan terima kasih juga saya sampaikan kepada Ibu Dr. Cut Fatimah Zuhra dan Dr. Ibu Sofia Lenny, S.Si, M.Si selaku Ketua dan Sekretaris Deaprtemen Kimia FMIPA USU. Ucapan terima kasih juga saya sampaikan kepada kak Sri Pratiwi Aritonang, M.Si, Cristina Simanjuntak, S.Si, Rosnani Harahap, S.Si selaku laboran yang telah memberikan bantuan dan saran kepada penulis. Juga rekan-rekan seperjuangan saya sebagai asisten Lab.Analitik Benhard, Hana, Yoanda, Athya, Achmad Muhajir, dan juga kepada adik-adik: Josua, Natasya, Sri, Admin, Indri, Aini, Dara, serta kepada teman saya:
Jelita Sitanggang, Winda Tambunan, Indah, Nur yang ikut membantu dan memberikan motivasi dan serta doa-doanya yang selalu menguatkan saya.
Semoga Tuhan membalas dengan segala yang terbaik. Tuhan Yesus Memberkati.
Amin
Medan, Juli 2019
Natalia Br. Simatupang
SINTESIS ZEOLIT DARI LIMBAH ABU TERBANG (Fly Ash) BATUBARA SEBAGAI ADSORBEN UNTUK PENGURANGAN ION LOGAM BERAT DARI AIR GAMBUT DENGAN METODE HIDROTERMAL
MENGGUNAKAN MODE KOLOM
ABSTRAK
Penelitian tentang sintesis zeolit dari abu terbang batubara dan aplikasinya sebagai adsorben untuk pengurangan ion logam berat dari air gambut telah dilakukan.
Tujuan dari penelitian ini adalah untuk (i) mengetahui pemanfaatan Sintesis Zeolit dari limbah batubara sebagai adsorben; (ii) mengetahui hasil effluent yang dihasilkan dari air gambut menjadi air bersih sesuai Peraturan Menteri Kesehatan Republik Indonesia. Zeolit disintesis dengan metode Hidrotermal dan dianalisis dengan X-Ray Fluoresensi (XRF). Spetrofotometri Serapan Atom (SSA). Kualitas air gambut dianalisis berdasarkan Peraturan Menteri Kesehatan Republik Indonesia No.492/2010 digunakan sebagai refrensi terhadap kadar ion logam air gambut sebelum dan sesudah diadsorpsi.Hasil-hasil penelitian menunjukkkan bahwa zeolit mampu mengadsorpsi ion logam Fe, Cd, Co, Mn, Na, Pb dan ion Cl.
Kualitas air gambut setelah diadsorbsi dengan zeolit menunjukkan bahwa kadar ion logam Fe, Cd, Co, Mn, Na, Pb dan ion Cl masih memenuhi kualitas air minum berdasarkan Permenkes No. 492/2010.
Kata Kunci : Air Gambut, Batubara Abu terbang, X-ray fluorescence
spectrometry, SpektrofotometriSerapan Atom
SYNTHESIS OF ZEOLITE FROM COAL FLY WASTE (Fly Ash) AS ADSORBEN FOR REDUCTION OF HEAVY METAL ION FROM PEAT WATER WITH HYDROTHERMAL METHOD USING COLUMN MODE
ABSTRACT
Research on the synthesis of zeolite from fly ash as an adsorbent material and its application has been done. The purposes of this study are (i) to determine the potential of zeolite produced from fly ssh as an adsorbent; (ii) to determine the quality of peat water refer to the water quality standards Permenkes No.
492/2010. Zeolites were synthesized using the Hydrothermal method. Then, it they were characterized with X-Ray Fluoresense (XRF). The metal ions of peat water before and after adsorbed with zeolit were analyzed using Atomic Adsorption Spectroscopy (AAS). The results show that zeolite may adsorb Fe, Cd, Co, Mn, Na, Pb and Cl ions from peat water, the quality of peat water after adsorption with zeolite show that the levels of metal ions of Fe, Cd, Co, Mn, Na, Pb and Cl still regands to the quality standards of water quality Permenkes No. 492/2010.
Keywords : Peat Water, Fly Ash, X-ray fluorescence spectrometry, Atomic
Absorption Spectrophotometry
DAFTAR ISI
Halaman
PERSETUJUAN i
PERNYATAAN ORISINALITAS ii
PENGHARGAAN iii
ABSTRAK iv
ABSTRACT v
DAFTAR ISI vi
DAFTAR TABEL ix
DAFTAR GAMBAR x
DAFTAR LAMPIRAN xi
BAB 1 PENDAHULUAN
1.1 Latar Belakang 1
1.2 Permasalahan 3
1.3 Pembatasan Masalah 4
1.4 Tujuan Penelitian 4
1.5 Manfaat Penelitian 4
1.6 Waktu dan Lokasi Penelitian 4
1.7 Metodologi Penelitian 5
BAB 2TINJAUAN PUSTAKA
2.1 Batubara 6
2.1.1 Cara Terbentuknya Batubara 6
2.1.2 Reaksi Pembentukan Batubara 7
2.1.3 Klasifikasi Kimia Batubara 7
2.1.4 Komposisi Kimia Batubara 8
2.2 Abu Terbang Batubara 9
2.2.1 Abu Terbang (Fly Ash) 9
2.2.2 Pengolahan Limbah B-3 10
2.3 Adsorpsi 10
2.3.1 Parameter Adsorpsi 12
2.4 Adsorben 13
2.4.1 Jenis-jenis Adsorben 14
2.5Zeolit 14
2.5.1 Struktur Zeolit 16
2.5.2 Sifat-sifat Zeoli 18
2.6Air Gambut 21
2.6.1 Sifat Air Gambut 22
2.6.1.1 Sifat Fisik 22
2.6.1.2 Sifat Biologi 23
2.6.1.3 Sifat Kimia 23
2.7 Kualitas Air 24
2.7.1 Syarat-syarat Air Bersih 24
2.8 Logam Berat 25
2.9XRF (X-Ray Fluorescence Spectrometry) 25 2.10Analisis Secara Spektrofotometri Serapan Atom (SSA) 27 BAB 3METODE PENELITIAN
3.1 Alatdan Bahan 29
3.1.1 Alat 29
3.1.2 Bahan 30
3.2 Prosedur Penelitian 30
3.2.1 Pengambilan dan Pengawetan Sampel 30
3.2.1.1 Abu Terbang (Fly Ash) 30
3.2.1.2 Air Gambut 30
3.2.2 Preparasi Sampel 31
3.2.3 Pembuatan Zeolit Sintesis 31
3.2.4 Penentuan Kadar Logam Besi Dengan SSA 31 3.2.4.1 Pembuatan Larutan Seri Standar Besi 31 3.2.4.2 Pembuatan Kurva Kalibrasi Besi 32 3.2.5 Penentuan Kadar Logam Mangan Dengan SSA 32 3.2.5.1 Pembuatan Larutan Standar Mangan 32 3.2.5.2 Pembuatan Kurva Standar Mangan 33 3.2.6 Penentuan Kadar Logam Klorid dengan Titrasi Argento 33 3.2.7 Karakterisasi Adsorpsi Komposit Zeolit 33
3.2.8 Penyediaan Reagent 33
3.2.9 Adsorpsi Ion Logam Dengan Mode Kolom 34
3.3 Bagan Penelitian 35
3.3.1 Pembuatan Zeolit Sintesis dan Kalsinasi Air Gambut 35
3.3.2 Penentuan Cl dalam Sampel 35
3.3.3 Preparasi dan Penentuan Kadar Besi pada Sampel 36 3.3.4 Preparasi dan Penentuan Kadar Mangan 36 BAB 4 HASIL DAN PEMBAHASAN
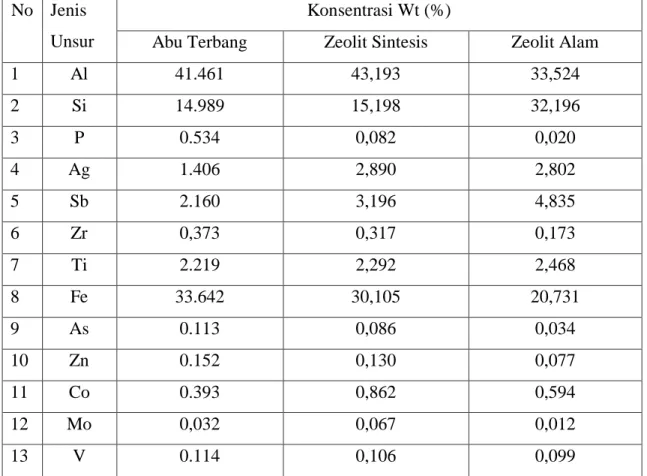
4.1 Hasil Uji Komposisin Unsur Logam Zeolit 37
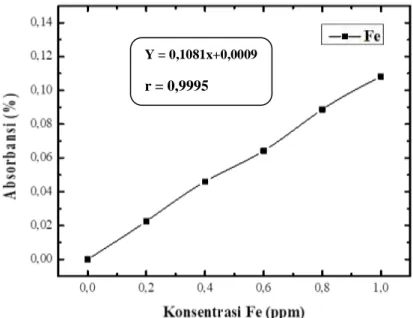
4.2 Penentuan Kandungan Logam Besi (Fe) 39
4.2.1 Persentase (%) Penurunan Konsentrasi Logam Besi (Fe) 40 4.2.2 Perhitungan Entalpi pada Logam Besi 41 4.2.3 Persentasi % Penurunan Konsentrasi Logam Besi (Fe) 42 4.3Penentuan Kandungan Logam Mangan pada Air Gambut 43
4.3.1 Persentase (%) Penurunan Konsentrasi Logam
Mangan (Mn) 44
4.3.2 Perhitungan Entalpi Pada Logam Mangan 45 4.3.3 Persentasi % Penurunan Konsentrasdi Logam Mangan 46 4.4 Penentuan Kandungan Logam Kadmium pada Air Gambut 47 4.4.1 Persentase (%) Penurunan Konsentrasi Logam Klorida (Cl) 49 4.5 Penentuan Kandungan Senyawa Adsorben Dalam Zeolit 49
4.5.1 Penentuan Kandungan Al
2O
349
4.5.2 Penentuan Kandungan SiO
250
BAB 5 KESIMPULAN DAN SARAN
5.1 Kesimpulan 51
5.2 Saran 51
DAFTAR PUSTAKA
DAFTAR TABEL
Nomor Tabel
Judul Halaman
2.2 Komposisi Kimia Batubara 8
2.4 Model Keseimbangan Jerapan Isoterm 15
2.6 Kandungan Zeolitr beserta rumus kimianya 16
2.9 Komposisi Kilogram Zeolit 20
4.1 Data Uji Komposisi Zeolit 37
4.2 Kondisi Alat Spektrofotometri Serapan Atom (SSA) Shimadzu AA-7000 Pada pengukuran Konsentrasi Logam Besi (Fe)
39
4.3 Data Adsorbansi Larutan Seri Standar Logam Besi 39
4.5 Persen adsorpsi pada logam Besi 41
4.6 Data Perhitungan Entalpi (∆H) pada Logam Besi (Fe) 41 4.7 Kondisi Alat Spektrofotometri Serapan Atom (SSA)
Shimadzu AA-7000 Pada pengukuran Konsentrasi Logam Mangan (Mn)
43
4.8 Data Absorbansi Larutan Seri Standar Logam Mangan (Mn)
43
4.10 Persen (%) Adsorpsi pada Logam Mangan (Mn) 45
4.11 Data Perhitungan Entalpi (∆H) pada Logam Mangan (Mn) 45
4.12 Data Volume Larutan Standar AgNO
347
DAFTAR GAMBAR
Nomor Gambar
Judul Halaman
2.3 Bongkahan Zeolit Alami dan Zeolit Sintesis 14
2.5 Struktur Zeolit Sintesis dan Kerangka Zeolit Sintesis 15
2.7 Rangka zeolit yang terbentuk 17
2.8 Unit Kerangka Zeolit 17
2.10 XRF 26
4.4 Kurva Kalibrasi Larutan Seri Standar Logam Besi (Fe) 40 4.9 Kurva Kalibrasi Larutan Seri Standar Logam Mangan
(Mn)
44
DAFTAR LAMPIRAN
Nomor lampiran
Judul Halaman
1 Peraturan Menteri Kesehatan Republik Indonesia 55 2 Data Hasil Air Gambut Sebelum Kontak Adsorben 59 3 Data Hasil Effluen air gambut sesudah kontak adsorben 60
4 Dokumentasi Penelitian 61
BAB 1 PENDAHULUAN
1.1 Latar Belakang
Di Indonesia, jumlah pemakaian batu bara di kalangan industri semakin meningkat. Kebanyakan industri telah mengganti sumber tenaga pada pembangkit uap/boiler dari minyak dengan batubara. Abu Batubara adalah sisa pembakaran yang berbentuk partikel halus amorf dan perubahan bahan mineral karena proses pembakaran. Dari proses pembakaran batubara pada unit pembangkit uap (boiler) akan terbentuk dua jenis abu yaitu abu terbang (fly ash) sekitar 80-90 % dan abu dasar (bottom ash) sekitar 10-20% (Edy, 2007).
Pada pembakaran dan pemecahan batubara (cracking), Menghasilkan gas buangan berupa CO, NO
x,dan SO
x, juga dihasilkan partikel-partikel lain seperti Karbon, SiO
2,Al
2O
3,dan oksida-oksida besi. Partikel-partikel tersebut dapat menimbulkan pencemaran bagi lingkungan karena mengandung unsur-unsur radioaktif alam pada saat pembakaran akan keluar bersama gas emisi. Jenis unsur radioaktif tersebut termasuk kedalam logam berat, apabila masuk kedalam tubuh manusia akan berdampak buruk (Wardani, 2008).
Logam berat menyebabkan keracunan bagi manusia dan pada makhluk hidup lainnya. Karena logam berat yang dihasilkan abu terbang (fly ash) tidak mengalami degradasi seiringnya waktu dan akan menjadi bioakumulatif dalam jaringan yang hidup (sama) yang dapat menyebabkan kematian (Naja, 2009).
Masalah penyediaan air bersih merupakan masalah global yang mendesak untuk segera ditangani. Masalah serupa telah lama ada bagi daerah bertanah gambut yang kandungan air tawarnya terbatas, sehingga daerah tesebut masihmenggunakan air gambut sebagai sumber air untuk kebutuhan sehari-hari.
Permasalahan yang timbul yaitu kualitas air gambutyang digunakan masyarakat
kurang memenuhi syarat sebagai air bersih. Khususnya didaerah kota kisaranyang
masyarakatnya masih mengkonsumsi air gambut, padahal air gambut tersebut
memiliki kandungan pH 3-4 yang akan mengganggu kesehatan.
Berdasarkan sifat kimia dan fisikanya, maka tingkat atau daya racun logam berat terhadap hewan air pada LC-50 selama 48 jam, akibat pengaruh sinergik antar logam, efek sub letal, bioakumulasi dan bahayanya terhadap orang yang mengkonsumsi ikan maka dapat diurutkan (dari tinggi ke rendah) sebagai berikut merkuri (Hg), kadmium (Cd), emas (Ag), Nikel (Ni), timah hitam (Pb), arsen (Ar), selenium (Sn), seng (Zn) (Darmono, 1995).
Kumar (2006) telah meneliti untuk membuktikan adsorpsi dari sintetis zeolit berhasil dilakukan dalam mode kolom, menghilangkan adsorpsi ion logam berat dari air limbah sintetik menggunakan alat sebagaimana adsorben telah dipelajari dalam mode kolom.
Industri-industri besar saat ini mulai berahlih menggunakan batubara sebagai bahan bakar alternatif pada pembangkit listrik tenaga uap(PLTU).Maka dilakukan Sintesis abu layang sebagai adsorben logam Cr dalam limbah penyamakan kulit (Yanti, 2009).
Hartanto (2016) telah meneliti mengenai abu terbang (fly ash) yang diubah menjadi zeolit. Abu batu bara berisi sekitar 70% abu terbang, abu terbang terdiri dari Aluminosilicate kaca, mullite (Al
6Si
2O
13) dan kuarsa (SiO
2). Bahan-bahan ini dapat digunakan sebagai sumber Al dan Si dalam sintetis zeolit. Yang digunakan sebagai adsorben gas NO
Xkhusunya gas NO, gas NO
2yang keduanya dapat bereaksi membentuk ozon dan larutan berair yang didalamnya terdapat logam berat yang berbahaya.
Adsorben dari abu layang yang merupakan limbah hasil pembakaran batubara di PLTU.Kandungan mineral dan struktur bangun dari abu layang sangat memungkinkan untuk digunakan menjadi bahan adsorben limbah zat warna.Sebelum digunakan sebagai bahan adsorben, abu layang disintesis menjadi zeolitlike material (ZLM) dengan proses dekomposisi. Penggunaan fly ash untuk menghilangkan logam berat sebagai adsorben dalam percobaan batch, yang dilakukan pada suhu kamar (Deniz, 2017).
Dari penelitian yang telah dilakukan Zahrul M, 2018. Pada industria tekstil, zat warna digunakan dalam proses pewarnaan kain dan benang.
Pengolahan limbah zat warna dari industria tekstil perlu dilakukan sebelum
dibuang kebadan air, karena kandungan zat warna yang tinggi akan mengganggu transmisi cahaya dan menyebabkan turunnya kadar oksigen terlarut dalam air, pH menjadi asam serta gangguan terhadap kehidupan air. Penggunaan adsorben pada limbah industri tekstil akan mengurangi kadar zat warna, sehingga limbah cair akan aman untuk dibuang kelingkungan sesuai dengan baku mutu yang ditetapkan oleh pemerintah. Di sisi lain, hal tersebut membantu penyelesaian masalah pembuangan limbah abu layang dari PLTU.
Zeolit merupakan sekelompok mineral aluminosilikat terhidrasi dengan saluran dan rongga tertentu. Oleh karena itu, abu batu bara dapat diubah menjadi zeolit dengan mudah. Kegunaan dari zeolit salah satunya pada industry minyak bumi digunakan sebagai cracking, pada industri kimia sebagai penukar ion dan pada pemurnian air sebagai pelunak air sadah.
Berdasarkan latar belakang diatas,maka penulis tertarik melakukan penelitian, membuat abu terbang (fly ash) batubara menjadi zeolit dengan metode hidrotermal sebagai adsorben dengan mode kolom untuk mengurangi kadar ion logam berbahaya pada air gambut denganjudul:”Sintesis Zeolit Dari abu terbang (fly ash)batu bara sebagai Adsorben Untuk Mengurangi Ion Logam dari Air Gambut Dengan Metode Hidrotermal Menjadi Air Bersih Menggunakan Mode Kolom”.
1.2 Permasalahan
1. Berdasarkan PP RI No.101 Tahun 2014, abu terbang dari sisa pembakaran batubara terdiri dari Aluminosilicate kaca, mullite (Al
6Si
2O
13) dan kuarsa (SiO
2). Bahan-bahan ini dapat digunakan sebagai sumber Al dan Si dalam sintesis zeolit. Dimana zeolit dapat digunakan sebagai adsorben.
2. Masalah penyediaan air bersih bagi daerahkota Kisaran yang kandungan
air tawarnya terbatas, sehingga daerah tesebut masihmenggunakan air
gambut sebagai sumber air untuk kebutuhan sehari-hari. Permasalahan
yang timbul yaitu kualitas air gambutyang digunakan masyarakat kurang
memenuhi syarat sebagai air bersih.
1.3 Pembatasan Masalah
1. Bahan baku utama dalam pembuatan zeolit digunakan adalah abu terbang (fly ash) batubara yang diambil dari tempat penimbunan limbah abu terbang (fly ash) batubara di Kawasan Industri Medan (KIM).
2. Sampel yang akan dialiri kedalam adsorben zeolit adalah air gambut yang berasal dari kota kisaran yang tercemar dari lapukan kayu yang membusuk.
3. Penelitian ini dilakukan dengan metode Hidrotermal dan Karakterisasi secara kuantitatif dan kualitatif.
1.4 Tujuan Penelitian
1. Untuk mengetahui pemanfaatan sintetis zeolit dari limbah batubara yaitu abu terbang (fly ash) sebagai adsorben.
2. Untuk mengetahui hasil effluent yang dihasilkan dari air gambut menjadi air bersih sesuai dengan baku mutu air yang memenuhi persyaratan Permenkes dengan Metode Hidrotermal menggunakan Mode Kolom.
1.5 Manfaat Penelitian
1. Hasil yang diperoleh dari penelitian ini diharapkan dapat menjadi salah satu informasi ilmiah mengenai pemanfaatan limbah Abu Terbang (Fly Ash) sebagai adsorben untuk mengurangi kadar ion logam.
2. Hasil yang diperoleh dari penelitian ini dapat menjadi salah satu informasi bahwa effluent dari air gambut yang telah diadsorpsi dapat memenuhi baku mutu air sesuai persyaratan Permenkes 492/2010.
1.6 Waktu danLokasi Penelitian
Penelitian ini dilakukan di Laboratorium Kimia Analitik F-MIPA USU
untuk proses penghalusan dan proses pengkoloman air gambut menjadi air
bersih. Untuk tahap selanjutnya dari karakterisasidan uji sampel menggunakan
XRF dan SSA dilakukan di Laboratorium UNIMED dan Riset Balai
Penindustrian (Baristan).
1.7 Metodologi Penelitian
Penelitian ini dilakukan secara eksperimen laboratorium.
1. Sampel diambil secara purposif yang diambil dari salah satu pabrik kimia di Kawasan Industri Medan (KIM)
2. Kemudian Abu Terbang (Fly Ash) disaring menggunakan ayakan dengan ukuran 200 Mesh
3. Lalu, pertama ditimbang sebanyak 50 gram abu terbang yang telah diayak dicampur dengan 250 ml HCl 6M selama 24 jam, kemudian dipanaskan selama 30 menit sambil terus diaduk , disaring dan diaging selama 24 jam 4. Kedua Ditimbang 5 gram Al powder dicampur dengan 2,525 gram NaOH
dilarutkan dalam 100 ml akuadest
5. Kemudian kedua larutan dicampur dan distirrer selam 1 jam dengan kecepatan 1000 rpm. Lalu diaging kembali selama 24 jam hingga terbentuk gel zeolit secara homogen.
6. Setelah itu diautoklaf selama 2 jam pada suhu 110
0C hingga terbentuk dua lapisan lalu didekantasi. Endapan disaring menggunakan kertas saring biasa dan dicuci dengan akuades hingga pH 7, lalu dioven selama 12 jam pada suhu 110
0C.
7. Dikalsinasi: alat dirangkai sesuai mode kolom, kemudian dimasukkan kapas, glass sutra, 10 cm zeolit sintesis, glass sutra lagi, lalu dialiri dengan air gambut sebanyak 250 ml. Effluent ditampung lalu dianalisa.
8. Analisa Kualitatif dan Kuantitatif kristalisasi menggunakan XRF (X- Ray
Fluorecence) untuk mengetahui komposisi kimia unsur termasuk unsur
oksida Fly Ash dan AAS (Model: Spektra AA50) untuk mengetahui unsur-
unsur ion logam yang terdapat didalam larutan effluen dari kolom.
BAB 2
TINJAUAN PUSTAKA
2.1 Batubara
Batubara adalah suatu mineral yang tersusun dari bahan organik dan bahan anorganik.Batubara digunakan sebagai sumber energi alternatif untuk menghasilkan listrik. Pada pembakaran batubara, menghasilkan polutan udara, seperti sulfur dioksida, yang dapat menyebabkan terjadinya hujan asam (Achmad, 2004).
2.1.1 Cara Terbentuknya Batubara
Pembentukan batubara secara umum dapat dibagi dalam dua tahap yaitu:
tahap peatification atau penggambutan (akibat proses biokimia) dan tahap coalification atau pembatubaraan (akibat proses geokimia). Tahap penggambutan merupakan tahap awal dari suatu proses pembentukan batubara.
Pada tahap ini diperkirakan sisa tumbuhan yang terakumulasi tersimpan dalam kondisi reduksi di daerah rawa yang selalu tergenang air dengan kedalaman sekitar 0,5 m sampai 10 m dari permukaan air. Sisa tumbuhan tersebut oleh aktivitas bakteri anaerob dan jamur diubah menjadi gambut (Stach, 1982).
Proses Pembentukan batubara terdiri atas dua tahapyaitu:
1. Tahap Biokimia (Penggambutan) adalah tahap ketika sisa-sisa tumbuhan yang terakumulasi tersimpan dalam kondisi bebas oksigen (anaerobik) di daerah rawa dengan sistem penisiran (drainage system) yang buruk dan selalu tergenang air. Material tumbuhan yang busuk tersebut melepaskan unsur H, N, O, dan C dalam bentuk senyawa CO
2,H
2O, dan NH
3,untuk menjadi humus. Selanjutnya oleh bakteri anaerobik dan fungi, material tumbuhan itu diubah menjadi gambut (Stach, 1982 )
2. Tahap pembatubaraan(Coalification) merupakan proses diagenesis
terhadap komponen organik dari gambut yang menimbulkan peningkatan
temperatur dan tekanan sebagai gabungan proses biokimia, kimia dan
fisika yang terjadi karena pengaruh pembebanan sedimen yang
menutupinya dalam kurun waktu geologi (Stach, 1982).
2.1.2 Reaksi Pembentukan Batubara
Proses pembentukan batubara atau coallification yang dibantu oleh faktor fisika, kimia alam akan mengubah cellulosa menjadi lignit, subbitumine, bitumine dan antrasit. Reaksi pembentukan batubara dapat digambarkan sebagai berikut.
Reaksi:
5(C
6H
10O
5) C
20H
22O
4+ 3CH
4+ 6CO
2+ CO + 8H
20 (2.1) Cellulosa lignit gas metana air
Keterangan :
Cellulosa (zat organik) yang merupakan zat pembentuk batubara. Unsur C dan Unsur H dalam lignit (Sukandarrumidi, 1995).
2.1.3 Klasifikasi Batubara
Berdasarkan tingkat proses pembentukannya yang dikontrol oleh tekanan, panas dan waktu, batubara umumnya dibagi yaitu:
1. Lignit
Lignit merupakan batubara peringkat rendah dimana kedudukan lignit dalam tingkat klasifikasi batubara berada pada daerah transisi dari jenis gambut ke batubara.Lignit adalah batubara yang berwarna cokelat kehitaman dan memiliki tekstur seperti kayu.
2. Sub-bituminus
Batubara jenis ini merupakan jenis lignit dan bitu minus.Batubara jenis ini memiliki warna hitam yang mempunyai kandungan air,zat terbang, dan oksigen yang tinggi serta memiliki kandungan karbon yang rendah.
3. Bituminus
Batubara jenis ini merupakan batubara yang berwarna hitam denga tekstur ikatan yang baik. Bituminus mengandung 68-86% unsur carbon (C) dan berkadar air 8-10%.
4. Antrasit
Antrasit merupakan batubara paling tinggi tingkatan yang mempunyai
kandungan karbon lebih dari 93% dan kandungan zat terbang kurang dari
10%.Antrasit umumnya lebih keras, kuat dan seringkali berwarna hitam mengkilat seperti kaca (Yunita, 2000).
2.1.4 Komposisi Kimia Batubara
Analisa fasa dengan metode X-Ray Difraction (XRD) dilakukan pada keempat batubara dari berbagai sumber untuk mendapatkan data komposisi mineral. Data pengukuran XRD dan hasil analisa kualitatif disajikan dalam Tabel 2.2 berikut.
Tabel 2.2 Komposisi Kimia Batubara
NO Element Bukit Asam Batu licin Prima Coal Sungai Danau
Wt. % Wt. % Wt. % Wt. %
1 SiO
211,400 (160) 13,810(170) 7,9909(140) 2,060(070) 2 TiO
20,417 (012) 0,825(0,25) 0,201(006) 0,112(003) 3 Al
2O
36,290(060) 9,100(080) 6,200(060) 2,630(040) 4 Fe
2O
31,860(050) 0,828(029) 0,870(030) 0,178(006)
5 MnO 0,010(0) 0,010(0) 0,004(0) 0,002(0)
6 CaO 0,426(015) 0,125(005) 0,175(006) 0,079(003) 7 MgO 0,127(004) 0,098(003) 0,253(008) 0,061(002) 8 Na
2O 0,129(006) 0,144(007) 0,557(029) 0,988(049) 9 K
2O 0,356(018) 0,162(008) 0,193(010) 0,013(001) 10 P
2O
50,049(003) 0,017(001) 0,029(001) 0,035(002) 11 SO
32,040(007) 1,330(060) 1,530(060) 0,851(042)
12 LOI 76,75 73,19 81,77 92,87
13 ZnO 0,005(0) 0,011(0) 0,003(0) 0,003(0)
14 NiO 0,003(002) 0,103(004) 0,003(002)
15 ZrO
20,018(001) 0,036(001) 0,012(001) 0,015(001) 16 Cs
2O 0,019(004) 0,021(005) 0,010(002) 0,012(0040)
17 CuO 0,003(0) 0,011(0) 0,002(0) 0,002(0)
18 As
2O
30,001(0)
19 SrO 0,015(001) 0,004(0) 0,006(0) 0,009(0)
20 V
2O
50,016(0) 0,035(001) 0,005(001) 0,008(0)
21 Cr
2O
30,007(005) 0,078(053) 0,003(0) 0,004(0)
22 CO
3O
40,001(0) 0,005(0) 0,001(0)
23 Cl 0,041(002) 0,033(002) 0,020(001) 0,050(003) (Jha, 2008).
2.2 Abu Batubara
Abu batubara adalah bagian dari sisa pembakaran batubara yang berbentuk partikel halus amorf dan abu tersebut merupakan bahan anorganik yang terbentuk dari perubahan bahan mineral (mineral matter) karena proses pembakaran (Rustanti, 2009).
2.2.1 Abu Terbang (fly ash)
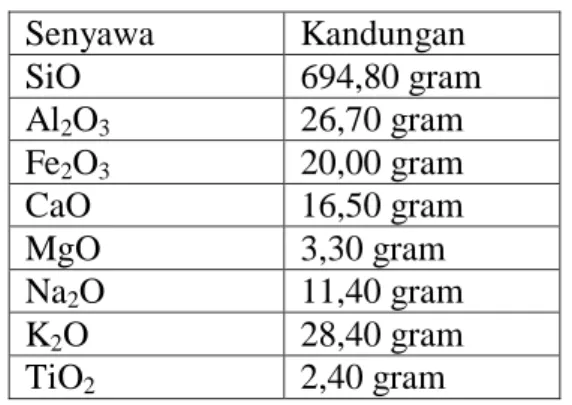
Abu terbang (Fly ash) mengandung unsur kimia antara lain silika (SiO
2), alumina (Al
2O
3), fero oksida (Fe
2O
3) dan kalsium oksida (CaO), juga mengandung unsur tambahan lain yaitu Magnesium Oksida (MgO), Titanium Oksida (TiO
2), Alkalin (Na
2O dan K
2O), Sulfur Trioksida (SO
3), Pospor Oksida (P
2O
5) dan Karbon (Yusri,2012).
Menurut ACI Committee 226, dijelaskan bahwa abu terbang (fly ash) mempunyai butiran yang cukup halus, yaitu lolos ayakan No.325 (45 mili mikron) 5–27 % dengan spesific gravity antara 2,15–2,6 dan berwarna abu-abu kehitaman.
Menurut ASTM C618 Abu terbang (fly ash) dibagi menjadi dua kelas yaitu fly ash kelas F dan kelas C. Perbedaan utama dari kedua Ashtersebut adalah banyaknya calsium, silika, aluminium dan kadarbesi di Ash tersebut. Walaupun kelas F dan kelas C sangat ketatditandai untuk digunakan fly ash yang memenuhi spesifikasi ASTM C618. Yang penting diketahui, bahwa tidak semua fly ash dapat memenuhi persyaratan ASTMC618, kecuali pada aplikasi untuk beton, persyaratan tersebut harus dipenuhi.
Fly ash kelas F: merupakan fly ash yang diproduksi dari pembakaran batubara
anthracite atau bituminous, mempunyai sifat pozzolanic dan untuk mendapatkan sifat cementitious harus diberi penambahan quick lime, hydrated lime, atau semen.
Fly ash kelas F ini kadar kapurnya rendah (CaO < 10%).
Fly ash kelas C: diproduksi dari pembakaran batubara lignite atau sub-
bituminous selain mempunyai sifat pozolanic juga mempunyai sifat self-
cementing (kemampuan untuk mengeras dan menambah strength apabila bereaksi dengan air) dan sifat initimbul tanpa penambahan kapur. Biasanya mengandung kapur (CaO) > 20%.
Menurut SNI S-15-1990-F tentang spesifikasi abu terbang sebagai bahan tambahan untuk pembuatan sintetis zeolit, abu batubara (fly ash) digolongkan menjadi 3 jenis yaitu :
- Kelas F : Abu terbang (fly ash) yang dihasilkan dari pembakaran batubara jenis antrasitdan bituminous.
- Kelas C : Abu terbang (fly ash) yang dihasilkan dari pembakaran batubara jenis lignite dan subbitumious.
- Kelas N : Pozzolan alam, seperti tanah diatome, shale tufa, abu gunung berapi atau pumik.
2.2.2 Pengolahan Limbah B-3
Menurut PP No. 101 tahun 2014 abu terbang (fly ash) digolongkan sebagai limbah B-3 (bahan berbahaya dan beracun) dengan bahan pencemar utama adalah logam berat (PP 85 tahun 1999).
Pemanfaatan limbah B-3 adalah kegiatan penggunaan kembali (reuse), daur ulang (recyle), perolehan kembali (recover) yang bertujuan untuk mengubah limbah B-3 menjadi produk yang dapat digunakan (PerMen LH No.2/2008).
2.3 Adsorpsi
Adsorpsi adalah proses dimana molekul-molekul fluyida menyentuh dan melekat pada permukaan padatan. Adsorpsi merupakan proses akumulasi adsorbat pada permukaan adsorbenyang disebabkan oleh gaya tarik antar molekul atau suatu akibat dari medangaya pada permukaan padatan (adsorben) yang menarik molekul-molekul gas,uap atau cairan. Hal ini disebabkan pada adsorpsi larutan melibatkan persaingan antara komponen larutan dengan situs adsorpsi.
Kecenderungan adsorben polar lebih kuat menyerap adsorbat polar
dibanding adsorbat non polar, demikian sebaliknya. Secara spesifikasi, ukuran
pori juga menentukan dalam proses adsorpsi suatu senyawa tertentu dalam
larutan. Jikas ukuran pori adsorben semakin kecil maka kemampuan adsorpsinya
semakin besar, dengan anggapan bahwa komponen yang teradsorpsi dapat memasuki rongga poribnya. Jumlah adsorben yang semakin banyak akan memberikan luas permukaan yang smakin besar bagi adsorbat untuk terdesorpsi ( Sembodo, 2006).
Menurut Martell dan Hancock (1996), adsorpsi dapat terjadi melalui beberapa mekanisme:
1. Mekanisme pemerangkapan
Silika gel maupun senyawa hibrida organo-silika merupakan adsorben yang berpori sehinga dimungkinkan untuk mengadsorpsi ion logam dengan menjebaknya dalam pori-pori. Mekanisme ini akan terjadi apabila ukuran pori dari adsorben lebih besar daripada ukuran ion yang akan diadsorpsi.
2. Mekanisme pertukaran ion
Mekanisme petukaran ion dapat ditinjau dari nilai elektronegatifitas pada adsorben. Pada silika gel terdapat gugus silanol (Si-OH) dan gugus siloksan (Si- O-Si) yang diperkirakan berperan dalam proses adsorpsi ion logam. Ikatan pada gugus silanol lebih bersifat ionik dibandingkan ikatan pada gugus silakson yang cenderung lebih bersifat kovalen. Akibatnya, atom H pada gugus silanol akan lepas dan tergantikan oleh ion logam yang bersifat elektropositif. Interaksi tersebut yang emungkinkan terjadinya adsorpsi ion logam melalui mekanisme pertukaran ion.
3. Pembentukan Ikatan Hidrogen
Dalam medium air, contoh: ion Pb(II) akan membentuk kompleks akuo oktahedral [Pb(H
2O)
6]
2+. Ikatan hidrogen dapat terjadi antara oksigen dari gugus H
2O dalam kompleks oktahedral dengan gugus aktif siloksan dan silanol pada silika gel maupun gugus aktif pada hibrida organo-silika.
4. Pembentukan kompleks
Adsorpsi ion Pb(II) pada silika gel maupun hibrida organo-silika dapat terjadi
melalui pembentukan kompleks antara gugus aktif adsorben sebagai ligan dengan
ion Pb(II) sebagai atom pusat. Berdasarkan teori HSAB, ion Pb(II) merupakan
golongan asam menengah, kemudian akan bereaksi dengan adsorben yang bersifat
basa keras, menengah atau lunak yang memiliki gugus aktif dan membentuk suatu
kompleks.
2.3.1 Parameter Adsorpsi 1. Kapasitas Adsorpsi
Kinetika kimia mencakup suatu pembahasan tentang kecepatan (laju) reaksi dan bagaimana proses reaksi berlangsung. Definisi tentang laju reaksi adalah 11 suatu perubahan konsentrasi pereaksi maupun produk dalam satuan waktu.Orde reaksi merupakan bagian dari persamaan laju reaksi.Orde reaksi terhadap suatu komponenmerupakan pangkat dari konsentrasi komponen itu, dalam persamaan laju reaksi.
2. Isoterm Adsorpsi Langmuir
Model kinetika adsorpsi Langmuir ini berdasarkan pada asumsi sebagai berikut: laju adsorpsi akan bergantung pada faktor ukuran dan struktur molekul adsorbat, sifat pelarut dan porositas adsorben, situs pada permukaan yang homogen dan adsorpsi terjadi secara monolayer. Proses adsorpsi heterogen memiliki dua tahap, yaitu: (a) perpindahan adsorbat dari fasa larutan ke permukaan adsorben dan (b) adsorpsi pada permukaan adsorben. Tahap pertama akan bergantung pada sifat pelarut dan adsorbat yang terkontrol.
Bagian yang terpenting dalam proses adsorpsi yaitu situs yang dimiliki oleh adsorben yang terletak pada permukaan, akan tetapi jumlah situs-situs ini akan berkurang jika permukaan yang tertutup semakin bertambah.
Persamaan isoterm adsorpsi Langmuir tersebut dapat ditulis dalam bentuk persamaan linier: