BAB 2
TINJAUAN PUSTAKA
Dalam bidang kedokteran gigi, perawatan gigi karena kerusakan gigi menyebabkan terbukanya tubulus dentin terhadap mikroorganisme yang akan menyebabkan terjadinya infeksi pulpa dan jaringan periradikular. Untuk menjaga vitalitas jaringan pulpa dan mencegah perubahan patologis jaringan periradikular maka daerah tubulus dentin harus ditutup dengan bahan dentinogenesis untuk memperbaiki jaringan gigi ketika karies mendegradasi dentin sampai mendekati pulpa (Ferracane dkk., 2010).
Kemampuan bahan untuk masuk ke dalam tubulus dentin yang terbuka berkaitan dengan jumlah tubulus dentin, ukuran tubulus dentin, ukuran partikel bahan, dan pengaturan reaksi bahan. Diameter tubulus dentin 2,0-3,2 µm pada dinding pulpa. Diameter tubulus dentin terbesar banyak terdapat di daerah servikal dengan penurunan yang signifikan pada daerah akar. Ukuran partikel bahan untuk menembus tubulus dentin harus lebih kecil dari diameter tubulus dentin (Hargreaves dan Cohen, 2011)
Sesuai dengan Fokus Area Kegiatan Penelitian, Pengembangan dan Rekayasa untuk Pembangunan Nasional (JAKSTRA 2000 – 2004), bidang kedokteran gigi mempunyai dua bidang fokus area penelitian yang dapat dilakukan yaitu: (1) bidang kesehatan (pencegahan dan pengobatan penyakit), (2) bahan baru dengan ruang lingkup penelitian antara lain bahan khusus berkinerja tinggi (keramik, polimer
komposit), engineering materials (materials science dan engineering), dan bahan baru dalam sudut pandang kesehatan yang berasal dari bahan yang bersifat alami. Kecendrungan masyarakat kembali memakai bahan alami dikenal sebagai new green wave, dimana gerakan ini berupaya menggunakan bahan alam sebagai obat-obatan. Sumber bahan baku obat hingga saat ini sebagian besar masih berasal dari alam, baik nabati maupun hewani (JAKSTRA 2000–2004).
Pemahaman mengenai interaksi antara bahan material gigi dengan jaringan gigi penting untuk diketahui, tidak hanya mengenai biokompatibilitas tetapi juga mengenai potensi dari bahan material gigi tersebut untuk merangsang respon jaringan gigi. Interaksi ini dipengaruhi oleh beberapa faktor, yaitu komposisi bahan, unsur kimiawi, konsentrasi, gambaran morfologi permukaan dentin dengan bahan, produk-produk degradasinya dan bagaimana respon jaringan terhadap bahan-bahan tersebut (Goldberg dan Smith, 2004).
Penelitian mengenai interaksi antara bahan material dengan jaringan gigi terutama bertujuan untuk mengidentifikasi efek toksik dari bahan-bahan terhadap sel-sel kemudian dilakukan penelitian lebih spesifik mengenai respon sel-selular spesifik. Dan banyak peneliti memberikan perhatian untuk memahami bagaimana bahan kedokteran gigi dapat merangsang regeneratif pulpadentinal kompleks (Goldberg dan Smith, 2004). Proteksi pulpodentinal kompleks adalah berupa pengaplikasian satu lapisan atau lebih bahan khusus diantara bahan restoratif dan jaringan gigi untuk mencegah rangsangan tambahan bagi jaringan pulpa akibat prosedur operatif, toksisitas bahan restoratif serta penetrasi bakteri akibat terjadinya kebocoran mikro.
Proteksi pulpodentinal kompleks juga berguna untuk memulihkan vitalitas pulpa (Ferracane dkk., 2010). Banyak faktor yang diperhatikan pada saat meneliti bahan kedokteran gigi.
2.1 Faktor-faktor Interaksi Bahan Kedokteran Gigi dengan Pulpodentinal Kompleks
2.1.1 Struktur dan komposisi dentin
Dentin terdiri dari mineral hidroksiapatit, air, dan bahan organik. Sekitar 90% dari bahan organik adalah kolagen, dan hampir semua kolagen tipe I. Dan 10% sisanya adalah matriks ekstraseluler organik yang terdiri dari protein noncollagenous dan proteoglycans. Dentin dibentuk selama perkembangan gigi sebagai respon terhadap banyak rangsangan, dijumpai pada gigi dalam beberapa bentuk yang ditandai oleh perbedaan dalam kandungan mineral dan struktur. Protein noncollagenous dan faktor pertumbuhan diasingkan dalam struktur dentin selama proses pembentukan gigi. Zat-zat ini termasuk berbagai matriks protein terfosforilasi dan nonphosphorylated, proteoglikan, metaloproteinase, berbagai faktor pertumbuhan (Transforming Growth Factor–Beta 1 (TGF- β1), Fibroblast Growth Factor (FGF-2), Insuline –like Growth Factor (IGF-I), IGF-II, Platelet-Derived Growth Factor (PDGF), dan Vascular Endothelial Growth Factor (VEGF, dan protein). Beberapa molekul tersebut ditemukan di dalam tulang, sedangkan yang lain lebih terdapat di dalam dentin, seperti sialoprotein dentin (DSP), sialophosphoprotein dentin (DSPP). Berdasarkan penelitian sebelumnya banyak dari molekul-molekul tersebut berperan
dalam mineralisasi dentin serta remineralisasi dentin. Kemampuan untuk mengekstrak molekul-molekul berpotensi bioaktif ini dari struktur dentin untuk memudahkan interaksi bahan dengan sel pulpa yang memiliki potensi secara alami dalam meningkatkan proses perbaikan pulpodentinal kompleks (Ferracane dkk., 2010).
2.1.2 Struktur dan komposisi pulpa
Selama pulpa dalam keadaan sehat ataupun terjadi inflamasi, pulpa mempunyai campuran sel yang kompleks, yaitu odontoblas, sel lir odontoblas, stem sel pulpa, fibroblas, sel sistem imun yaitu makrofag, limfosit, dll. Sel-sel imun ini meningkat pada saat proses inflamasi. Sistem saraf dan jaringan kapiler juga terdapat pada pulpa. Pulpa juga mengandung matriks kolagen ekstraselular tipe I, bronektin III, V, dan VI, fibronektin, dan banyak glukosaminoglikan yang ditemukan sebagai proteoglikan. Susunan molekul pada pulpa dan dentin berbeda signifikan, oleh karena itu pulpa tidak mengalami mineralisasi (Goldberg dan Smith, 2004).
2.1.3 Potensi bahan kedokteran gigi terhadap pulpodentinal kompleks
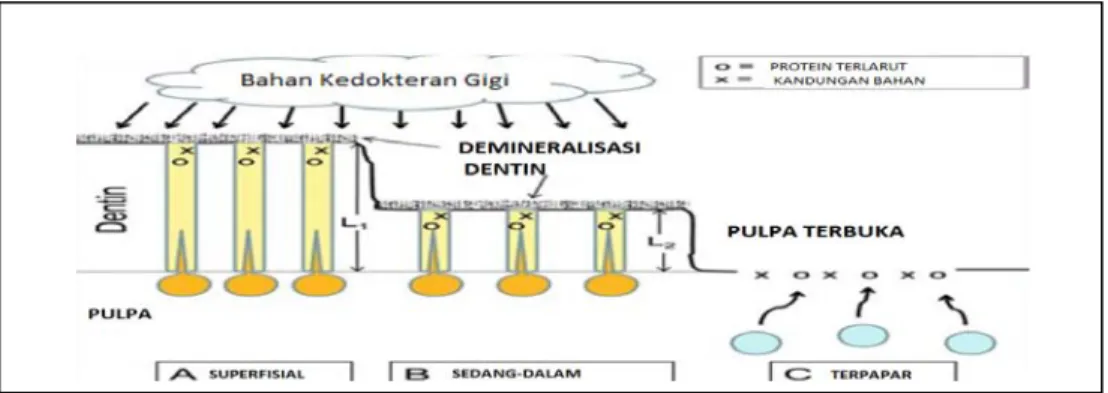
Bahan yang diletakkan pada daerah pulpodentinal kompleks berpotensi menghasilkan spektrum luas dari fisikokimia dan efek biologis (Gambar 2.1). Keberhasilan bahan kaping pulpa direk berkisar 44-97%, sedangkan keberhasilan bahan kaping pulpa indirek umumnya jauh lebih tinggi (Murray dkk., 2002). Beberapa efek mempunyai pengaruh yang berbeda, tergantung pada jaringan sehat atau karies, yang disebabkan oleh infeksi bakteri, inflamasi, dan respon sel pulpa.
Telah lama diketahui bahwa dentin mempunyai aktivitas enzim proteolitik dan saat ini diakui bahwa dentin mempunyai beberapa matriks metaloproteinase (MMP2,8, -9,-13,-20). Aktivitas MMP pada permukaan bahan dengan dentin dapat menyebabkan degradasi dari permukaan lapisan hibrida. Efek dari bahan toksik dapat mengganggu fungsi sel dalam pulpodentinal kompleks dan akhirnya menyababkan kematian sel (Silva dkk., 2009).
Gambar 2.1 Daerah Pulpodentinal Kompleks (Murray, 2002)
2.1.4 Sisa ketebalan dentin pada daerah pulpodentinal kompleks
Kelangsungan hidup odontoblas sangat bergantung pada sisa ketebalan dentin. Menurut Dahl dan Ǿrstavik (2010) melaporkan bahwa sisa ketebalan dentin adalah 1 mm atau lebih akan melindungi jaringan pulpa dari efek sitotoksik zinc phosphate dan semen ionomer kaca modifikasi resin selama proses luting. Murray dkk., 2002 melaporkan bahwa estimasi yang benar terhadap sisa ketebalan dentin adalah 0,5 mm,
dimana pada sisa ketebalan dentin 0,5 mm masih terdapat kelangsungan hidup odontoblas. Sisa ketebalan dentin dan sekresi dentin reaksioner saling berkaitan. Bagian terpenting dalam sekresi dentin reaksioner pada sisa ketebalan dentin antara 0,25 - 0,50 mm karena pada sisa ketebalan dentin 0,25 - 0,50 mm mempunyai molekul bioaktif untuk mendifusi sel odontoblas yang lebih banyak dibandingkan ketebalan di atas 0,5 mm. Dentin reaksioner tidak terjadi pada sisa ketebalan dentin di bawah 0,25 mm, karena sisa ketebalan dentin di bawah 0,25 mm menyebabkan kehilangan sel odontoblas dalam jumlah banyak. Aktivitas sisa ketebalan dentin memainkan peran utama dalam menentukan tingkat cedera pulpa dan respon perbaikan dari bahan kaping pulpa (Tabel 2.1).
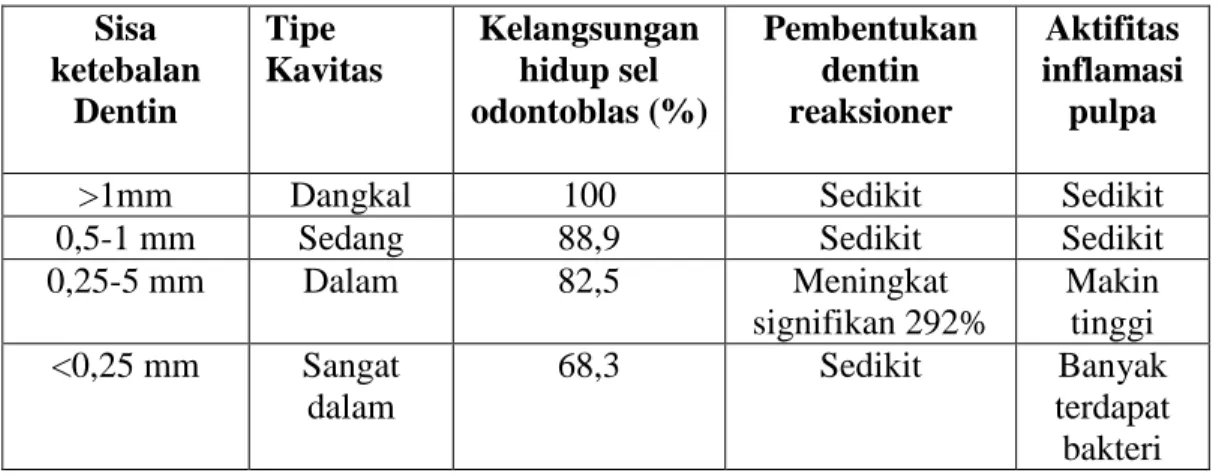
Tabel 2.1 Pengaruh Sisa Ketebalan Dentin terhadap Kelangsungan Hidup Sel Odontoblas, Aktifitas Dentin Reaksioner, dan Inflamasi Pulpa (Murray dkk., 2002).
Sisa ketebalan Dentin Tipe Kavitas Kelangsungan hidup sel odontoblas (%) Pembentukan dentin reaksioner Aktifitas inflamasi pulpa
>1mm Dangkal 100 Sedikit Sedikit
0,5-1 mm Sedang 88,9 Sedikit Sedikit
0,25-5 mm Dalam 82,5 Meningkat signifikan 292% Makin tinggi <0,25 mm Sangat dalam 68,3 Sedikit Banyak terdapat bakteri
2.2 Regenerasi Pulpodentinal Kompleks 2.2.1 Dentin reaksioner
Respon odontoblas terhadap cedera atau stimulus menghasilkan matriks ekstraseluler. Dentin tersier berfungsi untuk memperbaiki kerusakan jaringan. Proses dentin tersier berlangsung akibat reaksi odontoblas dan populasi sel yang ada, sehingga cedera yang terjadi biasanya lebih ringan ketika dentin reaksioner terbentuk. Beberapa literatur menunjukkan bahwa pulpa yang terpapar dapat menyebabkan kematian odontoblas dan menghilangkan potensi dentinogenesis reaksioner. Efek mekanis dari preparasi kavitas dan efek kimia dari bahan yang diaplikasikan pada permukaan dentin yang terpapar mampu memulai pembentukan dentin reaksioner, dengan demikian efek yang dihasilkan dari bahan penting untuk dipertimbangkan (Gambar 2.2) (Ferracane dkk., 2010).
2.2.2 Dentin reparatif
Dentin reparatif dibentuk sebagai respon cedera yang berkelanjutan atau rangsangan yang besar atau pun cedera yang mengakibatkan terjadinya pengendapan dentin reaksioner. Mineral dentin akan terbentuk dalam proses ini, yang merupakan tubular fibrodentin atau tubular dentin yang teratur, yang diproduksi oleh sel lir odontoblas yang berasal dari daerah yang terkena cedera. Proses ini terjadi akibat sel odontoblas yang asli telah mati akibat cedera. Faktor pertumbuhan seperti TGF – β berhubungan dengan diferensiasi sel lir odontoblas (Gambar 2.3) (Dahl dan Orstavik., 2010).
Gambar 2.2. Bahan Kedokteran Gigi Melepaskan Protein pada Gigi yang Mengalami Cedera. (A) Kedalaman Kavitas Superfisial, (B) Kavitas Sedang Sampai Dalam, (C)
Pulpa yang Terpapar (Ferracane dkk., 2010)
Gambar 2.3. (A) Odontoblas Dirangsang untuk Menghasilkan Matriks Ekstraselular, yang Digunakan untuk Mineralisasi Dentin Reaksioner. (B) Sel-sel lain dirangsang untuk Berdiferensiasi menjadi Sel Lir Odontoblas yang kemudian Dirangsang untuk Menghasilkan Matriks Ekstraselular yang menyebabkan Mineralisasi Dentin Reparatif (Ferracane dkk., 2010)
2.3 Mineral Trioxide Aggregate (MTA)
MTA dikembangkan oleh Mahmoud Torabinejad di Loma Linda University tahun 1993. Penelitian menunjukkan bahwa bahan dasar MTA adalah semen Portland
yang merupakan bahan yang digunakan dalam bidang bangunan yang harganya murah dan mudah diperoleh. Sejak diperkenalkan, MTA merupakan bahan kedokteran gigi yang terbukti telah menjadi salah satu bahan yang serbaguna dan biokompatibel pada saat ini.
Banyak peneliti yang mempelajari interaksi antara jaringan gigi dengan kalsium hidroksida dan interaksi jaringan gigi dengan bahan MTA. Hasil reaksi hidrasi dari MTA adalah kalsium hidroksida dimana terjadi pelepasan kalsium dan ion hidroksil dan meningkatnya pH lingkungan diatas 7,0 (Dreger cit. Chang, 2012). Berdasarkan pernyataan Queireoz dkk (2006) menyatakan bahwa kalsium hidroksida lebih ekonomis dan banyak beredar dibanding MTA, tetapi hasil akhir yang diharapkan tidak sebaik dibandingkan menggunakan MTA. Kalsium hidroksida kurang mampu beradaptasi dengan dentin, tidak dapat merangsang difrensiasi odontoblas secara konsisten, sitotoksik pada sel, dan menyebabkan defect tunnel sedangkan MTA merupakan bahan kaping pulpa non biologi yang memiliki sifat fisik yang lebih baik dalam hal sealing ability dan biokompatibilitasnya dibandingkan dengan bahan lainnya seperti kalsium hidroksida. Kemampuannya yang tinggi dalam hal sealing ability dapat mengurangi masuknya bakteri sehingga hal tersebut dapat mencegah kontaminasi. Sedangkan daya biokompatabilitas yang tinggi menghasilkan reaksi penyembuhan jaringan yang sangat baik, sehingga seringkali menyebabkanya terjadinya proses regenerasi jaringan yang sempurna pada tempat berkontaknya bahan dan jaringan tersebut. (Ferracane dkk., 2010; Lohbauer, 2010; Nagaraja, 2005; Kishore , 2005; Trimurni dkk., 2007).
MTA dapat mengeras dalam keadaan lembab, dan menyebabkan penyembuhan jaringan, kemampuannya dalam menginduksi sementogenesis, maka bahan ini dapat digunakan untuk memperbaiki perforasi baik di akar maupun daerah furkasi. Bahan ini juga dapat dipergunakan sebagai kaping pulpa, pulpotomi, bahan penutup ujung akar, apeksifikasi, memperbaiki perforasi daerah akar dan bifurkasi, serta sebagai bahan pengisi saluran akar (Gutmann dkk., 2006).
Walaupun banyak penelitian menunjukkan hasil yang sangat baik dari MTA, namun penggunaan bahan ini relatif masih jarang karena harganya yang relatif mahal, manipulasi yang sulit, dan waktu pengerasan yang panjang serta terdapatnya sedikit kandungan arsen pada MTA (Bramante dkk., 2008). Berdasarkan penelitian Bird dkk (2012) menyatakan bahwa tidak terjadi penetrasi MTA ke dalam tubulus dentin, diuji dengan menggunakan SEM (Gambar 2.4).
2.3.1 Kandungan MTA
MTA terdiri dari senyawa kompleks. Kandungan utama MTA adalah trikalsium silikat dan dikalsium silikat. Selain itu, MTA mengandung sedikit trikalsium aluminat dan tetrakalsium aluminoferrit. Untuk meningkatkan radiopak, bismut oksida ditambahkan dalam MTA. Trikalsium silikat dan dikalsium silikat dibuat dari kapur (CaO) dan silika (SiO2). Beberapa bahan baku lainnya seperti aluminium oksida (Al2O3) dan ferric oksida (Fe2O3) dipanaskan dalam klinker untuk membentuk empat fase yaitu trikalsium silikat, dikalsium silikat, trikalsium alumina dan tetrakalsium aluminoferrit. MTA Berdasarkan International Organization for Standardization (ISO 6876) (International Organization for Standardization, 1986) dan the American Dental Association (ADA) nomor 30 (ANSI/ADA.1991) (Rao dkk., 2009 dan Camilleri, 2010).
2.3.2. Kandungan logam berat pada MTA
MTA mengandung sedikit arsenik, timbal, kromium, zat besi. Zat besi menjadi penyebab diskolorasasi gigi. Produk lain yang terbentuk sebagai hasil dari reaksi setting MTA adalah kalsium hidroksida. Kalsium hidroksida terbentuk sebagai hasil dari reaksi hidrasi MTA (Camilleri, 2008). Kalsium hidroksida mempunyai pH tinggi dan bereaksi dengan ion fosfat untuk membentuk kalsium fosfat amorf yang pada akhirnya menghasilkan kalsium hidrosiapatit (CDHA). CDHA terdiri dari kalsium yang dilepaskan MTA, ion-ion fosfat dan hidroksil yang terkandung dalam cairan tubuh. Penelitian sebelumnya melaporkan bahwa jenis dan morfologi dari
CDHA dibentuk pada permukaan dentin dengan MTA dan tergantung pada pH, rasio Ca atau P, dan jenis cairan permukaan MTA dengan dentin yang terpapar (Chang, 2012). MTA yang terhidrasi larut dalam Fosfat Buffered Saline (PBS) menghasilkan lebih banyak mineral dibandingkan MTA larut dalam air suling (Han dan Okiji, 2010).
Kemampuan sealing ability MTA sangat baik, hal ini behubungan dengan morfologi permukaaan MTA dan dentin (Bird, 2012). Reyes-Carmona dkk., 2010 melaporkan bahwa lapisan permukaan MTA dengan dentin membentuk tag like structure sebagai hasil dari biomineralisasi. Bird dkk., 2012 juga melaporkan bahwa lapisan hidroksiapaptit terbentuk antara MTA dan dentin, ini disebabkan karena kemampuan sealing ability MTA yang sangat baik dengan adanya tag like structure pada permukaan MTA dan dentin. MTA memproduksi lebih banyak tag like structure daripada Portland cement. Tag like structure merupakan hasil dari pelepasan ion dissolusi dari MTA yang mengakibatkan pertumbuhan dan nukleasi pada lapisan apatit. Reyes-Carmona dkk., 2010 melaporkan bahwa ion kalsium yang dilepaskan dari semen menyebar melalui tubulus dentin dan bereaksi dengan ion fosfat dalam cairan jaringan, dan menghasilkan kalsium phosphat. Dan akhirnya, kalsium fosfat masuk pada ion lain dan matang menjadi apatit berkarbonasi (CDHA). Hal ini terjadi karena endapan mineral yang terbentuk pada lapisan mineral antara MTA dan dentin yang menghasilkan ikatan kimia antara MTA dan dentin (Sarkar dkk., 2005). Han dan Okiji (2011) menunjukkan bahwa dentin yang berkontak dengan MTA mengandung Ca dan Si dari silikat kalsium. Ca dan Si yang terdapat pada dentin disebabkan karena
bahan kimia dan struktural modifikasi, yang mengakibatkan resistensi asam tinggi dan menyebabkan kekuatan fisik.
2.4 Semen Ionomer Kaca Modifikasi Resin (SIKMR)
SIKMR dikembangkan untuk memperbaiki sifat fisik dan mengurangi sensitivitas air dari semen ionomer kaca konvensional. SIKMR merupakan bahan hibrid yang lebih kuat dan tidak rapuh diperkenalkan dengan penambahan monomer seperti HEMA. Pada dasarnya SIKMR memiliki komposisi yang sama dengan semen ionomer kaca konvensional hanya saja komponen air diganti menjadi campuran air dengan HEMA. SIKMR dapat mengeras dengan dua cara, yaitu kombinasi asam dan basa serta reaksi polimerisasi (Modena dkk., 2009).
Bahan ini mengandung bubuk kaca yang mampu memindahkan ion dan asam polimer yang larut dalam air seperti asam akrilik. Bahan ini mengandung monomer organik (biasanya HEMA) dan sistem inisiator. Inisiator umumnya sensitif terhadap cahaya sehingga kebanyakan SIKMR mengeras dengan cara di sinar dengan menggunakan lampu penyinaran biasa yang memancarkan sinar dengan panjang gelombang 470 nm (Goldberg, 2008; Modena dkk., 2009).
SIKMR memiliki tahap-tahap reaksi pengerasan yang terjadi melalui reaksi asam-basa antara bubuk alumino silikat dengan asam polikrilat, reaksi polimerisasi dari partikel-partikel resin yang ada di dalam semen; reaksi antara logam poliakrilat dengan resin hingga membentuk matriks semen yang lebih kuat. Dari ketiga reaksi tersebut, sebenarnya SIKMR mengeras dengan sistem “Dual Cure” yaitu reaksi
penggaraman (asam-basa) yang terjadi secara kimia dan polimerisasi yang terjadi akibat penyinaran (Petri dkk., 2007).
Pada umumnya SIKMR dapat membentuk ikatan yang kuat ke dentin dan enamel serta dapat melepaskan fluoride (F). Selain itu, bahan ini juga melepaskan beberapa ion seperti Na, Ca, Sr, Al, P dan Si . Ion – ion tersebut juga dilepaskan oleh SIK konvensional namun kadar ion phosphat yang dilepaskan SIKMR lebih rendah dibandingkan dengan konvensional (Goldberg, 2008).
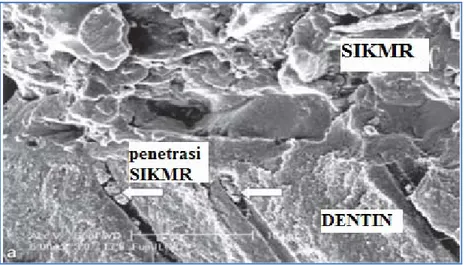
SIKMR ini terbukti bersifat sitotoksis terutama karena pelepasan HEMA dalam kadar tinggi dan bersifat mutagenik, akan tetapi data mengenai mutagenitas sangat sedikit dan sulit diinterpretasi. SIKMR menimbulkan respon inflamasi persisten tingkat menengah hingga berat pada pulpa dan pembentukan zona nekrotik yang besar (Nicholson dan Czarnecka,2008). Menurut Preenan, 2004 mengatakan bahwa terjadi penetrasi SIKMR ke dalam tubulus dentin (Gambar 2.5).
Gambar 2.5. Gambar SEM Permukaan SIKMR dengan Dentin, Penetrasi SIKMR ke dalam Tubulus Dentin (Preenan, 2004)
2.5 Abu Sekam Padi
Padi merupakan produk utama pertanian di negara-negara agraris, termasuk Indonesia. Sekam padi merupakan bagian terluar (kulit) dari butir padi dan produk samping yang dihasilkan dari industri penggilingan padi. Dari hasil penelitian sebelumnya telah dilaporkan bahwa sekitar 20% dari berat pada adalah sekam padi, dan bervariasi dari 13% sampai 29 % dari komposisi sekam adalah abu sekam padi atau rice husk ash (RHA) yang selalu dihasilkan setiap kali sekam dibakar (Putro dan Prasetyoko, 2007). Sekam padi dikategorikan sebagai biomassa yang dapat digunakan untuk berbagai kebutuhan tetapi mempunyai nilai ekonomis yang masih rendah sehingga perlunya dicari alternatif lain yang lebih bermanfaat dan penanganan sekam padi yang kurang tepat akan menimbulkan pencemaran lingkungan (BPPP, 2001). Padahal Abu sekam padi merupakan sumber silika potensial yang dapat digunakan sebagai bahan kedokteran (Indayani dkk., 2011). Nilai paling umum kandungan silika (SiO2) dalam abu sekam padi adalah 94 – 96 % dan apabila nilainya mendekati atau dibawah 90 % dijumpai dalam bentuk amorf terhidrat. Abu sekam padi apabila dibakar secara terkontrol pada suhu tinggi (500–6000
Menurut Balai Penelitian Pasca Panen (BPPP) sekam padi terdiri atas dua belahan yang disebut lemma dan palea yang saling bertautan. Pada proses penggilingan gabah, sekam akan terpisah dari butir beras dan menjadi bahan sisa atau limbah penggilingan.
C) akan menghasilkan abu silika (Putro dan Prasetyoko, 2007).
Berdasarkan derajat pembakaran abu sekam padi, warna abu sekam dapat diklasifikasi menjadi 3 lapisan warna, yaitu abu-abu, putih dan merah jambu. Berdasarkan hasil laboratorium, perbedaan warna ini mempunyai sifat permukaan dan kadar penghidrat yang berbeda. Abu sekam padi berwarna merah jambu jauh lebih reaktif dan mampu memberikan sifat pengerasan yang lebih baik (Zakaria, 2002).
Sekam mengandung senyawa organik berupa lignin dan kitin, selulosa, hemiselulosa, senyawa nitrogen, lipid, vitamin B, dan asam organik, sedangkan senyawa anorganik berupa silika (Makarim dan Suhartatik, 2009). Selulosa adalah penyusun utama dinding sel tumbuhan. Senyawa ini tidak larut dalam air dan terdiri atas unit-unit β-D-glukopiranosa yang disatukan oleh ikatan β1→4 membentuk rantai lurus panjang yang diperkuat oleh ikatan hidrogen. Selulosa yang terdapat pada sekam padi sebanyak 34,34-43,8%. Berdasarkan komposisi kimiawi yang terkandung, sekam bisa digunakan sebagai bahan baku pada industri kimia, terutama kandungan zat kimia furfural yang dapat digunakan sebagai bahan baku dalam berbagai industri kimia; sebagai bahan baku pada industri bahan bangunan, terutama kandungan silika (SiO2) yang dapat digunakan untuk campuran pada pembuatan semen dan digunakan sebagai sumber energi panas, kadar selulosa yang cukup tinggi dapat memberikan pembakaran yang merata dan stabil (Kalapathy dkk., 2002).
2.5.1 Silika abu sekam padi
Silikon dioksida (SiO2) atau biasa juga disebut silika pada umumnya ditemukan di alam dalam batu pasir, pasir silika atau quartzite. Zat ini merupakan material dasar pembuatan kaca dan keramik. Silika merupakan salah satu material oksida yang keberadaannya berlimpah di alam, khususnya di kulit bumi. silika bisa dalam bentuk amorf dan kristalin. Terdapat tiga bentuk kristal silika, yaitu quartz (kuarsa), tridymite, dan cristobalite. Pada tanaman, silika terakumulasi dalam bentuk phytolith yang merupakan bentuk primer dari silika amorf. Silika disebut kristalin jika mempunyai susunan atom yang teratur dan disebut amorf jika mempunyai susunan atom yang kurang teratur (Kalapathy dkk., 2002).
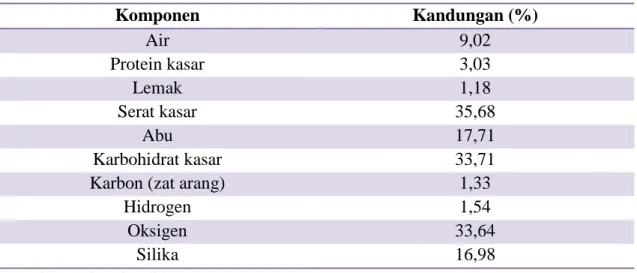
Tabel 2.2 Komposisi Sekam Padi beserta Zat Organiknya (Chandra dkk., 2012)
Komponen Kandungan (%) Air 9,02 Protein kasar 3,03 Lemak 1,18 Serat kasar 35,68 Abu 17,71 Karbohidrat kasar 33,71
Karbon (zat arang) 1,33
Hidrogen 1,54
Oksigen 33,64
Silika 16,98
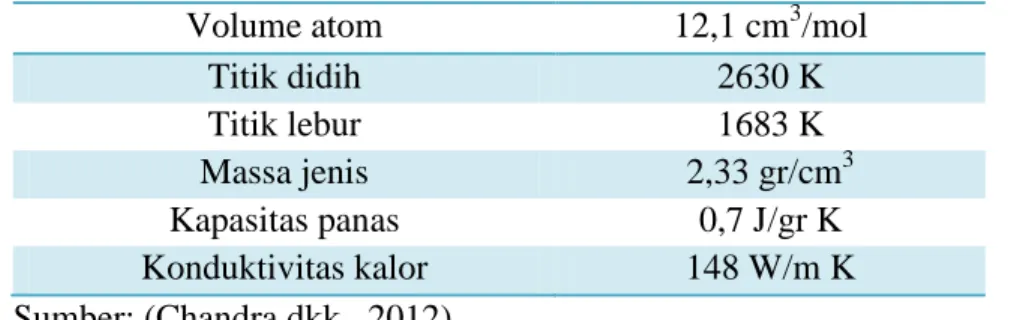
Tabel 2.3 Data Fisik Unsur Silika (Chandra dkk., 2012)
Volume atom 12,1 cm3/mol
Titik didih 2630 K Titik lebur 1683 K Massa jenis 2,33 gr/cm Kapasitas panas 3 0,7 J/gr K Konduktivitas kalor 148 W/m K Sumber: (Chandra dkk., 2012)
Silika merupakan bahan kimia yang pemanfaatan dan aplikasinya sangat luas mulai dari bidang elektronik, mekanis, medis, seni, dan bidang lainnya. Salah satu pemanfaatan serbuk silika yang cukup luas adalah sebagai penyerap kadar air di udara, (Harsono, 2002, cit Sitorus, 2009). Selain itu, silika juga digunakan sebagai penyaring molekuler, resin, pembantu peran katalis, dan pengisi dalam pembuatan polimer (Bansal dkk., 2006). Gugus -OH yang mampu membentuk ikatan hidrogen dengan gugus yang sama dari molekul lain yang mengakibatkan silika dapat digunakan sebagai pengering dan fasa diam pada kolom kromatografi (Narsito, 2005).
Silika abu sekam padi terbukti mempengaruhi pembentukan tulang. Silika merupakan bahan semi konduktor yang mempunyai potensi untuk mencapai sifat-sifat mekanis, morfologis, biokompatibilitas dan biodegradasi. Makanan yang mengandung silika dapat menstimulasi sel osteoblas dan osteo-blast-like cell untuk mensekresi kolagen tipe I dan marker bio-kimia lain pada maturasi sel tulang dan pembentukan tulang (Indahyani dkk., 2003).
Berdasarkan penelitian Indahyani dkk (2011) menyatakan bahwa silika yang berasal dari sekam padi mempunyai kemampuan untuk menstimulasi proliferasi osteoblast dan mempunyai nilai absorbansi yang paling tinggi.
2.5.2 Abu sekam padi nanopartikel (ASPn)
Nanoteknologi pertama kali diperkenalkan oleh seorang ahli Fisika, Richard P. Feynman pada tahun 1959. Erick Drexler kemudian memperkenalkan konsep nanoteknologi kepada masyarakat luas melalui buku yang berjudul “Engine of Creation” pada pertengahan tahun 1980. Kata depan nano-berasal dari bahasa yunani yang berarti kerdil dan satu nanometer sama dengan 10-9
Nanopartikel dikelompokan menjadi nanopartikel organik dan nanopartikel anorganik. Nanopartikel organik meliputi nanopartikel karbon, sedangkan nanopartikel anorganik meliputi nanopartikel logam mulia (seperti emas dan perak) dan nanopartikel semikonduktor (seperti titanium dioksida dan zinc oksida). Nanopartikel yang lebih berkembang adalah nanopartikel anorganik dengan fungsinya yang beraneka ragam. Silika pada sekam merupakan nanopartikel anorganik yang telah diuji sebagai alat yang berpotensi dalam dunia medis, yaitu
m. Nanopartikel merupakan produk yang dihasilkan dari nanoteknologi, sehingga nanopartikel dianggap suatu bahan yang mempunyai dimensi ukuran kurang dari 100 nm. Penelitian mengenai nanopartikel sedang berkembang pesat karena dapat diaplikasikan secara luas, seperti di bidang lingkungan, biomedis, optis, dan elektronik. Hal ini juga ditentukan oleh ukuran, bentuk, dan kristalinitas (Saunders, 2009).
mampu menghantarkan obat sampai ke target dan mengontrol pelepasan obat. Aplikasi lainnya, yaitu sebagai antimikroba, optik, elektronik, biosensor, biolabel, biofiltrasi, magnetik, mekanik, katalis, bioremediasi, pereduksi limbah industri, sumber energi (Moghaddam, 2010).
2.6 Kitosan
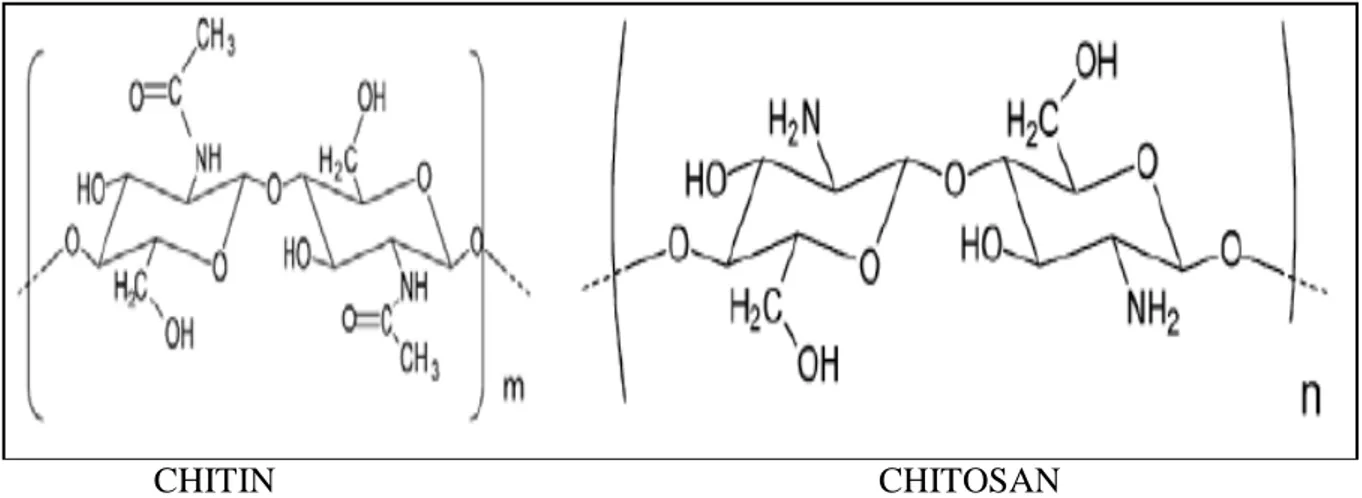
Kitosan (poly-β-1,4-glukosamin) merupakan biopolimer alami yang banyak di jumpai di alam setelah selulosa dan merupakan hasil N-diasetilisasi dari kitin. Kitin banyak terkandung pada hewan laut berkulit keras seperti udang, rajungan, kepiting, blangkas, serangga, moluska, dan dinding jamur seperti klas zygomycetes. Bahan ini pertama kali ditemukan oleh Rouget pada tahun 1859 (Gambar 2.7). Komposisi kitosan terdiri dari Karbon, Hidrogen, dan Nitrogen (Tabel 2.3) serta dapat larut dalam pelarut asam seperti asam asetat, asam formiat, asam laktat, asam sitrat dan asam hidroklorat. Kitosan tidak larut dalam air, alkali dan asam mineral encer kecuali di bawah kondisi tertentu yaitu dengan adanya sejumlah pelarut asam sehingga dapat larut dalam air, methanol, aseton dan campuran lainnya. Kelarutan kitosan dipengaruhi oleh bobot molekul dan derajat deasetilasi. Kitosan dalam bentuk terprotonisasi menunjukkan kerapatan muatan yang tinggi dan bersifat sebagai polielektrolit kationik dan sangat efektif berinteraksi dengan biomolekul bermuatan negatif dan biomolekul permukaan (Agusnar, 1997; Sugita dkk., 2009).
CHITIN CHITOSAN Gambar 2.6 Struktur Bangun Kitin dan Kitosan (Petri dkk., 2007)
Tabel 2.4 Komposisi Kimia Kitosan (Agusnar, 1997). Dalam persen
Karbon (C) Hidrogen ( H) Nitrogen (N)
Kitosan 40,30 5,83 6,35
Sumber: (Agusnar, 1997)
Kitosan tidak beracun dan memiliki sifat biokompatibel dan biodegradble serta mucoadhesion yang dapat menjadi keuntungan bagi aplikasi biomedis (Modena dkk., 2009).
Pawlowska cit Petri dkk., 2007 mengatakan bahwa bahan primer yang telah ditambahkan dengan kitosan dan diaplikasikan pada pulpa gigi tikus dapat menyebabkan sedikit perubahan patologis reversibel.
2.6.1 Kitosan blangkas (Tachypleus gigas)
Berdasarkan viskositasnya, berat molekul kitosan terdiri atas tiga yaitu kitosan bermolekul rendah, kitosan bermolekul sedang dan kitosan bermolekul tinggi. Kitosan bermolekul rendah dengan berat molekul dibawah 400.000 Mv dan kitosan bermolekul sedang dengan berat molekul 400.000-800.000 Mv berasal dari hewan laut dengan cangkang atau kulit yang lunak misalnya udang, cumi-cumi dan rajungan. Kitosan dengan berat molekul 800.000-1.100.000 Mv biasanya berasal dari hewan laut bercangkang keras misalnya kepiting, kerang dan blangkas (Gambar 2.8) (Trimurni dkk., 2006).
Gambar 2.7 Kitosan Blangkas (Trimurni dkk., 2006)
Kitosan blangkas merupakan kitosan bermolekul tinggi yang diperoleh dari cangkang blangkas. Blangkas disebut juga dengan Horseshoe-crab.Kitosan blangkas yang diuji oleh Trimurni Abidin dkk., 2006 mempunyai derajat deastilisasi 84,20% dengan berat molekul 893.000 Mv. Dari penelitian tersebut diketahui bahwa kitosan blangkas mempunyai berat molekul yang tinggi.
Pada penelitian tersebut juga dinyatakan bahwa kitosan blangkas yang mempunyai berat molekul tinggi dapat menstimulasi dentin reparatif dengan kemampuannya membentuk koagulum yang padat sebagai sub base membran yang memudahkan perlekatan sel-sel pulpa seperti dentinoblast untuk memudahkan migrasi dan proliferasi sel-sel pulpa dentinoblast.
2.6.2 Kitosan nanopartikel
Dalam perkembangannnya, kitosan dimodifikasi dalam bentuk magnetik Kitosan nanopartikel dengan ukuran partikelnya 100-400 nm untuk meningkatkan daya absorbsinya. Kitosan nanopartikel dapat dilihat mikrostrukturnya dengan menggunakan SEM (Scanning Electron Microscope).
Szeto dan Zhigang Hu cit Siregar (2009) menyiapkan kitosan nanopartikel dengan melarutkan kitosan dalam larutan asam lemah ditambahkan larutan yang bersifat basa, seperti amoniak, NaOH, atau KOH distirer dengan kecepatan 300 rpm sehingga diperoleh gel kitosan putih dan dibilas dengan aquadest sampai netral kemudian ditempatkan dalam ultrasonic bath untuk memecah partikel-partikel gel kitosan menjadi lebih kecil. Cheung cit Siregar (2009) menyiapkan kitosan nano dengan metode lain, yaitu dengan menambahkan larutan tripolipospat ke dalam larutan kitosan sehingga diperoleh emulsi kitosan sambil distirer dengan kecepatan 1200 rpm, dan ditambahkan asam asetat agar pH-nya 3,5 dengan hasil berupa suspen kitosan.
Lu E-Shi cit. Ningsih (2010) menyiapkan kitosan nanopartikel dengan menambahkan larutan tripolipospat (TPP) kedalam larutan suspensi kitosan yang dibuat dengan menambahkan asam asetat, kemudian distrier dengan kecepatan 1200 rpm terbentuk emulsi.
Kitosan blangkas yang diuji oleh Trimurni Abidin dkk, 2006 menunjukkan bahwa kitosan blangkas yang mempunyai berat molekul tinggi dapat menstimulasi dentin reparatif dengan kemampuannya membentuk koagulum yang padat sebagai sub base membran yang memudahkan perlekatan sel-sel pulpa seperti odontoblast untuk memudahkan migrasi dan proliferasi.
Ada yang menyebutkan (Tiyaboonchai, 2003) kitosan nanopartikel dapat dipakai sebagai pembawa penyaluran obat karena stabilitasnya yang baik, rendah toksik, metode persiapannya sederhana, dan dapat mengikuti rute pemberian obat. Kitosan nanopartikel sebagai agen penyalur obat sangat bermanfaat karena kitosan nano merupakan biopolimer alam yang biokompatibel, dapat larut dalam air, dapat menyalurkan obat dalam bentuk makromolekul, mempunyai berat molekul yang bervariasi sehingga mudah dimodifikasi secara kimia, membantu absorpsi antara substrat dan membran sel, serta ukuran partikel nanonya memiliki efektivitas yang lebih baik.
Henny dkk., 2013 melakukan penelitian dengan menambahkan kitosan molekul tinggi nano yang diperoleh dari blangkas (Tachypleus gigas) 0,15% berat kitosan pada SIKMR dan SIKMRn dan efeknya terhadap proliferasi sel. Hasil penelitian tersebut menunjukkan bahwa terjadi peningkatan viabilitas sel yang signifikan pada SIKMR dan SIKMRn yang ditambahkan 0,015% berat kitosan nano dari blangkas.
2.7 Alat Uji
2.7.1 Scanning Electron Microscope (SEM)
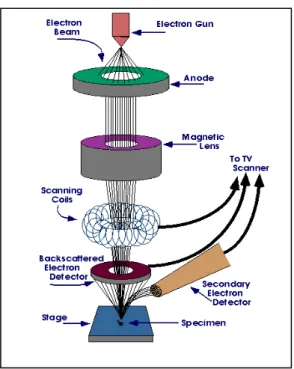
Scanning electron microscope (SEM) merupakan mikroskop elektron yang mampu menghasilkan gambar beresolusi tinggi dari sebuah permukaan sampel. Gambar yang dihasilkan oleh SEM digunakan untuk menentukan struktur permukaan dari sampel. SEM menerapkan prinsip difraksi elektron dengan pengukuran sama seperti mikroskop optik. Prinsip kerjanya adalah elektron yang ditembakkan akan dibelokkan oleh lensa elektromagnetik dalam SEM. Sistem kerja SEM terdiri atas sumber cahaya elektron, sistem lensa, detektor, dan layar TV. Sumber cahaya elektron dihasilkan di dalam suatu penembak elektron yang berbentuk filamen pemanas berupa tabung tanpa udara. Sumber cahaya elektron dipercepat dan difokuskan oleh sistem lensa magnetik yang berada di atas objek. Elektron dikumpulkan oleh detektor, diubah dalam bentuk voltase (energi listrik), kemudian disebar (Gambar 2.8) (Radiological and Eviromental Management,2010).
SEM dapat menghasilkan gambaran permukaan sampel dengan resolusi yang sangat tinggi dan dapat mengungkapkan detail berukuran kurang dari 1 nm. Gambaran sampel diambil (captured) secara digital dan akan ditampilkan pada layar monitor dan disimpan di dalam komputer. Pada gambar ditampilkan skema bagian-bagian dari SEM. Pembesaran pada SEM dapat dikendalikan mulai dari 10 sampai 500.000 kali. SEM memiliki kondenser dan lensa objektif yang berfungsi memfokuskan sinar kepada suatu tempat dan bukan menggambar keseluruhan spesimen (Materials Evaluation and Engineering, 2009).
Spesimen yang akan digambar oleh SEM harus dapat mengalirkan listrik (electrically conductive). Spesimen yang terbuat dari metal hanya memerlukan sedikit tindakan preparasi untuk digambar oleh SEM. Tetapi bagi spesimen yang tidak dapat mengantarkan listrik harus dilapisi (coating) dengan suatu zat yang bersifat sebagai konduktor. Pelapis yang biasa digunakan adalah emas, aloi emas/paladium, platinum, osmium, iridium, tungsten, chromium dan graphite. Syarat agar SEM dapat menghasilkan citra permukaan yang tajam adalah permukaan benda harus bersifat sebagai pemantul elektron atau dapat melepaskan elektron sekunder ketika ditembak dengan berkas elektron. Material yang memiliki sifat demikian adalah logam. Jika permukaan logam diamati di bawah SEM maka profil permukaan akan tampak dengan jelas. Sementara, pada profil permukaan bukan logam untuk diamati dengan SEM, permukaan material tersebut harus dilapisi dengan logam. Film tipis logam dibuat pada permukaan material tersebut sehingga dapat memantulkan berkas elektron. Metode pelapisan yang umum dilakukan adalah evaporasi dan sputtering . SEM memiliki beberapa keunggulan, diantaranya mampu menggambarkan area yang besar secara komparatif dari spesimen, mengukur komposisi dan sifat dasar dari spesimen, serta memiliki resolusi tinggi (MEE, 2009; REM, 2010).
Gambar 2.8. Cara Kerja SEM.(Radiological and Evironmental Management Purdue University, 2010)
Sinar elektron dihasilkan pada bagian atas mikroskop oleh electron gun. Elektron akan mengikuti jalur vertikal melalui mikroskop, yang tetap dalam keadaan vakum. Sinar melewati area elektromagnetik dan lensa, yang memfokuskan sinar turun ke arah sampel. Ketika sinar mengenai sampel, elektron dan sinar-X akan dikeluarkan dari sampel. Detektor akan mengumpulkan sinar-X, backscattered electron, dan elektron sekunder. Detektor akan merubahnya menjadi sinyal yang menghasilkan gambaran dan selanjutnya ditampilkan pada layar monitor (Lawes, 1987; Radiological and Evironmental Management Purdue University, 2010).
2.7.2 Energy Dispersive X-ray (EDX)
Energy Dispersive X-ray (EDX) adalah teknik mikroanalisis kimia yang digabungkan dengan scanning electron microscope (SEM). EDX merupakan suatu alat yang dapat mendeteksi sinar-X yang keluar dari sampel selama pemaparan pancaran elektron untuk mengkarakteristikkan komposisi kimia dari sampel yang dianalisa. Sistem ini terdiri dari 3 (tiga) komponen utama, yaitu detektor sinar-X yang dipisahkan dari ruang SEM dengan jendela polimer yang sangat tipis, untaian pengolahan getaran yang menentukan energi sinar-X yang dideteksi, dan peralatan analisa yang menginterpretasikan data sinar-X dan menampilkannya pada layar komputer. Alat ini dikendalikan oleh suatu program Windows-based user interface (UI) yang dinamakan Genesis. Program ini terletak di dalam komputer EDX (Materials Evaluation and Engineering, Inc. 2009).
Informasi analisa yang dapat diperoleh adalah analisa kualitatif, analisa kuantitatif, pemetaan elemen dan analisa profil garis. Untuk analisa kualitatif, nilai energi sinar-X sampel dari spektrum EDS dibandingkan dengan karakteristik energi sinar- X yang sudah diketahui untuk mendapatkan elemen yang terdapat pada sampel. Hasil kuantitatif dapat diperoleh dari hitungan sinar-X relatif pada karakteristik tingkat energi dari komponen sampel (Materials Evaluation and Engineering, Inc. 2009).
Spektrum EDX ditampilkan secara digital membentuk sumbu-X yang menggambarkan energi sinar-X dan sumbu Y menggambarkan intensitas (Gambar 2.9) (Russ, 1984).
2.8 Landasan Teori
MTA SIKMR KITOSAN ASP
HEMA Sitotoksik Flour Bahan hibrid yang lebih kuat & tidak rapuh Komposisi: C, O, F, Na, Al, Si Mikrostruktur SIKMR-dentin : Resin tag Asam amina Anti toxic Biokompatibel Menstimulasi dentin reparatif Produk alam mudah didapat dan relatif murah Komposisi: hidroksil & asetamida, C, H, N
-Silika tinggi (SiO2 >>>) Osteoinduksi Biokompatibilitas Biodegradasi Nilai absorbansi paling tinggi Produk alam mudah didapat dan relatif murah Komposisi: Si>>>, C, H, O biokompatibel biodegradabel sealing ability Mahal
Setting time lama
Mengandung Arsen Mengandung logam berat Komposisi : Ca, P, Si, O, Cl, C, Al, Mg, Fe Mikrostruktur MTA-dentin : tag like structure Bahan Bioaktif Proliferasi sel Dentinogenesis (Dentin reparatif)
2.9 Kerangka Konsep
Dentin yang terbuka akibat cedera fisiko-mekanis dapat diberikan ASPn + KMTn sebagai bahan kaping pulpa indirek dengan tujuan untuk merangsang dentinogenesis. ASP merupakan sumber silika potensial yang dapat digunakan sebagai bahan kedokteran gigi dengan kandungan silika (SiO2) dalam ASP adalah 94–96 %. Silika terbukti mempengaruhi pembentukan tulang dan gigi serta merupakan bahan semi konduktor yang mempunyai potensi untuk mencapai sifat-sifat mekanis, morfologis, biokompatibilitas dan biodegradasi. Dan berdasarkan penelitian Indahyani dkk (2011) menyatakan bahwa silika yang berasal dari sekam padi mempunyai kemampuan untuk menstimulasi proliferasi osteoblast dan mempunyai nilai absorbansi yang paling tinggi. Kitosan memiliki sifat-sifat seperti biokompatibel dan biodegradble serta mucoadhesion yang dapat menjadi keuntungan bagi aplikasi biomedis. Kitosan blangkas yang mempunyai berat molekul tinggi dapat menstimulasi dentin reparatif dengan kemampuannya membentuk koagulum yang padat sebagai sub base membran yang memudahkan perlekatan sel-sel pulpa seperti dentinoblas untuk memudahkan migrasi dan proliferasi sel-sel pulpa dentinoblas (Trimurni, 2006). - MTA - SIKMR - ASPn + KMTn Mikrostruktur & komposisi kimia Karakterisasi Biomaterial
Berkembangnya bahan material yang bergerak ke arah nanopartikel, maka dengan menggabungkan ASPn + KMTn sebagai perancah diharapkan dapat tercipta biomaterial baru yang dapat berinteraksi dengan permukaan dentin, maka untuk melihat mikrostruktur permukaan jaringan dentin dengan ASPn+KMTn diperlukan alat uji yaitu SEM dan untuk mengetahui komposisi kimia menggunakan EDX.
2.10 Hipotesis Penelitian
Dari uraian di atas dapat dibuat hipotesa yaitu :
1. Ada perbedaan mikrostruktur permukaan jaringan dentin yang diaplikasikan biomaterial gabungan ASPn + KMTn dengan MTA dan SIKMR.
2. Ada perbedaan kandungan aktif dalam mempertahankan jaringan pulpodentinal kompleks antara biomaterial gabungan ASPn + KMTn dengan MTA dan SIKMR.