PELEPASAN IBUPROFEN DARI MIKROKAPSUL
TERSALUT PADUAN LILIN LEBAH DAN
POLI(ASAM LAKTAT) SECARA
IN VITRO
PUTRIANNA M SINUHAJI
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
BOGOR
2012
ABSTRAK
PUTRIANNA M SINUHAJI. Pelepasan Ibuprofen dari Mikrokapsul Tersalut
Paduan Lilin Lebah dan Poli(asam laktat) Secara
In Vitro
. Dibimbing oleh
TETTY KEMALA dan AHMAD SJAHRIZA.
Ibuprofen sebagai obat antiradang memiliki laju eliminasi singkat
sehingga dapat menyebabkan iritasi lambung. Teknik mikroenkapsulasi dapat
digunakan untuk mengatasi masalah tersebut serta memberikan khasiat terapi
yang lebih baik melalui mekanisme pelepasan obat terkendali. Dalam penelitian
ini, mikroenkapsulasi ibuprofen dilakukan melalui proses pencampuran dan
metode emulsi-penguapan pelarut. Senyawa ibuprofen disalut menggunakan
paduan lilin lebah dan poli(asam laktat) (PLA) berdasarkan ragam komposisi
paduan lilin lebah:PLA (9:1, 8:2, 7:3 dan 6:4) dan konsentrasi gelatin (1%, 1.5%,
dan 2%) sebagai pengemulsi. Efisiensi enkapsulasi dilakukan pada media simulasi
usus pH 7.2. Efisiensi enkapsulasi tertinggi dihasilkan oleh paduan lilin
lebah:PLA 6:4 dengan konsentrasi gelatin 2% yaitu sebesar 84.21%. Uji
pelepasan ibuprofen menggunakan nisbah paduan lilin lebah:PLA 8:2 dan 6:4
menghasilkan rerata persentase pelepasan tertinggi pada menit ke-225 yaitu
sebesar 15.31% dan 19.25%. Pola pelepasan ibuprofen mengikuti model kinetika
orde ke-0 yang menjelaskan bahwa konsentrasi ibuprofen yang dilepaskan relatif
konstan pada setiap waktu pelepasan. Pengamatan morfologi permukaan
mikrokapsul menggunakan mikroskop elektron payaran (SEM) memperlihatkan
tonjolan halus berbentuk tidak beraturan yang tersebar pada permukaannya.
ABSTRACT
PUTRIANNA M SINUHAJI.
In Vitro
Releases of Ibuprofen From Microcapsules
Coated by Blend Beeswax and Poly(lactic acid). Supervised by TETTY
KEMALA and AHMAD SJAHRIZA.
Ibuprofen as an anti-inflammatory drug has a short elimination rate which
can causes gastric irritation. Microencapsulation technique can be used to
overcome these problems and provide a better therapeutic efficacy through
controlled drug release mechanism. In this research, microencapsulation of
ibuprofen carried out by blending process and emulsion-solvent evaporation
method. Ibuprofen was coated by blend beeswax and poly(lactic acid) (PLA) with
various compositions (9:1, 8:2, 7:3, and 6:4) and concentration of gelatin (1%,
1.5%, and 2%) as an emulsifier. Efficiency of encapsulation performed in
simulated intestinal medium pH 7.2. The highest value of ibuprofen encapsulation
efficiencies was equal to 84.21% had been produced by microcapsules with ratio
bees wax:PLA 6:4 and concentration of gelatin 2%. Release test of ibuprofen was
performed by beeswax:PLA blend with ratio 8:2 and 6:4 produces the highest
average percentage release about 15.31% and
19.25%
at minute 225 in the same
medium. The release pattern of ibuprofen had followed zero order kinetics model
explaining that concentration of ibuprofen released relative constant for each
release time. Observation of surface morphology of microcapsules using a
scanning electron microscop (SEM) showed subtle bulges irregularly shaped
scattered on its surface.
PELEPASAN IBUPROFEN DARI MIKROKAPSUL
TERSALUT PADUAN LILIN LEBAH DAN
POLI(ASAM LAKTAT) SECARA
IN VITRO
PUTRIANNA M SINUHAJI
Skripsi
Sebagai salah satu syarat memperoleh gelar
Sarjana Sains pada
Departemen Kimia
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
BOGOR
2012
Judul
: Pelepasan Ibuprofen dari Mikrokapsul Tersalut Paduan Lilin Lebah
dan Poli(asam laktat) Secara
In Vitro
Nama
: Putrianna M Sinuhaji
NIM
: G44096026
Disetujui,
Pembimbing I
Dr Tetty Kemala, SSi, MSi
NIP 19710407 199903 2
Pembimbing II
Drs Ahmad Sjahriza
NIP 19620406 198903 1 002
Diketahui,
Ketua Departemen
Prof Dr Ir Tun Tedja Irawadi, MS
NIP 19501227 197603 2 002
PRAKATA
Puji dan syukur penulis panjatkan kepada Tuhan Yang Maha Esa yang
senantiasa memberikan berkat dan rahmat-Nya sehingga karya ilmiah ini berhasil
diselesaikan. Karya ilmiah ini berjudul Pelepasan Ibuprofen dari Mikrokapsul
Tersalut Paduan Lilin Lebah dan Poli(asam laktat) Secara
In Vitro
dan disusun
berdasarkan penelitian yang dilaksanakan pada bulan Agustus hingga Desember
2011 di Laboratorium Kimia Anorganik, Laboratorium Kimia Organik,
Laboratorium Bersama Departemen Kimia FMIPA IPB, Laboratorium Pengujian
dan Penelitian Fakultas Farmasi Universitas Pancasila, dan Puspiptek Serpong
Tangerang.
Penulis mengucapkan terima kasih kepada Ibu Dr Tetty Kemala SSi, MSi
dan Bapak Drs Ahmad Sjahriza selaku pembimbing yang telah memberikan
bimbingan, saran, motivasi, dan doa selama penelitian. Penulis juga mengucapkan
terima kasih kepada staf-staf laboran Laboratorium Anorganik, yaitu Bapak
Syawal, Bapak Mulyadi, Bapak Caca dan Mba Nurul serta staf laboran lainnya
yaitu Bapak Sabur, Bapak Sulis dan Mas Eko atas bantuan dan fasilitas yang
diberikan.
Terima kasih yang tak terhingga penulis ucapkan kepada papa, mama,
keluarga, dan Wahyu Frans E Tampubolon atas kasih sayang, perhatian, bantuan,
semangat, dan doanya dari awal perkuliahan hingga masa penyusunan karya
ilmiah ini. Tidak lupa ungkapan terima kasih penulis sampaikan kepada sahabat,
teman-teman Ekstensi Kimia angkatan 3 dan juga teman-teman kosan M15 atas
semangat dan doa yang telah diberikan kepada penulis. Serta terima kasih kepada
seluruh pihak yang telah membantu penulis dalam menyelesaikan karya ilmiah ini
yang tidak dapat disebutkan satu per satu tanpa maksud mengurangi rasa terima
kasih. Semoga Tuhan memberikan balasan atas segala amal yang diperbuat dan
senantiasa menyertai hamba-Nya dengan kasih dan sayang-Nya.
Semoga karya ilmiah ini dapat memberikan manfaat.
Bogor, Februari 2012
RIWAYAT HIDUP
Penulis dilahirkan di Medan pada tanggal 30 Juni 1988 sebagai anak
tunggal dari Bapak B Sinuhaji dan Ibu Diana Roselina Gurning. Penulis lulus dari
SMA Negeri 1 Medan pada tahun 2006 dan pada tahun yang sama diterima di
Akademi Analisis Kimia Medan melalui jalur Seleksi Penerimaan Mahasiswa
Program Diploma (SPMPD). Penulis lulus dari Program Diploma pada tahun
2009 dengan Indeks Prestasi Kumulatif (IPK) 3.44 dan melanjutkan pendidikan
S1 melalui Program Alih Jenis Jurusan Kimia Fakultas Matematika dan Ilmu
Pengetahuan Alam Institut Pertanian Bogor (IPB) pada tahun yang sama.
Selama perkuliahan, penulis aktif sebagai staf pengajar di Focus dan di di
beberapa tempat bimbingan lainnya. Pada bulan Mei-Juli 2009, penulis mengikuti
kegiatan Praktik Kerja Lapangan PT Sinar Mas Agro Resources and Technology
Tbk (PT SMART Tbk) dengan judul Pengaruh Pemanasan
Refined Bleached
DAFTAR ISI
Halaman
DAFTAR TABEL ... vii
DAFTAR GAMBAR ... vii
DAFTAR LAMPIRAN ... viii
PENDAHULUAN ... 1
BAHAN DAN METODE
Alat dan Bahan ... 1
Lingkup Kerja ... 2
Metode Penelitian ... 1
Sintesis Poli(asam laktat) (PLA)
(Gonzales
et al.
1999) ... 2
Pengukuran Bobot Molekul PLA (Kaitian
et al.
1996) ... 2
Pembuatan Mikrokapsul Ibuprofen Menggunakan Paduan
Lilin Lebah-PLA (Modifikasi Rohman dan Fachrurrazi 2011) ... 2
Penentuan Panjang Gelombang Maksimum
dan Pembuatan Kurva Standar... 3
Uji Efisiensi Enkapsulasi ... 3
Uji Disolusi Secara
In Vitro
(Depkes 1995) ... 3
Morfologi Mikrokapsul ... 3
HASIL DAN PEMBAHASAN ... 3
Poli(asam laktat) (PLA) ... 3
Bobot Molekul PLA ... 4
Mikroenkapsulasi Ibuprofen Menggunakan Paduan Lilin Lebah-PLA ... 4
Panjang Gelombang Maksimum dan Kurva Standar ... 5
Efisiensi Enkapsulasi Ibuprofen ... 5
Morfologi Mikrokapsul Hasil Efisiensi Enkapsulasi ... 6
Pola Pelepasan Ibuprofen dari Mikrokapsul ... 7
Kinetika Pelepasan Ibuprofen ... 8
SIMPULAN DAN SARAN ... 8
Simpulan ... 8
Saran ... 9
DAFTAR PUSTAKA ... 9
vii
DAFTAR TABEL
Halaman
1 Komposisi mikrokapsul ibuprofen tersalut paduan lilin lebah-PLA... 2
2 Parameter pelepasan ibuprofen dari mikrokapsul ... 8
DAFTAR GAMBAR
Halaman
1 Reaksi pembentukan PLA (Kaitian
et al.
1996) ... 3
2 PLA hasil sintesis ... 3
3
Tahap pembentukan mirokapsul (i) emulsifikasi fase organik ke dalam fase
cair dan (ii) penguapan pelarut (Dubey
et al.
2009) ... 4
4 Mikrokapsul ibuprofen tersalut paduan lilin lebah-PLA ... 5
5 Efisiensi enkapsulasi mikrokapsul ibuprofen dengan konsentrasi gelatin
1%, 1.5%, dan 2%. ... 5
6 Foto mikroskop mikrokapsul formula DG
3tanpa penambahan
ibuprofen (a) dan dengan penambahan ibuprofen pada perbesaran 40x
(b) ... 6
7 Foto SEM mikrokapsul tanpa penambahan ibuprofen perbesaran 500x
(a) mikrokapsul DG
3perbesaran 1500x (a), 5000x (c) dan 10000x (d). ... 6
8 Pelepasan ibuprofen dari mikrokapsul formula BG
3(i) dan DG
3(ii) terhadap
DAFTAR LAMPIRAN
Halaman
1 Diagram alir penelitian ... 13
2 Data penentuan bobot molekul PLA ... 14
3 Absorbans larutan ibuprofen
apada berbagai panjang gelombang (λ) ... 15
4 Konsentrasi dan absorbans larutan ibuprofen pada pembuatan kurva
standar ibuprofen (λ
maks= 222 nm) ... 16
5 Efisiensi enkapsulasi ibuprofen dalam mikrokapsul tersalut
paduan lilin lebah-PLA ... 17
6 Pelepasan ibuprofen dari mikrokapsul pada waktu t... 18
7
Persentase rerata pelepasan ibuprofen dalam media basa dari
mikrokapsul tersalut paduan Lilin Lebah-PLA ... 20
8
Kinetika Pelepasan ibuprofen menggunakan model kinetika orde
PENDAHULUAN
Ibuprofen merupakan obat golongan non steroid yang memberikan efek analgesik, antipiretik, dan antiinflamasi. Senyawa ini terutama digunakan untuk mengobati artritis rematik dengan cara menghambat sintesis enzim prostaglandin sintetase (Gilman et al.
1996). Waktu paruh eliminasi yang singkat menyebabkan senyawa ini lebih sering dikonsumsi (Reynolds 1989). Hal ini akan mengakibatkan senyawa ibuprofen terakumulasi di lambung dalam konsentrasi yang tinggi sehingga terjadi iritasi dan pendarahan (Hadisoewignyo dan Fudholi 2007). Teknik mikroenkapsulasi dapat digunakan untuk mengatasi masalah tersebut serta memberikan khasiat terapi yang lebih baik. Mikroenkapsulasi merupakan proses penyalutan suatu bahan inti berupa padatan, cairan maupun gas menggunakan bahan penyalut seperti polimer dengan tujuan melindungi senyawa inti dari lingkungan (Shekhar et al. 2010).
Polimer poliester alifatik seperti poli(asam laktat) (PLA) telah banyak diaplikasikan sebagai bahan penyalut obat-obatan. Polimer ini bersifat biokompatibel yaitu dapat terdegradasi di dalam tubuh tanpa menimbulkan alergi dan mutasi (Cattelan et al. 2006). PLA juga bersifat mudah terdegradasi oleh panas, cahaya, bakteri, maupun oleh proses hidrolisis. Kelemahan polimer ini dapat diperbaiki melalui kopolimerisasi dengan monomer lain, pencampuran (blending) dengan polimer lain, dan plastisisasi dengan pemlastis biokompatibel (Hu et al. 2003).
Gao et al. (2009) telah berhasil memperbaiki sifat mekanik PLA melalui pencangkokan dengan poligliserol bercabang (HPG) yang digunakan sebagai bahan penyalut protein. Selain itu, Stevanovic dan Uskokovic (2009) telah berhasil melakukan pencampuran PLA dengan poliglikolida (PGA) menghasilkan poli(laktat-ko-glikolida) (PLGA) yang dapat digunakan sebagai bahan penyalut vitamin.
Selain polimer, lilin lebah juga dapat digunakan sebagai bahan untuk memperbaiki kerapuhan PLA. Ranjha et al. (2010) mengatakan bahwa lilin lebah dapat digunakan sebagai bahan pembuatan mikrokapsul karena memiliki beberapa kelebihan, yaitu stabil pada beberapa nilai pH dan tingkat kelembaban, biokompatibel, tidak imunogenik, efek minimal pada saluran pencernaan, dan tidak dose dumping.
Pencampuran lilin lebah dan PLA diharapkan dapat menghasilkan polimer kompartibel yang memiliki waktu degradasi dan permeabilitas yang lebih baik.
Metode emulsi-penguapan pelarut telah banyak digunakan untuk mengungkung obat hidrofobik melalui proses emulsifikasi minyak dalam air (o/w) (Park et al. 2005). Pembuatan mikrokapsul dengan metode ini menghasilkan mikrokapsul dengan ukuran yang seragam (Jain 2000). Emulsi yang terbentuk antara larutan paduan dan obat dengan air tidak stabil, maka diperlukan pengemulsi untuk menstabilkannya. Gelatin merupakan salah satu pengemulsi yang banyak digunakan dalam pembuatan mikrokapsul (Ranjha et al. 2010). Konsentrasi pengemulsi serta komposisi paduan lilin lebah-PLA akan mempengaruhi ukuran mikrokapsul yang dihasilkan dan banyaknya obat yang terenkapsulasi.
Penelitian ini bertujuan menghasilkan mikrokapsul ibuprofen tersalut paduan lilin lebah-PLA, menganalisis pengaruh dari variasi komposisi paduan dan konsentrasi pengemulsi terhadap efisiensi enkapsulasi ibuprofen, mempelajari morfologi mikrokapsul serta menjelaskan pola dan mekanisme pelepasan ibuprofen berdasarkan model kinetika orde reaksi ke-0, orde reaksi ke-1, dan Hickson-Crowell.
BAHAN DAN METODE
Alat dan Bahan
Alat-alat yang digunakan adalah reaktor sintesis PLA, neraca analitis Precisa XT 220A, oven Sanyo Drying MOV-212, mikroskop Carton, hotplate Nuova Thermolyne, stirrer PMC 502 Series, Spektrofotometer Vis tipe Shimadzu UV-1601, Seperangkat alat uji disolusi tipe 2 (dayung) RC-6 Dissolution Tester
(Universitas Pancasila Depok), mikroskop elektron payaran (SEM) Jeol-6 seri JSM-6510 LA (Puspiptek Tangerang Serpong), thermometer, viskometer ostwald, mortar, pengaduk magnet, dan alat-alat kaca.
Bahan-bahan yang digunakan adalah Ibuprofen, asam laktat pa (Merck), gelatin (bloom number 200), diklorometana (Merck), etil asetat, Na2HPO4.7H2O (Fisher Scientific Company), NaH2PO4.H2O (Fisher Scientific Company), lilin lebah dari daerah Cimanggis Depok dan akuades.
Lingkup Kerja
Penelitian ini dilakukan dalam beberapa tahapan (Lampiran 1), diantaranya sintesis PLA, penentuan bobot molekul PLA, pembuatan mikrokapsul ibuprofen tersalut paduan lilin lebah dan PLA, penentuan panjang gelombang maksimum dan kurva standar, uji efisiensi enkapsulasi, uji disolusi mikrokapsul, dan karakterisasi mikrokapsul menggunakan mikroskop dan SEM.
Metode Penelitian
Sintesis Poli(asam laktat) (PLA) (Gonzales
et al. 1999)
Pembuatan PLA dilakukandengan metode polikondensasi langsung tanpa penambahan katalis. Gelas piala 100 mL dibersihkan, dikeringkan, dan ditimbang bobotnya. Sebanyak 25 mL asam laktat dimasukkan ke dalam gelas piala tersebut, ditimbang, kemudian dipanaskan secara perlahan-lahan hingga mencapai suhu 120 °C selama 1 jam. Suhu pemanasan selanjutnya dinaikkan menjadi 140-150 °C dan dijaga konstan selama 24 jam. PLA yang dihasilkan didinginkan pada suhu ruang dan ditimbang bobotnya.
Pengukuran Bobot Molekul PLA (Kaitian
et al. 1996)
Pengukuran viskositas digunakan untuk menghitung bobot molekul rata-rata. PLA dilarutkan dalam etil asetat hingga diperoleh larutan PLA dengan konsentrasi 0.02%, 0.03%, 0.04%, dan 0.05% b/v, Pengukuran viskositas dilakukan menggunakan viskometer Ostwald pada suhu 25 °C (suhu konstan) dengan cara menghitung waktu alir pelarut dan waktu alir larutan PLA pada berbagai konsentrasi. Setelah itu, viskositas relatif (η relatif) ditentukan dengan cara membandingkan waktu alir pelarut dengan waktu alir larutan polimer (t0/t). Viskositas intrinsik [η] dicari dengan cara memplotkan η spesifik/[PLA] sebagai sumbu y dan konsentrasi sebagai sumbu x.
Bobot molekul (Mv) dan bobot molekul rata-rata ditentukan berdasarkan persamaan Mark-Houwink:
[η] = k(Mv)a
k dan a merupakan tetapan yang bergantung pada pelarut, polimer, dan suhu. Pelarut dan suhu yang digunakan pada penelitian ini adalah etil asetat dan 25 °C. Nilai k dan a secara berturut-turut adalah 1.58×10-4 dan 0.78.
Pembuatan Mikrokapsul Ibuprofen Menggunakan Paduan Lilin Lebah-PLA (modifikasi Rohman 2011 dan Fachrurrazi 2011)
Larutan paduan dibuat dengan melarutkan lilin lebah dan PLA dalam diklorometana, kemudian diaduk hingga homogen selama 30 menit. Setelah itu sebanyak 0.15 gram ibuprofen yang telah dilarutkan dengan 5 mL diklorometana dicampurkan ke dalam larutan paduan dan diaduk kembali selama 30 menit. Campuran tersebut kemudian didispersikan ke dalam 225 ml akuades yang telah mengandung gelatin sambil diaduk menggunakan motor pengaduk dengan kecepatan putar 800 rpm selama 90 menit. Mikrokapsul yang terbentuk kemudian didekantasi hingga mengendap. Mikrokapsul yang diperoleh kemudian disaring, dicuci dengan akuades, dikeringudarakan selama 24 jam lalu dikeringkan di dalam oven pada suhu 40 °C selama 1 jam.
Tabel 1 Komposisi mikrokapsul ibuprofen tersalut paduan lilin lebah-PLA
Formula Nisbah paduan (Lilin Lebah:PLA) Konsentrasi gelatin (%) AG1 9:1 1.0 AG2 9:1 1.5 AG3 9:1 2.0 BG1 8:2 1.0 BG2 8:2 1.5 BG3 8:2 2.0 CG1 7:3 1.0 CG2 7:3 1.5 CG3 7:3 2.0 DG1 6:4 1.0 DG2 6:4 1.5 DG3 6:4 2.0
Penentuan Panjang Gelombang Maksimum dan Pembuatan Kurva Standar
Larutan ibuprofen dalam bufer fosfat pH 7.2 dengan konsentrasi 10 ppm diukur absorbansnya pada panjang gelombang (λ) 210-240 nm menggunakan spekrofotometer ultraviolet. Panjang gelombang maksimum (λmaks) yang diperoleh digunakan untuk analisis selanjutnya.
Kurva standar dibuat dengan mengukur absorbans larutan ibuprofen dengan konsentrasi 2, 4, 6, 8, 10, 12, 14, 16, 18, dan 20 ppm pada panjang gelombang maksimum. Hasil yang diperoleh merupakan hubungan konsentrasi ibuprofen dengan absorbans.
Uji Efisiensi Enkapsulasi
Sebanyak 25 mg kapsul ditimbang dan digerus hingga halus kemudian dilarutkan
3
ke dalam 50 mL bufer fosfat pH 7.2. Campuran tersebut disaring dan filtratnya diencerkan sebanyak 10 kali. Setelah itu, filtrat dibaca absorbansnya dengan spektrofotometer UV/Vis pada panjang gelombang maksimum 222 nm. Absorbans yang diperoleh digunakan untuk menentukan konsentrasi ibuprofen dengan bantuan kurva standar.
Uji Disolusi Secara In Vitro (Depkes 1995)
Uji disolusi mikrokapsul dilakukan menggunakan alat disolusi tipe 2 (tipe dayung). Sebanyak 200 mg mikrokapsul ditimbang dan dimasukkan ke dalam chamber
disolusi. Uji disolusi dilakukan dalam media simulasi cairan usus (larutan bufer fosfat pH 7.2) selama 6 jam pada suhu (37 0.5) C dengan kecepatan pengadukan 100 rpm. Volume media disolusi yang digunakan sebanyak 900 mL. Pengambilan alikuot dilakukan setiap 15 menit dengan volume setiap kali pengambilan 10 mL. Setiap kali pengambilan alikuot, volume media yang terambil digantikan dengan larutan media yang baru dengan volume dan suhu yang sama. Konsentrasi ibuprofen dalam larutan alikuot diukur menggunakan spektrofotometer UV pada λmaks. Data yang diperoleh dibuat kurva hubungan antara persen pelepasan ibuprofen dan waktu disolusi, serta dikaji kinetika pelepasannya.
Morfologi Mikrokapsul
Pengamatan morfologi mikrokapsul dilakukan terhadap mikrokapsul kosong dan yang terisi ibuprofen menggunakan mikroskop dan SEM.
HASIL DAN PEMBAHASAN
Poli(asam laktat) (PLA)
PLA disintesis menggunakan metode polikondensasi secara langsung dengan suhu tinggi. Metode ini merupakan metode yang paling sederhana dibandingkan dengan metode pembuatan PLA lainnya (Gonzales et al. 1999). Pada tahap awal pembentukan PLA, monomer asam laktat dipanaskan terlebih dahulu di dalam reaktor sintesis PLA pada suhu 120oC. Hal ini bertujuan melepaskan air dan sekaligus terjadinya depolimerisasi pembentukan dimer asam laktat. Kemudian suhu dinaikkan menjadi 150oC selama 24 jam untuk mempercepat reaksi polimerisasi (Kemala 2010).
Gambar 1 Reaksi pembentukan PLA (Kaitian et al. 1996).
Reaksi pembentukan PLA merupakan reaksi yang dapat balik (Gambar 1). Oleh karena itu, molekul air yang dihasilkan harus langsung dipindahkan atau dihilangkan dengan menggunakan pompa vakum. Adanya molekul air akan menurunkan laju polimerisasi sehingga PLA yang dihasilkan memiliki bobot molekul yang lebih rendah. (Kaitian et al.1995).
PLA hasil sintesis berwarna kuning kecoklatan (Gambar 2). PLA ini diduga merupakan PLA dalam bentuk rasemiknya (D,L-PLA). Menurut Dutkiewicz et al.(2003), sintesis PLA pada suhu lebih dari 140°C akan menghasilkan PLA dalam bentuk rasemiknya. D,L-PLA lebih bersifat amorf dibandingkan L-PLA, oleh sebab itu penggunaan D,L-PLA lebih disukai dalam sistem penghantaran obat, karena mudah terdegradasi dan lebih mampu untuk mendispersikan obat secara homogen dalam matriks polimer (Gunatilake dan Adhikari 2003).
Gambar 2 PLA hasil sintesis
Bobot Molekul PLA
Tinggi rendahnya bobot molekul PLA yang dihasilkan dipengaruhi oleh penggunaan suhu pemanasan dan lamanya waktu polimerisasi yang optimal. Hal tersebut disebabkan oleh sifat PLA yang mudah terdegradasi oleh lingkungan maupun oleh reaksi hidrolisis dan enzimatik karena adanya ikatan ester dan gugus hidroksil pada rantai ujungnya. Penggunaan suhu yang terlalu tinggi dan waktu polimerisasi yang terlalu lama akan menurunkan bobot molekul dari PLA yang terbentuk. Panas yang dihasilkan pada sistem reaktor sintesis karena suhu yang terlalu tinggi akan menghidrolisis polimer PLA yang terbentuk, sehingga polimer tersebut akan kembali ke bentuk monomernya. Hal ini dikarenakan oleh reaksi polimerisasi yang bersifat dapat balik. Apabila dalam keadaan tersebut proses polimerisasi
n CH3 O HC C O Pemanasan H2O CH3 O H HC C O OH
+
masih dilanjutkan, polimer tersebut akan terdegradasi dan hangus (Kaitian et al. 1995). Pelarut etil asetat digunakan pada pengukuran bobot molekul PLA karena bersifat nonpolar, tidak beracun, dan tidak higroskopis. PLA hasil sintesis memiliki bobot molekul sebesar 8239.50 g mol-1 (Lampiran 2) dengan rendemen sebesar 58.8404%. PLA dengan bobot molekul rendah (kurang dari 10.000 g mol-1 dapat dibuat menggunakan metode polikondensasi langsung (Vroman dan Tighzert 2009).
Mikroenkapsulasi Ibuprofen Menggunakan Paduan Lilin Lebah-PLA
Mikrokapsul paduan lilin lebah dan PLA dibuat melalui proses pencampuran fisika yaitu tidak membentuk ikatan kovalen antara komponen-komponennya. Interaksi yang terjadi adalah ikatan van der Waals, ikatan hidrogen atau interaksi dipol-dipol (Rabek 1980). Metode yang digunakan untuk membuat mikrokapsul pada penelitian ini yaitu metode emulsifikasi obat dalam larutan polimer organik dan media dispersi air (o/w) (Birnbaum dan Brannon-Peppas 2004). Metode emulsi-penguapan pelarut cocok untuk membuat mikrokapsul obat dari poliester biodegaradabel seperti PLA (Dubey
et al. 2009). Metode ini memiliki beberapa keuntungan yaitu dilakukan pada suhu ruang dan menghasilkan mikrokapsul yang memiliki mekanisme pelepasan material yang dikungkung secara optimal karena material yang dikungkung terdispersi secara homogen pada matriks polimer sehingga dianggap ideal untuk sistem pengantaran obat (Obeidat 2009). Proses pada metode ini dilakukan dengan melarutkan polimer dalam pelarut volatil yang tidak dapat campur dengan fase cair (o/w emulsi) (Venkatesan et al. 2009). Fase organik yang digunakan pada penelitian ini adalah diklorometana. Selain diklorometana, dapat juga digunakan kloroform, tetapi membutuhkan waktu yang lebih lama untuk menguap dibandingkan dengan diklorometana. Kloroform menguap pada suhu 61°C, sedangkan diklorometana menguap pada suhu 39 °C. Mikrokapsul akan lebih cepat terbentuk ketika menggunakan diklorometana (Kemala et al. 2010). Yeo dan Park (2004) mengatakan bahwa diklorometana lebih mudah larut dalam air dibandingkan kloroform. Kelarutan yang tinggi dalam air akan membuat transfer massa antara fase dispersi dan fase pendispersi relatif cepat sehingga pengendapan polimer lebih
cepat. Pengemulsi yang digunakan dalam penelitian ini adalah gelatin yang memiliki kemampuan mengadsorpsi pada antarmuka Gugus hidrofil dari gelatin akan berikatan dengan molekul air sedangkan gugus lipofilnya akan berikatan dengan diklometana sehingga emulsi lebih stabil. Pendispersian ke dalam air berfungsi untuk menguapkan diklorometana dari emulsi dan mikrokapsul yang terbentuk akan mengendap. Mikrokapsul yang didapatkan selanjutnya didekantasi dan dibilas beberapa kali dengan akuades panas untuk menghilangkan sisa-sisa gelatin yang menempel pada mikrokapsul.
Mikrokapsul ibuprofen yang dihasilkan memiliki bentuk visual seperti serbuk, halus, kering, dan berwarna putih (Gambar 3).
Gambar 3 Mikrokapsul ibuprofen tersalut paduan lilin lebah-PLA.
Campuran dikatakan homogen jika tidak terlihat lagi perbedaan antara komponen-komponen penyusunnya, baik dalam bentuk, ukuran, maupun warna karena semua komponennya telah tercampur secara merata (Rosida 2007). Kemala et al. (2012) mengatakan bahwa pencampuran dua atau lebih cairan menghasilkan campuran homogen, maka dapat dikatakan kompartibel, Pada penelitian ini dapat disimpulkan bahwa campuran PLA dan lilin lebah adalah kompartibel.
Panjang Gelombang Maksimum dan Kurva Standar
Pelarut yang digunakan dalam pembuatan larutan ibuprofen adalah bufer fosfat pH 7.2. Nilai pH bufer tersebut dipilih untuk menyesuaikan dengan pH usus dan biasa digunakan sebagai media disolusi tablet ibuprofen (Depkes 1995).
Penentuan λmaks dilakukan pada daerah ultraviolet karena ibuprofen memiliki struktur ikatan terkonjugasi. Pengukuran sampel pada λmaks karena memiliki perubahan serapan untuk setiap satuan konsentrasi paling besar. Dengan demikian akan didapatkan kepekaan dan sensitivitas pengukuran yang maksimum (Sutrisna 2005). Panjang gelombang maksimum (λmaks) yang diperoleh yaitu 222
5
nm (Lampiran 3). Nilai λmaks larutan ibuprofen yang diperoleh tersebut sesuai dengan literatur, yaitu 222 nm (Depkes 1995). Linearitas menunjukkan kemampuan suatu metode analisis untuk memperoleh hasil pengujian yang sesuai dengan konsentrasi analit dalam contoh pada kisaran konsentrasi tertentu (AOAC 2002). Linearitas suatu metode analisis adalah ukuran yang menunjukkan tingkat kesesuaian atau korelasi antara kadar analit dan respons detektor, dinyatakan sebagai koefisien korelasi (R2) (Depkes 2001).
Persamaan regresi linear untuk kurva standar adalah y = 0.0451x + 0.0082 dengan nilai r sebesar 0.9998 (Lampiran 4). Menurut AOAC (2002) nilai ini memenuhi syarat yang ditetapkan, yaitu 0.9900. Nilai koefisien korelasi yang tinggi menunjukkan hubungan yang linear antara sinyal detektor yang terukur dan jumlah ibuprofen dalam contoh.
Efisiensi Enkapsulasi Ibuprofen
Efisiensi enkapsulasi merupakan parameter yang digunakan untuk menentukan keberhasilan proses enkapsulasi. Parameter ini menunjukkan berapa persen senyawa ibuprofen yang berhasil disalut dalam mikrokapsul. Semakin tinggi efisiensi ibuprofen dalam mikrokapsul maka semakin banyak ibuprofen yang tersalut didalam paduan.
Gambar 4 Efisiensi enkapsulasi mikrokapsul ibuprofen dengan konsentrasi gelatin = 1%; = 1.5%; = 2%.
Hasil uji efisiensi menunjukkan peningkatan efisiensi enkapsulasi dengan bertambahnya perbandingan PLA terhadap lilin lebah (Gambar 4). Efisiensi enkapsulasi
terendah dihasilkan oleh mikrokapsul AG1
sebesar 51.50% dan efisiensi enkapsulasi tertinggi oleh mikrokapsul DG3 yaitu sebesar 84.21%. Perbedaan hasil ini dipengaruhi oleh nisbah massa paduan. Pada mikrokapsul AG1, lilin lebah yang digunakan lebih banyak dibandingkan mikrokapsul DG3. Lilin lebah merupakan lemak hewan yang terdiri dari senyawa campuran alkana, alkena, monoester, diester, monohidroksiester, dan asam lemak. Monoester dari alkohol C24-C34 merupakan komponen terbanyak yaitu sekitar 40% (Jackson dan Eller 2006). Lilin lebah memiliki bobot molekul sekitar 868 g mol-1. Lilin lebah yang lebih banyak pada paduan menyebabkan komponen paduan dengan bobot molekul rendah bertambah sehingga akan lebih sulit untuk mengungkung ibuprofen. Hal ini sesuai dengan pernyataan Kim et al.(2003) yaitu efisiensi mikrokapsul berbeda pada penggunaan berat molekul polimer berbeda, semakin tinggi berat molekul polimer maka semakin tinggi efisiensi yang dihasilkan.
Selain itu, jenis dan konsentrasi pengemulsi juga merupakan faktor yang memberikan pengaruh terhadap efisiensi enkapsulasi. Ranjha et al. (2010) melaporkan bahwa tween 20 memberikan efisiensi enkapsulasi lebih tinggi dibandingkan gelatin. Hal ini dipengaruhi oleh nilai keseimbangan hidrofilik lipofilik (HLB) tween 20 yang lebih besar dibandingkan gelatin. HLB yang lebih besar dapat menurunkan tegangan antar muka lebih baik lagi sehingga dispersi emulsi dalam media pendispersi semakin meningkat. Konsentrasi pengemulsi juga memberikan pengaruh yang cukup besar. Hal ini berkesesuaian dengan hasil yang diperoleh. Pada nisbah paduan 6:4, 8:2 dan 9:1, dapat dilihat bahwa dengan meningkatnya konsentrasi gelatin maka efisiensi enkapsulasi juga meningkat. Namun, tidak demikian untuk nisbah paduan 7:3. Hal ini mungkin disebabkan oleh faktor kecepatan pengadukan yang tidak homogen atau waktu dispersi yang tidak seragam. Data perhitungan efisiensi enkapsulasi untuk semua formula mikrokapsul dapat dilihat pada Lampiran 5.
Morfologi Mikrokapsul Hasil Efisiensi Enkapsulasi
Morfologi mikrokapsul paduan lilin lebah-PLA diamati dengan menggunakan mikroskop (Gambar 5) dan SEM (Gambar 6).
AG(9:1) BG(8:2) CG(7:3) DG(6:4) Nisbah paduan lilin lebah:PLA
(a) (b)
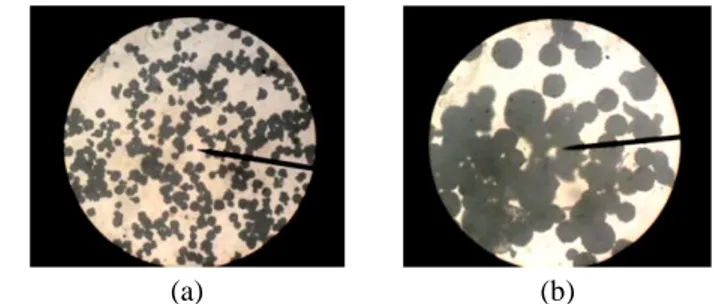
Gambar 5 Foto mikroskop mikrokapsul formula DG3 tanpa penambahan ibuprofen (a) dan dengan penambahan ibuprofen (b) pada perbesaran 40x.
(a) (b) (c) (d)
Gambar 6 Foto SEM mikrokapsul tanpa penambahan ibuprofen perbesaran 500x (Rohman 2011) (a) mikrokapsul DG3 perbesaran 1500x (a), 5000x (c) dan 10000x (d).
Mikrokapsul yang digunakan adalah mikrokapsul kosong dan mikrokapsul yang memiliki efisiensi enkapsulasi tertinggi (DG3). Hasil analisis mikrokapsul ibuprofen tersalut paduan lilin lebah-PLA menggunakan mikroskop menunjukkan bahwa mikrokapsul kosong tanpa penambahan ibuprofen (Gambar 5a) berbentuk bulat dan lebih terlihat transparan. Sementara itu, mikrokapsul DG3 (Gambar 5b) memperlihatkan bentuk yang bulat, lebih besar dan lebih gelap. Hal ini menunjukkan bahwa ibuprofen telah tersalut dalam matriks polimer. Pembuatan mikrokapsul kosong dilakukan menggunakan kondisi yang sama dengan mikrokapsul DG3.
Pengamatan morfologi mikrokapsul menggunakan SEM menunjukkan mikrokapsul tanpa penambahan ibuprofen (Gambar 6a) terlihat lebih halus dibandingkan dengan mikrokapsul dengan penambahan ibuprofen (Gambar 6b) yang memiliki tonjolan tidak beraturan yang tersebar pada permukaannya. Hal ini disebabkan adanya senyawa ibuprofen yang tersalut di dalam matriks polimer maupun dipermukaannya. Menurut Birnbaum dan Brannon-Peppas (2004), penyebaran senyawa aktif baik yang berwujud padat maupun cair dalam suatu kapsul dapat bermacam-macam. Senyawa aktif dapat terletak tepat di tengah-tengah kapsul atau tersebar di seluruh kapsul. Ukuran mikrokapsul yang dihasilkan diduga berkisar antara 30-180 μm. Jain (2000) mengatakan bahwa ukuran mikrokapsul yang digunakan
untuk drug delivery system tidak boleh lebih dari 250 μm.
Pola Pelepasan Ibuprofen dari Mikrokapsul
Disolusi adalah proses masuknya zat padat
ke dalam larutan. Menurut Kiortsis et al. (2005) proses disolusi obat terdiri atas 3
tahap, tahap pertama adalah proses penetrasi media disolusi ke dalam matriks kapsul (hidrasi), tahap kedua adalah tahap terjadinya pembengkakan dan erosi matriks kapsul, dan tahap ketiga adalah tahap terjadinya perpindahan senyawa obat yang telah lepas keluar dari matriks kapsul yang terhidrasi menuju ke media disolusi. Secara sederhana, disolusi merupakan proses zat padat melarut yang dikendalikan oleh afinitas antara zat padat dengan pelarut (Kemala 2010). Mikrokapsul yang di uji pada tahap ini adalah mikrokapsul formula BG3 dan DG3 yang memiliki efisiensi enkapsulasi lebih dari 80%. Proses disolusi pada penelitian ini dilakukan secara in vitro pada media simulasi usus, yaitu pada media basa (pH 7.2) selama 6 jam. Data hasil uji disolusi ibuprofen dapat dilihat pada Lampiran 6 dan 7.
Pelepasan ibuprofen dalam media basa untuk mikrokapsul formula BG3 dan DG3 berturut- turut adalah 5.67-15.31% dan 10.61-19.25%. Mikrokapsul formula DG3 memiliki persentase pelepasan ibuprofen lebih besar dari mikrokapsul formula BG3. Hal ini
7
disebabkan mikrokapsul formula DG3 memiliki efisiensi enkapsulasi lebih tinggi dari mikrokapsul formula BG3, yang berarti kandungan ibuprofen dalam mikrokapsul formula DG3 lebih banyak daripada kandungan ibuprofen dalam mikrokapsul formula BG3. Kandungan ibuprofen yang lebih banyak dalam mikrokapsul formula DG3 akan menghasilkan lebih banyak pori atau lubang pada mikrokapsul, oleh karena itu ketika senyawa obat lepas dari matriks polimer, maka pori-pori pada matriks polimer akan semakin banyak sehingga meningkatkan laju pelepasan senyawa obat (Cardinal 1984). Faktor lainnyayang dapat mempengaruhi laju pelepasan adalah ukuran dari mikrokapsul. Semakin kecil ukuran mikrokapsul, maka pelepasan senyawa inti dari matriks polimer akan semakin cepat. Hal ini dikarenakan luas permukaannya yang semakin besar. Hubungan antara persentase pelepasan ibuprofen dengan waktu ditunjukkan pada Gambar 7.
Gambar 7 Pelepasan ibuprofen dari mikrokapsul formula BG3(i) dan DG3(ii) terhadap waktu (menit).
Profil disolusi untuk kedua formula menunjukkan adanya initial burst release
pada menit ke-15 yaitu 5.67% untuk mikrokapsul formula BG3 dan 10.61 % untuk mikrokapsul formula DG3. Initial burst
release terjadi karena adanya obat yang tersalut pada permukaan. Pelepasan ibuprofen meningkat secara bertahap hingga mencapai waktu pelepasan maksimum yaitu pada menit ke-225. Hal ini berarti bahwa mikrokapsul yang dihasilkan telah memenuhi tujuan dalam
penelitian ini yaitu memperlama waktu pelepasan ibuprofen, yang mana waktu eliminasi ibuprofen komersial pada umumnya adalah 2 jam.
Kinetika Pelepasan Ibuprofen
Kinetika pelepasan obat digunakan untuk mengetahui laju pelepasan obat dan mekanismenya berdasarkan model yang sesuai. Umumnya kinetika pelepasan obat terkendali mengikuti orde ke nol atau ke satu (Singhvi dan Singh 2011). Mekanisme pelepasan ibuprofen dapat ditentukan dengan melihat nilai koefisien korelasi (R2) tertinggi yang dihasilkan oleh model kinetika untuk sistem penghantaran obat lepas terkendali. Penentuan model kinetika ini dilakukan dengan menggunakan software KinetDS 3.0 rev 2010.
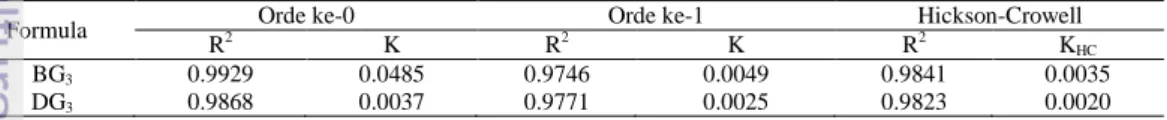
Mekanisme pelepasan ibuprofen dari mikrokapsul formula BG3 dan DG3 mengikuti model kinetika orde ke-0 berdasarkan nilai R2 yang diperoleh (Tabel 2). Pada Lampiran 6 dan 7, dapat dilihat bahwa persentase pelepasan ibuprofen pada formula BG3 dan DG3 meningkat namun tidak terlalu signifikan dengan bertambahnya waktu disolusi. Hal ini dipengaruhi oleh sifat dari matriks mikrokapsul yang mampu menahan laju pelepasan ibuprofen sehingga persentase ibuprofen yang dilepaskan setiap 15 menit tidak terlalu besar. Selain itu, adanya sinyal yang terukur dari media disolusi menandakan bahwa permukaan mikrokapsul telah mengalami pengikisan. Hubungan antara persentase ibuprofen dengan waktu tersebut kemudian diplot kedalam kurva dan mengikuti model kinetika orde ke-0 dengan nilai R2 untuk formula BG3 dan DG3 sebesar 0.9929 dan 0.9868%. Laju pelepasan ibuprofen terjadi secara bertahap dari menit ke-15 hingga menit ke-225 (Gambar 7). Setelah menit ke-225, laju pelepasan ibuprofen tidak lagi mengalami kenaikan melainkan turun secara perlahan-lahan. Hal ini berarti konsentrasi obat telah menurun. Selanjutnya kurva menjadi cenderung turun karena telah terjadinya kesetimbangan antara media dan cairan dalam mikrokapsul sehingga laju
Tabel 2 Parameter pelepasan ibuprofen dari mikrokapsul
Formula Orde ke-0 Orde ke-1 Hickson-Crowell
R2 K R2 K R2 KHC
BG3 0.9929 0.0485 0.9746 0.0049 0.9841 0.0035 DG3 0.9868 0.0037 0.9771 0.0025 0.9823 0.0020
pelepasan obat menjadi sangat kecil, terlihat dari nilai tetapan laju (K) yang diperoleh pada kedua formula. Mekanisme pelepasan ibuprofen menggunakan model kinetika Hickson-Crowell yang menjelaskan bahwa adanya pelepasan obat dapat dilihat dari perubahan permukaan area dan diameter dari partikel atau tablet (Singhvi dan Singh 2011). Perubahan ini dikarenakan oleh pengikisan yang terjadi pada permukaan hingga ke inti mikrokapsul.
SIMPULAN DAN SARAN
Simpulan
Mikroenkapsulasi ibuprofen menggunakan
paduan lilin lebah dan PLA menghasilkan mikrokapsul dengan bentuk visual seperti
serbuk halus, kering, dan berwarna putih. Efisiensi enkapsulasi tertinggi dihasilkan oleh mikrokapsul dengan nisbah paduan lilin lebah:PLA 6:4 dan konsentrasi gelatin 2% sebesar 84.21%. Pengamatan morfologi mikrokapsul menunjukkan ibuprofen berhasil disalut dan tersebar pada matriks polimer. Uji disolusi mikrokapsul dalam medium simulasi cairan usus menunjukkan bahwa mikrokapsul dengan efisiensi enkapsulasi lebih tinggi mengalami pelepasan ibuprofen yang lebih besar. Mikrokapsul yang dihasilkan memiliki waktu pelepasan ibuprofen yang lebih lama dibandingkan dengan mikrokapsul ibuprofen komersial. Kinetika pelepasan ibuprofen mengikuti model kinetika orde ke-0 yang menjelaskan bahwa konsentrasi pelepasan ibuprofen yang dilepaskan relatif konstan untuk setiap unit waktu pelepasan.
Saran
Ukuran mikrokapsul dan distribusinya perlu dianalisis menggunakan Particel Size Analyzer (PSA) serta dikaji pengaruhnya terhadap pelepasan obat. Selain itu, perlu dilakukan uji disolusi secara in vivo untuk mengetahui pelepasan ibuprofen dalam tubuh.
DAFTAR PUSTAKA
[AOAC] Association of official analytical chemists. 2002. AOAC International methods committee guidelines for validation of qualitative and quantitative food microbiological official methods of analysis. [terhubung berkala]. J AOAC Int. 85: 1–5. [2 Feb 2007].
Birnbaum DT, Brannon Peppas. 2004. Microparticle drug delivery systems in Cancer Therapy. Totowa: Humana Pr. Cardinal, J.R. (1984). Matrix systems. In:
Medical application of controlled release,Vol 1. Classes.
Cattelan AM, Bauer U, Trevenzoli M, Sasset L, Campostrini S, Facchin C, Pagiaro E, Gerzeli S, Cadrobbi P, Chiarelli A. 2006.Use of polylactid acid implants to correct facial lipoatrophy in human immunodeficiency virus 1-positive individuals receiving combination. antiretroviral therapy. Arch Dermatol
142:329-334.
Dubey R, Shami TC, Rao KUB. 2009. Microencapsulation technology and application. Defence Science Journal
29(1):82-95.
Dutkiewicz S, Lapienis DG, Tomaszewski W. 2003. Synthesis of poly(L(+) lactic acid) by polycondensation method in solution.
Fibres & Textiles in Eastern Europe 11 (4):66-70.
[Depkes RI] Departemen Kesehatan Republik Indonesia. 1995. Farmakope Indonesia. Jakarta: Depatemen Kesehatan RI.
[Depkes RI] Departemen Kesehatan Republik Indonesia. 2001. Petunjuk Operasional Penerapan CPOB. Ed ke-2. Jakarta: Departemen Kesehatan RI.
Fachrurrazie. 2011. Mikroenkapsulasi ibuprofen tersalut paduan poli(asam laktat) dan lilin lebah. [skripsi]. Bogor: Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor.
Gao X, Zhang X, Wu Z, Zhang X, Wang Z, Li C. 2009. Synthesis and physicochemical characterization of a novel amphiphilic polylactic acid-hyperbranched polyglycerol conjugate for protein delivery. Journal of Controlled Release 140:141-147.
Gilman AG, Hardman JG, Limbird LE. 1996. Goodman and gilmans the pharmacological basic’s of therapeutics. 9th edition. New York: The New Mc Graw Hill Company. Gunatilake PA, Adikari R. 2003.
Biodegradadable synthetic polymers for tissue engineering. European Cells and Materials 5:1-16.
9
Gonzales MF, Ruseckaite RA, Cuadrado TR. 1999. Structural changes of polylactic-acid (PLA) microspheres under hydrolytic degradation. Journal of Applied Polymer Science. 71:1223–1230.
Hadisoewignyo L, Fudholi A. 2007. Studi pelepasan in vitro ibuprofen dari matrikks xanthan gum yang dikombinasikan dengan suatu crosslinking agent. Majalah Farmasi Indonesia 18(3):33-140.
Hu Y, Rogunova M, Topolkaraev V, Hiltner A,
Baer E. 2003. Aging of
poly(lactide)/poly(ethylene glycol) blends: part 1. poly(lactide) with low stereoregularity. Journal of Microencapsulation 44: 5701–5710. Jackson MA, Eller FJ. 2006. Isolation of
long-chain aliphatic alcohols from beeswax using lipase-catalyzed methanolysis insupercritical carbon dioxide. Elvisier
37:173-177.
Jain RA. 2000. The manufacturing technique of various drug loaded biodegradable poly(lactide-co-glycolide) (PLGA) devices.
Biomaterials 21:2475-2490.
Kaitian X, Kozluca A, Denkbas EB, Piskin E. 1996. Poly(D,L-lacticacid) homopolimers: synthesis and characterisation. Turkey Journal of Chemistry 20:43-53.
Kim BK, Hwang SJ, Park JB, Park HJ. 2003. Characteristics of felodipinelocated poli(e-caprolactone) microspheres. Journal of Microencapsulation 22, 193–203.
Kiortsis S, Kachrimanis K, Broussali Th, Malamataris S. 2005. Drug release from tableted wet granulations comprising cellulosic and hydrophobic component.
Eur J Pharm Biopharm. 59:73-83. Kemala T. 2010. Mikrosfer paduan poli(asam
laktat) dengan poli(ɛ-kaprolakton) sebagai pelepasan terkendali ibuprofen secara in vitro [disertasi]. Jakarta: Program Pascasarjana, Universitas Indonesia. Kemala T, Budianto E, Soegiyono B. 2012.
Preparation and characterization of microspheres based on blend of poly(lactic acid) and poly(ɛ-caprolactone) with poly(vinyl alcohol) as emulsifier. Arabian Journal of Chemistry [in press].
Obeidat WM. 2009. Recent patents review in microencapsulation of pharmaceuticals using the emulsion solvent removal methods. Recent Patents on Drug Delivery & Formulation 3:178-192.
Park JH, Ye M, Park K. 2005. Biodegradable polymers for microencapsulation of drugs.
Molecules 10:146-161.
Ranjha NM, Khan H, Naseem S. 2010. Encapsulation and characterization of controlled release flurbiprofen loaded microspheres using beeswax as an encapsulating agent. J. Mater Sci.:Mater Med. 21:1621–1630.
Rabek JF. 1980. Experimental methods of polymer chemistry. New York: John Wiley and Sons.
Reynolds JE. 1989. Martindale: the extra pharmacopeia, Ed ke-29. London: Pharmaceutical Pr.
Rohman, RA. 2011. Optimasi dan evaluasi mikrokapsul tersalut paduan poliasamlaktat-lilin lebah [skripsi]. Bogor: Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor.
Rosida A. 2007. Pencirian paduan poli(asam laktat) dengan polikaprolakton [skripsi]. Bogor: Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor.
Shekhar K, Madhu MN, Pradeep B, Banji D. 2010. A review on microencapsulation. Journal of Microencapsulation 5:58-61. Singhvi G, Singh M. 2011. Review: in-vitro
drug release characterization models.
International Journal of Pharmaceutical Studies and Research 2(1):77-84.
Stevanovic M, Uskokovic D.2009. poly(lactide-co-glycolide)-based micro and nanoparticles for the controlled drug delivery of vitamins. Current Nanoscience
5:1-14
Sutrisna EM. 2005. Uji efek penurunan kadar glukosa darah ekstrak air buah jambu biji (Psidium guajava L.) pada kelinci.
Pharmacon 6(1):23-26.
Venkatesan P, Manavalan R, Valliappan K. 2009. Microencapsulation: a vital technique in novel drug delivery system. Journal of Pharmaceutical Science and Research
1(4):26-35.
Yeo Y, Park K. 2004. Control of encapsulation efficiency and initial burst in polymeric microparticle system. Archives of Pharmacal Research 27(1):1-12.
Yu L, Dean K, Li L. 2006. Polymer blends and composites from renewable resources.
11
Lampiran 1 Diagram alir penelitian
Larutan gelatin 1.5% Larutan gelatin 2.0% Larutan gelatin 1.0% Ibuprofen Paduan Karakterisasi Mikrokapsul
Mikroskop dan SEM
M i k r o k a p s u l
Uji Efisiensi enkapsulasi mikrokapsul
Uji disolusi mikrokapsul (Depkes 1995)
+
Campuran paduan-obat PLA
Lilin lebah
Sintesis Poli (asam laktat) (PLA) (Gonzales et al. 1999) Pengukuran BM PLA (Kaitian et al. 1996) (modifikasi Rohman 2011 dan Fachrurrazi 2011)
Penentuan panjang gelombang maksimum dan kurva standar
Lampiran 2 Data penentuan bobot molekul PLA
[PLA] (%b/v)
Laju alir
(detik) η relatif η spesifik η reduktif
0.00 37.69 1.00 - -
0.02 38.09 1.01 0.01 0.50
0.03 38.49 1.02 0.02 0.71
0.04 38.96 1.03 0.03 0.84
0.05 39.69 1.05 0.05 1.06
Contoh perhitungan ([PLA] = 0,02%) :
η relatif =
pelarut t
sampel t
η spesifik = η relatif – 1 η reduktif =
[PLA]
spesifik
= 1.01 – 1 = 38.09 = 0.01 = 0.01 37.69 0.02 = 1.01 = 0.50Grafik hubungan [PLA] terhadap η reduktif
Persamaan garis: y = 17.27x + 0.18 Viskositas intrinsik ([η]) = 0.18 [η] = k(Mv)a dimana : k = 1.58x10-4 dan a = 0.78 0.18 = 1.58x10-4 (Mv)0.78 Mv = 8239.50 g mol-1 y = 17.27x + 0.18 R² = 0.99 0.0 0.2 0.4 0.6 0.8 1.0 1.2 0 0.01 0.02 0.03 0.04 0.05 0.06 η r e d u kt if [PLA] (%b/v)
13
Lampiran 3 Absorbans larutan ibuprofen
apada berbagai panjang gelombang (λ)
Keterangan : a = larutan ibuprofen dengan konsentrasi 10 ppm b
= panjang gelombang maksimum λ (nm) absorbans 240 0.021 239 0.024 238 0.029 237 0.037 236 0.048 235 0.062 234 0.080 233 0.101 232 0.126 231 0.154 230 0.185 229 0.220 228 0.256 227 0.292 226 0.319 225 0.334 224 0.340 223 0.343 222b 0.345 221 0.343 220 0.335 219 0.323 218 0.312 217 0.301 216 0.294 215 0.289 214 0.286 213 0.285 212 0.284 211 0.286 210 0.290 209 0.298 208 0.310 207 0.328 206 0.354 205 0.391 204 0.438 203 0.499 202 0.581 201 0.689 200 0.794
Lampiran 4 Konsentrasi dan absorbans larutan ibuprofen pada pembuatan kurva
standar ibuprofen (λ
maks= 222 nm)
Grafik hubungan [ibuprofen] terhadap absorbans y = 0.0451x + 0.0082 R² = 0.9998 0 0.1 0.2 0.3 0.4 0.5 0.6 0.7 0.8 0.9 1 0 5 10 15 20 25 A b sor b an s [ibuprofen] (ppm) [ibuprofen] (ppm) Absorbans 2.00 0.105 4.00 0.186 6.00 0.276 8.00 0.365 10.00 0.462 12.00 0.548 14.00 0.637 16.00 0.736 18.00 0.824 20.00 0.908
15
Lampiran 5 Efisiensi enkapsulasi ibuprofen dalam mikrokapsul tersalut
paduan lilin lebah-PLA
Formula Massa ibuprofen (g) a (g) b (g) c [ibuprofen] (ppm) Efisiensi enkapsulasi (%) AG1 0.1503 0.4608 0.0250 0.387 8.3991 51.50 AG2 0.1505 0.4856 0.0253 0.470 10.2395 65.29 AG3 0.1503 0.4929 0.0251 0.526 11.4812 75.00 BG1 0.1505 0.4794 0.0251 0.485 10.5721 67.08 BG2 0.1504 0.4949 0.0252 0.470 10.2395 66.85 BG3 0.1503 0.4744 0.0251 0.588 12.8558 80.83 CG1 0.1501 0.4943 0.0251 0.509 11.1042 72.84 CG2 0.1503 0.4913 0.0252 0.470 10.2395 66.41 CG3 0.1504 0.4985 0.0252 0.480 10.4612 68.80 DG1 0.1500 0.4789 0.0253 0.515 11.2373 70.90 DG2 0.1504 0.4852 0.0254 0.525 11.4590 72.77 DG3 0.1501 0.4947 0.0252 0.589 12.8780 84.21 Keterangan :
a : massa total kapsul yang diperoleh
b : massa kapsul yang digunakan untuk penentuan efisiensi mikroenkapsulasi
c : absorban filtrat hasil disolusi kapsul setelah diencerkan 10 kali
Contoh perhitungan (formula AG
1) :
Y = 0.0082 + 0.0451x 0.387 = 0.0082 + 0.0451x X = 8.3991 Efisiensi enkapsulasi =
% 100 ) ( . ) ( ) ( . 1000 1 1000 1 g ibuprofen massa g b g a ekstraksi Vol mL L mg g fp ibuprofen =
% 100 1503 . 0 0250 . 0 4608 . 0 50 1000 1 1000 1 10 3991 . 8 g g g mL mL L mg g ppm = 51.50 %Lampiran 6 Pelepasan ibuprofen dari mikrokapsul pada waktu t
Mikrokapsul Formula BG3 (Ulangan I)
Bobot mikrokapsul
(g) Waktu (menit) Absorbans
[Ibuprofen] (ppm)
Persentase pelepasan ibuprofen (%b/b) 0.2007 0 0.000 0.0000 0.00 15 0.068 1.3348 5.99 30 0.070 1.3592 6.10 45 0.071 1.3969 6.26 60 0.080 1.5920 7.14 75 0.089 1.7916 8.03 90 0.100 2.0355 9.13 105 0.113 2.3171 10.39 120 0.121 2.4922 11.18 135 0.131 2.7206 12.20 150 0.133 2.7761 12.45 165 0.147 3.0665 13.75 180 0.150 3.1419 14.09 195 0.148 3.1020 13.91 210 0.155 3.2483 14.57 225 0.159 3.3525 15.03 240 0.142 2.9690 13.31 255 0.137 2.8603 12.83 270 0.138 2.8736 12.89 285 0.139 2.8891 12.96 300 0.138 2.8803 12.92 315 0.134 2.7871 12.50 330 0.132 2.7384 12.28 345 0.132 2.7361 12.27 360 0.111 2.2705 10.18
Mikrokapsul Formula BG3 (Ulangan II)
Bobot mikrokapsul
(g) Waktu (menit) Absorbans
[Ibuprofen] (ppm)
Persentase pelepasan ibuprofen (%b/b) 0.2007 0 0.000 0.0000 0.00 15 0.062 1.1929 5.35 30 0.069 1.3481 6.05 45 0.082 1.6364 7.34 60 0.085 1.7029 7.64 75 0.092 1.8581 8.33 90 0.098 1.9911 8.93 105 0.099 2.0133 9.03 120 0.109 2.2350 10.02 135 0.114 2.3459 10.52 150 0.132 2.7450 12.31 165 0.137 2.8559 12.81 180 0.145 3.0333 13.60 195 0.148 3.0998 13.90 210 0.156 3.2772 14.70 225 0.165 3.4767 15.59 240 0.140 2.9224 13.10 255 0.138 2.8780 12.91 270 0.138 2.8780 12.91 285 0.137 2.8559 12.81 300 0.136 2.8337 12.71 315 0.133 2.7672 12.41 330 0.131 2.7228 12.21 345 0.130 2.7007 12.11 360 0.115 2.3681 10.62
17
Mikrokapsul Formula DG3 (Ulangan I)
Bobot
mikrokapsul (g) Waktu (menit) Absorbans
[Ibuprofen] (ppm)
Persentase pelepasan ibuprofen (%b/b) 0.2003 0 0.000 0.0000 0.00 15 0.103 2.1109 9.48 30 0.129 2.6851 12.07 45 0.142 2.9601 13.30 60 0.139 2.9024 13.04 75 0.144 3.0133 13.54 90 0.147 3.0687 13.79 105 0.158 3.3171 14.90 120 0.161 3.3858 15.21 135 0.162 3.4013 15.28 150 0.169 3.5588 15.99 165 0.171 3.6098 16.22 180 0.180 3.8137 17.14 195 0.183 3.8647 17.37 210 0.198 4.2084 18.91 225 0.201 4.2683 19.18 240 0.189 4.0111 18.02 255 0.183 3.8780 17.43 270 0.164 3.4612 15.55 285 0.178 3.7627 16.91 300 0.171 3.6120 16.23 315 0.164 3.4568 15.53 330 0.156 3.2661 14.68 345 0.150 3.1508 14.16 360 0.139 2.9047 13.05
Mikrokapsul Formula DG3 (Ulangan II)
Bobot mikrokapsul
(g) Waktu (menit) Absorbans [Ibuprofen] (ppm)
Persentase pelepasan ibuprofen (%b/b) 0.2002 0 0.000 0.0000 0.00 15 0.126 2.6120 11.74 30 0.127 2.6341 11.84 45 0.129 2.6785 12.04 60 0.140 2.9224 13.14 75 0.146 3.0554 13.74 90 0.147 3.0776 13.84 105 0.152 3.1885 14.33 120 0.160 3.3659 15.13 135 0.163 3.4324 15.43 150 0.170 3.5876 16.13 165 0.175 3.6984 16.63 180 0.179 3.7871 17.03 195 0.187 3.9645 17.82 210 0.194 4.1197 18.52 225 0.202 4.2971 19.32 240 0.190 4.0310 18.12 255 0.182 3.8537 17.32 270 0.160 3.3659 15.13 285 0.176 3.7206 16.73 300 0.169 3.5654 16.03 315 0.163 3.4324 15.43 330 0.158 3.3215 14.93 345 0.149 3.1220 14.03 360 0.136 2.8337 12.74
Mikrokapsul Formula DG3 (Ulangan I)
Contoh perhitungan (mikrokapsul formula BG3, ulangan 1, menit ke-15):
% Pelepasan ibuprofen =
% 100 ) ( . . 1000 1 1000 1 g l mikrokapsu massa bufer Vol mL L mg g fp ibuprofen = 100% 2007 . 0 900 1000 1 1000 1 10 3348 . 1 g mL mL L mg g L mg = 5.99 % (b/b)Lampiran 7 Persentase rerata pelepasan ibuprofen dalam media basa dari
mikrokapsul tersalut paduan Lilin Lebah-PLA
Mikrokapsul Formula BG3
Waktu (menit) Persentase pelepasan ibuprofen (%b/b) Rerata persentase pelepasan ibuprofen (%b/b) Ulangan I Ulangan I 0 0.00 0.00 0.00 15 5.99 5.35 5.67 30 6.10 6.05 6.07 45 6.26 7.34 6.80 60 7.14 7.64 7.39 75 8.03 8.33 8.18 90 9.13 8.93 9.03 105 10.39 9.03 9.71 120 11.18 10.02 10.60 135 12.20 10.52 11.36 150 12.45 12.31 12.38 165 13.75 12.81 13.28 180 14.09 13.60 13.85 195 13.91 13.90 13.91 210 14.57 14.70 14.63 225 15.03 15.59 15.31 240 13.31 13.10 13.21 255 12.83 12.91 12.87 270 12.89 12.91 12.90 285 12.96 12.81 12.88 300 12.92 12.71 12.81 315 12.50 12.41 12.45 330 12.28 12.21 12.25 345 12.27 12.11 12.19 360 10.18 10.62 10.40
19
Mikrokapsul formula DG3
Waktu (menit) Persentase pelepasan ibuprofen (%b/b) Rerata persentase pelepasan ibuprofen (%b/b) Ulangan I Ulangan II 0 0.00 0.00 0.00 15 9.48 11.74 10.61 30 12.07 11.84 11.96 45 13.30 12.04 12.67 60 13.04 13.14 13.09 75 13.54 13.74 13.64 90 13.79 13.84 13.81 105 14.90 14.33 14.62 120 15.21 15.13 15.17 135 15.28 15.43 15.36 150 15.99 16.13 16.06 165 16.22 16.63 16.42 180 17.14 17.03 17.08 195 17.37 17.82 17.60 210 18.91 18.52 18.72 225 19.18 19.32 19.25 240 18.02 18.12 18.07 255 17.43 17.32 17.38 270 15.55 15.13 15.34 285 16.91 16.73 16.82 300 16.23 16.03 16.13 315 15.53 15.43 15.48 330 14.68 14.93 14.81 345 14.16 14.03 14.10 360 13.05 12.74 12.89
Lampiran 8 Kinetika pelepasan ibuprofen menggunakan model kinetika orde
reaksi ke-0, ke-1, dan Hickson-Crowell
Formula Model kinetika Persamaan regresi R2
BG3
Orde ke-0 Q = 0.0485 t + 4.7195 0.9929
Orde ke-1 Ln [A]t = 0.0049 t + 1.7189 0.9746 Hickson-Crowell Q1/3 = 0,0035 t + 1.75141/3 0.9841
DG3
Orde ke-0 Q = 0.0037 t + 10.6355 0.9868
Orde ke-1 Ln [A]t = 0.0025 t + 2.4004 0.9771 Hickson-Crowell Q1/3 = 0.0020 t + 2.21841/3 0.9823


![Grafik hubungan [PLA] terhadap η reduktif](https://thumb-ap.123doks.com/thumbv2/123dok/2462459.2760875/21.892.152.728.128.1103/grafik-hubungan-pla-terhadap-η-reduktif.webp)
![Grafik hubungan [ibuprofen] terhadap absorbans y = 0.0451x + 0.0082 R² = 0.9998 00.10.20.30.40.50.60.70.80.9105101520 25Absorbans [ibuprofen] (ppm) [ibuprofen] (ppm) Absorbans 2.00 0.105 4.00 0.186 6.00 0.276 8.00 0.365 10.00 0.462 12.00 0.548 14.00 0.637](https://thumb-ap.123doks.com/thumbv2/123dok/2462459.2760875/23.892.142.690.134.1175/grafik-hubungan-ibuprofen-absorbans-absorbans-ibuprofen-ibuprofen-absorbans.webp)